OPTIMASI SUHU AKTIVASI DAN DOSIS ZEOLIT SEBAGAI ADSORBEN SENG DAN BESI YANG TERKANDUNG DI DALAM LIMBAH CAIR
INDUSTRI SARUNG TANGAN KARET
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
VERA SIMANGUNSONG 050802003
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul :OPTIMASI SUHU AKTIVASI DAN DOSIS
ZEOLIT SEBAGAI ADSORBEN SENG DAN BESI YANG TERKANDUNG DIDALAM LIMBAH INDUSTRI SARUNG TANGAN KARET
Kategori :SKRIPSI
Nama :VERA SIMANGUNSONG
Nomor Induk Mahasiswa :050802003
Program Studi :SARJANA (S1) KIMIA
Departemen :KIMIA
Fakultas :MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Juli 2011
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Drs. Chairuddin, MSc Jamahir Gultom, Ph.D
NIP. 195912311987011001 NIP. 195209251977031001
Diketahui oleh :
Departemen Kimia FMIPA USU
Ketua,
PERNYATAAN
OPTIMASI SUHU AKTIVASI DAN DOSIS ZEOLIT SEBAGAI ADSORBEN SENG DAN BESI YANG TERKANDUNG DI DALAM LIMBAH CAIR
INDUSTRI SARUNG TANGAN KARET
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan
dan ringkasan yang masing – masing disebutkan sumbernya.
Medan, Juli 2011
PENGHARGAAN
Puji dan dan Syukur penulis panjatkan kepada Allah Bapa Yang Maha Kuasa, berkat kasih dan karunia-Nya penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini.
ABSTRAK
ABSTRACT
DAFTAR ISI
1.7.Metodelogi Penelitian 4
Bab 2 : TINJAUAN PUSTAKA 5
2.1. Lateks 5
2.1.1. Proses Pengolahan Lateks Pekat 5
2.1.2. Proses Pembuatan Sarung Tangan Karet 6 2.1.3. Tahap – tahap Pengolahan Lateks Pekat menjadi Sarung 7
Tangan Karet
2.2. Sifat Kimia Air Limbah 8
2.2.1. Limbah industri Karet 9
2.3. Logam 9
2.4. Seng 10
2.4.1. Manfaat Logam Seng 10
2.5. Besi 11
2.5.1. Manfaat Logam Besi 11
2.6. Toksisitas logam Berat 12
2.7. Spektrofotometer Serapan Atom 12
2.7.1. Prinsip Dasar Spektrofotometer Serapan Atom 13
2.7.2. Instrumentasi 14
2.7.3. Gangguan Pada SSA dan Cara Mengatasinya 15
3.3. Prosedur Penelitian 22
3.3.1. Penyediaan Zeolit Aktif 22
3.3.2. Pengaktifan Zeolit 22
3.3.3. Pembuatan Larutan Induk Zn 1000 mg/L 22 3.3.3.1. Pembuatan Larutan Standar Zn 100 mg/L 22 3.3.3.2. Pembuatan Larutan Standar Zn 10 mg/L 22
3.3.3.3. Pembuatan Larutan Standar Zn 0,5 mg/L; 1,0 mg/L; dan 23 1,5 mg/L
3.3.4. Pembuatan Larutan Induk Fe 1000 mg/L 23 3.3.4.1. Pembuatan Larutan Standar Fe 100 mg/L 23
3.3.4.2. Pembuatan Larutan Standar Fe 5 mg/L; 10 mg/L; dan 23 15 mg/L
3.3.5. Pembuatan Kurva Kalibrasi Untuk Zn 24 3.3.6. Pembuatan Kurva Kalibrasi Untuk Fe 24 3.3.7. Pengambilan Sampel dan Pengawetan Sampel 24
3.3.8. Preparasi Sampel 24
3.3.8.1. Penentuan Kandungan Zn Sebelum Penambahan Zeolit 24 Aktif
3.3.8.2. . Penentuan Kandungan Fe Sebelum Penambahan Zeolit 25 Aktif
3.3.8.3. Penyerapan Kandungan Zn dengan Penambahan Zeolit 25 Aktif
3.3.8.4. Penyerapan Kandungan Fe dengan Penambahan Zeolit 25 Aktif
3.4. Bagan Penelitian 27
3.4.1. Penyediaan Zeolit Aktif 27
3.4.2. Pengaktifan Zeolit 27
3.4.3. Pembuatan Larutan Standar Zn 28
3.4.4. Pembuatan Larutan Standar Fe 29
3.4.5. Penentuan Kandungan Zn dan Fe dalam Sampel 30 3.4.6. Penentuan Kandungan Zn dan Fe dalam Sampel dengan 31
DAFTAR TABEL
Tabel Halaman
1. Data absorbansi larutan standar Zn 47
2. Data absorbansi Zn didalam Sampel sebelum dan sesudah 48 penambahan zeolit aktif
3. Data penyerapan konsentrasi kandungan Zn didalam sampel 49 dengan variasi suhu dan dosis zeolit aktif
4. Data hasil penyerapan kandungan Zn didalam sampel dengan 50 variasi suhu dan dosis zeolit aktif
5. Data absorbansi larutan standar Fe 51
6. Data absorbansi Fe didalam Sampel sebelum dan sesudah 52 dengan variasi suhu dan dosis zeolit aktif
7. Data penyerapan konsentrasi kandungan Fe didalam sampel 53 dengan variasi suhu dan dosis zeolit aktif
ABSTRAK
ABSTRACT
BAB 1 PENDAHULUAN
1.1.Latar Belakang
Meningkatnya populasi manusia dan kebutuhannya, memacu perkembangan industri
yang semakin pesat. Sejalan dengan perkembangan yang pesat tersebut, permasalahan
lingkungan atau pencemaran menjadi aspek yang utama yang perlu mendapat perhatian
banyak pihak, karena banyaknya limbah yang dihasilkan dan dibuang oleh industri
ke alam bebas. Pengolahan limbah yang tidak baik akan menyebabkan pencemaran
lingkungan. Pencemaran lingkungan oleh logam berat terbukti mencemari perairan, yang
dapat berdampak buruk bagi masyarakat. Pada proses industri barang jadi sarung tangan
karet, logam berat dalam bentuk ZnO digunakan sebagai akselerator proses vulkanisasi
karet, sehingga ion Zn2+ terbawa dalam air limbah industri dengan konsentrasi mencapai 300 ppm, disamping itu air digunakan dalam tahap pencucian mesin dan wadah,
mengandung logam besi(Fe) dengan konsentrasi yang mencapai 50 ppm..
Sesuai SK Men.KLH No 03 tahun 2010 ambang batas konsentrasi logam Zn yang
dibuang ke lingkungan industri adalah 10 ppm, dan untuk logam Fe adalah 5 ppm.
Pada industri barang jadi sarung tangan karet, cara kimia yang umum digunakan
untuk menurunkan kandungan logam Zn2+ dalam air limbah adalah dengan menambahkan basa, umumnya NaOH atau Ca(OH)2 sampai pH sekitar 11, sehingga logam berat diendapkan sebagai hidroksidanya. Namun cara ini sangat mahal dan beresiko munculnya
pencemaran yang baru akibat kelebihan basa. Disamping itu, upaya pengurangan
kandungan besi (Fe) di dalam pengolahan air limbah industri sarung tangan karet sampai
saat ini masih belum diusahakan, oleh karena itu perlu dilakukan pengolahan terhadap
limbah sarung tangan karet yang lebih ramah dan lebih ekonomis. (Kresnawati,2007)
Zeolit merupakan bahan galian non logam atau mineral industri multi guna karena
penyaring molekul dan sebagai katalisator. Sifat zeolit alam sebagai penyerap,
dikarenakan mineral ini merupakan kelompok alumino silikat terhidrasi dengan unsur
utama terdiri dari kation alkali dan alkali tanah, mempunyai pori-pori yang dapat diisi
oleh molekul air. Molekul air ini sifatnya labil atau mudah terlepas, sehingga dengan
pemanasan daiatas 1000C, air pori tersebut dapat dilepas, sehingga terbentuk pori-pori zeolit yang dapat memungkinkan zeolit dapat menyerap molekul-molekul yang
mempunyai ukuran yang lebih kecil dari pori-pori zeolit tersebut.
Zeolit terdapat di beberapa daerah di Sumatera Utara yang diperkirakan
mempunyai cadangan zeolit yang berpotensi untuk dikembangkan manfaatnya, misalnya:
Kabupaten Tapanuli Utara (Sarulla), Kabupaten Dairi, dan Kabupaten Tobasa.
(http://www.tekmira.esdm.go.id/data/Zirkon/ulasan)
Penggunaan zeolit aktif sebagai penyerap telah banyak dilakukan dalam
penelitian sebelumnya, yaitu diantaranya: “Studi pemanfaatan Zeolit Alam Sebagai
Penyerap pada Proses Deionisasi Logam Besi dalam Minyak Nilam” ( skripsi Aksa Chrisna, Jurusan Kimia, FMIPA USU, 1996); “Perbandingan Ketelitian Hasil Penentuan Kadar Logam Ca dalam Batuan Zeolit Alam dengan Metode SSA” ( skripsi Esniwati,
terhadap struktur zeolit” (Skripsi Anita Sipayung, Jurusan Kimia, FMIPA USU, 1994). Hasil penelitiannya menunjukkan bahwa pada pemanasan zeolit alam Sarulla diatas
3000C menyebabkan destruksi struktur zeolit sehingga kehilangan sifat-sifatnya.
Dengan latar belakang hasil penelitian diatas penulis tertarik meneliti daya serap
zeolit aktif terhadap Fe dan Zn di dalam air limbah industri sarung tangan karet
1.2.Permasalahan
Berapakah suhu aktivasi dan dosis optimum zeolit yang digunakan sebagai adsorben,
sehingga kandungan Zn dan Fe didalam limbah cair industri sarung tangan karet
dapat diturunkan sampai jumlah seminimal mungkin.
1.3.Pembatasan Masalah
1. Penelitian ini dibatasi pada penentuan kandungan logam seng (Zn) dan besi (Fe)
didalam limbah cair industri sarung tangan karet sebelum dan sesudah
penambahan zeolit aktif.
2. Aktivasi zeolit dilakukan dengan menggunakan HCl 15%, kemudian dilanjutkan
dengan pemanasan, dengan variasi suhu 1500C, 2000C, 2500C, 3000C, dan 3500C. 3. Variasi dosis zeolit aktif yang digunakan sebagai penyerap adalah 25 gr, 50 gr, 75
gr, dan 100 gr untuk 100 ml limbah.
1.4.Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui berapakah suhu aktivasi dan dosis optimum
zeolit yang digunakan sebagai adsorben, sehingga kandungan Zn dan Fe didalam
limbah cair industri sarung tangan karet dapat diturunkan sampai jumlah seminimal
mungkin.
1.5.Manfaat Penelitian
Hasil penelitian ini diharapkan dapat digunakan sebagai sumber informasi yang
berguna tentang penggunaan zeolit aktif untuk menurunkan kandungan Zn, dan Fe
1.6.Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Analitik Fakultas Matematika dan
Ilmu Pengetahuan Alam Universitas Sumatera Utara, dan di Laboratorium Uji
Kualitas dan Mutu PT. Asian Agri Tebing Tinggi.
1.7.Metodelogi Penelitian
1. Penelitian ini adalah penelitian yang bersifat purposif.
2. Zeolit diambil secara acak dari Sarulla Kecamatan Pahae, Kabupaten Tapanuli
Utara, sedangkan sampel limbah cair industri sarung tangan karet diambil dari
pabrik sarung tangan karet PT. Maja Agung Binjai.
3. Sampel zeolit diaktivasi dengan metode kimia dan fisika, yaitu dengan
penambahan HCl 15%, diikuti pemanasan pada suhu 1500C, 2000C, 2500C, 3000C, dan 3500C.
4. Sampel limbah cair karet didestruksi dengan metode destruksi basah, dengan
menggunakan HNO3(P) dan HClO4(P).
5. Jumlah zeolit aktif yang ditambahkan ke dalam sampel divariasi yaitu 25 gr, 50
gr, 75 gr, 100 gr untuk 100 ml limbah.
6. Lamanya waktu aktivasi secara kimia dengan menggunakan HCl 15% adalah 24
jam, sedangkan lamanya aktivasi secara fisika (pemanasan) adalah selama 3 jam,
masing- masing untuk suhu aktivasi.
7. Penentuan kandungan seng (Zn) dan besi (Fe) didalam sampel dilakukan dengan
BAB 2
TINJAUAN PUSTAKA
2.1. Lateks
Sejak berabad –abad yang lalu, karet telah dikenal dan digunakan secara tradisional oleh penduduk asli daerah asalnya, yakni Brasil-Amerika Selatan. Akan tetapi meskipun
telah diketahui penggunaannya oleh COLUMBUS dalam pelayarannya ke Amerika
Selatan pada akhir abad ke- 15 dan bahkan oleh penjelah – penjelajah berikutnya pada awal abad ke-16, sampai saat itu karet masih belum menarik perhatian orang –orang Eropa.
Karet tumbuh secara liar dilembah –lembah sungai Amazon, dan secara tradisioanal diambil getahnya oleh penduduk setempat untuk digunakan dalam berbagai
keperluan, antara lain sebagai bahan untuk menyalakan api dan “bola” untuk permainan.
(Setyamidjaja, 1993)
Negara Indonesia merupakan negara produsen karet alam nomor dua didunia
dengan luas tanaman karet kira – kira 2,9 juta Ha dan produksi pertahunnya sekitar 1,1 juta ton. Produksi karet yang telah dipasarkan tersebut dalam bentuk olahyan lateks
pekat (concentrated lateks), Sheet atau Ribbed Smoked Sheet(RSS), karet remah atau
standard Indonesian Rubber (SIR), karet remah atau Standard Indonesian Rubber
(SIR). Lateks merupakan suatu system koloid, dimana partikel karet dilapisi oleh protein
dan fosfolipida yang terdispersi dalam serum. Lateks terdiri dari 25-45% hidrokarbon
karet, dan selebihnya merupakan bahan bukan karet. (Chen,S.F.1979)
2.1.1. Proses Pengolahan Lateks Pekat
1. Senyawa kimia sebagai bahan antikoagulan
Pemakaian bahan antikoagulan harus dibatasi, agar tidak menghabiskan banyak
biaya, dan penambahan bahan koagulan yaitu dosis asam dalam proses pencetakan
dilakukan secara perlahan – lahan karena dapat mempengaruhi proses pengeringan. Bahan yang digunakan sebagai antikoagulan adalah:
a Amoniak (NH4OH)
b Natrium Sulfit(Na2SO3)
c Soda (Na2CO3 dan Na2CO3.10H2O)
2. Senyawa kimia sebagai penggumpal (koagulan)
a Asam Cuka(CH3COOH)
b Asam Formiat (CHOOH)
3. Air Pengolahan
Dalam proses pengolahan karet, air berperan sangat penting dan dibutuhkan dalam
jumlah yang sangat besar.
Syarat – syarat air untuk pengolahan adalah :
- Sebagai bahan pengencer lateks, pelarut dan pengenceran bahan-bahan kimia. - Air harus jernih dan tidak berwarna, tidak boleh mengandung garam –
garam, terutama garam kapur.
- Air untuk pengolahan dipabrik persyaratannya tidak terlalu ketat, akan tetapi tidak boleh mengandung kotoran seperti tanah ataupun pasir.
2.1.2. Proses Pembuatan Sarung Tangan Karet
Sarung tangan karet dibuat dengan cara pembuatan dispersi pemvulkanisasi dari
lateks pekat dengan perlakuan komposisi jumlah bahan pengisi Titanium Oksida dan
Karakteristik sarung tangan karet harus sesuai dengan persyaratan mutu SNI 16 – 2623 – 1992, meliputi tegangan putus 270,1 N/ mm2, perpanjangan putus 801 %, modulus 1,2 N/ mm2, dan ketahanan sobek 680 N/ mm2 .
Adapun yang menjadi bahan – bahan dalam pengolahan lateks pekat menjadi sarung tangan karet adalah lateks pekat dengan kadar karet kering 60% , dan sebagai bahan anti
koagulan adalah NH4OH, Belerang, Texapon 10%, KOH 10%, dan sebagai zat
akseerator adalah ZnO, ZDEC, dan bahan pengisi adalah Titan Oksida, Silikon, dan
Tanin.
2.1.3. Tahap – Tahap Pengolahan Lateks Pekat menjadi Sarung Tangan Karet A. Pembuatan dispersi
1. Bahan – bahan akselerator tersebut dimasukkan dalam sebuah drum yang didalamnya dilengkapi peluru – peluru, kemudian drum ditutup rapat dan diletakkan dalam wadah yang berputar ( gilingan dispersi ) , Dan dibiarkan berputar selama 24 jam.
2. Hasil dispersi dicampurkan kedalam lateks pekat, diaduk sampai merata dan campuran
disimpan selama 3 – 5 hari untuk diperam ( maturing ). Pemeraman bertujuan agar campuran lebih homogen dan terjadi pemvulkanisasian.
3. Untuk mengetahui tahap vulkanisasi periksa campuran dengan memipet 10 ml
campuran dan tambahkan Chlorofom sambil diaduk 5 menit, dan gumpalan diperiksa.
B. Persiapan Cetakan
1. Pencelupan dengan asam, untuk membersihkan cetakan ( acid washing dip )
2. Pembilasan cetakan ( Formers drying)
3. Pencelupan cetakan kedalam larutan koagulan ( Coagulan dip)
C. Proses Pencetakan Sarung Tangan Karet
1. Pencelupan cetakan kedalam larutan koagulan ( coagulant dip ), proses pencelupan
dilakukan 2 kali
2. Pengeringan, untuk mengeringkan lapisan karet agar ketebalan merata
3. Penggulungan ( beading ), ujung dari sarung tangan harus digulung agar sarung tangan
karet pada waktu dimasuki tidak robek.
4. Pencucian ( leaching )untuk membersihkan kotoran, maupun sisa – sisa bahan kimia. 5. Pemberian powder agar sarung tangan tidak lengket
6. Vulkanisasi ( Curing ), yaitu pemasakan / vulkanisasi pada suhu 100 – 1200C selama ± 40 menit
7. Stripping, yaitu sarung tangan dilepas dari cetakan
8. Pembersihan powder, yaitu mengurangi tepung yang berlebihan
9. Sortasi, yaitu untuk melihat ada kebocoran ( pin holes ), testing dengan tekanan udara.
“Balai Riset Industi dan Standarisasi Vol III. No 2”
2.2. Sifat Kimia Air Limbah
Kandungan Bahan kimia yang ada dalam limbah cair dapat merugikan lingkungan
melalui berbagai cara. Bahan organik terlarut dapat menghabiskan oksigen dalam limbah
serta akan menimbulkan rasa dan bau yang tidak sedap pada penyediaan air bersih. Hal
yang lebih berbahaya adalah jika bahan organik yang terlarut bersifat toksik.
Bahan kimia yang ada dalam limbah cair umumnya dapat diklasifikasikan sebagai
bahan organik (protein, karbohidrat, lemak, minyak, detergen atau surfaktan, fenol) dan
bahan anorganik (sulfur, logam berat, nitrogen, gas). Kandungan logam Zn dalam air
limbah terbawa dari penambahan Zn0 dalam proses akselerator lateks pekat dengan bahan
dalam air limbah dapat terkandung dalam air bekas pencucian selama proses pengolahan
lateks pekat menjadi sarung tangan karet.
Air limbah sangat berbahaya bagi kesehatan manusia karena air limbah tersebut
dapat menjadi sumber penyakit disentri, kolera, antraks, dan lain – lain. Air limbah juga dapat mengganggu kenyamanan baik dari estetika dan bau yang ditimbulkan.
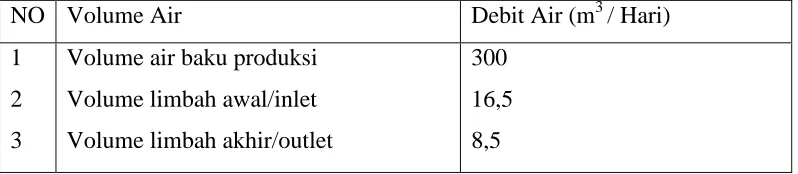
Tabel 2.2. Volume Penggunaan Air oleh Industri Sarung Tangan Karet
NO Volume Air Debit Air (m3 / Hari)
bahan organik dan anorganik serta mikroba sehingga diperkirakan dapat mengganggu
ekosistem perairan. Kualitas dan kuantitas air limbah dari industri karet ini sangat
bergantung pada jenis aktivitas dan besar kecilnya industri.
Pada umumnya air limbah industri ini berasal dari :
1. Air hasil proses produksi
2. Air hasil pencucian alat-alat, mesin, wadah, dan lain – lain 3. Air hasil proses pemanasan dan pendinginan
4. Air hasil laboratorium pengendalian mutu
Limbah industri yang dibuang tanpa diolah terlebih dahulu akan menimbulkan
pencemaran dan gangguan terhadap kesehatan manusia, keseimbangan lingkungan /
2.3. Logam
Logam menurut pengertian awam adalah barang yang padat dan berat yang
biasanya selalu digunakan oleh orang untuk alat-alat dapur atau untuk perhiasan, yaitu
besi, baja, emas, dan perak. Padahal masih banyak logam lain yang penting dan sangat
kecil serta berperan dalam proses biologis makhluk hidup misalnya selenium, kobalt,
mangan dan lain-lainya. (Vogel, A.I. 1979)
Logam berat dalam air limbah merupakan penyebab pencemaran lingkungan yang
potensial. Pencemaran logam berat pada umumnya berasal dari industri penyepuhan
logam, tekstil, barang jadi lateks, serta industri lain. Pada proses industri barang jadi
lateks, seperti sarung tangan digunakan logam berat dalam bentuk ZnO sebagai
akselerator proses vulkanisasi karet. Sehingga kemungkinan besar ion Zn2+ terbawa dalam air limbah industri sarung tangan tersebut.
“Balai Riset Industi dan Standarisasi Vol III. No 2”
2.4. Seng (Zn)
Seng (Zn) merupakan logam yang memiliki karakteristik cukup reaktif, berwarna putih
kebiruan, pudar bila terkena uap udara, dan terbakar bila terkena udara dengan api hijau
terang. Zn dapat bereaksi dengan asam dan basa, dan senyawa nonlogam. Zn memiliki
nomor atom 30 dan memiliki titik lebur 419,730 C.
Kadar Zn meningkat saat kontak dengan pipa plastik atau perabot yang
digalvanisasi. Zn diatmosfer meningkat sesuai dengan meningkatnya kegiatan industri
dan konsentrasi tinggi Zn ditemukan didaerah industri. Konsentrasi Zn dalam air laut
2.4.1. Manfaat Logam Seng(Zn)
a. Manfaat Sebagai Mikroelemen Tubuh
Zn dapat mempengaruhi proses metabolisme sel. Zn berperan dalam fungsi syaraf dan
reproduksi. Peran Zn dalam tingkat seluler, antaralain katalitik, struktur, dan pengaturan.
Peran Zn dalam proses katalitik, yaitu hampir 100 jenis enzim memiliki
kemampuan katalisator dalam reaksi kimia tergantung pada Zn. Zn berperan penting
dalam menyusun struktur protein dan membran sel. Kadar Zn ditemukan dalam semua
bagian tubuh manusia, 60% terdapat di otot, 30% terdapat di tulang, dan 5% terdapat di
kulit.
b. Manfaat Zn dalam Berbagai Jenis Industri
1. Sebagai akseleraor atau pengikat antara zat anti koagulan, bahan pengisi,
dengan lateks pekat.
2. Melapisi baja atau besi, guna mencegah korosi
3. Bahan tabung baterai
4. Bahan alloy seperti kuningan, nikel-perak, logam mesin ketik, dan bahan
penyepuhan listrik
5. Pembuatan uang sen Amerika sejak tahun 1982
6. Pelapisan cat khususnya dalam bidang industri automobile, digunakan untuk
pembuatan pipa rangka bangunan. (Widowati, 2008)
2.5. Besi (Fe)
Besi (Fe) merupakan logam transisi dan memiliki nomor atom 26. Bilangan oksidasi Fe
adalah +3 dan +2. Fe memiliki berat atom 55,845 g/mol, titik leleh 1.5380C, dan titik didih 2.8610C. .
Fe menempati urutan sepuluh besar sebagai unsur dibumi. Fe menyusun 5 – 5,6% dan kerak bumi dan menyusun 35% dari masa bumi. Fe menempati berbagai
lapisan bumi. Konsentrasi tertinggi terdapat pada lapisan dalam dari inti bumi dan
sejumlah kecil terdapat di lapisan terluar kerak bumi. Beberapa tempat di bumi biasanya
2.5.1. Manfaat Logam Fe
Hampir 90% Fe dalam tubuh hewan berikatan dengan protein, tetapi yang terpenting ialah
ikatannya dengan hemoglobin (Hb). Hb ini mengandung besi 3,4g/kg. Besi juga terdapat
dalam serum protein yang disebut “transferin” yang berperan dalam menstransfor besi
dari jaringan satu ke jaringan lain. Feritin adalah protein yang mengandung besi 200 gr/
kg ditemukan dalam limpa, hati, ginjal, dan sumsum tulang yang merupakan penyediaan
(deposit) dalam tubuh hewan.
Besi berperan dalam aktivitas beberapa enzim seperti sitokrom dan flavoprotein.
Wanita hamil memerlukan zat besi tambahan untuk menstabilkan kebutuhan Fe yang
hilang. Karena Fe pada wanita hamil diperlukan untuk mencukupi kebutuhan sel darah
yang membesar selama kehamilan dan juga untuk kebutuhan fetus dan plasenta. Kenaikan
kebutuhan Fe ini terjadi pada masa awal sampai pertengahan masa kehamilan, pada saat
fetus tumbuh dengn cepat dan kebutuhan Fe dapat mencapai 7-8 mg/hari. Total
kebutuhan Fe selama masa kehamilan diperkirakan mencapai 1000 mg. (Darmono, 2001)
2.6. Toksisitas Logam Berat
Toksisitas logam pada manusia menyebabkan beberapa akibat negatif, tetapi yang
terutama adalah timbulnya kerusakan jaringan, terutama jaringan detoksikasi dan ekskresi
(hati dan ginjal). Beberapa logam memiliki sifat karsinogenik (pembentuk kanker),
maupun teratogenik (salah bentuk organ). Daya toksisitas ini dipengaruhi oleh beberapa
faktor yaitu kadar logam yang termakan, lamanya mengkonsumsi, umur, spesies, jenis
kelamin, kebiasaan makan makanan tertentu, kondisi fisik, dan kemampuan jaringan
tubuh untuk mengakumulasi logam. Beberapa logam toksik dapat menyerang saraf
sehingga dapat menyebabkan kelainan tingkah laku.
Toksisitas logam pada manusia kebanyakan terjadi karena logam berat
nonesensial saja, walaupun tidak menutup kemungkinan adanya keracunan logam
esensial yang melebihi dosis. Toksisitas logam esensial kadang-kadang dijumpai pada
manusia, tetapi hanya terbatas pada logam tertentu saja, misalnya, Cu, Zn, dan Se.
2.7. Spektrofotometer Serapan Atom
Ada banyak sekali instrumen untuk mengukur penyerapan radiasi, dan sangat penting
untuk mengetahui sifat-sifat dari berbagai instrumen yang berbeda. Fotometer
merupakan instrument yang didisain untuk mengukur intensitas cahaya, dan biasanya
dilakukan dengan membandingkan intensitas tersebut dengan intensitas dari beberapa
sumber referensi radiasi. Spektrofotometer merupakan instrumen yang dapat membagi
peristiwa radiasi ke dalam spektrum dan digunakan untuk mengenal panjang gelombang
yang ada. Spektrofotometer merupakan instrumen yang menggabungkan dua fungsi,
yakni sebagai penghasil radiasi pada panjang gelombang tertentu dan sebagai
pengukuran intensitas radiasi tersebut. (Holme,D.J. 1983)
Spektrofotometri Serapan Atom (SSA) adalah spektrofotometri atom yang lebih
melibatkan proses penyerapan panjang gelombang yang dipancarkan oleh suatu unsur
atom yang dilewatkan melalui gas pembakar. Dalam beberapa tahun terakhir ini, SSA
telah menjadi salahsatu teknik analisis yang banyak digunakan. Kenyataannya, kita dapat
mengatakan bahwa SSA digunkan untuk menganalisa unsur anorganik. Sementara
kromatografi gas digunakan digunakan untuk analisa senyawa organik. (Kennedy,
J.H.1990)
2.7.1. Prinsip Dasar Spektrofotometer Serapan Atom
Spektroskopi atom didasarkan pada peristiwa absorpsi, fluoresensi, dan emisi. Namun
hanya absorpsi dan fluoresensin yang umumnya digunakan untuk spektroskopi molekular.
Alasan mengapa metode emisi tersebut. (Skoog, D.A. 1992)
Spektrofotometri serapan atom didasarkan pada kemampuan atom-atom pada
suatu unsur untuk dapat mengabsorpsi energi sinar matahari pada panjang gelombang
tertentu. Banyak energi sinar yang diabsorpsi berbanding lurus dengan jumlah atom-atom
yang mengabsorpsi. Atom terdiri dari inti atom yang mengandung proton bermuatan
positif, dan neutron berupa partikel yang netral, dimana inti atom dikelilingi oleh
elektron-elektron yang bermuatan negatif pada tingkat energi yang berbeda-beda. Jika
atom mengabsorpsi energi, maka elektron pada kulit terluar (elektron valensi) akan
state) ke keadaan tereksitasi dengan tingkat energi tang lebih tinggi (excited state).
Jumlah energi yang dibutuhkan untuk memindahkan elektron ketingkat energi tertentu
dinyatakan sebagai potensial eksitasi untuk tingkat energi tersebut, dimana pada waktu
kembali pada keadaan dasar, elektron melepaskan energi sebagai energi panas ataupun
energi sinar. (Clark, D.V. 1979)
2.7.2. Instrumentasi
Setiap alat SSA terdiri atas tiga komponen berikut :
a. Unit atomisasi
b. Sumber radiasi
c. Sistem pengukur fotometrik
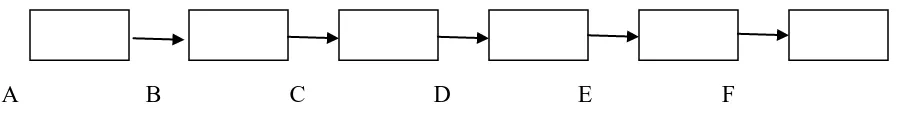
A B C D E F
Gambar 2.1. Skematis ringkas Spektrofotometer Serapan atom
Keterangan :
A : Lampu katoda berongga
B : Chopper
C : Tungku
D : Monokromator
E : Detektor
F : Meter bacaan nilai absorbansi
Atomisasi dapat dilakukan baik dengan nyala maupun dengan tungku. Untuk mengubah
unsur metalik menjadi uap atau hasil disosiasi diperlukan energi panas. Temperatur harus
Bahan bakar dan gas oksidator dimasukkan dalam kamar pencampur kemudian
dilewatkan melalui baffle menuju ke pembakar. Nyala akan dihasilkan. Sampel dihisap
masuk ke dalam kamar pencampur. Hanya tetesan kecil yang dapat melalui baffle.
Dengan gas asetilen dan oksidator udara tekan, temperatur dapat dikendalikan secara
elektris. Biasanya temperatur dinaikan secara bertahap, untuk menguapkan dan sekaligus
mendisosiasikan senyawa yang dianalisis. (Khopkar, S.M. 1990)
2.7.3. Gangguan Pada SSA dan Cara Mengatasinya
Gangguan nyata pada SSA adalah seringkali didapatkan suatu hasil yang tidak sesuai
dengan konsentrasi sampel yang ditentukan. Penyebab dari gangguan ini adalah faktor
matriks sampel, faktor kimia adanya gangguan molekuler yang bersifat radiasi.
Sampel dalam bentuk molekul karena disosiasi yang tidak sempurna akan
cenderung mengabsorpsi radiasi dari sumber radiasi. Demikian juga terjadinya ionisasi
atom akan menjadi sumber kesalahan pada SSA oleh karena spektrum radiasi oleh ion
jauh berbeda dengan spektrum absorpsi atom netral yang memang akan ditentukan. Ada
beberapa usaha untuk mengurangi gangguan kimia pada SSA yaitu dengan jalan:
1. Menaikkan temperatur nyala agar mempermudah penguraian untuk itu dipakai gas
pembakar campuran C2H2 + N2O yang memberikan nyala dengan temperatur yang tinggi.
2. Menambahkan elemen pengikat gugus atom penyangga, sehingga terikat kuat akan
tetapi atom yang ditentukan bebas sebagai atom netral. Misalnya, penentuan logam
yang terikat sebagai garam, dengan penambahan logam, yang lainnya akan terjadi
ikatan lebih kuat dengan anion pengganggu.
3. Pengeluaran unsur pengganggu dari matriks sampel dengan cara eksitasi.
2.8. Zeolit
2.8.1. Pengenalan Zeolit
Zeolit adalah senyawa zat kimia alumino-silikat berhidrat dengan kation natrium, kalium
dan barium. Secara umum, Zeolit memiliki melekular sruktur yang unik, dimana atom
silikon dikelilingi oleh 4 atom oksigen sehingga membentuk semacam jaringan dengan
pola yang teratur. Di beberapa tempat di jaringan ini, atom Silikon digantikan dengan
atom Aluminium, yang hanya terkoordinasi dengan 3 atom Oksigen. Atom Aluminium
ini hanya memiliki muatan 3+, sedangkan Silikon sendiri memiliki muatan 4+.
Keberadaan atom Aluminium ini secara keseluruhan akan menyebababkan Zeolit
memiliki muatan negatif. Muatan negatif inilah yang menyebabkan Zeolit mampu
mengikat kation.
Mineral zeolit terdiri dari zeolit alam dan zeolit sintetis, zeolit alam pertama kali
ditemukan pada tahun 1756 oleh Baron Axel Fredrick Cronstedt (ahli mineralogi
Swedia), sedangkan zeolit sintetis pertama kali ditemukan pada tahun 1948 oleh Richard
Barrer.
Secara umum, zeolit mempunyai kemampuan untuk menyerap molekul,
menukar ion, dan menjadi katalis, hal inilah yang membuat zeolit dapat
dikembangkan untuk keperluan industri. Hingga saat ini zeolit sintetis terus
dikembangkan, hal ini dengan pertimbangan zeolit ini memiliki sesuatu yang lain
dibandingkan dengan material oksida anorganik yang lain, yaitu karena kombinasi
dari berbagai sifat, antara lain karakter pori-pori mikro dari dimensi pori-pori yang
seragam, sifat pertukaran ion, kemampuan untuk membuat keasaman internal, dan
stabilitas dalam suhu yang tinggi. Hal inilah yang membuat zeolit menjadi unik
dibanding oksidaan organik yang lain. Karena sifat yang dimiliki maka zeolit
sintetis yang berkemampuan lebih baik dikembangkan dari zeolit alam, sehingga
zeolit ini akan menjadi suatu alternatif bahan pengolah limbah yang
Zeolit juga sering disebut sebagai 'molecular sieve' / 'molecular mesh' (saringan
molekuler) karena zeolit memiliki pori-pori berukuran melekuler sehingga mampu
memisahkan/menyaring molekul dengan ukuran tertentu.
(www.iqmal@ugm.ac.id, 2009)
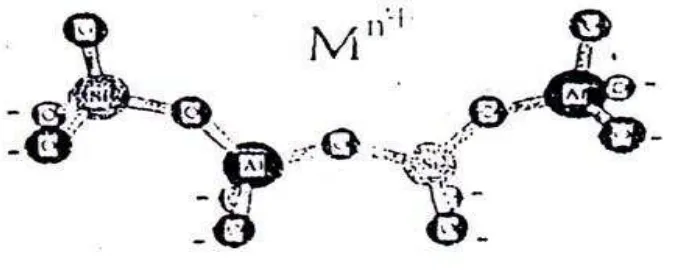
2.8.2. Struktur Zeolit
Kerangka dasar struktur zeolit terdiri dari unit-unit tetrahedral [AlO
4] dan [SiO4] yang saling berhubungan melalui atom O.
Gambar Kerangka Utama Penyusun Zeolit
Dalam struktur tersebut Si 4+
dapat diganti Al 3+
, sehingga rumus umum komposisi
zeolit dapat dinyatakan sebagai berikut :
M
x/n [(AlO2)x(SiO2)y] m H2O
Dimana : n = Valensi kation M (alkali / alkali tanah)
x,y= Jumlah tetrahedron per unit sel
m = Jumlah molekul air per unit sel
M = Kation alkali / alkali tanah
( Srihapsari, 2006)
2.8.3. Sifat - Sifat Zeolit
Zeolit mempunyai struktur berongga yang biasanya diisi oleh air dan kation yang bisa
Zeolit mempunyai sifat-sifat kimia, diantaranya :
1. Dehidrasi
Sifat dehidrasi zeolit berpengaruh terhadap sifat serapannya. Keunikan zeolit
terletak pada struktur porinya yang spesifik. Pada zeolit alam didalam pori-porinya
terdapat kation-kation atau molekul air. Bila kation-kation atau molekul air tersebut
dikeluarkan dari dalam pori dengan suatu perlakuan tertentu maka zeolit akan
meninggalkan pori yang kosong .
2. Penyerapan
Dalam keadaan normal ruang hampa dalam kristal zeolit terisi oleh molekul
air yang berada disekitar kation. Bila zeolit dipanaskan maka air tersebut akan keluar.
Zeolit yang telah dipanaskan dapat berfungsi sebagai penyerap gas atau cairan .
3. Penukar Ion
Ion-ion pada rongga berguna untuk menjaga kenetralan zeolit. Ion-ion ini
dapat bergerak bebas sehingga pertukaran ion yang terjadi tergantung dari ukuran
dan muatan maupun jenis zeolitnya. Sifat sebagai penukar ion dari zeolit antara lain
tergantung dari sifat kation, suhu, dan jenis anion .
4. Katalis
Zeolit sebagai katalis hanya mempengaruhi laju reaksi tanpa mempengaruhi
kesetimbangan reaksi karena mampu menaikkan perbedaan lintasan molekular dari
reaksi. Katalis berpori dengan pori-pori sangat kecil akan memuat molekul-molekul
kecil tetapi mencegah molekul besar masuk. Selektivitas molekuler seperti ini disebut
molecular sieve yang terdapat dalam substansi zeolit alam .
5. Penyaring / pemisah
Zeolit sebagai penyaring molekul maupun pemisah didasarkan atas perbedaan
bentuk, ukuran, dan polaritas molekul yang disaring. Sifat ini disebabkan zeolit
mempunyai ruang hampa yang cukup besar. Molekul yang berukuran lebih kecil dari
ruang hampa dapat melintas sedangkan yang berukuran lebih besar dari ruang hampa
2.8.4. Aktivasi Zeolit
Proses aktivasi zeolit alam dapat dilakukan dengan 2 cara, yang pertama yaitu secara
fisika melalui pemanasan dengan tujuan untuk menguapkan air yang terperangkap di
dalam pori-pori kristal zeolit, sehingga luas permukaannya bertambah (Khairinal, 2000).
Proses pemanasan zeolit dikontrol, karena pemanasan yang berlebihan kemungkinan akan
menyebabkan zeolit tersebut rusak.
Yang kedua aktivasi zeolit secara kimia dengan tujuan untuk membersihkan
permukaan pori, membuang senyawa pengotor dan mengatur kembali letak atom yang
dapat dipertukarkan. Proses aktivasi zeolit dengan perlakuan asam HCl pada konsentrasi
0,1N hingga 11N menyebabkan zeolit mengalami dealuminasi dan dekationisasi yaitu
keluarnya Al dan kation-kation dalam kerangka zeolit. Aktivasi asam menyebabkan
terjadinya dekationisasi yang menyebabkan bertambahnya luas permukaan zeolit karena
berkurangnya pengotor yang menutupi pori-pori zeolit. Luas permukaan yang bertambah
diharapkan meningkatkan kemampuan zeolit dalam sebagai penyerap. Tingginya
kandungan Al dalam kerangka zeolit menyebabkan kerangka zeolit sangat hidrofilik.
Sifat hidrofilik dan polar dari zeolit ini merupakan. hambatan dalam kemampuanya
sebagai penyerap. Proses aktivasi dengan asam dapat meningkatkan kristalinitas,
keasaman dan luas permukaan .
(Heraldy, 2003) juga mengkaji aktivasi asam terhadap zeolit alam asal Ponorogo
dan Wonosari. Asam yang dipergunakan adalah HCl, HNO
3, H2SO4 dan H3PO4. Hasilnya menunjukkan bahwa perlakuan asam terhadap zeolit alam asal Ponorogo dan Wonosari
meningkatkan daya serap zeolit terhadap limbah cair. Penelitian tersebut menyimpulkan
bahwa perlakuan asam telah berhasil melepaskan alumunium dari kerangka zeolit dan
mampu meningkatkan keasaman zeolit. Peningkatan keasaman zeolit disebutkan mampu
memperbesar kemampuan penyerapan zeolit. Hal itu terjadi karena banyaknya pori-pori
zeolit yang terbuka dan permukaan padatannya menjadi bersih dan luas. (Srihapsari,
2.8.5. Penggunaan Zeolit
1. Bidang peternakan
a. Penggemukan ternak
Sudah banyak laporan penelitian tentang penggunaan zeolit untuk
meningkatkan hasil peternakan. Pada umumnya zeolit yang digunakan adalah
jenis klipnotilolit. Dari sebuah penelitian menunjukkan bahwa peran zeolit
bukan sebagai mineral, tetapi cenderung sebagai penyangga zat- zat makanan
dalam rumen yang dapat meningkatkan efektivitas daya cerna dan
mengakibatkan meningkatnya mutu rasum.
2. Bidang bahan bangunan
Endapan zeolit jenis kabasit dan flipsit sudah dikenal sejak zaman Romawi
sebagai bahan bangunan untuk pembuatan alas jalan, fondasi rumah, saluran air,
jembatan, dan bahan perekat atau plester. Selain itu juga dipakai sebagai ornament
bangunan seperti dinding berukir, patung, dan lain- lain.
3. Bidang Lingkungan
a. Pengolahan air
Air yang dimaksud adalah air yang berasal dari air tanah, air sungai, dan
limbah industri, limbah rumah tangga, dan limbah pertanian. Air kotor ini
mengandung kotoran yang berupa bahan tidak terlarut, bahan terlarut, dan
koloid, sehingga air kotor harus ditangani secara mekanis, kimia maupun
biologi tergantung dari bahan pencemarnya, serta standar air bersih yang
diperlukan.
b. Penanganan limbah radio aktif
Penyerapan Cs137 dan Sr90 dari limbah radioaktif yang berkadar sangat rendah pertama kali dilakukan pada tahun 1960 oleh Armes. Meskipun kadar limbah
radioaktif tersebut sangat rendah, tetapi masih tetap berbahaya bagi mahluk
hidup, terutama manusia.
c. Penanganan udara tercemar
penting dalam udara seperti zat asam. Pencemaran udara yang tinggi akan
membahayakan manusia terutama bila terjadi di dalam ruangan tertutup.
Masalah tersebut dapat diatasi dengan jalan memperkaya zat asam di tempat-
tempat yang kekurangan zat tersebut. Mineral zeolit dapat digunakan untuk
meningkatkan konsentrasi zat asam dalam udara.
4. Bidang industri
Dalam industri kertas, jenis zeolit klioptilolit biasa dipakai sebagai bahan pengisi.
Klipnotilolit yang digunakan harus digerus, dan kotoran yang terikut seperti
oksida besi dan bahan-bahan organik yang dapat menurunkan derjat kecerahan
kertas harus dihilangkan dengan pemucatan.Dalam industri ban digunakan zeolit
sintesis A dan X untuk menjaga agar campuran bahan pembuat ban tidak
mengalami polimerisasi dan juga untuk menyerap komponen gas selama proses
vulkanisasi.dan dalam industri lain seperti industri plastik, industri deterjen, dll.(
BAB 3
METODELOGI PENELITIAN
3.1. Alat - alat
- Spektrofotometer Serapan Atom Perkin Elementer 1300
- Hotplate Fisons
- Botol Akuades
- Oven Yamato
- Tanur Sibata
- Siever (Ayakan) 100 mesh Schichemco
- Timbangan Analitik Shimadzu
- Alu dan Lumpang
- Desikator
- Beaker glass Pyrex
- Labu Erlenmeyer 250 mL Pyrex
- Indikator Universal
3.2. Bahan - bahan
- Limbah cair industri lateks
- Akuades
- HNO3 pekat p.a. (E.Merck)
- HClO4 pekat p.a. (E.Merck
- Zeolit Aktif
- HCl 15%
- Larutan induk logam Seng (Zn) 1000 ppm p.a. (E.Merck)
3.3. Prosedur Penelitian 3.3.1.Penyediaan Zeolit Aktif
Zeolit dikeringkan dalam oven, pada suhu 1100C, kemudian dihaluskan dengan menggunakan alu dan lumpang, kemudian diayak dengan ayakan 100 mesh.
3.3.2 Pengaktifan zeolit
Kedalam 100 gram zeolit 100 mesh ditambahkan 500 mL HCl 15%, diaduk dengan
pengaduk magnit selama 3 jam, kemudian dicuci dengan akuades sampai pH netral, lalu
dikeringkan dalam oven pada suhu 1100C , kemudian dihaluskan kembali dengan alu dan lumpang, dan diaktifkan pada suhu 1500C selama 3 jam, didinginkan dan disimpan dalam desikator. Prosedur yang sama dilakukan untuk suhu aktivasi 2000C, 2500C, 3000C, dan 3500C.
3.3.3 Pembuatan Larutan Induk Zn 1000 ppm
Sebanyak 4,3590 gram kristal ZnSO4.7H2O ditmbang dengan teliti, dan dilarutkan dengan akuades dalam gelas beaker, kemudian dipindahkan secara kuantitatif kedalam labu takar
1000 mL, lalu diencerkan sampai garis tanda dan dihomogenkan.
3.3.3.1 Pembuatan Larutan Standar Zn 100 ppm
Sebanyak 10 mL larutan induk Zn 1000 ppm dimasukkan dalam labu takar 100 mL, lalu
diencerkan dengan akuades sampai garis tanda dan dihomogenkan.
3.3.3.2 Pembuatan Larutan Standar Zn 10 ppm
Sebanyak 10 mL larutan standar Zn 100 ppm dimasukkan dalam labu takar 100 mL, lalu
diencerkan dengan akuades sampai garis tanda dan dihomogenkan
3.3.3.3 Pembuatan Larutan Standar Zn 0,5ppm; 1,0ppm;
1,5ppm
Disediakan 3 labu takar 100 mL, yang bersih dan kering, kemudian ke dalam labu takar
diencerkan dengan akuades sampai garis tanda dan dihomogenkan, sehingga diperoleh
larutan seri standar Zn 0,5 ppm; 1,0 ppm; 1,5 ppm.
3.3.4. Pembuatan Larutan Induk Fe 1000 ppm
Sebanyak 7,0161 gram kristal Fe(NH4)2(SO4)2 . 6H2O ditimbang dengan teliti, dilarutkan ke dalam beaker glass, lalu dimasukkan ke dalam labu takar 1000 mL yang telah berisi
akuades dan 20 mL H2SO4(P), ditambahkan larutan KMnO4 0,1 N sedikit demi sedikit sampai diperoleh larutan merah muda tetap ada, kemudian diencerkan sampai garis
tanda, sehingga diperoleh larutan standar Fe 1000 ppm.
3.3.4.1 Pembuatan Larutan Standar Fe 100ppm
Sebanyak 10 mL larutan induk Fe 1000 ppm dimasukkan dalam labu takar 100 mL, lalu
diencerkan dengan akuades sampai garis tanda dan dihomogenkan.
3.3.4.2 Pembuatan Larutan Standar Fe 5ppm, 10ppm, 15ppm
Disediakan 3 labu takar 100 mL, yang bersih dan kering, kemudian ke dalam labu takar
ini, secara terpisah dipipet sebanyak 5 mL, 10 mL, 15 mL larutan standar Fe 100 ppm
lalu diencerkan dengan akuades sampai garis tanda dan dihomogenkan, sehingga
diperoleh larutan seri standar Fe 5 ppm, 10 ppm, 15 ppm.
3.3.5. Pembuatan Kurva Kalibrasi untuk Zn
Masing – masing larutan seri standar Zn diukur absorbansinya dengan spektrofotometer
serapan atom pada λspesifik = 213,9 nm. Pengukuran dilakukan 3 kali untuk setiap konsentrasi larutan seri standar. Prosedur yang sama dilakukan terhadap akuades bebas
Zn sebagai blanko. ( Hasil dicantumkan pada tabel 1).
3.3.6. Pembuatan Kurva Kalibrasi Fe
Masing – masing larutan seri standar Fe diukur absorbansinya dengan spektrofotometer
serapan atom pada λspesifik = 248,30 nm. Pengukuran dilakukan 3 kali untuk setiap konsentrasi larutan seri standar. Prosedur yang sama dilakukan terhadap akuades bebas Fe
3.3.7. Pengambilan dan Pengawetan Sampel
Disediakan jerigen yang bersih dan kering, kemudian dimasukkan limbah cair industri
lateks kedalam jerigen, kemudian jerigen ditutup dengan rapat. Kemudian disediakan
beaker glass yang bersih dan kering, dan dituang kedalamnya limbah cair industri sarung
tangan karet, lalu ditambahkan HNO3(pekat) sampai pH = 2.
3.3.8. Preparasi Sampel
Dipipet sebanyak 25 mL sampel limbah cair sarung tangan karet, dimasukkan dalam
labu erlenmeyer 100 mL, kemudian ditambahkan campuran 8 mL HNO3(p) dan 2mL HClO4(p), lalu dipanaskan pada suhu 1100C selama 10 menit, didinginkan, kemudian ditambahkan 1mL HNO3(p), dan disaring dengan kertas saring whatman No.42, sehingga diperoleh filtrat berwarna jernih. Filtrat dimasukkan kedalam labu takar 25 mL,
diencerkan dengan akuades sampai garis batas, dan dihomogenkan.
3.3.8.1. Penentuan Kandungan Zn Sebelum Penambahan Zeolit
aktif
Aborbansi Zn didalam larutan diukur dengan Spektrofotometer Serapan Atom pada
λspesifik = 213,9 nm.
3.3.8.2. Penentuan Kandungan Fe Sebelum Penambahan Zeolit
aktif
Aborbansi Fe didalam larutan diukur dengan Spektrofotometer Serapan Atom pada
λspesifik = 248,30 nm.
3.3.8.3. Penyerapan Kandungan Zn dengan Penambahan Zeolit
Aktif
Sebanyak 100 mL limbah dimasukkan dalam beaker glass 250 mL, kemudian
ditambahkan 25 gram zeolit aktif, dan diaduk dengan magnetic stirrer selama waktu 3
Sebanyak 25 mL filtrat dipipet, dan dimasukkan ke dalam labu Erlenmeyer 100 mL,
kemudian ditambahkan campuran 8 mL HNO3(p) dan 2 mL HClO4(p), lalu dipanaskan pada suhu 1100C selama 10 menit, didinginkan, kemudian ditambahkan 1 mL HNO3(p), dan disaring dengan kertas saring whatman No.42, sehingga diperoleh filtrat berwarna
jernih. Filtrat dimasukkan kedalam labu takar 25 mL, diencerkan dengan akuades sampai
garis tanda, dihomogenkan, kemudian diukur absorbansi Zn dengan Spektrofotometer
Serapan Atom pada λspesifik = 213,9 nm. Prosedur yang sama dilakukan dengan penambahan zeolit aktif sebanyak 50 gram, 75 gram, dan 100 gram .
3.3.8.4. Penyerapan Kandungan Fe dengan Penambahan Zeolit
Aktif
Sebanyak 100 mL limbah dimasukkan dalam beaker glass 250 mL, kemudian
ditambahkan 25 gram zeolit aktif, dan diaduk dengan magnetic stirrer selama waktu 3
jam, kemudian disaring dengan kertas saring whatman No.42 dan filtratnya ditampung.
Sebanyak 25 mL filtrat dipipet, dan dimasukkan ke dalam labu Erlenmeyer 100 mL,
kemudian ditambahkan campuran 8 mL HNO3(p) dan 2 mL HClO4(p), lalu dipanaskan
pada suhu 1100C selama 10 menit, didinginkan, kemudian ditambahkan 1 mL HNO3(p), dan disaring dengan kertas saring whatman No.42, sehingga diperoleh filtrat berwarna
jernih. Filtrat dimasukkan kedalam labu takar 25 mL, diencerkan dengan akuades sampai
garis tanda, dihomogenkan, kemudian diukur absorbansi Fe dengan Spektrofotometer
Zeolit
Zeolit 100 mesh
100 gram zeolit 100 mesh
Zeolit Aktif 3.4. Bagan Penelitian
3.4.1. Penyediaan Zeolit Aktif
dikeringkan dalam oven pada suhu 1100C
dihaluskan
diayak dengan ayakan 100 mesh
3.4.2. Pengaktifan Zeolit
ditambahkan 500 mL HCl 15%
diaduk dengan magnetic stirrer selama 3 jam
dicuci dengan akuades sampai pH netral
dikeringkan dalam oven pada suhu 1100C
dihaluskan kembali
diaktifkan pada suhu 1500C selama 3 jam.
didinginkan
disimpan dalam desikator
Larutan Standar Seng 1000 ppm
Larutan Standar Seng 100 ppm
Larutan Standar Seng 10 ppm
Larutan Standar Seng 0,5 ppm; 1,0 ppm; 1,5 ppm
Hasil
3.4.3. Pembuatan Larutan Standar Zn
dipipet sebanyak 10 mL larutan standar seng
dimasukkan ke dalam labu takar 100 mL
diencerkan dengan akuades sampai garis batas
diaduk hingga homogen
dipipet sebanyak 10 mL larutan standar seng
dimasukkan ke dalam labu takar 100 mL
diencerkan dengan akuades sampai garis batas
diaduk hingga homogen
dipipet sebanyak 5 mL,10 mL, 15 mL larutan standar seng
dimasukkan kedalam 3 labu takar 100 mL
diencerkan dengan akuades sampai garis batas
diaduk hingga homogen
diukur absorbansinya dengan Spektrofotometer Serapan
Larutan Standar Besi 1000 ppm
Larutan Standar Besi 100 ppm
Larutan Standar Besi 5 ppm, 10 ppm, 15 ppm
Hasil
3.4.4. Pembuatan Larutan Standar Fe
dipipet sebanyak 10 mL larutan standar besi
dimasukkan ke dalam labu takar 100 mL
diencerkan dengan akuades sampai garis batas
diaduk hingga homogen
dipipet sebanyak 5mL, 10 mL, 15 mL larutan standar besi dimasukkan kedalam 3 labu takar 100 mL
diencerkan dengan akuades sampai garis batas
diaduk hingga homogen
Diukur absorbansinya dengan Spektrofotometer Serapan
25 mL sampel
Larutan sampel
Filtrat
Hasil
Residu 3.4.5. Penentuan Kandungan Zn dan Fe dalam Sampel
dimasukkan dalam labu Erlenmeyer 100 mL
ditambahkan campuran 8 mL HNO3(p) dan 2 mL HClO4(p)
dipanaskan pada suhu 1100C selama 10 menit
didinginkan
ditambahkan 1 mL HNO3(p)
disaring dengan kertas saring whatman No.42
dimasukkan dalam labu takar 25 mL
diencerkan dengan akuades sampai garis batas
100 mL limbah
Filtrat Residu
Larutan Sampel
Filtrat
Hasil
Residu
3.4.6. Penentuan kandungan Zn dan Fe dalam Sampel setelah penambahan zeolit aktif
dimasukkan dalam beaker glass 250 mL
ditambahkan 25 gram zeolit aktif
diaduk dengan magnetic stirrer selama 3 jam
disaring
dipipet sebanyak 25 mL
ditambahkan campuran 8 mL HNO3(p) dan 2 mL HClO4(p)
dipanaskan pada suhu 1100C selama 10 menit
didinginkan
ditambahkan sebanyak 1 mL HNO3 10%
disaring dengan kertas saring whatman No.42
dimasukkan dalam labu takar 25 mL
diencerkan dengan akuades sampai garis batas
BAB 4
HASIL DAN PEMBAHASAN 4.1. Hasil Penelitian
Data hasil pengukuran absorbansi dari suatu seri larutan standar Zn dengan menggunakan
Spektrofotometer Serapan Atom dicantumkan pada Lampiran tabel 1, sedangkan kurva
kalibrasi dicantumkan pada Lampiran gambar 1. Data pengukuran absorbansi Zn dalam
limbah cair sarung tangan karet sebelum dan sesudah penambahan zeolit aktif
dicantumkan pada Lampiran tabel 2, sedangkan data konsentrasi Zn dalam limbah
cair sarung tangan karet sebelum dan sesudah penambahan zeolit aktif dicantumkan pada
Lampiran tabel 3. Data persentase penyerapan kandungan Zn didalam sampel
dicantumkan pada Lampiran tabel 4.
Data pengukuran absorbansi dari suatu seri larutan standar Fe dengan
menggunakan Spektrofotometer Serapan Atom dicantumkan pada Lampiran tabel 5,
sedangkan kurva kalibrasi dicantumkan pada Lampiran gambar 2. Data pengukuran
absorbansi Fe dalam limbah cair sarung tangan karet sebelum dan sesudah penambahan
zeolit aktif dicantumkan pada Lampiran tabel 6, sedangkan data penentuan konsentrasi
Fe dalam limbah cair sarung tangan karet sebelum dan sesudah penambahan zeolit aktif
dicantumkan pada Lampiran tabel 7. Data persentase penyerapan kandungan Fe
didalam sampel dicantumkan pada Lampiran tabel 8.
4.1.1. Penentuan Zn
Penurunan persamaan garis regresi
Data absorbansi yang diperoleh untuk suatu seri larutan standar logam Zn diplotkan
terhadap konsentrasi larutan standar sehingga diperoleh suatu kurva kalibrasi berupa
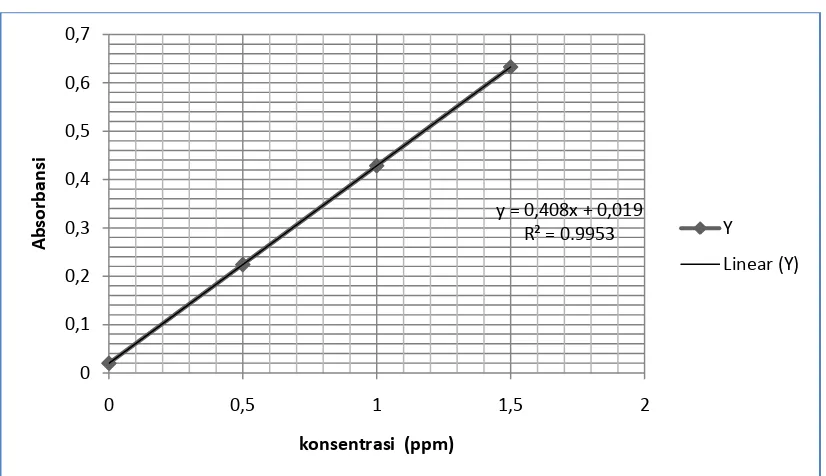
garis linear seperti pada lampiran gambar 1 halaman 46 Persamaan garis regresi untuk
kurva kalibrasi ini dapat diturunkan dengan metode Least Square, dimana konsentrasi
Tabel 4.1.2. Pengolahan Data Absorbansi Zn dengan menggunakan metode Least
Penurunan persamaan garis regresi :
Y = aX + b
Maka persamaan garis regresi adalah :
1. Perhitungan Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan berikut:
r = ∑( �− )( �− )
[∑ �− ∑ �− ) ]½ = ,
, = 0,9953
2. Penentuan Zn didalam sampel sebelum dan sesudah penambahan zeolit aktif dengan variasi suhu aktivasi dan dosis zeolit.
Contoh perhitungan:
- Untuk sampel limbah cair sarung tangan karet sebelum penambahan zeolit aktif
(S0), dengan metode destruksi basah diperoleh serapan (A) sebagai berikut :
A1 = 0,3878
A2 = 0,3910
A3 = 0,4031
Dengan mensubstitusikan nilai Y kepersamaan regresi,
Y = 0,4089X + 0,0196
Maka diperoleh konsentrasi Zn ( FP = 50 ):
X1 = 45,0232
X2 = 45,4145
X3 = 46,8941
Dengan demikian konsentrasi Zn adalah :
X=∑ �� = 137,3318
(X1 – )2 = (45,0203 – 45,7772)2 = 0,5685
(X1 – )2 = (45,4145 – 45,7772)2 = 0,1316
(X1 – )2 = (46,8941 – 45,7772)2 = 1,2475
∑(Xi – )2 = 1,9476
Maka : S = �−
�− =
,
= 0,9868
Didapat harga Sx = � � =
,
= 0,5679
Dari data hasil distribusi t student untuk n = 3, derajat kebebasan (dk) = n – 1 = 2 Untuk derjat kepercayaan 95% ( p = 0,05), nilai t = 4,30
Maka: d = t( P. dk ). Sx
d = 4,30 (0,05. 2) 0,5679
d = 0,2449
Dengan demikian konsentrasi total Zn dalam limbah cair lateks sebelum penambahan
zeolit aktif adalah : 45,7772 ± 0,2449 ppm
- Untuk sampel limbah cair lateks dengan penambahan dosis zeolit 25 gram dan
pemanasan pada suhu 1000C (S100), dengan metode destruksi basah diperoleh
serapan (A) sebagai berikut :
A1 = 0,3786
A2 = 0,3721
A3 = 0,3867
Y = 0,4089 X + 0,0196
Maka diperoleh konsentrasi Zn ( FP = 50 ):
X1 = 43,8983
X2 = 43,1034
X3 = 44,8887
Dengan demikian konsentrasi Zn adalah
� =∑ �
Dengan demikian konsentrasi total Zn dalam limbah cair lateks dengan penambahan dosis
zeolit 25 gram dan pemanasan pada suhu 1000C adalah :
3. Perhitungan jumlah Zn yang terserap
Jumlah Zn yang terserap dihitung dengan menggunakan persamaan:
[Zn] terserap = [Zn] awal – [Zn] sisa
Jumlah Zn yang tersisa yang dihitung seperti dijelaskan pada butir di atas, dicantumkan
pada Lampiran tabel 4.
Data – data ini digunakan untuk menghitung % Zn yang terserap dengan menggunakan persamaan :
% ��= � � � �
� � %
Hasil perhitungan yang diperoleh dicantumkan pada tabel yang sama.
4.1.2. Penentuan Fe
1. Penurunan persamaan garis regresi
Data absorbansi yang diperoleh untuk suatu seri larutan standar logam Fe diplotkan
terhadap konsentrasi larutan standar sehingga diperoleh suatu kurva kalibrasi berupa
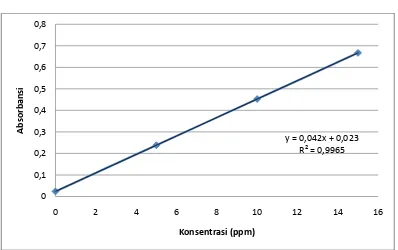
garis linear seperti pada lampiran gambar 2, halaman 50 . Persamaan garis regresi untuk
kurva kalibrasi ini dapat diturunkan dengan metode Least Square, dimana konsentrasi
dinyatakan sebagai Xi dan absorbansi dinyatakan sebagai Yi seperti pada tabel berikut:
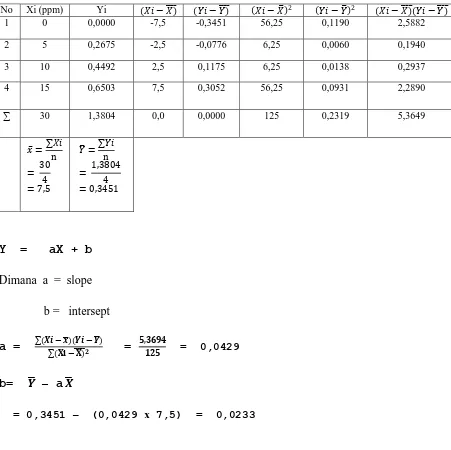
Tabel 4.1.2. Pengolahan Data Absorbansi Fe dengan menggunakan metode Least Square
Maka persamaan garis regresi adalah :
Y = 0,0429X + 0,0233
2. Perhitungan Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan berikut:
r = ∑( �− )( �− )
[∑ �− ∑ �− ) ]½ = ,
, = 0,9965
3. Penentuan Fe didalam sampel sebelum dan sesudah penambahan zeolit aktif dengan variasi suhu aktivasi dan dosis zeolit.
Contoh perhitungan:
- Untuk sampel limbah cair sarung tangan karet sebelum penambahan zeolit aktif
(S0), dengan metode destruksi basah diperoleh serapan (A) sebagai berikut :
A1 = 0,3202
A2 = 0,3311
A3 = 0,3177
Dengan mensubstitusikan nilai Y kepersamaan regresi,
Y = 0,0429 X + 0,0233
Maka diperoleh konsentrasi Fe ( FP = 5 ):
X1 = 34,6035
X2 = 35,8740
Dengan demikian konsentrasi Fe adalah :
penambahan zeolit aktif adalah :
45,7233 ± 0,2061 ppm
- Untuk sampel limbah cair sarung tangan karet dengan penambahan dosis zeolit 25
A1 = 0,3246
A2 = 0,3197
A3 = 0,3218
Dengan mensubstitusikan nilai Y kepersamaan regresi,
Y = 0,0429 X + 0,0233
Maka diperoleh konsentrasi Fe ( FP = 5 ):
X1 = 35,1165
X2 = 34,5450
X3 = 34,7900
Dengan demikian konsentrasi Fe adalah
d = 4,30 ( 0,05. 2 ) 0,1655
d = 0,0711
Dengan demikian konsentrasi total Fe dalam limbah cair sarung tangan karet dengan
penambahan dosis zeolit 25 gram dan pemanasan pada suhu 1000C adalah :
45,7233 ± 0,0711ppm
4. Perhitungan jumlah Fe yang terserap
Jumlah Fe yang terserap dihitung dengan menggunakan persamaan:
[Fe] terserap = [Fe] awal – [Fe] sisa
Jumlah Fe yang tersisa yang dihitung seperti dijelaskan pada butir di atas, dicantumkan
pada Lampiran tabel 8.
Data – data ini digunakan untuk menghitung % Fe yang terserap dengan menggunakan persamaan :
% Fe = �� � � ��
�� � �� 100%
4.2. Pembahasan 4.2.1. Seng (Zn)
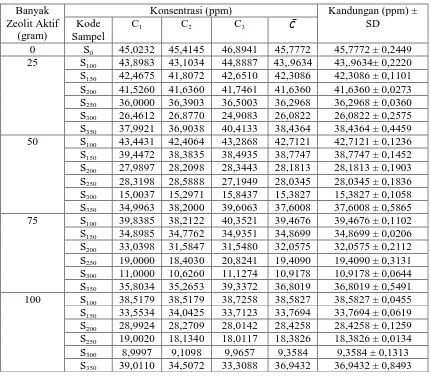
Pada Lampiran tabel 3, dicantumkan penyerapan Zn dalam limbah cair industri
sarung tangan karet dengan penambahan dosis zeolit aktif 25 gram, 50 gram; 75 gram,
dan 100 gram, dengan suhu aktivasi 1000 C, 1500 C, 2000 C, 250, 3000 C; dan 3500 C.
Dari hasil penelitian yang dilakukan diperoleh bahwa konsentrsi Zn menurun
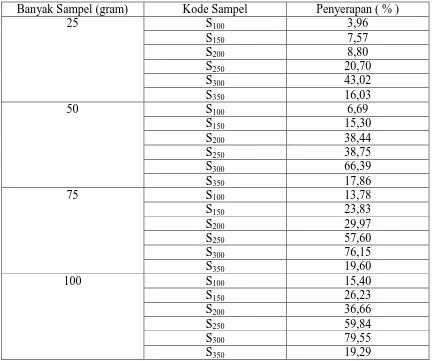
setelah dilakukan penambahan zeolit aktif, dimana penyerapan kandungan Zn paling
tinggi terjadi pada penambahan dosis 100 gram dan dengan suhu pengaktivan 3000C yaitu 79,55 %. Pada dosis penambahan dibawah 100 gram dengan suhu pengaktivan
zeolit dibawah 3000C diperoleh bahwa penyerapan kandungan Zn belum maksimal. Pada suhu pengaktifan diatas 3000C penyerapan kandungan Zn menurun drastis, hal ini dikarenakan pada suhu pengaktifan zeolit diatas 3000C sebagian zeolit mengalami destruksi, dan menyebabkan kemampuan zeolit untuk menyerap berkurang.
4.3.2. Besi
Pada Lampiran tabel 7, dicantumkan penyerapan Fe dalam limbah cair industri sarung
tangan karet dengan penambahan dosis zeolit aktif 25 gram, 50 gram, 75 gram; dan 100
gram, dengan suhu aktivasi 1000 C, 1500 C,2000 C, 250, 3000 C, dan 3500 C.
Seperti halnya Zn, penyerapan Fe dari hasil penelitian yang dilakukan
diperoleh, bahwa konsentrsi Fe menurun setelah dilakukan penambahan zeolit aktif,
dimana penyerapan kandungan Fe paling tinggi terjadi pada penambahan dosis 100 gram
dan dengan suhu pengaktivan 3000C yaitu 87,40%. Pada dosis penambahan di bawah 100 gram dengan suhu pengaktivan zeolit dibawah 3000C diperoleh bahwa penyerapan kandungan Fe juga belum maksimal. Pada suhu pengaktifan di atas 3000C penyerapan kandungan Femenurun drastis, hal ini dikarenakan pada suhu pengaktifan zeolit diatas
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
- Penyerapan Zn dan Fe oleh zeolit alam yang paling optimal adalah pada suhu aktivasi
3000C, dan dosis penambahan zeolit aktif sebanyak 100 gram untuk 100 ml sampel limbah cair sarung tangan karet, dimana penurunan kandungan Zn mencapai 79,55 %,
dan untuk penurunan kandungan Fe mencapai 87,4 %.
- Hasil yang diperoleh menunjukkan bahwa penambahan zeolit aktif kedalam sampel
dapat menurunkan konsentrasi Zn dari 45,7772 ppm menjadi 9,3584 ppm, dan
kandungan Fe dari 34,9298 menjadi 4,3977 ppm. Dibandingkan dengan SK.
Men. KLH. No. 03. Tahun 2010, hasil yang diperoleh telah memenuhi syarat, dan
berada dibawah ambang batas yang telah ditentukan sesuai dengan Surat Keputusan
tersebut diatas.
5.2. Saran
- Sebaiknya dilakukan penelitian daya serap zeolit terhadap kandungan logam dalam
limbah industri lainnya, dengan variasi aktivasi dengan basa.
- Sebaiknya penelitian ini diaplikasikan pada pengolahan limbah cair sarung tangan
DAFTAR PUSTAKA
Chen, S. F. 1979. Composition of Havea Latex Concentrated. Training Manual On Latex Rubber Analysis. Malaya.
Clark, D. V. 1979. Approach to Atomic Absorption Spectroscopy. Sydney-Australia:Anal Chem Consultants Pty. Ltd.
Darmono. 2001. Lingkungan Hidup dan Pencemaran dan Hubungannya dengan Toksikologin Senyawa Logam. Jakarta: UI Press.
Ginting, A., Dian, A. 2007. Karakterisasi Komposisi Kimia,Luas Permukaan Pori Dan Sifat Termal Dari Zeolit Bayah Tasikmalaya Dan Lampung. Serpong: BATAN.
Holme, D. J., Peck, H. 1983. Analytical Biochemistry. New York: Longman Group Limited.
Kennedy, J. H. 1990. Analytical Chemistry Principples. Second Edition. USA: Saunders College Publishing.
Khopkar, S. M. 1990. Konsep Dasar Kimia Analitik. Jakarta: UI Press.
Kresnawati, I.T.P. 2007. Biosorpsi Logam Zn. Indonesia: Balai Penelitian Bioteknologi Perkebunan Indonesia.
Mulja, M. 1995. Analisis Instrumental. Surabaya: Airlangga Press.
Saputra,R. 2008. Pemanfaatan zeolit sintetis sebagai alternatif pengolahan limbah industri. Bandung: Perpustakaan Geologi UGM.
Setyamidjaja, D. 1999. Karet Budidaya dan Pengolahan. Cetakan Keenam. Yogyakarta: Kanisius.
Skoog, D. A., West, D. M., Holler, F. J. 1992. Fundamentals of Analytical Chemistry. Sixth Edition. USA: Saunders College Publishing.
Srihapsari, D. 2006. Penggunaan Zeolit Alam yang Telah Diaktivasi Dengan Larutan HCl untuk Menyerap Logam-Logam Penyebab kesadahan air. Semarang: UNS Press.
Sugiharto. 1997. Dasar-Dasar Pengolahan Air Limbah. Cetakan Pertama. Jakarta: UI Press
Sutarti, M. 1994. Zeolit Tinjauan Literatur. Jakarta : Pusat Dokumentasi dan Informasi Ilmiah.
Vogel, A.I. 1979. Buku Teks Anorganik Kualitatif Makro dan Semimikro. Edisi Kelima. Jakarta: PT Kalman Media Pustaka.
Widowati, W., Sastiono. A., Jusuf.R. 2008. Efek Toksik Logam Pencegahan
Penanggulangan Pencemaran. Yogyakarta: Penerbit Andi.
Tabel 1. Data Absorbansi Larutan standar Zn
Gambar 1. Kurva Kalibrasi Larutan Standar Zn
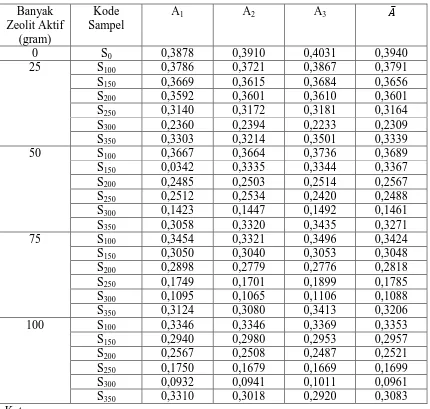
Tabel 2. Data Absorbansi Zn didalam Sampel dengan Variasi Suhu dan Dosis Zeolit Aktif
So = Sampel limbah cair lateks tanpa penambahan zeolit
S100 = Sampel limbah setelah penambahan zeolit aktif dengan pemanasan suhu 1000C
S150 = Sampel limbah setelah penambahan zeolit aktif dengan pemanasan suhu 1500C
S200 = Sampel limbah setelah penambahan zeolit aktif dengan pemanasan suhu 2000C
S250 = Sampel limbah setelah penambahan zeolit aktif dengan pemanasan suhu 2500C
S300 = Sampel limbah setelah penambahan zeolit aktif dengan pemanasan suhu 3000C
Tabel 3. Data Penyerapan Konsentrasi Zn didalam Sampel dengan Variasi Suhu dan Dosis Zeolit Aktif
Banyak Zeolit Aktif
(gram)
Tabel 4. Data Persentase Penyerapan Zn didalam Sampel dengan Variasi Suhu dan Dosis Zeolit Aktif
Banyak Sampel (gram) Kode Sampel Penyerapan ( % )
Tabel 5. Data Absorbansi Larutan standar Fe
Gambar 2. Kurva Kalibrasi Larutan Standar Fe
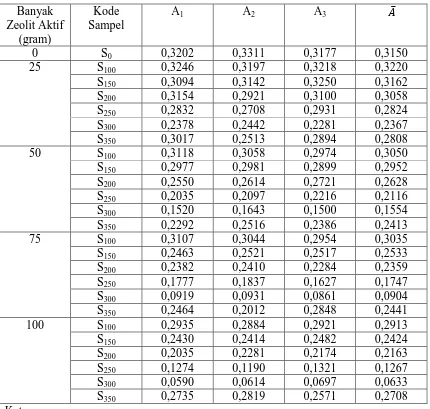
Tabel 6. Data Absorbansi Fe didalam Sampel dengan Variasi Suhu dan Dosis Zeolit Aktif
So = Sampel limbah cair lateks tanpa penambahan zeolit
S100 = Sampel limbah setelah penambahan zeolit aktif dengan pemanasan suhu 1000C
S150 = Sampel limbah setelah penambahan zeolit aktif dengan pemanasan suhu 1500C
S200 = Sampel limbah setelah penambahan zeolit aktif dengan pemanasan suhu 2000C
S250 = Sampel limbah setelah penambahan zeolit aktif dengan pemanasan suhu 2500C
S300 = Sampel limbah setelah penambahan zeolit aktif dengan pemanasan suhu 3000C
Tabel 7. Data Konsentrasi Fe didalam Sampel dengan Variasi Suhu dan Dosis Zeolit Aktif
Banyak Zeolit Aktif
(gram)
Tabel 8. Data Persentase Penyerapan Fe didalam Sampel dengan Variasi Suhu dan Dosis Zeolit Aktif
Banyak Sampel (gram) Kode Sampel Penyerapan ( % )