PENGETSAAN SiO
2BENTONIT ALAM TERPILAR SEBAGAI
KATALIS GAS HIDROGEN DARI AIR
Minto Supeno, Seri Bima Sembiring, Basuki W., H.R. Brahmana
Departemen Kimia FMIPA Universitas Sumatera Utara
Jl. Bioteknologi No. 1 Kampus USU Medan 20155
Abstrak
Berdasarkan analisis, maka bentonit Kecamatan Padang Tualang, Kabupaten Langkat merupakan jenis Na-Bentonit. Bentonit ini dijenuhi dengan larutan Natrium Klorida NaCl 1 M selama 1(satu) hari, tujuannya memperkaya Na-Bentonit. Na-Bentonit selanjutnya diaktivasi menggunakan Asam Sulfat (0,5-2) M selama 24 jam lalu dikeringkan. Material ini didiinterkalasi dan dipilarisasi menggunakan larutan Ti 0,82 M dan dikalsinasi pada suhu 350 oC. Menghasilkan bentonit terpilar TiO2 dan dianalisa menggunakan XRD, FTIR, Luas Permukaan (BET) dan SEM, dari data-data tersebut maka aktivasi untuk bentonit terpilar yang baik pada konsentrasi 1,5 M Asam Sulfat.
Pengetsaan bentonit terpilar TiO2 menggunakan larutan (HNO3/HF/CH3COOH/I2). Maksud pengetsaan ini untuk memperbanyak hole pada jarak antar layer dalam silikat, selanjutnya dipanaskan pada 400-500 oC selama 1 jam. Hasil etsa pada 450oC menghasilkan material luas permukaan terbesar 92,01 m2/g dan volum pori 0,044 cc/g, dan di foto SEM.
Dua bentonit yaitu Bentonit terpilar-TiO2, Bentonit terpilar yang telah dietsa masing-masing 4 gr dimasukkan dalam wadah berisi air 10 ml dan dihubungkan dengan manometer, lalu disinari dengan ultra violet pada panjang gelombang 180 nm untuk dilakukan uji terbentuknya gas hidrogen. Berdasarkan penemuan ini bentonit terpilar yang telah dietsa dapat menghasilkan gas hidrogen dengan total gas 78,5% selama 4 hari penyinaran UV.
Kata kunci:Bentonit Terpilar, Etching, Katalis
PENDAHULUAN
Serbuk fotokatalis semikonduktor telah banyak dipelajari, ditemukan bahwa aktivitas dari fotokatalis ini semakin baik dengan turunnya ukuran partikel yang menyebabkan kenaikkan luas permukaan. Penurunan pada ukuran partikel di bawah antara 5–10 nm menyebabkan perubahan struktur pita energi menjadi semikonduktor yang dikenal sebagai efek samping kwantum. Penelitian lebih lanjut telah dilakukan menghasilkan fotokimia dari berbagai macam ukuran dan bentuk, partikel semikonduktor kolokogenide seperti CdS, ZnS, CdSe, GgSe, ZnSe dan semikonduktor Oksida dari jenis ZnO, Fe2O3,
TiO2 telah banyak digunakan untuk
fotokatalis untuk memproduksi hidrogen dari air (Hirokazu Miyoshi,1989).
Pada penelitian ini dilakukan interkalasi pori-pori bentonit menggunakan TiO2 dan
suhu kalsinasi dari 300–500 oC Untuk menghasilkan bentonit terpilar–TiO2 Bagian
isolator yaitu oksida-oksidanya dapat dietsa untuk menghilangkan oksida-oksida dengan menggunakan campuran HF/H2O/NH4F atau
HF/HNO3/H2O atau dapat juga menggunakan
CF4/H2 yang menghasilkan lapisan silikon
yang bebas dari oksida dan silikon ini selanjutnya dietsa dengan larutan HF/HNO3/CH3COOH/I2 sehingga silikon
akan terlarut. Besarnya luas permukaan yang dihasilkan tergantung waktu yang digunakan untuk mengetsa. Semakin lama waktu digunakan SiO2 atau Si larut semua, hal
demikian tidak diharapkan sehingga waktu yang digunakan untuk mengetsa perlu dikontrol (Wouter I, 1999; SM Sze, 1997).
Jika teknik pengetsaan ini tercapai maka permukaan dan pori-pori bentonit terpilar menjadi lebih besar yang diduga menghasilkan makropori bentonit terpilar. Pemilaran dengan menggunakan TiO2 dan
pengetsaan Silikat bentonit ini dapat mengubah sifat fisik dan kimia, meningkatkan basal spasing (d001), luas
permukaan spesifik, volume total, keasaman permukaan dan menurunkan rerata jejari pori.
Bentonit terpilar TiO2 yang dietsa ini
dapat menjadi katalis dalam proses pembentukan gas hidrogen dari air.
METODE PENELITIAN
Lempung bentonit dengan komposisi SiO2 61,02%; Al2O3 15,21%; Fe2O3 4,89%;
TiO2 0,62%; CaO 2,08%; MgO 1,94%, K2O
0,46%, Na2O 3,45%, hilang pijar 10,31%
Berdasarkan komposisi ini maka bentonit Kecamatan Padang Tualang, Kabupaten Langkat, jenis Na-Bentonit. Bentonit ini diayak hingga lolos ayakan 100 mesh kemudian dicuci dengan akuades beberapa kali dan disaring dengan penyaring vakum dan dikeringkan dalam oven pada temperatur
100oC selama 5 jam, setelah kering lempung bentonit dikeringkan dan digerus sampai halus dan diayak menggunakan ayakan 100 mesh.
Penyediaan Na-Bentonit
Seratus gram lempung bentonit dari (3.3) selanjutnya didispersikan ke dalam 1,5 L larutan NaCl 1M perendaman dilakukan selama 1 minggu di mana setiap dua hari sekali larutan NaCl diganti dengan yang baru. Pada setiap penggantian larutan dilakukan pengadukan selama 24 jam dengan pemanasan 60-70oC selama 4 jam kemudian dilakukan pencucian sampai terbebas dari ion klorida, hal ini dilakukan sampai uji negatif terhadap perak nitrat. Penyaringan dilakukan menggunakan penyaring vakum dan dikeringkan bentonit dalam oven 100oC, setelah kering digerus dan diayak menggunakan ayakan 100 mesh.
Selanjutnya penjenuhan bentonit dilakukan menggunakan NaCl 6 M sambil diaduk selama 24 jam, kemudian disaring dengan penyaring vakum dan dicuci dengan akuades sampai terbebas dari ion klorida hal ini dibuktikan uji negatif terhadap AgNO3.
Selanjutnya dikeringkan dalam oven pada suhu 100oC. Setelah kering digerus sampai halus kemudian diayak menggunakan ayakan 100 mesh. Hasil penjenuhan lempung bentonit ini dinamakan Na-Bentonit.
Aktivasi Na-Bentonit dengan Asam
Masing-masing 35 gram bentonit-Na didispersikan ke dalam 150 ml larutan asam sulfat 0,5; 1; 1,5; 2,0 M sambil diaduk dengan penagaduk magnit selama 6 jam. Aktivasi asam dilakukan selama 24 jam kemudian disaring dengan penyaring vakum dan dicuci dengan akuades panas sampai terbebas dari ion sulfat, hal ini ditunjukkan uji negatif terhadap BaCl2. Na-bentonit
Interkalasi dan Pilarisasi Na-Bentonit
Ditimbang masing-masing 30 gram lempung Na-bentonit lalu didespersikan kedalam 1,5 l air bebas ion (Akuabides) dan diaduk dengan pengaduk magnit selama 6 jam. Kemudian ke dalam masing-masing Na-Bentonit dituangkan sedikit demi sedikit larutan komplek Ti 0,82 M, sambil diaduk dengan pengaduk magnit selama 10 jam. Hasil interkalasi dipisahkan dengan penyaring vakum kemudian dicuci beberapa kali dengan air bebas ion sampai terbebas ion klorida. Pencucian dihentikan jika filtrat diuji dengan perak nitrat tidak membentuk endapan putih. Lempung bentonit yang telah diinterkalasi dengan kompleks Ti dikeringkan dalam oven pada suhu 100oC. Setelah kering digerus sampai halus dan diayak dengan ayakan 100 mesh selanjutnya dikalsinasi pada suhu 350oC (Bask, 1992, Long dan Yang, 1999).
Pengetsaan Bentonit – TiO2
Etching SiO2 dan Si Pada Bentonit
menggunakan larutan Kimia, 20 g Bentonit terpilar ini selanjutnya dilarutkan dengan campuran (28 ml HF + 170 ml H2O + 113 g
NH4F) selama 2- 10 menit tujuan untuk
mengetsa silika, selanjutnya dipisahkan dan sedimen dikeringkan 100 0C dalam kondisi N2. 20 g sedimen selanjutnya direndam
dalam larutan (1 ml HF + 5 ml HNO3 + 2 ml
CH3COOH + 0,3 g I2/250ml H2O) selama 5–
10 menit yang bertujuan mengikis Silikon. Selanjutnya dipanaskan 400-500oC. Dengan teknik demikian akan dihasilkan bentonit terpilar makropori
Pengetsaan Bentonit Terpilar-TiO2 yang
dikalsinasi pada Suhu 400-500 oC
Bentonit Terpilar-TiO2 yang dikalsinasi
pada suhu 400oC diambil sebanyak 35 g, kemudian dimasukkan ke dalam wadah plastik. Selanjutnya ditambahkan larutan pengetsa (campuran antara: 3ml HF(p) + 5ml
HNO3 (p) + 3ml CH3COOH (glasial)/0,3 g I2/250
ml H2O). Kemudian diaduk dengan
menggunakan pengaduk plastik selama 10 menit. Setelah 10 menit, endapan dipisahkan dari larutannya dengan cara dekantasi menggunakan pipet tetes plastik. Endapan yang diperoleh dinetralkan pH-nya dengan menggunakan aqua bidestilata, kemudian didekantasi menggunakan pipet tetes plastik. Endapan yang diperoleh ditanur pada suhu 400, 450, 500 oC selama 1 jam. Kemudian hasilnya dianalisis dengan foto SEM dan Surface Area Analiser.
Pengujian Gas Hidrogen
4 gr bentonit terpilar TiO2 dan bentonit
terpilar TiO2 yang dietsa masing-masing
dimasukkan dalam erlemeyer 25 ml yang telah berisi 10ml air, lalu dihubungkan dengan manometer. Erlemeyer disinari dengan Ultraviolet dengan panjang gelombang 180 nm, penyinaran dilakukan selama 1 minggu. Gas yang terbentuk ditandai bergesernya manometer U.
HASIL DAN PEMBAHASAN
Berdasarkan analisa komposisi bentonit Kabupatan Langkat, maka bentonit di atas termasuk jenis Na-Bentonit atau swelling, bentonit ini seterusnya dikeringkan dalam oven pada 100oC dalam oven dan digerus dan diayak hingga lolos ayakan 100 mesh. Bentonit ini lalu direndam dalam NaCl 1M selama 1 minggu, supaya terjadi pengkayaan Na-bentonit setelah terbentuk natrium bentonit maka dimasukan oven 100 oC sampai kering setelah kering diayak hingga lolos ayakan 100 mesh. Tahap terakhir pengkayaan natrium bentonit dengan mendispersikan larutan NaCL 6 M atau NaCl jenuh selama 24 jam, lalu dicuci dan dikeringkan 100oC, material ini dinamakan Na-Bentonit.
dalam oven, tujuan aktivasi ini adalah meningkatkan jarak antar layer Na-Bentonit sehingga menjadi lebih besar.
Setelah jarak antar layer Na-Bentonit membesar baru dilakakukan interkalasi dan pilarisasi di mana Na-Bentonit teraktivasi didespersikan larutan komplek Ti 0,82 M sambil diaduk dengan pengaduk magnit selama 18 jam. Hasil interkalasi ini dipisahkan dengan pompa vakum, tujuan intekalasi untuk memasukan kompleks Ti kedalam jarak antar layer bentonit, selanjutnya di kalsinasi 350oC untuk membentuk pilar oksida yang lebih kokoh.
Analisa dilakukan dengan difraksi sinar-X, dengan menggunakan metode bubuk yang diradiasikan oleh Cu Kα, masing-masing 2 gram bentonit terpilar TiO2 dan lempung
teraktivasi diisikan ke dalam tempat sampel kemudian dibuat difraktogram dengan
λ=1,5425 A
Berdasarkan hasil pengukuran basal spasing (d001) ada peningkatan basal spacing
pada bentonit terpilar –TiO2 yang
menggunakan aktivasi asam 1M, sedangkan yang menggunakan aktivasi lebih besar 1,5 M bentonit terpilar TiO2 mengalami
kerusakan, hal ini dapat dilihat dari data difraksi sinar X. Peningkatan basal spasing, akan diikuti peningkatan luas permukaan, peningkatan porositas dan volum total.
Gambar 1. Hasil Difraktogram untuk Na-Bentonit
Dari hasil difraktogram Gambar 1, dapat diperoleh informasi bahwa bentonit ini masih
mengandung kaolinit, kuarsa, dan mika. Hal ini dapat dilihat dari Tabel 1 di bawah ini:
Tabel 1. Beberapa Mineral yang Terdapat pada Analisa Difraksi Sinar-X
Jenis mineral d (A) 2- Theta Na-Bentonit 14,91
13,88 4,70 3,04
5,92 6,36 18,84 29,28 Kaolinit 8,27
3,57 2,32
10,68 24,88 38,68
Kuarsa
Mika
4,07 2,51
3,34
21,80 35,68
3,34
Berdasarkan Tabel 1, maka Na-Bentonit ditandai dengan puncak pada 2-theta yaitu: 5,92; 6,36; 18,84; 29,28 dengan basal spacing d (A): 14,91; 13,88; 4,70; 3,04 dan puncak lain merupakan kaolinit, kuarsa, mika artinya bentonit ini belum diperkaya sehingga masih ada pengotornya.
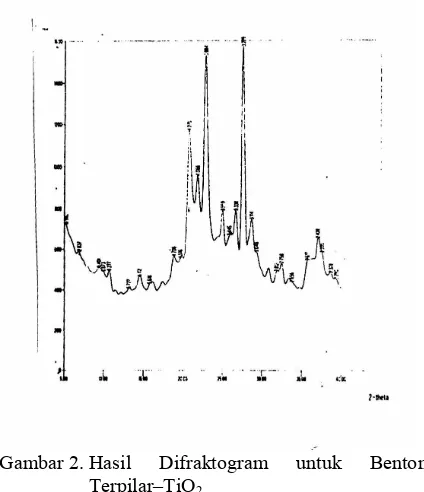
Gambar 2. Hasil Difraktogram untuk Bentonit Terpilar–TiO2
pada sudut 5 theta terjadi perubahan jarak antar lapis dari Na-Bentonit menjadi bentonit terpilar-TiO2 karena pengamatan atau
perubahan bentonit terpilar didaerah sudut theta 0–5. Dari Gambar 1 dan Gambar 2 telah terjadi perubahan puncak intensitas dan berubahnya jarak antar lapis d001.
Dari data difraksi sinar–x di atas (Gambar 1) dan (Gambar 2) dapat ditentukan jarak antar lapis, juga sebagai tanda pengenal dalam mengidentifikasi jenis-jenis mineral liat, untuk menghitung jarak antar lapis (d) mineral bentonit dapat digunakan rumus Bragg:
d = jarak antara bidang-bidang atom kristal
λ = panjang gelombang (1 A = 10-10
m)
θ = Sudut difraksi
n = order difraksi
Jarak antar lapis (d) untuk Na-Bentonit n =1
(b) Bentonit terpilar TiO2 menggunakan
asam sulfat 2,5 M dapat dihitung sebagai berikut:
Selanjutnya perubahan jarak antar lapis (Δd) adalah:
(Δd) = d(b) - d(a)
= 16,980 - 14,916 = 2,0633 A
Berdasarkan analisa difraksi sinar x maka dengan interkalasi dan pilarisasi menambah, meningkatkan porositas dengan basal spasing = 2,06 A.
Tabel 2. Hasil Perhitungan Basal Spacing (d) dari Bentonit Terpilar yang Menggunakan Berbagai Konsentrasi Asam Sulfat
Konsentrasi H2SO4 (M) Basal Spacing d001
Na-Bentonit 14,9167
0,5 M 15,6566
1 M 13,8857
1,5 M 16,8857
2,0 M 9,0554
Berdasarkan data Tabel 2, maka pilarisasi telah berhasil pada konsentrasi 1,5 M H2SO4 dengan d = 16,98039 A, berarti
pilarisasi TiO2 telah meningkatkan jarak
antar lapis sebesar d = 2,0633 A. Selanjutnya dilakukan analisa menggunakan data FTIR dihasilkan sebagai berikut:
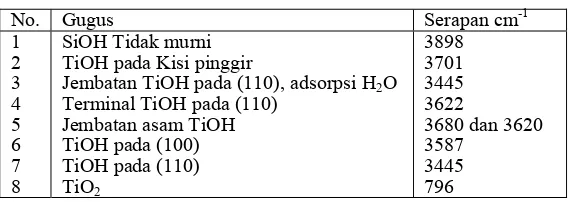
Tabel 2. Analisa Gugus dari FTIR
No. Gugus Serapan cm-1
SiOH Tidak murni TiOH pada Kisi pinggir
Jembatan TiOH pada (110), adsorpsi H2O Terminal TiOH pada (110)
Berdasarkan pengujian penyinaran ultraviolet pada panjang gelombang 180 nm pada wadah yang berisi bentonit terpilar dan bentonit terpilar yang dietsa dihasilkan gas hidrogen dengan total gas 60,4% dan 78,5%.
KESIMPULAN DAN SARAN
Kesimpulan
1. Bentonit terpilar TiO2 dibuat dari jenis
natrium bentonit dapat meningkatkan basal spacing, luas permukaan, volum pori total.
2. Bentonit terpilar TiO2 yang dietsa dapat
sebagai katalis.
Saran
Perlu diteliti gas hidrogen dari air ini dapat digunakan sebagai reaksi reduksi D-glukosa menjadi sorbitol
DAFTAR PUSTAKA
Barrer. R. M., 2002, “Zeolites And Clay Minerals as
Sorbent and Molecular Sieves”, Academic
Press, London.
Cool P., Vansant E.F., 2002, “Pillared Clays: Preparation, Characterization, and
Application”, Laboratory of Inorganic
Chemistry, Department of Chemistry, University of Antwerp (UIA), Belgium, pages: 265-286. http://www.Memsnet.org//mems//beginner/etch. Html,
2004, “Etching Processes”.
http://pearl 1. Lanl.gov/piriodi/elements/14. html, 2004, “Silicon”.
I. Palinko. K Lazar and I Kiricsi, 1999. “Cationic Mixed Pillared Layer Clay: Infrared and Massbouer Characteristics of the Pillaring Agent and Pillared Structures in Fe, Al and Cr, Al Pillared Bentonite”, J of Molecular Structure, 410-411.
Jui–Ming Yeh. Shir–Joe Lou. 2002, “Anticorrosively Enhanced PMMA–Clay Nanocomposite Material with Quaternary Alkylphosphonium Salt as an Intercalating Agent”, Chem. Mater. 14, 154-161.
Kharitonova G.V. Shein E.V. Vityazev V.G. Lapekina C.I. 2004, “Water Vapour Adsorption by Soil Aggregate Fractions”, Journal of International Agrophysics, Vol. 19, pages: 47-52, Russia.
Mihai Palverejem, Yu Liu and Thomas Pinnavaia, 2002 “Aluminated of Porous Clay Hetrostructure (PCH) Assembled from Synthetic Saponite Clay:Porous as Supermicroporous to small mesoporous acid chatalist”, Chem. Mater. 12., 2283-2288. M. H. Al-Qunaibit., W. K. Mekhemer., 2004, “The
Adsorption of Cu (II) Ion on Bentonite–a
Kinetic Study”, J. Colloid And Interface
Science. P 2 (1-6).
Proyek Kerja Dinas Pertambangan Daerah Sumatera Utara, 1999/2000, “Pengukuran Pencadangan Wilayah Pertambangan Bahan Galian Golongan C Komoditi Bentonit di Desa Tapus Kecamatan Saipar Dolok Hole, Kabupaten Tapanuli Selatan”, Medan.