IMUNITAS TERHADAP PENYAKIT
INFEKSI
DISUSUN OLEH :
Dr. SRI AMELIA, M.Kes
NIP. 197409132003122001
DEPARTEMEN MIKROBIOLOGI
FAKULTAS KEDOKTERAN
UNIVERSITAS SUMATERA UTARA
DAFTAR ISI
BAB I Pendahuluan ... 1
BAB II Tinjauan Pustaka Imunologi Infeksi A. Imunitas Terhadap Bakteri ... 3
B. Imunitas Terhadap Virus ... 8
C. Imunitas Terhadap Jamur ... 10
D. Imunitas Terhadap Parasit ... 11
Hipersensitivitas ... 15
Defisiensi Imun ... 20
Pengobatan Defisiensi Imun ... 31
Tekhnik Imunologik : Reaksi Antigen – Antibodi Invitro ... 32
BAB III Kesimpulan ... 35
BAB I PENDAHULUAN
Imunitas adalah resistensi terhadap penyakit terutama penyakit infeksi. Gabungan
sel, molekul dan jaringan yang berperan dalam resistensi terhadap infeksi disebut dengan
sistem imun dan reaksi yang dikoordinasi sel-sel dan molekul-molekul terhadap mikroba
dan bahan lainnya disebut respon imun. Sistem imun diperlukan tubuh untuk
mempertahankan keutuhannya terhadap bahaya yang dapat ditimbulkan berbagai bahan
dalam lingkungan hidup.
Mikroba dapat hidup ekstraseluler, melepas enzim dan menggunakan makanan
yang banyak mengandung gizi yang diperlukannya. Mikroba lain menginfeksi sel inang
dan berkembang biak intraseluler dengan menggunakan sumber energi sel inangnya. Baik
mikroba ekstraseluler maupun intraseluler dapat menginfeksi subyek lain, menimbulkan
penyakit dan kematian, tetapi banyak pula yang tidak berbahaya bahkan berguna untuk
sel inang.
Pertahanan imun terdiri dari sistem imun alamiah atau nonspesifik (native/innate)
dan didapat atau spesifik (acquired/adaptive). Mekanisme fisiologik imunitas nonspesifik
berupa komponen normal tubuh yang selalu ditemukan pada individu sehat dan siap
mencegah mikroba masuk ke tubuh dan dengan cepat menyingkirkan mikroba tersebut.
Jumlahnya dapat ditingkatkan oleh infeksi, misalnya jumlah sel darah putih meningkat
selama fase akut pada banyak macam penyakit. Disebut nonspesifik karena tidak
ditujukan terhadap mikroba tertentu, telah ada dan siap berfungsi sejak lahir. Sistem ini
merupakan pertahanan terdepan dalam menghadapi serangan berbagai mikroba dan dapat
memberikan respon langsung.
Sistem imun nonspesifik terdiri atas pertahan fisik / mekanik yaitu kulit, selaput
lendir, silia saluran nafas, batuk dan bersin. Selain pertahanan fisik juga terdapat
pertahanan biokimia termasuk lisozim, sekresi sebaseus, asam lambung, laktoferin, asam
neuraminik. Kemudian pertahanan humoral (komplemen,interferon dan CRP) serta
pertahan seluler (fagositosis, sel NK, sel mast dan basofil).
Sistem imun spesifik mempunyai kemampuan untuk mengenal benda yang
dikenal oleh sistem imun spesifik sehingga terjadi sensitisasi sel-sel imun tersebut. Benda
asing yang sama bila terpajan ulang akan dikenal lebih cepat, kemudian dihancurkan
olehnya. Oleh karena itu sistem ini hanya dapat menyingkirkan benda asing yang sudah
dikenal sebelumnya, maka sistem itu disebut spesifik. Sistem imun spesifik dibagi dua
kelompok yaitu sistem imun humoral, sel B melepas antibodi untuk menyingkirkan
mikroba ekstraseluler dan sistem imun seluler dimana sel T akan mengaktifkan mikroba
atau mengaktifkan sel Tc (Tcytotoxic) untuk membunuh sel yang terinfeksi.
Pada tulisan ini penulis akan menjelaskan tentang imunitas terhadap infeksi,
reaksi hipersensitivitas, defisiensi imun dan penanggulangannya, serta beberapa teknik
imunologi yang memakai dasar reaksi antigen dan antibodi. Mudah-mudahan apa yang
BAB II
TINJAUAN PUSTAKA
IMUNOLOGI INFEKSI
A. IMUNITAS TERHADAP BAKTERI
Bakteri dari luar yang masuk ke dalam tubuh (ekstraseluler) akan diserang sistem
imun nonspesifik berupa fagosit, komplemen (aktivasi jalur alternatif), protein fase akut
(APP) atau antibodi spesifik yang sudah ada dalam darah akibat pajanan terdahulu
dengan bakteri yang sama akan menetralisasi bakteri. Beberapa bakteri intraseluler
(dalam monosit, makrofag) seperti mikobakteria, L.monositogenes, Salmonella tifi dan
brusella dapat menghindari pengawasan sistem imun antibodi. Dalam hal ini tubuh akan
mengaktifkan sistem imun seluler (CD4+, CD8+ dan sel NK).
Menurut sifat patologik dinding sel, mikroorganisme dapat dibagi menjadi gram
-negatif, gram-positif, mikobakterium dan spirochaeta. Permukaan bakeri yang dilapisi
kapsul yang mengandung protein dan polisakarida, dapat merangsang sistem imun
humoral tubuh untuk membentuk antibodi. Di luar membran plasma, bakteri memiliki
dinding sel yang terdiri dari peptidoglikan. Bagian ini merupakan sasaran lisozim. Pada
bakteri gram-negatif dimana dinding selnya mengandung lapisan lipopolisakarida (LPS
atau endotoksin), lapsan ini menjadi aktivator poten makrofag.
Antibodi yang dibentuk terhadap toksin dapat menetralisasi efek toksin tetanus
dan difteri, sehingga dapat mencegah kerusakan jaringan. Mikroorganisme yang
mengandung lipid pada membran permukaan seperti N.meningitidis gram-negatif, dapat
dihancurkan immunoglobulin dengan aktivasi komplemen melalui jalur lisis. Pada akhir
respon imun, semua bakteri dihancurkan fagosit.
Imunitas Terhadap Bakteri Ekstraseluler
Bakteri ekstraseluler dapat hidup diluar sel pejamu, misalnya dalam sirkulasi,
jaringan ikat dan rongga-rongga jaringan seperti lumen saluran nafas dan saluran cerna.
Bakteri ekstraseluler ini kebanyakan bersifat patogen. Penyakit yang ditimbulkan bakteri
ini berupa inflamasi yag menimbulkan destruksi jaringan tempat infeksi dengan
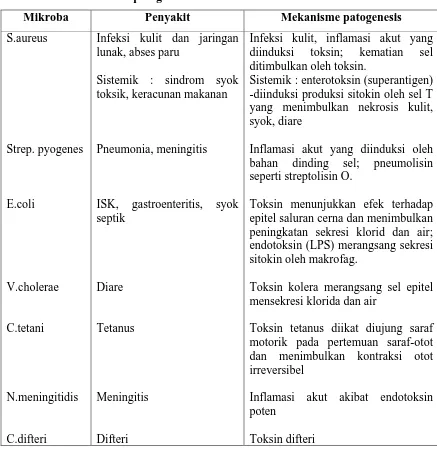
Tabel 1. Contoh mikroba patogen
Mikroba Penyakit Mekanisme patogenesis
S.aureus
Infeksi kulit dan jaringan lunak, abses paru
Sistemik : sindrom syok toksik, keracunan makanan
Pneumonia, meningitis
Infeksi kulit, inflamasi akut yang diinduksi toksin; kematian sel ditimbulkan oleh toksin.
Sistemik : enterotoksin (superantigen) -diinduksi produksi sitokin oleh sel T yang menimbulkan nekrosis kulit, syok, diare
Inflamasi akut yang diinduksi oleh bahan dinding sel; pneumolisin seperti streptolisin O.
Toksin menunjukkan efek terhadap epitel saluran cerna dan menimbulkan peningkatan sekresi klorid dan air; endotoksin (LPS) merangsang sekresi sitokin oleh makrofag.
Toksin kolera merangsang sel epitel mensekresi klorida dan air
Toksin tetanus diikat diujung saraf motorik pada pertemuan saraf-otot dan menimbulkan kontraksi otot irreversibel
Inflamasi akut akibat endotoksin poten
Toksin difteri
1. Imunitas nonspesifik
Komponen utama imunitas nonspesifik terhadap bakteri ekstraseluler adalah
komplemen, fagositosis dan respon inflamasi. Bakteri yang mengekspresikan manosa
pada permukaannya, dapat mengikat lektin yang homolog dengan C1q, sehingga
mengaktifkan komplemen jalur lektin, meningkatkan opsonisasi dan fagositosis.
sampingan aktivasi komplemen berperan dalam mengerahkan dan mengaktifkan leukosit
dalam inflamasi.
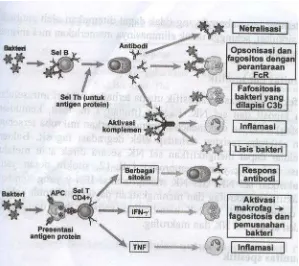
Gambar 1. Respon imun spesifik terhadap mikroba ekstraseluler dan toksinnya
Fagosit juga mengikat bakteri melalui berbagai reseptor permukaan lain seperti
reseptor bangkai (scavenger), Toll-like receptor yang semuanya meningkatkan aktivasi
leukosit dan fagositosis. Fagosit yang diaktifkan juga melepas sitokin yang menginduksi
infiltrasi leukosit ke tempat infeksi (inflamasi). Sitokin juga menginduksi panas dan
sintesis protein fase akut.
2. Imunitas spesifik
Antibodi merupakan komponen imun protektif utama terhadap bakteri
ekstraseluler yang berfungsi untuk menyingkirkan mikroba dan menetralisasi toksinnya.
Komplikasi lambat respon imun humoral ini menimbulkan penyakit yang
berkaitan dengan antibodi. Misalnya infeksi streptokokus di tenggorokan atau di kulit
yang menimbulkan manifestasi klinis. Demam reuma merupakan sekuela infeksi faring
oleh beberapa streptokokus hemolitik-β. Antibodi yang diproduksi terhadap protein
miokard yang dapat diendapkan di jantung dan akhirnya menimbulkan inflamasi
(karditis). Glomerulonefritis pasca infeksi streptokokus merupakan sekuela infeksi
streptokokus dikulit atau tenggorok oleh streptokokus-β tipe lain. Antibodi terhadap
bakteri tersebut membentuk kompleks dengan antigen bakteri dan diendapkan di
glomerulus ginjal menimbulkan nefritis.
Respon utama pejamu terhadap bakteri ekstraseluler adalah produksi sitokin oleh
makrofag yang diaktifkan menimbulkan inflamasi dan syok septik. Toksin berupa
superantigen mampu mengaktifkan banyak sel T sehingga menimbulkan produksi sitokin
dalam jumlah besar.
Imunitas terhadap Bakteri Intraseluler
Ciri utama bakteri intraseluler adalah kemampuannya untuk hidup dan
berkembang biak dalam fagosit. Mikroba tersebut mendapat tempat tersembunyi yang
tidak dapat ditemukan oleh antibodi dalam sirkulasi, sehingga untuk eliminasinya
memerlukan mekanisme imun seluler.
1. Imunitas nonspesifik
Efektor imunitas nonspesifik utama terhadap bakteri intraseluler adalah fagosit
dan sel NK. Fagosit (mulanya monosit, kemudian makrofag) menelan dan mencoba
menghancurkan mikroba tersebut, namun mikroba resisten terhadap efek degradasi
fagosit. Bakteri intraseluler dapat mengaktifkan sel NK secara langsung atau melalui
aktivasi makrofag yang memproduksi IL-12, sitokin poten yang mengaktifkan sel NK.
Sel NK memproduksi IFN-γ yang kembali mengaktifkan makrofag dan meningkatkan
daya membunuh bakteri yang dimakan. Jadi sel NK memberikan respon dini, dan terjadi
interaksi antara sel NK dan makrofag.
2. Imunitas spesifik
Proteksi utama respon imun spesifik terhadap bakteri intraseluler berupa imunitas
selular. Seperti telah diketahui sebelumnya, imunitas seluler terdiri dari dua tipe reaksi
yaitu aktivasi makrofag oleh CD4+Th1 yang memproduksi IFN-γ (DTH) yang memacu
pembunuhan mikroba dan lisis sel terinfeksi oleh CD8+ / CTL.
Makrofag yang diaktifkan sebagai respon terhadap mikroba intraseluler dapat
protein mikroba. CD4+ dan CD8+ bekerjasama dalam pertahanan terhadap mikroba.
Bakteri intraseluler seperti Listeria monocytogenes dimakan makrofag dan dapat hidup
dalam fagosom dan masuk dalam sitoplasma. CD4+ memberikan respon terhadap peptida
antigen MHC kelas II asal bakteri intravesikular, memproduksi IFN-γ yang mengaktifkan
makrofag untuk menghancurkan mikroba dalam fagosom. CD8+ memberikan respon
terhadap peptida MHC kelas I yang berasal dari antigen sitosol dan membunuh sel yang
terinfeksi.
Berbagai mikroba intraseluler seperti M.tuberkulosis mengembangkan berbagai
strategi untuk menghindari eliminasi oleh fagosit. Mikroorganisme yang resisten terhadap
fagosit seperti M.tuberkulosis atau parasit obligat intraseluler seperti M.lepra dikucilkan
makrofag dengan dibentuknya granuloma melalui bantuan sel Th1. Tuberkulosis masih
merupakan ancaman di banyak negara karena timbulnya resistensi terhadap obat-obatan.
Makrofag yang mengenal M.tuberkulosis melalui reseptor Toll-like mengikat lipoprotein
mikobakteri melepas mediator inflamasi seperti IL-12 dan nitrat oksida. Peptida
mikobakteri yang dipresentasikan makrofag memacu respon kuat Th1 yang melepas
IFN-γ yang selanjutnya merangsang makrofag membentuk granuloma selama infeksi primer.
Olehkarena mikobakteri sulit dihancurkan, makrofag mengucilkannya di dalam fagosom.
Pajanan awal dengan M.tuberkulosis menimbulkan infeksi primer. Kebanyakan
M.tuberkulosis ditemukan dalam granuloma. Makrofag matang membentuk sel raksasa
dan sel epiteloid atas pengaruh IFN-γ. Granulomata mengucilkan mikroba dengan baik
sehingga pusatnya menjadi hipoksik dan sel menjadi nekrotik yang menyerupai keju.
Nekrosis dengan perkejuan ini merupakan ciri khas tuberkulosis.
Tabel 2. Mekanisme bakteri menghindari dari efektor imun
Mekanisme menghindari efektor imun Contoh Bakeri ekstraseluler
- Variasi antigenik
- Pencegahan aktivasi komplemen - Resistensi terhadap fagosit - Reactive Oxygen Intermediate Bakteri intraseluler
- Mencegah pembentukan fagosom - Reactive Oxygen Intermediate - Membran fagosom rusak, masuk ke
B. IMUNITAS TERHADAP VIRUS
Virus merupakan obligat intraseluler yang berkembang biak di dalam sel, sering
menggunakan mesin sintesis asam nukleat dan protein pejamu. Dengan reseptor
permukaan sel. Dengan reseptor permukaan sel, virus masuk ke dalam sel dan dapat
menimbulkan kerusakan sel dan berbagai macam penyakit. Hal ini disebabkan karena
replikasi virus yang mengganggu sintesis protein dan fungsi sel normal, efek sitopatik
virus akibat sel terinfeksi dihancurkan dan mati.
Virus nonsitopatik dapat menimbulkan infeksi laten dan DNA virus menetap dalam
sel pejamu dan memproduksi protein yang dapat atau tidak mengganggu fungsi sel.
Sistem imun nonspesifik dan spesifik berperan sebagai efektor dalam usaha mencegah
infeksi dan mengeliminasi sel yang terinfeksi.
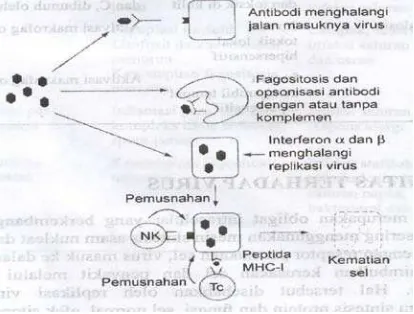
1. Imunitas nonspesifik
Prinsipnya adalah mencegah infeksi. Efektor yang berperan adalah IFN tipe I dan
sel NK yang membunuh sel terinfeksi. Infeksi banyak virus disertai produksi RNA yang
merangsang sekresi IFN tipe I oleh sel yang terinfeksi, melalui ikatan dengan reseptor
Toll-like. IFN tipe I mencegah replikasi virus dalam sel terinfeksi dan sel sekitarnya yang
tidak terinfeksi dengan menginduksi milieu anti-viral.
Sel NK membunuh sel yang terinfeksi oleh berbagai jenis virus dan merupakan
efektor imunitas penting terhadap infeksi dini virus, sebelum respon imun spesifik
berkembang. Sel NK juga dapat mengenal sel terinfeksi yang tidak mengekspresikan
MHC-I.
2. Imunitas spesifik 2.1. Imunitas humoral
Antibodi merupakan efektor dalam imunitas spesifik humoral terhadap infeksi
virus. Antibodi diproduksi dan hanya efektif terhadap virus pada awal infeksi dimana
virus masih terdapat di ekstraseluler sebelum masuk ke sel atau khusus untuk virus
sitopatik, bila virus dilepas oleh sel terinfeksi yang dihancurkan. Antibodi dapat
menetralisasi virus, mencegah virus menempel pada sel dan masuk ke dalam sel pejamu.
Antibodi berikatan dengan envelope virus atau antigen kapsid.
Untuk virus yang masuk ke tubuh melalui mukosa saluran nafas dan saluran
cerna, IgA disekresi untuk melawan virus tersebut. Imunisasi oral terhadap virus polio
bekerja untuk menginduksi imunitas mukosa tersebut. Antibodi juga dapat berperan
sebagai opsonin yang meningkatkan eliminasi partikel virus oleh fagosit. Aktivasi
komplemen juga ikut berperan dalam meningkatkan fagositosis dan mungkin juga
menghancurkan virus dengan envelop lipid langsung.
2.1. Imunitas seluler
Eliminasi virus yang menetap di sel dilakukan oleh sel CD8+/CTL. Fungsi
fisiologik utama CTL adalah memantau infeksi virus. CD8+ mengenal antigen virus yang
sudah dicerna di sitosol, biasanya disintesis endogen yang berhubungan dengan MHC-I
dalam setiap sel yang bernukleus.
Untuk diferensiasi penuh, CD8+ memerlukan sitokin yang diproduksi sel helper
CD4+ atau kostimulator yang diekspresikan pada sel terinfeksi. Bila sel terinfeksi adalah
sel jaringan dan bukan APC, sel terinfeksi dapat dimakan oleh APC profesional seperi sel
dendritik yang selanjutnya memproses antigen virus dan mempresentasikannya ke sel
CD8+. Selanjutnya sel CD8+ berproliferasi secara masif selama infeksi virus dan
kebanyakan sel yang berproliferasi adalah spesifik untuk beberapa peptida virus. Sel T
yang diaktifkan berdiferensiasi menjadi CTL yang membunuh setiap sel bernukleus yang
terinfeksi. Efek antivirus utama CTL adalah membunuh sel terinfeksi, mekanisme lain
melalui aktivasi nuklease dalam sel terinfeksi yang menghancurkan genom virus dan
Mekanisme virus mengindari respon imun : 1. Virus mengubah antigen (mutasi)
Antigen merupakan sasaran antibodi atau sel T yang memiliki jumlah yang
sangat besar terdiri dari strain yang berbeda genetiknya. Hal ini menyebabkan virus
dapat menjadi resisten terhadap respon imun yang ditimbulkan oleh infeksi terdahulu,
misalnya pandemi influenza. HIV-1 yang menjadi penyebab AIDS juga menunjukkan
sejumlah variasi antigen.
2. Virus menghambat presentasi antigen protein sitosolik yang berhubungan dengan molekul MHC-I
Akibatnya sel yang terinfeksi tidak dapat dikenali oleh sel CD8+/CTL. Untuk
keadaan seperti ini, sel NK dapat membunuh sel terinfeksi dengan virus teradaptasi
tersebut, karena sel NK dapat diaktifkan tanpa bantuan molekul MHC-I.
3. Virus memproduksi yang mencegah imunitas nonspesifik dan spesifik
Virus pox menyandi molekul yang dapat mengikat beberapa sitokin seperti IFN-γ,
TNF, IL-1, IL-18 dan kemokin dan molekul-molekul tersebut dapat dilepas oleh sel
terinfeksi dan dapat berfungsi sebagai antagonis sitokin. Virus sitomegalo memproduksi
molekul yang homolog dengan protein MHC-I dan dapat berfungsi kompetitif untuk
mengikat dan mempresentasikan antigen peptida. Virus Epstein-Barr memproduksi
protein homolog dengan sitokin IL-10 (supresif untuk makrofag) sehingga virus dapat
mencegah fungsi makrofag.
4. Virus dapat menginfeksi, membunuh atau mengaktifkan sel imunokompeten 5. HIV dapat tetap hidup dengan menginfeksi dan mengeliminasi sel T CD4+ yang merupakan kunci regulator respon imun terhadap antigen protein.
C. IMUNITAS TERHADAP JAMUR
Respon imun terhadap jamur belum banyak diketahui, namun diduga melibatkan
sel T dan makrofag. Infeksi jamur biasanya hanya mengenai bagian luar tubuh saja.
Tetapi beberapa jamur dapat menimbulkan penyakit sistemik yang berbahaya, biasanya
memasuki paru dalam bentuk spora. Kelainan yang terjadi sangat bergantung dari derajat
dan jenis respon imun pejamu. Gangguan dapat berupa manifestasi di saluran nafas,
namun kebanyakan hanya menimbulkan kesulitan pada pejamu yang
immunokompromais. Neutrofil dan fagosit berperan dalam menyingkirkan infeksi jamur.
Diduga mekanisme proteksi melalui mekanisme selluler, hal ini ditunjang dengan
seringnya penderita HIV menderita infeksi jamur.
Infeksi jamur sering disebut opportunistik, dimana dapat menimbulkan penyakit
berat pada orang-orang yang immunokompromais seperti penderita AIDS, orang yang
mendapat terapi kanker dan penolakan transplantasi yang menekan sumsum tulang dan
respon imun.
1. Imunitas nonspesifik
Efektor utamanya adalah makrofag dan neutrofil. Pasien dengan neutropenia
sangat rentan terhadap infeksi jamur opprtunis. Neutrofil diduga melepas bahan fingisidal
seperti Reactive Oxygen Intermediate dan enzim lisosom serta memakan jamur untuk
dibunuh intraseluler. Kriptokokus neoformans dapat menghambat produksi sitokin TNF
dan IL-12 oleh makrofag dan merangsang produksi IL-10 yang menghambat aktivitas
makrofag.
2. Imunitas spesifik
Cellular Mediated Immunity (CMI) merupakan efektor imunitas spesifik utama
pada infeksi jamur. CD4+ dan CD8+ bekerjasama untuk menyingkirkan Kriptokokus
neoformans yang cenderung mengkolonisasi paru dan otak pada pejamu
immunokompromais. Infeksi Kandida sering mulai pada permukaan mukosa dan CMI
diduga dapat mencegah penyebarannya ke jaringan. Pada semua keadaan tersebut, respon
Th1 adalah protektif sedangkan respon Th2 dapat merusak pejamu.
D. IMUNITAS TERHADAP PARASIT
Golongan parasit berupa protozoa (malaria, tripanosoma, toksoplasma, leishmania
dan amuba), cacing, ektoparasit (kutu, tungau) menunjukkan peningkatan angka
morbiditas dan mortalitas yang bermakna terutama di negara-negara sedang berkembang.
Kebanyakan infeksi parasit bersifat kronis yang disebabkan oleh imunitas nonspesifik
yang lemah dan kemampuan parasit untuk bertahan hidup terhadap imunitas spesifik.
Saat ini banyak antibiotik dan antiparasit yang tidak efektif lagi untuk membunuh parasit,
Vaksin terhadap parasit juga belum berkembang, hal ini disebabkan vaksinasi
sulit memberi proteksi terhadap protozoa karena memerlukan faktor humoral (IgG diduga
berperan penting ) dan seluler. Pada malaria, antibodi diduga protektif mencegah
merozoit memasuki sel darah merah. Imunitas terhadap jenis spesies yang satu tidak
protektif terhadap spesies yang lain.
Tripanosoma terus menerus menguji sistem imun dengan memproduksi pirogen
dan mantel antigen yang berubah-rubah / mutasi sehingga sulit dikenali dan dieliminasi
sistem imun. Toksoplasma melepaskan diri dari efek sistem imun, dapat menutupi diri
dengan laminin dan matriks protein ekstraseluler yang mencegah fagositosis dan
kerusakan oksidatif. Respon seluler terhadap toksoplasma sangat efektif.
Leishmania mempunyai kemampuan menginfeksi makrofag dan memerlukan
respon seluler untuk eradikasinya. IFN-γ yang diperoduksi sel Th1 diduga merupakan
sitokin terpenting untuk membunuh parasit. Sel T, terutama Tc, dapat menghancurkan
parasit intraseluler, misalnya Tripanosoma cruzi. Limfokin yang dilepas oleh sel T yang
disensitisasi dapat mengaktifkan makrofag untuk lebih banyak mengekspresikan
resseptor untuk Fc dan C3, berbagai enzim dan faktor lain yang dapat meningkatkan
sitotoksisitas.
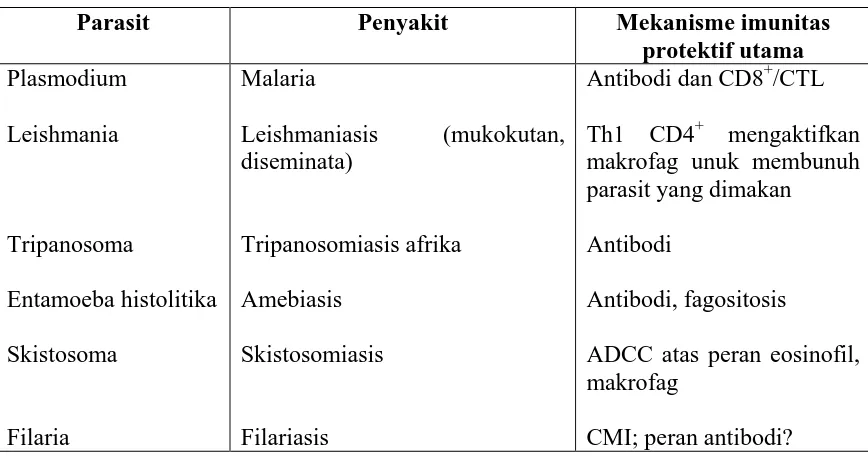
Tabel 3. Respon imun terhadap parasit yang menimbulkan penyakit
Parasit Penyakit Mekanisme imunitas
protektif utama
ADCC atas peran eosinofil, makrofag
1. Imunitas nonspesifik
Protozoa dan cacing mengaktifkan imunitas nonspesifik melalui mekanisme yang
berbeda, mikroba tersebut dapat tetap hidup dan berkembang biak dalam sel pejamu
karena mereka dapat beradaptasi dan menjadi resisten terhadap sistem imun pejamu.
Respon imun nonspesifik terhadap protozoa adalah fagositosis, tetapi banyak
parasit tersebut yang resisten terhadap efek bakterisidal makrofag, bahkan diantaranya
dapat hidup dalam makrofag. Banyak cacing memiliki lapisan permukaan yang tebal
sehingga resisten terhadap mekanisme sitosidal neutrofil dan makrofag. Beberapa cacing
juga mengaktifkan komplemen jalur alternatif. Banyak parasit ternyata mengembangkan
resistensi terhadap efek lisis komplemen.
2. Imunitas spesifik
Berbagai protozoa dan cacing berbeda dalam hal besar, struktur, sifat biokimiawi,
siklus hidup dan patogenitasnya. Hal ini menimbulkan respon imun spesifik yang berbeda
pula. Infeksi cacing biasanya terjadi kronik dan kematian pejamu akan merugikan parasit
sendiri. Infeksi kronik menimbulkan rangsangan antigen yang persisten yang
meningkatkan kadar immunoglobulin dalam sirkulasi dan pembentukan kompleks imun.
Pertahanan terhadap banyak infeksi cacing diperankan oleh aktivasi sel Th2 yang
menghasilkan IgE dan aktivasi eosinofil. IgE yang berikatan dengan permukaan cacing
diikat eosinofil. Selanjutnya eosinofil diaktifkan dan mensekresi granul enzim yang
menghancurkan parasit. Produksi IgE dan eosinofilia sering ditemukan pada infeksi
cacing.
Produksi IgE disebabkan sifat cacing yang merangsang subset Th2 sel CD4+,
yang melepas IL-4 dan Il-5. IL-4 merangsang produksi IgE dan IL-5 merangsang
perkembangan dan aktivasi eosinofil. Eosinofil lebih efektif dibanding leukosit lain
olehkarena eosinofil mengandung granul yang lebih toksik dibanding enzim proteolitik
dan Reactive Oxygen Intermediate yang diproduksi neutrofil dan makrofag. Cacing dan
ekstrak cacing dapat merangsang produksi IgE yang nonspesifik. Reaksi inflamasi yang
ditimbulkan diduga dapat mencegah menempelnya cacing pada mukosa saluran cerna.
Cacing biasanya terlalu besar untuk fagositosis. Degranulasi sel mast/ basofil
yang IgE dependen menghasilkan produksi histamin yang menimbulkan spasme usus
protein kationik, MBP dan neurotoksin. PMN dan makrofag menempel melalui IgA/IgG
dan melepas superoksida, oksida nitrit dan enzim yang membunuh cacing.
Pada filariasis limfatik, sumbatan oleh parasit di saluran limfe menimbulkan CMI
kronis, fibrosis dan akhirnya limfedema berat. Investasi persisten parasit kronis sering
disertai pembentukan kompleks antigen parasit dan antibodi spesifik yang dapat
diendapkan di dinding pembuluh darah dan glomerulus ginjal sehingga menimbulkan
vaskulitis dan nefritis. Penyakit kompleks imun dapat terjadi pada skistosoma dan
malaria.
Pada beberapa kasus, infeksi cacing tidak dapat dihancurkan dengan sistem imun
yang telah disebut diatas. Dalam hal ini badan berusaha mengucilkan parasit dengan
membentuk kapsul yang terdiri atas sel-sel inflamasi. Reaksi tersebut merupakan respon
seluler terhadap pelepasan antigen kronik setempat. Makrofag yang dikerahkan, melepas
faktor fibrogenik dan merangsang pembentukan granuloma dan fibrotik. Semua ini akibat
pengaruh sel Th1 dan defisiensi sel T akan mengganggu kemampuan tubuh untuk
membentuk granuloma dan kapsul. Pembentukan granuloma terlihat jelas di sekitar telur
cacing skistosoma di hati.
Mekanisme parasit menghindari sistem imun : 1. Pengaruh lokasi
Banyak parasit terlindung dari sistem imun oleh karena letaknya yang secara
anatomis tidak terpajan dengan sistem imun, misalnya parasit intraseluler seperti T.cruzi,
leishmania, plasmodium, T.spiralis, E.histolitika atau cacing yang hdup dalam lumen
saluran cerna.
2. Parasit mengubah antigen
Tripanosoma afrika dapat mengubah antigen mantel permukaannya melalui
proses variasi antigenik. Beberapa jenis malaria juga dapat melakukan hal ini. Ada dua
bentuk variasi antigenik. Pertama adalah perubahan yang stage spesific dalam ekspresi
antigen. Daam fase pematangan parasit memproduksi antigen yang berbeda dari fase
infektif, misalnya fase sporozoit parasit malaria antigeik berbeda dari merozoit yang
berperan pada infeksi kronis. Pada waktu respon imun berkembang terhadap infeksi
sporozoit, parasit berdiferensiasi, mengekspresikan antigen baru sehingga antigen lama
menerus diduga ditimbulkan oleh adanya variasi terprogram dalam ekspresi gen yang
menyandi antigen permukaan utama. Parasit lain menutupi dirinya dengan antibodi
sehingga sistem imun pejamu tidak megenalnya.
3. Supresi sistem imun pejamu
Parasit seperti larva T.spiralis, skistosoma dapat merusak sel limfoid atau jaringan
secara langsung. Antigen yang dilepas parasit dalam jumlah besar mengurangi reflek
respon imun pejamu. Anergi sel T ditemukan pada skistosomiasis berat yang mengenai
hati dan limpa dan pada infestasi filaria. Mekanismenya belum jelas. Pada filariasis
limfatik, infeksi kelenjar getah bening merusak arsitektur kelenjar dan mengakibatkan
defisiensi imun. Defisiensi imun juga terjadi pada malaria dan tripanosomiasis afrika
yang disebabkan karena produksi sitokin immunosupresif oleh makrofag dan sel T yang
diaktifkan dan defek dalam aktivasi sel T.
4. Resistensi
Parasit menjadi resisten terhadap respon imun selama menginvasi pejamu. Larva
skistosoma bergerak dari paru dan selama migrasi tersebut mengembangkan tegumen
yang resisten terhadap kerusakan oleh komplemen dan CTL.
5. Hidup dalam sel pejamu
Protozoa menghindari respon imun dengan memilih hidup dalam sel pejamu atau
dengan mengembangkan kista yang resisten terhadap efektor imun. Beberapa cacing
hidup di lumen saluran cerna dan terlindung dari efektor CMI.
HIPERSENSITIVITAS
Hipersensitivitas atau ”alergi”, menunjukkan suatu keadaan dimana respon imun
mengakibatkan reaksi yang berlebihan dan tidak sesuai yang merugikan inang. Reaksi itu
secara khas terjadi pada orang tertentu setelah kontak kedua dengan antigen khusus
(alergen). Kontak pertama merupakan peristiwa awal yang diperlukan dan menginduksi
sensitisasi terhadap alergen itu.
Ada empat jenis reaksi hipersensitivitas utama yaitu Tipe I, II dan III adalah
Tipe I : Hipersensitivitas Segera (Anafilaktik)
Hipersensitivitas jenis ini muncul sebagai reaksi jaringan yang terjadi dalam
beberapa menit setelah antigen bergabung dengan antibodi yang sesuai. Kalau reaksi itu
terjadi pada setiap anggota spesies, maka reaksi tersebut dinamakan anafilaksis. Kalau
reaksi hanya terjadi pada anggota tertentu dari suatu spesies, keadaan ini disebut dengan
atopi.
Mekanisme umum pada hipersensitivitas segera melibatkan langkah-langkah
berikut. Antigen menginduksi pembentukan antibodi IgE, yang mengikat erat bagian
Fc-nya basofil dan sel mast. Beberapa minggu kemudian, kontak kedua dengan antigen yang
sama mengakibatkan fiksasi antigen pada IgE yang terikat sel, pertautan silang
molekul-molekul IgE dan pelepasan zat perantara secara farmakologik aktif dari sel dalam waktu
beberapa menit.
Zat perantara pada hipersensitivitas anafilaktik ialah : a. Histamin
Histamin terdapat dalam keadaan telah terbentuk dalam trombosit dan dalam granula
sel mast jaringan dan basofil. Pembebasan zat ini menyebabkan vasodilatasi,
meningkatkan permeabilitas kapiler, dan kontraksi otot polos. Obat antihistamin
dapat menghambat tempat reseptor histamin dan relatif cukup efektif untuk rinitis
alergika, tetapi tidak untuk asma.
b. Prostaglandin dan Tromboksan
Kedua zat ini berhubungan dengan leukotrien, dan diturunkan dari asam arakidonat
lewat jalur siklooksigenase. Prostaglandin menyebabkan bronkokonstriksi dan dilatasi
serta peningkatan permeabilitas kapiler. Tromboksan menggumpalkan trombosit.
Zat perantara tersebut menjadi aktif hanya selama beberapa menit setelah dilepaskan,
zat-zat itu dinonaktifkan dengan enzim dan disintesis lagi dengan kecepatan lambat.
Terapi dan Pencegahan Reaksi Anaflaksis
Tujuan terapi adalah melawan daya kerja zat perantara dengan mempertahankan
saluran nafas, ventilasi dan fungsi jantung. Obat-obat yang dapat diberikan antara lain
epinefrin, antihistamin, kortikosteroid, atau natrium kromolin. Natrium kromolin
mengenali alergen dengan tes uji kulit, kemudian menghindari kontak dengan alergen
tersebut.
Atopi
Penyakit hipersensitivitas atopi menunjukkan predisposisi keluarga yang kuat dan
berhubungan dengan kadar IgE yang tinggi. Predisposisi terhadap atopi jelas bersifat
genetik, tetapi gejalanya diinduksi oleh alergen khusus, misalnya alergen lingkungan
(alergi pernafasan terhadap tepung sari, rumput atau debu rumah) atau makanan (alergi
usus terhadap kerang atau kacang-kacangan. Manifestasi klinis berupa demam, asma,
eksema, dan urtikaria. Banyak penderita memberi reaksi jenis segera terhadap uji kulit
(suntikan, tempelan, goresan) dengan menggunakan antigen penyebab.
Tipe II : Hipersensitivitas Sitotoksik
Antibodi yang diarahkan pada antigen permukaan sel akan mengaktifkan
komplemen (atau efektor lain) untuk merusak sel. Antibodi (IgG atau IgM) melekat pada
antigen lewat daerah Fab dan bekerja sebagai suatu jembatan ke komplemen lewat daerah
Fc. Akibatnya dapat terjadi lisis yang berperantara-komplemen, seperti yang terjadi pada
anemia hemolitik, reaksi transfusi ABO, atau penyakit hemolitik Rh.
Penisilin, Fenasetin dan Kuinidin, dapat melekat pada protein permukaan di sel
darah merah dan memicu pembentukan antibodi. Antibodi autoimun semacam itu (IgG)
kemudian bergabung dengan permukaan sel, dan mengakibatkan hemolisis. Infeksi
tertentu seperti Mycoplasma pneumoniae dapat menginduksi antibodi yang bereaksi
silang dengan antigen sel darah merah, mengakibatkan anemia hemolitik. Pada demam
reumatik, antibodi terhadap Streptokokus grup A bereaksi silang dengan jaringan jantung.
Pada sindrom Good-pasture, antibodi terhadap membran dasar ginjal dan paru-paru
mengakibatkan kerusakan berat terhadap selaput melalui aktivitas leukosit yang ditarik
oleh komplemen.
Tipe III : Hipersensitivitas Komplek Imun
Bila antibodi bergabung dengan antigen khususnya, maka akan terbentuk
retikuloendotelial, tetapi kadang-kadang kompleks ini tetap bertahan dan diendapkan
dalam jaringan, sehingga mengakibatkan beberapa penyakit. Pada infeksi bakteri atau
virus, kompleks imun ini dapat diendapkan pada organ tubuh (misal ginjal) sehingga
mengganggu fungsi organ tersebut. Pada penyakit autoimun, antigen ”self” dapat
menimbulkan antibodi yang mengikat antigen organ dan diendapkan dalam organ sebagai
kompleks, terutama dalam sendi (artritis), ginjal (nefritis), atau pembuluh darah
(vaskulitis). Dimanapun diendapkan, komleks imun ini mengaktifkan sistem komplemen,
dan sel polimorfonuklear ditarik ke tempat itu, dimana sel-sel ini menyebabkan radang
dan cedera jaringan. Reaksi hipersensitivitas tipe III yang khas adalah reaksi penyakit
serum.
Penyakit Serum
Setelah injeksi serum asing (atau obat tertentu), antigen perlahan-lahan
dibersihkan dari sirkulasi, dan produksi antibodi dimulai. Adanya antigen dan antibodi
secara serentak mengakibatkan pembentukan kompleks imun yang mungkin beredar atau
diendapkan di berbagai tempat. Beberapa hari sampai 2 minggu setelah injeksi serum
asing, menimbulkan gejala demam, urtikaria, artralgia, limfadenopati dan splenomegali.
Gejala tersebut meningkat sementara antigen dibuang lewat sistem imun, dan gejala
mereda bila semua antigen telah dibuang. Meskipun gejala baru tampak setelah beberapa
hari, penyakit serum digolongkan sebagai reaksi segera, karena gejala-gejalanya muncul
dengan cepat setelah terbentuk kompleks imun.
Penyakit Kompleks Imun
Contoh penyakit yang berhubungan dengan kompleks imun adalah
glomerulonefritis akut pasca streptokokus. Gejala timbul beberapa minggu setelah
terinfeksi streptokokus β-hemolitik grup A, terutama pada kulit. Kadar komplemen secara khas rendah, menimbulkan dugaan reaksi antigen antibodi. Tumpukan kental dari
immunoglobulin dan C3 yang terlihat di sepanjang selaput dasar glomerulus yang
diwarnai oleh imunofluoresensi, memberi kesan kompleks antigen-antibodi, namun
antigen streptokokus jarang terlihat. Kemungkinan kompleks imun tersebut disaring oleh
glomerulus, lalu memfiksasi komplemen , menarik polimorf, dan memulai proses
Tipe IV : Hipersensitivitas Berperantara Sel (Lambat)
Hipersensitivitas berperantara sel merupakan fungsi limfosit T, bukan fungsi
antibodi. Dikatakan respon lambat artinya respon dimulai beberapa jam (atau hari)
setelah kontak dengan antigen dan sering berlangsung selama beberapa hari. Respon ini
terutama terdiri dari infiltrasi sel berinti satu dan indurasi jaringan seperti yang terlihat
pada uji kulit tuberkulin.
Hipersensitivitas Kontak
Hipersensitivitas berperantara sel ini terjadi setelah sensitisasi dengan zat kimia
sederhana (nikel, formaldehida), bahan dari tumbuhan, pemakaian obat topikal
(sulfonamida, neomisin), bahan-bahan kosmetik, sabun dan lain sebagainya.
Molekul-molekul kecil tersebut memasuki kulit dan kemudian bertindak sebagai hapten melekat
pada protein tubuh untuk bertindak sebagai antigen lengkap. Hipersensitivitas
berperantara sel pun diinduksi, terutama dalam kulit. Bila kulit kontak lagi dengan zat
penyebab, orang yang telah peka itu akan mengalami eritema, gatal-gatal, vesikasi,
eksema atau nekrosis kulit dalam 12-48 jam. Pada sensitivitas kontak, sel yang membawa
antigen mungkin berupa sel langerhans dalam epidermis.
Hipersensitivitas Tipe-Tuberkulin
Hipersensitivitas lambat terhadap antigen mikroorganisme yang terdapat dalam
banyak penyakit menular dan telah digunakan untuk membantu menegakkan diagnosis.
Contoh khasnya adalah reaksi tuberkulin. Bila sejumlah kecil tuberkulin disuntikkan ke
dalam epidermis pasien yang sebelumnya pernah terinfeksi Mycobacterium tuberculosis,
hanya sedikit reaksi segera yang muncul, indurasi dan kemerahan mencapai puncaknya
pada 48-72 jam. Uji kulit positif menunjukkan bahwa orang tersebut pernah terinfeksi
oleh penyebab, tetapi ini tidak berarti bahwa penyakitnya masih ada. Namun bila uji kulit
negatif berubah menjadi positif menunjukkan infeksi baru dan mungkin sekarang masih
aktif.
Respon uji kulit yang positif dapat membantu diagnosis dan memberi sokongan
untuk kemoprofilaksis atau kemoterapi. Contoh uji kulit yang lain adalah uji lepromin
positif menunjukkan lepra tuberkuloid (dengan imunitas berperantara sel yang aktif),
sedang uji lepromin negatif menunjukkan lepra lepromatosa (dengan imunitas
koksidioidomikosis, histoplasmosis, blastomikosis) uji kulit jenis lambat yang positif
terhadap antigen khusus membantu menentukan kontak terhadap organismenya.
DEFISIENSI IMUN
Pertama kali ditemukan oleh Bruton tahun 1953 dimana beliau menemukan
hipogamaglobulinemia pada anak usia 8 tahun yang memiliki riwayat sepsis dan artritis
lutut sejak usia 4 tahun disertai dengan otitis media, sepsis pneumokokus dan
pneumonia.Analisa elektroforesis protein serum tidak menunjukkan fraksi globulin gama.
Anak tersebut tidak menunjukkan respon imun terhadap imunisasi dengan tifoid dan
difteri. Defisiensi itu merupakan salah satu jenis defisiensi jaringan limfoid yang dapat
terjadi pada pria dan wanita.
Kita harus mencurigai adanya defisiensi imun bila ditemukan tanda-tanda adanya
peningkatan kerentanan terhadap infeksi rekuren, kronis, oportunistik, dan respon buruk
terhadap antibiotika. Manifestasi lain munculnya hepatosplenomegali atau diare.
Defisiensi imun dapat primer dengan dasar genetik yang relatif jarang dan sekunder yang
lebih sering terjadi dan ditimbulkan oleh berbagai faktor sesudah lahir.
Awitan gejala klinis penyakit defisiensi kongenital biasanya jarang di bawah usia
3-4 bulan, karena ada efek proteksi antibodi maternal. Organ tubuh yang sering terkena
adalah saluran nafas yang diserang bakteri piogenik atau jamur. Gejala lain yang dapat
terjadi pada defisiensi imun adalah ruam kulit, diare, pertumbuhan terganggu, hati dan
limpa membesar, abses rekuren atau osteomielitis. Dapat terjadi penurunan resistensi
terhadap virus, bila terjadi defisiensi seluler.
DEFISIENSI IMUN NONSPESIFIK A. Defisiensi komplemen
Defisiensi fungsi komplemen berhubungan dengan peningkatan insiden infeksi
dan penyakit autoimun Lupus Eritematosus Sistemik (LES). Komponen komplemen
diperlukan tubuh untuk membunuh kuman, opsonisasi, kemotaksis, pencegahan penyakit
automun dan eliminasi kompleks antigen antibodi. Kebanyakan defisiensi komplemen
1. Defisiensi Komplemen Kongenital
Defisiensi ini mengakibatkan infeksi berulang dan penyakit kompleks imun
seperti lupus eritematosus sistemik dan glomerulonefritis.
a. Defisiensi inhibitor esterase C1 (C1 INH deficiency)
Defisiensi inhibitor esterase C1 berhubungan dengan angioedem herediter,
penyakit yang ditandai dengan edem lokal sementara tetapi sering terjadi. Defek tersebut
mengakibatkan aktivitas C1 yang tidak dapat dikontrol dan menimbulkan produksi kinin
yang meningkatkan permeabilitas kapiler. Kulit, saluran cerna dan nafas dapat terkena
dan edem laring yang fatal dapat terjadi.
b. Defisiensi komplemen C2 dan C4
Defisiensi ini menimbulkan penyakit serupa LES, yang disebabkan kegagalan
eliminasi kompleks imun yang komplemen dependen.
c. Defisiensi komplemen C3
Defisiensi komplemen C3 dapat menimbulkan beratnya rekurensi infeksi,
terutama yang berhubungan dengan infeksi mikroba piogenik misal streptokokus dan
stafilokokus. Tidak adanya C3 berarti fragmen kemotaktik C5 tidak diproduksi. Hal ini
disebabkan adanya mutasi pada C3 cDNA.
d. Defisiensi komplemen C5
Defisiensi C5 menimbulkan kerentanan terhadap infeksi bakteri yang
berhubungan dengan gangguan kemotaksis.
e. Defisiensi C6,C7 dan C8
Defisiensi C6,C7 dan C8 menimbulkan kerentanan terhadap septikemia
meningokokus dan gonokokus oleh karena lisis melalui jalur komplemen merupakan
mekanisme kontrol utama dalam imunitas Neisseria.
2. Defisiensi komplemen fisiologik
Defisiensi komplemen fisiologik hanya ditemukan pada neonatus yang
disebabkan karena kadar C3, C5 dan faktor B yang masih rendah.
3. Defisiensi komplemen didapat
Defisiensi komplemen didapat disebabkan oleh depresi sintesis, misalnya pada
sirosis hati dan malnutrisi protein. Pada anemia sel sabit ditemukan gangguan aktivasi
a. Defisiensi Clq,r,s
Defisiensi ini dilaporkan bersamaan dengan penyakit autoimun, terutama
penderita LES. Penderita ini sangat rentan terhadap infeksi bakteri.
b. Defisiensi C2 dan C4
Defisiensi C2 merupakan defisiensi yang paling sering terjadi. Defisiensi C2 dan
C4 dijumpai pada penderita LES.
c. Defisiensi C3
Penderita dengan defisiensi C3 menunjukkan infeksi bakteri rekuren. Pada
beberapa penderita disertai dengan glomerulonefritis kronik.
d. Defisiensi C5-C8
Penderita dengan defisiensi C5-C8 menunjukkan kerentanan yang meningkat
terhadap infeksi terutama Neisseria.
e. Defisiensi C9
Defisiensi C9 sangat jarang terjadi. Penderita dengan defisiensi ini tidak
menunjukkan tanda infeksi rekuren, mungkin karena lisis masih dapat terjadi atas
pengaruh C8 tanpa C9.
B. Defisiensi Interferon (IFN) dan Lisozim
Defisiensi IFN kongenital menimbulkan infeksi mononukleosis yang
fatal.Sedang defisiensi IFN dan Lisozim didapat biasanya ditemukan pada penderita
malnutrisi protein/kalori.
C. Defisiensi Sel NK
Defisiensi sel NK kongenital dilaporkan pada penderita osteoporosis (defek
osteoklas dan monosit). Kadar IgG, IgA dan kekerapan autoantibodi biasanya meningkat.
Defisiensi sel NK didapat biasanya terjadi akibat immunosupresi atau radiasi.
D. Defisiensi Sistem Fagosit
Fagosit dapat menghancurkan mikroorganisme dengan atau tanpa bantuan
komplemen. Defisiensi fagosit sering disertai infeksi berulang. Kerentanan terhadap
resiko infeksi meningkat bila jumlah sel tersebut turun sampai di bawah 500/mm3.
Meskipun defek terutama mengenai fagosit, tetapi defisiensi disini ditekankan pada sel
PMN.
a. Chronic Granulomatous Disease (CGD)
Penyakit ini mempunyai ciri-ciri : infeksi rekuren berbagai mikroba, baik gram
negatif (Eschericia, Serratia, Klebsiella) maupun gram positif (Stafilokokus). CGD
merupakan penyakit sex-linked resesif yang terjadi pada usia 2 tahun pertama. Pada
CGD ditemukan defek neutrofil, ketidakmampuan membentuk peroksid hydrogen atau
metabolit oksigen toksik lainnya.
b. Defisiensi Glucose-6-phosphate dehydrogenase (G6PD)
Merupakan penyakit immunodefisiensi yang x-linked dengan gambaran klinis
seperti CGD. Penyakit ini diduga akibat defisiensi generasi Nicotinamide Adenine
Dinucleotide Phosphate Dehydrogenase (NADPH). Gejalanya mulai terlihat pada usia di
bawah 2 tahun berupa kerentanan yang tinggi tehadap kuman yang mempunyai virulensi
rendah seperti S.epidermidis, Serratia marcescens dan Aspergillus. Kelainan klinis yag
ditemukan ialah lmfadenopati, hepatosplenomegali dan kelenjar getah bening yang terus
mengeluarkan cairan. Infeksi akut dan kronik terjadi di kelenjar getah bening, kulit,
saluran cerna, hati dan tulang. Dalam keadaan normal, fagositosis akan mengaktifkan
oksidase NADPH yang diperlukan untuk pembentukan peroksidase yang dibutuhkan
untuk membunuh kuman intraselular.
c. Sindrom Chediak-Higashi
Sindrom Chediak-Higashi sangat jarang ditemukan, ditandai dengan infeksi
rekuren, piogenik, terutama streptokokus dan stapilokokus. Prognosis buruk kebanyakan
pasien meninggal pada usia anak. Neutrofil mengandung lisosom besar abnormal yang
dapat bersatu dengan fagosom tetapi terganggu dalam kemampuannya melepas isinya
sehingga proses menelan dan menghancurkan mikroba terlambat. Pada sindrom ini
aktivitas sel NK dan enzim lisosom menurun.
d. Sindrom Job
Sindrom Job berupa pilek berulang, abses stafilokokus, eksim kronis dan otitis
media. Kemampuan neutrofil untuk menelan makanan tidak menunjukkan kelainan,
e. Sindrom leukosit malas (lazy leucocyte)
Sindrom leukosit malas berupa kerentanan terhadap infeksi mikroba yang berat.
Terjadi neutropenia, dan respon kemotaksis dan inflamassi terganggu.
DEFISIENSI IMUN SPESIFIK 1. Defisiensi imun primer sel B
Defisiensi sel B berupa gangguan perkembangan sel B. Berbagai akibat dapat
ditemukan mulai dari tidak adanya semua Ig atau satu kelas atau subkelas Ig. Penderita
dengan defisiensi semua jenis IgG akan lebih mudah menjadi sakit dibanding dengan
hanya menderita defisiensi kelas Ig tertentu saja. Istilah untuk defisiensi ini adalah
hipo-gamaglobulinemia.
a. X-linked hypogammaglobulinemia
Bruton pada tahun 1952 menggambarkan penyakit yang disebutnya
agammaglobulinemia. Hanya terjadi pada bayi laki-laki. Penyakit biasanya nampak pada
usia 5-6 bulan sewaktu IgG asal ibu mulai menghilang. Pada usia tersebut anak mulai
menderita infeksi berulang. Penyakit ini jarang terjadi (1:100.000). Pemeriksaan
imunologik menunjukkan tidak adanya Ig dari semua kelas Ig. Darah, sumsum tulang,
limpa dan kelenjar getah bening tidak mengandung sel B. Kerusakan utama adalah oleh
karena pre-sel B yang ada dalam kadar normal tidak dapat berkembang menjadi sel B
yang matang.
Bayi dengan defisiensi sel B menderita otitis media, rekuren, bronchitis,
septikemi, pneumoni, arthritis, meningitis dan dermatitis. Kuman penyebab biasanya
H.influenza dan S.pneumonia. Seringkali dijumpai sindrom malabsorbsi oleh karena
G.lamblia yang bermanifestasi di saluran cerna. Antibiotika biasanya tidak menolong.
Pemberian IgG yang periodik memberikan hasil yang efektif untuk 20-30 tahun.
Prognosis buruk dan biasanya diakhiri dengan penyakit paru kronik.
b. Common Variable Hypogammaglobulinemia
Penyakit mirip dengan hipogamaglobulinemia Bruton. Penyakit ini berhubungan
dengan insiden autoimun yang tinggi. Meskipun jumlah sel B dengan Ig normal,
kemampuan memproduksi atau melepas Ig mengalami gangguan. Kadar Ig serum
c. Defisiensi Immunoglobulin yang selektif (disgamaglobulinemia)
Defisiensi Ig yang selektif adalah penurunan kadar satu atau lebih Ig, tetapi kadar
Ig yang lain normal atau meningkat. Misalnya defisiensi IgA selektif, defisiensi ini
merupakan defisiensi imun yang sering dijumpai. Ditemukan pada 1 dari 700 orang
dalam masyarakat. Pada kasus ini, tidak adanya proteksi dari sIgA pada permukaan
mukosa sehingga menunjukkan infeksi sino-pulmoner dan infeksi gastrointestinal yang
rekuren. Ditemukan pula kasus defisiensi IgM selektif dan defisiensi IgG selektif. Namun
defisiensi tersebut jarang terjadi.
2. Defisiensi imun primer sel T
Penderita dengan defisiensi sel T kongenital sangat rentan terhadap infeksi virus,
jamur dan protozoa. Olehkarena sel T juga berpengaruh terhadap sel B, maka defisiensi
sel T disertai pula gangguan produksi Ig yang nampak dari tidak adanya respon terhadap
vaksinasi dan seringnya terjadi infeksi.
a. Aplasi timus kongenital (Sindrom DiGeorge)
Sindrom ini disebabkan defisiensi sel T akibat penderita sedikit memiliki sel T
dalam darah, kelenjar getah bening dan limpa. Diduga disebabkan karena adanya defek
pada perkembangan embrio dari lengkung farings ke-3 dan ke-4, yang terjadi sekitar 12
minggu setelah gestasi.
b. Kandidiasis Mukokutan Kronik
Penyakit ini ditandai dengan adanya infeksi jamur biasa yang nonpatogenik
seperti Kandida albikans pada kulit dan selaput lendir yang disertai dengan gangguan
fungsi sel T yang selektif. Penderita mempunyai imunitas yang normal terhadap mikroba
lain selain kandida dan imunitas humoralnya normal. Jumlah limfosit normal, tetapi sel T
menunjukkan kemampuan yang kurang untuk memproduksi MIF dalam respon terhadap
antigen kandida, meskipun respon terhadap antigen lain normal. Reaksi kulit lambat/DTH
terhadap kandida juga negatif.
c. Ataksia Telangiektasi (AT)
Merupakan penyakit autosomal resesif mengenai saraf, endokrin dan sistem
vaskuler. Ciri klinisnya berupa gerakan otot yang tidak terkoordinasi (staggering gait)
dan dilatasi pembuluh darah kecil (telangiektasi) yang jelas dapat dilihat di sklera mata,
Penyakit timbul pertama pada anak di bawah usia 2 tahun dan berhubungan
dengan infeksi sino-pulmoner berulang. Pada pasien yang lebih tua dapat timbul
karsinoma.
DEFISIENSI IMUN SPESIFIK FISIOLOGIK 1. Kehamilan
Defisiensi imun seluler dapat ditemukan pada kehamilan. Wanita hamil
memproduksi Ig yang meningkat atas pengaruh oestrogen. IgG diangkut melewati
plasenta oleh reseptor Fc pada akhir hamil 10 minggu.
2. Usia tahun pertama
Sistem imun pada satu tahun pertama sampai 5 tahun masih belum matang.
Meskipun neonatus menunjukkan jumlah sel T yang tinggi, semuanya berupa sel naif dan
tidak memberi respon adekuat terhadap antigen. Antibodi janin disintesis pada awal
minggu ke 20 tetapi kadar IgG dewasa baru dicapai pada usia 5 tahun. Pada usia beberapa
bulan, bayi tergantung dari IgG ibu.
3. Usia lanjut
Golongan usia lanjut lebih sering menderita infeksi dibanding anak muda. Akibat
involusi timus, jumlah sel T naif dan kualitas respon sel T makin berkurang . Jumlah sel
T memori meningkat tetapi semakin sulit untuk berkembang. Defisiensi seluler sering
disertai dengan meningkatnya kejadian kanker, kepekaan terhadap infeksi misalnya
tuberkulosis, gangguan penyembuhan infeksi dan fenomena autoimun. Penyakit
autoimun yang sering timbul pada usia lanjut disebabkan oleh penurunan aktivitas sel T.
Pada usia 60 tahun, jaringan timus hampir seluruhnya diganti oleh lemak dan edukasi sel
T dalam timus hampir hilang. Jadi pejamu tergantung pada persediaan sel T yang
diproduksi sebelumnya pada usia lebih muda. Pada usia lanjut, imunitas humoral juga
menurun, akibat menurunnya kemampuan sel T untuk menginduksi pematangan sel B
dalam sumsum tulang yang mengurangi kemajemukan sel B, namun sel B yang sudah tua
DEFISIENSI IMUN DIDAPAT SEKUNDER
Imunodefisiensi sekunder atau didapat merupakan defisiensi sekunder yang
tersering ditemukan. Defisiensi ini melibatkan fungsi fagosit dan limfosit yang terjadi
akibat infeksi HIV, malnutrisi, terapi sitotoksik dan lain sebagainya. Defisiensi imun
sekunder dapat meningkatkan kerentanan terhadap infeksi oportunistik.
1. Malnutrisi
Malnutrisi dan defisiensi zat besi dapat menimbulkan depresi sistem imun
terutama pada imunitas seluler. Anak dengan malnutrisi protein/kalori menunjukkan
atrofi timus dan jaringan limfoid sekunder, depresi respon sel T terhadap mitogen dan sel
alogeneik, pengurangan sekresi limfokin, gangguan respon terhadap uji kulit
hipersensitivitas tipe lambat dan antigen lingkungan. Kerentanan yang meninggi terhadap
infeksi sering membaik setelah diberikan diit yang cukup. Defisiensi seng (Zn) dan
magnesium menurunkan imunitas seluler, terutama sekresi sitokin Th1. Defisiensi ini
sering terjadi pasca operasi.
2. Infeksi
Infeksi dapat menimbulkan defisiensi imun. Malaria dan Rubella kongenital dapat
menimbulkan defisiensi antibodi. Campak diketahui menimbulkan defek imunitas selular
yang menimbulkan reaktivasi tuberkulosis. Campak dan infeksi virus lain dapat
menginfeksi tubuh menginduksi supresi Delayed Type Hypersensitivity (DTH)
sementara. Jumlah sel T dan respon limfosit terhadap antigen dan mitogen menurun.
Infeksi virus juga menimbulkan efek yang tidak diinginkan terhadap makrofag.
3. Obat, trauma, tindakan kateterisasi dan bedah
Obat sering menimbulkan defisiensi imun sekunder. Penggunaan steroid dan obat
sitotoksik menimbulkan imunosupresif. Pemberian obat, kateterisasi dan tindakan
pembedahan dapat menimbulkan imunokompromais. Contoh obat yang bersifat
imunosupresi antara lain sitotoksik, gentamisin, amikain, dan tobramisin. Obat-obat ini
mengganggu kemotaksis neutrofil. Tetrasiklin dapat menekan imunitas selular.
Kloramfenikol dapat menekan respon antibodi, sedang rifampisin dapat menekan
imunitas humoral dan selular. Jumlah neutrofil akan menurun akibat pemakaian obat
Pasien dengan trauma kurang mampu menghadapi patogen, mungkin akibat
pelepasan faktor dan menekan respon imun.
4. Penyinaran
Penyinaran dosis tinggi akan menekan seluruh jaringan limfoid, sedangkan
dengan dosis rendah dapat menekan aktivitas sel Ts secara selektif.
5. Penyakit berat
Defisiensi imun bisa didapat akibat menderita berbagai penyakit yang menyerang
kelenjar limfoid seperti penyakit Hodgkin, mieloma multiple, leukemia dan
limfosarkoma. Uremia dapat menekan sistem imun. Gagal ginjal dan diabetes dapat
menimbulkan defek fagosit sekunder.
6. Kehilangan imunoglobulin/leukosit
Defisiensi imunoglobulin dapat terjadi akibat tubuh kehilangan protein yang
berlebihan misalnya pada penyakit ginjal dan diare. Pada sindrom nefrotik ditemukan
kehilangan protein dan penurunan IgG, IgA yang berarti dengan IgM normal.
7. Stress
Stres akut dan kronis menunjukkan berbagai efek terhadap sistem imun. Sistem
imun berintegrasi dengan stres. Stres menghambat kerja sistem imun. Rangsangan stres
akut seperti bising, anxietas akut akan meningkatkan jumlah sel T dalam sirkulasi. Hal ini
disebabkan oleh saraf simpatis yang melepas katekolamin (misalnya epinefrin).Serat
saraf yang melepas katekolamin menginervasi kelenjar getah bening. Kadar tinggi
katekolamine juga dilepas ke dalam sirkulasi oleh medula kelenjar adrenal. Sel T
mengekspresikan reseptor untuk epinefrin dan rangsangan terhadap reseptor tersebut
mempengaruhi sel T untuk menurunkan ekspresi molekul integrin sehingga sel T dicegah
menempel pada endotel dan bermigrasi ke jaringan. Akibatnya sel T menumpuk di dalam
darah.
Stres yang berlangsung lebih dari beberapa jam, akan mempengaruhi sistem imun.
CD4+ terendah di pagi hari. Sekresi steroid ditingkatkan sebagai respon terhadap berbagai
stres fisiologik seperti latihan jasmani yang berat dan lama atau emosi.
8. AIDS (Acquired Immune Syndrome)
AIDS disebabkan oleh virus yang disebut HIV (Human Immunodeficiency Virus)
yang terdiri dari HIV-1 dan HIV-2. AIDS terbanyak disebabkan HIV-1 hanya beberapa
kasus yang disebabkan HIV-2. HIV adalah virus retro yang menginfeksi sistem imun
terutama CD4+ dan menimbulkan destruksi sel tersebut. Partikel HIV terdiri dari dua
untaian RNA dalam inti protein yang dilindungi envelope lipis asal sel pejamu. Transmisi
virus terjadi melalui cairan tubuh yang terinfeksi seperti hubungan seksual, kontak
homoseksual, penggunaan jarum yang terkontaminasi, transfusi darah atau produk darah
seperti hemofilia.
Patogenesis
Siklus hidup HIV adalah infeksi sel, produksi DNA virus dan integrasi ke dalam
genom, ekspresi gen virus, produksi partikel virus. Virus menginfeksi sel dengan
menggunakan glikoprotein envelope yang disebut gp120 (120KD glikoprotein) yang
terutama mengikat sel CD4+ dan reseptor kemokin (CXCR4 dan CCR5) dari sel
manusia. Oleh karena itu virus hanya dapat menginfeksi dengan efisien sel CD4+ dan
kemokin. Makrofag dan sel dendritik juga dapat diinfeksi oleh HIV.
Setelah berikatan dengan reseptor sel, membran virus bersatu dengan membran
sel pejamu dan virus masuk sitoplasma. Disini envelope virus dilepas oleh protease virus
dan RNA menjadi bebas. Kopi DNA dari RNA virus disintesis oleh enzim transkriptase
dan kopi DNA bersatu dengan DNA pejamu. DNA yang terintegrasi disebut provirus.
Bila sel terinfeksi seperti CD4+, makrofag dan sel dendritik diaktifkan beberapa rangsang
eksternal seperti mikroba yang dapat menimbulkan infeksi, sel akan memberikan respon
terhadap transkripsi banyak gen yang sering menimbulkan produksi sitokin. Provirus juga
dapat diaktifkan, sehingga diproduksi RNA dan protein virus.
Sekarang virus mampu membentuk struktur inti, migrasi ke membran sel,
memperoleh envelope lipid dari sel pejamu, dilepas berupa partikel virus yang dapat
menular dan siap menginfeksi sel lain. Integrasi provirus dapat tetap laten dalam sel
terinfeksi untuk berbulan-bulan atau tahun, tersembunyi dari sistem imun pejamu, bahkan
Gambar 3. Patogenesis AIDS
Fase penyakit HIV berhubungan dengan penyebaran virus dari tempat awal
infeksi ke jaringan limfoid ke seluruh tubuh. Respon imun pejamu sementara mengontrol
infeksi akut, tetapi tidak mencegah terjadinya infeksi kronisdari sel dan jaringan limfoid.
Sitokin yang diproduksi sebagai respon terhadap HIV dan mikroba lain dapat
meningkatkan produksi HIV dan berkembang menjadi AIDS. Setelah infeksi dapat
terjadi viremia akut singkat. Virus menginfeksi sel CD4+, makrofag dan sel dendritik
dalam darah dan organ limfoid. Sel dendritik dapat menangkap virus ditempat virus
masuk dan mengangkutnya ke organ limfoid perifer yang selanjutnya menginfeksi sel T.
Infeksi ini akan menyebabkan penurunan jumlah sel CD4+ yang disebabkan oleh
efek sitopatik virus dan kematian sel. Jumlah sel T yang hilang selama progres AIDS
diinfeksi kronis diaktifkan dan rangsang kronis menimbulkan apoptosis. Sel dendritik
yang terinfeksi juga akan mati.
Gambaran klinis
Pada awal infeksi timbul gejala viremia akut ringan. Gejala menghilang dalam
beberapa hari dan penyakit memasuki masa laten klinis. Selama masa laten ini biasanya
terjadi kehilangan sel CD4+ yang progresif dalam jaringan limfoid dan destruksi
gambaran jaringan limfoid. Jumlah sel CD4+ dalam darah mulai menurun dibawah
200/mm3 (normal 1500 sel/mm3) dan penderita rentan terhadap infeksi dan disebut
menderita AIDS.
Gambaran klinis dan manifestasi patologik AIDS disebabkan peningkatan
kerentanan terhadap infeksi dan beberapa jenis kanker. Penderita sering diinfeksi
mikroba intraseluler seperti Citomegalovirus, Pnemocystic carinii, Mycobacteria atipik
yang pada keadaan normal dapat ditanggulangi oleh sistem imun seluler. Penderita AIDS
juga menunjukkan penurunan jumlah sel CD8+ meskipun virus tidak menginfeksi sel
tersebut. Penderita AIDS juga rentan terhadap kanker dan limfoma sel B yang disebabkan
virus Epstein Barr dan tumor pembuluh darah kecil (sarkoma kaposi) yang disebabkan
virus herpes.
Penderita AIDS lanjut akan kehilangan berat badan akibat perubahan
metabolisme dan kurangnya kalori yang masuk tubuh. Demensia dapat terjadi oleh
infeksi mikroglia (makrofag dalam otak). Pada awal infeksi, antibodi dan respon CTL
terhadap antigen virus dapat terjadi, tetapi respon itu tidak dapat mencegah progres
penyakit. Antibodi terhadap gp120 dapat inefektif, karena virus cepat memutasi regio
gp120 yang merupakan sasaran antibodi. CTL juga tidak efektif membunuh virus karena
virus mencegah ekspresi MHC-I Oleh sel terinfeksi. Bila CTL berhasil menghancurkan
sel terinfeksi, virus akan dilepas dan menginfeksi lebih banyak sel.
PENGOBATAN DEFISIENSI IMUN
Pengobatan pasien dengan penyakit defisiensi imun umumnya mempunyai dua
tujuan yaitu :
1. Mengurangi kejadian dan dampak infeksi dengan :
Memantau dengan baik pasien terhadap infeksi.
Menggunakan antibiotika/antiviral yang benar.
Imunisasi aktif atau pasif bila memungkinkan.
2. Memberikan komponen sistem imun yang defektif dengan transfer pasif atau
transplantasi
Pemberian globulin gama kepada pasien dengan defisiensi Ig tertentu.
Infus sitokin seperti IL-2, GM-CSF, M-CSF dan IFN-γ kepada subyek
dengan penyakit tertentu.
Transfusi :
- Neutrofil kepada subyek dengan defisiensi fagosit.
- Polietilen glikol digabung dengan adenosin deaminase untuk SCID
- Limfosit autologus yang sudah mengalami transfection dengan gen
adenosin deaminase (ADA) pada Severe Combined Immunodefi –
ciency.
Transplantasi : timus fetal atau stem cell dari sumsum tulang dalam
memperbaiki kompetensi imun
Terapi gen somatik juga telah membrikan harapan dalam terapi penyakit genetik. Dimana dilakukan penyisipan gen normal ke populasi sel yang terkena penyakit dengan
maksud untuk membentuk gen normal yang sebelumnya tidak ada atau defisiensi.
TEKHNIK IMUNOLOGIK : REAKSI ANTIGEN-ANTIBODI INVITRO
Reaksi antigen dan antibodi bersifat sangat khusus. Suatu antigen hanya bereaksi
dengan antibodi yang ditimbulkan oleh jenisnya sendiri atau oleh antigen yang berkaitan
erat. Karena begitu khususnya, reaksi antara suatu antigen dan antibodi dapat digunakan
untuk mengenali salah satu pihak dengan memakai pihak lain. Spesifitas ini dipakai
sebagai dasar reaksi serologi. Reaksi silang yang mungkin terjadi diantara berbagai
antigen yang berkaitan dapat membatasi spesifitas uji.
Radioimunoassay (RIA)
Metode ini digunakan untuk mengkuantitasikan antigen atau hapten yang dapat
diberi label radioaktif. Ini didasarkan pada persaingan untuk antibodi khusus antara
Kompleks yang terbentuk antara antigen dan antibodi kemudian dapat dipisahkan dan
jumlah radiaktivitasnya diukur. Konsentrasi antigen atau hapten yang tidak diketahui
ditentukan dengan membandingkan hasil-hasil yang diperoleh dengan hasil dari beberapa
konsentrasi antigen standar. RIA adalah suatu metode yang sangat peka dan digunakan
untuk mengukur kadar hormon atau obat dalam serum. Suatu RIA yang khusus, uji
radioalergosorben (RAST), digunakan untuk mengukur jumlah antibodi IgE serum yang
bereaksi dengan suatu alergen yang dikenal.
Imunoassay Enzim (EIA)
Metode ini mempunyai banyak variasi bergantung pada konjugasi enzim dengan
antigen atau antibodi. Enzim dideteksi dengan mengukur aktivitas enzim dengan
substratnya. Meskipun hampir sepeka RIA, metode ini tidak memerlukan perlengkapan
khusus atau label radioaktif. Untuk mengukur antibodi, antigen yang dikenal diikat pada
suatu fase padat (misalnya lempeng mikrodilusi plastik), dieramkan dengan serum uji
yang telah diencerkan, dicuci dan dieramkan lagi dengan anti-imunoglobulin yang diberi
label dengan suatu enzim (misalnya horseradish peroksidase). Aktivitas enzim, yang
diukur dengan menambahkan substrat khusus dan melihat reaksi warna, merupakan
fungsi langsung dari jumlah antibodi yang terikat.
Fluorescence Immuno Assay (FIA)
Dengan menggunakan mikroskop fluoresen dan antibodi yang dilabel dengan
molekul fluoresen, potongan jaringan dapat diperiksa untuk sel yang mengekspresikan
antigen spesifik. Tehnik langsung dan tidak langsung dapat mengevaluasi secara
kualitatif dan kuantitatif berbagai sel yang berhubungan dengan molekul pada waktu
yang sama.
Cara FIA langsung digunakan untuk menemukan antigen, immunoglobulin atau
komplemen, yang melekat pada sel jaringan penderita. Cara tidak langsung lebih banyak
digunakan untuk menemukan antibodi. Pada cara ini, serum penderita direaksikan dengan
sel atau jaringan, kemudian ditambahkan anti antibodi yang bertanda fluoresen dan
diperiksa di bawah mikroskop ultraviolet. Cara ini dapat segera memberi hasil, tetapi
Enzyme Linked Immunosorbent Assay (ELISA)
ELISA digunakan untuk menemukan antibody. Dalam hal ini antigen mula-mula
diikat benda padat kemudian ditambah antibodi yang akan dicari. Setelah itu
ditambahkan lagi antigen yang bertanda enzim, seperti peroksidase dan fosfatase.
Akhirnya ditambahkan substrat kromogenik yang bila bereaksi dengan enzim
menimbulkan perubahan warna. Perubahan warna yang terjadi sesuai dengan jumlah
enzim yang diikat dan sesuai pula dengan kadar antibodi yang dicari. Dibanding dengan
BAB III KESIMPULAN
Imunitas terhadap infeksi dapat dibagi atas imunitas terhadap bakteri baik ekstraselular dan intraselular, imunitas terhadap virus, imunitas terhadap jamur,
dan imunitas terhadap parasit. Kesemua imunitas diatas berlangsung secara
nonspesifik dan spesifik baik humoral maupun selular.
Reaksi hipersensitivitas adalah respon imun yang berlebihan dan tidak sesuai yang merugikan inang. Terdiri dari 4 Tipe yaitu Tipe I hipersensitivitas segera
(anafilaksis), Tipe II hipersensitivitas sitotoksik, Tipe III hipersensitivitas
kompleks imun, Tipe IV hipersensitivitas berperantara sel (lambat).
Defisiensi imun adalah terganggunya respon imun baik nonspesifik maupun spesifik yang mengakibatkan peningkatan kerentanan terhadap infeksi
oportunistik, rekuren dan kronis serta peningkatan kerentanan terhadap terjadinya
kanker.
Pengobatan pasien dengan penyakit defisiensi imun umumnya mempunyai dua tujuan yaitu mengurangi kejadian dan dampak infeksi dengan menjauhi subyek
dari penyakit menular, memantau dengan baik pasien terhadap infeksi dan
memberikan komponen sistem imun yang defektif dengan transfer pasif atau
transplantasi
DAFTAR PUSTAKA
1. Baratawidjaja. Imunologi Dasar. Edisi 6. Balai Penerbit Fakultas Kedokteran
Universitas Indonesia. Jakarta. 2004.
2. Brooks, Butel, Ornston. Medical Microbiology. Appleton & lange.
3. Parslow, Stites, Terr, Imboden. Medical Immunology. 10th edition. Mc-Graw Hill