STUDI PERBANDINGAN KANDUNGAN BESI (Fe) DAN ALUMINIUM
(Al) DIDALAM AIR MINUM YANG DIPRODUKSI OLEH PDAM
TIRTANADI PADA UNIT PRODUKSI CABANG SEI AGUL,
MEDAN LABUHAN DAN SUNGGAL MEDAN
SKRIPSI
ANDY SURYANATA
110802051
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
STUDI PERBANDINGAN KANDUNGAN BESI (Fe) DAN ALUMINIUM
(Al) DIDALAM AIR MINUM YANG DIPRODUKSI OLEH PDAM
TIRTANADI PADA UNIT PRODUKSI CABANG SEI AGUL,
MEDAN LABUHAN DAN SUNGGAL MEDAN
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
ANDY SURYANATA
110802051
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : Studi Perbandingan Kandungan Besi (Fe) dan Aluminium Didalam Air Minum yang Diproduksi Oleh PDAM Tirtanadi Pada Unit Cabang Produksi Cabang Sei Agul, Medan Labuhan dan Sunggal Medan
Kategori : Skripsi
Nama : Andy Suryanata
Nomor Induk Mahasiswa : 110802051
Program Studi : Sarjana (S1) Kimia Departemen : Kimia
Fakultas : Matematika Dan Ilmu Pengetahuan Alam Universitas Sumatera Utara
Disetujui di : Medan, Mei 2015
Komisi Pembimbing :
Pembimbing 2, Pembimbing 1,
Drs Chairuddin, M.Sc Jamahir Gultom, Ph.D NIP.195909171987011001 NIP.195209251977031001
Disetujui oleh :
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
STUDI PERBANDINGAN KANDUNGAN BESI (Fe) DAN ALUMINIUM (Al) DIDALAM AIR MINUM YANG DIPRODUKSI OLEH PDAM
TIRTANADI PADA UNIT PRODUKSI CABANG SEI AGUL, MEDAN LABUHAN DAN SUNGGAL MEDAN
SKRIPSI
Saya mengakui bahwa skripsi iniadalah hasil karya sendiri, Kecuali beberapa kutipan dan ringkasan yang masing – masing disebutkan sumbernya.
Medan, Mei 2015
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa karena atas berkat karunia dan limpahan kasih-Nya Penulis dapat menyelesaikan penyusunan skripsi ini.
Dengan kerendahan hati penulis menyampaikan ucapan terima kasih yang sebesar-besarnya kepada Bapak Jamahir Gultom,Ph.D selaku Dosen pembimbing 1 dan Drs.Chairuddin,M.Sc selaku Dosen Pembimbing 2 yang telah meluangkan waktunya untuk memberikan bimbingan dan saran-saran yang membangun kepada penulis selama melakukan penelitian dan penulisan skripsi ini. Dan kepada ibu Dr.Rumondang Bulan,MS selaku Ketua Departemen Kimia FMIPA USU dan kepada Ibu Cut Fatimah Zuhra,M.Si selaku Dosen Wali yang telah membimbing penulis selama mengikuti masa perkuliahan dan Bapak Drs.Albert Pasaribu,M.Sc selaku Sekretaris Departemen Kimia FMIPA USU.
Ucapan terima kasih yang sebesar-besarnya kepada Ibunda tercinta yang selalu mendukung dan memberi nasehat serta dukungan moral kepada saya serta semangat, dan seluruh keluarga yang juga turut memberi dukungan hingga akhirnya penelitian ini dapat diselesaikan.
Ucapan terima kasih juga disampaikan kepada kak Tiwi selaku laboran di Laboratorium Analitik yang sudah membantu dan memberi masukan dan saran-saran, kepada teman-teman seperjuangan saya di Laboratorium Analitik, Bella, Emi, Fatya, Roberta dan Wiwi yang telah membantu penelitian saya,dan kepada sahabat saya wildi yang memberikan saran dan dukungan selama perkuliahan dan penelitian.Dan kepada kak dorkas dan bang zulfanri yang telah banyak mengajari saya dan adik-adik saya yang ikut mendukung dan membantu saya. Akhirnya saya mengucapkan terima kasih kepada teman-teman saya mahasiswa kimia stambuk 2011.
STUDI PERBANDINGAN KANDUNGAN BESI (Fe) DAN ALUMINIUM (Al) DIDALAM AIR MINUM YANG DIPRODUKSI OLEH PDAM
TIRTANADI PADA UNIT PRODUKSI CABANG SEI AGUL, MEDAN LABUHAN DAN SUNGGAL MEDAN
ABSTRAK
Telah dilakukan penelitian tentang studi perbandingan kandungan besi dan aluminium pada air minum yang diproduksi oleh PDAM Tirtanadi pada unit produksi cabang Sei Agul, Medan Labuhan dan Sunggal Medan. Sampel air minum diambil secara acak dari perumahan warga pada daerah sekitar cabang unit produksi. Penentuan kandungan logam Fe dilakukan dengan Spektrofotometer Serapan Atom (SSA) pada panjang gelombang 248,3 nm dan kandungan logam Al dilakukan dengan Spektrofotometer UV-Vis pada panjang gelombang 535 nm. Preparasi sampel untuk metode SSA adalah didestruksi basah dengan HNO3(p) dan sampel untuk spektrofotometri metode
aluminon dipreparasi dengan HCl(p). Dari hasil penelitian diperoleh kandungan Fe
dalam air minum pada unit produksi cabang Sei Agul, Medan Labuhan dan Sunggal masing – masing sebesar 7.016 mg/L; 1.145 mg/L dan 1.318 mg/L dan kandungan Al sebesar 49.677 mg/L; 81.256 mg/L dan 86.725 mg/L.
STUDY OF DIFFERENCE BETWEEN CONCENTRATION OF IRON (Fe) AND ALUMINIUM (Al) IN TAP WATER PRODUCED BY PDAM
TIRTANADI FROM SEI AGUL, MEDAN LABUHAN AND SUNGGAL MEDAN PRODUCTION UNITS
ABSTRACT
The research for study of difference between concentration of iron (Fe) and aluminium (Al) in tap water produced by PDAM Tirtanadi from Sei Agul, Medan Labuhan and Sunggal Medan production units. Tap water was taken randomly from civilian house near the production unit. The concentration of iron contained in tap water is analyzed by using Atomic Absorption Spectrophotometric Method at wavelength 248,3 nm and concentration of aluminium is analyzed by using Spectrophotometric Aluminon Method at wavelength 535 nm. Sample for Atomic Absorption Spectrophotometric Method is prepared by concentrated HNO3 and Sample for Spectrophotometric
Aluminon Method is prepared by concentrated HCl. The result of analysis of iron concentration in tap water produced by Sei Agul, Medan Labuhan and Sunggal Medan production units are 7.016 mg/L; 1.145 mg/L and 1.318 mg/L and aluminium concentration are 49.677 mg/L; 81.256 mg/L and 86.725 mg/L.
DAFTAR ISI
Bab 1. Pendahuluan
1.1 Latar Belakang 1
1.2 Permasalahan 3
1.3 Pembatasan Masalah 3
1.4 Tujuan Penelitian 3
1.5 Manfaat Penelitian 4
1.6 Lokasi Penelitian 4
1.7 Metodologi Penelitian 4
Bab 2. Tinjauan Pustaka
2.1 Air 5
2.3.1 Kontaminan Fisik 13
2.3.1.1 Kekeruhan 13
2.3.1.2 Warna 13
2.3.1.3 Bau dan Rasa 14
2.3.1.4 Padatan 14
2.3.1.5 Suhu 14
2.3.2 Kontaminan Kimiawi 15
2.3.2.1 Ion dalam Air 15
2.3.2.2 Jenis Non-Ionik dalam Air 16
2.3.2.3 Gas Terlarut 16
2.3.2.4 Logam Berat 16
2.3.3 Kontaminan Mikrobiologis 17
2.4 Koagulasi dan Flokulasi dalam Pengolahan Air 17
2.4.1 Koagulasi 17
2.4.1.1 Alum 18
2.4.1.2 Besi 19
2.5 Aluminium 20
2.6 Besi 21
2.7 Destruksi 22
2.8 Spektrofotometri 23
2.9 Spektrofotometri Serapan Atom 23
2.9.1 Prinsip Kerja Spektrofotometri Serapan Atom 24
Bab 3. Metodologi Penelitian
3.1 Alat – Alat Penelitian 25
3.2 Bahan – Bahan Penelitian 26
3.3 Prosedur Penelitian 26
3.3.1 Pembuatan Larutan Standar Fe3+ 26
3.3.1.1 Pembuatan Larutan Standar Fe3+ 1000 mg/L 26 3.3.1.2 Pembuatan Larutan Standar Fe3+ 100 mg/L 26 3.3.1.3 Pembuatan Larutan Standar Fe3+ 10 mg/L 27 3.3.1.4 Pembuatan Larutan Seri Standar Fe3+ 0,5; 1,0;
2,0; dan 2,5 mg/L 27
3.3.2 Pembuatan Larutan Standar Al3+ 27
3.3.2.1 Pembuatan Larutan Standar Al3+ 1000 mg/L 27 3.3.2.2 Pembuatan Larutan Standar Al3+ 100 mg/L 27 3.3.2.3 Pembuatan Larutan Standar Al3+ 10 mg/L 27 3.3.2.4 Pembuatan Larutan Seri Standar Al3+ 0,0; 1,0;
2,0; 3,0; 4,0; 5,0; 6,0 dan 7,0 mg/L 27
3.3.3 Preparasi Larutan Sampel 28
3.3.4 Penentuan Kandungan Besi (Fe) secara SSA 28 3.3.5 Penentuan Kandungan Aluminium (Al)
secara Spektrofotometri 28
3.4 Bagan Penelitian 29
3.4.1 Pembuatan Kurva Kalibrasi Fe3+ 29
3.4.2 Pembuatan Kurva Kalibrasi Al3+ 29
3.4.3 Penyediaan Larutan Sampel 30
3.4.1 Penentuan Kuantitatif Besi (Fe) dengan
Spektrofotometer Serapan Atom 30
3.4.2 Penentuan Kuantitatif Aluminium (Al) dengan
Spektrofotometer UV-Vis 31
Bab 4. 4.1 Hasil Penelitian
4.1.1 Logam Besi 32
4.1.1.1 Penurunan Persamaan Garis Regresi dengan
Metode Kurva Kalibrasi untuk Fe3+ 32 4.1.1.2 Penentuan Koefisien Korelasi 34 4.1.1.3 Penentuan Kandungan Besi dalam Sampel 34
4.1.1.3.1 Penentuan Kandungan Besi dalam Air
4.1.2 Logam Aluminium 36 4.1.2.1 Penurunan Persamaan Garis Regresi dengan
Metode Kurva Kalibrasi untuk Al3+ 37 4.1.2.2 Penentuan Koefisien Korelasi 38 4.1.2.3 Penentuan Kandungan Aluminium dalam Sampel 38
4.1.2.3.1 Penentuan Kandungan Aluminium dalam
Air Minum dalam mg/L 39
4.2 Pembahasan 40
Bab 5. Kesimpulan dan Saran
5.1 Kesimpulan 46
5.2 Saran 46
DAFTAR TABEL
Nomor Judul Halaman
Tabel
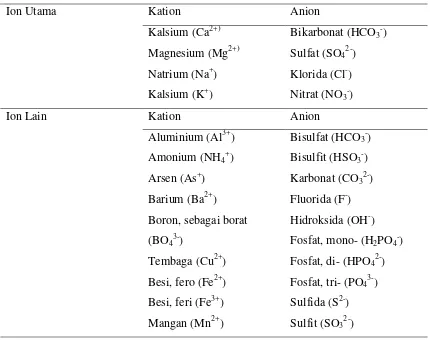
2.1 Jenis Ion Utama dan Ion Lain dalam Air 15
4.1 Data Hasil Pengukuran Absorbansi Besi pada Air PDAM
Cabang Sei Agul pada λspesifik = 248,3 nm 32 4.2 Data Hasil Penurunan Persamaan Garis Regresi untuk
Larutan Seri Standar Fe3+ 33
4.3 Data Hasil Pengukuran Absorbansi Aluminium pada Air
PDAM Cabang Sei Agul pada λspesifik = 535 nm 36 4.4 Data Hasil Penurunan Persamaan Garis Regresi untuk
DAFTAR GAMBAR
Nomor Judul Halaman
Gambar
2.1 Prekursor dan Produk Hujan Asam 12
DAFTAR LAMPIRAN
Nomor Judul Halaman
Lampiran
1 Data Hasil Pengukuran Absorbansi Larutan Seri Standar
Fe dengan SSA pada λspesifik = 248,3 nm 50
2 Data Hasil Pengukuran Absorbansi Larutan Seri Standar
Al dengan Spektrofotometer UV-Vis pada λspesifik = 535 nm 50
3 Kandungan Logam Fe dalam Sampel Air 50
4 Kandungan Logam Al dalam Sampel Air 50
5 Lampiran Peraturan Pemerintah No.82 Tahun 2001 51
6 Permenkes No.492/MENKES/PER/IV/2010 53
7 Kondisi Alat SSA merk AA-7000F pada Absorbansi Fe 54 8 Kondisi Alat Spektrofotometer UV-VIS Lamda 25
STUDI PERBANDINGAN KANDUNGAN BESI (Fe) DAN ALUMINIUM (Al) DIDALAM AIR MINUM YANG DIPRODUKSI OLEH PDAM
TIRTANADI PADA UNIT PRODUKSI CABANG SEI AGUL, MEDAN LABUHAN DAN SUNGGAL MEDAN
ABSTRAK
Telah dilakukan penelitian tentang studi perbandingan kandungan besi dan aluminium pada air minum yang diproduksi oleh PDAM Tirtanadi pada unit produksi cabang Sei Agul, Medan Labuhan dan Sunggal Medan. Sampel air minum diambil secara acak dari perumahan warga pada daerah sekitar cabang unit produksi. Penentuan kandungan logam Fe dilakukan dengan Spektrofotometer Serapan Atom (SSA) pada panjang gelombang 248,3 nm dan kandungan logam Al dilakukan dengan Spektrofotometer UV-Vis pada panjang gelombang 535 nm. Preparasi sampel untuk metode SSA adalah didestruksi basah dengan HNO3(p) dan sampel untuk spektrofotometri metode
aluminon dipreparasi dengan HCl(p). Dari hasil penelitian diperoleh kandungan Fe
dalam air minum pada unit produksi cabang Sei Agul, Medan Labuhan dan Sunggal masing – masing sebesar 7.016 mg/L; 1.145 mg/L dan 1.318 mg/L dan kandungan Al sebesar 49.677 mg/L; 81.256 mg/L dan 86.725 mg/L.
STUDY OF DIFFERENCE BETWEEN CONCENTRATION OF IRON (Fe) AND ALUMINIUM (Al) IN TAP WATER PRODUCED BY PDAM
TIRTANADI FROM SEI AGUL, MEDAN LABUHAN AND SUNGGAL MEDAN PRODUCTION UNITS
ABSTRACT
The research for study of difference between concentration of iron (Fe) and aluminium (Al) in tap water produced by PDAM Tirtanadi from Sei Agul, Medan Labuhan and Sunggal Medan production units. Tap water was taken randomly from civilian house near the production unit. The concentration of iron contained in tap water is analyzed by using Atomic Absorption Spectrophotometric Method at wavelength 248,3 nm and concentration of aluminium is analyzed by using Spectrophotometric Aluminon Method at wavelength 535 nm. Sample for Atomic Absorption Spectrophotometric Method is prepared by concentrated HNO3 and Sample for Spectrophotometric
Aluminon Method is prepared by concentrated HCl. The result of analysis of iron concentration in tap water produced by Sei Agul, Medan Labuhan and Sunggal Medan production units are 7.016 mg/L; 1.145 mg/L and 1.318 mg/L and aluminium concentration are 49.677 mg/L; 81.256 mg/L and 86.725 mg/L.
BAB 1
PENDAHULUAN
1.1. Latar Belakang
Air yang kita pergunakan setiap hari tidak lepas dari pencemaran yang diakibatkan oleh ulah manusia juga. Beberapa bahan pencemar seperti bahan mikrobiologik (bakteri, virus, parasit), bahan organik (pestisida, deterjen), dan beberapa bahan inorganik (garam, asam, logam), serta beberapa bahan kimia lainnya sudah banyak ditemukan dalam air yang kita pergunakan.(Darmono.1995).
Air bersih untuk keperluan publik umumnya dipasok oleh Perusahaan Daerah Air minum Daerah (PDAM). Hingga saat ini baru sebagian dari penduduk dapat memperoleh layanan PDAM tersebut akibat dari keterbatasan kemampuan perusahaan daerah tersebut. Unuk meningkatkan pelayanan, di beberapa kota besar dikelola oleh perusahaan swasta atau kerja sama antara PDAM dan perusahaan swasta.
Kebutuhan air bersih mengalami pertumbuhan lebih cepat dibandingkan dengan pertumbuhan kemampuan memasok air, sehingga secara relatif persentase penduduk yang dapat dilayani oleh PDAM semakin menurun. Akibatnya, pasokan air bersih lebih sering mengutamakan kuanitas (kecukupan) daripada mempertahankan mutu tinggi.
Sejak beberapa bulan terakhir ini, hal seperti diatas terjadi pada beberapa
Cabang PDAM Tirtanadi Medan, dimana kuantitatis air dan kualitas air yang dialirkan oleh PDAM sangat memprihatinkan.
melakukan pengaduan dan keberatan akan hal tersebut, namun kelihatannya belum ada perbaikan. Karena airnya masih tetap kotor, Menurut Pak Gultom bahwa air yang dipasok di wilayah Cabang Sei Agul bersumber dari Sumur Bor yang dibuat oleh PDAM Tirtanadi di jalan Sampul Gang Dos Roha Medan.
Hal yang serupa juga dialami oleh salah satu konsumen yang tinggal di daerah Belawan. Mereka menerima pasokan air dari unit produksi Cabang Medan Labuhan Medan. Air yang mereka peroleh juga kotor, penuh dengan endapan dan flok-flok berwarna coklatan kemerahan yang diduga merupakan hasil flokulasi yang tidak sempurna diendapkan dan disaring sebelum dialirkan ke konsumen.
Berdasarkan Penelitian Terdahulu, Alwin.(2007) telah melakukan penelitian berupa monitoring dan analisis kadar logam Aluminium dan Besi dalam sampel air yang diperoleh dari proses pengolahan air minum PDAM Tirtanadi Sunggal.Sampel diambil dari empat titik yaitu : Air Sungai Belawan, Air di Clarifier, Air di Reservoar dan Air Limbah. Monitoring dilakukan selama empat bulan dan hasil monitoring dan analisis terhadap kadar Aluminium adalah : Air Sungai Belawan berkisar 0,0737 s/d 0,172; Air di Clarifier 0,1894 s/d 0,2489; air di Reservoar 0,1740 s/d 0,2095; Air Limbah 0,2080 s/d 0,2326, kadar Besi adalah : Air Sungai Belawan 0,148 s/d 0,1775; Air di Clarifier 0,1935 s/d 0,2488; air di Reservoar 0,1789 s/d 0,2124; Air limbah 0,2124 s/d 0,2343.Hasil penelitian menunjukkan air dari proses pengolahan PDAM
Tirtanadi Sunggal memenuhi syarat kesehatan untuk diminum berdasarkan Parameter untuk logam Al dan Fe pada KEPMENKES RI No.907/MENKES/VII/2002.
1.2. Permasalahan
1. Berapakah kandungan logam Fe, dan Al didalam air minum yang diproduksi PDAM Tirtanadi Medan, pada unit produksi Cabang Sei Agul, Medan Labuhan dan Cabang Sunggal ?
2. Apakah Kandungan Fe dan Al didalam air minum yang diproduksi pada ketiga Cabang tersebut diatas telah memenuhi standar Peraturan Pemerintah No.82 tahun 2001 untuk air baku dan PERMENKES No.492/MENKES/PER/IV/2010 untuk air bersih ?
1.3. Pembatasan Masalah
2. Kandungan Logam yang ditentukan dalam penelitian ini dibatasi hanya untuk Fe dan Al.
3. Sampel air yang diambil untuk penelitian ini diambil langsung dari kran air dirumah penduduk di daerah unit produksi Sei Agul, Medan Labuhan dan Sunggal.
1.4. Tujuan Penelitian
Penelitian ini bertujuan untuk menentukan kandungan Fe dan Al didalam air minum
1.5. Manfaat Penelitian
Hasil penelitian merupakan informasi yang sangat bermanfaat bagi konsumen air PDAM Tirtanadi Medan pada ketiga cabang tersebut terutama tentang kandungan Fe dan Al didalam air yang mereka konsumsi setiap hari, apakah sudah memenuhi syarat sesuai dengan Peraturan Pemerintah No.82 tahun 2001 untuk air baku dan PERMENKES No.492/MENKES/PER/IV/2010 untuk air bersih.
1.6. Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Analitik FMIPA USU Medan, Laboratorium Baristand Medan, dan Laboratorium Pusat Penelitian Kelapa Sawit (PPKS) Medan.
1.7. Metodologi Penelitian
1. Penelitian ini merupakan Penelitian Laboratorium dan bersifat Purposif.
2. Sampel Air diambil secara acak dari air keran penduduk di wilayah pelayanan PDAM Tirtanadi Medan Cabang Sei Agul, Medan Labuhan dan Sunggal. 3. Pengukuran pH air langsung dilakukan pada saat pengambilan sampel.
4. Kandungan logam Fe ditentukan dengan menggunakan SSA pada λ=248,3 nm
di Laboratorium Baristand Medan.
5. Kandungan logam Al dilakukan secara Spektroktrofotometri λ=535 nm di
BAB 2
TINJAUAN PUSTAKA
2.1. Air
Air adalah zat yang dibutuhkan oleh semua makhluk hidup termasuk manusia, hewan serta tumbuh – tumbuhan. Manfaat air bermacam – macam misalnya untuk diminum, pembawa zat makanan, zat pelarut, pembersih dan lain sebagainya. Oleh karena itu penyediaan air bersih merupakan salah satu kebutuhan utama bagi manusia untuk kelangsungan hidupnya dan menjadi faktor penentu dalam kesehatan dan kesejahteraan masyarakat.
Air bersih mutlak diperlukan, karena merupakan salah satu media dari
berbagai macam penularan penyakit, terutama penyakit – penyakit perut. Dari penelitian – penelitian yang dilakukan, bahwasanya penduduk yang menggunakan air
bersih mempunyai kecenderungan lebih kecil untuk menderita sakit dibandingkan dengan penduduk yang tidak menggunakan air bersih. Melalui penyediaan air bersih, baik dari segi kualitas maupun kuantitasnya disuatu daerah, diharapkan dapat menghambat penyebab penyakit menular. Agar air yang masuk ke dalam tubuh manusia berupa minuman maupun makanan tidak mengandung bibit penyakit, maka pengolahan air baik yang berasal dari sumber air dan jaringan transmisi ataupun distribusi adalah sangat diperlukan. (Sastrawijaya,A.T. 2000)
Air yang tersebar di alam tidak pernah terdapa dala bentuk murni, tetapi bukan semua air sudah terpolusi. Sebagai contoh meskipun daerah pegunungan atau hutan yang terpencil dengan udara yang bersih dan bebas dari polusi, air hujan selalu mengandung bahan – bahan terlarut seperti CO2, O2, dan N2 serta bahan – bahan
2.1.1. Sifat Air
Air memiliki karakteristik yang khas yang tidak dimiliki oleh senyawa kimia yang lain. Karakteristik tersebut adalah sebagai berikut :
1. Pada kisaran suhu yang sesuai bagi kehidupan, yakni 0oC (32oF) – 100oC, air berwujud cair. Suhu 0oC merupakan titik beku (freezing point) dan suhu 100oC merupakan titik didih (boiling point) air. Tanpa sifat tersebut, air yang terdapat di dalam jaringan tubuh makhluk hidup maupun air yang terdapat di laut, sungai, danau, dan badan air yang lain akan berada dalam bentuk gas atau, sehingga tidak akan terdapat kehidupan di muka bumi ini, karena sekitar 60% - 90% bagian sel makhuk hidup adalah air.
2. Perubahan suhu air berlangsung lambat sehingga air memiliki sifat sebagai penyimpanan panas yang sangat baik. Sfat ini memungkinkan air tidak menjadi panas ataupun dingin dalam seketika. Perubahan suhu air yang lambat mencegah terjadinya stress pada makhluk hidup karena adanya perubahan suhu yang mendadak dan memlihara suhu bumi agar sesuai bagi makhluk hidup. Sifat ini juga menyebabkan air sangat baik digunakan sebagai pendingin mesin.
3. Air memerlukan panas yang tinggi dalam proses penguapan. Penguapan (evaporasi) adalah proses perubahan air menjadi uap air. Proses ini memerlukan energi panas dalam jumlah yang besar. Sebaliknya, proses perubahan uap air ini menjadi cairan (kondensasi) melepaskan energi panas yang besar. Pelepasan energi ini
merupakan salah satu penyebab mengapa kita merasa sejuk pada saat berkeringat. Sifat ini juga merupakan salah satu faktor utama yang menyebabkan terjadinya penyebaran panas secara baik di bumi.
5. Air memiliki tegangan permukaan yang tinggi. Suatu cairan dikatakan memiliki tegangan permukaan yang tinggi jika tekanan antar-molekul cairan tersebut tinggi. Tegangan permukaan yang tinggi menyebabkan air memiliki sifat membasahi suatu bahan secara baik (higher wetting ability). Tegangan permukaan yang tinggi juga memungkinkan terjadinya sistem kapiler, yaitu kemampuan untuk bergerak dalam pipa kapiler (pipa dengan lubang yang kecil). Dengan adanya sistem kapiler dan sifat sebagai pelarut yang baik, air dapat membawa nutrien dari dalam tanah ke jaringan tumbuhan (akar, batang, dan daun). Adanya tegangan permukaan memungkinkan beberapa organisme, misalnya jenis-jenis insekta, dapat merayap di permukaan air.
6. Air merupakan satu-satunya senyawa yang merenggang ketika membeku. Pada saat membeku, air merenggang sehingga es memiliki nilai densitas (massa/volume) yang lebih rendah daripada air. Dengan demikian, es akan mengapung di air. Sifat ini mengakibatkan danau-danau di daerah yang beriklim dingin hanya membeku pada bagian permukaan (bagian di bawah permukaan masih berupa cairan) sehingga kehidupan organisme akuatik tetap berlangsung. Sifat ini juga dapat mengakibatkan pecahnya pipa air pada saat ai di dalam pipa membeku. Densitas (berat jenis) air maksimum sebesar 1g/cm3 terjadi pada suhu 3,95oC. Pada suhu lebih besar maupun lebih kecil dair 3,95oC, densitas air lebih kecil dari satu (Moss,1993; Tebbut 1992).
2.2. Sumber Air
Saat ini, air merupakan sumber daya terbatas yang harus dikelola. Sumber air untuk berbagai keperluan berasal dari air permukaan (sungai, danau, dan waduk) dan air tanah. Sumber air tersebut pada hakikatnya berasal dari air dikenal sebagai air tanah. Jika air tanah dalam kondisi tekanan tinggi, air tanah tersebut dapat mengalir ke permukaan tanah secara otomatis sebagai mata air (spring).
Siklus hidrologi air tergantung pada proses evaporasi dan presipitasi air yang terdapat di permukaan bumi berubah menjadi uap air di lapisan atmosfer melalui proses evaporasi (penguapan) air sungai, danau, dan laut; serta proses evapotranspriasi atau penguapan air oleh tanaman. Uap air bergerak ke atas hingga membentuk awan yang dapat berpindah karena tiupan angin. Ruang udara yang mendapat akumulasi uap air secara kontinu akan menjadi jenuh. Oleh pengaruh udara dingin pada lapisan atmosfer, uap air tersebut mengalami sublimasi sehingga butiran-butiran uap air membesar dan akhirnya jatuh sebagai hujan. Zat yang bersifat higroskopis (menyerap air) dapat mempercepat integrasi pengikatan molekul uap air menjadi air. Sehingga, pada pembuatan hujan buatan, dilakukan penambahan zat yang bersifat higroskopis terhadap awan (NaCl atau urea).
Proses evaporasi yang berlangsung di laut lebih banyak daripada proses evaporasi di perairan daratan. Di laut, proses evaporasi juga melebihi proses prespitasi sehingga lautan meruakan sumber air utama bagi proses presipitasi. Sebaliknya, di daratan proses presipitasi lebih banyak daripada evaporasi. Di daratan, sekitar 50% air yang diperoleh melalui presipitasi akan mengalami evaporasi; dan sisanya tersimpan di danau, sungai, maupun sebagai air tanah. (Effendi.2003).
2.2.1. Air Permukaan
Air tawar berasal dari dua sumber, yaitu air permukaan (surface water) dan air tanah
(ground water). Air permukaan adalah air yang berada di sungai, danau, waduk, rawa,
Air hujan yang jatuh ke bumi dan menjadi air permukaan memiliki kadar bahan-bahan terlarut atau unsur hara yang sangat sedikit. Air hujan biasanya bersifat asam, dengan nilai pH sekitar 4,2. Hal ini disebabkan air hujan melarutkan gas-gas yang erdapatdi atmosfer, misalnya gas karbondioksida (CO2), sulfur (S), dan nitrogen
oksida (NO2) yang dapat membentuk asam lemah (Novotny dan Olem.1994).
Air permukaan selama ini merupakan sumber air baku utama untuk keperluan domestik. Air tanah mudah tercemar oleh kegiatan pertanian, peternakan, pemukiman, dan industri, sehingga air menjadi keruh dan kadang-kadang berbau. Akibat dari pencemaran tersebut, air permukaan membutuhkan pengolahan yang ekstensif dan membutuhkan biaya lebih tinggi dibandingkan pengolahan air tanah.
Berbagai kegiatan dapat berkontrbusi pada pencemaran air permukaan. Bergantung lokasi badan air, sumber kontaminan air permukaan umumnya berasal dari limbah industri, limbah domestik, limpasan air hujan dari pemukiman, limbah pertanian dan peternakan, erosi tanah, atau limbah rumah sakit. Jenis kontaminan air permukaan mencakup organisme patogen bahan organik dan minyak, nutrien (N dan P), bahan organik sintetik/toksik, bahan anorganik, sedimen, bahan radioaktif atau panas.
Pencemaran nutrien, misalnya dari limbah domestik dapat menyebabkan
Air laut tersedia dalam jumlah yang hampir tidak terbatas, tetapi biaya pengolahan sangat tinggi (2-5 kali lebih tinggi daripada pengolahan air tawar). Untuk menghilangkan garam terlarut dalam air laut biasanya digunakan desalinasi (destilasi, diaslisis dan reverse osmosis), pengolahan air laut sebagai sumber air bersih banyak dilakukan di negara – negara timur tengah.
Air di wilayah bergambut dikenal sebagai air gambut. Ciri mencolok air gambut adalah berwarna merah kecokelatan, kandungan bahan organik tinggi, keasaman tinggi (pH rendah sekitar 2 – 5). Di daerah tertentu, air gambut sering menjadi satu – satunya sumber air masyarakat di daerah bergambut.
2.2.2. Air Tanah
Air tanah memasok sebagian besar kebutuhan air domestik umat manusia, termasuk di negara – negara maju seperti Amerika Serikat, sebagian besar penduduknya mengambil air bersih dari air tanah. Air tanah dapat digunakan untuk berbagai tujuan dengan pengolahan yang minimal. Air tanah umumnya relatif jernih akibat efek penyaringan pori – pori tanah.
Air tanah tidak dapat dilihat dengan mudah oleh manusia. Hal ini menyebabkan air tanah kurang diperhatikan. Laju penggunaan/pengambilan air tanah
dibatasi oleh laju infiltrasi air di dalam tanah. Polutan dapat/tidak dapat dipasahkan dari air karena “efek filtrasi” tah bergantung pada tipe tanah dan tipe polutan (terlarut/tersuspensi).
Air tanah selama ini telah digunakan untuk memenuhi kebutuhan berbagai kegiatan, seperti perumahan dan industri. Namun di beberapa daerah penggunaan air sudah melampaui daya dukungnya, sehingga mengalami berbagai masalah seperti penurunan permukaan air, permukaan tanah, dan intrusi. Beberapa wilayah air tanah juga telah mengalami pencemaran oleh eschericia coli dan logam berat dari pemukiman, pembuangan sampah atau limbah industri.
Air tanah dipengaruhi oleh hujan, terutama hujan asam. Air hujan mempengaruhi tingkat kesadahan air, sebagaimana ditunjukkan pada Gambar. Pada saat air hujan masuk ke dalam lapisan tanah bagian atas (top soil), bakteri tanah meningkatkan kadar karbon dioksida selama proses respirasinya. Karbon dioksida dengan air membentuk asam karbonat. Batuan kapur yang terbentuk dari padatan kalsium karbonat dan magnesium karbonat bereaksi dengan asam karbonat membentuk Ca(HCO3)2 dan Mg(HCO3)2. Gibsum (CaSO4) dapat juga terdapat dalam
struktur lapisan tanah yang berakibat pada pembentukan kesadahan non-karbonat (Davis dan Cornwell. 1991).
2.2.3. Air Hujan
Air hujan berasal dari penguapan air permukaan. Air hujan sebagian bersar menguap balik ke atmosfer atau mengalir langsung ke sungai, sebagian lagi ke dalam tanah
menuju air tanah. Air hujan bersifat asam, mengandung partikel/debu dan polutan lain dari emisi. Karakteristik air hujan sangat dipengaruhi oleh kondisi pencemaran udara setempat. Air hujan berpotensi digunakan untuk daerah dataran tinggi atau daerah langka air permukaan dan air tanah.
Pencemaran air tidak hanya terjadi pada saat air berada di dalam atau di permukaan tanah, tetapi juga dapat terjadi pada saat air berada di udara (atmosfer). Pada saat air di udara, air bereaksi dengan karbon dioksida dan membentuk asam karbonat, sehingga air hujan bersifat asam, sesuai dengan persamaan reaksi :
2-Titik kesetimbangan pH air hujan bersih adalah sekitar pH 5,6. Nilai pH air hujan dapat mencapai 3,0 dan dapat berpengaruh negatif pada bangunan-bangunan dan produktivitas pertanian.
Reaksi kimia di dalam atmosfer mengonversi SO2, NOx, dan senyawa organik
yang mudah menguap (volatile organic carbons/VOCs) menjadi asam atau oksidan terkait sebagaimana diilustrasikan pada Gambar. Konversi utama sulfur dioksida adalah melalui reaksi prekursor dengan hidrogen peroksida dalam awan. Asam nitrat terbentuk reaksi NO2 dengan radikal OH yang terbentuk secara fotokimia. Ozon
terbentuk melalui proses yang melibatkan NOx dan VOCs.
Gambar 2.1. Prekursor dan produk hujan asam (Davis dan Cornwell.1991)
Perhatian pada hujan asam diberikan pada pengaruhnya terhadap kehidupan akuatik, kerusakan pada tanaman dan hutan (produktivitas tanaman), serta kerusakan pada bahan bangunan atau properti. Nilai pH yang rendah berpengaruh langsung pada ikan melalui gangguan pada siklus reproduksi atau pengaruh tidak langsung melalui pelarutan logam-ogam yang bersifat toksik. Nilai pH yang sangat rendah juga dapat memengaruhi produktivitas hasil pertanian, perikanan dan peternakan.
SO2 H2SO4 (Asam Sulfat)
NOx HNO3 (Asam Nitrat)
NOx + VOCs O3 (Ozon)
VOCs H2O2 (Hidrogen Peroksida)
H2O2 + O3 (dalam awan)
OH + O2 (dalam udara)
Oksidan (Permukaan basah)
Sinar matahari OH (dalam udara)
Sinar matahari
Parameter penting mutu air hujan mencakup pH, konduktivitas, TDS, kesadahan, kalsium, magnesium, klorida, dan Natrium (DST.2006). WHO merekomendasikan nilai parameter tersebut untuk air mium berturut-turut : 7-8,5, 500, 100, 75, 30, dan 200mg/l. WHO tidak mencantumkan persyaratan parameter natrium untuk air minum.
2.3. Kontaminan Air
2.3.1. Kontaminan Fisik
Air yang bersih adalah jernih, tidak berwarna, dan tidak berbau. Kebanyakan air mengandung bahan terlarut, tersuspensi, atau dalam bentuk koloid. Pengukuran secara
kuantitatif karakteristik tersebut adalah penting untuk penentuan mutu air. Kontaminan fisik meliputi kekeruhan, warna, bau dan rasa, padatan, serta suhu.
2.3.1.1. Kekeruhan
Kekeruhan (turbidity) merupakan karakteristik air yang terlihat pertama kali tentang kondisi air. Kekeruhan dapat dijadikan indikator mutu air. Air tampak keruh jika dalam air tersebut terdapat partikel-partikel tersuspensi atau koloid seperti tanah, bahan organik terdispersi, plankton, dan bahan anorganik lainnya. Air dengan tingkat kekeruhan tinggi sering terkait dengan tingginya kandungan mikroorganisme penyebab penyakit seperti virus, parasit, dan beberapa jenis bakteri.
2.3.1.2. Warna
2.3.1.3. Bau dan Rasa
Bau (odor) dan rasa (taste) dalam air dapat disebabkan oleh bahan-bahan asing yang masuk ke dalam air seperti senyawa organik, garam-garam anorganik, atau gas terlarut. Bahan-bahan tersebut dapat berasal dari berbagai sumber seperti kegiatan pertanian, domestik, industri atau sumber alami. Bau air sering berhubungan dengan proses pembusukan bahan organik dalam kondisi anaerobik yang menghasilkan gas H2S, amonia (NH3), amina, diamina, merkaptan, sulfida organik, dan skatol.
2.3.1.4. Padatan
Semua kontaminan air selain gas-gas terlarut, berkontribusi terhadap beban padatan dalam air tersebut, baik padatan terendapkan, tersuspensi, koloid, maupun terlarut. Padatan di dalam air dapat diklasifikasikan berdasarkan ukuran dan keadaannya, sifat-sifat kimia dan distribusi ukurannya. Bahan padatan dalam air dapat diklasifikasikan berdasarkan ukuran dan keadaannya seperti padatan terendapkan (> 10-2 mm), tersuspensi (> 10-3 mm), koloid (10-6 – 10-3 mm) atau terlarut (< 10-6 mm).
Kadar padatan dapat digunakan untuk menganalisis potensi penggunaan air dan untuk menentukan jenis proses yang paling sesuai untuk pengolahannya. Uji padatan terlarut (total dissolved solids/TDS) sering digunakan untuk menganalisis
sumber air untuk keperluan domestik, industri dan pertanian. Padatan terendapkan digunakan untuk menentukan padatan yang dapat mengendap secara gravitasi dalam periode waktu tertentu.
2.3.1.5. Suhu
2.3.2. Kontaminan Kimiawi
Pengukuran kadar bahan kimia dalam air untuk menentukan mutu air mencakup analisis keberadaan ion-ion spesifik (seperti kalsium, magnesium, dan timbal) atau pengukuran bahan kimia secara agregat (seperti alkalinitas, kesadahan, dan bahan organik).
2.3.2.1. Ion dalam Air
Air secara alami mengandung ion-ion terlarut. Berbagai jenis ion yang mungkin ada dalam air tanah atau air permukaan disajikan pada Tabel 2.1. Jenis ion yang banyak ditemui dalam air tanah adalah bikarbonat, sulfat, klorida kalsium, magnesium, dan natrium. Ion-ion tersebut kebanyakan berasal dari kontak air dengan berbagai deposit mineral di dalam tanah, tetapi beberapa jenis ion seperti amonium, karbonat, dan sulfida sering dihasilkan dari aktivitas bakteri dan mikroalga.
Tabel 2.1. Jenis ion utama dan ion lain dalam air (Chapman dan Kimstach.1997)
2.3.2.2. Jenis Non-ionik dalam Air
Mineral non-ionik yang sering terdapat di dalam permukaan air alami dan air tanah adalah silika (SiO2). Konsenterasi silika dalam air dapat berkisar antara 1 sampai 120
mg/L. Keberadaan silika dalam air dapat menyebabkan berbagai masalah, terutama dalam aplikasi unuk industri karena silika menyebabkan pembentukan kerak (scaling) dalam boiler dan alar pemindah panas (heat exchanger).
2.3.2.3. Gas Terlarut
Berbagai jenis gas seperti oksigen (O2), nitrogen (N2), karbondioksida (CO2), asam
sulfida (H2S), nitrogen oksida (NOx), ammonia (NH3), asam sianida (HCN), dan
sulfur dioksida (SO2) dapat terlarut di dalam air.
2.3.2.4. Logam Berat
Berbagai jenis logam berat terlarut bersifat toksik, seperti arsem (As), barium (Ba), kadmium (Cd), krom (Cr), timbal (Pb), merkuri (Hg), selenium (Se), dan perak (Ag). Logam-logam tersebut bersifat persisten, tidak dapat didegradasi secara biologis, serta bersifat bioakumulasi. Karakteristik ini menyebabkan tingkat toksisitas di dalam makhluk hidup (termasuk manusia) meningkat dengan bertambahnya waktu.
2.3.3. Kontaminan Mikrobiologis
Bakteri, virus, dan hewan kecil lainya pada dasarnya selalu ada di dalam air permukaan. Organisme tersebut kadang-kadang juga terdapat di dalam air tanah. Meskipun kebanyakan mikrooranisme di dalam lingkungan air sebenarnya tidak berbahaya, tetapi sebagian kecil mikrooganise yang ada di lingkungan tergolong mikroorganisme patogen dan dapat menyebabkan penyakit pada manusia. Jika jenis organisme ini terdapat di dalam sistem distribusi air bersih komunal, bahaya epidemi dapat terjadi. Oleh karena itu, sistem penyediaan air minum tidak boleh mengandung organisme patogen.(Suprihatin.2013)
2.4. Koagulasi dan Flokulasi dalam Pengolahan Air
Ukuran kecil daripada partikel koloid di dalam air, diikuti dengan fakta bahwa muatan negatif yang tersebar pada permukaan koloid, berarti bahwa suspensi koloid adalah sangat stabil.
Koagulasi dan flokulasi sering digunakan dalam pengolahan air minum dan preparasi air yang digunakan untuk industri. Teknik ini menetralisir muatan koloid di dalam air, dan mengabsorbsi mereka kedalam permukaan daripada presipitat yang terbentuk saat flokulasi. Substansi terlarut tertentu juga dapat diabsorbsi ke dalam flok
(materi organik, berbagai polutan, dll).(Degremont.1979)
2.4.1. Koagulasi
Koagulan adalah bahan-bahan atau substansi (senyawa kimia) yang ditambahkan ke dalam air untuk menghasilkan efek koagulasi. Sifat dan syarat penting koagulan adalah sebagai berikut (Davis dan Cornwell.1991).
a. Kation trivalen. Kation trivalen merupakan kation yang paling efektif untuk menetralkan muatan listrik koloid.
b. Tidak toksik. Persyaratan ini diperlukan untuk mnghasilkan air atau air limbah hasil pengolahan yang aman.
c. Tidak larut dalam kisaran pH netral. Koagulan yang ditambahkan harus terpresipitasi dari larutan, sehingga ion-ion tersebut tidak tertinggal dalam air.
2.4.1.1. Alum
Reaksi yang terjadi ketika alum ditambahkan ke dalam air yang mengandung alkalinitas adalah :
Al2(SO4)3.14H2O + 6 HCO3- 2 Al(OH)3(s) + 6 CO2 + 14 H2O + 3 SO4
2-Setiap mol alum yang ditambahkan akan menggunakan 6 mol alkalinitas dan menghasilkan 6 mol karbon dioksida. Reaksi tersebut akan mengubah kesetimbangan karbonat dan akan menurunkan pH. Namun, penurunan pH tidak terjadi secara drastis dan secara operasional koagulasi tidak bermasalah.
Reaksi yang terjadi ketika alum ditambahkan ke dalam air yang tidak mengandung alkainitas adalah:
Al2(SO4)3.14H2O 2 Al(OH)3(s) + 3 H2SO4 + 8 H2O
2.4.1.2. Besi
Besi dapat diperoleh dari garam sulfat Fe2(SO4)3.H2O atau garam klorida FeCl3.XH2O
yang tersedia dalam bentuk padatan atau larutan. Reaksi FeCl3 dalam air yang
mengandung alkalinitas adalah:
FeCl3 + 3 HCO3- Fe(OH)3(s) + 3 CO2 + 3 Cl
-Dan reaksinya dalam air yang tidak mengandung alkalinitas adalah:
FeCl3 + 3 H2O Fe(OH)3(s) + 3 HCl
2.4.2. Flokulasi
Flokulasi merupakan pembentukan flok-flok dari partikel-partikel kecil yang telah mengalami koagulasi. Untuk menghasilkan flokulasi yang lebih baik, biasanya dibantu dengan penambahan bahan-bahan pembantu koagulan atau disebut juga flokulan.
Ada empat jenis flokulan yang biasa digunakan, yaitu pengatu pH, silika aktif,
clay, dan polimer. Asam dan basa digunakan untuk mengatur pH air, sehingga kisaran
pH optimal koagulasi tercapai. Asam yang biasa digunakan adalah H2SO4. Kapur
[Ca(OH)2] atau soda abu (Na2CO3) digunakan untuk meningkatkan nilai pH.
Silika aktif dan clay memiliki muatan listrik sedikit negatif dan dapat bergabung dengan muatan listrik positif dari flok-flok alum atau besi. Dengan demikian, hal tersebut akan menghasilkan flok yang lebih besar yang akan mengendap lebih cepat.
Efisiensi koagulasi dan flokulasi dipengaruhi oleh beberapa faktor, yaitu konsenterasi dan jenis zat tersuspensi, pH, konsenterasi dan jenis flokulan, waktu dan kecepatan pengadukan, serta adanya beberapa macam ion terlarut tertentu (seperti fosfat, sulfat, dan sebagainya).
Dua faktor penting dalam penambahan koagulan adalah pH dan dosis koagulan. Dosis dan pH optimum ditentukan dari percobaan laboratorium menggunakan jar test. Kisaran pH optimum untuk alum adalah 5,5-6,5, koagulasi mungkin juga terjadi antara pH 5 dan 8. Garam feri memiliki kisaran pH untuk koagulasi efektif yang lebih besar daripada alum, yaitu pH 4-9.
Koagulasi dan flokulasi terdiri atas tiga tahap berikut.
a. Pelarutan pereaksi (reagen) melalui pengadukan cepat (misalnya 1 menit, 100 rpm), bila perlu pembubuhan bahan kimia (sesaat) untuk menyesuaikan pH. b. Pengadukan lambat untuk membentuk flok-flok (misalnya 15 menit, 20-40
rpm). Pengadukan terlalu cepat dapat merusak kembali flok yang telah terbentuk.
c. Pengendapan (sedimentasi) flok-flok yang terbentuk (misalnya 15 menit atau 30 menit, 0 rpm).(Suprihatin.2013)
2.5. Aluminium
Di perairan, aluminium (Al) biasanya terserap ke dalam sedimen atau mengalami presipitasi. Aluminium dan bentuk oksida aluminium bersifat tidak larut. Akan tetapi, garam-garam aluminium sangat mudah larut. Sumber utama aluminium adalah mineral aluminosilicate yang terdapat pada batuan dan tanah secara melimpah. Pada proses pelapukan batuan, aluminium berada dalam bentuk residu yang tidak larut, misalnya bauxite. Aluminium banyak digunakan di pabrik kertas, dyes, penyamakan, dan percetakan. Aluminium yang berupa alum [Al2(SO4)3.4H2O] digunakan sebagai
Aluminium merupakan unsur yang tidak berbahaya. Perairan alami biasanya memiliki kandungan aluminium kurang dari 1,0 mg/liter. Perairan asam (acidic) memiliki kadar aluminium yang lebih tinggi. Menurut Canadian Council of Resource and Environment Ministers (1987), untuk memelihara kehidupan organisme akuatik, kadar aluminium sebaiknya tidak lebih dari 0,005 mg/liter bagi perairan dengan pH < 6,5 dan tidak lebih dari 0,1 mg/liter (McNeely et al., 1979). Perairan bagi keperluan pertanian sebaiknya memiliki kadar aluminium sekitar 5,0 mg/liter. Kadar aluminium untuk keperluan air minum sekitar 0,2 mg/liter (WHO,1984 dalam Moore,1991). Bagi kepentingan industri, misalnya pembangkit listrik tenaga uap, kadar aluminium perairan tidak lebih dari 0,1 mg/liter.
Percobaan toksisitas aluminium terhadap avertebrata Chrinomus anthronicus
dan Chaoborus punctipennis menunjukkan bahwa kadar aluminium 1 mg/liter pada perairan dengan pH 3,5-6,5 tidak mengakibatkan terjadinya peningkatan mortalitas. Percobaan dengan menggunakan Daphnia catawba dan Holopedium gibberium
sebagai organisme uji memperlihatkan adanya peningkatan mortalitas (Havas dan Likens.1985 dalam Canadian Councl of Resource and Environment Ministers.1987). Pada perairan yang bersifat asam (pH sekitar 4,4-5,4), aluminium bersifat lebih toksik. Toksisitas aluminium maksimum terjadi pada pH 5,0-5,2 (Schofield dan Trojnar,1980 dalam Canadian Council of Resource and Environment Ministers,1987).
2.6. Besi
Pada pH sekitar 7,5-7,7 ion ferri mengalami oksidasi dan berikatan dengan hidroksida membentuk Fe(OH)3 yang bersifat tidak larut dan mengendap (presipitasi)
di dasar perairan, membentuk warna kemerahan pada substrat dasar. Oleh karena itu, besi hanya ditemukan pada perairan yang berada dalam kondisi anaerob (anoksik) dan suasana asam (Cole.1988).
Kadar besi pada perairan yang mendapat cukup aerasi (aerob) hampir tidak perna lebih dari 0,3 mg/liter (Rump an Krist, 1992). Kadar besi pada perairan alami berkisar antara 0,05 – 0,2 mg/liter (Boyd,1988). Pada air tanah dalam dengan kadar oksigen yang rendah , kadar besi dapat mencapai 10 – 100 mg/liter, sedangkan pada perairan laut sekitar 0,01 mg/liter. Air hujan mengandung besi sekitar 0,05 mg/liter (McNeely et al., 1979). Kadar besi > 1,0 mg/liter dianggap membahayakan organisme akuatik (Moore,1991). Air yang di peruntukkan bagi air minum sebaiknya memiliki kadar besi kurang dari 0,3 mg/liter (Moore,1991; Sawyer dan McCarty,1978) dan perairan yang diperuntukkan bagi keperlua pertanian sebaiknya kadar besi tidak lebih dari 20 mg/liter (McNeely et al.,1979).
2.7. Destruksi
Destruksi merupakan suatu cara perlakuan (perombakan) senyawa menjadi unsur-unsur sehingga dapat dianalisa. Metode destruksi materi organik dapat dilaukan
dengan dua cara yang selama ini dikenal dengan : 1. Metode destruksi basah
2. Metode destruksi kering
Ada tiga macam cara kerja destruksi basah dapat dilakukan, yaitu : 1. Destruksi basah mengunakan HNO3 dan H2SO4
2. Destruksi basah menggunakan HNO3, H2SO4, dan HClO4
3. Destruksi basah menggunakan HNO3, H2SO4, dan H2O2 (Apriyanto,1989)
Destruksi kering merupakan penguraian (perombakan) senyawa organik dalam sampel menjadi anorganik dengan jalan pengabuan sampel dan memerlukan suhu pemanasan tertentu (Raimon.1992).
2.8. Spektrofotometri
Warna adalah salah satu kriteria untuk mengindentifikasi suatu objek. Karena tiap spesies kimia mempunyai tingkatan- tingkatan energi yang berbeda, maka transmisi perubahan energinya juga berbeda. Dasar analisis spektroskopi adalah interaksi radiasi dengan spesies kimia. Selama analisis spektrokimia, perlu sekali digunakan cahaya dari satu panjang gelombang, yaitu radiasi monokromatis (Khopkar.2008).
Spektrofotometer adalah suatu alat yang dimana pita gelombang diukur yang dipilih dari sinar putih yang sesuai untuk dipancarkan. Pembacaanya bisa secara visual ataupun dengan alat fotolistrik. Spektrofotometri adalah pengukuran terhadap energi radiasi, baik berupa emisi, transmitansi, ataupun refleksi sebagai suatu fungsi
gelombang. Metode pengaturan intensitas sinar diurutkan berdasarkan penurunan relatif kepentingan : (1) jenis celah, (2) jenis pemecahan, (3) jenis polarisasi, dan (4) jenis jaraknya. Tiga yang pertama diaplikasikan dala instrumen baik spektrofotometer atau fotometer penyaring (Snell.1961).
2.9. Spektrofotometri Serapan Atom
Menurut Khopkar (1990) metode Spektrofotometri Serapan Atom memiliki beberapa keunggulan jika dibandingkan dengan metode-metode lain, yaitu :
1. Meningkatkan untuk menentukan konsenterasi hampir semua unsur pada tingkat runut
2. Kecepatan analisis dan ketelitian yang akurat sehingga tidak diperlukan pemisahan 3. Sebelum pengukuran tidak perlu dilakukan pemisahan unsur yang akan ditentukan
walaupun dalam sampel terdapat banyak unsur
2.9.1 Prinsip Kerja Spektrofotometri Serapan Atom
Prinsip spektrofotometri serapan atom didasarkan oleh adanya panjang gelombang terentu oleh atom-atom dalam keadaan dasar. Bila satu atom pada keadaan dasar diberi suatu radiasi, akan terjadi peristiwa eksitasi yaitu peristiwa dimana elektron -elektron dari keadaan dasar akan pindah ke tingkat energi yang lebih tingi. Atom akan membutuhkan energi pada saat eksitasi, energi ini didapat melalui penyerapan radiasi pada panjang gelombang tertentu, energi radiasi yang diserap akan sebanding dengan jumlah atom pada keadaan dasar yang menyerap radiasi tersebut. Dengan mengukur besarnya energi yang diserap (A) pada tabel media yang tetap (b), besarnya konsenterasi (c) dari suatu materi dapat ditentukan. Hukum Lambert Beer menyatakan : “ Besarnya absorbansi sebanding dengan tebal medium dan konsenterasinya pada
panjang gelombang tertentu” atau secara matematis ditulis sebagai A = ε . b . c dengan
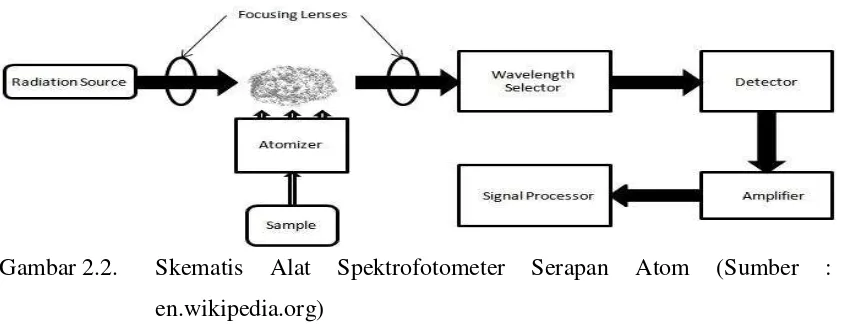
ε adalah koefisien ekstinsi molar. Suatu Spektrofotometer terdiri dari : sumber radiasi,
pembakar, monokromator, detektor dan pencatat (Raharjo.2002).
Secara Skematis Alat SSA dapat digambarkan sebagai berikut :
BAB 3
METODE PENELITIAN
3.1. Alat
- Atomic Absorbtion Spectrophotometer AA 7000-F
- Spektrophotometer UV-VIS Lamda 25
- Neraca Analitk Shimadzu ATX 224
- Hot plate Fisher
- Bola karet - Pipet tetes - Pengaduk Kaca
- Indikator pH Universal - Spatula
- Kertas saring Whatman No.42
- Kaca Arloji Pyrex
- Labu ukur Pyrex
- Corong Pyrex
- Beakerglass Pyrex
- Pipet volume Pyrex
- Maat Pipet Pyrex
3.2. Bahan
- HNO3(p) p.a(E. Merck)
- HCl 37% (p) p.a(E. Merck)
- Asam Asetat Glacial p.a(E. Merck)
- Aluminon 0,1% p.a(E. Merck)
- CH3COONH4 p.a(E. Merck)
- NH4OH 10% p.a(E. Merck)
- (NH4)2Fe(SO4)2.6H2O p.a(E. Merck)
- Al2(SO4)3.18H2O extra pure
- KMnO4 0,1N p.a(E.Merck)
3.3 Prosedur Penelitian
3.3.1. Pembuatan Larutan Standar Fe3+
3.3.1.1. Larutan Standar Fe3+ 1000 mg/L
Sebanyak 50 mL aquadest dimasukkan kedalam beakerglass, ditambahkan 20 mL H2SO4(p) secara perlahan – lahan ke dalam beakerglass.
Sebanyak 7,0219 g (NH4)2Fe(SO4)2.6H2O dimasukkan kedalam beakerglass
yang telah berisi campuran aquadest dan H2SO4(p), diaduk hingga seluruh kristal larut
sempurna, dimasukkan ke dalam labu ukur 1000 mL, ditambahkan KMnO4 0,1N
setetes demi setetes sampai diperoleh warna merah muda, ditambahkan aquadest hingga garis tanda dan dihomogenkan.
3.3.1.2. Larutan Standar Fe3+ 100 mg/L
3.3.1.3. Larutan Standar Fe3+ 10mg/L
Dipipet sebanyak 10 mL larutan induk Fe3+ 100 mg/L dan dimasukkan kedalam labu ukur 100 mL. Ditambahkan aquadest hingga garis tanda dan dihomogenkan.
3.3.1.4. Larutan Seri Standar Fe3+ 0,0; 0,5; 1,0; 1,5; 2,0; 2,5 mg/L
Dipipet sebanyak 0,0 ; 2,5 ; 5,0 ; 7,5 ; 10,0 dan 12,5 mL laruan Fe3+ 10 mg/L dan dimasukkan masing- masing kedalam labu ukur 50 mL, di buat sampai pH=3, ditambahkan aquadest sampai garis tanda dan dihomogenkan.
3.3.2. Pembuatan Larutan Standar Al3+
3.3.2.1. Larutan Standar Al3+ 1000 mg/L
Sebanyak 24,7005 g Al2(SO4)3.18H2O dimasukkan kedalam beakerglass, ditambahkan
2 mL HNO3 65%(p), diaduk dengan batang pegaduk sampai kristal larut, dimasukkan
ke dalam labu ukur 1000 mL, ditambahkan aquadest sampaigaris tanda dan dihomogenkan.
3.3.2.2. Larutan Standar Al3+ 100 mg/L
Dipipet sebanyak 10 mL larutan standar Al3+ 1000mg/L dan dimasukkan kedalam labu ukur 100 mL, ditambahkan aquadest hingga garis tanda dan dihomogenkan.
3.3.2.3. Larutan Seri Standar Al3+ 0,0; 1,0 ; 2,0 ; 3,0 ; 4,0 ; 5,0 ; 6,0 ; 7,0 mg/L
3.3.3. Preparasi Larutan Sampel
Sampel air diukur sebanyak 50 ml dimasukkan ke dalam beakerglass 250 mL, ditambahkan 5 mL HNO3 65%(p) dan dipanaskan diatas hot plate hingga volume 15-20
mL, kemudian ditambahkan 5 mL HNO3 65%(p) dan ditutup dengan kaca arloji,
direfluks dan ditambahkan HNO3 65%(p) sampai diperoleh larutan jernih, dicuci
dinding beakerglass dan kaca arloji dengan aquadest, disaring dengan kertas whatman No.42 dan dimasukkan ke dalam labu ukur 100 mL dan diatur pada pH = 3 dan ditambahkan aquadest hingga garis batas dan dihomogenkan.
3.3.4. Penentuan Kandungan Besi (Fe) Secara Spektrofotometri Serapan Atom
Larutan sampel yang telah didestruksi dianalisa secara kuantitatif dengan mengukur
absorbansinya pada λ = 248,3 nm dengan menggunakan alat SSA.
3.3.5. Penentuan Kandungan Aluminium (Al) Secara Spektrofotometri Visible
Sebanyak 50mL sampel dimasukkan ke dalam labu erlenmeyer, ditambahkan 10 mL HNO3 65%(p) dan 10 mL HCl 37%(p) , didiamkan sebentar, kemudian dipanaskan
sampai asap warna coklat hilang, diankat dan didinginkan, dipindahkan kedalam labu
ukur 50 mL ditambahkan aquadest sampai garis batas, dikocok dan disaring. Kemudian dipipet 5 mL filtrat ke dalam labu ukur 100 mL, ditambahkan 2 mL aluminon dan ditambahkan 2 mL buffer asetat, ditambahkan aquadest sampai garis batas, dan diukur absorbansinya dengan menggunakan spektrofotometer UV-VIS pada
3.4. Bagan Penelitian
3.4.1. Pembuatan Kurva Kalibrasi Fe3+
3.4.2. Pembuatan Kurva Kalibrasi Al3+
Larutan Seri Standar Fe 0,0 ; 0,5 ; 1,0 ; 1,5 ; 2,0 dan 2,5
Dibuat pada pH = 3
Diukur absorbansinya pada λ = 248,3 nm dengan Spektrofotometer Serapan Atom
Hasil
Larutan Seri Standar Al 0,0 ; 1,0 ; 2,0 ; 3,0 ; 4,0 ; 5,0 ; 6,0 dan 7,0 mg/L
Ditambahkan 2 mL aluminon Ditambahkan 2 mL buffer asetat Diukur absorbansinya dengan menggunakan Spektrofotometer
UV-VIS pada λ = 535 nm
3.4.3. Penyediaan Larutan Sampel
3.4.3.1.Penentuan Kuantitatif Besi (Fe) Dengan Spektrofotometer Serapan Atom
50 mL Sampel
Dimasukkan ke dalam beakerglass 250 mL Ditambahkan 5 mL HNO3(p)
Dipanaskan hingga volume 15 – 20 mL Ditambahkan 5 mL HNO3(p) dan ditutup
dengan kaca arloji
Direfluks dan ditambahkan HNO3(p)
sampai diperoleh larutan jernih Dicuci dinding beakerglass dan kaca arloji dengan aquadest
Disaring
Filtrat Residu
Dimasukkan kedalam labu ukur 100 mL Diatur pH = 3
Ditambahkan aquadest hingga garis tanda Residu
Filtrat
Dicuci dengan aquadest panas
Dihomogenkan
Dianalisis dengan Spektrofotometer Serapan Atom Pada λ = 248,3 nm
3.4.3.2.Penentuan Kuantitatif Aluminium (Al) Dengan Spektrofotometer UV-VIS
50 mL Sampel
Ditambahkan 10 mL HNO3 65%(p) dan 10 mL HCl
Didiamkan
Dipanaskan sampai asap warna coklat hilang Didinginkan
Dipindahkan ke labu ukur 50 mL
Ditambahkan aquadest hingga garis tanda Dikocok
Disaring
Filtrat Residu
Dipipet 5 mL dengan pipet volume Ditambahkan 2 mL aluminon Ditambahkan 2 mL buffer asetat
Diukur absorbansinya dengan menggunakan Spektrofotometer UV-VIS pada λ = 535 nm
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
4.1.1. Logam Besi (Fe)
Data hasil pengukuran absorbansi besi pada air PDAM cabang sei agul dengan metode SSA adalah seperti pada tabel 4.1 berikut:
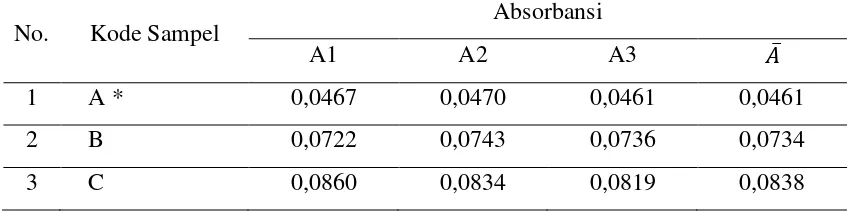
Tabel 4.1. Data Hasil Pengukuran Absorbansi Fe pada Air PDAM Cabang Sei Agul
dengan metode SSA pada λspesifik = 248,3 nm
No. Kode Sampel
Absorbansi
A1 A2 A3 �̅
1 A * 0,0467 0,0470 0,0461 0,0461
2 B 0,0722 0,0743 0,0736 0,0734
3 C 0,0860 0,0834 0,0819 0,0838
Keterangan :
*) = Sampel dengan derajat pengenceran 10 kali A = Air dari Cabang Sei Agul
B = Air dari Cabang Medan Labuhan C = Air dari Cabang Sunggal
4.1.1.1. Penurunan Persamaan Garis Regresi dengan Metode Kurva Kalibrasi untuk Larutan Standar Fe3+
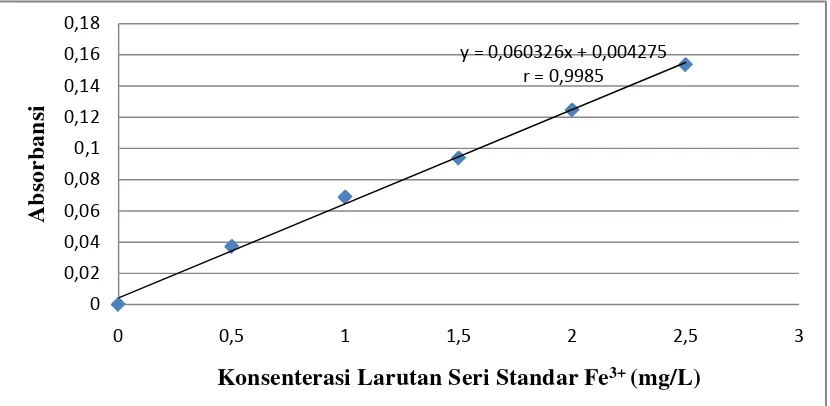
Gambar 4.1 Kurva Kalibrasi Larutan Seri Standar Fe3+
Persamaan garis regresi ini diturunkan dengan metode Least Square, dimana konsenterasi dari larutan standar dinyatakan sebagai Xi dan absorbansi dinyatakan sebagai Yi seperti pada tabel 4.2 berikut :
Tabel 4.2. Data Hasil Penurunan Persamaan Garis Regresi untuk Larutan Seri Standar Fe3+
y = 0,060326x + 0,004275 r = 0,9985
Penurunan persamaan garis regresi : Y = aX + b
Dimana a = slope b = intercept
�=∑(�� − ��)(�� − ��)
∑(�� − ��)2 =
0,263925
4,3750 = 0,060326
�=∑ �� − � ∑ ��
� =
0,4781−0,60326 .7,5
6 = 0,004275
Maka Persamaan Garis Regresi adalah : Y = 0,060326X + 0,004275
4.1.1.2 Penentuan Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai berikut :
�= ∑(�� − ��)(�� − ��)
�∑(�� − ��)2(�� − ��)2 =
0,263925
�(4,3750)(0,015958)= 0,9985
4.1.1.3. Penentuan Kandungan Besi dalam Sampel
Kandungan besi dapat ditentukan dengan menggunakan metode kurva kalibrasi dengan mensubstitusi nilai absorbansi yang diperoleh dari hasil pengukuran terhadap persamaan garis regresi dari kurv kalibrasi.
4.1.1.3.1. Penentuan Kandungan Besi dalam Air Minum dalam mg/L
A1 = 0,0467 A2 = 0,0470 A3 = 0,0461
Dengan mensubstitusikan nilai Y (absorbansi) ke persamaan garis regresi Y = 0,060326X + 0,004275 maka diperoleh :
Dengan derajat pengenceran = 10, maka diperoleh konsenterasi Fe total yaitu :
X1 = 7,03262
Dari data hasil distribusi t student untuk n = 3 , dengan derajat kebebasan (dk) = n-1 =
2 untuk derajat kepercayaan 95% (p – 0,05), t = 4,30 maka :
� =��0,05 � (� −1)���
Sehingga diperoleh hasil pengukuran kandungan besi dalam air PDAM cabang Sei Agul sebesar :
7,016043 ± 0,0197499 mg/L
Hasil perhitungan untuk kandungan besi pada air PDAM cabang Medan Labuhan dan Sunggal terlampir pada lampiran 3.
4.1.2. Logam Aluminium (Al)
Dari hasil pengukuran absorbansi aluminium pada air PDAM cabang Sei Agul dengan metode Spektrofotometri Visible adalah seperti pada Tabel 4.3 berikut :
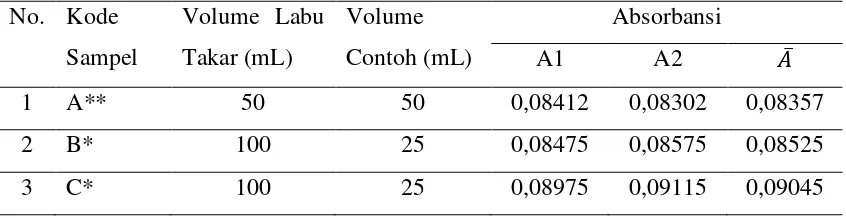
Tabel 4.3. Data Hasil Pengukuran Absorbansi Aluminium pada Air PDAM Cabang
Sei Agul dengan metode Spektrofotometri pada λspesifik = 535 nm
No. Kode Sampel
Volume Labu Takar (mL)
Volume Contoh (mL)
Absorbansi
A1 A2 �̅
1 A** 50 50 0,08412 0,08302 0,08357
2 B* 100 25 0,08475 0,08575 0,08525
3 C* 100 25 0,08975 0,09115 0,09045
Keterangan
*) = Sampel dengan derajat pengenceran 50 kali **) = Sampel dengan derajat pengenceran 20 kali
A = Air dari Cabang Sei Agul
B = Air dari Cabang Medan Labuhan
4.1.2.1. Penurunan Persamaan Garis Regresi dengan Metode Kurva Kalibrasi untuk Larutan Standar Al3+
Data absorbansi yang diperoleh untuk suatu seri larutan standar Al3+ diplotkan terhadap konsenterasi larutan standar sehingga diperoleh kurva kalibrasi berupa garis
linear seperti pada gambar 4.2 berikut ini :
Gambar 4.2. Kurva Kalibrasi Larutan Seri Standar Al3+
Persamaan garis regresi ini diturunkan dengan metode Least Square, dimana konsenterasi dari larutan standar dinyatakan sebagai Xi dan absorbansi dinyatakan sebagai Yi seperti pada tabel 4.4 berikut :
Tabel 4.4. Data Hasil Penurunan Persamaan Garis Regresi untuk Larutan Seri Standar Al3+ y = 0,076063x + 0,007992
��=∑ ��
Penurunan persamaan garis regresi : Y = aX + b
Maka Persamaan Garis Regresi adalah : Y = 0,076063X + 0,007992
4.1.2.2. Penentuan Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai berikut :
�= ∑(�� − ��)(�� − ��)
�∑(�� − ��)2(�� − ��)2 =
3,19465
�(42)(0,2432) = 0,9995
4.1.2.3. Penentuan Kandungan Aluminium dalam Sampel
4.1.2.3.1. Penentuan Kandungan Aluminium dalam Air Minum dalam mg/L
Dari data pengukuran absorbansi aluminium untuk sampel air PDAM dari cabang sei agul diperoleh absorbansi sebagai berikut :
A1 = 0,08412 A2 = 0,08302
Dengan mensubstitusikan nilai Y (absorbansi) ke persamaan garis regresi Y = Y = 0,076063X + 0,007992 maka diperoleh :
Dengan derajat pengenceran = 50, volume labu takar = 50mL dan volume contoh = 50mL maka diperoleh konsenterasi Al total yaitu :
Dari data hasil distribusi t student untuk n = 2 , dengan derajat kebebasan (dk) = n-1 = 1 untuk derajat kepercayaan 95% (p – 0,05), t = 4,30 maka :
� =��0,05 � (� −1)���
� = 4,30 (0,05 � 1)0,3624 = 0,077916
Sehingga diperoleh hasil pengukuran kandungan aluminium dalam air PDAM cabang Sei Agul sebesar :
49,6775 ± 0,077916 mg/L
Hasil perhitungan untung kandungan aluminium pada air PDAM cabang Medan Labuhan dan Sunggal terlampir pada lampiran 6.
4.2. Pembahasan
Besi (Fe) dan Aluminium (Al) merupakan mineral mikro essensial,yaitu logam dalam satuan miligram atau mikrogram per kilogram berat badan yang peranannya sudah jelas dan sangat dibutuhkan dalam proses metabolisme tubuh. Kebutuhan akan logam besi (Fe) dan aluminium (Al) dalam tubuh dapat terpenuhi melalui asupan makanan sehari – hari. Namun asupan yang mengakibatkan kelebihan kadar logam besi (Fe) dan aluminium dalam tubuh justru akan bersifat toksik terhadap tubuh.
Aluminium terdapat dalam bentuk silikat dan hydrous aluminium oksida dan hidroksida. Aluminium tidak ditemukan sebagai logam murni dan hanya memiliki satu keadaan oksidasi. Sistem transportasi dan distribusi dari aluminium dalam lingkungan tergantung dengan sifat kimianya dan karakteristik daripada sistem lingkungan. Pada pH > 5,5, secara alami senyawa aluminium terdapat dalam bentuk tidak larut kecuali dengan banyaknya jumlah material organik terlarut, yang dapat mengikat aluminium dan menyebabkan peningkatan konsenterasi aluminium pada aliran sungai dan danau.
Beberapa proses yang mempengaruhi mobilitas aluminium dan transportasi substrat dalam lingkungan. Hal ini meliputi spesiasi kimia, jalur aliran hidrologi, faktor ruang dan waktu yang berhubungan dengan interaksi antara tanah dan air, dan komposisi dari material geologis didalam tanah. Mobilisasi terjadi utama dalam daerah aliran sungai dengan tanah yang dangkal, tanah yang asam dan permukaan air yang buruk buffernya yang terkena endapan asam.
Dalam sistem air permukaan dan air tanah, keseimbangan akhirnya dibentuk yang mengontrol sejauh mana penguraian aluminium dapat terjadi. Solubilitas daripada aluminium dalam kesetimbangan dengan fase padat dari aluminium hidroksida yang sangat bergantung dengan pH. Dalam keadaan asam dan untuk tingkat yang lebih rendah dibawah kondisi alkali, kelarutan aluminium meningkat. Ion
trivalen merupakan spesies dominan dibawah pH 5 dan sebuah kation hidroksil mendominasi diatas pH > 6,2 dan merupakan titik solubilitas minimum.
Proses pengasaman alami menghasilkan peningkatan kelarutan dari aluminium dan dalam kondisi asam yang normal aluminium dapat muncul sebagai kation yang dapat bertukar. Ion aluminium menggantikan kalsium pada bagian pertukaran muatan tetap. Sistem pertukaran kation pada tanah asam menghasilkan banyaknya cadangan ion aluminium yang dapat dibawa kedalam larutan ketika garam yang mudah larut meresap melalui tanah. Ligan, seperti fluorida dan anion organik, yang membentuk kompleks aluminium bergabung dengan aluminium dan mempertahankan konsenterasi aluminium yang lebih tinggi dari yang diperkirakan, terutama pada pH antara 5 – 7.
Mobilisasi daripada aluminium dengan kondisi asam menghasilkan banyak aluminium tersedia untuk penyerapan tanaman. Aluminium di akumulasi oleh tanaman yang terkena larutan nutrien terutama bagian akar. Potensial untuk akumulasi daripada aluminium oleh tanaman telah dipelajari pada beberapa spesies tanaman air. Tidak mengherankan, bioakumulasi oleh organisme berkaitan dengan ketersedian hayati daripada aluminium.
Aluminium adalah konstituen dan utama dari debu turunan dari tanah dan partikulat dari pembakara batubara. Permukaan air tawar dan air tanah konsenterasi aluminium dapat bervariasi secara substansial bergantung dengan faktor - faktor fisikokimia maupun mineralogi. Aluminium dapat terdapat dalam jumlah dan bentuk
yang berbda didalam air. Aluminium dapat mengendap ataupun larut. Aluminium terkonsenterasi dalam sedimen dan dalam bahan partikulat, terutama pada pH netral dengan konsenterasi mulai dari 20.000 sampai 80.000 mg/Kg. Aluminium adalah salah satu unsur paling banyak ditanah dan konsenterasinya sangat bervariasi. Range dari 700 sampai 100.000 dikutip oleh Survey Geologi U.S.(Paula.1998)
terdiri dari penambahan garam aluminium pada dosis dan pH optimum, diikuti dengan proses flokulasi, sedimentasi, dan filtrasi.(Health Canada,1993)
Aluminium masuk kedalam atmosfer sebagai konstituen utama dari partikulat atmosfer yang berasal dari erosi tanah, penambangan atau aktivitas pertanian, erupsi vulkanik, atau pembakaran batu bara. Konsentrasi atmosfer aluminium menunjukkan variasi temporal dan spasial yang luas. Tingkat udara aluminium berkisar dari 0,0005 µg/m3 atas antartika sampai lebih dari 1µg/m3 untuk tempat industri.
Aluminium juga terdapat didalam makanan secara alami atau dalam makanan yang menggunakan aditif yang mengandung aluminium. Penggunaan alat memasak aluminium, peralatan dan juga pembungkus makanan dapat meningkatkan aluminium didalam makanan; namun besarnya peningkatan ini umumnya tidak merupakan kepentingan praktis. Makanan yang secara alami mengandung banyak mengandung aluminium adalah kentang, bayam dan teh. Produk olahan susu, tepung, dan formula bayi mungkin tinggi dalam aluminium jika mereka mengandung aditif makanan berbasis aluminium.(FAO/WHO,1989;Pennington & Schoen,1995;WHO,1997).
Besi dan Aluminium pada air minum diperkirakan berasal dari penggunaan koagulan berupa Garam Fe3+ ataupun tawas (Al2SO4) biasanya sering digunakan PAC
(Poly Aluminium Chloride) dalam proses flokulasi pada pengolahan air minum.
Penggunaan garam aluminium sebagai koagulan dalam pengolahan air dapat mengakibatkan peningkatan konsenterasi daripada aluminium daripada air yang telah diproses. Dimana konsenterasi residu adalah tinggi, aluminium juga dapat terdeposit didalam sistem distribusi. Gangguan dari deposit dengan perubahan dalam laju aliran dapat meningkatkan tingkat aluminium dalam air keran dan menyebabkan warna yang tidak diinginkan dan kekeruhan(WHO.1996). Konsenterasi daripada aluminium yang mana masalah seperti itu mungkin terjadi dan sangat tergantung pada beberapa parameter mutu air dan faktor operasional di pabrik pengolahan air.
Dari hasil penelitian yang dilakukan diperoleh kandungan logam besi (Fe) dalam air minum yang diproduksi oleh PDAM unit produksi Sei Agul, Medan Labuhan dan Sunggal Medan masing – masing adalah 7,016 mg/L; 1,145 mg/L dan 1,318 mg/L. Kandungan logam aluminium masing – masing adalah 49,677 mg/L; 81,256 mg/L dan 86,725 mg/L. Kandungan logam besi dan aluminium pada air minum yang diperoleh pada penelitian ini apabila dibandingkan dengan data yang ada dalam lampiran Peraturan Pemerintah No.82 Tahun 2001 dan Permenkes No.492/MENKES/PER/IV/2010, menunjukkan kandungan logam besi dan aluminium dalam air minum berada diatas batas yang diizinkan (Kandungan Fe 0,3 ppm dan Kandungan Al 0,2 ppm). Dengan membandingkan hasil yang diperoleh dengan Peraturan Pemerintah No.82 Tahun 2001 dan Permenkes No.492/MENKES/PER/IV/2010 bahwa air minum yang diproduksi oleh ketiga
cabang unit produksi mengandung kandungan logam Fe dan Al yang tinggi yang dapat membahayakan kesehatan.
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari hasil penelitian yang telah dilakukan diperoleh kesimpulan sebagai berikut : 1. Kandungan Fe dalam air minum yang diproduksi PDAM unit produksi Cabang Sei
Agul, Medan Labuhan dan Sunggal masing – masing adalah sebagai berikut : 7,016 mg/L; 1,145 mg/L dan 1,318 mg/L. Kandungan Al dalam air minum yang diproduksi PDAM unit produksi Cabang Sei Agul, Medan Labuhan dan Sunggal masing – masing adalah sebagai berikut 49,677 mg/L; 81,256 mg/L dan 86,725 mg/L.
2. Kandungan Fe dan Al yang terkandung dalam Air PDAM Cabang Sei Agul tidak sesuai dengan standar Peraturan Pemerintah No.82 tahun 2001 untuk air baku dan PERMENKES No.492/MENKES/PER/IV/2010 untuk air bersih,
5.2 Saran
DAFTAR PUSTAKA
Agusnar,H. 2007. Kimia Lingungan. Medan:USU-Press
Apriyanto.R. 1987. Sampel Pretreatment and Separation. John Wiley and Sons. New York
ATSDR. 1992. Toxicological profile for aluminium. Atlanta, GA, US Department of Health and Human Services, Public Health Service, Agency for Toxic Substances and Disease Registry (TP-91/01) http://www.health.vic.gov.au/archive/archive2014/nphp/enhealth/council/pubs/ pdf/alumin.pdf
Boyd,C.E. 1988. Water Quality ini Warmwater Fish Ponds. Fourth Printing. Auburn University Agricltural Experiment Station. Alabama, USA
Canadian Council of Resource and Environment Ministers. 1987. Canadian Water Quality. Canadian Council of Resource and Environment Ministers, Ontario, Canada
Chapman,D, Kimstach,V.1997. Selection of Water Quality Variables. In Chapman,D. 1997. Water Quality Assesments. Second Edition. London:E&FNSPON
Cole,G.A. 1988. Textbook of Limnology. Third Edition. Waveland Press,Inc., Illinois, USA
Davis,M.L, Cornwell,D.A.1991. Introduction to Environmental Engineering. Second Edition Newyork: Mc Graw-Hill. Inc
Degremont. 1979. Water Treatment Handbook.Fifth Edition. A Halsted Press Book. John Wiley and Sons. New York
DST. 2006.The Pilot Project on Rain Water Harvesting in Manipur. New Delhi : Department of Science and Technology (DST). Govt of India Technology Bhavan, New Mehrauli road.
Eekenfelder,W.W. 1989. Industrial Water Pollution Control. Second Edition. Mc Graw-Hill.Inc. New York
FAO/WHO. 1989. Aluminium. In: Toxicological Evaluation Of Certain Food Additives and Contaminants. Thirty-third meeting of the Joint FAO/WHO Expert Committee on Food Addittives.Geneva,World Health Organization,pp. 113-154 (WHO Food Additives Series 24)http://www.health.vic/gov.au
/archive/archive2014/nphp/enhealth/council/pub/pdf/alumin.pdf
Health Canada. 1993. Guidelines for Canadian drinking water quality. Water treatment principles and applications: a manual for the production of drinking water. Ottawa, Ontario,Health Canada, Environmental Health Directorate. Printed and distributed by Canadian Water and Wastewater Associaton, Ottawa, Ontariohttp://www.health.vic.gov.au/archive/archive2014/nphp
/enhealth/council/pubs/pdf/alumin.pdf
Khopkar,S.M. 2003. Konsep Dasar Kimia Analitik. Jakarta: UI-Press
Krist,H and Rump,H.H. 1992. Laboratory Manual for The Examination of Water, Waste Water and Soil. Second Edition. VCH VerslagsgesellschaftmbH, Weinheim, Germany
Mackereth,F.J.H.,Heron,J. And Talling,J.F. 1989. Water Analysis. Freshwater Biological Associatio, Cumbria, UK
Manahan,S.E. 1983. Environmental Chemistry. Fourth Edition. Brooks/Cole Publishing Company. Monterey, California
McNeely,R.N., Nelmanis,V.P., and Dwyer,L.1979. Water Source Book, A Guide to Water Quality Parameter. Inland Waters Directorate, Water Quality Branch, Ottawa , Canada
Moore,J.W. 1991. Inorganic Contaminats of Surface Water. Springer-Verlag. New York
Moss,B. 1993. Ecology of Freshwaters. Second Edition. Black Well Scientific Publications. London
Nathanson,J.A.1997. Basic Environmental Technology. Second Edition. New Jersey: Prentice Hall
Novotny,V. And Olem,H. 1994. Water Quality, Prevention, Identification, and Management of Diffuse Pollution. Van Nostrans Reinhold, New York