UJI STABILITAS OBAT ANTI PERADANGAN
INDOMETASIN FARNESIL YANG TERSALUT GEL
KITOSAN-GOM GUAR
DEBBY ISDARULYANTI
Skripsi
sebagai salah satu syarat memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
DEBBY ISDARULYANTI. Stabilitas Obat Anti-peradangan Indometasin Farnesil
Tersalut Gel Kitosan-Gom Guar. Dibimbing oleh PURWANTININGSIH SUGITA,
BAMBANG SRIJANTO, dan BUDI ARIFIN.
Gel kitosan yang dimodifikasi oleh hidrokoloid alami gom guar dengan
glutaraldehida sebagai penaut silang berpotensi sebagai penyalut untuk digunakan dalam
sistem pengantaran obat dalam bentuk mikrokapsul. Mekanisme pelepasan obat dari
membran kitosan-gom guar telah dipelajari melalui uji difusi. Sementara laju pelepasan
indometasin farnesil dalam medium usus telah dipelajari melalui uji disolusi. Sebagai
sediaan obat yang baru, mikrokapsul indometasin farnesil ini perlu diuji stabilitasnya.
Tujuannya adalah untuk menentukan kestabilan dan usia guna mikrokapsul indometasin
farnesil.
Sediaan obat dibuat dengan mencampurkan 228.6 ml kitosan 1.75% (b/v), 38.10 ml
larutan gom guar dengan ragam konsentrasi 0.05, 0.19, dan 0.33% (b/v), 7.62 ml
glutaraldehida dengan ragam konsentrasi 4, 4.5, dan 5% (v/v), dan 100 mg indometasin
farnesil dalam 250 ml etanol 96%. Campuran homogen yang diperoleh kemudian
dikeringkan semprot menjadi granul.
ABSTRACT
DEBBY ISDARULYANTI. Stability Test of Anti Inflammatory Drug Indomethacin
Farnesil Coated with Chitosan-Guar Gum Gel. Supervised by PURWANTININGSIH
SUGITA, BAMBANG SRIJANTO, and BUDI ARIFIN.
Chitosan gel modified by guar gum natural hydrocolloid with glutaraldehyde as
cross-linker are potential as coating agent to be used drug as delivery system in
microcapsule form. Mechanism of drug release from chitosan-guar gum membrane has
been studied by diffusion test, whereas release rate of indomethacin farnesil in intestines
medium has been studied by dissolution test. As a new product preparation, the stability
of this indomethacin farnesil microcapsule need to be studied. This research aimed to
determine stabilities and shelf life of indomethacin farnesil microcapsule.
Drug preparations were made by mixing 228.6 ml 1.75 % (w/v) chitosan solutions,
38.1 ml 0.05, 0.19, and 0.33% (w/v) guar gum solutions, 7.62 ml 4, 4.5, and 5% (v/v)
glutaraldehyde solutions, 100 mg of indomethacin farnesil solubilized in 250 ml 96%
ethanol. The homogenous mixture obtained was then spray dried into granules.
The stability was tested using accelerated test in climatic chamber under
temperature of (40±2) °C and relative humidity (75±5)% for 3 month. The moisture
content was measured by using moisture analyzer and the indomethacin farnesil content
was measured with specrofotometer ultaraviolet at wavelangeth of 320.4 nm every week.
All nine formulas showed high (>10%) and fluctuating water content, whereas
indometchin farnesil content decreasing with varied degradation rate: zero order (formula
2, 4, and 5), second order (formula 3 and 7), and third order (formula 1, 6, and 8
−
9).
Formula 6 with guar gum and glutaraldehyde concentration 0.19% (w/v) and 5.00% (v/v),
respectively, in chitosan solutions at constant concentration, 1.75% (w/v) was the most
stable with encapsulated indomethacin farnesil after 12
thweeks, the degradation rate
constant, and shelf life were 77.67%, 0.0008 (%w/v)
-2week
-1, and 4.28 week or 30 days,
respectively.
Menyetujui
Pembimbing I,
Dr. Purwantiningsih Sugita, MS
NIP 131 779 513
Pembimbing II, Pembimbing III,
Ir. Bambang Srijanto
Budi Arifin, SSi
NIP 680 003 303 NIP 132 321 568
Mengetahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor,
Dr. drh. Hasim, DEA
NIP 131 578 806
Tanggal lulus:
Judul :
Stabilitas Obat Anti Peradangan Indometasin Farnesil Tersalut Gel
Kitosan-Gom Guar
Nama :
Debby Isdarulyanti
PRAKATA
Puji syukur Penulis panjatkan kepada Allah SWT atas segala berkat yang
memampukan Penulis menyelesaikan karya ilmiah ini. Penelitian ini bertujuan
mengevaluasi stabilitas mikrokapsul kitosan-gom guar. Selain itu berguna untuk
menentukan usia guna dari mikrokapsul tersebut. Penelitian ini dilaksanakan sejak bulan
Mei–Desember 2007 di Laboratrium Teknologi Farmasi dan Medis, BBPT Serpong,
Laboratorium Kimia Organik dan Laboratorium Bersama, Departemen Kimia, Fakultas
Matematika dan Ilmu Pengetahuan Alam, IPB.
Penulis mengucapkan terima kasih kepada semua pihak yang telah membantu
Penulis selama penelitian dan juga penyusunan karya ilmiah ini, terutama Dr. Ir.
Purwantiningsih Sugita, MS, Ir. Bambang Srijanto, dan Budi Arifin, SSi selaku
pembimbing yang selalu menyempatkan waktu untuk berkonsultasi; kepada Tuti
Wukirsari, SSi atas arahan-arahan yang begitu berharga selama Penulis menjalani
penelitian; serta kepada Bapak dan Ibu yang selama ini telah berjuang keras agar Penulis
bisa tetap sekolah sampai akhirnya dapat menyusun karya ilmiah ini. Penulis juga
mengucapkan terima kasih kepada Pusat Studi Biofarmaka atas bantuannya dalam
analisis FTIR, Laboratorium Zoologi LIPI dalam analisis morfologi dengan SEM, Seafast
PAU IPB atas pengunaan alat pengering semprot, dan para laboran di Kimia Organik atas
bantuan teknisnya selama Penulis menjalani penelitian.
Pada kesempatan ini, Penulis juga mengucapkan terima kasih kepada Direktorat
Jendral Pendidikan Tinggi Depdiknas melalui Hibah Bersaing XIV Dikti tahun 2007 dan
Departemen Kimia melalui Hibah Penelitian Internal tahun 2006 yang telah mendanai
penelitian ini.
Akhir kata, semoga karya ilmiah ini dapat bermanfaat.
Bogor, Februari 2008
RIWAYAT HIDUP
Penulis dilahirkan di Bandung pada tanggal 19 Februari 1986 dari pasangan Tatang
Rukmana dan Iis Prihatini. Putri pertama dari dua bersaudara.
Tahun 2000 Penulis masuk Sekolah Menengah Umum 5 Cimahi, Bandung dan
pada tahun 2003 lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui jalur
Undangan Seleksi Masuk IPB (USMI). Penulis memilih Departemen Kimia, Fakultas
Matematika dan Ilmu Pengetahuan Alam.
DAFTAR ISI
Halaman
DAFTAR TABEL ... vi
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... viii
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Kitosan dan Gel Kitosan ... 1
Gom Guar ... 3
Indometasin Farnesil ... 3
Mikroenkapsulasi ... 4
Uji Stabilitas ... 4
BAHAN DAN METODE
Bahan dan Alat ... 4
Ekstraksi Indometasin Farnesil dari Dialon dan Penentuan Kadarnya ... 5
Pembuatan Mikrokapsul ... 5
Uji Stabilitas ... 5
Pencirian Mikrokapsul dengan SEM ... 5
HASIL DAN PEMBAHASAN
Kadar Indometasin Farnesil dalam Obat Dialon ... 6
Pembuatan Mikrokapsul ... 6
Uji Stabilitas ... 6
Pencirian Morfologi Mikrokapsul ... 9
SIMPULAN DAN SARAN ... 10
DAFTAR PUSTAKA ... 11
DAFTAR TABEL
Halaman
1
Spesifikasi kitosan niaga ... 2
2
Konsentrasi infar dalam mikrokapsul kitosan-gom guar... 7
3 Persamaan laju penguraian infar semua formula mikrokapsul ... 8
4
Persentase infar yang masih tersalut setelah uji stabilitas 3 bulan... ... 8
5
Usia guna mikrokapsul kitosan-gom guar dengan zat aktif infar... 9
DAFTAR GAMBAR
Halaman
1 Struktur kitosan... 2
2
Struktur hidrogel kitosan (a) ikatan silang kitosan-kitosan, (b) jaringan polimer
hibrid, (c) jaringan semi IPN, dan (d) kitosan berikatan silang ionik... 2
3
Struktur gom guar... 3
4
Struktur indometasin farnesil ... 3
5
Morfologi mikrokasul ... 4
6
Mikrokapsul (a) tanpa dan (b) dengan penambahan infar ... 6
7
Foto-foto SEM permukaan mikrokapsul (a) kosong dan (b) berisi infar ... 6
8
Kurva kadar air formula 1
−
5 ... 7
9
Kurva kadar air formula 6
−
9 ... 7
DAFTAR LAMPIRAN
Halaman
1
Kadar air dan kadar abu kitosan (AOAC 1999) ... 14
2
Penentuan bobot molekul kitosan (Tarbojejevich & Cosani 1996) ... 15
3
Penentuan derajat deasetilasi (Domzsy & Robert dalam Khan
et al
. 2002)... 17
4
Preparasi bahan-bahan yang digunakan ... 18
5
Diagram alir penelitian ... 19
6
Penentuan kemurnian infar dalam ekstrak obat metode spektrofotometri secara
simultan ... 20
7
Spektrum infar 99.2% dari PT Eisai Indonesia (a), vitamin E ( -tokoferol) (b),
dan infar hasil ekstrak obat Dialon dengan spektrofotometer UV .. ... 22
8
Kadar air mikrokapsul infar (%) hasil uji stabilitas dipercepat pada T=(40±2) °C
dan RH (75±5)% selama 3 bulan... 23
9
Deret standar infar untuk penentuan konsentrasi infar dalam ekstrak etanol
mikrokapsul. ... 24
10
Konsentrasi infar (%b/b) hasil uji stabilitas dipercepat pada T=(40±2) °C dan RH
(75±5)% selama 3 bulan... 25
11
Penentuan orde reaksi penguraian infar dalam mikrokapsul formula 1 (kitosan
1.75% [b/v], gom guar 0.05% [b/v], dan glutaraldehida 4.00% [v/v])... 26
12
Penentuan orde reaksi penguraian infar dalam mikrokapsul formula 2 (kitosan
1.75% [b/v], gom guar 0.05% [b/v], dan glutaraldehida 4.50% [v/v])... 27
13
Penentuan orde reaksi penguraian infar dalam mikrokapsul formula 3 (kitosan
1.75% [b/v], gom guar 0.05% [b/v], dan glutaraldehida 5.00% [v/v])... 28
14
Penentuan orde reaksi penguraian infar dalam mikrokapsul formula 4 (kitosan
1.75% [b/v], gom guar 0.19% [b/v], dan glutaraldehida 4.00% [v/v])... 29
15
Penentuan orde reaksi penguraian infar dalam mikrokapsul formula 5 (kitosan
1.75% [b/v], gom guar 0.19% [b/v], dan glutaraldehida 4.50% [v/v])... 30
16
Penentuan orde reaksi penguraian infar dalam mikrokapsul formula 1 (kitosan
1.75% [b/v], gom guar 0.19% [b/v], dan glutaraldehida 5.00% [v/v])... 31
17
Penentuan orde reaksi penguraian infar dalam mikrokapsul formula 1 (kitosan
1.75% [b/v], gom guar 0.33% [b/v], dan glutaraldehida 4.00% [v/v])... 32
18
Penentuan orde reaksi penguraian infar dalam mikrokapsul formula 1 (kitosan
1.75% [b/v], gom guar 0.33% [b/v], dan glutaraldehida 4.50% [v/v])... 33
PENDAHULUAN
Indometasin farnesil (infar) merupakan salah satu senyawa aktif obat yang sangat efektif sebagai obat anti peradangan nonsteroid (NSAID). Obat ini bersifat tidak larut dalam air dan penggunaannya dalam dosis tinggi dapat menyebabkan pendarahan pada saluran pencernaan. Pengendalian pelepasan obat indometasin pernah dilakukan dengan membuatnya dalam bentuk sediaan mikrokapsul (Tiyaboonchai & Ritthidej 2003; Yamada et al. 2001)
Kitosan merupakan aminopolisakarida yang diperoleh melalui deasetilasi kitin. Kitin merupakan biopolimer yang paling melimpah di alam setelah selulosa, dan banyak terkandung dalam limbah. Kitosan memiliki sifat tidak beracun, biokompatibel, biodegradabel, bioadhesif, dan mampu membentuk ikatan silang secara kovalen pada gugus aminonya (Varhosaz & Reza 2005). Selain itu, kitosan merupakan biopolimer polikationik sehingga dapat membentuk gel dalam suasana asam, misalnya di dalam lambung (Sakinnen 2003). Karena sifat-sifat tersebut, kegunaan kitosan dalam industri farmasi dipelajari secara luas sebagai sistem pengantaran obat terkendali.
Kitosan dalam bentuk gel atau lembaran telah digunakan sebagai penyalut obat anti-peradangan ketoprofen (Yamada et al. 2001), indometasin (Rana et al. 2004), dan propanolol hidroklorida (Sutriyo et al. 2005). Namun, gel kitosan yang dihasilkan mudah rapuh. Beberapa penelitian telah dilakukan untuk memodifikasi sifat gel kitosan, di antaranya dengan menambahkan poli(vinil alkohol) (PVA) sebagai bahan saling tembus (interpenetrating agent) dan glutaraldehida sebagai penaut silang (Wang et al. 2004). Penambahan dua bahan tersebut dapat memperbaiki gel kitosan yang terbentuk dengan menurunkan waktu gelasi dan meningkatkan kekuatan mekanik gel. Hidrokoloid alami juga telah banyak ditambahkan untuk memodifikasi gel kitosan, antara lain gom guar (Sugita et al. 2006a), alginat (Sugita et al. 2006b dan Cardenas et al
2003), karboksimetil selulosa (Sugita et al.
2006c), dan gom xantan (Sugita et al. 2007a). Keempat hasil modifikasi tersebut berpotensi sebagai membran dan secara mekanik lebih kuat daripada gel kitosan.
Berdasarkan penelitian Sugita et al.
(2006a) gel kitosan yang terbentuk dengan penambahan penaut-silang glutaraldehida dan gom guar sebagai bahan saling tembus,
memiliki sifat reologi yang lebih baik dan berpotensi sebagai sistem pengantaran obat. Gom guar sendiri pernah dimanfaatkan untuk memperbaiki sistem pengantaran obat untuk mengobati radang dan kanker usus besar (Kshirsagar 2000).
Mekanisme difusi obat ketoprofen dari membran kitosan-gom guar telah dipelajari oleh Nata et al. (2007b). Sementara laju disolusi infar dalam medium usus telah dipelajari Mubarok (2007). Waktu paruh pelepasan infar dalam uji disolusi ini, ialah 51 menit. Kedua penelitian tersebut menunjukkan hasil bahwa mikrokapsul kitosan-gom guar mengalami pembesaran pori ketika kontak dengan cairan.
Mikrokapsul kitosan-gom guar dengan zat aktif infar merupakan sediaan obat yang baru, sehingga perlu dilakukan uji stabilitas untuk mengetahui kestabilan dan usia gunanya. Hal ini perlu dilakukan agar mutu, keamanan, dan khasiat obat selama penggunaan terjamin (Anonim 2005).
Uji stabilitas yang dipercepat dilakukan dalam penelitian ini selama 3 bulan dengan suhu (40±2) °C dan kelembapan relatif (Relative Humidity, RH) (75±5)%. Pemilihan kondisi ini didasarkan pada pembagian wilayah oleh International Conference on Harmonization (ICH). Indonesia masuk ke dalam zona 4, yaitu daerah tropis atau lembap dan panas (Agoes 2001).. Uji stabilitas yang dilakukan dibatasi pada uji stabilitas kimia (kadar infar) dan fisika (kadar air). Data hasil pengukuran kadar infar digunakan untuk menentukan orde reaksi yang merupakan parameter kinetika reaksi penguraian infar, yang diperoleh dengan menggunakan metode grafis.
TINJAUAN PUSTAKA
Kitosan dan Gel Kitosan
UJI STABILITAS OBAT ANTI PERADANGAN
INDOMETASIN FARNESIL YANG TERSALUT GEL
KITOSAN-GOM GUAR
DEBBY ISDARULYANTI
Skripsi
sebagai salah satu syarat memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
DEBBY ISDARULYANTI. Stabilitas Obat Anti-peradangan Indometasin Farnesil
Tersalut Gel Kitosan-Gom Guar. Dibimbing oleh PURWANTININGSIH SUGITA,
BAMBANG SRIJANTO, dan BUDI ARIFIN.
Gel kitosan yang dimodifikasi oleh hidrokoloid alami gom guar dengan
glutaraldehida sebagai penaut silang berpotensi sebagai penyalut untuk digunakan dalam
sistem pengantaran obat dalam bentuk mikrokapsul. Mekanisme pelepasan obat dari
membran kitosan-gom guar telah dipelajari melalui uji difusi. Sementara laju pelepasan
indometasin farnesil dalam medium usus telah dipelajari melalui uji disolusi. Sebagai
sediaan obat yang baru, mikrokapsul indometasin farnesil ini perlu diuji stabilitasnya.
Tujuannya adalah untuk menentukan kestabilan dan usia guna mikrokapsul indometasin
farnesil.
Sediaan obat dibuat dengan mencampurkan 228.6 ml kitosan 1.75% (b/v), 38.10 ml
larutan gom guar dengan ragam konsentrasi 0.05, 0.19, dan 0.33% (b/v), 7.62 ml
glutaraldehida dengan ragam konsentrasi 4, 4.5, dan 5% (v/v), dan 100 mg indometasin
farnesil dalam 250 ml etanol 96%. Campuran homogen yang diperoleh kemudian
dikeringkan semprot menjadi granul.
ABSTRACT
DEBBY ISDARULYANTI. Stability Test of Anti Inflammatory Drug Indomethacin
Farnesil Coated with Chitosan-Guar Gum Gel. Supervised by PURWANTININGSIH
SUGITA, BAMBANG SRIJANTO, and BUDI ARIFIN.
Chitosan gel modified by guar gum natural hydrocolloid with glutaraldehyde as
cross-linker are potential as coating agent to be used drug as delivery system in
microcapsule form. Mechanism of drug release from chitosan-guar gum membrane has
been studied by diffusion test, whereas release rate of indomethacin farnesil in intestines
medium has been studied by dissolution test. As a new product preparation, the stability
of this indomethacin farnesil microcapsule need to be studied. This research aimed to
determine stabilities and shelf life of indomethacin farnesil microcapsule.
Drug preparations were made by mixing 228.6 ml 1.75 % (w/v) chitosan solutions,
38.1 ml 0.05, 0.19, and 0.33% (w/v) guar gum solutions, 7.62 ml 4, 4.5, and 5% (v/v)
glutaraldehyde solutions, 100 mg of indomethacin farnesil solubilized in 250 ml 96%
ethanol. The homogenous mixture obtained was then spray dried into granules.
The stability was tested using accelerated test in climatic chamber under
temperature of (40±2) °C and relative humidity (75±5)% for 3 month. The moisture
content was measured by using moisture analyzer and the indomethacin farnesil content
was measured with specrofotometer ultaraviolet at wavelangeth of 320.4 nm every week.
All nine formulas showed high (>10%) and fluctuating water content, whereas
indometchin farnesil content decreasing with varied degradation rate: zero order (formula
2, 4, and 5), second order (formula 3 and 7), and third order (formula 1, 6, and 8
−
9).
Formula 6 with guar gum and glutaraldehyde concentration 0.19% (w/v) and 5.00% (v/v),
respectively, in chitosan solutions at constant concentration, 1.75% (w/v) was the most
stable with encapsulated indomethacin farnesil after 12
thweeks, the degradation rate
constant, and shelf life were 77.67%, 0.0008 (%w/v)
-2week
-1, and 4.28 week or 30 days,
respectively.
Menyetujui
Pembimbing I,
Dr. Purwantiningsih Sugita, MS
NIP 131 779 513
Pembimbing II, Pembimbing III,
Ir. Bambang Srijanto
Budi Arifin, SSi
NIP 680 003 303 NIP 132 321 568
Mengetahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor,
Dr. drh. Hasim, DEA
NIP 131 578 806
Tanggal lulus:
Judul :
Stabilitas Obat Anti Peradangan Indometasin Farnesil Tersalut Gel
Kitosan-Gom Guar
Nama :
Debby Isdarulyanti
PRAKATA
Puji syukur Penulis panjatkan kepada Allah SWT atas segala berkat yang
memampukan Penulis menyelesaikan karya ilmiah ini. Penelitian ini bertujuan
mengevaluasi stabilitas mikrokapsul kitosan-gom guar. Selain itu berguna untuk
menentukan usia guna dari mikrokapsul tersebut. Penelitian ini dilaksanakan sejak bulan
Mei–Desember 2007 di Laboratrium Teknologi Farmasi dan Medis, BBPT Serpong,
Laboratorium Kimia Organik dan Laboratorium Bersama, Departemen Kimia, Fakultas
Matematika dan Ilmu Pengetahuan Alam, IPB.
Penulis mengucapkan terima kasih kepada semua pihak yang telah membantu
Penulis selama penelitian dan juga penyusunan karya ilmiah ini, terutama Dr. Ir.
Purwantiningsih Sugita, MS, Ir. Bambang Srijanto, dan Budi Arifin, SSi selaku
pembimbing yang selalu menyempatkan waktu untuk berkonsultasi; kepada Tuti
Wukirsari, SSi atas arahan-arahan yang begitu berharga selama Penulis menjalani
penelitian; serta kepada Bapak dan Ibu yang selama ini telah berjuang keras agar Penulis
bisa tetap sekolah sampai akhirnya dapat menyusun karya ilmiah ini. Penulis juga
mengucapkan terima kasih kepada Pusat Studi Biofarmaka atas bantuannya dalam
analisis FTIR, Laboratorium Zoologi LIPI dalam analisis morfologi dengan SEM, Seafast
PAU IPB atas pengunaan alat pengering semprot, dan para laboran di Kimia Organik atas
bantuan teknisnya selama Penulis menjalani penelitian.
Pada kesempatan ini, Penulis juga mengucapkan terima kasih kepada Direktorat
Jendral Pendidikan Tinggi Depdiknas melalui Hibah Bersaing XIV Dikti tahun 2007 dan
Departemen Kimia melalui Hibah Penelitian Internal tahun 2006 yang telah mendanai
penelitian ini.
Akhir kata, semoga karya ilmiah ini dapat bermanfaat.
Bogor, Februari 2008
RIWAYAT HIDUP
Penulis dilahirkan di Bandung pada tanggal 19 Februari 1986 dari pasangan Tatang
Rukmana dan Iis Prihatini. Putri pertama dari dua bersaudara.
Tahun 2000 Penulis masuk Sekolah Menengah Umum 5 Cimahi, Bandung dan
pada tahun 2003 lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui jalur
Undangan Seleksi Masuk IPB (USMI). Penulis memilih Departemen Kimia, Fakultas
Matematika dan Ilmu Pengetahuan Alam.
DAFTAR ISI
Halaman
DAFTAR TABEL ... vi
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... viii
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Kitosan dan Gel Kitosan ... 1
Gom Guar ... 3
Indometasin Farnesil ... 3
Mikroenkapsulasi ... 4
Uji Stabilitas ... 4
BAHAN DAN METODE
Bahan dan Alat ... 4
Ekstraksi Indometasin Farnesil dari Dialon dan Penentuan Kadarnya ... 5
Pembuatan Mikrokapsul ... 5
Uji Stabilitas ... 5
Pencirian Mikrokapsul dengan SEM ... 5
HASIL DAN PEMBAHASAN
Kadar Indometasin Farnesil dalam Obat Dialon ... 6
Pembuatan Mikrokapsul ... 6
Uji Stabilitas ... 6
Pencirian Morfologi Mikrokapsul ... 9
SIMPULAN DAN SARAN ... 10
DAFTAR PUSTAKA ... 11
DAFTAR TABEL
Halaman
1
Spesifikasi kitosan niaga ... 2
2
Konsentrasi infar dalam mikrokapsul kitosan-gom guar... 7
3 Persamaan laju penguraian infar semua formula mikrokapsul ... 8
4
Persentase infar yang masih tersalut setelah uji stabilitas 3 bulan... ... 8
5
Usia guna mikrokapsul kitosan-gom guar dengan zat aktif infar... 9
DAFTAR GAMBAR
Halaman
1 Struktur kitosan... 2
2
Struktur hidrogel kitosan (a) ikatan silang kitosan-kitosan, (b) jaringan polimer
hibrid, (c) jaringan semi IPN, dan (d) kitosan berikatan silang ionik... 2
3
Struktur gom guar... 3
4
Struktur indometasin farnesil ... 3
5
Morfologi mikrokasul ... 4
6
Mikrokapsul (a) tanpa dan (b) dengan penambahan infar ... 6
7
Foto-foto SEM permukaan mikrokapsul (a) kosong dan (b) berisi infar ... 6
8
Kurva kadar air formula 1
−
5 ... 7
9
Kurva kadar air formula 6
−
9 ... 7
DAFTAR LAMPIRAN
Halaman
1
Kadar air dan kadar abu kitosan (AOAC 1999) ... 14
2
Penentuan bobot molekul kitosan (Tarbojejevich & Cosani 1996) ... 15
3
Penentuan derajat deasetilasi (Domzsy & Robert dalam Khan
et al
. 2002)... 17
4
Preparasi bahan-bahan yang digunakan ... 18
5
Diagram alir penelitian ... 19
6
Penentuan kemurnian infar dalam ekstrak obat metode spektrofotometri secara
simultan ... 20
7
Spektrum infar 99.2% dari PT Eisai Indonesia (a), vitamin E ( -tokoferol) (b),
dan infar hasil ekstrak obat Dialon dengan spektrofotometer UV .. ... 22
8
Kadar air mikrokapsul infar (%) hasil uji stabilitas dipercepat pada T=(40±2) °C
dan RH (75±5)% selama 3 bulan... 23
9
Deret standar infar untuk penentuan konsentrasi infar dalam ekstrak etanol
mikrokapsul. ... 24
10
Konsentrasi infar (%b/b) hasil uji stabilitas dipercepat pada T=(40±2) °C dan RH
(75±5)% selama 3 bulan... 25
11
Penentuan orde reaksi penguraian infar dalam mikrokapsul formula 1 (kitosan
1.75% [b/v], gom guar 0.05% [b/v], dan glutaraldehida 4.00% [v/v])... 26
12
Penentuan orde reaksi penguraian infar dalam mikrokapsul formula 2 (kitosan
1.75% [b/v], gom guar 0.05% [b/v], dan glutaraldehida 4.50% [v/v])... 27
13
Penentuan orde reaksi penguraian infar dalam mikrokapsul formula 3 (kitosan
1.75% [b/v], gom guar 0.05% [b/v], dan glutaraldehida 5.00% [v/v])... 28
14
Penentuan orde reaksi penguraian infar dalam mikrokapsul formula 4 (kitosan
1.75% [b/v], gom guar 0.19% [b/v], dan glutaraldehida 4.00% [v/v])... 29
15
Penentuan orde reaksi penguraian infar dalam mikrokapsul formula 5 (kitosan
1.75% [b/v], gom guar 0.19% [b/v], dan glutaraldehida 4.50% [v/v])... 30
16
Penentuan orde reaksi penguraian infar dalam mikrokapsul formula 1 (kitosan
1.75% [b/v], gom guar 0.19% [b/v], dan glutaraldehida 5.00% [v/v])... 31
17
Penentuan orde reaksi penguraian infar dalam mikrokapsul formula 1 (kitosan
1.75% [b/v], gom guar 0.33% [b/v], dan glutaraldehida 4.00% [v/v])... 32
18
Penentuan orde reaksi penguraian infar dalam mikrokapsul formula 1 (kitosan
1.75% [b/v], gom guar 0.33% [b/v], dan glutaraldehida 4.50% [v/v])... 33
PENDAHULUAN
Indometasin farnesil (infar) merupakan salah satu senyawa aktif obat yang sangat efektif sebagai obat anti peradangan nonsteroid (NSAID). Obat ini bersifat tidak larut dalam air dan penggunaannya dalam dosis tinggi dapat menyebabkan pendarahan pada saluran pencernaan. Pengendalian pelepasan obat indometasin pernah dilakukan dengan membuatnya dalam bentuk sediaan mikrokapsul (Tiyaboonchai & Ritthidej 2003; Yamada et al. 2001)
Kitosan merupakan aminopolisakarida yang diperoleh melalui deasetilasi kitin. Kitin merupakan biopolimer yang paling melimpah di alam setelah selulosa, dan banyak terkandung dalam limbah. Kitosan memiliki sifat tidak beracun, biokompatibel, biodegradabel, bioadhesif, dan mampu membentuk ikatan silang secara kovalen pada gugus aminonya (Varhosaz & Reza 2005). Selain itu, kitosan merupakan biopolimer polikationik sehingga dapat membentuk gel dalam suasana asam, misalnya di dalam lambung (Sakinnen 2003). Karena sifat-sifat tersebut, kegunaan kitosan dalam industri farmasi dipelajari secara luas sebagai sistem pengantaran obat terkendali.
Kitosan dalam bentuk gel atau lembaran telah digunakan sebagai penyalut obat anti-peradangan ketoprofen (Yamada et al. 2001), indometasin (Rana et al. 2004), dan propanolol hidroklorida (Sutriyo et al. 2005). Namun, gel kitosan yang dihasilkan mudah rapuh. Beberapa penelitian telah dilakukan untuk memodifikasi sifat gel kitosan, di antaranya dengan menambahkan poli(vinil alkohol) (PVA) sebagai bahan saling tembus (interpenetrating agent) dan glutaraldehida sebagai penaut silang (Wang et al. 2004). Penambahan dua bahan tersebut dapat memperbaiki gel kitosan yang terbentuk dengan menurunkan waktu gelasi dan meningkatkan kekuatan mekanik gel. Hidrokoloid alami juga telah banyak ditambahkan untuk memodifikasi gel kitosan, antara lain gom guar (Sugita et al. 2006a), alginat (Sugita et al. 2006b dan Cardenas et al
2003), karboksimetil selulosa (Sugita et al.
2006c), dan gom xantan (Sugita et al. 2007a). Keempat hasil modifikasi tersebut berpotensi sebagai membran dan secara mekanik lebih kuat daripada gel kitosan.
Berdasarkan penelitian Sugita et al.
(2006a) gel kitosan yang terbentuk dengan penambahan penaut-silang glutaraldehida dan gom guar sebagai bahan saling tembus,
memiliki sifat reologi yang lebih baik dan berpotensi sebagai sistem pengantaran obat. Gom guar sendiri pernah dimanfaatkan untuk memperbaiki sistem pengantaran obat untuk mengobati radang dan kanker usus besar (Kshirsagar 2000).
Mekanisme difusi obat ketoprofen dari membran kitosan-gom guar telah dipelajari oleh Nata et al. (2007b). Sementara laju disolusi infar dalam medium usus telah dipelajari Mubarok (2007). Waktu paruh pelepasan infar dalam uji disolusi ini, ialah 51 menit. Kedua penelitian tersebut menunjukkan hasil bahwa mikrokapsul kitosan-gom guar mengalami pembesaran pori ketika kontak dengan cairan.
Mikrokapsul kitosan-gom guar dengan zat aktif infar merupakan sediaan obat yang baru, sehingga perlu dilakukan uji stabilitas untuk mengetahui kestabilan dan usia gunanya. Hal ini perlu dilakukan agar mutu, keamanan, dan khasiat obat selama penggunaan terjamin (Anonim 2005).
Uji stabilitas yang dipercepat dilakukan dalam penelitian ini selama 3 bulan dengan suhu (40±2) °C dan kelembapan relatif (Relative Humidity, RH) (75±5)%. Pemilihan kondisi ini didasarkan pada pembagian wilayah oleh International Conference on Harmonization (ICH). Indonesia masuk ke dalam zona 4, yaitu daerah tropis atau lembap dan panas (Agoes 2001).. Uji stabilitas yang dilakukan dibatasi pada uji stabilitas kimia (kadar infar) dan fisika (kadar air). Data hasil pengukuran kadar infar digunakan untuk menentukan orde reaksi yang merupakan parameter kinetika reaksi penguraian infar, yang diperoleh dengan menggunakan metode grafis.
TINJAUAN PUSTAKA
Kitosan dan Gel Kitosan
O
NH2
OH CH2OH
O
NH2
OH CH2OH
O O
O
n
Gambar 1 Struktur kitosan.
Kitosan, (C6H11NO4)n, dapat berupa
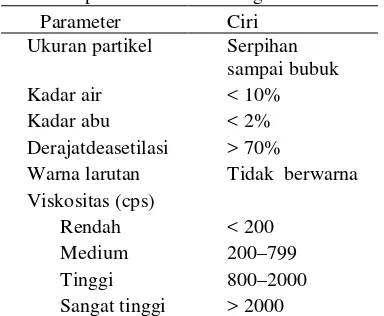
padatan amorf putih, serpihan bening, atau bubuk berwarna gading, yang tidak larut dalam air, alkohol, aseton, dan larutan basa, tetapi larut dalam asam organik maupun anorganik. Kitosan larut dalam kebanyakan asam organik pada pH sekitar 4, tetapi tidak larut pada pH lebih besar dari 6.5. Dalam asam anorganik, seperti HCl dan HNO3, kitosan larut pada konsentrasi 1.1%, tetapi tidak larut pada kadar 10% (Jamaludin 1994). Mutu kitosan ditentukan dari nilai derajat deasetilasi (DD), kadar abu, kadar air, dan viskositas yang ditunjukkan pada Tabel 1.
Tabel 1 Spesifikasi kitosan niaga* Parameter Ciri Ukuran partikel Serpihan
sampai bubuk Kadar air < 10% Kadar abu < 2% Derajatdeasetilasi > 70%
Warna larutan Tidak berwarna Viskositas (cps)
Rendah < 200 Medium 200–799 Tinggi 800–2000 Sangat tinggi > 2000 *Sumber: Anonim (1987) dalam Jamaludin (1994)
Kitosan membentuk gel dalam larutan asam asetat 1%. Gel ialah jejaring tiga dimensi dari molekul primer, yang terentang pada seluruh volume gel dan memerangkap sejumlah pelarut di dalamnya [Oakenfull (1984) dalam Nuraini (1994); Tobolsky (1943) dalam Fardiaz (1989)]. Gel yang dapat menahan air dalam strukturnya disebut hidrogel (Wang et al. 2004). Berdasarkan sifatnya, hidrogel dapat digolongkan menjadi hidrogel kimia dan fisika. Hidrogel kimia dibentuk dari reaksi ireversibel, yang melibatkan ikatan silang secara kovalen, sedangkan, hidrogel fisika dibentuk oleh reaksi yang dapat-balik, dengan ikatan-silang terjadi secara ionik (Stevens 2001 dan Berger
et al. 2004). Contoh hidrogel kimia adalah hidrogel kitosan.
Ikatan-silang kovalen dalam hidrogel kitosan dapat dibedakan menjadi empat bagian. Pertama, ikatan-silang kitosan-kitosan. Kedua, jaringan polimer hibrida (
hybrid polymer network [HPN]). Ketiga, jaringan polimer saling-tembus tanggung atau utuh (semi- interpenetrating polymer network (IPN) atau full-IPN,). Keempat, kitosan berikatan silang ionik. Keempat jenis ikatan kovalen dalam hidrogel kitosan ditampilkan pada Gambar 2 (Berger et al. 2004).
Gambar 2 Struktur hidrogel kitosan: (a) ikatan silang kitosan-kitosan, (b) jaringan polimer hibrida, (c) jaringan semi-IPN, dan (d) kitosan berikatan silang ionik.
Ikatan silang kitosan-kitosan terjadi antara dua unit struktural pada rantai polimer kitosan yang sama. Reaksi penautan silang pada HPN terjadi antara satu unit dari struktur rantai kitosan dan unit lain dari struktur polimer tambahan. Jaringan semi-IPN atau full-IPN terjadi jika ditambahkan polimer lain yang tidak bereaksi dengan larutan kitosan sebelum terjadi ikatan silang. Jaringan semi-IPN, terbentuk jika polimer yang ditambahkan hanya melilit, sementara pada full-IPN, terbentuk jika ditambahkan dua senyawa penaut-silang yang terlibat pada jejaringan (Berger et al. 2004).
gom guar, dan glutaraldehida berturut-turut 2.5% (b/v), 4.86% (b/v), dan 0.33% (v/v), dengan sifat reologi kekuatan gel, titik pecah (break point), ketegaran (rigidity), pembengkakan (swelling), dan pengerutan (sineresis; shrinking) pada kondisi optimum berturut-turut 553.439 g/cm2; 0.968 cm; 4.147 g/cm; 4.0772 g; dan 1.2738 g.
Nata et al. (2007b) melaporkan bahwa membran kitosan-gom guar sebelum diuji difusi tidak menunjukkan adanya pori, tetapi setelah diuji difusi terdapat lubang-lubang kecil dangkal yang tidak menembus membran. Proses pembengkakan membran yang disertai dengan pembukaan pori ini dapat membuat obat terlepas ketika mikrokapsul berinteraksi dengan cairan di dalam tubuh. Sementara itu, Mubarok (2007) melaporkan bahwa mikrokapsul optimum infar tersalut kitosan-gom guar terjadi pada komposisi penyalut gom guar 0.05% (b/v) dan glutaraldehida 4% (v/v) dalam larutan kitosan yang konsentrasinya dibuat tetap, yaitu 1.75% (b/v). Perilaku disolusi mikrokapsul optimum ini dalam medium yang menyerupai pH usus [larutan bufer fosfat pH 7.2-air (1:4)] mengikuti kinetika reaksi orde pertama dengan tetapan laju pelepasan (k) infar dari mikrokapsul sebesar 0.0136 menit-1 dan waktu paruh, t1/2, 51 menit.
Gom Guar
Gom guar merupakan hidrokoloid alami yang diperoleh dari biji Cyamopsis tetragonolobus dan Cyamopsis psoraloides
(famili Leguminosae yang ditemukan di barat laut India dan Pakistan (Nussinovitch 1997). Pengolahan yang dilakukan meliputi pemisahan secara mekanik terhadap kulit biji, lalu lembaganya dibuang, dan endosperma yang mengandung gom digiling menjadi tepung halus (Fardiaz 1989). Gom guar merupakan galaktomanan dengan D-galaktosa berikatan (1 6) pada rantai tulang punggung (1 4) D-manopiranosa (Gambar 3) (Chaplin 2005).
HO H H O H H OH CH2OH
H O O O CH2 O H H
CH2OH H H H OH O H H OH H H OH H n OH OH
Gambar 3 Struktur gom guar.
Gom guar tidak bermuatan, dan juga bersifat kompatibel dengan hampir semua hidrokoloid. Secara khusus dengan karaginan atau gom xantan, dapat terjadi interaksi sinergis. Interaksi gom guar dengan kitosan tidak menghasilkan gel, tetapi hanya meningkatkan kekentalan karena derajat substitusi rantai molekulnya yang tinggi mengurangi interaksi (Fardiaz 1989).
Gom guar berfungsi sebagai bahan saling tembus yang diharapkan dapat menghasilkan sifat gel kitosan yang lebih baik. Sifat jaringan serta interaksi yang mengikat keseluruhan gel menentukan kekuatan, stabilitas, dan tekstur gel. Untuk memperkuat jaringan internal gel ini biasanya digunakan molekul lain sebagai pembentuk ikatan-silang, dalam penelitian ini digunakan glutaraldehida.
Indometasin Farnesil
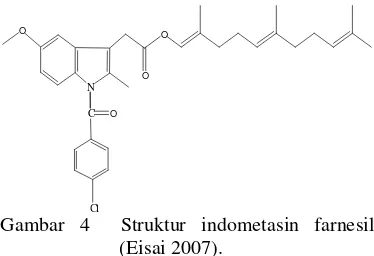
Indometasin farnesil dengan rumus kimia C34H40ClNO4 (562.15 g/mol) merupakan senyawa yang tidak larut dalam air dan lazim digunakan sebagai senyawa aktif dalam obat analgesik atau obat anti peradangan yang aktif pada jaringan (Gambar 4). Indometasin farnesil yang digunakan dalam penelitian diekstraksi dari obat Dialon yang diperoleh dari PT Eisai. Dialon merupakan farnesol larut lemak yang diesterifikasi dengan indometasin, didistribusikan dengan baik dan menunjukkan afinitas yang tinggi di dalam jaringan daerah radang. Studi klinis menunjukkan bahwa Dialon sangat bermanfaat terhadap artritis reumatoid, osteoartritis, dan lumbago.
C O N O O O Cl
Gambar 4 Struktur indometasin farnesil (Eisai 2007).
Indometasin farnesil berupa cairan berminyak warna kuning muda. Obat ini sangat mudah larut dalam aseton, kloroform, asetonitril, atau eter; larut dalam etanol absolut; sedikit larut dalam metanol; serta tidak larut dalam air.
biosintesis prostaglan-din. Penyerapan infar terjadi di saluran pencernaan, tetapi jika jumlahnya berlebihan dapat mengakibatkan pendarahan pada saluran pencernaan
Dosis oral infar untuk orang dewasa sebesar 200 mg, dua kali sehari pada pagi dan malam hari setelah makan. Waktu paruh indometasin farnesil di dalam darah ialah 5–6 jam setelah pemberian, dan hilang dari dalam darah setelah 24 jam (Eisai 2007).
Mikroenkapsulasi
Mikroenkapsulasi merupakan suatu teknik penyalutan bahan yang ukurannya sangat kecil, hasilnya disebut mikrokapsul (Yoshizawa 2004). Mikroenkapsulasi dapat dilakukan secara fisika atau kimia. Pembuatan mikrokapsul yang termasuk metode fisika ialah pengeringan semprot (spray drying), piringan pemutar (rotating dish), stationary extrusion nozzle, centrifugal extrusion nozzle, submerged extrusion nozzle, dan pelapisan suspensi udara. Sementara metode kimia antara lain polimerisasi antarmuka, polimerisasi in-situ, polimerisasi matriks, penguapan pelarut, dan pemisahan fase (Beneta 1996).
Mikrokapsul merupakan partikel kecil yang berisi senyawa aktif atau bahan inti yang dibungkus oleh suatu lapisan atau cangkang. Mikrokapsul komersial biasanya berdiameter 3−800 m dan berisi 10−90% bobot. Sebagian besar kapsul terbuat dari polimer organik baik alami maupun sintetik (Beneta 1996).
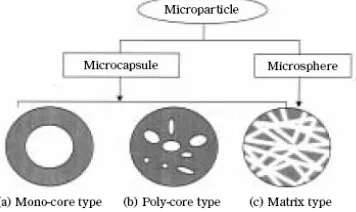
Mikrokapsul dapat diklasifikasikan ke dalam tiga kategori dasar berdasarkan morfologinya, yaitu berinti tunggal, berinti banyak, dan jenis matriks (Yoshizawa 2004) (Gambar 5). Mikrokapsul yang berinti banyak terkadang tidak beraturan bentuknya. Mikrokapsul yang dihasilkan dengan metode pengeringan semprotberinti banyak dan tidak beraturan dengan diameter sekitar 10−300 m (Beneta 1996).
Gambar 5 Morfologi mikrokapsul (Yoshizawa 2004).
Kelebihan mikrokapsul di antaranya adalah dapat mengendalikan pelepasan obat yang dienkapsulasi serta melindungi bahan yang dienkapsulasi dari oksidasi dan reaksi deaktivasi oleh lingkungan. Selain itu, mikrokapsul juga mempertahankan bau dan rasa dari bahan yang dienkapsulasi, dan memudahkan penanganan bahan obat yang berupa bubuk (Yoshizawa 2004).
Uji Stabilitas
Stabilitas didefinisikan sebagai kemampuan suatu produk untuk bertahan dalam batas yang ditetapkan sepanjang periode penyimpanan dan penggunaan, dengan sifat yang sama seperti ketika produk dibuat. Stabilitas dapat dipengaruhi oleh beberapa faktor, yaitu suhu, radiasi, dan kelembapan. Selain itu, ukuran partikel, pH, sifat air dan pelarut yang digunakan, sifat kemasan, dan keberadaan bahan kimia lain yang merupakan kontaminan atau berasal dari pencampuran produk berbeda yang sengaja ditambahkan juga dapat memengaruhi stabilitas sediaan farmasi (Agoes 2001). Oleh karena itu, perlu dilakukan uji stabilitas untuk mengetahui berapa lama obat tersebut dapat digunakan dengan aman dan masih memiliki khasiat. Uji stabilitas yang biasa dilakukan terhadap sediaan farmasi adalah uji stabilitas fisika, kimia, mikrobiologi, stabilitas terapi, dan stabilitas toksikologi.
Setiap sediaan obat baru harus diuji stabilitasnya untuk mengetahui usia guna dari sediaan tersebut sebagai syarat registrasi. Selain itu, juga untuk mengevaluasi formula obat yang dibuat. ICH menetapkan aturan uji stabilitas obat-obatan dalam dokumen Q1A. Berdasarkan dokumen tersebut uji stabilitas untuk bahan aktif atau sediaan farmasi baru, dapat dilakukan dalam jangka panjang atau dipercepat. Uji jangka panjang dilakukan selama 12 bulan pada suhu (30±2) °C dan RH (60±5)% atau (25±2) °C dan RH (65±5)%, sedangkan untuk uji dipercepat dilakukan selama 6 bulan pada suhu (30±2) °C dan RH (60±5)% (ICH 2003) atau selama 3 bulan pada suhu (40±2) °C dan RH (75±5) % (Agoes 2001 & ICH 2003).
BAHAN DAN METODE
Bahan dan Alat
Cikarang Bekasi yang memiliki kadar air 10.80%, kadar abu 0.53% (Lampiran 1), BM 3090.45 g mol-1 (Lampiran 2), dan DD 70.13% (Lampiran 3), air suling, CH3COOH 98% teknis, glutaraldehida 25%, standar vitamin E ( -tokoferol) 98% Merck, etanol absolut, etanol 96% teknis, gom guar, Tween-80, obat Dialon dan standar indometasin farnesil 99.2% dari PT Eisai Indonesia, kertas saring Whatman, dan kapsul No 00.
Peralatan yang digunakan meliputi FTIR Bruker jenis Tensor 37 di Pusat Studi Biofarmaka IPB, mositure analyzer Precise HA 60, mikroskop elektron payaran (SEM) JOEL-JSM-5310LV di Laboratorium Zoologi LIPI Cibinong Bogor, oven J.P. Selecta, pengering semprot Buchi 190 di Seafast PAU IPB, penghomogen Armfield L4R, viskometer Ostwald 100 ml Pyrex, spektrofotometer ultraviolet (UV) Shimadzu Pharmaspec 1700 di Laboratorium Bersama FMIPA IPB,
climatic chamber di Laboratorium Farmasi dan Medika BPPT, serta alat-alat kaca lainnya.
Ekstraksi Indometasin Farnesil dari Dialon dan Penentuan Kadarnya
Sebanyak 30 g obat Dialon dilarutkan dalam 1l etanol 96%. Larutan yang terbentuk disaring dengan kertas Whatman, lalu dipekatkan. Ekstrak pekat ditimbang sebanyak 0.0108 g dan dilarutkan dalam 100 ml etanol 96%. Dibuat pula deret standar infar 0, 2, 4, 6, 8, 12, dan 18 ppm, serta deret standar vitamin E 0, 2, 8, dan 18 ppm dalam etanol 96%. Kedua deret standar tersebut diukur absorbansnya pada λmaks infar (320.2 nm), dan vitamin E (290.6 nm)yang diperoleh dari pengukuran sebelumnya, begitu juga ekstrak infar yang disiapkan sebelumnya.
Pembuatan Mikrokapsul (Mubarok 2007)
Mula-mula dibuat larutan kitosan 1.75% (b/v) dengan pelarut asam asetat 1% (v/v) (Lampiran 4). Sebanyak 228.6 ml larutan ini ditambahkan 38.1 ml larutan gom guar dengan ragam kadar 0.05, 0.19, dan 0.33% (b/v) sambil diaduk sampai homogen. Setelah itu, dilakukan penambahan 7.62 ml glutaraldehida perlahan-lahan sambil diaduk, dengan ragam kadar 4, 4.5, dan 5% (v/v). Campuran diaduk dengan pengaduk megnetik selama 20 menit untuk penyeragaman.
Campuran kitosan-gom guar tersebut kemudian dicampurkan dengan 100 mg infar yang telah dilarutkan dalam 250 ml etanol
96%, dan diberi 5 ml Tween-80 2% sambil diaduk. Campuran akhir ini diaduk selama 1 jam pada suhu kamar sebelum dibuat menjadi mikrokapsul dengan alat pengering semprot sampai terbentuk serbuk halus. Alat pengering semprot yang digunakan mempunyai ukuran diameter lubang 1.5 mm dan diatur pada suhu
inlet 170−185 °C, suhu outlet 65−95 °C, pompa dengan laju alir 60 rpm, dan tekanan semprot pada skala 2 bar. Mikrokapsul kosong tanpa penambahan infar juga dibuat. Pembuatan mikrokapsul dilakukan sebanyak dua kali ulangan. Diagaram alir penelitian ini ditampilkan pada Lampiran 5.
Uji Stabilitas
Setiap formula mikrokapsul dikemas ke dalam kapsul, 1 kapsul berisi 200 mg. Mikrokapsul yang sudah dikemas dimasukkan ke dalam botol cokelat 100 ml. Setiap botol cokelat diisi 18 kapsul, masing-masing 2 kapsul dari sembilan formula yang berbeda. Karena pengamatan dilakukan setiap minggu sampai 12 minggu, disiapkan 12 botol seperti itu.
Botol yang berisi kapsul disimpan di dalam climatic chamber dengan suhu (40±2) °C dan RH (75±5)% selama 3 bulan. Seminggu sekali mikrokapsul diukur kadar infar dan kadar airnya. Begitu pula pada minggu ke-0, yaitu bersamaan dengan dimasukkannya mikrokapsul ke dalam
climatic chamber.
Kadar infar diukur dengan mengekstraksi 0.1000 g mikrokapsul sebanyak 3 kali, masing-masing dengan 15 ml etanol 96% selama 1 jam. Absorbansnya diukur pada panjang gelombang 320.4 nm dengan spektrofotometer UV. Sementara kadar airnya diukur dengan moisture analyzer.
Pencirian Mikrokapsul dengan SEM
HASIL DAN PEMBAHASAN
Kadar Indometasin Farnesil dalam Obat Dialon
Analisis hasil ekstraksi obat Dialon dengan spektrofotometer UV secara simultan menunjukkan bahwa dalam 0.0108 g ekstrak obat terkandung 0.0106 g infar (Lampiran 6), sehingga kadar infar dalam ekstrak obat adalah 98.15%. Sisanya adalah bahan pengisi tambahan, yaitu vitamin E dan natrium dodesil sulfat. Tingginya kadar infar dalam ekstrak ini juga dibuktikan dengan kedekatan
λmaks antara infar hasil ekstraksi dan standar , berturut-turut 320.4 nm dan 320.2 nm dalam pelarut etanol 96% (Lampiran 6).
Pembuatan Mikrokapsul
Banyaknya mikrokapsul hasil pengeringan semprot adalah kira-kira 1.500 g untuk setiap 500 ml campuran mikrokapsul. Mikrokapsul ini berbentuk serbuk halus berwarna kuning, kering, mudah rapuh, dan higroskopis. Mikrokapsul kosong, memiliki warna kuning kecokelatan (Gambar 6). Hal ini diduga akibat warna kuning dari infar lebih muda dibandingkan dengan warna larutan kitosan.
(a)
(b)
Gambar 6 Mikrokapsul (a) tanpa dan (b) dengan penambahan infar.
Berdasarkan hasil pencirian mikrokapsul dengan SEM, mikrokapsul kosong (Gambar 7a) seragam bentuk dan ukurannya daripada mikrokapsul yang berisi infar (Gambar 7b). Kisaran diameter mikrokapsul kosong 1.43– 5.74 m, sedangkan yang berisi infar 1.43– 12.20 m. Bertambahnya diameter mikrokapsul menunjukkan bahwa infar telah tersalut oleh kitosan-gom guar. Namun, penyalutannya tidak seragam, yang diduga karena sebagian gel kitosan-gom guar tidak menyalut infar atau hanya sedikit, atau hanya menempel di permukaan membran.
(a)
(b)
Gambar 7 Foto-foto SEM permukaan mikrokapsul (a) kosong dan (b) berisi infar.
Uji Stabilitas
ICH 2003 memasukkan negara Indonesia ke dalam zona ke-4 (panas dan lembap/tropis). Oleh karena itu, uji stabilitas dipercepat untuk sediaan obat yang diproduksi dan digunakan di Indonesia dilakukan pada suhu 40±2 °C dan RH 75±5 %. Uji dilakukan selama 3 bulan. Dengan penggunaan waktu yang singkat, tetapi diimbangi oleh penggunaan suhu dan RH yang ekstrem, hasil yang diperoleh diharapkan dapat mewakili masa kedaluwarsa sesungguhnya. Uji stabilitas yang dilakukan pada penelitian ini meliputi pengukuran kadar air dan kadar infar.
20 kV ×3500
Kadar Air
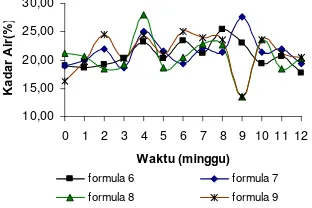
Kadar air yang rendah ( 10%) sangat diharapkan dari suatu sediaan obat, agar kestabilannya lebih lama. Namun, kadar air untuk 9 formula mikrokapsul dalam penelitian ini (Lampiran 8) tergolong tinggi (>10%), yaitu 16.47–21.13% dan berfluktuasi (Gambar 8 dan 9). Kadar air yang tinggi ini diduga diakibatkan oleh sifat membran kitosan-gom guar yang higroskopis. Sugita et al. (2006a) melaporkan bahwa gom guar memiliki kemampuan yang tinggi dalam menyerap air. Sementara kadar air yang berfluktuatif diduga diakibatkan oleh diameter mikrokapsul yang dibuat kurang seragam.
10,00 15,00 20,00 25,00 30,00
0 1 2 3 4 5 6 7 8 9 10 11 12
Waktu (m inggu)
K a d a r A ir (% )
f ormula 1 formula 2 f ormula 3
f ormula 4 formula 5
Gambar 8 Kurva kadar air formula 1−5.
10,00 15,00 20,00 25,00 30,00
0 1 2 3 4 5 6 7 8 9 10 11 12
Waktu (minggu) K a d a r A ir (% )
formula 6 formula 7
formula 8 formula 9
Gambar 9 Kurva kadar air formula 6−9.
Air yang terserap akan membengkakkan mikrokapsul sehingga pori-porinya membesar dan infar yang berada di dalamnya mudah terlepas. Tingginya kadar air juga menyokong pertumbuhan mikroorganisme dan memacu beberapa reaksi kimia yang bersifat merusak (Winarno 1997). Mikrob yang tumbuh biasanya bakteri atau jamur, di antaranya
Staphylococcus aureus. Adanya mikrob dan jamur pada obat dapat mengurangi khasiatnya.
Kadar Indometasin Farnesil
Penetapan kadar infar dalam mikrokapsul selama uji stabilitas dilakukan secara spektrofotometri. Kurva standar yang
digunakan disajikan pada Lampiran 9. Kadar infar yang tersalut membran kitosan-gom guar pada minggu ke-0 untuk semua formula mikrokapsulsekitar 5−9%(b/b) (Tabel 2).
.
Tabel 2 Konsentrasi infar dalam mikrokapsul kitosan-gom guar
[Infar]d (%b/b) Fa [GG]
b
(%b/b)
[Glu]c
(%b/b) minggu ke-0
minggu ke-12 1 0.05 4.00 8.85 6.12
2 4.50 9.72 7.21
3 5.00 8.14 5.32
4 0.19 4.00 6.43 4.27
5 4.50 6.09 4.65
6 5.00 5.71 5.34
7 0.33 4.00 8.67 5.65
8 4.50 5.31 3.83
9 5.00 7.93 4.25
a) formula mikrokapsul; b) konsentrasi gom guar; c)
konsentrasi glutaraldehida;
d) konsentrasi indometasin farnesil
Sebagaimana ditunjukkan pada Tabel 2, setelah 3 bulan penyimpanan kadar infar yang tersalut menurun untuk semua formula mikrokapsul. Hal tersebut biasa terjadi pada suatu sediaan obat yang diuji stabilitasnya. Namun, sediaan obat yang stabil hanya mengalami penurunan kadar zat aktif tidak lebih dari 10%. Penurunan kadar infar yang tersalut diduga terjadi karena membran kitosan-gom guar membengkak saat disimpan di dalam climatic chamber. Menurut Nata et al. (2007b) suhu yang tinggi (40±2 °C) dan didukung dengan kadar air yang tinggi (Huang et al. 2006) dapat membengkakkan membran, sehingga pori-pori pada permukaannya akan membesar dan menyebabkan zat aktif di dalamnya mudah terlepas. Semakin lama mikrokapsul ini dikondisikan pada suhu yang tinggi diduga semakin banyak infar yang terlepas. Hal ini terlihat pada Lampiran 10: dari minggu ke minggu kadar infar yang masih tersalut cenderung menurun.
[ ] [ ]
t = 0 −kt……...……...(1)[ ]
t =ln[ ]
0 −ktln ………...(2)
[ ] [ ]
ktt + Α = Α 0 1 1 …..…………...(3)
[ ]
t[ ]
kt+ = 2 2 1 2 2 1 0 ..……...…...(4) dengan
k = tetapan laju reaksi penguraian infar
t = waktu (minggu)
[A]0 = kadar infar tersalut pada minggu ke-0
[A]t = kadar infar yang tersisa pada
minggu ke-t
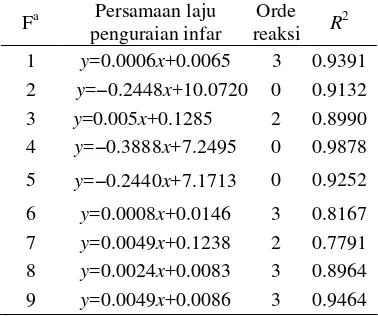
Berdasarkan nilai R2 terbesar yang diperoleh diketahui mikrokapsul formula 2 ,4 , dan 5 cenderung mengikuti orde reaksi ke-0. Sementara formula 3 dan 7 cenderung mengikuti reaksi orde ke-2, serta formula 1, 6, dan 8−9 cenderung mengikuti orde reaksi ke-3. (Tabel 3). Data yang lengkap disajikan pada Lampiran 11−19. Kecilnya nilai R2 yang diperoleh untuk semua formula pada keempat orde, diduga karena mikrokapsul yang dihasilkan dari pengeringan semprot tidak seragam, diameternya 1.43–12.20 m (Gambar 7b).
Tabel 3 Persamaan laju penguraian infar semua formula mikrokapsul
Fa Persamaan laju penguraian infar
Orde reaksi R
2
1 y=0.0006x+0.0065 3 0.9391
2 y=−0.2448x+10.0720 0 0.9132 3 y=0.005x+0.1285 2 0.8990
4 y=−0.3888x+7.2495 0 0.9878
5 y=−0.2440x+7.1713 0 0.9252
6 y=0.0008x+0.0146 3 0.8167 7 y=0.0049x+0.1238 2 0.7791
8 y=0.0024x+0.0083 3 0.8964 9 y=0.0049x+0.0086 3 0.9464
a) formula mikrokapsul
Setelah diperoleh persamaan dan orde reaksi, persentase infar yang masih tersalut setelah 3 bulan (%[A]t) dapat dihitung
berdasarkan persamaan
0
[A] [A]
%[A] t
t = x. 100%...(5)
[A]t diperoleh dari persamaan orde reaksi
(Tabel 3) dengan memasukkan t = 12 minggu, sedangkan [A]0 diperoleh dari nilai intersep persamaan tersebut. Hasil perhitungan %[A]t ditampilkan pada Tabel 4, nilainya 35.64−77.67%.
Tabel 4 Persentase infar yang masih tersalut setelah uji stabilitas selama 3 bulan
Fa [A]0 b (%b/b)
[A]12c (%b/b)
[A]hd
(%)
[A]te
(%) 1 8.77 6.04 31.12 68.88 2 10.07 7.13 29.17 70.83 3 7.78 5.30 31.83 68.17 4 7.25 2.58 64.36 35.64 5 7.17 4.24 40.83 59.17 6 5.85 4.54 22.33 77.67 7 8.08 5.48 32.20 67.80 8 7.76 3.67 52.70 47.30 9 7.62 4.15 45.54 54.46
a) formula mikrokapsul; b) kadar infar minggu ke-0; c) kadar infar minggu ke-12; d) % infar yang hilang; e) % infar yang masih tersalut
Menurut Agoes (2001), suatu sediaan obat dikatakan stabil jika kadar zat aktif yang masih tersalut setelah uji stabilitas jangka panjang sekurang-kurangnya 90%. Persentase infar untuk semua formula setelah 3 bulan rata-rata menunjukkan nilai yang kecil, kecuali formula 2 (70.83%) dan 6 (77.67%), dan seluruhnya masih lebih rendah daripada batas minimum untuk uji stabilitas. Formula yang stabilitasnya terbaik ialah formula 6 (kitosan 1.75 % [b/v], gom guar 0.19 % [b/v], dan glutaraldehida 5.00 % [v/v]), diikuti berturut-turut oleh formula 2, 1, 3, 7, 5, 9, 8, dan formula 4 (kitosan 1.75% [b/v], gom guar 0.19% [b/v], dan glutaraldehida 4.50% [v/v]) (Tabel 4).
Penentuan Usia Guna Berdasarkan Orde Reaksinya
Hasil uji stabilitas selanjutnya digunakan untuk menentukan usia guna mikrokapsul. Batasan 90% kadar indometasin farnesil yang masih tersalut sebagai syarat stabilitas obat dijadikan dasar penentuan usia guna dari sediaan tersebut:
Orde ke-0 k 0 ] A [ 1 . 0 guna
Orde ke-1 k 9 . 0 In guna
Usia =− ...(7)
Orde ke-2 k 0 ] A [ 9 1 guna
Usia = ...(8)
Orde ke-3 k 2 0 ] A [ 62 . 1 19 . 0 guna
Usia = ...(9)
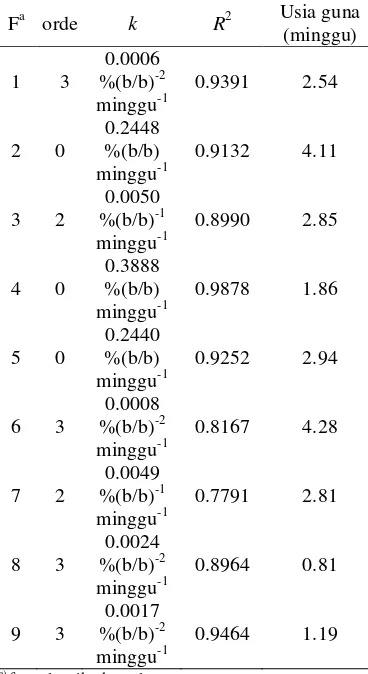
Hasil perhitungan usia guna yang ditampilkan pada Tabel 5, menunjukkan bahwa kesembilan formula mikrokapsul memiliki usia guna relatif rendah (paling lama kurang lebih satu bulan). Berdasarkan usia guna ini, mikrokapsul kitosan-gom guar yang dibuat belum dapat mengendalikan pelepasan obat infar dengan baik. Urutan formula mikrokapsul dari usia guna terpanjang sampai terpendek ialah formula 6 (4.28 minggu 30 hari), 2, 5, 3, 7, 1, formula 4 (1.86 minggu 13 hari), 9, dan formula 8 (0.81 minggu 6 hari).
Tabel 5 Usia guna mikrokapsul kitosan-gom guar dengan zat aktif infar
Fa orde k R2 Usia guna
(minggu)
1 3
0.0006 %(b/b)-2 minggu-1
0.9391 2.54
2 0
0.2448 %(b/b) minggu-1
0.9132 4.11
3 2
0.0050 %(b/b)-1 minggu-1
0.8990 2.85
4 0
0.3888 %(b/b) minggu-1
0.9878 1.86
5 0
0.2440 %(b/b) minggu-1
0.9252 2.94
6 3
0.0008 %(b/b)-2 minggu-1
0.8167 4.28
7 2
0.0049 %(b/b)-1 minggu-1
0.7791 2.81
8 3
0.0024 %(b/b)-2 minggu-1
0.8964 0.81
9 3
0.0017 %(b/b)-2 minggu-1
0.9464 1.19
a) formula mikrokapsul
Berdasarkan kedua parameter uji stabilitas mikrokapsul formula 6 (kitosan 1.75% [b/v], gom guar 0.19% [b/v], dan glutaraldehida 5.00 %[v/v]) menunjukkan stabilitas yang paling baik. Persentase infar yang masih tersalut paling besar dan usia gunanya juga paling panjang. Sementara itu, persentase infar paling kecil ditunjukkan oleh formula 4, dan usia guna paling pendek dimiliki formula 8 walaupun tidak berbeda jauh dengan usia guna mikrokapsul formula 4. Keduanya sulit untuk dibandingkan karena laju penguraiannya mengikuti orde yang berbeda
Menurut Berger et al. (2004) dan Sugita et al. (2006a) penambahan senyawa pengikat silang menyebabkan jejaring gel semakin rapat dan cairan akan sulit masuk. Penambahan gom guar dengan konsentrasi sama pada mikrokapsul formula 4 dan 6 mampu melemahkan ikatan, hanya saja kekuatan ikatan membran pada mikrokapsul formula 4 lebih lemah karena glutaraldehida yang ditambahkan lebih sedikit, yaitu 4.00% [v/v]. Karena itu, ketika disimpan pada suhu
climatic chamber yang tinggi (40±2 °C) membran mikrokapsul formula 4 akan lebih membengkak dibandingkan dengan membran formula 6 dan mengakibatkan infar didalamnya terlepas lebih cepat.
Mikrokapsul formula 6 yang didapati paling baik stabilitasnya bukanlah komposisi gel yang paling kokoh ataupun yang paling rapuh. Mikrokapsul formula 7 (kitosan 1.75% [b/v], gom guar 0.33% [b/v], dan glutaraldehida 4.00% [v/v]) yang diperkirakan paling rapuh dan mikrokapsul formula 3 (kitosan 1.75% [b/v], gom guar 0.05% [b/v], dan glutaraldehida 5.00% [v/v]) yang diduga paling kokoh, justru memiliki stabilitas lebih rendah, baik dilihat dari kadar infar yang masih tersalut maupun usia gunanya. Kekuatan membran yang sangat besar (konsentrasi glutaraldehida tinggi dan gom guar rendah) agaknya membuat infar banyak yang tersalut di permukaannya dan sulit tersalut di kedalaman mikrokapsul. Sebaliknya jika kekuatan membran rendah (konsentrasi glutaraldehida rendah dan konsentrasi gom guar tinggi), jejaring gel yang terbentuk akan renggang. Kedua hal ini menyebabkan infar akan mudah lepas sehingga persentase infar yang masih tersalut lebih rendah dan usia gunanya lebih singkat.
Pencirian Morfologi Mikrokapsul
dan 5. Hal ini dilakukan karena ketersediaan sampel yang mencukupi untuk pencirian dengan SEM. Hasil SEM pada Gambar 10 menunjukkan diameter mikrokapsul formula 3 (1.98−15.60 m) lebih besar daripada formula 4 (1.49−11.70 m) dan 5 (2.72 −9.18 m) yang telah diuji stabilitasnya, dan juga lebih besar daripada mikrokapsul yang belum diuji stabilitasnya (1.43−12.20 m).
(a)
(b)
(c)
Gambar 10 Foto-foto SEM permukaan mikro-kapsul setelah uji stabilitas: formula 3 (a), formula 4 (b), dan formula 5 (c).
Konsentrasi gom guar untuk formula 4 dan 5 (0.19% [b/v]) lebih besar dari formula 3 (0.05% [b/v]), sedangkan konsentrasi glutaraldehida formula 3 (5.00% [v/v]) > 5 (4.50% [v/v]) > 4 (4.00% [v/v]). Semakin rendah konsentrasi gom guar dan semakin
tinggi konsentrasi glutaraldehida, maka jejaring gel semakin rapat. Hal ini menyebabkan infar sulit masuk ke dalam membran formula 3. Namun, kenyataannya diameter mikrokapsul formula 3 lebih besar daripada formula 4 dan 5 yang diduga memiliki jejaring yang lebih renggang. Jejaring gel yang renggang diduga mengakibatkan infar mudah masuk dan keluar, sehingga mikrokapsul formula 4 dan 5 setelah uji stabilitas memiliki diameter lebih kecil. Mikrokapsul formula 5 memiliki konsentrasi glutaraldehida lebih tinggi daripada formula 4, sehingga diemeternya lebih kecil.
SIMPULAN DAN SARAN
Simpulan
Kesembilan formula mikrokapsul yang dibuat menunjukkan stabilitas kurang baik dan usia gunanya relatif pendek. Dari 9 formula tersebut, mikrokapsul formula 6 dengan komposisi penyalut gom guar 0.19% [b/v] dan glutaraldehida 5.00% [v/v] dalam larutan kitosan yang dibuat tetap (1.75% [b/v]), merupakan mikrokapsul yang paling stabil dengan persentase infar yang masih tersalut, tetapan laju reaksi, dan usia guna berturut-turut 77.67%, 0.0008 (%b/b) -2minggu-1, dan 4.28 minggu atau 30 hari. Diameter mikrokapsul formula 3 (1.98−15.60 m) lebih besar daripada diameter formula 4 (1.49−11.70 m) dan 5 (2.72−9.18 m) yang telah diuji stabilitasnya, dan juga lebih besar daripada diameter mikrokapsul yang belum diuji stabilitasnya (1.43−12.20 m).
Saran
Bahan baku yang digunakan maupun mirokapsul yang dihasilkan sebaiknya disimpan di dalam eksikator selama penanganannya karena bersifat higroskopis dan sangat berpengaruh terhadap stabilitas mikrokapsul yang dibuat. Penambahan silika gel dalam botol untuk uji stabilitas juga diduga perlu agar kadar airnya lebih stabil sehingga zat aktif tidak mudah terurai. Selain itu, perlu dilakukan analisis denga mikroskop elektron transmisi untuk mengetahui ketebalan gel yang dihasilkan.
20 kV x 2000
2.72 -9.18 m
20 kV x 2000
20 kV x 2000
1.49 -11.7 m
DAFTAR PUSTAKA
Abreu FR de, Sergio PCF. 2005. Preparation and characterization of carboxymethyl chitosan. Polimerous: Ciencia e Tecnologia 15:79-83.
Agoes G. 2001. Studi Stabilitas Sediaan Farmasi. Bandung: Fakultas Teknologi Farmasi Program Pasca Sarjana Institut Teknologi Bandung.
[Anonim]. 2005. Spray drying as a microfabrication process. Upperton Particle Technologies. http://wawen\situs\upperton [24 Okt 2005].
[AOAC]. Association of Official Analytical Chemist. 1999. Official Methods of Analysis of AOAC International. 5th Revision. Volume 2. Cunnif P (Editor). Maryland: AOAC International.
Atkins PW. 1996. Kimia Fisik. Jilid 2. Ed ke-4. Kartohadiprodjo II, penerjemah;. Indarto PW, editor; Jakarta: Erlangga. Terjemahan dari: Physical Chemistry.
Berger J et al. 2004. Structure and interactions in covalently and ionically crosslinked chitosan hydrogels for biomedical application. Eur J Pharm Biopharm 57:19-34.
Beneta S. 1996. Microcapsulation Method and Industrial Application. New York: Marcel Dekker.
Cardenas A, Monal WA, Goycoolea FM, Ciapara IH, Peniche C. 2003. Diffusion through membranes of polyelectrolyte complex of chitosan and alginate.
Macromol Biosci 3:535-539.
Chaplin M. 2005. Guar gum. London: South Bank University. http://chem.skku. ac.kr/~wkpark/tutor/mirror/www.martin.ch aplin.btinternet.co.uk/hygua.html [3 Agu 2003].
[Eisai]. 2007. Dialon. Bogor: PT Eisai Indonesia.
Fardiaz D. 1989. Hidrokoloid. Bogor: Pusat Antar Universitas Pangan dan Gizi, Institut Pertanian Bogor.
Huang J, Wang X, Yu X. 2006. Solute permeation through the polyurethane-NIPAAm hydrogel membranes with various cross-linking densities. J Desalination 192:125-131.
[ICH]. International Conference on Harmonization. 2003. Guidance for Industry Q1A (R2) Stability Testing of New Drug Substances and Products. Revision 2.U.S. Department of Health and Human Services Food and Drug Administration. http://www.fda.gov/cber/guidelines.htm. [12 Apr 2007].
Jamaludin MA. 1994. Isolasi dan pencirian kitosan limbah udang windu (Penaeus monodon fabricus) dan afinitasnya terhadap ion logam Pb2+, Cr6+, dan Ni2+ [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Khan TA, Kok KP, Hung SC. 2002. Reporting degree of deacetylation values of chitosan: the influence of analytical methods. J Pharm Pharmeceut Sci 5:205-212.
Kshirsagar NA. 2000. Drug delivery system.
Indian J Pharmacol 32: 54-61.S
Mubarok M. 2007. Uji disolusi obat anti-peradangan yang tersalut gel kitosan-gom guar [Skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Nata F, Sugita P, Sjachriza A, Arifin B. 2007b. Diffusion behavior of ketoprofen through chitosan-guar gum membranes.
Perilaku Difusi Ketoprofen Melalui Membran Kitosan-Gom Guar. Prosiding Seminar International Conference and Workshop on Basic science and Applied Science.[6-7 Agustus 2007].
Nuraini D. 1994. Pengaruh jenis hidrokoloid terhadap pembentukan gel cincau hitam (Mesona palustris BL) [tesis]. Bogor: Program Pasca Sarjana, Institut Pertanian Bogor.
Nussinovitch A. 1997. Hydrocolloid Applications. Israel: Chapman-Hall.
human/rat/rabbit epidermal sheet. J Pharm Pharmaceut Sci 8:10-17.
Sakinnen M. 2003. Biopharmaceutical evaluation of microcrystalline chitosan as release-rate-controlling hydrophilic polymer in granules for gastro-retentive drug delivery [disertasi]. Helsinki: Faculty of Science, University of Helsinki.
Stevens MP. 2001. Kimia Polimer. Sopyan I, penerjemah. Jakarta: Pradnya Paramita. Terjemahan dari: Polymer Chemistry: An Introduction.
Sugita P, Sjachriza A, Lestari SI. 2006a. Sintesis dan optimalisasi gel kitosan-gom guar. J Nature 9:32-36.
Sugita P, Sjachriza A, Wahyono D. 2006b. Sintesis dan optimalisasi gel kitosan-alginat. J Sains Teknol Indones 8:133-137.
Sugita P, Sjachriza A, Rachmanita. 2006c. Sintesis dan optimalisasi gel kitosan-karboksimetilselulosa. Di dalam: Arifin B, Wukirsari T, Gunawan S, Wahyuni WT, editor. Sintesis dan Optimalisasi Gel Kitosan-Karboksimetil Selulosa. Prosiding Seminar Nasional Himpunan Kimia Indonesia; Auditorium Rektorat IPB Darmaga, 12 Sep 2006. Bogor: Departemen Kimia FMIPA Institut Pertanian Bogor. .hlm. 380-386.
Sugita P, Sjachriza A, Utomo D.W. 2007a. Optimization synthesis chitosan-xanthan gum gel for metal adsorption. Sintesis dan Optimalisasi Gel Kitosan-Gom Xantan.
Proceeding of 1st International Conference on Chemical Sciences; Yogyakarta, 24-26 Mei 2007.
Sutriyo, Joshita D, Indah R. 2005. Perbandingan pelepasan propanolol hidroklorida dari matriks kitosan, etil selulosa, dan hidroksipropil metil selulosa.
Maj Ilmu Kefarmasian 2:145-153.
Tarbojevich M, Cosani A. 1996. Molecular weight determination of chitin and chitosan. Di dalam Muzarelli RAA & Peter MG (Editor) 1997. Chitin Handbook.
Grottammare: European Chitin Society 85-108.
Tiyaboonchai W, Ritthidej GC. 2003. Development of indomethacin sustained release microcapsules using chitosan-carboxymethyl cellulose complex coacervation. Songklanakrin J Sci Technol
25:245-254.
Varhosaz J, Reza A. 2005. Effect of citic acids as cross-lingking agent on insulin loaded chitosan microspheres. Iranian Polym J
14: 647-656.
Wang T, Turhan M, Gunasekaram S. 2004. Selected properties of pH-sensitive, biodegradable chitosan-poly(vinyl alcohol) hydrogel. Society of Chemical Industry.
Polym Int 53:911-918.
Winarno. FG. 1997. Kimia Pangan dan Gizi.
Jakarta: Gramedia.
Yamada T, Onishi H, Machida Y. 2001. In vitro and in vivo evaluation of sustained release chitosan-coated ketoprofen microparticles. Yakugaku Zasshi 121:239-245.
Lampiran 1 Kadar air dan kadar abu kitosan
Analisis kadar air
Penentuan kadar air kitosan dilakukan dengan menggunakan alat mosture analizer. Sebanyak
±
1.0000 g kitosan dimasukkan ke dalam cawan aluminium, kemudian cawan beserta isinya dimasukkan ke dalam alat mosture analizer sampai bobot yang terbaca konstan.Analisis kadar abu (AOAC 1999)
Penentuan kadar abu kitosan dilakukan dengan metode gravimetri. Cawan porselen dibersihkan dan dimasukkan ke dalam tanur untuk menghilangkan sisa-sisa kotoran yang menempel dalam cawan, kemudian didinginkan dalam desikator dan ditimbang. Sebanyak
±
0.5000 g kitosan dimasukkan ke dalam cawan tersebut dan dibakar dalam tanur pengabuan dengan suhu 600 oC sampai diperoleh