PELAPISAN KOMPOSIT HIDROKSIAPATIT-KITOSAN
PADA LOGAM STAINLESS STEEL 316 UNTUK
MENINGKATKAN KETAHANAN KOROSI
ADI IRIANTO MARIST
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
ADI IRIANTO MARIST. Pelapisan Komposit Hidroksiapatit-Kitosan pada
Logam Stainless
Steel
316 untuk Meningkatkan Ketahanan Korosi
.
Dibimbing
oleh SRI MULIJANI dan SULISTIOSO GIAT SUKARYO.
Logam yang digunakan untuk proses implantasi harus memiliki ketahanan
korosi yang baik agar tidak mudah terkorosi ketika diimplan ke dalam tubuh.
Ketahanan korosi logam stainless
steel
316 dapat ditingkatkan melalui pelapisan
logam oleh komposit hidroksiapatit-kitosan dengan nisbah komposisi
hidroksiapatit (gram) dan kitosan 3% (mL) 0.2:0, 0.2:0.1, 0.2:0.5, 0.2:1.0, dan
0.2:1.5. Keberadaan kitosan selain untuk meningkatkan ketahanan korosi dari
logam tetapi juga untuk mempertahankan posisi hidroksiapatit tetap pada
permukaan logam. Ketahanan korosi meningkat seiring dengan meningkatnya
jumlah kitosan yang ditambahkan dengan komposisi hidroksiapatit-kitosan
optimum 0.2:1.0.
ABSTRACT
ADI IRIANTO MARIST. Hydroxyapatite-Chitosan Composite Coating on
Stainless Steel 316 to Improve Corrosion Resistance. Under direction of SRI
MULIJANI and SULISTIOSO GIAT SUKARYO.
Metals that were used in bone implantation should have good corrosion
resistance that were not easily corroded when implanted into the body. Metal
corrosion resistance of stainless steel 316 can be enhanced through the metal
coating by hydroxyapatite-chitosan composite with composition ratio of
hydroxyapatite (gram) and chitosan 3% (mL) 0.2:0, 0.2:0.1, 0.2:0.5, 0.2:1.0, and
0.2:1.5. Besides improving the corrosion resistance of metal, the presence of
chitosan also maintain the position of hydroxyapatite on metal surfaces. Corrosion
resistance increases with increasing amount of chitosan added and the best
composition of hydroxyapatite-chitosan composite was 0.2:1.0.
PELAPISAN KOMPOSIT HIDROKSIAPATIT-KITOSAN
PADA LOGAM STAINLESS STEEL 316 UNTUK
MENINGKATKAN KETAHANAN KOROSI
ADI IRIANTO MARIST
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Pelapisan Komposit Hidroksiapatit-Kitosan pada Logam Stainless Steel
316 untuk Meningkatkan Ketahanan Korosi
Nama : Adi Irianto Marist
NIM : G44070045
Menyetujui
Pembimbing I,
Pembimbing II,
Dr. Sri Mulijani, MS
Drs. Sulistioso Giat Sukaryo, MT
NIP 196304011991032001
NIP 195708261988011001
Mengetahui
Ketua Departemen Kimia
Prof. Dr. Ir. Tun Tedja Irawadi, MS.
NIP 195012271976032002
PRAKATA
Puji dan syukur kehadirat Allah SWT atas rahmat dan karunia-Nya yang
berlimpah sehingga penulis dapat menyelesaikan karya ilmiah ini. Penelitian ini
dilaksanakan dari bulan Januari sampai Juni 2011 yang bertempat di
Laboratorium Kimia Anorganik, Departemen Kimia dan Laboratorium Biofisika,
Departemen Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut
Pertanian Bogor serta Laboratorium PTBIN BATAN-PUSPITEK Serpong.
Penulis mengucapkan terima kasih kepada yang terhormat Ibu Dr. Sri
Mulijani, MS selaku pembimbing satu dan Bapak Drs. Sulistioso Giat Sukaryo,
MT selaku pembimbing kedua atas petunjuk dan bimbingan yang telah diberikan
kepada penulis selama penelitian dan penyusunan karya ilmiah ini. Terima kasih
kepada Bapak Syawal dan Bapak Chacha yang telah membantu penulis dalam
pemakaian alat dan bahan di laboratorium.
Ungkapan terima kasih kepada Papa, mama, adikku dan seluruh keluarga
atas dukungan dan kasih sayangnya. Ucapan terima kasih kepada Retno, Danang,
dan Randi yang telah memberikan semangat, motivasi dan dorongan dalam
menyusun karya ilmiah ini.
Semoga tulisan ini dapat bermanfaat bagi penulis maupun bagi pembaca.
Bogor, Juni 2011
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 30 Maret 1989 dari ayah Moch.
Sugiarto dan ibu Iriani Sjam. Penulis merupakan putra pertama dari dua
bersaudara.
Tahun 2000 penulis menyelesaikan sekolah di SDN Cijujung I Bogor dan
pada tahun 2003 penulis menyelesaikan sekolahnya di SLTPN 8 Bogor. Tahun
2007 penulis lulus dari SMAKBo dan pada tahun yang sama lulus seleksi masuk
IPB melalui jalur Undangan Seleksi Masuk IPB. Penulis memilih Program Studi
Kimia, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
DAFTAR ISI
Halaman
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... vii
PENDAHULUAN
... 1METODE
... 1Bahan dan Alat
... 1Lingkup Kerja
... 1HASIL DAN PEMBAHASAN
... 3Cangkang Telur
... 3Hidroksiapatit
... 3Pelapisan Hidroksiapatit-Kitosan
... 6Ketahanan Korosi
... 8SIMPULAN DAN SARAN
... 9Simpulan
... 9Saran
... 9DAFTAR PUSTAKA
... 9DAFTAR GAMBAR
Halaman
1 Pola difraksi sinar-X serbuk cangkang telur.. ... 3
2 Pola difraksi sinar-X Hidroksiapatit Dahlan
et al.
(2009) ... 4
3 Pola difraksi sinar-X Hidroksiapatit Pramanik
et al.
(2005)... 4
4 Pola difraksi sinar-X hidroksiapatit sintesis dan komersil ... 5
5 Hasil SEM hidroksiapatit sintesis dan komersil ... 5
6 Spektrogram inframerah hidroksiapatit komersil dan sintesis ... 5
7 Sel elektroforesis deposisi ... 7
8 Pola difraksi sinar-X SS 316 dilapisi hidroksiapatit-kitosan ... 7
9 Pola difraksi sinar-X komposit hidroksiapatit-kitosan Yildirim (2004) ... 8
10 Hasil uji korosi ... 9
DAFTAR LAMPIRAN
Halaman
1 Bagan alir penelititan ... 13
2 Data JCPDS ... 14
3 Tabel data analisis hasil XRD ... 18
4 Perhitungan kadar kalsium ... 21
5 Pola difraksi sinar-X kitosan ... 22
6 Data uji korosi ... 23
PENDAHULUAN
Berbagai macam jenis kecelakaan terjadi tiap tahunnya, baik itu ringan ataupun berat yang memungkinkan terjadinya kerusakan pada tulang. Kerusakan tulang dapat diatasi melalui pemasangan pen (implantasi) pada bagian tulang yang patah untuk mengembalikan posisi patahan tulang ke posisi semula (reposisi) dan mempertahankan posisi itu selama masa penyembuhan patah tulang (imobilisasi) (Oktavia 2009).
Logam yang digunakan dalam proses
implant harus memiliki sifat biokompatibilitas
yang tinggi agar keberadaannya di dalam tubuh tidak dianggap sebagai benda asing. Penggunaan logam yang memiliki biokompatibilitas rendah dapat menyebabkan korosi pada logam oleh cairan tubuh. Korosi logam pen dapat menimbulkan reaksi peradangan (inflamasi) di sekitar jaringan yang diimplankan sehingga apabila digunakan dalam jangka waktu lebih lama akan sangat berbahaya bagi tubuh (Manivasagam et al.
2010).
Ketahanan korosi dapat ditingkatkan melalui pelapisan logam oleh suatu material yang biokompatibel terhadap tubuh. Material tersebut harus cenderung tidak bereaksi (inert) ketika digunakan sebagai pengganti fungsi dari jaringan tubuh yang berkontak langsung dengan cairan tubuh (Karokaro et al. 2008). Salah satu material yang dapat digunakan untuk melapisi logam pen ialah hidroksiapatit (HAp).
Hidroksiapatit (Ca10(PO4)6(OH)2) dapat berikatan kuat dengan tulang, membentuk lapisan pada permukaan jaringan tulang, dan mempercepat pembentukan tulang pada permukaan yang diimplantasi (Pang dan Zhitomirsky 2005; Maachaou et al. 2008). Hidroksiapatit memiliki keterbatasan penggunaan yaitu sulit dijaga agar tetap pada tempatnya setelah diimplantasikan di tulang. Kelemahan ini diatasi dengan mengkombinasikan hidroksiapatit dalam matriks polimer seperti kitosan (Maachaou et al. 2008).
Proses pelapisan logam dengan apatit dapat dilakukan dengan berbagai macam metode seperti elektroforesis deposisi (EPD), sol gel, plasma spraying, ion sputtering, laser
ablation, hydrothermal, dan biomimetic (Pal
et al. 2005). Penelitian ini menggunakan
metode elektroforesis deposisi (EPD) untuk melapisi logam stainless steel (SS) 316 dengan komposit hidroksiapatit-kitosan. Kelebihan penggunaan metode EPD adalah
murah, pelapisan yang tipis dan merata, proses pada temperatur rendah, tanpa fase transformasi selama pelapisan dan kekuatan pelapisan yang tinggi (Javidi et al. 2008). Kelebihan utama metode EPD ialah kemampuannya dalam mengontrol stokiometri deposit. Derajat stokiometri deposit elektroforesis diatur dari kandungan komposisi serbuk yang digunakan (Pang dan Zhitomirsky 2005).
Penelitian ini bertujuan untuk meningkatkan ketahanan korosi logam stainless steel 316 dengan melapiskan komposit hidroksiapatit-kitosan pada logam tersebut menggunakan metode elektroforesis deposisi.
METODE
Bahan dan Alat
Alat-alat yang digunakan adalah alat-alat kaca, pipet ukur, hot plate, tanur, oven, spektrofotometer serapan atom (SSA), alat difraksi sinar-X (XRD), alat potensiostat/ galvanostat, alat elektroforesis deposisi PS-520, mikroskop stereo, FTIR dan mikroskop elektron payaran (SEM).
Bahan-bahan yang digunakan adalah cangkang telur, akuades, P2O5, kitosan, larutan asam asetat 2%, logam SS 316 dan 316L, etanol, larutan infus NaCl 0.9%, larutan NaOH 10 M, dan larutan H2SO4:HCl:air (1:1:1).
Lingkup Kerja
Penelitian terdiri dari beberapa tahap (Lampiran 1). Tahap pertama preparasi cangkang telur. Tahap kedua penentuan kadar Ca dalam serbuk cangkang telur menggunakan SSA. Tahap ketiga adalah sintesis hidroksiapatit metode kering. Tahap keempat ialah perlakuan terhadap logam SS 316. Tahap kelima adalah pelapisan logam SS 316 dengan metode elektroforesis deposisi (EPD). Tahap keenam adalah uji mikrostruktur, uji korosi, dan uji analisis fase XRD.
Preparasi Cangkang Telur (Modifikasi Prabakaran et al. 2005)
2
pada suhu 1000 °C selama 6 jam sehingga diperoleh serbuk cangkang telur yang berwarna putih. Serbuk cangkang telur dilakukan analisis pencirian dengan XRD untuk mengetahui fase yang terkandung di dalamnya.
Penentuan Kadar Kalsium Menggunakan SSA
Sebanyak 0.1 gram sampel serbuk cangkang telur dilarutkan dalam 1 mL HNO3 pekat kemudian diencerkan dengan aquadest hingga volume 50 mL. Deret standar dari CaCO3 disiapkan dengan cara yang sama dalam deret konsentrasi Ca 0, 2, 4, 8, 12, dan 16 ppm. Sampel dan deret standar yang telah siap kemudian diukur menggunakan SSA.
Sintesis Hidroksiapatit Metode Kering (Modifikasi Dahlan et al. 2009 dan Pramanik
et al. 2005)
Sebanyak 4.6430 gram P2O5 dan 8.9195 gram serbuk cangkang telur setelah pemanasan dicampur dan dimiling selama 6 jam (perbandingan antara P2O5 dan CaO sebesar 46.43% dan 50.52%). Campuran kemudian disintering pada suhu 1250 °C selama 2 jam agar terbentuk hidroksiapatit murni. Kemudian dilakukan analisis pencirian dengan XRD untuk mengetahui fase yang terkandung di dalamnya dan analisis mikrostruktur menggunakan SEM.
Perlakuan Logam Stainless Steel 316 (Modifikasi Lu Xiong et al. 2006)
Logam stainless steel 316 terlebih dahulu dipotong membentuk koin yang memiliki diameter sebesar 1.5 cm. Koin logam kemudian diamplas dengan kertas amplas yang memiliki kekasaran 60. Logam lalu direndam di dalam larutan H2SO4:HCl:air (1:1:1) selama 1 jam pada suhu 60 °C. Logam yang telah direndam dalam larutan H2SO4:HCl:air (1:1:1) dicuci dengan air suling lalu direndam dalam larutan NaOH 10 M selama 24 jam. Kemudian logam dicuci dengan air suling dan dikeringkan di udara terbuka selama 24 jam.
Pelapisan Logam SS 316 dengan Metode Elektroforesis Deposisi (EPD) (Modifikasi Pang dan Zhitomirsky 2007 dan Bowo 2009)
Pelapisan logam SS dengan hidroksiapatit-kitosan menggunakan metode EPD dilakukan dengan membuat larutan kitosan 3% terlebih dahulu melalui pelarutan 3 gram kitosan
dalam larutan asam asetat 2% hingga volume 100 mL. Larutan kitosan yang telah dibuat kemudian dilarutkan ke dalam 25 mL etanol dengan variasi volume kitosan 0, 0.1, 0.5, 1.0, dan 1.5 mL dan ditambahkan 0.2 gram hidroksiapatit sedikit demi sedikit dengan diaduk pada kecepatan pengadukan 500 rpm hingga homogen. Larutan koloid hidroksiapatit-kitosan yang telah terbentuk dihubungkan dengan dua elektroda, sebagai elektroda bermuatan negatif digunakan logam SS 316 yang merupakan target pelapisan dan sebagai elektroda bermuatan positif digunakan karbon. Selama proses elektroforesis deposisi, hidroksiapatit dan kitosan yang terdispersi akan bergerak karena pengaruh arus listrik sehingga akan menempel pada permukaan logam SS 316. Sumber tegangan yang digunakan ialah 120 V selama 2 menit.
Uji Analisis Fase Menggunakan XRD
Sampel yang akan dianalisis ditempatkan pada suatu spesimen holder yang kemudian diletakkan pada guaniometer dan dirotasikan pada sudut kalibrasi (2θ) tertentu. Hasil yang diperoleh berupa suatu difraktogram yang menunjukkan fase yang terdapat dalam sampel. Jenis fase yang terkandung ditentukan melalui perbandingan terhadap data Joint Committee on Powder Diffraction Standards
(JCPDS) (Lampiran 2).
Uji Ketahanan Korosi
Proses uji ketahanan korosi dilakukan dengan menggunakan perangkat potensiostat/ galvanostat model 273 pada potensial -20 mV sampai 20 mV dalam media pengkorosi larutan infus NaCl 0.9%. Logam yang akan diuji dirangkai pada working electrode dan dimasukkan ke dalam labu yang berisi media pengkorosi selanjutnya counter electrode dan
reference electrode dirangkai pada labu dan
dihubungkan pada perangkat potensiostat/ galvanostat. Laju korosi dapat diperoleh dengan adanya aliran pergerakan elektron pada reaksi elektrokimia. Laju korosi (mpy) ditentukan menggunakan rumus :
R mpy = 0.129 . BE . I D Keterangan :
R : Laju korosi (mpy)
BE : Berat ekivalen logam (gram) I : Arus korosi (µA/cm2)
Uji Mikrostruktur dengan SEM
Sampel ditempelkan pada cell holder
kemudian disalut emas dalam keadaan vakum selama waktu dan kuat arus tertentu dengan
ion coater. Sampel dimasukkan pada tempat
sampel dalam alat SEM dengan tegangan tertentu. Gambar yang dihasilkan berupa topografi dengan segala tonjolan, lekukan, dan lubang pada permukaan.
HASIL DAN PEMBAHASAN
Cangkang Telur
Proses pembentukan senyawa hidroksiapatit yang berkualitas dan murni memerlukan biaya yang tidak murah. Penggunaan cangkang telur sebagai sumber kalsium dalam pembentukan senyawa hidroksiapatit merupakan solusi yang tepat untuk memangkas biaya produksi hidroksiapatit (Dasgupta et al. 2004). Cangkang telur mengandung kalsium karbonat (94%), kalsium fosfat (1%), senyawa organik (4%), dan magnesium karbonat (1%). Tingginya kadar kalsium yang dimiliki cangkang telur, mendorong penggunaan limbah cangkang telur sebagai sumber kalsium alami dalam proses pembuatan hidroksiapatit (Pankaew et al. 2010). Selain itu cangkang telur juga tidak mengandung senyawa beracun sehingga dapat digunakan dalam bidang farmasi dan pangan (Murakami dan Rodrigues 2007).
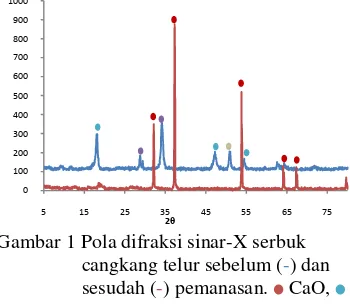
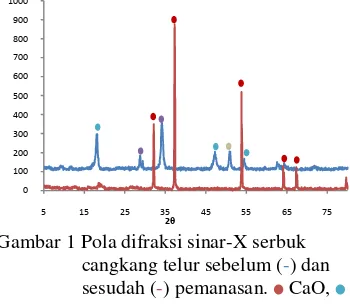
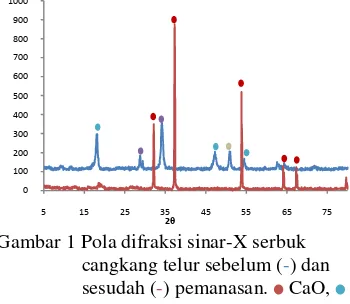
Gambar 1 menunjukkan bahwa pada serbuk cangkang telur sebelum pemanasan terdapat fase CaCO3, Ca3(PO4)2 dan MgCO3. Keberadaan fase CaCO3 ditunjukkan dengan adanya puncak pada sudut 2θ 18.500°, 47.250°, dan 54.449°, fase Ca3(PO4)2 pada 28.750° dan 34.150° serta fase MgCO3 pada 50.850° (Lampiran 3). Preparasi awal cangkang telur dengan memanaskan cangkang telur pada suhu 1000 °C selama 6 jam mengakibatkan kalsium karbonat yang terkandung di dalam cangkang telur berubah menjadi kalsium oksida (Bahrololoom et al.
2009). Puncak fase CaO berada pada sudut 2θ
32.150°, 37.300°, 53.799°, 64.099°, dan 67.300° (Lampiran 3). Pemanasan ini juga dimaksudkan untuk menghilangkan karbonat yang merupakan zat pengganggu dalam proses kristalisasi hidroksiapatit (Dahlan et al. 2009). Ion karbonat dapat menempati posisi pada struktur hidroksiapatit, yaitu pada posisi pertama menggantikan gugus OH- membentuk
senyawa apatit karbonat tipe A Ca10(PO4)6CO3 (AKA) dan posisi kedua menggantikan gugus PO43- membentuk senyawa apatit karbonat tipe B Ca10(PO4)3(CO3)3(OH)2 (AKB) (Aoki 1991, diacu dalam Septiarini 2009). Serbuk cangkang telur yang telah dikalsinasi pun harus disimpan di dalam wadah yang tertutup rapat untuk menghindari masuknya ion karbonat dan air dari udara ke dalam serbuk cangkang telur yang dapat mengganggu proses pembentukan hidroksiapatit. Kadar CaO yang terkandung di dalam serbuk cangkang telur setelah pemanasan berdasarkan hasil analisis menggunakan SSA sebesar 56.64% (Lampiran 4).
Gambar 1 Pola difraksi sinar-X serbuk cangkang telur sebelum (-) dan sesudah (-) pemanasan. CaO, CaCO3, Ca3(PO4)2, MgCO3.
Hidroksiapatit
Hidroksiapatit merupakan suatu material bioaktif yang berpotensial digunakan sebagai pelapis dalam implantasi komposit. Bioaktif hidroksiapatit memiliki kesamaan struktur dan komposisi dengan komponen anorganik dari jaringan keras biologis seperti material pada struktur tulang dan gigi (Pal et al. 2005; Deptula et al. 2006; Sasikumar dan Vijayaraghavan 2006). Hidroksiapatit membentuk ikatan langsung dengan jaringan tulang tanpa melalui proses enkapsulasi fibrin (Song et al. 2003). Balamurugan et al. (2002) mengemukakan bahwa hidroksiapatit selain memiliki kemampuan melindungi logam pen
dari korosi ketika diimplankan di dalam tubuh juga meningkatkan laju pertumbuhan jaringan tulang.
Sintesis senyawa kalsium fosfat seperti hidroksiapatit dapat dibagi menjadi dua metode yaitu metode kering dan metode basah. Metode basah terdiri atas tiga jenis diantaranya metode presipitasi, teknik hidrotermal, dan hidrolisis (Pankaew et al.
2010). Metode presipitasi merupakan metode yang sering digunakan dalam sintesis
0 100 200 300 400 500 600 700 800 900 1000
5 15 25 35 45 55 65 75
4
hidroksiapatit karena mudah mengontrol komposisi dan karakteristik fisik dari hidroksiapatit, murah, dan mudah penggunaanya (Pankaew et al. 2010). Metode presipitasi memiliki kelemahan diantaranya sulit mengatur nilai pH di atas 9 untuk mencegah pembentukan kalsium hidroksiapatit yang tidak sempurna. Kristal kalsium hidroksiapatit yang tidak sempurna mudah mengalami dekomposisi membentuk trikalsium fosfat saat proses sintering (Balamurugan et al. 2006). Metode kering memiliki kelebihan yang tak kalah dengan metode basah. Sintesis hidroksiapatit menggunakan metode kering merupakan metode yang lebih sederhana untuk mendapatkan hidroksiapatit dengan hasil kristal yang lebih banyak (Pramanik et al.
2005).
Prinsip metode kering ialah menggunakan sifat dasar atom yang dapat bergerak bervibrasi semakin cepat ketika temperatur ditingkatkan. Sintesis hidroksiapatit menggunakan metode kering dari serbuk garam anorganik atau oksida membutuhkan pencampuran mekanik yang ekstensif dan perlakuan pada temperatur tinggi (Beganskienė et al. 2006). Temperatur yang tinggi pada metode kering dapat meningkatkan aktivitas ion sehingga akan menaikkan proses kristalisasi senyawa hidroksiapatit. Struktur kristalitas hidroksiapatit yang dihasilkan sangat berpengaruh terhadap sifat bioaktif yang dimiliki oleh hidroksiapatit (Pramanik et al.
2005). Selain itu penggunaan temperatur tinggi dapat menghilangkan zat pengganggu dalam proses kristalisasi hidroksiapatit seperti karbonat yang banyak terkandung dalam cangkang telur (Dahlan et al. 2009).
Dahlan et al. (2009) melakukan sintesis hidroksiapatit menggunakan cangkang telur sebagai sumber kalsium dan pereaksi (NH4)2HPO4 sebagai sumber fosfor. Sintesis dilakukan melalui proses sintering campuran kedua bahan tersebut pada variasi suhu 900oC (selama 2 dan 4 jam) dan 1000oC (selama 2, 4 dan 6 jam). Dahlan et al. (2009) menjelaskan bahwa semakin tinggi suhu selama sintering akan menghasilkan hidroksiapatit dengan derajat kristalinitas yang juga semakin tinggi. Demikian pula dengan waktu pemanasan yang juga berbanding lurus dengan derajat kristalinitas sampel. Berdasarkan pola hasil XRD (Gambar 2) memperlihatkan adanya fase lain yang muncul selain hidroksiapatit, yaitu apatit karbonat tipe A, apatit karbonat tipe B, dan okta kalsium fosfat. Metode ini dinilai
masih belum menghasilkan hidroksiapatit yang murni.
Gambar 2 Pola difraksi sinar-X hidroksiapatit hasil Dahlan et al. (2009) pada sintering 1000 oC selama 4 jam.
Pramanik et al. (2005) melakukan sintesis hidroksiapatit melalui sintering campuran antara CaO dengan P2O5 pada suhu 1250
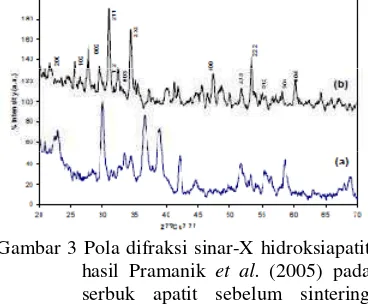
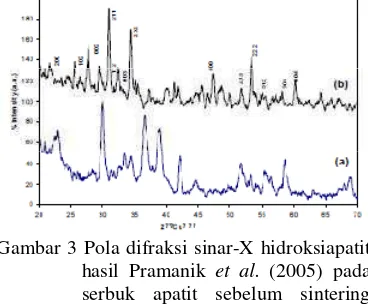
o C selama 1.5 jam dengan perbandingan CaO 50.52% dan P2O5 46.43%. Ditambahkan pula sejumlah pengisi dan aditif pada campuran yang kemudian dimiling menggunakan milling ball selama 16 jam. Sebelum disintering campuran terlebih dahulu dibentuk menjadi pelet pada tekanan 60 MPa. Pelet yang telah disintering kemudian dihancurkan dan disintering kembali pada suhu dan waktu yang sama. Metode ini tergolong tidak ringkas dan memakan waktu lama sehingga tidak bisa dilakukan untuk dunia industri dalam skala besar.
Gambar 3 Pola difraksi sinar-X hidroksiapatit hasil Pramanik et al. (2005) pada serbuk apatit sebelum sintering kedua (a) dan setelah sintering kedua (b).
Sintesis hidroksiapatit metode kering pada penelitian ini merupakan modifikasi metode Dahlan et al. (2009) dan Pramanik et al.
P2O5 seperti metode Pramanik et al. (2005). Proses sintering pada penelitian ini sama seperti Pramanik et al. (2005) yang menggunakan perbandingan campuran CaO 50.52% dan P2O5 46.43%, dimiling dan disintering pada suhu 1250 oC. Metode ini dinilai lebih sederhana karena proses miling hanya dilakukan selama 6 jam dan tidak disintering dalam bentuk pelet melainkan dalam bentuk serbuk serta tidak ada penambahan bahan aditif atau pengisi walaupun proses sintering dilakukan sedikit lebih lama yaitu selama 2 jam. Hidroksiapatit yang dihasilkan oleh metode ini pun lebih murni dibanding metode Dahlan et al. (2009) dan Pramanik et al. (2005), dibuktikan dari hasil pola difraksi sinar-X Gambar 2, 3, dan 4. Berdasarkan perbandingan terhadap metode Dahlan et al. (2009) dan Pramanik et al.
(2005), dapat dipastikan bahwa proses sintesis metode kering pada penelitian ini memiliki potensi yang baik untuk digunakan di masa mendatang dalam dunia industri.
Gambar 4 Pola difraksi sinar-X hidroksiapatit sintesis (-) dan komersil (-). Hidroksiapatit, CaO, dan AKA.
(a)
(b)
Gambar 5 Hasil SEM hidroksiapatit sintesis (a) dan komersil (b) perbesaran 5 µ m.
Sintesis hidroksiapatit metode kering menggunakan pereaksi P2O5 harus dengan perhatian ekstra. Senyawa P2O5 merupakan senyawa korosif dan sangat reaktif terhadap air menghasilkan panas dan asam fosfat. Setelah P2O5 dan CaO dari cangkang telur dicampur dan dimiling selama 6 jam, campuran harus terlebih dahulu didiamkan selama 24 jam dalam wadah tertutup untuk menstabilkan campuran setelah proses miling dan menghindari adanya ledakan ketika kontak dengan udara. Hidroksiapatit hasil sintesis dibandingkan komersil memiliki kualitas yang lebih baik karena tidak menunjukkan adanya puncak fase AKA seperti pada hidroksiapatit komersil (Gambar 4) dan ukuran molekul hidroksiapatit sintesis lebih kecil dan halus dibandingkan hidroksiapatit komersil (Gambar 5). Puncak fase AKA berada pada sudut 2θ 31.580°. Hidroksiapatit hasil sintesis juga masih belum murni karena masih menunjukkan adanya puncak fase dari CaO di sudut 2θ 37.485° (Lampiran 3). Fase CaO yang terdapat di dalam hidroksiapatit hasil sintesis dapat diminimalisasi melalui penelitian lebih lanjut dengan menambahkan P2O5 lebih banyak pada proses sintesis untuk memperoleh hidroksiapatit yang lebih murni.
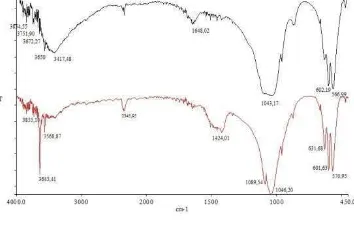
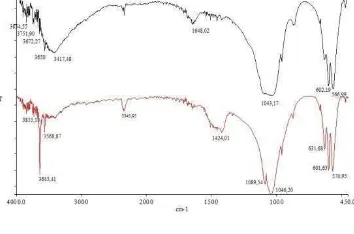
Gambar 6 Spektrogram inframerah hidroksiapatit komersil (-) dan sintesis (-).
Spektrogram inframerah hidroksiapatit memiliki pita pada 1000-1100 cm-1 dan 500-600 cm-1 yang merupakan gugus PO4 yang dimiliki hidroksiapatit, dan pita superposisi gugus OH hidroksiapatit pada 1550-1700 cm-1 (Denilchenko et al. 2009). Gambar 6 menunjukkan bahwa hidroksiapatit komersil dan sintesis memiliki semua pita tersebut, namun terdapat pita tambahan pada 0 50 100 150 200 250 300 350 400
10 20 30 40 50 60 70 80
6
hidroksiapatit sintesis yaitu pada 3670-3570 cm-1 yang merupakan pita ion OH -hidroksiapatit yang mengalami vibrasi peregangan dan pita gugus ion karbonat pada 1420-1485 cm-1 sedangkan hidroksiapatit komersil memiliki pita tambahan pada 3500-3100 cm-1 yang merupakan pita gugus OH terhidrasi (Denilchenko et al. 2009; Pramanik
et al. 2005). Hidroksiapatit komersil pun
memiliki pita ion OH- yang mengalami vibrasi peregangan, tetapi intensitasnya tidak setinggi pita ion OH- pada hidroksiapatit sintesis (Gambar 6). Hal ini diakibatkan oleh adanya air pada hidroksiapatit komersil sehingga pita ion OH- vibrasi peregangan bergeser menjadi pita gugus OH yang terhidrasi. Keberadaan pita karbonat pada hidroksiapatit sintesis disebabkan oleh masih adanya kandungan CaO dalam hidroksiapatit ini yang dapat mengikat CO2 dari udara membentuk CaCO3.
Pelapisan Hidroksiapatit-Kitosan
Hidroksiapatit adalah komponen anorganik utama yang terdapat pada tulang dan merupakan salah satu kandidat terbaik untuk memperbaiki tulang dan meregenerasinya karena sifat bioaktif dan osteokonduktivitasnya. Kelemahan terbesar hidroksiapatit ialah mudah rapuh saat berkontak dengan darah atau cairan tubuh sehingga sulit digunakan untuk meregenerisasi tulang. Cara untuk mengatasi permasalahan ini melalui pengkombinasian hidroksiapatit dengan matriks polimer seperti kitosan untuk lebih meningkatkan osteokonduktivitas, biodegradabilitas dan kekuatan mekaniknya (Zainol et al. 2008). Penambahan kitosan selain untuk menahan hidroksiapatit tetap pada posisinya juga untuk meningkatkan laju pelapisan dari proses pelapisan hidroksiapatit pada logam SS 316 (Pang dan Zhitomirsky 2007). Pang dan Zhitomirsky (2007) pun menyatakan bahwa kitosan memiliki aktivitas antimikroba, biokompatibel, dan dapat meningkatkan ketahanan korosi.
Pembuatan komposit hidroksiapatit-kitosan dapat dilakukan dengan berbagai metode diantaranya dengan pencampuran secara mekanik atau presipitasi in situ untuk menghasilkan komposit hidroksiapatit-kitosan yang berukuran nano (Zainol et al. 2008). Proses pembuatan komposit hidroksiapatit-kitosan dengan metode presipitasi menggunakan prinsip koopresipitasi dengan meneteskan larutan kitosan yang mengandung asam fosfat ke dalam suspensi kalsium
hidroksida (Danilchenko et al. 2009). Komposit hidroksiapatit-kitosan pada penelitian ini dibuat melalui pencampuran secara mekanik dengan mencampurkan kitosan dan suspensi hidroksiapatit yang kemudian diaduk secara mekanik membentuk komposit campuran.
Logam SS 316 sebelum dilapisi dengan komposit hidroksiapatit-kitosan harus terlebih dahulu mengalami perlakuan awal untuk memperkuat penempelan komposit pada permukaan logam. Permukaan logam harus dibuat kasar melalui pengamplasan dan perendaman dalam larutan H2SO4:HCl:air (1:1:1) selama 1 jam pada suhu 60 °C. Perendaman dalam larutan larutan H2SO4:HCl:air (1:1:1) selain untuk meningkatkan kekasaran permukaan logam juga untuk menghilangkan lapisan oksida alami yang dimiliki logam seperti lapisan krom oksida. Perendaman logam pada larutan NaOH 10 M selama 24 jam dimaksudkan untuk meningkatkan kehidrofilikan dari logam (Lu Xiong et al. 2006). Tingkat kehidrofilikan permukaan logam merupakan salah satu parameter penting yang mempengaruhi respon sel dan jaringan biologis terhadap logam implantasi. Permukaan material implantasi yang hidrofilik akan lebih merangsang pertumbuhan tulang pada tahap regenerasi tulang (Hsu Chuan et al. 2011).
Gambar 7 Sel elektroforesis deposisi (Boccaccini et al. 2010).
Metode EPD termasuk metode tua namun efektif dalam proses deposisi elektroda bermuatan oleh partikel yang berasal dari suspensi koloid stabil di bawah pengaruh penggunaan arus langsung karena mampu membentuk lapisan deposit dengan homogenitas mikrostruktur tinggi, mampu mengendalikan ketebalan lapisan, dan mampu membentuk lapisan film yang tipis atau tebal pada substrat yang memiliki berbagai bentuk kompleks tiga dimensi (Boccaccini et al.
2010). Metode ini dibagi menjadi dua tahap proses yaitu tahap migrasi partikel bermuatan yang berada di dalam cairan pelarut oleh adanya aksi dari penggunaan medan listrik (tahap elektroforesis) dan tahap koagulasi partikel membentuk lapisan pada elektroda (tahap deposisi) (Meng et al. 2008).
Pelapisan dengan ketebalan kurang dari 1µm hingga lebih dari 500 µm dapat dibentuk menggunakan metode EPD melalui pengkombinasian lamanya waktu dan besar tegangan listrik. Selain waktu dan besar tegangan listrik yang digunakan, terdapat parameter lain yang berpengaruh dalam metode EPD yaitu ukuran partikel, distribusi dan bentuk serta konstanta dielektrik yang dimiliki media suspensi (Javidi et al. 2008). Tegangan listrik yang digunakan pada metode EPD sangat berpengaruh terhadap laju dan struktur lapisan yang terbentuk, oleh karena itu tegangan listrik harus selalu dijaga konstan ketika proses pelapisan berlangsung.
Kitosan sebelum dicampur dengan hidroksiapatit terlebih dahulu dilarutkan dalam asam asetat encer. Pelarutan ini dimaksudkan untuk memprotonisasi kitosan agar dalam proses EPD kitosan dapat bergerak menuju logam SS 316 yang akan dilapiskan akibat adanya efek beda potensial, begitu juga dengan hidroksiapatit yang bermuatan positif akan ikut menempel. Kitosan dapat meningkatkan laju pelapisan hidroksiapatit,
disebabkan kitosan terabsorbsi ke dalam partikel hidroksiapatit sehingga akan meningkatkan stabilitas dari partikel hidroksiapatit dan meningkatkan muatan partikel yang mempercepat proses pelapisan (Pang dan Zhitomirsky 2007).
Pelapisan komposit hidroksiapatit-kitosan pada penelitian ini menggunakan tegangan sebesar 120 v selama 2 menit. Penggunaan tegangan ini didasari dari penelitian sebelumnya Bowo (2009) yang menyatakan bahwa tegangan 120 v selama 2 menit merupakan tegangan terbaik menghasilkan lapisan yang merata. Penggunaan tegangan lebih rendah dari 20 volt akan menghasilkan deposit dengan ukuran partikel hidroksiapatit yang rendah sedangkan penggunaan tegangan lebih dari 200 volt selama lebih dari 10 detik akan menghasilkan deposit dengan ukuran partikel hidroksiapatit yang lebih besar. Peningkatan muatan listrik yang digunakan dapat menaikkan laju deposisi, tetapi partikel deposisi memiliki waktu yang lebih sedikit untuk menyusun kembali sehingga lapisan yang terbentuk akan lebih berpori yang menyebabkan kekerasan lapisan hidroksiapatit menjadi berkurang (Meng et al. 2008).
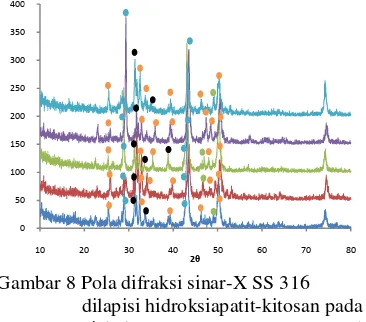
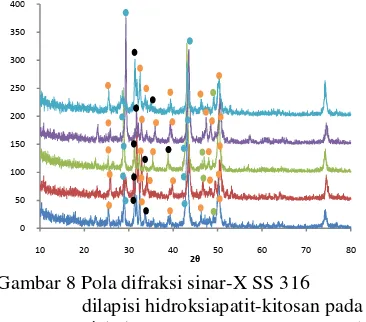
Gambar 8 Pola difraksi sinar-X SS 316 dilapisi hidroksiapatit-kitosan pada nisbah 0.2:0 (-), 0.2:0.1 (-), 0.2:0.5 (-), 0.2:1.0 (-), 0.2:1.5 (-). Hidroksiapatit, CaCO3, AKB, dan AKA.
Lapisan yang menempel pada permukaan logam SS 316 ternyata tidak murni hidroksiapatit-kitosan. Gambar 8 menjelaskan bahwa selain hidroksiapatit terdapat pula fase lain yang menempel pada permukaan logam, yaitu CaCO3, AKA, dan AKB. Sudut 2θ dari puncak fase CaCO3, AKA, dan AKB disajikan pada Lampiran 3. Adanya fase CaCO3, AKA, dan AKB disebabkan tanpa adanya pemanasan pada suhu 900 °C setelah proses pelapisan menggunakan EPD. Septiarini
0 50 100 150 200 250 300 350 400
10 20 30 40 50 60 70 80
8
(2009) menyatakan bahwa pemanasan di atas suhu 900 °C tidak dapat dilakukan karena logam baja tahan karat lokal tidak tahan pada suhu di atas 650 °C, selain itu pemanasan pada suhu tersebut pun dapat merusak kitosan yang menempel pada permukaan logam. Munculnya fase CaCO3 disebabkan adanya reaksi antara karbonat yang berasal dari udara terhadap CaO yang terkandung pada hidroksiapatit hasil sintesis. Fase CaCO3 dapat dihilangkan dengan menyempurnakan tahap sintesis hidroksiapatit agar lebih menghasilkan hidroksiapatit yang lebih murni tanpa kandungan CaO.
Pola difraksi sinar-X komposit hidroksiapatit-kitosan yang melapisi logam SS 316 (Gambar 8) tidak menunjukkan adanya fase kitosan. Keberadaan kitosan dapat ditunjukkan pada adanya puncak di sudut 2θ
10° dan 20° dari pola difraksi sinar-X (Lampiran 5). Tidak adanya puncak fase kitosan pada Gambar 8 bukan berarti kitosan tidak menempel pada logam SS 316. Yildirim (2004) menyatakan bahwa fase kitosan akan muncul pada pola difraksi sinar-X komposit hidroksiapatit-kitosan apabila kandungan kitosan pada komposit melebihi dari 30% (Gambar 9).
Gambar 9 Pola difraksi sinar-X komposit hidroksiapatit-kitosan Yildirim (2004) dengan komposisi hidroksiapatit 0% (a), 30% (b), 70% (c), dan 100% (d).
Ketahanan Korosi
Peristiwa korosi merupakan proses degradasi material yang berlangsung sedikit demi sedikit akibat adanya serangan elektrokimia yang terjadi ketika suatu logam ditempatkan di dalam lingkungan elektrolitik berlawanan, khususnya lingkungan dalam tubuh manusia (Adya et al. 2005). Ketahanan korosi yang dimiliki baja SS disebabkan
terbentuknya suatu lapisan tipis oksida krom yang menghalangi proses oksidasi besi. Lapisan ini mampu mengurangi kecepatan proses karat selambat mungkin karena lapisan tersebut terbentuk dengan sangat rapat. Seiring dengan berjalannya waktu, lapisan oksida krom yang terdapat pada permukaan SS tidak akan bertahan terhadap kondisi lingkungan fisiologi tubuh sehingga memungkinan ion krom terlepas ke dalam tubuh manusia. Lepasnya ion tersebut ke dalam tubuh dapat menimbulkan alergi karena bersifat karsinogenik (Prabakaran et al. 2006). Baja SS 316 L memiliki ketahanan korosi yang lebih kuat dibandingkan baja 316 (Yildirim 2004), hal ini disebabkan baja 316 L memiliki kandungan karbon paling rendah (Tabel 1). Ketahanan logam akan semakin meningkat apabila kandungan karbon dibuat serendah mungkin, tetapi kandungan karbon harus tetap dipertahankan agar logam paduan baja bersifat gelas atau keras.
Tabel 1 Komposisi SS 316 dan 316 L
% 316 316 L
C Maks 0.08 Maks 0.03
Mn 2 2
Si 0.75 0.75
P 0.045 0.045
S 0.03 0.03
Cr 16-18 16-18
Mo 2-3 2-3
Ni 10-14 10-14
N 0.1 0.1
Sumber: Aalco Metals (2007)
dibandingkan laju korosi yang dimiliki logam SS 316 L. Data rincian analisis korosi ditunjukkan pada Lampiran 6.
Gambar 10 Hasil uji korosi SS 316 ( ), SS 316 L ( ), dan SS 316 dilapisi hidroksiapatit-kitosan pada nisbah 0.2:0 ( ), 0.2:0.1 ( ), 0.2:0.5 ( ), 0.2:1.0 ( ), dan 0.2:1.5 ( ). Penambahan sebanyak 0,1 dan 0,5 mL kitosan 3% memiliki nilai laju korosi yang lebih tinggi dibandingkan pelapisan SS 316 dengan hidroksiapatit tanpa penambahan kitosan. Hal ini disebabkan pada lapisan hidroksiapatit tanpa kitosan memiliki ketebalan yang lebih tebal dibandingkan lapisan komposit hidroksiapatit-kitosan. Ketebalan lapisan penghalang yang melapisi logam merupakan salah satu faktor penting dalam ketahanan korosi. Lapisan yang semakin tebal akan semakin memberikan perlindungan logam terhadap korosi. Lapisan pada logam SS 316 tanpa penambahan kitosan memang memiliki ketebalan yang lebih tebal, tetapi lapisan yang hanya terdiri dari hidroksiapatit akan memiliki ketahanan mekanik yang rendah. Lapisan ini akan lebih mudah rapuh dibandingkan lapisan dengan adanya penambahan kitosan (Maachaou et al.
2008).
Berbeda terhadap lapisan dengan penambahan kitosan 3% sebanyak 1 dan 1.5 mL, lapisan ini memiliki nilai laju korosi yang lebih rendah daripada lapisan hanya hidroksiapatit dan dinilai memiliki ketahanan korosi terbaik. Ketahanan korosi yang dimiliki lapisan ini lebih baik karena penyebaran komposit yang lebih merata pada lapisan (Lampiran 7). Penyebaran lapisan yang lebih merata ini disebabkan oleh jumlah kitosan yang ditambahkan lebih banyak sehingga hasil deposisi yang terbentuk akan lebih baik (Pang dan Zhitomirsky 2007). Volume kitosan yang digunakan tidak melebihi 1.5 mL karena berdasarkan percobaan penambahan kitosan 3% di atas 1.5 mL tidak bisa melakukan
proses pelapisan di tegangan 120 V. Kitosan memiliki konduktivitas yang rendah sehingga apabila jumlah kitosan terlalu banyak akan menurunkan tegangan dan menghambat proses pelapisan. Jumlah kitosan yang terlalu banyak dapat meningkatkan viskositas larutan, menurunkan mobilitas elektroforetik, dan menurunkan hasil deposit komposit hidroksiapatit-kitosan pada permukaan logam (Pang dan Zhitomirsky 2007). Penambahan kitosan pada pelapisan logam SS 316 dengan hidroksiapatit selain dapat meningkatkan ketahanan mekanik lapisan hidroksiapatit yang menempel pada logam, dapat pula meningkatkan ketahanan korosi dari logam SS 316 bahkan memiliki ketahanan korosi yang lebih baik dibandingkan logam SS 316 L (Gambar 10). Hal ini sesuai dengan pernyataan Pang dan Zhitomirsky (2007) yang menjelaskan bahwa kitosan dapat meningkatkan ketahanan korosi dari suatu material.
SIMPULAN DAN SARAN
Simpulan
Metode sintesis hidroksiapatit yang digunakan pada penelitian ini merupakan metode kering baru yang lebih sederhana, mudah, singkat dan lebih menghasilkan kristal hidroksiapatit yang lebih murni sehingga dapat diproduksi dalam jumlah besar di industri. Pelapisan hidroksiapatit dengan penambahan kitosan selain untuk meningkatkan ketahanan mekanik dari hidroksiapatit tetapi juga untuk meningkatkan ketahanan korosi yang dimiliki logam tersebut.
Saran
Penelitian lebih lanjut dibutuhkan untuk menyempurnakan sintesis hidroksiapatit menggunakan metode ini agar diperoleh hidroksiapatit yang lebih murni serta menggunakan tegangan dan waktu yang lebih bervariasi saat proses pelapisan menggunakan EPD.
DAFTAR PUSTAKA
Aalco Metals. 2010. Stainless steel grade 316 [terhubung berkala] http://www.aalco
10
.co.uk/technical/datasheets/Aalco_Datashe et_St_St_316.pdf [30 September 2010]. Adya N, Alam M, Ravindranath T, Mubeen
A, Saluja B. 2005. Corrosion in titanium dental implants: literature review. Journal
of Indian Prosthodontic Society 5(3):
126-131.
Bahrololoom ME, Javidi M, Javadpour S, Ma J. 2009. Characterisation of natural hydroxyapatite extracted from bovin cortical bone ash. Journal of Ceramic
Processing Research 10(2): 129-138.
Balamurugan A et al. 2006. Synthesis and structural analysis of sol gel derived stoichiometric monophasic hydroxy-apatite. Ceramics Silikary 50(1): 27-31. Balamurugan A, Kannan S, Rajeswari S.
2002. Bioactive sol-gel hydroxy-apatite surface for biomedical applications-in vitro study. Trends Biomater Artif Organs
16(1): 18-20.
Beganskienė A, Bogdanovičienė I, Kareiva A. 2006. Calcium acetylacetonate – a novel calcium precursor for sol-gel preparation of Ca10(PO4)6(OH)2. Chemija 17(2–3): 16– 20.
Boccaccini RA, Keim S, Ma R, Li Y, Zhitomirsky I. 2010. Electrophoretic deposition of biomaterials. J R Soc Interface 7: S581–S613
Bowo H. 2009. Pelapisan senyawa apatit pada permukaan baja tahan karat 316 L dengan metode deposisi elektroforesis [skripsi]. Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Dahlan K, Prasetyanti F, Sari YW. 2009. Sintesis hidroksiapatit dari cangkang telur menggunakan dry method. Jurnal
Biofisika 5(2): 71-78.
Danilchenko SN et al. 2009. Chitosan-hydroxyapatite composite biomaterials made by a one step co-precipitation method: preparation, characterization and in vivo tests. Journal of Biology Physics
and Chemistry 9(3): 119-126.
Dasgupta P, Singh A, Adak S, Purohit KM. 2004. Synthesis and characterization of hydroxyapatite produced from eggshell.
International Symposium of Research Students on Materials Science and
Engineering; Chennai, 20-22 Desember
2004. India: Department of Metallurgical and Materials Engineering, Indian Institute of Technology Madras. Hlm 1-6.
Deptula A et al. 2006. Sol-gel-derived hydroxyapatite and its application to
sorption of heavy metals. Science and
Technology 45: 2198-2203.
Hsu Chuan et al. 2011. Effect of water aging on the apatite formation of a low-modulus Ti–7.5Mo alloy treated with aqueous NaOH. J Mater Sci 46:1369–1379
Javidi M, Javadpour S, Bahrololoom ME, Ma J. 2008. Electrophoretic deposition of natural hydroxyapatite on medical grade 316 L stainless steel. Mater Sci Eng C. articles in press.
Karokaro M, Purniawan A, Fellicia DM. 2008. Karakterisasi lapisan pasif korosi implant commercial pure titanium grade 2 dengan variasi kekasaran permukaan pada cairan tubuh buatan. Jurnal Ilmiah Sains
dan Teknologi 7(2): 97-105.
Lu Xiong et al. 2007. Preparation of HA/chitosan composite coatings on alkali treated titanium surfaces through sol–gel techniques. Materials Letters 61: 3970– 3973.
Maachou H et al. 2008. Characterization and in vitro bioactivity of chitosan/ hydroxyapatite composite membrane prepared by freeze-gelation method.
Trends Biomater Artif Organs 22(1):
16-27.
Manivasagam G, Dhinasekaran D, Rajaminickam A. 2010. Biomedical implants: corrosion and its prevention – a review. Recent Patents on Corrosion
Science 2: 40-54.
Meng X, Kwon T, Kim K. 2008. Hydroxyapatite coating by electrophoretic deposition at dynamic voltage. Dental
Materials Journal 27(5): 666-671.
Murakami FS, Rodrigues PO. 2007. Physicochemical study of CaCO3 from egg shells. Ciênc Tecnol Aliment
Campinas 27(3): 658-662.
Oktavia D. 2009. Menyambung tulang dengan logam, amankah? [terhubung berkala] http://beta.padang-today.com/?mod= artikel&today=detil&id=286 [1 Desember 2010].
Pal S, Roy S, Bag S. 2005. Hydroxyapatite Coating over Alumina-Ultra High Molecular Weight Polyethylene Composite Biomaterials. Trends Biomater
Artif Organs 18(2): 106-109.
Pang X, Zhitormisky I. 2005. Electrodeposition of composite hydroxyapatite–chitosan films. Materials
Chemistry and Physics 94: 245–251.
hydroxyapatite-chitosan coatings. Materials
Characterization 58: 339-348.
Pankaew P, Hoonnivathana E, Limsuwan P, Naemchanthara K. 2010. Temperature effect on calcium phosphate synthesized from chicken eggshells and ammonium phosphate. Journal of Applied Sciences
10(24): 3337-3342.
Prabakaran K, Thamaraiselvi TV, Rajeswari S. 2005. Electrochemical evaluation of hydroxyapatite reinforced phosphoric acid treated 316 L stainless steel. Trends
Biomater Artif Organs 19(2): 84-87.
Pramanik S, Agarwal AK, Rai KN. 2005. Development of high strength hydroxyapatite for hard tissue replacement. Trends Biomater Artif
Organs 19(1): 46-51.
Radice S, Kern P, Michler J. Textor M. 2005. Bioactive coatings for implants by electrophoretic deposition. European Cells
and Materials 10(5): STE8.
Sasikumar S, Vijayaraghavan R. 2006. Low temperature synthesis of nanocrystalline hydroxyapatite from egg shells by combustion method. Trends Biomater Artif
Organs 19(2): 70-73.
Septiarini S. 2009. Pelapisan apatit pada baja tahan karat local dan ternitridasi dengan metode sol-gel [skripsi]. Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Song C et al. 2003. Sol-gel preparation and preliminary in vitro evaluation of fluorapatite/hydroxyapatite solid solution films. J Mater Sci Technol 19(5): 495-498. Suharno B, Kurniawan A. 2005. Studi perbandingan ketahanan korosi dan struktur mikro baja COR CF8M (SS 316) yang dibuat dengan feronikel lokal dan nikel impor. Jurnal Teknologi 1: 26-37. Yildirim E. 2004. Preparation and
characterization of chitosan /calcium phosphate based composite biomaterials [disertasi]. Department of Materials Science and Engineering, Izmir Institute of Technology, Turkey.
Zainol I, Zakaria FA, Saliman MR, Derman MA. 2008. Preparation and characterization of chitosan/ nanohydroxyapatite composites. Solid
State Science and Technology
Lampiran 1 Bagan alir penelititan
Preparasi
Cangkang Telur
Sintesis
Hidrosiapatit
Penentuan Kadar
Ca (SSA)
Analisis Fase
XRD
Pelapisan Komposit
Hidroksiapatit-Kitosan
Perlakuan Logam
Uji Analisis Fase XRD
Uji Mikrostruktur
Uji Korosi
Analisis Fase XRD
14
Lampiran 2 Data JCPDS
a.
Data JCPDS Hidroksiapatit
Lanjutan Lampiran 2
c.
JCPDS AKB
16
Lanjutan Lampiran 2
e.
JCPDS CaCO
3Lanjutan Lampiran 2
18
Lampiran 3 Tabel data analisis hasil XRD
Data analisis hasil XRD serbuk cangkang telur sebelum pemanasan
2
θ
Intensitas
Fase
18.500
197
CaCO
328.750
84
Ca
3(PO
4)
234.150
256
Ca
3(PO
4)
247.250
105
CaCO
350.850
106
MgCO
354.449
68
CaCO3
Data analisis hasil XRD serbuk cangkang telur sesudah pemanasan
2
θ
Intensitas Fase
32.150
350
CaO
37.300
876
CaO
53.799
519
CaO
64.099
127
CaO
67.300
107
CaO
Lanjutan Lampiran 3
Data analisis hasil XRD Hap komersil
2
θ
Intensitas
fase
25.780
185
Hap
31.580
259
AKA
31.700
231
Hap
32.120
204
Hap
32.900
98
Hap
33.940
98
Hap
39.640
62
Hap
46.480
79
Hap
49.320
102
Hap
53.080
61
Hap
63.880
44
Hap
Data analisis hasil XRD Hidroksiapatit-kitosan (0,2:0)
2
θ
Intensitas
Fase
25.448
30
Hap
28.984
75
CaCO
331.378
78
AKA
31.737
44
Hap
32.479
50
AKA
33.676
25
AKA
39.109
15
Hap
43.151
207
CaCO
346.287
16
Hap
49.039
18
AKB
50.248
79
Hap
Data analisis hasil XRD Hidroksiapatit-kitosan (0,2:0,1)
2
θ
Intensitas
Fase
25.870
45
Hap
28.991
26
CaCO
331.047
28
AKA
31.814
106
Hap
32.143
50
Hap
32.905
65
Hap
34.095
29
Hap
39.781
20
Hap
43.556
91
CaCO
320
Lanjutan Lampiran 3
Data analisis hasil XRD Hidroksiapatit-kitosan (0,2:0,5)
2
θ
Intensitas
Fase
25.346
16
Hap
28.884
132
CaCO
331.263
40
AKA
31.654
19
Hap
32.396
25
AKA
35.424
18
Hap
38.850
25
AKA
43.101
218
CaCO
347.020
17
AKB
48.946
8
Hap
50.335
96
Hap
Data analisis hasil XRD Hidroksiapatit-kitosan (0,2:1,0)
2
θ
Intensitas
Fase
25.854
20
Hap
29.361
215
CaCO
331.460
13
AKA
31.755
54
Hap
32.137
28
Hap
32.880
38
Hap
34.041
14
Hap
39.405
33
Hap
43.521
158
CaCO
347.429
35
AKB
48.460
22
Hap
50.542
71
Hap
Data analisis hasil XRD Hidroksiapatit-kitosan (0,2:1,5)
2
θ
Intensitas
Fase
25.504
34
Hap
28.944
16
CaCO
331.446
80
AKA
31.800
40
Hap
32.543
52
AKA
33.752
20
AKA
39.448
21
Hap
43.201
80
CaCO
3Lampiran 4 Perhitungan kadar kalsium
Kurva deret standar kalsium
Bobot contoh (g)
: 0.1079 gram
Volume contoh (v)
: 50 mL
Faktor pengenceran (fp)
: 100
Absorbansi contoh (y)
: 0.3162
Konsentrasi contoh (x)
: y = 0.033850 x + 0.020477
x =
y – 0.0204770.033850
x =
. . .x = 8.7362 ppm
Kadar kalsium
: % Kalsium =
x . v . fpg
% Kalsium =
8.7362 ppm . g⁄ mg. 50 mL . 1 L⁄ mL. 1000.1075 gram
. 100%
% Kalsium = 40.48 %
Kadar CaO
: % CaO = %Kalsium .
Mr. CaOAr. Ca
% CaO = 40.48 % .
56.08 gram/mol
40.08 gram/mol
% CaO = 56.64 %
y = 0.033850x + 0.020477 R = 0.9998
0,0 0,1 0,2 0,3 0,4 0,5 0,6
0 5 10 15 20
A
b
so
rb
a
n
si
22
Lampiran 5 Pola difraksi sinar-X kitosan
0 50 100 150 200 250 300 350
5 15 25 35 45 55 65
In
t
e
n
s
it
as
Lampiran 6 Data uji kor
1.
Data uji korosi 316
24
Lanjutan Lampiran 6
Lanjutan Lampiran 6
26
Lanjutan Lampiran 6
Lanjutan Lampiran 6
28
Lanjutan Lampiran 6
Lanjutan Lampiran 6
30
Lampiran 7 Mikrostruktur lapisan hidroksiapatit-kitosan pada 316 (perbesaran 4×)
316 dilapisi Hap-kitosan (0.2:1.5)
316 dilapisi Hap-kitosan (0.2:1.0)
316 dilapisi Hap-kitosan (0.2:0.5) 316 dilapisi Hap-kitosan (0.2:0.1)
ABSTRAK
ADI IRIANTO MARIST. Pelapisan Komposit Hidroksiapatit-Kitosan pada
Logam Stainless
Steel
316 untuk Meningkatkan Ketahanan Korosi
.
Dibimbing
oleh SRI MULIJANI dan SULISTIOSO GIAT SUKARYO.
Logam yang digunakan untuk proses implantasi harus memiliki ketahanan
korosi yang baik agar tidak mudah terkorosi ketika diimplan ke dalam tubuh.
Ketahanan korosi logam stainless
steel
316 dapat ditingkatkan melalui pelapisan
logam oleh komposit hidroksiapatit-kitosan dengan nisbah komposisi
hidroksiapatit (gram) dan kitosan 3% (mL) 0.2:0, 0.2:0.1, 0.2:0.5, 0.2:1.0, dan
0.2:1.5. Keberadaan kitosan selain untuk meningkatkan ketahanan korosi dari
logam tetapi juga untuk mempertahankan posisi hidroksiapatit tetap pada
permukaan logam. Ketahanan korosi meningkat seiring dengan meningkatnya
jumlah kitosan yang ditambahkan dengan komposisi hidroksiapatit-kitosan
optimum 0.2:1.0.
ABSTRACT
ADI IRIANTO MARIST. Hydroxyapatite-Chitosan Composite Coating on
Stainless Steel 316 to Improve Corrosion Resistance. Under direction of SRI
MULIJANI and SULISTIOSO GIAT SUKARYO.
Metals that were used in bone implantation should have good corrosion
resistance that were not easily corroded when implanted into the body. Metal
corrosion resistance of stainless steel 316 can be enhanced through the metal
coating by hydroxyapatite-chitosan composite with composition ratio of
hydroxyapatite (gram) and chitosan 3% (mL) 0.2:0, 0.2:0.1, 0.2:0.5, 0.2:1.0, and
0.2:1.5. Besides improving the corrosion resistance of metal, the presence of
chitosan also maintain the position of hydroxyapatite on metal surfaces. Corrosion
resistance increases with increasing amount of chitosan added and the best
composition of hydroxyapatite-chitosan composite was 0.2:1.0.
PENDAHULUAN
Berbagai macam jenis kecelakaan terjadi tiap tahunnya, baik itu ringan ataupun berat yang memungkinkan terjadinya kerusakan pada tulang. Kerusakan tulang dapat diatasi melalui pemasangan pen (implantasi) pada bagian tulang yang patah untuk mengembalikan posisi patahan tulang ke posisi semula (reposisi) dan mempertahankan posisi itu selama masa penyembuhan patah tulang (imobilisasi) (Oktavia 2009).
Logam yang digunakan dalam proses
implant harus memiliki sifat biokompatibilitas
yang tinggi agar keberadaannya di dalam tubuh tidak dianggap sebagai benda asing. Penggunaan logam yang memiliki biokompatibilitas rendah dapat menyebabkan korosi pada logam oleh cairan tubuh. Korosi logam pen dapat menimbulkan reaksi peradangan (inflamasi) di sekitar jaringan yang diimplankan sehingga apabila digunakan dalam jangka waktu lebih lama akan sangat berbahaya bagi tubuh (Manivasagam et al.
2010).
Ketahanan korosi dapat ditingkatkan melalui pelapisan logam oleh suatu material yang biokompatibel terhadap tubuh. Material tersebut harus cenderung tidak bereaksi (inert) ketika digunakan sebagai pengganti fungsi dari jaringan tubuh yang berkontak langsung dengan cairan tubuh (Karokaro et al. 2008). Salah satu material yang dapat digunakan untuk melapisi logam pen ialah hidroksiapatit (HAp).
Hidroksiapatit (Ca10(PO4)6(OH)2) dapat berikatan kuat dengan tulang, membentuk lapisan pada permukaan jaringan tulang, dan mempercepat pembentukan tulang pada permukaan yang diimplantasi (Pang dan Zhitomirsky 2005; Maachaou et al. 2008). Hidroksiapatit memiliki keterbatasan penggunaan yaitu sulit dijaga agar tetap pada tempatnya setelah diimplantasikan di tulang. Kelemahan ini diatasi dengan mengkombinasikan hidroksiapatit dalam matriks polimer seperti kitosan (Maachaou et al. 2008).
Proses pelapisan logam dengan apatit dapat dilakukan dengan berbagai macam metode seperti elektroforesis deposisi (EPD), sol gel, plasma spraying, ion sputtering, laser
ablation, hydrothermal, dan biomimetic (Pal
et al. 2005). Penelitian ini menggunakan
metode elektroforesis deposisi (EPD) untuk melapisi logam stainless steel (SS) 316 dengan komposit hidroksiapatit-kitosan. Kelebihan penggunaan metode EPD adalah
murah, pelapisan yang tipis dan merata, proses pada temperatur rendah, tanpa fase transformasi selama pelapisan dan kekuatan pelapisan yang tinggi (Javidi et al. 2008). Kelebihan utama metode EPD ialah kemampuannya dalam mengontrol stokiometri deposit. Derajat stokiometri deposit elektroforesis diatur dari kandungan komposisi serbuk yang digunakan (Pang dan Zhitomirsky 2005).
Penelitian ini bertujuan untuk meningkatkan ketahanan korosi logam stainless steel 316 dengan melapiskan komposit hidroksiapatit-kitosan pada logam tersebut menggunakan metode elektroforesis deposisi.
METODE
Bahan dan Alat
Alat-alat yang digunakan adalah alat-alat kaca, pipet ukur, hot plate, tanur, oven, spektrofotometer serapan atom (SSA), alat difraksi sinar-X (XRD), alat potensiostat/ galvanostat, alat elektroforesis deposisi PS-520, mikroskop stereo, FTIR dan mikroskop elektron payaran (SEM).
Bahan-bahan yang digunakan adalah cangkang telur, akuades, P2O5, kitosan, larutan asam asetat 2%, logam SS 316 dan 316L, etanol, larutan infus NaCl 0.9%, larutan NaOH 10 M, dan larutan H2SO4:HCl:air (1:1:1).
Lingkup Kerja
Penelitian terdiri dari beberapa tahap (Lampiran 1). Tahap pertama preparasi cangkang telur. Tahap kedua penentuan kadar Ca dalam serbuk cangkang telur menggunakan SSA. Tahap ketiga adalah sintesis hidroksiapatit metode kering. Tahap keempat ialah perlakuan terhadap logam SS 316. Tahap kelima adalah pelapisan logam SS 316 dengan metode elektroforesis deposisi (EPD). Tahap keenam adalah uji mikrostruktur, uji korosi, dan uji analisis fase XRD.
Preparasi Cangkang Telur (Modifikasi Prabakaran et al. 2005)
PENDAHULUAN
Berbagai macam jenis kecelakaan terjadi tiap tahunnya, baik itu ringan ataupun berat yang memungkinkan terjadinya kerusakan pada tulang. Kerusakan tulang dapat diatasi melalui pemasangan pen (implantasi) pada bagian tulang yang patah untuk mengembalikan posisi patahan tulang ke posisi semula (reposisi) dan mempertahankan posisi itu selama masa penyembuhan patah tulang (imobilisasi) (Oktavia 2009).
Logam yang digunakan dalam proses
implant harus memiliki sifat biokompatibilitas
yang tinggi agar keberadaannya di dalam tubuh tidak dianggap sebagai benda asing. Penggunaan logam yang memiliki biokompatibilitas rendah dapat menyebabkan korosi pada logam oleh cairan tubuh. Korosi logam pen dapat menimbulkan reaksi peradangan (inflamasi) di sekitar jaringan yang diimplankan sehingga apabila digunakan dalam jangka waktu lebih lama akan sangat berbahaya bagi tubuh (Manivasagam et al.
2010).
Ketahanan korosi dapat ditingkatkan melalui pelapisan logam oleh suatu material yang biokompatibel terhadap tubuh. Material tersebut harus cenderung tidak bereaksi (inert) ketika digunakan sebagai pengganti fungsi dari jaringan tubuh yang berkontak langsung dengan cairan tubuh (Karokaro et al. 2008). Salah satu material yang dapat digunakan untuk melapisi logam pen ialah hidroksiapatit (HAp).
Hidroksiapatit (Ca10(PO4)6(OH)2) dapat berikatan kuat dengan tulang, membentuk lapisan pada permukaan jaringan tulang, dan mempercepat pembentukan tulang pada permukaan yang diimplantasi (Pang dan Zhitomirsky 2005; Maachaou et al. 2008). Hidroksiapatit memiliki keterbatasan penggunaan yaitu sulit dijaga agar tetap pada tempatnya setelah diimplantasikan di tulang. Kelemahan ini diatasi dengan mengkombinasikan hidroksiapatit dalam matriks polimer seperti kitosan (Maachaou et al. 2008).
Proses pelapisan logam dengan apatit dapat dilakukan dengan berbagai macam metode seperti elektroforesis deposisi (EPD), sol gel, plasma spraying, ion sputtering, laser
ablation, hydrothermal, dan biomimetic (Pal
et al. 2005). Penelitian ini menggunakan
metode elektroforesis deposisi (EPD) untuk melapisi logam stainless steel (SS) 316 dengan komposit hidroksiapatit-kitosan. Kelebihan penggunaan metode EPD adalah
murah, pelapisan yang tipis dan merata, proses pada temperatur rendah, tanpa fase transformasi selama pelapisan dan kekuatan pelapisan yang tinggi (Javidi et al. 2008). Kelebihan utama metode EPD ialah kemampuannya dalam mengontrol stokiometri deposit. Derajat stokiometri deposit elektroforesis diatur dari kandungan komposisi serbuk yang digunakan (Pang dan Zhitomirsky 2005).
Penelitian ini bertujuan untuk meningkatkan ketahanan korosi logam stainless steel 316 dengan melapiskan komposit hidroksiapatit-kitosan pada logam tersebut menggunakan metode elektroforesis deposisi.
METODE
Bahan dan Alat
Alat-alat yang digunakan adalah alat-alat kaca, pipet ukur, hot plate, tanur, oven, spektrofotometer serapan atom (SSA), alat difraksi sinar-X (XRD), alat potensiostat/ galvanostat, alat elektroforesis deposisi PS-520, mikroskop stereo, FTIR dan mikroskop elektron payaran (SEM).
Bahan-bahan yang digunakan adalah cangkang telur, akuades, P2O5, kitosan, larutan asam asetat 2%, logam SS 316 dan 316L, etanol, larutan infus NaCl 0.9%, larutan NaOH 10 M, dan larutan H2SO4:HCl:air (1:1:1).
Lingkup Kerja
Penelitian terdiri dari beberapa tahap (Lampiran 1). Tahap pertama preparasi cangkang telur. Tahap kedua penentuan kadar Ca dalam serbuk cangkang telur menggunakan SSA. Tahap ketiga adalah sintesis hidroksiapatit metode kering. Tahap keempat ialah perlakuan terhadap logam SS 316. Tahap kelima adalah pelapisan logam SS 316 dengan metode elektroforesis deposisi (EPD). Tahap keenam adalah uji mikrostruktur, uji korosi, dan uji analisis fase XRD.
Preparasi Cangkang Telur (Modifikasi Prabakaran et al. 2005)
2
pada suhu 1000 °C selama 6 jam sehingga diperoleh serbuk cangkang telur yang berwarna putih. Serbuk cangkang telur dilakukan analisis pencirian dengan XRD untuk mengetahui fase yang terkandung di dalamnya.
Penentuan Kadar Kalsium Menggunakan SSA
Sebanyak 0.1 gram sampel serbuk cangkang telur dilarutkan dalam 1 mL HNO3 pekat kemudian diencerkan dengan aquadest hingga volume 50 mL. Deret standar dari CaCO3 disiapkan dengan cara yang sama dalam deret konsentrasi Ca 0, 2, 4, 8, 12, dan 16 ppm. Sampel dan deret standar yang telah siap kemudian diukur menggunakan SSA.
Sintesis Hidroksiapatit Metode Kering (Modifikasi Dahlan et al. 2009 dan Pramanik
et al. 2005)
Sebanyak 4.6430 gram P2O5 dan 8.9195 gram serbuk cangkang telur setelah pemanasan dicampur dan dimiling selama 6 jam (perbandingan antara P2O5 dan CaO sebesar 46.43% dan 50.52%). Campuran kemudian disintering pada suhu 1250 °C selama 2 jam agar terbentuk hidroksiapatit murni. Kemudian dilakukan analisis pencirian dengan XRD untuk mengetahui fase yang terkandung di dalamnya dan analisis mikrostruktur menggunakan SEM.
Perlakuan Logam Stainless Steel 316 (Modifikasi Lu Xiong et al. 2006)
Logam stainless steel 316 terlebih dahulu dipotong membentuk koin yang memiliki diameter sebesar 1.5 cm. Koin logam kemudian diamplas dengan kertas amplas yang memiliki kekasaran 60. Logam lalu direndam di dalam larutan H2SO4:HCl:air (1:1:1) selama 1 jam pada suhu 60 °C. Logam yang telah direndam dalam larutan H2SO4:HCl:air (1:1:1) dicuci dengan air suling lalu direndam dalam larutan NaOH 10 M selama 24 jam. Kemudian logam dicuci dengan air suling dan dikeringkan di udara terbuka selama 24 jam.
Pelapisan Logam SS 316 dengan Metode Elektroforesis Deposisi (EPD) (Modifikasi Pang dan Zhitomirsky 2007 dan Bowo 2009)
Pelapisan logam SS dengan hidroksiapatit-kitosan menggunakan metode EPD dilakukan dengan membuat larutan kitosan 3% terlebih dahulu melalui pelarutan 3 gram kitosan
dalam larutan asam asetat 2% hingga volume 100 mL. Larutan kitosan yang telah dibuat kemudian dilarutkan ke dalam 25 mL etanol dengan variasi volume kitosan 0, 0.1, 0.5, 1.0, dan 1.5 mL dan ditambahkan 0.2 gram hidroksiapatit sedikit demi sedikit dengan diaduk pada kecepatan pengadukan 500 rpm hingga homogen. Larutan koloid hidroksiapatit-kitosan yang telah terbentuk dihubungkan dengan dua elektroda, sebagai elektroda bermuatan negatif digunakan logam SS 316 yang merupakan target pelapisan dan sebagai elektroda bermuatan positif digunakan karbon. Selama proses elektroforesis deposisi, hidroksiapatit dan kitosan yang terdispersi akan bergerak karena pengaruh arus listrik sehingga akan menempel pada permukaan logam SS 316. Sumber tegangan yang digunakan ialah 120 V selama 2 menit.
Uji Analisis Fase Menggunakan XRD
Sampel yang akan dianalisis ditempatkan pada suatu spesimen holder yang kemudian diletakkan pada guaniometer dan dirotasikan pada sudut kalibrasi (2θ) tertentu. Hasil yang diperoleh berupa suatu difraktogram yang menunjukkan fase yang terdapat dalam sampel. Jenis fase yang terkandung ditentukan melalui perbandingan terhadap data Joint Committee on Powder Diffraction Standards
(JCPDS) (Lampiran 2).
Uji Ketahanan Korosi
Proses uji ketahanan korosi dilakukan dengan menggunakan perangkat potensiostat/ galvanostat model 273 pada potensial -20 mV sampai 20 mV dalam media pengkorosi larutan infus NaCl 0.9%. Logam yang akan diuji dirangkai pada working electrode dan dimasukkan ke dalam labu yang berisi media pengkorosi selanjutnya counter electrode dan
reference electrode dirangkai pada labu dan
dihubungkan pada perangkat potensiostat/ galvanostat. Laju korosi dapat diperoleh dengan adanya aliran pergerakan elektron pada reaksi elektrokimia. Laju korosi (mpy) ditentukan menggunakan rumus :
R mpy = 0.129 . BE . I D Keterangan :
R : Laju korosi (mpy)
BE : Berat ekivalen logam (gram) I : Arus korosi (µA/cm2)
Uji Mikrostruktur dengan SEM
Sampel ditempelkan pada cell holder
kemudian disalut emas dalam keadaan vakum selama waktu dan kuat arus tertentu dengan
ion coater. Sampel dimasukkan pada tempat
sampel dalam alat SEM dengan tegangan tertentu. Gambar yang dihasilkan berupa topografi dengan segala tonjolan, lekukan, dan lubang pada permukaan.
HASIL DAN PEMBAHASAN
Cangkang Telur
Proses pembentukan senyawa hidroksiapatit yang berkualitas dan murni memerlukan biaya yang tidak murah. Penggunaan cangkang telur sebagai sumber kalsium dalam pembentukan senyawa hidroksiapatit merupakan solusi yang tepat untuk memangkas biaya produksi hidroksiapatit (Dasgupta et al. 2004). Cangkang telur mengandung kalsium karbonat (94%), kalsium fosfat (1%), senyawa organik (4%), dan magnesium karbonat (1%). Tingginya kadar kalsium yang dimiliki cangkang telur, mendorong penggunaan limbah cangkang telur sebagai sumber kalsium alami dalam proses pembuatan hidroksiapatit (Pankaew et al. 2010). Selain itu cangkang telur juga tidak mengandung senyawa beracun sehingga dapat digunakan dalam bidang farmasi dan pangan (Murakami dan Rodrigues 2007).
Gambar 1 menunjukkan bahwa pada serbuk cangkang telur sebelum pemanasan terdapat fase CaCO3, Ca3(PO4)2 dan MgCO3. Keberadaan fase CaCO3 ditunjukkan dengan adanya puncak pada sudut 2θ 18.500°, 47.250°, dan 54.449°, fase Ca3(PO4)2 pada 28.750° dan 34.150° serta fase MgCO3 pada 50.850° (Lampiran 3). Preparasi awal cangkang telur dengan memanaskan cangkang telur pada suhu 1000 °C selama 6 jam mengakibatkan kalsium karbonat yang terkandung di dalam cangkang telur berubah menjadi kalsium oksida (Bahrololoom et al.
2009). Puncak fase CaO berada pada sudut 2θ
32.150°, 37.300°, 53.799°, 64.099°, dan 67.300° (Lampiran 3). Pemanasan ini juga dimaksudkan untuk menghilangkan karbonat yang merupakan zat pengganggu dalam proses kristalisasi hidroksiapatit (Dahlan et al. 2009). Ion karbonat dapat menempati posisi pada struktur hidroksiapatit, yaitu pada posisi pertama menggantikan gugus OH- membentuk
[image:43.595.325.500.273.