ENDAH KUSUMAWATI
BANDAR UDARA SOEKARNO-HATTA
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS
DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Kajian Q Fever pada Sapi Perah Impor dari Australia yang Masuk Melalui Bandar Udara Soekarno-Hatta adalah karya saya sendiri dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Juni2012
ENDAH KUSUMAWATI. Study of Q Fever in Imported Dairy Cattle from Australia through the Soekarno-Hatta Airport. Under direction of MIRNAWATI B. SUDARWANTO and TRIOSO PURNAWARMAN.
Q fever is worldwide distributed zoonosis caused by Coxiella burnetii. This intracelluar bacterium infects a wide range of animals and associated with reproductive disorders in domestic ruminants. It can lead an acute and chronic infections and caused flu-like syndrome, hepatitis, pneumonia or endocarditis. The aim of this research is to study Q fever in imported dairy cattle from Australia through the Soekarno-Hatta airport. Forty-six samples of serum and whole blood were taken from imported dairy cattle. Two diagnostic methods used in this study were serological test using enzyme-linked immunosorbant assay (ELISA) and nested polymerase chain reaction (nested PCR). The result of serological test showed that 23 (50%) out of 46 samples were positive but Coxiella burnetii DNA were not detected by nested PCR. These data revealed that Q fever have infected imported dairy cattle from Australia through Soekarno-Hatta airport with 50% of seroprevalence.
RINGKASAN
ENDAH KUSUMAWATI. Kajian Q Fever pada Sapi Perah Impor dari Australia yang Masuk Melalui Bandar Udara Soekarno-Hatta. Dibimbing oleh MIRNAWATI B. SUDARWANTO dan TRIOSO PURNAWARMAN.
Kegiatan importasi berisiko masuknya berbagai penyakit ke Indonesia. Hewan sapi dengan produknya yang diimpor dalam jumlah yang banyak akan menyebabkan masuknya penyakit baru (eksotik) yang dapat menular pada hewan dan manusia ke dalam wilayah Indonesia. Q fever merupakan penyakit yang bersifat zoonosis yaitu dapat ditularkan dari hewan ke manusia atau sebaliknya. Hewan ternak yang dapat terserang adalah sapi, kambing, domba maupun ternak ruminansia lain. Penularan dapat terjadi melalui kontak langsung dengan hewan, makanan asal ternak yang terinfeksi seperti daging, susu, produk ternak lainnya maupun oleh partikel debu yang terkontaminasi agen penyebab.
Coxiella burnetii adalah mikroorganisme penyebab penyakit Q fever, berbentuk pleomorfik (bentuknya tidak tetap, batang atau kokoid), bersifat obligat intraseluler, berukuran lebar 0.2-0.4 µm dan panjang 0.4-1.0 µm, struktur menyerupai spora (spora like). C. burnetii mempunyai membran yang sama seperti bakteri gram negatif, mempunyai bentuk besar (large form/large cell variant) dan bentuk kecil (small form/small cell variant). Agen penyebab tahan terhadap kondisi psikokimia, seperti lingkungan panas, kering, dan tahan terhadap beberapa konsentrasi desinfektan, seperti 0.05% hipoklorit, 5% peroksida, 1:100 larutan lisol, glutaraldehid, etanol dan gas formaldehid. Pada bahan pangan asal hewan dan olahannya C. burnetii dapat bertahan hidup 1 bulan pada daging yang disimpan dalam cold storage (suhu -18 °C sampai dengan -20 °C), 42 bulan pada susu segar yang disimpan dalam suhu 4-6 °C dan lebih dari 40 bulan pada susu skim. C. burnetii dapat dikembangkan sebagai senjata biologis yang berpotensi sebagai ancaman terorisme (bioterrorisme) seperti halnya Bacillus anthracis.
dengan sanitasi, higiene personal, dan biosekuriti. Hewan target adalah sapi perah impor dari Australia yang dilalu-lintaskan melalui Bandar Udara Soekarno-Hatta. Sampel yang diambil berupa serum dan whole blood, masing-masing sebanyak 46 sampel. Pengambilan sampel menggunakan rumus detect diseases dengan asumsi prevalensi 6.12 % dan tingkat kepercayaan 95 %, artinya prevalensi akan terpenuhi jika minimal ada 1 yang positif Q fever dari jumlah sampel tersebut. Sampel serum diuji dengan enzyme-linked immunosorbent assay (ELISA) menggunakan CHEKIT Q-Fever (Coxiella burnetii) Antibody Test Kit dan sampel whole blood diuji dengan menggunakan nested polymerase chain reaction (PCR).
Hasil uji serologi menunjukkan sebanyak 23 sampel (50%) positif Q fever dari 46 sampel dengan rata-rata persentase nilai positif adalah 92.54%. Hasil nested PCR dengan menggunakan primer OMP1, OMP2, OMP3 dan OMP4 dari 46 sampel whole blood adalah negatif. Pada umumnya jumlah sampel yang positif C. burnetii pada pemeriksaan serologis cenderung lebih tinggi jika dibandingkan dengan pemeriksaan dengan metode PCR. Pada pemeriksaan serologis, hewan yang positif antibodi terhadap C. burnetii adalah hewan yang telah terinfeksi dalam waktu lama, sementara agen penyebabnya sendiri belum tentu ada dalam tubuh hewan. Negatif nested PCR dapat disebabkan karena sifat C. burnetii yang merupakan bakteri intraseluler, pada fase akut dapat ditemukan di darah namun pada fase kronis bakteri banyak terakumulasi dalam sel fagosit yang terdapat di organ seperti jantung, hati, plasenta dan susu.
©Hak cipta milik IPB, tahun 2012 Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah; Pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
KAJIAN
Q FEVER
PADA SAPI PERAH IMPOR
DARI AUSTRALIA YANG MASUK MELALUI
BANDAR UDARA SOEKARNO-HATTA
ENDAH KUSUMAWATI
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Kesehatan Masyarakat Veteriner
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Nama : Endah Kusumawati NIM : B251100194
Disetujui
Komisi Pembimbing
Diketahui
Ketua Program Studi Kesehatan Masyarakat Veteriner
Dr. drh. Denny Widaya Lukman, M.Si.
Dekan Sekolah Pascasarjana IPB
Dr. Ir. Dahrul Syah, M.Sc. Agr.
Tanggal Ujian : Tanggal Lulus :
Prof. Dr. drh. Hj. Mirnawati B. Sudarwanto
Ketua
Dr. drh. Trioso Purnawarman, M.Si.
PRAKATA
Puji syukur penulis panjatkan kepada Allah SWT atas rahmat, karunia dan hidayahNya sehingga tesis ini dapat diselesaikan. Penelitian ini berjudul “Kajian Q Fever pada Sapi Perah Impor dari Australia yang Masuk Melalui Bandar Udara Soekarno-Hatta” yang dilaksanakan sejak bulan Januari hingga Mei 2012.
Penulis mengucapkan terima kasih kepada Ibu Prof. Dr. drh. Hj. Mirnawati B. Sudarwanto dan Bapak Dr. drh. Trioso Purnawarman, M.Si, selaku dosen pembimbing yang telah meluangkan waktu, pikiran, tenaga serta motivasi dalam membimbing penyelesaian tesis. Ucapan terima kasih kepada Kepala Badan Karantina Pertanian yang telah memberikan kesempatan untuk melanjutkan pendidikan Pascasarjana. Terima kasih juga disampaikan kepada Dr. Denny Widaya Lukman, M.Si. selaku Ketua Program Studi Kesehatan Masyarakat Veteriner dan Prof. Dr. drh. A.Winny Sanjaya, MS. sebagai penguji luar komisi. Kepada drh. Rahmat Setya Aji, M.Si dan Nunung Nuraeni, S.Si, M.Epid yang telah membantu penelitian ini. Ucapan yang sama ditujukan kepada seluruh pengajar dan staf bagian Kesehatan Masyarakat Veteriner Fakultas Kedokteran Hewan IPB yang telah banyak membantu proses pendidikan dan berlangsungnya penelitian. Terima kasih disampaikan juga kepada teman-teman Kelas Khusus Karantina Hewan (Siti Khadijah, Fitria Kusumaningrum, Wulandari, Amanatin, Agus Jaelani, Trifera Melaningrum, Gatot Santoso, Platika Widiyani, Made Ary, Ali Imran, Donni Muksydayan, Hari Yuwono Adi, Endang Sri Pertiwi dan Helmi), Kepala Balai Besar dan segenap staf Balai Besar Karantina Pertanian Soekarno Hatta yang telah membantu selama pengumpulan sampel sampai dengan pelaksanaan pengujian laboratorium, drh. Mazdani Daulay, M.Sc, keluarga besar Balai Besar Karantina Pertanian Makassar, Budi Ismanto, dan Bambang Urip yang turut serta membantu proses penelitian dan memberikan motivasi. Terima kasih dan penghargaan juga disampaikan kepada G. Sigit Pramono dan Ayesha Kartika Fajar Pramesti (sumber motivasi), almarhum ayahanda Soewadji, ibu, mami, kakak dan adikku, atas segala doa, perhatian, semangat dan kasih sayang yang diberikan.
Semoga karya ilmiah ini bermanfaat untuk ilmu pengetahuan dan kemaslahatan umat manusia.
Bogor, Juni 2012
Penulis dilahirkan di Karanganyar Jawa Tengah pada tanggal 18 Juni 1980 sebagai anak ke-5 dari 9 (sembilan) bersaudara dari ayah Soewadji dan ibu Sri Suprapti. Pendidikan dasar sampai menengah atas dijalani di SD Negeri I Buran Tasikmadu Karanganyar tahun 1992, SMP Negeri I Karanganyar tahun 1995, SMU Negeri I Kebakkramat Karanganyar 1998, lulus Sarjana Kedokteran Hewan Universitas Airlangga tahun 2004 dan menjadi Dokter Hewan pada tahun 2005. Kesempatan untuk melanjutkan ke Program Magister pada Program Studi Kesehatan Masyarakat Veteriner Fakultas Kedokteran Hewan Institut Pertanian Bogor dengan dukungan biaya perkuliahan dari DIPA Badan Karantina Pertanian Departemen Pertanian.
Penulis bekerja sebagai Pegawai Negeri Sipil di Balai Besar Karantina Pertanian Makassar dari tahun 2006 sampai dengan sekarang. Selama mengikuti perkuliahan, penulis menjadi pegawai yang diperbantukan sementara di Balai Besar Karantina Pertanian Soekarno-Hatta.
xvii
Enzyme-linked immunosorbent assay (ELISA) ... 16
Nested Polymerase Chain Reaction (PCR) ... 17
Pencegahan dan Pengendalian ... 19
Besaran dan Metode Pengambilan Sampel ... 22
Uji Serologis (ELISA) ... 23
Identifikasi DNA C. burnetii dengan Metode Nested PCR ... 24 Ekstraksi DNA (Qiagen Kit) ... 24
Spektrofotometer (NanoVue PlusTM)... 25
xviii HASIL DAN PEMBAHASAN
Hasil ELISA ... Hasil Nested PCR ... Pembahasan Umum ...
SIMPULAN DAN SARAN ...
29 31 34
39
DAFTAR PUSTAKA ... 41
xix
DAFTAR TABEL
Halaman
1
2
3
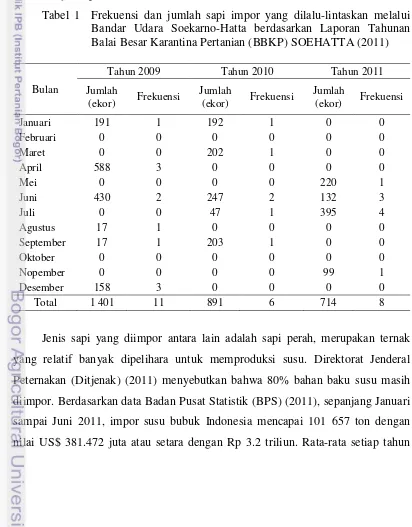
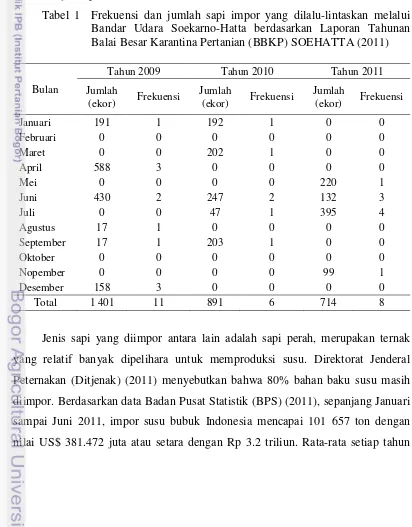
Frekuensi dan jumlah sapi impor yang dilalu-lintaskan melalui Bandar Udara Soekarno-Hatta berdasarkan Laporan Tahunan Balai Besar Karantina Pertanian (BBKP) SOEHATTA (2011) ...
Interpretasi hasil ELISA ...
Hasil uji serologi terhadap Q fever dengan metode ELISA ...
1
23
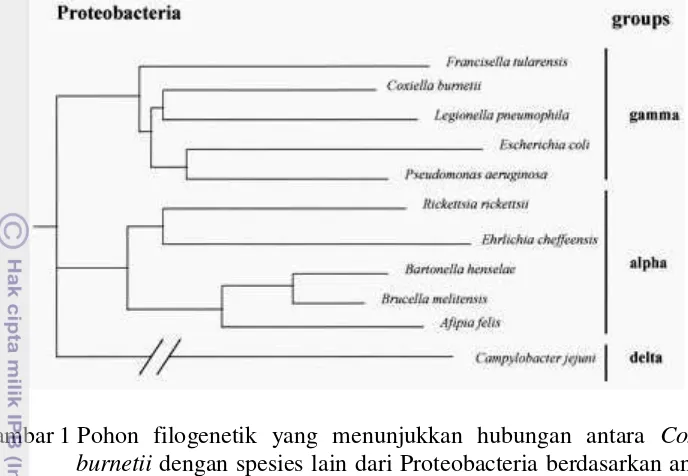
xx Coxiella burnetii dengan spesies lain dari Proteobacteria
berdasarkan analisis sekuen 16S rRNA ...
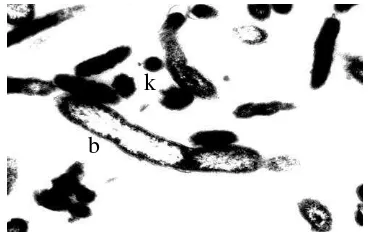
Coxiella burnetii dengan mikrograf elektron pada pembesaran 75 000 kali, (k) bentuk kecil, (b) bentuk
Metode ELISA (CHEKIT Q-fever (Coxiella burnetii) antibody test kit, IDEXX, Switzerland) ...
xxi
DAFTAR LAMPIRAN
Halaman
1
2
3
4
Kuisioner kajian penyakit Q fever ...
Hasil pengujian ELISA ...
Konsentrasi dan tingkat kemurnian DNA ...
Sertifikat analisis CHEKIT Q-fever (Coxiella burnetii) antibody test kit ...
49
53
55
PENDAHULUAN
Latar Belakang
Keanekaragaman sumber daya hayati merupakan modal dasar dan faktor
dominan dalam penyelenggaraan pembangunan nasional. Seiring dengan
perkembangan ekonomi, perdagangan dan teknologi informasi mengakibatkan
meningkat pula frekuensi lalu-lintas dan jumlah komoditi hewan beserta
produknya di masing-masing kegiatan ekspor, impor, dan antar area. Frekuensi
dan jumlah sapi impor yang dilalu-lintaskan melalui Bandar Udara
Soekarno-Hatta disajikan pada Tabel 1.
Tabel 1 Frekuensi dan jumlah sapi impor yang dilalu-lintaskan melalui Bandar Udara Soekarno-Hatta berdasarkan Laporan Tahunan Balai Besar Karantina Pertanian (BBKP) SOEHATTA (2011)
Bulan
Tahun 2009 Tahun 2010 Tahun 2011
Jumlah
yang relatif banyak dipelihara untuk memproduksi susu. Direktorat Jenderal
Peternakan (Ditjenak) (2011) menyebutkan bahwa 80% bahan baku susu masih
diimpor. Berdasarkan data Badan Pusat Statistik (BPS) (2011), sepanjang Januari
sampai Juni 2011, impor susu bubuk Indonesia mencapai 101 657 ton dengan
2
Indonesia mengimpor bahan baku dan produk jadi susu sebesar US$ 600 juta atau
kurang lebih Rp 5.1 triliun. Impor terbanyak berasal dari Selandia Baru dengan
nilai sebesar US$ 126.65 juta, Australia senilai US$ 85.297 juta, Amerika Serikat
senilai US$ 77.610 juta, Filipina sebanyak US$ 19.247 juta, Singapura senilai
US$ 15.528 juta dan negara lainnya US$ 57.137 juta. BPS juga mencatat,
pergerakan impor susu dari bulan ke bulan menunjukan kenaikan, April 2011
impor susu hanya sebesar US$ 58.368 juta, Mei naik US$ 70.865 juta, Juni naik
menjadi US$ 77.432 juta. Lonjakan susu impor yang masuk ke Indonesia seiring
dengan pertumbuhan industri susu yang mencapai level 6 sampai 7% per tahun.
Kegiatan importasi beresiko masuknya berbagai penyakit ke Indonesia.
Keputusan importasi pada akhirnya harus mempertimbangkan
kepentingan-kepentingan lain baik ekonomi dan politis. Analisa risiko merupakan suatu proses
komplek yang sebenarnya tidak hanya ditujukan untuk menjamin keamanan dan
kesehatan pangan secara fisik, tetapi juga secara rohani, karena dalam tahap
analisa risiko sudah termasuk verifikasi kehalalan produk yang akan diimport
dimana merupakan orientasi penting bagi masyarakat Indonesia. Kebijakan
importasi yang didasari murni oleh analisa risiko tidak akan memberikan efek
yang merugikan berbagai pihak yang terkait dengan kegiatan importasi itu sendiri
apabila kondisi negara sudah cukup memadai dengan pilihan tidak melakukan
importasi. Kondisi yang memadai tersebut harus mencakup kesiapan negara akan
ketersediaan ternak dan produksinya untuk memenuhi kebutuhan dalam negeri.
Program swasembada pangan merupakan program yang tepat untuk mendukung
kebijakan importasi.
Program Swasembada Daging Sapi Tahun 2014 (PSDS 2014) merupakan
salah satu program prioritas pemerintah dalam lima tahun ke depan untuk
mewujudkan ketahanan pangan asal ternak berbasis sumber daya lokal.
Pencapaian swasembada daging sapi merupakan tantangan yang tidak ringan,
karena pada tahun 2009 impor daging mencapai 7.0 x 104 ton dan sapi bakalan
setara dengan 250.8 x 103 ton daging (Ditjenak 2010).
Data menunjukkan bahwa Indonesia mengimpor sapi rata-rata
6.5 x 105 ekor per tahun yang sebagian besar berasal dari Australia (Asosiasi
negara asal dan pertama ditemukannya Query fever (Q fever) pada pekerja rumah
potong hewan di Brisbane pada tahun 1935 (Acha dan Szyfres 2003). Hewan sapi
dengan produknya yang diimpor dalam jumlah yang banyak akan menyebabkan
masuknya penyakit baru (eksotik) yang dapat menular pada hewan dan manusia
ke Indonesia.
Q fever merupakan penyakit yang bersifat zoonosis yaitu dapat ditularkan
dari hewan ke manusia atau sebaliknya. Hewan ternak yang dapat terserang
adalah sapi, kambing, domba maupun ternak ruminansia lain. Penularan dapat
terjadi melalui kontak langsung dengan hewan terinfeksi, melalui makanan asal
ternak terinfeksi seperti daging, susu, produk ternak lainnya maupun oleh partikel
debu yang terkontaminasi agen penyebab. Q fever tersebar luas di seluruh dunia
bahkan telah menjadi masalah kesehatan masyarakat di banyak negara seperti
Amerika, Perancis, Inggris, Italia, Jerman, Spanyol, Kanada, Jepang, Australia,
Thailand, Taiwan, Malaysia, dan beberapa negara lain di Asia Tenggara
(Fournier et al. 1998). Akibat distribusi geografis Q fever yang sangat luas dan
letak geografis Indonesia yang berdekatan wilayah dengan negara-negara endemik
Q fever terutama Australia, maka perlu diwaspadai penyebaran infeksi penyakit
ini di Indonesia.
Penelitian tentang Q fever di beberapa negara sudah demikian maju, bahkan
sekuensing genom dari C. burnetii secara lengkap sudah dilakukan, mengingat
C. burnetii mempunyai potensi untuk dipakai sebagai senjata biologis
(Seshadri et al. 2003). Laporan epidemiologi dari banyak negara menyebutkan
bahwa orang yang sering kontak langsung dengan ternak, seperti peternak, pekerja
rumah potong, masyarakat yang tinggal di daerah kumuh (urban area) berpeluang
besar terserang Q fever. Indonesia dengan jumlah penduduk yang sebagian besar
adalah petani yang tidak terlepas dari hewan ternak serta banyaknya lokasi kumuh
di perkotaan sangat rentan terhadap infeksi Q fever. Penentuan diagnosis yang
cepat dan akurat terhadap Q fever sangat dibutuhkan sebagai upaya pengendalian
4
Perumusan Masalah
Penelitian terhadap penyebab Q fever di Indonesia sampai saat ini masih
jarang dilakukan karena gejala klinis bentuk akut infeksi Q fever yang tidak begitu
menciri, seperti terjadinya pneumonia, keguguran ataupun tingginya kasus
hepatitis dan endokarditis. Temuan kasus klinik belum pernah didiagnosa kearah
adanya Q fever, sehingga kurang diperhatikan oleh pemerintah dan masyarakat.
Di satu sisi dampak jangka panjang penyakit ini sangat membahayakan dan fatal
bagi manusia. Di sisi lain Indonesia merupakan pengimpor ternak terutama sapi,
baik sapi bakalan, sapi perah maupun daging beku dari Amerika, Australia, New
Zealand dan beberapa negara lain. Selain itu era globalisasi akan meningkatkan
arus lalu lintas perdagangan ternak dan juga mobilitas manusia, yang juga
berdampak terhadap cepatnya penyebaran penyakit khususnya zoonosa seperti
Q fever ataupun yang lainnya.
Laporan World Health Organization (WHO) menyatakan bahwa pada tahun
1955 Q fever pertama kali ditemukan di Indonesia dari 188 serum sapi yang
diperiksa secara serologis positif mengandung antibodi C. burnetii menggunakan
cappilary tube agglutination test (CAT) (Kaplan dan Bertagna 1955). Penelitian
selanjutnya dilakukan oleh Rumawas (1976) menunjukkan bahwa dari 323 sampel
darah sapi yang diambil dari Bogor, Bandung, Surabaya dan Semarang ditemukan
4 sampel (1.2%) positif antibodi terhadap Q fever menggunakan metode CAT.
Vanpeenen et al. (1978) juga melakukan penelitian penyakit Q fever pada pekerja
di Indonesia secara seroepidemiologi.
Penelitian selanjutnya dilaporkan Miyashita et al. (2001) pada kasus
pneumonia yang diderita oleh seseorang yang pernah tinggal di Indonesia dan
ditemukan positif terinfeksi C. burnetii. Hasil seroprevalensi Q fever di Bogor
pada domba dan kambing menunjukkan sebesar 31.88% dan 20.29%
menggunakan metode indirect immunofluorescent antibody (IFA), sedangkan
dengan metode nested polymerase chain reaction (nested PCR) terhadap 245 ekor
sapi bali dan Brahman cross ditemukan 15 ekor (6.12%) positif DNA C. burnetii
serta pada 165 ekor kambing dan domba ditemukan 6 ekor (3.64%) positif DNA
Data di atas dapat dijadikan dasar untuk melakukan penelitian tentang
keberadaan penyakit Q fever di Indonesia terutama pada hewan sapi yang diimpor
dari Australia, hal ini penting dilakukan karena sampai saat ini volume importasi
sapi masih tinggi untuk mewujudkan swasembada daging tahun 2014.
Tujuan
Penelitian ini bertujuan untuk (1) melakukan suatu kajian tentang penyakit
Q fever dan keberadaan C. burnetii pada sapi perah impor dari Australia, dan (2)
mengkaji faktor risiko penyebaran C. burnetii ke lingkungan berkaitan dengan
sanitasi, higiene personal, dan biosekuriti.
Manfaat
Penelitian ini diharapkan dapat memberikan gambaran data yang pasti dan
akurat tentang keberadaan C. burnetii sebagai penyebab penyakit Q fever
sehingga dapat dijadikan pertimbangan ilmiah dalam hal importasi sapi perah dari
Australia.
Hipotesa
Hipotesa penelitian ini adalah (1) C. burnetii sebagai penyebab Q fever
ditemukan dan menginfeksi sapi perah impor dari Australia, dan (2) terdapat
faktor risiko penyebaran C. burnetii ke lingkungan peternakan berkaitan dengan
TINJAUAN PUSTAKA
Sejarah
Nama lain dari penyakit demam Q atau Q fever di beberapa negara adalah
Acute Q fever, Chronic Q fever, Coxiella burnetii fever, Coxiella burnetii borne
diseases, Australian Q fever, Australian Q, Balkan influenza, Balkan Nine Mile
Fever, Coxiella burnetii infection, Derrick-bunet diseases, Hibernovenal
bronchopneumoni, Q fever pneumonia, Querry fever dan Puzzling fever (Acha
dan Szyfres 2003).
Nama Q fever berasal dari kata “Querry” (Q) yang pertama kali ditemukan
oleh Edward Holbrook Derrick pada tahun 1937. Kejadian penyakit ini bermula
pada pekerja rumah potong hewan di Brisbane Queensland Australia yang
menderita demam namun tidak jelas penyebabnya (Baca dan Paretsky 1983).
Meskipun telah dilakukan penelitian terhadap penyakit tersebut pada saat itu,
namun belum berhasil menemukan penyebab utama dari Q fever, sehingga
dinamakan penyakit Maladi Q (Query) fever. Pada tahun 1939 Macfarlane
Burnett menyatakan bahwa penyebab Q fever adalah riketsia, dari ordo
Rickettsiales, famili Rickettsiaceae dengan nama spesies Rickettsia diaporica,
namun untuk mengenang jasa Macfarlane Burnett diubah menjadi Rickettsia
burnetii (Maurin dan Raoult 1999).
Berdasarkan analisis sekuen 168 rRNA yang dilakukan Maurin dan Raoult
(1999), ternyata Rickettsia burnetii secara filogenik lebih dekat dengan
Pseudomonas aeruginosa, Francisella tularensis, Escherichia coli, dan
Legionella pneumophila dalam kelompok famili Proteobacteria subdivisi gamma.
Namun demikian ternyata masih mempunyai perbedaan dengan kelompok
tersebut dan akhirnya berdiri sendiri dengan nama Coxiella burnetii seperti
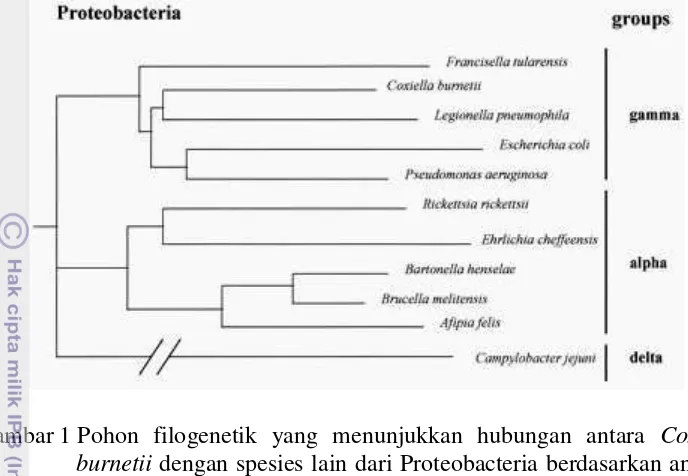
Gambar 1 Pohon filogenetik yang menunjukkan hubungan antara Coxiella burnetii dengan spesies lain dari Proteobacteria berdasarkan analisis sekuen 16S rRNA (Maurin dan Raoult 1999).
Organisme
C. burnetii adalah mikroorganisme pleomorfik (bentuknya tidak tetap,
batang atau kokoid), bersifat obligat intraseluler, berukuran lebar 0.2-0.4 µm dan
panjang 0.4-1.0 µm, struktur menyerupai spora (spora like) (Fournier et al. 1998).
C. burnetii mempunyai membran yang sama seperti bakteri gram negatif namun
secara umum sulit dilihat dengan teknik pewarnaan Gram, sehingga dipakai
pewarnaan Gimenez yang umum digunakan untuk pewarnaan spesimen klinik
atau kultur laboratorium. Alternatif lain adalah menggunakan pewarnaan Stamps
dengan pewarna 2% basic fuchsin dan counterstained methylen blue (Baca dan
Paretsky 1983; Maurin dan Raoult 1999). C. burnetii mempunyai bentuk besar
(large form/large cell variant) dan bentuk kecil (small form/small cell variant)
9
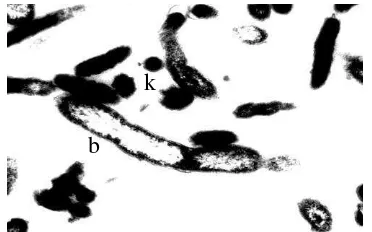
Gambar 2 Coxiella burnetii dengan mikrograf elektron pada pembesaran 75 000 kali, (k) bentuk kecil, (b) bentuk besar (Fournier et al.
1998).
Bentuk besar adalah bentuk vegetatif yang menginfeksi monosit dan sel
makrofag, sedangkan bentuk kecil terdapat ekstraseluler dan diduga merupakan
bentuk yang infeksius. C. burnetii memiliki 2 bentuk antigen yaitu antigen fase I
dan fase II. Antigen fase I ditemukan di alam atau hewan, sedangkan fase II
ditemukan setelah passage di telur tertunas atau sel kultur. Antigen fase I bersifat
lebih patogenik dibandingkan dengan fase II. Perbedaan antara kedua fase antigen
ini sangat penting di dalam diagnosa. Antigen fase I mempunyai susunan
lipopolisakarida (LPS) yaitu L-vironosa dihidroksistreptosa dan galaktosamin
uronil (1.6) glukosamin, bersifat halus dan berperan dalam menentukan
patogenitasnya, sedangkan fase II terlihat kasar dan tidak ditemukan rantai
sakarida vironosa dan hidroksistreptosa, seperti pada Gambar 3 (Fournier et al.
1998).
Gambar 3 Antigen fase I (a) dan fase II (b) C. burnetii (Fournier et al. 1998).
Pada infeksi Q fever akut, antibodi terhadap antigen fase II lebih dominan
dibandingkan dengan terhadap fase I. Namun pada kasus kronis, antibodi terhadap
antigen fase I lebih memegang peran penting. Kedua antibodi ini dapat bertahan
hingga berbulan-bulan setelah infeksi (Field et al. 2002; Harris et al. 2000). b
k
Menurut Centers for Diseases Control (CDC 2005) pada penderita akut Q fever
dapat dideteksi dengan peningkatan antibodi IgG fase II serta IgM fase I dan fase
II, sedangkan pada kondisi kronis Q fever terlihat peningkatan antibodi IgG dan
IgA fase I.
Center for Food Security and Public Health (CFSPH 2007) menyebutkan
bahwa agen penyebab tahan terhadap kondisi psikokimia, seperti lingkungan
panas, kering dan tahan terhadap beberapa konsentrasi desinfektan, seperti 0.05%
hipoklorit, 5% peroksida dan 1:100 larutan lisol serta glutaraldehid, etanol dan gas
formaldehid. C. burnetii pada bahan pangan asal hewan dan olahannya dapat
bertahan hidup 1 bulan pada daging yang disimpan dalam cold storage (suhu
-18 °C sampai dengan -20 °C), 42 bulan pada susu segar yang disimpan dalam
suhu 4-6 °C dan lebih dari 40 bulan pada susu skim (CFSPH 2007). C. burnetii
dapat dikembangkan sebagai senjata biologis yang berpotensi sebagai ancaman
terorisme (bioterrorisme) seperti halnya Bacillus anthracis (Maurin dan Raoult
1999; CDC 2005).
Epidemiologi
Q Fever pada Hewan
Hewan yang dapat terinfeksi C. burnetii antara lain sapi, kambing, domba,
anjing, kucing, kuda, kerbau, babi, unta, kelinci, reptil, kodok, burung merpati,
kalkun, ayam, bebek, rodensia, ikan, dan caplak (Arricau-Bouvery dan Rodolaksis
2005; Parker et al. 2006; Muskens et al. 2007). Burung dan rodensia merupakan
pembawa C. burnetii di alam, sedangkan sapi, kambing, dan domba merupakan
reservoir utama (Acha dan Szyfres 2003; Kim et al. 2005; Van den Brom dan
Vellema 2009).
Penularan Q fever dapat terjadi melalui kontak langsung dengan sumber
penularan, partikel debu, bahan makanan asal hewan, susu, dan luka yang
terkontaminasi serta melalui transfusi darah (Baca dan Paretsky 1983; Fournier
et al. 1998). C. burnetii dapat mengkontaminasi lingkungan jika ada hewan yang
melahirkan, yaitu melalui cairan amnion, plasenta, feses, dan urin secara terus
11
manusia karena kejadian pada kambing lebih lama dibandingkan domba, yaitu
selama dua kali masa kebuntingan (Hatchette et al. 2003; Arricau-Bouvery dan
Rodolaksis 2005). Mikroorganisme C. burnetii berkembangbiak dan tumbuh
subur di dalam plasenta dan cairan amnion, sehingga pada hewan bunting infeksi
Q fever bersifat laten (Kloppert et al. 2004).
Caplak merupakan sumber penularan antar hewan di alam, dari hewan liar
ke hewan pelihara, dan diantara hewan pelihara melalui feses caplak yang
terinhalasi. Caplak dapat berperan sebagai perantara pada hewan tetapi tidak pada
manusia. Penyebaran antar hewan pelihara dapat juga terjadi melalui kontak
seksual karena agen penyebab ditemukan pada semen sapi (Marrie 2000; Maurin
dan Raoult 1999).
Beberapa negara seperti Amerika, Perancis, Inggris, Italia, Jerman, Spanyol,
Kanada, Jepang, Australia, Thailand, Korea, Taiwan, Malaysia, dan beberapa
negara lain di Asia Tenggara, Q fever merupakan masalah kesehatan masyarakat
yang penting. Penelitian tentang Q fever telah banyak dilakukan dan bahkan
sekuensing genom dari C. burnetii telah dilakukan secara lengkap (Seshadri et al.
2003). Hal ini dilakukan karena C. burnetii berpotensi untuk dipakai sebagai
provinsi yang berbeda di Oman ternyata 52% seropositif terhadap C. burnetii.
Selain itu, terdapat hubungan yang nyata antara kasus infeksi C. burnetii pada
hewan dan pada manusia. Setiyono et al. (2005) menetapkan kriteria baru untuk
uji serologis terhadap Q fever dengan metode IFA, dan penggunaan PCR juga
telah dievaluasi serta dapat dipakai untuk mendeteksi C. burnetii (Ogawa et al.
Q Fever pada Manusia
Menurut Van den Brom dan Vellema 2009, kejadian Q fever pada manusia
berhubungan erat dengan pekerjaan (occupational disease), seperti peternak,
pembeli dan pengunjung yang datang ke peternakan; dokter hewan; pekerja di
peternakan, rumah potong hewan, penyamakan kulit, pengolahan daging, susu dan
wol; peneliti dan pegawai laboratorium serta pekerja di kebun binatang. Penularan
antar manusia jarang terjadi, tetapi dapat melalui transfusi (darah, sumsum tulang
belakang), saliva, dan hubungan seksual. Selain itu bisa tertular selama
menangani keguguran dan otopsi pada manusia (Milazzo et al. 2001). Beberapa
faktor yang mempermudah seseorang terserang Q fever yaitu tidak divaksinasi
Q fever dan yang mengalami imunosupresan karena menderita penyakit tertentu,
misalnya AIDS, kanker, limpoma, tumor, diabetes, hepatitis, gangguan jantung,
gangguan ginjal kronis atau penerima transplan organ (Norlander 2000).
Hasil penelitian Marrie (2003) menunjukkan bahwa C. burnetii dapat
menimbulkan pneumonia yang fatal pada manusia. Penularan Q fever secara
aerosol dapat menimbulkan lesi yang hebat pada paru-paru (Stein et al. 2005).
Q Fever sebagai Penyebab Food-borne Diseases
Kim et al. 2005 menyatakan bahwa jika sapi perah terinfeksi C. burnetii
maka mikroorganisme tersebut dapat ditemukan dalam susu, hal ini merupakan
salah satu sumber penularan dari hewan ke manusia (Rodolaksis et al. 2009).
Penelitian Hirai et al. (2005) menemukan 131 sampel (53.7%) positif DNA
C. burnetii dari 244 sampel susu yang dijual di supermarket di Tokyo
menggunakan metode nested PCR. Fretz et al. (2007) menemukan 17 sampel
(4.7%) dari 359 sampel susu sapi positif DNA C. burnetii menggunakan metode
nested PCR di Zwitzerland, tetapi tidak ditemukan pada susu domba dan
kambing.
Q Fever di Indonesia
Kaplan dan Bertagna (1955) melakukan penelitian tentang keberadaan
Q fever di Indonesia menggunakan metode CAT terhadap 188 serum sapi yang
13
323 sampel darah sapi yang diambil dari Bogor, Bandung, Surabaya dan
Semarang , didapatkan 4 sampel (1.2%) positif antibodi Q fever dengan metode
CAT (Rumawas 1976). Miyashita et al. (2001) menemukan infeksi Q fever dari
penderita pneumonia yang pernah tinggal di Indonesia. Penelitian
seroepidemiologi terbaru terhadap spotted fever group rickettsia (SFGR) di
Indonesia dilakukan oleh Richards et al. (2003) di Kepulauan Gag yang
menunjukkan bahwa reaktor yang bereaksi positif sebanyak 2.1-20.4%.
C. burnetii secara serologis dan molekuler telah ditemukan pada hewan
ruminansia (domba, kambing, sapi) dan juga manusia, sehingga kemungkinan
penularan kepada hewan lain dan bahan pangan asal hewan (susu, telur) di
beberapa wilayah di Indonesia sudah terjadi. Hal ini didasarkan pada hasil
seroprevalensi di kota Bogor pada domba dan kambing menunjukkan seropositif
masing-masing 31.88% dan 20.29% menggunakan metode IFA. Penelitian pada
sapi bali dan brahman cross ditemukan 6.12% positif DNA C. burnetii, serta pada
kambing dan domba 3.64% positif C. burnetii menggunakan metode nested PCR
(Mahatmi 2006).
Gejala Penyakit
Hewan yang terinfeksi C. burnetii tidak selalu menunjukkan gejala klinis,
bahkan lebih sering tidak ada gejala yang tampak. Fase akut C. burnetii dapat
ditemukan di dalam darah, jantung, hati dan limpa hewan yang terinfeksi.
Penyakit umumnya berlanjut menjadi kronis dan secara terus menerus hewan akan
mengekskresikan bakteri melalui tinja dan urin (Smith 1999; Ho et al. 1995).
Gejala umum pada ruminansia ditandai dengan anoreksia, rhinitis, frekuensi
pernafasan meningkat, abortus, retensio plasenta, endometritis, tidak fertil dan
beberapa ditemukan lahir dalam keadaan lemah, kecil dan mati (Arricau-Bouvery
dan Rodolaksis 2005). Sapi perah kadang-kadang terlihat pneumonia, sedangkan
pada anak domba terjadi diare dan gangguan pernafasan (Van den Brom dan
Vellema 2009).
Infeksi C. burnetii pada hewan umumnya bersifat subklinis, yang ditandai
dengan penurunan nafsu makan, gangguan pernapasan ringan dan gangguan
C. burneii sering bersifat akut dan menahun serta dapat menimbulkan kondisi
yang fatal, yaitu kegagalan fungsi hati, radang tulang, radang otak, gangguan pada
pembuluh darah dan endokarditis yang berakibat kematian (Raoult 2002).
Ho et al. (1995) menyatakan bahwa beberapa kasus pneumonia pada anak-anak di
Jepang ternyata disebabkan oleh Q fever.
Penularan pada manusia jarang terjadi, tetapi dapat melalui transfusi (darah,
sumsum tulang belakang), saliva dan hubungan seksual. Selain itu dilaporkan bisa
tertular selama menangani keguguran dan otopsi pada manusia (Milazzo et al.
2001). Manusia yang terserang penyakit Q fever umumnya menunjukkan gejala
klinis yang tidak spesifik atau asymptomatis (60%), spesifik atau symptomatis
(38%) dan beberapa penyakit lainnya (2%), sehingga sulit dibedakan dengan
gejala dari penyakit lain. Gejala akut pada umumnya seperti flu (flu like
syndrome), misalnya demam, sakit kepala, berkeringat, menggigil, lelah (fatigue),
pegal-pegal, sakit tenggorokan, batuk, dada sakit, muntah, diare dan penurunan
bobot badan.
Penyakit Q fever yang tidak terobati dalam kurun waktu dua minggu, dapat
berlanjut menjadi pneumonia (30-50%), hepatitis, infeksi kulit, hepatomegali,
miokarditis, perikarditis, meningoencefalitis, uveitis, artritis, tromboplebitis,
pleuritis dan pankreatitis. Wanita hamil yang terinfeksi C. burnetii akan
mengalami keguguran pada semester pertama atau lahir prematur, bayi dengan
bobot badan rendah dan plasentitis pada saat melahirkan (Arricau-Bouvery dan
Rodolaksis 2005; CFSPH 2007; Maurin dan Roault 1999). Kematian pada kasus
akut dapat mencapai 1-2% (CDC 2005; CFSPH 2007; Delsing dan Kullberg
2008).
Kasus Q fever akut akan menjadi kronis sebanyak 2-10% jika selama 6-12
bulan tidak diberikan pengobatan yang efektif, yaitu terjadi endokarditis, infeksi
osteoartikular, pneumoni fibrosis, sindrom kelelahan kronis (chronic fatique
syndrome), dan masalah kehamilan (Maurin dan Roault 1999; Schimmer et al.
2008). Kematian pada penderita kasus kronis bisa mencapai 25-65% (bila
mempunyai faktor imunosupresan dan atau abnormal valvular). Sindrom
kelelahan kronis ditandai dengan seringnya mengalami kelelahan yang panjang
15
dan waktu tidur berubah. Sindrom ini terjadi setelah infeksi akut yang
berlangsung lebih dari satu bulan (Arricau-Bouvery dan Rodolaksis 2005; CDC
2005; Delsing dan Kullberg 2008). Gambaran darah dari orang yang menderita
penyakit Q fever akut ditandai dengan peningkatan laju endap darah, jumlah sel
darah putih cenderung rendah sampai normal, trombositopenia serta urinalisis
yang abnormal, seperti hematuria, leukosituria, proteinuria (Ergar et al. 2006).
Masa inkubasi penyakit Q fever pada manusia bervariasi mulai 2-5 minggu
dan beberapa kasus mencapai lebih dari 6 minggu (Maurin dan Roault 1999;
CFSPH 2007; Delsing dan Kullberg 2008). Masa inkubasi dipengaruhi oleh dosis
infeksi C. burnetii (Maurin dan Roault 1999). Orang yang terinfeksi 1-10 sel
mikroorganisme C. burnetii dapat menimbulkan gejala klinis (CFSPH 2007).
Teknik Diagnosa
Gejala dan tanda dari penyakit Q fever tidak spesifik sehingga sulit
membuat diagnosa tanpa didukung dengan tes laboratorium. Diagnosa yang
diperlukan untuk menegaskan Q fever adalah dengan melakukan tes darah untuk
mendeteksi kehadiran antibodi terhadap C. burnetti. IFA, ELISA, dan CFT adalah
uji yang dapat diandalkan dan umum digunakan di laboratorium. C. burnetii
mungkin dapat diidentifikasi pada jaringan yang terinfeksi (plasenta, hati,
paru-paru fetus yang mati dan jaringan lain), susu, telur, kotoran, cairan vagina dengan
menggunakan PCR. Pembuatan preparat histopatologi dengan pewarnaan Ziehl
neelsen, Gimenez, Stamp, Giemsa, Immunohistokimia pada placenta atau jaringan
lain, apabila positif akan terlihat C. burnetii yang terbentuk pleomorfik, kecil,
bulat atau seperti benang.
Beberapa penelitian serodiagnosa memberikan gambaran yang sangat
berguna untuk mengetahui seroprevalensi Q fever di suatu daerah secara luas
dalam waktu relatif singkat (Setiyono et al. 2008). Metode serodiagnosa yang
telah diterapkan untuk pemeriksaan Q fever adalah capilary tube agglutination
test (CAT), complement fixation test (CFT), enzyme-linked immunosorbent assay
(ELISA) dan indirect immunofluorescent antibody (IFA) (Cetinkaya et al. 2000;
Enzyme-Linked Immunosorbent Assay (ELISA)
Enzyme-Linked Immunosorbent Assay (ELISA) adalah suatu metoda
immunokimia yang berdasarkan reaksi spesifik antara antigen dengan antibodi
yang memiliki sensitivitas dan spesifisitas yang tinggi dengan menggunakan
enzim sebagai indikatornya. Antigen atau antibodi yang dilabel dengan enzim dan
diikatkan dengan pendukung immunosorbent akan membentuk antigen-antibodi
kompleks. Metoda ELISA dengan antigen kompetitif, antibodi dilapiskan pada
immunosorbent (substrat padat), kemudian antigen sampel dan antigen yang
berlabel enzim dimasukan kedalam immunosorbent sehingga terjadi kompetisi
antara antigen sampel dengan antigen berlabel enzim untuk berikatan dengan
antibodi dan terbentuk kompleks antibodi-antigen. Tambahan substrat yang
spesifik terhadap kerja enzim, akan dihasilkan reaksi yang menghasilkan warna.
Hasil warna tersebut dapat dilihat secara visual atau diukur dengan menggunakan
kolorimeter atau spektrofotometer. Ciri utama metoda ini adalah menggunakan
suatu indikator enzim untuk reaksi immunologi (Burgess 1995).
Teknik ELISA dapat digunakan untuk pemeriksaan sampel dalam jumlah
banyak, waktu yang singkat dan mempunyai tingkat sensitivitas yang tinggi tetapi
spesifitasnya rendah. Adapun kekurangan teknik ELISA diantaranya sering
menimbulkan reaksi positif palsu, hal ini disebabkan karena antigen standar yang
digunakan umumnya dipropagasi dalam sel kultur, sehingga ada kemungkinan
antibodi dalam serum berikatan dengan epitop-epitop lain yang ada di permukaan
sel kultur. Reaksi silang yang pernah dilaporkan adalah dengan Microbacterium
pneumonia dan Bordetella pertusis (Setiyono et al. 2005; Slaba et al. 2005).
Field et al. (2002) membandingkan dua uji serologis untuk mendiagnosa
Q fever yaitu teknik ELISA dan IFA. Hasil studi tersebut memperlihatkan bahwa
teknik ELISA memberikan sensitivitas 95% dan spesifitas 88%, sedangkan
menggunakan IFA sensitivitas 99% dan spesifitas 98%. Penelitian yang sama juga
dilaporkan Setiyono (2003) bahwa ELISA mempunyai tingkat sensitifitas dan
spesifitas masing-masing 93.8% dan 83.3%. Teknik ELISA baik digunakan untuk
tes skrining dengan jumlah sampel yang banyak dan spesifitasnya dapat
ditingkatkan dengan mengkombinasi IFA. Hasil penelitian yang dilakukan
17
yang berumur antara 10-24 bulan di Turki sejak tahun 2001-2004 dengan
menggunakan uji ELISA Chekit Q fever (Idexx Laboratories, Broomfield, CO,
USA). Penelitian yang sama juga dilakukan oleh Cekani et al. (2008) dengan
teknik ELISA menggunakan Chekit Q fever enzyme immunoassay dan
memperoleh 9.8% seropositif pada domba dan kambing (dari 1085 ekor) serta
7.9% seropositif pada sapi 9 dari 571 ekor di Albania.
Penelitian yang dilakukan terhadap 34 ekor domba menggunakan uji
serologis (ELISA dan IFA) serta uji molekuler (PCR) didapatkan 24% positif
dengan ELISA, 32% positif dengan IFA dan 44% positif dengan PCR. Tujuh ekor
domba yang seronegatif, dilakukan pengujian dengan PCR dan diperoleh hasil
positif, hal ini menunjukkan PCR mempunyai sensitifitas lebih tinggi
dibandingkan uji serologis (Berri et al. 2001). Perbandingan uji serologis dan
molekuler dalam mendiagnosa Q fever fase akut menunjukkan bahwa apabila
serum sampel yang diambil satu sampai dua minggu setelah infeksi dapat
didiagnosa dengan kedua metode uji. Bila diambil pada minggu ketiga sampai
keempat sebaiknya menggunakan uji serologis, sedangkan uji molekuler hanya
untuk mengonfirmasi hasil uji yang seronegatif (Fournier dan Raoult 2003).
Nested Polymerase Chain Reaction (PCR)
Polymerase chain reaction (PCR) ditemukan pertama kali oleh Kary B.
Mullis tahun 1983. PCR adalah teknik yang didasari oleh penggunaan
oligonukleotida pendek sebagai primer dan taq DNA polymerase sebagai enzim
untuk menggandakan sejumlah rangkaian DNA khas C. burnetii pada sampel
yang diperiksa. polymerase chain reaction memiliki tingkat akurasi yang sangat
tinggi untuk deteksi DNA khas C. burnetii pada serum dan leukosit manusia
(Zhang et al. 1998; Ogawa et al. 2004). Mahatmi et al. 2006 melakukan penelitian
dengan menggunakan sampel jantung dan hati untuk melihat C. burnetii pada fase
kronis.
Nested PCR adalah suatu teknik perbanyakan replikasi sampel DNA
menggunakan bantuan enzim DNA polymerase yang menggunakan dua
pasang primer untuk mengamplifikasi fragmen. Pasangan primer yang pertama
umumnya. Pasangan primer yang kedua biasanya disebut nested primers
(sepasang primer tersebut terletak di dalam fragmen pertama) yang berikatan di
dalam fragmen produk PCR yang pertama untuk memungkinkan terjadinya
amplifikasi produk PCR yang kedua dimana hasilnya lebih pendek dari yang
pertama. Nested PCR adalah PCR yang sangat spesifik dalam
melakukan amplifikasi karena jika ada fragmen yang salah diamplifikasi maka
kemungkinan bagian tersebut diamplifikasi untuk kedua kalinya oleh primer yang
kedua sangat rendah (Chauhan et al. 2009).
Nested PCR merupakan variasi dari reaksi polymerase chain reaction biasa
(PCR). Nested PCR dan PCR biasa keduanya berguna untuk memperbanyak
fragmen DNA tertentu dalam jumlah banyak. Pada nested PCR digunakan 2
pasang primer sedangkan pada PCR biasa hanya menggunakan 1 pasang
primer. Oleh karena itu, hasil fragmen DNA dari nested PCR lebih spesifik (lebih
pendek) dibandingkan dengan PCR biasa. Waktu yang diperlukan dalam reaksi
nested PCR lebih lama daripada PCR biasa karena pada nested PCR dilakukan
2 kali reaksi PCR sedangkan pada PCR biasa hanya 1 kali reaksi PCR. Selain itu,
keuntungan nested PCR adalah meminimalkan kesalahan amplifikasi gen dengan
menggunakan 2 pasang primer (Chauhan et al. 2009).
Menurut Louise et al 2001, secara umum, PCR adalah suatu proses
perbanyakan DNA secara in vitro melalui beberapa tahap, yaitu denaturasi,
penempelan primer, dan pemanjangan. Prinsip kerja nested PCR tidak jauh
berbeda dengan PCR biasa, namun nested PCR akan bekerja menggunakan dua
pasang primer untuk mengamplifikasi fragmen DNA spesifik melalui dua proses
PCR secara terpisah. Pertama-tama DNA mengalami denaturasi lalu memasuki
fase penempelan, di mana sepasang primer pertama melekat di kedua utas tunggal
DNA dan mengamplifikasi DNA di antara kedua primer tersebut dan terbentuklah
produk PCR pertama. Kemudian produk PCR pertama tersebut dijalankan pada
proses PCR kedua di mana pasangan primer kedua (nested primer) akan
mengenali sekuen DNA spesifik yang berada di dalam fragmen produk PCR
pertama dan memulai amplifikasi bagian di antara kedua primer tersebut.
Hasilnya adalah sekuens DNA yang lebih pendek daripada sekuens DNA hasil
19
Modifikasi metode Qiao untuk mendeteksi DNA C. burnetii pada telur
ayam ras dan lokal dapat menghasilkan konsentrasi DNA yang cukup dan tingkat
kemurnian DNA yang tinggi. Metode nested PCR mampu mendeteksi DNA
C. burnetii pada konsentrasi ≥ 300 pg. Metode nested PCR mempunyai spesifitas
yang tinggi (concerved) dan 50 kali lebih sensitif dibandingkan dengan PCR biasa
untuk mendeteksi DNA C. burnetii (Purnawarman 2011).
Pencegahan dan Pengendalian
Pencegahan pada hewan dapat dilakukan dengan menggunakan vaksin yang
diproduksi dalam telur berembrio. Plasenta sapi atau domba perlu ditanam atau
dibakar setelah itu di area kelahiran dibersihkan dengan desinfektan (lisol, bleach
atau hidrogen peroksida) untuk mengurangi penularan di lapangan dan hewan
yang bunting atau sedang melahirkan dijaga dari hewan lain.
NNDSS (2003) melaporkan bahwa sejak tahun 2000-2003 dilakukan upaya
pencegahan penyakit ini, yaitu melakukan program vaksinasi Q fever pada pekerja
di industri pengolahan daging dan RPH. Tahun 2001-2004 dilaksanakan vaksinasi
pada hewan ternak dan pekerja di peternakan (ternak potong dan perah).
Penggunaan vaksin Q fever yang aman memerlukan pemeriksaan potensi vaksin
dengan uji dermal, uji serologis atau proliferasi limfosit secara invitro. Kesesuaian
antara strain antigen C. burnetii sebagai bahan vaksin dengan wilayah endemis
sangat berperan terhadap daya perlindungan dan efektifitas vaksinasi.
Vaksin Q fever (Q Vax) dibuat dengan inaktivasi antigen fase I C. burnetii
strain Henzerling yang mengandung antigen kompleks LPS-protein dan
disuntikan secara subkutan dengan dosis tunggal sebesar 30 mikrogram per dosis
(Waag et al. 2002). Vaksin baru dapat diberikan kepada hewan atau manusia
apabila hasil tes serologis tidak ditemukan antibodi terhadap Q fever.
Pengobatan
Penyakit Q fever dapat disembuhkan apabila pengobatan dilakukan sedini
mungkin (Maurin dan Raoult 1999). Pencegahan penyakit Q fever selain vaksinasi
adalah (1) memberikan edukasi pada individu atau kelompok yang berisiko; (2)
dari plasenta, sisa abortan dan fetus; (3) karantina ternak yang akan diimpor; (4)
autoclave dan disinfeksi peralatan laboratorium; (5) pasteurisasi susu pada suhu
lebih dari 62.7 °C selama 30 menit atau 71.6 °C selama 15 detik dan sterilisasi
pada suhu 130 °C selama 5 detik serta pesteurisasi telur pada suhu lebih dari
60 °C selama 6.2 menit atau 61.1 °C selama 3.5 menit dapat membunuh
mikroorganisme C. burnetii (CFSPH 2007; Marrie 2000; Mine 2008)
Antibiotika yang digunakan untuk pengobatan kasus Q fever akut pada
manusia adalah doksisiklin. Penyakit yang kronis pengobatan dapat berlangsung
selama 2-3 tahun. Doksisiklin dan quinolon tidak boleh dipakai untuk ibu hamil.
Ibu hamil dapat diobati dengan antibiotik co-trimoksazol (kombinasi
trimethoprim-sulfametoksazol), namun pengobatan ini dapat menyebabkan
kematian fetus pada beberapa kasus. Seseorang yang sembuh dari Q fever akan
tetap membawa penyakit tersebut selama hidupnya.
Efektifitas pengobatan hewan dengan antibiotik hanya sedikit diketahui.
Pemberian antibiotika (tetrasiklin) ke hewan diberikan melalui air minum.
Antimikroba yang digunakan tidak untuk membunuh hewan yang menjadi karier
tetapi untuk menekan jumlah hewan yang mengalami aborsi. Pengawasan
Q fever yang terbaik di peternakan melalui vaksinasi, seleksi dan pemilihan
BAHAN DAN METODE
Waktu dan Tempat
Penelitian dilaksanakan di Laboratorium Karantina Hewan Balai Besar
Karantina Pertanian Soekarno-Hatta Cengkareng Banten, pada bulan Januari
sampai dengan Mei 2012.
Bahan dan Alat
Bahan penelitian adalah serum dan whole blood sapi perah impor dari
Australia. Bahan untuk uji serologi yaitu kit ELISA (CHEKIT Q-fever (Coxiella
burnetii) Antibody Test Kit, IDEXX, Switzerland) dengan lot number QFT1135T.
Bahan untuk uji nested PCR yaitu Qiagen kit, etanol, nuclease free water (NFW),
10x PCR bufer, MgCl2 50 mM (Vivantis), dNTP 10 mM (Vivantis), taq DNA
polymerase (Vivantis) 5 U/µl, 10x TAE, etidium bromida, 100 pb DNA ladder,
loading dye, DNA C. burnetii sebagai kontrol positif dan Staphylococcus aureus
sebagai kontrol negatif. Primer PCR yang digunakan adalah produk Sigma
(OMP1, OMP2, OMP 3 dan OMP4).
Alat yang dipakai adalah biosafety cabinet, ELISA reader, komputer, DNA
thermal cycler, kamera, vortex, refrigerator, spektrofotometer (NanoVue PlusTM),
microwave, elektroforesis, freezer, UV lumination, inkubator, sentrifus,
multichanel/singel pipet & tip, shaker.
Metode Penelitian
Pra penelitian berupa pemberian kuisioner untuk mengkaji risiko
penyebaran Q Fever ke lingkungan berkaitan dengan sanitasi, higiene personal
Gambar 4 Rancangan penelitian.
Besaran dan Metode Pengambilan Sampel
Pengambilan sampel dilakukan secara acak sederhana (simple random
sampling). Estimasi besaran sampel yang diambil, dihitung menggunakan rumus
Detect Diseases yaitu sebagai berikut (Martin 1987):
n = [1-(1-a)1/D] [N-{(D-1)/2}]
= [1-(1-0,95)1/36.6588] [599-{(36.6588-1)/2}]
= 45.6387
= 46
Keterangan: (a) adalah tingkat konfidensi (95%), (D) adalah jumlah hewan
yang sakit dalam populasi dengan prevalensi 6.12% (Mahatmi 2006), (N) adalah
populasi sapi perah yang diimpor dari Australia selama tahun 2011 yang masuk
melalui Bandar Udara Soekarno-Hatta, (n) adalah besaran sampel. Sapi Perah
Darah
Nested PCR
Serum
Analisa Data secara Deskriptif
ELISA Whole blood
23
Uji Serologis ELISA
Sampel serum dan kontrol diencerkan 1:400 dengan Chekit-wash solution.
100 µl sampel dan kontrol yang telah diencerkan dimasukkan ke dalam sumur
microtiter plate. Mencampur isi dalam sumur dengan cara menggoyang sebentar
microtiter plate secara lembut atau dengan menggunakan shaker. Microtiter plate
diinkubasi selama 60 menit (±5 menit) pada suhu 37 ºC (±2 ºC), setelah itu
dilakukan pencucian dengan 300 µl Chekit-wash solution sebanyak tiga kali.
Dilakukan aspirasi isi cairan di dalam sumur setelah dicuci. Aspirasi terakhir
diketuk-ketuk dengan kuat pada bahan yang mudah menyerap. 100 µl konjugat
Chekit-Q-Fever-Anti-Ruminant-Ig-PO dimasukkan pada setiap sumur. Microtiter
plate ditutup dan diinkubasi selama 60 menit (±5 menit) dengan suhu 37 ºC
(±2ºC) pada ruang yang lembab, setelah itu dilakukan pencucian dengan 300 µl
Chekit-wash solution sebanyak tiga kali. Dilakukan aspirasi isi cairan di dalam
sumur setelah dicuci. Aspirasi terakhir diketuk-ketuk dengan kuat pada bahan
yang mudah menyerap. 100 µl Chekit-TMB-Substrate dimasukkan dalam setiap
sumur. Inkubasi pada suhu ruang (18 ºC-25 ºC) selama 15 menit. Reaksi warna
dihentikan dengan menambahkan 100 µl Chekit-Stop Solution TMB pada setiap
sumur. Stop solution sebaiknya dimasukkan dengan urutan dan kecepatan yang
sama seperti memasukkan substrat. Hasil dibaca dengan fotometer pada panjang
gelombang 450 nm (Gambar 5). Uji yang valid adalah jika OD kontrol positif
tidak lebih dari 2.0 dan OD kontrol negatif tidak lebih dari 0.5. Perbedaan antara
kontrol positif dan negatif harus ≥ 0.3. Hasil dihitung dengan rumus:
OD sample – OD neg
Nilai (%) : X 100%
ODpos – ODneg
Interpretasi hasil ELISA dapat dilihat pada Tabel 2 :
Tabel 2 Interpretasi hasil ELISA
Nilai < 30% ≥30% - <40% ≥40%
Gambar 5 Metode ELISA (CHEKIT Q-fever (Coxiella burnetii) antibody test kit, IDEXX, Switzerland).
Jika hasil sampel yang dicurigai pada pengujian ke dua sama, maka
sebaiknya mengambil sampel yang baru pada hewan yang sama dan diuji lagi.
Jika sampel yang baru hasilnya tetap dicurigai maka secara epidemiologis perlu
dipertimbangkan. Sampel diuji dengan metode yang berbeda.
Identifikasi DNA C. burnetii dengan Metode Nested PCR Ekstraksi DNA (Qiagen Kit)
Sebanyak 20 µl proteinase K dimasukkan ke dalam tabung mikrosentrifus
ukuran 1.5 ml. Sebanyak 50-100 µl darah yang mengandung antikoagulan dan
PBS ditambahkan sampai mencapai volume 220 µl, kemudian 200 µl bufer AL
ditambahkan tanpa tambahan etanol. Homogenisasi dilakukan dengan vortex dan
diinkubasi pada suhu 56 ºC selama 10 menit. Etanol (96-100%) sebanyak 200 µl
ditambahkan ke dalam sampel dan dihomogenkan dengan vortex, kemudian
dipindahkan ke dalam DNeasy mini spin column setelah itu dimasukkan ke dalam
tabung koleksi (collection tube) 2 ml. Sentrifus dilakukan pada 6 000 g (8 000
rpm). Flow through dan tabung koleksi dibuang, kemudian DNeasy mini spin
column ditempatkan pada tabung koleksi. Bufer AW1 sebanyak 500 µl
ditambahkan dan disentrifus selama 1 menit pada 6 000 g (8 000 rpm). Flow
25
pada tabung koleksi, kemudian ditambahkan 500 µl bufer AW2. Sentrifus selama
3 menit pada 20 000 g (14 000 rpm) untuk mengeringkan membran DNeasy. Flow
through dan tabung koleksi dibuang dan DNeasy mini spin column ditempatkan
ke dalam tabung mikrosentrifus ukuran 1.5 ml. Sebanyak 200 µl bufer AE
dipipet ke dalam membran DNeasy. Inkubasi pada suhu ruang selama 1 menit dan
sentrifus selama 1 menit pada 6 000 g (8 000 rpm) untuk mengelusi. Hasil DNA
dapat diperoleh secara maksimal dengan mengulangi elusi seperti langkah
sebelumnya. Hasil DNA yang diperoleh diukur tingkat kemurnian dan
konsentrasinya, kemudian dilanjutkan dengan polymerase chain reaction (PCR).
Spektrofotometer (NanoVue PlusTM)
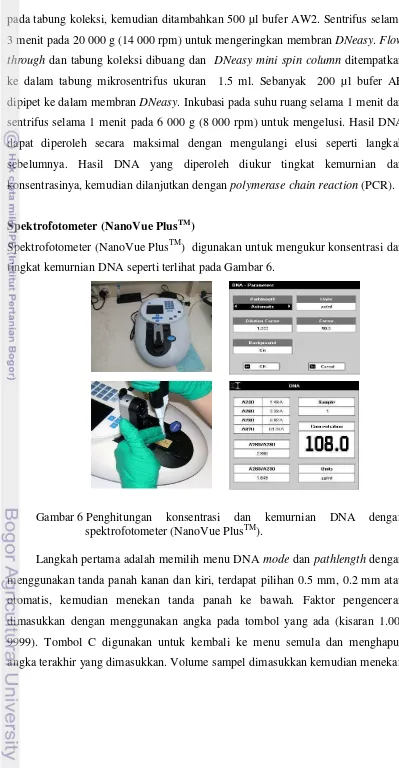
Spektrofotometer (NanoVue PlusTM) digunakan untuk mengukur konsentrasi dan
tingkat kemurnian DNA seperti terlihat pada Gambar 6.
Gambar 6 Penghitungan konsentrasi dan kemurnian DNA dengan spektrofotometer (NanoVue PlusTM).
Langkah pertama adalah memilih menu DNA mode dan pathlength dengan
menggunakan tanda panah kanan dan kiri, terdapat pilihan 0.5 mm, 0.2 mm atau
otomatis, kemudian menekan tanda panah ke bawah. Faktor pengenceran
dimasukkan dengan menggunakan angka pada tombol yang ada (kisaran
1.00-9999). Tombol C digunakan untuk kembali ke menu semula dan menghapus
tanda panah ke bawah dan memasukkan volume diluent. Menekan tanda OK
untuk menghitung faktor pengenceran dan kembali ke parameters screen.
Background correction pada 320 nm akan terlihat, kemudian tanda panah ke
bawah ditekan. Unit pengukuran ada beberapa pilihan yaitu μg/ml, ng/μl dan μg/μl, kemudian tanda panah ke bawah ditekan. Tanda OK ditekan untuk melihat result screen. Sebanyak 2 µl sampel blanko dimasukkan kemudian tanda
QA/100% ditekan, lempeng dibersihkan dengan air dan tisu sebelum memasukkan
sampel berikutnya. Rasio dari nilai absorbansi pada panjang gelombang 1 dan 2
dihitung. Konsentrasi didasarkan pada absorbansi panjang gelombang pertama.
Deteksi C. burnetii pada Darah Sapi dengan Metode Nested PCR
Larutan DNA yang akan digunakan sebagai sampel merupakan hasil
pengukuran konsentrasi dan kemurnian DNA menggunakan spektrofotometer.
Primer oligonukleotida yang digunakan adalah produk Sigma yaitu primer OMP1 (5’-AGT AGA AGC ATC CCA AGC ATT G-3’), OMP2 (5’-TGC CTG CTA GCT GTA ACG ATT G-3’), OMP3 (5’-GAA GCG CAA GAA GAA CAC-3’) dan OMP4 (5’-TTG GAA GTT ATC ACG CAG TTG-3’) yang didisain dari sekuen nukleotida gen com 1 yang mengkode OMP 27 kD.
Amplifikasi DNA pertama (first PCR) dilakukan dalam volume 50 µl yang
berisi 34.25 µl nuclease free water (NFW), 5 µl 10x PCR bufer, 1.5 µl MgCl2 50
mM (Vivantis), 1 µl dNTP 10 mM (Vivantis), 1.5 µl primer OMP1 10 µM, 1.5 µl
primer OMP2 10 µM, 0.25 µl Taq DNA polymerase (Vivantis) dan 5 µl DNA
template. Analisis PCR dilakukan berturut-turut, yaitu suhu 94 ºC, 2 menit
(pre-denaturasi), 1 putaran, kemudian denaturasi pada suhu 94 ºC, 1 menit, pelekatan
(annealing) pada suhu 68 ºC, 1 menit dan pemanjangan (extention) pada suhu
72 ºC, 1 menit selama 35 kali siklus serta suhu 72 ºC, 7 menit dan hold
temperature 4 ºC, 1 putaran dalam DNA thermal cycler. Proses amplifikasi
selama kurang lebih 2.5 jam, setelah selesai siap untuk dilakukan elektroforesis
dan nested PCR.
Amplifikasi kedua (nested PCR) dilakukan dalam volume 50 µl yang berisi
37.25 µl nuclease free water (NFW), 5 µl 10x PCR bufer, 1.5 µl MgCl2 50 mM
27
primer OMP2 10 µM, 0.25 µl Taq DNA polymerase (Vivantis) dan 2 µl amplikon
DNA template dari first PCR. Analisis PCR dilakukan berturut-turut, yaitu suhu
94 ºC, 2 menit (pre-denaturasi), 1 putaran, kemudian denaturasi pada suhu 94 ºC,
1 menit, pelekatan (annealing) pada suhu 57 ºC, 1 menit dan pemanjangan
(extention) pada suhu 72 ºC, 1 menit selama 35 kali siklus serta suhu 72 ºC,
7 menit dan hold temperature 4 ºC, 1 putaran dalam DNA thermal cycler. Setelah
proses amplifikasi selesai kemudian dilakukan elektroforesis.
Produk amplifikasi PCR dianalisa dengan elektroforesis menggunakan 1.5%
gel agarose. Cara pembuatan 1.5% gel agarose yaitu sebanyak 1.5 gram agarose
ditambahkan ke dalam 100 ml x TAE, kemudian dihomogenkan menggunakan
microwave selama 5 menit dan diwarnai dengan etidium bromida (0.5 µg/ml)
selama 30 menit). Setelah cetakan agarose menjadi padat kemudian direndam
dengan 10x TAE, maka ke dalam sumur dimasukkan sampel, kontrol positif,
kontrol negatif dan DNA molecular weight standards (100 pb DNA ladder) yang
telah dicampur loading dye dengan perbandingan 1:9. Elektroforesis dijalankan
dengan tegangan 120 volt selama 50 menit, kemudian dilihat hasilnya
menggunakan UV lumination pada 320 nm dan dipotret dengan kamera. Hasil
PCR dinyatakan positif apabila terlihat adanya produk yang spesifik dari primer
eksternal (OMP1-OMP2) yang menghasilkan fragmen 501 pb dan nested PCR
dari primer internal (OMP3-OMP4) yang menghasilkan fragmen 438 pb.
Beberapa peralatan pengujian nested PCR dapat dilihat pada Gambar 7.
Analisis Hasil
Data yang digunakan untuk kajian Q fever adalah hasil identifikasi
C. burnetii dengan menggunakan uji serologis dengan teknik ELISA dan metode
deteksi spesifik nested PCR. Data dianalisis secara deskriptif dalam bentuk tabel
dan gambar (Mattjik dan Sumertajaya 2002).
HASIL DAN PEMBAHASAN
Q fever merupakan penyakit zoonosa yang sangat infeksius, menyebar luas
hampir di seluruh dunia, menginfeksi orang yang berhubungan dengan
pekerjaannya (occupational hazard) dan dapat ditularkan melalui makanan
(foodborne diseases) (Vaidya et al. 2008). Mikroorganisme ini dilaporkan mampu
menyebar sejauh 18.3-20 km dari sumber infeksi yang dibawa oleh angin (aerosol
transmission), mempunyai dosis infeksi yang rendah (low infectious dose), stabil
di lingkungan dan beberapa kondisi psikokimia (stable in the environment).
Berdasarkan estimasi World Health Organization (WHO) apabila C. burnetii
disebarkan ke suatu wilayah dengan populasi penduduk sebesar 5 juta, maka
125 000 orang akan sakit dan 150 orang meninggal (CFSPH 2007; Marrie 2003).
Data penelitian terhadap keberadaan C. burnetii sebagai penyebab penyakit
Q fever di Indonesia adalah nyata secara serologi dan molekuler, walaupun masih
perlu dibuktikan dengan melakukan isolasi dan identifikasi mikroorganisme
C. burnetii. Q fever termasuk penyakit eksotik di Indonesia, yaitu penyakit
zoonosa yang belum ditemukan atau dilaporkan terjadi di Indonesia (Komnas
2010).
Hasil ELISA
Jumlah sampel yang digunakan dalam penelitian ini adalah 46 sampel yang
terdiri dari 46 sampel serum darah dan 46 sampel darah utuh (whole blood). Hasil
pengujian serologis dengan metode ELISA (CHEKIT Q-fever (Coxiella burnetii)
antibody test kit, IDEXX, Switzerland) memperlihatkan dari 46 sampel serum
darah sapi perah, 23 sampel (50%) positif Q fever sedangkan 23 sampel lainnya
menunjukkan hasil negatif.
Penggunaan metode ini dinyatakan valid jika Optical Density (OD) kontrol
positif tidak lebih dari 2.0 dan OD kontrol negatif tidak lebih dari 0.5, perbedaan
antara kontrol positif dan negatif harus lebih besar atau sama dengan 0.3. Hasil
positif terhadap Q fever pada uji ini apabila nilai (%) sama dengan atau lebih
jika nilai (%) adalah kurang dari 30%. Hasil uji serologi terhadap Q fever dengan
metode ELISA dapat dilihat pada Tabel 3.
Tabel 3 Hasil uji serologi terhadap Q fever dengan metode ELISA
Jenis
Hasil penelitian ini menunjukkan seropositif sebanyak 50% dengan rata-rata
persentasi nilai positif adalah 92.54%. Sampel serum darah sapi perah berasal dari
sapi perah impor dari Australia yang merupakan negara endemis dan pertama kali
ditemukan kasus Q Fever. ELISA (CHEKIT Q-fever (Coxiella burnetii) antibody
test kit, IDEXX, Switzerland) mempunyai sensitifitas 100% dan spesifitas 100%
jika dibandingkan dengan CFT dengan korelasi 98%. ELISA digunakan dalam
diagnosa karena mudah dikerjakan dan handal. Jumlah sampel yang positif
C. burnetii pada pemeriksaan serologis pada umumnya cenderung lebih tinggi jika
dibandingkan dengan pemeriksaan dengan metode PCR. Hewan yang positif
antibodi terhadap C. burnetii pada pemeriksaan serologis adalah hewan yang
telah terinfeksi dalam waktu lama, sementara agen penyebabnya sendiri belum
tentu ada dalam tubuh hewan (Mahatmi et al. 2006).
Sampel serum darah sapi perah berasal dari sapi perah yang diimpor dari
Australia yang merupakan negara endemis dan pertama kali ditemukan kasus
Q Fever. Penelitian terbaru dilakukan oleh Cooper et al. (2011) terhadap sapi
potong di daerah Queensland dengan tingkat insidensi Q fever tertinggi di
Australia, sebanyak 16.8% (SK 95%; 16.7-16.8%) seropositif terhadap Q Fever.
ELISA mempunyai sensitifitas dan spesifitas yang tinggi, hal ini sesuai
dengan penelitian Vaidya et al. (2011) terhadap 920 sampel yang berupa swab
genital dan feses, susu, urin dan serum. Sampel dikoleksi dari 88 ekor sapi, 33
ekor kerbau, 43 ekor domba dan 53 ekor kambing dengan riwayat gangguan
reproduksi dan diskrining terhadap C. burnetii. Sampel diuji dengan trans-PCR,
real-time PCR, IFA, ELISA dan metode isolasi. Prevalensi terhadap Q fever
secara keseluruhan adalah 13.82%, sedangkan untuk masing-masing hewan
prevalensi Q fever pada sapi sebesar 12.78%, kerbau sebesar 16.66%, domba