IRMA ROSIANA ELIZABETH
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Silika dari Sekam oleh
Fusarium oxysporum
. Dibawah bimbingan LAKSMI
AMBARSARI dan YUSMANIAR
Nanopartikel silika memiliki kelebihan diantaranya yaitu, luas permukaan
besar, ketahanan panas, kekuatan mekanik dan inert sehingga digunakan sebagai
prekursor katalis, adsorben, dan filter komposit. Biosintesis merupakan metode
dalam mensintesis nanopartikel melalui sel mikroba dengan melibatkan reaksi
enzimatis. Penelitian ini bertujuan menghasilkan produk biosintesis nanopartikel
silika oleh
F.oxysporum
dengan optimasi fase pertumbuhan dan jumlah substrat
berupa sekam.
F.oxysporum
ditumbuhkan dalam kondisi pH media 4-6, suhu
inkubasi 27ºC, dan sistem aerasi 200 rpm.
Keberadaan enzim ekstraseluler
F.oxysporum
dilihat berdasarkan kemampuannya dalam mereduksi silika yang
terkandung dalam sekam. Jumlah substrat optimum ditentukan dengan dua
perlakuan yaitu 5 gram dan 2.5 gram sekam. Pemanenan biomassa
F.oxysporum
dilakukan pada jam ke-72, yaitu saat sel memasuki fase stasioner berdasarkan
kurva pertumbuhan. Hasil analisis SEM untuk kedua jenis perlakuan jumlah
substrat menunjukkan partikel terlihat beragregat satu dengan lainnya dan
memiliki ukuran partikel relatif tidak berbeda, dengan variasi ukuran antara
200-1000 nm. Tiga puncak tertinggi ditemukan dalam spektrum absorbsi FTIR, yaitu
berada pada 3408.18 cm
-1untuk gugus
H2O, 1639.04 cm
-1untuk gugus CO3
2-, dan
1078.71 cm
-1untuk gugus Si-O-Si. Sekam dengan perlakuan
F.oxysporum
by
Fusarium oxysporum
and Its Characterization. Under supervision of LAKSMI
AMBARSARI and YUSMANIAR.
Silica nanoparticles have many advantages such as large surface, heat
resistance, mechanical strength, and inert. Therefore has been used as a precursor
catalyst, an adsorben, and a composit filter. Biosynthesis is a method to find the
nanoparticles through enzymatical mechanism from microbe. This research aims
to produce the silica nanoparticles by
F.oxysporum
with a phase growth and an
amount of rice husk as substrate optimization.
F.oxysporum
is
grown in a media
pH 4-6, incubation temperature 27ºC, and 200 rpm aeration system. The presence
of extracellular enzymes
F.oxysporum
views based on their ability in reducing the
silica which is contained in the rice husk. The number of optimum substrate is
determined by the two treatments, 2.5 gram and 5 gram of rice husks. The
IRMA ROSIANA ELIZABETH
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Biokimia
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
NIM : G84061307
Disetujui
Komisi Pembimbing
Dr. Laksmi Ambarsari, MS
Yusmaniar, MSi
Ketua
Anggota
Diketahui
Dr. I Made Artika, M. App. Sc.
Ketua Departemen Biokimia
tanggal 17 Februari 1988. Penulis merupakan anak kedua dari dua bersaudara dari
Ibu Indriyani Diah Rahayu dan Ayah Popo Suherman. Pendidikan akademik
penulis dimulai pada tahun 1994 di SDN 10 Cakung Jakarta Timur, kemudian
melanjutkan ketingkat SMP di SMPN 234 Jakarta Timur. Setelah menamatkan
SMA di SMAN 89 Jakarta Timur, penulis melanjutkan kuliah di IPB melalui jalur
USMI (Undangan Seleksi Masuk IPB).
Penulis memilih mayor Biokimia dan Ilmu komunikasi sebagai keahlian
pendukung (minor) pada tingkat kedua. Selama mengikuti perkuliahan, penulis
juga menjadi asisten praktikum untuk sejumlah mata kuliah seperti Biologi dasar,
Pengantar Penelitian Biokimia, Biokimia Klinis, Keteknikan Asam Nukleat dan
Protein, Metabolisme, serta Biokimia Umum. Selain itu, Penulis pernah menjalani
Praktik Lapang di Seksi Vaksin, Bidang Produk Biologi PPOMN, Badan POM
RI.
Laporan Praktik Lapangan: Uji Kontrol Kualitas Vaksin BCG, Sirih Merah
sebagai Obat anti Diabetes Melitus, Pemanfaatan Dedak Padi sebagai Pencegahan
Hiperlipidemia, dan Sup Instan Singkong merupakan beberapa karya ilmiah yang
hidayah-Nya sehingga penulis dapat menyelesaikan penelitian dan karya ilmiah
mengenai Biosintesis dan Karakterisasi Nanopartikel Silika dari Sekam oleh
Fusarium oxysporum
. Penelitian ini telah berlangsung selama 6 bulan dari bulan
Maret hingga Agustus 2010. Tempat penelitian dilaksanakan di Laboratorium
Biokimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian
Bogor.
Penulis menyampaikan rasa terima kasih kepada Dr. Laksmi Ambarsari, MS
dan Yusmaniar, MSi selaku dosen pembimbing yang telah mengarahkan penulis
dalam penelitian ini. Tidak lupa pula penulis sampaikan ucapan terima kasih
kepada seluruh staf laboran di Laboratorium Biokimia atas bantuan yang telah
diberikan. Ucapan terima kasih yang paling besar penulis sampaikan kepada
kedua orang tua, mama dan aa Teten atas kasih sayang dan do
’
a yang tiada henti.
Karya ilmiah ini juga di dedikasikan untuk papa. Terima kasih juga untuk seluruh
keluarga di Cengkareng untuk mami Ina, papa Didi, mba Pipi, mba Dede, mami
Yanli, om Rudy, dan ka Iwan, untuk keluarga di Bandung, teman-teman Biokimia
43, untuk sahabat-sahabat di Ponah, Ratna Idola, Sheila, Sifa, Indri, Yuli, Evi,
Shabrina, Erni, dan Riri, serta semua Guru, keluarga, dan sahabat yang tidak bisa
disebutkan satu persatu,
atas do’a,
ilmu, dukungan, perhatian dan kasih sayangnya
selama ini.
Karya ilmiah ini tidak lepas dari kekurangan, sehingga penulis mengharapkan
adanya kritik dan saran dari pembaca. Akhir kata penulis berharap semoga skripsi
ini dapat bermanfaat bagi semua pihak.
Bogor, Januari 2011
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN ... x
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Nanoteknologi dan Nanopartikel ... 2
Biosintesis Nanopartikel ... 3
Fusarium Oxysporum
... 4
Pertumbuhan Sel Kapang ... 5
Silika (SiO2) dan Sekam ... 6
Metode Analisis Nanopartikel Silika ... 7
BAHAN DAN METODE
Bahan dan Alat ... 9
Metode Penelitian ... 9
HASIL DAN PEMBAHASAN
Hasil Peremajaan dan Penumbuhan Isolat Cair
Fusarium oxysporum
...10
Kurva Pertumbuhan dan Hasil Pemanenan Isolat
Fusarium oxysporum
...12
Nanopartikel Silika sebagai Hasil Biosintesis oleh
F.oxysporum
...13
SIMPULAN DAN SARAN
Simpulan ...17
Saran ...17
DAFTAR PUSTAKA ... 17
1 Mekanisme reduksi biosintesis nanopartikel Ag. ... 3
2
Fusarium oxysporum
. ... 5
3 Spora Aseksual
Fusarium oxysporum
. ... 5
4 Pertumbuhan spora kapang. ... 6
5 Kurva pertumbuhan fungi. ... 6
6 Pemrosesan padi ... 7
7 Skema kerja SEM. ... 8
8 Skema kerja FTIR. ... 9
9 Skema kerja XRD ... 9
10
F.oxysporum
berumur 4 hari dalam media PDA ... 11
11 Pengamatan mikroskopis
F. oxysporum
perbesaran 10x10. ... 11
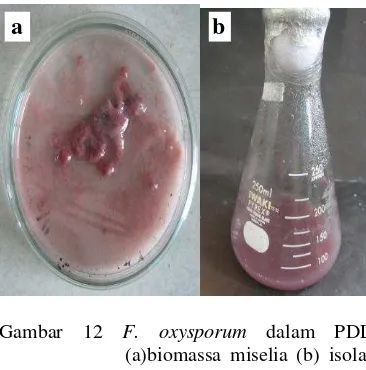
12
F. oxysporum
dalam PDL ... 11
13 Kurva pertumbuhan
F.oxysporum
. ... 12
14 Proses pemurnian. ... 14
15 Hasil analisis SEM nanopartikel silika dengan 5 gram sekam. ...14
16 Hasil analisis SEM sekam tanpa perlakuan
F.oxysporum
. ...14
17 Hasil analisis SEM silika gel perbesaran 1000 x. ... 14
18 Hasil analisis FTIR. ...15
19 Hasil analisis SEM nanopartikel silika dengan 2.5 gram sekam ...16
20 Puncak difraksi nanopartikel silika kristalin (
crystoballite)
. ... 16
21 Puncak difraksi sekam tanpa perlakuan
F.oxysporum.
... 16
Halaman
1 Komposisi media PDA dan media PDL ...21
2 Bagan alur pembuatan media ... 22
3 Bagan alur proses ... 23
4 Biosintesis nanopartikel ... 24
5 Pertumbuhan
F.oxysporum
... 25
6 Data kurva pertumbuhan ... 26
yang melibatkan partikel dengan dimensi
ukuran 100 nm atau kurang, yaitu
nanopartikel. Studi mengenai nanopartikel khususnya nanopartikel logam saat ini sedang berkembang pesat dan mendapat perhatian
yang lebih dari para peneliti karena
pemanfaatan yang luas dalam menciptakan teknologi baru di bidang kimia, elektronika, kesehatan, dan bioteknologi (Marlina 2008;
Moghaddam 2010). Nanopartikel silika
memiliki beberapa sifat diantaranya, luas permukaan besar, ketahanan panas yang baik, kekuatan mekanik yang tinggi, dan inert sehingga digunakan sebagai prekursor katalis (Benvenutti dan Yoshitaka 1998), sebagai adsorben (Kalapathy et al. 2000), dan sebagai filter komposit (Jamarun et al. 1997).
Berbagai metode dikembangkan dalam sintesis nanopartikel. Secara umum, diketahui terdapat 3 metode utama yang dikembangkan dalam sintesis nanopartikel. Metode sintesis tersebut diantaranya adalah sintesis secara kimia, sintesis fisika, dan sintesis secara biologi. Metode sintesis nanopartikel silika secara fisika dan kimia telah dilakukan Hadiyawarman et al. (2008) dan Fatmawati
(2010). Hadiyawarman et al. (2008)
menggunakan metode simple mixing, yaitu dengan menggunakan resin berupa suatu polimer epoxy dan perlakuan suhu. Metode ini memerlukan perlakuan yang lebih sulit,
yaitu seperti suhu, waktu pemanasan,
pengadukan, dan penggunaan resin kimiawi. Proses yang berlangsung sangat sensitif terhadap lingkungan, bila nanosilika yang dibuat memiliki kontak langsung dengan lingkungan pada saat perlakuan pengadukan menggunakan mixer, maka tidak terbentuk nanopartikel yang baik (Hadiyawarman et al.
2008). Fatmawati (2010) memerlukan suhu 850ºC dalam waktu 6 jam untuk mengubah sekam padi menjadi nanopartikel silika, namun demikian hasil yang didapat adalah
silika berukuran mikrometer kemudian
dilanjutkan dengan perlakuan fisik dan kimia.
Perlakuan fisik miling selama 36 jam
menghasilkan nanopartikel silika kristalin 32.377 nm dan perlakuan kimia dengan
presipitasi HCL-NaOH menghasilkan
nanopartikel silika berukuran 31.375 nm.
Biosintesis dipertimbangkan sebagai
metode alternatif tanpa perlakuan sulit dalam sintesis nanopartikel selain metode sintesis
secara kimia dan fisika. Proses ini
berlangsung ramah terhadap lingkungan,
merupakan pengembangan teknologi baru dengan menghasilkan nanopartikel melalui sel mikroba dengan melibatkan reaksi enzimatis (Moghaddam 2010).
Beberapa mikroorganisme memiliki
kemampuan untuk melakukan sintesis
nanopartikel logam, baik eukariot maupun
prokariot. Prokariot yang memiliki
kemampuan tersebut adalah bakteri, seperti
Pseudomonas aeruginosa dan Eschericia coli.
Eukariot yang mampu mensintesis
nanopartikel adalah fungi dan alga. Jenis fungi yang dapat digunakan adalah Fusarium oxysporum dan alga yang dapat digunakan
adalah Sargassum wightii (Moghaddam
2010).
Fusarium oxysporum dilaporkan sebagai mikroorganisme dengan penanganan yang lebih mudah bila dibandingkan dengan mikroorganisme lain (Moghaddam 2010).
Fusarium oxysporum dapat digunakan untuk menghasilkan nanopartikel logam. Fungi tersebut dapat bertahan dan tumbuh dalam konsentrasi ion logam yang tinggi, sehingga memiliki ketahananan untuk melawan kondisi
ekstrim dalam sintesis nanopartikel.
Biosintesis nanopartikel logam dilakukan dengan menggunakan perangkat yang terdapat pada fungi tersebut (Duran et al. 2005).
Fusarium oxysporum mampu
menghasilkan enzim, toksin, polisakarida, dan antibiotik secara ekstraseluler (Bilgrami dan
Dube 1976 dalam Sari 2006). Fusarium
oxysporum dikenal sebagai fungi penyebab penyakit layu pembuluh dan bersifat patogen bagi sebagian tanaman akibat toksin yang dikeluarkan (Efendi et al. 2008). Enzim
ekstraseluler spesifik yang dihasilkan
Fusarium oxysporum mampu menciptakan mekanisme dalam sintesis nanopartikel logam dengan mereduksi substrat dalam proses sintesis nanopartikel logam (Duran et al
2005).
Pemanfaatan Fusarium oxysporum untuk
biosintesis nanopartikel logam sedang
berkembang. Fusarium oxysporum dapat
digunakan untuk biosintesis nanopartikel perak berukuran 20-50 nm (Duran et al. 2002), nanopartikel emas (Mukherjee 2002), serta nanopartikel titania dan silika berukuran 5-15 nm (Bansal et al. 2005). Bansal et al. (2005) memanfaatkan bahan alam berupa pasir untuk sintesis nanopartikel silika. Keberadaan silika (SiO2) dalam tanaman
Padi (Oryza sativa) yang merupakan anggota keluarga gramineae diketahui mengandung silika. Soepardi (1982) mengatakan bahwa kandungan silika tertinggi padi terdapat pada sekam. Sekam padi dapat digunakan sebagai
sumber substrat dalam biosintesis
nanopartikel silika (SiO2). Sekam padi adalah
bahan pertanian berbasis limbah yang murah
dan kaya akan sejumlah silika. Proses
penggilingan gabah akan menghasilkan 16,3-28% sekam dan sebanyak 16.98% silika terkandung dalam sekam (Balai Penelitian Pasca Panen Pertanian 2001). Material anorganik silika yang terkandung dalam
sekam, berada dalam bentuk dasar
(amorphous silica) (Bansal 2006).
Sintesis silika secara kimia dan fisika tidak hanya mahal dan membahayakan lingkungan, tetapi juga membutuhkan kondisi yang lebih sulit, yaitu perlakuan temperatur, tekanan, dan pH ekstrim. Penelitian mengenai pemanfaatan sekam yang merupakan limbah pertanian sebagai sumber substrat silika oleh Fusarium oxysporum dan biotransformasinya menjadi nanopartikel silika kristalin belum banyak dilakukan. Penelitian mengenai biosintesis nanopartikel silika dari sekam oleh Fusarium oxysporum perlu dilakukan.
Penelitian ini bertujuan menghasilkan produk biosintesis berstruktur silika kristalin dan berbentuk nanopartikel silika dengan optimasi fase pertumbuhan dan jumlah substrat. Karakterisasi nanopartikel silika berdasarkan ukuran untuk analisis SEM (Scanning Electron Microscope), komposisi
kimiawi untuk analisis FTIR (Fourier
Transformer Infrared Spectroscopy), dan
struktur untuk analisis XRD (Xray
Difraction). Hipotesis penelitian ini adalah terdapat enzim ekstraseluler F.oxysporum
yang dapat mereduksi silika dari sekam padi dan karakterisasi produk biosintesis berupa silika berukuran nano. Hasil penelitian ini diharapkan dapat digunakan sebagai data awal
dalam optimasi perlakuan biosintesis
nanopartikel silika dari sekam oleh
F.oxysporum dan dilanjutkan ke skala produksi yang lebih besar.
TINJAUAN PUSTAKA
Nanoteknologi dan Nanopartikel
Konsep nanoteknologi pertama kali
diperkenalkan oleh seorang ahli Fisika bernama Richard P. Feyman dalam suatu kuliah perkumpulan ahli Fisika di Amerika pada tahun 1979. Eric Drexler kemudian
memperkenalkan konsep nanoteknologi
kepada masyarakat luas melalui buku yang bejudul Engines of Creation pada pertengahan tahun 1980 (Park 2007).
Website resmi NASA memberikan definisi mengenai nanoteknologi, yaitu merupakan
teknologi dalam pembentukan bahan
fungsional, sumber, dan sistem melalui pengaturan berdasarkan skala atau ukuran (1-100 nm) dan didapatkan dengan pemanfaatan fenomena umum, secara fisika, kimia, serta biologi dalam skala yang lebih besar.
Nanoteknologi didefinisikan sebagai
teknologi dalam skala atom dengan dimensi kurang dari 100 nanometer dalam kamus bahasa inggris Oxford. Kata depan nano- berasal dari bahasa yunani, yang berarti satu nanometer sama dengan 10-9 meter. Produk yang dihasilkan dalam pemrosesan melalui nanoteknologi berdasarkan ukuran partikel dan berdasarkan definisi sebelumnya adalah nanopartikel. Nanopartikel dianggap sebagai bahan dengan dimensi ukuran kurang dari 100 nm. Luas permukaan nanopartikel dibuat sangat besar sehingga ukuran partikelnya menjadi sangat kecil, yaitu kurang dari 100 nm. Luas permukaan menentukan ukuran, struktur, dan ukuran agregasi partikel (Park 2007).
Nanopartikel dapat dihasilkan dalam tiga bentuk yaitu: (1) nanopartikel alami, (2)
nanopartikel antropogenik, dan (3)
nanopartikel buatan. Nanopartikel alami terbentuk secara sendirinya serta mencakup bahan yang mengandung nanokomponen dan kemungkinan ditemukan di atmosfir seperti garam laut yang dihasilkan oleh evaporasi air laut kedalam bentuk spray air, debu tanah, abu vulkanik, sulfat dari gas biogenik, dan bahan organik dari gas biogenik. Kandungan dari masing-masing nanopartikel alami tersebut di dalam atmosfer bergantung kepada kondisi bumi. Nanopartikel antropogenik merupakan nanopartikel yang terbentuk secara kebetulan dihasilkan dalam bentuk bahan bakar fosil. Nanopartikel antropogenik lain berada dalam bentuk asap dan partikulat yang dihasilkan dari oksidasi gas, seperti sulfat dan nitrat. Sedangkan, nanopartikel buatan merupakan nanopartikel yang dibentuk untuk tujuan tertentu dan kemungkinan ditemukan dalam satu atau beberapa bentuk yang berbeda (Lead 2007; Park 2007).
dimanfaatkan dalam berbagai bidang aplikasi (Park 2007).
Nanopartikel digunakan melalui
pemanfaatan yang luas untuk menemukan teknologi baru di bidang kimia, elektronika, kesehatan, dan bioteknologi. Nanopartikel, khususnya nanopartikel logam dimanfaatkan dalam berbagai aplikasi, seperti antimikroba, optika, elektronika, biomedis, biosensor, biolabel, biofiltrasi, magnetika, mekanika,
katalis, bioremediasi, pereduksi limbah
industri, dan sumber energi (Marlina 2008; Moghaddam 2010). Aplikasi tersebut juga termasuk pembuatan baterai, remediasi tanah, dan bahan pembuatan peledak (Park 2007). Aplikasi nanopartikel yang luas berimplikasi
dengan banyaknya metode yang
dikembangkan dalam sintesis nanopartikel logam.
Biosintesis Nanopartikel
Secara umum, diketahui terdapat 3 metode utama yang dikembangkan dalam sintesis nanopartikel logam, diantaranya sintesis secara kimia, sintesis fisika, dan sintesis secara biologi (Moghaddam 2010). Sintesis nanopartikel secara biologi (biosintesis) dipertimbangkan sebagai metode paling baik
dalam membuat nanopartikel, daripada
metode sintesis secara kimia dan fisika. Hal tersebut dikarenakan sintesis nanopartikel secara biologi memiliki nilai pemanfaatan dan
komersil yang lebih tinggi, memiliki
simpanan reduktan yang banyak, energi yang dikeluarkan lebih sedikit, serta nilai produksi yang tinggi. Produksi nanopartikel dalam skala besar dengan menggunakan metode kimia dan fisik biasanya menghasilkan partikel yang lebih besar dalam ukuran mikrometer, metode sintesis nanopartikel
secara biologi dapat menghasilkan
nanopartikel yang baik dalam skala besar. Biosintesis juga merupakan metode yang lebih disarankan daripada kedua metode lainnya karena prosesnya bersifat bersih, nontoksik, murah, dan ramah lingkungan. Pertimbangan perlakuan kondisi juga perlu
diperhatikan, bahwa metode fisika
memerlukan temperatur tinggi dan metode kimia membutuhkan tekanan tinggi. Hal
tersebut menandakan metode sintesis
nanopartikel secara fisik dan kimia
memerlukan kondisi yang lebih sulit
dibandingkan dengan biosintesis nanopartikel (Moghaddam 2010).
Biosintesis nanopartikel merupakan
pengembangan teknologi baru dengan
menghasilkan nanopartikel logam dari sel mikroba serta melibatkan reaksi enzimatis.
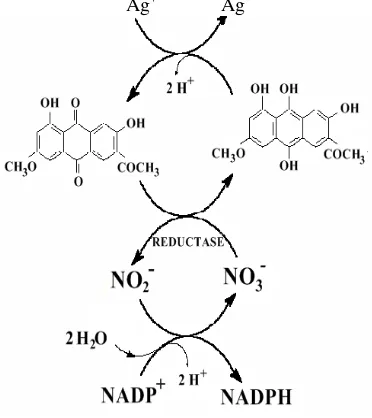
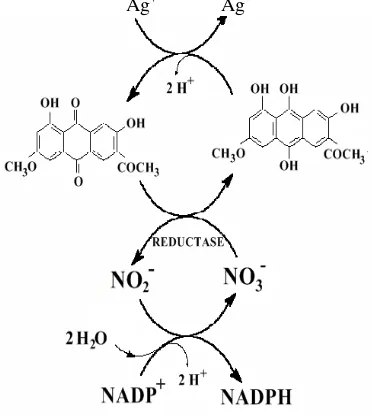
Biosintesis nanopartikel berlangsung dalam mekanisme khusus yang bervariasi meliputi, sistem efluksi, reaksi oksidasi-reduksi, bioabsorpsi, bioakumulasi, presipatsi logam, dan sistem transport spesifik logam. Salah satu mekanisme untuk membuat nanopartikel logam, adalah dengan menggunakan enzim spesifik yang dapat mereduksi, seperti NADH reduktase (Moghaddam 2010).
Assay protein dalam biosintesis
nanopartikel Ag menunjukkan bahwa NADH reduktase diketahui sebagai enzim yang terlibat dalam proses biosintesis nanopartikel logam dan merupakan faktor penting yang bertanggung jawab dalam proses biosintesis. Reduktase memperoleh elektron dari NADH
dan mengoksidasinya menjadi NAD+,
kemudian reduktase mereduksi NO3- menjadi
NO2-. Enzim ini di dalam F.oxysporum
berkonjugasi dengan donor elektron bernama anthraquinon. Enzim ini kemudian mereduksi ion logam dan mengubahnya menjadi bentuk
lain (Gambar 1) (Duran et al. 2005;
Moghaddam 2010).
Enzim reduktase yang dihasilkan
F.oxysporum dalam biosintesis nanopartikel silika bersifat spesifik, F.monoliforme tidak
menghasilkan enzim ekstraseluler yang
dipergunakan dalam biosintesis nanopartikel silika (Bansal et al. 2002). Nanopartikel silika yang terbentuk kemungkinan adalah produk dari pertukaran elektron oleh reduktase spesifik F.oxysporum. Biosintesis dengan
mempergunakan enzim ekstraseluler ini
berlangsung dalam beberapa menit, sehingga biosintesis dapat menghasilkan nanopartikel dalam proses yang cepat (Duran et al. 2005; Moghaddam 2010).
Ag+ Ag
Berdasarkan enzim pereduksi yang
dihasilkan mikroba, teknik biosintesis
nanopartikel logam diklasifikasikan menjadi biosintesis intraseluler dan biosintesis ekstraseluler. Biosintesis secara intraseluler
melaksanakan proses sintesis yang
berlangsung di dalam sel. Proses detoksifikasi logam berbahaya dimediasikan oleh suatu reaksi enzimatis yang berlangsung melalui bioreduksi. logam dan terjadi di dalam sel. Melalui mekanisme tersebut, nanopartikel didapatkan dari sel dengan metode tertentu (Moghaddam 2010).
Proses reduksi tidak terjadi di dalam sel mikroba pada biosintesis ekstraseluler dari
nanopartikel logam. Pereaksi biologis
dibutuhkan untuk bioreduksi dalam bentuk biolikuid. Enzim yang berperan dalam bioreduksi disekresikan keluar sel. Air yang telah menyimpan biomassa selama sehari
digunakan dalam metode biosintesis
ekstraseluler. Pereaksi biologis berupa enzim dibebaskan oleh biomassa kedalam air steril. Air steril yang mengandung enzim tersekresi digunakan sebagai reduktan untuk mereduksi ion logam dan menciptakan nanopartikel logam (Moghaddam 2010).
Biosintesis ekstraseluler memiliki dua keuntungan. Proses tambahan diperlukan untuk mendapatkan nanopartikel yang berada dalam biomassa dalam metode intraseluler, yaitu dengan ultrasound atau reaksi kimiawi dengan menggunakan detergen. Biosintesis ekstraseluler tidak perlu dilakukan proses tersebut. Biosintesis ekstraseluler dianggap
sebagai proses yang lebih murah.
Keuntungan-keuntungan tersebut yang
membuat metode biosntesis ekstraseluler, lebih banyak digunakan bagi pengembangan proses ekstraseluler dalam biosintesis logam (Moghaddam 2010).
Beberapa mikroorganisme memiliki
kemampuan dalam mensintesis nanopartikel logam, baik eukariot maupun prokariot. Prokariot yang memiliki kemampuan tersebut adalah bakteri. Sedangkan mikroorganisme
eukariot yang mampu mensintesis
nanopartikel adalah fungi dan alga. Meskipun banyak mikroorganime yang dapat digunakan,
fungi F.oxysporum dilaporkan sebagai
mikroorganisme dengan penanganan yang lebih mudah bila dibandingkan dengan mikroorganisme lain (Moghaddam 2010).
Fusarium Oxysporum
Fungi adalah organisme dengan sel-sel berinti sejati (eukariot), biasanya berbentuk benang, bercabang-cabang, tidak berklorofil,
dan dinding selnya mengandung kitin serta
selulosa. Fungi merupakan organisme
heterotrof, absortif, dan membentuk beberapa macam spora. Bagian vegetatif fungi biasanya berupa benang-benang yang disebut sebagai hifa. Kumpulan benang-benang hifa disebut miselium. Fungi dapat bereproduksi aseksual
melalui spora aseksual (konidia) dan
reproduksi seksual melalui spora seksual. Berdasarkan sistem reproduksinya, fungi dibedakan atas beberapa kelas, diantaranya askomikotina, basidiomikotina, oomikotina, dan deuteromikotina (Semangun 1996 dalam Sari 2006).
Deuteromikotina merupakan cendawan tingkat tinggi yang mempunyai hifa bersekat. Jenis fungi ini memiliki karakteristik dengan tidak diketahui siklus reproduksi seksualnya, sehingga dikenal dengan fungi imperfek.
Salah satu fungi yang tergolong
deuteromikotina adalah Fusarium sp
(Semangun 1996 dalam Sari 2006).
Fusarium oxysporum masuk kedalam kelas Deuteromikotina, ordo Hypomiseta atau
Monilia. Fusarium oxysporum masuk
kedalam famili Tuberkulariceae dengan letak
konidia pada sporodochium. Fusarium
oxysporum juga termasuk kedalam kelompok Fragmonospora, yaitu memiliki konidia satu atau lebih, berseptat, bening atau berwarna,
dan berbentuk sabit atau kumparan
(Thompson dan Lim 1995 dalam Sari 2005). Fusarium oxysporum yang merupakan spesies yang dapat tumbuh dalam lingkung anaerob ini biasanya ditumbuhkan pada medium PDA (Potato Dextrose Agar) dan dapat mencapai diameter 3.5-5.0 cm. Miselia tampak banyak seperti kapas, kemudian menjadi seperti beludru, berwarna putih atau salem dan biasanya sedikit keunguan yang tampak lebih kuat dekat permukaan medium (Gandjar et al.1999) (Gambar 2).
Fusarium oxysporum dalam siklus
hidupnya mengalami fase patogenesa dan saprogenesa atau merupakan saprofit tanah tetapi dapat bersifat patogen bagi banyak tumbuhan. Fungi ini hidup sebagai parasit pada tanaman inang yang masuk melalui luka akar, kemudian patogen berkembang dalam jaringan tanaman. Spesies ini dapat diisolasi dari biji atau serealia, kacang tanah, kacang kedelai, buncis, kapas, pisang, umbi bawang, kentang, jeruk, apel, dan bit (Gandjar et al.1999).
Fusarium oxysporum menghasilkan
beberapa macam bentuk spora aseksual yaitu,
makrokonidia, mikrokonidia, dan
merupakan bentuk spora yang yang paling sering dihasilkan dalam semua keadaan. Spora ini bersepta 0 hingga 2, terbentuk lateral pada fialid yang sederhana, atau terbentuk pada
fialid yang terdapat pada konidiofor
bercabang pendek, umumnya terdapat dalam jumlah banyak sekali, terdiri dari aneka bentuk dan ukuran, berbentuk elips sampai silindris, lurus atau sedikit bengkok, dan
berukuran (5.0x12.0)x(2.2-3.5) μm.
Makrokonidia merupakan spora yang sangat khas terdapat pada galur Fusarium sp. Makrokonidia terbentuk pada fialid yang terdapat pada konidiofor bercabang, bersepta 3-5, berbentuk fusiform, sedikit membengkok, meruncing pada kedua ujungnya dengan sel kaki berbentuk pediselata, umumnya bersepta 3, dan berukuran (20)27-(46)50x3.0-4.5(5)
μm. Klamidospora terdapat dalam hifa atau dalam konidia, berwarna hialin, berdinding halus atau sedikit kasar, berbentuk semibulat dengan diameter 5.0-15 μm., terletak terminal atau interkalar, dan berpasangan atau tunggal (Booth 1971).
Gambar 2 Fusarium oxysporum.
Gambar 3 Spora Aseksual Fusarium
oxysporum (a) makrokonidia (b) konidiofor (c) fialid (d)
mikrokonidia (e)
Khlamidospora.
Fusarium oxysporum mampu
menghasilkan enzim, toksin, polisakarida, dan antibiotik secara ekstraseluler (Bilgrami dan
Dube 1976 dalam Sari 2006). Fusarium
oxysporum dikenal sebagai fungi penyebab penyakit layu pembuluh dan bersifat patogen bagi sebagian tanaman akibat toksin yang dikeluarkan (Efendi et al. 2008). Enzim
spesifik disekresikan oleh Fusarium
oxysporum diluar sel (ekstraseluler). Enzim yang ekstraseluler tersebut dapat mereduksi substrat tertentu (Sari 2006).
Pertumbuhan Sel Kapang
Definisi pertumbuhan didalam sudut
pandang mikrobiologi adalah pertambahan volume sel karena adanya pertambahan
protoplasma dan asam nukleat yang
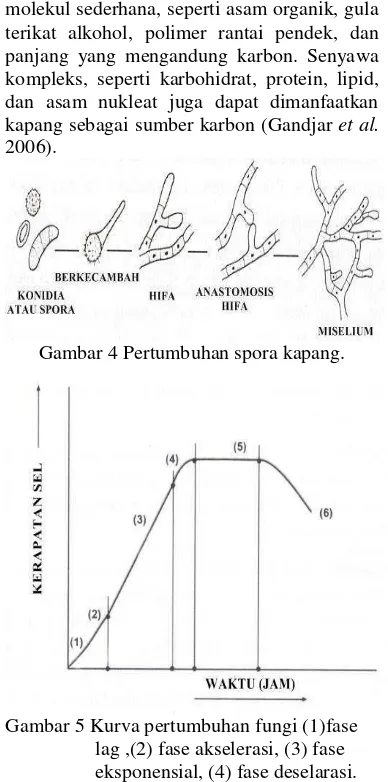
melibatkan sintesis DNA dan pembelahan mitosis (Gandjar et al. 2006). Pertumbuhan volume sel tersebut bersifat irreversibel, artinya tidak dapat kembali ke volume semula. Benang-benang hifa yang terbentuk membuktikan terjadi pertumbuhan pada suatu sel kapang (Gandjar et al. 2006).
Pertumbuhan sel kapang berawal dari sesuatu yang semula tidak terlihat, yaitu suatu spora atau konidia, menjadi benang-benang hifa (Gambar 4). Benang-benang hifa yang dapat terlihat secara makroskopik disebut miselium. Miselium menyebabkan timbulnya kekeruhan pada media cair dalam waktu tertentu. Kekeruhan media berbanding lurus dengan pertambahan biomassa miselium kapang dan dapat digambarkan dengan kurva pertumbuhan (Gandjar et al. 2006).
Kurva pertumbuhan diperoleh dengan menghitung kekeruhan media dalam waktu
tertentu. Kurva pertumbuhan umumnya
melewati beberapa fase, antara lain: (1) fase lag, (2) fase akselerasi, (3) fase eksponensial, (4) fase deselerasi, (5) fase stasioner, dan (6) fase kematian (Gambar 5). Fase-fase yang dilewati suatu sel dalam kurva pertumbuhan
tersebut dapat memberikan informasi
mengenai faktor-faktor lingkungan yang mempengaruhi pertumbuhan suatu biomassa sel kapang di dalam media, seperti suhu
optimum, derajat keasaman optimum,
perlakuan substrat, dan aerasi. Selain itu, informasi mengenai waktu saat enzim-enzim ekstraseluler dikeluarkan untuk menguraikan senyawa-senyawa kompleks serta nutrien-nutrien juga dapat diketahui (Gandjar et al.
2006).
yang diperlukan. Secara umum, nutrien yang diperlukan dalam bentuk karbon, nitrogen, sulfur, fosfor, kalium, magnesium, natrium, kalsium, natrium mikro (besi, mangan, zinc, kobalt, molibdenum) dan vitamin. Karbon menempati posisi yang unik karena semua organisme hidup memiliki karbon sebagai salah satu pembangun tubuh (Gandjar et al.
2006).
Kapang adalah mikroorganisme heterotrof karena tidak memiliki kemampuan untuk mengoksidasi senyawa karbon. Senyawa karbon yang dapat dimanfaatkan kapang untuk membuat materi sel baru berkisar dari molekul sederhana, seperti asam organik, gula terikat alkohol, polimer rantai pendek, dan panjang yang mengandung karbon. Senyawa kompleks, seperti karbohidrat, protein, lipid, dan asam nukleat juga dapat dimanfaatkan kapang sebagai sumber karbon (Gandjar et al.
2006).
Gambar 4 Pertumbuhan spora kapang.
Gambar 5 Kurva pertumbuhan fungi (1)fase lag ,(2) fase akselerasi, (3) fase eksponensial, (4) fase deselarasi. (5) fase stasioner, (6) fase kematian.
Silika (SiO2) dan Sekam
Silika merupakan material yang tersedia di alam dan secara kuantitatif memiliki jumlah yang melimpah. Tanaman berperan secara signifikan dalam siklus biogeokimia silika. Silika berada di dalam tanah berbentuk silika larut air (H4SiO4). Tanaman menyerap silika,
dipolimerisasi dan dipresipitasi menjadi
bentuk silica amorphous. Beberapa
karbohidrat dan protein tanaman diketahui memiliki peran dalam polimerisasi biosilika
menjadi bentuk silica amorphous sama
dengan bentuk silika yang terdapat di biosfer. Tanaman mati akan meninggalkan silika kembali kedalam tanah dan berlangsung aktivitas mikrobial (Soepardi 1982).
Silika terakumulasi dalam bentuk phytolit
yang merupakan bentuk primer dari silica amorphous (SiO2 dengan 5-15% H2O).
Berbagai jenis tanaman baik dikotil maupun
monokotil memproduksi phytolit. Jenis
tanaman dikotil yang memprodukisi phytolit
diantaranya mytaceae, casuarinaceae,
proteaceae, xantorhoeceae, dan mimosceaee. Jenis tanaman monokotil yang memproduksi
phytolit adalah equistaceae dan gramineae (Bansal 2006).
Keberadaan silika (SiO2) dalam tanaman
gramineae telah diketahui sejak tahun 1938. Padi (Oryza sativa) yang merupakan anggota
keluarga gramineae dan diketahui
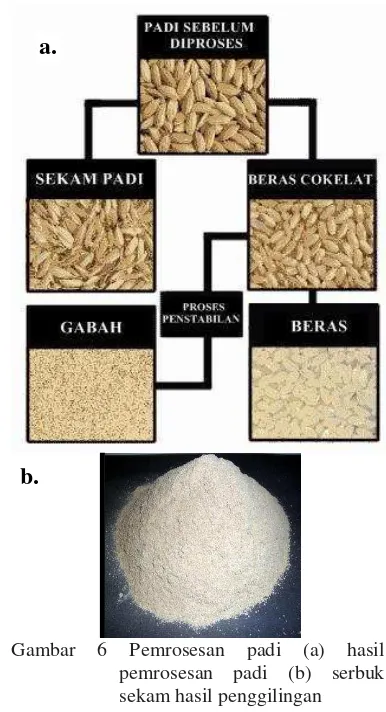
mengandung silika. Menurut Soepardi (1982), kandungan silika tertinggi pada padi terdapat pada sekam bila dibandingkan dengan bagian tanaman padi lain seperti helai daun, pelepah daun, batang, dan akar. Sekam dalam padi (gramineae) merupakan lapisan keras yang membungkus kariopsis butir gabah, terdiri atas dua belahan yang disebut lemma dan palea yang saling bertautan. Sekam akan terpisah dari butir beras dan menjadi bahan sisa pertanian atau limbah penggilingan pada proses penggilingan padi (Bansal 2006)
(Gambar 6). Proses penggilingan gabah akan dihasilkan 16,3-28% sekam. Sekam dikategorikan sebagai biomassa yang dapat digunakan untuk berbagai kebutuhan seperti bahan baku industri, pakan ternak, dan energi
(Balai Penelitian Pasca Panen Pertanian 2001).
Ditinjau dari komposisi kimiawinya, sekam mengandung beberapa unsur penting seperti terlihat pada Tabel 1. Sebanyak 16.98% silika terkandung dalam sekam. Material anorganik silika yang terkandung dalam sekam, berada dalam bentuk dasar (amorphous silica) (Balai Penelitian Pasca
Panen Pertanian 2001; Bansal 2006).
Gambar 6 Pemrosesan padi (a) hasil pemrosesan padi (b) serbuk sekam hasil penggilingan
Tabel 1(a) Komposisi kimiawi sekam
Komponen Kandungan (%)
Kadar air 9.02
Protein kasar 3.03
Lemak 1.18
Serat kasar 35.68
Abu 17.71
Karbohidrat kasar 33.71
Karbon (zat arang) 1.33
Hidrogen 1.54
Oksigen 33.64
Silika (SiO2) 16.98
Sumber : Balai Penelitian Pasca Panen Pertanian (2001).
Tabel 1(b) Komposisi kimiawi sekam
Komponen Kandungan (%)
H2O 2.40-11.35
Crudeprotein 1.70-7.26
Crude fat 0.38-2.98 Ekstrak nitrogen bebas 24.70-38.79
Crude fiber 31.37-49.92
Abu 13.16-29.04
Pentosa 16.94-21.95
Selulosa 34.34-43.80
Lignin 21,40-46.97
Sumber : Ismunadji (1988) dalam Laksmono (2000).
Komposisi kandungan kimia seperti yang di deskripsikan dalam Tabel 1, sekam antara lain dapat dimanfaatkan untuk (1) bahan baku industri bahan bangunan, terutama kandungan silika (SiO2) yang dapat digunakan untuk
campuran pada pembuatan semen, bahan isolasi, husk-board dan campuran pada industri bata merah; (2) sumber energi panas karena kadar selulosanya cukup tinggi sehingga dapat memberikan pembakaran yang merata dan stabil. Sekam memiliki kerapatan jenis (bulk density) 125 kg/m3, dengan nilai kalori 3.300 kkal/ kg sekam (Balai Penelitian Pasca Panen Pertanian 2001).
Silika adalah material anorganik yang penting. Silika secara khusus digunakan pada berbagai aplikasi, seperti resin, penyaring molekuler, pembantu peran katalis, dan pengisi dalam pembuatan polimer. Selain itu, saat ini silika sedang dikembangkan dalam bidang aplikasi biomedis (Bansal 2006). Silika yang dikembangkan saat ini, adalah silika sebagai bahan nanostrukur anorganik yang berpori. Silika berbentuk nanopartikel memiliki beberapa kelebihan sebagai partikel berdensitas rendah, partikel yang bersifat stabil secara termal, dan juga sebagai struktur yang dapat dikemas dalam bentuk kapsul, serta tahan terhadap proses mekanik dalam aplikasi pemanfaatnnya (Bansal 2006). Nanopartikel silika memiliki beberapa sifat diantaranya, luas permukaan besar, ketahanan panas yang baik, kekuatan mekanik yang tinggi, dan inert sehingga digunakan sebagai prekursor katalis (Benvenutti dan Yoshitaka 1998), sebagai adsorben (Kalapathy et al. 2000), dan sebagai filter komposit (Jamarun et al. 1997).
Metode Analisis Nanopartikel Silika
Produk sintesis berupa nanopartikel silika dari bahan dasar sekam dianalisis dengan menggunakan tiga jenis instrumentasi, yaitu SEM (Scanning Electrone Microscope), FTIR (Fourier Transformer Infrared Spectroscopy)., dan XRD (Xray Diffraction). Analisis SEM, FTIR, dan XRD dapat
menentukan bahwa produk biosintesis
berukuran nano, berkomposisi kimiawi silika, dan berstruktur nanopartikel silika kristalin sudah terbentuk atau belum.
Scanning electrone microscope (SEM)
SEM adalah jenis mikroskop elektron yang mampu menampilkan gambar permukaan objek pengamatan dengan resolusi gambar
yang tinggi. SEM digunakan untuk
pengamatan detail permukaan objek. Sistem
a.
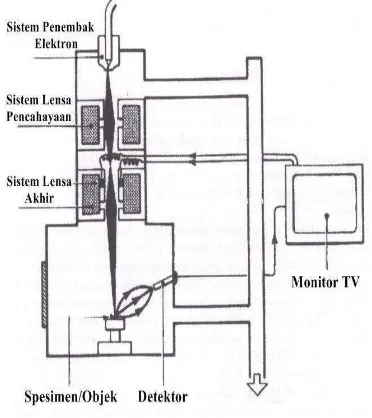
kerja SEM terdiri dari sumber cahaya elektron, sistem lensa, detektor, dan layar TV (Balaz 2008).
SEM bekerja melalui mekanisme kerja sehingga mampu menghasikan tampilan
gambar objek amatan. Gambar 7
menggambarkan mekanisme kerja SEM. Sumber cahaya elektron dihasilkan didalam suatu penembak elektron yang berbentuk filamen pemanas berupa tabung tanpa udara. Sumber cahaya elektron ini dipercepat dan difokuskan oleh sistem lensa magnetik yang berada diatas objek. Elektron dikumpulkan oleh detektor, diubah dalam bentuk voltase (energi listrik), kemudian disebar (Balaz 2008). Elektron dengan cepat mengenai permukaan objek untuk menginduksi radiasi-radiasi yang membentuk suatu bayangan yang dapat diperagakan melalui suatu tabung sinar katode. Proses yang terjadi didalam tabung katode mirip pembentukan gambar televisi. Objek yang akan dilalui radiasi elektron sebelumnya telah difiksasi dan dilapisi dengan logam berat seperti emas didalam hampa udara untuk mencegah distorsi (Dharmaputra 1989).
Hasil pencitraan SEM lebih baik bila dibandingkan dengan mikroskop cahaya konvensional. SEM memiliki jangkauan pandang yang luas terhadap objek yang diamati sehingga menghasilkan gambar detail permukaan objek yang sangat jelas. Struktur permukaan objek lebih terlihat curam dari pada hasil pencitraan mikroskop cahaya konvensional yang terlihat datar, sehingga SEM mampu mencitrakan objek dengan kontras yang baik (Balaz 2008).
Gambar 7 Skema kerja SEM.
SEM memiliki resolusi yang jauh lebih tinggi bila dibandingkan mikroskop cahaya kovensional. Hal tersebut dikarenakan SEM
mempergunakan sumber cahaya berupa
elektron yang memiliki energi sangat besar beberapa ribu elektronvolt, energi tersebut 1000 kali lebih kuat bila dibandingkan dengan energi yang dihasilkan dari cahaya tampak (2-3Ev). Resolusi SEM yang baik membuat SEM memiliki daya pisah hingga 50 nm dan dapat memperbesar bayangan hingga 8000-400000 kali (Balaz 2008).
FTIR (Fourier Transformer Infrared Spectroscopy)
Metode spektroskopi Inframerah (IR) didasarkan kepada absopsi cahaya IR oleh suatu molekul. Metode ini berguna untuk menentukan gugus fungsional suatu sampel. Jika suatu molekul ditempatkan di dalam
suatu daerah elektromagnetik (sinar
inframerah), akan terjadi perubahan bentuk energi dari daerah elektromagnetik ke
molekul. Kemampuan molekul dalam
mengabsorpsi radiasi berdasarkan sifat khas masing-masing molekul, yaitu perubahan dalam tingkat loncatan energetik elektron, pergerakan getaran dari atom, dan rotasi suatu molekul (Hendrayana et al. 1994; Balaz 2008).
Sumber radiasi (Z) pada FTIR berupa laser inframerah. Cahaya inframerah memiliki energi yang lebih rendah bila dibandingkan dengan ultraviolet dan sinar tampak. Hal tersebut menentukan tebal sampel (S) yang dipakai, tebal Sampel yang dipakai pada FTIR lebih tipis daripada spektrofotometer lainnya, yaitu sekitar 0.02 mm. Sampel (S) berupa padatan digerus dalam mortar bersama KBr kering dalam jumlah sedikit (0.5-2 mg sampel dengan 100 mg KBr kering). Campuran tersebut dipres diantara dua sekrup memakai kunci, kemudian terbentuk tablet sampel tipis yang diletakkan di tempat sel FTIR dengan lubang mengarah ke sumber radiasi (Z). Sampel dibiarkan terkena radiasi IR didalam FTIR. Radiasi dari sumber (Z) pergi melalui contoh (S) dan lewat melalui prisma (P).
Prisma (P) merupakan tempat terjadi
pemisahan komponen cahaya monokromatik
(Gambar 8). Rotasi perlahan prisma
untuk menghubungkan antara instrumen dengan komputer. Hasil peaks terlihat didalam monitor sesuai dengan gugus fungsi yang khas untuk masing-masing molekul (Hendrayana et al. 1994; Balaz 2008).
Gambar 8 Skema kerja FTIR.
XRD (X-Ray Diffraction)
Sinar X merupakan radiasi
elektromagnetik dengan panjang gelombang 10-10 m. Sinar ini terbentuk akibat pembagian spektrum elektromagnetik antara sinar γ dan ultraviolet. Sinar X mampu menyelidiki struktur kristal dari suatu padatan pada tingkat atomik. Bagian dalam suatu atom yang merupakan suatu padatan berada di daerah yang sama dengan panjang gelombang sinar X, kemudian sinar X dapat melewati padatan. Hal tersebut merupakan alasan mengapa sinar X dipantulkan dari atom kedalam kristal (Balaz 2008).
Difraksi sinar X membutuhkan sumber cahaya, contoh yang belum diketahui, dan sebuah detektor sebagai pengumpul sinar X (Gambar 9). Hasil dari pengukuran difraksi sinar X adalah pola yang digambarkan sebagai sebagai garis (peaks) dengan intensitas yang
berbeda-beda. Posisi garis (peaks)
menjelaskan karakteristik contoh yang diamati (Balaz 2008).
Gambar 9 Skema kerja XRD
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang dipergunakan dalam penelitian ini adalah isolat fungi Fusarium oxysporum (koleksi LIPI Biologi), sekam, akuades steril, sejumlah fenol-kloroform dan silika gel. Media yang dipergunakan adalah
media agar dekstrosa kentang (Potato
Dextrose Agar) yang terdiri atas 1000 mg/L ekstrak kentang dengan 200 g/L kentang, 15 g/L agar kentang, dan 20 g/L dekstrosa dan media agar dekstrosa cair (Potato Dextrose Liquid) yang terdiri atas ekstrak kentang
dengan 200 g/L kentang, 20 g/L dekstrosa dalam akuades steril. Beserta bahan tambahan lain, seperti HCL dan NaOH.
Alat-alat yang digunakan, meliputi neraca analitik OHAUS GA 200 Laminar Air Flow,
inkubator, inkubator bergoyang,
spektrofotometer Genesys 10UV, Beckman
High Speed Centrifuge, otoklaf TOMY High Pressure Steam Sterilzer ES-315, serta
peralatan laboartorium yang biasa
dipergunakan di laboratorium mikrobiologi.
Selain itu, instrumen seperti Scanning
Electron Microscope (SEM), Transmission Electron Microscope (TEM), serta X-Ray Diffraction (XRD) juga digunakan untuk katakterisasi nanopartikel.
Metode Penelitian
Penelitian ini dilakukan dalam empat tahap pengerjaan, yaitu meliputi: pembuatan media pertumbuhan, peremajaan dan pembuatan isolat cair Fusarium oxysporum, pembuatan kurva pertumbuhan dan pemanenan isolat
Fusarium oxysporum, serta sintesis nanopartikel silika. Penelitian dilakukan di
Laboratorium Biokimia FMIPA IPB,
Labortaorium Pusat Antar Universitas (PAU) IPB, Laborartorium Fisika Program Material Sains UI untuk analisis dengan SEM dan XRD, serta Laboratorium Pengujian Balai
Besar Riset Pengolahan Produk dan
Bioteknologi Kelautan dan Perikanan, Badan Riset Kelautan dan Perikanan-Kementarian Kelautan dan Perikanan untuk FTIR.
Pembuatan media pertumbuhan
Media pertumbuhan yang digunakan dalam penelitian ini adalah media Potato Dekstrose Agar (PDA) dan Potato Dekstrose Liquid
(PDL). Komposisi media PDA, yaitu 1000 ml/l air suling dengan 200 g/L kentang, 15 g/L agar kentang, dan 20 g/L dekstrosa. Komposisi media PDL, yaitu 1000 ml/L air suling dengan 200 g/L kentang, dan 20 g/L
dekstrosa. Antibiotik kloramfenikol
ditambahkan kedalam media sebanyak 250 mg/l (Dharmaputra et al. 1989).
dan PDL dengan pH 4 (Sari 2006). Media disterilisasi dengan autoklaf pada suhu 121oC dan tekanan 1 atm selama 15 menit.
Peremajaan dan pembuatan isolat cair
Fusarium oxysporum.
Isolat Fusarium oxysporum yang akan diremajakan diambil dengan menggunakan
coreborer dan dipindahkan kedalam cawan petri berisi media PDA. Cawan ditutup dan disegel menggunakan plastik wrap. Proses ini
dilakukan di dalam laminar air flow.
Fusarium oxysporum yang telah ditumbuhkan pada media PDA, kemudian diinkubasi pada suhu 27ºC selama 96 jam sampai fungi memenuhi cawan petri.
Isolat stok Fusarium oxysporum yang ditumbuhkan dalam PDA diinokulasikan
menggunakan coreborer pada labu
Erlenmeyer berisi 10 mL PDL yang merupakan suatu inoculum starter. Hasil
inokulasi ditutup dengan kapas dan
alumunium foil steril. Inoculum starter
selanjutnya diinkubasi dengan inkubator bergoyang dengan kecepatan 200 rpm pada suhu 27ºC selama 12-18 jam.
Sebanyak 1% atau sebanyak 500 μL
inoculum starter diinokulasikan kedalam 50 mL media PDL. Hasil inokulasi ditutup dengan kapas dan alumunium foil steril. Isolat selanjutnya diinkubasi dengan inkubator bergoyang dengan kecepatan 200 rpm pada suhu 27ºC.
Pembuatan kurva pertumbuhan dan pemanenan isolat Fusarium oxysporum
Fusarium oxysporum diukur biomassa pertumbuhannya yang tumbuh dalam media cair dekstrosa kentang (PDL) pada pembuatan
kurva pertumbuhan. Isolat Fusarium
oxysporum cair dalam PDL diukur optical density (OD) dengan spektrofotometer pada panjang gelombang 600 nm dan interval waktu 12 jam, yaitu jam ke-0, 12, 24, 36, 48, 60, 72, 84, dan 96.
Isolat Fusarium oxysporum yang dipanen adalah isolat yang telah ditumbuhkan pada medium PDL dan diinkubasi dalam inkubasi bergoyang dalam waktu sesuai informasi yang didapatkan berdasarkan kurva pertumbuhan. Setelah diinkubasi dilakukan pemanenan
fungi dengan menggunakan teknik
sentrifugasi pada kecepatan 6000 rpm selama 30 menit. Tahap selanjutnya adalah dilakukan pencucian pelet menggunakan air destilata
untuk menghilangkan sisa media dan
kemudian dilakukan proses sentrifugasi pada kecepatan 6000 rpm selama 30 menit.
Sintesis nanopartikel silika
Perlakuan pertama dilakukan dengan 50 mL air destilata yang mengandung 5 gram sekam diautoklaf dalam labu Erlenmeyer 250 mL. Perlakuan kedua dilakukan dengan 50 mL air destilata yang mengandung 2.5 gram sekam diautoklaf dalam labu Erlenmeyer 250
mL. Kemudian, biomassa Fusarium
oxysporum yang telah dipanen sebanyak 10 gram diresuspensikan dalam air destilata yang mengandung sekam. Reaksi antara biomassa fungi dilaksanakan di inkubator bergoyang pada 200 rpm pada 27ºC selama 24 jam.
Suspensi difiltrasi sehingga dapat
dipisahkan antara miselia fungi dan sekam dari komponen air (filtrat produk). Filtrat yang didapat diberi perlakuan fenol-kloroform (1:1) dan disentrifugasi pada 6000 rpm selama 10 menit untuk menghilangkan protein ekstraseluler fungi dari pelarut cair.
Tahap selanjutnya adalah kristalisasi nanopartikel silika, yaitu filtrat nanopartikel silika dibuat dalam bentuk kristal dengan teknik spray dry, sehingga diperoleh dalam bentuk serbuk. Bubuk tersebut dikarakterisasi dengan SEM, FTIR, dan XRD.
HASIL DAN PEMBAHASAN
Hasil Peremajaan dan Penumbuhan Isolat Cair Fusarium oxysporum
Peremajaan F.oxysporum merupakan
proses berkelanjutan yang dilakukan dengan tujuan menjaga agar kondisi isolat kapang yang dipergunakan masih dalam kondisi yang baik. Kondisi tersebut diperoleh jika isolat kapang tumbuh tanpa kontaminasi dan tercukupi nutrisi pertumbuhannya. Fungi
Fusarium oxysporum membutuhkan media tumbuh yang mengandung senyawa organik sebagai sumber karbon, seperti karbohidrat, asam organik, dan karbon dioksida (Gandjar
et al. 2006). Unsur karbon tersebut diperoleh dari media PDA (Potato Dekstrose Agar). Spora isolat F.oxysporum akan tertanam dalam cawan petri berisi media PDA pada proses peremajaan. Benang-benang hifa akan terbentuk dalam 1-2 hari. Benang-benang hifa terbentuk semakin banyak membentuk miselia pada hari ke-4. Miselia berwarna putih dan sedikit keunguan dengan diameter 3-5 cm di hari ke-4 (Gambar 10).
Pemeriksaan mikroskopis akan
membuktikan bahwa benang yang tumbuh
adalah isolat F.oxysporum. Gambar 11
terjalin. cabang-cabang hifa tumbuh dalam jumlah yang tidak sedikit menjauhi hifa yang pertama tumbuh. Gandjar et al. (2006) mengatakan bahwa pada titik percabangan
hifa dapat terjadi lisis dinding sel
(anastomosis) sehingga protoplasma akan mengalir ke semua sel hifa. Dalam kondisi tersebut, miselia akan terbentuk dalam jumlah yang banyak.
Masing-masing hifa memiliki lebar 5-10
μm (Pelczar & Chan 2008). Hal tersebut
dijadikan dasar untuk membedakan dengan sel bakteri yang pada umumnya memiliki
diameter 1 μm. Karakteristik khas dari suatu
F.oxysporum bila dibandingkan dengan fungi jenis lain ditunjukkan dalam Gambar 11 bahwa miselia terdiri dari hifa bersekat dan terdapat nukleus. Pelczar & Chan (2008) mengatakan bahwa sekat membagi hifa menjadi sel berisi nukleus tunggal.
Hasil peremajaan yang tumbuh dengan
baik tanpa kontaminan berdasarkan
pemeriksaan mikroskopis dijadikan sebagai inokulum. Inokulum merupakan sumber bahan yang mengandung spora sel kapang dan dengan sengaja ditambahkan pada substrat (Gandjar et al. 2006). Sumber substrat yang dipergunakan dalam pembuatan isolat cair
berasal dari media cair PDL (Potato
Dekstrose Liquid) dengan pH 4.
Gambar 10 F.oxysporum berumur 4 hari dalam media PDA
Gambar 11 Pengamatan mikroskopis F.
oxysporum perbesaran 10x10.
Suatu inocoloum starter dipersiapkan terlebih dahulu dalam pembuatan isolat cair.
Inocoloum starter berfungsi dalam mengaktifkan isolat F.oxysporum didalam
media PDL, sehingga diharapkan
F.oxysporum sudah siap untuk tumbuh. 4/5 bagian ruang kosong labu Erlenmeyer
dipersiapkan dalam pembuatan suatu
inocoloum starter. 4/5 bagian ruang kosong labu Erlenmeyer merupakan salah satu usaha untuk memaksimalkan sistem aerasi dalam penumbuhan F.oxysporum di media cair PDL.
Aerasi dilakukan karena F.oxysporum
merupakan organisme aerob, sehingga
persediaan oksigen yang cukup diperlukan bagi pertumbuhan. Oksigen dibutuhkan untuk melakukan reaksi enzimatis dan proses respirasi (Sari 2006). Inocoloum starter
ditumbuhkan dalam kondisi suhu 27ºC dan di
aerasi dengan shaker orbital dengan
kecepatan 200 rpm selama 12-18 jam. Inocoloum starter yang berumur 18 jam akan terlihat keruh berwarna putih. Kekeruhan dalam inocoloum starter mengindikasikan bahwa terdapat miselia F.oxysporum yang sudah siap untuk tumbuh. Inocoloum starter
diinoukulasikan sebanyak 1% dari jumlah volume PDL, kemudian diinkubasi pada suhu 27ºC dan di aerasi dengan shaker orbital
dengan kecepatan 200 rpm.
Miselia akan terbentuk berupa suatu benang-benang putih yang semakin lama semakin menebal dan berwarna keunguan dalam beberapa hari. Gandjar et al. (2006) mengatakan hifa vegetatif tumbuh kedalam
medium cair seperti akar-akar yang
bercabang. Miselia tumbuh di dalam media seperti benang tebal, berwarna keunguan, dan menyebabkan warna media yang semula bening berubah menjadi keruh serta berwarna keunguan (Gambar 12).
Gambar 12 F. oxysporum dalam PDL
(a)biomassa miselia (b) isolat cair
Kurva Pertumbuhan dan Hasil Pemanenan Isolat Fusarium oxysporum
Kurva pertumbuhan memberikan informasi mengenai pertumbuhan jumlah isolat kapang
F.oxysporum yang tumbuh pada waktu-waktu
tertentu sesuai dengan fase-fase yang
dilewatinya. Kurva pertumbuhan dapat
menentukan fase pertumbuhan optimum bagi
Fusarium oxysporum dalam menghasilkan enzim ekstraseluler yanga mampu mereduksi
substrat tertentu. Kurva pertumbuhan
F.oxysporum dibuat dengan menghubungkan
Optical Density (OD) dengan berbagai interval waktu pengamatan.
Optical Density (OD) ditentukan
berdasarkan kekeruhan media yang diukur dengan instrumen berupa spektrofotometer
pada panjang gelombang 600 nm.
Spektrofotometer bekerja berdasarkan hukum Lambert-Beer yaitu menghitung banyaknya energi radiasi gelombang cahaya yang tidak diteruskan atau yang diserap oleh kekeruhan
media. Cahaya yang diserap media
berbanding lurus dengan pertumbuhan sel kapang.
Kurva pertumbuhan F.oxysporum dibuat dengan interval waktu 12 jam (Gambar 13). Warna media yang semula bening mulai berubah menjadi keruh pada jam ke-12, sehingga mengindikasikan bahwa pada jam ke-12 terjadi fase lag dan akselerasi. Fase lag adalah fase penyesuaian sel-sel dengan lingkungannya, sedangkan fase akselerasi adalah fase saat sel bersiap untuk aktif membelah (Gandjar et al. 2006). Peningkatan OD sangat pesat terjadi pada jam ke-24 dan 36. Fase eksponensial terjadi pada jam
ke-12 sampai ke-36. Fase eksponensial
merupakan fase perbanyakan jumlah sel yang sangat banyak dan aktivitas sel meningkat (Gandjar et al. 2006). Titik deselarasi terjadi pada jam ke-48, dimulai dari titik ini biomassa
F.oxysporum dapat dipanen (Gandjar et al. 2006).
Gambar 13 Kurva pertumbuhan F.oxysporum.
Pemanenan biomassa F.oxysporum
dilakukan pada jam ke-72, yaitu saat sel memasuki fase stasioner berdasarkan kurva pertumbuhan yang diperoleh. Fase stasioner ditentukan sebagai waktu panen bagi
F.oxysporum karena diharapkan pada fase tersebut jumlah sel yang tumbuh relatif seimbang, sehingga jumlah miselia yang tumbuh relatif banyak (Gandjar 2006). Hal tersebut juga sesuai dengan penelitian yang dilakukan Bansal et al. (2002) dan Bansal et al (2005), F.oxysporum ditumbuhkan selama 72 jam dalam kondisi aerasi pada kecepatan
shaker 200 rpm dan diinkubasi pada suhu 27ºC. (Mukherjee 2002) mengatakan bahwa
F.oxysporum yang ditumbuhkan pada jam
ke-72 telah terdapat keberadaan protein,
ditunjukkan dengan pita yang terbentuk dalam elektroforesis. Pita elektroforesis dalam penelitian tersebut mengindikasikan sejumlah
protein yang berasal dari biomassa
F.oxysporum.
Proses pemanenan biomassa F.oxysporum
dilakukan dengan mempergunakan teknik sentrifugasi. Sentrifugasi merupakan suatu
teknik untuk memisahkan substansi
berdasarkan berat jenis molekul. Substansi yang lebih berat akan berada di dasar, sedangkan substansi yang lebih ringan akan terletak di atas dalam teknik sentrifugasi. Hal tersebut dapat terjadi karena adanya gaya sentrifugal (Harjadi 2006).
Berat jenis biomassa F.oxysporum lebih besar bila dibandingkan dengan media,
sehingga biomassa F.oxysporum menjadi
pelet yang terletak dibawah dan media menjadi supernatan pada saat diberi gaya sentrifugal dengan kecepatan 6000 rpm selama 15 menit. Supernatan berupa media PDA kemudian dipisahkan dari peletnya. Pencucian pelet dengan akuades steril dilakukan sebanyak dua kali. Hal tersebut dilakukan agar biomassa F.oxysporum berupa pelet bebas dari media PDL. F.oxysporum
yang telah dipanen dan bebas dari media PDL kemudian siap diberikan substrat dalam proses biosintesis.
Biomassa F.oxysporum sudah dapat diukur bobotnya dalam 72 jam (3 hari), sebab sudah terlihat jelas miselia yang menebal. Rata-rata biomassa F.oxysporum yang terbentuk dalam 50 mL PDL adalah 9.834 gram bobot basah. Bobot basah yang tumbuh berbeda-beda untuk
setiap ulangannya (Tabel 2). Inocoloum
starter F.oxysporum yang diinokulasikan kedalam 50 mL PDL mengandung jumlah benang-benang miselia yang relatif tidak sama
mempengaruhi perbedaan jumlah biomassa yang tumbuh dalam isolat cair.
Sebanyak 9.834 gram bobot basah
biomassa dapat menghasilkan 0.361 gram
bobot kering. Penyusutan biomassa
F.oxysporum disebabkan karena komponen utama sel adalah air (Gandjar et al. 2006). Air yang terkandung di dalam sel akan teruapkan ke udara pada proses pengeringan.
Tabel 2 Biomassa F. oxysporum dalam PDL. Volume PDB (mL) Bobot basah (g) Bobot kering (g)
50 13.780 0.221
50 10.632 0.371
50 5.091 0.491
Rata-rata 9.834 0.361
Nanopartikel Silika sebagai Hasil Biosintesis oleh F.oxysporum
Biosintesis nanopartikel silika dilakukan
dengan menumbuhkan F.oxysporum dalam
media yang mengandung sekam padi sebagai sumber silika sekaligus sebagai substrat bagi
pertumbuhan F.oxysporum. Sekam yang
mengandung 16.98% silika (Balai Penelitian Pasca Panen Pertanian 2001) dapat diubah menjadi nanopartikel silika secara biosintesis
dengan menggunakan F.oxysporum.
Komponen yang terkandung dalam sekam, yaitu selulosa dapat dimanfaatkan oleh
F.oxysporum sebagai substrat dalam siklus hidupnya (Soepardi et al. 1982). Selulosa merupakan polisakarida dari monomer berupa D-glukosa dengan subunit monomer berupa selobiosa yang banyak ditemukan di hampir semua jaringan tumbuhan sebagai komponen penyusun dinding sel tumbuhan dan dikenal sebagai serat di dalam suatu tumbuhan. Sebanyak 34.34-43.80 % selulosa terkandung dalam sekam (Hawab 2004).
Penelitian ini mempergunakan dua jenis perlakuan jumlah substrat sekam untuk menentukan jumlah substrat optimum yang mampu dimanfaatkan F.oxysporum dan dapat
disintesis menjadi nanopartikel silika.
Perlakuan pertama mempergunakan 5 gram sekam dan 10 gram biomassa F.oxysporum
berumur 72 jam. Perlakuan kedua
mempergunakan 2.5 gram sekam dan 10 gram
biomassa F.oxysporum berumur 72 jam.
Sekam ditambah dengan 50 mL akuades, kemudian di autoklaf. Proses sterilisasi ini
perlu dilakukan untuk menghilangkan
kontaminan dari substrat yang akan
dimanfaatkan F.oxysporum. Kultur diinkubasi 27ºC dan diaerasi 200 rpm selama 24 jam. Warna kultur berubah menjadi cokelat
kehitaman setelah F.oxysporum diberi
perlakuan dengan substrat berupa sekam. Produk hasil kultur berupa filtrat dipisahkan dari substrat berupa sekam dan sel kapang F.oxysporum dalam proses filtrasi. Produk biosintesis akan berada di filtrat karena enzim spesifik F.oxysporum yang berperan dalam biosintesis dikeluarkan secara ekstraseluler (Duran et al. 2005). Filtrat,
sekam, dan biomassa F.oxysporum dapat
dipisahkan dengan mudah satu dengan lainnya, karena ukuran partikel yang
berbeda-beda. Filtrat yang merupakan produk
biosintesis akan lolos melalui penyaring, sedangkan sekam dan biomassa tertahan pada penyaring. Sekam dan biomassa juga dengan mudah dapat dipisahkan, karena ukuran miselia biomassa F.oxysporum lebih besar dari partikel sekam.
Filtrat hasil biosintesis perlu dilakukan
pemurnian dengan fenol:kloroform 1:1.
Pelarut organik ini dapat memurnikan filtrat
hasil biosintesis dari protein melalui
mekanisme denaturasi protein (Lestari 2008). Hal tersebut dilakukan karena nanopartikel sebagai produk biosintesis yang terbentuk lebih baik bila dibandingkan dengan produk biosintesis tanpa perlakuan ekstraksi fenol-kloroform, yaitu tanpa pengotor (Bansal et al. 2005). Pelarut organik akan berada di lapisan paling bawah pada saat proses sentrifugasi. Lapisan tengah merupakan lapisan gumpalan protein dan lapisan air atas adalah filtrat hasil proses biosintesis (Gambar 14).
Proses analisis produk hasil biosintesis
dilakukan dengan menggunakan tiga
instrumen Scanning Electron Microscope
(SEM), Fourier Transformer InfraRed
Spectroscopy (FTIR), dan Xray Difraction
(XRD). Gambar 15 menunjukkan hasil
(SEM) produk biosintesis hasil reaksi
F.oxysporum dengan 5 gram sekam selama 24 jam pada perbesaran 2000 kali. Partikel terlihat beragregat satu dengan lainnya. Gambar 16 dan Gambar 17 merupakan
sekam tanpa perlakuan F.oxysporum dan
silika gel. Keduanya diperlakukan sebagai pembanding atau kontrol negatif, untuk membuktikan bahwa produk biosintesis telah mengindikasikan berukuran nano. Partikel hasil biosintesis terlihat memiliki berbagai variasi ukuran antara 200-1000 nm (Gambar 15). Ukuran partikel sekam tanpa perlakuan
ekstraseluler yang dikeluarkan F.oxysporum
telah bekerja dalam mereduksi sekam
sehingga terbentuk produk biosintesis dengan ukuran 200-1000 nm.
Produk hasil biosintesis yang merupakan
suatu nanopartikel silika kemudian
dibandingkan dengan silika gel sebagai kontrol negatif. Ukuran silika gel standar berdasarkan analisis SEM pada Gambar 17 adalah 15-5000 μm. Ukuran silika gel standar tersebut jauh lebih besar bila dibandingkan produk hasil biosintesis yang memiliki ukuran 200-1000 nm. Hasil tersebut mengindikasikan bahwa dalam produk hasil biosintesis, sebagian partikel telah berada dalam ukuran nano.
Gambar 14 Proses pemurnian (a)pelarut organik dan pelet (b) filtrat.
Gambar 15 Hasil analisis SEM nanopartikel silika dengan 5 gram sekam perbesaran 2000 x.
Gambar 16 Hasil analisis SEM sekam tanpa perlakuan F.oxysporum perbesaran 500 x (Ahmad et al. 2009).
Gambar 17 Hasil analisis SEM silika gel perbesaran 1000 x.
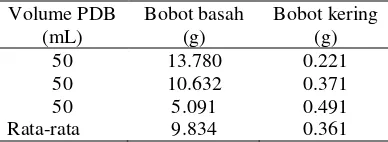
Hasil analisis SEM dapat didukung dengan analisis FTIR. Analisis FTIR dilakukan untuk memperdalam analisis produk biosintesis bahwa produk yang terbentuk adalah silika. Analisis ini didasarkan kepada spektrum inframerah pada setiap gugus fungsional suatu molekul yang bersifat spesifik. Nilai spektrum absorbsi inframerah setiap gugus fungsi dapat dilihat pada Lampiran 7. Menurut Balaz (2008) setiap gugus fungsi memiliki nilai spektrum absorbsi yang khas, yaitu gugus fungsi MOH memiliki nilai spektrum absorbsi 3700-2900 cm-1, gugus H2O memiliki nilai
spektrum absorbsi 3700-2900 cm-1, gugus CO32- memiliki nilai spektrum absorbsi
1600-1300 cm-1, NO32- memiliki nilai spektrum
absorbsi 1500-1250 cm-1, BO32- memiliki nilai
spektrum absorbsi 1300-1200 cm-1, SO4
2-memiliki nilai spektrum absorbsi 1200-1050 cm-1, PO43- memiliki nilai spektrum absorbsi
1100-950cm-1, SixOy 2-
memiliki nilai spektrum absorbsi 1200-900 cm-1, ASO43- memiliki nilai
spektrum absorbsi 900-750 cm-1, VO42-
memiliki nilai spektrum absorbsi900-750cm-1, dan WO4
2-
memiliki nilai spketrum absorbsi
850-750 cm-1. Spektrum absorbsi yang
diinginkan sebagai hasil biosintesis adalah spektrum absorbsi untuk gugus fungsi SixOy2-.
Spektrum absorbsi untuk gugus fungsi SixOy
2-berada pada rentang 1200-900 cm-1 (Balaz 2008) dan menurut (Handayani 2009) gugus Si-O-Si berada pada rentang spektrum absorbsi 1000-1110 cm-1.
Spektrum FTIR bagi silika gel berada pada spektrum absorbsi 1105.2 cm-1 (Gambar 18 a). Spektrum silika gel digunakan sebagai pembanding atau kontrol positif. Kontrol positif dapat membuktikan bahwa produk hasil biosintesis adalah silka secara kimiawi.
Hasil FTIR produk biosintesis pada
penambahan substrat sekam sebanyak 5 gram ditunjukkan dalam Gambar 18 b. Sebanyak 12 puncak ditemukan dalam spektrum absorbsi FTIR, yaitu 3408.18 cm-1, 2924.29 cm-1,
2852.59 cm-1, 1639,04 cm-1, 1415.77 cm-1, 1324.49 cm-1, 1078 cm-1, 1046.95 cm-1, 793.12 cm-1, 616.55 cm-1, 531.49 cm-1, dan 468.33 cm-1. Namun demikian, setidaknya terdapat tiga puncak yang memiliki puncak tertinggi, yaitu berada pada spektrum absorbsi 3408.18 cm-1, 1639.04 cm-1, dan 1078.71cm-1.
Hasil spektrum FTIR bagi produk
biosintesis dengan penambahan 5 gram substrat sudah mengindikasikan silika. Puncak
dengan spektrum absorbsi 1078.71 cm-1
diindikasikan sebagai silika karena spektrum absorbsi untuk gugus SixOy
berada pada rentang 1200-900 cm-1 (Balaz 2008). Hal tersebut juga diperkuat dengan bukti bahwa nilai serapan absorbsi produk biosintesis tidak berbeda jauh dengan nilai spektrum silika gel standar, yaitu 1105.2 cm-1.
Gugus fungsi lain selain SixOy2ditemukan
dalam analisis FTIR produk biosintesis, yaitu
gugus fungsi CO3
yang berada pada spektrum absorbsi 1639.04 cm-1 dan H2O
yang berada pada spektrum absorbsi 3408.18
cm-1. Keberadaan gugus fungsi yang
mengandung karbon dan air, menandakan bahwa masih terdapat selulosa yang belum dimanfaatkan oleh F.oxysporum. Selulosa merupakan komponen yang berasal dari sekam.
Proses sintesis kedua dilakukan dengan mempergunakan sebanyak setengah dari jumlah sintesis pertama, yaitu dengan jumlah substrat sebanyak 2.5 gram. Sintesis kedua mendapatkan perlakuan yang sama seperti pada sintesis pertama. Substrat yang telah steril kemudian diberikan 10 gram biomassa
F.oxysporum. Kultur diinkubasi 27ºC dan diaerasi 200 rpm selama 24 jam. Hasil SEM pada 1000 kali perbesaran dapat diamati pada Gambar 19.
Gambar 19 Hasil analisis SEM nanopartikel silika dengan 2.5 gram sekam perbesaran 1000 x
Hasil pengamatan dengan SEM pada produk biosintesis mempergunakan 2.5 gram sekam, memperlihatkan bahwa partikel berada dalam berbagai variasi ukuran partikel dan beragregasi. Ukuran partikel relatif tidak berbeda jauh dengan perlakuan 1 yang
mempergunakan 5 gram sekam, yaitu
memiliki ukuran 200-1000 nm. Hal yang sama terjadi pada perlakuan 2 bahwa
nanopartikel yang terbentuk masih
mengandung selulosa yang belum
dimanfaatkan oleh F.oxysporum. Faktor
waktu inkubasi pada saat F.oxysporum
memanfaatkan substrat berupa sekam
merupakan faktor diluar faktor eksperimental yang juga mempengaruhi hasil produk biosintesis nanopartikel silika.
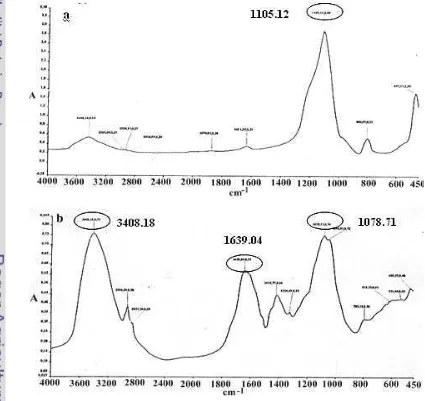
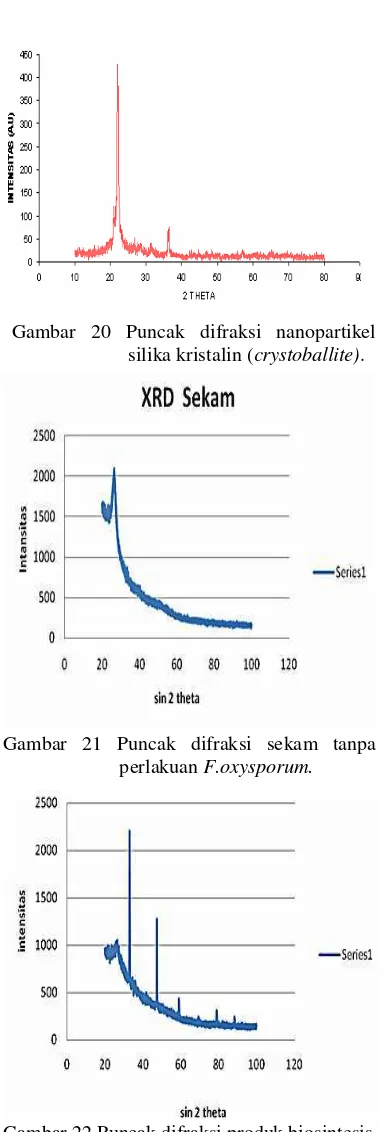
Karakteristik struktur produk biosintesis dianalisis dengan menggunakan XRD. Hasil analisis dengan XRD berupa puncak-puncak difraksi. Gambar 20 merupakan puncak difraksi khas untuk nanopartikel silika dengan struktur kristalin (crystoballite). Gambar 21 merupakan puncak difraksi untuk sekam tanpa
perlakuan F.oxysporum dan diperlakukan
sebagai kontrol negatif. Material anorganik silika yang terkandung dalam sekam, berada dalam struktur dasar (amorphous silica) (Bansal 2006). Gambar 22 merupakan puncak difraksi produk biosintesis yang merupakan
sekam dengan perlakuan F.oxysporum.
Puncak difraksi produk biosintesis berbeda dengan puncak difraksi sekam dan mendekati struktur puncak difraksi khas nanopartikel kristalin. Berdasarkan hasil tersebut dapat dikatakan bahwa sekam dengan perlakuan
F.oxysporum mengalami perubahan struktur
dari bentuk dasar (amorphous) dan
mengindikasikan berbentuk nanopartikel
silika kristalin (crystoballite).
Gambar 20 Puncak difraksi nanopartikel silika kristalin (crystoballite).
Gambar 21 Puncak difraksi sekam tanpa perlakuan F.oxysporum.
Gambar 22 Puncak difraksi produk biosintesis
Biosintesis nanopartikel merupakan
pengembangan metode baru dengan
menghasilkan nanopartikel logam dari sel mikrob serta melibatkan reaksi enzimatis.