Ganoderma sp. PENYEBAB PENYAKIT AKAR PADA POHON
SENGON (Paraserianthes falcataria (L) Nielsen.)
RATNA JAMILAH
E44060043
DEPARTEMEN SILVIKULTUR
FAKULTAS KEHUTANAN
INSTITUT PERTANIAN BOGOR
RINGKASAN
Ratna Jamilah. E44060043. Potensi Trichoderma harzianum (T38) dan
Trichoderma pseudokoningii (T39) sebagai Agen Antagonis terhadap
Ganoderma sp. Penyebab Penyakit Akar pada Tanaman Sengon (Paraserianthes falcataria (L) Nielsen.). Di bawah Bimbingan Dr. Ir. Elis Nina Herliyana, M.Si dan Dr. Ir. Darmono Taniwiryono, M.Sc
Sengon merupakan salah satu tanaman kehutanan yang banyak dikembangkan dalam program pembangunan hutan. Dalam pengelolaannya, tanaman sengon kerap kali diserang fungi busuk akar (Ganoderma sp.). Isolat
Trichoderma harzianum (T38) dan isolat Trichoderma pseudokoningii (T39) merupakan pilihan alernatif dalam mengendalikan Ganoderma sp. secara hayati. Penelitian ini bertujuan untuk mengetahui potensi isolat T38 dan T39 sebagai agen antagonis dalam pengendalian Ganoderma sp..
Bahan dan alat yang digunakan dalam penelitian ini adalah isolat
Ganoderma sengon L6, L12, L3, K2, dan K1, isolat T38 dan T39, cawan Petri, dan PDA steril. Uji antagonisme dalam penelitian ini dilakukan dengan cara metode biakan ganda dengan perbandingan 1 : 1 secara in-vitro dalam satu cawan konfrontasi. Kemudian setelah hari kelima dilakukan pengamatan zona penghambatan dan persen penghambatan. Analisis statistik menggunakan model RAL 2 faktor. Variabel yang digunakan adalah persen penghambatan.
Pertumbuhan isolat Ganoderma sp. dari yang paling cepat berturut-turut kemudian semakin lambat adalah Ganoderma K2, L12, K1, L3 dan L6. Sedangkan pada isolat Trichoderma sp. jenis yang paling cepat tumbuh adalah jenis isolat T39 dibandingkan dengan isolat T38. Kedua jenis fungi antagonis yang diuji isolat T39 memiliki potensi antagonistik yang lebih kuat dibanding isolat T38 dengan kemampuan menghambat pertumbuhan fungi patogen dengan persentase penghambatan lebih tinggi berturut-turut pada isolat Ganoderma L12, L6, dan L3.
Hasil pengamatan secara visual menunjukan bahwa, isolat T38 dan T39 mampu menghambat pertumbuhan koloni patogen berdasarkan hasil uji in-vitro
pada PDA. Zona penghambatan tidak muncul pada cawan konfrontasi. Isolat T39 memiliki potensi antagonistik (rata-rata persen penghambatan) yang lebih kuat (32.6%) dibanding isolat T38 (27.4%). Isolat Ganoderma sp. yang pertumbuhannya sangat terhambat adalah isolat Ganoderma L12, dengan rata-rata persen penghambatan 38.1% dan isolat Ganoderma L6 dengan rata-rata persen penghambatan 39.6%.
Ratna Jamilah. E44060043. Potential of Trichoderma harzianum (T38) and
Trichoderma pseudokoningii (T39) as Agent Antagonists against Ganoderma
sp. Root Cause of Plant Disease Sengon (Paraserianthes falcataria (L) Nielsen.). Under the guidance of Dr. Ir. Elis Nina Herliyana, M.Si and Dr. Ir. Darmono Taniwiryono, M.Sc.
Sengon is one of many forest plants that developed in the forest development program. In its management, sengon often attacked by root rot fungi (Ganoderma sp.). Isolates of Trichoderma harzianum (T38) and Trichoderma pseudokoningii (T39) are alternative options in controlling Ganoderma sp . biologically. This research aims to determine the potential of T38 and T39 isolates as antagonist agents in Ganoderma sp. controling.
Materials and tools those used in this research are isolates of sengon’s
Ganoderma (L6, L12, L3, K2, and K1) and isolates of Trichoderma (T38 and T39), Petri dishes, and sterile PDA. Antagonism test in this research carried out by dual culture method with a ratio of 1: 1 by in vitro in one cup of confrontation. Five days later, made the observation about zone and percent of inhibition. Statistical analysis that used in this research was RAL 2 factors model. Variable that used is the percent of inhibition.
Growth rank of Ganoderma sp. isolates from most rapid until the slower are K2, L12, K1, L3 and L6 Ganoderma. While the isolates of Trichoderma sp. the fastest growing type is the type of T38 isolates compared with T39 isolates. Both types of antagonists fungal were tested by T39 isolates have stronger antagonistic potency than T38 isolates with the ability to inhibit the growth of fungal pathogens. Percentage of inhibition in a row on Ganoderma isolates are L12, L6, and L3.
The visual observation showed that, T38 and T39 isolates can inhibit the growth of colonies of pathogens based on in vitro test results on the PDA. Zone of inhibition does not appear on the confrontation cup. Isolate of T39 has the antagonistic potential (average of inhibitation percent) a stronger (32.6%) than T38 isolates (27.4%). Isolates of Ganoderma sp. whose growth is stunted is L12
Ganoderma isolates, with 38.1% average of inhibition percent and L6 Ganoderma
isolates with 39.6% average of inhibitation percent.
POTENSI Trichoderma harzianum (T38) DAN Trichoderma
pseudokoningii (T39) SEBAGAI ANTAGONIS TERHADAP
Ganoderma sp. PENYEBAB PENYAKIT AKAR PADA POHON
SENGON (Paraserianthes falcataria (L) Nielsen.)
RATNA JAMILAH
E44060043
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Kehutanan Pada Departemen Silvikultur Fakultas Kehutanan
Institut Pertanian Bogor
DEPARTEMEN SILVIKULTUR
FAKULTAS KEHUTANAN
INSTITUT PERTANIAN BOGOR
pseudokoningii (T39) sebagai Agen Antagonis terhadap
Ganoderma sp. Penyebab Penyakit Akar pada Tanaman Sengon (Paraserianthes falcataria (L) Nielsen.)
Nama : Ratna Jamilah NIM : E44060043
Menyetujui : Dosen Pembimbing,
Dr. Ir. Elis Nina Herliyana, M.Si Dr. Ir. Darmono Taniwiryono, M.Sc NIP. 19670421 199103 2 001 NIK. 110 400 12
Mengetahui :
Plh. Ketua Departemen Silvikultur
Dr. Ir. Noor Farikhah Haneda, M.Si NIP. 19660921 199003 2 001
PERNYATAAN
Dengan ini saya menyatakan bahwa skripsi berjudul ”Potensi Trichoderma harzianum (T38) dan Trichoderma pseudokoningii (T39) sebagai Agen Antagonis terhadap Ganoderma sp. Penyebab Penyakit Akar pada Tanaman Sengon (Paraserianthes falcataria (L) Nielsen.)” adalah benar-benar hasil karya ilmiah saya sendiri dengan bimbingan dosen pembimbing dan belum pernah digunakan sebagai karya ilmiah pada perguruan tinggi atau lembaga manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir skripsi ini.
Bogor, April 2011
KATA PENGANTAR
Syukur yang tidak terhingga penulis panjatkan ke khadirat Allah SWT atas berkah dan hidayah-Nya sehingga penulis dapat menyelesaikan karya ilmiah ini. Tema yang dipilih dalam penelitian ini berjudul “Potensi Trichoderma harzianum
(T38) dan Trichoderma pseudokoningii (T39) sebagai Agen Antagonis terhadap
Ganoderma sp. Penyebab Penyakit Akar pada Tanaman Sengon (Paraserianthes falcataria (L) Nielsen.)”.
Dalam penyusunan karya ilmiah ini penulis memperoleh begitu banyak bantuan dan dukungan. Untuk itu dalam kesempatan ini penulis mengucapkan terimakasih kepada seluruh pihak yang telah banyak membantu dalam kegiatan pelaksanaan hingga penyusunan karya ilmiah ini.
Penulis menyadari bahwa masih banyak terdapat kekurangan dalam penulisan skipsi ini, oleh karena itu saran dan kritik yang membangun sangat penulis harapkan. Semoga skripsi ini dapat digunakan sebagai referensi untuk kepentingan ilmu pengetahuan dan bermanfaat dalam pelaksanaan penelitian berikutnya.
Bogor, April 2010
vi
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 07 Februari 1989 dari pasangan suami istri Rachmat Djiono dan Sugiati. Penulis memulai jenjang pendidikan formal pada tahun 1994-2000 di SDN 01 Duren Tiga, Jakarta Selatan.Penulis melanjutkan pendidikan di SLTPN 182 Kalibata, Jakarta Selatan dari tahun 2000-2003.
Kemudian pada tahun yang sama penulis melanjutkan pendidikan di SMU Muhammadiyah 04 Cawang, Jakarta Timur dan lulus pada tahun 2006. Pada tahun 2006 penulis diterima sebagai mahasiswa di Perguruan Tinggi Negeri Institut Pertanian Bogor (IPB) melalui jalur USMI (Undangan Seleksi Masuk IPB). Penulis kemudian diterima sebagai mahasiswa Program Studi Silvikultur, Departemen Silvikultur, Fakultas Kehutanan. Penulis aktif di organisasi mahasiswa, yakni sebagai Koordinator Seksi bidang PDD TGC (Tree Grower Community) Fakultas Kehutanan dari tahun 2008-2009, penulis juga aktif mengikuti seminar seperti, panitia pelatihan fungi tiram pada tahun 2008 dan panitia Go Green Bekasi Planting Project pada tahun 2008 serta seminar yang lain. Penulis juga pernah mengikuti Praktek Pengenalan Ekosistem Hutan (P2EH) di Kamojang dan Sancang serta Praktek Pengelolaan Hutan (PPH) di Hutan Pendidikan Gunung Walat (HPGW). Penulis juga melaksanakan Praktik Kerja Profesi (PKP) di PT. Erna Djuliawati Kalimantan-Tengah dan kemudian dilanjutkan dengan penelitian di Laboratorium Patologi Hutan IPB dan di Laboratorium Bioteknologi LRPI Bogor. Untuk memperoleh gelar sarjana Kehutanan IPB, penulis menyelesaikan skripsi dengan judul “Potensi
UCAPAN TERIMA KASIH
Segala puji syukur kepada Allah SWT yang telah melimpahkan segala rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan karya ilmiah ini sebagai salah satu syrarat untuk mendapatkan gelar sarjana di Fakultas Kehutanan, Institut Pertanian Bogor. Tema yang dipilih dalam penelitian ini berjudul “Potensi
Trichoderma harzianum (T38) dan Trichoderma pseudokoningii (T39) sebagai Agen Antagonis terhadap Ganoderma sp. Penyebab Penyakit Akar pada Tanaman Sengon (Paraserianthes falcataria (L) Nielsen.)”. Atas selesainya penyusunan karya ilmiah ini penulis mengucapkan terima kasih yang sebesar-besarya kepada:
1. Ibu Dr. Ir. Elis Nina Herliyana, M.Si dan Dr. Ir. Darmono Taniwiryono, M.Sc selaku dosen pembimbing untuk kesempatan yang diberikan serta bimbingan, arahan, dan kesabarannya selama penelitian mulai dari perencanaan hingga penyusunan tugas akhir ini sehingga penulis dapat menyelesaikannya dengan baik.
2. Keluarga tercinta bapak Rachmat Djiono, ibu Sugiati dan mama Rosida tersayang serta adik-adikku tercinta (Lukman Muharom dan Fatma Syafira) atas segala kasih sayang, bantuan baik dari segi moril maupun materil, semangat, motivasi dan doanya.
3. Keluarga bapak BJ Basuki dan ibu Nadia Damayanti serta beserta adik Ahadiah Nur Maisaroh yang telah membantu baik dari segi moril dan materil, semangat, serta doa dan motivasinya.
4. Permana Zainal yang selalu menemani, membantu, memberikan semangat serta motivasi kepada penulis sehingga penulis dapat menyelesaikan karya ilmiah ini.
5. Bapak Dr. Ir. Basuki Wasis sebagai dosen moderator pada seminar hasil penelitian.
6. Bapak Ir. Siswoyo, M.Si selaku dosen penguji serta bapak Ir. Kasno, M.Sc sebagai dosen moderator pada sidang penelitian.
viii
8. Teman-teman penghuni kontrakan Pongah Wulan, Dina, Gina, Dewi, dan yang lainnya atas penghiburan, deskripsi masa depan dan harapan yang telah kalian tanamkan.
9. Teman-temanku Enike Ratna Sari, Helga Sugiarti, Dedi Mulyana, Randhi F. Kiswantara, Niechi Valentino, Hania Purwitasari, Noviandri Asmar, Linda, dan Suke, adik angkatan Nur Syamsi, Uan Subhan, Umar Atik, Renando Mieko maupun kakak angkatan Irvan Kemal Putra dan yang lainnya serta teman satu angkatan yang tidak bisa penulis sebutkan satu persatu, atas bantuan semangat, doa, dukungan dan penghiburannya. 10. Serta civitas Fakultas Kehutanan IPB angkatan 2006 dan seluruh keluarga
besar Fakultas Kehutanan atas dukungan serta kehadiran dalam seminar hasil penelitian.
DAFTAR ISI
1.2 Tujuan Penelitian ... 3
1.3 Hipotesa Penelitian ... 3
1.4 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Potensi Agen Antagonis dalam Pengendalian Hayati ... 4
2.1.1 Pengertian ... 4
2.1.2 Mekanisme Antagonisme ... 5
2.2 Sengon (P. falcataria) ... 6
2.3 Ganoderma sp., T. harzianum dan T pseudokoningii. ... 7
2.3.1 Ganoderma sp. ... 7
2.3.2 T. harzianum dan T. pseudokoningii. ... 9
BAB III METODE PENELITIAN ... 12
3.1 Lokasi dan Waktu Penelitian ... 12
3.2 Bahan dan Alat Penelitian ... 12
3.2.1 Media Tumbuh ... 12
3.2.2 Sumber Inokulum ... 12
3.2.3 Peralatan ... 13
3.3 Metode Penelitian ... 13
x
... Halaman
3.3.2 Analisis Statistik ... 15
BAB IV HASIL DAN PEMBAHASAN ... 17
4.1 Hasil ... 17
4.2 Pembahasan ... 22
BAB V KESIMPULAN DAN SARAN ... 25
5.1. Kesimpulan ... 25
5.2. Saran ... 25
DAFTAR PUSTAKA ... 26
DAFTAR TABEL
No. Uraian Halaman 1. Jenis Perlakuan Ganoderma sp. dengan Trichoderma sp.……….. 15
2. Rekapitulasi Hasil Sidik Ragam terhadap Variabel yang Diamati……. 20 3. Hasil Uji Duncan Pengaruh Jenis Isolat Ganoderma sp. terhadap
Persen Penghambatan……….. 21 4. Hasil Uji Duncan Pengaruh Jenis Isolat Trichoderma sp. terhadap
Persen Penghambatan……….. 22 5. Pertumbuhan Ganoderma sp. pada Cawan Petri (kontrol)………. 30 6. Pertumbuhan Trichoderma sp. pada Cawan Petri (kontrol)... 30 7. Persen Penghambatan Uji Antagonis Trichoderma sp dan Ganoderma
xii
DAFTAR GAMBAR
No. Uraian Halaman
1. Ganoderma sp. secara mikroskopis... 9 2. T. harzianum secara miskropkopis... 10 3. T. pseudokoningii secara mikroskopis... 11 4. Metode biakan ganda Ganoderma sp. dan Trichoderma sp. pada
Cawan konfrontasi berdiameter 9 cm...……….... 14 5.
Pertumbuhan Koloni Ganoderma sp………... 17
6. Pertumbuhan Koloni Trichoderma sp………. 18
7. Pertumbuhan Isolat Ganoderma sp.di Cawan Petri pada Hari Ke-10. 7A Isolat Ganoderma L12. 7B Isolat Ganoderma L6. 7C Isolat
8. Pertumbuhan Isolat Trichoderma sp.di Cawan Petri pada Hari Ke-5. 8A Isolat T38. 8B Isolat T39...
9. Penghambatan Pertumbuhan In-Vitro Ganoderma sp. oleh
Trichoderma sp... 19 10. Pertumbuhan Isolat Ganoderma sp. dan Trichoderma sp. pada Cawan
Konfrontasi 10A Isolat Ganoderma L12*T38. 10B Isolat
Ganoderma L12*T39. 10C Isolat Ganoderma L6*T38. 10D Isolat
Ganoderma L6*T39. 10E Isolat Ganoderma L3*T38. 10F Isolat
Ganoderma L3*T39. 10G Isolat Ganoderma K2*T38. 10H Isolat
Ganoderma K2*T39. 10I Isolat Ganoderma K1*T38. 10J Isolat
DAFTAR LAMPIRAN
No. Uraian Halaman 1. Pertumbuhan Ganoderma sp.………. 30
2. Pertumbuhan Trichoderma sp.……… 30 3. Persen Penghambatan Uji Antagonis Trichoderma sp dan Ganoderma
sp………. 30 4. Hasil Uji Sidik Ragam terhadap Variabel yang Diamati dengan
Menggunakan Sofware SAS 9………... 31 5. Hasil Uji Lanjut Duncan Pengaruh Jenis Isolat Ganoderma sp.
terhadap Persen Penghambatan dengan Menggunakan Sofware SAS 9…………...
… 32 6. Hasil Uji Lanjut Duncan Pengaruh Jenis Isolat Trichoderma sp.
terhadap Persen Penghambatan dengan Menggunakan Sofware SAS 9…………...
1
BAB I
PENDAHULUAN
1.1 Latar Belakang
Peran Hutan Tanaman Industri (HTI) sebagai penyediaan bahan baku kayu di Indonesia kini semakin meningkat. Bagian terbesar kayu dari HTI luar Jawa adalah untuk kayu pulp. HTI kayu pulp didominasi oleh Acacia mangium, Acacia crassicarpa, Eucalyptus pellita, Eucalyptus urophylla, Tectona grandis dan
Paraserianthes falcataria (L) Nielsen (sengon). HTI tersebut umumnya dilakukan secara monokultur dan seringkali dihubungkan dengan peningkatan resiko serangan hama penyakit, terutama bila benihnya berasal dari induk pohon yang secara genetik keragamannya rendah atau berkerabat (Rimbawanto 2008).
Tanaman yang banyak dikembangkan pada program pembangunan hutan, HTI di Indonesia saat ini salah satunya adalah sengon. Salah satu kelebihan dari pohon sengon adalah pertumbuhannya yang cepat dan kegunaan kayunya yang beragam. Masyarakat pedesaan di pulau Jawa banyak menggunakan kayu sengon untuk bahan konstruksi di bawah atap, mebel sederhana, peti kemas, pembuatan pulp, kertas dan papan sambung. Sengon juga mempunyai manfaat yang cukup besar dalam upaya rehabilitasi lahan kritis, maka pemerintah melalui Departemen Kehutanan, telah lama mencanangkan program ‘sengonisasi’ (Atmosuseno 1998). Serangan penyakit busuk akar yang disebabkan oleh fungi Ganoderma sp.
pada tanaman sengon telah banyak dilaporkan (Basset dan Peters, 2003; Solomon
et al., 1993; Widyastuti, 2007). Serangan Ganoderma sp. di lapangan sulit dideteksi karena gejalanya mirip dengan gejala kekeringan. Meskipun tanaman sudah menunjukkan gejala sakit, namun terkadang tubuh buah Ganoderma sp.
belum terbentuk. Beberapa tanaman yang tampak sehat ditemukan tubuh buah
Ganoderma sp. di pangkal batangnya (Basset dan peters, 2003).
Ganoderma sp. adalah fungi polyporus yang mempunyai daerah penyebaran tempat tumbuh yang cukup luas dan dikenal sebagai penyebab penyakit akar pada banyak jenis tanaman berkayu. Di hutan alam fungi ini cenderung menyerang pohon-pohon tua atau yang telah mengalami penurunan pertumbuhan, dan juga dapat menyebabkan pembusukan kayu yang sudah mati. Pada HTI dan perkebunan fungi ini telah dilaporkan menjadi patogen akar yang potensial dan telah banyak menyerang beberapa jenis tanaman (Semangun, 2000).
Infeksi patogen lebih mudah terjadi melalui luka dan lentisel, pada tanaman sering ditemukan bagian leher akar pecah, dan ini merupakan tempat yang baik bagi infeksi fungi. Patogen kemudian kebagian yang lebih dalam dari akar. Serangan akan lebih tinggi akan ditemukan pada tanaman okulasi dibandingkan dengan tanaman biji. Hal ini disebabkan pada tanaman okulasi ada bagian-bagian luka, sehingga memudahkan Ganoderma sp. untuk mengadakan infeksi (Sinulingga, 1989). Infeksi atau penularan penyakit ini terjadi melalui kontak akar tanaman sehat dengan sumber infeksi didalam tanah seperti potongan akar padat dan batang yang mengandung koloni patogen (Haryono dan Widyastuti, 2001).
Pengendalian Ganoderma sp. secara hayati dapat dilakukan dengan cara pemanfaatan mikroorganisme. Pengalaman menunjukkan bahwa pengendalian penyakit yang bersifat tidak membahayakan kehidupan makhluk hidup dan lingkungan adalah pengendalian yang ramah lingkungan. Pengendalian hayati menggunakan agen antagonis dengan satu kali pemakaian dapat menekan pertumbuhan dan perkembangan patogen untuk jangka waktu yang relatif panjang tanpa menimbulkan pencemaran lingkungan (Cook dan Baker, 1989 dalam Muthahanas dan Listiana, 2008).
3
potensi T. harzianum (T38) dan T. pseudokoningii (T39) sebagai agen pengendalian Ganoderma sp. secara hayati.
1.2 Tujuan Penelitian
Tujuan penelitian ini adalah untuk mengetahui potensi fungi antagonis T. harzianum (T38) dan T. pseudokoningii (T39) terhadap Ganoderma sp. yang menyerang tanaman sengon. Penelitian ini dilakukan untuk mengetahui efektifitas isolat T. harzianum (T38) dan T. pseudokoningii (T39) dalam menghambat pertumbuhan Ganoderma sp. pada tanaman sengon dan memberikan informasi yang berkaitan dengan kemampuan isolat tersebut sebagai agen antagonis terhadap Ganoderma sp..
1.3 Hipotesa Penelitian
1. Fungi agen antagonis dapat berinteraksi dengan patogen penyakit tanaman secara in vitro.
2. Fungi agen antagonis memiliki kemampuan yang berbeda dalam menekan perkembangan fungi.
1.4 Manfaat Penelitian
BAB II
TINJAUAN PUSTAKA
2.1 Potensi Agen Antagonis dalam Pengendalian Hayati
2.1.1 Pengertian
Pengurangan dampak negatif penggunaan pestisida kimia sintetik dapat dilakukan dengan berbagai cara, salah satunya yaitu dengan mengenalkan kepada masyarakat tentang pengendalian penyakit secara terpadu dalam penanganan patogen tanaman. Salah satu komponen dalam pengendalian penyakit secara terpadu adalah pengendalian hayati. Pengendalian hayati patogen tanaman dapat dilakukan dengan pemanfaatan mikroorganisme antagonis yang dapat menekan atau menghambat perkembangan patogen tanaman. Cook dan Baker (1989) dalam Muthahanas dan Listiana (2008) mendefinisikan pengendalian hayati penyakit tanaman sebagai upaya pengurangan kepadatan inokulum patogen penyebab penyakit atau aktifitas patogen yang dapat menyebabkan penyakit tanaman, dengan menggunakan satu atau beberapa mikroorganisme lainnya, manipulasi lingkungan dan tanaman inang atau penggunaan mikroorganisme antagonis.
Antagonisme merupakan asosiasi antara organisme dari spesies yang sama, dari genus yang sama atau dari genus yang berbeda bahkan mungkin berasal dari famili yang berbeda, yang saling mempengaruhi baik secara langsung maupun tidak langsung (Baker dan Cook, 1989 dalam Purwantisari dan Hastuti,
2009). Belakangan ini pengendalian hayati mendapat perhatian yang serius dari para ahli entomologi dan penyakit tanaman. Beberapa teknik pengendalian penyakit telah dikembangkan seperti fisik, kimia, hayati, kultur, sanitasi, karantina, eradikasi dan imunisasi (Agrios, 1996).
5
inang dengan cara menghasilkan toksin atau enzim, (3) menghambat transportasi makanan, hara mineral, dan air, (4) mengkonsumsi kandungan sel inang setelah terjadi kontak (Agrios, 1996).
Keuntungan menggunakan agen antagonis sebagai pengendali hayati antara lain : organisme yang digunakan lebih aman daripada berbagai bahan kimia proteksi, tidak terakumulasi dalam rantai makanan, terjadi proses reproduksi sehingga dapat mengurangi pemakaian berulang-ulang, patogen jarang menjadi resisten terhadap agen pengendalian hayati dibandingkan dengan resistensinya terhadap bahan kimia dan dapat dipakai untuk pengendalian bersama-sama dengan cara proteksi yang telah ada (Suwanto et al., 1996).
2.1.2 Mekanisme Antagonisme
Mekanisme antagonisme antara fungi antagonis dengan fungi patogen dalam pengendalian hayati terjadi dalam bentuk antibiosis, kompetisi, dan mikroparasitisme. Antibiotik adalah senyawa kimia bersifat racun, yang dihasilkan oleh mikroorganisme yang dapat menghambat atau membunuh mikroorganisme lain (Agrios, 1996). Di antara antibiotik yang sangat penting dalam pengendalian patogen adalah panisilin streptomisin, tetrasiklin, dan sikloheksimida.
Menurut Yudoamidjojo et al. (1989), zat antibiotik ideal hendaknya memiliki sifat-sifat sebagai berikut : (1) harus mempunyai kemampuan untuk merusak atau menghambat mikroorganisme patogen spesifik, (2) tidak mengakibatkan patogen menjadi parasit, (3) tidak menimbulkan efek sampingan pada inang dan (4) konsentrasi antibiotik di dalam jaringan harus dapat mencapai taraf cukup tinggi sehingga mampu menghambat atau mematikan penyebab infeksi.
sedangkan pada nekrotrofik parasit merusak sel inang sebelum atau segera setelah terjadi interaksi (Achmad, 1997).
2.2 Sengon (P. falcataria)
Adapun spesies P. falcatariamemiliki sistem klasifikasi sebagai berikut : Divisio : Spermatophyta
Subdivisio : Angiospermae Famili : Leguminosae Subfamili : Mimosaceae Klas : Dicotyledonae Ordo : Rosales Genus : Paraserianthes
Species : Paraserianthes falcataria (L) Nielsen
Nama daerah : Jeunjing, sengon laut (Jawa), tedehu pute (Sulawesi), rawe, selawoku, selaku merah, seka, sika, sika bot, sikas, tawasela (Maluku), bae, bai, wahogon, wai, wikkie (Irian Jaya) (Marta, 2005).
Sengon merupakan pohon multiguna, baik daun, batang, maupun sistem perakarannya dapat dipergunakan untuk beragam keperluan. Daun sengon, sebagaimana daun-daun dari famili Mimosaceae lainnya merupakan pakan ternak yang sangat baik mengandung protein yang tinggi, sehingga disukai hewan ternak. Selain sebagai pakan ternak, daun sengon yang berguguran akan bertindak sebagai pupuk hujau yang baik bagi tanah dan tanaman di sekitarnya. Tajuk pohon yang bebentuk perisai dan pohonnya yang besar dimanfaatkan sebagai pohon peneduh.
7
2.3 Ganoderma sp., T. harzianum dan T. pseudokoningii
Fungi adalah organisme eukariotik, berspora, tidak berklorofil, berupa sel atau benang–benang halus yang disebut dengan hifa. Kumpulan hifa disebut dengan miselium. Pada umumnya fungi berkembangbiak secara seksual dan aseksual (Tjitrosoepomo, 1994). Karena fungi tidak mempunyai zat warna untuk melakukan fotosintesis dan kemosintesis, maka fungi mendapatkan makanannya untuk energi dan pembangunan tubuh dengan cara hidup sebagai parasit (pada organisme lain atau) atau sebagai saprofit (dengan menguraikan bahan organik yang mati) (Tjitrosoepomo, 1994).
Untuk mendapatkan gambaran dari golongan fungi seluruhnya dapat diberikan ihtisar sebagai berikut (Alexopoulos et al., 1996). Thallophyta yang tidak berklorofil dibagi atas, 1. Phylum Schizomycophyta (Bakteri); 2. Phylum Myxomycophyta (Fungi lendir); 3. Phylum Eumycophyta (Fungi benar). Phylum Eumycophyta terbagi atas 4 klas, yaitu, 1. Klas Phycomycetes (Fungi ganggang); 2. Klas Ascomycetes; 3. Klas Deuteromycetes atau Fungi imperfecti (Fungi tak sempurna); 4. Klas Basidiomycetes. Fungi Ganoderma sp. dan fungi T. harzianum, dan fungi T. pseudokoningii masuk dalam kategori Phylum Eumycophyta (fungi benar).
2.3.1 Ganoderma sp.
Ganoderma adalah fungi poliporus yang banyak dijumpai tumbuh di dalam vegetasi berkayu, yaitu pada tonggak-tonggak berbagai jenis kayu dan sebagian pada batang-batang kayu pohon hidup. Fungi ini dideskripsikan pertama kali oleh Karsten (1881). Turner (1981) melaporkan bahwa paling sedikit terdapat 15 species Ganoderma di berbagai tempat di dunia,yang menyebabkan penyakit busuk pangkal batang. Sampai saat ini telah ditemukan lebih dari 250 jenis dan marga Ganoderma di seluruh dunia. Dari jumlah tersebut masih ada yang tumpang tindih (hanya sinonimnya), sehingga jumlah sebenarnya kurang dari 250 (Susanto, 1998).
tubuh buah seperti mempunyai tangkai. Seringkali banyak tubuh buah terbentuk berdekatan, saling menutupi atau sa1ing bersambungan. sehingga menjadi suatu susunan yang besar (Sumardi dan Widiastuti, 2001).
Disamping hidup sebagai parasit, Ganoderma sp. mampu hidup sebagai saprofit dengan memanfaatkan sisa-sisa tanaman, seperti sisa-sisa akar dalam tanah, ranting-ranting, dan batang pohon di hutan (Semangun, 2000).
Ganoderma sp. memiliki klasifikasi sebagai berikut : Kingdom : Fungi
Phylum : Basidiomycota Kelas : Basidiomycetes Ordo : Polyporales Keluarga/Family : Ganodermataceae Genus : Ganoderma
Spesies : Ganoderma sp.
(http://en.wikipedia.org/wiki/Ganoderma_lucidum)
Basidiomycetes dipandang sebagai cendawan yang perkembangannya paling tinggi di antara kelompok cendawan. Organ yang khas pada basidiomiset yaitu basidium, sebuah sel cendawan yang terdapat di ujung, yang sesuai dengan askus. Dari basidium ini lazimnya dipisahkan ke luar empat buah basidiospora. Basidiospora ini berinti tunggal dan haploid (Gambar 1).
9
Sumber: Mudarwan, 2009
Gambar 1 Ganoderma sp. secara mikroskopis.
2.3.2 T. harzianum dan T. pseudokoningii
Klasifikasi Trichoderma sp. menurut Semangun (2000) adalah sebagai berikut:
Kingdom : Fungi Phylum : Ascomycota Class : Ascomycetes Subclass : Hypocreomycetidae Ordo : Hypocreales
Family : Hypcreaceae Genus : Trichoderma
Species : T. harzianum dan T. pseudokoningii
Trichoderma merupakan fungi Deuteromycetes dengan konidiofor tegak, bercabang banyak, agak berbentuk kerucut, dapat membentuk klamidospora. Pada umumnya koloni dalam biakan tumbuh dengan cepat, berwarna putih sampai hijau (Cook and Baker, 1989). Bentuk sempurna dari fungi ini secara umum dikenal sebagai Hipocreales atau kadang-kadang Eurotiales, Clacipitales dan Spheriales. Spesies dalam satu kelompok yang sama dari Trichoderma dapat menunjukkan spesies yang berbeda pada Hypocrea sebagai anamorf. Hal ini dimungkinkan karena terdapat banyak perbedaan bentuk seksual dari Trichoderma (Chet, 1987). Koloni Trichoderma pada media biakan PDA tumbuh dengan cepat pada suhu
25-5 µm
30º C. Koloni ini akan berubah warna menjadi hijau tua sedangkan bagian bawahnya tidak berwarna (Samuel et al, 2005).
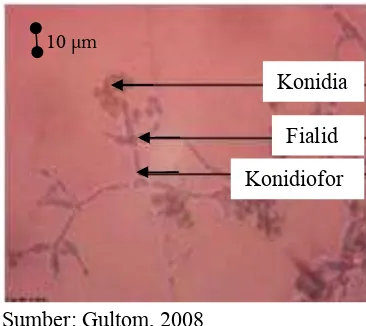
Fungi T. harzianum mempunyai hifa bersepta, bercabang dan mempunyai dinding licin, tidak berwarna, diameter 1.5-12 µm. Percabangan hifa membentuk sudut siku-siku pada cabang utama. Cabang-cabang utama konidiofor berdiameter 4-5 µm dan menghasilkan banyak cabang-cabang sisi yang dapat tumbuh satu-satu tetapi sebagian besar berbentuk dalam kelompok yang agak longgar dan kemudian berkembang menjadi daerah-daerah seperti cincin. Pada ujung konidiofor terbentuk konidiospora berjumlah 1-3, berbentuk pendek, dengan kedua ujungnya meruncing dibandingkan dengan bagian tengah, berukuran 5-7 x 3-3.5 µm, diujing konidiofor terdapat konidia berbentuk bulat, berdinding rata dengan warna hijau suram, hijau keputihan, hijau terang atau agak kehijauan (Gambar 2) (Gandjar et al, 1999). Beberapa ciri morfologi fungi T. harzianum
yang menonjol antara lain koloninya berwarna hijau muda sampai hijau tua yang memproduksi konidia aseksual berbentuk globus dengan konidia tersusun seperti buah anggur dan pertumbuhannya cepat (fast grower) (Harman, 1998).
Sumber: Gultom, 2008
Gambar 2 T. harzianum secara mikroskopis.
Koloni T. pseudokoningii berkembang pesat, dengan miselium udara sedikit, pada awalnya berwarna krem, secara bertahap dengan berubah menjadi kehijauan, pertama di sebagian koloni, kemudian seluruh koloni. Secara mikroskopis, Hifa hialin memiliki lebar sampai dengan 10 μm. Konidiofor bercabang menyerupai piramida, bercabang di sudut kanan sebelum ujung cabang
Konidia
Fialid
Konidiofor
11
dan pada cabang di bagian bawah (Gambar 3) (Hook, 2000 dalam Mycobank, 2000).
Sumber: Hook, 2000 dalam Mycobank 2000
Gambar 3 T. pseudokoningii secara mikroskopis.
Morfologi beberapa spesies Trichoderma menurut Cook and Baker (1989), sebagai berikut:
• T. harzianum Rifai : Umum ditemukan pada tanah, konidiofor berakhir pada fialid; fialospora halus, berwarna hijau, berukuran antara 2,4-3,2 X 2,2-2,8 mm; koloni cepat tumbuh.
• T. pseudokoningii Rifai : Umum ditemukan pada tanah, berdaptasi pada kondisi kelembaban tanah yang sangat tinggi. fialid ramping dan berbentuk labu. Konidia elliptik, pendek dan silindris, halus berdinding kebiruan dan hijau, 3,5-4,5 x 2,0-2,5 μm koloni cepat tumbuh.
Genus dari Trichoderma terdiri atas beberapa fungi saprofit yang umum ditemukan dalam tanah, kayu lapuk, dan sisa tanaman, yang mana dapat mudah dikenali terutama karena sporanya yang berwarna hijau (Chet, 1987).
Konidia Konidiofor
BAB III
METODE PENELITIAN
3.1 Lokasi dan Waktu Penelitian
Kegiatan uji antagonis Ganoderma sp. terhadap Trichoderma sp. dilaksanakan pada bulan Oktober 2009 sampai dengan November 2009. Kegiatan ini dilaksanakan di Laboratorium Pathologi Hutan IPB dan Laboratorium bioteknologi LRPI Bogor.
3.2 Bahan dan Alat Penelitian
3.2.1 Media Tumbuh
Alat yang digunakan dalam pembuatan media Potato Dextrose Agar
(PDA) adalah cawan Petri, tabung Erlenmeyer, pisau, kain kasa, pengaduk, panci,
lamine air flow dan autoclave, sedangkan bahan yang digunakan antara lain kentang 200 gram, dekstrosa 20 gram, agar-agar 17 gram, antibiotik dan aquades 1 liter. Cara kerja dalam pembuatan media PDA adalah kentang dikupas kemudian dicuci bersih dengan air dan dipotong-potong kecil dibentuk segiempat, kentang direbus dengan 1 liter aquades sampai mendidih, kemudian rebusan kentang tadi disaring menggunakan kain kasa dan diambil sarinya (aquades bekas rebusan), lalu ditambahkan lagi aquades hingga mencapai volume akhir 1 liter, dekstrosa dan agar-agar dimasukkan dan dicampur rata. Setelah mendidih dan tercampur rata, larutan didinginkan dan ditambahkan antibiotik, lalu ditempatkan ke dalam tabung Erlenmeyer yang ditutup dengan kapas dan aluminium foil, kemudian dimasukan kedalam autoklaf selama 15 menit dengan suhu 121ºC. Penuangan PDA dilakukan di dalam tempat atau kondisi steril (lamine air flow).
3.2.2 Sumber Inokulum
Inokulum fungi patogen yang digunakan dalam penelitian ini ada 5 isolat
13
(T38) dan T. pseudokoningii (T39) dari koleksi Dr. Ir. Darmono Taniwiryono, M.Sc di Lab. Bioteknologi LRPI, Bogor. Masing-masing isolat diperbanyak untuk memperoleh persediaan dalam jumlah yang cukup pada saat melakukan uji antagonis.
3.2.3 Peralatan
Alat yang digunakan yaitu berupa gelas piala, Erlenmeyer, pengaduk kaca, tabung reaksi, cawan Petri, lampu Bunsen, jarum ose, cork borrer, autoclave, neraca analitik, oven, lamine air flow, kompor, kamera, kapas, korek api, tally sheet dan alat tulis. Beberapa peralatan seperti cawan Petri, Erlenmeyer, gelas piala, harus disterilisasikan terlebih dahulu dengan menggunakan oven pada suhu 50 ºC selama 1x24jam, sedangkan untuk jarum ose, cork borrer disterilisasikan dengan cara pembakaran.
3.3 Metode Penelitian
3.3.1 Metode Uji Antagonis
Uji antagonisme dalam penelitian ini dilakukan dengan cara metode biakan ganda dengan perbandingan 1 : 1 secara in-vitro dalam satu cawan konfrontasi. Koloni patogen Ganoderma sp. diinokulasikan dalam cawan konfrontasi terlebih dahulu sebelum memasukan koloni fungi antagonis dengan masa inkubasi selama 5 hari sehingga isolat Ganoderma sp. berukuran cukup besar. Kemudian isolat T38 dan T39 ditumbuhkan pada cawan konfrontasi pada sisi yang berlawanan dengan jarak 5cm dari koloni fungi antagonis (Gambar 4).
Zona penghambatan adalah panjang wilayah dalam cawan konfrontasi yang tidak ditumbuhi oleh kedua isolat yang saling antagonis. Pengukuran dilakukan dengan cara mengukur panjang dari zona kosong tersebut. Persentase Penghambatan dihitung dengan rumus yang dipakai Rohana (1998) :
Kelima isolat Ganoderma sp. (L12, L6, L3, K2, dan K1) ditanamkan dalam cawan konfrontasi bersama dengan isolat T38 dan T39. Masing-masing perlakuan memiliki tiga ulangan. Perlakuan yang digunakan dalam penelitian ini dijelaskan pada Tabel 1.
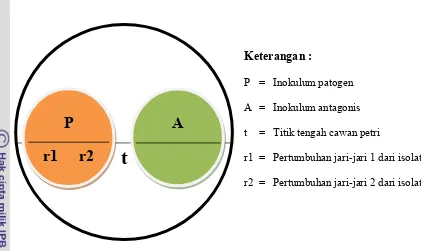
t
A = Inokulum antagonis
t = Titik tengah cawan petri
r1 = Pertumbuhan jari-jari 1 dari isolat
r2 = Pertumbuhan jari-jari 2 dari isolat
Gambar 4 Metode biakan ganda Ganoderma sp. dan Trichoderma sp. pada Cawan konfrontasi berdiameter 9 cm.
15
Tabel 1. Jenis perlakuan Ganoderma sp. dengan Trichoderma sp.
Perlakuan Keterangan
L12 x T38 Isolat Ganoderma L12 ditanamkan bersama Isolat T38
L12 x T39 Isolat Ganoderma L12 ditanamkan bersama Isolat T39
L6 x T38 Isolat Ganoderma L6 ditanamkan bersama Isolat T38
L6 x T39 Isolat Ganoderma L6 ditanamkan bersama Isolat T39
L3 x T38 Isolat Ganoderma L3 ditanamkan bersama Isolat T38
L3 x T39 Isolat Ganoderma L3 ditanamkan bersama Isolat T39
K1 x T38 Isolat Ganoderma K1 ditanamkan bersama Isolat T38
K1 x T39 Isolat Ganoderma K1 ditanamkan bersama Isolat T39
K2 x T38 Isolat Ganoderma K2 ditanamkan bersama Isolat T38
K2 x T39 Isolat Ganoderma K2 ditanamkan bersama Isolat T39
3.3.2 Analisis Statistik
Variabel yang diamati dalam penelitian ini adalah persen penghambatan. Sebagaimana diketahui bahwa faktor yang berpengaruh pada pengendalian secara hayati suatu patogen adalah tanaman inang, patogen atau parasit, lingkungan fisik, dan antagonis (Purwantisari dan Hastuti 2009). Penelitian ini menggunakan analisis statistik dengan model RAL (Rancangan Acak Lengkap) dua faktor. Faktor yang digunakan dalam penelitian ini adalah faktor jenis isolat Ganoderma
sp. dan faktor jenis isolat Trichoderma sp.. Faktor jenis isolat Ganoderma sp. terdiri dari isolat L12, L6, L3, K2 dan K1. Faktor jenis isolat Trichoderma sp. terdiri dari isolat T38 dan T39. Model RAL digunakan karena penelitian ini dilakukan dengan merekayasa lingkungan fisik dan tidak menyertakan tanaman inang. Sehingga faktor pengendalian hayati yang diukur hanya faktor patogen (Ganoderma sp.) dan faktor antagonis (Trichoderma sp.). Pengolahan data menggunakan software SAS 9.
17
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil
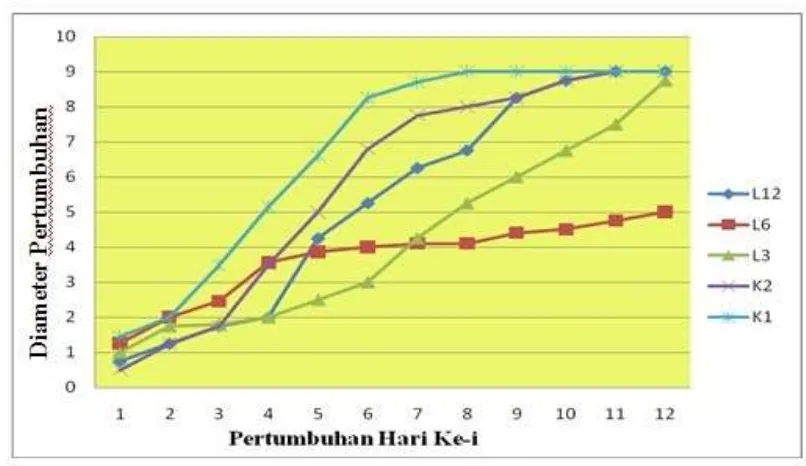
Berdasarkan hasil pengamatan yang dilakukan, diperoleh bahwa pertumbuhan diameter koloni Ganoderma sp. berkembang secara bertahap dan mampu memenuhi cawan petri rata-rata pada hari ke-10. Sedangkan koloni
Trichoderma sp. mampu berkembang secara pesat dan memenuhi cawan petri pada hari ke-5.
Berikut pertumbuhan Ganoderma sp. dan pertumbuhan Trichoderma sp.
Gambar 6 Pertumbuhan Koloni Trichoderma sp.
A B C
D E
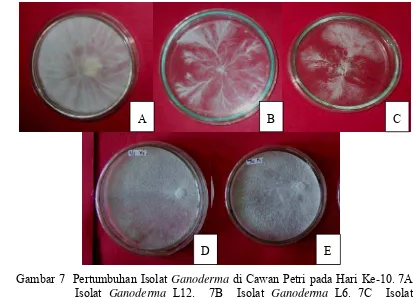
Gambar 7 Pertumbuhan Isolat Ganoderma di Cawan Petri pada Hari Ke-10. 7A Isolat Ganoderma L12. 7B Isolat Ganoderma L6. 7C Isolat
Ganoderma L3. 7D Isolat Ganoderma K2. 7E Isolat Ganoderma
K1
B
A C
19
A B
Gambar 8 Pertumbuhan Isolat Trichoderma sp.di Cawan Petri pada Hari Ke-5. 8A Isolat T38. 8B Isolat T39.
Hasil pengamatan terhadap uji antagonisme isolat T38 dan T39 dengan
Ganoderma sp. adalah sebagai berikut :
Gambar 9 Penghambatan Pertumbuhan in-vitro Ganoderma sp. oleh Trichoderma
sp.
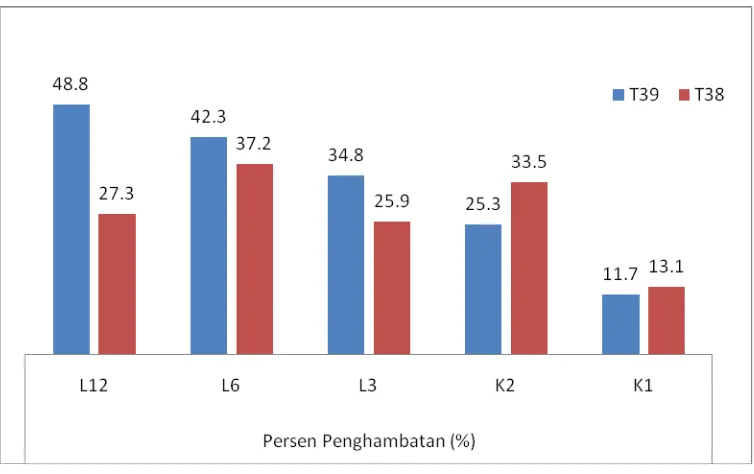
Berdasarkan hasil pengamatan, isolat T39 dan T38 mampu menghambat pertumbuhan koloni Ganoderma L12, L6, L3, K2 dan K1 berturut-turut sebesar rata-rata 27.3, 37.2, 25.9, 33.5 dan 13.1% pada media PDA (Gambar 2). Isolat T39 menghambat pertumbuhan isolat Ganoderma L12, L6, L3, K2 dan K1 berturut-turut sebesar rata-rata 48.8, 42.3, 34.8, 25.3 dan 11.7% pada media PDA (Gambar 2). Hasil pengamatan menunjukan bahwa isolat T38 dan T39 yang diantagoniskan dengan Ganoderma L12, L6, L3, K2 dan K1 tidak menimbulkan
zona penghambatan terhadap kedua patogen tersebut pada media PDA. Dengan nilai rata-rata penghambatan uji antagonis isolat T39 sebesar 32.6% dan isolat T38 sebesar 27.4%.
A
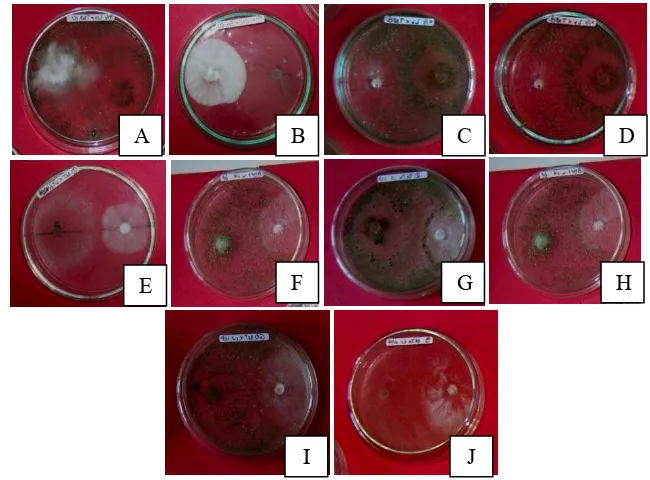
Gambar 10 Pertumbuhan Isolat Ganoderma sp. dan Trichoderma sp. pada Cawan Konfrontasi. 10A Isolat Ganoderma L12*T38. 10B Isolat
Ganoderma L12*T39. 10C Isolat Ganoderma L6*T38. 10D Isolat
Ganoderma L6*T39. 10E Isolat Ganoderma L3*T38. 10F Isolat
Ganoderma L3*T39. 10G Isolat Ganoderma K2*T38. 10H Isolat
Ganoderma K2*T39. 10I Isolat Ganoderma K1*T38. 10J Isolat
Ganoderma K1*T39.
Tabel 2. Rekapitulasi Hasil Sidik Ragam terhadap Variabel yang Diamati
21
Pada hasil data sidik ragam, tidak terlihat perbedaan yang signifikan pada tingkat kepercayaan 95% dari kedua faktor yang diuji. Faktor isolat Ganoderma
sp. hanya berbeda nyata pada tingkat kepercayaan 90%. Faktor isolat
Trichoderma sp. dan interaksi dari kedua faktor tidak berbeda nyata pada tingkat kepercayaan 90%.
Tabel 3. Hasil Uji Duncan Pengaruh Jenis Isolat Ganoderma sp. terhadap Persen Penghambatan
Keterangan: Huruf yang sama dibelakang angka menunjukkan pengaruh yang tidakberbeda nyata pada tingkat kepercayaan 95%.
Tabel 4. Hasil Uji Duncan Pengaruh Jenis Isolat Trichoderma sp. terhadap Persen
Keterangan: Huruf yang sama dibelakang angka menunjukkan pengaruh yang tidak berbeda nyata pada tingkat kepercayaan 95%.
4.2 Pembahasan
Hasil pengamatan visual uji antagonisme Trichoderma sp. dengan
Ganoderma sp. memperlihatkan bahwa pertumbuhan jari-jari koloni Ganoderma
sp. ke arah titik tengah cawan konfrontasi lebih lambat terjadi dari pertumbuhan
Trichoderma sp.. Purwantisari dan Hastuti (2009) menyatakan bahwa
Trichoderma sp. merupakan jenis yang potensial untuk pengendalian penyakit secara hayati. Hasil penelitian yang dilakukan mendukung pendapat tersebut, dimana Trichoderma sp. T38 dan T39 mampu menghambat pertumbuhan koloni patogen berdasarkan hasil uji in-vitro pada PDA.
Perlakuan kontrol koloni Ganoderma sp. menunjukan pertumbuhan diameter koloni patogen yang lebih lambat dibandingkan pertumbuhan koloni
Trichoderma sp.. Setelah dilakukan pengujian pada satu cawan konfrontasi,
Trichoderma sp. mampu menghambat pertumbuhan Ganoderma sp. Fungi yang tumbuh cepat mampu mengungguli dalam penguasaan ruang dan pada akhirnya bisa menekan pertumbuhan fungi lawannya (Suharna dan Widhiastuti, 1966 dalam Purwantisari dan Hastuti, 2009).
masing-23
masing isolat untuk menghambat pertumbuhan mikrooganisme pesaing. Perbedaan ini diduga dipengaruhi oleh jenis, jumlah, dan kualitas dari antibiotik atau zat lain yang dihasilkan Trichoderma sp. yang dapat menghambat pertumbuhan Ganoderma sp.. Adanya penghambatan terhadap pertumbuhan diameter koloni patogen Ganoderma sp. diduga karena adanya enzim dan senyawa metabolit yang terdapat pada fungi antagonis Trichoderma sp. yang mampu merusak dinding sel patogen Ganoderma sp. sehingga menyebabkan pertumbuhan diameter koloni patogen menjadi lambat.
Terbentuknya zona penghambatan antar organisme pada media padat merupakan indikasi bekerjanya mekanisme antibiosis. Bekerjanya mekanisme antibiosis dikuatkan oleh tertekannya pertumbuhan fungi patogen pada media padat. Pada penelitian ini tidak ditemukannya zona penghambatan, hal ini dapat disebabkan karena media yang digunakan adalah PDA. Ternetralisir pengaruh metabolit penghambat pertumbuhan patogen pada PDA (Achmad 1991). Tetapi dapat juga disebabkan tidak terjadinya mekanisme antibiosis dan Trichoderma sp. diduga tidak menghambat pertumbuhan koloni Ganoderma sp. setelah terjadi kontak hifa.
Menurut Smith dan Moss (1985), beberapa anggota genus Trichoderma
sp. menghasilkan toksin (mycotoxin) yaitu trichodermin. Toksin ini dihasilkan oleh cendawan, bila berada atau hidup pada tanaman hidup, bahan yang mengurai, dan produk-produk yang disimpan di gudang. Selain itu, adanya aktifitas metabolik hifa yang tinggi pada bahan organik dapat juga menyerang dan menghancurkan propagul patogen yang ada disekitarnya (Lewis dan Papavizas 1984).
antibiotik (Wells 1988). Anggraeni (2004) menyatakan bahwa Trichoderma sp. dapat digunakan sebagai agen biokontrol melawan beberapa cendawan petogenik tular tanah. Selama Trichoderma sp. tumbuh aktif menghasilkan sejumlah besar enzim ekstra selular ß (1.3) glukonase, dan kitinase, yang dapat melarutkan dinding sel patogen (Lewis dan Papavizas 1984).
25
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Hasil pengujian menunjukan antagonisme antara isolat T38 dan T39 dengan kelima isolat fungi patogen tersebut tidak menimbulkan terbentuknya zona penghambatan pada media PDA. Kemampuan antagonistik kedua isolat fungi antagonis juga ditunjang oleh pertumbuhan diameter koloni yang lebih pesat dibanding kelima isolat patogen Ganoderma sp. pada PDA.
Pertumbuhan isolat Ganoderma sp. dari yang paling cepat berturut-turut kemudian semakin lambat adalah Ganoderma K2, L12, K1, L3 dan L6. Isolat T38 dan T39 mampu menghambat pertumbuhan koloni kelima jenis fungi patogen, berdasarkan hasil percobaan in vitro pada PDA. Kemampuan tersebut menunjukan bahwa kedua jenis fungi antagonis diharapkan dapat dimanfaatkan sebagai agensia dalam pengendalian penyakit akar Ganoderma sp..
Dari kedua jenis fungi antagonis yang diuji isolat T39 memiliki potensi antagonistik yang lebih kuat dibanding isolat T38 dengan kemampuan menghambat pertumbuhan fungi patogen dengan persentase penghambatan lebih tinggi berturut-turut pada isolat Ganoderma L12, L6 dan L3.
5.2. Saran
DAFTAR PUSTAKA
Achmad S. 1991. Kemampuan Rhizopogon sp. untuk Perlindungan Hayati terhadap Penyebab Penyakit Lodoh pada Pinus merkusii [Tesis]. Bogor: Program Pascasarjana, IPB.
Achmad S. 1997. Mekanisme Serangan Patogen dan Pertahanan Inang serta Pengendalian Hayati Penyakit Lodoh pada Pinus merkusii. [Disertasi] Bogor: Program Pascasarjana, IPB.
Anggraeni I. 2004. Identifikasi dan Patogenitas Penyakit Akar pada Acacia mangium Willd. Buletin Penelitian Hutan. 645: 61-73.
Anonim. 2011. Ganoderma Lucidum.
http://en.wikipedia.org/wiki/Ganoderma_lucidum [02 Mei 2011]
Agrios GN. 1996. Ilmu Penyakit Tumbuhan. Ed. ke-3 . Busnia M., Penerjemah; Martoredjo T., editor. Yogyakarta: Gajah Mada Univ. Press. Terjemahan dari: Plant Pathology. 803p.
Alexopoulos CJ, Mims CW, Blackwel M. 1996. Introductory Mycology. New York: John Willey and Sons inc. 868p.
Atmosuseno BS. 1998. Budidaya, Kegunaan, dan Prospek Sengon. Jakarta : Penebar Swadaya. 1189p.
Besset K Peters. 2003. Ganoderma: A Significant Root Pathogen. Arborilogical
Services Inc. Publication. http://www.arborilogical.com/articles/ganoderma.htm. [6 Februari 2010]
Chet I (Ed.). 1987. Innovative Approaches to Plant Diseases Control. John Wiley and Sons, A Wiley-Interscience Publication, USA. pp. 11-210.
Cook RJ, Baker KF. 1989. The Nature on Practice of Biological Control of Plant Pathogens. ABS press, The American Phytopathological Society, St. Paul, Minesota 539 p.
Gandjar I, Samson RA, Tweel-Vermeulen K, Oetari A, Santoso I. 1999. Pengenalan Kapang Tropik Umum. Universitas Indonesia. Depok, Jakarta. Hlm. 133-134.
Garret SD. 1956. Biology of Root Infecting Fungi. University Press Cambridge. England. 293 p.
27
Haryono, Widyastuti SM. 2001. Potensi Antagonistik Tiga Trichoderma spp terhadap 8 Penyakit Akar Tanaman Kehutanan. Buletin Kehutanan (41). Kehutanan UGM. Yogyakarta.
Jong SC, Birmingham JM. 1992. Medicinal Benefits of the Mushroom
Ganoderma. J. of Advances in Applied Microbiology, 37: 101-134.
Karsten P. 1881. "Enumeratio Boletinearum et Polyporearum Fennicarum, Systemate novo dispositarum". Rev. Mycol. (Toulouse) 3: 16-19.
Lewis JA, Papavizas GC. 1983. Production of Clamidospores and Conidia by
Trichoderma sp. In Liquid and Solid Growth Media. J. Soil Biology and Biochemistry, 15 (4): 351-357.
Marta AK. 2005. Pengaruh Berbagai Jenis Serbuk Kayu Sengon (Paraserianthes falcataria) pada Makanan Buatan (Artificial Diet) terhadap Pertumbuhan Larva Boktor (Xystrocera festiva Pascoe) [Skripsi]. Bogor : Fakultas Kehutanan. Institut Pertanian Bogor. Tidak dipublikasikan.
Mudawarman. 2009. Fungi. file:///D:/SKRIPSI/perbaikan%20sidang/FUNGI%20%C2%AB%20Mudarw
an%E2%80%99s%20Blog.htm [15 Mei 2011]
Murrill WA. 1908. Polyporaceae (Agaricales). J. North America Flora 9 (2): 73-131.
Muthahanas I, Listiana E. 2008. Skrining Streptomyces sp. Isolat Lombok sebagai Pengendali Hayati Beberapa Fungi Patogen Tanaman. J. Crop Argo 1(2): 130-136.
Mycobank. 2000. Trichoderma Pseudokoningii Rifai 1969. http://www.mycobank.org/BioloMICSServer.aspx?Link=T&Rec=340304. [28 Mei 2011].
Purwantisari S, Hastuti RB. 2009. Uji Antagonisme Fungi Patogen Phytophthora infestans Penyebab Penyakit Busuk Daun dan Umbi Tanaman Kentang dengan Menggunakan Trichoderma sp. Isolat Lokal. J. BIOMA 11(1): 24-32.
Rifai MA. 1964. A Revision of Genus Trichoderma. University of Sheffield, England, page 56.
Rimbawanto A. 2008. Pemuliaan Tanaman dan Ketahanan Penyakit pada Sengon. Yogyakarta: Balai Besar Penelitian Bioteknologi dan Pemuliaan Tanaman Hutan.
Samuel GJ, P Chaverri, DF Farr, EB Mc Cray. 2005. Trichoderma Online, Systematic Botany and Microbiology Laboratory, ARS, USDA. http://nt.arsgrin.gov/taxadesciptions/keys/TrichodermaIndex.cfm [14 Mei 2011]
Semangun H. 2000. Penyakit-Penyakit Tanaman Perkebunan Indonesia. Yogyakarta: Gajah Mada Univ Press. 808p.
Sinulingga W. 1989. Pengendalian Biologi Penyakit Cendawan Akar Putih pada Tanaman Karet. Pusat Penelitian Perkebunan Sei. Putih, Galang. Hal. 1-7. Smith JE, Moss MO. 1985. Mycotoxin, Formation Analysis and Significance.
John Willey and Sons, inc. New York. 148p.
Solomon JD, Leininger TD., Wilson AD, Anderson RL, Thompson LC, McCracken FI. 1993. Ash Pests: A Guide to Major Insect, Diseases, Air Pollution Injury and Chemical Injury. Gen. Tech. Rep. SO-96. New Orleans, LA: U.S. Department of Agriculture, Forest Service , Southern Forest Experiment Station. 45p.
Sumardi, Widiastuti SM. 2001. Pemanfaatan Sabut Kelapa untuk Pengembangan Budidaya Fungi Ganoderma sebagai Bahan Obat Tradisional di Daerah Sekitar Hutan. J. ASPI 2(5): 12-52.
Susanto, A. 1998. "Sifat-sifat Biokimiawi dan Fabrikasi Ganoderma, Fungi Patogen Pohonan" Jurnal Perlindungan Tanaman Indonesia, Vol. 4 (2): 83-91.
Suwanto A, Friska AH, Sudirman LMI. 1996. Karakteristik Pseudomonas fluorescens B29 dan B39: Profil DNA Genom, Uji Hipersensitif dan Asai senyawa Biotik. J. Hayati 3(1): 15-20.
Tjitrosoepomo, Gembong. 1994. Morfologi Tumbuhan, Gadjah Mada University Press;Yogyakarta.
Turner PD. 1981. Diseases and Disorders of the Oil Palm in Malaysia. Oxford University Press.
Wells HD. 1998. Trichoderma as A Biocontrol Agent. dalam Biocontrol of Plant Disease , Vol 1. Mukerji KG, Garg KL (ed.). CRC Press, Inc. Boca Raton, Florida. 72-79.
Widyastuti SM. 2007. Peran Trichoderma spp. dalam Revitalisasi Kehutanan di Indonesia. Yogyakarta: Gajah Mada University Press, 255p.
29
Lampiran 1. Pertumbuhan Ganoderma sp.
Tabel 5. Pertumbuhan Ganoderma sp. pada Cawan Petri (Kontrol)
Lampiran 2. Pertumbuhan Trichoderma sp.
Tabel 6. Pertumbuhan Trichoderma sp. pada Cawan Petri (Kontrol)
Lampiran 3. Persen Penghambatan Uji Antagonis Trichoderma sp dan
Ganoderma sp.
Tabel 7. Persen Penghambatan Uji Antagonis Trichoderma sp dan Ganoderma sp.
Fungi
Pertumbuhan Hari Ke-i (cm)
1 2 3 4 5 6 7 8 9 10
L12 0.75 1.25 1.75 2 4.25 5.25 6.25 6.75 8.25 8.74
L6 1.25 2 2.45 3.55 3.85 4 4.1 4.1 4.4 4.5
L3 1 1.75 1.8 2 2.5 3 4.25 5.25 6 6.75
K2 0.5 1.25 1.75 3.5 5 6.8 7.75 8 8.25 8.75
K1 1.45 2 3.5 5.15 6.6 8.25 8.7 9 9 9
Fungi
Pertumbuhan Hari Ke-i (cm)
1 2 3 4 5
T39 0.5 1.25 4.5 6.35 8.75
T38 0.25 1 5.25 7.5 9
Fungi
Persen Penghambatan (%)
Rata-rata (%)
L12 L6 L3 K2 K1
T39 48.8 42.3 34.8 25.3 11.7 32.6
31
Lampiran 4. Hasil Uji Sidik Ragam terhadap Variabel yang Diamati dengan Menggunakan Sofware SAS 9
The GLM Procedure
Dependent Variable: Persen Penghambatan
Source DF Sum of Squares Mean Square F Value Pr > F Model 9 3755.921563 417.324618 1.46 0.2293 Error 20 5716.893133 285.844657 Corrected Total 29 9472.814697
R-Square Coeff Var Root MSE Persen Penghambatan Mean 0.396495 56.41979 16.90694 29.96633
Source DF Type I SS Mean Square F Value Pr > F
F1 4 2799.780413 699.945103 2.45 0.0796 F2 1 203.684963 203.684963 0.71 0.4086
Lampiran 5. Hasil Uji Lanjut Duncan Pengaruh Jenis Isolat Ganoderma sp. terhadap Persen Penghambatan dengan Menggunakan Sofware SAS 9
The GLM Procedure
Duncan's Multiple Range Test for Persen Penghambatan
Note: This test controls the Type I comparisonwise error rate, not the experimentwise error rate.
Alpha 0.05 Error Degrees of Freedom 20 Error Mean Square 285.8447
Number of Means 2 3 4 5 Critical Range 20.36 21.37 22.02 22.46
Means with the same letter are not significantly different. Duncan Grouping Mean N F1
A 39.592 6 L6
A
A 38.060 6 L12
A
B A 30.367 6 L3
B A
B A 29.397 6 K2
B
33
Lampiran 6. Hasil Uji Lanjut Duncan Pengaruh Jenis Isolat Trichoderma sp. terhadap Persen Penghambatan dengan Menggunakan Sofware SAS 9
The GLM Procedure
Duncan's Multiple Range Test for RESPON
Note: This test controls the Type I comparisonwise error rate, not the experimentwise error rate.
Alpha 0.05 Error Degrees of Freedom 20 Error Mean Square 285.8447
Number of Means 2 Critical Range 12.88
Means with the same letter are not significantly different.
Duncan Grouping Mean N F2
A 32.572 15 T39
A