EKSTRAK KAYU SECANG (Caesalpinia sappan)
RETNO DJULAIKA
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Pencarian dan Pengoptimuman
Sidik Jari Kromatografi Cair Kinerja Tinggi Ekstrak Kayu Secang (Caesalpinia
sappan) adalah karya saya dengan arahan dari komisi pembimbing dan belum
diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir tesis ini.
Bogor, Juli 2011
Retno Djulaika
ABSTRACT
RETNO DJULAIKA. Optimization High Performance Liquid Chromatographic
Fingerprint of sappan wood (Caesalpinia sappan). Under direction of LATIFAH
K. DARUSMAN and RUDI HERYANTO
Mixture design has been applied for optimization of Caesalpinia sappan
chromatographic fingerprint. The design applied for unreplicated and simultaneous optimization of HPLC mobile phase mixture. Ethanol extracts with highest antioxidant activity resulted from sonication extraction method was chosen for HPLC analysis . The reversed phase chromatographic mobile phase in simplex centroid design consist of varying proportion of methanol 50 %, methanol: water: TFA (25: 75: 0.025 v/v), and methanol: water: TFA (15: 85: 0.035 v/v). Ethanol 70 % extract of sappan analyzed with ten mobile phase and monitored at 254 and 280 nm. Correlation between HPLC mobile phase and a number of peak analyzed statistically by SAS 9.2. The root mean square errror of calibration (RSMEC) and root mean square errror of calibration (RSMEP) at 254 and 280 nm, were 8.3006 and 8.29659, 3.88730 and 4.85193 respectively. Optimum condition obbtained when ethanol 70 % extract eluted by methanol: water: TFA (15: 85: 0.035 v/v), with the 15 number of peaks.
RETNO DJULAIKA. Pencarian dan Pengoptimuman Sidik Jari Kromatografi Cair Kinerja Tinggi Ekstrak Kayu Secang (Caesalpinia sappan). Dibimbing oleh LATIFAH K. DARUSMAN dan RUDI HERYANTO.
Secang (Caesalpinia sappan) merupakan bahan baku obat herbal yang memiliki khasiat sebagai pembersih darah, antikanker, immunostimulan, antimikroba, serta antibakteri. Sejauh ini kualitas secang ditentukan berdasarkan kandungan senyawa tunggal yaitu brazilin. Hal ini dinilai kurang memadai karena khasiat obat herbal disumbangkan oleh sejumlah senyawa kimia yang bekerja secara sinergis.
Penggunaan sidik jari kromatografi cair kinerja tinggi (KCKT) untuk kontrol kualitas obat herbal dapat menjadi pendekatan yang efektif karena dapat menjelaskan karakteristik obat herbal secara komprehensif. Pada penelitian ini dilakukan pengoptimuman sidik jari KCKT ekstrak kayu secang menggunakan bantuan mixture design. Kayu secang yang digunakan berasal dari Semarang dengan kadar air 8.44 ± 0.24 % dan siap untuk diekstraksi. Ekstraksi dilakukan dengan dua teknik yang berbeda yaitu teknik sonikasi dengan waktu ekstraksi 3 x 0.5 jam dan maserasi dengan waktu ekstraksi 3 x 24 jam menggunakan pelarut etanol 70 %, memberikan nilai rendemen dan IC50 berturut-turut 10.30 ± 2.24 %
dan 25.37 ± 0.45 µg/mL, 12.87 ± 0.52 % dan 89.92 ± 3.11 µg/mL. Ekstrak etanol secang dipisahkan dengan KCKT fase terbalik menggunakan sepuluh kombinasi fase gerak sesuai mixture design yang mengambil bentuk simplex-centroid.
Rancangan ini digunakan untuk mempelajari pengaruh fase gerak tunggal, campuran dua fase gerak, dan campuran tiga pelarut terhadap sidik jari kromatografi yang dihasilkan. Fase gerak yang digunakan pada penelitian ini adalah metanol 50 %, metanol:air:TFA (25:75:0.025 v/v), dan metanol:air:TFA (15:85:0.035 v/v).
Jumlah puncak yang muncul pada kromatogram KCKT ekstrak kulit kayu secang dihitung berdasarkan kriteria nilai resolusi dan rasio sinyal terhadap derau (S/N). puncak diakui dan dihitung jika memiliki nilai resolusi 1 dan nilai S/N 3. Nilai resolusi 1 digunakan sebagai batasan karena suatu puncak dikatakan terpisah apabila memiliki nilai resolusi 1 (Dong 2006). Nilai S/N 3 dipilih karena nilai ini umum digunakan untuk menentukan nilai limit deteksi (Bliesner 2006). Informasi nilai resolusi dan S/N diperoleh melalui pengolahan kromatogram ekstrak menggunakan perangkat lunak LC solution yang terintegrasi dengan KCKT Shimadzu varian LC-20 AD yang digunakan pada penelitian ini.
Model interaksi fase gerak yang menggambarkan pengaruh fase gerak KCKT terhadap jumlah puncak KCKT dibangun dari sepuluh data dengan menggunakan perangkat lunak SAS 9.2.
Pengolahan data dimulai dengan menentukan nilai koefisien setiap interaksi fase gerak KCKT menggunakan persamaan:
ŷ = b1x1 + b2x2 + b3x3 + b12x1x2 + b13x1x3 + b23x2x3 + b123x1x2x3
model interaksi fase gerak. Untuk panjang gelombang 254 nm didapatkan model interaksi fase geraknya ŷ = 20.78x2 + 14.87x3, sedangkan model interaksi fase
gerak pada panjang gelombang 280 nm adalah ŷ = 9.30x2 + 13.76x3. Model
interaksi fase gerak yang dibangun menunjukkan bahwa fase gerak yang berpotensi meningkatkan puncak pada deteksi dengan panjang gelombang 254 dan 280 nm adalah metanol:air:TFA (25:75:0.025) dan metanol:air:TFA (15:85:0.035).
Nilai root mean square error of calibration (RMSEC) dan root mean
square error of prediction (RMSEP) untuk panjang gelombang 254 dan 280 nm
berturut-turut adalah 8.30060 dan 8.29659, 3.88730 dan 4.85913. Berdasarkan nilai RMSEC dan RMSEP, model interaksi fase gerak terbaik dibangun dari data pada panjang gelombang deteksi 280 nm karena memiliki nilai RMSEC dan RSMEP yang lebih kecil dibanding pada panjang gelombang 254 nm.
Optimasi dilakukan berdasarkan profil KCKT yang diperoleh, model interaksi fase gerak terbaik, dan plot kontur ekstrak. Kondisi optimum pada deteksi dengan panjang gelombang 280 nm dicapai saat ekstrak etanol 70 % dipisahkan dengan fase gerak metanol: air: TFA (15:85:0.035 v/v) yaitu dengan jumlah puncak terdeteksi 15.
© Hak Cipta Milik IPB, tahun 2010
Hak Cipta dilindungi Undang-undang
Dilarang mengutip sebagian atau seluruhnya karya tulis ini tanpa mencantumkan atau menyebutkan sumber. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
PENCARIAN DAN PENGOPTIMUMAN FASE GERAK SIDIK
JARl KROMATOGRAFI CAIR KINERJA TINGGI EKSTRAK
KAYU SECANG (
Caesalpinia sappan
)
RETNO DJULAIKA
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Kimia
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Sappan)
Nama : Retno Djulaika
NIM : G451090101
Disetujui Komisi Pembimbing
Prof. Dr. Ir. Latifah K. Darusman, M.S. Ketua
Diketahui
Ketua Program Mayor Kimia Dekan Sekolah Pascasarjana
Prof. Dr. Purwantiningsih Sugita, M.S. Dr. Ir. Dahrul Syah, M.Se.Agr.
PRAKATA
Puji dan syukur penulis panjatkan ke hadirat Allah SWT atas rahmat dan karunia-Nya sehingga karya ilmiah ini dapat diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Februari sampai Juli 2011 ini ialah Pencarian dan Pengoptimuman Fase Gerak Sidik Jari Kromatografi Cair
Kinerja Tinggi Ekstrak Kayu Secang (Caesalpinia sappan).
Ucapan terima kasih yang tulus kepada Prof. Dr. Ir. Latifah K. Darusman, M.S. dan Rudi Heryanto S.Si, M.Si selaku pemnimbing, atas segala curahan waktu, bimbingan, arahan, serta dorongan moral, Dr. Irmanida Batubara, S.Si, M.Si selaku penguji luar komisi yang telah memberikan banyak saran untuk perbaikan tesis ini. Di samping itu, penghargaan penulis sampaikan pada Wulan Tri Wahyuni S.Si, M.Si, Ibu Ani andriati S.Si, M.Si yang telah memberikan banyak saran dan masukan, Agung Zaim STP, M.Si dari Pusat Studi Biofarmaka IPB yang telah membantu selama pengujian bahan. Terimakasih kepada Pusat Studi Biofarmaka yang telah memberikan tema penelitian dalam grup penelitian kayu secang. Ungkapan terima kasih juga disampaikan kepada Ibu, Bapak, Abang Zulfahmi, Nabiha, Abida, dan Tsabita serta seluruh keluarga, atas segala doa, kasih sayang, dan pengorbanannya, Yenti Hariyani, Tri Hayati, Yusridah Hasibuan dan rekan-rekan pascasarjana mayor kimia angkatan 2009 atas dorongan semangat dan bantuannya serta kepada Kementerian Agama Republik Indonesia yang telah mendanai pendidikan penulis selama menjalani program pascasarjana Kimia IPB.
Semoga karya ilmiah ini bermanfaat
Bogor, Juli 2011
RIWAYAT HIDUP
Penulis dilahirkan di Pekalongan pada tanggal 08 Agustus 1977 dari pasangan Bapak Djahri dan Ibu Suwarsi (alm). Penulis merupakan anak keempat dari empat bersaudara.
Tahun 1996 penulis lulus dari SMAN Wiradesa dan pada tahun yang sama lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB (USMI). Pendidikan sarjana ditempuh di Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam. Selama mengikuti perkuliahan, penulis pernah menjadi asisten mata kuliah Kimia Dasar (D-3 Kehutanan), dan Biokimia (S1-FKH) pada tahun 2000.
Halaman
DAFTAR TABEL ... xix
DAFTAR GAMBAR ... xxi
DAFTAR LAMPIRAN ... xxiii
PENDAHULUAN ... 1
Metode Pengujian DPPH ... 10
Pengoptimuman Kondisi Kromatografi ... 10
Analisis Data Pemisahan Kromatografi Cair Kinerja Tinggi (KCKT) ... 11
HASIL DAN PEMBAHASAN ... 12
DAFTAR TABEL
Halaman
1 Tiga faktor simplex-centroid ... 9
2 Penentuan kadar air ... 14
3 Nilai IC50 ekstrak kayu secang………. ... 15
4 Desain variabel dan respon ………. ... 18
5 Model interaksi fase gerak pada panjang gelombang 254 dan 280 nm…... 19
6 Nilai RMSEC dan RSMEP pada panjang gelombang 254 dan 280 nm….. 20
DAFTAR GAMBAR
Halaman 1 Tanaman secang ... 3 2 Reaksi penangkapan radikal bebas DPPH ... 5 3 Simplex-lattice, simplex-centroid, simplex-centroid dengan axial design ... 8
4 Komposisi fase gerakKCKT sesuai dengan mixture design ... 12
5 Kromatogram KCKT ekstrak etanol 70 % dengan fase gerak
metanol: air: TFA (15:85:0.035 v/v) ... 17
6 Sidik jari KCKT pada panjang gelombang 280 nm ... 22
DAFTAR LAMPIRAN
Halaman 1 Bagan alir penelitian ... 25 2 Penentuan kadar air ... 26 3 Penentuan aktivitas antioksidan ... 26
PENDAHULUAN
Latar Belakang
Secang (Caesalpinia sappan L.) merupakan salah satu tanaman yang
memiliki banyak khasiat dalam pengobatan di antaranya sebagai pembersih darah,
antikanker (Park et al. 2002; Eun et al. 2005), ekspektoran, antioksidan
(Yingming et al. 2004), immunostimulan, antimikroba (Lim et al. 2007),
antikomplementary, antibakteri (Xu & Lee 2004) serta antimikroba (Lim et al.
2007). Secang dapat dikembangkan sebagai bahan antioksidan dalam kosmetik
dan antijerawat (Batubara et al. 2010). Di Indonesia, secara tradisional secang
digunakan untuk perawatan kulit oleh masyarakat di kepulauan Sumbawa. Secang
juga digunakan sebagai pewarna merah alami pada minuman tradisional
masyarakat Betawi, yang dikenal dengan nama bir pletok. Oleh karena banyaknya
manfaat dari secang maka perlu dilakukan kendali mutu ekstrak secang.
Metode yang umum digunakan dalam proses standardisasi/kontrol kualitas
bahan baku atau ekstrak penyusun obat herbal adalah dengan menunjukkan kadar
satu atau beberapa senyawa penciri. Namun demikian, analisis senyawa penciri
untuk kontrol kualitas dinilai kurang memadai karena khasiat tanaman obat
disumbangkan oleh sejumlah senyawa kimia yang bekerja secara sinergis (Liang
et al. 2004) sehingga diperlukan suatu metode analisis untuk mengatasi masalah
tersebut. Salah satunya adalah dengan menggunakan pendekatan multi komponen
atau analisis sidik jari.
Analisis sidik jari kromatografi telah digunakan dalam kontrol kualitas
tanaman dan produk akhirnya, serta menjadi teknik yang sangat berguna untuk
kontrol kualitas obat-obat herbal (Lai et al. 2007; Delaroza dan Scarminio 2008).
Analisis sidik jari membantu dalam hal klasifikasi dan validasi spesies botani serta
kontrol kualitas dari tanaman obat (Borges et al. 2007). Model kontrol kualitas
berdasarkan sidik jari kromatografi dapat menjadi teknik alternatif untuk
memonitor kualitas tanaman obat. Seluruh senyawa kimia yang dikandung oleh
tanaman obat tertentu dapat ditampilkan dalam sidik jari kromatografi sehingga
2009). Teknik ini telah direkomendasikan untuk kontrol kualitas tanaman obat
oleh Food and Drug Administration (FDA) dan European Medicines Agency
(EMEA) (Borges et al. 2007). Bahkan pada tahun 2004, State Food & Drug
Administration of China (SFDA) mewajibkan semua obat-obat suntik yang dibuat
dari tanaman obat atau material kasarnya harus distandarisasi dengan sidik jari
kromatografi (Lai et al. 2007).
Dalam rangka mengembangkan model kontrol kualitas tanaman secang,
diperlukan sidik jari kromatografi ekstrak secang yang informatif dan mampu
menampilkan semaksimal mungkin komponen kimia dengan resolusi yang baik.
Sidik jari ekstrak secang yang informatif dapat diperoleh melalui pengoptimuman
faktor-faktor yang mempengaruhi waktu retensi, resolusi, jumlah puncak, dan luas
puncak kromatografi. Faktor tersebut meliputi metode dan pelarut ekstraksi,
kondisi instrumen kromatografi, dan fase gerak kromatografi (Borges et al. 2007).
Penelitian ini merupakan pengembangan penelitian sebelumnya yang
dilakukan oleh Sa´diah et al. (2010) yang telah mengembangkan kontrol kualitas
ekstrak etanol 50 % kayu secang berdasarkan senyawa penciri brazilin, dengan
fase gerak metanol dan trifluoraasetat 0.05 % (TFA 0.05 %) secara gradien. Pada
penelitian ini akan dikembangkan metode kontrol kualitas ekstrak etanol 70 %
kayu secang berdasarkan analisis sidik jari kromatografi cair kinerja tinggi
(KCKT) dengan tetap melibatkan senyawa penciri. Pengoptimuman dilakukan
terhadap fase gerak KCKT. Komposisi fase gerak KCKT menentukan baik
tidaknya pemisahan setiap senyawa yang dikandung dalam ekstrak secang dalam
KCKT.
Tujuan
Penelitian bertujuan melakukan pengoptimuman fase gerak KCKT dengan
mixture design untuk memperoleh sidik jari kromatografi ekstrak secang yang
TINJAUAN PUSTAKA
Secang (Caesalpinia sappan)
Tanaman secang termasuk famili fabaceae. Tanaman ini merupakan
tumbuhan perdu yang memanjat atau pohon kecil, berduri banyak, dengan tinggi
mencapai 5-10 m. Batang dan percabangannya berduri, berwarna coklat
keunguan, sedangkan ranting dan tunasnya berbulu kecoklatan. Daunnya
bertumpu, bersirip ganda, dan panjangnya mencapai 50 cm. Bunganya berwarna
kuning dan berbuah polong yang merekah setelah matang. Akarnya berserabut
dan berwarna gelap (Gambar 1).
Gambar 1. Tanaman secang (dokumen pribadi).
Tanaman secang tersebar di Asia Tenggara, Afrika, dan Amerika. Hasil
isolasi yang dilakukan terhadap secang menunjukkan adanya senyawa diterpenoid
(Yodsaue 2007), senyawa aktif flavonoid dan fenolik, yaitu 4-0-metilsapanol,
protosappanin A, protosappanin B, protosappanin E, brazilin, brazilein, caesalpini,
brazilide A, neosapanone, 7,3,4-trihidroksi-3-benzil-2H (Batubara at al. 2010).
Secang merupakan salah satu tanaman yang memiliki banyak khasiat dalam
pengobatan di antaranya sebagai pembersih darah, antikanker (Park et al. 2002;
Lee 2004), serta immunostimulan, antimikroba (Lim et al. 2007). Secang dapat
dikembangkan sebagai bahan antiioksidan dalam kosmetik. Ekstrak metanol
maupun ekstrak etanol 50% merupakan ekstrak yang paling berpotensi sebagai
antijerawat berdasarkan aktivitasnya menghambat pertumbuhan bakteri
propionibakterium acnes, serta menghambat aktivitas lipase (Batubara et al.
2010).
Ekstraksi
Ekstraksi merupakan metode pemisahan suatu zat terlarut secara selektif
dari suatu bahan dengan pelarut tertentu. Pemilihan metode yang tepat tergantung
pada tekstur, kandungan air tanaman yang diekstraksi, dan jenis senyawa yang
akan diisolasi (Harborne 1987).
Metode ekstraksi maserasi umum digunakan untuk mengekstraksi sampel
yang relatif tidak tahan panas. Metode ini hanya dilakukan dengan merendam
sampel dalam suatu pelarut dengan jangka waktu tertentu, biasanya dilakukan
selama 24 jam tanpa menggunakan pemanas. Kelebihan metode ini diantaranya
sederhana dan bisa menghindari kerusakan komponen senyawa akibat panas.
Kelemahan metode ini ditinjau dari segi waktu dan penggunaan pelarut yang tidak
efektif dan efisien karena jumlah pelarut relatif banyak dan waktunya lebih lama
(Meloan 1999).
Metode ekstraksi sonikasi memanfaatkan gelombang ultrasonik dengan
frekuensi 42 kHz yang dapat mempercepat waktu kontak antara sampel dan
pelarut meskipun pada suhu ruang. Hal ini menyebabkan proses perpindahan
massa senyawa bioaktif dari dalam sel tanaman ke pelarut menjadi lebih cepat.
Sonikasi mengandalkan energi gelombang yang menyebabkan proses kavitasi,
yaitu proses pembentukan gelembung-gelembung kecil akibat adanya transmisi
gelombang ultrasonik untuk membantu difusi pelarut ke dalam dinding sel
tanaman (Ashley et al. 2001).
Aktivitas Antioksidan
Secara umum, antioksidan didefinisikan sebagai senyawa yang dapat menunda,
adalah zat yang dapat menunda atau mencegah terjadinya reaksi oksidasi radikal
bebas. Terdapat dua kategori antioksidan yaitu antioksidan alami dan antioksidan
sintetik. Antioksidan alami dapat berupa senyawa fenolik (tokoferol, flavonoid,
dan antioksidan), senyawa nitrogen (alkaloid, turunan klorofil, asam amino, dan
amina), atau karotenoid seperti asam askorbat (Apak et al. 2007).
Antioksidan memiliki banyak manfaat bagi kesehatan seperti mencegah
penyakit kanker, mencegah penuaan dini, kerusakan kulit dan penyakit-penyakit
lain (Yuwono 2009). Sebagian besar penyakit jerawat dengan kondisi kronis dapat
disebabkan oleh stres oksidatif, sehingga diperlukan antioksidan untuk
mengurangi stres oksidatif tersebut pada penderita penyakit jerawat kronis
(Batubara et al. 2009).
Aktivitas antioksidan dapat diukur dengan menggunakan metode
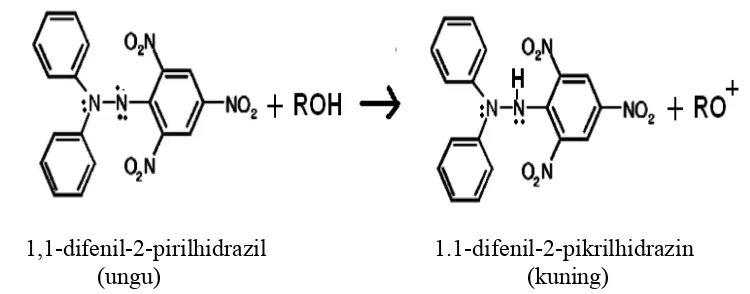
penangkapan radikal bebas stabil DPPH (1,1-diphenyl-2-picrylhidracyl). DPPH
adalah suatu radikal bebas stabil, berwarna ungu dalam larutan dan dapat bereaksi
dengan radikal lain membentuk suatu senyawa stabil. Selain itu DPPH juga dapat
bereaksi dengan atom hidrogen (berasal dari suatu antioksidan) membentuk DPPH
tereduksi (DPPH Hidrazin) yang stabil. Aktivitas antioksidan dinyatakan dengan
persentase penghambatan (inhibisi) yang diperoleh dari nilai absorbansi blanko
dikurangi absorbansi sampel. Metode DPPH adalah metode yang cepat, mudah,
dan sensitif untuk mengukur aktivitas antioksidan suatu ekstrak tumbuhan
(Pourmorad 2006).
1,1-difenil-2-pirilhidrazil 1.1-difenil-2-pikrilhidrazin (ungu) (kuning)
Gambar 2. Reaksi penangkapan radikal bebas DPPH (Prakash 2001).
Sidik Jari Kromatografi Cair Kinerja Tinggi (KCKT)
Kromatografi Cair Kinerja Tinggi (KCKT) memisahkan komponen
berdasarkan interaksi komponen dengan fase gerak berupa cairan dan fase diam.
Fase gerak mengalir dengan bantuan tekanan. Komponen yang dipisahkan
teramati sebagai puncak dengan waktu retensi tertentu. Kadar komponen
ditunjukkan oleh luas masing-masing puncak (Ahuja & Rasmussen 2007).
Hasil pemisahan KCKT disajikan dalam kromatogam atau sidik jari
kromatografi. Parameter yang diukur pada analisis sidik jari KCKT meliputi
waktu retensi, resolusi, jumlah puncak, dan luas puncak. Parameter yang banyak
digunakan untuk evaluasi sidik jari kromatografi adalah jumlah puncak (Borges et
al. 2007; Delaroza & Scarminio 2008). Puncak yang diharapkan adalah puncak
yang tajam. Beberapa parameter kromatogram diantaranya adalah nilai resolusi,
jumlah pelat teoritis (N), dan rasio sinyal terhadap derau (S/N).
(1) Resolusi menggambarkan keterpisahan dua buah pita atau puncak. Puncak
dikatakan benar-benar terpisah jika memiliki nilai R > 1.5, ukuran keterpisahan
antar puncak dapat dihitung dengan menggunakan rumus R=2(tRB–tRA)/wA+wB;
(2) Jumlah pelat teoritis (N) berhubungan dengan efisiensi kolom yang berkaitan
dengan kemampuan untuk menghasilkan puncak yang tajam, N dihitung secara
eksperimental melalui persamaan N = tR2/W atau N = 16 VR2/W; (3) Rasio sinyal
terhadap derau (S/N), sinyal adalah informasi yang diinginkan, selain
menghasilkan sinyal yang diinginkan, instrumen yang digunakan juga
menghasilkan noise atau derau, yang dapat merupakan nilai limit deteksi alat,
pengaruh arus, atau interferen (Currell 2000).
KCKT banyak digunakan untuk kontrol kualitas Tradicional Chinese
medicines (TCM) karena memiliki katelitian yang tinggi, sensitif, dan memiliki
ketersalinan yang baik (Zhang et al. 2008). Sidik jari kromatografi memberikan
informasi yang lebih banyak, valid, dan efisien dalam kontrol kualitas obat herbal
dibandingkan dengan metode analisis tradisional (Lai et al. 2007). Sidik jari
kromatografi obat herbal yang dihasilkan bersifat sangat khas. Sidik jari
mempresentasikan senyawa aktif yang terdapat dalam obat herbal dan interaksi
yang terjadi antara komponen aktif maupun antara komponen aktif dengan fase
kualitas Schisandra chinensis (Zhu et al. 2007), green tea (Almeida & Scarminio
2007), Bauhinia variegata (Delaroza & Scarminio 2008), Resina draconis (Cao et
al. 2008), dan Ganoderma lucidum (Chen et al. 2008), Ayurvedic churna
(Chitlange et al. 2009), Phyllanthus niruri (Wahyuni 2010), Artemisia selengensis
(Peng et al. 2011). Sidik jari juga cocok digunakan untuk identifikasi dan
membedakan sampel yang berasal dari daerah berbeda (Zhu et al. 2007).
Pengoptimuman Fase Gerak KCKT dengan Mixture Design
Pengoptimuman kondisi pemisahan KCKT dilakukan untuk memperoleh
hasil pemisahan dengan resolusi yang baik, robust, dan cepat. Pengoptimuman
dapat dilakukan terhadap fase gerak, fase diam, suhu pemisahan, dan kondisi
deteksi. Pengoptimuman fase gerak paling sering dilakukan (Borges et al. 2007).
Rancangan percobaan yang sering digunakan pada pengoptimuman fase gerak
ialah mixture design (Borges et al. 2007; Delaroza & Scarminio 2008),
mixture-mixture design (Wahyuni 2010).
Mixture design digunakan saat suatu sistem terdiri atas campuran beberapa
komponen yang jumlah totalnya konstan, yaitu 100%. Respon yang diperoleh
merupakan fungsi dari proporsi relatif tiap komponen dalam sistem. Pada mixture
design dapat digunakan 2 komponen atau lebih. Bertambahnya jumlah komponen
yang terlibat akan menambah jumlah dimensi ruang yang dipakai untuk
menggambarkan mixture. Saat 2 komponen terlibat, maka profil campuran
komponen akan mengikuti garis lurus, saat tiga komponen akan berbentuk
segitiga, berbentuk tetrahedron saat empat komponen digunakan, dan seterusnya.
Objek paling sederhana yang menggambarkan dimensi mixture disebut sebagai
simplex. Pada praktiknya metode simplex banyak digunakan dalam optimasi.
Kelebihan metode ini adalah mudah dan cepat. Daerah optimum adalah jenis
optimasi selektivitas pada pemisahan dengan KCKT, yaitu perubahan elusi
x1 x1 x1
x2 x3 x2 x3 x2 x3
(a) (b) (c)
Gambar 3. Simplex-lattice (a), simplex-centroid (b), simplex-centroid dengan axial design (c)
Saat digunakan tiga komponen mixture design dapat mengikuti rancangan
simplex-lattice, simplex-centroid, maupun simplex-centroid dengan axial design.
Contoh sederhana ketiga rancangan tersebut ditunjukkan pada Gambar 3. Pada
rancangan campuran berbentuk simplex-lattice titik-titik yang digunakan tersebar
di sepanjang sisi simplex . Jika diamati lebih lanjut rancangan ini fokus pada
pengaruh komponen tunggal dan kombinasi dua komponen dengan berbagai
ragam proporsi terhadap respon yang dihasilkan. Pada rancangan
simplex-centroid, selain pengaruh sistem tunggal dan biner dipelajari juga pengaruh
kombinasi tiga komponen (pada titik tengah/centroid). Untuk k faktor yang
terlibat, jumlah eksperimen ialah 2k-1 buah dan melibatkan kombinasi proporsi 1,
½, sampai 1/k. Pada simplex–centroid dengan axial design, pengaruh komponen
tiga komponen diperbanyak dengan menambah titik pada daerah axial (Brereton
2005).
Pada rancangan percobaan mengikuti simplex-centroid ada tujuh titik yang diukur
yaitu, 3 titik faktor tunggal, 3 titik interaksi 2 faktor, dan 1 titik interaksi 3 faktor
(Tabel 1).
Pengolahan data dimulai dengan menentukan nilai koefisien setiap interaksi
fase gerak KCKT menggunakan persamaan berikut (Almeida & Scarminio 2007)
ŷ = a1x1 + a1x1 + a2x2 + a3x3 ……….. (2)
ŷ = a1x1 + a1x1 + a2x2 + a3x3 + a1a2x1x2 + a1a3x1x3 + a2a3x2x3 ……… (3)
ŷ = a1x1 + a1x1 + a2x2 + a3x3 + a1a2x1x2 + a1a3x1x3 + a2a3x2x3 + a1a2a3x1x2x3… (4)
Tabel 1. Tiga faktor simplex-centroid
BAHAN DAN METODE
Tempat dan Waktu Penelitian
Penelitian dilaksanakan sejak Februari sampai dengan Juli 2011 di Pusat
Studi Biofarmaka LPPM IPB.
Alat dan Bahan
Alat yang digunakan di antaranya peralatan gelas, perangkat ekstraksi, sonikator
Branson 1510, dan sistem KCKT Shimadzu LC-20 AD yang dilengkapi dengan
detektor larik diode, sistem pompa gradien, sistem injeksi loop, dan kolom oven.
Bahan yang digunakan adalah kayu secang (Caesalpinia sappan) yang berasal
dari Semarang. Pelarut ekstraksi etanol 70 %, DPPH (2,2-
diphenyl-1-picrylhidracyl), kolom kromatografi C18 LiChospher (5 µm, 250 mm x 4 mm),
dan fase gerak KCKT metanol 50 %, metanol:air:TFA (25:75:0.025 v/v), dan
metanol:air:TFA (15:85:0.035 v/v)
Metode Penelitian
Kayu secang dikeringkan, digiling, dan diukur kadar airnya. Simplisia secang
diekstraksi dengan teknik maserasi dan teknik sonikasi menggunakan pelarut
etanol 70 % dengan perbandingan serbuk kayu dan pelarut 1:100. Ekstrak yang
diperoleh disaring dengan kertas saring dan dikeringkan menggunakan rotary
evaporator pada suhu 30oC. Uji aktivitas antioksidan dilakukan terhadap ekstrak
hasil maserasi dan sonikasi. Ekstrak yang memiliki nilai IC50 tertinggi dipisahkan
dengan KCKT menggunakan kombinasi fase gerak yang ditentukan dengan
mixture design dan dimonitor pada panjang gelombang 254 nm dan 280 nm untuk
mendapatkan fase gerak optimum (Lampiran 1).
Preparasi Sampel.
Kayu secang dikeringkan menggunakan oven bersuhu 40oC hingga kadar airnya
kurang dari 10%. Sampel yang telah kering dihaluskan hingga menjadi serbuk
Penentuan Kadar Air (AOAC 2006).
Sebanyak 3 gram sampel ditimbang, digunakan wadah yang telah dikeringkan
pada suhu 105oC selama 30 menit dan ditara. Sampel kemudian dikeringkan
dalam oven bersuhu 105oC hingga diperoleh bobot konstan. Kadar air diperoleh
sebagai nisbah selisih bobot sampel awal dengan bobot sampel setelah
dikeringkan terhadap bobot sampel sebelum dikeringkan. Kadar air sampel
ditentukan sebanyak 3 kali ulangan (Lampiran 2).
Ekstraksi maserasi (Meloan 1999)
Ekstraksi sampel secang dilakukan dengan teknik maserasi menggunakan pelarut
etanol 70%. Sebanyak 1 gram serbuk kayu secang direndam dengan 100 ml
pelarut selama 24 jam. Maserat dipisahkan dari residu dengan penyaringan. Ke
dalam residu ditambahkan kembali pelarut dan tahapan ekstraksi diulang sampai
hingga tiga kali. Maserat dari setiap ulangan ekstraksi digabung dan dikeringkan
dengan penguap putar.
Ekstraksi sonikasi (Melecci et al. 2006).
Ekstraksi sampel secang juga dilakukan dengan menggunakan teknik sonikasi.
Serbuk kayu secang sebanyak 1 gram diekstraksi dengan 100 mL pelarut etanol
70% dalam ultrasonic cleaning bath dengan frekuensi 42 kHz pada suhu ruang
selama 30 menit. Maserat dipisahkan dari residu dengan penyaringan. Ke dalam
residu ditambahkan kembali pelarut dan tahapan diulang sebanyak tiga kali.
Maserat dari setiap ulangan ekstraksi digabung dan dikeringkan dengan penguap
putar.
Metode Pengujian DPPH (2,2-diphenyl-1-picrylhidracyl) (Batubara 2010).
Aktivitas antioksidan diukur dengan metode penangkapan radikal bebas stabil
DPPH. Ekstrak sebanyak 1 mg dilarutkan dalam etanol dengan konsentrasi 10.0,
13.33, 16.67, 33.33, 66.67, 100 µg/mL. 100 µL sampel dimasukkan dalam well
plate dengan 100 µL DPPH, diinkubasi selama 30 menit dan diukur serapannya
(0,1,0) x2
Pengoptimuman Kondisi Kromatografi (Almeida & Scarminio 2007)
Pengoptimuman kondisi kromatografi dilakukan terhadap komposisi fase gerak
yang disusun sesuai mixture design dengan bentuk simplex-centroid dengan axial
design (Gambar 4). Fase gerak yang digunakan terdiri atas metanol 50 % (x1),
metanol:air:TFA (25:75:0.025 v/v) (x2), dan metanol:air:TFA (15:85:0.035 v/v)
(x3). Fase gerak yang digunakan disaring terlebih dahulu menggunakan membran
filter 0.45 um. Panjang gelombang deteksi KCKT yang digunakan adalah 254 nm
dan 280 nm.
Pada analisis dengan KCKT, 50 mg ekstrak secang hasil sonikasi dilarutkan
dalam 5 mL pelarut ekstraksi. Sebanyak 100 µL ekstrak tersebut dilarutkan
dengan 1900 µL fase gerak dan disaring dengan membran filter 0.45 um sebanyak
dua kali. Selanjutnya 20 µL larutan sampel yang telah disaring diinjeksikan ke
dalam kolom C18. Suhu dijaga konstan pada suhu 40oC dengan laju alir fase gerak
1 mL/menit. Jumlah puncak yang muncul pada kromatogram setiap ekstrak
dihitung. Puncak yang dihitung ialah puncak yang memiliki rasio sinyal terhadap
derau ≥3 dan nilai resolusi ≥ 1.
x1 Metanol 50 %
Gambar 4. Komposisi fase gerak KCKT sesuai mixture design
Analisis Data Pemisahan Kromatografi Cair Kinerja Tinggi (KCKT).
Pengaruh fase gerak KCKT terhadap jumlah puncak yang ditampilkan sidik jari
kromatografi dimodelkan dengan bantuan pangolahan statistika. Perangkat lunak
SAS 9.2 digunakan untuk membangun model interaksi fase gerak dari data
pemisahan KCKT tersebut. Data yang digunakan untuk membangun model adalah
(1,0,0)
(0,1/2,1/2) (metanol:air:TFA (15:85:0.035 v/v)
data yang terletak pada sisi dan pusat simplex mengikuti bentuk simplex-centroid
dengan axial-design.
Preparasi dan ekstraksi kulit kayu secang
Kayu secang berasal dari Semarang yang diperoleh dari Pusat Studi
Biofarmaka, dengan kadar air sebesar 8.44% (Tabel 2) dan siap diekstraksi
(Lampiran 2). Hasil tersebut menunjukkan bahwa dalam 100 gram sampel kayu
secang terkandung 8.44 gram air yang terikat secara fisik dan dapat hilang oleh
pemanasan pada suhu sekitar 105oC. Kadar air kurang dari 10% diharapkan
mengurangi resiko kerusakan sampel kulit kayu secang akibat serangan jamur dan
bakteri dan memenuhi standar material untuk uji bahan baku herbal (BPOM
2004).
Tabel 2. Nilai hasil penentuan kadar air
Ulangan Bobot sampel awal (g) Bobot sampel akhir (g)
Rata-rata 1.0062 0.9218 8.440
Std deviasi
0.00025 0.00242 0.24269
Kayu secang dihaluskan hingga berukuran 80 mesh sebelum ekstraksi
dilakukan. Hal ini bertujuan untuk meningkatkan luas permukaan sampel
sehingga daerah kontak sampel dengan pelarut ekstraksi lebih besar dan proses
ekstraksi berlangsung lebih optimal (Sembiring et al. 2006). Pada uji
pendahuluan, ekstraksi dilakukan dengan menggunakan 2 teknik yang berbeda
yaitu teknik maserasi pada suhu ruang dan teknik sonikasi. Pelarut yang
digunakan adalah etanol 70 %. Ekstraksi maserasi memberikan rendemen 12.87±
0.52 % sedangkan ekstraksi sonikasi memberikan rendemen 10.30 ± 0.45 %.
Teknik maserasi memberikan rendemen yang lebih tinggi diduga disebabkan oleh
waktu ekstraksi yang cukup lama sehingga senyawa yang terekstrak juga semakin
Pengujian aktivitas antioksidan metode DPPH
Aktivitas biologis yang di uji pada penelitian ini adalah aktivitas
antioksidan dengan metode DPPH dalam ekstrak kayu secang karena antioksidan
bermanfaat bagi kesehatan kulit dan dapat ditambahkan pada kosmetika (Batubara
et al. 2010), serta berkaitan dengan penelitian yang dilakukan oleh Sa’diah et al.
2010 dalam rangka pengembangan formula sediaan salep dan metode kontrol
kualitas ekstrak kayu secang sebagai antijerawat.
Metode DPPH (2,2-difenyl-1-pikrilhidrazil) merupakan senyawa radikal
nitrogen. DPPH akan mengambil atom hidrogen yang terdapat dalam suatu
senyawa, misalnya senyawaan fenol membentuk DPPH tereduksi (DPPH
Hidrazin) yang stabil (Prakash 2001). Mekanisme terjadinya reaksi DPPH ini
berlangsung melalui transfer elektron. Larutan DPPH berwarna ungu tetapi
setelah membentuk DPPH tereduksi (DPPH Hidrazin) warnanya berubah menjadi
kuning dengan intensitas perubahan warna tergantung pada kekuatan aktivitas
antioksidannya. Hasil uji aktivitas antioksidan dengan metode DPPH dapat dilihat
pada Tabel 3 sementara data selengkapnya ditunjukkan pada Lampiran 3.
Tabel 3. Nilai IC50 ekstrak kayu secang
Ekstrak etanol 70 % IC50 (µg/mL)
Teknik maserasi
Teknik sonikasi
89.92 ± 3.11
25.37 ± 2.24
Nilai IC50 yang diperoleh pada penelitian ini lebih tinggi dari nilai IC50
brazilin dari ekstrak metanol 50 % teknik maserasi kulit kayu secang yang telah
dilaporkan oleh Batubara et al. (2010) yaitu 8.8 µM dan Sa’diah et al. 2010 yang
melaporkan bahwa ekstrak etanol 50 % kayu secang asal Semarang memiliki nilai
IC50 sebesar 9.60 ± 0.92 µg/mL. Kadar dan jenis senyawa metabolit sekunder
dalam tanaman sejenis tidak selalu sama, kandungan senyawa metabolit sekunder
tersebut dipengaruhi oleh kandungan hara dan kondisi tanah tempat tumbuh.
Selain itu juga dipengaruhi oleh umur tanaman ketika dipanen, waktu panen, dan
penanganan pasca panen (Briskin 2002). Bagian tanaman dan usia tanaman yang
ada. Selain itu perbedaan konsentrasi pelarut dan teknik ekstraksi juga
mempengaruhi jenis-jenis senyawa metabolit sekunder yang terekstrak (Harborne
1987). Faktor-faktor di atas diduga menyebabkan terjadinya perbedaan nilai IC50
yang diperoleh dalam penelitian ini dengan nilai IC50 yang telah dilaporkan pada
penelitian-penelitian sebelumnya.
Ekstrak etanol teknik sonikasi dipilih untuk tahap pengoptimuman fase
gerak KCKT karena memiliki nilai IC50 yang lebih rendah. Selain itu teknik
ekstraksi sonikasi dipilih dengan pertimbangan bahwa teknik sonikasi lebih cepat
dan efisien dibandingkan dengan ekstraksi menggunakan teknik maserasi. Waktu
yang dibutuhkan untuk ekstraksi sonikasi adalah 3 x 0.5 jam sedangkan untuk
maserasi memerlukan waktu 3 x 24 jam.
Pengoptimuman kondisi KCKT
Pada penelitian ini panjang gelombang deteksi yang digunakan adalah 254
nm dan 280 nm. Panjang gelombang deteksi KCKT yang digunakan mengacu
pada penelitian terdahulu terhadap ekstrak kulit kayu secang. Batubara et al.
(2010) mengisolasi brazilin pada panjang gelombang 280 nm. Isolasi senyawa
5-hidroxy-1,4-naphtoquinone dilakukan pada panjang gelombang 254 nm (Lim
2007).
Fase gerak yang digunakan pada penelitian ini adalah metanol 50 %,
metanol: air :TFA (25:75:0.025 v/v), dan metanol :air :TFA (15:85:0.035 v/v).
Ketiga pelarut ini bersifat polar. Metanol dan air umum digunakan sebagai fase
gerak pada KCKT fase terbalik. Menurut Synder & Kirkland (1979) metanol dan
air memiliki selektivitas berlainan sehingga akan memberikan kecepatan elusi
yang bervariasi. Metanol dan air memiliki viskositas dan titik didih yang nilainya
di pertengahan, dapat bercampur dengan baik, sesuai untuk detektor ultraviolet,
dan mudah diperoleh.
Fase gerak yang digunakan pada penelitian juga ini mengacu pada
penelitian terdahulu yang telah dilakukan terhadap secang. Fase gerak yang telah
dilaporkan untuk pemisahan ekstrak kayu secang adalah metanol:air (l:l v/v)
Ekstrak etanol secang dipisahkan dengan KCKT fase terbalik
menggunakan sepuluh kombinasi fase gerak sesuai mixture design yang
mengambil bentuk simplex-centroid dengan axial design. Rancangan ini
digunakan untuk mempelajari pengaruh fase gerak tunggal, campuran dua fase
gerak, dan campuran tiga pelarut terhadap sidik jari kromatografi yang dihasilkan.
Jumlah puncak yang muncul pada kromatogram KCKT ekstrak kayu
secang dihitung berdasarkan kriteria nilai resolusi dan rasio sinyal terhadap derau
(S/N). puncak diakui dan dihitung jika memiliki nilai resolusi 1 dan nilai S/N
3. Nilai resolusi 1 digunakan sebagai batasan karena suatu puncak dikatakan
terpisah apabila memiliki nilai resolusi 1 (Dong 2006). Nilai S/N 3 dipilih
karena nilai ini umum digunakan untuk menentukan nilai limit deteksi (Bliesner
2006). Informasi nilai resolusi dan S/N diperoleh melalui pengolahan
kromatogram ekstrak menggunakan perangkat lunak LC solution yang terintegrasi
dengan KCKT Shimadzu varian LC-20 AD yang digunakan pada penelitian ini.
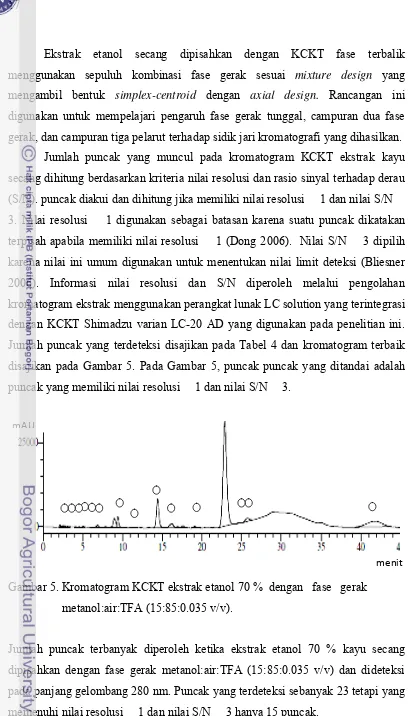
Jumlah puncak yang terdeteksi disajikan pada Tabel 4 dan kromatogram terbaik
disajikan pada Gambar 5. Pada Gambar 5, puncak puncak yang ditandai adalah
puncak yang memiliki nilai resolusi 1 dan nilai S/N 3.
Gambar 5. Kromatogram KCKT ekstrak etanol 70 % dengan fase gerak
metanol:air:TFA (15:85:0.035 v/v).
Jumlah puncak terbanyak diperoleh ketika ekstrak etanol 70 % kayu secang
dipisahkan dengan fase gerak metanol:air:TFA (15:85:0.035 v/v) dan dideteksi
pada panjang gelombang 280 nm. Puncak yang terdeteksi sebanyak 23 tetapi yang
memenuhi nilai resolusi 1 dan nilai S/N 3 hanya 15 puncak.
menit
Tabel 4. Desain variable dan respon
No X1 X2 X3
Komposisi fase gerak Jumlah puncak
metanol air TFA 245 nm 280 nm
Pemisahan dengan fase gerak metanol 50 % pada panjang gelombang 280 nm
menghasilkan 7 puncak tetapi tidak ada yang memenuhi nilai resolusi 1 dan
nilai S/N 3 (Lampiran 4). Adanya TFA dalam fase gerak berpotensi
meningkatkan jumlah puncak yang dihasilkan. TFA merupakan senyawa asam
kuat dan biasa ditambahkan dalam fase gerak KCKT pada konsentrasi rendah
sebagai ion pairing agent (Sadek 2002).
Kecepatan elusi ekstrak etanol bervariasi tergantung komposisi fase
geraknya. Ekstrak terelusi paling cepat ketika dipisahkan dengan fase gerak
metanol 50 %. Hal ini terjadi karena ekstrak etanol yang relatif bersifat polar
mengalami retensi yang kecil oleh fase diam yang bersifat nonpolar.
Dari hasil pemisahan yang dilakukan pada penelitian dapat dilihat bahwa
penambahan pelarut metanol ke dalam fase gerak menyebabkan waktu retensi
turun. Semakin banyak metanol yang ditambahkan maka waktu retensinya juga
turun atau dengan kata lain elusi yang terjadi semakin cepat. Penambahan pelarut
organik yang relatif kurang polar seperti metanol dan asetonitril ke dalam fase
gerak menyebabkan tekanan air berkurang sehingga menyebabkan waktu retensi
berkurang (Dong 2006).
Analisis Data Pemisahan Kromatografi Cair Kinerja Tinggi (KCKT)
Model interaksi fase gerak yang menggambarkan pengaruh fase gerak
KCKT terhadap jumlah puncak KCKT dibangun dari sepuluh data dengan
menggunakan perangkat lunak SAS 9.2.
Pengolahan data dimulai dengan menentukan nilai koefisien setiap interaksi fase
gerak KCKT menggunakan persamaan:
ŷ = b1x1 + b2x2 + b3x3 + b12x1x2 + b13x1x3 + b23x2x3 + b123x1x2x3
Interaksi yang memiliki nilai mutlak t-hitung lebih besar dari t-tabel pada selang
kepercayaan 95% atau nilai p lebih kecil dari α digunakan untuk membangun
model interaksi fase gerak. Model interaksi fase gerak pada masing-masing
panjang gelombang disajikan pada Tabel 5.
Tabel 5. Model interaksi fase gerak pada panjang gelombang 254 dan 280 nm λ (nm) Model interaksi fase gerak
254
280
20.78x2 + 14.87x3
9.30x2 + 13.76x3
Dua interaksi linear menjadi bagian model interaksi linear pada panjang
gelombang deteksi 254 maupun 280 nm. Interaksi yang terjadi antara ekstrak
etanol 70 % dengan fase gerak yang mengandung TFA (x2 dan x3)menunjukkan
interaksi yang sinergis, atau dengan kata lain fase gerak yang mengandung TFA
berpotensi meningkatkan jumlah puncak yang dapat dideteksi. Koefisien interaksi
menunjukkan jumlah puncak dugaan yang terjadi. Sebagai contoh pada panjamg
gelombang 280 nm notasi 9x2 menunjukkan bahwa jumlah puncak dugaan saat
ekstrak dipisahkan dengan fase gerak metanol: air: TFA (25:75:0.025 v/v) adalah
9 buah ternyata jumlah puncak yang terdeteksi adalah 10 buah. Demikian juga
untuk notasi 13.76x3 yang menunjukkan bahwa jumlah puncak dugaan ada 14
buah ternyata jumlah puncak yang terdeteksi ada 15 buah.
Model interaksi fase gerak juga digunakan untuk menentukan jumlah
puncak dugaan dari data yang digunakan membangun model. Nilai root mean
square error of calibration (RMSEC) dan root mean square error of prediction
RSMEC dan RSMEP menunjukkan kesesuaian jumlah puncak dugaan dengan
jumlah puncak yang dideteksi pada data yang digunakan membangun model
interaksi fase gerak. Semakin kecil nilai RMSEC dan RMSEP, semakin baik
model interaksi fase gerak yang dibangun (Naes et al. 2002 dalam Wahyuni
2010). berdasarkan nilai RMSEC dan RMSEP, model interaksi fase gerak
dibangun dari data pada panjang gelombang deteksi 280 nm karena memiliki nilai
RMSEC dan RSMEP yang lebih kecil dibanding pada 254 nm.
Tabel 6. Nilai RMSEC dan RMSEP pada 254 dan 280 nm
parameter 254 nm 280 nm
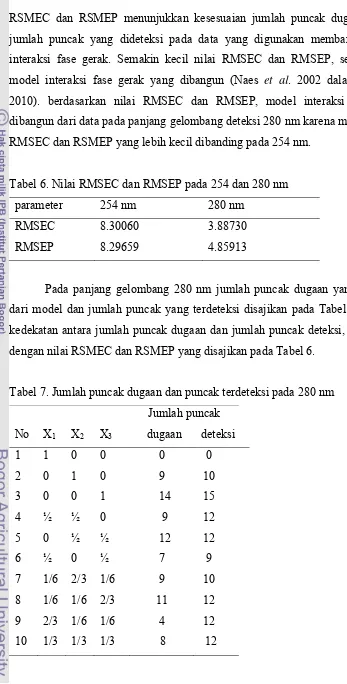
Pada panjang gelombang 280 nm jumlah puncak dugaan yang diperoleh
dari model dan jumlah puncak yang terdeteksi disajikan pada Tabel 7. Terlihat
kedekatan antara jumlah puncak dugaan dan jumlah puncak deteksi, dan sepakat
dengan nilai RSMEC dan RSMEP yang disajikan pada Tabel 6.
Tabel 7. Jumlah puncak dugaan dan puncak terdeteksi pada 280 nm
Pemilihan kondisi optimum pada panjang gelombang deteksi 280 nm
didasarkan pada tiga hal yaitu profil kromatogram atau banyaknya puncak yang
terdeteksi, model yang dibangun, dan kontur plot.
1. Berdasarkan profil kromatogram
Pada Gambar 5 dapat diamati bahwa pemisahan ekstrak dengan fase gerak
metanol: air: TFA (15:85:0.035 v/v) yang terletak di ujung segitiga kanan bawah
menghasilkan jumlah puncak lebih banyak dengan resolusi yang lebih baik
dibanding kromatogram yang dihasilkan fase gerak KCKT lainnya sejumlah 15
puncak, meskipun secara keseluruhan kromatogram yang dihasilkan belum begitu
bagus karena puncak-puncak yang muncul masih menumpuk di depan.
Kromatogram dapat diperbaiki dengan mengubah fase gerak yang digunakan agar
diperoleh jumlah puncak yang lebih banyak atau mengubah cara elusi isokratik
menjadi elusi gradien serta parameter alat. Semakin banyak jumlah puncak yang
terdeteksi berarti semakin banyak pula jenis senyawa dalam ekstrak yang dapat
terdeteksi sehingga kontrol kualitas yang dibangun juga semakin bagus.
Gambar 5. Sidik jari KCKT ekstrak etanol kayu secang pada 280 nm.
2. Berdasarkan model
Kondisi optimum pada panjang gelombang 280 nm dicapai saat ekstrak
etanol 70 % dipisahkan dengan fase gerak metanol: air: TFA (15:85:0.035 v/v).
Kondisi optimum diperoleh berdasarkan model interaksi fase gerak. Ketika
variabel bebas dimasukkan ke dalam model, maka puncak dugaan tertinggi
(respon tertinggi) atau disebut kondisi optimum terjadi ketika ekstrak dipisahkan
dengan fase gerak x3 menghasilkan 14 puncak dugaan.
3. Berdasarkan plot kontur
Gambar 6 menyajikan kontur plot yang dihasilkan saat ekstrak etanol 70 %
dipisahkan dengan berbagai jenis fase gerak KCKT. Dapat diamati bahwa puncak
optimum berada pada daerah x3 yaitu pada pemisahan dengan fase gerak
metanol:air:TFA (15:85:0.035 v/v) dengan jumlah puncak lebih besar dari 12,
sepakat dengan hasil penelitian yang dilakukan yaitu puncak yang terdeteksi
ketika dipisahkan dengan fase gerak metanol:air:TFA (15:85:0.035 v/v) adalah 15
buah.
Gambar 6. Kontur plot ekstrak etanol pada panjang gelombang 280 nm.
SIMPULAN DAN SARAN
Simpulan
Ekstraksi kayu secang dengan metode sonikasi dan maserasi menggunakan
pelarut etanol 70 % menghasilkan rendemen dan IC50 berturut-turut 10.30 ± 0.45
% dan 25.37 ± 2.24 µg/mL, 12.87 ± 0.52 % dan 89.92 ± 3.11 µg/mL. Model interaksi fase gerak terbaik dibangun pada panjang gelombang 280 nm dengan nilai RSMEC dan RSMEP berturut-turut 3.88730 dan 4.85913. Kondisi optimum pada panjang gelombang 280 nm diperoleh saat digunakan metanol: air: TFA (15:85:0.035 v/v) sebagai fase gerak kromatografi cair kinerja tinggi (KCKT) dengan jumlah puncak yang dihasilkan sebanyak 15 buah.
Saran
Ahuja S, Rasmussen H. 2007. HPLC Method Development for Pharmaceuticals. Amsterdam: Elsevier Academic Press.
Akowuah GA, Zhari I, Norhayati I, Mariam A. HPLC and HPTLC densitometric
determination of andrographolides and antioxidant potential of Andrographis
paniculata. J of Food Composition and Analysis 19:118-126.
Almeida AA & Scarminio S. 2007. Statustical mixture design optimization of extraction media and mobile phase composition for the characterization of
green tea. J. Sep. Sci 30: 414-420.
[AOAC] Association of Analytical Chemist. 2006. Official Methods of Analysis of
the Association of Official Analytical Chemist. Edisi ke-18. Washington
DC:AOAC.
Apak R et al. 2007. Comparative evaluation of various total antioxidant capacity
assay applied to phenolic compounds with the CUPPRAC assay. Molecules
12:1496-1547.
Ashley K, Andrew RN, Cavazosa L, Demange M. 2001. Ultrasonic extraction as a sample preparation technique for elemental analysis by atomic spectrometry.
Journal of Analytical Atomic Spectrometry 16:1147-1153.
Batubara I, Mitsunaga T, Ohashi H. 2009. Screening anti-acne potency of Indonesian medicinal plants: antibacterial, lipase inhibition and antioxidant
activities. J Wood Sci 55:230-235.
Batubara I, Mitsunaga T, Ohashi H. 2010. Brazilin from Caesalpinia sappan
wood as an antiacne agent. J Wood Sci 56: 77-81.
Bliesner DM. 2006. Validating Chromatographic Methods: A Practical Guide.
New Jersey: John Wiley & Sons, Inc.
Borges CN, Bruns RE, Almeida AA, Scarminio IS. 2007. Mixture-mixture design for the fingerprint optimization of chromatographic mobile phases and
extraction solutions for Camellia sinensis. Anal Chim Acta 595: 28-37.
Brereton. 2005. Optimization Strategies. Bristol: Elsevier Ltd
Cao Yuhua et al. 2008. Comparison of microemulsion electrokinetic
chromatography with HPLC for fingerprint analysis of Resina draconis. Anal
Chen Y et al. 2008. Quality control and original discriminatin of Ganoderma
lucidum based of HPLC fingerprint and combined chemometric methods.
Anal Chem Acta 623:146-156.
Chitlange et al. 2009. HPLC fingerprint for quality control of Terminalia arjuna
containing Ayurvedic churna formulation. J of AOAC International.
Currell G. 2000. Analytical Instrumentation: Performance Characteristic and
Quality. New Jersey: John Wiley & Sons, Inc.
Delaroza F, Scarminio IS. 2008. Mixture Design optimization of extraction and
mobile phase media for fingerprint analysis of Bauhinia variegata L. J Sep
Sci 31: 1034-1041.
Dong MW. 2006. Modern HPLC for Practicing Scientist. New Jersey: John Wiley
& Sons, Inc.
Eun et al. 2005. Caesalpinia sappan induces cell death by increasing the
expression of p53 and p21WAFI/CIPI in head and neck cancer cells. The
American Journal of Chinese Medicine 33:405-414.
Harborne JB. 1987. Metode Fitokimia. Padmawinata K, Soediro I, penerjemah;
Niksolihin S, Editor, editor. Bandung: Penerbit ITB. Terjemahan dari:
Phytochemical method.
Lai X, Zhao Y, Wang B, Liang H. 2007. Chromatographic Fingerprint Analysis of
the Flowers of Abelmoschus manihot using HPLC with Photodiode Array
Detection. Anal Let 40: 2192-2202.
Liang YZ, Xie P, Chan K. 2004. Quality Control of herbal medicine. J
Chromatogr B 812: 53-70.
Lim MY, Ju HJ, Eun YJ, Chi HL, & Hoi SL. 2007. Antimicrobial activity of
5-hidroxy-1,4-naphthoquinone isolated from Caesalpinia sappan toward
intestinal bacterial. Food Chem 100:1254-1258.
Melecchi MIS et al. 2006. Optimization of the sonication extraction method of
Hibiscus tiliaceus L. flowers. Ultrasonic Sonochemistry 13:242-250.
Meloan CE. 1999. Chemical Separation. New York: J Wiley.
Otto M. 1999. Chemometrics. New York: J Wiley.
Park KJ et al. 2002. Cytotoxic effects of Korean medicinal herbs determined with
Peng L, Wang Y, Zhu H, Chen Q. 2011. Fingerprint profile of active compound
for Artemisia selengensis by HPLC-PAD combined with chemometrics. Food
Chem 125:1064-1071.
Pourmorad F, Hosseinimehr SJ, Shahabimajd N. 2006. Antioxidant activity,
phenol, and flavonoid contents of some selected Iranian medicinal plants. Afr
J Biotechnol 5:1142-1145.
Prakash A. 2001. Antioxidant activity. Analytical progress 19:2.
Sa´diah, Batubara I, Rafi M. 2010. Pengembangan formula sediaan salep dan
metode kontrol kualitas ekstrak kayu (Caesalpinia sappan) sebagai
antijerawat. Laporan Penelitian Hibah Kompetitif Penelitian Kerjasama
Internasional dalam Rangka Publikasi Internasional. Sep 2010
Safitri R. Ekstraksi dan identifikasi antioksidan dari tumbuhan jamu kayu secang [Laporan Penelitian]. Bandung: Fakultas MIPA Universitas Padjajaran; 2000 Sembiring BB, Ma’mun, Ginting EI. 2006. Pengaruh kehalusan bahan dan lama
ekstraksi terhadap mutu ekstrak temulawak (Curcuma xanthorriza Roxb.).
Bull Littro XVII(2): 53-58
Synder LR, Kirkland JJ. 1979. Introduction to Modern Liquid Chromatography.
Ed ke-2. New York: John Wiley & Sons, Inc.
Wahyuni WT. Pengoptimuman dan validasi sidik jari kromatografi cair kinerja
tinggi ekstrak Phyllanthus niruri [Tesis]. Bogor: Program Pascasarjana
Institut Pertanian Bogor; 2010.
Xu HX, Lee SF. 2004. The antibacterial principle of Caesalpinia sappan.
PhytotherRes 18:647-651.
Yingming P, Ying L, Hengshan W, Min L. 2004. Antioxidant activities of several
chinese medicine herbs. Food Chemistry 88: 347-350.
Youdsaue O et al. 2008. Pharginin A-K, diterpenoids from the seeds of
Caesalpinia sappan Linn. Phytochemistry 69: 1242-1249.
Yuwono A. 2009. Antioxidant and health disease. [terhubung berkala] http://farmacology.org/specialistmedic/internist [2 maret 2009]
Zhang S, Ouyang F, Wang C, Gu M. 2008. Fingerprint of tablet of corydalis tuber
for alleviating pain by HPLC. J of Liquid Chromatogr & Related
Zhu M, Cao Y, Fan G. 2007. Microwave-assisted extraction and fingerprint
studies of Schisandra chinensis (Turcz) by HPLC. J of Liquid Chromatogr &
Related Technologies 30:123-133.
Lampiran 1. Bagan alir penelitian
Ekstraksi sonikasi dengan etanol 70% Pengukuran kadar air
Ekstrak dengan aktivitas antioksidan tertinggi Uji DPPH
Lampiran 2. Penentuan kadar air
Ulangan Bobot sampel awal (g) Bobot sampel akhir
(g)
Rata-rata 1.0062 0.9218 8.440
Std deviasi 0.00025 0.00242 0.24269
Penghitungan kadar air
Kadar air = bobot sampel awal – bobot sampel akhir X 100 %
Lampiran 4. Kromatogram KCKT
Data 1. (x1:x2:x3 = 1:0:0) pada panjang gelombang 254 nm
Data 1. (x1:x2:x3 = 1:0:0) pada panjang gelombang 280 nm
mAU
menit
mAU
Data 2. (x1:x2:x3 = 0:1:0) pada panjang gelombang 254 nm
menit
Data 2. (x1:x2:x3 = 0:1:0) pada panjang gelombang 280 nm
menit
Data 3. (x1:x2:x3 = 0:0:1) pada panjang gelombang 254 nm
Data 3. (x1:x2:x3 = 0:0:1) pada panjang gelombang 280 nm
Data 4. (x1:x2:x3 = 1/2:1/2:0) pada panjang gelombang 254 nm
mAU
Data 5. (x1:x2:x3 = 0:1/2:1/2) pada panjang gelombang 254 nm
Data 5. (x1:x2:x3 = 0:1/2:1/2) pada panjang gelombang 280 nm
Data 6. (x1:x2:x3 = 1/2:0:1/2) pada panjang gelombang 254 nm
Data 6. (x1:x2:x3 = 1/2:0:1/2) pada panjang gelombang 280 nm
Data 7. (x1:x2:x3 = 1/6:2/3:1/6) pada panjang gelombang 254 nm
Data 7. (x1:x2:x3 = 1/6:2/3:1/6) pada panjang gelombang 280 nm
mAU
Data 8. (x1:x2:x3 = 1/6:1/6:2/3) pada panjang gelombang 254 nm
Data 8. (x1:x2:x3 = 1/6:1/6:2/3) pada panjang gelombang 280 nm
Data 9. (x1:x2:x3 = 2/3:1/6:1/6) pada panjang gelombang 254 nm
Data 9. (x1:x2:x3 = 2/3:1/6:1/6) pada panjang gelombang 280 nm
Data 10. (x1:x2:x3 = 1/3:1/3:1/3) pada panjang gelombang 254 nm
Data 10. (x1:x2:x3 = 1/3:1/3:1/3) pada panjang gelombang 280 nm
ABSTRACT
RETNO DJULAIKA. Optimization High Performance Liquid Chromatographic
Fingerprint of sappan wood (Caesalpinia sappan). Under direction of LATIFAH
K. DARUSMAN and RUDI HERYANTO
Mixture design has been applied for optimization of Caesalpinia sappan
chromatographic fingerprint. The design applied for unreplicated and simultaneous optimization of HPLC mobile phase mixture. Ethanol extracts with highest antioxidant activity resulted from sonication extraction method was chosen for HPLC analysis . The reversed phase chromatographic mobile phase in simplex centroid design consist of varying proportion of methanol 50 %, methanol: water: TFA (25: 75: 0.025 v/v), and methanol: water: TFA (15: 85: 0.035 v/v). Ethanol 70 % extract of sappan analyzed with ten mobile phase and monitored at 254 and 280 nm. Correlation between HPLC mobile phase and a number of peak analyzed statistically by SAS 9.2. The root mean square errror of calibration (RSMEC) and root mean square errror of calibration (RSMEP) at 254 and 280 nm, were 8.3006 and 8.29659, 3.88730 and 4.85193 respectively. Optimum condition obbtained when ethanol 70 % extract eluted by methanol: water: TFA (15: 85: 0.035 v/v), with the 15 number of peaks.
PENDAHULUAN
Latar Belakang
Secang (Caesalpinia sappan L.) merupakan salah satu tanaman yang
memiliki banyak khasiat dalam pengobatan di antaranya sebagai pembersih darah,
antikanker (Park et al. 2002; Eun et al. 2005), ekspektoran, antioksidan
(Yingming et al. 2004), immunostimulan, antimikroba (Lim et al. 2007),
antikomplementary, antibakteri (Xu & Lee 2004) serta antimikroba (Lim et al.
2007). Secang dapat dikembangkan sebagai bahan antioksidan dalam kosmetik
dan antijerawat (Batubara et al. 2010). Di Indonesia, secara tradisional secang
digunakan untuk perawatan kulit oleh masyarakat di kepulauan Sumbawa. Secang
juga digunakan sebagai pewarna merah alami pada minuman tradisional
masyarakat Betawi, yang dikenal dengan nama bir pletok. Oleh karena banyaknya
manfaat dari secang maka perlu dilakukan kendali mutu ekstrak secang.
Metode yang umum digunakan dalam proses standardisasi/kontrol kualitas
bahan baku atau ekstrak penyusun obat herbal adalah dengan menunjukkan kadar
satu atau beberapa senyawa penciri. Namun demikian, analisis senyawa penciri
untuk kontrol kualitas dinilai kurang memadai karena khasiat tanaman obat
disumbangkan oleh sejumlah senyawa kimia yang bekerja secara sinergis (Liang
et al. 2004) sehingga diperlukan suatu metode analisis untuk mengatasi masalah
tersebut. Salah satunya adalah dengan menggunakan pendekatan multi komponen
atau analisis sidik jari.
Analisis sidik jari kromatografi telah digunakan dalam kontrol kualitas
tanaman dan produk akhirnya, serta menjadi teknik yang sangat berguna untuk
kontrol kualitas obat-obat herbal (Lai et al. 2007; Delaroza dan Scarminio 2008).
Analisis sidik jari membantu dalam hal klasifikasi dan validasi spesies botani serta
kontrol kualitas dari tanaman obat (Borges et al. 2007). Model kontrol kualitas
berdasarkan sidik jari kromatografi dapat menjadi teknik alternatif untuk
memonitor kualitas tanaman obat. Seluruh senyawa kimia yang dikandung oleh
tanaman obat tertentu dapat ditampilkan dalam sidik jari kromatografi sehingga
2009). Teknik ini telah direkomendasikan untuk kontrol kualitas tanaman obat
oleh Food and Drug Administration (FDA) dan European Medicines Agency
(EMEA) (Borges et al. 2007). Bahkan pada tahun 2004, State Food & Drug
Administration of China (SFDA) mewajibkan semua obat-obat suntik yang dibuat
dari tanaman obat atau material kasarnya harus distandarisasi dengan sidik jari
kromatografi (Lai et al. 2007).
Dalam rangka mengembangkan model kontrol kualitas tanaman secang,
diperlukan sidik jari kromatografi ekstrak secang yang informatif dan mampu
menampilkan semaksimal mungkin komponen kimia dengan resolusi yang baik.
Sidik jari ekstrak secang yang informatif dapat diperoleh melalui pengoptimuman
faktor-faktor yang mempengaruhi waktu retensi, resolusi, jumlah puncak, dan luas
puncak kromatografi. Faktor tersebut meliputi metode dan pelarut ekstraksi,
kondisi instrumen kromatografi, dan fase gerak kromatografi (Borges et al. 2007).
Penelitian ini merupakan pengembangan penelitian sebelumnya yang
dilakukan oleh Sa´diah et al. (2010) yang telah mengembangkan kontrol kualitas
ekstrak etanol 50 % kayu secang berdasarkan senyawa penciri brazilin, dengan
fase gerak metanol dan trifluoraasetat 0.05 % (TFA 0.05 %) secara gradien. Pada
penelitian ini akan dikembangkan metode kontrol kualitas ekstrak etanol 70 %
kayu secang berdasarkan analisis sidik jari kromatografi cair kinerja tinggi
(KCKT) dengan tetap melibatkan senyawa penciri. Pengoptimuman dilakukan
terhadap fase gerak KCKT. Komposisi fase gerak KCKT menentukan baik
tidaknya pemisahan setiap senyawa yang dikandung dalam ekstrak secang dalam
KCKT.
Tujuan
Penelitian bertujuan melakukan pengoptimuman fase gerak KCKT dengan
mixture design untuk memperoleh sidik jari kromatografi ekstrak secang yang
TINJAUAN PUSTAKA
Secang (Caesalpinia sappan)
Tanaman secang termasuk famili fabaceae. Tanaman ini merupakan
tumbuhan perdu yang memanjat atau pohon kecil, berduri banyak, dengan tinggi
mencapai 5-10 m. Batang dan percabangannya berduri, berwarna coklat
keunguan, sedangkan ranting dan tunasnya berbulu kecoklatan. Daunnya
bertumpu, bersirip ganda, dan panjangnya mencapai 50 cm. Bunganya berwarna
kuning dan berbuah polong yang merekah setelah matang. Akarnya berserabut
dan berwarna gelap (Gambar 1).
Gambar 1. Tanaman secang (dokumen pribadi).
Tanaman secang tersebar di Asia Tenggara, Afrika, dan Amerika. Hasil
isolasi yang dilakukan terhadap secang menunjukkan adanya senyawa diterpenoid
(Yodsaue 2007), senyawa aktif flavonoid dan fenolik, yaitu 4-0-metilsapanol,
protosappanin A, protosappanin B, protosappanin E, brazilin, brazilein, caesalpini,
brazilide A, neosapanone, 7,3,4-trihidroksi-3-benzil-2H (Batubara at al. 2010).
Secang merupakan salah satu tanaman yang memiliki banyak khasiat dalam
pengobatan di antaranya sebagai pembersih darah, antikanker (Park et al. 2002;
Lee 2004), serta immunostimulan, antimikroba (Lim et al. 2007). Secang dapat
dikembangkan sebagai bahan antiioksidan dalam kosmetik. Ekstrak metanol
maupun ekstrak etanol 50% merupakan ekstrak yang paling berpotensi sebagai
antijerawat berdasarkan aktivitasnya menghambat pertumbuhan bakteri
propionibakterium acnes, serta menghambat aktivitas lipase (Batubara et al.
2010).
Ekstraksi
Ekstraksi merupakan metode pemisahan suatu zat terlarut secara selektif
dari suatu bahan dengan pelarut tertentu. Pemilihan metode yang tepat tergantung
pada tekstur, kandungan air tanaman yang diekstraksi, dan jenis senyawa yang
akan diisolasi (Harborne 1987).
Metode ekstraksi maserasi umum digunakan untuk mengekstraksi sampel
yang relatif tidak tahan panas. Metode ini hanya dilakukan dengan merendam
sampel dalam suatu pelarut dengan jangka waktu tertentu, biasanya dilakukan
selama 24 jam tanpa menggunakan pemanas. Kelebihan metode ini diantaranya
sederhana dan bisa menghindari kerusakan komponen senyawa akibat panas.
Kelemahan metode ini ditinjau dari segi waktu dan penggunaan pelarut yang tidak
efektif dan efisien karena jumlah pelarut relatif banyak dan waktunya lebih lama
(Meloan 1999).
Metode ekstraksi sonikasi memanfaatkan gelombang ultrasonik dengan
frekuensi 42 kHz yang dapat mempercepat waktu kontak antara sampel dan
pelarut meskipun pada suhu ruang. Hal ini menyebabkan proses perpindahan
massa senyawa bioaktif dari dalam sel tanaman ke pelarut menjadi lebih cepat.
Sonikasi mengandalkan energi gelombang yang menyebabkan proses kavitasi,
yaitu proses pembentukan gelembung-gelembung kecil akibat adanya transmisi
gelombang ultrasonik untuk membantu difusi pelarut ke dalam dinding sel
tanaman (Ashley et al. 2001).
Aktivitas Antioksidan
Secara umum, antioksidan didefinisikan sebagai senyawa yang dapat menunda,
adalah zat yang dapat menunda atau mencegah terjadinya reaksi oksidasi radikal
bebas. Terdapat dua kategori antioksidan yaitu antioksidan alami dan antioksidan
sintetik. Antioksidan alami dapat berupa senyawa fenolik (tokoferol, flavonoid,
dan antioksidan), senyawa nitrogen (alkaloid, turunan klorofil, asam amino, dan
amina), atau karotenoid seperti asam askorbat (Apak et al. 2007).
Antioksidan memiliki banyak manfaat bagi kesehatan seperti mencegah
penyakit kanker, mencegah penuaan dini, kerusakan kulit dan penyakit-penyakit
lain (Yuwono 2009). Sebagian besar penyakit jerawat dengan kondisi kronis dapat
disebabkan oleh stres oksidatif, sehingga diperlukan antioksidan untuk
mengurangi stres oksidatif tersebut pada penderita penyakit jerawat kronis
(Batubara et al. 2009).
Aktivitas antioksidan dapat diukur dengan menggunakan metode
penangkapan radikal bebas stabil DPPH (1,1-diphenyl-2-picrylhidracyl). DPPH
adalah suatu radikal bebas stabil, berwarna ungu dalam larutan dan dapat bereaksi
dengan radikal lain membentuk suatu senyawa stabil. Selain itu DPPH juga dapat
bereaksi dengan atom hidrogen (berasal dari suatu antioksidan) membentuk DPPH
tereduksi (DPPH Hidrazin) yang stabil. Aktivitas antioksidan dinyatakan dengan
persentase penghambatan (inhibisi) yang diperoleh dari nilai absorbansi blanko
dikurangi absorbansi sampel. Metode DPPH adalah metode yang cepat, mudah,
dan sensitif untuk mengukur aktivitas antioksidan suatu ekstrak tumbuhan
(Pourmorad 2006).
1,1-difenil-2-pirilhidrazil 1.1-difenil-2-pikrilhidrazin (ungu) (kuning)
Gambar 2. Reaksi penangkapan radikal bebas DPPH (Prakash 2001).