UJI EFEK
VIRGIN COCONUT OIL
(VCO)
TERHADAP BERAT BADAN DAN PENURUNAN
KADAR GULA DARAH (KGD) TIKUS PUTIH
DIABETES YANG DIINDUKSI STREPTOZOTOCIN
(STZ)
TESIS
Oleh
AFRIADI
057014001
PROGRAM MAGISTER FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
UJI EFEK VIRGIN COCONUT OIL (VCO)
TERHADAP BERAT BADAN DAN PENURUNAN KADAR GULA
DARAH (KGD)
TIKUS PUTIH DIABETES YANG DIINDUKSI STREPTOZOTOCIN
(STZ)
TESIS
Untuk memperoleh Gelar Magister Sains
dalam Program Studi Magister Farmasi
pada Fakultas Farmasi Universitas Sumatera Utara
Oleh
AFRIADI
057014001
PROGRAM STUDI MAGISTER FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
Judul : Uji Efek Virgin Coconut Oil (VCO) Terhadap Berat Badan Dan Penurunan Kadar Gula Darah (KGD) Tikus Putih
Diabetes yang Diinduksi Sterptozotocin (STZ)
Pemrasaran : Afriadi
NIM : 057014001
Program Studi : Ilmu Farmasi
Menyetujui, Komisi Pembimbing :
Prof. Dr. Urip Harahap, Apt. Ketua
dr. Dharma Lindarto, SpPD KEMD. Anggota
Ketua Progarm Studi,
Prof. Dr. Urip Harahap, Apt.
Dekan,
KATA PENGANTAR
Puji Syukur kehadirat Allah SWT yang telah memberikan rahmat kepada
kita semua sehingga penulis dapat menyelesaikan tesis sebagai syarat untuk
mendapatkan gelar Magister pada Program Magister Ilmu Farmasi, Fakultas
Farmasi Universitas Sumatera Utara Medan.
Penulis mengucapkan terima kasih sebesar-besarnya kepada Ibunda Rosna
Taher dan istri tercinta Ernoviya, juga Kakak dan Abang yang telah memberikan
semangat, motivasi dan bantuan baik materil maupun moril sehingga penulis
dapat menyelesaikan tesis ini untuk mendapatkan gelas magister.
Ucapan terima kasih yang sebesar-besarnya juga penulis sampaikan kepada
:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt. Dekan Fakultas Farmasi
Universitas Sumatera Utara yang telah membantu penulis memberikan
masukkan dalam tesis juga urusan administrasi di Program Magister Ilmu
Farmasi.
2. Bapak Prof. Dr. Urip Harahap, Apt. Ketua Program Doktor dan Magister
Farmasi Universitas Sumatera Utara Medan dan sebagai dosen pembimbing
yang telah membimbing penulis hingga dapat menyelesaikan tesis ini.
3. Bapak dr. Dharma Lindarto, SpPD., KEMD, sebagai dosen pembimbing yang
telah membimbing penulis hingga dapat menyelesaikan tesis ini.
4. Teman-teman yang telah memberikan semangat, motivasi sehingga penulis
Penulis sadar masih banyak kekurangan dalam tesis namun dengan rendah hati
kami berharap tesis ini dapat jadi pedoman bagi peneliti yang ingin melakukan
penelitian tentang vco maupun diabetes.
Akhirnya penulis mengucapkan terima kasih atas kritik dan saran agar tesis
ini menjadi lebih baik.
Medan, Juli 2010
Penulis
Abstrak
Indonesia memiliki sumber daya alam yang potensial untuk
dikembangkan, terutama tumbuhan-tumbuhan karena bebarapa diantaranya
berkhasiat sebagai obat untuk penyakit degenaratif seperti halnya diabetes
melitus. Virgin Coconut Oil (VCO) yang berasal dari kelapa hijau diduga dapat
menurunkan kadar gula darah pada penderita diabetes melitus.
Telah dilakukan pengujian efek VCO dengan dosis bervariasi terhadap
kadar gula darah (KGD) dan berat badan pada tikus putih diabetes melitus yang
diinduksi streptozotosin (STZ). Metode yang digunakan adalah metode
eksperimental di laboratorium dengan desain rancangan acak lengkap (RAL).
Data dianalisis secara Anava (analisis variansi) dan dilanjutkan dengan uji beda
rata-rata duncan menggunakan program Statistical and Product Service Solution
(SPSS).
Berdasarkan hasil penelitian VCO dosis 2,0 ml/kg bb menurunkan kadar
gula darah (KGD) lebih kecil dibandingkan dengan VCO dosis 4,0 ml/kg bb
sedang VCO dosis 801 ml/kg bb menunjukkan penurunan KGD yang tidak
berbeda nyata dengan glibenklamid 1 mg/kg bb. Pengaruh pada berat badan tikus
yang diberi VCO menunjukkan peningkatan sesuai dengan dosis VCO.Ini
mengisyaratkan bahwa VCO yang diuji berkemampuan menurunkan kadar gula
darah dan meningkatkan berat badan pada tikus putih diabetes yang diinduksi
Abstract
Indonesia is endowed with rich natural potensial for development,
especially the plants some or them have the medical efficacy for degenerative
disease treatment such as diabetes mellitus. Virgin coconut oil (VCO) derivated
from coconut has been assumed to decrease the concentration of glucose in blood
with diabetes mellitus.
The study of VCO effect in various dosage on conentration of blood
glucose and body weight of rat with streptozotocin (STZ) induced diabetes
mellitus has been conducted. The method used was experimental method in
laboratory by randomized complete design. The data was analyzed by Anava
(Analysis of Varians) and continued with mean variance test of Dancan by using
the Statistical and Product Service Solution(SPSS)program.
The result of this research showed,2.0 ml/kg bw of VCO decrease the
concentration of blood glucose less than 4.0 ml/kg bw of VCO, where 8.0 ml/kg
bw of VCO the insignificant decrease in concentration of blood glucose with 1
mg/kg bw of glibenklamid.The observation of body weight of rat was also
conducted high dosage of VCO administered to rat showed the increasing of body
weight of mice.That result indicated that VCO was effective for decreasing blood
glucose concentration and increasing body weight in STZ induced diabetes
DAFTAR ISI
KATA PENGANTAR iv
ABSTRAK vi
ABSTRACT vii
DAFTAR ISI viii
DAFTAR TABEL xi
DAFTAR GAMBAR xii
DAFTAR LAMPIRAN xiii
BAB I PENDAHULUAN 1
1.1 Latar Belakang 1
1.2 Kerangka Pikir Penelitian 3
1.3 Perumusan Masalah 4
1.4 Hipotesis 4
1.5 Tujuan Penelitian 4
1.6 Manfaat Penelitian 4
BAB II TINJAUAN PUSTAKA 6
2.1 Uraian Tumbuhan 6
2.1.1 Morfologi Tumbuhan 6
2.1.2 Sistematika Tumbuhan 7
2.1.3 Faktor-faktor yang Mempengaruhi Pertumbuhan Tanaman
Kepala 7
2.1.3.1 Keadaan Iklim 7
2.1.3.1 Keadaan Tanah 8
2.3 Kandungan Kimia Minyak Kelapa 13
2.4 Manfaat Minyak Kelapa 14
2.5 Insulin 15
2.6 Diabetes Melitus 16
2.6.1 Defenisi 16
2.6.2 Klasifikasi 16
2.6.3 Diagnosis Diabetes Melitus 22
2.6.4 Diabetes Melitus pada Hewan 23
2.6.5 Efek Akut Diabetes Melitus 27
2.6.6 Komplikasi Diabetes Melitus 28
2.6.7 Obat Antidiabetes Oral 29
BAB III METODOLOGI PENELITIAN 31
3.1 Alat-alat 32
3.2 Bahan-bahan 32
3.2.1 Bahan Uji 32
3.2.2 Bahan Kimia 32
3.2.3 Hewan Percobaan 32
3.3 Penyediaan Bahan Uji 32
3.4 Pembuatan VCO 32
3.5 Penyiapan Penginduksi, Bahan Uji dan Obat Pembanding untuk
Pengujian Farmakologi 33
3.6 Prosedur Kerja Untuk Pengujian Farmakologi 34
3.7 Pembedahan Hewan Uji 35
3.8 Pembuatan Preparat Pankreas pada Tikus Putih 35
3.10 Analisis Data 39
3.11 Definisi Operasional 39
BAB IV HASIL PEMBAHASAN 40
BAB V KESIMPULAN DAN SARAN 48
5.1 Kesimpulan 48
5.2 Saran 48
DAFTAR PUSTAKA 49
LAMPIRAN 51
Tabel 2.2 Komposisi asam lemak minyak kelapa 14
Tabel 3.1 Matriks rancangan percobaan 31
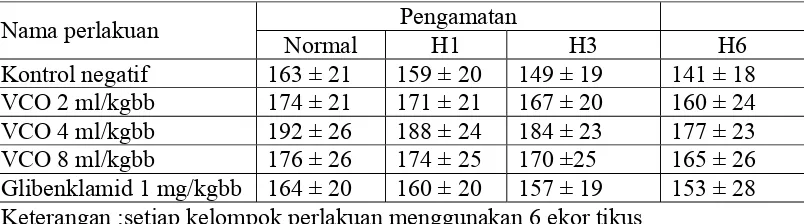
Tabel 4.1 Perubahan KGD tikus diabetes yang diinduksi STZ (purata ±
SEM) 40
Tabel 4.2 Uji beda rata-rata lanjutan Duncan pada hari ke 3 42
Tabel 4.3 Uji beda rata-rata lanjutan Duncan pada hari ke 6 43
Tabel 4.4 Perubahan berat badan sebelum dan setelah pemberian STZ 46
Gambar 1.1 Skema yang mengambarkan kerangka pikir penelitian 4
Gambar 2.1 Mediasi insulin dalam proses uptake glukosa 21
Gambar 2.2 Sturuktur Kimia Aloksan 23
Gambar 2.3 Struktur Kimia Streptozotocin 26
Gambar 3.1 Alat glukotes 36
Gambar 3.2 Petunjuk penggunaan alat 38
Gambar 4.1 Diagram yang menunjukkan keadaan KGD selama 6 hari 41
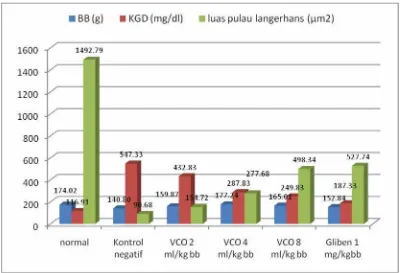
Gambar 4.2 Hubungan antara berat badan dan kadar gula darah 47
Lampiran 1 Gambar buah kelapa hijau (Cocos nucifera) 51
Lampiran 2 Data Pengukuran Berat Badan dan KGD pada diabetes
dengan
perlakuan yang berbeda 52
Lampiran 3 Data Perubahan KGD 54
Lampiran 4 Analisa statistik nilai KGD pada tikus diabetes yang diberi
masing-masing perlakuan 55
Lampiran 5 Berat tikus putih sehat sebagai kontrol normal 64
Lampiran 6 Tabel komversi dosis 65
Abstrak
Indonesia memiliki sumber daya alam yang potensial untuk
dikembangkan, terutama tumbuhan-tumbuhan karena bebarapa diantaranya
berkhasiat sebagai obat untuk penyakit degenaratif seperti halnya diabetes
melitus. Virgin Coconut Oil (VCO) yang berasal dari kelapa hijau diduga dapat
menurunkan kadar gula darah pada penderita diabetes melitus.
Telah dilakukan pengujian efek VCO dengan dosis bervariasi terhadap
kadar gula darah (KGD) dan berat badan pada tikus putih diabetes melitus yang
diinduksi streptozotosin (STZ). Metode yang digunakan adalah metode
eksperimental di laboratorium dengan desain rancangan acak lengkap (RAL).
Data dianalisis secara Anava (analisis variansi) dan dilanjutkan dengan uji beda
rata-rata duncan menggunakan program Statistical and Product Service Solution
(SPSS).
Berdasarkan hasil penelitian VCO dosis 2,0 ml/kg bb menurunkan kadar
gula darah (KGD) lebih kecil dibandingkan dengan VCO dosis 4,0 ml/kg bb
sedang VCO dosis 801 ml/kg bb menunjukkan penurunan KGD yang tidak
berbeda nyata dengan glibenklamid 1 mg/kg bb. Pengaruh pada berat badan tikus
yang diberi VCO menunjukkan peningkatan sesuai dengan dosis VCO.Ini
mengisyaratkan bahwa VCO yang diuji berkemampuan menurunkan kadar gula
darah dan meningkatkan berat badan pada tikus putih diabetes yang diinduksi
Abstract
Indonesia is endowed with rich natural potensial for development,
especially the plants some or them have the medical efficacy for degenerative
disease treatment such as diabetes mellitus. Virgin coconut oil (VCO) derivated
from coconut has been assumed to decrease the concentration of glucose in blood
with diabetes mellitus.
The study of VCO effect in various dosage on conentration of blood
glucose and body weight of rat with streptozotocin (STZ) induced diabetes
mellitus has been conducted. The method used was experimental method in
laboratory by randomized complete design. The data was analyzed by Anava
(Analysis of Varians) and continued with mean variance test of Dancan by using
the Statistical and Product Service Solution(SPSS)program.
The result of this research showed,2.0 ml/kg bw of VCO decrease the
concentration of blood glucose less than 4.0 ml/kg bw of VCO, where 8.0 ml/kg
bw of VCO the insignificant decrease in concentration of blood glucose with 1
mg/kg bw of glibenklamid.The observation of body weight of rat was also
conducted high dosage of VCO administered to rat showed the increasing of body
weight of mice.That result indicated that VCO was effective for decreasing blood
glucose concentration and increasing body weight in STZ induced diabetes
BAB I PENDAHULUAN
1.1 Latar Belakang
Indonesia merupakan salah satu negara penghasil tanaman obat yang
potensial dengan keanekaragaman hayati yang dimilikinya. Pada hutan tropika di
Indonesia, tumbuh subur sekitar 30.000 spesies tumbuhan berbunga dan
diperkirakan sekitar 3.689 spesies di antarannya merupakan tumbuhan obat. Dari
sejumlah tanaman obat tersebut menurut Dirjen POM baru sebanyak 283 spesies
tumbuhan obat yang sudah digunakan dalam industri obat tradisional
(Djauhariya dan Hernani, 2004). Ini menunjukkan bahwa masih banyak tumbuhan
obat yang berpotensi untuk dikembangkan.
Sebagian besar tumbuhan telah banyak menarik perhatian ilmuan untuk
diteliti lebih lanjut terutama tumbuhan yang bermanfaat untuk pengobatan
berbagai penyakit, terutama penyakit degenaratif seperti halnya diabetes mellitus
(Djauhariya dan Hernani, 2004).
Diabetes adalah suatu penyakit akibat gangguan produksi atau penggunaan
insulin. Insulin adalah hormon yang diperlukan untuk mengubah gula, karbohidrat
dan zat makanan lain menjadi energi yang digunakan untuk proses hidup. Sampai
saat ini penyebab diabetes masih merupakan misteri, walaupun faktor genetik,
kegemukan dan kurangnya olah raga memiliki peranan penting (ADA, 2008).
Diabetes melitus merupakan salah satu penyakit yang menjadi masalah
pada kesehatan masyarakat, termasuk dalam urutan keempat prioritas penelitian
nasional untuk penyakit degeneratif setelah penyakit kardiovaskular,
Kasus penyakit diabetes mellitus sekarang ini banyak terjadi di Indonesia
maupun di negara lain. Menurut penelitian diabetes di Surabaya dan hasil analis
data dari poliklinik diabetes di seluruh Indonesia, diperkirakan jumlah penderita
diabetes di Indonesia pada tahun 1994 adalah 2,5 juta jiwa. Pada tahun 2000
penderita meningkat menjadi 4 juta jiwa. Pada tahun yang sama paling sedikit 240
juta penduduk dunia menderita diabetes (Ribawan dan Hernani, 2004). Di negara
lain seperti Amerika Serikat sekitar 5-10% dari penderita diabetes penduduk tipe 1
selebihnya adalah tipe 2 (ADA, 2008). Sekarang sudah banyak obat-obatan untuk
diabetes melitus terlebih obat hipoglikemik, tetapi karena penggunaannya terus
menerus untuk menjaga kadar gula darah agar terkontrol, tentu banyak biaya yang
dikeluarkan dan ini menjadi beban bagi penderita, sehingga perlu dicari obat
alternatif lain bagi penderita diabetes, yaitu obat yang berasal dari tumbuhan.
Berdasarkan hal-hal tersebut di atas, perlu dilakukan penelitian tumbuhan
yang memiliki khasiat hipoglikemik. Salah satu jenis tanaman obat yang
berpotensi dan sudah dikembangkan adalah kelapa. Kelapa sangat populer di
masyarakat karena memiliki banyak manfaat bagi kehidupan manusia. Beragam
manfaat tersebut diperoleh dari daging buah, air, sabut, tempurung, daun dan
batangnya. Bagian terpenting dari kelapa adalah buahnya karena bagian tersebut
dapat diolah menjadi berbagai produk seperti kopra, dessicated coconut, santan
kelapa dan minyak kelapa (Alamsyah, 2005).
Minyak kelapa pada umumnya dibagi menjadi 2 (dua) kategori utama
yaitu RBD (Refined, Bleached and Deodorized) dan Virgin. Perbedaannya adalah
pada proses pembuatan dan pemilihan buahnya yang mempengaruhi kualitas,
coconut oil (VCO) merupakan salah satu hasil olahan dari buah kelapa (Cocos nucifera) yang diperoleh melalui pendinginan tanpa penambahan bahan kimia.
Pada masyarakat, umumnya minyak kelapa sering digunakan untuk
menggoreng, melembutkan rambut dan menyembuhkan berbagai penyakit
misalnya diabetes mellitus, kolesterol, penyakit jantung, influensa, luka bakar,
antikerut, dan penuaan dini (Sutarmi, dkk., 2005).
Berdasarkan hal di atas maka peneliti merasa perlu dan tertarik
melakukan penelitian sesuai dengan bidang kefarmasian, yaitu untuk mengetahui
pengaruh VCO terhadap besarnya penurunan kadar gula darah akibat pemberian
Streptozotocin (STZ). Hasil tersebut diharapkan akan memberi informasi ilmiah
untuk menjadikan VCO sebagai salah satu alternatif pengobatan diabetes melitus
yang banyak dialami masyarakat.
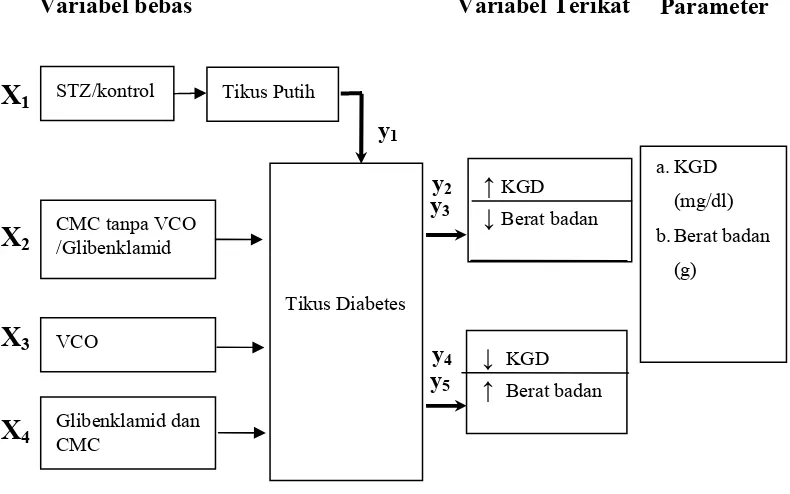
1.2 Kerangka Pikir Penelitian
Kerangka penelitian ini terdiri dari 2 variabel yaitu variabel bebas dan
variabel terikat ditunjukkan pada Gambar 1.1.
Variabel bebas Variabel Terikat Parameter
STZ/kontrol
1.3 Perumusan Masalah
Berdasarkan latar belakang yang dipaparkan di atas, maka rumusan
permasalahan penelitian adalah:
a. apakah VCO menurunkan kadar gula darah tikus putih yang diinduksi
STZ.?
b. apakah VCO meningkatkan berat badan tikus diabetes yang diinduksi
STZ.?
c. apakah ada perbedaan efek pemberian VCO dengan glibenklamid?
1.4 Hipotesis
Berdasarkan rumusan masalah di atas, maka hipotesis penelitian adalah:
a. VCO dapat menurunkan kadar gula darah tikus putih yang diinduksi STZ.
b. VCO dapat meningkatkan berat badan tikus diabetes yang diinduksi STZ.
c. tidak ada perbedaan efek diabetes yang VCO dengan glibenklamid.
1.5 Tujuan Penelitian
Berdasarkan hipotesis di atas, maka tujuan penelitian ini adalah untuk:
a. mengetahui efek penurunan kadar gula darah tikus putih yang diinduksi
STZ oleh VCO
b. mengetahui efek VCO terhadap peningkatan berat badan tikus diabetes
yang diinduksi STZ.
c. mengetahui perbedaan efek penurunan kadar gula darah antara VCO
dengan glibenklamid.
1.6 Manfaat Penelitian
Manfaat penelitian ini diharapkan:
a. sebagai bahan pertimbangan bahwa VCO dapat digunakan sebagai obat
b. menunjang program pemerintah dalam pengembangan obat tradisional
sehingga dapat diikutsertakan dalam pelayanan kesehatan masyarakat
c. menambah inventaris obat antidiabetes yang mudah didapat dengan harga
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan terdiri dari morfologi tumbuhan, sistematika,
faktor-faktor yang mempengaruhi pertumbuhan tanaman kelapa.
2.2 Morfologi Tumbuhan
a. Batang
Batang tumbuhan tegak lurus ke atas sesuai dengan arah sinar matahari,
tidak bercabang dan tidak berkambium. Di ujung batang terdapat titik tumbuh
yang berfungsi membentuk daun, batang dan bunga. Tinggi pohon kelapa
bergantung pada faktor iklim, kesuburan tanah serta lingkungan lahan.
b. Akar
Tanaman kelapa berakar serabut dan membutuhkan banyak unsur hara
makro C, H, O, N, S, P, K, Ca, Mg maupun unsur mikro seperti Cl.
c. Daun
Daun kelapa berbentuk memanjang dan bertulang sejajar dan tumbuh
lebih cepat pada musim hujan.
d. Bunga
Bunga kelapa merupakan bunga berkarang dikenal dengan sebutan
mayang. Bunga jantan dan betina terdapat dalam satu pohon, bunga betina terletak
di pangkal cabang dan bunga jantan di ujung cabang.
e. Buah
dibuahi, bunga betina mulai tumbuh menjadi buah kira-kira 3-4 minggu setelah
mayang terbuka. Buah mencapai ukuran maksimum pada usia 9-10 bulan
(Wahyuni, 2000).
2.1.2 Sistematika Tumbuhan
Sistematika tumbuhan kelapa (Suhardiman, 1999)
Divisi : Spermatophyta
Sub Divisi : Angiospermae
Kelas : Monocotyledoneae
Bangsa : Palmales
Suku : Palmae
Genus : Cocos
Spesies : Cocos nucifera
Tanaman kelapa merupakan tanaman asli daerah tropis dan dapat dijumpai
di seluruh wilayah Indonesia. Kelapa dapat tumbuh dan berkembang dengan baik
bila ditanam di tempat yang sesuai dengan syarat tumbuh tanaman kelapa. Faktor
iklim dan tanah merupakan faktor paling dominan dalam pertumbuhan kelapa.
2.1.3 Faktor-faktor yang Mempengaruhi Pertumbuhan Tanaman Kelapa
2.1.3.1 Keadaan Iklim
a. Suhu
Tanaman kelapa tumbuh dengan baik pada suhu antara 27-280C. Pada
suhu di bawah 200C dan di atas 300C pertumbuhan tanaman kelapa tidak baik dan
b. Curah hujan
Tanaman kelapa dengan baik pada curah hujan 1.000-2.250 mm per
tahun. Untuk mendapatkan hasil yang baik curah hujan yang dikehendaki adalah
1.500-2.000 mm per tahun yang tersebar merata sepanjang tahun. Tanaman kelapa
tidak akan tumbuh dan berkembang bila ditanam di daerah dengan curah hujan
tidak merata. Apabila curah hujan lebih dari 50 mm per tahun maka produksi
kelapa akan rendah.
c. Sinar matahari
Tanaman kelapa akan tumbuh baik dan produktif bila intensitas
penyinaran matahari tinggi. Jumlah penyinaran yang dibutuhkan tidak kurang dari
2000 jam/tahun
d. Kelembaban
Kelembaban yang dibutuhkan kelapa agar tumbuh baik dan produktif
adalah 70-80% dengan kelembaban minimum 65%.
e. Ketinggian tempat
Ketinggian tanah yang cocok untuk tanaman kelapa adalah 0-600 M di
atas permukaan laut dan yang terbaik adalah kurang dari 400 M di atas permukaan
laut.
2.1.3.2 Keadaan Tanah
Kelapa dapat tumbuh subur pada pH 5-8, dan tumbuh optimum pada pH
5,5-6,5. Tanah yang mengandung fosfor dan kalium sangat baik bagi pertumbuhan
kelapa. Di pesisir pantai, pohon kelapa dapat tumbuh dengan baik dan produktif
meski pun kandungan NaCl tinggi karena ada infiltrasi dari air laut. Hal ini
disebabkan air yang bergerak banyak mengandung oksigen yang penting untuk
2.2 VCO
VCO merupakan minyak yang berasal dari buah kelapa (Cocos nucifera)
tua segar yang diolah pada suhu rendah (<600C), dimasak dan dijaga warnanya
tidak boleh sampai coklat tua. Selain itu dilakukan juga proses pemutihan dan
hidrogenasi sehingga menghasilkan minyak murni. Proses tersebut dikenal dengan
sebutan minyak perawan (Virgin Coconut Oil) atau ada juga yang menamainya
minyak dara (Sutarmi dan Rozaline, 2005).
Banyak cara yang dilakukan untuk menghasilkan minyak VCO. Umumnya
terdiri dari proses vakum pada suhu 600C, fermentasi, enzimatis dan pendinginan.
a. Proses vakum pada suhu 600C
i. Daging buah kelapa tua segar dicungkil
ii. Daging buah kelapa dicuci sampai bersih
iii. Daging buah kelapa diparut
iv. Hasil parutan dimasukkan kedalam mesin pemeras tanpa air
(menghasilkan santan)
v. Santan dimasukkan kedalam alat vakum pada suhu 600C
vi. Biarkan beberapa jam sampai terbentuk minyak
vii. Minyak disaring
viii. Minyak siap dikemas dan digunakan
b. Proses fermentasi
i. Daging buah kelapa tua segar dicungkil
ii. Daging buah kelapa dicuci sampai bersih
iii. Daging buah kelapa diparut
iv. Hasil parutan dimasukkan kedalam mesin pemeras tanpa air
v. Santan dimasukkan kedalam tabung fermentasi, biarkan selama 12 jam
pada suhu 300-350C. Setelah 12 jam akan terbentuk 4 lapisan yaitu
endapan tepung, air, blondo dan minyak.
vi. Kran tabung fermentasi dibuka untuk memisahkan lapisan-lapisan
tersebut.
vii. Lapisan minyak yang diperoleh dimasukkan kedalam galon air mineral
(posisi galon terbalik dan ujungnya diberi kran). Diamkan beberapa jam
akan terbentuk 2 lapisan yaitu blondo dan minyak. Pada tahap ini
minyak yang dihasilkan adalah VCO, tetapi kadar airnya masih tinggi.
viii. VCO dimasukkan kedalam mesin vakum selama 4 jam pada suhu 600C,
tujuannya mengurangi kadar air dalam VCO kemudian disaring.
ix. VCO sudah dapat dikemas dan digunakan.
c. Proses enzimatis
i. Daging buah kelapa tua segar dicungkil
ii. Daging buah kelapa dicuci sampai bersih
iii. Daging buah kelapa diparut
iv. Hasil parutan dimasukkan kedalam mesin pemeras tanpa air
(menghasilkan santan)
v. Hasil perasan (santan) dicampur dengan enzim. Pada proses ini dapat
menggunakan enzim yang barasal dari nenas (anannase) atau pepaya
(papain). Biarkan beberapa jam, lalu timbul 3 lapisan yaitu minyak,
blondo dan air
vi. Minyak disaring menggunakan penyaring ukuran 400 mes dan saringan
1 mikron.
d. Proses pendinginan terdiri atas 2 cara pembuatan yaitu :
Cara mixer
i. Daging buah kelapa tua segar dicungkil
ii. Daging buah kelapa dicuci sampai bersih
iii. Daging buah kelapa diparut
iv. Hasil parutan dimasukkan ke dalam mesin pemeras tanpa air
(menghasilkan santan)
v. Santan didinginkan pada suhu 1-100C
vi. Mixer sampai terbentuk gumpalan
vii. Gumpalan dipanaskan pada suhu 450C (selama 60 menit) sapai
gumpalan mencair. Setelah mencair akan terbentuk 3 lapisan yaitu
minyak, blondo dan air, lalu lapisan minyak diambil
viii. Minyak di vakum pada suhu 600C untuk mengurangi kadar air dalam
minyak
ix. Minyak disaring menggunakan penyaring ukuran 400 mes dan 1
mikron
x. Minyak siap dikemas dan digunakan
Cara sentrifugal
i. Daging buah kelapa tua segar dicungkil
ii. Daging buah kelapa dicuci sampai bersih
iii. Daging buah kelapa diparut
iv. Hasil parutan dimasukkan ke dalam mesin pemeras tanpa air
(menghasilkan santan)
v. Santan didinginkan pada suhu 1-100C
vii. Wadah yang berisi santan dimasukkan kedalam alat setrifugal terbentuk
4 lapisan yaitu tepung, air, blondo dan minyak, lalu lapisan minyak
diambil
viii. Minyak divakum pada suhu 600C untuk mengurangi kadar air dalam
minyak
ix. Minyak disaring menggunakan penyaring ukuran 400 mes dan 1 mikron
x. Minyak siap dikemas dan digunakan
Masing- masing proses tersebut mempunyai kelebihan dan kekurangan :
a. Proses vakum pada suhu 600C
Kelebihan proses ini, adalah kadar air yang dikandung minyak sedikit
dan rasanya segar dan jernih.
Kekurangan proses ini, adalah warnanya sedikit kuning dan waktu yang
dibutuhkan untuk menghasilkan minyak lama yaitu 24-48 jam.
b. Proses fermentasi
Kelebihan proses ini, adalah minyak yang dihasilkan lebih banyak.
Menurut berbagai penelitian kadar asam laurat paling tinggi diperoleh
dengan proses ini (46-55%). Selain menghasilkan lemak berantai
sedang, keberadaan vitamin E dan enzim-enzim yang terkandung dalam
daging buah kelapa dapat tetap dipertahankan. Cara ini paling mudah
diterapkan ditingkat rumah tangga.
Kekurangan proses ini, adalah terbawanya banyak enzim kedalam
minyak, prose dari kelapa sampai diolah menjadi minyak membutuhkan
c. Proses enzimatis
Kelebihan proses ini, adalah prosesnya lebih cepat dibandingkan dengan
proses fermentasi.
Kekurangan proses ini, adalah cara ini dapat mengeluarkan
enzim-enzim yang terkandung dalam minyak kelapa.
d. Proses pendinginan
Kelebihan proses ini, adalah waktu yang singkat untuk membuat
minyak, rasa manis dan aroma segar seperti air kelapa muda.
Kekurangan proses ini, adalah diperlukan investasi yang cukup besar
karena harga alat pendukung masih mahal (Sutarmi dan Rozaline,
2005).
2.3 Kandungan Kimia Minyak Kelapa
Secara kimiawi minyak kelapa terbentuk dari rantai karbon, hidrogen dan
oksigen yang disebut asam lemak. Asam lemak digabung oleh satu molekul
gliserol membentuk gliserida. Gliserida yang terdapat pada minyak dan lemak
adalah trigliserida (lipida). Diperlukan tiga molekul asam lemak yang dikombinasi
dengan satu molekul trigliserida (Kuncoro dan Maloedyn, 2005).
Komponen minyak kelapa terdiri dari asam lemak jenuh (90%) dan asam
lemak tak jenuh (10%). Dalam minyak kelapa murni terdapat MCFA (medium
chain fatty acid). MCFA merupakan komponen asam lemak berantai sedang yang memiliki banyak fungsi, antara lain mampu merangsang produksi insulin sehingga
proses metabolisme glukosa dapat berjalan normal. Selain itu MCFA juga
bermanfaat dalam mengubah protein menjadi sumber energi. Minyak kelapa
murni juga mengandung asam laurat dan asam lemak jenuh berantai pendek,
nutrisi makanan menjadi energi. Fungsi lain dari zat ini antara lain sebagai
antivirus antiprotozoa (Sutarmi dan Rozaline, 2005).
Tabel 2.2. Komposisi asam lemak minyak kelapa
No. Jenis Uji Satuan Persyaratan Mutu
1
Air dan senyawa yang menguap Bilangan iod
Asam lemak bebas (dihitung sebagai asam laurat) 6.7 Asam stearat (C18) 6.8 Asam oleat (C18 : 1) 6.9 Asam linoleat (C18 : 2) 6.10 Asam linolenat (C18:3) Cemaran mikroba
7.1 Angka lempeng total Cemaran Logam :
8.1 Timbal (Pb) 8.2 Tembaga (Cu) 8.3 Besi (Fe) 8.4 Cadmium (Cd) Cemaran Arsen (As)
%
Khas kelapa segar,tidak tengik Normal, khas minyak kelapa Tidak berwarna hingga kuning pucat
Catatan:ND = No detection (tidak terdeteksi)
Dikutip dari Badan Standardisasi Nasional (2008), Minyak kelapavirgin (VCO)
2.4 Manfaat Minyak Kelapa
VCO mampu mengatasi penyakit degeneratif seperti diabetes mellitus,
jantung, kegemukan dan kolesterol. Diabetes mellitus di Indonesia dikenal dengan
nama kencing manis. Kencing manis adalah glikosuria (glukosa dalam urin)
Dalam kondisi ini produksi insulin atau enzim menurun sehingga metabolisme
terganggu. Hal ini menyebabkan glukosa tidak bisa masuk kedalam sel-sel
sehingga konsentrasi glukosa darah meningkat. Timbunan glukosa tersebut tidak
dapat dimanfaatkan untuk menghasilkan energi dan akhirnya dibuang bersama
urin.
Insulin berfungsi mengubah glukosa menjadi energi sel dengan cara
mentransfer glukosa ke darah dalam sel-sel yang membutuhkan. Selain itu insulin
juga mengubah glukosa menjadi energi cadangan (glikogen dan lemak).
Kandungan MCFA (medium chain fatty acid) dalam VCO mampu
merangsang produksi insulin yaitu hormon pengangkut zat gula ke dalam sel-sel
tubuh. Selain itu VCO juga dapat menembus dinding usus tanpa bantuan enzim
sehingga sel mampu menghasilkan energi lebih cepat (Sutarmi dan Rozaline,
2005).
2.5 Insulin
Insulin merupakan salah satu hormon dalam tubuh manusia yang
dihasilkan oleh sel ß pulau langerhans yang terdapat dalam kelenjar pankreas.
Hormon ini menurunkan kadar glukosa, asam lemak, dan asam amino dalam
darah (Sheerwood, 1996).
Peranan insulin dalam pengaturan kadar glukosa darah tidak lepas dari
pengaruh faktor lainnya juga, seperti (a) hati berperan sebagai glukostat, (b)
kelenjar pankreas sebagai penghasil hormon lain selain insulin yaitu glukagon, (c)
kelenjar adenohipofisis mensekresi hormon-hormon yang bersifat diabetogenik
seperti ACTH, GH, TSH; (d) kelenjar adrenal yang mensekresi hormon epinefrin
dari bagian medula dan glukokortikoid dari bagian kortek-nya, (e) kelenjar tiroid
(f) kerja fisik atau exercise yang bersifat memperkuat efek insulin terhadap metabolisme karbohidrat.
2.6 Diabetes Mellitus
2.6.1 Definisi
Diabetes adalah suatu penyakit yang ditandai bahwa tubuh tidak dapat
menghasilkan atau terjadi gangguan dalam penggunaan insulin (ADA, 2008).
2.6.2 Klasifikasi
Tipe utama penyakit diabetes adalah sebagai berikut:
a. Diabetes mellitus tipe 1
Diabetes tipe 1 atau insulin dependent diabetes mellitus (IDDM) adalah
diabetes mellitus yang selalu membutuhkan terapi insulin dari luar untuk
pengaturan aktivitas. Diabetes tipe 1 adalah kondisi yang ditandai oleh tingginya
level glukosa darah yang disebabkan oleh ketidakcukupan atau ketiadaan hormon
insulin, sehingga gula darah tidak dapat masuk ke dalam sel untuk digunakan
sebagai energi. Kondisi ini hanya bisa diobati dengan pemberian insulin. Pada saat
didiagnosa hanya sedikit sel β sehat yang memproduksi insulin. Kerusakan sel β
secara agresif menyebabkan penyakit nampak dalam beberapa bulan pada anak
yang masih muda, meskipun ada juga proses yang akan berlanjut dalam beberapa
tahun, bahkan pada beberapa kasus ada yang berlanjut lebih dari 10 tahun..
Diabetes tipe 1 diperkirakan 5-10% diderita oleh penduduk Amerika. Diabetes
mellitus jenis ini paling sering terdapat pada anak-anak dan dewasa muda.
Pemberian insulin sangat penting untuk merubah glukosa, karbohidrat dan zat
makanan lainnya untuk dijadikan energi. Pemberian insulin eksogen terutama
tidak hanya untuk menurunkan kadar glukosa plasma melainkan juga untuk
Komplikasi penyakit yang dapat terjadi pada diabetes tipe 1 adalah:
i. Penyakit jantung, orang yang menderita diabetes harus berhati – hati
kemungkinan akan mengalami penyakit jantung dan pembuluh darah.
Diabetes dapat meningkatkan resiko serangan jantung, strok, dan
komplikasi yang erat hubungannya dengan sistem sirkulasi.
ii. Nefropati, diabetes dapat menyebabkan kerusakan ginjal, tidak hanya
menyebabkan gagal fungsi ginjal namun juga akan kehilangan
kemampuan untuk menyaring produk – produk sampah dalam darah,
hal ini yang disebut dengan nefropati.
iii. Komplikasi pada mata, diabetes dapat menyebabkan permasalahan
pada mata dan bahkan dapat terjadi kebutaan. Penderita diabetes
memiliki resiko kebutaan yang lebih besar dari orang normal tanpa
diabetes. Pengetahuan dan pengobatan secara dini dapat
menyelamatkan mata dari kebutaan.
iv. Diabetes neuropati dan kerusakan sel saraf, salah satu komplikasi yang
paling umum diderita pasien diabetes adalah neuropati. Neuropati
merupakan kerusakan sel saraf yang berkelanjutan dan menyebar ke
seluruh tubuh, yaitu yang menghubungkan spinal cord dengan otot,
kulit, pembuluh darah dan organ-organ lainnya.
v. Komplikasi pada kaki, penderita diabetes dapat mengalami
permasalahan pada kaki. Permasalahan pada kaki sering terjadi ketika
terjadi kerusakan saraf kaki atau sedikitnya aliran darah yang masuk.
vi. Komplikasi pada kulit, sekitar satu dari tiga penderita diabetes akan
pernah mengalami kelainan kulit akibat dari diabetes selama hidup
adanya kelainan pada kulit dan hal ini dapat segera dicegah jika
penanganannya sedini mengkin.
vii. Depresi, semangat hidup turun, sedih dan hidup seperti tidak punya
harapan. Perasaan ini akan dialami selama 2 sampai 3 minggu bahkan
lebih pada tingkat depresi yang lebih serius (ADA, 2008).
b. Diabetes melitus tipe 2
Diabetes tipe 2 sering juga disebut noninsulin dependent diabetes mellitus
(NIDDM), sebab tidak membutuhkan penambahan hormon insulin untuk mempertahankan keseimbangan glukosa darah. Diabetes tipe 2 merupakan akibat
lemahnya kemampuan pankreas mensekresikan insulin, selain itu juga lemahnya
aksi insulin, menjadi penyebab menurunnya sensitivitas insulin. Penurunan
sensitivitas insulin terjadi pada pintu masuk di permukaan sel tubuh yang
dinamakan reseptor insulin. Reseptor insulin akan memberikan signal pada
transporter glukosa untuk memungkinkan lewatnya glukosa yang dibawa oleh
hormon insulin masuk ke dalam sel. Di dalam mitokondria, gula kemudian akan
digunakan untuk menghasilkan energi yang diperlukan untuk melangsungkan
fungsi setiap sel tubuh.
Penyebab terjadinya penurunan sensitivitas insulin adalah karena
peningkatan kebutuhan sekresi insulin untuk mempertahankan kadar glukosa
darah. Meningkatnya sekresi insulin akan menginduksi kegagalan sel β pankreas
menghasilkan insulin. Orang obesitas dan kurang olah raga mempunyai resiko
terhadap penyakit diabetes tipe 2, dengan gejala penurunan sensitivitas insulin
yang ditandai dengan : (a) jumlah insulin di dalam darahnya meningkat lebih
tinggi dibandingkan dengan orang normal, (b) penyuntikan insulin tidak dapat
Menurut Media Informasi Peresepan Rasional bagi Tenaga Kesehatan
Indonesia (2001) pada penderita diabetes tipe 2, terdapat tiga kemungkinan
kondisi abnormal. Pertama, mutlak kekurangan insulin dalam arti sekresi hormon
insulin berkurang karena kerusakan sel-sel β pankreas. Kedua, relatif kekurangan
insulin karena sekresi insulin tidak mencukupi dengan adanya kebutuhan
metabolisme yang meningkat (misalnya pada pasien yang kelebihan berat badan).
Ketiga, resisten terhadap insulin dan hiperinsulinemia karena penggunaan insulin
yang kurang sempurna. Gejala-gejala yang sering muncul pada diabetes tipe 2
adalah cepat lelah; sering kencing; sering lapar dan sering haus; penglihatan
menjadi kabur; lambatnya penyembuhan penyakit kulit, gusi dan infeksi saluran
kencing; terasa gatal pada bagian kelamin; mati rasa pada kaki atau tungkai; dan
penyakit jantung. Obesitas atau kelebihan simpanan lemak sering mengiringi atau
mendahului terjadinya penyakit diabetes tipe 2.
Pada penderita diabetes mellitus tipe sering 2 ditemukan penurunan sensitivitas
insulin. Penurunan sensitivitas insulin adalah kelainan metabolik yang dicirikan
oleh menurunnya sensitivitas jaringan terhadap insulin. Menurut NDIC (2006)
penurunan sensitivitas insulin adalah kondisi diam yang meningkatkan rantai
perkembangan penyakit diabetes mellitus dan penyakit jantung. Penurunan
sensitivitas insulin terjadi ketika jaringan gagal merespon insulin secara normal.
Diabetes tipe 2 sering disertai oleh penurunan sensitivitas insulin pada organ
sasaran yang mengakibatkan penurunan responsivitas, baik terhadap insulin
endogenus maupun eksogenus (Rimbawan dan Siagian 2004). Penurunan
sensitivitas insulin mungkin terjadi pada banyak tahapan dalam aksi biologi
insulin, dari awal telah terjadi pengikatan permukaan sel reseptor pada proses
Penurunan sensitivitas insulin biasanya paling banyak ditemukan pada kegemukan
dengan polycystic ovary syndrome (PCOS) pada wanita (65%), tetapi dapat juga
ditemukan pada 20 persen dari lean PCOS pada wanita (Dale et al., 1998). Orang
dengan diabetes tipe 2 mempunyai banyak insulin dalam tubuhnya, tetapi respon
tubuhnya terhadap insulin dalam keadaan yang tidak normal dan mengalami
penurunan sensitivitas insulin, artinya tubuh resisten terhadap insulin dalam
keadaan normal.
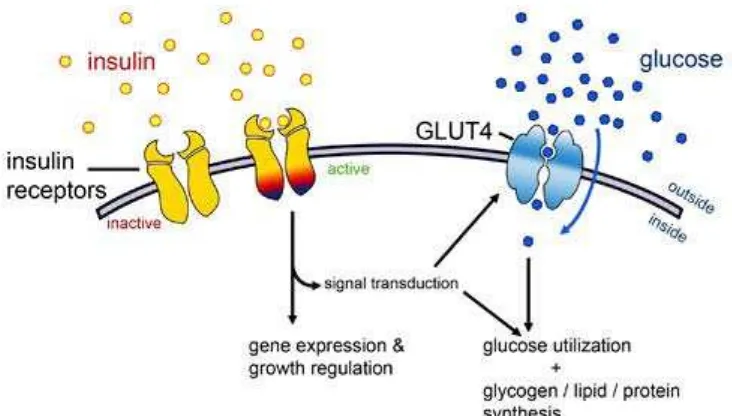
Proses uptake glukosa yang dimediasi oleh insulin ditunjukkan pada
Gambar 2.1. Insulin yang diproduksi sel β pankreas akan menempati reseptornya,
yang kemudian akan menghasilkan signal transduction pada transporter glucose
untuk dapat melakukan penyerapan glukosa, sehingga glukosa yang tersebar
dalam darah akan masuk ke dalam sel.
Menurut Rimbawan dan Siagian (2004) penurunan sensitivitas insulin
pada penderita diabetes tipe 2 dapat disebabkan oleh kerusakan signal
transduction. Kerusakan ini dapat dimulai dari insulin abnormal sampai kerusakan penerima insulin pada pengangkut glukosa.
Hubungan langsung antara penurunan sensitivitas insulin dan kegemukan
telah diketahui dengan baik, dan kegemukan adalah salah satu faktor penting
untuk memprediksi diabetes tipe 2.
Kegemukan berhubungan dengan lemahnya signal insulin, dan pola
tertentu dari penyimpanan lemak (misalnya penyimpanan lemak dalam perut)
lebih berhubungan dengan penurunan sensitivitas insulin. Meskipun otot rangka
biasanya dianggap sebagai jaringan utama yang menggunakan glukosa,
Gambar 2.1 Mediasi insulin dalam proses uptake glukosa dikutip dari Cartailler(2004)
Diabetes dapat terjadi pada semua orang tanpa melihat umur dan ras,
namun ada beberapa kelompok memiliki resiko menderita diabetes tipe 2 yang
lebih besar dari pada yang lain yaitu Afrika, Amerika, dan Asia Amerika/Pasifik
(ADA, 2008).
Diabetes tipe 2 sering kali dijumpai pada pria maupun wanita berusia di
atas 40 tahun yang memiliki kelebihan berat badan. Sampai saat ini, diabetes tipe
2 dikenal sebagai serangan diabetes bagi orang dewasa, karena kasus tersebut
tidak dijumpai pada anak-anak. Diabetes tipe 2 dapat menjadi pintu gerbang bagi
berbagai penyakit yang dapat mengancam kehidupan, resiko terbesarnya adalah
meningkatnya resiko kemungkinan berkembangnya penyakit jantung koroner
(PJK) (D’Adamo and Whitney, 2007).
c. Diabetes pada masa kehamilan
Diabetes pada masa kehamilan di alami sekitar 4% pada semua wanita
hamil, sekitar 135.000 kasus di Amerika setiap tahunnya. Pada pasien-pasien ini
d. Pra-diabetes
Pra-diabetes merupakan suatu kondisi yang terjadi ketika kadar glukosa
darah seseorang lebih tinggi dari normalnya, tetapi tidak sampai didiagnosis
sebagai diabetes tipe 2. Ada sekitar 54 juta orang Amerika menderita pra-diabetes,
dan sekitar 20,8 juta orang menjadi menderita diabetes (ADA, 2008).
2.6.3 Diagnosis Diabetes Mellitus
Diagnosis diabetes mellitus dapat ditegakkan dengan cara mengaitkan
simptom-simptom klasik dengan hiperglikemia yang jelas, atau dengan kriteria
diagnostik yang spesifik pada pasien asimptomatik. Penapisan (skrining) harus
dilakukan pada pasien dengan riwayat keluarga yang jelas menderita diabetes
mellitus, dengan obesitas yang bermakna, dengan infeksi kulit, genital atau
tractus urinarus yang kumat-kumatan; atau dengan riwayat kehamilan yang menunjukkan diabetes mellitus pada kehamilan, prematuritas, atau berat badan
bayi lebih dari 4,5 kg. Pada pasien dengan kadar glukosa plasma lebih dari 160
mg/dl atau kadar gula darah puasa di atas 115 mg/dl adalah indikasi untuk
melakukan pemeriksaan diagnostik dan tindakan lanjut yang ketat.
a. Pasien-Pasien Simptomatik
Apabila seorang pasien ditemukan gejala-gejala berupa poliuria (sering
berkemih) bersama-sama dengan polidipsia (rasa haus yang berlebihan) dan
penurunan berat badan serta kadar glukosa plasma yang lebih dari 200 mg/dl
maka pasien itu sudah dapat dianggap menderita diabetes tanpa perlu
b. Pasien-Pasien Asimptomatik
Pemeriksaan diagnostik hendaknya dilakukan apabila hasil pemeriksaan
penapisan rutin abnormal atau bila terdapat kecurigaan yang kuat bahwa
pasien menderita diabetes mellitus.
i. Kadar glukosa plasma puasa
Penderita dikatakan diabetes mellitus bila kadar glukosa plasma puasanya
lebih dari 140 mg/dl, yang dapat ditunjukkan pada sedikitnya dua kali
pemeriksaan.
ii. Uji toleransi glukosa oral
Pasien diberi glukosa 75 g pada pagi hari setelah puasa semalaman.
Hasil uji yang normal menunjukkan:
a. Kadar glukosa plasma kurang dari 115 mg/dl
b. Kadar glukosa plasma 2 jam
sesudah minum glukosa tidak lebih dari 140 gg/dl dan tidak ada kadar
glukosa yang melebihi 200 mg/dl. Nilai di antara normal dan diabetes
mellitus menunjukkan toleransi glukosa yang terganggu (Woodley dan
Whelan, 1995).
2.6.4 Diabetes Mellitus pada Hewan
Keadaan diabetes dapat diinduksi pada hewan dengan cara
pankreatektomi, uji toleransi glukosa dan secara kimia menggunakan diabetagon
seperti streptozotocin dan aloksan (Marzoeki, 1993). Kadar gula darah normal
pada tikus adalah 50-135 mg/dl (Carvalho, 2003).
Aloksan (2,4,5,6-tetraoksipirimidin; 5,6-dioksiurasil) merupakan senyawa
hidrofilik dan tidak stabil (Gambar 2.2). Waktu paro pada suhu 37°C dan pH
diabetogenik, aloksan dapat digunakan secara intravena, intraperitoneal dan
subkutan. Dosis intravena yang digunakan biasanya 65 mg/kg BB, sedangkan
intraperitoneal dan subkutan adalah 2-3 kalinya (Agung, 2006).
Aloksan secara cepat dapat mencapai pankreas, aksinya diawali oleh
pengambilan yang cepat oleh sel β Langerhans. Pembentukan oksigen reaktif
merupakan faktor utama pada kerusakan sel tersebut. Pembentukan oksigen
reaktif diawali dengan proses reduksi aloksan dalam sel β Langerhans. Aloksan
mempunyai aktivitas tinggi terhadap senyawa seluler yang mengandung gugus
SH, glutation tereduksi (GSH), sistein dan senyawa sulfhidril terikat protein
(misalnya SH-containing enzyme). Hasil dari proses reduksi aloksan adalah asam
dialurat, yang kemudian mengalami reoksidasi menjadi aloksan, menentukan
siklus redoks untuk membangkitkan radikal superoksida. Reaksi antara aloksan
dengan asam dialurat merupakan proses yang diperantarai oleh radikal aloksan
intermediet (HA˙). Radikal superoksida dapat membebaskan ion ferri dari
ferinitin, dan mereduksi menjadi ion ferro. Selain itu, ion ferri juga dapat
direduksi oleh radikal aloksan. Radikal superoksida mengalami dismutasi menjadi
hidrogen peroksida, berjalan spontan dan kemungkinan dikatalisis oleh
superoksida dismutase. Salah satu target dari oksigen reaktif adalah DNA pulau
Langerhans pankreas. Kerusakan DNA tersebut menstimulasi poly
ADP-ribosylation, proses yang terlibat pada DNA repair. Adanya ion ferro dan hidrogen peroksida membentuk radikal hidroksi yang sangat reaktif melalui reaksi
Gambar 2.2 Struktur kimia aloksan (Agung, 2006)
Faktor lain selain pembentukan oksigen reaktif adalah gangguan pada
homeostatis kalsium intraseluler. Aloksan dapat meningkatkan konsentrasi ion
kalsium bebas sitosolik pada sel β Langerhans pankreas. Efek tersebut diikuti oleh
beberapa kejadian : influks kalsium dari cairan ekstraseluler, mobilisasi kalsium
dari simpanannya secara berlebihan, dan eliminasinya yang terbatas dari
sitoplasma. Influks kalsium akibat aloksan tersebut mengkaibatkan depolarisasi
sel β Langerhans, lebih lanjut membuka kanal kalsium tergantung voltase dan
semakin menambah masuknya ion kalsium ke sel. Pada kondisi tersebut,
konsentrasi insulin meningkat sangat cepat, dan secara signifikan mengakibatkan
gangguan pada sensitivitas insulin perifer dalam waktu singkat. Selain kedua
faktor tersebut di atas, aloksan juga diduga berperan dalam penghambatan
glukokinase dalam proses metabolisme energi (Agung, 2006).
Streptozotosin (STZ) atau 2-deoksi-2-[3-(metil-3-nitrosoureido)-D-gluko
piranose] diperoleh dari Streptomyces achromogenes dapat digunakan untuk
menginduksi baik DM tipe 1 maupun tipe 2 pada hewan uji. Struktur kimia
streptozotosin ditunjukkan pada Gambar 2.3. Dosis yang digunakan untuk
intraperitoneal adalah lebih dari 40 mg/kg BB. STZ juga dapat diberikan secara
berulang, untuk menginduksi DM tipe 1 yang diperantarai aktivasi sistem imun.
Untuk menginduksi DM tipe 2, STZ diberikan intravena atau intraperitoneal
dengan dosis 100 mg/kg BB pada tikus yang berumur 2 hari kelahiran, pada 8-10
minggu tikus tersebut mengalami gangguan respon terhadap glukosa dan
sensitivitas sel β terhadap glukosa. Di lain pihak, sel α dan δ tidak dipengaruhi
secara signifikan oleh pemberian streptozotosin pada neonatal tersebut sehingga
tidak membawa dampak pada perubahan glukagon dan somatostatin.
Patofisiologis tersebut identik pada DM tipe II (Agung, 2006).
STZ menembus sel β Langerhans melalui tansporter glukosa GLUT 2.
Aksi STZ intraseluler menghasikan perubahan DNA sel β pankreas. Alkilasi DNA
oleh STZ melalui gugus nitrosourea mengakibatkan kerusakan pada sel β
pankreas. STZ merupakan donor NO yang mempunyai kontribusi terhadap
kerusakan sel tersebut melalui peningkatan aktivitas guanil siklase dan
pembentukan cGMP. NO dihasilkan sewaktu STZ mengalami metabolisme dalam
sel. Selain itu STZ juga mampu membangkitkan oksigen reaktif yang mempunyai
peran tinggi dalam kerusakan sel β pankreas. Pembentukan anion superoksida
karena aksi STZ dalam mitokondria dan peningkatan aktivitas xantin oksidase.
Dalam hal ini, STZ menghambat siklus Krebs dan menurunkan konsumsi oksigen
mitokondria. Produksi ATP mitokondria yang terbatas selanjutnya mengakibatkan
Gambar 2.3 Struktur kimia streptozotosin (Agung, 2006)
2.6.5 Efek Akut Diabetes Mellitus
Ketika kadar glukosa darah meninggi ke tingkat ketika jumlah glukosa
yang difiltrasi melebihi kapasitas sel-sel tubulus melakukan reabsorbsi, glukosa
akan terdapat dalam urin (glukosuria). Glukosa dalam urin menimbulkan efek
osmotik yang menarik H2O bersamanya, menimbulkan diuresis osmotik yang
ditandai oleh poliuria (sering berkemih). Cairan yang berlebihan keluar dari tubuh
menyebabkan dehidrasi, yang pada gilirannya akan menyebabkan kegagalan
sirkulasi perifer karena volume darah turun secara signifikan. Kegagalan sirkulasi,
apabila tidak diperbaiki, dapat menyebabkan kematian karena aliran darah ke otak
turun atau menimbulkan gagal ginjal sekunder akibat tekanan filtrasi yang tidak
adekuat. Selain itu, sel-sel kehilangan air karena tubuh mengalami dehidrasi
akibat perpindahan osmotik air dari dalam sel ke cairan ekstrasel yang hipertonik.
Sel-sel otak sangat peka terhadap penciutan, sehingga timbul gangguan fungsi
sistem saraf. Gejala khas lain pada diabetes mellitus adalah polidipsia (rasa haus
berlebihan), yang sebenarnya merupakan mekanisme kompensasi untuk mengatasi
dehidrasi (Sheerwood, 1996). Oleh karena terjadi defisiensi glukosa intrasel,
nafsu makan (appetite) meningkat, sehingga timbul polifagia (pemasukan
makanan berlebihan). Akan tetapi, walaupun terjadi peningkatan pemasukan
makanan, berat tubuh menurun secara progresif akibat defisiensi insulin pada
metabolisme lemak dan protein. Sintesis trigliserida menurun saat lipolisis
meningkat, sehingga terjadi mobilisasi besar-besaran asam lemak dari simpanan
trigliserida. Peningkatan asam lemak dalam darah digunakan oleh sel sebagai
pengeluaran berlebihan badan keton mencakup beberapa asam seperti asam
asetoasetat yang berasal dari penguraian tidak sempurna lemak oleh hati, ketosis
ini menyebabkan asidosis metabolik progresif. Asidosis menekan fungsi otak dan,
apabila cukup parah, dapat menyebabkan koma diabetes dan kematian
(Sheerwood, 1996).
Tindakan kompensasi untuk asidosis metabolik adalah peningkatan
ventilasi untuk meningkatkan pengeluaran CO2 pembentuk asam. Ekshalasi salah
satu badan keton, yaitu aseton menyebabkan nafas berbau buah. kadang-kadang
karena bau ini seorang pasien kolaps akibat koma diabetes secara salah disangka
orang yang lewat sebagai peminum anggur yang pingsan karena kebanyakan
minum. Orang dengan diabetes tipe 1 jauh lebih rentan mengalami ketosis
daripada pengidap diabetes tipe 2 (Sheerwood, 1996).
Efek tidak adanya insulin pada metabolisme protein, menyebabkan
pergeseran ke arah katabolisme protein. Penguraian protein-protein otot
menyebabkan otot rangka lisut dan melemah dan pada diabetes anak, penurunan
pertumbuhan keseluruhan. Penurunan asupan asam amino disertai peningkatan
penguraian protein meyebabkan peningkatan asam amino dalam darah.
Peningkatan asam amino dalam sirkulasi darah dapat digunakan untuk
glukoneogenesis, yang semakin memperparah hiperglikemia (Sheerwood, 1996).
2.6.6 Komplikasi Diabetes Mellitus
Komplikasi-komplikasi diabetes mellitus dapat dibagi menjadi dua
kategori:
a. Komplikasi Metabolik Akut, misal Seperti ketoasidosis diabetik dan
b. Komplikasi-komplikasi Vaskular Jangka Panjang, melibatkan
pembuluh-pembuluh kecil (mikroangiopati) dan pembuluh-pembuluh-pembuluh-pembuluh sedang dan besar
(makroangiopati). Mikroangiopati merupakan lesi spesifik diabetes yang
menyerang kapiler dan arteriola retina (retinopati diabetik), glomerulus ginjal
(nefropati diabetik), otot-otot dan kulit. Makroangiopati diabetik mempunyai
gambaran histopatologik berupa arteriosklerosis (Price dan Wilson, 1995).
2.6.7 Obat Antidiabetes Oral
a. Sulfonilurea: tolbutamida, klorpropamida, tolazamida (Tolinase),
glibenklamida, glikazida, glipizida, dan glikidon. Empat obat terakhir
dinamakan obat-obat generasi kedua, yang daya kerjanya atas dasar 10-100
kali lebih kuat daripada obat pertama yang termasuk obat-obat generasi ke-1.
Sulfonilurea menstimulasi sel ß dari pulau Langerhans, sehingga sekresi
insulin ditingkatkan. Di samping itu kepekaan sel-sel ß bagi kadar glukosa
darah juga diperbesar melalui pengaruhnya atas protein transpor glukosa. Obat
ini hanya efektif pada penderita diabetes mellitus tipe 2 yang tidak begitu
berat, yang sel-sel β-nya masih bekerja cukup baik. Ada indikasi bahwa
obat-obat ini juga memperbaiki organ tujuan bagi insulin dan menurunkan absorbsi
insulin oleh hati.
b. Biguanida : metformin. Berbeda dengan sulfonilurea, obat-obat ini tidak
menstimulasi pelepasan insulin dan tidak menurunkan kadar gula darah pada
orang sehat. Zat ini juga menekan nafsu makan (efek anorexia) hingga berat
badan tidak meningkat, sehingga layak diberikan pada penderita yang
overweight. Penderita ini biasanya mengalami resistensi insulin, sehingga
c. Glukosidase-inhibitors: akarbose dan mignitol. Obat-obat ini termasuk
kelompok obat-obat baru, yang berdasarkan persaingan inhibisi enzim ά
-glukosidase di mukosa duodenum, sehingga reaksi penguraian di/polisakarida
menjadi monosakarida dihambat. Dengan demikian glukosa dilepaskan lebih
lambat dan absorbsinya dalam darah juga kurang cepat, lebih rendah dan
merata, sehingga memuncaknya kadar gula darah dihindarkan. Kerja ini mirip
dengan efek dari makanan yang kaya akan serat gizi.
d. Thiazolidindion : troglitazon adalah kelompok obat baru yang pada tahun
1996 dipasarkan di AS dan Inggris. Kegiatan farmakologisnya luas dan berupa
penurunan kadar glukosa dengan jalan meningkatkan kepekaan bagi insulin
dari otot, jaringan lemak dan hati. Sebagai efeknya penyerapan glukosa ke
dalam jaringan lemak dan otot meningkat. Begitu juga menurunkan kadar
trigliserida/asam lemak bebas dan mengurangi glukoneogenesis dalam hati.
Zat ini tidak mendorong pankreas untuk meningkatkan pelepasan insulin
seperti sulfonilurea.
e. Miglitinida : repaglinida (novonorm)
Kelompok obat terbaru ini (ditemukan pada tahun 1999) bekerja menurut
suatu mekanisme khusus, yakni mencetuskan pelepasan insulin dari pankreas
segera setelah makan. Miglitinida harus diminum tepat sebelum makan dan
karena reabsorbsinya cepat, maka mencapai kadar puncak dalam 1 jam.
Insulin yang dilepaskan kadar glukosa darah secukupnya. Ekskresinya juga
cepat sekali, dalam waktu 1 jam sudah dikeluarkan dari tubuh (Tjay dan
Rahardja, 2002).
BAB III
METODOLOGI PENELITIAN
VCO yang diperoleh dimaksudkan untuk mengetahui efek hipoglikemik
dan mengamati langsung praparat histologi pankreas tikus diabetes yang diinduksi
STZ.
Metode yang digunakan dalam penelitian ini adalah metode eksperimental
di laboratorium dengan kondisi lingkungan yang homogen pada percobaan,
meliputi tikus putih galur wistar, kelamin jantan, kondisi kandang dan makanan.
desain rancangan digunakan adalah rancangan acak lengkap (RAL). Data
dianalisis dengan Anava (analisis variansi) dan dilanjutkan dengan uji beda
rata-rata Duncan menggunakan program Statistical and Product Service Solution
(SPSS). Model rancangan acak lengkap (RAL) dan matriks percobaan ditunjukkan pada Tabel 3.1
Tabel 3.1 Matriks rancangan percobaan
Pengulangan Perlakuan
1 2 3 4 5 6 Total
K K1 K2 K3 K4 K5 K6 6
V1 V11 V12 V13 V14 V15 V16 6
V2 V21 V22 V23 V24 V25 V26 6
V3 V31 V32 V33 V34 V35 V36 6
G G1 G2 G3 G4 G5 G6 6
Keterangan :K= Kontrol Negatif (CMC 0,5%); V1 = VCO dosis 2 ml/kg bb; V2 =VCO dosis 4 ml/kg bb;V3=VCO dosis 8 ml/kg bb;G=Glibenklamid
Penelitian ini terdiri dari beberapa tahap yaitu penyediaan sampel,
penyediaan sedian uji, pengujian efek hipoglikemik dan uji preparat histologi
pankreas.
3.1 Alat - alat
Alat-alat yang digunakan dalam penelitian ini meliputi alat-alat gelas
laboratorium, neraca listrik (Chyo JP2-600), neraca hewan (Presica Geniweigher,
GW–1500), aluminium foil, mortir dan stamfer, kandang tikus, oral sonde, spuit 1
ml (Terumo), spuit 3 ml (Terumo), glukometer (Accutrend-Roche), kertas saring,
alat bedah. Mikrotum, mikroskop, dan kamera digital.
3.2 Bahan - bahan
3.2.1 Bahan Uji
Buah kelapa (Cocos nucifera).
3.2.2 Bahan Kimia
Etanol 96% (E-Merck), aqua pro injeksi, asam sitrat (E-Merck), natrium
sitrat (E-Merck), Streptozotocin, Glibenklamid, glucocard test Accutrend II.
3.2.3 Hewan Percobaan
Hewan yang digunakan adalah tikus putih jantan dengan berat badan 150 –
200 gram sebanyak 30 ekor. Sebelum percobaan dimulai terlebih dahulu tikus
dipelihara selama 2 minggu dalam kandang yang baik untuk menyesuaikan
lingkungannya (Ditjen POM, 1979).
Sampel yang digunakan adalah daging kelapa tua segar. Pengambilan
sampel dilakukan secara purposif yaitu tanpa membandingkan dengan sampel
buah kelapa yang lain. Sampel diambil dari Teluk Kijing, propinsi Jambi.
3.4 Pembuatan VCO
Kulit kelapa tua segar dikupas, kemudian dibelah dua dan di cuci sampai
bersih. Selanjutnya diparut, parutan yang diperoleh segera (tidak lebih dari 20
menit) dicampurkan dengan air bersih dengan perbandingan 3 (tiga) biji kelapa : 1
(satu) liter air bersih, lalu diperas dengan kain kasa. Hasilnya disebut santan, di
tempatkan dalam wadah transparan kemudian di mikser dengan waktu ± 10 menit
untuk 1 (satu) liter santan. Hasil mikser didiamkan selama 8 jam.
Hasil pendiaman santan yang dimikser akan terbentuk 3 (tiga) lapisan, yaitu
lapisan atas: blondo, Lapisan tengah: VCO, dan lapisan bawah: air. Lapisan VCO
diambil dan disaring 2 (dua) kali dengan kertas saring, sehingga diperoleh VCO
murni dan disimpan dalam wadah tertutup.
3.5Penyiapan Penginduksi, Bahan Uji dan Obat Pembanding untuk Pengujian Farmakologi
3.5.1 Pembuatan Larutan Asam Sitrat 0,1 M
Ditimbang 2,1 g asam sitrat dilarutkan dalam akuades hingga 100 ml
3.5.2 Pembautan Larutan Natrium Sitrat 0,1 M
Ditimbang 2,9 g natrium sitrat dilarutkan dalam akuades 100 ml.
3.5.3 Pembuatan Larutan Dapar Sitrat pH 4,5
Diambil 26,75 ml larutan asam sitrat dan 34,25 ml larutan natrium sitrat,
lalu dicukupkan dengan akuades hingga 100 ml.
Ditimbang 335,7 mg serbuk streptozotocin, dilarutkan seperlunya dalam
larutan dapar sitrat pH 4,5.
3.5.5 Pembuatan Suspensi CMC 0,5%
Sebanyak 0,5 g CMC ditaburkan dalam lumpang yang berisi 25 ml akuades
panas. Didiamkan 15 menit hingga diperoleh massa yang transparan, setelah
dikembangkan, digerus lalu diencerkan dengan sedikit air. Kemudian dimasukkan
dalam erlenmeyer yang telah dikalibrasi 100 ml. Volumenya dicukupkan dengan
akuades hingga 100 ml.
3.5.6 Pembuatan Suspensi Glibenklamid 0,02% dalam Larutan CMC 0,5%
Sebanyak 20 mg glibenklamid digerus, dan ditambahkan larutan CMC 0,5%
sedikit demi sedikit sambil digerus terus lalu diencerkan dengan sedikit air.
Kemudian dimasukkan ke dalam erlenmeyer yang telah dikalibrasi 100 ml,
dicukupkan dengan akuades hingga 100 ml.
3.6 Prosedur Kerja Untuk Pengujian Farmakologi
Tikus dipuasakan (tidak makan tapi tetap minum) selama lebih kurang 18
jam. Kemudian berat badan ditimbang dan diukur kadar gula darah puasa.
Diberikan secara intravena (iv) Larutan streptozotocin 40 mg/kg bb. Lalu diukur
kadar gula darah tikus pada hari ke-3 dan ke-7. Pada hari ke-7, hewan yang
memiliki kadar gula darah (KGD) lebih tinggi dari 250 mg/dl dipisahkan dan
dijadikan sebagai hewan uji. Hewan yang KGD lebih rendah dari 250 mg/dl
diinduksi kembali.
Kemudian masing – masing tikus diberi:
Kelompok 1 : Tanpa pemberian glibenklamid dan bahan uji
Kelompok 2 : Sediaan VCO dosis 2 ml/kg bb (per oral).
Kelompok 4 : Sediaan VCO dosis 8 ml/kg bb (per oral).
Kelompok 5 : Larutan glibenklamid dosis 1 mg/kg bb (per oral).
lalu diukur kadar gula darah tikus pada hari ke-3 dan ke-6. Pada hari ke-6, hewan
uji dilakukan pembedahan dan bagian organ pankreas dilakukan uji preparat
histologi di Fakultas Kedokteran USU. Diamati luas pankreas pada
masing-masing perlakuan
.
3.7 Pembedahan Hewan Uji
Hewan uji dimatikan dengan cara dislokasi leher. Hewan yang telah mati
dipasung di atas papan fiksasi dengan perut mengarah ke atas. Pemotongan
dilakukan pada bagian kulit perut secara menyilang sampai terlihat bagian organ
bagian dalam perut tikus. Selanjutnya diambil organ pankreas tikus, lalu disimpan
dalam wadah khusus yang berisi larutan fisiologis.
3.8 Pembuatan Preparat Pankreas pada Tikus Putih
Setelah pankreas dikeluarkan dari tubuh tikus putih maka dilakukan
pembuatan preparat pankreas dengan langkah sebagai berikut:
a. sampel pankreas yang telah diambil lalu di fiksasi dengan larutan formalin
10% selama 3-4 jam
b. setelah itu dilakukan dehidrasi dengan aseton sebanyak 3 kali,
masing-masing selama 2 jam
c. dilakukan cleaning (pembersihan) dengan menggunakan toluen sebanyak
3 kali, masing-masing selama 1-2 jam
d. dilakukan proses embedding yaitu perendaman sampel di paraffin cair
e. lalu dilakukan proses pencetakan blok paraffin
f. tahap cutting (pemotongan) blok paraffin yaitu:
i. menggunakan alat mikrotom sehingga menghasilkan lembaran yang
ketebalannya 2 µm
ii. lembaran tersebut diletakkan di penangas air yang suhunya 30 0C
iii. lembaran yang telah direndam dalam penangas dilengketkan pada
objek glas
iv. lalu sampel tersebut dipanaskan di oven selama 2-3 menit
g. pewarnaan (staining)
Sebelum pewarnaan, sampel yang telah dipanaskan di oven lalu direndam
dalam xylol sebanyak 3 kali masing-masing selama 5-10 menit.
Selanjutnya dilakukan pencucian/pembilasan dengan menggunakan,
alkohol 90% selama 5-10 menit, lalu alkohol 80% selama 5-10 menit, lalu
alkohol 70% selama 5-10 menit. Setelah itu dilakukan proses pewarnaan
dengan menggunakan larutan haemotoxylin selama 2-3 menit dilanjutkan
dengan larutan Eosin selama 2-3 menit. Kemudian sampel tersebut
dicuci/dibilas menggunakan alkohol 70% selama 5-10 menit, lalu alkohol
80% selama 5-10 menit, dan kemudian alkohol 90% selama 5-10 menit.
h. sampel dikeringkan pada suhu kamar selama 3-5 menit
i. lalu ditutup dengan objek glass.
j. lalu diamati di bawah mikroskop
Alat glukotes ini terdiri dari beberapa perangkat. Perangkat alat glukotest ini
ditunjukkan pada Gambar 3.1 dan cara penggunaan ditunjukkan pada Gambar 3.2.
Keterangan : 1. Glukotes
2. Strip
3. Kalibrasi
4. Alat Penusuk
Gambar 3.1 :Alat Glukotes
4 3
2
1
Gambar 3.1 : Alat Glukotes
3.9.1 Prosedur Penggunaan
a. Dimasukkan strip kalibrasi ke dalam
tempat masuknya strip. Pada layar akan
tampak nomor seri strip.
b. Dibuka bungkus strip sampai garis
tanda.
c. Dimasukkan strip kedalam alat.
d. Pada layar akan muncul nomor seri dan
kadar gula darah pada pengukuran
terakhir secara bergantian.
e. Darah disentuhkan ke ujung strip sampai
penuh.
f. Kadar gula darah akan tampak pada
layar setelah 30 detik.
(Anonim, 2001).
3.9.2 Prinsip Pengukuran
Sampel darah akan masuk kedalam tes strip melalui aksi kapiler. Glukosa
yang ada pada darah akan bereaksi dengan glukosa oksidase dan kalium
ferisianida yang ada dalam strip dan dihasilkan kalium ferosianida. Kalium
ferosianida yang dihasilkan sebanding dengan konsentrasi glukosa yang ada pada
sampel darah. Oksidasi kalium ferosianida akan menghasilkan muatan listrik yang
akan diubah oleh alat glukotes untuk ditampilkan sebagai konsentrasi glukosa
pada layar.
Glukosa oksidase
β–D–glukosa + kalium ferisianida asam glukonat + kalium ferosianida
oksidasi
Kalium ferosianida kalium ferisianida + e-
(Anonim, 2001).
3.10 Analisis Data
Rancangan penelitian yang digunakan pada penelitian ini adalah rancangan
acak lengkap, menggunakan perhitungan statistik ANAVA dengan uji rata – rata
lanjutan Duncan dengan taraf kepercayaan 95%.
3.11 Definisi Operasional
a. Bahan uji adalah suspensi Glibenklamid 1 mg/kg berat badan; VCO dosis 2;
4 dan 8 ml/kg berat badan yang diberikan kepada tikus diabetes secara
b. Pengukuran kadar gula darah (KGD) adalah ± 4 jam setelah pemberian
bahan uji pada hari yang telah ditentukan.
c. H1 adalah menunjukkan hari pada saat pemberian bahan uji pertama kali
pada tikus diabetes.
d. H3 adalah menunjukkan hari ke-3 pada saat pemberian bahan uji pada tikus
diabetes.
e. H6 adalah menunjukkan hari ke-6 pada saat pemberian bahan uji pada tikus
diabetes
f. Pengukuran berat badan tikus setelah H6 sebelum dilakukan pembedahan.
BAB IV
HASIL DAN PEMBAHASAN
Dosis VCO ditentukan berdasarkan pada penggunaannya secara empiris di
masyarakat yaitu 45 ml (3 x 1 sendok makan) per hari, selanjutnya dikonversikan
ke dosis tikus yaitu 0,81 ml/200 gram berat badan setara dengan 4 ml/kg berat
badan (Laurence & Bacharach, 1864). Variasi dosis yang dibuat adalah 2; 4 dan 8
ml/kg bb. Pengamatan perubahan kadar gula darah (KGD) selama 6 hari dengan
pemberian VCO setiap hari sesuai dosis masing-masing.
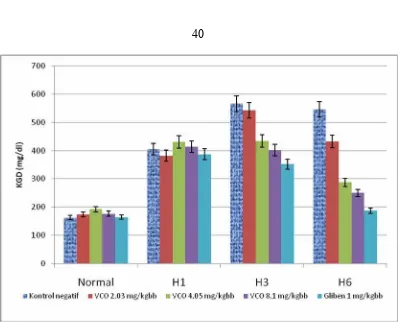
Hasil penelitian kenaikan KGD pada tikus diabetes yang diamati selama 6
hari ditunjukkan pada Tabel 4.1 dan Gambar 4.1.
Tabel 4.1 Perubahan KGD tikus diabetes yang diinduksi STZ (Rerata ± SEM)
Pengamatan Nama perlakuan
Normal H1 H3 H6
Kontrol negatif 162.9 ± 24.7 405 ± 122 567 ± 61 547 ± 63
VCO 2 ml/kgbb 174.0 ± 22.0 382 ± 69 543 ± 64 433 ± 30
VCO 4 ml/kgbb 192.2 ± 18.8 431 ± 137 434,5 ± 131 288 ± 77
Glibenklamid 1 mg/kgbb 164.6 ± 20.4 387 ± 103 352 ± 104 187 ± 101
Keterangan :setiap kelompok perlakuan menggunakan 6 ekor tikus
40
Gambar 4.1:Diagram yang menunjukkan keadaan KGD selama 6 hari dengan
pemberian VCO, glibenklamid dan kontrol negatif (CMC 0,5%)
P<0,05
Diagram di atas menunjukkan KGD tikus diabetes yang diinduksi STZ
dengan setiap kelompok yang terdiri dari 6 ekor. Berdasarkan grafik di atas
nampak bahwa pada hari pertama (H1) masing-masing kelompok pemberian VCO
di atas 250 mg/dl, ini menunjukkan bahwa hewan yang digunakan telah
memenuhi persyaratan sebagai hewan uji. KGD tikus diabetes nampak tidak
berbeda, hal ini didukung dari analisis statistik Anava bahwa pada hari pertama
terjadi peningkatan KGD semua kelompok perlakuan tidak berbeda nyata. Respon
KGD terhadap dosis STZ 40 mg/kg bb yang diberikan, nampak adanya respon
yang seragam pada hewan percobaan.
Pada hari ketiga (H3) nampak bahwa kelompok kontrol negatif tikus
diabetes tanpa pemberian VCO dan glibenklamid dan kelompok tikus diabetes
dengan pemberian VCO dosis 2 ml/kg bb menunjukkan peningkatan KGD, ini
mengisyaratkan bahwa pada hari ketiga masih terjadi kerusakan sel β sehingga
KGD terus mengalami peningkatan, sedangkan pemberian VCO dosis 2 ml/kg bb
terjadi penurunan dibanding kontrol negatif (Gambar 4.1 dan Tabel 4.2) namun
tidak menunjukkan perbesaran yang signifikan. Artinya ketersediaan hayati VCO
yang terabsorpsi dalam darah belum dapat memberikan efek penurunan KGD
yang signifikan.
Kelompok tikus diabetes dengan pemberian VCO dosis 4; 8 ml/kg bb dan
glibenklamid 1 mg/kg bb mengalami penurunan KGD yang berbeda nyata
(Gambar 4.1 dan Tabel 4.2). Ketersediaan hayati VCO pada dosis 4 dan 8 ml/kg
bb yang terabsorpsi telah dapat menurunkan KGD pada tikus diabetes (Tabel
4.2).
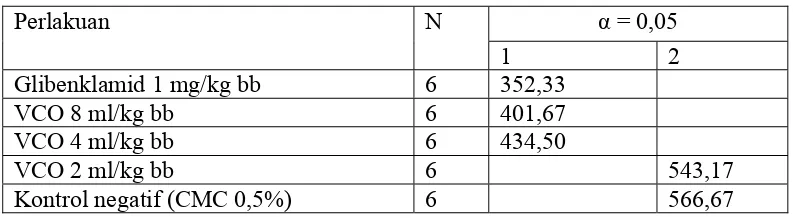
Tabel 4.2 Uji beda rata-rata lanjutan Duncan pada hari ke-3
α = 0,05
Perlakuan N
1 2
Glibenklamid 1 mg/kg bb 6 352,33
VCO 8 ml/kg bb 6 401,67
VCO 4 ml/kg bb 6 434,50
VCO 2 ml/kg bb 6 543,17