STUDI PEMERIKSAAN DAN PENETAPAN KADAR KALSIUM DALAM SAWI PAHIT(Brassica juncea), SAWI MANIS(Brassica rapa chinensis), BIJI MELINJO(Gnetum Gnemon) DAN DAUN KEMANGI(Ocimum basilicum)
SKRIPSI
Oleh : LENA 040804041
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
STUDI PEMERIKSAAN DAN PENETAPAN KADAR KALSIUM DALAM SAWI PAHIT(Brassica juncea), SAWI MANIS(Brassica rapa chinensis), BIJI MELINJO(Gnetum Gnemon) DAN DAUN KEMANGI(Ocimum basilicum)
SKRIPSI
Diajukan Untuk Melengkapi Salah Satu Syarat Untuk Mencapai Gelar Sarjana Farmasi
Pada Fakultas Farmasi Universitas Sumatera Utara
OLEH : LENA 040804041
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
PENGESAHAN SKRIPSI
STUDI PEMERIKSAAN DAN PENETAPAN KADAR KALSIUM DALAM SAWI PAHIT(Brassica juncea), SAWI MANIS(Brassica rapa chinensis), BIJI MELINJO(Gnetum Gnemon) DAN DAUN KEMANGI(Ocimum basilicum)
Oleh: LENA 040804041
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : Agustus 2008
Disetujui Oleh:
Pembimbing I, Panitia Penguji,
(Dra. Salbiah, M.Si., Apt.) (Drs. Muchlisyam, M.Si., Apt. NIP. 131 653 994
)
NIP: 130 809 700
Pembimbing II, (Dra. Masfria, M.S., Apt NIP: 131 569 406
.)
(Dra. Sudarmi, M.Si.,Apt.) (Drs. Immanuel S. Meliala, Msi., Apt. NIP: 131 283 719 NIP: 131 283 718
)
Dekan,
NIP: 131 283 71
(Prof. Dr. Sumadio Hadisahputra, Apt.)
Puji dan syukur penulis panjatkan kehadirat Allah SWT yang telah memberikan
rahmat dan hidayah-Nya kepada penulis sehingga penulis dapat menyelesikan skripsi ini
sebagai salah satu syarat dalam memperoleh gelar sarjana farmasi pada Fakultas Farmasi
Universitas Sumatera Utara.
Terima kasih penulis sampaikan kepada Mama tercinta atas doa, kasih sayang dan
kerja kerasnya dalam menghantarkan penulis meraih cita-cita. Doa yang tulus penulis
panjatkan untuk Papa tercinta Alm. Ahmad Effendi Rambe yang telah banyak memberikan
penulis inspirasi. Penulis juga menyampaikan terima kasih kepada saudara, sepupu dan
keponakan dari keluarga besar Zainoen Oemar atas doa dan dukungannya kepada penulis.
Terima kasih penulis sampaikan kepada Ibu Dra. Masfria, MS., Apt dan Ibu Dra.
Sudarmi, M.Si.,Apt. atas waktu dan kesabarannya membimbing penulis selama penelitian
hingga penulisan skripsi ini.
` Penulis juga menyampaikan terima kasih kepada Bapak Dekan Fakultas Farmasi Prof.
Dr. Sumadio Hadisahputra.Apt., Bapak/Ibu staf pengajar Fakultas Farmasi USU yang telah
mendidik penulis selama perkuliahan serta penasehat akademik penulis Ibu Prof. Dr. Siti
Morin Sinaga, Msc, Apt. yang telah memberikan bimbingan kepada penulis selama ini.
Selanjutnya ucapan terimaksih penulis sampaikan kepada Ibu Kepala Laboratorium
BAPEDALDA Sumatera Utara serta staf yang telah membantu penulis dalam penelitian.
Penulis juga tidak lupa mengucapkan terima kasih kepada sahabat-sahabat penulis
Imagipho bersaudara Ocha, Yeni, Memel, Indah, Vini, Riri yang telah menghiasi kehidupan
penulis dan Mimin yang telah banyak membangkitkan semangat penulis.
Terakhir penulis mengucapkan terima kasih kepada rekan-rekan Asisten
senior, junior Fakultas Farmasi Seluruh pegawai Fakultas Farmasi Universitas Sumatera
Utara yang telah banyak membantu penulis.
Akhirnya penulis berharap semoga skripsi ini berguna bagi ilmu pengetahuan pada
umumnya dan ilmu farmasi khususnya. Penulis menyadari penulisan ini belum sempurna
oleh karena keterbatasan kemampuan penulis. Atas kekurangan dan kelemahan ini penulis
mohon maaf.
Medan, Agustus 2008
Penulis
RIMA ELFITRA RAMBE
ABSTRAK
Masyarakat saat ini semakin menyadari perlunya konsumsi makanan sehari-hari
seperti sayur-sayuran yang tidak hanya memenuhi kebutuhan serat tetapi juga mengandung
cukup penting dalam menunjang pertumbuhan dan perkembangan manusia terutama untuk
pembentukan tulang.
Maka dilakukan pemeriksaan serta penetapan kadar kalsium yang terdapat dalam
sayur-sayuran yang dikonsumsi sehari-hari oleh masyarakat diantaranya sayur sawi pahit,
sawi manis, biji melinjo serta daun kemangi.
Penetapan kadar kalsium yang terdapat dalam sayur-sayuran tersebut dilakukan
dengan menggunakan metode Spektrofotometri Serapan Atom, yaitu diukur pada panjang
gelombang 422,45 nm.
Dari hasil analisis diperoleh kadar kalsium pada masing-masing sampel yaitu sawi
pahit sebesar 1,16 ± 0,06 mg/100 g, sawi manis sebesar 14,08 ± 0,27 mg/100 g, biji melinjo
sebesar 0,25 ± 0,03 mg/100 g, dan daun kemangi sebesar 37,18 ±2,89 mg/100 g.
ABSTRACT
Nowadays, the community has realized the needs to consume daily food like
needs less of them, but calcium has the important function to support the growth and
development for the body especially for bone development.
So there is need to do research for the exactly value inside vegetables that always
consume daily by community, for example mustard cabbage, Chinese white cabbage, melinjo
and basil.
Calcium determination had been done by Atomic Absorbtion Spectrophotometry
method where the determination of the calcium was measuring with 422.45 nm wavelengths.
The analysis result of calcium for samples were 1,16 ± 0,06 mg/100 g in mustard
cabbage; 14,08 ± 0,27 mg/100 g in Chinese white cabbage; 0,25 ± 0,03 mg/100 g in melinjo,
and 37,18 ±2,89 mg/100 g.
DAFTAR ISI
LEMBAR PENGESAHAN ... ii
ABSTRAK ... iii
ABSTRACT ... iv
DAFTAR ISI ... v
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN ... x
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 4
1.3 Hipotesis ... 4
1.4 Tujuan ... 4
BAB II METODOLOGI PENELITIAN ... 5
2.1 Alat-Alat ... 5
2.2 Bahan-Bahan ... 5
2.3 Sampel ... 5
2.3.1 Pengambilan Sampel ... 5
2.3.2 Penyiapan Sampel ... 5
2.4 Lokasi Penelitian ... 6
2.5 Pembuatan Pereaksi HNO3 2.6 Proses Dekstruksi ... 6
5N ... 6
2.7 Pembuatan Larutan Sampel ... 6
2.8 Analisa Kuantitatif ... 7
2.8.1 Pembuatan Kurva Kalibrasi Larutan Baku Kalsium ... 7
2.8.1 Analisa Kalsium dalam Sawi Pahit ... 7
2.8.2 Analisa Kalsium dalam Sawi Manis ... 7
2.8.3 Analisa Kalsium dalam Biji Melinjo ... 8
2.8.3 Analisa Kalsium dalam Daun Kemangi ... 8
2.9 Uji Perolehan Kembali ... 8
2.10 Analisa Data secara Statistik ... 9
BAB III HASIL DAN PEMBAHASAN ... 11
3.1 Kurva Kalibrasi ... 11
3.1.1 Penentuan Panjang Gelombang Maksimum Ca ... 11
3.1.2 Kurva Kalibrasi Logam Ca ... 12
3.2 Analisa Kalsium dalam Sampel ... 12
3.3 Uji Perolehan Kembali (% Recovery) ... 13
3.4 Batas Deteksi dan Batas Kuantitasi ... 14
BAB IV KESIMPULAN DAN SARAN ... 15
4.1 Kesimpulan ... 15
4.2 Saran ... 15
DAFTAR PUSTAKA ... 16
DAFTAR TABEL
Halaman
Tabel 1 Tabel Nilai Qkritis
sisi ... 9 pada taraf kepercayaan 95% (P=0,05) pada uji dua
DAFTAR GAMBAR
Halaman
Gambar 1. Kurva penetapan panjang gelombang maksimum logam Ca...11
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Data hasil pengukuran absorbansi larutan standar Ca ... 16
Lampiran 2. Data hasil pengukuran Ca dalam sawi manis, sawi pahit,
biji melinjo dan daun kemangi... 17
Lampiran 3. Perhitungan Persamaan Regresi untuk logam Ca ... 18
Lampiran 4. Contoh Perhitungan Kadar Kalsium pada Sampel ... 20
Lampiran 5 Analisa Data Statistik untuk Menghitung Kadar logam Ca pada Sawi Pahit... 21
Lampiran 6. Analisa Data Statistik untuk Menghitung Kadar logam Ca pada Sawi Manis... 22
Lampiran 7. Analisa Data Statistik untuk Menghitung Kadar logam Ca pada Biji Melinjo... 24
Lampiran 8. Analisa Data Statistik untuk Menghitung Kadar logam Ca pada Daun Kemangi... 25
Lampiran 9. Perhitungan (%) Perolehan Kembali Sampel ... 26
Lampiran 10. Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ)
logam Ca…... 27
Lampiran 11. Gambar Sawi Pahit dan Sawi Manis ... 28
Lampiran 12. GambarBiji Melinjo dan Daun Kemangi ... 29
senior, junior Fakultas Farmasi Seluruh pegawai Fakultas Farmasi Universitas Sumatera
Utara yang telah banyak membantu penulis.
Akhirnya penulis berharap semoga skripsi ini berguna bagi ilmu pengetahuan pada
umumnya dan ilmu farmasi khususnya. Penulis menyadari penulisan ini belum sempurna
oleh karena keterbatasan kemampuan penulis. Atas kekurangan dan kelemahan ini penulis
mohon maaf.
Medan, Agustus 2008
Penulis
RIMA ELFITRA RAMBE
ABSTRAK
Masyarakat saat ini semakin menyadari perlunya konsumsi makanan sehari-hari
seperti sayur-sayuran yang tidak hanya memenuhi kebutuhan serat tetapi juga mengandung
cukup penting dalam menunjang pertumbuhan dan perkembangan manusia terutama untuk
pembentukan tulang.
Maka dilakukan pemeriksaan serta penetapan kadar kalsium yang terdapat dalam
sayur-sayuran yang dikonsumsi sehari-hari oleh masyarakat diantaranya sayur sawi pahit,
sawi manis, biji melinjo serta daun kemangi.
Penetapan kadar kalsium yang terdapat dalam sayur-sayuran tersebut dilakukan
dengan menggunakan metode Spektrofotometri Serapan Atom, yaitu diukur pada panjang
gelombang 422,45 nm.
Dari hasil analisis diperoleh kadar kalsium pada masing-masing sampel yaitu sawi
pahit sebesar 1,16 ± 0,06 mg/100 g, sawi manis sebesar 14,08 ± 0,27 mg/100 g, biji melinjo
sebesar 0,25 ± 0,03 mg/100 g, dan daun kemangi sebesar 37,18 ±2,89 mg/100 g.
ABSTRACT
Nowadays, the community has realized the needs to consume daily food like
needs less of them, but calcium has the important function to support the growth and
development for the body especially for bone development.
So there is need to do research for the exactly value inside vegetables that always
consume daily by community, for example mustard cabbage, Chinese white cabbage, melinjo
and basil.
Calcium determination had been done by Atomic Absorbtion Spectrophotometry
method where the determination of the calcium was measuring with 422.45 nm wavelengths.
The analysis result of calcium for samples were 1,16 ± 0,06 mg/100 g in mustard
cabbage; 14,08 ± 0,27 mg/100 g in Chinese white cabbage; 0,25 ± 0,03 mg/100 g in melinjo,
and 37,18 ±2,89 mg/100 g.
DAFTAR ISI
BAB I PENDAHULUAN 1.1Latar Belakang
Mineral terdapat di dalam tubuh dan memegang peranan penting dalam
pemeliharaan fungsi tubuh, baik tingkat sel, jaringan, organ maupun fungsi tubuh
secara keseluruhan. Keseimbangan mineral di dalam tubuh diperlukan untuk
pengaturan kerja enzim, pemeliharaan keseimbangan asam basa, pemeliharaan
kepekaan otot dan saraf terhadap rangsangan (Almatsier, 2002).
Kalsium berperan dalam pembentukan tulang dan gigi. Bersama-sama
dengan fosfor, kalsium menyusun kristal hidroksiapatit yang merupakan bagian
dari tulang dan gigi. Karena itu keduanya harus berada dalam jumlah yang cukup.
Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh, yaitu
1,5-2% dari berat badan (Almatsier, 2002).
Jumlah yang dianjurkan per hari untuk anak-anak dengan usia 0-8 tahun
sebesar 600 mg, 9-14 tahun sebesar 700 mg, 15-17 tahun sebesar 600 mg, dewasa
sebesar 500 mg dan wanita hamil dan menyusui sebesar 1200 mg (Gaman,1992).
Mineral yang dipilih untuk diperiksa adalah kalsium. Alasan pemilihan
kalsium karena kalsium merupakan mineral yang terdapat paling banyak di dalam
tubuh serta dibutuhkan dalam jumlah yang cukup besar. Mineral tersebut dapat
diperoleh dari daging, sayuran, buah-buahan, susu, dan keju (Sivakali, 2007).
Membangun kesehatan masyarakat adalah upaya untuk meningkatkan
kesehatan masyarakat agar lebih baik daripada sebelumnya. Setiap orang
kesehatan perorangan, keluarga, masyarakat serta lingkungan. Kiat membangun
kesehatan masyarakat tidak terlepas dari pemanfaatan aneka tanaman sebagai
bahan obat dan sayur-mayur (Pitojo, 1996).
Sawi merupakan tanaman semusim. Sawi berdaun lonjong, halus, tidak
berbulu, dan tidak berkrop. Pada umunya pola pertumbuhan daunnya berserak
(roset) sehingga sukar membentuk krop. Tanaman ini mempunyai akar tunggang
dengan akar samping yang banyak, tetapi dangkal. Hampir setiap orang gemar
sawi karena rasanya segar (enak) dan banyak mengandung vitamin A, vitamin B,
dan sedikit vitamin C. Namun, daun sawi rasanya agak pahit (Rubatzky, 1998)
Melinjo merupakan tumbuhan tahunan berbentuk pohon yang b
dioecious, ada indivi
dimanfaatkan sebagai bahan bangunan. Daunnya tunggal berbentuk oval dengan
ujung tumpul. Melinjo tidak menghasilka
termasuk tumbuhan berbunga. Yang dianggap sebagai buah sebenarnya adalah
Tumbuhan kemangi mengandung minyka atsiri seperti egenol, sineol,
methyl chavicol, protein, kalsium, fosfor, besi, belerang, vitamin A, dan vitamin
C. Menurut catatan Departemen Kesehatan Republik Indonesia, kemangi
mengandung gizi yang bermanfaat bagi kesehatan tubuh (Pitojo, 1996)
Kalsium dalam tumbuhan diambil sebagai kation divalen (Ca2+) dari dalam
tanah dan jarang kekurangan dalam kondisi normal. Kalsium penting untuk
pembelahan sel. Ia berperan dalam spindel mitosis selama pembelahan sel dan
pembelahan sel, gejala kekurangan kalsium terlihat pada daerah meristematik
(Hopkins, 1995).
Sampel tersebut yang dipilih karena sampel merupakan sayur-sayuran
dengan kandungan kalsium yang cukup tinggi berdasarkan Daftar Komposisi
Bahan Makanan yang dikeluarkan oleh Direktorat Gizi Departemen Kesehatan
Republik Indonesia. Selain itu sampel tersebut mudah diperoleh di pasar-pasar
tradisional.
Terdapat berbagai metode penetapan kadar kalsium di dalam literatur
antara lain kompleksometri (Rivai,1994) dan spektrofotometri serapan atom
(Helrich, 1990). Dalam hal ini, penulis memilih menggunakan spektofotometri
serapan atom karena metode ini cepat, bahan yang digunakan sedikit, dapat
mengukur kadar logam dalam jumlah kecil dan spesifik untuk setiap logam tanpa
dilakukan pemisahan.
Berdasarkan hal di atas, penulis ingin mengetahui ada tidaknya serta
besarnya kandungan kalsium dalam sawi pahit (Brassica juncea), sawi manis
biji melinjo (Gnetum gnemon), dan daun kemangi (Ocimum
basilicum) melalui penetapan kadar secara spektrofotometri serapan atom.
1.2 Perumusan Masalah
a. Apakah terdapat kalsium dalam sawi pahit (Brassica juncea), sawi
manis (Brassica chinensis), biji melinjo (Gnetum gnemon) dan
b. Berapakah kadar kalsium yang terdapat dalam sawi pahit (Brassica
juncea), sawi manis (Brassica chinensis), biji melinjo (Gnetum
gnemon) dan daun kemangi (Ocimum basilicum)
c.
1.3 Hipotesis
a. Sawi pahit (Brassica juncea), sawi manis (Brassica chinensis), biji
melinjo (Gnetum gnemon) dan daun kemangi (Ocimum Basilicum)
mengandung kalsium
b. Sawi pahit (Brassica juncea), sawi manis (Brassica chinensis), biji
melinjo (Gnetum gnemon) dan daun kemangi (Ocimum Basilicum)
mempunyai kadar yang cukup untuk memenuhi kebutuhan kalsium
manusia
1.4 Tujuan
Untuk mengetahui besarnya kandungan kalsium yang terdapat dalam sawi
pahit (Brassica juncea), sawi manis (Brassica chinensis), biji melinjo (Gnetum
gnemon) dan daun kemangi (Ocimum basilicum) sehingga dapat digunakan
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tanaman 2.1.1 Sawi Pahit
Taksonomi tumbuhan sawi pahit :
Kingdom : Plantae
Divisi : Spermatophyta
Subdivisi : Magnoliophyta
Kelas : Magnoliopsida
Ordo : Brassicales
Famili : Brassicaceae
Genus : Brassica
Spesies : Brassica juncea
Sawi pahit merupakan tanaman semusim. Bentuknya hampir menyerupai
caisim. Sawi berdaun lonjong, halus, dan tidak berbulu. Tanaman sawi
mempunyai batang pendek dan lebih langsing daripada petsai. Hampir setiap
orang gemar sawi karena rasanya segar (enak) dan banyak mengandung vitamin
A, vitamin B, dan sedikit vitamin C. Namun, daun sawi rasanya agak pahit
(Sunarjono, 2007).
2.1.2 Sawi Manis
Taksonomi tumbuhan sawi manis :
Divisi : Spermatophyta
Subdivisi : Magnoliophyta
Kelas : Magnoliopsida
Ordo : Brassicales
Famili : Brassicaceae
Genus : Brassica
Spesies : Brassica chinensis
Tanaman ini masih terus merupakan salah satu sayuran penting Asia,
khususnya di Cina. Daunnya bertangkai, berbentuk agak oval, berwarna hijau tua,
dan mengkilap, tidak membentuk kepala, tumbuh agak tegak atau setengah
mendatar, tersusun dalam spiral yang rapat, melekat pada batang yang tertekan.
Daun berwarna hijau tua cerah atau ungu, dan perbungaannya dipanen pada waktu
atau beberapa hari setelah berbunga (Rubatzky, 1998)
2.1.3 Melinjo
Taksonomi tumbuhan melinjo :
Kingdom : Plantae
Divisi : Spermatophyta
Subdivisi : Gnetophyta
Kelas : Gnetopsida
Ordo : Gnetales
Famili : Gnetaceae
Genus : Gnetum
Melinjo (Gnetum gnemon L.) atau dalam bahasa Sunda disebut Tangkil
adalah suatu spesies tanaman berbiji terbuka (Gymnospermae) berbentuk pohon
yang berasal dari Asia tropik dan Pasifik Barat. Melinjo dikenal pula dengan
nama belinjo, mlinjo (bahasa Jawa), tangkil (bahasa Sunda) atau bago (bahasa
Melayu dan bahasa Tagalog). Melinjo banyak ditanam di pekarangan sebagai
peneduh atau pembatas pekarangan dan terutama dimanfaatkan "buah" dan
daunnya.Berbeda dengan anggota Gnetum lainnya yang biasanya merupakan
liana, melinjo berbentuk pohon (Anonim a, 2008)
2.1.4 Kemangi
Taksonomi tumbuhan kemangi :
Kingdom : Plantae
Divisi : Spermatophyta
Subdivisi : Magnoliophyta
Kelas : Magnoliopsida
Ordo : Lamiales
Famili : Lamiaceae
Genus : Ocimum
Spesies : Ocimum basilicum
Kemangi merupakan suatu terna, tinggi 60–70cm; batang halus dengan
daun pada setiap ruas; daun berwarna hijau muda, bentuk oval. 3-4cm panjang,
berambut halus di permukaan bagian bawah; bunganya berwarna putih, kurang
daun lebih sedikit dan tanaman cenderung cepat menua dan mati. Aroma daunnya
khas, kuat namun lembut dengan sentuhan aroma
2.2 Kalsium
2.2.1 Peranan Kalsium dalam Tubuh
Mineral berperan dalam berbagai tahap metabolisme. Keseimbangan
ion-ion mineral dalam cairan tubuh diperlukan untuk pengaturan kerja enzim-enzim,
pemeliharaan keseimbangan asam-basa, membantu transfer ikatan-ikatan penting
melalui membran sel dan pemeliharaan kepekaan otot dan syaraf terhadap
rangsangan (Almatsier, 2004 ).
Mineral yang terdapat dalam tubuh dan makanan terutama terdapat dalam
bentuk ion-ion. Mineral yang terdapat sebagai ion positif seperti Na+, K+, Ca++ dan
terdapat sebagai ion negatif seperti Cl
-Mineral kalsium dibutuhkan untuk perkembangan tulang. Kalsium sangat
penting terutama untuk anak-anak, wanita hamil, dan wanita menyusui. Jumlah , fosfat. Ion-ion ini terdapat dalam cairan
tubuh. Pada tulang dan gigi mineral berada dalam bentuk garam terutama sebagai
garam kalsium dan fosfat (Poedjiadi, 1994).
Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh,
yaitu 1,5-2% dari berat badan. Kira-kira 99% kalsium dalam tubuh terdapat pada
tulang dan gigi, terutama dalam bentuk hidroksiapatit. Absorpsi kalsium terjadi di
dalam usus halus. Peningkatan kebutuhan akan kalsium pada masa pertumbuhan,
yang dianjurkan per hari untuk anak-anak dengan usia 0-8 tahun sebesar 600 mg,
9-14 tahun sebesar 700 mg, 15-17 tahun sebesar 600 mg, dewasa sebesar 500 mg
dan wanita hamil dan menyusui sebesar 1200 mg (Gaman,1992).
2.2.2 Kalsium dalam Tumbuhan
Kalsium dalam tumbuhan diambil sebagai kation divalen (Ca2+
Dalam analisis spektrofotometri digunakan suatu sumber radiasi yang
menjorok ke dalam daerah ultraviolet spektrum itu. Dari spektrum ini dipilih ) dari dalam
tanah dan jarang kekurangan dalam kondisi normal. Kalsium penting untuk
pembelahan sel. Ia berperan dalam spindel mitosis selama pembelahan sel dan
membentuk kalsium pektat dalam lamela tengah. Karena perannya dalam
pembelahan sel, gejala kekurangan kalsium terlihat pada daerah meristematik
(Hopkins, 1995).
Kalsium mempunyai peranan penting di dalam metabolisme tumbuhan.
Secara khusus terlibat dalam pembelahan sel, karena kalsium dalam bentuk
kalsium pektat merupakan komponen integral dari lamela tengah. Pektin
merupakan polimer asam galakturonik yang membentuk garam dengan kalsium.
Sebagai tambahan, kalsium ditemukan dalam vakuola. Kalsium tidak dapat
dipindahkan setelah diambil dari tanah, sehingga simptom kekurangan terjadi
pada jaringan muda (Ting, 1982)
panjang-panjang gelombang tertentu dengan lebar pita kurang dari 1 nm. Proses
ini memerlukan penggunaan instrumen yang lebih rumit dan karenanya lebih
mahal. Instrumen yang digunakan untuk maksud ini adalah spektrofotometer, dan
seperti tersirat dalam nama ini, instrumen ini sebenarnya terdiri dari dua
instrumen dalam satu kotak , sebuah spektrometer dan fotometer (Basset, 1994).
Spektrometer adalah alat yang menghasilkan sinar dari spektrum dan
panjang gelombang tertentu, dan fotometer adalah alat pengukur intensitas cahaya
yang ditransmisikan atau yang diabsorpsi. Jadi spektrofotometer digunakan untuk
mengukur energi secara relatif jika energi tersebut ditransmisikan, direfleksikan,
atau diemisikan sebagai fungsi dari panjang gelombang (Khopkar, 2002).
2.5 Spektrofotometri Serapan Atom
Peristiwa serapan atom pertama kali diamati oleh Fraunhofer, ketika
mengamati garis-garis hitam pada spektrum matahari. Spektroskopi serapan atom
pertama kali digunakan pada tahun 1955 oleh Walsh. Sesudah itu, tidak kurang
dari 65 unsur diteliti dan dapat dianalisis dengan cara tersebut. Spektroskopi
serapan atom digunakan untuk analisis kuantitatif unsur-unsur logam dalam
jumlah sekelumit (trace) dan sangat kelumit (ultratrace). Cara analisis ini
memberikan kadar total unsur logam dalam suatu sampel dan tidak tergantung
pada bentuk molekul dari logam dalam sampel tersebut.
Spektrofotometri serapan atom adalah suatu metode yang merupakan
bentuk dari spektrofotometri serapan yang digunakan untuk mendeteksi
logam dalam larutan sampel menjadi atom-atom logam berbentuk gas yang
digunakan untuk analisa kuantitatif dari logam dalam sampel. Metode
Spektrofotometri Serapan Atom mempunyai banyak kesamaan dengan
spektrofotometri serapan lainnya dalam hal alat yang terdiri dari sumber sinar,
monokromator dan detektor (Bender, 1987).
Karena garis-garis spektrum serapan atom sangat sempit dan juga
energi-energi transisi atom itu khas (untuk masing-masing unsur) maka metode analisis
yang berdasarkan pengukuran serapan (absorbansi) atom juga mempunyai sifat
spesifik yang tinggi. Kecilnya lebar garis spektrum serapan atom menimbulkan
masalah pada pengukuran absorbannya. Sebagaimana diketahui, lebar rata-rata
garis puncak serapan atom antara 0,002-0,005 nm sehingga diperlukan suatu
monokromator yang dapat memberikan sinar dengan lebar pita panjang
gelombang yang lebih sempit daripada 0,002-0,005 nm, dan hal ini sulit untuk
dilaksanakan.
Untunglah pada tahun 1955, Walsh berhasil mengatasi hal ini dengan
memakai suatu sumber sinar khusus yang memancarkan spektrum garis yang
mana salah satu garis spektrumnya mempunyai panjang gelombang yang sama
dengan panjang gelombang yang akan digunakan pada analisis dengan metode
spekroskopi serapan atom (Rohman, 2007).
Atom memiliki dua bentuk keadaan, yaitu keadaan dasar dan keadaan
tereksitasi. Keadaan dasar menunjukkan elektron pada atom berada pada tingkat
energi terendah yang mungkin ditempatinya (secara alami atom berada dalam
elektron tersebut dan menghasilkan keadaan tereksitasi. Energi dapat diberikan
pada atom dengan berbagai cara. Energi tersebut dapat dalam bentuk cahaya,
muatan listrik atau panas (Volland, 2005). Teknik ini digunakan untuk
menetapkan kadar suatu logam tertentu dengan cara mengukur intensitas emisi
atau serapan radiasi pada panjang gelombang tertentu dengan mengalirkan larutan
zat ke dalam api (Ditjen POM, 1995).
Bila suatu larutan yang mengandung logam yang dianalisa masuk ke
dalam nyala, maka akan terjadi peristiwa berikut:
a. Penguapan pelarut yang meninggalkan residu padat
b. Penguapan zat padat menjadi atom-atom penyusunnya yang mula-mula
berada dalam keadaan dasarnya.
c. Beberapa atom dapat tereksitasi oleh energi termal nyala ke tingkatan
energi yang lebih tinggi.
Jumlah atom-atom yang berada dalam keadaan tak tereksitasi jauh lebih
besar dibandingkan atom-atom tereksitasi. Atom-atom yang berada dalam
keadaan dasar ini mampu menyerap energi cahaya pada panjang gelombang
tertentu. Jauhnya penyerapan berbanding lurus dengan banyaknya atom keadaan
dasar yang berada dalam nyala (Vogel, 1989).
Ada beberapa kendala yang masih ditemui dalam penggunaan
Spektrofotometri Serapan Atom. Kendala-kendala ini antara lain gangguan kimia,
efek ionisasi dan efek viskositas pada kecepatan nebulisasi (Bender, 1987).
Berbagai faktor dapat mempengaruhi pancaran nyala suatu unsur tertentu
dapat dikelompokkan sebagai gangguan spektrum dan gangguan kimia
(Vogel,1989).
Terbentuknya atom-atom gas dalam keadaan status dasar yang merupakan
dasar Spektroskopi Nyala dapat dihalangi oleh dua bentuk utama gangguan kimia,
yaitu:
a. Pembentukan senyawa stabil
Pembentukan senyawa stabil menyebabkan tidak sempurnanya disosiasi zat yang
akan dianalisis atau pembentukan itu mungkin timbul dari pembentukan
senyawa-senyawa refraktori di dalam nyala yang tak dapat berdisosiasi menjadi atom-atom
penyusunnya. Sebagai contoh penetapan kalsium dengan adanya sulfat atau fosfat,
dan pembentukan oksida yang bersifat refraktori dari titanium, vanadium,
alumunium (Vogel, 1989).
Pembentukan senyawa stabil dapat diatasi dengan cara berikut:
1. Meningkatkan temperatur nyala dapat membentuk atom-atom gas bebas.
2. Menambahkan unsur penyangga yang berlebihan ke dalam larutan sampel
yang dianalisa.
M-X + R ↔ R-X + M
Reaksi di atas menunjukkan penambahan unsur penyangga (R) yang
berlebih akan menyebabkan bertambahnya konsentrasi atom logam gas
(M), karena unsur penyangga tersebut akan mengikat unsur pengganggu
(X). Hal ini akan terjadi jika hasil reaksi R-X merupakan senyawa yang
3. Mengekstraksi unsur pengganggu dengan pelarut organik yang tidak
bercampur dengan larutan sampel yang diperiksa (Vogel, 1989).
b. Ionisasi atom gas keadaan status dasar dalam nyala
Ionisasi akan mengurangi serapan dalam Spektrofotometri Serapan Atom. Cara
mengatasinya adalah menggunakan nyala yang bekerja pada temperatur serendah
mungkin yang masih memberikan hasil analisa unsur yang akan ditetapkan.
Ionisasi atom yang akan ditetapkan dapat juga dikurangi dengan menambahkan
penekan ionisasi, biasanya suatu larutan yang mengandung kation yang
mempunyai potensial ionisasi lebih rendah dari potensial ionisasi atom logam
yang dianalisis (Vogel, 1989).
BAB III
METODOLOGI PENELITIAN
3.1 Alat-alat
Alat-alat yang digunakan dalam penelitian ini terdiri dari spektrofotometer
serapan atom (Shimadzu AA-6300), Lampu Ca 10 mA, tanur
(Gallenkamp-Muffle furnace), neraca analitik (Shimadzu), hot plate (Schott), oven (Fisher
Scientific/Isotemp® ), pisau stainless, lemari asam dan alat-alat gelas.
3.2 Bahan-bahan
HNO3 (E. Merck), larutan standar kalsium 1000 mcg/ml (E. Merck), dan
air suling (Lab. Kimia Farmasi kuantitatif Fakultas Farmasi USU).
3.3 Sampel
3.3.1 Pengambilan sampel
Sampel yang digunakan adalah sampel segar dan matang dari sawi pahit,
sawi manis, biji melinjo, dan daun kemangi yang diambil secara purposif di pasar
pagi Petisah kecamatan Medan Baru. Sampel tersebut ditanam di Brastagi.
Bagian tanaman yang diambil sebagai sampel adalah batang dan daun untuk sawi
pahit dan sawi manis, bagian daun untuk kemangi serta lapisan pertama dan
ketiga untuk biji melinjo. Sampel yang diambil adalah sampel yang matang.
Metode pengambilan sampel purposif ini ditentukan atas dasar pertimbangan
bahwa sampel yang tidak terambil mempunyai karakteristik yang sama dengan
3.3.2 Penyiapan sampel
Sawi manis, sawi pahit dan daun kemangi segar yang akan dijadikan
sampel terlebih dahulu dipisahkan perhelai. Helaian sampel dan biji melinjo
kemudian dicuci dengan air suling hingga bersih, ditiriskan, dianginkan, dirajang,
dan dikeringkan dalam oven dengan suhu 35-40ºC sampai kering (Haswell, 1991).
3.4 Lokasi Penelitian
Penelitian dilakukan di dua lokasi yaitu dekstruksi dilakukan di Lembaga
Penelitian Fakultas MIPA Universitas Sumatera Utara dan pengukuran kadar
dengan Spektrofotometer Serapan Atom dilakukan di Lembaga Pengkajian
Pangan, Obat dan Kosmetik MUI kota Medan.
3.5 Pembuatan Pereaksi Larutan HNO3 5N
Larutan HNO3
Sampel sawi pahit (Brassica juncea), sawi manis
65% b/v sebanyak 340 ml diencerkan dengan air suling
sebanyak 1000 ml (Helrich, 1990).
3.6 Proses Dekstruksi
biji
melinjo (Gnetum gnemon), dan daun kemangi (Ocimum basilicum) yang
masing-masing ditimbang seksama yaitu sebanyak 60 g untuk sawi pahit, 40 g untuk sawi
manis, 30 g untuk biji melinjo dan 10 g untuk daun kemangi yang telah kering
dimasukkan ke dalam krusibel porselen, lalu diabukan dalam tanur dengan suhu
560oC selama 2 jam dan dibiarkan hingga dingin. Abu dibasahi dengan 10 tetes
aquadest dan ditambahkan 3-4 ml HNO3 5N secara hati-hati. Kemudian kelebihan
porselen dimasukkan kembali ke dalam tanur dan diabukan selama 6 jam dengan
suhu 560oC, kemudian didinginkan (Helrich, 1990).
3.7 Pembuatan Larutan Sampel
Abu yang telah dingin dilarutkan dengan 5 ml HNO3 5 N, lalu dikeringkan
di atas penangas air dalam lemari asam. Residu dilarutkan dalam 5 ml HNO3 5 N
dan dimasukkan ke dalam labu tentukur 50 ml. Residu dibilas dengan air suling
sebanyak 3 kali. Hasil pembilasan dimasukkan ke dalam labu tentukur. Kemudian
larutan dicukupkan volumenya dengan air suling hingga 50 ml, dan disaring ke
dalam erlenmeyer. Filtrat ini digunakan sebagai larutan sampel.
3.8 Analisa Kuantitatif
3.8.1 Pembuatan Kurva Kalibrasi Larutan Baku Kalsium
Larutan baku kalsium (1000 mcg/ml) dipipet sebanyak 10 ml dan
dimasukkan dalam labu tentukur 100 ml. Ditambahkan 10 ml HNO3 5N dan
diencerkan dengan air suling hingga garis tanda (LIB I, konsentrasi larutan baku
100 mcg/ml). Dari LIB I dipipet sebanyak 10 ml dan dimasukkan ke dalam labu
tentukur 100 ml, diencerkan dengan air suling hingga garis tanda (LIB II,
konsentrasi larutan baku 10 mcg/ml). Dari LIB II masing-masing dipipet 2; 6; 15;
20; 25; dan 30 ml, dimasukkan ke dalam labu tentukur 100 ml, diencerkan dengan
air suling hingga garis tanda sehingga diperoleh larutan dengan konsentrasi 0,2;
0,6; 1,5; 2; 2,5; dan 3 mcg/ml lalu diukur absorbansinya pada panjang gelombang
422,45 nm. Dibuat kurva kalibrasi untuk larutan baku kalsium. Data dapat dilihat
3.8.2 Analisa Kalsium dalam sampel
Masing-masing larutan sampel diencerkan. Untuk sampel sawi pahit
dipipet 10 ml larutan sampel kemudian dimasukkan ke dalam labu takar 50 ml
dan diencerkan dengan air suling hingga garis tanda, homogenkan, diperoleh
larutan pengukuran untuk sampel sawi pahit. Untuk sampel sawi manis dan daun
kemangi dipipet 10 ml larutan sampel kemudian dimasukkan ke dalam labu takar
50 ml dan diencerkan dengan air suling hingga garis tanda, homogenkan. Dari
larutan pengenceran pertama dipipet 5 ml lalu dimasukkan ke dalam labu tentukur
50 ml dan diencerkan dengan air suling hingga garis tanda, homogenkan,
diperoleh larutan pengukuran untuk sampel sawi manis dan daun kemangi. Untuk
sampel biji melinjo digunakan larutan sampel sebagai larutan pengukuran.
Masing-masing larutan pengukuran sampel diukur absorbansinya dengan
spektrofotometri serapan atom pada panjang gelombang 422,45 nm. Nilai
absorbansi yang diperoleh berada dalam nilai absorbansi kurva kalibrasi larutan
baku sehingga konsentrasi kalsium dapat dihitung dengan menggunakan
persamaan regresinya.
3.9 Analisa Data secara Statistik
Untuk mengetahui diterima atau tidaknya data penelitian maka data yang
diperoleh dianalisis secara statisik dengan Qtest
Q
yang dirumuskan sebagai berikut :
│Nilai yang dicurigai – Nilai yang terdekat │
hitung
Selanjutnya nilai Q
= ( Nilai tertinggi - Nilai Terendah)
hitung dibandingkan dengan nilai Qkritis, jika nilai Qhitung lebih
dicurigai dengan nilai-nilai yang lain), begitu juga sebaliknya jika nilai Qhitung
lebih besar dari Qkritis maka hipotesis nul ditolak (ada perbedaan antara nilai yang
dicurigai dengan nilai-nilai yang lain).
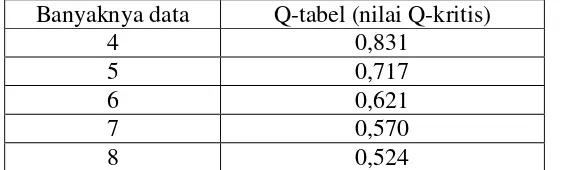
Tabel1. Tabel Nilai Qkritis
Banyaknya data
pada taraf kepercayaan 95% (P=0,05) pada uji dua sisi
Q-tabel (nilai Q-kritis)
4 0,831
5 0,717
6 0,621
7 0,570
8 0,524
Jika hipotesis nul ditolak. Maka dilakukan Q test kembali tanpa mengikutsertakan
data yang dicurigai. Perhitungan ini dilakukan terus-menerus hingga diperoleh
hipotesis yang diterima.
Kadar logam yang diperoleh dapat dihitung dengan rumus
Kadar logam (µ) = X ± t × SD/ n
3.10 Uji Perolehan Kembali
Uji perolehan kembali dilakukan dengan menambahkan larutan baku
logam Ca yang jumlahnya diketahui ke dalam sampel kemudian dianalisis dengan
Perhitungan perolehan kembali dapat dihitung dengan rumus sebagai berikut :
% Perolehan kembali =
A A F
C C C
*
−
x 100
Keterangan :
CF = konsentrasi total sampel
CA = konsentrasi sampel sebenarnya (awal)
BAB IV
HASIL DAN PEMBAHASAN
4.1 Penentuan Panjang Gelombang Maksimum
Panjang gelombang maksimum kalsium diperoleh dengan menggunakan
lampu Ca pada alat Spektrofotometer Serapan Atom.
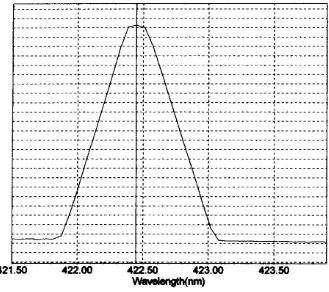
Gambar 1. Kurva penetapan panjang gelombang maksimum kalsium
Berdasarkan grafik penetapan panjang gelombang maksimum kalsium dengan
menggunakan Spektrofotometri Serapan Atom diperoleh panjang gelombang
422,45 nm. Pengukuran sampel pada panjang gelombang ini menunjukkan bahwa
4.2 Penentuan Kurva Kalibrasi
Kurva kalibrasi kalsium diperoleh dengan cara mengukur absorbansi
dari larutan standar kalsium dengan berbagai konsentrasi pada panjang gelombang
422,45 nm (Data kalibrasi kalsium dapat dilihat pada Lampiran 1 halaman 17). Dari data kalibrasi kalsium diperoleh kurva kalibrasi yang dapat dilihat pada
gambar di bawah.
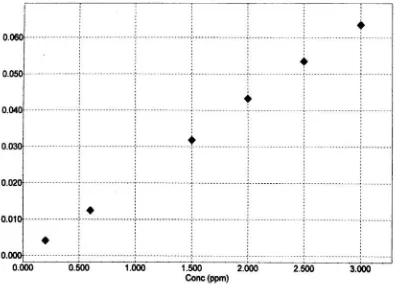
Gambar 2. Kurva Kalibrasi Ca pada panjang gelombang 422,45 nm
Berdasarkan data kalibrasi pada gambar 2 diperoleh hubungan linier antara absorbansi dan konsentrasi dengan persamaan garis regresi yaitu : Y =
0,021348X - 0,000086 dan nilai koefisien korelasi (r) sebesar 0,9993 (perhitungan
3.3 Analisa Kalsium dalam Sampel
Dari hasil pengukuran absorbansi larutan sampel maka dapat dihitung
kadar sampel yang diperoleh (tabel data dapat dilihat pada Lampiran 4 halaman 21). Dari data tersebut diperoleh kadar rata-rata kalsium yang dapat dilihat pada
tabel di bawah ini :
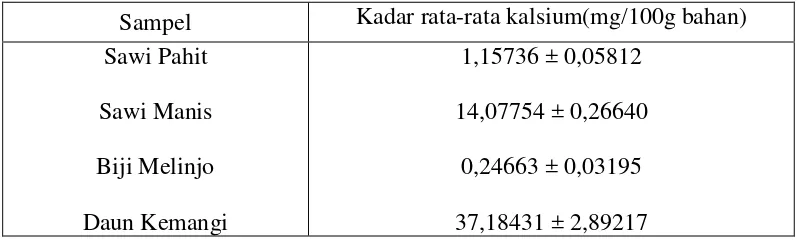
Tabel 2. Kadar rata-rata logam Ca dalam Sampel
Sampel Kadar rata-rata kalsium(mg/100g bahan) Sawi Pahit
Sawi Manis
Biji Melinjo
Daun Kemangi
1,15736 ± 0,05812
14,07754 ± 0,26640
0,24663 ± 0,03195
37,18431 ± 2,89217
Menurut Daftar Komposisi Bahan Makanan yang dikeluarkan oleh Direktorat
Gizi Departemen Kesehatan Republik Indonesia diketahui bahwa kadar kalsium
untuk 100 g bahan makanan yaitu 220 mg dalam sawi, 160 mg dalam melinjo dan
35 mg dalam daun kemangi.
Dalam penelitian diperoleh kadar rata-rata kalsium sebesar 1,16 ± 0,06
mg/100 g untuk sawi pahit; 14,08 ± 0,27 mg/100 g untuk sawi manis dan 0,25 ±
0,03 mg/100 g untuk biji melinjo. Kadar sawi pahit, sawi manis dan biji melinjo
yang diperoleh lebih kecil dari kadar kalsium dalam Daftar Komposisi Bahan
Makanan DepKes RI. Perbedaan ini mungkin dikarenakan tidak disebutkannya
bagian yang digunakan dari masing-masing sampel serta perbedaan topograpi dari
tempat penanaman sampel. Selain itu, untuk sampel sawi tidak ditetapkan jenis
Untuk daun kemangi diperoleh kadar rata-rata kalsium sebesar 37,18 ± 2,89
mg/100 g dimana kadar ini mendekati nilai dari kadar kalsium dalam Daftar
Komposisi Bahan Makanan DepKes RI.
3. 4 Uji Perolehan Kembali (% Recovery)
Uji perolehan kembali dilakukan terhadap sampel biji melinjo dengan
perulangan sebanyak 6 kali sesuai dengan prosedur pengujian sampel.
Berdasarkan statistik, hasil uji perolehan kembali (%) kalsium pada sampel Biji
Melinjo adalah sebesar 84,76%. Hasil uji perolehan kembali ini memenuhi
batas-batas yang ditentukan yaitu 80% - 110% (Harmita,2004). Dari hasil yang
diperoleh tersebut maka dapat disimpulkan bahwa metode ini memberikan
ketepatan yang memuaskan. Data dapat dilihat pada lampiran 9 halaman 29.
3.5 Batas Deteksi dan Batas Kuantitasi
Pada analisa kalsium diperoleh batas deteksi sebesar 0,0576 dan batas
kuantitasi 0,1921 (data kurva kalibrasi dapat dilihat pada lampiran 1 halaman 17) sehingga pengukuran sampel dapat memenuhi kriteria cermat dan seksama
BAB IV
KESIMPULAN DAN SARAN
4.1 Kesimpulan
Pengukuran larutan sampel dengan menggunakan Spektrofotometri
Serapan Atom menunjukkan bahwa sampel sawi pahit, sawi manis, biji melinjo
dan daun kemangi mengandung kalsium. Hal ini dapat dilihat dengan pengukuran
yang dilakukan dengan menggunakan lampu Ca pada panjang gelombang 422,45
nm.
Hasil penetapan kadar kalsium menunjukkan bahwa kadar kalsium pada
masing-masing sampel yaitu sawi pahit sebesar 1,16 ± 0,06 mg/100 g bahan, sawi
manis sebesar 14,08 ± 0,27 mg/100 g bahan, biji melinjo sebesar 0,25 ± 0,03
mg/100 g bahan, dan daun kemangi sebesar 37,18 ± 2,89 mg/100 g bahan.
4.2 Saran
Disarankan kepada peneliti selanjutnya agar dapat meneliti kandungan
mineral yang lain seperti besi dan magnesium yang terdapat dalam sampel
sayuran di atas sehingga dapat digunakan sebagai sumber mineral. Selain itu,
kepada masyarakat agar mengkonsumsi sayur-sayuran yang beragam karena
DAFTAR PUSTAKA
Almatsier, S. (2002). Prinsip Dasar Ilmu Gizi. Cetakan II. Jakarta: PT.Gramedia Pustaka Utama. Hal 228, 235-236, 238, 242-246, 249-252, 255-257
Anonim a. (2008). Sawi Putih. Tanggal akses 21 Agustus 2008
Anonim b. (2008). Melinjo. Tanggal akses 21 Agustus 2008 http://id.wikipedia.org/wiki/Melinjo
Basset, J. Et al. (1991). Vogel’s Textbook of Quantitative Inorganic Analysis Including Elementary Instrumental Analysis. Longman Group Limited. London. Diterjemhkan oleh Hadyana, A.(1994). Buku Ajar Vogel Kimia Analisis Kunatitatif Anorganik. Jakarta: Penerbit Buku Kedokteran EGC. Hal 942-943, 955-957
Gaman, P.M. (1982). Ilmu Pangan. Penerjemah: Gardjito, M., dkk. Edisi ke-2. Yogyakarta: Gadjah Mada University Press. Hal 135, 137
Hariana, A. (2006). Tumbuhan Obat dan Khasiatnya . Seri 2. Jakarta: Penabur Swadaya. Hal 26-27, 117
Harmita, 2004. Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. ”Majalah Ilmu Kefarmasian”. Volume I. No. 3. Hal 117-135
Haswell, S.J. (1991). Atomic Absorption Spectrometry. Amsterdam: Elsevier. p.200.
Helrich,K. (1990). Official Methode of Analysis of the Association of Official Analytical Chemists. Fifteenth Edition. USA: Association of Official Analytical Chemists Inc. P.27, 28, 42
Hopkins, W.G., (1995). Introduction to Plant Physiolog. USA: John Wiley & Sons, Inc. P.74
Pitojo, S. (1999). dya dan Selasih. Cetakan II. Ungaran: Trubus Agriwidya. Hal 3, 4
Rivai, H. (1995). Asas Pemeriksaan Kimia. Cetakan I. Jakarta: UI-Press. Hal 249. Ditjen POM. (1979). Farmakope Indonesia. Edisi ke-III. Jakarta: Departemen Kesehatan RI. Hal 651, 716
Sivakali, N. (2007). Terapi Jus Buah-buahan dan Sayur-sayuran. Cetakan pertama. Jakarta: Prestasi Pustaka Publisher. hal 116.
Lampiran 1. Data hasil pengukuran absorbansi larutan standar Ca
No Konsentrasi (ppm) Absorbansi
1. 2. 3. 4. 5. 6.
0,2000 0,6000 1,5000 2,0000 2,5000 3,0000
Lampiran 2. Perhitungan Persamaan Regresi untuk logam Ca
No. Konsentrasi (mcg/ml Absorbansi
Y
Persamaan garis regresi dengan rumus : Y = aX + b Keterangan : a = slope
2,80014 – 2,04526
131,4 – 96,04
0,75488
b =
=
=
=
= -0,000086
Koefisien korelasi dapat ditentukan sebagai berikut :
r =
=
=
=
= 0,9993
Jadi persamaan garis regresi adalah :
Y = 0,021348416X - 0,000086312
dengan r = 0,9993
(21,9) (0,2087) – (9,8) (0,46669)
6(21,9) – (9,8)2
4,57053 – 4,573562
131,4 – 96,04
-0,003052
35,36
(∑x2) (∑y) – (∑x) (∑xy) n (∑x2) – (∑x)2
n (∑xy) – (∑x) (∑y)
[
n (∑x2) – (∑x)2] [
n (∑y2) – (∑y)2]
6 (0,46669) – (9,8) (0,2087)[
6 (21,9) – (9,8)2] [
6 (0,00994587) – (0,2087)2]
2,80014 – 2,04526
[
131,4 – 96,04] [
0,05967522 – 0,04355569]
0,75488
Lampiran 3. Contoh Perhitungan Kadar Kalsium pada Sampel Misalnya untuk kalsium pada sawi pahit
Dengan menggunakan persamaan garis regresi untuk kalsium
Y = 0,021348X - 0,000086
Keterangan : Y = Absorbansi
X = Konsentrasi (mcg/ml)
0,0546=0,021348X - 0,000086
X = 2,5616 mcg/ml
Dengan menggunakan rumus :
C x V x Fp Kadar (mcg/g) =
BS
Keterangan : C = Konsentrasi (mcg/ml)
V = Volume larutan sampel (ml)
Fp = Faktor pengenceran
BS = Berat sampel (g)
Maka kadarnya adalah :
2,5616 mcg/ml x 50 ml x 5 Kadar (mcg/g) =
60,005g
= 10,6724 mcg/g = 1,06724 mg/100 g
Fp sawi pahit = 5
Fp sawi manis = 50
Fp biji melinjo = 1
Lampiran 4. Data hasil pengukuran Ca dalam sawi manis, sawi pahit, biji melinjo dan daun kemangi
1. Sayur sawi pahit
No 2. Sayur Sawi Manis
Lampiran 5. Analisa Data Statistik untuk Menghitung Kadar logam Ca pada
Dilakukan uji penolakan hasil analisis dengan Q-test. Data ke-2 adalah data yang
paling menyimpang
10,6725 – 11,2974
Qhitung = = 0,3813
12,3112 – 10,6725
Nilai Qkritis pada taraf kepercayaan 95% adalah 0,621
Rata-rata kadar kalsium dengan selang kepercayaan 95% pada sawi pahit
μ = X ± t ½ α s/√n
μ = 11,5736 ± 2,57. 0,5568/√6
Lampiran 6. Analisa Data Statistik untuk Menghitung Kadar logam Ca pada
Dilakukan uji penolakan hasil analisis dengan Q-test. Data ke-6 adalah data yang
paling menyimpang
128,7365 – 141,3250
Qhitung = = 0,6830
147,1676 – 128,7365
Nilai Qkritis pada taraf kepercayaan 95% adalah 0,621
Qhitung > Qkritis
No
; maka tidak semua data diterima sehingga dilakukan uji statistik
dengan tidak mengikutsertakan data ke-6
Dilakukan uji penolakan hasil analisis dengan Q-test. Data ke-1 adalah data yang
paling menyimpang
147,1676 – 143,3558
Qhitung = = 0,6524
147,1676 – 141,3250
Nilai Qkritis
s = ∑(X – X)
pada taraf kepercayaan 95% adalah 0,717
n-1
2
22,0388913 s =
5-1
s = 2,3473
Rata-rata kadar kalsium dengan selang kepercayaan 95% pada sawi pahit
μ = X ± t ½ α s/√n
μ = 140,7754 ± 2,78. 2,3473/√6
Lampiran 7. Analisa Data Statistik untuk Menghitung Kadar logam Ca pada
Dilakukan uji penolakan hasil analisis dengan Q-test. Data ke-6 adalah data yang
paling menyimpang
1,9734 – 2,3402
Qhitung = = 0,4149
2,8552 – 1,9734
Nilai Qkritis pada taraf kepercayaan 95% adalah 0,621
Karena Qhitung < Qkritis ; maka semua data diterima
Lampiran 8. Analisa Data Statistik untuk Menghitung Kadar logam Ca pada Dilakukan uji penolakan hasil analisis dengan Q-test. Data ke-6 adalah data yang
paling menyimpang
320,5784 – 366,2676
Qhitung = = 0,5660
401,3082 – 320,5784
Nilai Qkritis pada taraf kepercayaan 95% adalah 0,621
Karena Qhitung < Qkritis ;
SD =
maka semua data diterima
Lampiran 9. Perhitungan (%) Perolehan Kembali Sampel
Larutan baku kalsium yang ditambahkan pada masing-masing perlakuan recovery
adalah sebesar 0,45 ml dimana konsentrasi larutan baku tersebut adalah 100
mcg/ml, sehingga konsentrasi larutan baku yang ditambahkan dapat dihitung
sebagai berikut
C*A
Massabasah Volume×konsentras
=
Contoh perhitungan larutan baku yang ditambahkan
Konsentrasi larutan baku yang ditambahkan diperoleh dari
Keterangan : CF = konsentrasi sampel yang diperoleh setelah penambahan
larutan baku
= konsentrasi larutan baku yang ditambahkan
Contoh perhitungan % Perolehan kembali pada kalsium Biji Melinjo :
% Perolehan kembali
= 86,19% Dilakukan uji penolakan hasil analisis dengan Q-test. Data ke-6 adalah data yang
paling menyimpang
82,19 – 83,41
Qhitung = = 0,2455
87,16 – 82,19
Nilai Qkritis pada taraf kepercayaan 95% adalah 0,621
Lampiran 10. Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ)
2,765236410 x 10-10
496,1221664 x 10-10
185,8096134 x 10-10
3474,866704 x 10-10
463,4203398 x 10-10
2106,222521 x 10-10
n=7 ∑(Y-Yi)2 =
6729,206581 x 10-10
Simpangan Baku (SB)
Lampiran 11. Gambar Sawi Pahit dan Sawi Manis
Gambar 1. Gambar Sawi Pahit
Lampiran 12. Gambar Biji Melinjo dan Daun Kemangi
Gambar 3. Gambar Biji Melinjo
Gambar 4. Gambar Daun Kemangi
Gambar 5. Gambar Alat Tanur