EFEKTIVITAS PENGGUNAAN BISKUIT YANG
MENGANDUNG IMUNOGLOBULIN Y (IgY)
ANTI
Escherichia coli
O157:H7
SEBAGAI
PENCEGAHAN DIARE
NADHRAH ALHAN
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa tesis berjudul Efektivitas Penggunaan Biskuit Yang Mengandung Imunoglobulin Y (IgY) Anti Escherichia Coli
O157:H7 Sebagai Pencegahan Diare adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Februari 2017
Nadhrah Alhan
RINGKASAN
NADHRAH ALHAN. Efektivitas Penggunaan Biskuit Yang Mengandung Imunoglobulin Y (IgY) Anti Escherichia coli O157:H7 Sebagai Pencegahan Diare. Dibimbing oleh FACHRIYAN H. PASARIBU dan AGUSTIN INDRAWATI.
Bakteri Escherichia coli O157:H7 merupakan bakteri patogen yang mempunyai peran cukup penting dalam penyakit diare yang disebarkan melalui makanan. Bakteri ini dapat menyebabkan hemolytic uremic syndrome karna menghasilkan racun shiga like toxin, gagal ginjal dan kematian. Tujuan penelitian ini adalah untuk mengetahui efektivitas penggunaan biskuit yang mengandung imunoglobulin Y (IgY) anti E.coli O157:H7 sebagai pencegahan diare. Salah satunya adalah dengan memanfaatkan kuning telur ayam sebagai sumber antibodi (immunoglobulin) dan juga berperan sebagai nutraceutical food. Imunoglobulin ayam terbentuk dalam darah sebagai pemaparan antigen dan akan di transfer ke dalam kuning telur yang disebut dengan yolk imunoglobulin. Jenis dan jumlah antibodi spesifik dalam kuning telur menggambarkan jenis dan jumlah antibodi serum darah yang diperoleh dari infeksi alami maupun vaksinasi.
Vaksinasi ayam dilakukan empat kali selama satu bulan menggunakan antigen (suspensi bakteri) yang diinaktivasi pada suhu 56oC dengan menambahkan Freunds Adjuvant Complete atau Freunds Adjuvant Inomplete. Respon antibodi dan antigen terlihat pada uji Agar Gel Precipitation Test dengan adanya garis presipitasi yang menunjukkan keseimbangan antara konsentrasi antigen dan antibodi berikatan silang dengan determinan antigen. Untuk mengetahui kosentrasi IgY pada kuning telur dapat dilakukan dengan metode
Bradford dan berat molekul protein dengan metode SDS-PAGE. Selanjutnya dilakukan pembuatan biskuit IgY dengan menggunakan telur yang positif mengandung IgY untuk diaplikasikan kepada hewan coba yaitu Mus musculus. Imunisasi pasif dibagi pada tujuh perlakuan; kelompok pertama adalah Mus musculus diinfeksi E.coli O157:H7, kelompok kedua sampai keempat diinfeksi
E.coli O157:H7 dan diberikan biskuit IgY dengan dosis 60 mg, 80 mg, dan 100 mg. Kelompok kelima sampai ketujuh diberi biskuit dosis 60 mg, 80 mg, dan 100 mg dan diinfeksi bakteri E.coli O157:H7. Pengamatan gejala diare maupun gejala fisik lainnya dilakukan selama tujuh hari dan dilanjutkan dengan pengamatan histopatologi ginjal meliputi perubahan pada tubulus, degenerasi sel, nekrosis sel dan hemorhagi.
perubahan nafsu makan, fisik mencit menjadi lemas dan kurang aktif. Untuk gambaran histopatologi ginjal mencit menunjukkan kerusakan yang berbeda pada setiap perlakuan. Hal ini mengindikasikan pemberian IgY secara peroral selama tujuh hari belum menunjukkan perlindungan pada organ ginjal dari pemaparan bakteri E.coli O157:H7.
SUMMARY
NADHRAH ALHAN. The Effectiveness Of Use Biscuit Containing Immunoblobulin Y (IgY) Anti-Escherichia coli O157:H7 in Prevention Diarrhea. Supervised by FACHRIYAN H. PASARIBU dan AGUSTIN INDRAWATI.
Escherichia coli O157:H7 has an important role in diarrhea disease, it spreads through foods. This bacteria could cause hemolytic uremic syndrome
because it produses shiga like toxin, kidney failure and even death. The purpose of this research is to observe effectivity of biscuit that carried Yolk Imunoglobulin (IgY) and as anti to e.coli as prevention against diarrhea. Egg yolk used as antibody and as nutraceutical food. Immunoglobulin is formed in blood and then transferred into yolk that named yolk imunoglobulin. Kind and amount of spesific antibody in the yolk represent kind and amount of antibody in blood serum that obtained from infection or vaccinantion.
Vaccination of chickens done four times during a month using antigen (bacteria suspension) that inactivated in 560C temperature and then added Freunds Adjuvant Complete or Freunds Adjuvant Inomplete. Antibody and antigen respond could be seen in Agar Gel Precipitation Test, it formed precipitation line that showed equality between antigen and antibody and antibody tied with antigen determinant. To observe IgY concentrasion in yolk could be done with bradford
method and protein molecul mass with SDS-PAGE. After that biscuit production that made from egg yolk with positive contain IgY to be applicate to trial animal
Mus musculus. Passive immunitation divided into 7 treatments: The first group is
Mus musculus infected with E.coli O157: H7, the second to fourth groups infected with E.coli O157: H7 and given biscuits IgY at a dose of 60 mg, 80 mg, and 100 mg. The fifth to seventh group were given biscuits dose of 60 mg, 80 mg, and 100 mg and infected with bacteria E.coli O157: H7. Observation of diarrhea symptons or any other physically symptons was observed for 7 days and then continued with observing kidney histopathologyincluded changing of tubulus, sel degeneration, sel necrosion and hemorhagi.
The result showed that respond to IgG anti E.coli O157:H7 in blood serum formed in third week after vaccination and respond to IgY anti E.coli O157:H7 in yolk could be seen in 6th week after vaccinantion. The different in those respond is caused by in immunoglobulin that first formed in blood as effect of existence of antigen and then transferred into yolk by blood. IgY was detected yolk with the concentrations 2,361 mg/ml and the weight of protein moleculer IgY of heavy chain is 48 kDa and light chain 20 kDa.. In the application of biscuit with different dosage during the observation the animal is not death but the group showed different symptoms if diarrhea, change of desirement to eat, physically weak and inactive. Result of histopath of kidney showed different kind of damages in every treatment. It indicates that treatment of IgY for 7 days is not giving any much protection to kidney as prevention against E.coli O157:H7.
Hak Cipta Milik IPB, Tahun 2017
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Mikrobiologi Medik
EFEKTIVITAS PENGGUNAAN BISKUIT YANG
MENGANDUNG IMUNOGLOBULIN Y (IGY)
ANTI
Escherichia coli
O157:H7
SEBAGAI
PENCEGAHAN DIARE
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2017
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan November 2015 ini ialah dengan judul Efektivitas Penggunaan Biskuit Yang Mengandung Imunoglobulin Y (IgY) Anti Escherichia coli O157:H7Sebagai Pencegahan Diare. Shalawat dan salam semoga selalu tercurahkan untuk Baginda Rasulullah SAW beserta keluarga dan para sahabatnnya.
Rasa terima kasih penulis ucapkan kepada Bapak Prof Dr Drh Fachriyan H. Pasaribu dan Ibu Dr Drh Agustin Indrawati, M. Biomed selaku pembimbing yang banyak memberikan arahan, masukan, bimbingan dan waktunya selama proses penelitian dan penulisan tesis ini.
Ucapan terima kasih juga penuliskan sampaikan kepada Bapak Prof Dr Drh I Wayan T. Wibawan, MS selaku dosen penguji luar komisi pembimbing atas saran dan masukan untuk perbaikan tesis ini. Kemudian terima kasih kepada semua Bapak dan Ibu Dosen Program Studi Mikrobiologi Medik yang telah memberikan bimbingan dan ilmu pengetahuan yang diberikan selama menempuh pendidikan pascasarjana di Sekolah Pascasarjana Institut Pertanian Bogor. Ucapan terima kasih kepada Bapak Agus, Bapak Nur, Mba Adeh, Mba Selyn, dan seluruh teman-teman satu angkatan Program Studi Mikrobiologi Medik tahun 2013 dan angkatan 2014 atas bantuan, motivasi, dan keceriaannya selama ini.
Ungkapan terima kasih juga penulis sampaikan kepada orang tua tercinta Ayahnda Azhar dan Ibunda Sidrati, kembaran (adik Hilya Aniq), Uwa serta seluruh keluarga, atas segala doa dan kasih sayangnya. Penulis juga berkesempatan mengucapkan terimakasih kepada GaGaca Minang, teman-teman HIMAWIPA, dan Bowchil Team atas dukungan moril selama menempuh studi di Sekolah Pascasarjana Institut Pertanian Bogor. Penulis berharap semoga karya ilmiah ini bermanfaat.
Bogor, Februari 2017
DAFTAR ISI
DAFTAR TABEL xiv
DAFTAR GAMBAR xiv
DAFTAR LAMPIRAN xiv
1 PENDAHULUAN 1
Latar Belakang 1
Rumusan Masalah 2
Tujuan Penelitian 2
Manfaat Penelitian 2
Hipotesa 2
2 TINJAUAN PUSTAKA 3
Escherichia coli 0157:H7 (EHEC) 3
Imunoglobulin Y (IgY) 3
Struktur Imunoglobulin Y 5
Penyakit Diare 5
3 METODE PENELITIAN 6
Waktu dan Tempat Penelitian 6
Alat dan Bahan 6
Prosedur Penelitian 6
Analisis Data 9
4 HASIL DAN PEMBAHASAN 10
Identifikasi Escherichia coli O157:H7 10
Kosentrasi Kuning Telur 11
Aplikasi biskuit IgY 12
Gambaran Histopatologi 13
5 KESIMPULAN DAN SARAN 17
Kesimpulan 17
Saran 17
DAFTAR PUSTAKA 18
LAMPIRAN 21
DAFTAR TABEL
1. Hasil Uji AGPT serum dan kuning telur pasca vaksinasi 11
2. Rata-rata pertambahan BB (gr) 13
3. Hasil skoring histopatologi ginjal 16
DAFTAR GAMBAR
1. Struktur Imunoglobulin Y (wikipedia.com) 5
2. (a) Koloni E.coli pada blood agar (b) Koloni E.coli pada media EMB 10
3. (a) AGPT serum darah positif IgG pada minggu ketiga (M3) dan keempat (M4) pasca infeksi (b) AGPT kuning telur positif IgY pada minggu ketuju (M7) pasca infeksi. Antigen E.coli O157:H7 (1 dan 2) 11
4. Pita Protein IgY E.coli O157: H7. (1) marker Umum (2) sampel 1 IgY tanpa purifikasi (3) sampel 2 IgY tanpa purifikasi (4) sampel 1 IgY
purifikasi (5) sampel 2 IgY purifikasi. 12
5. Ginjal mencit kelompok kontrol diinfeksikan E.coli O157:H7 tanpa biskuit IgY mengalami Tubulonephritis non suppurativa (1) nekrosis epitel tubulus proximalis (2) hemorhagi (3) infiltrasi sel mononuclear
(4) selaput fibrosis. 13
6. Ginjal mencit diinfeksikan E.coli O157:H7 dan diberikan biskuit IgY 60 mg mengalami tubulonephrotic et hemorhagica (1) degenerasi nekrosis sel epitel tubulus proximalis (2) hemorhagi (3) pembendungan
darah. 13
7. Ginjal mencit diinfeksikan E.coli O157:H7 dan diberikan biskuit IgY
dosis 80 mg mengalami tubular necrosis et haemorhagica
(1) degenerasi sel epitel (2) hemorhagi 14
8. Ginjal mencit diinfeksikan E.coli O157:H7 dan diberikan biskuit
IgY dosis 100 mg mengalami tubular necrosis et haemorhagica
(1) degenerasi epitel dinding tubulus proximalis (2) hemorhagi. 14
9. Ginjal mencit diberikan biskuit IgY dosis 60 mg dan diinfeksikan
E.coli O157:H7 mengalami tubular necrosis et haemorhagica (1) degenerasi epitel dinding tubulus proximalis (2) hemorhagi. 14
10. Ginjal mencit diberikan biskuit IgY dosis 80 mg dan diinfeksikan
E.coli O157:H7 mengalami tubular necrosis et haemorhagica (1) degenerasi epitel dinding tubulus proximalis (2) hemorhagi. 14
11. Ginjal mencit diberikan biskuit IgY dosis 100 mg dan diinfeksikan
E.coli O157:H7 mengalami tubular necrosis et haemorhagica (1) degenerasi epitel dinding tubulus proximalis (2) hemorhagi. 15
DAFTAR LAMPIRAN
1. Data nafsu makan mencit 23
2. Data kejadian diare pada mencit 24
1
1
PENDAHULUAN
Latar Belakang
Diare merupakan suatu penyakit dengan tanda adanya perubahan bentuk dan konsistensi dari tinja yang berbentuk cair atau setengah cair yang dikeluarkan oleh penderita jika terinfeksi baik bakteri, virus maupun parasit. Infeksi umumnya terjadi karena adanya kontaminasi bakteri pada makanan, air, kontak langsung dengan hewan yang terinfeksi, dan juga perpindahan dari satu orang ke orang lain (Rey et al.
2006). Sampai saat ini diare masih merupakan masalah kesehatan di berbagai negara walaupun sudah terjadi perbaikan kesehatan dan ekonomi masyarakat, namun kasus diare tetap tinggi ( Zein et al. 2014 ).
Diare hingga saat ini masih merupakan salah satu penyebab utama kesakitan dan kematian hampir di seluruh daerah di dunia dan menyerang semua kelompok usia. Di negara berkembang, anak-anak menderita diare lebih dari 12 kali per tahun, 15-34% mengalami kematian dan 50-60% diantaranya mengalami dehidrasi (Zein et al. 2014).
Penyakit diare di Indonesia merupakan salah satu masalah kesehatan masyarakat yang utama, hal ini disebabkan karena masih tingginya angka kejadian diare yang menimbulkan banyak kematian terutama pada balita. Angka kejadian diare di Indonesia dari tahun ke tahun cenderung meningkat. Pada tahun 2014 angka kejadian diare mencapai 2549 kasus di lima daerah Indonesia (Kemenkes RI 2014).
Banyak faktor yang menyebabkan kasus diare ini, diantaranya Escherichia coli
O157:H7 yaitu bakteri yang mempunyai peran cukup penting dalam penyakit zoonosis yang disebarkan melalui makanan (Campbell et al. 2001). Bakteri ini dapat menyebabkan hemolytic uremic syndrome, gagal ginjal bahkan kematian. Patogenitas bakteri ditentukan oleh kemampuannya menghasilkan satu atau lebih sitotoksin yang sangat potensial yang dikenal dengan nama Shiga like toxin (Barlow et al. 2006). Strain EHEC memiliki faktor virulensi intimin yang berperan dalam proses penempelan dan pelekatan pada sel epitel saluran pencernaan yang memproduksi hemolisin sehingga menimbulkan diare berdarah (Suardana et al. 2010).
Tindakan pencegahan dan pengobatan untuk mengurangi angka penderita diare penting dilakukan. Salah satunya adalah dengan memanfaatkan potensi lain dari kuning telur ayam yang dapat digunakan sebagai sumber antibodi (immunoglobulin) terhadap penyakit dan juga berperan sebagai nutraceutical food (Sunwoo et al. 2002). Imunoglobulin ayam akan terbentuk dalam darah sebagai bentuk pemaparan antigen yang mudah di transfer ke dalam kuning telur yang biasa dikenal dengan IgY (yolk imunoglobulin). Jenis dan jumlah antibodi spesifik dalam kuning telur menggambarkan jenis dan jumlah antibodi serum darah yang diperoleh dari infeksi alami maupun vaksinasi (Poetrie 2007).
Penggunaan IgY ini sudah banyak dikembangkan seperti IgY kering sebagai
2
dengan rheumatoid dalam darah, sehingga tidak menimbulkan efek samping. Indrawati (2010) juga menambahkan, bahwa aplikasi telur 3 in one pada makanan dapat mengatasi flu burung bahkan diare karena keberadaan kandungan zat kebal dalam telur ini dapat diandalkan sebagai pencegahan melalui pengebalan pasif untuk manusia dan hewan dari serbuan penyakit.
Rumusan Masalah
Diare merupakan masalah serius yang disebabkan oleh bakteri E.coli O157:H7.
Shiga like toxin yang dihasilkannya dapat menyebabkan hemolytic uremic syndrome
yang ditandai dengan diare berdarah karena terjadinya infeksi saluran pencernaan. Strain EHEC memiliki faktor virulensi intimin yang berperan dalam proses penempelan dan pelekatan pada sel epitel saluran pencernaan yang memproduksi hemolisin sehingga menimbulkan diare berdarah (Suardana et al. 2010). Menurut WHO, penyakit diare merupakan salah satu penyebab utama kematian balita di negara berkembang.
Pada manusia bakteri E.coli O157:H7 bersifat verotoksigenik yang telah menyebabkan 16.000 kasus penyakit melalui makanan (Food Borne Diseases) , di negara Amerika terdapat 900 orang meninggal per tahunnya (Sartika et al. 2005). Sementara itu negara Indonesia di kota Palembang dari 129 pasien (usia 5 bulan sampai 5 tahun) ditemukan 33 koloni bakteri E.coli O157:H7 dari 4 orang pasien. Di kota Makasar dari 28 pasien 6 diantaranya positif ditemukannya E.coli O157:H7 pada feses pasien (Suarni et al. 2015).
Sampai sekarang belum ada vaksin yang dapat mengatasi bakteri patogen ini. Oleh karena itu perlu dilakukan penelitian terkait penanganan diare yang diakibatkan oleh E.coli O157:H7 untuk memberikan solusi yang efektif dan ekonomis pada penderita diare dengan penggunaan IgY anti E.coli O157:H7.
Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui efektivitas penggunaan biskuit yang mengandung imunoglobulin Y (IgY) anti E.coli O157:H7 sebagai pencegahan diare.
.
Manfaat Penelitian
Penelitian ini diharapkan dapat menghasilkan suatu produk (biskuit) yang mengandung IgY anti E. coli O157:H7 untuk pencegahan penyakit diare.
Hipotesa
3
2
TINJAUAN PUSTAKA
Escherichia coli 0157:H7 (EHEC)
Escherichia coli O157:H7 pertama kali diisolasi di Amerika Serikat pada tahun 1975 di daerah California dari seorang wanita yang menderita diare berdarah. Laporan pertama isolasi E.coli O157:H7 dari sapi yang berumur kurang dari tiga minggu yang menderita Colibacillosis di Argentina tahun 1977. Sejak munculnya wabah diare berdarah yang pertamakali disebabkan oleh E.coli O157 pada tahun 1982, maka sejak itulah hewan ruminansia yang sehat terutama sapi diketahui sebagai reservoir bagi E. coli O157:H7 (Andriani 2008).
Bakteri E.coli 0157:H7 adalah bakteri yang biasanya hidup di usus manusia dan hewan yang menghasilkan toksin yang disebut shiga like toksin sebagai penyebab utama wabah diare berdarah yang dapat menyebabkan kerusakan pada ginjal. Pada manusia menimbulkan gejala diare berair, hemorhagi kolitis, dan hemolitic uremic syndrome (HUS) (Frenzen et al. 2005).
Dari struktur morfologinya, bakteri E.coli O157:H7 berbentuk batang, bakteri gram negatif, dinding sel memiliki lapisan luar yang terdiri dari lipopolisakarida dan peptidoglikan sebagai lapisan utamanya. Serotipe bakteri ini dapat mengontaminasi daging dan jika terkontaminasi akan menimbulkan penyakit pada manusia. Cliver (1990) menyatakan bahwa terinfeksi E.coli O157:H7 merupakan ancaman yang serius dan biasanya ditularkan dari konsumsi daging sapi atau susu yang kurang masak. Virulensi EHEC (Enterohemorrhagic Escherichia coli)sebagai agen zoonosis pada manusia ditentukan oleh kemampuannya untuk melakukan perlekatan dan penyerangan pada sekum dan kolon serta kemampuannya untuk menghasilkan toksin. Faktor-faktor resiko yang berpengaruh terhadap penyebaran infeksi E.coli
O157:H7 dapat terjadi secara internal maupun eksternal. Faktor resiko yang berkaitan dengan tingkat penyebaran E.coli O157:H7 antara lain pada feses hewan, umur hewan, perubahan pakan, transportasi dan keadaan lingkungan sekitar. Faktor penyebab lainnya yang berkaitan dengan infeksi E.coli O157:H7 yaitu sumber air yang terkontaminasi E.coli dan faktor kebersihan (Welinder et al. 2005). Menurut Gie
et al. (2015) pemeliharaan ternak yang dikelola kurang baik akan beresiko terjadinya penyebaran infeksi E.coli O157:H7 pada sapi yang cukup tinggi dan pencemaran lingkungan peternakan pun dapat terjadi melalui kontaminasi terutama air. Sedangkan pada manusia infeksi bakteri ini bisa melalui makanan baik itu makanan masak atau setengah masak seperti daging, mengkonsumsi sayuran yang kurang bersih dan mengkonsumsi air yang tidak memenuhi standar SNI (Standar Nasional Indonesia) serta lingkungan yang tidak bersih.
Imunoglobulin Y (IgY)
4
dikenal sebagai pabrik biologis penghasil IgY. IgY ini terbentuk karena adanya respon imun terhadap antigen yang diinjeksikan pada ayam karena sistem imun ayam sangat responsif terhadap protein asing atau pemaparan mikroorganisme (vaksinasi atau infeksi alami) sehingga telur yang dihasilkan mengandung antibodi (Mustofa 2004). Hal ini diperkuat oleh Carlender (2002) yang menjelaskan ayam memiliki sensitivitas tinggi terhadap protein asing sehingga dapat memberikan respon pebentukan antibodi yang sangat baik dimana biosintesis antibodi akan berlangsung dalam sistem imun ayam dan selanjutnya ditransfer ke embrio melalui telur sehingga antibodi dapat ditemukan dalam telur ayam.
Secara umum, untuk memproduksi antibodi spesifik di dalam telur dapat dilakukan dengan menyuntik ayam menggunakan antigen tertentu yang dikehendaki (vaksin, bakerin, toksoid atau bahan biologis lain). Cara penyuntikan dapat dilakukan secara intra vena, intra muskular atau sub kutan tergantung dari preparasi antigen yang dikehendaki (Soejoedono et al. 2006). Rawendra (2005) menambahkan IgY kuning telur yang merupakan hasil transfer IgY serum darah kedalam folikular epitelium ovari dan terakumulasi pada kuning telur selama oogenesis untuk memberikan kekebalan pada anak ayam yang dikenal dengan antibody cross-placental mamalia.
Ayam petelur merupakan hal yang bersifat fisiologis dan tidak perlu melakukan tindakan intervensi yang berlebihan pada ayam. Penggunaan telur (IgY) diharapkan dapat mengurangi resiko itu dan digunakan sebagai sumber antitetanus. Hal ini sangat mungkin dilakukan karena antibodi di dalam darah induk ayam dapat ditransfer secara baik ke dalam telur dalam jumlah yang cukup banyak. Titer IgY dalam darah dan dalam telur tidak berbeda secara signifikan. Konsentrasi IgY pada kuning telur konstan sampai oosit matang (maturasi) dengan kandungan 10–20 mg/ml (Carlander 2002). Sehingga telur dapat digunakan sebagai sumber protein hewani dan sebagai pabrik produksi antibodi. Biaya produksi imunoglobulin pada telur unggas sangat murah dan efisien.
Imunoglobulin Y pada kuning telur ayam hanya mampu bertahan pada suhu pemanasan dibawah 60°C, tetapi tidak tahan terhadap pemanasan 75°C (Soejoedono
et al. 2006). IgY dapat bertahan pada pH diatas 4 namun aktivits IgY akan menurun pada pH 2 dengan suhu 37°C (Carlander 2002). Selain itu IgY banyak dimanfaatkan sebagai imunisasi pasif untuk melawan penyakit yang disebabkan oleh bakteri, virus, maupun antigen lainnya sebagaimana yang dijelaskan Wibawan (2010) bahwa IgY spesifik untuk berbagai bakteri dapat digunakan untuk mencegah penyakit bakterial dan mampu menjadi imunisasi pasif terhadap EPEC pada ayam. Selain itu IgY juga terbukti mampu menghambat perkembangan pertumbuhan E.coli patogen dan
Staphylococcus aureus sebagai penyebab mastitis pada sapi perah (Zhen et al. 2014), penyakit koksidiosis pada ayam (Lee et al. 2009), dan virus White Spot Syndrome
5
Struktur Imunoglobulin Y
Antibodi yang dibentuk akibat reaksi terhadap suatu antigen akan berbeda susunan asam aminonya dengan antibodi terhadap antigen yang lain. Hal ini disebut sebagai spesivitas antibodi (Wibawan et al. 2003). Satu unit struktur antibodi adalah glikoprotein yang terdiri dari empat rantai polipeptida. Semua antibodi memiliki struktur yang sama yaitu dua rantai pendek (VL) dan dua rantai panjang (VH). Kedua bentuk tersebut dihubungkan dengan bentuk kovalen (disulfida). Imunoglobulin utama yang terdapat pada kuning telur ayam adalah Imunoglobulin Y (IgY) (Gambar 1). IgY lebih berperan sebagai sistemik antibodi dari pada sekretori antibodi, namun IgY dapat ditemukan dalam saluran pencernaan duodenum, trachea, dan seminal plasma. Mekanisme transfer IgY dari serum ke dalam kuning telur berlangsung seperti proses transfer antibodi lintas plasenta pada mamalia.
Gambar 1 Struktur Imunoglobulin Y (wikipedia.com) Penyakit Diare
Penyakit diare masih sering menimbulkan KLB (Kejadian Luar Biasa) dengan penderita yang banyak dalam waktu yang singkat. Sampai saat ini penyakit diare masih merupakan masalah kesehatan utama setiap orang di negara-negara berkembang termasuk masyarakat di Indonesia, karena kurangnya pemahaman dan penyuluhan tentang penyebab diare. Melihat kondisi negara Indonesia yang sebagian besar penduduknya masih hidup di bawah garis kemiskinan, penyakit diare masih menjadi penyakit yang sering menyerang masyarakat Indonesia (Nursalam 2005).
6
3
METODE PENELITIAN
Waktu dan Tempat Penelitian
Penelitian ini dilakukan pada bulan November 2015 s/d Juni 2016 di Laboratorium Bakteriologi Divisi Mikrobiologi Medik Departemen Ilmu Penyakit Hewan dan Kesehatan Masyarakat Veteriner Fakultas Kedokteran Hewan Institut Pertanian Bogor dan Unit Kandang UPHL Fakultas Kedokteran Hewan Hewan Institut Pertanian Bogor.
Alat dan Bahan
Alat yang digunakan dalam penelitian ini adalah tabung reaksi, spuit, vortex, lemari pendingin untuk penyimpanan, alat-alat AGPT, sentrifus, tube, pinset, timbangan analitik, beaker glass, spatula, penangas air, gelas ukur, cawan petri,
alumunium foil, kertas saring, pipet tetes, oven, inkubator, mikropipet, spidol, panci, piring, mixer, oven, camera digital.
Bahan yang digunakan adalah isolat bakteri E. coli O157:H7, mencit, ayam betina siap bertelur, pakan ayam, serum ayam, media Blood Agar, media TSA, PEG 35%, PEG 2%, agarose, telur ayam, tepung, media blood agar, Freunds Adjuvant Complete, Freunds Adjuvant Inomplete , PBS, NaCl, media brain heart broth, PEG 6000, Coomasive Briliant Blue, methanol, asam sulfat, Bovine serum albumin (BSA), bahan-bahan biskuit, dll.
Prosedur Penelitian
Kultur Bakteri
Isolat bakteri yang digunakan dalam penelitian ini adalah isolat E.coli
O157:H7 yang diperoleh dari koleksi Laboratorium Bakteriologi IPHK Fakultas Kedokteran Hewan IPB yang sebelumnya telah dikarakterisasi. Bakteri E.coli
O157:H7 dibiakkan pada media blood agar untuk proses selanjutnya. Pembuatan antigen untuk vaksin bakteri E. coli O157:H7
Kultur bakteri diremajakan pada media blood agar, lalu diinkubasi pada suhu 37°C selama 24 jam. Kultur bakteri dibiakkan pada media brain heart infusion
7
dan digunakan sebagai vaksin untuk memproduksi antibodi. Dilakukan penambahan
Freunds Adjuvant Complete dengan mencampurkan antigen dengan perbandingan 1:1 (Wibawan et al. 1992).
Imunisasi Ayam Petelur
Produksi antibodi anti E.coli O157:H7 menggunakan sepuluh ayam petelur berumur 20 minggu yang siap bertelur. Proses imunisasi dilakukan dengan melakukan vaksinasi pada ayam pemberian antigen sebanyak 4 kali dengan interval 1 minggu. Minggu pertama disuntikkan antigen E. coli O157:H7 tanpa adjuvant secara intravena sebanyak 0,5 ml (109 CFU) per ekor (Carlender 2002). Minggu kedua, antigen dicampur dengan Freunds Adjuvant Complete melalui subkutan sebanyak 1 ml (109 CFU), sedangkan pada minggu ketiga dan keempat menggunakan
Freunds Adjuvant Inomplete sebanyak 1 ml (109 CFU) secara intramuscular (Hermans et al. 2014). Serum darah dikoleksi pada minggu pertama pasca imunisasi dan telur dikoleksi setelah minggu keenam imunisasi. Keberadaan antibodi diuji menggunakan teknik Agar Gel Precipitation Test.
Persiapan Antigen terlarut untuk uji AGPT
Isolat bakteri E. coli O157:H7 ditumbuhkan pada 50 ml media BHI, diinkubasi pada suhu 37 °C selama 18 jam. Suspensi disentrifugasi pada kecepatan 10000 rpm selama 10 menit. Pelet yang dihasilkan diresuspensikan dengan 5 ml NaCl, dan dilakukan 2 kali pencucian. Pelet ditambahkan dengan 0,5 ml HCl 0,2 N kemudian ditangas pada suhu 52 °C selama 1 jam. Selanjutnya homogenat dititrasi dengan NaOH 1 N, menggunakan indikator Phenol Red.Suspensi disentrifugasi pada 10000 rpm selama 10 menit, dilakukan 2 kali.Supernatan yang dihasilkan nantinya digunakan sebagai antigen terlarut (Wibawan & Laemmler 1992).
Uji AGPT (Agar Gel Presipitation Test)
Uji AGPT dilakukan untuk melihat keberadaan IgY pada serum darah ayam sebagai respon vaksinasi bakteri E.coli O157:H7. Agar gel dibuat dengan melarutkan 0.5 gr agarose dan 0,05 Na Azid yang dilarutkan dalam 20 ml PBS pH dengan 7.2 dan 20 ml aquades. Larutan dipanaskan dalam penangas air sampai larut dan sampai berwarna bening. Kemudian dituangkan di atas objek glass sebanyak 4 ml tunggu sampai keras. Cetak sumur-sumur dengan alat gel puncher. lsi sumur dengan antigen terlarut (tengah) dan serum (pinggir) masing-masing sumur sebanyak 25 µl. Simpan pada box yang diberi tisu basah (aquades steril). lnkubasi pada suhu ruang selama 24 sampai 48 jam. Hasil positif apabila ada garis presipitasi antara antibodi (serum) dan antigen (Layi dan Bergan 2003).
Panen telur (IgY)
8
yang diuji adalah telur yang dihasilkan ayam yang sudah positif uji serum darah pada uji AGPT.
Ekstraksi IgY telur ayam
Proses ekstraksi IgY dengan metode pemurnian Water soluble fraction. Kuning telur dipisahkan dari bagian putihnya kemudian diletakkan diatas kertas saring untuk memisahkan bagian putih telur yang menempel pada kuningnya. Membran kuning telur ditusuk dengan pinset agar cairan kuning telur dapat diambil, kemudian dimasukkan dalam gelas ukur. Kuning telur tersebut dilarutkan pada miliQ pH 4 sebanyak empat kali volume kuning telur (1:4). Setelah dihomogenkan dengan
magnetic stirer lalu ditambahkan lagi dengan miliQ pH 2 hingga pH suspensi 5.0 sampai 5.2 dan diinkubasi pada suhu 4°C minimal 12 jam. Suspensi disentrifusi pada 3.000 rpm dengan suhu 4°C selama 20 menit dan diperoleh supernatan yang disebut dengan Water Soluble Fraction (WSF).WSF ini dibuat menjadi pH 7,5, dipekatkan dengan PEG 6.000 sebanyak 12% (Akita & Nakai (1992)).
Suspensi WSF dihomogenkan dan disentrifugasi dengan kecepatan 3.000 rpm pada suhu 20 °C selama 15 menit. Dilakukan pencucian pelet dengan cara menambahkan amonium sulfat 40% dan disentrifugasi dengan kecepatan 11.700 rpm selama 15 menit. Pencucian ini dilakukan tiga kali, kemudian pelet dilarutkan dalam PBS pH 7,4 sebanyak 5 ml. Suspensi ini didialisis dalam larutan PBS pH 8 selama 24 jam.
Uji Kosentrasi Protein Kuning Telur
Dilakukan dengan metode Bradford yang terdiri dari 100 mg Coomasive Briliant Blue yang dilarutkan dalam 50 ml methanol 95% yang ditambakan 100 ml asam fosfat 85%. Larutan diencerkan dengan aquades hingga volume 1 liter dan disaring dengan kertas saring. Kemudianan larutan protein standar Bovine serum albumin (BSA) digunakan untuk membuat grafik kosentrasi protein standar sebelum mengukur kosentrasi sampel telur. Larutkan dan homogenkan BSA 1 mg ke 1 ml aquades, ambil 100 µl dari setiap tabung dan masukkan ke tabung baru yang sebelumnya telah diisi 5 ml larutan bradford. Pembacaan kosentrasi WSF kuning telur dilakukan dengan spektofotometer pada panjang gelombang 595 nm (Priyanka
et al. 2013)
Pembuatan Biskuit IgY
Pembuatan biskuit IgY dilakukan dengan mencampurkan mentega 150 gr, kuning telur 2 buah, gula halus 70 gr menggunakan mixer. Lalu tambahkan tepung terigu 150 gr, susu bubuk 10 gr dan meizena 15 gr, diaduk selama 15 menit dan dicetak. Biskuit dipanggang pada suhu 40oC menggunakan oven.
Aplikasi IgY spesifik E. coli O157:H7 pada mencit
9
1. Mencit diinfeksi 9x108 CFU E.coli O157:H7
2. Mencit diinfeksi 9x108 CFU E.coli O157:H7 dan diberikan biskuit dengan dosis 60 mg setelah 2 hari pasca infeksi
3. Mencit diinfeksi 9x108 CFU E.coli O157:H7 dan diberikan biskuit dengan dosis 80 mg setelah 2 hari pasca infeksi
4. Mencit diinfeksikan 9x108 CFU E.coli O157:H7 dan diberikan biskuit dengan dosis 100 mg setelah 2 hari pasca infeksi
5. Mencit diberi biskuit dosis 60 mg dan diinfeksi 9x108 CFU E.coli
O157:H7 setelah 2 hari pasca pemberian biskuit
6. Mencit diberi biskuit dosis 80 mg dan diinfeksi 9x108 CFU E.coli
O157:H7 setelah 2 hari pasca pemberian biskuit
7. Mencit diberi biskuit dosis 100 mg dan diinfeksi 9x108 CFU E.coli
O157:H7 setelah 2 hari pasca pemberian biskuit Pengamatan Histopatologi ginjal
Pengamatan histopatologi ginjal meliputi perubahan pada tubulus, pelebaran lumen tulubus, akuolisasi lumen tululus, sel epitel tubulus proximalis, degenerasi sel, nekrosis sel, pengamatan selaput fibrosis di bagian perifer dan pendarahan (hemorhagi). Derajat kerusakan ginjal dikuantitatifkan sebagai berikut:
0 = tidak terjadi kerusakan jaringan ginjal + = bila terjadi 1-2 kriteria diatas
++ = bila ditemukan 2-4 kriteria diatas
+++ = bila ditemukan lebih dari 4 kriteria diatas
Analisis Data
10
4
HASIL DAN PEMBAHASAN
Identifikasi Escherichia coli O157:H7
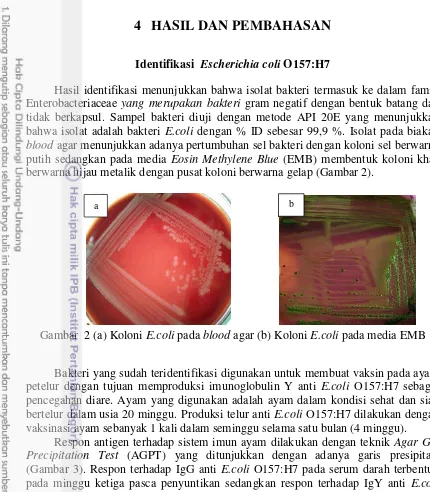
Hasil identifikasi menunjukkan bahwa isolat bakteri termasuk ke dalam famili Enterobacteriaceae yang merupakan bakteri gram negatif dengan bentuk batang dan tidak berkapsul. Sampel bakteri diuji dengan metode API 20E yang menunjukkan bahwa isolat adalah bakteri E.coli dengan % ID sebesar 99,9 %. Isolat pada biakan
blood agar menunjukkan adanya pertumbuhan sel bakteri dengan koloni sel berwarna putih sedangkan pada media Eosin Methylene Blue (EMB) membentuk koloni khas berwarna hijau metalik dengan pusat koloni berwarna gelap (Gambar 2).
Gambar 2 (a) Koloni E.coli pada blood agar (b) Koloni E.coli pada media EMB
Bakteri yang sudah teridentifikasi digunakan untuk membuat vaksin pada ayam petelur dengan tujuan memproduksi imunoglobulin Y anti E.coli O157:H7 sebagai pencegahan diare. Ayam yang digunakan adalah ayam dalam kondisi sehat dan siap bertelur dalam usia 20 minggu. Produksi telur anti E.coli O157:H7 dilakukan dengan vaksinasi ayam sebanyak 1 kali dalam seminggu selama satu bulan (4 minggu).
Respon antigen terhadap sistem imun ayam dilakukan dengan teknik Agar Gel Precipitation Test (AGPT) yang ditunjukkan dengan adanya garis presipitasi (Gambar 3). Respon terhadap IgG anti E.coli O157:H7 pada serum darah terbentuk pada minggu ketiga pasca penyuntikan sedangkan respon terhadap IgY anti E.coli
O157:H7 pada kuning telur terlihat pada minggu keenam pasca penyuntikan (Tabel 1). Perbedaan respon ini dikarenakan immunoglobulin yang terbentuk pertamakali dalam darah merupakan bentuk dari pemaparan antigen, kemudian ditransfer oleh darah ke dalam kuning telur. Rawendra (2005) dalam penelitiannya menyatakan bahwa pengukuran aktivitas netralisasi dan koleksi kuning telur positif IgY dilakukan 2 minggu setelah IgY positif pada serum darah, karena injeksi dosis pertama akan menghasilkan antibodi spesifik di dalam serum. Injeksi dengan sel-sel bakteri akan memunculkan reaksi antibodi sepuluh sampai empat belas hari pasca injeksi.
11
Tabel 1 Hasil Uji AGPT serum dan kuning telur pasca vaksinasi
Vaksinasi Serum darah Kuning telur
Pra Vaksinasi -
-Minggu 1 -
-Minggu 2 -
-Minggu 3
-Minggu 4
-Minggu 5
-Minggu 6
Minggu 7
Minggu 8
Minggu 9
Gambar 3 (a) AGPT serum darah positif IgG pada minggu ketiga (M3) dan keempat (M4) pasca infeksi (b) AGPT kuning telur positif IgY pada minggu ketuju (M7) pasca infeksi. Antigen E.coli O157:H7 (1 dan 2)
Garis presipitasiterjadi karena adanya keseimbangan antara konsentrasi antigen dan antibodi dalam kuning telur maupun serum. Berdifusi membentuk antigen antibodi komplek dimana molekul antibodi berikatan silang dengan determinan antigen.
Kosentrasi Kuning Telur
Hasil pengukuran kosentrasi IgY didapatkan sebanyak 2,361 mg/ml. Hasil ini relatif lebih rendah dibandingkan dengan hasil IgY WSF yang dihasilkan oleh Chae
et al. (2006) yaitu 5 mg/ml. Namun hasil purifikasi yang dilakukan oleh Carlender (2002) dengan metode yang sama menunjukkan total IgY yang lebih rendah, yaitu 2.21 mg/ml. Perbedaan konsentrasi IgY yang diperoleh dapat terjadi karena beberapa faktor, antara lain IgY hilang pada proses pencucian, tertinggal dalam tabung atau alat-alat lain. Cahyaningsih (2016) menambahkan bahwa rendahnya IgY yang dihasilkan disebabkan oleh proses dan lama penyimpanan yang dapat mempengaruhi konsentrasi protein dalam telur sehingga diperlukan ketelitian dalam purifikasi.
a b
M4
M4
M4 M3
M3
M3
M7
M7 M7
M7
M7 M7
12
Ekstraksi purifikasi IgY dilakukan menggunakan SDS-PAGE. Dari hasil ekstraksi IgY didapatkan beberapa profil pita protein, yaitu pita protein IgY rantai berat yang berada pada 48 kDa, dan pita protein IgY rantai ringan yang memiliki berat molekul 20 kDa (Gambar 4). Chae et al. (2006) menjelaskan dalam penelitiannya massa pita molekul protein IgY adalah berkisar antara 92-12 kDa.
Gambar 4 Pita Protein IgY E.coli O157: H7. (1) marker Umum (2) sampel 1 IgY tanpa purifikasi (3) sampel 2 IgY tanpa purifikasi (4) sampel 1 IgY purifikasi (5) sampel 2 IgY purifikasi.
Aplikasi biskuit IgY
Pengujian efektivitas biskuit yang mengandung IgY dilakukan pada hewan coba mencit (Mus musculus) dengan dosis yang berbeda. Selama percobaan berlangsung tidak terjadi kematian namun kelompok perlakuan memberikan perbedaan pada gejala diare. Pada Kelompok A1 yang diinfeksi E.coli O157:H7 tanpa pemberian biskuit IgY mengalami diare pada hari kedua pasca infeksi, sedangkan pada kelompok mencit yang diinfeksikan E.coli O157:H7 dan diberi biskuit IgY setelah dua hari pasca infeksi (A2, A3, A4) menunjukkan gejala diare pada hari keempat. Sementara itu pada kelompok mencit diberi biskuit IgY dan diinfeksi E.coli O157:H7 setelah dua hari pasca pemberian biskuit (A5, A6, A7) menunjukkan gejala diare pada hari kelima. Perbedaan gejala diare ini karenakan pemberian biskuit IgY sebelum diinfeksikan E.coli O157:H7 mampu meminimalisir koloni bakteri pada mukosa usus walaupun tidak mampu mencegah terjadinya diare secara sempurna.
Gejala fisik lainnya yang ditunjukkan pada setiap kelompok perlakuan adanya perubahan pada nafsu makan yang menyebabkan fisik mencit menjadi lemas dan kurang aktif. Sesuai yang disampaikan Suwito (2009) bahwa akan terlihat gejala klinis pada hewan dan manusia jika terinfeksi E.coli O157:H7 yaitu dengan kehilangan nafsu makan, muntah, kelelahan sampai diare berdarah.
Biskuit IgY yang dikonsumsi mencit dalam pengamatan selama tujuh hari tidak berpengaruh terhadap pertambahan berat badan (BB) mencit (p value ≥ 0,05).
48 kda
13
Walaupun demikian terdapat variasi rata-rata pertambahan berat badan mencit pada ketujuh kelompok perlakuan selama tujuh hari (Tabel 2).
Tabel 2 Rata-rata pertambahan BB (gr)
Perlakuan Rata-rata Pertambahan BB (gr) p value
A1 A2 A3 A4 A5 A6 A7
3 ± 0,707a 2,8 ± 1,095 a 2,8 ± 0,836 a 3,2 ± 0,447 a 2,8 ± 0,836 a 2 ± 0,100 a 1,8 ± 0,836 a
0,115
Ket: (A1) diinfeksi E.coli O157:H7 (A2) diinfeksi E.coli O157:H7 dan diberikan biskuit dosis 60 mg (A3) dinfeksikan E.coli O157:H7 dan diberikan biskuit dosis 80 mg (A4) diinfeksikan E.coli O157:H7 dan diberikan biskuit dosis 100 mg (A5) diberikan biskuit dosis 60 mg dan diinfeksikan E.coli O157:H7 (A6) diberikan biskuit dosis 80 mg dan diinfeksikan E.coli O157:H7 (A7) diberikan biskuit dosis 100 mg dan diinfeksikan E.coli
O157:H7.
Gambaran Histopatologi
Kerusakan organ ginjal yang disebabkan oleh bakteri E.coli O157:H7 terdiri dari kapsula menebal, hemorhagi, infiltrasi sel limfosit bahkan degenerasi sampai nekrosis pada tubulus proksimal. Hal ini mengindikasikan pemberian IgY secara peroral tidak efektif memberikan perlindungan dari pemaparan bakteri E.coli
O157:H7 pada mencit. Gambaran perubahan histopatologi dari ketujuh perlakuan terlihat dari gambar dibawah ini.
Gambar 5 Ginjal mencit kelompok kontrol diinfeksikan E.coli O157:H7 tanpa biskuit IgY mengalami Tubulonephritis non suppurativa (1) nekrosis epitel tubulus proximalis (2) hemorhagi (3) infiltrasi sel mononuclear (4) selaput fibrosis.
Gambar 6 Ginjal mencit diinfeksikan E.coli
O157:H7 dan diberikan biskuit IgY 60 mg mengalami tubulonephrotic et hemorhagica
(1) degenerasi nekrosis sel epitel tubulus proximalis (2) hemorhagi (3) pembendungan darah.
14
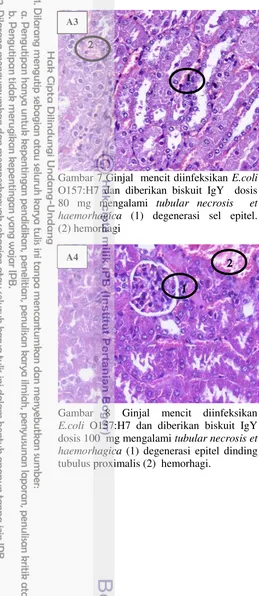
Gambar 7 Ginjal mencit diinfeksikan E.coli
O157:H7 dan diberikan biskuit IgY dosis 80 mg mengalami tubular necrosis et haemorhagica (1) degenerasi sel epitel. (2) hemorhagi
Gambar 8 Ginjal mencit diinfeksikan
E.coli O157:H7 dan diberikan biskuit IgY dosis 100 mg mengalami tubular necrosis et haemorhagica (1) degenerasi epitel dinding tubulus proximalis (2) hemorhagi.
Gambar 9 Ginjal mencit diberikan biskuit IgY dosis 60 mg dan diinfeksikan E.coli
O157:H7 mengalami tubular necrosis et haemorhagica (1) degenerasi epitel dinding tubulus proximalis (2) hemorhagi.
Gambar 10 Ginjal mencit diberikan biskuit IgY dosis 80 mg dan diinfeksikan E.coli
O157:H7 mengalami tubular necrosis et haemorhagica (1) degenerasi epitel dinding tubulus proximalis (2) hemorhagi.
A5
A6
15
Gambar 11 Ginjal mencit diberikan biskuit IgY dosis 100 mg dan diinfeksikan
E.coli O157:H7 mengalami tubular necrosis et haemorhagica (1) degenerasi epitel dinding tubulus proximalis (2) hemorhagi.
Pada kelompok A1 (Gambar 5) yang hanya diinfeksikan E.coli O157:H7 ginjal mencit mengalami kerusakan yang parah. Terjadinya infiltrasi sel mononuclear di interstisial dimana terdapatnya cairan yang mengelilingi jaringan di bagian interstitial dan terdapat selaput fibrosis dibagian perifer. Adanya perubahan pada tubulus proksimal yang membengkak dengan sitoplasma sehingga menyebabkan degenerasi bahkan sampai nekrosis pada sel epitel tubulus proximalis. Hal inilah yang menyebabkan lumen tulubus proximal mengalami penyempitan hingga menutup (Zulfiani et al. 2011).
Selain itu terjadinya pendarahan (hemoraghica) dimana kondisi ini ditandai dengan keluarnya darah dari dalam vaskula akibat kerusakan dinding vaskula. Eritrosit yang keluar dari pembuluh darah pecah dengan cepat dan difagositosis oleh makrofag yang terdapat di sekitar jaringan yang mengalami peradangan. Terjadinya hemorhagi akibat dari bahan toksik yang merusak endotel kapiler seperti keracunan yang dapat menghambat penggumpalan darah sehingga terjadi pendarahan dan toksin uremik yang dapat merusak endotel pembuluh darah.
Pada kelompok A2 (Gambar 6) mencit diinfeksikan E.coli O157:H7 dan diberikan biskuit IgY 60 mg mengalami tubulo nephrotic et hemorrhagica. Dari gambaran histopatologi terlihat adanya degenerasi nekrosis sel epitel tubulus proximalis sehingga terjadinya perubahan morfologi sel akibat rusaknya permukaan sel epitel. Selain itu terdapat pembendungan darah pada ginjal. Hal ini disebabkan oleh gangguan sirkulasi dalam darah karena kurang oksigen dan zat gizi dalam tubuh inang (Parameswari et al. 2013).
Kerusakan histopatologi mencit menunjukkan perbedaan pada kelompok perlakuan lain yaitu A3, A4, A5, A6, dan A7. Skoring histopatologi ditunjukkan pada Tabel 3.
16
Tabel 3 Hasil skoring histopatologi ginjal
Perlakuan Skor Skor Patologi
A1
Infilrasi sel, degenerasi, nekrosis, selaput fibrosis, hemorhagi
Degenerasi, nekrosis, pembendungan darah, hemorhagi
Degenerasi dan hemorhagi Degenerasi dan hemorhagi Degenerasi dan hemorhagi Degenerasi dan hemorhagi Degenerasi dan hemorhagi
Kerusakan organ ginjal dari setiap perlakuan berbeda (Tabel 3). Perlakuan A3, A4, A5, A6, dan A7 menunjukkan kerusakan yang tidak separah A1 dan A2. Pemberian biskuit IgY pasca infeksi E.coli O157:H7 pada dosis 80 mg (A3) dan 100 mg (A4) menunjukkan bahwa sel epitel tubulus proximalis hanya mengalami cedera ringan yang menyebabkan nekrosis pada sel. Selain itu pendarahan yang dialami tidak begitu parah dan perlahan bisa normal kembali. Nekrosis merupakan kematian dari suatu sel akibat adanya kerusakan akut karena peradangan sel. Kerusakan pada ginjal disebabkan oleh berbagai faktor seperti bahan toksin, obat obatan, atau konsentrasi tinggi dari zat yang berpotensial merusak dan berbahaya seperti zat kimia. Kerusakan tubulus proksimal ginjal terlihat dari adanya penyempitan pada tubulus proksimalis (Revathi & Yogananda 2006).
Pemberian biskuit sebelum diinfeksi E.coli O157:H7 juga menunjukkan kerusakan yang tidak begitu parah. Hal ini menandakan dengan pemberian biskuit dengan dosis 60 mg, 80 mg, dan 100 mg sebelum diinfeksikan E.coli O157:H7 mampu meningkatkan kekebalan tubuh mencit walaupun tidak sempurna. Mekanisme pemberian IgY peroral yang menempel pada berbagai patogen enterik yang terdapat pada permukaan mukosa pencernaan dapat mencegah perlekatan dan pertumbuhan bakteri. Herman et al. (2014) melakukan imunisasi pasif pada ayam broiler menggunakan IgY secara peroral menyatakan bahwa pemberian imunisasi peroral mampu mengurangi kolonisasi bakteri Campylobacter jejuni
pada mukosa usus.
17
5
KESIMPULAN DAN SARAN
Kesimpulan
Imunisasi pasif menggunakan biskuit IgY anti E.coli O157:H7 dengan dosis 60 mg, 80 mg, dan 100 mg selama tujuh hari masih menunjukkan gejala diare dan belum menunjukkan perlindungan pada organ ginjal.
Saran
18
DAFTAR PUSTAKA
Andriani. 2008. Eschericia coli Sebagai Penyebab Penyakit Zoonosis. J Litbang Deptan. 173–176.
Asemota H, Suzette C, Angel AJV, Wayne M. 2013. Purification of Avian IgY with Trichloroacetic Acid (TCA). J Chromatograph Separat Techniq. 4: 9. Azis M, Dhinintya HN, Aurita SR, Kristiyani DM, Norma DL, Juni H. 2013.
Waktu Produksi Yolk Immunoglobulin (IGY) Kuning Telur Ayam yang Diimunisasi Streptococcus mutans. Maj Ked Gi: 20(1): 31-34
Barlow RS, Gobius KS, Desmarchelier PM. 2006. Shiga toxin-producing E. coli
in ground beef. Int. J Food Microbiol. 111: 1-5.
Cahyaningsih T. 2016. Pengaruh Pemberian IgY Spesifik Staphylococcus aureus Sebagai Pencegahan Staphylococcosis Pada Kelinci. Tesis: Sekolah Pascasarjana IPB.
Campbell GR, Prosser J, Glover A, Killham K. 2001. Detection of Escherichia coli O157:H7 in soil and water using multiplex PCR. J of Applied Microbiology. 91:1004-1010.
Carlander D. 2002. Avian IgY Antibody: in vitro and in vivo. Dissertation: Acta Universitatis Upsaliensis, Uppsala.
Carlander D, Wilhelmson M, Larsson A. 2002. Immunoglobulin Y Level in Egg Yolk From Tree Chiken Genotypes. Food and Agricultular Immunology. 15(1): 35-40.
Chae HS, Singh HK, Ahn CN, Yoo YM, Jeong SG, Ham JS, Kim DW. 2006. Effects of Egg Yolk Antibodies Produced in Response to Different Antigenic Fractions of E. coli O157:H7 on E. coli Suppression. Asian-Aust J. 19(11): 1665–1670.
Cliver. 1990. Salmonella In Foodborne Diseases. Academic Press, Inc. 185-204. Efrizal. 2007. Peran Imunoglobulin (Igy) Sebagai Anti Adhesi Dan Opsonin
Untuk Pencegahan Serangan Salmonella enteritidis. Tesis: Sekolah Pascasarjana IPB.
Frenzen, Paul D. 2005. Economic Cost of Illness due to Escherichia coli O157 Infections in the United States. J Of Food Protection. 68: 2623-2630.
Gie JLT, Yatri D. 2015. Identifikasi Escherichia Coli O157:H7 Pada Susu Sapi Perah Dan Lingkungan Peternakan. J Kedokteran Hewan. 9: 2.
Hermans D, Steendam K, Verbrugghe E, Verlinden M, Martel A, Seliwiorstow T, Heyndrickx M, Haesebrouck F, Zutter L ,Deforce D, Pasmans F. 2014. Passive immunization to reduce Campylobacter jejuni colonization and transmission in broiler chickens.Veterinary Research. 45: 27.
Indrawati A 2010. Telur Ayam 3 in one dan Anti Diare: Produksi, Efikasi, dan Aplikasinya. Laporan Akhir Penelitian Institut Pertanian Bogor.
Ko KY, Ahn DU. 2007. Preparation of Immunoglobulin Y from Egg Yolk Using Ammonium Sulfate Precipitation and Ion Exchange Chromatography. Poultry Science. 86: 400–407.
19
Lu, Y.N, Liu, J.J, Jin, L.J. 2009. Passive immunization of crayfish (Procambius clarkiaii) with chicken egg yolk immunoglobulin (IgY) against white spot syndrome virus (WSSV). Appl Biochem Biotechnol. 159: 750-8.
Mainil JG, Daube G. 2005. Verotoxigenic Escherichia coli from animal, humans
and foods: Who’s who? J Appl Microbiol. 98: 1332–1344.
Mustofa Z. 2004. Peran Imunogglobulin (IgY) Sebagai Anti Adhesi dan Opsonin untuk Pecegahan Serangan Escherichia coli Enteropatogenik (EPEC) K 1.1.
Tesis: Sekolah Pascasarjana IPB.
Parameswari W, Sasanti AD, Muslim. 2013. Populasi Bakteri, Histologi, Kelangsungan Hidup Dan Pertumbuhan Benih Ikan Gabus (Channa Striata) Yang Dipelihara Dalam Media Dengan Penambahan Probiotik. J Akuakultur Rawa Indonesia. 1(1) : 76-89
Peter CH, Councell FT, Keys C, and Monday SR. 2011. Virulence characterization of Shiga-toxigenic Escherichia coli isolates from wholesale produce. Microbiol. 77 (1): 343-345.
Poetri ON. 2007. Peran Antibodi Kuning Telur (IgY) Sebagai Anti Adhesi dan Opsonin Untuk Pencegahan Serangan Mutan Streptococcus serotipe d
(Streptococcus sobrinus). Tesis: Sekolah Pascasarjana IPB.
Rawendra R. 2005. Prospek Pengembangan Imunoglobulin Y (IgY) Kering Beku Sebagai Nutraceutical Food anti Enterophagenic Escherichia coli (EPEC).
Disertasi: Sekolah Pascasarjana IPB.
Revathi K, Yogananda M. 2006. Effect of bromadiolone on haematology, liver and kidney in Mus musculus. J of Environmental Biology. 27(1): 135-140. Rey JS, Sanchez JE, Blanco J, Hermoso de Mendoza M, Hermoso de Mendoza A.
Garcia C, Gil N, Tejero R, Rubio. 2006. Prevalence, serotypes and virulence genes of Shiga toxin-producing E. coli isolated from ovine and caprine milk and other dairy products in Spain. Inter. J Food Microbiol. 107: 212-217. Sartika, Indrawani, dan Sudiarti. (2005). Analisis Mikrobiologi Escherichia coli
O157:H7 Pada Hasil Olahan Hewan Sapi Dalam Proses Produksinya.
J Makara Kesehatan. 9(1): 23-28.
Schade R, Christian S, Coenraad H, Michael E. 1996. The Production Of avian (Egg Tolk) antibodies: IgY. [internet]. [diunduh 2015 Desemberr 12]. Tersedia pada: https://eurl-ecvam.jrc.ec.europa.eu/about-ecvam/archive-publications /publication/ WorkshopReport21.pdf.
Schade R, Esteban GC, Rodolfo S, Pablo AC. 2005. Chicken Egg Yolk Antibodies (IgY-technology): A Review of Progress in Production and Use in Research and Human and Veterinary Medicine. ATLA. 33: 1-26.
Soejoedono RD, Wibawan TW, Zinatul H. 2006. Pemanfaatan Telur Ayam Sebagai Pabrik Biologis: Produksi Yolk Immunoglobulin (IgY) Anti Plaque dan Diare dengan Titik Berat pada Anti Streptococcus mutan, Escherichia coli dan Salmonella Enteridis: Laporan Kemajuan Riset Unggulan Terpadu XII-2. Suardana IW, Artama WT, Asmara W, Daryono BS. 2010. Identifikasi
Escherichia coli O157:H7 serta Deteksi Gen Shiga Like Toxin 1 dan 2 Asal Feses Hewan, Daging dan Feses Manusia. J Veteriner. 11(4): 264-270.
20
Sun H, Sirui C, Xia C, Guiyun X, Lujiang Q. 2013. Correlation analysis of the total IgY level in hen serum, egg yolk and offspring serum. J of Animal Science and Biotechnology. 4: 10.
Sunwoo HH, Lee EN, Mennien K, Suresh MR, Sim JS. 2002. Growth Inhibitory Effect of Chicken Egg Yolk Antibody (IgY) on Escherichia coli O157:H7.
J Of Food Science. 67: 1486-1494.
Suwito W. 2009. Dampak Verotoksigenik Dan Enterohemoragik Escherichia Coli (Vtec Dan Ehec) Pada Hewan, Manusia Dan Makanan. Wartazoa. 19: 2.
Thenmozhi M. 2010. Isolation Of Potentially Pathogenic Escherichia Coli O157:H7 From The Water Sources. International J of Pharma and Bio Sciences. 4(3): 0975-6299.
Welinder OC, Kaijser B. 2005. Enterohemorrhagic Escherichia coli (EHEC).
Scand J Infect. 37(7): 405-416.
Wibawan IWT, Laemmler Ch. 1992. Reatinship between group B Steptococcal serotypes and cell surface hydrophobicity. J Vet Med. 39: 376-382.
Wibawan IWT, Fachriyan HP, Rudi R. 2010. Produksi Antibodi (IgY) Terhadap
Entero PathogenicEscherichia coli (EPEC) dalam Kuning Telur. J Kedokteran Hewan. 4: 1.
Zein U, Khalid HS, Josia G. 2014. Diare Akut Disebabkan Bakteri. [internet]. [diunduh 2015 November 4]. Tersedia pada: http://library.usu.ac.id/ download/fk/penydalam-umar5.pdf.
21
23
Lampiran 1 Data nafsu makan mencit Kelompok
Perlakuan
Data nafsu makan hari ke-
1 2 3 4 5 6 7
24
Lampiran 2 Data kejadian diare pada mencit Kelompok
Perlakuan
Kejadian diare hari ke-
1 2 3 4 5 6 7
25
Lampiran 3 Pertambahan berat badan mencit
Kelompok Berat badan (gr) hari ke- Pertambahan
1 2 3 4 5 6 7 berat (gr)
A1 1 20 22 22 23 25 23 23 3
2 20 21 22 22 24 23 23 2
3 20 23 23 24 25 24 24 3
4 21 21 22 22 23 23 24 2
5 21 22 22 22 22 23 23 2
Rata rata A1 20 22 22 23 24 23 23 3
A2 1 21 22 23 23 22 23 23 2
2 20 23 23 22 22 22 22 2
3 20 22 23 23 22 23 24 2
4 20 22 23 24 23 23 24 3
5 21 22 23 24 25 24 23 3
Rata rata A2 20 22 23 23 23 23 23 3
A3 1 21 21 22 23 23 24 23 2
2 20 22 22 23 24 24 24 3
3 21 22 24 24 23 23 23 3
4 20 23 23 23 23 22 23 2
5 20 23 23 23 22 23 23 2
Rata rata A3 20 22 23 23 23 23 23 3
A4 1 20 23 23 23 24 24 24 3
2 20 21 23 23 24 24 23 3
3 21 22 23 23 24 24 24 3
4 20 22 22 23 23 24 23 2
5 21 22 23 23 24 24 24 3
Rata rata A4 20 22 23 23 24 24 23 3
A5 1 21 23 23 24 24 22 22 3
2 20 23 24 22 25 24 24 3
3 21 22 23 23 24 24 24 3
4 21 22 24 23 23 24 23 3
5 20 22 22 22 22 22 23 2
Rata rata A5 21 22 23 23 24 23 23 3
A6 1 20 23 24 25 23 23 23 3
2 21 23 23 24 24 22 22 3
3 20 23 24 23 23 22 23 3
4 21 22 23 23 24 23 22 2
5 20 22 23 24 24 24 23 3
Rata rata A6 20 23 23 24 24 23 23 3
A7 1 21 23 24 23 23 23 23 3
2 20 20 20 24 23 22 23 2
3 20 22 24 23 22 22 22 2
4 21 23 23 23 23 22 22 2
5 21 21 23 24 24 22 22 2
26
RIWAYAT HIDUP
Penulis bernama lengkap Nadhrah Alhan, dilahirkan di Bukittinggi pada 21 November 1991 sebagai anak kembar dari dua bersaudara dari Bapak Azhar dan ibu Sidrati.
Penulis menyelesaikan pendidikan Sekolah Dasar di SDN 11 Batuhampar, Kecamatan Akabiluru, Kabupaten Lima Puluh Kota, Sumatera Barat pada tahun 2003. Pendidikan tingkat pertama diselesaikan di MtsN Kota Payakumbuh pada tahun 2006, sedangkan pendidikan tingkat atas diselesaikan di SMA Negeri 1 Kota Payakumbuh pada tahun 2009.
Pada tahun 2009, penulis diterima sebagai mahasiswa di Fakultas Matematika dan Ilmu Pengetahuan Alam pada Program Studi Biologi Universitas Negeri Padang (UNP) dan lulus sebagai Sarjana Sains (S.Si) tahun 2013.