Helmina Br. Sembiring JURNAL PENELITIAN MIPA Volume 1, Nomor 1 Desember 2007
34
PEMBUATAN SURFAKTAN
tert
-BUTIL GALAKTOSIDA MELALUI
REAKSI ASETALISASI GALAKTOSA DENGAN
tert
-BUTANOL
Helmina Br. Sembiring
Departemen Kimia FMIPA Universitas Sumatera Utara Jl. Bioteknologi No. 1 Kampus USU Medan 20155
Abstract
A surfactant tert-butyl galactoside has been synthesized from galactose and tert-butanol in asetalization reaction. Acetalization of galactoside with tert-butanol in petroleum ether as a solvent using p-TSA as catalyst gave tert-butyl galactoside. The product was characterized by analysis spectroscopy FT-IR, 1H-NMR and the measurement of surface tesion. The compound of tert-butyl galactoside was a surfactant with critical micelle concentration (CMC) was 0,02%and hydrophilic-lypophilic balance (HLB) value 3,93.
Keywords:Asetalisasi, KKM, dan HLB
PENDAHULUAN
Surfaktan merupakan zat aktif permukaan yang berperan untuk menurunkan tegangan permukaan. Aktivitas kerja dari suatu surfaktan ini disebabkan karena sifat ganda dari molekulnya yang terdiri dari bagian gugus hidrofil dan lipofil. Bagian polar suatu surfaktan dapat bermuatan positif (surfaktan kationik), negatif (surfaktan anionik), netral (surfaktan non ionik), sedangkan bagian lopofilnya merupakan suatu alkil (Genaro, 1990).
Kedua gugus ini mempunyai keseimbangan hidrofilik dan lipofilik yang menggolongkan jenis surfaktan tersebut apakah bersifat sebagai pengemulsi, pembasah, penglarut, detergen atau anti busa, dan sebagainya (Martin, A.,1993). Surfaktan telah digunakan dalam jumlah yang sangat besar untuk berbagai kebutuhan rumah tangga, detergen dan produk-produk pembersih lainnya (Belitz, et al., 1986). Kirk, et al., 1998, telah melakukan reaksi asetalisasi antaran glukosa dengan kloropropanol, dimana pada asetalisasi terjadi pada posisi gugus hidroksil C1 hemiasetal dengan gugus hidroksil dari kloropropanol.
Berdasarkan hal tersebut peneliti telah mensintesis suatu bahan surfaktan baru turunan dari salah satu monosakarida yaitu galaktosa. Melalui reaksia asetalisasi dengan tert-butanol dengan menggunakan pelarut organik seperti petroleum eter dan katalis p-TSA. Reaksinya menghasilkan senyawa target yaitu tert-butil galaktosida yang mempunyai gugus eter, hidroksil, dan alkil yang merupakan ciri khas suatu surfaktan.
BAHAN DAN METODE
Bahan
Galaktosa, tert-butanol, petroleum eter, p-TSA, natrium asetat, natrium sulfat anhidrat, benzena, dan alumina 60 G. Semuanya diperoleh dari E’Merck.
Metode
Pembuatan tert-Butil Galaktosida
Sebanyak 9 g (0,05 mol) galaktosa dan 50 ml tert-butanol (berlebih) dimasukkan ke dalam labu leher tiga 500 ml, yang telah dilengkapi dengan pengaduk magnet, termometer, penangas minyak, pendingin leibig, pendingin bola, dan corong penetes yang telah dipasang sedemikian rupa. Kemudian ditambahkan sebanyak 100 ml petroleum eter dan 0,2 g (0,0013 mol) katalis p-TSA. Kemudian campuran diaduk selama 2 jam pada suhu 50–60 ºC. Selanjutnya direfluks hingga tidak ada air yang diperoleh dari destilat yang ditampung pada corong pisah setelah diuji dengan kuprisulfat anhidrat. Hasil reaksi didinginkan pada suhu kamar dan selanjutnya ditambahkan 0,2 g natrium sulfat anhidrat, lalu diaduk. Selanjutnya disaring, filtrat yang diperoleh diuapkan melalui rotarievaporator. Residu yang diperoleh dianalisis melalui kromatografi lapis tipis selanjutnya dimurnikan melalui kromatogafi kolom dengan menggunakan adsorben alumina 60 G dan eluen benzena. Hasil pemurnian yang diperoleh tersebut dianalisis melalui spektroskopi FT-IR dan 1
Helmina Br. Sembiring JURNAL PENELITIAN MIPA Volume 1, Nomor 1 Desember 2007
35
Pengukuran Tegangan Permukaan dan Penentuan Nilai HLB Galaktosa dan tert-Butil
Galaktosida
Galaktosa dilarutkan dengan akuades dalam labu takar dengan kadar 1%. Kemudian larutan induk ini diencerkan menjadi 0,00001%; 0,00005%; 0,0001%; 0,0003%; 0,0005%; 0,0008%;0,001%; 0,003%; 0,005%; 0,007%; 0,01%; 0,02%; 0,03%; 0,04%; 0,05%; 0,06%; 0,1% dan 0,5%. Alat Du Nuoy Tensiometer dikalibrasi pada suhu 30 ºC dengan akuades (tegangan permukaan air sebesar 71,06 dyne/cm (Gennaro, 1990). Sedangkan tegangan permukaan air hasil kalibrasi sebesar 80,80 dyne/cm. Kemudian diukur tegangan permukaan masing-masing konsentrasi larutan di atas. Selanjutnya ditetapkan tegangan permukaan dengan penggunaan faktor koreksi. Masukkan harga-harga tegangan permukaan (dyne/cm)-vs-log konsentrasi larutan (%). Melalui kurva diperoleh nilai KKM galaktosa. Selanjutnya dari nilai KKM dapat dihitung nilai HLB dengan menggunakan persamaan berikut:
Prosedur yang sama dilakukan juga terhadap surfaktan tert-butil galaktosida.
HASIL DAN PEMBAHASAN
Asetalisasi sebanyak 9 g galaktosa dengan 50 ml tert-butanol dalam pelarut petroleum eter, dan katalis p-TSA dengan pengadukan selama dua jam pada suhu 50–60oC dan direfluks hingga bebas air, dapat dihasilkan tert-butil galaktosida sebanyak 6 g (50,8%). Mekanisme reaksi yang terjadi diperkirakan sebagai berikut:
Hasil analisis spektroskopi FT-IR tert-butil galaktosida memberikan puncak-puncak serapan pada daerah bilangan gelombang 3373, 2974, 2939, 2875, 1471, 1365, 1201, dan 750 cm. Selanjutnya dari analisis spektroskopi 1H-NMR, memberikan puncak-puncak geseran kimia pada daerah 1,7 ppm; 3,8 ppm; 4,3 ppm; dan 7,8ppm.
Pengukuran tegangan permukaan galaktosa dan tert-butil galaktosida dilakukan dengan menggunakan tensiometer cincin Du Nuoy dengan konsentrasi yang bervariasi (Tabel 1).
Helmina Br. Sembiring JURNAL PENELITIAN MIPA Volume 1, Nomor 1 Desember 2007
36
Table 1. Data hasil pengukuran Tegangan Permukaan (γ) dari Galaktosa dan tert-butil galaktosida
γ Terbaca (dyne/cm) γ Setelah Koreksi No. Konsentrasi Larutan
dalam Air (%)
Logaritma
Konsentrasi Galaktosa tert-butil
Galaktosida Galaktosa
tert-butil Galaktosida
1. 0,000010 -5,0 77,6 73,8 67,51 64,20
2. 0,000050 -4,3 74,3 70,8 64,64 61,59
3. 0,000100 -4,0 73,1 69,4 63,60 60,37
4. 0,000200 -3,69 72,1 67,5 62,72 58,72
5. 0,000300 -3,52 70,6 66,3 61,42 57,68
6. 0,000500 -3,30 69,8 65,3 60,72 56,81
7. 0.000800 -3,09 68,7 64,3 59,76 55,94
8. 0,002000 -2,69 66,9 63,5 58,20 55,24
9. 0,003000 -2,53 65,8 62,4 57,24 54,28
10. 0,005000 -2,52 65,4 61,6 56,90 53,58
11. 0,007000 -2,30 65,1 60,5 56,60 52,63
12. 0,010000 -2,15 64,6 75,5 56,20 50,02
13. 0,020000 -2,00 61,6 57,5 53,60 50,02
14. 0,030000 -1,69 58,9 57,5 51,24 50,02
15. 0,040000 -1,52 58,9 57,5 51,24 50,02
16. 0,050000 -1,30 58,9 57,5 51,24 50,02
17. 0,060000 -1,22 58,9 57,5 51,24 50,02
18. 0,100000 -1,00 58,9 57,5 51,24 50,02
19. 0,500000 -0,30 58,9 57,5 51,24 50,02
Faktor Koreksi 0,87
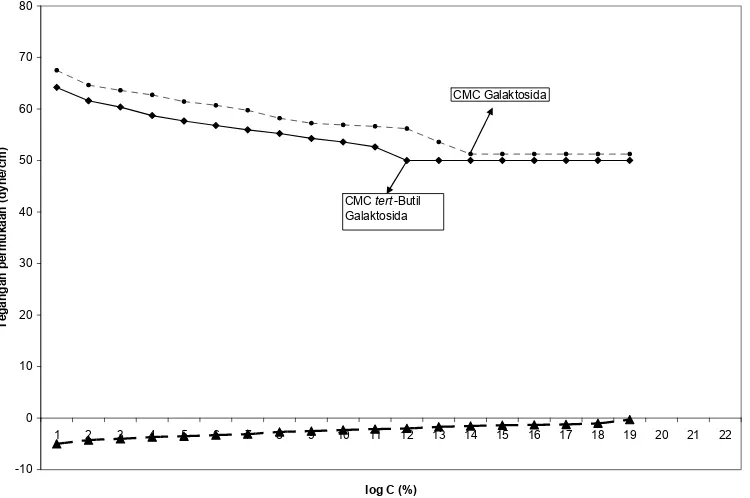
Hasil pengukuran ini diplotkan dengan konsentrasi sehingga diperoleh grafik tegangan permukaan - vs - log C.
Dari grafik ini dapat dilihat tegngan permukaan menurun sejalan dengan naiknya konsentrasi larutan galaktosa maupun larutan tert
-butil galaktosida dalam air. Akhirnya menjadi konstan walapun konsentrasi senyawa tersebut dinaikkan (Deorge,R.F.,1982). Hal ini disebabkan karena galaktosa maupun tert-butil galaktosida beragregasi membentuk misel. Konsentrasi di mana misel terbentuk disebut konsentrasi kritis misel (KKM).
-10 0 10 20 30 40 50 60 70 80
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22
log C (%)
T
e
g
a
n
g
a
n
p
e
rm
u
k
a
a
n
(d
y
n
e
/c
m
)
CMC Galaktosida
CMC tert-Butil Galaktosida
Helmina Br. Sembiring JURNAL PENELITIAN MIPA Volume 1, Nomor 1 Desember 2007
37 Dari Gambar 1 dapat dilihat nilai KKM
galaktosa sebesar 0,03%, yang mana dapat menurunkan tegangan permukaan hingga 51,24 dyne/cm. Sedangkan tegangan permukaan air sebesar 71,06 dyne/cm pada suhu 30oC. Dari harga KKM tersebut maka dapat diperoleh harga HLB sebesar 4,07. Sedangkan KKM untuk tert-butil galaktosida sebesar 0,02 yang mana dapat menurunkan tegangan permukaan air sebesar 50,02 dyne/cm. Dari harga KKM tersebut maka diperoleh harga HLB sebesar 3,93. Penurunan tegangan permukaan ini disebabkan karena adanya interaksi molekul-molekul air dengan galaktosa maupun dengan tert-butil galaktosida yang mengandung gugus hidrofil (gugus hidroksil) dan gugus hidrofob (gugus metilen) dari galaktosa dan tert-butil galaktosida tersebut. Dengan adanya interaksi ini maka ikatan hidrogen dari molekul air di bagian permukaan semakin lemah. Terlihat adanya perbedaan harga KKM dan harga HLB dari galaktosa dengan tert-butil galaktosida. Harga KKM dan HLB tert-butil galaktoseda lebih kecil dari pada galaktosa. Hal ini disebabkan karena lebih banyak dijumpai gugus hidrofob para tert-butil galaktosida, dan ini akan menyebabkan lebih cepat beragregasi membentuk misel. Dari harga HLB yang diperoleh tert butil galaktosida tersebut termasuk surfaktan non ionik yang berfungsi sebagai zat pengemulsi dengan sistem disfersi w/o. Terbentuknya tert-butil galaktosida dapat juga dibuktikan dari penurunan harga KKM dan harga HLB yang diperoleh dari kedua senyawa tersebut.
KESIMPULAN DAN SARAN
Kesimpulan
Dari data dan uraian di atas dapat disimpulkan bahwa:
1. Asetalisasi galaktosa dengan tert-butanol dapat terjadi secara selektif pada gugus hidroksil hemiasetal, yang dilakukan dalam suasana bebas
air dengan menggunakan katalis p-TSA menghasilkan tert-butil galaktosida sebanyak 50,8%.
2. Senyawa tert-butil galaktosida yang diperoleh ternyata mampu menurunkan tegangan permukaan dengan nilai CMC sebesar 0,02% dengan harga HLB sebesar 3,93.
Saran
Untuk mengacu kepada sekala industri, penerapan reaksi asetalisasi dalam pembuatan surfaktan tert-butil galaktosida, masih memerlukan penelitian yang lebih lanjut mengenai kondisi reaksi yang obtimum untuk mendapatkan rendemen reaksi yang lebih besar.
DAFTAR PUSTAKA
Belitz, H.D., 1986, ”Food Chemisry”, Springer-Perlag, Jerman, Hal. 347-349.
Brahmana, H.R., et al.,1993, “Sintesa Ester Sukrosa Asam Lemak dari Beberapa Minyak yang Dapat Dimakan Sebagai Pengemulsi dalam Bahan Makanan dan Kosmetik”, Lembaga Penelitian USU, Medan.
Deorge R.F., 1992, “Buku Teks Wilson dan Gisvold Kimia Farmasi dan Medisinal Organik”, Edisi ke-8, Bagian I, Philadelphia, Toronto.
Fesenden, R.J. dan Fesenden, J.S., 1994, “Kimia Organik”, Edisi ke-3, Erlangga.
Genaro, R.A., 1990, “Remington’s Pharmaceutical Science”, 18th Ed., Marck Publishing Company, Easton, Pensilvania.
Kirk,O., et al., 1998, “Preparation and Properties or a New Type of – Base Cationic Surfactants”,
J.Sur.& Det.,1,1, 37 – 40.
Martin, A., et al., 1993, “Farmasi Fisik”, Edisi ke-3, Jilid 2, UI-Press, Hal.922 – 944.