KETAMINE DAN PROPOFOL MENGGUNAKAN
METODE GRAVIMETRIK PADA ANJING
I GUSTI NGURAH SUDISMA
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
Saya menyatakan dengan sebenar-benarnya bahwa segala pernyataan dalam disertasi saya yang berjudul :
“Keterpilihan dan Kebakuan Dosis Anestesi Ketamine dan Propofol Menggunakan Metode Gravimetrik pada Anjing”.
adalah gagasan atau hasil penelitian saya sendiri dengan bimbingan dari komisi pembimbing, kecuali yang dengan jelas ditunjukkan rujukannya. Disertasi ini belum pernah diajukan untuk memperoleh gelar apapun di perguruan tinggi lain. Semua data dan informasi yang digunakan telah dinyatakan secara jelas dan dapat diperiksa kebenarannya.
Bogor, September 2011 Yang membuat pernyataan,
anaesthetic doses of ketamine and propofol in dogs by a gravimetric method. Under the supervision of Setyo Widodo,Dondin Sajuthi, and Harry Soehartono.
Inhalation anaesthetic agents have been used worldwide for anaesthesia in animals with improving safety and efficacy, but these agents are expensive, difficult or impossible to use for bronchoscopies and laryngoscopies, more over, these may couse organ toxicity, have an operating theatre pollution on personnel, and possible environmental damage caused by nitrous oxide and the halogenated volatile anaesthetics. A suitable alternative methode to compare with and reduce those side effects of inhalation anaesthesia agents is needed.
The aim of this study was to evaluate quality of anaesthesia by gravimetric infusion anaesthesia with ketamine HCl and propofol to get a standard dose of ketamine HCl and propofol in dogs. The quality of anaesthesia, duration of actions, and the physiological response of anaesthesia were evaluated in two steps of the study. In the first step, twenty four male domestic dogs were used in this experiment and divided randomly into six groups. In the second step, twenty male domestic dogs were used and divided randomly into five groups.
In the first step, group 1, group 2, and group 3 were preanaestheted intramuscularly with 0.03 mg/kg BW atropine and 2 mg/kgBW xylazine respectively. Group 4 to 6 received in the same way 0.03 mg/kgBW atropine and 0.2 mg/kgBW midazolam respectively. Group 1 and 4 were induced then with 4 mg/kgBW ketamine HCl, group 2 and 5 with 4 mg/kgBW propofol, and group 3 and 6 were induced with a combination dose of 4 mg/kgBW ketamine HCl and propofol respectively. The quality of anaesthesia, duration of action and the physiological responses were evaluated. From the first step, group 3 was elected the best premedication for the second step.
In the second step, all group received 0.03 mg/kgBW atropine sulfate and 2 mg/kgBW xylazine intramuscularly and were then induced intravenously with 4 mg/kgBW Ketamine HCl and propofol respectively. Following the anaesthesia, group I, II, III in second step received intravenous infusion of mixed ketamine HCl and propofol in saline by a gravimetric method to maintain the anaesthesia status. The doses of mixture were arranged at the rate of 0.2, 0.4, and 0.6 mg/kgBW/ minute respectively. Group IV was only infused with 0.4mg/kgBW/minute propofol in saline and compared to the inhalation anaesthesia, and group V was given isoflurane of 1.0 – 2.0 %. The quality of
anaesthesia, duration of action, heart rate (HR), capillary refill time (CRT), noninvasive
blood pressure (NIBP), electrocardiogram (ECG), respiratory rate (RR), blood oxygen
saturation (SpO2), end tidal CO2 (ET CO2), and rectal temperature (RT) were measured.
All groups showed rapid and smooth inductions, prolonged surgical stage, and rapid recovery. Animals of groups I and II yielded minimal physiological effects. The HR, RR, ET CO2, SpO2, CRT, NIBP, RT, and ECG wave were relatively stable. The combination
of group III showed SpO2 depression, and an increase in instability of HR, RR and ET
CO2. Group IV showed a decrease in HR, SpO2 and respiratory depression. All
combinations showed no significant influence (P>0,05) on the electrocardiogram. The combination of ketamine HCl-propofol at the dose rates of 0.2 and 0.4 mg/kgBW/minute was an ideal dose of gravimetric method of infusion.
I GUSTI NGURAH SUDISMA. Keterpilihan dan kebakuan dosis anestesi ketamine dan propofol menggunakan metode gravimetrik pada anjing. Dibimbing oleh Setyo Widodo,Dondin Sajuthi, dan Harry Soehartono.
Anestesi umum mempunyai resiko jauh lebih besar daripada prosedur pembedahan yang dijalankan, untuk itu diperlukan pemilihan anestetikum yang aman dan ideal. Anestesi inhalasi digunakan sebagai pilihan anestesi yang cukup aman saat ini, tetapi peralatannya rumit dan mahal, tidak mungkin diterapkan pada prosedur bronkoskopi dan laringoskopi, sulit digunakan untuk penanganan pasien di lapangan, menyebabkan keracunan organ, menyebabkan polusi ruangan bedah, dan menyebabkan kerusakan lapisan ozon. Suatu metode alternatif yang aman dibandingkan terhadap efek-efek samping anestesi inhalasi sangat diperlukan.
Penelitian ini bertujuan untuk mendapatkan keterpilihan dan kebakuan dosis anestesi kombinasi ketamine HCl dengan propofol secara infusi gravimetrik pada anjing. Dua puluh empat anjing jantan domestik dibagi enam kelompok perlakuan dan masing-masing empat ekor sebagai ulangan digunakan pada penelitian tahap pertama. Penelitian tahap kedua menggunakan 20 ekor anjing jantan domestik dibagi lima kelompok perlakuan masing-masing empat ekor sebagai ulangan.
Penelitian tahap pertama, grup 1, 2, dan grup 3 dipreanestesi dengan atropine sulfate 0,03 mg/kgBB dan xylazine HCl 2 mg/kgBB secara intramuskuler. Grup 4 sampai 6 dipreanestesi dengan atropine sulfate 0,03 mg/kgBB dan midazolam 0,2 mg/kgBB secara intramuskuler. Grup 1 dan 4 diinduksi secara intravena dengan ketamine HCl 4 mg/kg BB, Grup 2 dan 5 diinduksi secara intravena dengan propofol 4 mg/kg BB, dan Grup 3 dan 6 diinduksi secara intravena dengan kombinasi ketamine HCl 4 mg/kg BB dan propofol 4 mg/kg BB. Dilakukan evaluasi terhadap kualitas anestesi, durasi, dan respon fisiologis. Diperoleh bahwa Grup 3 adalah perlakuan terpilih sebagai preanestesi dan induksi terbaik untuk penelitian tahap kedua.
Penelitian tahap kedua, semua perlakuan dipreanestesi atropine sulfate 0,03 g/kgBB dan xylazine HCl 2 mg/kgBB secara intramuskuler, setelah 10 menit diinduksi intravena dengan ketamine HCl dan propofol dosis 4 mg/kg BB, dan 15 menit kemudian diinfusi secara gravimetrik dengan campuran ketamine HCl 2mg/ml dan propofol 2mg/ml dalam cairan infusi NaCl 0,9% sampai menit ke-120. Dilakukan infusi ketamine HCl-propofol dosis 0,2 mg/kg/menit, 0,4 dan dosis 0,6 mg/kg/menit masing-masing pada grup I, II, dan III. grup IV diinfusi hanya dengan propofol 0,4 mg/kg/menit, serta grup V dianestesi dengan isofluran 1,0 – 2,0%. Sebelum dan selama hewan teranestesi dilakukan pemeriksaan terhadap kualitas anestesi, durasi, frekuensi denyut jantung, capillary refill time (CRT), noninvasive blood pressure (NIBP), elektrokardiogram (EKG), frekuensi respirasi, end tidal CO2 (ET CO2), dan saturasi oksigen (Sp O2
Penelitian tahap pertama menunjukkan bahwa kombinasi preanestesi atropine sulfate–xylazine HCl (0,03 & 2 mg/kgBB) secara intramuskuler, setelah 10 menit diinduksi intravena dengan ketamine HCl-propofol (@ 4 mg/kg BB, memberikan kualitas anestesi yang baik dan aman sehingga dapat digunakan untuk preanestesi dan induksi anestesi pada anjing. Penelitian tahap kedua
jantung, respirasi, ET CO2, Sp O2, nilai CRT, NIBP, suhu tubuh, dan EKG.
Sedangkan grup III menunjukkan penurunan tajam terhadap Sp O2 dan
peningkatan tidak stabil terhadap denyut jantung, respirasi, serta ET CO2.
Pemeliharaan status teranestesi pada grup IV menyebabkan tertekannya respirasi, Sp O2, dan penurunan denyut jantung. Keseluruhan kombinasi perlakuan
anestetika tidak mempengaruhi gambaran listrik jantung. Penelitian ini menunjukkan kombinasi ketamine HCl-propofol dosis 0,2-0,4 mg/kg/menit secara infusi gravimetrik menghasilkan kualitas anestesi yang baik dan dapat digunakan untuk pemeliharan status teranestesi sebagai kebakuan dosis anestesi pada anjing.
©Hak Cipta milik IPB, tahun 2011
Hak Cipta dilindungi Undang-Undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebut sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah.
b. Pengutipan tidak merugikan kepentingan yang wajar IPB.
KETAMINE DAN PROPOFOL MENGGUNAKAN
METODE GRAVIMETRIK PADA ANJING
I GUSTI NGURAH SUDISMA
Disertasi
sebagai salah satu syarat untuk memperoleh gelar Doktor pada
Program Mayor Ilmu Biomedis Hewan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Penguji Luar Komisi Ujian Tertutup :
1. Dr. dra. Hj. Ietje Wientarsih, Apt., MSc.
2. drh. Deni Noviana, PhD.
Penguji Luar Komisi Ujian Terbuka :
1. Dr. dr. Bambang Joewono Oetoro, Sp.An (KNA) (Dokter Spesialis Anestesi, Konsultan Neuroanestesi Brawijaya Women & Children Hospital, Tahir Neurosience, Sahid Sahirman Memorial Hospital, Jakarta).
2. Dr. Nastiti Kusumorini
Nama : I Gusti Ngurah Sudisma NIM : B361070011
Mayor : Ilmu Biomedis Hewan (IBH)
Disetujui
Komisi Pembimbing
Ketua
Dr. drh. Setyo Widodo
Prof. drh. Dondin Sajuthi, M.S.T., Ph.D.
Anggota Anggota
drh. R. Harry Soehartono, MApp Sc., Ph.D.
Diketahui
Ketua Program Mayor Dekan Sekolah Pascasarjana Ilmu Biomedis Hewan, Institut Pertanian Bogor,
drh. Agus Setiyono, MS., Ph.D., AP Vet Dr. Ir. Dahrul Syah, M.Sc.Agr
Puji dan syukur penulis panjatkan kehadirat Tuhan Yang Maha Esa atas
berkatNya penulis dapat menyelesaikan disertasi yang berjudul “Keterpilihan dan
Kebakuan Dosis Anestesi Ketamine dan Propofol menggunakan Metode
Gravimetrik pada Anjing”.
Ucapan terima kasih penulis sampaikan kepada Dr. drh. Setyo Widodo
selaku ketua komisi pembimbing, Prof. drh. Dondin Sajuthi, M.S.T., Ph.D. dan drh.
R. Harry Soehartono, MApp Sc., Ph.D. selaku anggota komisi pembimbing yang
telah banyak memberi saran, nasihat, pengarahan dan pembimbingan yang tulus dan
penuh kesabaran. Penghargaan yang dalam penulis sampaikan kepada Direktur
Jendral Pendidikan Tinggi, Rektor Universitas Udayana, Dekan FKH Universitas
Udayana, Rektor Institut Pertanian Bogor, Dekan Sekolah Pascasarjana IPB, Ketua
Program Mayor IBH Pascasarjana IPB , Direktur Rumah Sakit Hewan IPB, Ketua
Departemen KRP FKH IPB, Ketua Departemen AFF FKH IPB, yang telah
membantu fasilitas dan pelayanan selama studi dan penelitian. Penulis juga
menyampaikan terima kasih kepada rekan mahasiswa pascasarjana IPB dan
teman-teman dalam suka-duka di Asrama Bali Bogor atas dukungan yang tulus dan
kerjasamanya yang penuh kekeluargaan.
Dengan rasa cinta kasih penulis sampaikan terima kasih yang tulus kepada
istri tercinta dr. Ni Gusti Ayu Ketut Widiastiti serta anak tersayang I Gusti Ayu
Dewi Sawitri, I Gusti Ngurah Bagus Nala Purusatama, dan I Gusti Ngurah Bagus
Aryha Wirasha atas kesabaran, dorongan semangat dan pengorbanan selama masa
studi. Kepada kedua orangtua ayah dan ibu, kedua mertua, serta seluruh keluarga
penulis sampaikan terimakasih atas segala pengorbanan, pengertian dan doa yang
tidak pernah putus.
Penulis menyadari bahwa tulisan ini masih jauh dari sempurna, oleh karena
itu segala kritik dan saran yang bersifat membangun sangat penulis harapkan.
Akhirnya penulis berharap semoga tulisan ini bermanfaat.
Bogor, September 2011
i
KATA PENGANTAR
Puji dan syukur penulis panjatkan kehadhirat Tuhan Yang Maha Esa yang
telah melimpahkan segala karuniaNya, sehingga penulisan disertasi ini dapat
diselesaikan. Penulisan disertasi ini berjudul “Keterpilihan dan kebakuan dosis
anestesi campuran ketamine dan propofol menggunakan metode gravimetrik pada
anjing”, diajukan untuk memenuhi syarat memperoleh gelar Doktor (S3) pada
Program Doktor (S3) Mayor Ilmu Biomedis Hewan (IBH) Program Pascasarjana
Institut Pertanian Bogor.
Penelitian disertasi ini dirancang untuk mengetahui kualitas, efektivitas,
dan keamanan pemeliharaan status teranestesi secara infusi gravimetrik dengan
kombinasi ketamine dan propofol pada anjing. Hasil penelitian ini juga
diharapkan mendapatkan keterpilihan dan kebakuan kombinasi dan dosis
ketamine-propofol sebagai agen anestesi secara infusi gravimetrik pada anjing.
Dengan demikian, pemeliharaan status teranestesi dengan kombinasi ketamine
dan propofol secara infusi gravimetrik diharapkan menghasilkan potensi anestesi
umum yang baik dan aman. Kombinasi ketamine dan propofol diharapkan dapat
menciptakan kondisi sedasi, analgesi, dan relaksasi yang oftimal serta adequat
untuk dilakukan tindakan atau prosedur diagnostik maupun terapeutik tanpa
menimbulkan gangguan hemodinamik, respiratorik, dan metabolik yang dapat
mengancam.
Penulisan disertasi ini telah mendapat masukan dan pengujian oleh dra. Hj.
Ietje Wientarsih, Apt., MSc. dalam bidang Farmasi, drh. Deni Noviana, Ph.D
dalam bidang Bedah, Dr. dr. Bambang Joewono Oetoro, Sp.An (KNA) dalam
bidang Anestesi dan oleh Dr. Nastiti Kusumorini dalam bidang
Neuro-Fisiologi.
Penulis menyadari bahwa penulisan dan isi disertasi ini sudah tentu sangat
jauh disebut sempurna, untuk itu penulis sangat mengharapkan saran dan masukan
serta kritik demi kesempurnaannya.
Bogor, September 2011
ii
RIWAYAT HIDUP
I Gusti Ngurah Sudisma, dilahirkan di Badung Bali pada tanggal 30
Januari 1969, merupakan putra pertama dari tiga bersaudara, pasangan dari
Ayahanda I Gusti Ngurah Made Arta dan Ibunda I Gusti Ayu Martini. Menikah
dengan dr. Ni Gusti Ayu Ketut Widiastiti dan telah dikaruniai satu orang putri
I Gusti Ayu Dewi Sawitri (12 tahun), dua orang putra I Gusti Ngurah Bagus Nala
Purusatama (4 tahun) dan I Gusti Ngurah Bagus Aryha Wirasha (2 tahun).
Pendidikan Sekolah Dasar (SD), Sekolah Menengah Pertama (SMP), dan
Sekolah Menengah Atas (SMA) penulis tempuh di Bali. Pada tahun 1988 penulis
diterima di Program Studi Kedokteran Hewan (PSKH) Universitas Udayana lewat
jalur Penelusuran Minat dan Kemampuan (PMDK), tahun 1992 penulis berhasil
memperoleh gelar Sarjana Kedokteran Hewan (Drs.Med.Vet) dan ditempat yang
sama penulis meraih gelar Dokter Hewan (drh) pada tahun 1994. Sejak tahun
1997 penulis dianggkat menjadi staf dosen (PNS) di FKH Universitas Udayana
Bali. Pada akhir tahun 2002, penulis mendapat kesempatan melanjutkan
pendidikan jenjang Magister (S-2) di Program Studi Sains Veteriner (SVT)
Program Pascasarjana Institut Pertanian Bogor, tahun 2004 memperoleh gelar
Magister (M.Si.). Pada akhir tahun 2007 penulis mendapat kesempatan
melanjutkan pendidikan jenjang Doktor (S-3) di Program Mayor Ilmu Biomedis
Hewan (IBH) Sekolah Pascasarjana Institut Pertanian Bogor, lewat jalur Beasiswa
Pendidikan Pascasarjana (BPPS) dari Direktorat Jenderal Pendidikan Tinggi
Departemen Pendidikan Nasional.
Bogor, September 2011
iii
Tinjauan Anestetikum Umum. ...………...……….... 29
Ketamine HCl. ...………..……... 29
Propofol. ... 31
Xylazine ………...………... 34
Midazolam. ………...………... 36
Atropine ……….………...………... 39
Perubahan Aspek Fisiologi dalam Anestesi ..………..…..…. 40
Sistem Kardiovaskuler. ………...……….. 41
Capillary Refill Time (CRT). ………... 45
Klasifikasi Status Pasien. ... 54
Pemantauan Anestesi. ... 55
MATERI DAN METODE PENELITIAN ………....…... 57
Waktu dan Tempat Penelitian. ... 57
Materi Penelitian……..…….…....………... 57
Metode Penelitian ……….………... 61
iv
Gambaran Darah. …...……….……… 68
Protokol dan Pelaksanaan Penelitian. ……….…....……….. 69
Rancangan Penelitian dan Analisis Statistik. ... 69
HASIL DAN PEMBAHASAN. ... 71
Penelitian Pendahuluan. ...….………... 71
Penelitian Tahap Pertama. …….………... 72
Waktu Anestesi. .………... 73
Penelitian Tahap Kedua. ...….………... 108
Waktu Anestesi. .………... 108
KESIMPULAN DAN SARAN. ...………... 145
Kesimpulan. ...…...………... 145
Saran. ... 146
DAFTAR PUSTAKA. ... 147
v
DAFTAR TABEL
No Teks Hal
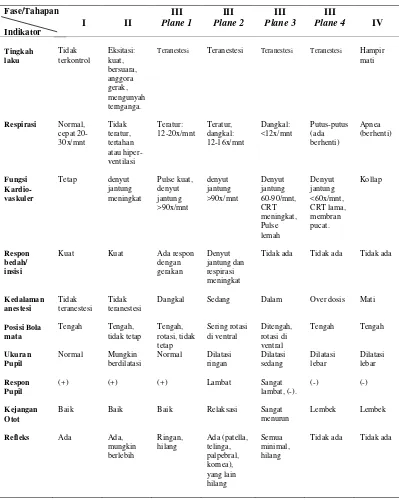
1. Tahapan dan indikasi status teranestesi oleh anestetikum umum. ... 22
2. Perubahan fisiologi yang diperiksa selama periode anestesi ... 40
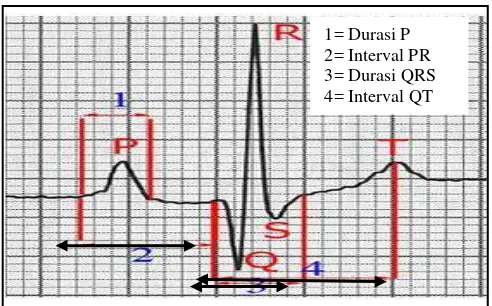
3. Kriteria elektrokardiogram (EKG) dan tekanan darah normal pada anjing... 44
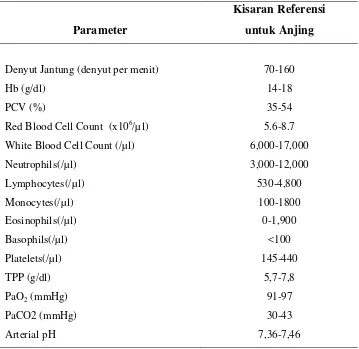
4. Kriteria normal pemeriksaan darah pada anjing... 48
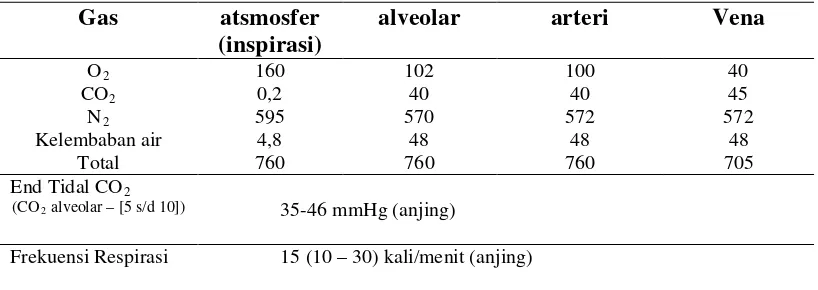
5. Tekanan gas respirasi dan gas darah normal pada anjing (mmHg)... 49
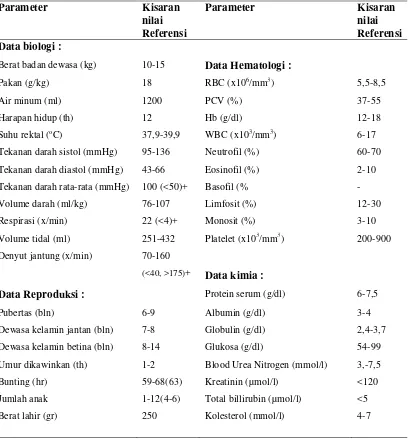
6. Data fisiologi anjing... 53
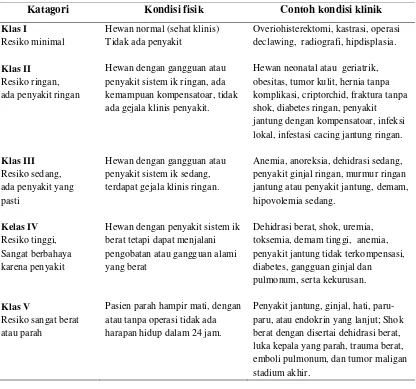
7. Klasifikasi status pasien pada prosedur anestesi ... 54
8. Data hasil edaran kuesioner kepada Dokter Hewan Praktek di Jawa dan Bali dengan responden 87 tempat praktek Dokter Hewan dari 110 kuesioner yang diedarkan (79%). ………... 72
9. Nilai rata-rata ± simpangan baku (rata-rata ± SD) waktu induksi, durasi, dan waktu pemulihan selama perlakuan preanestesi dan induksi anestesi pada anjing. …… 74
10. Nilai rata-rata ± simpangan baku (rata-rata ± SD) denyut jantung, frekuensi respirasi, suhu rektal dan nilai saturasi O2 selama preanestesi dan induksi anestesi pada anjing. ... 82
11. Nilai rata-rata ± simpangan baku (rata-rata ± SD) tekanan darah tidak langsung (NIBP : SAP, DAP, MAP) dan CO2 respirasi selama perlakuan preanestesi dan induksi anestesi pada anjing.……….……… 95
12. Nilai rata-rata ± simpangan baku (rata-rata ± SD) elektrokardiogram (EKG) sadapan II gelombang P dan gelombang R selama perlakuan preanestesi dan induksi anestesi pada anjing……….. 98
13. Nilai rata-rata ± simpangan baku (rata-rata ± SD) elektrokardiogram (EKG) sadapan II interval PR, komplek QRS, interval QT) dan nilai CRT selama perlakuan preanestesi dan induksi anestesi pada anjing……….. 101
14. Nilai rata-rata ± simpangan baku (rata-rata ± SD) waktu induksi, durasi, sadar, dan waktu pemulihan selama pemberian induksi atropine-xylazine-ketamine-propofol dan pemeliharaan anestesi secara infusi gravimetrik dengan ketamine dan propofol pada anjing. ……….. 109
15. Nilai rata-rata ± simpangan baku (rata-rata ± SD) denyut jantung, frekuensi respirasi, suhu rektal dan nilai saturasi O2 selama pemberian induksi atropine-xylazine-ketamine-propofol dan pemeliharaan anestesi secara infusi gravimetrik dengan ketamine dan propofol pada anjing. ……….. 116
16. Nilai rata-rata ± simpangan baku (rata-rata ± SD) tekanan darah tidak langsung (NIBP : SAP, DAP, MAP) dan CO2 respirasi selama pemberian induksi atropine-xylazine-ketamine-propofol dan pemeliharaan anestesi secara infusi gravimetrik dengan ketamine dan propofol pada anjing. ……….. 123
vi
18. Nilai rata-rata ± simpangan baku (rata-rata±SD) elektrokardiogram (EKG) sadapan
II interval PR, komplek QRS, interval QT) dan nilai CRT selama pemberian induksi atropine-xylazine-ketamine-propofol dan pemeliharaan anestesi secara
infusi gravimetrik dengan ketamine dan propofol pada anjing. ………..………….. 135
19. Nilai rata-rata indeks eritrosit darah selama pemberian induksi atropin-xilazin-ketamin-propofol dan pemeliharaan anestesi secara infus gravimetrik dengan ketamin dan propofol pada anjing. ………. 138
20. Nilai rata-rata jumlah sel darah putih , diferensial leukosit, dan kimia darah selama pemberian induksi atropin-xilazin-ketamin-propofol dan pemeliharaan anestesi secara infus gravimetrik dengan ketamin dan
vii
DAFTAR GAMBAR
No Teks Hal
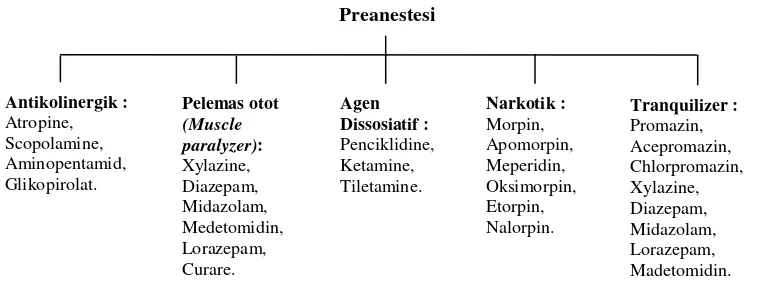
1. Klasifikasi agen preanestesi yang digunakan pada anestesi umum. ... 10
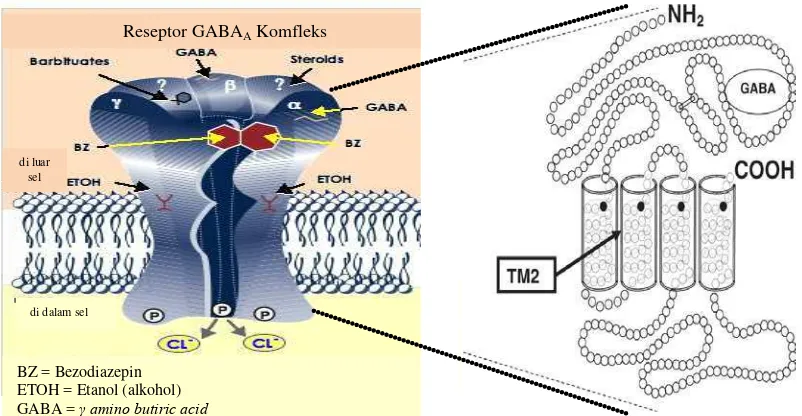
2. Reseptor GABAA terdiri dari lima subtipe (pentamer) 2α, βß, dan 1 , masing masing subtipe mempunyai N-terminal binding site, terdiri dari 450 asam amino, 4-transmembran (TM) sebagai saluran ion dan tempat terikatnya anestetika. ... 25
3. Skema reseptor N-methyl D-aspartat (NMDA) komfleks. ... 26
4. Anestesi umum bekerja dengan cara mempengaruhi aktivitas transmitter-gate ion channel dengan cara meningkatkan (+) sinyal inhibitori dan/atau menghambat (-) sinyal eksitatori neurotransmiter (Cameron JW 2006)... 27
5. Anestetika volatil (isofluran) bekerja pada reseptor GABAAsubunit α dan anestetika intravena (propofol) bekerja pada reseptor GABAAsubunit . ... 29
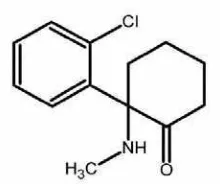
6. Struktur kimia ketamine HCl. ... 30
7. Struktur kimia propofol... 32
8. Struktur kimia xylazine HCl. ... 35
9. Struktur kimia midazolam... 37
10. Struktur kimia atropine... 39
11. Diagram gambaran gelombang elektrokardiogram (EKG)... 44
12. Diagram alir penelitian tahap pertama pada anjing... 59
13. Diagram alir penelitian tahap kedua pada anjing... 61
14. Perubahan rata-rata denyut jantung selama perlakuan kombinasi preanestesi dan induksi anestesi pada anjing. …..………... 77
15. Perubahan rata-rata frekuensi respirasi selama perlakuan kombinasi preanestesi dan induksi anestesi pada anjing. ………... 79
16. Perubahan rata-rata suhu rektal selama perlakuan kombinasi preanestesi dan induksi anestesi pada anjing. ………... 83
17. Perubahan rata-rata saturasi O2 selama perlakuan kombinasi preanestesi dan induksi anestesi pada anjing . ………..…………... 85
18. Perubahan rata-rata tekanan darah sistol (SAP) selama perlakuan preanestesi dan induksi anestesi pada anjing……… 87
19. Perubahan rata-rata tekanan darah diastol (DAP) selama perlakuan preanestesi dan induksi anestesi pada anjing………... 89
20. Perubahan rata-rata tekanan darah rata-rata (MAP) selama perlakuan preanestesi dan induksi anestesi pada anjing……… 91
21. Perubahan rata-rata end tidal CO2 (ET CO2) selama perlakuan preanestesi dan induksi anestesi pada anjing………. 93
viii
23. Perubahan rata-rata frekuensi respirasi selama pemberian induksi
atropine-xylazine-ketamine-propofol dan pemeliharaan anestesi secara infusi gravimetrik
dengan ketamine dan propofol pada anjing. ………...……… 114
24. Perubahan rata-rata suhu rektal selama pemberian induksi
atropine-xylazine-ketamine-propofol dan pemeliharaan anestesi secara infusi gravimetrik dengan
ketamine dan propofol pada anjing. ……… 117
25. Perubahan rata-rata nilai saturasi O2 selama pemberian induksi
atropine-xylazine-ketamine-propofol dan pemeliharaan anestesi secara infusi gravimetrik dengan
ketamine dan propofol pada anjing. ………..…...………... 119
26. Perubahan rata-rata tekanan darah sistol (SAP) selama pemberian induksi
atropine-xylazine-ketamine-propofol dan pemeliharaan anestesi secara infusi gravimetrik
dengan ketamine dan propofol pada anjing. ……….…. 121
27. Perubahan rata-rata tekanan darah diastol (DAP) selama pemberian induksi
atropine-xylazine-ketamine-propofol dan pemeliharaan anestesi secara infusi
gravimetrik dengan ketamine dan propofol pada anjing. ……….…….. 124
28. Perubahan rata-rata tekanan darah rata-rata (MAP) selama pemberian induksi
atropine-xylazine-ketamine-propofol dan pemeliharaan anestesi secara infusi
gravimetrik dengan ketamine dan propofol pada anjing. ……….…………. 126
29. Perubahan rata-rata end tidal CO2 (ET CO2) selama pemberian induksi
atropine-xylazine-ketamine-propofol dan pemeliharaan anestesi secara infusi gravimetrik
dengan ketamine dan propofol pada anjing. ……….…. 128
30. Perubahan rata-rata nilai CRT selama pemberian induksi
atropine-xylazine-ketamine-propofol dan pemeliharaan anestesi secara infusi gravimetrik dengan
ix
DAFTAR LAMPIRAN
No Teks Hal
1. Contoh cara pembuatan campuran Ketamine-Propofol sebanyak 100 ml ….. 153
2. Nilai rata-rata ± simpangan baku (rata-rata±SD) darah dan kimia darah selama pemberian induksi atropine-xylazine-ketamine-propofol dan pemeliharaan anestesi secara infusi gravimetrik dengan ketamine dan
PENDAHULUAN
Latar Belakang
Anestesi merupakan tahapan yang sangat penting dan strategis pada tindakan
pembedahan, karena pembedahan tidak dapat dilakukan bila belum dilaksanakan
anestesi. Sejarah membuktikan bahwa ilmu bedah mengalami revolusi pesat setelah
ditemukan eter sebagai anestesi umum. Sebelum ditemukan anestesi, tindakan
pembedahan tidak dapat dilakukan dengan baik dan ilmu bedah tidak mengalami
perkembangan. Setelah Thomas Green Morton melakukan demonstrasi menggunakan
eter sebagai anestesi umum untuk pembedahan tumor leher di rumah Sakit Umum
Massachusetts pada 16 Oktober 1846, penanganan pasien dengan tindakan
pembedahan dapat dilakukan dengan baik dan ilmu bedah berkembang sangat pesat.
Anestesi umum adalah tahapan yang sangat penting dan mempunyai resiko
jauh lebih besar dari prosedur pembedahan, karena anestesi yang dalam akan
mengancam nyawa pasien. Pemberian agen anestetikum yang kurang atau tidak
mencukupi menyebabkan pasien akan tetap merasakan sakit, tetapi apabila dosis
anestetikum yang diberikan dalam keadaan cukup atau berlebihan akan dapat
mengancam terjadinya kematian. Guna mencegah dua kejadian yang ekstrim tersebut,
harus dilakukan pemilihan anestetikum yang memenuhi kriteria ideal, yaitu
anestetikum yang menghasilkan sedasi, analgesi, relaksasi, ketidaksadaran, dan aman
untuk sitem vital, serta mudah diaplikasikan (Fossum 1997; Miller 2010).
Anestesi umum yang dinyatakan cukup aman dan sering digunakan untuk
anjing adalah anestesi inhalasi, tetapi anestesi inhalasi memerlukan perangkat yang
rumit, mahal, dan tidak praktis untuk menangani kasus pembedahan di lapangan.
Anestesi inhalasi tidak dapat digunakan untuk penanganan presedur bronkoskopi dan
laringoskopi, serta menyebabkan polusi terhadap individu yang berada di ruangan
operasi. Anestesi inhalasi, seperti gas nitrogen oksida dan anestesi yang diuapkan
dengan halogen mengakibatkan pencemaran lingkungan dan penipisan lapisan ozon
Data penggunaan anestesi pada praktek kedokteran hewan di Indonesia
menunjukkan bahwa penggunaan anestesi inhalasi hanya 10,5%, anestesi injeksi
81%, dan anestesi gabungan 8,5%. Penanganan pasien dengan melakukan
pembedahan diluar ruangan operasi (eksitu) cukup besar, yaitu 43%. Anestetika yang
paling banyak digunakan adalah injeksi kombinasi ketamine-xylazine. Kombinasi ini
menghasilkan anestesi tidak stabil, memerlukan pengulangan pemberian, pemulihan
lama, mempunyai efek samping kejang dan muntah. Dengan demikan proses
pembedahan menjadi terganggu.
Mengatasi kelemahan anestesi inhalasi dan untuk mengatasi permasalahan
penggunaaan anestesi di lapangan, digunakan metode anestesi intravena total (total
intraveous anesthesia, TIVA). Anestesi intravena total menggunakan anestetika
secara intravena (IV) untuk induksi dan pemeliharaan anestesi. Penggunaan mesin
pompa infusi dengan komputer pada metode TIVA menghasilkan jumlah infusi yang
stabil dan akurat. Metode TIVA mirip dengan penggunaan alat penguap (vaporizer)
pada anestesi inhalasi sehingga anestesi menjadi lebih stabil, tetapi pompa infusi yang
digunakan masih mahal dan rumit serta tidak cocok untuk penanganan pasien di
lapangan. Metode alternatif yang lebih praktis dan paling memungkinkan adalah
metode infusi gravimetrik. Metode infusi gravimetrik menggunakan anestetikum
parenteral melalui tetes infusi intravena secara terus menerus. Anestetikum dicampur
dalam kantong cairan dan cairan anestetikum dialirkan melalui tetes infusi intravena
berdasarkan gaya gravitasi dengan dosis dan kecepatan tetes tertentu (Amadasun dan
Edomwonyi 2005).
Anestetikum parenteral yang dapat diberikan melalui tetes infusi intravena
adalah propofol (BBraun 2009). Propofol adalah agen anestetikum parenteral
generasi terbaru yang diperkenalkan pada praktek kedokteran hewan pada tahun
1990-an. Propofol merupakan substansi parenteral sebagai agen induksi pada anestesi
umum inhalasi, mempunyai waktu induksi dan pemulihan yang singkat, serta
pengeluaran dari tubuh yang cepat (Stoelting 1999; Dzikiti et al. 2007). Propofol
mempunyai molekul mirip alkohol, molekulnya akan bekerja dan berikatan pada
reseptor GABAA subtipe ß3 sehingga menyebabkan ketidaksadaran dan pada reseptor
GABAA
Mengatasi efek samping ketamine, dapat dikombinasikan dengan preanestesi
sedatif hipnotik golongan αβ-adrenoceptor seperti xylazine atau golongan benzodiazepin seperti diazepam atau midazolam. Golongan benzodiazepin
memperkuat kerja GABA yang merupakan neurotransmiter inhibitori utama pada
otak, mampu menekan refleks-refleks polisinaps dan berpengaruh terhadap medulla
spinalis (Brander et al. 1991). Midazolam bekerja pada reseptor benzidiazepin
dengan cara meningkatkan pengikatan GABA pada reseptor GABA
subtipe ß2, lebih dari setengah jumlah reseptor terdapat pada SSP, akan
menyebabkan sedasi. Propofol menghasilkan pengaruh menghilangkan kesadaran dan
pelemas otot yang baik, menyebabkan hipotensi arterial, bardikardi, depresi respirasi,
dan mengancam nyawa pasien terutama apabila diberikan secara cepat dengan dosis
yang tinggi. (Franks 2008; Miler 2010; Stawicki 2007). Pengaruh anestesi dan efek
samping propofol sangat berhubungan dengan dosis dan keuntungan penggunaaan
propofol dapat diperoleh dengan cara mengkombinasikan dengan anestetikum lain
seperti ketamine (McKelvey dan Hollingshead 2003). Ketamine mempunyai tempat
kerja yang berbeda dengan propofol. Mekanisme kerja ketamine secara antagonis
pada reseptor N-methyl-D-aspartate (NMDA), mempunyai pengaruh analgesik kuat
dan mampu meningkatkan pengaruh anestesi apabila dikombinasikan dengan
propofol untuk induksi anestesi pada manusia (Lerche et al. 2000). Ketamine dosis
rendah menghasilkan analgesik yang baik (Intelisano et al. 2008), tetapi ketamine
menyebabkan kekejangan otot dan peningkatan denyut jantung (Pathak et al.1982;
Kul et al. 2001).
A
Xylazine HCl adalah golongan alpha
, sehingga
menimbulkan penghambatan SSP, mencegah hipertonus otot, meningkatkan efek
sedasi dan hipnotik (Stawicki 2007). Midazolam lebih potensial dibandingkan
diazepam (Lumb dan Jones 1996; Muir et al. 2000).
2-adrenoceptor stimulant atau alpha-2
adrenergic receptor agonist. Xylazine bekerja melalui mekanisme yang menghambat
tonus simpatik karena xylazine mengaktivasi reseptor postsinap α2-adrenoseptor
penurunan peristaltik, relaksasi saluran cerna, dan sedasi. Xylazine menyebabkan
relaksasi otot melalui penghambatan transmisi impuls intraneural pada susunan syaraf
pusat dan dapat menyebabkan muntah. Xylazine juga dapat menekan termoregulator
(Adams 2001). Pemberian atropine sulfat secara bersamaan sebagai preanestesi, dapat
menurunkan pengaruh hipersalivasi dan bradikardi dari xylazine (Bishop 1996).
Atropine adalah agen menghambat muskarinik atau antimuskarinik dengan
mekanisme kerja secara kompetisi dengan reseptor acetilkolin. Penggunaan
kombinasi atropine sulfat, xylazine HCl atau midazolam sebagai preanestesi akan
memberikan pengaruh lebih baik terhadap anestesi serta meningkatkan potensi
anestetikum. Preanestesi juga sangat penting pada hewan untuk tujuan merestrain
sebelum dilakukan anestesi.
Penelitian ini dirancang untuk mengetahui kualitas, efektivitas, dan keamanan
pemeliharaan status teranestesi secara infusi gravimetrik dengan kombinasi ketamine
dan propofol pada anjing. Hasil penelitian ini juga diharapkan mendapatkan
keterpilihan dan kebakuan kombinasi dan dosis ketamine-propofol sebagai agen
anestesi secara infusi gravimetrik pada anjing. Dilakukan evaluasi terhadap waktu
anestesi untuk menentukan kualitas anestesi, evaluasi terhadap fungsi kardiovaskuler
dan respirasi untuk menentukan tingkat keamanan penggunaan anestesi. Evaluasi
fungsi kardiovaskuler terdiri dari frekuensi denyut jantung, tekanan darah
(noninvasive blood pressure/NIBP), capillary refill time (CRT), dan
elektrokardiogram (EKG), sedangkan evaluasi fungsi respirasi terdiri dari frekuensi
respirasi, end tidal CO2 (ET CO2), dan saturasi oksigen (Sp O2
).
Kerangka Pemikiran
Pembedahan hanya dapat dilakukan dengan baik apabila hewan telah dibius
atau dianestesi. Anestesi juga sangat diperlukan untuk membuat diagnosis dan
tindakan medis lainnya pada hewan. Banyak diagnosis, tindakan medis, dan terutama
tindakan pembedahan tidak dapat dilakukan sebelum dilakukan anestesi. Anestesi
merupakan tahapan yang sangat penting pada proses pembedahan dan penggunaan
hewan yang dianestesi serta mempunyai resiko jauh lebih besar dibanding prosedur
pembedahan yang dijalankan.
Diperlukan pemilihan anestetikum yang ideal yang memenuhi kriteria
komponen anestesi : sedasi, analgesi, relaksasi (immobilisasi), ketidaksadaran, aman
dan nyaman untuk sistem vital, ekonomis serta mudah diaplikasikan. Sampai saat ini
belum ditemukan anestesi umum yang benar-benar aman dan memenuhi kriteria
ideal. Anestesi umum inhalasi yang dipandang aman, memerlukan perangkat yang
rumit, mahal, dan mempunyai waktu induksi (onset) yang relatif lambat.
Keterbatasan anestesi inhalasi adalah tidak bisa digunakan untuk penanganan
bronkoskopi dan laringoskopi serta tidak praktis untuk menangani hewan di
lapangan.
Anestesi umum alternatif yang masih mungkin dilakukan adalah anestesi umum
parenteral. Anestesi parenteral lebih ekonomis dan praktis untuk penanganan hewan
di lapangan, tetapi menghasilkan anestesi yang tidak stabil dan sering memerlukan
pengulangan atau penambahan dosis anestesi karena waktu anestesi sudah selesai
sedangkan tindakan medis atau pembedahan belum selesai dilakukan. Pilihan anestesi
yang lebih memungkinkan adalah anestesi parenteral intravena dengan metode
anestesi intravena total (TIVA, total intraveous anesthesia). Penggunaan mesin
pompa infusi dengan komputer pada metode TIVA menghasilkan anestesi yang stabil
dan akurat, sehingga metode TIVA mirip dengan penggunaan alat penguap
(vaporizer) pada anestesi inhalasi. Pompa infusi yang digunakan pada metode TIVA
masih mahal dan rumit serta tidak cocok untuk penanganan pasien di lapangan.
Metode anestesi yang lebih praktis dan memungkinkan adalah metode infusi
gravimetrik melalui tetes intravena. Metode infusi gravimetrik menggunakan
anestetikum parenteral melalui tetes infusi intravena secara terus menerus,
anestetikum dicampur dalam kantong cairan dan cairan anestetikum dialirkan melalui
tetes infusi intravena berdasarkan gaya gravitasi dengan dosis dan kecepatan tetes
tertentu.
Ketamine HCl adalah salah satu jenis anestesi umum injeksi yang dapat
seperti anjing. Ketamine HCl adalah anestetikum disosiatif dari golongan
nonbarbiturat mempunyai sifat menghilangkan rasa sakit (analgesik) yang kuat serta
reaksi anestesinya tidak menyebabkan ngantuk (sedasi) (Pathak et al.1982; Kul et al.
2001). Ketamine menghasilkan pengaruh anestesi melalui mekanisme yang bekerja
pada reseptor N methyl D aspartate (NMDA). Ketamine diklasifikasikan sebagai
antagonis reseptor NMDA, pada daerah tempat kerja PCP. Afinitas ketamine sangat
kuat pada reseptor NMDA, sehingga menghasilkan pengaruh analgesik yang sangat
kuat (Stawicki 2007). Antagonis NMDA akan menghambat refleks nosiseptik spinal,
menghambat konduksi rasa sakit ke talamus dan daerah kortek. Penghambatan
reseptor NMDA dengan dosis ketamine yang rendah akan menghasilkan pengaruh
analgesik yang baik (Intelisano et al. 2008).
Propofol termasuk agen anestetikum intravena short acting hyptotic yang dapat
diberikan secara berulang atau secara infusi terus menerus. Propofol menghasilkan
pengaruh anestesi melalui mekanisme yang bekerja pada reseptor GABAA (Intelisano
et al. 2008). Propofol memperbesar pengaruh GABA yang mempunyai fungsi
menghambat aksi (inhibitory) sistem syaraf pusat, meningkatkan konduksi Cl- yang menyebabkan hiperpolarisasi sehingga tingkat rangsangan sel (excitability)
menurunkan, menyebabkan sedasi dan relaksasi (Mihic dan Harris 1997; Intelisano et
al. 2008). Molekul propofol akan bekerja dan berikatan pada reseptor GABAA pada
membran sel syaraf pada otak khususnya reseptor GABAA subtipe ß3 bagian N265
(ßN265) sehingga menyebabkan ketidaksadaran dan pada reseptor GABAA subtipe
ß2 sehingga menyebabkan sedasi. Propofol menghasilkan pengaruh menghilangkan
kesadaran dan sedasi yang baik, tetapi subtipe ß3 yang terdapat pada reseptor
GABAA merespon terjadinya depresi respirasi akibat propofol (Henschel et al .2008).
Efek samping penggunaaan propofol adalah hipotensi, apnea, dan rasa sakit pada
tempat suntikan (Stawicki 2007). Propofol akan menghasilkan sedasi yang baik
dengan efek samping yang minimal apabila digunakan pada dosis yang rendah. Efek
samping propofol berhubungan dengan dosis penggunaan dan keuntungan
anestetikum lain untuk menurunkan dosis dan meminimalkan pengaruh buruk yang
ditimbulkan.
Kombinasi campuran propofol dengan ketamine merupakan anestetika
parenteral yang paling umum digunakan sebagai agen induksi untuk anestesi umum
inhalasi. Anestesi pada manusia dengan metode TIVA menggunakan propofol dan
ketamine, menunjukkan hasil yang sangat memuaskan secara klinik. Metode TIVA
dengan propofol digunakan secara luas pada pasien manusia yang ditangani diluar
ruang operasi. Kombinasi propofol dan ketamine akan berpotensi menghasilkan
sedasi dan relaksasi yang baik karena potensi propofol serta menghasilkan analgesi
yang kuat karena potensi ketamine. Kombinasi propofol dan ketamine dapat
menurunkan dosis hipnotik propofol dan mengurangi pengaruh depresi
kardiovaskuler dan respirasi akibat propofol.
Dengan demikian, pemeliharaan status teranestesi dengan kombinasi ketamine
dan propofol secara infusi gravimetrik diharapkan menghasilkan potensi anestesi
umum yang baik dan aman. Kombinasi ketamine dan propofol diharapkan dapat
menciptakan kondisi sedasi, analgesi, dan relaksasi yang oftimal serta adequat untuk
dilakukan tindakan atau prosedur diagnostik maupun terapeutik tanpa menimbulkan
gangguan hemodinamik, respiratorik, dan metabolik yang dapat mengancam.
Tujuan Penelitian
Tujuan umum penelitian ini adalah untuk mendapatkan keterpilihan anestetika
yang memenuhi kriteria komponen dasar anestesi (sedasi, analgesi, relaksasi, aman,
dan mudah diaplikasikan), sedangkan secara khusus tujuan penelitian ini adalah :
1. Memperoleh kombinasi dan dosis preanestesi dan induksi anestesi
pada anjing.
2. Memperoleh metode pemeliharaan status teranestesi secara infusi
gravimetrik pada anjing.
3. Menjadikan campuran ketamine dengan propofol sebagai keterpilihan
Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan manfaat :
1. Memberikan keyakinan untuk pemeliharaan status teranestesi secara infusi
gravimetrik selama masa pembiusan pada anjing.
2. Kombinasi bahan anestetikum dan dosis ketamine dan propofol dapat dipilih
sebagai kebakuan anestetikum pada anjing.
3. Metode dan hasil kajian anestesi infusi gravimetrik pada anjing dapat
dijadikan acuan dalam mengkaji anestesi pada spesies lain maupun manusia.
Hipotesis
1. Kombinasi preanestesi atropine-xylazine atau atropine-midazolam dengan induksi
ketamine dan propofol menghasilkan waktu induksi (onset) yang lebih singkat,
waktu anestesi (duration of action) yang lebih lama dan waktu pemulihan
(recovery) yang lebih cepat.
2. Kombinasi ketamine dan propofol secara gravimetrik melalui infusi intravena,
TINJAUAN PUSTAKA
Anestesi
Istilah anestesi dimunculkan pertama kali oleh dokter Oliver Wendell Holmes
(1809-1894) berkebangsaan Amerika, diturunkan dari dua kata Yunani : An berarti
tidak, dan Aesthesis berarti rasa atau sensasi nyeri. Secara harfiah berarti ketiadaan
rasa atau sensasi nyeri. Dalam arti yang lebih luas, anestesi berarti suatu keadaan
hilangnya rasa terhadap suatu rangsangan. Pemberian anestetikum dilakukan untuk
mengurangi dan menghilangkan rasa nyeri baik disertai atau tanpa disertai hilangnya
kesadaran. Seringkali anestesi dibutuhkan pada tindakan yang berkaitan dengan
pembedahan. Anestetikum yang diberikan pada hewan akan membuat hewan tidak
peka terhadap rasa nyeri sehingga hewan menjadi tenang, dengan demikian tindakan
diagnostik, terapeutik, atau pembedahan dapat dilaksanakan lebih aman dan lancar
(Tranquilli et al. 2007; Miller 2010).
Perjalanan waktu sepanjang sejarah menunjukkan bahwa anestesi pada hewan
digunakan untuk menghilangkan rasa dan sensasi terhadap suatu rangsangan yang
merugikan (nyeri), menginduksi relaksasi otot, dan terutama untuk membantu
melakukan diagnosis atau proses pembedahan yang aman. Alasan lain penggunaan
anestesi pada hewan adalah untuk melakukan pengendalian hewan (restraint),
keperluan penelitian biomedis, pengamanan pemindahan (transportasi) hewan liar,
pemotongan hewan yang humanis, dan untuk melakukan ruda paksa (euthanasia).
Secara umum tujuan pemberian anestetikum pada hewan adalah mengurangi atau
menghilangkan rasa nyeri dengan meminimalkan kerusakan organ tubuh dan
membuat hewan tidak terlalu banyak bergerak. Semua tujuan anestesi dapat dicapai
dengan pemberian obat anestetikum secara tunggal maupun dalam bentuk balanced
anesthesia, yaitu mengkombinasikan beberapa agen anestetikum maupun dengan
Preanestesi
Preanestesi adalah pemberian zat kimia sebelum tindakan anestesi umum
dengan tujuan utama menenangkan pasien, menghasilkan induksi anestesi yang halus,
mengurangi dosis anestetikum, mengurangi atau menghilangkan efek samping
anestetikum, dan mengurangi nyeri selama operasi maupun pasca operasi (Debuf
1991; McKelvey dan Hollingshead 2003). Pemilihan preanestetikum
dipertimbangkan sesuai dengan spesies, status fisik pasien, derajat pengendalian,
jenis operasi, dan kesulitan dalam pemberian anestetikum (Booth dan Branson 1995).
Preanestetikum yang paling umum digunakan pada hewan adalah atropine,
acepromazin, xylazine, diazepam, midazolam, dan opioid atau narkotik. Atropine
digunakan untuk mengurangi salivasi, peristaltik dan mengurangi bradikardia akibat
anestesi. Acepromazin digunakan sebagai penenang atau tranquilizer. Xylazine,
medetomidin, diazepam, dan midazolam digunakan sebagai agen sedatif dan
merelaksasi otot. Opioid atau narkotik digunakan untuk mengurangi rasa sakit, seperti
disajikan pada Gambar 1.
Gambar 1. Klasifikasi agen preanestesi yang digunakan pada anestesi umum
(Sumber: Warren 1983; McKelvey dan Hollingshead 2003).
Klasifikasi Anestesi
Keadaan teranestesi dapat dihasilkan secara kimia dengan obat-obatan dan
secara fisik melalui penekanan sensori pada syaraf. Obat-obatan anestetika umumnya
diklasifikasikan berdasarkan rute penggunaannya, yaitu: 1). Topikal misalnya melalui
kutaneus atau membrana mukosa; 2). Injeksi seperti intravena, subkutan,
intramuskular, dan intraperitoneal; 3). Gastrointestinal secara oral atau rektal; dan 4).
Respirasi atau inhalasi melalui saluran nafas (Tranquilli et al. 2007).
Anestetetikum juga dapat diklasifikasikan berdasarkan daerah atau luasan
pada tubuh yang dipengaruhinya, yaitu : 1). Anestesi lokal, terbatas pada tempat
penggunaan dengan pemberian secara topikal, spray, salep atau tetes, dan infiltrasi.
2). Anestesi regional, mempengaruhi pada daerah atau regio tertentu dengan
pemberian secara perineural, epidural, dan intratekal atau subaraknoid. 3). Anestesi
umum, mempengaruhi seluruh sistem tubuh secara umum dengan pemberian secara
injeksi, inhalasi, atau gabungan (balanced anaesthesia) (Adams 2001; McKelvey dan
Hollingshead 2003).
Anestesi Lokal
Anestetikum lokal adalah suatu bahan kimia yang mampu menghambat
konduksi syaraf perifer tanpa menimbulkan kerusakan permanen pada syaraf
tersebut. Mekanisme kerja anestetikum lokal dengan cara menghambat (blok) saluran
ion sodium (Na) pada syaraf perifer, konduksi atau aksi potensial pada syaraf
terhambat sehingga respon nyeri secara lokal hilang. Anestetikum lokal mencegah
proses depolarisasi membran syaraf secara lokal melalui penghambatan saluran ion
Na, sehingga membran akson tidak dapat bereaksi dengan neurotransmitter
acetilkolin dan membran akan tetap dalam keadaan semipermiabel serta tidak terjadi
perubahan potensial. Keadaan tersebut menyebabkan aliran inpuls yang melewati
syaraf berhenti, sehingga semua rangsangan tidak sampai ke SSP. Sifat hambatan
syaraf umumnya bersifat lokal, selektif, dan tergantung pada dosis atau jumlah obat
yang diberikan (Tranquilli et al. 2007; Miller 2010).
Sifat sifat yang harus dimiliki oleh obat anestetikum lokal adalah poten,
artinya efektif dalam dosis rendah, daya penetrasinya baik, mula kerjanya cepat, masa
kerjanya lama, toksisitas sistemik rendah, tidak mengiritasi jaringan, pengaruhnya
Penggunaan anestetikum lokal bisa dilakukan dengan meneteskan pada
permukaan daerah yang akan dianestesi (surface aflication), dengan melakukan
injeksi secara sub-kutan pada daerah yang akan dianestesi (subdermal, intradermal),
serta dengan melakukan pemblokiran pada daerah tertentu (field block anestesi).
Anestetikum yang sering digunakan sebagai anestetikum lokal adalah procaine HCI
2% - 4%, Lidocaine 0,5 - 2%, Lidocaine 4%, Tetracaine, bupivacaine 0,25% atau
0,5%, Dibucain, Pehacaine, Lidonest, dan Chlor buthanol dengan dosis pemberian
secukupnya (Quantum statis, QS). Lidocaine dan bupivacaine dapat diencerkan
dengan larutan salin (bukan air) untuk menurunkan konsentrasinya. Bupivacaine
mempunyai onset lebih lambat (20 menit) dan durasi lebih panjang (6 jam)
dibandingkan lidocaine (onset lebih cepat dan durasi 1-2 jam) (Adams 2001; Sudisma
2006; Tranquilli et al. 2007).
Anestesi Regional
Anestesi regional adalah tindakan menghilangnya nyeri yang dilakukan
dengan cara menyuntikkan anestetikum lokal pada lokasi syaraf yang menginervasi
regio atau daerah tertentu sehingga menyebabkan hambatan konduksi inpuls yang
reversibel. Anestetikum regional dapat menghilangkan rasa nyeri pada suatu daerah
atau regio tertentu secera reversibel tanpa disertai hilangnya kesadaran. Mekanisme
kerja dan jenis anestetikum yang digunakan sama dengan anestetikum lokal, tetapi
daerah atau luasan pada tubuh yang dipengaruhi adalah daerah atau regio tertentu.
Anestesi regional dibedakan berdasarkan rute pemberiannya, yaitu secara epidural,
spinal atau intrathekal atau subaraknoid, dan blok pleksus brakhialis (Adams 2001;
McKelvey dan Hollingshead 2003).
Anestesi epidural dihasilkan dengan cara menginjeksikan anestetikum lokal
diantara duramater dan periosteum dari canalis spinalis (epidural space).
Anestetikum tidak langsung mengenai medula spinalis, sehingga efek anestesi terjadi
setelah 15-20 menit pemberian. Anestesi epidural menghambat sensasi dan kontrol
motorik daerah abdominal, pelvis, ekor, dan kaki belakang. Anestesi ini biasanya
pembedahan daerah pelvis, dan amputasi daeran kaki belakang. Pada hewan kecil
dilakukan antara tulang lumbar terakhir dan tulang sakral 1. Sedangkan pada hewan
besar dilakukan antara tulang coccigia 1 dan 2. Anestetikum yang digunakan sama
dengan anestetikum lokal, seperti lidocaine 2%, bupivacain 0,5%, ropivacain 0,75%
atau mepivacaine 2% dengan dosis pemberian 1ml/5kg BB. Lidocain menghasilkan
durasi sekitar 1-2 jam dan bupivacain sekitar 6 jam (McKelvey dan Hollingshead
2003).
Spinal atau intrathekal atau subaraknoid anestesi sama dengan anestesi
epidural tetapi dilakukan melalui duramater dan subaraknoid dimana jarum
menembus duramater dan subaraknoid sehingga anestetikum masuk ke dalam dan
langsung mengenai syaraf spinal, menghasilkan anestesi yang segera dan lebih
cepat. Anestesi ini mengakibatkan resiko berontak dan rasa sakit yang memerlukan
kesembuhan lebih lama. Anestetikum yang digunakan sama dengan anestetikum
lokal. Sedangkan blok pleksus brakhialis adalah anestesi regional dengan cara
menyuntikkan anestetikum lokal di daerah perjalanan fleksus brakhialis yang
menginervasi daerah kaki depan (Adams 2001; McKelvey dan Hollingshead 2003;
Sudisma 2006; Tranquilli et al. 2007).
Anestesi Umum
Anestesi umum adalah keadaan hilangnya nyeri di seluruh tubuh dan
hilangnya kesadaran yang bersifat sementara yang dihasilkan melalui penekanan
sistem syaraf pusat karena adanya induksi secara farmakologi atau penekanan
sensori pada syaraf. Agen anestesi umum bekerja dengan cara menekan sistem
syaraf pusat (SSP) secara reversibel (Adams 2001). Anestesi umum merupakan
kondisi yang dikendalikan dengan ketidaksadaran reversibel dan diperoleh melalui
penggunaan obat-obatan secara injeksi dan atau inhalasi yang ditandai dengan
hilangnya respon rasa nyeri (analgesia), hilangnya ingatan (amnesia), hilangnya
respon terhadap rangsangan atau refleks dan hilangnya gerak spontan (immobility),
Mekanisme kerja anestesi umum pada tingkat seluler belum diketahui secara
pasti, tetapi dapat dihipotetiskan mempengaruhi sistem otak karena hilangnya
kesadaran, mempengaruhi batang otak karena hilangnya kemampuan bergerak, dan
mempengaruhi kortek serebral karena terjadi perubahan listrik pada otak. Anestesi
umum akan melewati beberapa tahapan dan tahapan tersebut tergantung pada dosis
yang digunakan. Tahapan teranestesi umum secara ideal dimulai dari keadaan terjaga
atau sadar kemudian terjadi kelemahan dan mengantuk (sedasi), hilangnya respon
nyeri (analgesia), tidak bergerak dan relaksasi (immobility), tidak sadar
(unconsciousness), koma, dan kematian atau dosis berlebih (Tranquilli et al. 2007;
Miller 2010).
Anestesi umum yang baik dan ideal harus memenuhi kriteria : tiga komponen
anestesi atau trias anestesi (sedasi, analgesi, dan relaksasi), penekanan refleks,
ketidaksadaran, aman untuk sistem vital (sirkulasi dan respirasi), mudah
diaplikasikan dan ekonomis. Dengan demikian, tujuan utama dilakukan anestesi
umum adalah upaya untuk menciptakan kondisi sedasi, analgesi, relaksasi, dan
penekanan refleks yang optimal dan adekuat untuk dilakukan tindakan dan prosedur
diagnostik atau pembedahan tanpa menimbulkan gangguan hemodinamik,
respiratorik, dan metabolik yang dapat mengancam (Wolfensohn dan Lloyd 2000;
Adams 2001; Tranquilli et al. 2007; Miller 2010).
Agen anestesi umum dapat digunakan melalui injeksi, inhalasi, atau melalui
gabungan secara injeksi dan inhalasi. Anestetikum dapat digabungkan atau
dikombinasikan antara beberapa anestetikum atau dengan zat lain sebagai
preanestetikum dalam sebuah teknik yang disebut balanced anesthesia untuk
mendapatkan efek anestesi yang diinginkan dengan efek samping minimal.
Anestetika umum inhalasi yang sering digunakan pada hewan adalah halotan,
isofluran, sevofluran, desfluran, dietil eter, nitrous oksida dan xenon. Anestetika
umum yang diberikan secara injeksi meliputi barbiturat (tiopental, metoheksital, dan
pentobarbital), cyclohexamin (ketamine, tiletamin), etomidat, dan propofol
Anestesi umum inhalasi merupakan salah satu metode anestesi umum yang
dilakukan dengan cara memberikan agen anestesi yang berupa gas dan atau cairan
yang mudah menguap melalui alat anestesi langsung ke udara inspirasi. Mekanisme
kerja anestesi umum inhalasi sangat rumit dan sampai saat ini masih merupakan
misteri, karena pemberian anestetikum inhalasi melalui pernapasan menuju organ
sasaran yang jauh adalah suatu hal yang unik. Hiperventilasi akan menaikkan ambilan
anestetikum dalam alveolus dan hipoventilasi akan menurunkan ambilan alveolus.
Kelarutan zat inhalasi dalam darah adalah faktor utama yang penting dalam
menentukan induksi dan pemulihan anestesi inhalasi. Induksi dan pemulihan akan
berlangsung cepat pada zat yang tidak larut dan lambat pada zat yang larut. Kadar
alveolus minimal atau minimum alveolar cencentration (MAC) adalah kadar minimal
zat anestesi dalam alveolus pada tekanan satu atmosfir yang diperlukan untuk
mencegah gerakan pada 50% pasien yang dilakukan rangsangan insisi standar.
Immobilisasi tercapai pada 95% pasien apabila kadar anestetikum dinaikkan di atas
30% nilai MAC. Dalam keadaan seimbang, tekanan parsial anestetikum dalam alveoli
sama dengan tekanan zat dalam darah dan otak tempat kerja anestetikum (Latief et al.
2007; McKelvey dan Hollingshead 2003).
Anestetika umum inhalasi yang pertama kali dikenal dan digunakan untuk
membantu pembedahan adalah N2O. Kemudian menyusul, eter, kloroform, etil
klorida, halotan, metoksifluran, enfluran, isofluran, desfluran, sevofluran, dan xenon.
Anestetika umum inhalasi yang umum digunakan saat ini adalah N2
Nitrous oxide (N
O, halotan,
enfluran, isofluran, desfluran, sevofluran, dan xenon. Obat obat anestesi yang lain
ditinggalkan, karena efek sampingnya yang tidak dikehendaki. Misalnya, eter mudah
terbakar dan meledak, menyebabkan sekresi bronkus berlebihan, mual dan muntah,
kerusakan hati, dan baunya yang sangat merangsang. Kloroform menyebabkan
aritmia dan kerusakan hati. Metoksifluran menyebabkan kerusakan hati, toksik
terhadap ginjal, dan mudah terbakar (Latief et al. 2007; McKelvey dan Hollingshead
2003; Tranquilli et al. 2007).
2O) atau dinitrogen monoksida adalah anestesi inhalasi yang
ini bersifat anestetikum lemah, tetapi analgesianya kuat, sehingga jarang digunakan
secara tunggal. Anestetikum yang sering dikombinasikan dengan N2O adalah
halotan. Pada akhir anestesi setelah N2O dihentikan, akan cepat keluar mengisi
alveoli, sehingga terjadi pengenceran oksigen dan terjadi hipoksia difusi. Mengatasi
hipoksia difusi, biasanya diberikan 100% oksigen selama 5 – 10 menit. Potensi N2O
digunakan pada hewan tidak baik, karena mempunyai MAC yang tinggi. MAC N2
Halotan sering digunakan sebagai induksi anestesi dikombinasikan dengan
N
O
pada manusia mendekati 100%, tetapi pada anjing hampir 200% dan kucing
mendekati 250% (Latief et al. 2007; McKelvey dan Hollingshead 2003).
2
Desfluran adalah halogenasi eter yang rumus bangun dan efek klinisnya mirip
dengan isofluran. Desfluran sangat mudah menguap dibandingkan anestetikum
lainnya, sehingga perlu menggunakan vaporizer khusus. Potensi desfluran sangat
rendah (MAC 6,0%), bersifat simpatomimetik, menyebabkan takikardia dan O, karena halotan adalah analgesik lemah tetapi sifat anestesinya kuat sehingga
kombinasi keduanya sangat ideal. Pemeliharaan anestesi dengan halotan biasanya
digunakan dosis 1-2% pada napas spontan atau dosis 0,5-1% pada napas terkendali,
dan dapat disesuaikan dengan respon klinis pasien. Nilai MAC halotan adalah
moderat, potensinya berada diantara metoksifluran dan isofluran, yaitu 0,3 – 0,75%.
Halotan mempunyai tekanan uap yang tinggi, sehingga memerlukan ketelitian
penggunaan vaporizer yang lebih tinggi. Penggunaan vaporizer yang memiliki tingkat
ketelitian kurang, dapat menyebabkan konsentrasi halotan mencapai 30%, padahal
konsentrasi normal halotan yang diperlukan untuk anestesi adalah 1-2%, sehingga
penggunaan halotan memerlukan vaporizer khusus. Halotan menyebabkan
vasodilatasi cerebral, meningkatkan aliran darah pada otak yang sulit dikendalikan.
Kelebihan dosis halotan menyebabkan depresi napas, menurunkan tonus simpatik,
terjadi hipotensi, bradikardi, vasodilatasi perifer, depresi vasomotor, dan depresi
miokardium. Halotan dimetabolisme 20% di hati secara oksidatif menjadi komponen
bromin, klorin, dan asam trikloro asetat. Halotan menyebabkan gangguan hati dan
pasca pemberian sering menyebabkan pasien meninggal (Latief et al. 2007;
hipertensi. Pengaruh depresi nafasnya sama dengan isofluran dan merangsang jalan
napas atas sehingga tidak dapat digunakan sebagai induksi anestesi.
Isofluran merupakan halogenasi eter dan secara kimia sangat mirip dengan
metoksifluran dan sevofluran. Rentang keamanan isofluran lebih lebar dibandingkan
halotan dan metoksifluran, sehingga sangat umum digunakan pada hewan terutama
anjing dan kuda walaupun dengan harga yang lebih mahal. Penggunaaan isofluran
pada dosis anestesi atau subanestesi menurunkan metabolisme otak terhadap oksigen,
tetapi akan meningkatkan aliran darah di otak dan tekanan intrakranial, sehingga
menjadi pilihan pada pembedahan otak. Pengaruh terhadap jantung dan curah jantung
(cardiac output) sangat minimal, sehingga dapat digunakan pada pasien dengan
kelainan jantung. Potensi isofluran lebih kecil dibandingkan halotan karena
mempunyai nilai MAC lebih tinggi dibandingkan halotan. Pemeliharaan anestesi
dengan isofluran biasanya digunakan konsentrasi 1,5 – 2,5 % isofluran dalam oksigen
(Latief et al. 2007; McKelvey dan Hollingshead 2003).
Anestesi umum injeksi merupakan metode anestesi umum yang dilakukan
dengan cara menyuntikkan agen anestesi langsung melalui muskulus atau pembuluh
darah vena. Anestesi injeksi biasanya digunakan untuk induksi pada hewan kecil
maupun pada hewan besar dan dapat juga digunakan untuk pemeliharaan anestesi.
Anestetika injeksi yang baik memiliki sifat-sifat tidak mengiritasi jaringan, tidak
menimbulkan rasa nyeri pada saat diinjeksikan, cepat diabsorsi, waktu induksi,
durasi, dan masa pulih dari anestesi berjalan mulus, tidak ada tremor otot, memiliki
indeks terapeutik tinggi, tidak bersifat toksik, mempunyai pengaruh minimal terhadap
organ tubuh terutama saluran pernapasan dan kardiovaskular, cepat dimetabolisme,
tidak bersifat akumulatif, dapat dikombinasikan dengan obat lain seperti relaksan
otot, analgesik, dan sudah diketahui antidotanya. Beberapa anestetika injeksi yang
sering digunakan pada hewan adalah golongan barbiturat seperti thiopental sodium,
methoheksital, dan pentobarbital. Golongan lainnya yang juga sering digunakan pada
hewan adalah golongan cycloheksamin (ketamine dan tiletamin), etomidat, dan
Semua golongan barbiturat untuk keperluan anestesi berada dalam bentuk
garam sodium dan dilarutkan dalam air menjadi larutan 2,5 atau 5%. Tiga klas
golongan barbiturat yang digunakan pada hewan adalah ultrashort-acting
barbiturates (metoheksital), short-acting barbiturates (tiopental), dan
intermediate-acting barbiturates (pentobarbital). Sedangkan long-acting barbiturates
(penobarbital) biasanya digunakan untuk sedatip dan antikonvulsi, bukan untuk
anestesi. Barbiturat menimbulkan sedasi, hipnosis, dan depresi pernafasan tergantung
dosis dan kecepatan pemberian serta pengaruh analgesia yang ditimbulkan sedikit.
Efek utama golongan barbiturat adalah depresi pusat pernafasan, depresi pusat
vasomotor, dan miokardium sehingga menurunkan curah jantung dan tekanan darah.
Etomidat berbentuk kristal putih, dapat larut dalam air, etanol, dan propilin
glikol. Etomidat adalah sedatif hipnotik imidazol yang biasanya digunakan sebagai
induksi anestesi pada anjing dan kucing. Kombinasi anestetikum dengan etomidat
menghasilkan relaksasi otot yang baik tetapi tidak menghasilkan analgesia dan
durasinya sangat singkat seperti propofol, karena metabolisme etomidat sangat cepat.
Etomidat mempunyai pengaruh yang minimal terhadap fungsi kardiovaskuler seperti
denyut jantung, curah jantung, dan tekanan darah. Etomidat dapat diberikan secara
infusi dengan kecepatan dosis 50 -150 µ/kg/menit.
Ketamine adalah anestetikum umum injeksi golongan nonbarbiturat, termasuk
golongan phenilsycloheksamin. Ketamine mempunyai efek analgesia yang sangat
kuat akan tetapi efek sedasi dan hipnotiknya kurang (tidur ringan). Ketamine
meningkatkan tekanan darah sistol maupun diastol kira kira 20- 25%, karena adanya
aktivitas syaraf simpatik meningkat dan depresi baroreseptor. Pemberian anestetikum
ketamine secara tunggal dosis 10-15 mg/kg berat badan secara intra muskular pada
anjing menimbulkan kekejangan otot dan hipersalivasi serta durasi kerja anestesi
yang sangat pendek. Mengatasi kerugian penggunaan anestetikum ketamine secara
tunggal, ketamine sering dikombinasikan dengan obat lain sebagai preanestesi.
Propofol adalah anestesi umum injeksi turunan alkil penol
(2,6-diisopropylphenol), mempunyai pH netral, dan dapat diberikan dalam bentuk emulsi
sangat aman diberikan secara intravena dan dapat diberikan secara berulang-ulang
atau sebagai alternatif dapat diberikan secara infusi terus-menerus. Propofol
mempunyai efek analgesia yang sangat ringan akan tetapi efek sedasi dan
hipnotiknya sangat kuat. Efek samping penggunaaan propofol adalah hipotensi,
apnea, dan rasa sakit pada tempat suntikan. Efek samping utama yang sangat
dihindari dari propofol adalah penekanan sistem respirasi. Efek samping tersebut
sangat berkaitan dengan dosis dan kecepatan penyuntikannya, keuntungan
penggunaan propofol akan diperoleh dengan cara mengkombinasikan dengan agen
anestetikum lain untuk menurunkan dosis dan meminimalkan pengaruh buruk yang
ditimbulkan (Stawicki 2007).
Tahapan Anestesi Umum
Tahapan anestesi sangat penting untuk diketahui terutama dalam
menentukan tahapan terbaik untuk melakukan pembedahan, memelihara tahapan
tersebut sampai batas waktu tertentu, dan mencegah terjadinya kelebihan dosis
anestetikum. Tahapan anestesi dapat dibagi dalam beberapa langkah, yaitu:
preanestesi, induksi, pemeliharaan, dan pemulihan (McKelvey dan Hollingshead
2003).
Tahap preanestesi merupakan tahapan yang dilakukan segera sebelum
dilakukan anestesi, dimana data tentang pasien dikumpulkan, pasien dipuasakan,
serta dilakukan pemberian preanestetikum. Induksi adalah proses dimana hewan akan
melewati tahap sadar yang normal atau conscious menuju tahap tidak sadar atau
unconscious. Agen induksi dapat diberikan secara injeksi atau inhalasi. Apabila agen
induksi diberikan secara injeksi maka akan diikuti dengan intubasi endotracheal tube
untuk pemberian anestetikum inhalasi atau gas menggunakan mesin anestesi. Waktu
minimum periode induksi biasanya 10 menit apabila diberikan secara intramuskular
(IM) dan sekitar 20 menit apabila diberikan secara subkutan (SC). Tahap induksi
ditandai dengan gerakan tidak terkoordinasi, gelisah dan diikuti dengan relaksasi
yang cepat serta kehilangan kesadaran. Idealnya, keadaan gelisah dan tidak tenang
Preanestesi dan induksi anestesi dapat diberikan secara bersamaan, seperti pemberian
acepromazin, atropine, dan ketamine dicampur dalam satu alat suntik dan diberikan
secara intravena (IV) pada anjing. (Adams 2001; McKelvey dan Hollingshead 2003;
Tranquilli et al. 2007).
Selanjutnya hewan akan memasuki tahap pemeliharaan status teranestesi.
Pada tahap pemeliharaan ini, status teranestesi akan terjaga selama masa tertentu dan
pada tahap inilah pembedahan atau prosedur medis dapat dilakukan. Tahap
pemeliharaan dapat dilihat dari tanda-tanda hilangnya rasa sakit atau analgesia,
relaksasi otot rangka, berhenti bergerak, dilanjutkan dengan hilangnya refleks
palpebral, spingter ani longgar, serta respirasi dan kardiovaskuler tertekan secara
ringan. Begitu mulai memasuki tahap pemeliharaan, respirasi kembali teratur dan
gerakan tanpa sengaja anggota tubuh berhenti. Bola mata akan bergerak menuju
ventral, pupil mengalami konstriksi, dan respon pupil sangat ringan. Refleks menelan
sangat tertekan sehingga endotracheal tube sangat mudah dimasukkan, refleks
palpebral mulai hilang, dan kesadaran mulai hilang. Anestesi semakin dalam
sehingga sangat nyata menekan sirkulasi dan respirasi. Pada anjing dan kucing,
kecepatan respirasi kurang dari 12 kali per menit dan respirasi semakin dangkal.
Denyut jantung sangan rendah dan pulsus sangat menurun karena terjadi penurunan
seluruh tekanan darah. Nilai CRT akan meningkat menjadi 2 atau 3 detik. Semua
refleks tertekan secara total dan terjadi relaksasi otot secara sempurna serta refleks
rahang bawah sangat kendor. Apabila anestesi dilanjutkan lebih dalam, pasien akan
menunjukkan respirasi dan kardiovaskuler lebih tertekan dan pada keadaan dosis
anestetikum berlebih akan menyebabkan respirasi dan jantung berhenti. Dengan
demikian, pada tahap pemeliharaan sangat diperlukan pemantauan dan pengawasan
status teranestesi terhadap sistim kardiovaskuler dan respirasi (McKelvey dan
Hollingshead 2003; Tranquilli et al. 2007 ).
Ketika tahap pemeliharaan berakhir, hewan memasuki tahap pemulihan yang
menunjukkan konsentrasi anestetikum di dalam otak mulai menurun. Metode atau
mekanisme bagaimana anestetikum dikeluarkan dari otak dan sistem sirkulasi adalah
injeksi dikeluarkan dari darah melalui hati dan dimetabolisme oleh enzim di hati dan
metabolitnya dikeluarkan melalui sistem urinari. Pada hewan kucing, ketamine tidak
mengalami metabolisme dan dikeluarkan langsung tanpa perubahan melalui ginjal.
Kadar anestetikum golongan tiobarbiturat di dalam otak dapat dengan cepat menurun
karena dengan cepat disebarkan ke jaringan terutama otot dan lemak, sehingga hewan
akan sadar dan terbangun dengan cepat mendahului ekskresi anestetikum dari dalam
tubuh hewan. Anestetikum golongan inhalasi akan dikeluarkan dari tubuh pasien
melalui sistem respirasi, molekul anestetikum akan keluar dari otak memasuki
peredaran darah, alveoli paru-paru, dan akhirnya dikeluarkan melalui nafas. Tanda
tanda adanya aktivitas refleks, ketegangan otot, sensitivitas terhadap nyeri pada
periode pemulihan dinyatakan sebagai kesadaran kembali (McKelvey dan
Hollingshead 2003).
Durasi atau lama waktu kerja anestetikum dan kualitas anestesi dapat dilihat
dari pengamatan perubahan fisiologis selama stadium teranestesi. Dikenal dua waktu
induksi pada durasi anestesi. Waktu induksi 1 adalah waktu antara anestetikum
diinjeksikan sampai keadaan hewan tidak dapat berdiri. Waktu induksi 2 adalah
waktu antara anestetikum diinjeksikan sampai keadaan hewan tidak ada refleks pedal
atau hewan sudah tidak merasakan sakit (stadium operasi). Durasi adalah waktu
ketika hewan memasuki stadium operasi sampai hewan sadar kembali dan merasakan
sakit jika daerah disekitar bantalan jari ditekan. Waktu siuman atau recovery adalah
waktu antara ketika hewan memiliki kemampuan merasakan nyeri bila syaraf
disekitar jari kaki ditekan atau mengeluarkan suara sampai hewan memiliki
kemampuan untuk duduk sternal, berdiri atau jalan (Moens dan Fargetton 1990;
Verstegen dan Petcho 1993; McKelvey dan Hollingshead 2003).
McKelvey dan Hollingshead (2003) dan Tranquilli et al. (2007) menyatakan
bahwa untuk memonitor anestesi dilakukan pengamatan tahap-tahap anestesi umum.
Kualitas status teranestesi dapat dilihat dari perubahan fisiologis sebagai tanda
kedalaman anestesi, seperti disajikan pada Tabel 1.
Tabel 1 Tahapan dan indikasi status teranestesi oleh anestetikum umum
Teranestesi Teranestesi Teranestesi Teranestesi Hampir mati
Stadiun 1 atau stadium analgesi adalah stadium awal anestesi yang terjadi
segera setelah dilakukan anestesi secara inhalasi atau injeksi. Hewan pada stadium ini