ISOLASI SELULOSA AMPAS SAGU DENGAN
DELIGNIFIKASI MENGGUNAKAN HIDROGEN PEROKSIDA
HISYAM
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
HISYAM. Isolasi Selulosa Ampas Sagu dengan Delignifikasi Menggunakan
Hidrogen Peroksida. Dibimbing oleh TUN TEDJA IRAWADI dan HENNY
PURWANINGSIH.
Isolasi selulosa ampas sagu telah berhasil dilakukan dalam penelitian ini
dengan melalui beberapa tahap, yaitu penghilangan senyawa ekstraktif,
penghilangan pati, dan penghilangan hemiselulosa. Proses penghilangan pati
sampel bebas ekstraktif dengan ekstraksi menggunakan air pada suhu 80
oC
membutuhkan banyak air dan waktu yang lama. Dengan menggunakan HCl 3%
pada suhu 80
oC, waktu yang diperlukan lebih singkat. Rendemen sampel bebas
pati hasil ekstraksi dengan air panas sebesar 41.5%, lebih tinggi daripada hasil
ekstraksi dengan HCl 3%, yaitu 26.3%. Selulosa ikut terhidrolisis pada proses
ekstraksi dengan HCl 3%, dibuktikan dengan munculnya serapan C=O pada
spektrum inframerah transformasi fourier (FTIR). Kadar lignin hasil delignifikasi
dengan H
2O
20.75, 1, dan 1.5% berturut-turut 22.2, 18.7, dan 14.6%, sedangkan
rendemennya 43.6, 41.4, dan 39.4%. Spektrum FTIR hasil isolasi selulosa dengan
metode penghilangan pati menggunakan air lebih mirip dengan selulosa komersial
dibandingkan dengan yang metode penghilangan patinya menggunakan HCl 3%.
ABSTRACT
HISYAM. Isolation of Cellulose from Sago Waste by Using Hydrogen Peroxide
Delignification. Supervised by TUN TEDJA IRAWADI and HENNY
PURWANINGSIH.
ISOLASI SELULOSA AMPAS SAGU DENGAN
DELIGNIFIKASI MENGGUNAKAN HIDROGEN PEROKSIDA
HISYAM
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul Skripsi : Isolasi
Selulosa
Ampas
Sagu
dengan
Delignifikasi
Menggunakan Hidrogen Peroksida
Nama
: Hisyam
NIM
: G44061225
Disetujui
Pembimbing I
Prof Dr Ir Tun Tedja Irawadi, MS
NIP 19501227 197603 2 002
Pembimbing II
Henny Purwaningsih, SSi, MSi
NIP 19741201 200501 2 001
Diketahui
Ketua Departemen Kimia
Prof Dr Ir Tun Tedja Irawadi, MS
NIP 19501227 197603 2 002
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala rahmat
dan karunia-Nya sehingga karya ilmiah ini dapat diselesaikan. Tulisan ini disusun
berdasarkan hasil penelitian yang dilaksanakan pada bulan Desember 2010 hingga
Juli 2011 di Laboratorium Terpadu Departemen Kimia FMIPA IPB. Penelitian ini
dilakukan untuk mengisolasi selulosa dari ampas sagu.
Penulis mengucapkan terima kasih kepada Prof Dr Ir Tun Tedja Irawadi,
MS dan Henny Purwaningsih, SSi, MSi selaku pembimbing yang telah memberi
banyak arahan, inspirasi, dan saran selama penulis melaksanakan penelitian ini.
Penulis juga mengucapkan terima kasih kepada Mamah dan Abah yang telah
memberi banyak kasih sayang, semangat, dan doa selama penulis menempuh
studi, penelitian, dan penulisan karya ilmiah ini.
Penulis juga mengucapkan terima kasih kepada Kak Yono dan Indah yang
telah banyak membantu dalam pelaksanaan penelitian ini. Tidak lupa, ungkapan
terima kasih juga penulis sampaikan kepada rekan-rekan peneliti di Laboratorium
Terpadu Departemen Kimia FMIPA IPB (Roni, Muti, dan Irfan) dan teman-teman
Kimia angkatan 43 lainnya.
Semoga karya ilmiah ini bermanfaat.
Februari 2012
RIWAYAT HIDUP
Penulis adalah anak tunggal dari Bapak Dede Achmad Rifa’i da
n Ibu Euis
Yudi Sumiarsih yang dilahirkan di Bogor pada tanggal 30 April 1988. Penulis
lulus dari SMU Negeri 3 Bogor pada tahun 2006. Penulis kemudian diterima di
Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB
(USMI) pada tahun yang sama dan memilih Mayor Kimia di Fakultas Matematika
dan Ilmu Pengetahuan Alam.
DAFTAR ISI
Halaman
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... vii
PENDAHULUAN ... 1
BAHAN DAN METODE
... 2
Alat dan Bahan ... 2
Preparasi Contoh Ampas Sagu ... 2
Penghilangan Senyawa Ekstraktif dan Pati ... 2
Delignifikasi dan Penghilangan Hemiselulosa ... 2
Penentuan Kadar Lignin ... 2
Analisis FTIR ... 3
HASIL DAN PEMBAHASAN
... 3
Pengaruh Penghilangan Senyawa Ekstraktif dan Pati ... 3
Delignifikasi dan Penghilangan Hemiselulosa ... 4
Analisis FTIR ... 5
SIMPULAN DAN SARAN
... 0
Simpulan ... 6
Saran ... 7
DAFTAR PUSTAKA ... 7
DAFTAR TABEL
Halaman
1 Pengaruh konsentrasi H2O2 terhadap rendemen holoselulosa ... 4
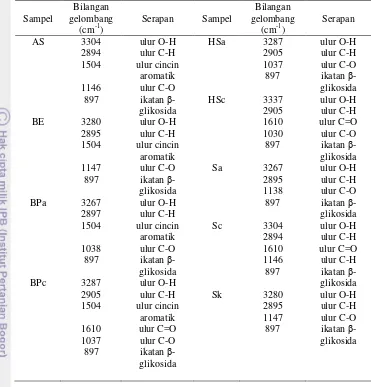
2 Hasil analisis FTIR ... 6
DAFTAR GAMBAR
Halaman
1
AS (ampas sagu), BE (AS bebas bahan ekstraktif), BPa (hasil ekstraksi BE
dengan air panas), dan BPc (hasil ekstraksi AS dengan HCl 3%) ... 3
2 Pengaruh konsentrasi H2O2 terhadap kadar lignin ... 4
3 Reaksi kesetimbangan hidrogen peroksida ... 4
4 Reaksi hidrogen peroksida dengan anion hidroperoksida... 4
5 Hasil delignifikasi ... 4
6 Holoselulosa (HSa) hasil delignifikasi BPa ... 5
7 Selulosa komersial, Sa, dan Sc... 5
DAFTAR LAMPIRAN
Halaman
1 Bagan alir penelitian ... 10
2 Kadar air, kadar abu, dan kadar lignin ampas sagu ... 11
3 Rendemen BE, BPa, dan BPc ... 12
4 Kadar lignin dan rendemen hasil delignifikasi ... 13
PENDAHULUAN
Tanaman sagu (Metroxylon sago) tumbuh di daerah tropis seperti Malaysia, Indonesia, dan Thailand. Sekitar 60 juta ton pati sagu diproduksi di kawasan Asia Tenggara (Wang
et al. 1996 dalam Sun et al. 1999). Potensi sagu di Indonesia saat ini telah mencapai lebih dari 50% potensi sagu dunia. Areal penanaman sagu di Indonesia tersebar di banyak daerah seperti Papua, Maluku, Riau, Sulawesi Utara, Sulawesi Selatan, dan Sulawesi Tenggara (Susanto 2006). Industri umumnya hanya memproses sagu untuk menghasilkan pati, sedangkan limbahnya berupa ampas sagu dibuang.
Industri ekstraksi pati sagu menghasilkan 3 jenis limbah, yaitu residu selular empulur sagu berserat (ampas), kulit luar batang sagu (bark), dan air buangan (wastewater). Jumlah ampas sagu sekitar 14% berdasar bobot total batang sagu (Kiat 2006). Semakin banyak produksi pati sagu, semakin banyak pula limbah ampas sagu yang dihasilkan. Hal tersebut dapat mencemari lingkungan berupa bau dan meningkatkan keasaman tanah (pH<4) (Syakir et al. 2009). Industri ekstraksi pati sagu di Indonesia masih menggunakan teknologi yang sederhana sehingga ampas sagu masih cukup banyak mengandung pati. Oleh karena itu, ampas sagu biasanya dimanfaatkan sebagai campuran bahan pakan ternak dan media untuk fermentasi rumen dan pelepah sagu yang digunakan dalam industri pulp dan kertas (Kiat 2006). Ampas sagu mengandung 58.21% pati, 22.45% selulosa, 11.8% hemiselulosa, 1.6% senyawa ekstraktif, dan 8.95% lignin (Irawadi 2010).
Ampas sagu dapat digunakan sebagai pupuk dan media tumbuh tanaman (Bintoro 2008), sebagai arang briket, sumber bahan organik bagi tanah, dan pengisi adonan perekat dalam kayu lapis (Matitaputty & Alfons 2006). Sebagian besar penelitian limbah sagu sejauh ini diarahkan pada pemanfaatan limbah ampas sagu sebagai bahan baku pembuatan bahan bakar hayati dan substrat pertumbuhan cendawan atau bakteri untuk memproduksi enzim-enzim ekstraselular (Sharim et al. 2008). Selain itu, selulosa ampas sagu juga dapat dimodifikasi menjadi selulosa asetat dengan anhidrida asetat sehingga dapat diaplikasikan pada teknologi plastik, membran, dan fase diam kromatografi kolom. Oleh karena itu, proses isolasi selulosa merupakan tahap yang penting. Santi (2006), Irfana (2010), dan Cahyani (2010) telah melakukan modifikasi
sederhana asetilasi terhadap ampas sagu yang digunakan sebagai fase diam kromatografi kolom untuk pemisahan ekstrak temu lawak.
Isolasi selulosa dari ampas sagu harus melewati beberapa tahap, yaitu penghilangan senyawa ekstraktif, pati, lignin, dan hemiselulosa. Senyawa ekstraktif dihilangkan dengan cara direfluks menggunakan pelarut toluena-etanol (2:1) (modifikasi Fang et al.
2000) dan pati dihilangkan dengan cara diekstraksi menggunakan air panas atau larutan HCl 3% dengan suhu 80 oC (Setyawati
et al. 2002). Tahapan penghilangan lignin sangat penting karena senyawa lignin mengikat kuat selulosa dan hemiselulosa sehingga berpengaruh terhadap struktur kerapatan serat pada sagu (Maeda 1986 dalam Sun et al. 1999). Proses bleaching
(pemucatan) dan delignifikasi biasanya menggunakan senyawa klorin dan turunannya yang dapat menghasilkan limbah organoklorin. Organoklorin merupakan senyawa beracun yang mudah larut dalam lemak sehingga dapat tersebar melalui rantai makanan. Seiring dengan perkembangan kesadaran masyarakat terhadap kelestarian lingkungan, berbagai penelitian dikembangkan untuk mencari pengganti klorin pada proses bleaching. Senyawa alternatif yang dapat digunakan antara lain oksigen, ozon, dan hidrogen peroksida (Nascimento 1995 dalam Fang et al. 2000). Senyawa hidrogen peroksida atau H2O2 merupakan bahan pemutih yang lebih ramah lingkungan dibandingkan dengan senyawa klorin. Bahan pemutih ini sering digunakan untuk pemutihan biji-bijian, seperti gandum, kedelai, dan beras (Metzger 2002 dalam Retnowati 2008). Selanjutnya, hemiselulosa dihilangkan dengan ekstraksi menggunakan larutan NaOH 20% sehingga dihasilkan residu selulosa murni.
BAHAN DAN METODE
Alat dan BahanAlat-alat yang digunakan di antaranya adalah alat-alat kaca, oven, hot plate,
pengaduk magnet, mesin penggiling, radas penyaringan vakum, dan spektrofotometer FTIR Prestige-21 Shimadzu.
Bahan-bahan yang dipakai antara lain ampas sagu dari pabrik tepung sagu Cimahpar Bogor, akuades, HCl, pereaksi iodin, H2O2, toluena, etanol, dan NaOH.
Preparasi Contoh Ampas Sagu Ampas sagu dicuci di bawah aliran air keran hingga baunya hilang lalu dikeringkan di bawah sinar matahari selama 2 hari. Ampas sagu kering kemudian digiling dalam blender selama 5 menit dan diayak hingga terpisah dari bagian berseratnya. Bagian yang wujudnya menyerupai tepung (AS) kemudian disimpan dalam wadah dan ditutup rapat. Bagan alir penelitian dapat dilihat pada Lampiran 1.
Penghilangan Senyawa Ekstraktif (modifikasi Fang et al. 2000) dan Pati (Sun
et al. 2005)
Sebanyak 12 g AS diekstraksi dengan 240 mL campuran toluena-etanol (1:2) dengan suhu 85 oC selama 2 jam untuk menghilangkan senyawa ekstraktif. Residu bebas senyawa ekstraktif kemudian dikeringkan dalam oven selama 48 jam. Ampas sagu bebas senyawa ekstraktif (BE) ditimbang dan dihitung rendemennya.
Proses penghilangan pati ampas sagu dilakukan dengan 2 cara, yaitu ekstraksi dengan air panas dan ekstraksi dengan larutan HCl encer panas. Proses penghilangan pati dengan air panas ialah sebagai berikut: sebanyak 20 g BE diekstraksi dengan 500 mL air panas pada suhu 80 oC dan diaduk selama 30 menit. Filtrat diuji dengan larutan iodin. Jika uji iodin memberikan hasil positif (berwarna ungu), maka residu diekstraksi kembali dengan air panas yang baru hingga filtrat menunjukkan hasil negatif. Banyaknya penambahan air dihitung. Residu bebas pati dikeringkan dalam oven dengan suhu 60 oC selama 48 jam. Residu bebas pati kering hasil ekstraksi dengan air panas (BPa) kemudian ditimbang dan dihitung rendemennya.
Proses penghilangan pati dengan HCl encer ialah sebagai berikut: sebanyak 30 g AS
diekstraksi dengan 600 mL HCl 3% pada suhu 80 oC sambil diaduk hingga filtrat menunjukkan hasil uji iodin negatif. Waktu yang diperlukan hingga filtrat bebas pati dihitung. Kemudian residu dibilas dengan air hingga netral lalu dikeringkan dalam oven dengan suhu 60 oC selama 48 jam. Residu bebas pati kering hasil ekstraksi dengan HCl encer (BPc) kemudian ditimbang dan dihitung rendemennya.
Delignifikasi dan Penghilangan Hemiselulosa
Sebanyak 5 g BPc masing-masing diekstraksi dengan 125 mL H2O2 0.75, 1, dan 1.5% pH 12. Ekstraksi dilakukan dengan suhu 60 oC selama 12 jam. Campuran lalu disaring dan residu dikeringkan dalam oven bersuhu 60 oC selama 48 jam. Rendemen hasil delignifikasi dihitung. Proses delignifikasi yang terbaik menghasilkan holoselulosa (HSc) dengan warna paling putih, rendemen tinggi, dan kadar lignin rendah. Sebanyak 5 g sampel BPa juga dihilangkan ligninnya dengan proses delignifikasi menggunakan 125 mL H2O2 1.5% pH 12 untuk menghasilkan holoselulosa (HSa).
Sebanyak 5 g sampel HSc dan HSa masing-masing diekstraksi dengan 100 mL NaOH 20% selama 4 jam pada suhu kamar. Campuran lalu disaring. Residu dicuci dengan air dan etanol hingga bebas basa, lalu dikeringkan dalam oven bersuhu 60 oC selama 48 jam. Residu tersebut merupakan selulosa (Sc dan Sa).
Sampel lignin dikeringkan dalam oven 105 oC hingga bobotnya tetap kemudian ditimbang.
Analisis FTIR
Sebanyak 2 mg sampel yang halus dicampurkan ke dalam 198 mg KBR. Campuran digerus kemudian dibentuk menjadi pelet dengan diberi tekanan. Setelah terbentuk, pelet dianalisis dengan FTIR. Sampel yang dianalisis meliputi AS, BE, BPa, BPc, HSc, HSa, Sc, Sa, dan selulosa komersial (Sk).
HASIL DAN PEMBAHASAN
Pengaruh Penghilangan Senyawa Ekstraktif dan Pati
Ampas sagu (AS) (Gambar 1a) yang digunakan dalam penelitian ini memiliki kadar air, kadar abu, dan kadar lignin berturut-turut sebesar 13.49, 5.82, dan 8.95% (Lampiran 2). Warna ampas sagu yang cokelat menunjukkan keberadaan senyawa lignin yang memiliki gugus kromofor, yaitu etilena dan karbonil, serta gugus auksokrom yang dapat meningkatkan intensitas warna, yaitu alkoksil dan hidroksil.
Gambar 1 AS (ampas sagu) (a), BE (AS bebas bahan ekstraktif) (b), BPa (hasil ekstraksi BE dengan air panas) (c), dan BPc (hasil ekstraksi AS dengan HCl 3%) (d).
Proses penghilangan senyawa ekstraktif menjadikan ampas sagu lebih halus dan lebih terang (Gambar 1b). Rendemen ampas sagu bebas ekstraktif (BE) sebesar 93.74% (Lampiran 3a). Toluena bersifat nonpolar
sehingga dapat melarutkan senyawa ekstraktif yang bersifat nonpolar seperti lemak dan malam, sedangkan etanol bersifat polar sehingga dapat melarutkan senyawa ekstraktif yang bersifat polar. Oleh karena itu, campuran toluena-etanol dapat melarutkan senyawa ekstraktif berbobot molekul rendah, baik yang bersifat polar maupun bersifat nonpolar (Fengel & Wegener 1985). Kandungan senyawa ekstraktif dalam ampas sagu sangat rendah sehingga tahap penghilangan senyawa ekstraktif dapat dihilangkan dalam proses isolasi selulosa.
Sampel BE diekstraksi dengan air panas menghasilkan ampas sagu bebas pati (BPa) dengan warna lebih cokelat (Gambar 1c). Proses ekstraksi ini dilakukan sebanyak 16 kali dan memerlukan air panas sebanyak 8 liter sampai uji iodin negatif. Jika filtrat yang diuji iodin masih berwarna ungu atau biru, sampel masih mengandung pati. Warna biru terbentuk karena adanya interaksi rantai amilosa yang berbentuk spiral dengan molekul-molekul iodin. Satu kali ekstraksi lamanya 30 menit, maka total waktu yang diperlukan selama penghilangan pati adalah 8 jam. Air panas bersuhu 80 oC dapat melarutkan amilosa (Fessenden & Fessenden 1999). Amilosa dapat larut dalam air karena bersifat polar. Semakin tinggi suhu air yang digunakan, semakin banyak amilosa yang larut. Rendemen BPa didapatkan sebesar 41.46% (Lampiran 3b).
Sampel AS diekstraksi dengan HCl 3% dengan suhu 80 oC untuk menghilangkan pati. HCl akan menghidrolisis pati menjadi glukosa (Achmadi 1990). Suhu tidak boleh lebih dari 80 oC karena dapat mengakibatkan ampas sagu menjadi gosong (berwarna hitam). Larutan HCl akan memutuskan ikatan glikosida amilosa dan amilopektin sehingga menjadi satuan glukosa yang mudah larut. Warna ampas sagu bebas pati (BPc) berubah menjadi cokelat setelah dicuci dengan air hingga netral (Gambar 1d). Proses penghilangan pati dengan larutan HCl tidak memerlukan waktu yang lama dan air yang banyak seperti pada proses penghilangan pati dengan air panas. Hanya diperlukan waktu 45 menit, namun rendemen yang dihasilkan lebih rendah, yakni 26.33% (Lampiran 3c). Hal ini menunjukkan bahwa selama proses penghilangan pati dengan HCl 3%, sebagian selulosa juga ikut terurai menjadi glukosa.
menggunakan pelarut H2O2 0.75%. Kadar lignin terendah sebesar 14.55% diperoleh dengan pelarut H2O2 1.5% (Lampiran 4a). Kadar lignin ampas sagu awal dengan koreksi kadar pati 58.21% didapatkan sebesar 21.42% (Lampiran 2). Terjadi pengurangan kadar lignin sebesar 6.87% setelah proses delignifikasi dengan pelarut H2O2 1.5%.
Delignifikasi dan Penghilangan Hemiselulosa
Gambar 2 Pengaruh konsentrasi H2O2 terhadap kadar lignin.
Proses delignifikasi dilakukan dengan suhu 60 oC agar sampel tidak gosong dan H2O2 tidak menguap. Proses delignifikasi terjadi karena radikal bebas mendestruksi lignin sehingga terpecah-pecah menjadi molekul berbobot rendah yang larut dalam air (Kuznetsov et al. 2009). NaOH ditambahkan dalam proses delignifikasi untuk meningkatkan pH dan mengurangi ikatan hidrogen antarmolekul selulosa sehingga lignin dapat terpisahkan (Saad et al. 2002). Proses delignifikasi harus dilakukan dengan keadaan basa (pH 12) agar reaksi kesetimbangan hidrogen peroksida menjadi anion hidroperoksida (HOO–)bergeser ke arah kanan (Gambar 3).
Gambar 3 Reaksi kesetimbangan hidrogen peroksida.
Reaksi ini bergeser ke arah kanan karena berkurangnya konsentrasi H+ akibat bereaksi dengan OH– yang berasal dari natrium hidroksida. Semakin tinggi konsentrasi hidrogen peroksida, semakin banyak anion hidroperoksida yang dihasilkan. Spesi aktif anion hidroperoksida dapat mengeliminasi gugus kromoforik lignin. Anion ini merupakan nukleofili yang dapat menyerang gugus etilena dan karbonil yang terdapat pada senyawa lignin. Spesi aktif anion hidroperoksida dapat bereaksi kembali dengan hidrogen peroksida menghasilkan radikal bebas hidroksil (HO·).
Gambar 4 Reaksi hidrogen peroksida dengan anion hidroperoksida.
Radikal bebas hidroksil (HO·) yang dihasilkan dari dekomposisi hidrogen peroksida dapat berperan dalam proses delignifikasi dan melarutkan hemiselulosa (Pan et al. 1999).
Semakin rendah kadar lignin, warna akan semakin putih. Proses delignifikasi dengan H2O2 1.5% menghasilkan holoselulosa yang paling putih (Gambar 5). Seluruh hasil delignifikasi sampel BPc memiliki struktur yang sangat keras sehingga perlu digiling menjadi tepung dengan untuk proses selanjutnya.
Gambar 5 Hasil deliginifikasi.
Tabel 1 menunjukkan bahwa semakin tinggi konsentrasi H2O2, rendemen cenderung semakin rendah. Rendemen terendah sebesar 39.37% diperoleh pada proses penghilangan lignin menggunakan pelarut H2O2 1.5% (Lampiran 4b). Hal ini terjadi karena semakin tinggi konsentrasi H2O2, lignin yang terurai semakin banyak. Rendemen yang diperoleh untuk setiap proses ekstraksi penghilangan lignin tidak jauh berbeda.
Tabel 1 Pengaruh konsentrasi H2O2 terhadap rendemen holoselulosa.
Konsentrasi H2O2 (%)
Rendemen holoselulosa (%) 0.75 1 1.5 43.59 41.43 39.37
Hasil penelitian menunjukkan bahwa proses delignifikasi yang terbaik adalah ekstraksi dengan pelarut H2O2 1.5% karena dihasilkan holoselulosa dengan warna paling putih dan kadar lignin paling rendah. Proses delignifikasi ini digunakan untuk sampel BPa. Holoselulosa yang dihasilkan dari proses ini, berwarna putih transparan, tipis, dan keras (Gambar 6).
Gambar 6 Holoselulosa (HSa) hasil delignifikasi BPa.
Sampel HSa dan holoselulosa dengan kadar lignin terendah (HSc) masing-masing diekstraksi dengan NaOH 20% selama 4 jam dengan suhu kamar untuk menghilangkan sisa lignin dan hemiselulosa. Proses ekstraksi dengan NaOH 20% dapat mengakibatkan terbukanya untaian bagian kristalin selulosa sehingga sebagian besar lignin akan lebih terpapar keluar. Larutan NaOH dalam air protik polar, maka keberadaannya di antara rantai selulosa dapat memutus ikatan hidrogen intra- dan antar-kristalin rantai selulosa (Klemm et al. 1998 dalam Kiat 2006). Terbentuknya interaksi baru yang lebih kuat antara gugus hidroksil selulosa ampas sagu dan larutan NaOH menyebabkan terbukanya bagian kristalin selulosa tersebut. Selain itu, hemiselulosa larut di dalam larutan NaOH 20% sehingga dihasilkan selulosa murni, yaitu Sa dan Sc. Sa berwarna putih dengan tekstur yang lebih halus dan empuk dibandingkan dengan HSa, sedangkan Sc bertekstur keras dan berwarna lebih putih daripada HSc (Gambar 7). Baik Sa maupun Sc memiliki tekstur seperti selulosa komersial setelah dihaluskan.
Gambar 7 Selulosa komersial (a), Sa (b), dan Sc (c).
Analisis FTIR
Spektrum inframerah selulosa dicirikan oleh serapan pada bilangan gelombang sekitar 3400 cm-1 (ulur O-H), 2800–3000 cm-1 (ulur C-H), 1000–1100 cm-1 (ulur C-O), dan 897 cm-1 (ikatan β-glikosida) (Gupta 1987 dalam Sun et al. 1999). Hasil analisis FTIR menunjukkan AS mengandung selulosa
(Tabel 2). Spektrum inframerah BE lebih halus dan serapannya lebih lemah dibandingkan dengan AS (Lampiran 5a). Namun, secara keseluruhan letak bilangan gelombang serapan spektrum inframerah BE tidak jauh berbeda dengan AS. Proses penghilangan senyawa ekstraktif dapat tidak dilakukan pada proses isolasi selulosa karena kadar senyawa ekstraktif rendah dan spektrum inframerah AS mirip dengan BE.
Terjadi perbedaan spektrum FTIR BPa dan BPc. BPc memiliki serapan ulur C=O karena terjadi pembukaan cincin glukosa dalam keadaan asam (Fessenden & Fessenden 1999). Namun, serapan ulur O-H, ulur H, ulur C-O, dan ikatan β-glikosida pada BPc lebih tinggi dibandingkan dengan BPa (Lampiran 5b). Gugus-gugus fungsi yang dimiliki oleh selulosa sama dengan pati. Oleh karena itu, proses penghilangan pati menurunkan intensitas serapan pada bilangan gelombang sekitar 3260–3280 (ulur O-H), 2900 (ulur C-H), dan 1040 cm-1 (ulur C-O) pada spektrum BPa dan BPc dibandingkan dengan AS (Lampiran 5e dan 5f).
Struktur lignin memiliki gugus aromatik. Ulur C-H aromatik terletak pada bilangan gelombang 1500, 1605, dan 3017 cm-1 (Silverstein et al. 2005). Selain itu, serapan benzena tersubstitusi pada bilangan gelombang 750–850 cm-1 juga menunjukkan keberadaan lignin (Creswell et al. 2005). Proses penghilangan lignin BPa berhasil karena terjadi penurunan intensitas serapan pada bilangan gelombang 3000, 1500, dan 1720 cm-1 (ulur C=O lignin), serta 750–850 cm-1 (Lampiran 5e). Ikatan β-glikosida pada 897 cm-1 terlihat jelas pada spektrum inframerah HSa dan HSc. Spektrum inframerah HSa secara keseluruhan memiliki intensitas serapan lebih rendah dibandingkan dengan HSc (Lampiran 5c). Serapan C-H aromatik lignin masih terlihat pada bilangan gelombang 1504 cm-1 spektrum inframerah HSc yang menunjukkan bahwa proses delignifikasi masih menyisakan lignin. Serapan gugus C=O terlihat pada spektrum HSc yang diduga berasal dari struktur glukosa rantai terbuka (Lampiran 5f).
Proses penghilangan hemiselulosa dengan ekstraksi menggunakan NaOH 20% dapat melarutkan sisa lignin tersebut. Terbukti Sa memiliki kadar lignin lebih rendah daripada HSa sebagaimana ditunjukkan oleh intensitas serapan inframerah Sa pada bilangan gelombang 3000 dan 750–850 cm-1 yang lebih rendah dibandingkan dengan HSa (Lampiran 5e). Hemiselulosa memiliki serapan
Tabel 2 Hasil analisis FTIR
Sampel
Bilangan gelombang
(cm-1)
Serapan Sampel
Bilangan gelombang
(cm-1)
Serapan AS BE BPa BPc 3304 2894 1504 1146 897 3280 2895 1504 1147 897 3267 2897 1504 1038 897 3287 2905 1504 1610 1037 897 ulur O-H ulur C-H ulur cincin aromatik ulur C-O ikatan β -glikosida ulur O-H ulur C-H ulur cincin aromatik ulur C-O ikatan β -glikosida ulur O-H ulur C-H ulur cincin aromatik ulur C-O ikatan β -glikosida ulur O-H ulur C-H ulur cincin aromatik ulur C=O ulur C-O ikatan β -glikosida HSa HSc Sa Sc Sk 3287 2905 1037 897 3337 2905 1610 1030 897 3267 2895 1138 897 3304 2894 1610 1146 897 3280 2895 1147 897 ulur O-H ulur C-H ulur C-O ikatan β -glikosida ulur O-H ulur C-H ulur C=O ulur C-O ikatan β -glikosida ulur O-H ulur C-H ulur C-O ikatan β -glikosida ulur O-H ulur C-H ulur C=O ulur C-H ikatan β -glikosida ulur O-H ulur C-H ulur C-O ikatan β -glikosida
inframerah asam uronat (1593 cm-1) dan xilan (1150 cm-1) (Fang et al. 2000). Selain itu, hemiselulosa memiliki gugus-gugus fungsi yang hampir sama dengan selulosa. Oleh karena itu, proses penghilangan hemiselulosa juga mengakibatkan penurunan intensitas serapan pada bilangan gelombang sekitar 3267, 2897, 1593, 1150, dan 1037 cm-1 (Lampiran 5e). Spektrum Sa mirip dengan spektrum Sk dengan serapan lebih lemah. Terlihat perbedaan spektrum Sc dan Sk pada bilangan gelombang 1610 cm-1 (Lampiran 5d). Spektrum Sc memiliki serapan gugus C=O yang sangat besar akibat proses penghilangan pati dengan HCl 3%. Namun, serapan gugus-gugus fungsi selulosa yang dimiliki Sc lebih kuat daripada Sa dan Sk (Lampiran 5d). Hal ini menunjukkan bahwa kemurnian Sc lebih tinggi dibandingkan dengan Sa.
SIMPULAN DAN SARAN
SimpulanSaran
Perlu dicari metode penghilangan pati yang lain karena proses penghilangan pati dengan air panas menghabiskan banyak waktu dan air. Katalis juga diperlukan pada proses delignifikasi dengan menggunakan H2O2 agar dapat berlangsung dengan waktu yang lebih singkat.
DAFTAR PUSTAKA
Achmadi SS. 1990. Kimia Kayu. Bogor: IPB Pr.
Bintoro MH. 2008. Bercocok Tanam Sagu. Bogor: IPB Pr.
Cahyani RD. 2010. Asetilasi selulosa ampas sagu dan aplikasinya sebagai fase diam kromatografi kolom [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Creswell et al. 1972. Spectrum Analysis of Organic Compound. Minnesota: Burgess.
Fang JM, Sun RC, Tomkinson J. 2000. Isolation and characterization of hemicelluloses and cellulose from rye straw by alkaline peroxide extraction.
Cellulose 7:87-107.
Fengel D, Wegener G. 1985. Kayu: Kimia, Ultrastruktur, Reaksi-reaksi. Hardjono S, Soenardi P, penerjemah; Yogyakarta: Penerbit Universitas Gajah Mada. Terjemahan dari: Wood: Chemistry, Ultrastructure, Reactions.
Fessenden RJ, Fessenden JS. 1999. Organic Chemistry. Ed ke-3. California: Wadsworth.
Irawadi TT. 2010. Teknologi separasi bahan aktif temu lawak menggunakan biopolimer termodifikasi berbasis limbah produksi sagu [laporan penelitian]. Bogor: Lembaga Penelitian dan Pengabdian kepada Masyarakat, Institut Pertanian Bogor.
Irfana L. 2010. Isolasi dan asetilasi ampas sagu dengan katalis I2 serta aplikasinya sebagai fasa diam kromatografi kolom [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Kiat LJ. 2006. Preparation and characterization of carboxymethyl sago waste and it’s hydrogel [tesis]. Malaysia:
Master of Science, Universiti Putra Malaysia.
Kuznetsov et al. 2009. Abies wood delignification by acetic acid-hydrogen peroxide mixturre under the action of TiO2 catalysts and UV irradiation. Siberian Fed Univ 2:19-24.
Matitaputty PR, Alfons JB. 2006. Inovasi teknologi pakan berbahan dasar “ela sagu” untuk ternak. Di dalam: Prosiding Lokakarya Sagu dalam Revitalisasi Pertanian Maluku; Ambon 29-31 Mei 2006. Ambon: Fakultas Pertanian Universitas Pattimura. hlm 120-131.
Pan et al. 1999. Atmospheric acetic acid pulping of rice straw. Holzforschung
53:49-55.
Retnowati DS. 2008. Pemutihan enceng gondok menggunakan H2O2 dengan katalisator natrium bikarbonat [skripsi]. Semarang: Fakultas Teknik Universitas Negeri Dipenogoro.
Saad MB et al. 2002. Effect of delignification with NaOH and H2O2 in the enzymatic hydrolysis of sugarcane bagasse pretreated by steam explosion. Ind Biotechnol 4:11-20.
Santi. 2006. Onggok sagu termodifikasi sebagai fase diam dalam kromatografi kolom [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Setyawati, Muawanah, Hisdayanti. 2002. Hidrolisis pati sagu menjadi glukosa menggunakan katalisator asam klorida. J Teknol Ind 1:19-22.
Sharim Z et al. 2008. Production of reducing sugars by Trichoderma sp. KUPM0001 during solid substrate fermentation of sago starch processing waste hampas. Res J Microbiol 4:25-33.
Silverstein RM et al. 2005. Spectrometric Identification of Organic Compounds. Ed ke-7. New York: Wiley.
SNI 0492. 2008. Cara Uji Kadar Lignin Pulp dan Kayu Metode Klason. Jakarta: Badan Standardisasi Nasional.
Sun RC, Jones GL, Tomkinson J, Bolton J. 1999. Fractional isolation and partial characterization of non-starch polysaccharides and lignin from sago pith.
Industrial Crops and Products 19:211-220.
Susanto AN. 2006. Potensi dan perhitungan luas lahan sagu untuk perencanaan ketahanan pengan spesifik lokasi di
Provinsi Maluku. Di dalam: Prosiding Lokakarya Sagu dalam Revitalisasi Pertanian Maluku; Ambon, 29-31 Mei 2006. Ambon: Fakultas Pertanian Universitas Pattimura. hlm 173-184.
Syakir M, Bintoro MH, Agusta H. 2009. Pengaruh ampas sagu dan kompos terhadap produktivitas lada perdu. J Litri
4:168-173.
9
10
Lampiran 1 Bagan alir penelitian
Analisis FTIR
AS
BE
BPa
BPc
HSa
HSc
Sa
Sc
Sk
Serbuk Ampas Sagu (AS)
30 g sampel AS diekstraksi
dengan 600 mL HCl 3% pada
suhu 80
oC selama 30 menit
Selulosa (Sa)
5 g HSc diekstraksi dengan 100
mL NaOH 20 % selama 4 jam
pada suhu kamar
Uji iodin filtrat negatif
5 g BPa diekstraksi dengan 125 mL
1.5% H
2O
2pH 12, 55
o
C, 12 jam
12 g sampel AS diekstraksi dengan
240 mL toluena:etanol (1:2) pada
suhu 85
oC selama 2 jam
20 g BE diekstraksi dengan 500 mL
air panas pada suhu 80
oC dan
diaduk selama 30 menit
5 g BPc diekstraksi dengan 125
mL 0.75, 1, 1.5% H
2O
2pH 12,
55
oC, 12 jam
5 g HSa diekstraksi dengan 100
mL NaOH 20 % selama 4 jam
pada suhu kamar
11
Lampiran 2 Kadar air, kadar abu, dan kadar lignin ampas sagu
(a) Kadar air ampas sagu
Bobot awal (g) Bobot cawan kosong (g) Bobot cawan + bobot kering
(g) Bobot kering (g) Bobot kering (g) Kadar air (%)
2.5042 65.8810 68.0446 2.1636 0.3406 13.60
2.5002 51.0674 53.2296 2.1622 0.3380 13.52
2.5033 64.0889 66.2559 2.1670 0.3363 13.43
2.5021 63.9248 66.0919 2.1671 0.3350 13.39
Rerata kadar air 13.49
(b) Kadar abu ampas sagu
Bobot awal (g)
Bobot cawan kosong (g)
Bobot cawan + bobot abu (g)
Bobot abu (g)
Kadar abu (%)
2.0027 60.2987 68.0446 0.0583 5.83
2.0104 47.0636 53.2296 0.0581 5.81
Rerata kadar abu 5.82
(c) Kadar lignin ampas sagu
Bobot awal (g)
Bobot kertas saring (g)
Bobot kertas saring + bobot lignin (g)
Bobot lignin (g)
Kadar lignin (%)
1.0172 1.0988 1.1947 0.0959 9.43
1.0100 1.1116 1.1972 0.0856 8.48
Rerata kadar lignin 8.95
* Kadar lignin dengan koreksi penghilangan pati
100% pati kadar 100 awal sampel lignin Kadar pati bebas sampel lignin Kadar 21.42% 100% 58.21 100 8.95 pati bebas sampel lignin
Kadar
12
Lampiran 3 Rendemen BE, BPa, dan BPc
(a) Rendemen BE
Bobot AS (g) Bobot BE (g) Rendemen BE (%)
Bobot yang hilang selama proses penghilangan senyawa
ekstraktif (%)
12.1231 11.1051 91.60 8.40
12.0287 11.5334 95.88 4.12
Rerata 93.74 6.26
(b)Rendemen BPa
Bobot BE (g)
Bobot wadah (g)
Bobot wadah + bobot BPa (g)
Bobot BPa (g)
Rendemen BPa (%)
Bobot yang hilang (%)
20.0987 1.2175 9.7605 8.5430 42.51 57.49
20.0327 1.3225 9.4172 8.0947 40.41 59.59
Rerata 41.46 58.54
(c) Rendemen BPc
Bobot AS (g)
Bobot wadah (g)
Bobot wadah + bobot BPc (g)
Bobot BPc (g)
Rendemen BPc (%)
Bobot yang hilang (%)
30.1420 0.9532 8.8822 7.9290 26.31 73.69
30.2160 0.8908 8.6225 7.7317 25.59 74.41
30.1150 0.7785 8.1506 7.3721 24.48 75.52
30.0549 0.7768 9.0917 8.3149 27.67 72.33
30.0820 1.1927 9.2516 8.0589 26.79 73.21
30.1370 1.0741 9.6981 8.6240 28.62 71.38
30.0532 1.1845 8.1935 7.0090 23.32 76.68
30.1063 1.0733 8.5657 7.4924 24.89 75.11
30.1922 0.7958 8.7068 7.9110 26.20 73.80
60.1908 2.5601 20.3092 17.7491 29.49 70.51
13
Lampiran 4 Kadar lignin dan rendemen hasil delignifikasi
(a)Kadar lignin hasil delignifikasi
Konsentrasi H2O2 (%)
Bobot awal (g)
Bobot kertas saring (g)
Bobot kertas saring + bobot lignin
(g)
Bobot lignin (g)
Kadar lignin (%)
Rerata (%)
0.75 1.0024 1.1531 1.3816 0.2285 22.80
22.17 0.75 1.0103 1.0932 1.3109 0.2177 21.55
1 1.0074 1.1333 1.3219 0.1886 18.72
18.64 1 1.0096 1.0939 1.2813 0.1874 18.56
1.5 1.0017 1.1072 1.1667 0.1463 14.61
14.55 1.5 1.0061 1.0982 1.2441 0.1459 14.50
(b)
Rendemen hasil delignifikasiKonsentrasi H2O2 (%)
Bobot awal (g)
Bobot kertas saring (g)
Bobot kertas saring + bobot HSc
(g)
Bobot HSc
(g)
Rendemen (%)
Rerata (%)
0.75 5.0515 0.4941 2.6550 2.1604 42.78
43.59 0.75 5.0471 0.3868 2.6283 2.2415 44.41
1 5.0450 0.4994 2.5402 2.0408 40.45
41.43 1 5.0568 0.7244 2.8693 2.1449 42.42
1.5 5.0715 0.4259 2.3967 1.9708 38.86
14
Lampiran 5 Spektrum FTIR AS, BE, BPa, BPc, HSc, HSa, Sa, Sc, dan Sk
(a) Spektrum FTIR AS dan BE.
15
lanjutan Lampiran 5
(c) Spektrum FTIR HSa dan HSc.
16
lanjutan Lampiran 5
(e) Spektrum FTIR AS, BE, BPa, HSa, dan Sa.