Dengan ini saya menyatakan bahwa tesis Evaluasi Nilai Biologis dan Indeks Glikemik Mi Jagung Substitusi Kering dan Instan adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi dan kutipan dari karya penulis lain, yang diterbitkan maupun yang tidak diterbitkan, telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, April 2011
Biological Value Evaluation and Index Glycemic of Dry Corn Noodle and Instant Corn Noodle Substitution
and , .
Corn flour is potentially used as a raw material in noodle formulation. The previous study showed that 30% of corn flour was used as a substitute of wheat flour in dried and instant noodle. The corn flour substituted noodle applied drying or frying process at a high temperature, which may affect the nutritional content and biological value of the noodle. For this reason the effect of heating process (drying or frying) during noodle processing on chemical composition and biological value of corn flour substituted noodle was studied. The wet noodle was dried in oven at 60oC for 70 minutes to produce dried noodle and fried in cooking oil at 160oC for 4 minutes to produce instant noodle. The noodles were evaluated in terms of chemical composition and glycemic index. Commercial instant noodles were also analyzed as a comparison.
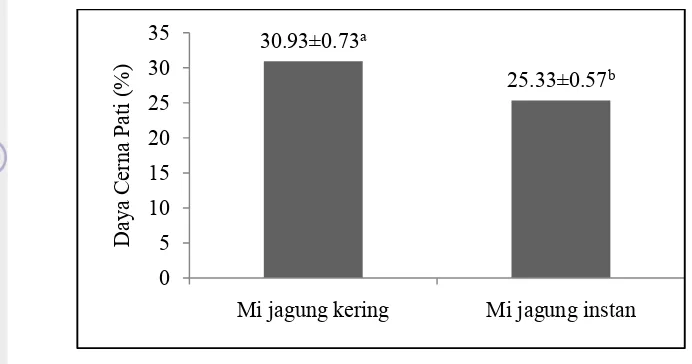
The amylose content of dried noodle substituted with 30% corn flour was 30.99% which was higher than that of instant noodle substituted with 30% corn flour (28.85%). The content of resistant starch of corn flour substitued dried and instant noodle corn was 14.80% and 17.25% respectively. Starch and soluble fiber digestibility of dried corn noodle was significantly different from these of instant corn noodle, which were 30.93% and 0.49%, and 25.33% and 0.68% respectively, whereas protein digestibility was relatively the same. The glycemic index of dried and instant corn noodle substitution and commercial noodle was categorized as a low glycemic index (54.18%; 51.33 and 48.65%), whereas the glycemic load of them was 26.12; 22.18 and 18.63 respectively and was categorized as a high and middle glycemic load. Drying or frying process did not significantly affect the glycemic index of both dried and instant corn noodle substituted.
. Evaluasi Nilai Biologis dan Indeks Glikemik Mi Jagung
Substitusi Kering dan Instan. dan
.
Tepung jagung merupakan salah satu bahan pangan yang berpontensi untuk dikembangkan, salah satunya digunakan dalam formulasi produk mi. Hasil penelitian sebelumnya menunjukkan bahwa tepung jagung dapat menyubstitusi tepung terigu hingga 30%. Karakteristik mutu fisik mi jagung substitusi kering dan instan yang dihasilkan adalah mi yang kenyal, sedikit agak keras, tidak lengket, agak elastis dan tidak mudah putus. Proses pemanasan memiliki pengaruh signifikan terhadap komposisi kimia dan nilai gizi dari produk yang kaya karbohidrat. Pengaruh pemanasan terhadap karakteristik fungsional karbohidrat berkaitan erat dengan indeks glikemik. Makanan yang memiliki indeks glikemik rendah atau tidak cepat menaikkan kadar glukosa darah dibutuhkan oleh penderita diabetes. Kajian mengenai pengaruh pemanasan terhadap evaluasi nilai biologis dan indeks glikemik pada proses produksi mi jagung substitusi ini penting bagi penderita diabetes untuk lebih selektif dalam memilih dan mengkonsumsi bahan pangan.. Tujuan penelitian ini adalah untuk (1) menentukan pengaruh pemanasan terhadap komposisi kimia dan nilai evaluasi biologis mi kering dan mi instan yang disubstitusi dengan tepung jagung dan; (2) menentukan indeks glikemik mi jagung substitusi kering dan instan dibandingkan dengan mi terigu komersial.
Penelitian dibagi menjadi tiga tahap yaitu tahap pembuatan dan karakterisasi tepung jagung dengan metode kering, tahap pembuatan mi jagung substitusi kering dan instan, dan pengukuran IG produk mi jagung kering, mi jagung instan dan mi komersil. Proses pembuatan mi jagung substitusi kering dan instan adalah memformulasikan 30% tepung jagung dengan tepung terigu. Campuran tepung jagung dan tepung terigu ditambahkan bahan tambahan lain, kemudian dibentuk lembaran, dan untaian mi, dipotong dan dikukus pada suhu 95oC selama 15 menit. Selanjutnya mi yang telah dikukus dikeringkan dengan oven pada suhu 60 oC selama 70 menit sehingga diperoleh mi jagung kering, atau digoreng pada suhu 160 oC selama 4 menit untuk mi jagung instan.
Mi jagung subsitusi kering dan instan dianalisis komposisi kimia, evaluasi nilai biologis dan indeks glikemik ( ). Analisis kimia mencakup analisis proksimat, analisis kadar pati metode hidrolisa asam dan analisis kadar amilosa. Analisis nilai biologis meliputi kadar pati resisten secara , kadar serat pangan metode enzimatis, daya cerna pati secara enzimatis dan daya cerna protein secara dengan teknik multienzim. Analisis kadar glukosa darah sukarelawan dilakukan untuk penetapan indeks glikemik mi jagung substitusi kering dan instan serta mi komersial.
Daya cerna protein mi jagung substitusi kering dan instan relatif sama yaitu sebesar 81.87% dan 80.26%.
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Judul Tesis : Evaluasi Nilai Biologis dan Indeks Glikemik Mi Jagung Substitusi Kering dan Instan
Nama : Nono Hartono NRP : F251080041 Progam Studi : Ilmu Pangan
Menyetujui Komisi Pembimbing
Dr. Ir. Feri Kusnandar, M.Sc Dr. Ir. Nurheni Sri Palupi, M.Si
Ketua Anggota
Mengetahui
Ketua Program Studi Dekan Sekolah Pascasarjana Ilmu Pangan
Dr. Ir. Ratih Dewanti Haryadi, M.Sc Dr. Ir.Dahrul Syah, M.Sc
Alhamdulillah, penulis panjatkan puji dan syukur kehadirat Allah SWT atas rahmat dan karunia=Nya sehingga penulisan tesis dengan judul Evaluasi Nilai Biologis dan Indeks Glikemik Mi Jagung Substitusi Kering dan Instan” dapat diselesaikan. Tesis ini disusun sebagai salah syarat untuk memperoleh gelar Magister Sains pada Sekolah Pascasarjana, Institut Pertanian Bogor.
Pada kesempatan ini penulis menyampaikan ucapan terima kasih kepada:
1. Bapak Dr. Ir. Feri Kusnandar, M.Sc dan Ibu Dr. Ir. Nurheni Sri Palupi, M.Si selaku dosen pembimbing yang telah banyak memberikan arahan, bimbingan dan pendanaan sehingga penulis dapat menyelesaikan tesis ini.
2. Ibu Dr. Ir. Didah Nur Faridah, M.Si selaku dosen penguji luar komisi yang telah banyak memberikan saran untuk penyempurnaan tesis ini.
3. Kedua orang tua (H. Rudika dan Hj. Ina), kakak tercinta (Runiah, Sulastri, Kartini, Adnan dan Deli), keponakan tercinta (Rafli, Dia, Putri dan Shaznaz) serta keluarga besar atas doa, pengorbanan, semangat dan kasih sayang yang telah diberikan.
4. Bapak Nurwahid, Bapak Rojak, Mba Ari beserta staf Teknisi Laboratorium
Departemen Ilmu dan Teknologi Pangan,
5. Sahabat seperjuangan IPN 2008 : Mba (Alina Primasari, Avrilia, Luna, Elisa,
Nunung, Titin, Erlina, Nindira), Mas (Andi, Zaki, Arif, Anas, Wahyu, Isak, Nanang) atas segala bantuan dan motivasinya
6. Ayu Anggraeni yang telah memberikan semangat dan motivasi.
7. Teman=teman Al=Fath (Erik, Ridwan, Irfan, Aan, Zali, Gonggo, Fian) yang telah membantu penulis secara moril.
Ucapan terima kasih yang sebesar=besarnya kepada Tim Manajemen Program KP3T (Kerjasama Penelitian Pertanian dengan Perguruan Tinggi) Departemen Pertanian atas bantuan dana penelitian yang telah diberikan sehingga penelitian ini dapat berjalan. Semoga karya ilmiah ini bermanfaat.
Bogor, April 2011
!
Pada tahun 2003 penulis lulus dari SMUN 1 Arjawinangun, Kabupaten Cirebon. Pendidikan Sarjana ditempuh di Program Studi Teknologi Hasil Perikanan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor dan lulus tahun 2008. Pada tahun yang sama penulis melanjutkan jenjang Magister Sains di Program Studi Ilmu Pangan, Sekolah Pascasarjana, Institut Pertanian Bogor.
Hal
JUDUL ... i
ABSTRACT ... ii
RINGKASAN ... iii
DAFTAR ISI ... v
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... ix
I. PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Tujuan Penelitian... 4
1.3 Hipotesis Penelitian ... 4
1.4 Manfaat Penelitian... 4
II. TINJAUAN PUSTAKA ... 5
2.1 Jagung ... 5
2.1.1 Struktur Biji Jagung ... 5
2.1.2 Komposis Kimia Jagung ... 6
2.2 Tepung Jagung ... 8
2.2.1 Definisi Tepung Jagung ... 8
2.2.2 Komposisi Kimia dan Teknologi Produksi Tepung Jagung ... 8
2.3 Mi Jagung ... 10
2.3.1 Definisi dan Keunggulan Mi jagung ... 10
2.3.2 Teknologi Produksi dan Karakteristik Mi Jagung Substitusi... 11
2.4 Indeks dan Beban Glikemik ... 13
2.4.1 Indeks Glikemik ... 13
2.4.1.1 Definisi Indeks Glikemik ... 13
2.4.1.2 Pemecahan dan Penyerapan Karbohidrat ... 14
2.4.1.3 Faktor=Faktor yang Mempengaruhi Indeks Glikemik... 15
2.4.2 Beban Glikemik ... 19
2.5 Diabetes Mellitus ... 20
III. METODOLOGI ... 22
3.1 Waktu dan Tempat Penelitian ... 22
3.2 Bahan dan Alat ... 22
3.2.1 Bahan ... 22
vi
3.3 Tahapan Penelitian ... 23
3.3.1 Pembuatan Tepung Jagung ... 24
3.3.2 Pembuatan Mi Jagung Substitusi Kering dan Instan ... 25
3.3.3 Pengukuran Indeks Glikemik ... 26
3.4 Metode Analisis ... 27
3.4.1 Analisis Kimia ... 28
3.4.1.1 Analisis Proksimat (AOAC 1995) ... 28
3.4.1.2 Analisis Kadar Pati Metode Hidrolisa Asam (Modifikasi Sudarmadji 1997) ... 28
3.4.1 3 Analisis Kadar Amilosa (Apriyantono . 1989) ... 29
3.4.2 Analisis Evaluasi Nilai Biologis ... 30
3.4.2.1 Analisis Kadar Pati Resisten secara (Modifikasi Goni . 1996) ... 30
3.4.2.2 Analisis Kadar Serat Pangan Metode Enzimatis (AOAC 1995) ... 31
3.4.2.3 Analisis Daya Cerna Pati secara Enzimatis (Muchtadi . 1989) ... 33
3.4.2.4 Analisis Daya Cerna Protein secara in vitro dengan Teknik Multienzim ... 34
3.4.3 Pengukuran Indeks dan Beban Glikemik (Miller . 1996) ... 35
3.4.3.1 Pengukuran Indeks Glikemik ... 35
3.4.3.2 Pengukuran Beban Glikemik ... 36
3.5 Rancangan Percobaan (Steel dan Torrie 1993) ... 36
IV. HASIL DAN PEMBAHASAN ... 38
4.1 Komposisi Kimia Tepung Jagung, Mi Jagung Substitusi Kering dan Instan serta Mi Komersial ... 38
4.2 Evaluasi Nilai Biologis Mi Jagung Substitusi Kering dan Instan ... 41
4.2.1 Pati Resisten ... 41
4.2.2 Daya Cerna Pati ... 44
4.2.3 Serat Pangan ... 46
4.2.4 Daya Cerna Protein ... 48
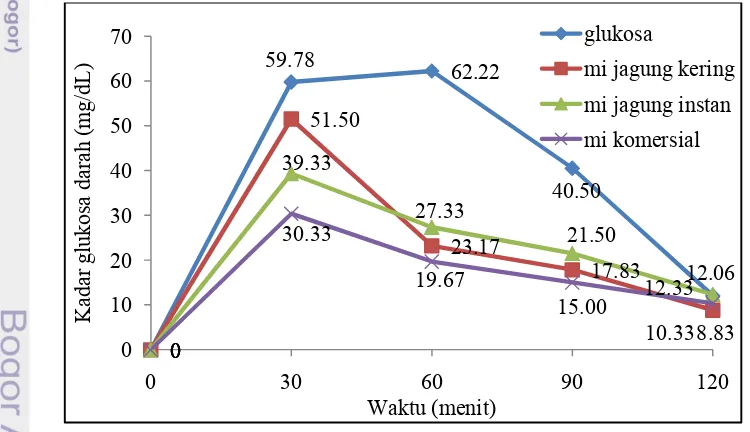
4.3 Indeks Glikemik Mi Jagung Substitusi Kering dan Instan serta Mi Komersial ... 50
V. KESIMPULAN DAN SARAN ... 55
VI. DAFTAR PUSTAKA ... 56
vii Hal
1. Komposisi kimia jagung ... 6
2. Kandungan amilosa dan amilopektin dari beberapa varietas jagung ... 7
3. Komposisi kimia tepung jagung ... 9
4. Indeks dan beban glikemik serelia, mi dan pasta ... 20
5. Tahapan kegiatan penelitian dan analisis ... 23
6. Hasil analisis kimia tepung jagung, mi jagung substitusi kering dan instan serta mi komersial ... 38
7. Kandungan serat pangan mi jagung substitusi kering dan instan ... 47
viii Hal
1. Struktur biji jagung ... 5
2. Teknologi proses produksi mi jagung ... 12
3. Kurva pengukuran indeks glikemik ... 14
4. Pembuatan tepung jagung dengan penggilingan kering ... 24
5. Pembuatan mi jagung substitusi kering dan instan tepung jagung 30% ... 26
6. Pengukuran indeks glikemik ... 27
7. Kadar pati resisten mi jagung substitusi kering dan instan ... 42
8. Daya cerna pati mi jagung substitusi kering dan instan ... 45
9. Daya cerna protein mi jagung substitusi kering dan instan ... 49
ix Hal
1. Form pengukuran indeks glikemik ... 64
2. Penentuan glukosa, fruktosa dan gula invert dalam suatu bahan dengan metode Luff=Schoorl ... 64
3. Analisis data kimia tepung jagung, mi jagung substitusi kering dan instan ... 65
4. Uji t kadar air ... 65
5. Uji t kadar abu ... 66
6. Uji t kadar protein ... 66
7. Uji t kadar lemak ... 67
8. Uji t kadar karbohidrat ( ) ... 68
9. Uji t kadar pati ... 68
10. Uji t kadar amilosa... 69
11. Uji t kadar amilopektin ... 69
12. Analisis data pati resisten ... 70
13. Uji t pati resisten ... 70
14. Analisis data daya cerna pati ... 71
15. Uji t daya cerna pati ... 71
16. Analisis data serat pangan ... 71
17. Uji t serat pangan tak larut... 72
18. Uji t serat pangan larut ... 72
19. Uji t serat pangan total ... 73
20. Analisis data daya cerna protein ... 73
21. Uji t daya cerna protein ... 73
22. Indeks glikemik mi jagung substitusi kering ... 74
23. Indeks glikemik mi jagung substitusi instan ... 76
24. Indeks glikemik mi komersil ... 77
25. Perhitungan beban glikemik ... 77
26. Uji Duncan indeks glikemik ... 78
"#" $%"&"'(
Mi merupakan produk pangan yang dibuat dari adonan terigu atau tepung lainnya sebagai bahan utama dengan atau tanpa penambahan bahan tambahan lainnya. Di Indonesia dikenal dua macam mi, yaitu mi basah dan mi kering. Mi basah umumnya memiliki masa simpan hanya sekitar 36 jam. Mi kering adalah mi mentah yang mengalami proses pemananasan dengan cara pengeringan dengan oven dan memiliki kadar air sekitar 10%. Mi kering mempunyai masa simpan hingga beberapa bulan, tergantung kadar air dan cara penyimpanannya. Salah satu
contoh dari dari mi kering adalah mi instan (Astawan 2005). Mi instan ( ) adalah mi mentah yang telah mengalami pengukusan dan
penggorengan (Kusnandar 2009). Salah satu bahan pangan yang potensial untuk dikembangkan dalam formulasi produk mi adalah jagung.
Mi jagung merupakan mi yang dibuat dengan bahan utama hasil olahan jagung (tepung jagung). Mi jagung dapat dihasilkan dari 100% tepung jagung atau substitusi dalam tepung terigu. Perbedaan yang mendasar dari kedua mi jagung tersebut adalah adanya perlakuan pregelatinisasi pada pembuatan mi jagung 100% tepung jagung, sedangkan pada mi jagung substitusi hanya mencampurkan dengan tepung terigu. Rendahnya kandungan protein gluten menjadi penyebab pregelatinisasi tersebut dilakukan. Penelitian sebelumnya menunjukkan tepung jagung yang optimal untuk diformulasikan dalam pembuatan mi jagung substitusi kering (Putra 2008) dan instan (Stevanus 2010) adalah substitusi 30% tepung jagung. Karakteristik mutu fisik mi jagung substitusi kering dan instan yang dihasilkan adalah mi yang kenyal, sedikit agak keras, tidak lengket, agak elastis dan tidak mudah putus.
2 Proses pengolahan yang melibatkan panas merupakan salah satu cara yang merubah kandungan dan kualitas gizi khususnya karbohidrat pangan (pati, amilosa, serat pangan dan pati resisten) (Collings . 1981). Proses penggorengan yang melibatkan transfer panas dari minyak ke dalam pangan
menyebabkan denaturasi protein, gelatinisasi pati pada kadar air yang rendah, pembentukan dan warna. Penggorengan dapat meningkatkan terbentuknya
pati resisten yang dapat dijadikan indikator penurunan daya cerna pati pada produk kentang goreng (Pokorny (1999).
Pada pembuatan spageti (terigu) menurunkan daya cerna pati sebesar 23.4% dan 27.4%, serta meningkatkan pembentukan pati resisten tipe III sebesar 2.2% dan 1.5%. Nilai daya cerna pati yang rendah dan tingginya pati resisten merupakan indikator terhadap penurunan indeks glikemik pangan (Casigrahi . 1992). Pengeringan tepung yang berasal dari kacang=kacangan dengan oven pada suhu 75 oC selama 6 jam meningkatkan daya cerna protein sebesar 12=15 % dibandingkan kontrol. Proses pemanasan menyebabkan terputusnya ikatan peptida protein menjadi asam amino yang mudah dicerna enzim (Cabrejas . 2009). Pemanasan dengan cara pengukusan biasa dan bertekanan meningkatkan daya cerna pati (ditunjukkan dengan rendahnya pembentukan pati resisten), daya cerna protein dan pembentukan pati serat pangan larut dan tak larut dari berbagai varietas beras (Sagum dan Arcot 2000).
Pengaruh pemanasan terhadap karakteristik fungsional karbohidrat berkaitan erat dengan indeks glikemik (IG). Pangan dengan jenis yang sama bila diolah dengan cara yang berbeda dapat memiliki IG yang berbeda, karena pengolahan dapat menyebabkan perubahan struktur dan komposisi kimia pangan
(Rimbawan dan Siagian 2004). Indeks glikemik (IG) pangan merupakan pendekatan untuk memilih pangan khususnya pangan berkarbohidrat. Pendekatan
yang baru dalam menentukan kecepatan kenaikan kadar glukosa darah adalah beban glikemik. Beban glikemik memberikan informasi yang lebih lengkap mengenai pengaruh konsumsi aktual karbohidrat per saji terhadap peningkatan kadar gula darah (Powell . 2002).
3 dibandingkan indeks glikemik kentang yang diproses tunggal (direbus atau dilumatkan) yaitu 57% dan 83% (Jimoh . 2008). Penyimpanan produk intermediet kentang pada suhu 5 oC dan kemudian diolah dengan cara direbus, dioven dan dilumatkan menurunkan indeks glikemik kentang yaitu 76%, 73% dan
75% dibandingkan indeks glikemik produk kentang yang tidak mengalami penyimpanan dingin yaitu 104%, 95% dan 106% dengan roti sebagai standar.
Proses penyimpanan menginisiasi pembentukan pati resisten melalui proses retrogradasi amilosa yang sulit untuk dicerna oleh enzim pencernaan dan lambat diubah menjadi glukosa (Tahvonen . 2006).
Kajian pengaruh pengolahan produk menunjukkan sukarelawan yang mengkonsumsi produk lentil yang telah mengalami proses perebusan selama 20 menit atau dikeringkan selama 12 jam pada suhu 121.1 oC menyebabkan perbedaan respon kenaikan glukosa darah. Pengeringan selama 12 jam menyebabkan peningkatan kadar glukosa darah sukarelawan sebesar 2.44 ± 0.3 mmol/l dibandingkan perebusan selama 20 menit yang hanya 0.87 !0.11 mmol/l. Peningkatan pelepasan glukosa pada pangan yang dikeringkan disebabkan oleh proses pengeringan menurunkan senyawa antinutrisi yang tidak tahan panas sehingga meningkatkan ketersediaan pati untuk dipecah enzim menjadi glukosa dan dicerna dalam tubuh (Jenkins . 1982).
Proses pengeringan beras instan varietas pada suhu 150 oC mampu menurunkan indeks glikemik beras menjadi 59.9% !0.03 atau tergolong kategori sedang. Indeks glikemik beras instan varietas sangat dipengaruhi oleh suhu pengeringan dibandingkan lama proses pengeringan yang memberikan peningkatan indeks glikemik yaitu 63.6% !0.01 (Jaisut . 2008).
Makanan yang memiliki indeks glikemik rendah atau tidak cepat menaikkan kadar glukosa darah dibutuhkan oleh penderita diabetes. Kasus
4 substitusi ini penting bagi penderita diabetes untuk lebih selektif dalam memilih dan mengkonsumsi bahan pangan. Penelitian ini mempelajari pengaruh proses pemanasan (pengeringan dengan oven atau penggorengan) terhadap komposisi kimia dan evaluasi nilai biologis serta indeks glikemik dari mi jagung substitusi
kering dan instan dibandingkan dengan mi komersial.
)*)"' $'$% # "'
Penelitian ini bertujuan untuk:
1. Menentukan pengaruh pemanasan (pengeringan dengan oven atau penggorengan) terhadap komposisi kimia dan evaluasi nilai biologis mi jagung substitusi kering dan instan.
2. Menentukan indeks glikemik mi jagung substitusi kering dan instan dibandingkan dengan mi komersial.
+ ,-#$. . $'$% # "'
Proses pemanasan (pengeringan dengan oven atau penggorengan) berpengaruh terhadap komposisi kimia, evaluasi nilai biologis dan indeks glikemik dari mi jagung substitusi kering dan instan.
/ "'0""# $'$% # "'
Jagung (" L) adalah jenis rerumputan/ dan termasuk tanaman semusim. Biji jagung disebut kariopsis yaitu memiliki dinding ovari atau perikarp yang menyatu dengan kulit biji atau testa membentuk daging buah (Takdir . 2007). Berikut penjelasan mengenai struktur biji jagung dan komposisi kimia dari beberapa varietas jagung di Indonesia.
# )&#) * "()'(
Biji jagung yang telah matang terdiri atas empat bagian utama yaitu perikarp, lembaga, endosperm dan (Gambar 1). Perikarp merupakan lapisan pembungkus biji yang cepat mengalami perubahan selama proses pembentukan biji. Pada waktu kariopsis muda sel=selnya kecil dan tipis, tetapi seiring dengan bertambahnya umur biji sel=sel tersebut berkembang. Pada taraf tertentu lapisan ini membentuk membran yang dikenal sebagai kulit biji atau aleuron yang secara morfologi adalah bagian endosperm. Bobot lapisan aleuron sekitar 3% dari keseluruhan biji (Inglett 1987).
Gambar 1. Struktur biji jagung (Shukla dan Cheryn 2001).
Lembaga merupakan bagian dari biji jagung yang cukup besar. Pada biji jagung tipe gigi kuda bagian lembaga meliputi 11.5% dari bobot keseluruhan biji. Lembaga tersusun atas dua bagian yaitu skutelum dan poros embrio (
6 dan keselurahannya terdiri atas karbohidrat. $ adalah bagian yang menghubungkan biji dengan janggel (Inglett 1987 ).
-1,-. . 1 " "()'(
Analisis kimia jagung menunjukkan masing=masing fraksi mempunyai sifat yang berbeda seperti yang ditampilkan Tabel 1. Lembaga dicirikan oleh tingginya kadar lemak (33%), protein (18.4%) dan mineral (10.5%). Kulit ari jagung dicirikan oleh kandungan karbohidrat yang tinggi yaitu 86.7%. Di sisi lain, endosperm kaya akan pati (87.6%), protein (8%) dan kadar lemak yang relatif rendah (0.8%). Proses pengolahan dengan menghilangkan sebagian dari fraksi biji jagung mempengaruhi mutu gizi produk akhir. Informasi komposisi kimia tersebut bermanfaat bagi industri pangan untuk menentukan jenis bahan dan
proses yang harus dilakukan agar diperoleh mutu produk yang sesuai dengan yang diinginkan. Berdasarkan data tersebut dapat ditentukan apakah produk yang akan
diolah memerlukan biji jagung utuh, kulit ari atau penghilangan lembaga (Suarni dan Widowati 2007).
Tabel 1 Komposisi kimia jagung utuh
Komponen Biji utuh Endosperm Jumlah (% bk) Lembaga Kulit ari Tip cap
Protein 3.7 8.0 18.4 3.7 9.1
Lemak 1.0 0.8 33.2 1.0 3.8
Karbohidrat 87.6 2.7 8.8 86.7 =
Abu 0.8 0.3 10.5 0.8 1.6
Pati 71.3 87.6 8.3 7.3 5.3
Gula 0.34 0.62 10.8 0.34 1.6
Sumber: Inglett (1987)
Protein utama dalam jagung adalah glutelin yang juga dikenal glutenin. Glutelin merupakan protein yang memiliki berat molekul tinggi dan larut alkali. Fraksi glutelin merupakan protein endosperm yang tersisa setelah ekstraksi protein larut garam dan alkohol (zein). Protein lain dalam jagung adalah zein yang
7 jenis protein zein yaitu α=zein yang larut pada etanol 95% dan β=zein yang larut pada etanol 60%. Protein α=zein mengandung lebih banyak histidin, arginin, prolin dan metionin daripada β=zein (Johnson 1991).
Lemak pada jagung terutama terdapat pada bagian lembaga yaitu sekitar
33.2% dari total lemak jagung. Dengan tingginya kandungan lemak pada lembaga, dalam pembuatan mi jagung bagian lembaga dipisah karena lemak dapat
menyebabkan ketengikan sehingga memperpendek daya simpan mi (Laszity 1986). Kandungan amilosa dan amilopektin beberapa varietas lokal dan unggul nasional dapat dilihat pada Tabel 2.
Tabel 2. Kandungan amilosa dan amilopektin dari beberapa varietas jagung
Varietas Amilosa (%) Amilopektin (%)
Srikandi putih* 31.05 68.95
Srikandi kuning* 30.14 69.86
Lokal nonpulut* 28.50 71.50
Lokal pulut* 4.25 95.75
Pioneer 21 ** 23.04 43.52
Sumber: * Suarni dan Widowati (2007) dan ** Etikawati (2007)
Komponen utama jagung adalah pati sekitar 70% dari bobot biji. Komponen karbohidrat lain adalah gula sederhana (1=3%) yaitu glukosa, sukrosa dan fruktosa. Pati jagung terdiri atas dua jenis polimer glukosa yaitu amilosa dan amilopektin. Amilosa merupakan rantai unit=unit D=glukosa yang panjang, tidak bercabang dan digabungkan oleh ikatan α (1→4), sedangkan amilopektin strukturnya bercabang. Ikatan glikosidik yang menggabungkan residu glukosa yang berdekatan dalam rantai amilopektin adalah ikatan α (1→4) tetapi titik percabangan amilopektin merupakan ikatan α (1→6) (Singh . 2003).
Bahan yang mengandung amilosa tinggi jika direbus amilosanya terekstrak oleh air panas sehingga terlihat warna putih seperti susu (Lehninger 1982).
8 Komposisi kimia jagung bervariasi tergantung varietas, cara menanam, iklim dan tingkat kematangan sehingga diperlukan seleksi untuk mendapatkan varietas jagung yang memiliki komposisi kimia yang tepat untuk dibuat mi. Komposisi kimia jagung putih tidak berbeda dengan jagung kuning, tetapi tidak
mengandung pro=vitamin A, komposisi kimia tersebut tidak menyebar merata pada bagian=bagian biji jagung (Suarni dan Widowati 2007).
$,)'( "()'(
$0 ' . $,)'( "()'(
Tepung jagung didefinisikan sebagai tepung yang diperoleh dari penggilingan atau penumbukan biji jagung (" Linn) dari berbagai varietas (putih dan kuning). Persyaratan SNI 01=3727=1995, kadar air tepung jagung tidak lebih 10% dengan kehalusan minimal 99% untuk lolos ayakan 60 mesh dan minimal 70% lolos ayakan 80 mesh. Penggilingan biji jagung ke dalam bentuk tepung merupakan suatu proses memisahkan kulit, endosperm, lembaga dan
. Endosperm merupakan bagian biji jagung yang digiling menjadi tepung dan memiliki kadar karbohidrat yang tinggi. Kulit memiliki kandungan serat yang tinggi sehingga dalam pembuatan tepung jagung, kulit harus dipisahkan dari endosperm karena batas maksimal jumlah serat kasar dalam tepung jagung adalah 1.5%. Lembaga merupakan bagian dari biji yang mengandung lemak tertinggi, sehingga harus dipisahkan untuk mencegah tepung cepat rusak karena reaksi oksidasi lemak. $ harus dipisahkan dalam pembuatan tepung jagung karena dapat menyebabkan adanya butir=butir hitam pada tepung jagung yang mengakibatkan kontaminasi produk (Juniawati 2003).
-1,-. . 1 " 2"' $&'-%-( -2)&. $,)'( "()'(
Kandungan komposisi kimia tepung jagung ditampilkan pada Tabel 3.
Komposisi terbesar pada tepung jagung adalah karbohidrat yang tersusun atas pati.
Pati merupakan simpanan karbohidrat dalam tumbuh=tumbuhan dan merupakan
9 Penggunaan tepung jagung yang kurang dari 100 mesh menghasilkan mi jagung dengan tekstur yang kasar dan kehilangan padatan selama pemasakan yang lebih tinggi (Sigit 2008).
Tabel 3. Komposisi kimia tepung jagung
Komposisi kimia Kadar (%)
Air 10.9
Abu 0.4
Protein 5.8
Lemak 0.9
Karbohidrat ( ) 82.0
Pati 68.2
Serat makanan 7.8
Sumber: Juniawati (2003)
Proses pembuatan tepung dapat dilakukan dengan dua cara yaitu penggilingan kering ( ) dan penggilingan basah ( ). Penggilingan kering adalah penggilingan jagung kering dengan dua kali penggilingan yaitu penggilingan kasar dan halus. Penggilingan dengan metode kering menggunakan alat untuk penggilingan kasar dan
untuk penggilingan halus (Pratama 2008).
Penggilingan jagung dengan metode kering menghasilkan rendemen tepung jagung yang lebih tinggi dibandingkan menggunakan penggilingan basah. Hal ini disebabkan pada penggilingan basah banyak komponen jagung yang terbuang pada saat pembersihan dan pencucian. Tepung jagung dari penggilingan kering dapat menghasilkan tepung yang bisa disimpan dalam bentuk kering dengan kadar air maksimal 14% (Nobel dan Andrizal 2003).
Pada penggilingan basah, jagung digiling dengan menggunakan penggilingan batu yang biasa digunakan untuk menggiling kedelai pada pembuatan tahu. Keuntungan proses penggilingan basah adalah kemudahan untuk
mencapai derajat kehalusan yang tinggi, mencegah kenaikan suhu bahan yang terlalu tinggi dan memperkecil kerugian akibat oksidasi bahan baku. Penggilingan basah terutama digunakan untuk mendapatkan tepung yang halus dan biasanya membutuhkan air dalam jumlah besar (Pratama 2008).
10 10 kg jagung pipil atau rendemen sekitar 29%. Proses produksi tepung jagung dengan penggilingan kering dilakukan dalam beberapa tahap yaitu penggilingan awal (penggilingan kasar), pencucian dan perendaman, penggilingan tahap akhir (penggilingan halus), serta pengayakan.
Penggilingan tahap awal dilakukan dengan menggunakan
yang menghasilkan , kulit, lembaga dan . Pemisahan kulit, lembaga,
dan dilakukan dengan cara pencucian dan perendaman, mengendap dan kulit serta lembaga mengapung. % jagung dikering=anginkan selama 2 jam (hingga kadar air ±17%) untuk mempermudah ke tahap penggilingan selanjutnya. Kadar air yang tinggi dapat menyebabkan bahan menempel pada
sehingga menimbulkan kemacetan pada alat, sedangkan kadar air yang terlalu rendah akan menyebabkan partikel tepung setelah penggilingan lebih besar (tidak halus) (Faridi dan Faubion 1995).
Tahap akhir adalah penggilingan jagung dengan menggunakan (penggiling halus) untuk menghasilkan tepung yang lebih kecil ukurannya. Tepung jagung dari penggilingan tahap akhir kemudian diayak dengan menggunakan pengayak berukuran 100 mesh. Pengayakan ini bertujuan agar ukuran partikel tepung seragam. Perbedaan ukuran partikel yang tidak seragam menyebabkan terbentuknya (noda) berwarna putih karena ukuran partikel yang lebih besar membutuhkan waktu yang lebih lama untuk menyerap air, sehingga bagian yang tidak menyerap air tersebut membentuk noda berwarna putih (Faridi dan Faubion 1995).
+ "()'(
+ $0 ' . 2"' $)'(()%"' "()'(
Mi jagung merupakan mi yang dibuat dengan bahan utama hasil olahan jagung (tepung atau jagung). Mi jagung berbahan baku tepung jagung dapat
11 Salah satu keunggulan mi jagung dibandingkan mi terigu adalah mi jagung tidak memerlukan penambahan pewarna. Warna kuning mi jagung berasal dari karotenoid yang terdapat dalam jagung, sedangkan mi terigu dalam pengolahannya ditambahkan dengan pewarna kuning yaitu tartrazine (Astawan
dan Kasih 2008). Perbedaan antara mi jagung dengan mi terigu adalah komponen pembentuk tekstur mi. Pembentuk tekstur yang elastis dan kompak pada mi terigu
adalah gluten. Adanya gluten pada tepung terigu menyebabkan terbentuknya tekstur yang elastis dan kompak setelah tepung terigu ditambahkan air, sehingga adonan tersebut dapat dibentuk menjadi lembaran. Hal tersebut tidak dapat terjadi ketika tepung jagung ditambahkan air, sehingga dibutuhkan bahan atau proses tertentu agar terbentuk adonan yang memiliki tekstur elastis dan kompak (Kusnandar . 2009).
+ $&'-%-( -2)&. 2"' " "&#$ .# & "()'( )3.# #).
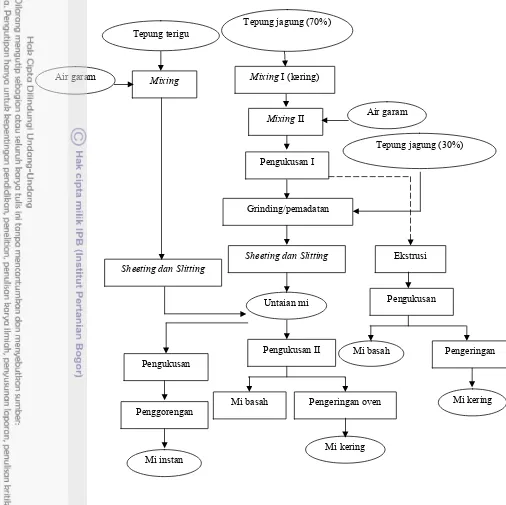
Produksi mi jagung dengan teknologi kalendering diawali dengan pencampuran tepung jagung dengan larutan garam (1% garam dilarutkan dalam air) dan guar gum 1%. CMC dan alginat dapat berfungsi sebagai pengikat komponen=komponen adonan, sehingga ketika mi dimasak tidak mudah terlepas. Penambahan guar gum dengan konsentrasi 1% memiliki pengaruh yang paling besar dalam mengurangi kelengketan dan (Faldillah 2005). Dalam teknologi kalendering untaian mi dibentuk dengan memotong lembaran adonan, sedangkan teknologi ekstrusi untaian mi dibentuk dengan menekan adonan mi ke dalam lubang kecil pada alat ekstruder. Teknologi proses pembuatan mi jagung dapat dilihat pada Gambar 2.
Penggunaan tepung jagung dalam mi dibatasi oleh karakteristik fungsional
tepung jagung, terutama disebabkan oleh kandungan protein gluten yang rendah dan karakteristik protein tepung jagung tidak mengandung protein gliadin dan
glutenin sebagaimana pada tepung gandum yang bertindak sebagai pengikat untuk membentuk tekstur adonan yang & (Juniawati 2003).
12 Gambar 2. Teknologi proses produksi mi jagung (Kusnandar . 2009).
Perbedaan dengan produksi mi jagung instan adalah bahan tambahannya
yaitu CMC ( # ) (1%) serta (0.3%)
(Stevanus 2010). Proses pemanasan dalam produksi mi jagung substitusi kering dan instan juga berbeda. Mi jagung substitusi kering setelah proses pengukusan mengalami proses pengeringan dengan oven suhu 60oC selama 70 menit (Putra 2008), sedangkan mi jagung substitusi instan melibatkan proses penggorengan suhu 160oC selama 4 menit (Stevanus 2010). Karakteristik fisik mi jagung
Tepung terigu
' # Air garam
( (
( (
Tepung jagung (70%)
' # I (kering)
' # II Air garam
Tepung jagung (30%)
Pengukusan I
Grinding/pemadatan
Untaian mi
Pengukusan II
Mi basah Pengeringan oven
Mi kering Pengukusan
Penggorengan
Mi instan
Ekstrusi
Mi basah Pengeringan
13 substitusi kering dan instan yang dihasilkan memiliki tingkat kekerasan yang tinggi, kenyal, tidak lengket dan tidak mudah putus.
Parameter mutu mi dapat dilihat dari mutu fisik, kimia dan organoleptik. Mi kering yang bermutu baik (sebelum dimasak) memiliki tekstur yang kuat
(tidak rapuh/mudah patah), permukaan yang halus dan warna kuning yang seragam. Apabila dimasak (direbus dalam air), mi cepat mengalami rehidrasi
(untuk mi instan kurang dari 3 menit), tidak hancur/larut dalam air rebusan ( rendah, yaitu <2%), tidak lengket, cukup elastik dan tidak terlalu mengembang (Putra 2008). Mi jagung instan menyumbangkan energi sekitar 360 kilo kalori/kemasan, sedangkan mi instan komersial menyumbangkan 420 kilo kalori/kemasan. Tingginya energi yang terdapat pada mi jagung instan menunjukkan bahwa produk tersebut dapat dijadikan bahan pangan alternatif pengganti nasi (Stevanus 2010).
/ '2$&. 2"' $3"' % &$1 & / '2$&. % &$1 &
/ $0 ' . '2$&. % &$1 &
Indeks glikemik pangan merupakan tingkatan pangan menurut efeknya ( ) terhadap kadar gula darah. Pangan yang menaikkan gula darah dengan cepat, memiliki indeks glikemik tinggi dan sebaliknya (Rimbawan dan Siagian 2004). Indeks glikemik juga dapat didefinisikan sebagai rasio antara luas kurva respon glukosa makanan yang mengandung karbohidrat total setara 50 g gula terhadap luas kurva respon glukosa setelah makan 50 g glukosa, pada hari yang berbeda dan orang yang sama. Kedua tes tersebut dilakukan pada pagi hari setelah puasa 10 jam dan penentuan kadar gula ditentukan selama 2 jam. Dalam
14 Gambar 3. Kurva pengukuran indeks glikemik (Glycemic index foundation 2010)
Menurut Powell . (2002), bahan pangan dapat diklasifikasikan berdasarkan IG=nya sebagai berikut: bahan pangan dengan nilai IG rendah (<55),
bahan pangan dengan nilai IG sedang (55=69) dan bahan pangan dengan nilai IG tinggi (>70) dengan standar glukosa. Skala yang digunakan dalam mengukur
indeks glikemik adalah dari 0 sampai 100, dimana nilai tertinggi dari pangan menyebabkan peningkatan kecepatan penyerapan terhadap gula darah (Gambar 3).
/ $1$ "4"' 2"' $'5$ ","' " 3-4 2 "#
Kecepatan kenaikan kadar gula darah bahan pangan sangat ditentukan kecepatan pemecahan karbohidrat dan penyerapannya oleh tubuh. Pemecahan dan penyerapan karbohidrat dalam tubuh terlebih dahulu harus diubah menjadi komponen yang lebih kecil yaitu glukosa. Enzim yang dapat memecah karbohidrat adalah α=amilase yang terdapat dalam air liur yang dihasilkan oleh kelenjar saliva dan pankreas. Enzim α=amilase stabil pada kisaran pH 5=5.8. Enzim α=amilase yang berasal dari saliva menjadi inaktif oleh pH rendah lambung. Enzim α=amilase yang berasal dari pankreas memecah pati di usus menjadi unit=unit dimerik terutama maltosa (Sardesai 2003).
Pati yang dicerna dan diserap oleh tubuh menyebabkan kenaikan kadar gula darah ( ). Puncak kenaikan terjadi sekitar 15=45 menit setelah
K
ad
ar
g
lu
k
o
sa
d
ar
ah
Waktu (jam) IG tinggi
IG rendah
15 mengkonsumsi tergantung kecepatan pencernaan dan penyerapan karbohidrat dalam tubuh manusia. Kadar glukosa darah kembali normal setelah dua atau tiga jam. Hormon yang diproduksi oleh tubuh untuk menurunkan kadar glukosa darah adalah hormon insulin. Hormon insulin diproduksi di kelenjar Langherns pada
pankreas. Hormon insulin bertugas meningkatkan laju transport glukosa ke dalam sel dan laju pengubahan glukosa menjadi glikogen (Wardlaw 1999). Menurut
Sardesai (2003), kadar glukosa darah normal berkisar antara 55=140 mg/dl dan minimum sebesar 40=60 mg/dl.
/ + "&#- 6 "&#- 5"'( $1,$'(" )4 '2$&. % &$1 &
Pengenalan karbohidrat berdasarkan efek terhadap kenaikan kadar gula darah dan respon insulin berguna sebagai acuan dalam menentukan jumlah dan jenis pangan sumber karbohidrat yang tepat untuk menjaga kesehatan. Infromasi IG pangan, penting bagi penderita diabetes mellitus/DM untuk memilih makanan yang tidak menaikkan kadar gula darah secara drastis sehingga kadar gula darah dapat dikontrol pada tingkat yang aman (Rimbawan dan Siagian 2004).
Perbedaan IG suatu pangan ditentukan tidak hanya oleh satu faktor tetapi beberapa faktor yang saling berkaitan. Varietas tanaman yang berbeda juga menyebabkan perbedaan pada IG. Faktor yang mempengaruhi IG pangan, yaitu proses ukuran partikel, keberadaan gula, kadar serat, pengolahan, perbandingan amilosa dengan amilopektin, pati resisten, lemak, protein serta zat antigizi pangan (Rimbawan dan Siagian 2004).
&) "' ," # &$% 2"' &$3$ "2""' ()%". Semakin kecil ukuran partikel pangan menyebabkan meningkatnya daya cerna pati sebagai akibat dari ketersediaan luas permukaan untuk enzim pecernaan bekerja dibandingkan ukuran
partikel yang lebih besar (Singh . 2010). Morfologi granula pati kentang yang besar menyebabkan penurunan kecepatan hidrolisis pati yang lebih rendah yaitu
16 Ketersediaan gula pada bahan pangan juga berkontribusi terhadap indeks glikemik pangan. Karbohidrat sederhana tidak semuanya memiliki IG lebih tinggi daripada karbohidrat komplek. Jenis gula yang terdapat dalam pangan mempengaruhi indeks glikemik pangan tersebut. Fruktosa memiliki indeks
glikemik sangat kecil (IG=23), sedangkan sukrosa memiliki IG sedang (IG=65). Kehadiran gula dalam pangan juga menghambat gelatinisasi pati dengan cara
mengikat air (Ludwig 2000).
$ "# "'("'. Serat pangan merupakan komponen makanan (karbohidrat komplek) dalam tanaman yang tidak dapat dicerna dan diserap oleh saluran pencernaan manusia. Serat pangan terdiri dari komponen serat larut ((
) /SDF) dan komponen serat tidak larut (
) /IDF). Dalam bentuk utuh, serat pangan bertindak sebagai penghambat fisik pada pencernaan. Serat tidak larut berfungsi mempertebal kerapatan atau ketebalan campuran makanan dalam saluran pencernaan, sedangkan serat larut dapat menurunkan respon glikemik (Astawan dan Wresdiyati 2004).
Menurut Astawan dan Wresdiyati (2004), konsumsi makanan yang diperkaya dengan serat pangan larut contohnya guar gum dan pektin dapat menurunkan peningkatan gula darah. Serat pangan seperti guar gum, pektin, , berpengaruh terhadap penurunan indeks glikemik sebesar 44%, 29%, 29% dan 23 % (DFDC 2001). Menurut Prijatmoko (2007), jagung yang mengandung serat yaitu 1.5% menaikkan gula darah sebesar 13.4 mg/dl dibandingkan nasi yang mengandung serat 0.5% menaikkan kadar gula darah 35.6 mg/dl dan kentang yang mengandung serat 0.9% menaikkan kadar gula darah 18.1 mg/dl.
Studi yang dilakukan terhadap 8 orang sukarelawan yang diberikan suplemen yang telah ditambah serat pangan menunjukkan penurunan level
kenaikan glukosa darah sebesar 6=39% pada periode 30=60 menit pengukuran indeks glikemik. Bahan pangan yang memiliki kandungan serat pangan yang tinggi cenderung menurunkan kapasitas level glukosa darah (DFDC 2001).
17 ikatan rantai polisakarida menjadi gula sederhana. Ikatan glikosidik pada serat pangan juga mengalami kerusakan. Pelepasan ikatan antar molekul serat atau depolimerisasi menghasilkan solubilisasi, jika proses tersebut terus berlangsung maka fragmen alkohol yang mudah larut terbentuk. Hal ini menyebabkan
penurunan kandungan serat pangan. Proses depolimerisasi moderat yang disebabkan proses panas sedikit mempengaruhi kandungan serat pangan, tetapi
sifat fungsional serat pangan berubah. Selain serat pangan, proses panas juga mempengaruhi timbulnya sejumlah reaksi lain selama proses. Reaksi=reaksi tersebut antara lain terbentuknya produk dari reaksi ' dan pati resisten (FAO/WHO 1997).
Pengeringan beras instan varietas dengan suhu 150 oC pada selang waktu 30, 60 dan 120 menit signifikan menurunkan daya cerna pati masing=masing 26.3%, 25.3% dan 24.8% dibandingkan daya cerna pati standar yaitu 31.8%. Pengeringan mempengaruhi kinerja dari enzim alfa amilase untuk memecah pati beras yang telah mengalami pemanasan atau menurunkan daya cerna pati sebesar 6% dengan meningkatnya waktu pengeringan. Peningkatan suhu pengeringan ternyata lebih signifikan berkontribusi menurunkan daya cerna pati beras dibandingkan waktu pengeringan. Pengeringan beras pada suhu 150 oC selama 120 menit menurunkan daya cerna pati 11% lebih rendah dibandingkan pengeringan pada suhu 130 oC pada selang waktu yang sama. Penurunan daya cerna pati akibat proses pengeringan berkontribusi besar terhadap penurunan indeks glikemik pangan beras menjadi 59.9% (Jaisut . 2008).
1 %-." 2"' "1 %-,$&# '. Perbandingan amilosa=amilopektin dapat menyebabkan daya cerna pati yang berbeda. Karakteristik amilosa yang
18
"# $. .#$'. Pati resisten merupakan komponen pati yang tidak dapat dicerna oleh enzim pencernaan orang sehat (Haliza . 2006). Pati resisten diklasifikasikan ke dalam empat tipe yang berbeda berdasarkan resistensinya. Pati resisten tipe 1 yaitu pati yang secara fisik sulit dicerna (pati yang terikat pada
dinding sel dan ukuran partikel yang besar hasil penggilingan yang tidak sempurna). Contoh pati resisten tipe 1 yaitu biji yang telah digiling, biji=bijian,
kacang=kacangan dan umbi=umbian. Pati resisten tipe 2 yaitu pati yang masih dilindungi oleh konformasi atau struktur granula pati dan tidak tergelatinisasi, contohnya ubi jalar, pisang dan pati jagung yang banyak mengandung amilosa. Pati resisten tipe 3 merupakan pati yang terbentuk selama proses pengolahan atau biasa disebut pati yang terbentuk akibat proses retrogradasi. Dan pati resisten tipe 4 adalah pati resisten yang terbentuk akibat modifikasi pati secara kimia, misalnya pati hidroksipropil, asetat, fosfat dan sitrat (Asp dan Bjorck 1992).
Konsumsi bahan pangan yang tinggi kandungan pati resisten menyebabkan penurunan level gula darah dan insulin dibandingkan mengkonsumsi pangan karbohidrat lainnya. Sukarelawan penderita diabetes tipe II dimintakan mengkonsumsi produk coklat ( ) yang telah ditambahkan pati resisten menunjukkan penurunan kadar glukosa darah dibandingkan mengkonsumsi coklat yang tidak ditambahkan pati resisten. Penurunan level glukosa tersebut menunjukkan bahwa pati resisten mampu menurunkan laju pelepasan glukosa darah (Haralampu 2000).
$1"& 2"' -#$ '. Pangan yang mengandung lemak dan protein tinggi cenderung memperlambat laju pengosongan lambung, sehingga pencernaan
makanan di usus halus juga diperlambat. Oleh karena itu, pangan berkadar lemak tinggi mempunyai IG lebih rendah daripada pangan sejenis yang berlemak rendah
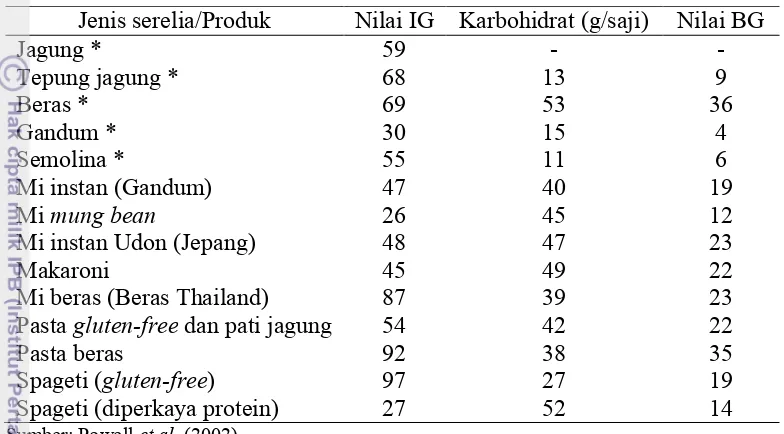
19 Indeks glikemik berbagai jenis serelia, mi dan pasta disajikan pada Tabel 4. Serelia memiliki nilai indeks glikemik yang berbeda=beda, tetapi dari beberapa jenis serelia (jagung, beras, gandum, dan semolina) hanya gandum yang memiliki nilai IG rendah yaitu 30. Mi yang memiliki nilai IG rendah adalah mi yang terbuat
dari gandum, makaroni, mi instan Udon (Jepang) dan spageti yang diperkaya protein (Powell . 2002). Pangan yang memiliki IG tinggi menyebabkan
pengeluaran insulin dalam jumlah besar sebagai akibat dari kenaikan glukosa darah yang tinggi dan cepat. Hal tersebut menyebabkan peningkatan rasa lapar setelah makan dan penumpukan lemak pada jaringan adipose dalam tubuh (Jones 2002).
/ $3"' % &$1 &
Indeks glikemik memberikan informasi kecepatan perubahan karbohidrat menjadi glukosa darah, tetapi tidak memberikan informasi mengenai banyaknya karbohidrat dan dampak pangan tertentu terhadap kadar glukosa darah. Salah satu langkah yang dapat ditempuh untuk mengetahui banyaknya karbohidrat terhadap kenaikan glukosa dapat dilihat dari beban glikemik. Beban glikemik memberikan informasi yang lebih lengkap mengenai pengaruh konsumsi aktual karbohidrat per saji terhadap peningkatan kadar gula darah yang ditunjukkan oleh indeks glikemik (Powell . 2002).
Beban glikemik bahan pangan dapat diklasifikasikan yaitu BG rendah (< 10), BG sedang (11=19) dan BG tinggi (>20). Perhitungan beban glikemik yaitu IG pangan dikalikan dengan kandungan karbohidrat pangan yang disajikan dibagi seratus. Beban glikemik mi dan pasta dari berbagai jenis bahan ditampilkan pada Tabel 4. Mi instan (gandum), mi dan mi instan Udon (Jepang)
memiliki beban glikemik masing=masing yaitu 19, 12 dan 23 serta tergolong kategori sedang. Beban glikemik pasta yang terbuat dari berbagai bahan tergolong
beban glikemik yang tinggi. Nilai indeks glikemik yang tinggi pada bahan pangan tidak langsung menunjukkan kecepatan peningkatan gula darah, tetapi ditentukan oleh kandungan karbohidrat yang disajikan (Powell . 2002).
20 produk mi instan Udon (Jepang) dan makaroni yaitu 48 dan 45 dengan jumlah karbohidrat persajian yaitu 47 g dan 49 g memiliki beban glikemik yang tergolong tinggi yaitu 23 dan 22 (Powell . 2002).
Tabel 4. Indeks dan beban glikemik serelia, mi dan pasta
Jenis serelia/Produk Nilai IG Karbohidrat (g/saji) Nilai BG
Jagung * 59 = =
Tepung jagung * 68 13 9
Beras * 69 53 36
Gandum * 30 15 4
Semolina * 55 11 6
Mi instan (Gandum) 47 40 19
Mi 26 45 12
Mi instan Udon (Jepang) 48 47 23
Makaroni 45 49 22
Mi beras (Beras Thailand) 87 39 23
Pasta & dan pati jagung 54 42 22
Pasta beras 92 38 35
Spageti ( & ) 97 27 19
Spageti (diperkaya protein) 27 52 14
Sumber: Powell . (2002).
Bahan pangan dengan beban glikemik yang tinggi lebih mencerminkan peningkatan kadar glukosa darah, dibandingkan dengan nilai indeks glikemik yang tinggi. Konsumsi dalam jangka panjang terhadap bahan pangan yang mimiliki nilai beban glikemik yang tinggi dapat dikaitkan dengan resiko penyakit diabetes tipe 2 (Powell . 2002).
7 "3#$. $%% #).
Penyakit Diabetes Mellitus (DM) yang juga dikenal sebagai penyakit kencing manis atau penyakit gula darah adalah golongan penyakit kronis yang ditandai dengan peningkatan kadar gula dalam darah sebagai akibat adanya
21 Pada orang normal, karbohidrat yang berupa makanan yang mengandung pati ketika dikonsumsi akan diubah menjadi glukosa dalam saluran pencernaan, dengan bantuan insulin. Glukosa ini kemudian akan dibawa oleh darah keseluruh tubuh dan masuk kedalam sel untuk dimanfaatkan sebagai energi. Pada penderita
diabetes mellitus gula tidak dapat masuk ke dalam sel, hal ini disebabkan karena jumlah insulin yang diproduksi kelenjar pankreas sangat rendah atau aktivitas
reseptor insulin menurun sehingga sel tidak dapat memberikan respon yang baik terhadap insulin sehingga kadar glukosa dalam darah meningkat. Kadar glukosa normal manusia berkisar antara 70 = 150 mg/dL, sedangkan bagi penderita diabetes kadar glukosa darah puasa mencapai 126 mg/dl atau lebih dan pemeriksaan gula darah 2 jam setelah puasa (minimal 8 jam puasa) mencapai level 180 mg/dl. Diabetes mellitus digolongkan dalam dua tipe yaitu tipe 1 dan tipe 2 (WHO 1999).
Diabetes tipe 1 atau dikenal juga sebagai diabetes mellitus tergantung insulin, tubuh hanya memproduksi sedikit sekali insulin atau tidak sama sekali. Diabetes tipe I, disebabkan karena adanya penyakit autoimun. Sistem imun meyerang dan merusak sel=sel beta pada pankreas yang memproduksi insulin dan tubuh tidak dapat mengubah glukosa menjadi energi (WHO 1999).
+ !"&#) 2"' $1,"# $'$% # "'
Penelitian dilaksanakan pada Bulan Desember 2009 sampai Juni 2010 di Laboratorium Pilot Plant dan Evaluasi Sensori Seafast Center IPB, serta Laboratorium Pengolahan Pangan, Kimia Pangan, serta Biokimia Pangan dan Gizi Departemen Ilmu dan Teknologi Pangan.
+ "4"' 2"' %"# + "4"'
Bahan baku yang digunakan meliputi bahan baku utama dan bahan baku tambahan serta bahan kimia. Bahan baku utama antara lain jagung varietas Pioneer 21 dan tepung terigu cakra kembar, sedangkan bahan tambahan dalam pembuatan mi yaitu guar gum, CMC, K2CO3, Na2CO3, garam, baking soda dan air. Bahan kimia yang digunakan untuk analisis diantaranya adalah HCl, NaOH, asam asetat, aseton, kertas saring, heksan, amilosa standar, buffer fosfat 0.1 M pH 6 dan pH 7, buffer asetat pH 5 dan pH 6, alumunium foil, asam dinitrosalsilat (DNS), iod, etanol, eter, asam tanat, Folin=Denis, maltosa standar, glukosa standar, amiloglukosidase (SIGMA A7095), α=amilase from * (SIGMA
86250), pepsin (SIGMA P7000), peptidase (SIGMA P7500), pankreatin (SIGMA P1750), α=amilase solution Type XII A=bacterial from
(SIGMA A3403), kimotripsin (SIGMA C4129), dan tripsin (SIGMA T4799).
+ %"#
Peralatan yang digunakan terdiri peralatan penepungan, produksi mi jagung dan peralatan untuk analisis kimia dan evaluasi biologis serta indeks
glikemik. Peralatan penepungan adalah , , ,
dan pengering kabinet. Peralatan untuk produksi mi jagung diantaranya adalah
23 analitik (Precisa XT 220A), penangas (Therolyne Cimarec 3), dan glukometer
Merk+ $ , .
+ + "4","' $'$% # "'
Penelitian dibagi menjadi tiga tahap yaitu tahap produksi dan karakterisasi
kimia tepung jagung, tahap proses dan karakterisasi sifat kimia dan evaluasi nilai biologis mi jagung substitusi kering dan instan, dan pengukuran indeks glikemik
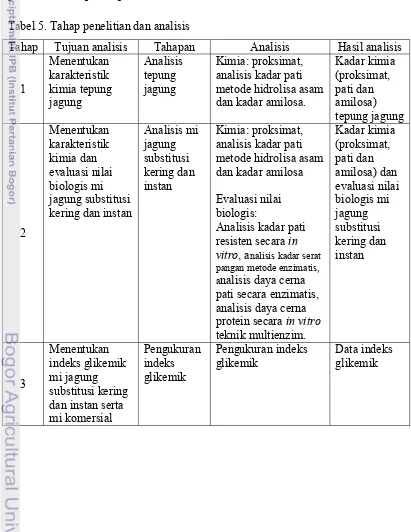
[image:39.595.106.517.249.781.2]mi jagung substitusi kering dan instan serta mi komersial. Secara garis besar tahap penelitian ditampilkan pada Tabel 5.
Tabel 5. Tahap penelitian dan analisis
Tahap Tujuan analisis Tahapan Analisis Hasil analisis
1 Menentukan karakteristik kimia tepung jagung Analisis tepung jagung Kimia: proksimat, analisis kadar pati metode hidrolisa asam dan kadar amilosa.
Kadar kimia (proksimat, pati dan amilosa) tepung jagung 2 Menentukan karakteristik kimia dan evaluasi nilai biologis mi jagung substitusi kering dan instan
Analisis mi jagung substitusi kering dan instan Kimia: proksimat, analisis kadar pati metode hidrolisa asam dan kadar amilosa
Evaluasi nilai biologis:
Analisis kadar pati resisten secara
24
+ + $13)"#"' $,)'( "()'(
Pembuatan tepung jagung bertujuan mengevaluasi karakteristik kimia tepung jagung dengan melakukan analisis proksimat, analisis kadar pati metode hidrolisa asam dan kadar amilosa. Proses penepungan diawali dengan
penggilingan jagung pipil dengan , dari tahap penggilingan tersebut terpisah (pecahan biji jagung), kulit ari dan lembaga. Hasil penggilingan
jagung pipil dicuci dan di endapkan untuk memisahkan bagian yang terapung (lembaga dan kulit ari) dengan bagian yang mengendap. % dikering= anginkan hingga kadar air ±17%. % kering digiling dengan menggunakan
[image:40.595.106.506.85.746.2], kemudian dimasukkan ke dalam ayakan bertingkat ukuran 100 mesh, sehingga dihasilkan tepung jagung dengan ukuran lolos ayakan 100 mesh. Alur proses penepungan jagung ditunjukkan pada Gambar 4.
Gambar 4. Pembuatan tepung jagung dengan penggilingan kering
Lembaga, kulit dan
Penggilingan I ( )
Jagung pipil kering
Pengayakan 100 mesh Pemisahan endosperm dari
lembaga, kulit dan
Penirisan dan pengeringan % , lembaga,
dan kulit
% jagung
Penggilingan II ( )
Tepung kasar
25
+ + $13)"#"' "()'( )3.# #). $ '( 2"' '.#"'
Pembuatan mi jagung substitusi kering dan instan digunakan untuk mengevaluasi karakteristik kimia dan evaluasi nilai biologis. Analisis kimia mi jagung substitusi meliputi proksimat, kadar pati metode hidrolisa asam dan kadar
amilosa. Analisis evaluasi nilai biologis yaitu kadar pati resisten secara , kadar serat pangan metode enzimatis, daya cerna pati secara enzimatis dan daya
cerna protein secara dengan teknik multienzim. Proses pembuatan mi jagung substitusi diawali dengan mencampur sejumlah bahan kering yang terdiri dari tepung terigu (70%), tepung jagung (30%). Pada pembuatan mi jagung instan bahan kering yang dicampurkan adalah CMC ( # ) (1%) serta (0.3%), sedangkan untuk mi jagung kering, bahan kering yang dicampurkan adalah guar gum (0.5%), K2CO3 (0.1%), dan Na2CO3 (0.1%). Bahan yang telah tercampur merata ditambahkan larutan garam (garam 1% dan air 40%) dan dicampur kembali dalam # sehingga terbentuk adonan. Adonan yang telah tercampur sempurna (kalis) dibentuk bulatan=bulatan agar memudahkan proses pembentukan lembaran mi. Adonan ditekan dengan cara dimasukkan ke dalam grinder dengan ukuran diameter 0.3 cm sebanyak 2 kali, kemudian campuran dibentuk lembaran secara bertahap dengan alat .
26 Gambar 5. Pembuatan mi jagung substitusi kering dan instan tepung jagung 30 %
+ + + $'()&) "' '2$&. % &$1 &
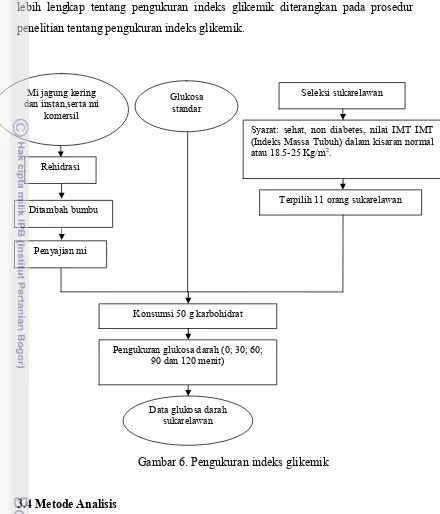
Penelitian tahap tiga ini bertujuan untuk (1) menganalisis nilai indeks glikemik masing=masing produk mi, (2) membandingkan indeks glikemik mi jagung substitusi kering dan instan terhadap indeks glikemik mi komersial. Waktu rehidrasi mi jagung kering 5 menit, mi jagung instan selama 3.30 menit dan mi komersial selama 3 menit seperti yang ditunjukkan pada Gambar 6. Penjelasan
Air garam (garam 1% dan
air 40%) Tepung terigu
(70%)
Pencampuran I (kering)
Pencampuran II
Untaian mi
( , dan
Pengeringan oven (T = 60oC, t = 70 menit) Penggorengan
(T = 160oC t = 4 menit)
Pendinginan
Mi jagung substitusi instan
Tepung jagung (30%)
Adonan
Pengukusan mi mentah (T = 95oC; t = 15 menit)
Bahan tambahan
kering
Pendinginan
27 lebih lengkap tentang pengukuran indeks glikemik diterangkan pada prosedur penelitian tentang pengukuran indeks glikemik.
Gambar 6. Pengukuran indeks glikemik
+ / $#-2$ '"% . .
Metode analisis yang dilaksanakan yaitu analisis kimia (tepung jagung dan
mi jagung substitusi), analisis evaluasi nilai biologis (mi jagung substitusi) dan pengukuran indeks glikemik (mi jagung substitusi dan mi komersial). Analisis kimia mencakup proksimat, kadar pati metode hidrolisa asam dan kadar amilosa. Analisis evaluasi nilai biologis meliputi kadar pati resisten secara , kadar serat pangan metode enzimatis, daya cerna pati secara enzimatis dan daya cerna
Data glukosa darah sukarelawan Mi jagung kering
dan instan,serta mi komersil
Seleksi sukarelawan
Syarat: sehat, non diabetes, nilai IMT IMT (Indeks Massa Tubuh) dalam kisaran normal atau 18.5=25 Kg/m2.
Terpilih 11 orang sukarelawan
Konsumsi 50 g karbohidrat
Pengukuran glukosa darah (0; 30; 60; 90 dan 120 menit)
Rehidrasi
Ditambah bumbu
Penyajian mi
28 protein secara dengan teknik multienzim. Pengukuran indeks glikemik dilakukan dengan pengukuran kadar glukosa darah 8 orang sukarelawan.
+ / '"% . . 1 "
Analisis kimia yang dilakukan meliputi proksimat, kadar pati metode hidrolisa asam dan kadar amilosa.
+ / '"% . . -&. 1"# 8 997:
Pengujian analisis proksimat terdiri dari analisis kadar air, abu, protein, lemak, sedangkan karbohidrat diperoleh dengan cara “ ”. Analisis kadar air dilakukan dengan menggunakan metode oven, kadar abu dengan pengabuan kering, kadar lemak dengan metode soxhlet dan kadar protein dengan metode Mikro=Kjeldahl.
+ / '"% . . "2" "# $#-2$ 2 -% ." ."1 8 -2 0 &". )2" 1"2* 99;:
Prinsip pengukuran kadar pati adalah dengan melakukan hidrolisis pati dalam sampel menjadi gula dengan menggunakan asam, kemudian larutan sampel diukur kadar gulanya. Kadar pati adalah glukosa dikalikan 0.9.
$ . ","' ."1,$% ,"# 4 2 -% ." "."1
Sampel ditimbang sebanyak 0.1 g dan dimasukkan ke dalam erlenmeyer 250 ml, kemudian ditambahkan 50 ml akuades dan diaduk selama 1 jam. Suspensi disaring dengan kertas saring dan dicuci dengan akuades hingga volume filtrat 250 ml. Filtrat tersebut mengandung karbohidrat yang larut sehingga dibuang.
Residu dicuci dengan 10 ml eter sebanyak 5 kali untuk menghilangkan lemak, setelah eter menguap cuci kembali dengan 150 ml alkohol 10% untuk
29
$'$'#)"' #-#"% ()%" ,$ $2)&. 2$'("' $#-2$ )006 4-- %
Larutan sampel yang telah diencerkan diambil 25 ml dan dimasukkan ke dalam erlenmeyer, kemudian ditambah 25 ml larutan Luff=Schoorl. Dibuat pula percobaan blanko yaitu 25 ml larutan Luff=Schoorl ditambah 25 ml akuades.
Campuran kemudian dimasukkan kedalam bersuhu 100 oC selama 10 menit dan didinginkan dengan air mengalir. Setelah campuran dingin,
ditambahkan 15 ml KI 20% dan tambahkan 25 ml H2SO4 26,5%. Penambahan larutan H2SO4 dilakukan secara perlahan=lahan. Iodium yang dibebaskan dititrasi dengan larutan Na=thiosulfat 0.1 N memakai indikator pati sebanyak 2=3 ml, untuk memperjelas perubahan warna pada akhir titrasi sebaiknya pati ditambahkan pada saat titrasi hampir berakhir. Di catat ml Na=thiosulfat yang terpakai untuk proses perhitungan.
$ 4 #)'("' &"2" ,"# ."1,$%<
Dengan mengetahui selisih antara titrasi blanko dan titrasi contoh, kadar gula reduksi setelah (setelah hidrolisa dengan HCl 30%) dalam bahan dapat dicari dengan menggunakan tabel selisih (Lampiran 2). Selisih kadar gula reduksi sesudah dengan sebelum (penentuan gula reduksi) dikalikan 0.9 dan faktor pengenceran merupakan kadar pati dalam bahan.
+ / + '"% . . "2" 1 %-." 8 , 5"'#-'- 9=9:
Prinsip pengukuran amilosa adalah berdasarkan pembentukan warna biru akibat reaksi amilosa dengan iod yang diukur dengan spektrofotometer pada panjang gelombang 625 nm.
$13)"#"' &) >" .#"'2"
Amilosa murni ditimbang sebanyak 40 mg, dimasukkan kedalam labu
takar 100 ml, lalu ditambahkan etanol 1 ml dan NaOH 1 N sebanyak 9 ml. Campuran kemudian dipanaskan dalam air mendidih selama kurang lebih 10
30 didiamkan selama 20 menit, lalu diukur intensitas warnanya dengan spektrofotometer pada panjang gelombang 625 nm.
$'$#","' ."1,$%
Sampel sebanyak 100 mg dimasukkan kedalam labu takar 100 ml, dan
ditambahkan 1 ml etanol dan 9 ml NaOH 1 N. Campuran kemudian dipanaskan dalam air mendidih selama kurang lebih 10 menit sampai semua bahan
membentuk gel dan didinginkan. Pindahkan seluruh campuran ke dalam labu takar 100 ml dan ditepatkan sampai tanda tera dengan akuades. Sampel dipipet 5 ml, lalu dimasukkan kedalam labu takar 100 ml, ditambahkan 1 ml asetat 1 N dan 2 ml larutan iod. Setelah itu larutan ditambahkan akuades hingga tanda tera, dikocok, didiamkan selama 20 menit, dan diukur intensitas warnyanya dengan spektrofotometer pada panjang gelombang 625 nm. Kadar amilosa dihitung berdasarkan persamaan garis yang diperoleh dari kurva standar. Absorbansi yang diperoleh diplotkan pada kurva standar. Kadar amilosa dihitung berdasarkan rumus sebagai berikut:
Kadar amilosa (%) =
Keterangan: A = absorbansi sampel pada panjang gelombang 620 nm S = slope kemiringan pada kurva standar
Fp = faktor pengencaran W = berat sampel
+ / '"% . . >"%)". %" -%-( .
Analisis evaluasi nilai biologis meliputi beberapa analisis yaitu kadar pati resisten secara , kadar serat pangan metode enzimatis, daya cerna pati secara enzimatis, dan daya cerna protein secara dengan teknik multienzim.
+ / '"% . . "2" "# $. .#$' .$ " " 8 -2 0 &". -' 99?:
31 ml buffer KCl=HCl), divortex dan diinkubasikan dalam bergoyang pada suhu 40 oC selama 60 menit.
Setelah proses inkubasi selesai, sampel dipindahkan dan ditempatkan pada suhu ruang. Kemudian ditambahkan 9 ml buffer fosfat 0.1 M pH 6.9 (sesuaikan
pH dengan HCl 2 M atau NaOH 0.5 M). Larutan enzim α=amilase (40 mg α= amilase per ml buffer fosfat) ditambahkan sebanyak 1 ml, divortex dan diinkubasi
selama 16 jam pada bergoyang bersuhu 37 oC. Setelah inkubasi, sampel disentrifus dengan kecepatan 3000 rpm selama 15 menit dan supernatan dibuang. Sampel dicuci dengan 10 ml akudes dan disentrifus serta supernatan kembali dibuang.
Kedalam residu ditambahkan 3 ml akuades dan 3 ml KOH 4 M, kemudian divortex dan kembali diinkubasi pada bergoyang selama 30 menit pada suhu ruang. Campuran kemudian ditambahkan 5.5 ml HCl 2 M dan 3 ml buffer natrium asetat 0.4 M pH 4.75 9 (sesuaikan pH dengan HCl 2 M atau NaOH 0.5 M) dan divortex. Setelah itu, campuran ditambahkan 80 µl enzim amiloglucosidase (AMG), divortex dan kembali dilakukan inkubasi pada bergoyang pada suhu 60 oC selama 45 menit. Campuran kemudian disentrifus dengan kecepatan 3000 rpm selama 15 menit dan supernatan diambil. Sampel dicuci dengan menambahkan 10 ml akuades dan kembali disentrifus serta supernatan digabungkan dengan yang sebelumnya. Supernatan kemudian diencerkan 25=1000 ml tergantung kandungan pati resisten dari sampel. Supernatan yang diperoleh dianalisis gula dengan menggunakan metode Luff= Schoorl. Kadar pati resisten sampel adalah kadar glukosa dikalikan 0.9 dan faktor pengenceran.
+ / '"% . . "2" $ "# "'("' $#-2$ '@ 1"# . 8 997:
Analisis kadar serat pangan dilakukan dengan mereaksikan sampel dengan
32
$ . ","' ."1,$%
Sampel yang telah diekstrak lemaknya dengan pelarut petroleum eter pada suhu kamar selama 15 menit ditimbang sebanyak 1 gram dan dimasukkan kedalam erlenmeyer, kemudian ditambahkan 25 ml buffer natrium fosfat 0.1 M
pH 6. Penambahan buffer dimaksudkan untuk menstabilkan ezim termamil. Sampel ditambahkan 100 µl termamil lalu dipanaskan sambil ditutup dan
diinkubasi (suhu = 100 oC selama waktu = 15 menit) sambil sesekali diaduk. Sampel didinginkan kemudian ditambahkan 20 ml akuades dan ditambahkan HCl 4 M hingga pH 1.5.
Sampel ditambahkan 100 mg pepsin, lalu erlenmeyer ditutup dan diinkubasikan pada suhu 40 oC sambil diaduk selama 60 menit. Pengaturan pH hingga 1.5 dimaksudkan untuk mengkondisikan agar aktivitas enzim pepsin maksimum. Sampel ditambahkan 20 ml akuades dan diatur pH=nya hingga 6.8 dengan cara ditambahkan NaOH. Sampel ditambahkan 100 ml enzim pankreatin, lalu erlenmeyer ditutup dan diinkubasi pada suhu 40 oC selama 60 menit sambil diaduk, kemudian sampel ditambahkan HCl kembali hingga pH 4.5. Kemudian sampel disaring sehingga diperoleh endapan yang dicuci dengan menggunakan 10 ml akuades sebanyak 2 kali. Pengukuran yang sama juga dilakukan untuk blanko. Dengan cara yang sama tetapi tanpa adanya sampel (hanya akuades). Nilai blanko harus diperiksa ulang terutama jika menggunakan enzim dari kemasan yang baru.
$'()&) "' $. 2) 8.$ "# 1"&"'"' # 2"& %" )#:
Residu dari hasil persiapan sampel dicuci dengan 10 ml etanol 95% dan 10 ml aseton masing=masing sebanyak 2 kali, lalu dikeringkan pada suhu 105 oC sampei berat tetap (sekitar 12 jam) dan dimasukkan dalam desikator dan
ditimbang (D1). Suspensi yang telah kering diabukan dalam tanur 500 oC selama 5 jam, didinginkan dalam desikator dan ditimbang (I1).
%# "# 8.$ "# 1"&"'"' %" )#:
33 selama 24 jam, kemudian dimasukkan kedalam desikator dan ditimbang (D2). Sampel yang telah kering diabukan dengan suhu 500 oC selama 5 jam, didinginkan dalam desikator, dan ditimbang (I2).
$ 4 #)'("' .$ "# ,"'("'<
D1 = I1 = B1
Serat makanan tidak larut (%bk) = 100%
W #
D2 = I2 = B2
Serat makanan larut (%bk) = 100%
W #
Nilai TDF (% bk) = Nilai IDF + SDF
Keterangan: Angka 1 menunjukkan berat sampel pada analisis serat makanan tidak larut dan 2 menunjukkan berat sampel pada analisis serat makanan larut.
W = berat sampel (g)
D = berat setelah analisis dan dikeringkan (g) I = berat setelah diabukan (g)
B = berat blanko bebas serat (g)
+ / + '"% . . "5" $ '" "# .$ " " '@ 1"# . 8 ) 4#"2 9=9:
Analisis daya cerna pati dilakukan dengan mereaksikan sampel yang mengandung 1 g pati dengan enzim α=amilase sehingga akan terjadi pemecahan pati menjadi maltosa, kemudian daya cerna pati diukur sebagai jumlah maltosa pada sampel dibagi dengan jumlah maltosa dari pati standar.
Sebanyak 1 g tepung atau pati murni dimasukkan dalam erlenmeyer 250 ml, lalu ditambahkan dengan 100 ml air destilata. Wadah ditutup dengan alumunium foil dan dipanaskan dalam wadah hingga mencapai suhu 90 o
C sambil diaduk. Setelah mencapai suhu 90 oC, sampel segera diangkat dan didinginkan. Dari larutan tersebut dipipet sebanyak 2 ml ke dalam tabung reaksi tertutup, lalu ditambahkan 3 ml akuades dan 5 ml buffer fosfat 0.1 M pH 7. Masing=masing sampel dibuat dua kali, salah satunya adalah blanko. Tabung ditutup dan diinkubasi pada suhu 37 oC selama 15 menit. Larutan diangkat dan ditambahkan 5 ml larutan α=amilase (1 mg/ml dalam buffer fosfat 0.05 M pH 7) untuk sampel dan 5 ml buffer fosfat 0.1 M pH 7 untuk blanko sampel. Inkubasi dilanjutkan selama 30 menit.
34 larutan ditambahkan 10 ml akuades dan dibuat homogen dengan vortex, lalu diukur absorbansinya pada panjang gelombang 520 nm yang ditunjukkan dari warna oranye=merah yang terbentuk dari reaksi campuran tersebut. Kurva standar diperoleh dari perlakuan DNS terhadap 0.0, 0.2, 0.4, 0.6, 0.8, dan 1.0 larutan
maltosa murni 0.5 mg/ml yang ditepatkan menjadi 1 ml dengan akuades. A = a
Daya cerna pati (%) = 100% B = b # Keterangan: A = kadar maltosa sampel
a = kadar maltosa blanko sampel B = kadar maltosa pati murni b = kadar maltosa blanko pati murni
+ / / '"% . . "5" $ '" -#$ ' .$ " " 2$'("' $&' &
)%# $'@ 1 8 ) 4#"2 9=9:
Pengukuran daya cerna protein dengan teknik multienzim dilakukan dengan mempersiapkan pereaksi, kemudian melakukan pengukuran daya cerna protein. Nilai pH pada menit ke=10 dicatat untuk menghitung daya cerna protein sampel menggunakan persamaan regresi Y = 210.464 – 18.103x. Pengukuran pH dilakukan pada menit ke=10, karena pH suspensi protein pada menit tersebut setelah dihidrolisis dengan larutan multienzim berkorelasi baik dengan daya cerna protein yang ditetapkan secara biologis menggunakan tikus.
$ . ","' ,$ $"&.
Pereaksi yang dipersiapkan antara lain larutan HCl 0.1 N, larutan NaOH 0.1 N dan larutan enzim. Pembuatan larutan enzim adalah dengan mencampuran 1.6 mg tripsin, 3.1 mg kimotripsin, dan 1.3 mg peptidase per ml akuades. Larutan enzim diatur pH=nya menjadi 8 dengan larutan NaOH atau HCl 0.1 N dan
ditempatkan pada .
-.$2)
35 diaduk dalam penangas air 37 oC dan pH dicatat setelah menit ke=10. Daya cerna protein dihitung menggunakan rumus sebagai berikut:
Y = 210.464 – 18.103x
Keterangan: Y = daya cerna protein (%)
x = pH suspensi sampel pada menit ke= 10.
+ / + $'()&) "' '2$&. % &$1 & 2"' $3"' % &$1 & 8 %%$ 99?: + / + $'()&) "' '2$&. % &$1 &
Pengukuran nilai indeks glikemik dilakukan pada mi jagung substitusi kering dan instan dan mi komersil. Waktu rehidrasi yang dibutuhkan untuk
masing=masing mi adalah 3.30 menit dan 5 menit untuk mi jagung substitusi kering dan instan, serta 3 menit untuk mi instan komersial. Mi yang disajikan pada sukarelawan adalah setara dengan 50 g karbohidrat dan ditambahkan bumbu.
Uji indeks glikemik dilakukan dengan menggunakan darah manusia sebagai objek