OPTIMASI PROSES REVERSE OSMOSIS
PADA RECOVERY DAN PEMEKATAN
KOMPONEN FLAVOR LIMBAH CAIR PASTEURISASI
RAJUNGAN
NINIK PURBOSARI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Optimasi Proses Reverse
Osmosis pada Recovery dan Pemekatan Komponen Flavor Limbah Cair Pasteurisasi Rajungan adalah karya saya dengan arahan komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Januari 2009
ABSTRACT
NINIK PURBOSARI. Optimization Reverse Osmosis Process in Recovery and Concentrated Flavor Component from Liquid Waste of Crab Meat Pasteurization. Supervised by JOKO SANTOSO and UJU.
Flavor components recovery from liquid waste of crab meat pasteurization is an economic way for upgrading waste treatment. The process itself is environmental friendly. An appropriate membrane technology, such as reverse osmosis (RO) is useful for this purpose. RO which its pore sizes are generally <1 kDa might produce higher yield compared to other methods. Hence, this study was aimed to observe the influence of transmembrane pressure (TMP), temperature and pH on flux and rejection level as parameters of membrane performance. Response Surface Method (RSM) was used to determine the optimum condition of membrane productivity and then applied on concentration process of flavor. Flavor compounds were subsequently characterized for their proximate composition, non protein nitrogen (NPN) and amino acid profile. The results showed that TMP and temperature affected the membrane performance, however was not pH. Optimum condition of RO performance was at TMP 716 kPa,
and 35 oC. Rejection level of protein by RO was up to 100%, it means these
compounds cannot penetrate into membrane. The concentration process yielded 1,10% protein as flavor components or 1,64 fold than the initial feed. NPN as a flavor component contributed 0,21 % of flavoring (10% more concentrated than the initial feed). Moreover, the amino acids were dominated by glutamic acid and leucine which contributed 20% and 10% of total amino acid in the concentrate, respectively.
Keywords: crab meat pasteurization, flavor recovery, liquid waste treatment, optimization, reverse osmosis, Response Surface Method (RSM)
RINGKASAN
NINIK PURBOSARI. Optimasi Proses Reverse Osmosis pada Recovery dan
Pemekatan Komponen Flavor Limbah Cair Pasteurisasi Rajungan. Dibimbing oleh JOKO SANTOSO dan UJU.
Limbah rajungan jika tidak dimanfaatkan dengan optimal dapat menjadi sumber pencemaran bagi lingkungan. Pemanfaatan limbah cair rajungan masih terbatas, diantaranya untuk pembuatan petis yang dilakukan secara tradisional. Alternatif pemanfaatan yang bernilai ekonomis adalah proses recovery komponen
flavor terkait kandungan berbagai komponen flavor dalam rajungan. Proses
recovery flavor banyak dilakukan dengan evaporasi atau freeze concentration.
Masalah yang muncul pada proses evaporasi adalah hilangnya sebagian
komponen volatil flavor karena panas, sedangkan proses freeze concentration
menghasilkan rendemen yang rendah. Penggunaan teknologi membran reverse
osmosis (RO) yang ramah lingkungan dan tingkat rejeksi yang tinggi diharapkan akan menghasilkan rendemen yang lebih besar.
Tujuan penelitian ini adalah untuk mengetahui pengaruh tekanan transmembran (TMP), suhu, dan pH terhadap nilai fluks dan rejeksi yang merupakan tolok ukur kinerja membran. Kondisi optimum yang diperoleh
selanjutnya diaplikasikan untuk proses recovery dan pemekatan komponen flavor
yang didapat.
Faktor tekanan transmembran dan suhu berpengaruh terhadap fluks dan rejeksi yang dihasilkan, sedangkan pH tidak berpengaruh. Respon fluks menghasilkan nilai yang mendekati optimum pada kondisi tekanan transmembran
716 kPa dan suhu 35 oC. Nilai rejeksi permeat berkisar 76,89 – 99,77%,
sedangkan rejeksi pada proses pemekatan berkisar 89 – 100%. Tingkat rejeksi membran RO bisa mencapai 100%, artinya semua komponen, termasuk protein sebagai makromolekul tidak dapat melewati membran RO dimana ukuran porinya sangat kecil.
Fluks pada proses pemekatan mempunyai pola penurunan terbesar pada awal-awal proses pemekatan. Hal ini disebabkan pengaruh polarisasi konsentrasi pada permukaan membran. Semakin tinggi konsentrasi maka terjadinya polarisasi semakin mudah.
Proses pemekatan menghasilkan komponen flavor protein 1,10% atau 1,64 kali dibandingkan dengan feed awal. Protein yang berhasil di-recovery sebesar 48%. Non protein nitrogen (NPN) sebagai komponen flavor memberikan
kontribusi pada flavouring sebesar 0,21% (lebih pekat 10% dibandingkan dengan
feed awal). Asam glutamat dan leusin merupakan asam amino dominan terbesar
© Hak cipta milik IPB, tahun 2009 Hak cipta dilindungi undang-undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau meyebutkan sumber.
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan kritik atau tinjauan suatu masalah.
b. Pengutipan tidak merugikan kepentingan yang wajar IPB.
OPTIMASI PROSES REVERSE OSMOSIS
PADA RECOVERY DAN PEMEKATAN
KOMPONEN FLAVOR LIMBAH CAIR PASTEURISASI
RAJUNGAN
NINIK PURBOSARI
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Departemen Teknologi Hasil Perairan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Optimasi Proses Reverse Osmosis pada Recovery dan Pemekatan Komponen Flavor Limbah Cair Pasteurisasi Rajungan
Nama : Ninik Purbosari
NRP : C351060031
Disetujui Komisi Pembimbing
Dr. Ir. Joko Santoso, M.Si Uju, S.Pi, M.Si Ketua Anggota
Diketahui
Ketua Program Studi Dekan Sekolah Pascasarjana Teknologi Hasil Perairan
Dr. Ir. Sri Purwaningsih, M.Si Prof. Dr. Ir. Khairil A. Notodiputro,MS
PRAKATA
Puji syukur penulis panjatkan ke hadirat Allah SWT, sebagai penentu segala peristiwa, yang telah memberikan ridhoNya sehingga karya ilmiah ini dapat diselesaikan. Tema yang dipilih dalam penelitian ini adalah recovery flavor
dan teknologi membran dengan judul “Optimasi Proses Reverse Osmosis pada
Recovery dan Pemekatan Komponen Flavor Limbah Cair Pasteurisasi Rajungan”. Karya tulis ini berisi beberapa gagasan dari penulis tentang pemanfaatan limbah cair rajungan dan penggunaan teknologi membran yang ramah lingkungan yang dapat memberikan nilai tambah terhadap limbah tersebut. Proses penelitian digambarkan dengan cukup jelas dan hasil yang diperoleh dibahas dengan membandingkan dengan hasil penelitian sebelumnya.
Karya ilmiah ini dapat diselesaikan dengan berbagai hambatan dan tantangan, dan tentu saja dengan segala kemudahan yang mengiringinya, tak lepas dari bantuan berbagai pihak. Untuk itulah pada kesempatan ini penulis ingin menyampaikan ungkapan terima kasih kepada :
1. Orang tua tercinta, atas segala pengorbannya, yang tak mungkin bisa
terbalas,
2. Mertua tercinta (almarhum) yang telah berjasa besar dalam melahirkan
seseorang yang sekarang menjadi pendamping hidup penulis,
3. Suami tercinta, imam keluarga yang senantiasa mencurahkan segala cinta
dan semangat kepada penulis,
4. Anak-anak tersayang atas keberadaannya selama ini,
5. Seluruh keluarga besar, kakak-kakak dan adik-adik yang telah
memberikan semangat dalam menyelesaikan studi ini,
6. Bapak Dr. Ir Joko Santoso, M.Si selaku dosen pembimbing sekaligus guru
kehidupan, yang telah banyak memberikan ilmu, bimbingan dan arahan, baik dalam keseharian maupun dalam penyusunan tesis,
7. Bapak Uju, S.Pi, M.Si sebagai dosen pembimbing, atas pengorbanan
8. Ibu Ir. Wini Trilaksani, M.Sc atas semua masukan yang diberikan untuk perbaikan dan pengkayaan tesis ini,
9. Ibu Dr. Tati Nurhayati, S.Pi, M.Si. atas waktu yang diluangkan untuk
berkonsultasi, dan kerelaannya meminjamkan peralatan selama penulis melaksanakan penelitian,
10.Kustiariyah, S.Pi, M.Si, Kania Arbiaty S.Pi, dan Oktafrina, S.Si yang
sudah banyak membantu penulis selama studi,
11.Teman-teman angkatan THP 06 : Mbak Tia, Uci, Mbak Puji, Mas Candra,
Mas Aim, Pak Mad, Pak Max ,dan Pak Dani atas kebersamaannya dalam suka dan duka,
12.Teman-teman yang selalu membantu selama penelitian dan penulisan
tesis: Ujang, Gilang, Glori, si Jeng Dede, dan Mbak Ria TIP,
13.Semua pihak yang telah memberikan kontribusinya, yang tidak dapat
disebutkan satu per satu. Semoga Allah memberikan balasan kebaikan atas semua yang telah dilakukan.
Akhir kata, semoga karya ilmiah ini bermanfaat.
Bogor, Januari 2009
RIWAYAT HIDUP
Penulis dilahirkan di Solo pada tanggal 16 Juni 1975 sebagai anak ke-lima dari enam bersaudara pasangan S. Prabowo dan Sumarni. Pendidikan Sekolah Menengah Atas (SMA) ditempuh di SMAN 1 Solo, lulus tahun 1994. Pendidikan sarjana ditempuh di Program Studi Teknologi Hasil Perikanan, Fakultas Perikanan dan Ilmu Kelautan IPB, lulus pada tahun 1999. Penulis bekerja sebagai dosen di Politeknik Negeri Lampung sejak tahun 2000 sampai dengan sekarang. Penulis menikah pada tahun 2002 dengan Setia Gunawan dan dikaruniai dua buah hati, Saskia Shafa’ Qolby Gunawan dan Ilham Rabbani As Sajjad Gunawan. Tahun 2006 penulis diterima di Program Pascasarjana IPB, Program Studi Teknologi Hasil Perairan.
OPTIMASI PROSES REVERSE OSMOSIS
PADA RECOVERY DAN PEMEKATAN
KOMPONEN FLAVOR LIMBAH CAIR PASTEURISASI
RAJUNGAN
NINIK PURBOSARI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Optimasi Proses Reverse
Osmosis pada Recovery dan Pemekatan Komponen Flavor Limbah Cair Pasteurisasi Rajungan adalah karya saya dengan arahan komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Januari 2009
ABSTRACT
NINIK PURBOSARI. Optimization Reverse Osmosis Process in Recovery and Concentrated Flavor Component from Liquid Waste of Crab Meat Pasteurization. Supervised by JOKO SANTOSO and UJU.
Flavor components recovery from liquid waste of crab meat pasteurization is an economic way for upgrading waste treatment. The process itself is environmental friendly. An appropriate membrane technology, such as reverse osmosis (RO) is useful for this purpose. RO which its pore sizes are generally <1 kDa might produce higher yield compared to other methods. Hence, this study was aimed to observe the influence of transmembrane pressure (TMP), temperature and pH on flux and rejection level as parameters of membrane performance. Response Surface Method (RSM) was used to determine the optimum condition of membrane productivity and then applied on concentration process of flavor. Flavor compounds were subsequently characterized for their proximate composition, non protein nitrogen (NPN) and amino acid profile. The results showed that TMP and temperature affected the membrane performance, however was not pH. Optimum condition of RO performance was at TMP 716 kPa,
and 35 oC. Rejection level of protein by RO was up to 100%, it means these
compounds cannot penetrate into membrane. The concentration process yielded 1,10% protein as flavor components or 1,64 fold than the initial feed. NPN as a flavor component contributed 0,21 % of flavoring (10% more concentrated than the initial feed). Moreover, the amino acids were dominated by glutamic acid and leucine which contributed 20% and 10% of total amino acid in the concentrate, respectively.
Keywords: crab meat pasteurization, flavor recovery, liquid waste treatment, optimization, reverse osmosis, Response Surface Method (RSM)
RINGKASAN
NINIK PURBOSARI. Optimasi Proses Reverse Osmosis pada Recovery dan
Pemekatan Komponen Flavor Limbah Cair Pasteurisasi Rajungan. Dibimbing oleh JOKO SANTOSO dan UJU.
Limbah rajungan jika tidak dimanfaatkan dengan optimal dapat menjadi sumber pencemaran bagi lingkungan. Pemanfaatan limbah cair rajungan masih terbatas, diantaranya untuk pembuatan petis yang dilakukan secara tradisional. Alternatif pemanfaatan yang bernilai ekonomis adalah proses recovery komponen
flavor terkait kandungan berbagai komponen flavor dalam rajungan. Proses
recovery flavor banyak dilakukan dengan evaporasi atau freeze concentration.
Masalah yang muncul pada proses evaporasi adalah hilangnya sebagian
komponen volatil flavor karena panas, sedangkan proses freeze concentration
menghasilkan rendemen yang rendah. Penggunaan teknologi membran reverse
osmosis (RO) yang ramah lingkungan dan tingkat rejeksi yang tinggi diharapkan akan menghasilkan rendemen yang lebih besar.
Tujuan penelitian ini adalah untuk mengetahui pengaruh tekanan transmembran (TMP), suhu, dan pH terhadap nilai fluks dan rejeksi yang merupakan tolok ukur kinerja membran. Kondisi optimum yang diperoleh
selanjutnya diaplikasikan untuk proses recovery dan pemekatan komponen flavor
yang didapat.
Faktor tekanan transmembran dan suhu berpengaruh terhadap fluks dan rejeksi yang dihasilkan, sedangkan pH tidak berpengaruh. Respon fluks menghasilkan nilai yang mendekati optimum pada kondisi tekanan transmembran
716 kPa dan suhu 35 oC. Nilai rejeksi permeat berkisar 76,89 – 99,77%,
sedangkan rejeksi pada proses pemekatan berkisar 89 – 100%. Tingkat rejeksi membran RO bisa mencapai 100%, artinya semua komponen, termasuk protein sebagai makromolekul tidak dapat melewati membran RO dimana ukuran porinya sangat kecil.
Fluks pada proses pemekatan mempunyai pola penurunan terbesar pada awal-awal proses pemekatan. Hal ini disebabkan pengaruh polarisasi konsentrasi pada permukaan membran. Semakin tinggi konsentrasi maka terjadinya polarisasi semakin mudah.
Proses pemekatan menghasilkan komponen flavor protein 1,10% atau 1,64 kali dibandingkan dengan feed awal. Protein yang berhasil di-recovery sebesar 48%. Non protein nitrogen (NPN) sebagai komponen flavor memberikan
kontribusi pada flavouring sebesar 0,21% (lebih pekat 10% dibandingkan dengan
feed awal). Asam glutamat dan leusin merupakan asam amino dominan terbesar
© Hak cipta milik IPB, tahun 2009 Hak cipta dilindungi undang-undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau meyebutkan sumber.
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan kritik atau tinjauan suatu masalah.
b. Pengutipan tidak merugikan kepentingan yang wajar IPB.
OPTIMASI PROSES REVERSE OSMOSIS
PADA RECOVERY DAN PEMEKATAN
KOMPONEN FLAVOR LIMBAH CAIR PASTEURISASI
RAJUNGAN
NINIK PURBOSARI
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Departemen Teknologi Hasil Perairan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Optimasi Proses Reverse Osmosis pada Recovery dan Pemekatan Komponen Flavor Limbah Cair Pasteurisasi Rajungan
Nama : Ninik Purbosari
NRP : C351060031
Disetujui Komisi Pembimbing
Dr. Ir. Joko Santoso, M.Si Uju, S.Pi, M.Si Ketua Anggota
Diketahui
Ketua Program Studi Dekan Sekolah Pascasarjana Teknologi Hasil Perairan
Dr. Ir. Sri Purwaningsih, M.Si Prof. Dr. Ir. Khairil A. Notodiputro,MS
PRAKATA
Puji syukur penulis panjatkan ke hadirat Allah SWT, sebagai penentu segala peristiwa, yang telah memberikan ridhoNya sehingga karya ilmiah ini dapat diselesaikan. Tema yang dipilih dalam penelitian ini adalah recovery flavor
dan teknologi membran dengan judul “Optimasi Proses Reverse Osmosis pada
Recovery dan Pemekatan Komponen Flavor Limbah Cair Pasteurisasi Rajungan”. Karya tulis ini berisi beberapa gagasan dari penulis tentang pemanfaatan limbah cair rajungan dan penggunaan teknologi membran yang ramah lingkungan yang dapat memberikan nilai tambah terhadap limbah tersebut. Proses penelitian digambarkan dengan cukup jelas dan hasil yang diperoleh dibahas dengan membandingkan dengan hasil penelitian sebelumnya.
Karya ilmiah ini dapat diselesaikan dengan berbagai hambatan dan tantangan, dan tentu saja dengan segala kemudahan yang mengiringinya, tak lepas dari bantuan berbagai pihak. Untuk itulah pada kesempatan ini penulis ingin menyampaikan ungkapan terima kasih kepada :
1. Orang tua tercinta, atas segala pengorbannya, yang tak mungkin bisa
terbalas,
2. Mertua tercinta (almarhum) yang telah berjasa besar dalam melahirkan
seseorang yang sekarang menjadi pendamping hidup penulis,
3. Suami tercinta, imam keluarga yang senantiasa mencurahkan segala cinta
dan semangat kepada penulis,
4. Anak-anak tersayang atas keberadaannya selama ini,
5. Seluruh keluarga besar, kakak-kakak dan adik-adik yang telah
memberikan semangat dalam menyelesaikan studi ini,
6. Bapak Dr. Ir Joko Santoso, M.Si selaku dosen pembimbing sekaligus guru
kehidupan, yang telah banyak memberikan ilmu, bimbingan dan arahan, baik dalam keseharian maupun dalam penyusunan tesis,
7. Bapak Uju, S.Pi, M.Si sebagai dosen pembimbing, atas pengorbanan
8. Ibu Ir. Wini Trilaksani, M.Sc atas semua masukan yang diberikan untuk perbaikan dan pengkayaan tesis ini,
9. Ibu Dr. Tati Nurhayati, S.Pi, M.Si. atas waktu yang diluangkan untuk
berkonsultasi, dan kerelaannya meminjamkan peralatan selama penulis melaksanakan penelitian,
10.Kustiariyah, S.Pi, M.Si, Kania Arbiaty S.Pi, dan Oktafrina, S.Si yang
sudah banyak membantu penulis selama studi,
11.Teman-teman angkatan THP 06 : Mbak Tia, Uci, Mbak Puji, Mas Candra,
Mas Aim, Pak Mad, Pak Max ,dan Pak Dani atas kebersamaannya dalam suka dan duka,
12.Teman-teman yang selalu membantu selama penelitian dan penulisan
tesis: Ujang, Gilang, Glori, si Jeng Dede, dan Mbak Ria TIP,
13.Semua pihak yang telah memberikan kontribusinya, yang tidak dapat
disebutkan satu per satu. Semoga Allah memberikan balasan kebaikan atas semua yang telah dilakukan.
Akhir kata, semoga karya ilmiah ini bermanfaat.
Bogor, Januari 2009
RIWAYAT HIDUP
Penulis dilahirkan di Solo pada tanggal 16 Juni 1975 sebagai anak ke-lima dari enam bersaudara pasangan S. Prabowo dan Sumarni. Pendidikan Sekolah Menengah Atas (SMA) ditempuh di SMAN 1 Solo, lulus tahun 1994. Pendidikan sarjana ditempuh di Program Studi Teknologi Hasil Perikanan, Fakultas Perikanan dan Ilmu Kelautan IPB, lulus pada tahun 1999. Penulis bekerja sebagai dosen di Politeknik Negeri Lampung sejak tahun 2000 sampai dengan sekarang. Penulis menikah pada tahun 2002 dengan Setia Gunawan dan dikaruniai dua buah hati, Saskia Shafa’ Qolby Gunawan dan Ilham Rabbani As Sajjad Gunawan. Tahun 2006 penulis diterima di Program Pascasarjana IPB, Program Studi Teknologi Hasil Perairan.
DAFTAR ISI
Halaman
DAFTAR TABEL... xiii
DAFTAR GAMBAR ... iv
DAFTAR LAMPIRAN...xv
1. PENDAHULUAN ...1
1.1 Latar Belakang ...1
1.2 Perumusan Masalah ...2
1.3 Tujuan dan Manfaat Penelitian ...3
1.4 Hipotesis...3
2. TINJAUAN PUSTAKA...4
2.1 Limbah Cair Perikanan ...4
2.2 Komponen Flavor ...5
2.2.1 Komponen flavor secara umum ...5
2.2.2 Komponen flavor pada rajungan...6
2.3 Proses Filtrasi dengan Membran...9
2.3.1 Reverse osmosis (RO) ...10
2.3.2 Kinerja membran reverse osmosis...11
2.4 Faktor-faktor yang Mempengaruhi Kinerja Membran...14
2.4.1 Fouling dan polarisasi konsentrasi...14
2.4.2 Tekanan transmembran ...15
2.4.3 Konsentrasi bahan ...15
2.4.4 Suhu ...16
2.4.5 pH...16
2.4.6 Tekanan osmotik ...16
2.4.7 Rejeksi...17
3. METODOLOGI PENELITIAN...18
3.1 Waktu dan Tempat ...18
3.2 Bahan dan Alat...18
3.3 Tahapan Penelitian ...19
3.3.1 Penentuan waktu tunak (steady state) ...20
3.3.3 Pengaruh suhu ...21 3.3.5 Pengaruh pH...21 3.4 Analisis dan Karakterisasi...21 3.4.1 Analisis non protein nitrogen (NPN) ...22 3.4.2 Analisis kandungan protein...22 3.4.3 Analisis asam amino ...23 3.4.4 Analisis proksimat...24 (a) Kadar air ...24 (b) Kadar abu...24 (c) Kadar protein ...25 (d) Kadar lemak...25 (e) Kadar karbohidrat ...26 3.5 Rancangan Percobaan ...26 3.6 Penentuan Optimasi Proses ...27
4. HASIL DAN PEMBAHASAN
4.1 Karakteristik Limbah Cair Pasteurisasi Rajungan ...28 4.1.1 Sifat fisik, nilai proksimat, dan kadar NPN ...28 4.1.2 Asam amino ...29 4.2 Pengaruh Parameter Operasi terhadap Kinerja Membran...31 4.2.1 Penentuan waktu tunak (steady state) ...31 4.2.2 Pengaruh parameter operasi terhadap fluks ...32 4.2.3 Rejeksi...35 4.3 Proses Pemekatan...38 4.3.1 Respon fluks selama proses pemekatan ...38 4.3.2 Respon rejeksi selama proses pemekatan ...41 4.3.3 Karakteristik hasil recovery dan pemekatan limbah cair
pasteurisasi rajungan ...42
5. KESIMPULAN ...48 5.1 Kesimpulan ...48 5.2 Saran...48
DAFTAR PUSTAKA ...50
DAFTAR TABEL
Halaman
1 Beban limbah cair dari beberapa jenis operasi
pengolahan perikanan...4 2 Komponen flavor dalam fraksi NPN dari berbagai sumber...6 3 Komposisi komponen flavor ekstrak daging rajungan (snow crab) ...7 4 Komponen flavor penyebab aroma khas daging rajungan...8 5 Pengelompokkan proses membran berdasarkan kisaran
DAFTAR GAMBAR
Halaman
1 Perbandingan antara proses osmosis dan reverse osmosis...10 2 Proses RO dengan sistem cross flow...12 3 Lokasi terjadinya fouling pada membran...14 4 Diagram alir tahapan proses penelitian ...19 5 Nilai fluks dan waktu tunak limbah cair pasteurisasi rajungan
selama proses filtrasi dengan membran RO...32 6 Permukaan respon fluks terhadap suhu dan TMP...34 7 Permukaan respon rejeksi terhadap TMP dan suhu ...38 8 Hubungan antara waktu pemekatan dengan nilai fluks...39 9 Hubungan antara faktor konsentrasi dengan fluks ...39 10 Kromatogram HPLC asam amino limbah pasteurisasi rajungan
DAFTAR LAMPIRAN
1 PENDAHULUAN
1.1 Latar Belakang
Rajungan tergolong hewan dasar (bentos) pemakan daging yang termasuk satu famili dengan kepiting. Saat ini rajungan merupakan komoditas ekspor unggulan hasil perikanan, khususnya untuk ekspor ke Jepang, Uni Eropa, dan Amerika Serikat. Nilai ekspor rajungan olahan ke pasar produktif tersebut mencapai 2.811 ton dengan nilai 24.037.475 US$ (DKP 2005).
Produksi rajungan mengalami peningkatan 4.866 ton per tahun (DKP 2004). Peningkatan produksi akan diikuti dengan peningkatan jumlah limbah yang dihasilkan, baik limbah padat berupa cangkang atau kulit dan limbah cair berupa air perebusan. Volume limbah cair yang dihasilkan oleh industri rajungan yang
diolah secara mekanis mencapai 29-44 m3/ ton rajungan, sedangkan yang diolah
secara konvensional berkisar 1-2 m3/ ton rajungan. Limbah cair ini menghasilkan
nilai Biochemical Oxygen Demand (BOD), Chemical Oxygen Demand (COD),
dan Total Suspended Solid (TSS) masing-masing 4.400, 6.300, dan 620 mg/l
(Islam et al. 2004). Nilai tersebut lebih tinggi dibandingkan limbah hasil
pengolahan tuna, udang, dan tiram. Sementara itu nilai baku mutu limbah cair untuk industri pengolahan ikan adalah : BOD 75 mg/l, COD 100 mg/l, dan TSS 60 mg/l (SK Gubernur DKI Jakarta Nomor 582 Tahun 1995). Limbah rajungan yang melebihi batas normal tersebut berpotensi menimbulkan pencemaran lingkungan jika tidak dimanfaatkan secara optimal. Hal ini menjadi masalah yang harus dicarikan solusinya.
Selama ini pemanfaatan limbah rajungan masih terbatas pada limbah padat, dimana cangkang rajungan dimanfaatkan sebagai bahan baku industri pakan dan pembuatan kitin serta kitosan (Hartati et al. 2002). Pemanfaatan limbah cair masih dilakukan secara tradisional, diantaranya untuk pembuatan petis.
Pemanfaatan lain yang bisa dilakukan adalah pengambilan atau recovery
komponen flavor dalam limbah tersebut mengingat adanya kandungan komponen flavor yang cukup tinggi dalam rajungan.
sebagian komponen volatil flavor karena panas (Kranawetter et al. 2005),
sedangkan proses freeze concentration menghasilkan rendemen yang rendah
(Jayarajah dan Lee 1988). Salah satu teknologi alternatif kompetitif yang bisa digunakan adalah teknologi membran yang hemat energi dan ramah lingkungan (Sheu dan Wiley 1983). Selain itu komponen volatil tetap terjaga.
Salah satu teknologi membran adalah reverse osmosis (RO) yang
diharapkan dapat menghasilkan rendemen yang lebih tinggi dibanding proses ultrafiltrasi (UF) karena secara teoritis tingkat rejeksi (komponen tertahan) RO lebih tinggi daripada UF. Teknologi RO telah banyak digunakan untuk proses
recovery flavor pada apel, lemon, dan mangga (Matsuura et al. 1975; Kane et al. 1995; Olle et al. 1997).
Terbatasnya informasi tentang kinerja membran RO yang optimal untuk
proses recovery flavor, khususnya pda limbah pasteurisasi rajungan, menjadi
alasan kuat dilakukannya penelitian ini. Untuk itulah pada penelitian ini dicari kondisi optimum kinerja RO yang diaplikasikan untuk pemekatan komponen flavor hasil proses recovery.
1.2 Perumusan Masalah
Pemanfaatan limbah cair rajungan yang masih terbatas pada pembuatan petis dengan jumlah kecil dan bersifat tradisional, merupakan tantangan sekaligus masalah yang harus dipecahkan, karena jika limbah tersebut tidak dimanfaatkan secara optimal maka akan menjadi sumber pencemar lingkungan. Kandungan beberapa jenis komponen flavor yang cukup tinggi dalam rajungan
memungkinkan untuk dilakukannya proses recovery komponen tersebut. Proses
recovery flavor selama ini dilakukan dengan cara evaporasi yang menyebabkan
hilangnya beberapa komponen volatil, dan proses freeze concentration yang
penggunaan RO untuk proses recovery tersebut juga belum diketahui, dimana ada beberapa faktor yang mempengaruhi, diantaranya tekanan transmembran, suhu, dan pH.
1.3 Tujuan dan Manfaat Penelitian
Tujuan dari penelitian adalah :
(a) Mengetahui pengaruh tekanan transmembran, suhu, dan pH bahan pada
kinerja membran RO.
(b) Mendapatkan kondisi optimal kinerja membran RO.
(c) Melakukan pemekatan dan karakterisasi komponen flavor hasil pemekatan
limbah cair rajungan dengan teknologi RO. Manfaat dari penelitian adalah :
(a) Dapat mengoptimalkan kinerja membran RO dengan pemakaian variabel
terpilih yang berpengaruh.
(b) Dihasilkannya produk hasil recovery limbah cair rajungan melalui pemurnian dan pemekatan dengan teknologi RO.
1.4 Hipotesis
Hipotesis yang digunakan dalam penelitian ini adalah :
(a) Tekanan transmembran, suhu, dan pH bahan berpengaruh terhadap kinerja
RO.
(b) Terdapat komponen flavor hasil pemekatan limbah cair rajungan.
2 TINJAUAN PUSTAKA
2.1 Limbah Cair Perikanan
Limbah cair yang dihasilkan dari pengolahan hasil perikanan mengandung banyak protein dan lemak, akibatnya menghasilkan nilai BOD dan TSS yang cukup tinggi. Kadar BOD dan TSS tersebut berbeda-beda tergantung jenis industri yang sangat dipengaruhi oleh tingkat produksi, jenis bahan mentah, kesegaran, dan jenis produk akhir yang dihasilkan (Gonzales 1996). Karakteristik limbah cair dari berbagai jenis industri hasil perikanan dapat dilihat pada Tabel 1.
Tabel 1 Beban limbah cair dari beberapa jenis operasi pengolahan perikanan
Beban limbah cair BOD COD Minyak/
lemak Padatan Tersuspen si Pengolahan ikan (manual)
332 kg/t - 0,348 kg/t 1,42 kg/t
Pengolahan ikan (mekanik)
11,9 kg/t - 2,28 kg/t 8,92 kg/t
Fillet ikan herring 3.482-10.000
mg/l
- 857-6.000 mg/l
-
Pengalengan tuna 6,8-20 kg/t 11,4-64 kg/t 1,7-13 kg/t 3,8-17
kg/t
Pabrik sardin 9,22 kg/t - 1,74 kg/t 5,41 kg/t
Pengolahan kepiting
4,8-5,5 kg/t 7,2-7,8 kg/t 0,21-0,3 kg/t 0,7-0,78
kg/t Pengolahan
kerang
18,7 kg/t - 0,461 kg/t 6,35 kg/t
Cairan darah dari pabrik makanan ikan
23.500-34.000 mg/l
93.000 mg/l 0-1,92% -
Air dari pengepresan daging
13.000-76.000 mg/l
- 60-1 560 mg/l -
Udang beku 160 mg/l 1,780 mg/l - -
Pengalengan ikan 941,69 mg/l 1.401,78
mg/l
- -
Makanan ikan 245,23 mg/l 949,05 g/l 6.976 mg/l -
Limbah cair dalam industri hasil perikanan dilepaskan melalui tahapan sebagai berikut : perlakuan bahan mentah (pencairan dan persiapan), pembersihan (pencucian dan preparasi), dehidrasi, pengepresan, penyaringan, pemanasan, pendinginan, dan pembersihan alat. Cairan ini mengandung darah dan potongan-potongan ikan dan kulit, isi perut, dan kondensat dari operasi pemasakan dan air pendingin dari kondensor (Jenie dan Rahayu 1990).
Limbah pengolahan rajungan diduga mengandung sejumlah senyawa yang terlarut diantaranya asam amino, nukleotida, peptida, dan asam organik (Cha et al. 1993). Limbah tersebut berasal dari effluent industri perikanan jenis krustasea sebesar 28,6% (pencucian) dan 71,4% (proses).
2.2 Komponen Flavor
2.2.1 Komponen flavor secara umum
Flavor adalah kombinasi dari rasa, bau, dan perasaan yang ditimbulkan
oleh adanya senyawa cita rasa (flavoring agents) yang biasanya terdapat dalam
jumlah yang sangat kecil dalam bahan pangan. Flavor dapat dibuat dari campuran berbagai komponen flavor, baik yang alami maupun sintetik. Berdasarkan bentuk fisiknya flavor dapat diklasifikasikan menjadi tiga kelas yaitu bentuk padat
(solid), bentuk cair (liquid), dan bentuk pasta (paste). Protein, lemak, dan karbohidrat adalah komponen struktural pada sel makhluk hidup yang merupakan sumber terbesar pembentuk flavor (Supran 1978).
Komponen pembentuk flavor pada produk perikanan lebih banyak ditemukan pada daging moluska dan krustasea. Komponen flavor non volatil
pada shellfish merupakan komponen larut air dan mempunyai bobot molekul yang
kreatin, asam mino bebas, nukleotida dan basa purin, serta urea. Komponen flavor yang terdapat dalam fraksi NPN dari berbagai sumber disajikan pada Tabel 2.
Berdasarkan hasil penelitian terhadap daging remis, udang dan kepiting
mempunyai aroma dan cita rasa (flavorfull) yang lebih tinggi daripada daging
ikan. Demikian juga asam-asam amino bebas yang terkandung dalam krustasea memiliki jumlah yang lebih banyak jika dibandingkan dengan ikan. Taurin, prolin, glisin, alanin, dan arginin dalam tingkat yang tinggi merupakan karakteristik umum yang ditemukan pada setiap krustasea (Konosu dan Yamaguchi 1982). Senyawa alkilpirazine dan sulfur merupakan kontributor penting pemberi flavor pada krustasea yang dimasak. Pan dan Kuo (1994) melaporkan bahwa komponen volatil dari alkohol tidak jenuh dan aldehida dengan atom karbon kurang dari 10 merupakan kontributor penting dalam memberikan flavor pada shellfish segar atau mentah.
Hayashi et al. (1981) dan Trilaksani et al. (1997) melaporkan bahwa
komponen utama penyusun flavor dalam makanan laut terdiri dari asam amino bebas berberat molekul rendah, nukleotida, asam organik, dan gula. Flavor yang mengandung 15 jenis asam amino terikat dan 17 asam amino bebas diperoleh dari
proses recovery limbah cair industri pengolahan tiram (Shiau dan Chai 1999).
Spurvey et al. (2001) menyatakan komponen-komponen flavor tersebut bersifat
[image:31.595.115.559.543.753.2]larut dalam air.
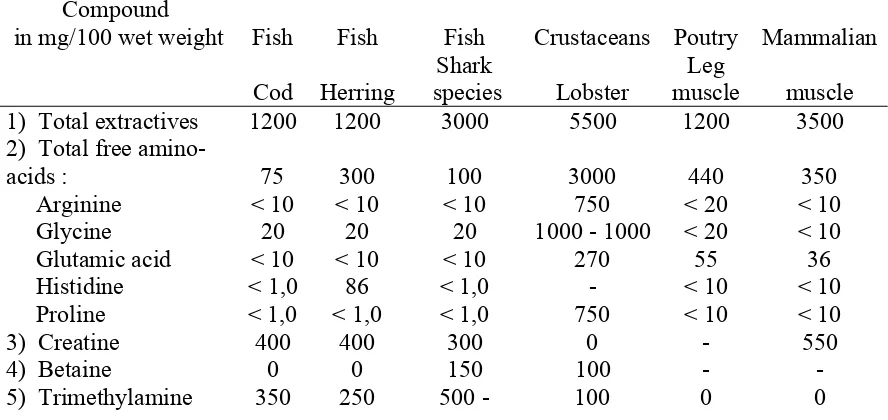
Tabel 2 Komponen flavor dalam fraksi NPN dari berbagai sumber Compound
in mg/100 wet weight Fish Fish Fish Crustaceans Poutry Mammalian
Cod Herring
Shark
species Lobster
Leg
muscle muscle
1) Total extractives 1200 1200 3000 5500 1200 3500
2) Total free
amino-acids : 75 300 100 3000 440 350
Arginine < 10 < 10 < 10 750 < 20 < 10
Glycine 20 20 20 1000 - 1000 < 20 < 10
Glutamic acid < 10 < 10 < 10 270 55 36
Histidine < 1,0 86 < 1,0 - < 10 < 10
Proline < 1,0 < 1,0 < 1,0 750 < 10 < 10
3) Creatine 400 400 300 0 - 550
4) Betaine 0 0 150 100 - -
oxide 1000
6) Anserine 150 0 0 0 280 150
7) Carnosine 0 0 0 0 180 200
8) Urea 0 0 200 - - 35
Sumber : Huss (1995)
2.2.2 Komponen flavor pada rajungan
Rajungan merupakan salah satu produk perikanan yang bernilai ekonomis tinggi dan disukai oleh pasar dunia karena memiliki flavor yang khas. Rajungan banyak mengandung glisin, arginin, prolin dan taurin. Keempat jenis asam amino bebas ini yang paling berperan dalam pembentukan komponen rasa aktif rajungan.
Konosu et al. (1978); Yamaguchi dan Watanabe (1990) melaporkan bahwa
komponen penyebab rasa khas dari daging rajungan adalah sejumlah komponen flavor yang larut air, antara lain : taurin, asam aspartat, threonin, serin, sarkosin, asam glutamat, prolin, glisin, alanin, asam α-aminobutirat, valin, metionin, leusin, tirosin, fenilalanin, ornitin, lisin, histidin, metilhistidin, triptopan, arginin, citosine monophosphate (CMP), adenosine monophosphate (AMP), guanine monophosphate (GMP), inosine monophosphate (IMP), adenosine diphosphate (ADP), adenosin, hypoxanthine, inosine, guanine, citosin, trimrthylamine oxides (TMAO), homarin, ribosa, asam laktat, asam suksinat, Na+, K+, Cl-, ~I dan PO4 3-.
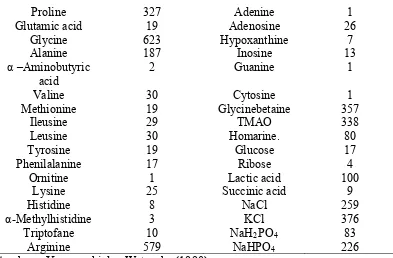
[image:32.595.113.512.645.747.2]Yamaguchi dan Watanabe (1990) melaporkan bahwa asam glutamat memegang peranan penting dalam memberikan rasa umami pada rajungan. Ketika asam glutamat dihilangkan, maka karakteristik dari flavor rajungan menjadi turun. Asam glutamat dalam bentuk garam yaitu monosodium glutamat (MSG) meupakan senyawa cita rasa yang memberikan rasa enak pada rajungan (flavor potentiator) (Winarno 1997). Komposisi komponen flavor rajungan (snow crab) disajikan pada Tabel 3.
Tabel 3 Komposisi komponen flavor ekstrak daging rajungan (snow crab)
Komponen Flavor Jumlah
(mg/100ml)
Komponen Flavor Jumlah
(mg/100ml)
Tau 243 CMP 6
Asp 10 AMP 32
Thr 14 GMP 4
Ser 14 IMP 5
Proline 327 Adenine 1
Glutamic acid 19 Adenosine 26
Glycine 623 Hypoxanthine 7
Alanine 187 Inosine 13 α –Aminobutyric
acid
2 Guanine 1
Valine 30 Cytosine 1
Methionine 19 Glycinebetaine 357
Ileusine 29 TMAO 338
Leusine 30 Homarine. 80
Tyrosine 19 Glucose 17
Phenilalanine 17 Ribose 4
Ornitine 1 Lactic acid 100
Lysine 25 Succinic acid 9
Histidine 8 NaCl 259
α-Methylhistidine 3 KCl 376
Triptofane 10 NaH2PO4 83
Arginine 579 NaHPO4 226
Sumber : Yamaguchi dan Watanabe (1990)
Cha et al. (1993) menemukan sejumlah komponen flavor pada rajungan salju (snow crab) masak. Komponen flavor tersebut berupa senyawa aldehida (11 jenis), keton (14 jenis), alkohol (13 jenis), asam (5 jenis), senyawa aromatik (21 jenis), senyawa nirogen (24 jenis), senyawa sulfur (10 jenis), furans (98 jenis), dan senyawa lainnya (16 jenis).
Chung (1999) melaporkan bahwa komponen volatil penyebab aroma khas
daging rajungan karang (Charybdis feriatus) yang terdeteksi sebanyak 177
[image:33.595.117.510.80.338.2]komponen, 130 diantaranya telah dapat diidentifikasi. Komponen flavor tesebut dapat dilihat pada Tabel 4.
Tabel 4 Komponen flavor penyebab aroma khas daging rajungan
Golongan Contoh senyawa
Asam -
Aldehida pentenal, hexanal, 2-methyl-(E)butenal, (E)-2-pentenal,
benzaldehyde, cyclopentanecarboxaldehide, nonanal,1,3 dimetil benzaldehide
Aromatik benzene, toluene, ethylbenzene, p-xylene, m-xylene, o-xylene, isopropil benzene, propylbenzene, styrene, C4-benzene, 1,3-dietil benzene
Ester n-butyl acetate, metyl (E, E) farnesate, dietyl phthalate,
dibutil phthalate
Furans 2-ethylfuran, 2 penthylfuran, S-hexyldihidro-2(3H)furanone
Piridin Pyridine, 2-rnethylpyridine, 3-metilpyridine
Naptalen Naphtalene, 2-methyhzaphthalene, 1-methylnapthalene,
C2-napthalene, C3-napthalene
Pirazin Pyrazine, methyl pyrazine, 2-isopropyl pyrazine,
2-acetyl-3-methyl pyrazine
Alkohol 2-methyl-propanol, 2 propen-l-ol, 2 pentanol, BHT, phenol,
nerolidol, 1 phenylethanol
Keton 3-buten-2-one, 2,3-butadione, 3-hexanone, 2-heptanone,
(E,E)3,5-octadien-2-one
Sulfur Hydrogen sulfide, carbon disulfide, 2-methylthiazole,
5-ethyl-3,4-dimethylthiazole, 3,5-dimethyl-1,2,4 trithiolane, 3-methyl-2-thiophencarboxaldehyde, 1,2,4-trithiolane, N,N-dimethyl ethanethioamide
Terpen Limone, camphor, β-ionone
Senyawa lain Trimetilamin, trimetilazole, 2,3-dihidro-5-metil 1H-indene, 2,3-dididro-4-metil-1H-indene
Sumber : Chung (1999)
Yamaguchi dan Watanabe (1990) melaporkan bahwa beberapa komponen
yang memberikan kontribusi pada taste rajungan adalah : glisin, alanin, asam
glutamat, arginin, AMP, GMP, CMP, dan ion-ion anorganik seperti Na+, K+, Cl-, dan PO43-. Lioe et al. (2005) melaporkan bahwa selain asam glutamat bebas dan
2.3 Proses Filtrasi dengan Membran
Filtrasi merupakan proses pemisahan dua atau lebih komponen dalam suatu aliran fluida (Brock 1983). Membran merupakan lapisan tipis dari suatu material berpori yang dapat digunakan untuk proses pemisahan. Pori-pori yang kecil pada membran dapat berfungsi sebagai penghalang secara fisik, sehingga mampu meloloskan dan menghalangi molekul senyawa tertentu (Wenten 1999).
[image:35.595.115.519.330.465.2]Menurut Renner dan El-Salam (1991), proses membran dikelompokkan ke dalam tiga kelas yaitu mikrofiltrasi, ultrafiltasi, dan reverse osmosis. Beberapa parameter yang menjadi indikator pengelompokkan tersebut disajikan pada Tabel 5.
Tabel 5 Pengelompokkan proses membran berdasarkan kisaran ukuran partikel yang direjeksi.
Parameter Mikrofiltrasi Ultrafiltrasi Reverse Osmosis
Ukuran
partikel tertahan
>106 Da 0,01 – 10 um
103 – 106 Da 0,001 – 0,002 um
< 103 Da < 0,001 um
Tekanan (bar) < 2 1 - 15 > 20
Mekanisme penahanan
Penyaringan molekul
Penyaringan molekul Penyaringan
molekul/ difusi
Fluks ( l m-2h-1) > 300 30 - 300 3 - 30
Sumber : Renner dan EI-Salam (1991)
Membran mikrofiltrasi dan ultrafiltrasi telah banyak diaplikasikan dalam industri pangan untuk tujuan pengkonsentrasian dan pemurnian biopolimer. Beberapa senyawa makromolekul yang telah diperoleh dari proses membran diantaranya adalah protein, dan polisakarida (Carrere et al. 1998; Jorda et al.
2002; Yeh dan Dong 2003; Cho et al. 2003). Keunggulan proses pemisahan
dengan menggunakan membran dibandingkan dengan filtrasi konvensional dalam pemurnian larutan umpan antara lain (Mulder 1996):
- merupakan teknologi yang sederhana, - dioperasikan pada suhu ruang,
- dapat dilakukan secara kontinyu,
- membran dapat dikombinasikan dengan proses lainnya, tanpa mengalami perubahan fase, baik kimia maupun fisika,
- biaya operasi relatif rendah,
- tidak menggunakan bahan tambahan atau kimia, - relatif mudah untuk meningkatkan skala operasinya.
2.3.1 Reverse osmosis (RO)
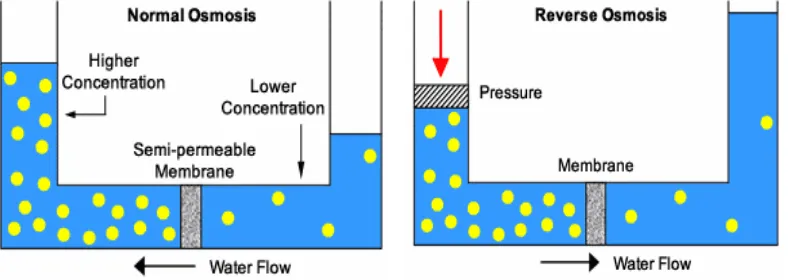
Proses reverse osmosis (RO) merupakan kebalikan dari proses osmosis
(normal osmosis), dimana pada proses osmosis, terjadi perpindahan pelarut dari larutan yang lebih encer (potensial kimia rendah) ke larutan yang lebih pekat
(potensial kimia tinggi) (Gambar 1). Sebaliknya pada proses reverse osmosis
[image:36.595.118.512.300.440.2]pelarut dipaksa berpindah dari larutan pekat ke larutan yang lebih encer dengan bantuan tekanan kerja (Wenten 1999).
Gambar 1 Perbandingan antara proses osmosis dan reverse osmosis
(Sumber : http://www.watertiger.net)
Membran RO digunakan untuk memisahkan zat terlarut yang memiliki bobot molekul yang rendah seperti garam anorganik atau molekul organik kecil
seperti glukosa dan sukrosa dari larutannya. Membran ini lebih dense/padat
sehingga memerlukan tahanan hidrodinamik yang lebih besar untuk melakukan proses pemisahan. Hal ini menyebabkan tekanan operasi pada RO akan sangat besar untuk menghasilkan fluks yang sama pada proses mikrofiltrasi dan ultrafiltrasi (Wenten 1999).
Proses reverse osmosis mempunyai beberapa keuntungan dibandingkan
dengan proses membran lainnya. Keuntungan tersebut adalah rendemen yang lebih tinggi, terkait dengan ukuran pori yang digunakan (Sheu dan Wiley 1983). Selain itu, dengan partikel yang tertahan berukuran lebih kecil dibandingkan
dengan membran lainnya, maka diharapkan keluaran bahan (permeat) yang
Penggunaan teknologi membran khususnya RO semakin berkembang dengan diaplikasikannya teknologi tersebut dalam bidang industri. Matsuura et al. (1975) berhasil merecovery komponen flavor dari apple juice dengan teknik
reverse osmosis (RO). Lee et al. (1982) melaporkan penggunaan proses ultrafiltrasi dan RO untuk pemurnian dan pengkonsentrasian betalaine. Lebih
lanjut Sheu dan Wiley (1983) melaporkan bahwa teknologi reverse osmosis
mampu merecovery flavor volatil dari apple juice sebesar 85%. Teknologi
membran juga dapat diaplikasikan untuk proses recovery komponen flavor yaitu
protein dari limbah pencucian tiram (Shiau dan Chai 1999).
2.3.2 Kinerja membran reverse osmosis
Kinerja membran RO pada prinsipnya sama dengan membran yang lain dimana dalam pemisahan terutama dipengaruhi oleh karakteristik membran yang digunakan. Penilaian terhadap karakteristik membran diantaranya meliputi struktur, ukuran pori, serta sifat fisika-kimia lainnya. Parameter utama yang digunakan dalam penilaian kinerja membran filtrasi adalah fluks dan rejeksi (Osada dan Nakagawa 1992).
Scott dan Hughes (1996) mendefinisikan fluks sebagai jumlah volume permeat (filtrat) yang diperoleh pada operasi pemisahan per satuan luas permukaan membran dan per satuan waktu dan rejeksi sebagai kemampuan suatu membran untuk menahan partikel berukuran tertentu. Wenten (1999) menyatakan bahwa nilai rejeksi menunjukkan kemampuan suatu membran untuk menahan suatu komponen agar tidak melewati pori membran.
Nilai rejeksi membran juga menunjukkan tingkat penolakan membran terhadap suatu komponen. Tingkat penolakan membran tergantung pada
Molecular Weight Cut Off (MWCO), yaitu suatu nilai ukuran molekul yang mendekati nilai tertentu yang dapat diterima oleh membran dengan faktor penolakan sebesar 0,99 dalam suatu larutan encer (Toledo 1991).
Faktor penting dari membran RO adalah fluks permeat dan selektivitas, dimana fluks dapat ditingkatkan dengan cara mengurangi ketebalan membran. Untuk itu pada umumnya membran RO mempunyai struktur asimetrik dengan lapisan atas yang tipis dan dense serta matriks penyokong dengan tebal 50 – 150
Sistem operasi filtrasi membran dapat dilakukan dengan dua cara, yaitu sistem dead-end dan sistem cross flow. Sistem dead-end umpan dilewatkan secara tegak lurus dengan membran, dan hanya mempunyai satu fraksi saja yaitu retentat (molekul yang tidak dapat melewati pori). Pada sistem cross flow, umpan berupa larutan dialirkan sejajar dengan permukaan membran. Hasil proses pada sistem
cross flow terdiri dari dua fraksi, yaitu molekul-molekul yang dapat melewati pori-pori membran yang disebut permeat dan molekul berukuran besar yang tidak dapat melewati pori disebut retentat atau konsentrat. Sistem operasi cross flow
lebih menguntungkan dibanding sistem dead-end, karena laju cross flow dapat
berfungsi sebagai aliran penyapu secara kontinyu terhadap retentat yang menutupi
permukaan membran (Gould et al. 2004). Kecepatan aliran cross flow akan
semakin kecil dengan semakin dekatnya dengan dinding pori membran dan mencapai nilai nol ketika pada permukaan dinding pori membran (Wenten 1999). Proses RO dengan sistem cross flow dapat dilihat pada Gambar 2.
Jika fluks permeat (J) didefinisikan sebagai jumlah volume cairan yang melewati membran per satuan luas permukaan membran dalam satuan waktu.
Model Hagen-Poiseuille memprediksi besarnya nilai fluks permeat tersebut seperti yang disajikan dalam persamaaan sebagai berikut :
Gambar 2 Proses RO dengan sistem cross flow
(www.inge.ag/en/technologie/funktionsweise.html)
ΔΧΔΡ =
η ε
8 2
R
J (1)
Keterangan :
J = fluks permeat (ms-1)
ε = porositas membran
R = jari-jari membran (m)
ΔP = selisih tekanan dalam membran dengan luar membran (Pa)
ΔX = ketebalan membran (m)
Ketebalan membran, porositas, dan jari jari pori merupakan karakter yang unik dari suatu membran dan biasanya digabungkan menjadi satu yang biasa disebut dengan tahanan membran internal (Bai dan Leow 2002). Jika K
merupakan koefisien permeabilitas membran (m Pa -1 s-1) dan Rm merupakan
tahanan membran internal (Pa s m-'), dan hubungan Rm = 1/K dan harga Rm
dinyatakan dengan persamaan (2) sebagai berikut :
(2)
2
εR 8
Rm= ΔΧ
Maka melalui substitusi nilai Rm pada persamaan fluks (persamaan (1)) akan diperoleh persamaan (3):
ΔΧ ΔΡ = ΔΧ ΔΡ = ΔΡ = 8 η εR εR 8 η ηRm J 2 2 (3) Keterangan :
J = fluks permeat (ms-1)
ε = porositas membran
R = jari-jari membran (m)
ΔP = selisih tekanan dalam membran dengan luar membran (Pa)
Rm = tekanan membran internal (Pas m-1)
ΔX = ketebalan membran (m)
η = viskositas cairan yang melewati pori membran (Pas)
Nilai fluks juga dapat dinyatakan dalam bentuk fungsi dari koefisien permeabilitas dan tekanan transmembran dengan persamaan (4) sebagai berikut :
(4)
ΔΡ = K.
J
2.4 Faktor-faktor yang Mempengaruhi Kinerja Membran
Faktor-faktor yang mempengaruhi kinerja membran merupakan faktor yang berpengaruh terhadap nilai fluks dan rejeksi yang dihasilkan. Faktor tersebut antara lain fouling dan polarisasi konsentrasi, konsentrasi bahan, suhu, pH bahan, tekanan trasmembran, dan laju alir bahan. Nilai fluks juga dipengaruhi oleh adanya tekanan osmosis pada proses membran.
Masalah utama dalam proses filtrasi dengan membran adalah menurunnya fluks selama proses filtrasi berlangsung. Secara umum dua faktor yang menyebabkan menurunnya fluks adalah fouling dan polarisasi konsentrasi.
1. Fouling
Fouling merupakan perubahan yang bersifat irreversibel yang disebabkan oleh interaksi secara fisik dan kimia antara membran dan partikel yang terdapat dalam larutan yang dipisahkan. Hal ini akan meyebabkan nilai fluks menurun
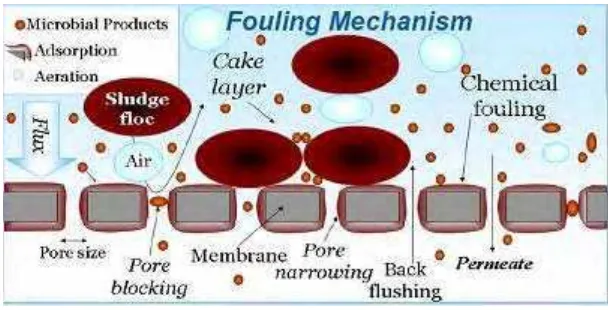
(Wenten 1999). Menurut Gould et al. (2004), fouling pada membran dapat
terjadi pada 3 lokasi yaitu di dekat, pada, atau dalam membran yang berupa
penyumbatan pori (pore blocking), pembentukan lapisan cake dan penyumbatan
pori membran bagian dalam atau interior pore fouling (Gambar 3).
[image:40.595.157.461.322.477.2]
Gambar 3 Lokasi terjadinya fouling pada membran
http://www.ete.wur.nl
2. Polarisasi konsentrasi
Fenomena polarisasi konsentrasi muncul ketika proses mikrofiltrasi atau ultrafiltrasi dilakukan untuk memisahkan bahan-bahan seperti hidrokoloid, protein dan molekul besar lainnya. Molekul-mulekul ini akan terejeksi dan menumpuk serta akan menutupi permukaan membran atau bahkan sampai membentuk lapisan gel atau cake (Cheryan 1998). Pada kondisi ini fluks tidak dipengaruhi lagi oleh tekanan tetapi dikendalikan oleh mekanisme perpindahan massa. Penggunaan tekanan yang lebih tinggi lagi tidak akan dapat meningkatkan besarnya fluks.
Tekanan transmembran merupakan driving force dalam proses filtrasi dengan menggunakan membran. Tekanan transmembran didefinisikan sebagai perbedaan tekanan antara sisi rententat dan permeat (persamaan 5).
(5) 2
ut
in Po
P
P= +
Keterangan : Pin = Tekanan pada saat masuk (Pa)
Pout = Tekanan pada saat keluar (Pa)
Fluks permeat akan meningkat dengan semakin meningkatnya tekanan transmembran, tetapi korelasi ini hanya berlaku pada umpan air murni atau pada kondisi tekanan rendah, konsentrasi umpan rendah, dan laju alir umpan yang tinggi (Mulder 1996). Jika umpan berupa larutan lain, maka besarnya fluks akan naik sampai batas tertentu, tetapi setelah mencapai tekanan tertentu fluks tidak akan meningkat walaupun tekanan dinaikkan. Pada tekanan rendah, fluks akan meningkat secara tidak linier pada peningkatan tekanan, sedangkan pada tekanan tinggi, fluks relatif konstan. Tekanan yang digunakan berkisar antara 30-40 bar
(Lee et al. 1982); Sheu and Wiley (1983) menggunakan tekanan sebesar 35- 45
bar untuk proses pengkonsentrasian apple juice.
2.4.3 Konsentrasi bahan
Konsentrasi bahan yang tinggi menyebabkan penurunan fluks sehingga suatu saat fluks akan dapat bernilai nol. Model teori film menyatakan bahwa fluks akan menurun secara eksponensial jika konsentrasi bahan meningkat dan fluks akan mencapai nol jika terjadi konsentrasi bahan sama dengan konsentrasi gel (Mulder 1996). Kondisi ini berlaku pada setiap suhu dan tipe aliran yang berbeda.
2.4.4 Suhu
Suhu yang lebih tinggi akan menyebabkan fluks yang lebih besar baik pada pressure controlled region maupun mass transfer controlled region. Suhu yang lebih tinggi akan menyebabkan penurunan viskositas bahan dan proses difusi akan menjadi lebih besar. Suhu yang tinggi menyebabkan retensi gula pada
(Sheu and Wiley 1983). Suhu yang lebih tinggi dilaporkan tidak memberikan efek pada recovery total asam. Suhu operasional membran berkisar 20 – 45 oC.
2.4.5 pH
Tingkat keasaman atau pH memberikan pengaruh pada kinerja membran. Nilai pH akan berpengaruh terhadap kelarutan zat yang akan dipisahkan oleh membran. Kuo dan Cheryan (1983) melaporkan bahwa pH memberikan pengaruh
terhadap kelarutan garam pada proses pengasaman whey sehingga menyebabkan
peningkatan fluks. Hal yang sama dilaporkan oleh D’Souza dan Wiley (2003) dimana fluks terendah terjadi pada pH isoelektrik protein, dan tertinggi pada nilai yang bergeser dari pH isoelektrik.
2.4.6 Tekanan osmotik
Makromolekul umumnya tertahan pada permukaan membran, sedangkan molekul berberat molekul rendah dapat menembus membran sebagai permeat. Kontribusi utama tekanan osmotik yang diperoleh dari makromolekul yang tertahan pada permukaan membran rendah, sehingga biasanya diabaikan (Wenten 1999). Proses dimana nilai fluks dan rejeksi tinggi serta koefisien perpindahan massa yang rendah, maka konsentrasi dari makromolekul yang tertahan pada permukaan membran menjadi semakintinggi sehingga tekanan osmotik tidak dapt diabaikan. Jika tekanan osmotik tidak diabaikan, maka persamaan fluks menjadi (persamaan 6).
) (
) (
Rm J
η π
Δ − ΔΡ
= (6)
Keterangan :
∆P = beda tekanan hidraulik
∆π = beda tekanan osmotik
η = viskositas cairan yang melewati pori membran (Pas)
Rm = tekanan membran internal (Pas m-1)
2.4.7 Rejeksi
bersamaan dengan berbedanya bobot molekul larutan yang dilewatkan (Mulder 1996). Nilai rejeksi membran dari suatu komponen dapat dihitung berdasarkan persamaan sebagai berikut (D’souza dan Wiley 2003; Kumar et al. 2003) :
r p
C C 1
R= −
Keterangan :
R = tingkat rejeksi membran Cp = konsentrasi permeat
Cr = konsentrasi retentat
3 METODOLOGI PENELITIAN
3.1 Waktu dan Tempat
di Laboratorium Mikrobiologi dan Biokimia, Departemen Teknologi Hasil Perairan, FPIK IPB, dan analisis kandungan asam amino dilakukan di Laboratorium Pasca Panen Pertanian Cimanggu Bogor.
3.2 Bahan dan Alat
Bahan baku yang digunakan pada penelitian ini adalah "limbah cair" pasteurisasi dari industri pasteurisasi rajungan. Sumber bahan baku tersebut diambil dari industri pengolahan rajungan di wilayah Losari dan Cirebon. Bahan untuk analisis proksimat dan NPN diantaranya asam borat, dietil eter, dan TCA 7%. Analisis asam amino menggunakan standar murni asam amino, bufer asam asetat, larutan pengering dan derivatisasi berupa metanol, picolotiocianat, dan triethylamine. NaOH 0, 1 N digunakan untuk mencuci membran.
Peralatan utama yang digunakan pada penelitian ini adalah : satu unit membran RO (CSM Model No RE 75-1812-50GPD). Modul membran yang
digunakan reverse osmosis dengan nilai 95% NaCI. Peralatan dan bahan
pendukung lain yang digunakan meliputi pemanas listrik, gelas ukur, pH meter,
stop watch dan termometer, thermostat, filter ukuran 0,3 mikron. Alat-alat untuk analisis diantaranya : cawan porselen, desikator, timbangan analitik, biuret, labu erlenmeyer, gelas piala, gelas pengaduk, thermostat, 1 unit HPLC dengan kolom Pico tag 3,9 x 150 nm, pipet tetes, micro pipet, pH meter, dan spektrofotometer.
3.3 Tahapan Penelitian
Penelitian ini dilaksanakan dalam enam tahapan. Tahapan tersebut dalam
rangka penentuan optimasi proses membran RO untuk recovery komponen
flavor dengan rejeksi tertinggi. Tahapan tersebut adalah prefiltrasi, penentuan
waktu tunak (steady state), perlakuan tekanan transmembran, suhu dan pH
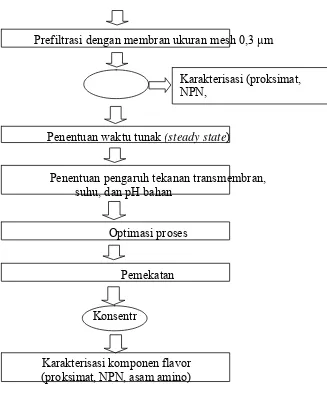
bahan terhadap nilai fluks dan rejeksi untuk seleksi variabel, optimasi proses, pemekatan, dan karakterisasi flavor yang dihasilkan (Gambar 4).
Limbah Karakterisasi (proksimat,
Prefiltrasi dengan membran ukuran mesh 0,3 μm
Penentuan waktu tunak (steady state)
Penentuan pengaruh tekanan transmembran, suhu, dan pH bahan
Optimasi proses
Pemekatan
Karakterisasi (proksimat, NPN,
Konsentr
[image:45.595.166.493.93.490.2]Karakterisasi komponen flavor (proksimat, NPN, asam amino)
Gambar 4 Diagram alir tahapan proses penelitian
Sebelum proses recovery, dilakukan pre-filtrasi dengan filter ukuran 0,3
mikron. Pada proses recovery sejumlah limbah cair dimasukkan ke dalam
wadah kemudian dipanaskan pada suhu tertentu. Untuk memanaskan dan mempertahankan bahan pada suhu tertentu, wadah dilengkapi dengan pemanas
listrik dan thermostat. Produk hasil proses membran (permeat dan retentat)
diresirkulasikan ke dalam wadah. Pada waktu tertentu dilakukan sampling terhadap permeat untuk pengukuran fluks dan nilai rejeksi. Permeat hasil sampling ditampung untuk diukur kandungan protein dengan menggunakan metode Bradford.
Nilai tunak fluks (steady state) yang diperoleh dari hasil pengukuran
variabel yaitu perlakuan faktor-faktor yang berpengaruh terhadap kinerja membran yaitu tekanan transmembran, suhu, dan pH. Selanjutnya dari variabel yang terpilih tersebut akan digunakan untuk proses optimasi RO.
Kondisi optimum dari kinerja RO selanjutnya digunakan untuk proses
pemekatan bahan. Proses pemekatan bahan dilakukan dengan cara memasukkan ±
0,8 l limbah cair ke dalam wadah bahan. Selama proses berlangsung fraksi
permeat yang berupa air tidak diresirkulasikan tetapi dibiarkan dalam wadahnya,
sehingga fraksi retentat sebagai konsentrat menjadi semakin pekat. Indikator
proses dievaluasi dengan melihat hubungan antara faktor konsentrasi dengan nilai
fluks. Faktor konsentrasi didefinisikan sebagai perbandingan antara volume
umpan di awal proses dengan volume retentatnya (Cheryan 1998). Proses akhir
adalah karakteristik hasil recovery flavor yang didapatkan.
Setiap proses membran selesai dilakukan, membran dicuci dengan cara meresirkulasikan larutan pembersih dengan NaOH 1% sehingga pH larutan menjadi 10,5 - 11,0. Fluks membran diuji kembali hingga mencapai fluks semula.
3.3.1 Penentuan waktu tunak (steady state) fluks (Uju 2005)
Waktu tunak fluks ditentukan dengan menghitung fluks permeat sejak kondisi variabel parameter proses terpasang. Jeda waktu pengukuran dan penghitungan fluks permeat dilakukan setiap satu menit sekali selama satu jam dan selanjutnya dilakukan setiap 5 menit. Fluks dianggap tunak jika 5-10 kali pengukuran memperoleh nilai yang sama.
Pengaruh tekanan transmembran dilihat dengan mencobakan beberapa nilai tekanan pada proses recovery pada kisaran 345 – 552 kPa. Setiap tekanan yang dicobakan diukur nilai fluks dan rejeksinya.
3.3.3 Pengaruh suhu
Pengaruh suhu dilihat dengan mencobakan beberapa nilai suhu pada proses recovery yaitu 30, 35, dan 40 oC. Setiap tekanan yang dicobakan diukur nilai fluks dan rejeksinya.
3.3.4 Pengaruh pH
Dicobakan beberapa nilai pH pada proses recovery yaitu 4; 6,5; dan 9.
Setiap pH yang dicobakan diukur nilai fluks dan rejeksinya.
3.4 Analisis dan Karakterisasi
Variabel parameter operasi proses yang diteliti meliputi pengaruh tekanan transmembran, suhu, dan nilai pH. Indikator kinerja membran dilihat dengan mengukur fluks permeat, sedangkan indikator kualitas produk (retentat) yang dihasilkan ditentukan dengan mengukur nilai rejeksi membran. Sampling dan pengukuran nilai rejeksi dilakukan pada keadaan kondisi fluks steady state.
Analisis bahan dilakukan pada raw material, pre-filtrasi, dan hasil akhir proses RO (produk utama/retentat). Analisis meliputi uji fisik dengan melihat warna dan bau, dan analisis kimia meliputi uji proksimat, non protein nitrogen (NPN), dan asam amino. Analisis komponen flavor (asam amino) menggunakan HPLC, sedangkan kandungan protein dengan metode Bradford.
Persentase bahan terlarut hasil recovery dari proses pengkonsentrasian dapat dihitung
berdasarkan rumus berikut ini (Sheu dan Wiley 1983):
% 100 bahan
x volume terlarut
%
konsentrat x volume
terlarut %
(%) x
Recovery =
Penghitungan non protein nitrogen (NPN) menggunakan metode pengukuran nitrogen bebas. Senyawa nitrogen yang terdapat dalam contoh diuraikan oleh NaOH, kemudian amoniak yang dibebaskan diikat dengan asam borat dan dititar dengan larutan asam standar. Sampel ditimbang sebanyak 5 g, dimasukkan ke dalam labu didih 250 ml, kemudian ditambahkan 100 ml air suling dan 10 ml NaOH 30% (natrium hidroksida dilarutkan ke dalam 350 ml air). Selanjutnya dihubungkan dengan alat penyuling. Penyulingan dilakukan selama lebih kurang 20 menit, sebagai penampung digunakan 10 ml larutan asam borat 2% yang telah dicampur indikator (10 ml hijau bromkresol 0,1% dicampur dengan 2 ml merah metil 0,1% dalam alkohol 95%). Setelah itu ujung pendingin dibilas dengan air suling, kemudian dilakukan titrasi dengan larutan HCl 0,1 N sampai warna larutan yang semula berwarna biru atau hijau berubah menjadi violet. Larutan blanko dibuat sama dengan langkah di atas, hanya saja tidak ditambah dengan sampel.
Perhitungan :
x 100%
a
0,014 x d x a) (b (%) bebas
Nitrogen = −
dimana:
a = bobot sampel (g)
b = volume HCl 0,1 N yang dipergunakan peniteran sampel (ml) c = volume HCl 0,1 N yang dipergunakan peniteran blanko (ml) d = normalitas HCl
3.4.2 Analisis kandungan protein (Bradford 1976)
Konsentrasi protein ditentukan menggunakan metode Bovine Serum
Albumin (BSA) sebagai standar. Persiapan pereaksi Bradford dilakukan dengan
melarutkan 25 mg comassie brilliant blue G-250 dalam 12,5 ml etanol 95%, lalu
ditambahkan dengan 25 ml asam fosfat 85% (w/v). Jika sudah larut dengan sempurna, maka ditambahkan akuades hingga mencapai volume 0,5 l dan disaring dengan kertas saring Whatman No 1 sesaat sebelum digunakan.
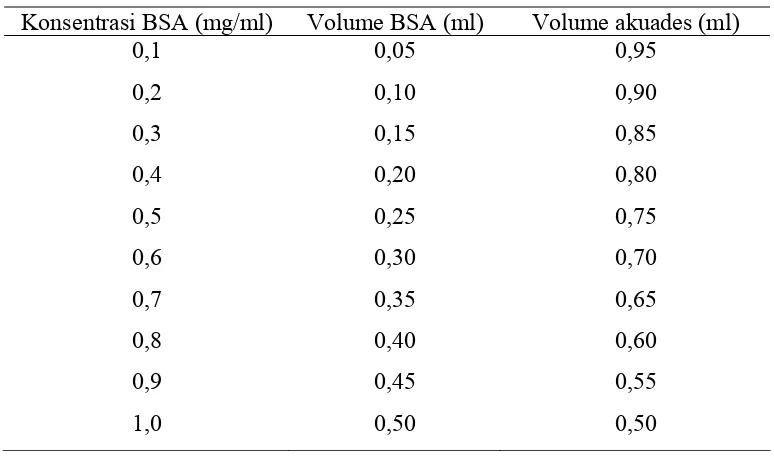
selama 5 menit dan diukur dengan spektrofotometer pada λ 595 nm. Larutan standar diberi perlakuan yang sama dengan larutan sampel dengan konsentrasi 0,1 – 1,0 mg/ml. Tabel komposisi volume larutan dalam pembuatan larutan standar konsentrasi 0,1 – 1,0 mg/ml dari larutan stok BSA konsentrasi 2 mg/ml disajikan pada Tabel 6.
Tabel 6 Pembuatan larutan standar BSA konsentrasi 0,1 – 1,0 mg/ml
Konsentrasi BSA (mg/ml) Volume BSA (ml) Volume akuades (ml)
0,1 0,05 0,95
0,2 0,10 0,90
0,3 0,15 0,85
0,4 0,20 0,80
0,5 0,25 0,75
0,6 0,30 0,70
0,7 0,35 0,65
0,8 0,40 0,60
0,9 0,45 0,55
1,0 0,50 0,50
3.4.3 Analisis asam amino (AOAC 1995)
Pengukuran asam amino dilakukan dengan menggunakan High
Performance Liquid Chromatography (HPLC). Tahapan meliputi hidrolisis, derivatisasi, dan injeksi. Tahap hidrolisis, sampel ditimbang sebanyak 0,25 – 0,50 gram kemudian dimasukkan ke dalam tabung 25 ml, setelah itu ditambahkan HCl
6N sebanyak 5 – 10 ml dan dipanaskan selama 24 jam pada suhu 100 oC
kemudian disaring.
Tahap derivatisasi, sampel diambil 30 ml dan ditambahkan larutan pengering berupa metanol, picolotiocianat, dan triethylamine, setelah itu dikeringkan atau divakumkan. Proses selanjutnya ditambahkan 30 ml larutan derivatisasi berupa metanol, picolotiocianat, dan triethylamine, lalu didiamkan selama 20 menit kemudian ditambahkan bufer 20 ml natrium asetat 1 M. Tahap akhir adalah diinjeksikan ke alat. Larutan standar yang digunakan adalah asam amino standar (asam amino murni).
Kondisi alat yang digunakan adalah sebagai berikut:
Kolom = Pico tag 3,9 x 150 nm
Kecepatan alir = 1,5 ml/menit
Batas tekanan = 3000 Psi
Program = gradien
Fase gerak = asetonitril 60%
buffer natrium asetat 1M
Detektor = UV
Panjang Gelombang = 254 nm
Perhitungan :
Fk BM sampel bobot standar i konsentras standar area luas contoh area luas (mg/g) amino
asam = x x x
Kadar
3.4.4 Analisis proksimat
(a) Kadar air (Apriyantono et al. 1989)
Cawan porselen kosong dipanaskan dalam oven pada suhu 105 oC selama
12 jam. Kemudian cawan tersebut didinginkan dalam desikator dan ditimbang beratnya (A gram). Selanjutnya cawan tersebut diisi sampel dan ditimbang (B
gram). Cawan berisi sampel dimasukkan dalam oven pada suhu 105 oC sampai
beratnya konstan (kurang lebih 16 jam), kemudian didinginkan dalam desikator dan setelah dingin ditimbang (C gram). Kadar air dapat dihitung dengan persamaan :
100% x A) (B C) B ( (%) air Kadar − − =
(b) Kadar abu (Apriyantono et al. 1989)
Analisis kadar abu dilakukan dengan cara : cawan porselen kosong
dipanaskan dalam oven tanur pengabuan selama 30 menit pada suhu 400 oC.
Kemudian didinginkan dalam desikator, seteleh dingin ditimbang beratnya (A gram). Dilanjutkan penimbangan sampel dan cawan bersama-sama (B gram), kemudian dimasukkan dalam tanur pengabuan sampai beratnya tetap (warna keabu-abuan). Pengabuan dilakukan dua tahap. Tahap pertama pada suhu 400
oC, dilanjutkan suhu 550 oC sampai bebas dari arang. Setelah itu sampel dan
x100% A) B ( A) C ( (%) abu Kadar − − =
(c) Kadar protein (Apriyantono et al. 1989)
Sampel ditimbang sebanyak 2 g dan dimasukkan dalam labu Kjeldahl 100
ml, dan ditambahkan 2 buah tablet Kjeldahl, kemudian ditambah 15 ml H2SO4
lalu didestruksi selama ± 30 menit sampai diperoleh cairan hijau jernih. Cairan didinginkan, kemudian ditambah akuades 5 ml dan dipindahkan ke tabung destilasi dengan hati-hati, lalu dibilas lagi dengan akuades 5-10 ml. Selanjutnya ke dalam tabung destilasi ditambahkan 10-12 ml NaOH (60 gram NaOH + 5 g Na2S2O3.5H2O dalam 100 ml akuades) sampai cairan berwarna coklat kehitaman.
Hasil destilasi ditampung dengan gelas erlenmeyer 125 ml yang berisi 10 ml
larutan H3BO3 dan 2-3 tetes indikator campuran metil merah dan metil biru.
Hasil destilasi ini kemudian dititrasi dengan larutan HCl 0,02 N sampai terjadi perubahan warna menjadi abu-abu. Larutan blanko juga dibuat tanpa menggunakan sampel.
Kadar protein dapat dihitung dengan rumus :
% 100 (mg) sampel berat 4,007 x1 HCl N x blanko) HCl ml sampel HCl (ml
N(%)= − x
Protein (%) = N (% ) x 6,25
(d) Kadar lemak (Apriyantono et al. 1989)
Labu lemak dikeringkan dalam oven, kemudian didinginkan dalam
desikator dan ditimbang (W1). Sampel ditimbang 5 g (W2) dimasukkan dalam
kertas saring kemudian ditutup dengan kapas. Kertas saring berisi sampel tersebut kemudian dimasukkan dalam alat ekstrak soxhlet lalu dipasang alat kondensor di atasnya dan labu lemak di bawahnya. Pelarut dietil eter dituangkan ke dalam labu lemak secukupnya. Refluks dilakukan minimal 5 jam sampai pelarut turun kembali ke labu lemak berwarna jernih. Destilasi pelarut yang ada dalam labu lemak ditampung pelarutnya. Selanjutnya labu lemak yang berisi hasil ekstrasi
tetap, kemudian didinginkan dalam desikator, labu lemak ditimbang kembali (W3). Berat lemak dihitung dengan rumus :
x100% (g)
W
(g) ) W (W (%) lemak Kadar
2 1 3− =
(e) Kadar karbohidrat
Karbohidrat dihitung by difference dengan persamaan :
Karbohidrat (%) = 100% - (% kadar abu + % kadar air + % kadar protein + % kadar lemak)
3.5 Rancangan Percobaan
Rancangan percobaan yang digunakan dalam tahap penelitian ini adalah two level factorial design (Box et al. 1979; Montgomery 2001). Tiga parameter atau variabel yang dipilih meliputi tekanan transmembran, suhu dan pH, sedangkan respon yang diukur adalah fluks (J) dan rejeksi (Robs). Sementara itu,
batasan taraf nilai variabel yang digunakan disajikan pada Tabel 7.
Tabel 7 Penentuan taraf nilai variabel yang digunakan
Nilai pengkodean dan taraf sebenarnya Parameter
-1 0 -1
TMP (x1) kPa 345 103,5 552
Suhu (x2) oC 30 35 40
pH (x3) 4 6,5 9
Model rancangan percobaan untuk mengetahui hubungan linier dari variabel tekanan transmembran dan laju alir bahan terhadap respon nilai fluks dan rejeksi diberikan pada persamaan di bawah ini :
Y = a
o+
∑
a
ix
i+
∑
a
ijx
ix
j i i<jKeterangan:
Y = respon dari masing-masing perlakuan
xi ; xj = variabel bebas
ao = intersep
ai = koefisien regresi orde pertama
3.6 Penentuan Optimasi Proses
Untuk menentukan optimasi proses digunakan model kuadratik pengaruh
faktor respon dengan metode respon permukaan (Response Surface Method) (Box
et al. 1979; Montgomery 2001) dengan rancangan CCD (Central Composite Design). Model rancangan tersebut adalah sebagai berikut :
i i ii j
i j i ij i
i i
o ax a xx a x
a +Σ +Σ +Σ 2
= Υ
<
Keterangan :
Y = respon dari masing-masing perlakuan
xi ; xj = variabel bebas variabel
ao = intersep
ai = koefisien regresi orde pertama
aij = koefisien interaksi untuk interaksi variabel i dan j
aii = koefisien kuadratik variabel
4 HASIL DAN PEMBAHASAN
4.1 Karakteristik Limbah Cair Pasteurisasi Rajungan
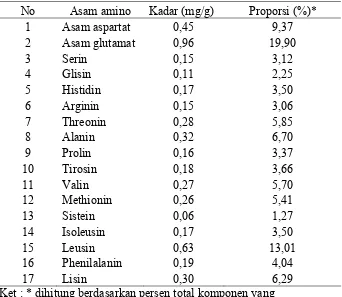
Karakteristik limbah cair pasteurisasi rajungan meliputi sifat fisik dan kimia. Sifat fisik meliputi warna dan bau, sedangkan sifat kimia meliputi nilai proksimat bahan baku, kadar NPN, dan kadar asam amino.
4.1.1 Sifat fisik, nilai proksimat, dan kadar NPN
Limbah cair hasil pasteurisasi rajungan mempunyai warna coklat keruh dengan bau segar khas rajungan. Warna coklat keruh limbah cair disebabkan oleh adanya bahan-bahan terlarut dan tersuspensi di dalamnya, baik bahan organik maupun anorganik. Bahan-bahan organik ini berasal dari serpihan daging, darah dan juga lendir pada proses pengolahan. Bahan organik meliputi protein sebesar 0,88%, lemak 0,21%, dan karbohidrat sebesar 0,08%. Kandungan protein merupakan bahan organik paling tingg