PENGARUH PEMBERIAN VITAMIN C TERHADAP JUMLAH
SPERMA DAN MORFOLOGI SPERMA MENCIT JANTAN
DEWASA (Mus musculus, L.) YANG DIPAPARKAN
MONOSODIUM GLUTAMATE (MSG)
T E S I S
Oleh
S U P A R N I
077008008/BM
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
MEDAN
2009
ΣΕ Κ Ο Λ
Α
Η
Π Α
Σ Χ
Α Σ Α Ρ ϑΑ
Ν
PENGARUH PEMBERIAN VITAMIN C TERHADAP JUMLAH
SPERMA DAN MORFOLOGI SPERMA MENCIT JANTAN
DEWASA (Mus musculus, L.) YANG DIPAPARKAN
MONOSODIUM GLUTAMATE (MSG)
T E S I S
Diajukan Sebagai Salah Satu Syarat untuk Memperoleh Gelar Magister Kesehatan dalam Program Studi Ilmu Biomedik
pada Sekolah Pascasarjana Universitas Sumatera Utara
Oleh
S U P A R N I
077008008/BM
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
Judul Tesis : PENGARUH PEMBERIAN VITAMIN C TERHADAP JUMLAH SPERMA DAN MORFOLOGI SPERMA
MENCIT JANTAN DEWASA (Mus musculus, L.)
YANG DIPAPARKAN MONOSODIUM
GLUTAMATE (MSG) Nama Mahasiswa : Suparni
Nomor Pokok : 077008008
Program Studi : Biomedik
Menyetujui Komisi Pembimbing
(Dr. Drs. Syafruddin Ilyas, M.Biomed) Ketua
(dr. Dedi Ardinata, M.Kes, AIFM) Anggota
Ketua Program Studi, Direktur,
(dr. Yahwardiah Siregar, PhD) (Prof. Dr. Ir. T. Chairun Nisa B, M.Sc)
Telah diuji pada
Tanggal: 29 Agustus 2009
PANITIA PENGUJI TESIS
Ketua : Dr. Drs. Syafruddin Ilyas, M.Biomed Anggota : 1. dr. Dedi Ardinata, M.Kes, AIFM 2. Prof. Em. dr. Yasmeini Yazir
ABSTRAK
Monosodium Glutamate (MSG) menyebabkan terjadinya penurunan jumlah sperma yang bentuknya normal dan peningkatan jumlah sperma yang bentuknya abnormal. MSG akan menimbulkan terjadinya stress oksidatif yang ditandai dengan terbentuknya radikal bebas. Vitamin C berfungsi sebagai antioksidan dengan cara menetralisir radikal bebas dan menghambat peroksidasi lipid. Pemberian vitamin C mencegah penurunan jumlah sperma dan menurunkan bentuk sperma yang abnormal. Tujuan dari penelitian ini adalah untuk mengetahui bagaimana pengaruh pemberian vitamin C terhadap jumlah sperma dan morfologi sperma mencit jantan dewasa (Mus musculus, L.) yang ditimbulkan oleh pemberian MSG.
Subjek penelitian adalah mencit jantan dewasa (Mus musculus, L.) strain DD Webster dewasa fertil berumur ± 3 βυλαν δενγαν βερατ βαδαν 25-35 gram, sebanyak 25 ekor yang di bagi dalam 5 kelompok perlakuan masing-masing terdiri dari 5 ekor mencit jantan dewasa. Kelompok pertama sebagai kontrol negatif yang diberi dengan NaCl 0,9 % 0,5 ml selama 30 hari, kelompok ke-dua kontrol positif diberi MSG 4 mg/g bb intraperitoneal (IP) dilarutkan dengan NaCl 0,9 % 0,5 ml selama 15 hari, 15 hari berikutnya diberi NaCl 0,9% 0,5 ml, kelompok ke-tiga diberi MSG 4 mg/g bb (IP) selama 30 hari, kelompok keempat diberi MSG 4 mg/g bb 15 hari pertama dan dilanjutkan dengan pemberian vitamin C 0,2 mg/g bb oral 15 hari berikutnya, kelompok ke-lima diberi MSG 4 mg/g bb (IP) 15 hari pertama dilanjutkan dengan pemberian MSG 4 mg/g bb ditambah vitamin C 0,2 mg/g bb 15 hari berikutnya. Penelitian ini telah mendapat persetujuan dari komite etik penelitian USU. Pemeriksaan jumlah sperma dilakukan dengan menggunakan kamar hitung Improved Neubauer dan pemeriksaan morfologi sperma dibuat sediaan hapusan yang diwarnai dengan Giemsa.
Diperoleh hasil bahwa pemberian MSG 4 mg/g bb dan vitamin C 0,2 mg/g bb terdapat perbedaan jumlah sperma dan terdapat perbedaan rata-rata persentase morfologi sperma normal pada tiap kelompok perlakuan tetapi tidak menunjukkan hasil yang bermakna (p>0,05), hal ini menunjukkan jumlah sperma dan morfologi sperma normal tidak dipengaruhi oleh pemberian MSG dan vitamin C secara tersendiri maupun bersamaan pada perlakuan.
Kata Kunci: MSG, Vitamin C, Sperma.
ABSTRACT
Monosodium glutamate (MSG) decreased normal sperm count and increased abnormal sperm count. MSG caused stress oxidative by formation of free radicals. Vitamin C as an antioxidant by neutralizing free radicals and prevent lipid peroxidation. Intake vitamin C prevents decreased normal sperm and increased abnormal sperm count.
The aim of this study is to investigate the effect of intake vitamin C to sperm count and sperm morphology of adult male mice (Mus musculus, L.) which is exposed MSG.
Subject of this study was 25 adult male mice (Mus Musculus, L) strain DD Webster fertile, age ±3 mοντησ ολδ, βοδψ ωειγητ 25-35 gram and divided 5 groups. The first group, as negative control which is given 0,5 ml of NaCl 0,9% intraperitoneal (IP) for 30 days. The second group, as a positive control which is given MSG 4 mg/g BW (IP) for 15 days, then the next 15 days, the mice is given 0,5 ml of NaCl 0,9%. The third group is given MSG 4 mg/g BW (IP) for 30 days. The fourth group is given MSG 4 mg/g BW for 15 days and 15 days later they are given orally o,2 mg/g BW of vitamin C. The fifth group is given MSG 4 mg/g BW (IP) for 15 days and 15 days later the mice is given MSG 4 mg/g BW (IP) and orally 0,2 mg/g BW of vitamin C. All the experimental procedures and animal maintenance confirmed to the strict guidelines of institutional animal ethics committee USU. The sperm count using Improved Neubauer counting chamber and the morphology of the sperm using Giemsa smear.
The result of injection MSG 4 mg/g BW and supplement vitamin C 0,2 mg/g BW is the difference of sperm count and mean of normal sperm morphology percentage in each groups but not significant (p>0,05), that means sperm count and normal sperm morphology is not affected by MSG and vitamin C, combined or separated, in each groups.
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada Allah swt, atas limpahan berkat dan
karunianya, sehingga penulis dapat menyelesaikan Tesis ini dengan judul “Πενγαρυη Pemberian Vitamin C terhadap Jumlah Sperma dan Morfologi Sperma Mencit Jantan
Dewasa (Mus musculus, L.) yang Dipaparkan Monosodium Glutamate (MSG)”
sebagai salah satu syarat dalam menyelesaikan jenjang pendidikan strata 2 pada
Program Studi Biomedik Sekolah Pascasarjana Universitas Sumatera Utara.
Proses penulisan tesis ini tidak terlepas dari bimbingan, bantuan, dukungan
dan do’α δαρι βερβαγαι πιηακ, παδα κεσεmπαταν ινι υχαπκαν τεριmα κασιη σαψα sampaikan kepada yang terhormat:
1. Prof. Chairuddin P. Lubis, DTM&H, Sp.A(K), Rektor Universitas Sumatera
Utara.
2. Prof. Dr. Ir. T. Chairun Nisa B, MSc, Direktur Sekolah Pascasarjana
Universitas Sumatera Utara.
3. dr. Yahwardiah Siregar, PhD, Ketua Program Studi Biomedik Sekolah
Pascasarjana Universitas Sumatera Utara.
4. Dr. Drs. Syafruddin Ilyas, M.Biomed, Ketua Komisi Pembimbing yang
senantiasa bersedia meluangkan waktu untuk membimbing, memberikan
masukan dan pemikiran dengan penuh kesabaran kepada penulis untuk
menyelesaikan tesis ini.
5. dr. Dedi Ardinata, S.Ked, M.Kes, Anggota Komisi Pembimbing yang telah
banyak memberikan bimbingan dan transfer ilmu, masukan serta dukungan
yang diberikan untuk penyelesaian tesis ini.
6. Prof. Em. dr. Yasmeini Yazir, Dosen Pembanding yang telah memberikan
masukkan mulai dari usulan penelitian hingga penyelesaian tesis ini.
7. Prof.dr. Gusbakti Rusip, MSc, PKK, Dosen Pembanding yang juga banyak
8. Seluruh Dosen Program Studi Biomedik Sekolah Pascasarjana Universitas
Sumatera Utara, yang telah memberikan pembelajaran dan selama penulis
mengikuti pendidikan.
9. Ir. Zuraidah Nasution, M.Kes, Direktur Politeknik Kesehatan Medan yang
telah memberi kesempatan kepada penulis untuk melanjutkan pendidikan
strata 2 di Program Studi Biomedik Pascasarjana Universitas Sumatera
Utara.
10.dr. Fachri Nasution, DAN, Ketua Jurusan Analis Kesehatan Politeknik
Kesehatan Medan yang telah memberi dukungan kepada penulis untuk
melanjutkan pendidikan strata 2 di Program Studi Biomedik Pascasarjana
Universitas Sumatera Utara.
Kepada Ibunda Almarhummah dan Ayahanda, ananda mengucapkan terima
kasih tak terhingga atas kasih sayang serta dukungannya. Kepada suamiku tercinta Ir.
Agustin, terima kasih atas pengertian, perhatian dan dukungan semangat, serta
anak-anakku tersayang (Gusni Rahmah dan Muhammad Yusuf) yang selama dua tahun ini
banyak waktu bersama yang terlewatkan, menjadi inspirasi untuk dapat
menyelesaikan pendidikan ini.
Kepada teman-teman Biomedik seangkatan 2007, terima kasih atas bantuan
morilnya, kalian adalah teman-temanku yang terbaik.
Medan, Agustus 2009
Penulis
RIWAYAT HIDUP
1. Nama : Suparni
2. Tempat/Tanggal lahir : Tanjung Morawa/25 Agustus 1966
3. Agama : Islam
4. Status : Menikah
5. Alamat : Dusun I Gg Rame Desa Telaga Sari Tanjung Morawa
6. Telepon/Hp : 081361615388
7. Pendidikan :
SD Negeri 101881 Tanjung Morawa Tahun 1974-1979
SMP Bersubsidi Tanjung Morawa Tahun 1980-1982
SMAK Depkes RI Medan Tahun 1982-1985
Sarjana (S1) Fakultas Biologi UMA Tahun 1994-1998
Sekolah Pasacasarjana, Program Biomedik, USU Tahun 2007-2009
8. Riwayat Pekerjaan :
Guru SMAK Depkes RI Medan Tahun 1986-2001
Dosen AAK Depkes RI Medan Tahun 1998-2001
DAFTAR ISI
Halaman
ABSTRAK ... i
ABSTRACT ... ii
KATA PENGANTAR ... iii
RIWAYAT HIDUP ... v
DAFTAR ISI ... vi
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN ... x
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 4
1.3 Landasan Teori ... 4
1.4 Tujuan Penelitian ... 6
1.5 Hipotesis ... 7
1.6 Manfaat Penelitian ... 7
BAB II TINJAUAN PUSTAKA ... 8
2.1 Monosodium Glutamate (MSG) ... 8
2.2 Vitamin C ... 14
2.3 Fisiologi Reproduksi Mencit Jantan ... 17
BAB III METODE PENELITIAN ... 22
3.1 Tempat dan Waktu ... 22
3.2 Variabel Penelitian ... 22
3.3 Definisi Operasional ... 22
3.4 Bahan dan Alat Penelitian ... 23
3.6 Pelaksanaan Penelitian ... 25
3.7 Analisa Data dan Pengujian Hipotesis .……….... 29
3.8 Jadwal Penelitian ………... 30
BAB IV HASIL DAN PEMBAHASAN …... 31
4.1 Hasil Penelitian ... 31
4.2 Pembahasan ... 36
BAB V KESIMPULAN DAN SARAN ... 39
5.1 Kesimpulan ... 39
5.2 Saran ... 39
DAFTAR PUSTAKA ... 40
DAFTAR TABEL
Nomor Judul Halaman
3.1. Jadwal Penelitian... 30
4.1. Pengamatan Berat Badan Awal dan Akhir Mencit Jantan Dewasa. 31
4.2. Jumlah Sperma Di Dalam Suspensi Cauda Epididimis Mencit
Jantan Dewasa ... 33
4.3. Morfologi Sperma Normal di dalam Suspensi Cauda Epididimis
DAFTAR GAMBAR
Nomor Judul Halaman
1.1. Landasan Teori... 6
3.1. Kamar Hitung Improved Neubauer ... 27
3.2. Morfologi Sperma Vas Deferen Mencit (Washington et al., 1983) Gambar A adalah Sperma Normal, dengan Kepala Seperti Kait Pancing, Gambar B, C dan D adalah Sperma Abnormal (B = Sperma dengan Kepala Seperti Pisang, C = Sperma Tidak Beraturan, dan D = Sperma Terlalu Bengkok) ... 29
4.1. Grafik Berat Badan Awal Dan Berat Badan Akhir... 32
4.2. Grafik Jumlah Sperma ... 33
4.3. Grafik Morfologi Sperma Normal... 35
DAFTAR LAMPIRAN
Nomor Judul Halaman
1. Surat Ethical Clearence ... 44
2. Surat Keterangan tentang Hewan Mencit (Mus musculus L.) dari
LPPT- UGM ... 45
3. Hasil Uji Statistik Berat Badan Awal dan Berat Badan Akhir
Mencit Jantan Dewasa ... 46
4. Hasil Uji Statistik Jumlah Sperma Mencit Jantan Dewasa ... 52
5. Hasil Uji Statistik Morfologi Sperma Normal Mencit Jantan
Dewasa ... 55
BAB I
PENDAHULUAN
1.1. Latar Belakang
Monosodium glutamate (MSG) sudah lama digunakan di seluruh dunia
sebagai penambah rasa makanan dengan L-Glutamic acid sebagai komponen asam
amino (Geha et al., 2000), disebabkan penambahan MSG akan membuat rasa
makanan menjadi lebih lezat (Loliger, 2000). Adapun rata-rata asupan MSG per hari
pada masyarakat di negara industri sekitar 0,3-1,0 g, tetapi adakalanya bisa menjadi
lebih tinggi tergantung pada jenis makanan dan pilihan rasa seseorang (Geha et al.,
2000). Asupan MSG terbanyak dijumpai pada masyarakat Korea yang mencapai 1,6
g/hari (Loliger, 2000), sedangkan di Indonesia sekitar 0,6 g per hari. Di Amerika
Serikat, Food and Drugs Administration (FDA, 1995) mengkategorikan MSG sebagai
bahan yang aman untuk dikonsumsi dan Prawirohardjono et al (2000) melaporkan
tidak ada perbedaan gejala yang bermakna antara kelompok orang sehat yang
mengkonsumsi kapsul MSG 1,5 g per hari selama tiga hari, kelompok orang sehat
yang mengkonsumsi kapsul MSG 3 g per hari selama tiga hari dan kelompok plasebo.
Tetapi, ada laporan yang menyatakan asupan MSG dalam jumlah besar menimbulkan
beberapa gejala pada orang yang sensitif seperti kebas pada belakang leher yang
berangsur-angsur menjalar ke lengan dan punggung, badan lemah dan jantung
berdebar, gejala-gejala ini dikenal sebagai Chinese restaurant syndrome (Geha et al.,
Olney (1969) mendapati penyuntikan MSG secara subkutan pada mencit baru
lahir menimbulkan terjadinya nekrosis akut neuron pada beberapa bagian otak yang
sedang berkembang termasuk hipotalamus, yang ketika dewasa mencit tersebut
mengalami kekerdilan tulang rangka, obesitas dan sterilitas pada mencit betina.
Penelitian terhadap mencit jantan dewasa yang disuntikkan MSG secara
subkutan selama 6 hari dengan dosis 4 mg/g berat badan dan 8 mg/g berat badan
menyebabkan peningkatan kadar glukosa eritrosit, peningkatan kadar peroksidasi
lipid, kadar total glutation dan protein yang terikat glutation serta peningkatan
aktivitas enzim glutathione reductase (GR), glutathione-S-transferase (GST) dan
glutathione peroxidase (GPX). Hal ini menggambarkan bahwa dengan pemberian
MSG 4 mg/g berat badan mengakibatkan terjadinya stress oksidatif yang diantisipasi
tubuh dengan meningkatkan kadar glutation dengan cara meningkatkan aktivitas
enzim metaboliknya (Ahluwalia et al., 1996). Pemberian MSG 4 g/kg berat badan
secara intraperitoneal pada tikus Wistar jantan dewasa selama 15 hari (paparan jangka
pendek) dan 30 hari (paparan jangka panjang) memperlihatkan terjadinya penurunan
berat testis, penurunan jumlah sperma yang bentuknya normal dan peningkatan
jumlah sperma yang bentuknya abnormal, penurunan kadar asam askorbat di dalam
testis dan peningkatan kadar peroksidasi lipid di dalam testis. Pada kelompok paparan
jangka pendek memperlihatkan penurunan jumlah sperma yang bentuknya normal
lebih rendah dan peningkatan jumlah sperma dengan ekor abnormal lebih besar serta
kerusakan oksidatif lebih besar bila dibandingkan dengan kelompok paparan jangka
Pemberian vitamin C secara oral dengan dosis 200-1000 mg/hari pada
laki-laki infertil meningkatkan jumlah sperma secara in vivo. Vitamin C merupakan
antioksidan mampu menetralisir hidroksil, superoksid, dan radikal peroksidasi
hidrogen dan mencegah aglutinasi sperma (Agarwal et al., 2005).
Penelitian yang dilakukan pada testis tikus yang dipaparkan Cadmium (Cd) 10
mg/g berat badanmemperlihatkan bahwa pemberian vitamin C 10 mg/kg berat badan
secara intraperitoneal mampu mengurangi kadar MDA dalam testis dan peningkatan
jumlah sperma disertai penurunan persentase sperma yang berbentuk abnormal, pada
pemberian vitamin E 100 mg/kg berat badan secara intraperitoneal memperlihatkan
efek yang mirip pada pemberian vitamin C, akan tetapi efek dari vitamin E lebih
rendah (Acharya et al., 2006).
Penelitian yang dilakukan pada kelinci usia 5 bulan yang diberi suplemen
vitamin C 1,5 g/L dan vitamin E 1 g/L pada minumannya dan kombinasi vitamin C
ditambah vitamin E (1,5 g/L+1 g/L) selama 12 minggu memperlihatkan penurunan
kadar thiobarbituric acid-reactive di dalam cairan semen serta peningkatan libido
(waktu reaksi), volume ejakulasi, konsentrasi sperma, jumlah sperma yang
dikeluarkan, indeks motilitas sperma, total sperma yang bergerak, volume sperma,
konsentrasi ion hidrogen (pH), dan konsentrasi fruktosa semen serta penurunan
jumlah sperma bentuk abnormal dan sperma yang mati dan peningkatan kadar
glutathione S-transferase (GST) di dalam cairan semen (Yousef et al., 2003).
Pemberian vitamin C 0,2 mg/g berat badan secara oral selama 36 hari pada
radikal bebas yang ditimbulkan oleh senyawa Plumbum asetat 0,1% yang ditandai
oleh berkurangnya kadar malondialdehyde di dalam sekresi epididimis (Fauzi, 2008).
Penelitian terhadap pasien infertil dengan keadaan oligosperma, motilitas
sperma rendah dan jumlah sperma bentuk normal yang rendah, setelah diberikan
suplemen vitamin C 1000 mg per hari selama 2 bulan, memperlihatkan peningkatan
jumlah sperma, motilitas sperma dan jumlah sperma yang morfologinya normal
(Akmal et al., 2006).
Berdasarkan hasil penelitian yang diperoleh oleh Nayanatara (2008) akan
pengaruh pemberian MSG dapat menimbulkan terjadinya stress oksidatif pada testis
tikus Wistar dan penelitian-penelitian yang lain akan efek pemberian vitamin C
sebagai antioksidan terhadap testis. Maka penelitian ini bertujuan untuk mengetahui
pengaruh pemberian vitamin C terhadap jumlah sperma dan morfologi sperma pada
mencit jantan dewasa (Mus musculus, L) yang telah dipaparkan dengan MSG.
1.2. Perumusan Masalah
Bagaimana pengaruh pemberian vitamin C terhadap jumlah sperma dan
morfologi sperma mencit jantan dewasa (Mus musculus, L.) akibat yang ditimbulkan
oleh pemberian Monosodium glutamate (MSG).
1.3. Landasan Teori
Pemberian MSG dengan dosis 4 mg/g berat badan akan menimbulkan
bebas yang akan dilawan oleh tubuh mencit cara meningkatkan aktivitas enzim
glutathione reductase (GR), glutathione-S-transferase (GST), glutathione peroxidase
(GPX) yang berfungsi untuk meningkatkan produksi glutathion yang merupakan anti
oksidan. Radikal bebas yang terbentuk tersebut juga menimbulkan terjadinya proses
peroksidasi lipid yang ditandai dengan peningkatan kadar malondialdehyde (MDA).
Hal ini kemudian akan menyebabkan penurunan kadar asam askorbat di dalam testis
yang berakibat terhadap penurunan jumlah sperma. Oleh karena vitamin C dapat
bersifat sebagai antioksidan dengan cara menetralisir radikal bebas dan menghambat
peroksidasi lipid, maka diharapkan dengan pemberian vitamin C dapat menghambat
terjadinya peroksidasi lipid, mencegah penurunan kadar asam askorbat dalam testis
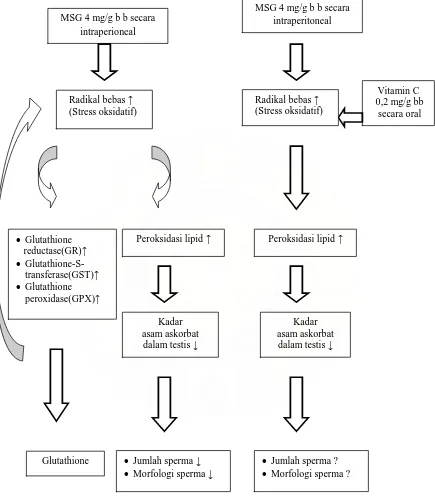
Gambar 1.1. Landasan Teori
MSG 4 mg/g b b secara intraperioneal
Vitamin C 0,2 mg/g bb
secara oral
! Jumlah sperma ↓ ! Morfologi sperma ↓ Radikal bebas ↑
(Stress oksidatif)
Kadar asam askorbat
dalam testis ↓ ! Glutathione
reductase(GR)↑ !
Glutathione-S-transferase(GST)↑ ! Glutathione
peroxidase(GPX)↑
Peroksidasi lipid ↑
Glutathione
MSG 4 mg/g b b secara intraperitoneal
Radikal bebas ↑ (Stress oksidatif)
Peroksidasi lipid ↑
Kadar asam askorbat dalam testis ↓
1.4. Tujuan Penelitian
1.4.1. Tujuan Umum
Untuk mengetahui bagaimana pengaruh pemberian vitamin C terhadap jumlah
sperma dan morfologi sperma mencit jantan dewasa (Mus musculus, L.) akibat yang
ditimbulkan oleh pemberian Monosodium glutamate (MSG).
1.4.2. Tujuan khusus
a. Untuk mengetahui pengaruh pemberian vitamin C terhadap jumlah sperma
mencit jantan dewasa yang dipaparkan MSG.
b. Untuk mengetahui pengaruh pemberian vitamin C terhadap morfologi
sperma mencit jantan dewasa yang dipaparkan MSG.
1.5. Hipotesis
Ho : a. Tidak ada pengaruh pemberian vitamin C terhadap peningkatan jumlah
sperma mencit jantan dewasa yang dipaparkan MSG.
b. Tidak ada pengaruh pemberian vitamin C terhadap peningkatan
morfologi normal sperma mencit jantan dewasa yang dipaparkan MSG.
Ha : a. Ada pengaruh pemberian Vitamin C terhadap peningkatan jumlah
sperma mencit jantan dewasa yang dipaparkan MSG.
b. Ada pengaruh pemberian Vitamin C terhadap peningkatan morfologi
1.6. Manfaat Penelitian
1. Dijadikan bahan pertimbangan kepada masyarakat dan pemerintah untuk
memperhatikan penggunaan MSG dalam kehidupan sehari-hari.
2. Bisa dijadikan referensi untuk penelitian selanjutnya akan dampak konsumsi
BAB II
TINJAUAN PUSTAKA
2.1. Monosodium Glutamate (MSG)
2.1.1. Sejarah Penemuan MSG
MSG ditemukan pertama kali oleh Ikeda pada tahun 1909 dari mengisolasi
garam metalik asam glutamat dari tumbuhan laut (genus Laminaria) atau disebut
‘κονβυ’ δι ϑεπανγ (Ηαλπερν, 2002), mεmιλικι χιτα ρασα ψανγ κηασ δισεβυτ υmαmι συατυ
elemen rasa yang dijumpai pada makanan alamiah seperti kaldu. Karakteristik umami
berbeda dengan empat rasa yang lain pahit, manis, asin dan asam, berupa sedap, lezat
atau enak (Loliger, 2000), rasa umami ini bertahan lama dan di dalamnya terdapat
komponen L-glutamate (suatu asam amino non esensial) dan 5’-ribonucleotide
(Yamaguchi dan Ninomiya, 2000). MSG banyak digunakan pada masakan Cina dan
Asia Tenggara yang dikenal dengan nama Ajinomoto, Sasa, Vetsin, Miwon atau
Weichaun (Geha et al., 2000).
2.1.2. Sifat Kimia dan Metabolisme MSG
MSG bersifat sangat larut dalam air (Geha et al., 2000), glutamat yang
terdapat dalam MSG merupakan suatu asam amino yang banyak dijumpai pada
makanan, kandungan glutamat 20% dari total asam amino pada beberapa makanan
baik bebas maupun terikat dengan peptida ataupun protein (Garattini, 2000).
Sementara glutamat yang terdapat di dalam MSG dan yang berasal dari hidrolisa
bebas akan meningkatkan kadar glutamat dalam plasma darah (Gold, 1995).
Selanjutnya glutamat di dalam mukosa usus halus akan diubah menjadi alanin dan
di dalam hati akan diubah menjadi glukosa dan laktat. Adapun kadar puncak glutamat
yang dicapai hewan dewasa setelah konsumsi oral 1 g/kg berat badan, kadar terendah
dijumpai pada kelinci dan meningkat secara progesif pada monyet, anjing, mencit,
tikus dan marmut. Adapun faktor-faktor yang mempengaruhi kadar puncak asam
glutamat plasma adalah rute pemberian (oral<subkutan<intraperitoneal), konsentrasi
MSG dalam larutan (2%, 10%), dan usia (hewan baru lahir memetabolisme asam
glutamat lebih rendah dari pada dewasa) (Garattini, 2000).
Berikut rumus kimia MSG (Loliger, 2000):
Diperkirakan seorang dengan berat badan 70 kg setiap harinya dapat
memperoleh asupan asam glutamat sekitar 28 g yang berasal dari makanan dan hasil
pemecahan protein dalam usus. Pertukaran asam glutamat setiap harinya dalam tubuh
sekitar 48 g. Tapi jumlahnya dalam darah sedikit sekitar 20 mg karena kecepatannya
mengalami ekstraksi dan penggunaan oleh beberapa jaringan termasuk otot dan hati
(Garattini, 2000).
Glutamat merupakan suatu neurotransmitter yang penting untuk komunikasi
antar neuron, jika berlebihan akan dipompakan kembali ke dalam sel glial sekitar
Glutamat akan membuka saluran kalsium neuron sehingga kalsium masuk ke dalam
sel. Reaksi kimia yang berlangsung dalam sel secepatnya melepaskan bahan-bahan
kimiawi yang merangsang neuron yang berdekatan. Asam arakidonat merupakan
salah satu hasil reaksi kimia yang akan bereaksi dengan enzim dan menghasilkan
radikal bebas seperti radikal hidroksil (Gold, 1995).
2.1.3. Efek Biologi MSG
Normalnya MSG yang berlebihan tidak dapat melewati sawar darah otak,
tetapi terdapat beberapa bagian di dalam otak yang tidak dilindungi sawar darah otak
seperti hipotalamus, organ circumventricular, batang otak, kelenjar hipofise dan
testosterone (Gold, 1995). Sehingga pemberian MSG secara suntikan subkutan pada
mencit baru lahir dapat menimbulkan terjadinya nekrosis neuron akut pada otak
termasuk hipotalamus yang ketika dewasa akan mengalami hambatan perkembangan
tulang rangka, obesitas dan sterilitas pada betina (Olney, 1969). Terdapat adanya
laporan akan timbulnya gejala yang tidak menyenangkan pada manusia setelah
mengkonsumsi MSG seperti kebas pada belakang leher yang berangsur-angsur
menjalar kedua lengan dan punggung, perasaan lemah dan jantung berdebar-debar
(Stegink et al., 1981), sakit kepala, rasa terbakar, tekanan pada wajah dan nyeri dada
(Schaumburg et al., 1969). Kumpulan gejala tersebut dikenal dengan istilah Chinese
Restaurant Syndrome yang umumnya timbul setelah mengkonsumsi makanan Cina
yang banyak mengandung MSG (Kenney, 1986).
Penelitian terhadap tikus yang pada makanan standarnya ditambah MSG 100
berupa peningkatan kadar glukosa darah, triasigliserol, insulin dan leptin. Keadaan
tersebut disebabkan terjadinya stress oksidatif berupa peningkatan kadar
hiperperoksidasi lipid dan penurunan bahan-bahan antioksidan, tetapi hal tersebut
dapat dicegah dengan penambahan serat pada makanan (Diniz et al., 2005). Begitu
juga pemberian MSG 4 mg/g berat badan secara subkutan selama 10 hari pertama
kelahiran kemudian dilakukan pemeriksaan pada hari ke-25 memperlihatkan
peroksidasi lipid meningkat secara bermakna (Babu et al., 1994). Keadaan stress
oksidatif juga dijumpai setelah pemberian MSG 4 mg/g berat badan secara
intraperitoneal memperlihatkan peningkatan pembentukan MDA di hati, ginjal dan
otak tikus. Pemberian makanan yang mengandung vitamin C, E dan quercetin secara
bersamaan mengurangi kadar MDA yang muncul akibat pemberian MSG tersebut
(Farombi dan Onyema, 2006).
Penelitian terhadap tikus Sprague-Dawley baru lahir yang mengalami lesi
nukleus arkuatus setelah penyuntikan MSG 4 g/kg berat badan secara subkutan pada
hari ke 1, 3, 5, 7 dan 9, setelah 10 minggu memperlihatkan adanya plak aterosklerotik
pada permukaan lumen dinding aorta, degenerasi endotelium, inti endotelium
mengalami edema, adanya vesikel dengan berbagai ukuran pada jaringan
subendotelium serta sel otot polos mengalami migrasi dari tunika media ke tunika
intima melalui interna elastika yang robek. Juga disertai peningkatan kadar kolesterol
total, low density lipoprotein (LDL), kadar nitic oxide berkurang sedangkan kadar
2.1.4. Efek MSG terhadap Fungsi Reproduksi
Federation of American Societies for Experimental Biology (FASEB) juga
melaporkan adanya dua kelompok orang yang cenderung mengalami kompleks gejala
MSG, kelompok pertama orang yang tidak toleran terhadap konsumsi MSG dalam
jumlah besar dan kelompok kedua orang dengan penyakit asma tidak terkontrol,
orang-orang ini cenderung mengalami kompleks gejala MSG, perburukan gejala
asma yang bersifat sementara setelah mengkonsumsi MSG dengan dosis antara 0,5 g
sampai 2,5 g (FDA, 1995).
Penelitian terhadap pasien infertil dengan keadaan oligosperma, motilitas
sperma rendah dan jumlah sperma bentuk normal yang rendah, setelah diberikan
suplemen vitamin C 1000 mg per hari selama 2 bulan, memperlihatkan peningkatan
jumlah sperma, motilitas sperma dan jumlah sperma yang morfologinya normal
(Akmal et al., 2006).
Pada mencit baru lahir (usia 2 sampai 11 hari) yang disuntikkan MSG 4 mg/g
berat badan secara subkutan menimbulkan terjadinya disfungsi sistem reproduksi
jantan dan betina yang manifestasinya akan muncul pada usia dewasa berupa pada
mencit betina menimbulkan kehamilan lebih sedikit dan ovarium lebih kecil dan pada
mencit jantan menimbulkan penurunan berat testis (Pizzi et al., 1977, Miskowiak et
al., 1993).
Pemberian MSG 4 mg/g berat badan secara intraperitoneal pada tikus yang
baru lahir selama 2 hari sampai usia 10 hari dan diperiksa pada usia pra pubertas dan
dan peningkatan kadar kortikosteron, penurunan berat testis, jumlah sel sertoli dan sel
leydig per testis, serta penurunan kadar Luteinizing Hormone (LH), Follicle
Stimulating Hormone (FSH), Thyroid (T), dan Free T4 (FT4). Sementara pada saat
dewasa memperlihatkan hiperleptinemia yang lebih tinggi dan penurunan kadar FSH
dan LH lebih rendah tetapi kadar T dan FT4 normal, dan tidak tampak perubahan
struktur testis (Miskowiak et al., 1993).
Penelitian selanjutnya memperlihatkan bahwa salah satu mekanisme yang
mungkin berperan dalam timbulnya efek toksik akibat pemberian MSG pada sistem
reproduksi jantan mungkin diperantarai melalui efeknya dalam menurunkan kadar
asam askorbat. Penelitian tersebut dilakukan terhadap tikus Wistar jantan dewasa
yang disuntikkan MSG dengan dosis 4 g/kg berat secara intraperitoneal badan selama
15 hari (kelompok jangka pendek) dan selama 30 hari (kelompok jangka panjang),
memperlihatkan berkurangnya berat testis, jumlah sperma, kadar asam askorbat
dalam testis dan meningkatnya jumlah sperma yang bentuknya abnormal. Pada
kelompok jangka pendek memperlihatkan penurunan jumlah sperma bentuknya
normal dan peningkatan jumlah sperma dengan ekor abnormal secara bermakna
ketika dibandingkan dengan kelompok jangka panjang. Kadar asam askorbat dalam
testis menurun secara bermakna pada kelompok jangka pendek ketika dibandingkan
dengan kelompok jangka panjang (Nayanatara et al., 2008). Penelitian lanjutan yang
dilakukan Vinodini et al (2008) memperlihatkan bahwa MSG dengan dosis 4 g/kg
berat badan secara intra peritoneal selain menimbulkan terjadinya penurunan berat
kadar peroksidasi lipid dalam testis dan pada kelompok jangka pendek
memperlihatkan kerusakan oksidatif yang lebih besar bila dibandingkan dengan
kelompok jangka panjang.
2.2. Vitamin C
2.2.1. Sejarah Penemuan Vitamin C
Asam askorbat alami banyak terdapat pada buah-buahan seperti jeruk, jeruk
lemon, semangka, strawberi, mangga dan nenas serta sayur-sayuran berwarna hijau
seperti brokoli dan kembang kol (Padayatty et al., 2003). Hewan juga dapat
memproduksi asam askorbat, dari glukosa-D atau galaktosa-D seperti pada
tumbuh-tumbuhan (Naidu, 2003). Akan tetapi manusia dan golongan primata lainnya, babi
dan kelelawar pemakan buah tidak dapat mensintesa asam askorbat karena tidak
memiliki enzim gluconolactone oxidase (Luck et al., 1995). Baik asam askorbat yang
alami maupun sintetis memiliki rumus kimia yang identik dan tidak terdapat
perbedaan aktivitas biologi maupun bioavailabilitasnya (Naidu, 2003).
2.2.2. Sifat Kimia dan Metabolisma Vitamin C
Vitamin C adalah asam xyloascorbat-L (asam askorbat, AA), dengan hasil
oksidasi pertamanya asam dehidroaskorbat (dehydro AA) yang juga mempunyai
aktivitas vitamin C (Hughes, 1973), bersifat larut dalam air dan labil serta berperan
penting dalam biosintesa kolagen, karnitin dan berbagai neurotransmitter (Naidu,
2003). Asam askorbat adalah merupakan 6 karbon lakton yang disintesa dari glukosa
Asam askorbat merupakan donor elektron dan reducing agent karena dapat
mendonorkan dua elektron dari dua ikatan antara karbon kedua dan ketiga dari 6
molekul karbon, hal tersebut menyebabkan dia berfungsi sebagai antioksidan karena
mampu mencegah zat komposisi yang lain teroksidasi. Setelah vitamin C
mendonorkan elektronnya, dia akan menghilang dan digantikan oleh radikal bebas
semidehydroaskorbic acid atau radikal ascorbyl, bila dibandingkan dengan radikal
bebas yang lain, radikal ascorbyl ini relatif stabil dan tidak reaktif (Padayatty et al.,
2003). Bila radikal ascorbyl dan dehydroascorbic acid sudah dibentuk maka dia akan
dapat direduksi kembali menjadi asam askorbat sedikitnya dengan tiga jalur enzim
yang terpisah dengan cara mereduksi komponen yang terdapat di sistem biologi
seperti glutation, akan tetapi pada manusia hanya sebagian yang direduksi kembali
menjadi asam askorbat. Dehydroascorbic acid yang telah terbentuk kemudian
dimetabolisme dengan cara hidrolisis (Padayatty et al., 2003).
2.2.3. Efek Kimia Vitamin C
Asam askorbat berfungsi sebagai anti oksidan, anti aterogenik,
imunomodulator dan mencegah flu (Naidu, 2003). Untuk dapat berfungsi baik
tinggi di dalam tubuh (Gupta et al., 2007).
Pemberian suplemen vitamin C, vitamin E dan quercetin pada tikus yang
diberi MSG dengan dosis 4 mg/g berat badan dapat menurunkan kadar MDA yang
muncul akibat MSG. Vitamin E menurunkan kadar lipid peroksidasi di hati diikuti
oleh vitamin C dan kemudian quercetin, sementara vitamin C dan quercetin
menunjukkan kemampuan lebih besar dalam melindungi otak dari kerusakan
dibandingkan dengan vitamin E (Farombi dan Onyema, 2006).
2.2.4. Efek Vitamin C terhadap Fungsi Reproduksi
Asam askorbat memberikan efek baik kepada integitas dari struktur tubular
maupun terhadap fungsi sperma. Defisiensi asam askorbat telah lama dihubungkan
dengan jumlah sperma yang rendah, peningkatan jumlah sperma yang abnormal,
mengurangi motilitas dan aglutinasi. Pada beberapa penelitian telah dibuktikan bahwa
asupan asam askorbat dapat memperbaiki kualitas sperma. Efek yang menguntungkan
dari asam askorbat ini mungkin adalah hasil dari pemecahan radikal bebas yang
sering timbul akibat polusi lingkungan dan metabolisme selular yang dapat
menyebabkan kerusakan oksidatif dari DNA (Agarwal et al., 2005).
Stres oksidatif dapat dibatasi dengan menggunakan antioksidan berupa
suplemen vitamin E dan C. Vitamin C dapat menetralisir radikal hidroksil,
superoksid, dan hidrogen peroksida dan mencegah aglutinasi sperma. Vitamin C
sedikit jumlahnya pada cairan semen laki-laki infertil. Vitamin C dapat meningkatkan
jumlah sperma in vivo pada laki-laki infertil dengan dosis oral sekitar 200-1000
Begitu juga, kelinci usia 5 bulan yang diberi suplemen vitamin C 1,5 g/L dan
vitamin E 1 g/L pada minumannya dan kombinasi vitamin C + vitamin E (1,5 g/L+1
g/L) selama 12 minggu memperlihatkan penurunan kadar thiobarbituric acid-reactive
di dalam cairan semen serta peningkatan libido (waktu reaksi), volume ejakulasi,
konsentrasi sperma, jumlah sperma yang dikeluarkan, indeks motilitas sperma, total
sperma yang bergerak, volume sperma, konsentrasi ion hidrogen (pH), dan
konsentrasi fruktosa semen serta penurunan jumlah sperma bentuk abnormal dan
sperma yang mati dan peningkatan kadar glutathione S-transferase (GST) di dalam
cairan semen. Hal ini menyimpulkan bahwa pemberian suplemen vitamin C, vitamin
E dan kombinasi keduanya menurunkan produksi radikal bebas dan dapat
memperbaiki kualitas cairan semen tapi perbaikan lebih besar kelihatan berasal dari
vitamin E (Yousef et al., 2003).
2.3. Fisiologi Reproduksi Mencit Jantan
Sistem reproduksi mencit jantan terdiri atas testis dan kantong skrotum,
epididimis dan vas deferens, sisa sistem ekskretori pada masa embrio yang berfungsi
untuk transport sperma, kelenjar asesoris, uretra dan penis. Selain uretra dan penis,
semua struktur ini berpasangan (Rugh, 1967).
2.3.1. Testis
Setiap testis ditutupi dengan jaringan ikat fibrosa, tunika albuginea, bagian
tipisnya atau septa akan memasuki organ untuk membelah menjadi lobus yang
testis dan bagian arteri testicular yang masuk disebut sebagai hilus. Arteri memberi
nutrisi setiap bagian testis, dan kemudian akan kontak dengan vena testiskular yang
meninggalkan hilus (Rugh, 1967).
Epitel tubulus seminiferus berada tepat di bawah membran basalis yang
dikelilingi oleh jaringan ikat fibrosa yang tipis. Antara tubulus adalah stroma
interstisial, terdiri atas gumpalan sel leydig ataupun sel sertoli dan kaya akan darah
dan cairan limfe. Sel interstisial testis mempunyai inti bulat yang besar dan
mengandung granul yang kasar. Sitoplasmanya bersifat eosinofilik. Diyakini bahwa
jaringan interstisial menguraikan hormon jantan testosterone. Epitel seminiferus tidak
mengandung sel spermatogenik secara eksklusif, tetapi mempunyai nutrisi yang
menjaga sel sertoli, yang tidak dijumpai di tubuh lain. Sel sertoli bersentuhan dengan
dasarnya ke membran basalis dan menuju lumen tubulus seminiferus. Di dalam inti
sel sertoli terdapat nukleolus yang banyak, satu bagian terdiri atas badan yang bersifat
asidofilik di sentral dan sisanya badan yang bersifat basidofilik di perifer. Sel sertoli
diperkirakan mempunyai banyak bentuk tergantung aktivitasnya. Pada masa istirahat
berhubungan dekat dengan membran basalis di dekatnya dan inti ovalnya paralel
dengan membran. Sel sertoli sebagai sel penyokong untuk metamorfosis spermatid
menjadi spermatozoa dan retensi sementara dari spermatozoa matang, panjang,
piramid dan intinya berada tegak lurus dengan membran basalis. Sitoplasma dekat
lumen secara umum mengandung banyak kepala spermatozoa yang matang
2.3.2. Spermatogenesis
Sel germinal primordial mencit jantan muncul sekitar 8 hari kehamilan,
dengan jumlah hanya 100, yang merupakan awal dari jutaan spermatozoa yang akan
diproduksi dan masih berada di daerah ekstra gonad. Karena sel germinal kaya akan
alkalin fosfatase untuk mensuplai energi pergerakannya melalui jaringan embrio,
maka sel germinal dapat dikenal dengan teknik pewarnaan. Pada hari ke 9 dan 10
kehamilan sebagian mengalami degenerasi dan sebagian lain mengalami proliferasi
dan bahkan bergerak (pada hari ke 11 dan 12) ke daerah genitalia. Pada saat itu
jumlahnya mencapai sekitar 5000 dan identifikasi testis dapat dilakukan. Proses
proliferasi dan differensiasi berlangsung di daerah medulla testis. Pada kasus steril,
kehilangan sel germinal berlangsung selama perjalanan dari bagian ekstra gonad
menuju daerah genitalia. Menuju akhir masa fetus, aktivitas mitosis sel germinal
primordial dalam bagian genitalia berkurang dan beberapa sel mulai degenerasi
menjelang hari ke-19 kehamilan. Tidak berapa lama setelah kelahiran, sel tampak
lebih besar, yaitu spermatogonia. Setelah itu akan ada spermatogonia dalam testis
mencit sepanjang hidupnya. Ada 3 jenis spermatogonia: tipe A, tipe intermediate dan
tipe B (Rugh, 1967).
Tipe A adalah induk stem cell yang mampu mengalami mitosis sampai
menjadi spermatozoa. Spermatogonia tipe A yang paling besar dan mengandung inti
kromatin yang mirip partikel debu halus dan nukleolus kromatin tunggal terletak
eksentrik. Kromosom metafasenya panjang dan tipis. Dapat meningkat, melalui
dan mengandung inti kromatin serpihan kasar di atas atau dekat permukaan dalam
membran inti. Terdapat plasmosom mirip nukleolus yang terletak di tengah.
Kromosom metafase biasanya pendek, bulat, dan mirip kacang. Spermatogonia tipe B
membelah dua untuk meningkatkan jumlahnya atau berubah menjadi spermatosit
primer, lebih jauh dari membran dasar. Diperkirakan lamanya dari metafase
spermatogonia menjadi profase meiosis sekitar 3 sampai 9 hari, menuju metafase
kedua selama 4 hari atau kurang, dan menuju spermatozoa imatur selama 7 hari atau
lebih. Maka, waktu dari metafase spermatogonia menjadi spermatozoa imatur paling
sedikit 10 hari (Rugh, 1967).
Sel tipe A pertama kali muncul 3 hari setelah kelahiran. Ketika jumlahnya
meningkat, sel germinal primordial yang merupakan asalnya dan kemudian berada
di samping membran dasar, akan berkurang jumlahnya. Pembelahan meiosis dalam
testis mulai 8 hari setelah kelahiran. Tanda pertama bahwa spermatogonia B akan
metamorfosis menjadi spermatosit primer adalah pembesaran dan bergerak menjauhi
membran dasar. Spermatosit primer membelah menjadi 2 spermatosit sekunder yang
lebih kecil, yang kemudian membelah menjadi 4 spermatid. Mereka mengalami
metamorfosis radikal menjadi spermatozoa matur dengan jumlah yang sama,
kehilangan sitoplasmanya dan berubah bentuk (Rugh, 1967).
Antara tahap spermatosit primer dan sekunder, materi kromatin harus
membelah. Sintesa premeiotik DNA terjadi di spermatosit primer selama fase
istirahat dan berakhir sebelum onset profase meiosis, rata-rata selama 14 jam. Tidak
spermatogenesis mencit pada dasarnya sama dengan mamalia lain. Satu siklus epitel
seminiferus selama 207±6 ϕαm, δαν 4 σικλυσ ψανγ mιριπ τερϕαδι ανταρα σπερmατογονια
A dan spermatozoa matur. Produksi spermatozoa matur dari sel spermatogonia
berlangsung 5 minggu pada mencit. Testis dan khususnya spermatozoa matur,
merupakan sumber hyaluronidase terkaya, dan enzim ini efektif membubarkan sel
cumulus sekitar ovum matur pada saat fertilisasi. Setiap spermatozoa membawa
enzim yang cukup untuk membersihkan jalan melalui sel cumulus menuju matriks jel
ovum. Bahan asam hialuronik semen cenderung bergabung ke sel granulosa sel
BAB III
METODE PENELITIAN
3.1. Tempat dan Waktu
Penelitian telah dilaksanakan di Laboratorium Terpadu Universitas Sumatera
Utara dimulai dari tanggal 30 Mei sampai dengan 22 Juli 2009.
3.2. Variabel Penelitian
3.2.1. Variabel Independen
a. Monosodium Glutamate (MSG).
b. Vitamin C.
3.2.2. Variabel Dependen
a. Jumlah sperma.
b. Morfologi sperma.
3.3. Definisi Operasional
a. Jumlah sperma adalah banyaknya sperma yang diperoleh dari cauda
epididimis dalam sperma/ml suspensi.
b. Morfologi sperma normal dan abnormal yang diperoleh dari cauda
epididimis.
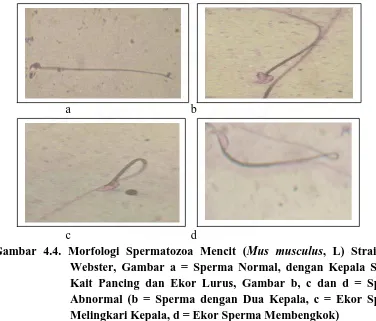
1) Morfologi sperma normal yaitu mempunyai bentuk kepala seperti kait
2) Morfologi sperma abnormal mempunyai bentuk kepala tidak beraturan,
dapat berbentuk seperti pisang, atau tidak beraturan (amorphous), atau
terlalu bengkok, dan ekornya tidak lurus bahkan tidak berekor, atau hanya
terdapat ekornya saja tanpa kepala (Washington et al., 1983).
3.4. Bahan dan Alat Penelitian
3.4.1. Bahan Penelitian
Bahan biologis. Bahan biologis yang akan digunakan dalam penelitian ini
adalah mencit jantan (Mus musculus L.) strain DD Webster dewasa fertil berumur ± 3
bulan dengan berat badan 25-35 gram yang diperoleh dari Unit Pra Klinik LPPT
Universitas Gajah Mada (UGM) Yogyakarta. Jumlah hewan uji perkelompok
ditentukan dengan rumus (t-1) (n-1) ≥ 15. ϑικα t adalah jumlah perlakuan (dalam
penelitian ini ada 5 kelompok perlakuan) dan n adalah jumlah ulangan perkelompok,
maka jumlah n yang diharapkan (teoritis) adalah 5 (Federer, 1963). Sehingga jumlah
keseluruhan hewan coba yang diperlukan dalam penelitian ini adalah sebanyak 25
ekor yang dipilih dari hasil perbanyakan untuk keperluan penelitian. Persetujuan
ethical clearance dari Komisi Etika Penelitian Kesehatan Wilayah Sumatera Utara
Medan.
Bahan kimia. Bahan kimia yang dibutuhkan untuk meneliti efek pemberian
vitamin C terhadap jumlah sperma dan morfologi sperma mencit jantan dewasa yang
dipaparkan MSG adalah Monosodium glutamate murni, Vitamin C, NaCl 0,9%,
3.4.2. Peralatan Utama Penelitian
Alat utama yang digunakan dalam penelitian antara lain: jarum oval (Gavage),
bak bedah dan dissecting set, gelas arloji, cawan petri, batang pengaduk, timbangan
(balance) dengan ketelitian 0,01 gram, objek glas, cover glass, spuit insulin 1 ml,
kamar hitung Improved Neubauer dan mikroskop cahaya.
3.5. Disain Penelitian
Jenis penelitian ini adalah penelitian eksperimental yang didisain mengikuti
Rancangan Acak Lengkap (RAL). Penelitian ini terdiri atas 5 kelompok perlakuan,
yaitu:
a) Kelompok I (P0) = terdiri dari 5 ekor mencit jantan dewasa yang diberi
larutan NaCl 0,9% sebanyak 0,5 ml secara intraperitoneal selama 30 hari.
b) Kelompok II (P1) = terdiri dari 5 ekor mencit jantan dewasa yang diberi MSG
4 mg/g berat badan yang dilarutkan dalam 0,5 ml larutan NaCl 0,9% secara
intraperitoneal setiap hari selama 15 hari selanjutnya 15 hari berikutnya
diberikan larutan NaCl 0,9% sebanyak 0,5 ml secara intraperitoneal setiap
hari.
c) Kelompok III (P2) = terdiri dari 5 ekor mencit jantan dewasa yang diberi
MSG 4 mg/g berat badan yang dilarutkan dalam 0,5 ml larutan NaCl 0,9%
secara intraperitoneal setiap hari selama 30 hari.
d) Kelompok IV (P3) = terdiri dari 5 ekor mencit jantan dewasa yang diberi
secara intraperitoneal setiap hari selama 15 hari pertama, selanjutnya 15 hari
berikutnya diberikan vitamin C 0,2 mg/g berat badan yang dilarutkan dalam
0,5 ml aquadest secara oral setiap hari.
e) Kelompok V (P4) = terdiri dari 5 ekor mencit jantan dewasa yang diberi MSG
4 mg/g berat badan yang dilarutkan dalam 0,5 ml larutan NaCl 0,9% secara
intraperitoneal setiap hari selama 15 hari pertama, selanjutnya 15 hari
berikutnya pemberian MSG diteruskan disertai dengan pemberian vitamin C
0,2 mg/g berat badan yang dilarutkan dalam 0,5 ml aquadest secara oral setiap
hari.
Mencit ditempatkan ke dalam kelompok secara random.
P4
P3
P2
P1
P0
0 15 30 (hari) Λαρυταν ΝαΧλ 0,9 %
ΜΣΓ Λαρυταν ΝαΧλ 0,9%
ΜΣΓ ΜΣΓ
ςιταmιν Χ
ΜΣΓ ΜΣΓ + ςιταmιν Χ
ΜΣΓ
3.6. Pelaksanaan Penelitian
3.6.1. Pemeliharaan Hewan Percobaan
Mencit ditempatkan di dalam kandang yang terbuat dari bahan plastik (ukuran
30x20x10 cm) yang ditutup dengan kawat kasa. Dasar kandang dilapisi dengan
sekam padi setebal 0,5-1 cm dan diganti setiap tiga hari. Cahaya ruangan dikontrol
persis 12 jam terang (pukul 06.00 sampai dengan pukul 18.00) dan 12 jam gelap
(pukul 18.00 sampai dengan pukul 06.00), sedangkan suhu dan kelembaban ruangan
dibiarkan berada pada kisaran alamiah. Pakan (pelet komersial) dan minum (air
PAM) disuplai setiap hari secara berlebih. Persetujuan ethical clearance dari Komisi
Etika Penelitian Kesehatan Wilayah Sumatera Utara Medan.
3.6.2. Pengamatan
Setelah 30 hari perlakuan, masing-masing hewan coba dikorbankan dengan
cara dislokasi leher dan selanjutnya dibedah. Selanjutnya dilakukan pengamatan
sebagai berikut:
3.6.2.1.Pengambilan sekresi cauda epididimis
Untuk mendapatkan sperma di dalam sekresi cauda epididimis dilakukan menurut
Soehadi dan Arsyad (1983) sebagai berikut: Setelah 30 hari perlakuan, masing-masing
hewan percobaan dikorbankan dengan cara dislokasi leher dan selanjutnya dibedah.
Kemudian organ testis beserta epididimis sebelah kanan diambil dan diletakkan ke
dalam cawan petri yang berisi NaCl 0,9%. Di bawah mikroskop bedah dengan
pembesaran 400 kali cauda epididimis dipisahkan dengan cara memotong bagian
epididimis dimasukkan ke dalam gelas arloji yang berisi 1 ml NaCl 0,9%, kemudian
bagian proximal cauda dipotong sedikit dengan gunting lalu cauda ditekan dengan
perlahan hingga sekresi cairan epididimis keluar dan tersuspensi dengan NaCl 0,9%.
Suspensi sperma dari cauda epididimis yang telah diperoleh dapat digunakan untuk
pengamatan yang meliputi: jumlah sperma, dan morfologi sperma.
3.6.2.2.Pengamatan sperma
Pengamatan sperma dilakukan sebagai berikut:
Suspensi sperma yang telah diperoleh terlebih dahulu dihomogenkan.
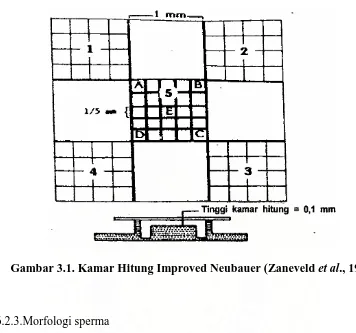
Selanjutnya diambil sebanyak 10 ∝l sampel dan dimasukkan ke dalam kotak-kotak
hemositometer Improved Neubauer serta ditutup dengan kaca penutup. Di bawah
mikroskop cahaya dengan perbesaran 400 kali, hemositometer diletakkan dan dihitung
jumlah sperma pada kotak/bidang A,B,C,D, dan E. Hasil perhitungan jumlah sperma
kemudian dimasukkan ke dalam rumus penentuan jumlah sperma/ml suspensi sekresi
cauda epididimis sebagai berikut:
dimana N = jumlah sperma yang dihitung pada kotak A,B,C,D,dan E. ϑυmλαη σπερmα = Ν / 2 ξ 105 σπερmα/mλ
Gambar 3.1. Kamar Hitung Improved Neubauer (Zaneveld et al., 1986)
3.6.2.3.Morfologi sperma
Untuk menentukan morfologi sperma, diambil sperma dari cauda epididimis
tersebut di atas dan dibuat sediaan hapus pada kaca objek, dikeringkan. Kemudian
diberi alkohol 70% selama 15 menit, dikeringkan dan diberi perwarnaan Giemsa
selama 15 menit. Setelah itu dibilas dengan air kran dan dikeringkan. Kemudian
dengan mikroskop cahaya dihitung dengan jumlah 100 sperma, ditentukan persentasi
sperma yang normal dan abnormal. Untuk mendapatkan hasil akhirnya, jumlah
persentase sperma yang normal kiri dan kanan cauda epididimis dijumlah kemudian
diambil rata-ratanya. Ciri sperma normal yaitu mempunyai bentuk kepala seperti kait
kepala tidak beraturan, dapat berbentuk seperti pisang, atau tidak beraturan
(amorphous), atau terlalu bengkok, dan ekornya tidak lurus bahkan tidak berekor,
atau hanya terdapat ekornya saja tanpa kepala (Gambar 3.2).
A B C D
Gambar 3.2. Morfologi Sperma Vas Deferen Mencit (Washington et al., 1983) Gambar A adalah Sperma Normal, dengan Kepala Seperti Kait Pancing, Gambar B, C dan D adalah Sperma Abnormal (B = Sperma dengan Kepala Seperti Pisang, C = Sperma Tidak Beraturan, dan D = Sperma Terlalu Bengkok)
3.7. Analisa Data dan Pengujian Hipotesis
Semua data dipresentasikan dalam bentuk rata-rata ± σιmπανγαν βακυ
(ρατα-rata ± ΣD). Dιλακυκαν υϕι νορmαλιτασ δαν ηοmογενιτασ δατα. ϑικα δατα βερδιστριβυσι
[image:44.612.123.499.211.496.2]dilanjutkan dengan uji Post Hoc analisis Benferroni taraf 5% untuk melihat perbedaan
antar kelompok kontrol dan masing-masing perlakuan.
Jika distribusi data tidak normal dan atau tidak homogen, maka dilakukan
transformasi data. Kemudian diuji lagi normalitas dan homogenitas data. Apabila
masih tidak normal distribusinya dan data tidak homogen maka diuji dengan uji
Mann Whitney untuk membandingkan antara 2 kelompok perlakuan (kontrol vs
perlakuan). Pada kelompok data lebih dari 2 kelompok maka dilakukan uji Friedman.
Semua analisa data dilakukan dengan menggunakan SPSS versi 15,0. Dalam
penelitian ini, hanya perbedaan rata-rata pada 〈 ≤ 0,05 ψανγ διανγγαπ βερmακνα
(signifikan).
3.8. Jadwal Penelitian
Keseluruhan kegiatan penelitian dari persiapan sampai pada penulisan hasil
penelitian adalah lebih kurang tujuh minggu. Urutan kegiatan dan jadwal pelaksanaan
[image:45.612.114.459.358.437.2]secara lengkap dapat dilihat pada tabel berikut ini.
Tabel 3.1. Jadwal Penelitian
No Kegiatan Minggu Ke
1 2 3 4 5 6 7
1 PERSIAPAN √
2 PELAKSANAAN √ √ √ √
3 ANALISA DATA √
BAB IV
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
4.1.1. Berat Badan Awal dan Akhir Mencit Jantan Dewasa
Dari penelitian ini diperoleh hasil pengukuran berat badan awal dan berat
badan akhir mencit jantan dewasa (Mus musculus, L) strain DD Webster adalah
[image:46.612.120.510.362.531.2]sebagai berikut:
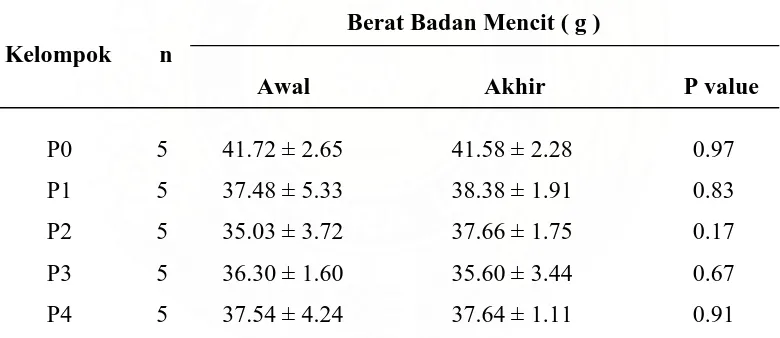
Tabel 4.1. Pengamatan Berat Badan Awal dan Akhir Mencit Jantan Dewasa
Berat Badan Mencit ( g ) Kelompok n
Awal Akhir P value
P0 5 41.72 ± 2.65 41.58 ± 2.28 0.97
P1 5 37.48 ± 5.33 38.38 ± 1.91 0.83
P2 5 35.03 ± 3.72 37.66 ± 1.75 0.17
P3 5 36.30 ± 1.60 35.60 ± 3.44 0.67
P4 5 37.54 ± 4.24 37.64 ± 1.11 0.91
Nilai adalah rata-rata ± SD
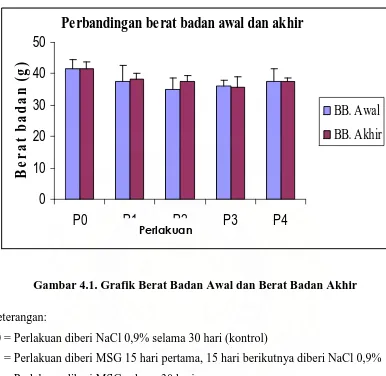
Berdasarkan Tabel 4.1 di atas hasil uji statistik berat badan awal dan berat
badan akhir subjek terjadi perubahan tidak bermakna baik yang diberi MSG dan
Perbandingan berat badan awal dan akhir
0
10
20
30
40
50
P0
P1
P2
P3
P4
[image:47.612.125.511.111.487.2]Kelompok
B
e
r
a
t
b
a
d
a
n
(
g
)
BB. Awal
BB. Akhir
Gambar 4.1. Grafik Berat Badan Awal dan Berat Badan Akhir
Keterangan:
P0 = Perlakuan diberi NaCl 0,9% selama 30 hari (kontrol)
P1 = Perlakuan diberi MSG 15 hari pertama, 15 hari berikutnya diberi NaCl 0,9%
P2 = Perlakuan diberi MSG selama 30 hari
P3 = Perlakuan diberi MSG 15 hari pertama, 15 hari berikutnya diberi Vitamin C
P4 = Perlakuan diberi MSG 15 hari pertama, 15 hari berikutnya diberi MSG +
Vitamin C
4.1.2. Jumlah Sperma Mencit Jantan Dewasa
Dari penelitian ini diperoleh hasil jumlah sperma di dalam suspensi cauda
epididimis mencit jantan dewasa (Mus musculus, L) strain DD Webster sebagai
berikut:
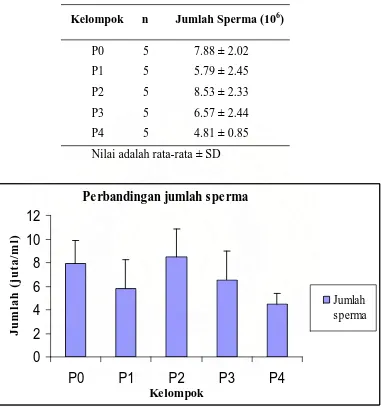
Tabel 4.2. Jumlah Sperma di dalam Suspensi Cauda Epididimis Mencit Jantan Dewasa
Kelompok n Jumlah Sperma (106)
P0 5 7.88 ± 2.02
P1 5 5.79 ± 2.45
P2 5 8.53 ± 2.33
P3 5 6.57 ± 2.44
P4 5 4.81 ± 0.85
Nilai adalah rata-rata ± SD
Perbandingan jumlah sperma
0
2
4
6
8
10
12
P0
P1
P2
P3
P4
Kelompok
J
u
m
la
h
(
ju
ta
/m
l)
Jumlah spermaGambar 4.2. Grafik Jumlah Sperma
Berdasarkan Tabel 4.2 dan Gambar 4.2 di atas diperoleh hasil pada subjek P1
(5.79±2.45), P3 (6.57±2.44), dan P4 (4.81±0.85) jumlah sperma lebih rendah bila
dibandingkan dengan P0 (7.88±2.02), dan pada P2 (8.53±2.33) jumlah sperma lebih
bila dibandingkan dengan P1 pada perlakuan yang diberi MSG. Dan pada P4 jumlah
sperma lebih rendah bila dibandingkan dengan P3 pada perlakuan yang diberi MSG
dan Vitamin C baik tersendiri maupun bersamaan.
Dari hasil penelitian ini terdapat perbedaan rata-rata jumlah sperma pada tiap
kelompok perlakuan tetapi perbedaan tersebut tidak bermakna. Berdasarkan hasil uji
statistik rata-rata jumlah sperma pada setiap kelompok perlakuan p>0,05, yang berarti
tidak ada pengaruh pemberian MSG dan Vitamin C pada setiap kelompok perlakuan.
4.1.3. Morfologi Sperma Mencit
Dari penelitian ini diperoleh hasil morfologi sperma normal di dalam suspensi
cauda epididimis kanan dan kiri mencit jantan dewasa (Mus musculus, L) strain DD
Webster sebagai berikut:
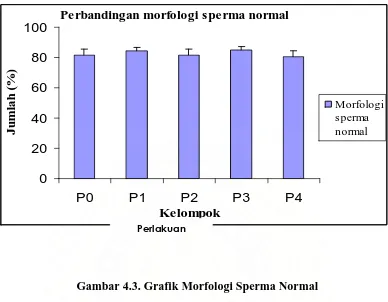
Tabel 4.3. Morfologi Sperma Normal di dalam Suspensi Cauda Epididimis Mencit Jantan Dewasa
Kelompok n Morfologi Sperma Normal (%)
P0 5 81.70 ± 3.62
P1 5 84.20 ± 2.33
P2 5 81.70 ± 3.85
P3 5 85.00 ± 2.42
P4 5 80.80 ± 3.82
Pe rbandingan morfologi spe rma normal
0
20
40
60
80
100
P0
P1
P2
P3
P4
Kelompok
J
u
m
la
h
(
%
)
[image:50.612.123.511.113.415.2]Morfologi sperma normal
Gambar 4.3. Grafik Morfologi Sperma Normal
Berdasarkan Tabel 4.3 dan Gambar 4.3 di atas diperoleh hasil pada subjek P1
(84.20±2.33) persentase rata-rata morfologi sperma normal lebih tinggi bila
dibandingkan dengan P0 (81.70±3.62), P2 (81.70±3.85) dibanding dengan P0
terdapat hasil yang sama persentase rata-rata morfologi sperma normal, P3
(85.00±2.42) persentase rata-rata morfologi sperma normal lebih tinggi bila
dibandingkan dengan P0, dan P4 (80.80±3.82) persentase rata-rata morfologi sperma
normal lebih rendah bila dibandingkan dengan P0. Sedangkan P2 persentase rata-rata
morfologi sperma normal lebih rendah bila dibandingkan dengan P1 pada perlakuan
yang diberi MSG, dan P4 persentase rata-rata morfologi sperma normal lebih rendah
bila dibandingkan dengan P3 pada perlakuan yang diberi MSG dan Vitamin C baik
tersendiri maupun bersamaan.
Berdasarkan hasil uji statistik rata-rata persentase morfologi sperma normal
pada subjek p>0,05, yang berarti tidak ada pengaruh pemberian MSG dan pemberian
Vitamin C pada subjek antara kelompok perlakuan. Dari hasil penelitian ini terdapat
perbedaan rata-rata persentase morfologi sperma normal pada tiap kelompok
perlakuan tetapi tidak menunjukkan hasil yang bermakna.
Aaa a b
c d
[image:51.612.120.496.303.624.2]4.2. Pembahasan
Dari hasil penimbangan berat badan mencit jantan dewasa dapat dilihat bahwa
berat badan awal dan akhir tidak dipengaruhi oleh pemberian MSG dan vitamin C
secara tersendiri maupun bersamaan (Tabel 4.1 dan Gambar 4.1), hal ini dapat dilihat
pada perlakuan. Berarti ada perbedaan tidak bermakna terhadap berat badan awal dan
akhir pada subjek diantara kelompok perlakuan.
Dari hasil perhitungan jumlah sperma di dalam suspensi cauda epididimis
pada kelompok perlakuan diperolehrata-rata jumlah sperma pada P2 lebih tinggi bila
dibandingkan dengan P0 (kontrol), tetapi pada rata-rata jumlah sperma menunjukkan
hasil yang tidak bermakna pada subjek, yang berarti tidak ada pengaruh pemberian
MSG pada subjek antara kelompok perlakuan.
Penelitian Nayanatara et al., (2008), bahwa pemberian MSG 4 g/kg berat
badan secara intraperitoneal pada tikus Wistar jantan dewasa selama 30 hari (paparan
jangka panjang) memperlihatkan terjadinya penurunan berat testis, penurunan jumlah
sperma yang bentuknya normal dan peningkatan jumlah sperma yang bentuknya
abnormal, penurunan kadar asam askorbat di dalam testis dan peningkatan kadar
peroksidasi lipid di dalam testis.
Pada penelitian ini rata-rata jumlah sperma pada P4 lebih rendah bila
dibandingkan dengan P3, berarti pemberian Vitamin C tidak memberikan pengaruh
terhadap jumlah sperma. Bahwa hal ini menunjukkan jumlah sperma tidak
dipengaruhi oleh pemberian MSG dan vitamin C secara tersendiri maupun bersamaan
Menurut penelitian Agarwal et al., (2005), stres oksidatif dapat diatasi dengan
menggunakan antioksidan berupa suplemen vitamin E dan C. Vitamin C dapat
menetralisir radikal hidroksil, superoksid, dan hidrogen peroksida dan mencegah
aglutinasi sperma. Vitamin C sedikit jumlahnya pada cairan semen laki-laki infertil.
Vitamin C dapat meningkatkan jumlah sperma in vivo pada laki-laki infertil dengan
dosis oral sekitar 200-1000 mg/hari.
Dari pemeriksaan morfologi sperma normal di dalam suspensi cauda
epididimis kanan dan kiri subjek diperoleh hasil rata-rata persentase morfologi
sperma normal P1, dan P3 lebih tinggi bila dibandingkan dengan P0 (kontrol). Pada
rata-rata persentase morfologi sperma normal P2 bila dibandingkan dengan P0
hasilnya sama, sedangkan pada persentase rata-rata morfologi sperma normal P4
lebih rendah bila dibandingkan dengan P3, berarti pemberian Vitamin C tidak
memberikan pengaruh terhadap morfologi sperma normal. Bahwa hal ini
menunjukkan morfologi sperma normal tidak dipengaruhi oleh pemberian MSG dan
vitamin C secara tersendiri maupun bersamaan pada perlakuan.
Pada penelitian ini menggunakan subjek Mus musculus, L. diperoleh hasil
jumlah sperma dan morfologi sperma normal terdapat adanya hasil yang lebih tinggi
dan lebih rendah bila dibandingkan dengan kontrol, ada perbedaan hasil tetapi tidak
bermakna p>0.05. Hal ini tidak sejalan dengan penelitian yang dilakukan Nayantara,
et al., (2008) menggunakan subjek rat, perbedaan hasil pada penelitian ini
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Tidak ada pengaruh pemberian Vitamin C terhadap jumlah sperma dan
morfologi sperma mencit jantan dewasa (Mus musculus. L) yang dipaparkan
Monosodium Glutamate (MSG).
5.2. Saran
Sebaiknya dilakukan penelitian lebih lanjut dengan menggunakan MSG dan
DAFTAR PUSTAKA
Acharya, U., Mishra, M., Tripathy, R., & Mishra, I. (2006), Testicular dysfunction and antioxidant defense system of Swiss mice after chromic acid exposure. Reprod Toxicol, 22, 87-91.
Agarwal, A., Prabakaran, S. & Said, T. (2005), Prevention of oxidative stress injury to sperm. J Androl, 26, 654-60.
Ahluwalia, P., Tewari K. & Choudary, P. (1996), Studies on the effects of monosodium glutamate (MSG) on oxidative stress in erythrocytes of adult male mice. Toxicol Lett, 84, 161-5.
Akmal, M., Qadri, J. Q., Al-Waili, N. S., Thangal, S., Haq, A. & Saloom, K. Y. (2006), Improvement in human semen quality after oral supplementation of vitamin C. J Med Food, 9, 440-2.
Babu, G. N., Bawari, M. & Ali, M. M. (1994), Lipid peroxidation potential and antioxidant status of circumventricular organs of rat brain following neonatal monosodium glutamate. Neurotoxicology, 15, 773-7.
Diniz, Y. S., Faine, L. A., Galhardi, C. M., Rodrigues, H. G., Ebaid, G. X., Burneiko, R. C., Cicogna, A. C. & Novelli, E. L. (2005), Monosodium glutamate in standard and high-fiber diets: metabolic syndrome and oxidative stress in rats. Nutrition, 21, 749-55.
Farombi, E. O. & Onyema, O. O. (2006), Monosodium glutamate-induced oxidative damage and genotoxicity in the rat: modulatory role of vitamin C, vitamin E and quercetin. Hum Exp Toxicol, 25, 251-9.
Fauzi, T. (2008), Pengaruh pemberian timbal asetat dan vitamin C terhadap peroksidasi lipid dan kualitas spermatozoa di dalam sekresi epididimis mencit jantan (Mus musculus L.) strain DDW. Biomedic. Medan, Univeristas Sumatera Utara.
FDA (1995) FDA and monosodium gtamate (MSG) avaiable at
http://www.fda.gov/opacom/backgrounders/msg.html
Garattini, S. (2000), Glutamic acid, twenty years later. Journal of Nutrition, 130, 901S-909S.
Geha, R., Beiser, A., Ren, C. Patterson, R., Greenberger, P., Grammer, L., Ditto, A., Harris K., Saughnessy, M., Yarnold, P., Corrent, J. & Saxon, A. (2000), Review of alleged reaction to monosodium glutamate and outcome of a multicenter double-blind placebo-controlled study. The Journal of Nutrition, 130, 1058S-1062S.
Gold, M. (1995), Monosodium glutamate.
Gupta, A. D., Dhundasi, S. A., Ambekar, J. G. & Das, K. K. (2007), Effect of l-ascorbic acid on antioxidant defense system in testes of albino rats exposed to nickel sulfate. J Basic Clin Physiol Pharmacol, 18, 255-66.
Halpern, B. (2002), What’ ιν α ναmε ? Αρε ΜΣΓ ανδ υmαmι τηε σαmε ? Chemical Sense.
Hayati A, Mangkoewidjojo S, Hinting A, Moedjopawiro S. (2006), Hubungan kadar MDA spermatozoa dengan integritas membran spermatozoa tikus (Rattus novergicus L) setelah pemaparan 2-methoxyethanol. J Berk. Penel. Hayati 11:151-154
Hsieh, Y., Chang, C. & Lin, C (2006), Seminal malondialdehyde concentration but not glutathione peroxidase activity is negatively correlated with seminal concentration and motility. Int J Biol Sci, 2(1), 23-29.
Kenney, R. (1986), The Chinese restaurant syndrome: an anecdote revisited. Food Chem Toxicol., 351