Coptotermes curvignathus Holmgren (Isoptera: Rhinotermitidae)
FARAH DIBA
IN ST
ITUT PERTAN
IA
N
B O G O R
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Saya yang bertanda tangan di bawah ini:
Nama : Farah Diba
NRP. : P14600007
Asal Program Studi : Ilmu Pengetahuan Kehutanan Asal Universitas : Universitas Tanjungpura Pontianak
NIP. : 132 146 233
Alamat Asal : Komplek UNTAN No. P 42
Jl. Imam Bonjol Pontianak Kalimantan Barat
Menyatakan dengan sebenarnya bahwa disertasi yang berjudul:
STUDI ANATOMI, FISIOLOGI DAN BIOAKTIFITAS
SEKRESI PERTAHANAN DIRI RAYAP TANAH
Coptotermes curvignathus Holmgren (Isoptera: Rhinotermitidae)
Adalah karya saya sendiri, termasuk semua isi dan data hasil penelitian yang saya kerjakan sejak Bulan Juli 2003 sampai Bulan Juli 2005, dibimbing oleh 5 (lima) dosen pembimbing, yaitu: Prof. Dr. Ir. Dodi Nandika, MS sebagai ketua komisi; Prof. Dr. Ir. Rudy C. Tarumingkeng, MF; Dr. dr. Sri Budiarti; Dr. Ir. Anton Apriyantono, MS dan Dr. Ir. Achmad, MS sebagai anggota. Data hasil penelitian pada disertasi belum pernah diajukan dalam bentuk apapun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka.
Bogor, 23 Mei 2006
Defensive Secretions of Subterranean Termites Coptotermes
curvignathus Holmgren (Isoptera: Rhinotermitidae). Under supervision
of Dodi Nandika as the chairman, Rudy C Tarumingkeng, Sri Budiarti, Anton Apriyantono and Achmad as advisory committee members.
Termites possess rigid totalitarian societies in which morphologically specialized individuals execute specific tasks: the king and queen to reproduce, the workers to forage and feed, and the soldiers to defend the colonies. Soldier caste of subterranean termite’s C. curvignathus has chemical defensive secretions to destroy their enemy. The aims of this research were (1) to study the morphology and ultra structure of soldier C. curvignathus defense glands; (2) to isolate and characterize C. curvignathus defensive secretions; (3) to determine the toxicity of C. curvignathus soldier defensive secretion against ants; (4) to determine the antibacterial activity of C. curvignathus soldier defensive secretion extract; (5) to determine the antifungal activity of C. curvignathus soldier defensive secretion extract; (6) to identify the bioactive components of C. curvignathus soldier defensive secretion extract which has function as antibacterial, antifungal and toxic to ants.
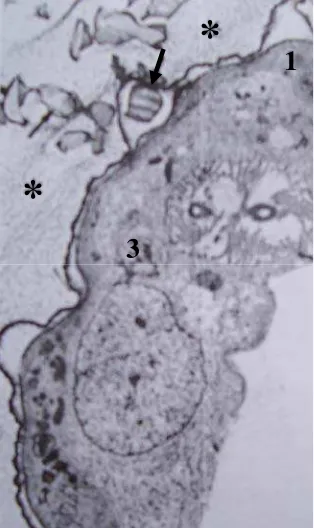
Result of the research showed that soldier defensive secretions are produced in frontal gland, with 2.5 + 0.10 mm long and ∅ 0.8 + 0.16 mm. This frontal gland is almost entirely occupying termite’s abdomen and has very thin cell wall (4 – 10 μm) and forming by cell class 1 and class 3. Soldier defensive secretions was extracted by non polar until polar solution, including n-hexane, ethyl acetate, ethanol and aquabidestilata. The yield value was range between 27.9081% – 38.0982%; pH 4-5.5; viscosity 0.00002 – 0.0005 poise; and 27 – 27.5oC; the extract color was white and grey.
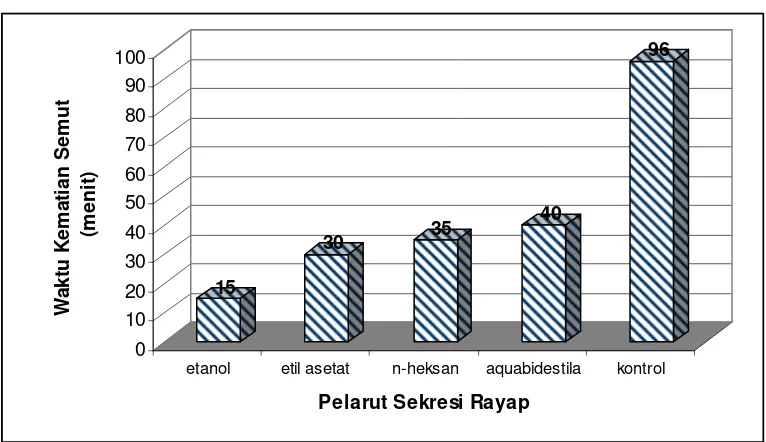
Time for 100 percent mortality of Odontoponera denticulata ant on toxicity test showed that ethanol extract is the fastest with 54 hours then followed by ethyl acetate extract; n-hexane extract and aquabidestilata extract which was 74 hours, 79 hours and 82 hours, respectively. Time for the first ant mortality was occurred on ethanol extract at 15 minute, and then followed by ethyl acetate extract; n-hexane extract and aquabidestilata extract which was 30 minutes, 35 minutes and 40 minutes, respectively.
was linier from low until highest concentration of ethyl acetate extract. The inhibition value for concentration extract 2% is 2.5%, concentration 4% is 6.5 %, concentration 6% is 30.5%, and concentration 8% and 10% is 100%. Dilution of pine seed on ethyl acetate extract increased seed germination. Average value of germination of pine seed was 41.33%, meanwhile on control seed the average value of germination is 30.67%. Dilution of pine seed on ethyl acetate extract also decreased the damping-off on pine seed. The average value of damping-off on control seed was 41.33%, meanwhile on treated seed only 13.33%.
GCMS analysis on ethanol extract showed that soldier defensive secretion extract of C. curvignathus termites consist of 5 compounds, while ethyl acetate extract consisted of 6 compounds. Ethanol extract consist of 20% alkenes and 80% aldehyde, meanwhile ethyl acetate extract consist of 50% aldehyde and 34% ester and 16% alcohol. The soldier defensive secretions of C. curvignathus consist of 7 compound of aldehyde, and Pentadecanal and Tetradecanal is the highest compound which contains of 72.81% and 60.17% respectively. From this research, it is concluding that defensive secretions of C. curvignathus have ability as antibacterial and antifungal and potential to be antibiotics.
Keywords : Coptotermes curvignathus, soldier defensive secretions,
Pertahanan Diri Rayap Tanah Coptotermes Curvignathus Holmgren (Isoptera: Rhinotermitidae). Di bawah bimbingan Dodi Nandika sebagai ketua komisi, Rudy C. Tarumingkeng, Sri Budiarti, Anton Apriyantono dan Achmad sebagai anggota.
Rayap tanah Coptotermes curvignathus Holmgren merupakan spesies yang paling penting sebagai hama bangunan. Serangannya pada bangunan terjadi hampir di seluruh kota besar di Indonesia, dengan nilai kerugian ekonomis yang sangat besar. Prajurit rayap ini memiliki pertahanan diri yang khas, yaitu mengeluarkan sekresi kimia yang mengandung racun dalam mengusir atau membunuh musuh. Penelitian ini bertujuan untuk: (1) mempelajari struktur morfologi kelenjar penghasil sekresi pertahanan rayap C. curvignathus; (2) mengkarakterisasi sekresi pertahanan rayap; (3) mempelajari daya racun ekstrak sekresi pertahanan rayap terhadap semut; (4) mempelajari daya racun ekstrak sekresi pertahanan rayap terhadap bakteri patogen; (5) mempelajari daya racun ekstrak sekresi pertahanan rayap terhadap cendawan penyakit lodoh; dan (6) mengidentifikasi komponen ekstrak sekresi pertahanan rayap C. curvignathus yang memiliki daya racun terhadap semut, bakteri patogen dan cendawan penyakit lodoh.
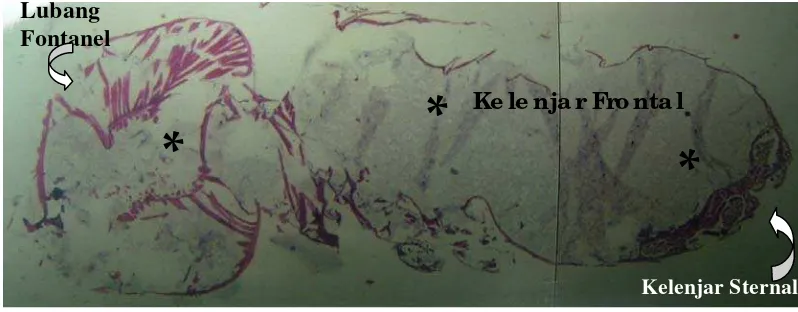
Hasil penelitian menunjukkan bahwa sekresi pertahanan diri kasta prajurit rayap C. curvignathus diproduksi dalam kelenjar frontal (frontal gland) yang memenuhi hampir seluruh abdomen rayap dengan ukuran panjang 2,5 + 0,10 mm dan diameter 0,8 + 0,16 mm, dan berujung pada lubang fontanel yang terletak di kepala rayap yang berukuran diameter 0,2 + 0,18 mm. Ekstraksi sekresi pertahanan rayap dilakukan dengan pelarut n-heksan, etil asetat, etanol, dan aquabidestilata, dengan jumlah rayap 4000 ekor untuk masing-masing pelarut. Nilai rendemen ekstrak 27,9081% – 38,0982%; nilai pH 4-5,5; nilai viscositas 0,00002 - 0,0005 poise; suhu 27 - 27,5oC ; dan warna ekstrak putih susu dan abu-abu. Pada pengujian daya racun ekstrak sekresi rayap terhadap semut Odontoponera denticulata, waktu untuk mencapai mortalitas semut sebesar 100 persen tercepat pada ekstrak etanol yang dicapai dalam waktu 54 jam, kemudian diikuti dengan ekstrak etil asetat, n-heksan dan aquabidestilata berturut-turut 74 jam, 79 jam dan 82 jam.
Sementara itu, pada pengujian terhadap cendawan penyebab lodoh pada benih pinus, ekstrak sekresi pertahanan rayap pada semua pelarut tidak dapat menghambat pertumbuhan cendawan Fusarium oxysporum, sedangkan pada cendawan Rhizoctonia solani hanya ekstrak etil asetat yang dapat menghambat pertumbuhan cendawan. Nilai aktivitas anticendawan ekstrak etil asetat semakin meningkat dari konsentrasi rendah ke konsentrasi tinggi. Pada konsentrasi 2% daya hambat pertumbuhan cendawan rata-rata sebesar 2,5%, konsentrasi 4% meningkat menjadi 6,5 %, konsentrasi 6% meningkat menjadi sebesar 30,5% dan pada konsentrasi 8% dan 10% masing-masing nilai daya hambat sebesar 100%. Pelapisan benih pinus dengan ekstrak sekresi rayap dalam pelarut etil asetat meningkatkan daya berkecambah benih yang ditanam pada media dengan cendawan R. solani, dengan nilai rata-rata sebesar 41,33%, sedangkan pada benih kontrol hanya sebesar 30,67%. Disamping itu juga mampu menekan serangan penyakit lodoh karena pada benih kontrol terjadi serangan sebesar 41,33%, sedangkan pada benih perlakuan hanya sebesar 13,33%.
Hasil analisis GCMS terhadap ekstrak etanol diperoleh 5 komponen senyawa yang berdasarkan golongan terdiri dari 20% golongan alkana dan 80% golongan aldehid. Sementara itu pada ekstrak etil asetat terdapat 6 komponen yang berdasarkan golongan terdiri dari 50% golongan aldehid, 34% golongan ester dan 16% golongan alkohol. Senyawa yang mendominasi ekstrak sekresi pertahanan diri rayap C. curvignathus adalah golongan aldehid (7 komponen). Senyawa yang memiliki persentase terbesar dari golongan aldehid adalah senyawa Pentadecanal dan Tetradecanal masing-masing sebesar 72,81% dan 60,17% Dari penelitian disimpulkan bahwa sekresi pertahanan diri rayap C. curvignathus memiliki potensi sebagai antimikroba, sebagai bahan pelindung benih pinus dari serangan cendawan penyakit lodoh dan memiliki potensi sebagai bahan antibiotik baru.
BIOAKTIFITAS SEKRESI PERTAHANAN DIRI
RAYAP TANAH
Coptotermes curvignathus Holmgren (Isoptera: Rhinotermitidae)
FARAH DIBA
Disertasi
Sebagai salah satu syarat untuk memperoleh gelar Doktor pada
Program Studi Ilmu Pengetahuan Kehutanan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Nama : Farah Diba
NRP. : P14600007
Program Studi : Ilmu Pengetahuan Kehutanan
Disetujui : Komisi Pembimbing
Prof. Dr. Ir. Dodi Nandika, MS Ketua
Prof. Dr.Ir. Rudy C. Tarumingkeng, MF Dr. dr. Sri Budiarti Anggota Anggota
Dr. Ir. Anton Apriyantono, MS Dr. Ir. Achmad, MS Anggota Anggota
Diketahui :
Ketua Program Studi IPK Dekan Sekolah Pascasarjana
Dr. Ir. Rinekso Soekmadi, MSc Dr. Ir. Khairil Anwar Notodiputro, MS
hidayah dan rahmat-Nya sehingga penyusunan disertasi ini dapat diselesaikan. Disertasi dengan judul : “Studi Anatomi, Fisiologi Dan Bioaktifitas Sekresi Pertahanan Diri Rayap Tanah Coptotermes curvignathus Holmgren (Isoptera: Rhinotermitidae)” merupakan salah satu syarat untuk memperoleh gelar Doktor di Program Studi Ilmu Pengetahuan Kehutanan, Sekolah Pascasarjana IPB.
Penulis mengucapkan terima kasih yang mendalam dan penghargaan yang tinggi kepada komisi pembimbing Prof. Dr. Ir. Dodi Nandika, MS; Prof. Dr. Ir. Rudolf C. Tarumingkeng, MF; Dr. dr. Sri Budiarti; Dr. Ir. Anton Apriyantono, MS; dan Dr. Ir. Achmad, MS yang telah memberikan pengarahan dengan penuh kesabaran dan motivasi tinggi untuk kemajuan berpikir ilmiah. Terima kasih kepada penguji luar komisi Dr. Ir. Idham Sakti Harahap, MS, Prof. Ir. Surjono Surjokusumo, MSF, PhD serta Dr. James Sinambela yang telah memberi saran perbaikan disertasi.
Penulis menyampaikan terima kasih yang mendalam kepada suami tercinta Pramudi Kintaman yang dengan penuh kesabaran, pengertian dan selalu memberi semangat kepada penulis selama penelitian sampai menyelesaikan disertasi ini (wish you be my soulmates ever and after). Rasa terima kasih yang mendalam kepada ayahanda Ir. H. Faisal Makmur Mukti (alm) dan ibunda Hj. Dahniar Rusli, juga kepada ayah mertua Drs. Radjidi Zachry dan ibunda Nila Mawarni, yang telah memberi kasih sayang dan teladan tentang pentingnya pendidikan bagi kehidupan dunia dan yaumil akhir. Ucapan terima kasih kepada keluarga besar penulis yang telah banyak membantu dengan do’a dan kesabaran selama penulis berada di Bogor : abangda Ir. Fahrizal, MP dan mbak Dra. Dwi Nugrohoyekti beserta ponakanku yang beranjak dewasa Dhani dan Kiki serta Tiara yang manis, keluarga adinda Elsa Tri Mukti, ST, MT dan Rudi Sugiono, ST, MT beserta ponakanku yang lucu Bima dan Rangga, adinda Andres Duanta Ponti, adinda Adilla Zuchruf, dan keluarga adinda Yano Erman dan Dany Fitriana.
Penulis mengucapkan terima kasih kepada Rektor Universitas Tanjungpura Pontianak, Prof. Hj. Asniar Subagiyo Ismail, SE, MM yang memberikan dukungan selama penulis melanjutkan sekolah, Dekan Fakultas Kehutanan Prof. Ir. Sakoento, MS, Ketua Jurusan Teknologi Hasil Hutan Ir. Evy Wardenaar, MP serta staf pengajar Fakultas Kehutanan UNTAN yang terus mendukung perjalanan ilmiah ini. Ucapan terima kasih kepada Direktorat Jendral Pendidikan Tinggi Departemen Pendidikan Nasional yang telah memberikan Beasiswa Pendidikan Program Pascasarjana kepada penulis, selama pendidikan Program Magister dan Program Doktoral.
Penulis mengucapkan terima kasih karena mendapatkan bantuan yang sangat berharga berupa diskusi selama penelitian berlangsung dan kiriman jurnal yang membantu proses penelitian dari Prof. Dr. Glenn D. Prestwich dari Utah University, Amerika Serikat, Prof. Andre Quennedey dari Gabriel University, Dijon Perancis, Rebecca B. Rosengaus, Ph.D.dari Northeastern University, Boston Amerika Serikat, Prof Chuah Cheng Hock dari Malaya University, Malaysia , Dr. Ir. Dwi Setianingsih, MS dan Ir. Hendra Adijuwana, MST dari Institut Pertanian Bogor.
Penulis menyampaikan terima kasih atas bantuan finansial yang diberikan dalam pelaksanaan penelitian oleh Hibah Pasca. Penelitian ini merupakan bagian dalam penelitian Hibah Penelitian Tim Pascasarjana (Hibah Pasca) yang berjudul: Pengendalian Terpadu Koloni Rayap Tanah Genus Coptotermes Pada Lingkungan Permukiman di Pulau Jawa Berdasarkan Informasi Genetik dan Kelas Bahaya Rayap dengan ketua peneliti Prof. Dr. Rudy C Tarumingkeng, MF dan dibiayai selama 3 (tiga) tahun oleh Badan Penelitian, Pengembangan dan Pengabdian Pada Masyarakat Ditjen Dikti Departemen Pendidikan Nasional.
Pada disertasi ini mungkin masih ditemukan beberapa kekurangan, oleh karena itu kritik dan saran akan penulis terima dengan baik. Semoga disertasi ini bermanfaat bagi masyarakat secara umum maupun perkembangan iptek khususnya dalam bidang entomologi hutan. Termites, What an amazing world!!
Bogor, 23 Mei 2006
©Hak Cipta milik Farah Diba, tahun 2006
Hak cipta dilindungi
anak kedua dari tiga bersaudara dari pasangan yang berbahagia Ir H. Faisal Makmur Mukti (alm) dan Hj. Dahniar Rusli. Penulis menamatkan Sekolah Dasar Pertiwi Pontianak pada tahun 1983, kemudian melanjutkan ke SMP Negeri 1 Pontianak dan lulus pada tahun 1986. Pada tahun 1989 penulis lulus dari SMA Negeri 1 Pontianak kemudian melanjutkan studi di Fakultas Pertanian Jurusan Kehutanan Universitas Tanjungpura Pontianak.
Penulis menikah dengan Pramudi Kintaman pada tanggal 26 Juli 1992. Pada tahun 1994 penulis lulus dengan mendapat gelar Sarjana Kehutanan dan diterima sebagai staf pengajar di Fakultas Kehutanan Universitas Tanjungpura Pontianak. Pada tahun 1997 penulis mendapat Beasiswa Pendidikan Pasca Sarjana dari Direktorat Jendral Pendidikan Tinggi Departemen Pendidikan Nasional untuk mengikuti program magister pada Program Pascasarjana Institut Pertanian Bogor program studi Ilmu Pengetahuan Kehutanan, lulus dengan mendapatkan gelar Magister Sains pada tahun 1999. Pada tahun 2000 penulis kembali mendapatkan Beasiswa BPPS dari Ditjen DIKTI Departemen Pendidikan Nasional untuk melanjutkan pendidikan Program Doktor di IPB dengan bidang studi Ilmu Pengetahuan Kehutanan minat Entomologi Hutan.
Sebagian hasil penelitian dalam disertasi ini telah dipresentasikan pada Seminar 1st International Conference of Crop Security, Universitas Brawijaya, Malang, 20 - 22 September 2005 dengan judul “Utilization Soldier Defensive Secretions From Subterranean Termites Coptotermes curvignathus Holmgren (Isoptera:Rhinotermitidae) To Inhibition Damping-Off On Pine Seed (Pinus merkusii Jungh Et De Vriese), Seminar Nasional Masyarakat Peneliti Kayu (MAPEKI) VIII 3 – 5 September 2005 di Tenggarong, Kutai Kartanegara, Kalimantan Timur dengan judul: “Karakterisasi Eksudat Pertahanan Rayap Tanah Coptotermes curvignathus Holmgren (Isoptera:Rhinotermitidae) dan Seminar Nasional MAPEKI VII di Universitas Hasanuddin Makassar, 5 – 6 Agustus 2004, dengan judul “ Kajian Aktivitas Antimikroba Eksudat Rayap Tanah Coptotermes curvignathus Holmgren (Isoptera:Rhinotermitidae). Hasil penelitian juga telah diterima dan akan diterbitkan dalam Jurnal Teknologi Hasil Hutan Fakultas Kehutanan Institut Pertanian Bogor dengan judul : “Morphology of Subterrranean Termites Defense Glands of Coptotermes curvignathus Holmgren (Isoptera : Rhinotermitidae)”.
DAFTAR GAMBAR... i
DAFTAR TABEL... iii
DAFTAR LAMPIRAN... iv
PENDAHULUAN... 1
Latar Belakang... 1
Tujuan Penelitian... 3
Manfaat Penelitian... 3
Hipotesis………..………... 3
TINJAUAN PUSTAKA………...….... 4
Sistem Pertahanan Diri Rayap Tanah Coptotermes curvignathus... 4
Antimikroba………...……….………....…….... 7
Bakteri Escherichia coli...………...………... 9
Bakteri Staphylococcus aureus... 9
Cendawan Fusarium oxysporum... 10
Cendawan Rhizoctonia solani... 10
Purifikasi dan Identifikasi Kandungan Senyawa Aktif... 11
METODE PENELITIAN..…………...……….………... 13
Tempat dan Waktu Penelitian...………... 13
Bahan dan Alat Penelitian...……….…………... 13
Tahapan Penelitian………..……….. 14
HASIL DAN PEMBAHASAN... 31
Karakteristik Morfologi Prajurit Rayap C. curvignathus... 31
Karakteristik Anatomi Kelenjar Sekresi Pertahanan Prajurit Rayap C. curvignathus... 33
Karakterisasi Sekresi Pertahanan Rayap C. curvignathus... 39
Aktivitas Sekresi Rayap C. curvignathus Terhadap Semut O. denticulata... 44
Aktivitas Sekresi Rayap C. curvignathus Terhadap Bakteri Patogen E. coli dan S. aureus... 48
Aktivitas Sekresi Rayap C. curvignathus Terhadap Cendawan patogen... 56
Identifikasi Ekstrak Sekresi Pertahanan Rayap C. curvignathus... 65
KESIMPULAN DAN SARAN... 75
Kesimpulan... 75
Saran... 76
DAFTAR PUSTAKA………. 77
1 Tahapan Umum Pelaksanaan Penelitian... 15 2 Media pengujian toksisitas ekstrak sekresi pertahanan diri rayap
C. curvignathus terhadap Semut O. denticulata... 19 3 Media pengujian pertahanan diri rayap tanah C. curvignathus
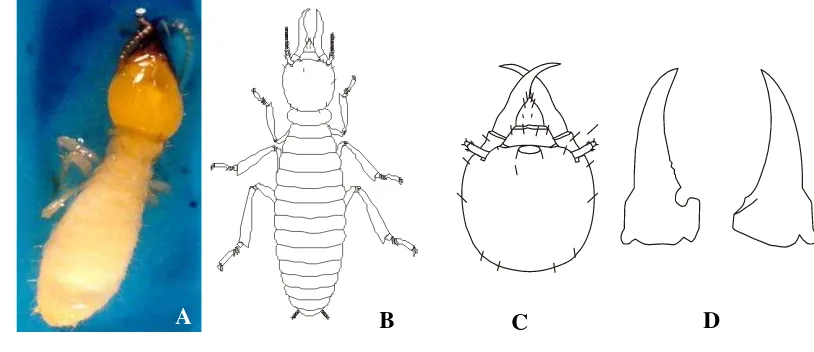
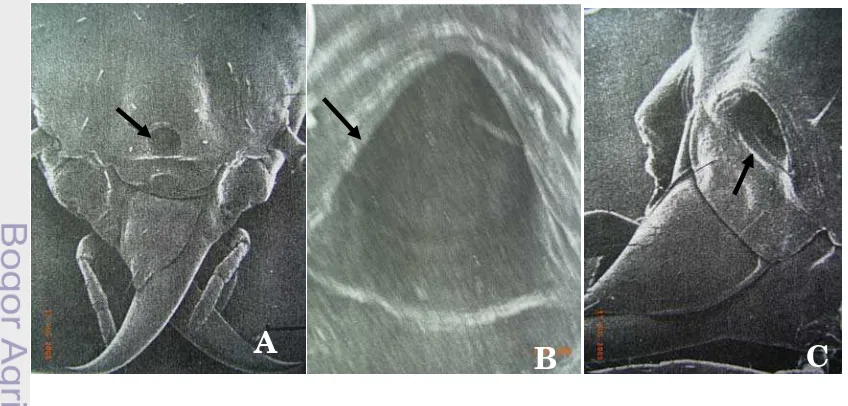
terhadap semut O. denticulata... 20 4 Kasta Prajurit (A,B), Bentuk Kepala (C), Bentuk Mandibel (D)
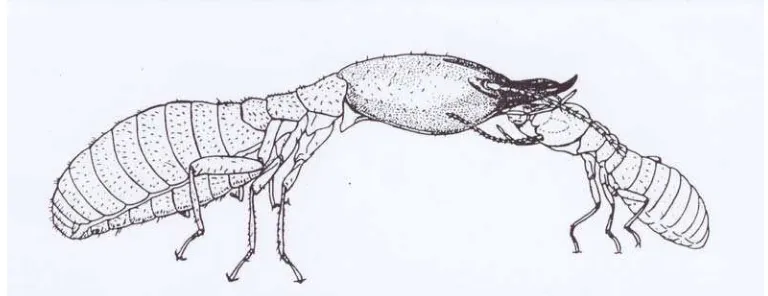
Rayap Tanah C. curvignathus... 31 5 Kasta pekerja rayap memberi makan kepada kasta prajurit
(Noirot, 1969)... 32 6 Kelenjar Frontal Kasta Prajurit Rayap Tanah C. curvignathus
(Perbesaran 40x)... 34 7 Lubang Fontanel Kasta Prajurit Rayap Tanah C. curvignathus
A :Perbesaran 100x B :Perbesaran 400x………... 34 8 Kelenjar Frontal Kasta Prajurit Rayap Tanah C. curvignathus
A :Perbesaran 100x B :Perbesaran 400x... 35 9 Kelenjar Sternal Kasta Prajurit Rayap Tanah C. curvignathus
Perbesaran 400x... 36 10 Kelenjar Frontal Kasta Prajurit Rayap C. lacteus
(Perbesaran 5.600x, Quennedey, 1998)... 37 11 Skema Letak Kelenjar Frontal Kasta Prajurit Rayap Tanah
C. curvignathus... 38 12 Lubang Fontanel Kasta Prajurit Rayap Tanah C. curvignathus... 38 13 Botol berisi ekstrak sekresi pertahanan rayap C. curvignathus... 41 14 Waktu kejadian kematian semut O. denticulata pertama
dalam media pengujian toksisitas sekresi pertahanan
rayap tanah C. curvignathus... 45 15 Waktu kematian seluruh semut O. denticulata dalam
media pengujian toksisitas sekresi pertahanan
rayap tanah C. curvignathus... 46 16 Semut O. denticulata (perbesaran 100x)... 46 17 Kasta prajurit rayap tanah C. curvignathus melakukan
penyerangan terhadap semut O. denticulata
dalam media pengujian... 47 18 Waktu kematian semut O. denticulata dalam media pengujian
pertahanan diri rayap C. curvignathus... 48 19 Area Penghambatan Pertumbuhan Bakteri S. aureus dan E.coli
oleh ekstrak Sekresi Pertahanan Rayap C. curvignathus... 50 20 Zona penghambatan pertumbuhan bakteri oleh ekstrak sekresi
pertahanan rayap C. curvignathus dalam berbagai pelarut... 51 21 Struktur dinding dan membran sel bakteri: (A) Gram Positif;
(B) Gram Negatif ; (C) Lapisan peptidoglikan
(Sumber : Cano dan Colome, 1986)... 52
22 Zona Penghambatan Pertumbuhan Bakteri S. aureus dan E. coli oleh Ekstrak Sekresi Rayap Dalam Pelarut Etanol Konsentrasi
0 – 70 persen (searah anak panah)……….. 53 23 Koloni cendawan F. oxysporum (A) dan R. solani (B) pada
media PDA (Potato Dextrose Agar)... 56 24 Pertumbuhan cendawan patogen F. oxysporum (A) dan
R. solani (B) pada media PDA yang ditambahkan ekstrak sekresi
pertahanan rayap tanah C. curvignathus konsentrasi 10%... 58 25 Pertumbuhan cendawan R. solani pada media PDA yang
ditambahkan ekstrak sekresi rayap C. curvignathus
dalam pelarut etil asetat... 59 26 Penghambatan pertumbuhan cendawan patogen R. solani
olehekstrak sekresi rayap tanah C. curvignathus
dalam pelarut etil asetat... 60 27 Pertumbuhan benih pinus yang dilapisi ekstrak sekresi rayap
C. curvignathus dalam pelarut etil asetat konsentrasi 8%... 61 28 Daya berkecambah benih pinus yang direndam selama satu jam
dalam ekstrak sekresi rayap C. curvignathus dalam pelarut
etil asetat konsentrasi 8% ... 62 29 Daya berkecambah benih pinus yang direndam dalam
ekstrak sekresi rayap tanah C. curvignathus dalam pelarut
etil asetat konsentrasi 8% ... 63 30 Serangan lodoh pada benih pinus yang direndam dalam
ekstrak sekresi rayap C. curvignathus dalam pelarut
etil asetat konsentrasi 8% ... 64 31 Kromatogram Komponen Bioaktif Ekstrak Sekresi Pertahanan
Rayap C. curvignathus Dalam PelarutEtanol... 65 32 Kromatogram Komponen Bioaktif Ekstrak Sekresi Pertahanan
Diri Rayap Tanah C. curvignathus Dalam Pelarut Etil Asetat... 66 33 Perbandingan Jumlah Komponen Dari Dua Pelarut Ekstrak
Sekresi Pertahanan Diri Rayap C. curvignathus... 67 34 Struktur Kimia Senyawa Pentadecanal... 68 35 Struktur Kimia Senyawa Tetradecanal... 68 36 Hubungan Evolusi Rayap Famili Rhinotermitidae Berdasarkan
Sekresi Kimia Pertahanan Diri Pada Subfamili Rhinotermitidae……... 73
1 Rendemen ekstrak sekresi pertahanan rayap C. curvignathus
pada empat pelarut yang berbeda... 36 2 Suhu, pH, viskositas dan warna ekstrak sekresi pertahanan
rayap C. curvignathus pada pelarut yang berbeda... 39 3 Konsentrasi hambat tumbuh minimal (MIC) ekstrak sekresi
rayap terhadap bakteri S. aureus dan E. coli serta perbandingannya terhadap ekstrak serangga
dan tumbuhan lainnya... 65
4 Klasifikasi Tingkat Aktivitas Anti Cendawan (AFA)... 74
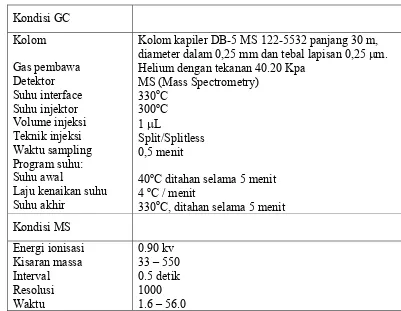
5 Kondisi GCMS merk Shimadzu QP 5050... 93
6 Komponen Ekstrak Sekresi Rayap C. curvignathus Dalam Pelarut Etanol... 95 7 Komponen Ekstrak Sekresi Rayap C. curvignathus
Dalam Pelarut Etil Asetat... 96 8 Komposisi Kimia Sekresi Pertahanan Diri Rayap
Dari Kelenjar Frontal Famili Rhinotermitidae
dan Termitidae... 99 9 Keragaman Sistem Pertahanan Diri Pada
Beberapa Serangga Sosial………... 106
1 Rata-rata waktu kematian semut O. denticulata dalam
pengujian ekstrak sekresi pertahanan diri rayap C. curvignathus dalam berbagai pelarut...…….…. 114 2 Rata-rata waktu kematian 2 ekor semut O. denticulata yang
diletakkan pada kelompok rayap C. curvignathus dengan
jumlah anggota kelompok yang berbeda... 114 3 Rata-rata area penghambatan pertumbuhan bakteri S. aureus
dan E. coli oleh ekstrak sekresi pertahanan diri rayap C. curvignathus (milimeter)... 114 4 Rata-rata area penghambatan pertumbuhan
bakteri S. aureus dan E. coli pada berbagai konsentrasi
ekstrak etanol(milimeter)... 115 5 Rata-rata penghambatan pertumbuhan cendawan
patogen R. solani dan F. oxysporum oleh ekstrak sekresi pertahanan diri rayap C. curvignathus pada
media PDA dengan konsentrasi 10%... 115 6 Rata-rata penghambatan pertumbuhan cendawan
patogen R. solani oleh ekstrak sekresi pertahanan diri rayap C. curvignathus dalampelarut etil asetat pada
media PDA dengan berbagai konsentrasi... 115 7 Analisis Ragam Pengaruh Perendaman Benih
Pinus merkusii Dalam Ekstrak Sekresi Rayap
Terhadap Daya Berkecambah Benih... 116 8 Analisis Ragam Pengaruh Perendaman Benih
Pinus merkusii Dalam Ekstrak Sekresi Rayap
Yang Ditanam Pada Media Dengan Cendawan Patogen
Terhadap Daya Berkecambah Benih... 116 9 Analisis Ragam Pengaruh Perendaman Benih
Pinus merkusii Dalam Ekstrak Sekresi Rayap
Yang Ditanam Pada Media Dengan Cendawan Patogen
Terhadap Serangan Penyakit Lodoh... 116
Sudah lebih dari seratus juta tahun serangga memiliki sistem pertahanan
kimiawi yang sangat unik. Pemangsa serangga harus berhadapan dengan sekresi
pertahanan diri yang disemprotkan oleh serangga ke tubuh pemangsa. Sekresi
pertahanan diri tersebut sangat beracun dan ada juga yang mengeluarkan bau
menyengat yang membuat pemangsa serangga menghindar. Serangga mengeluar-
kan sekresi pertahanan diri yang panas dan dapat membuat iritasi serta beracun.
Salah satu serangga yang memiliki sistem pertahanan kimiawi adalah rayap, yang
memiliki kelenjar penghasil sekresi pertahanan diri yang terletak pada abdomen
sebagai senjata untuk mempertahankan diri.
Sistem pertahanan kimia kasta prajurit rayap dalam menghadapi pemangsa
terdiri dari tiga sistem : pertama, gigitan terhadap bagian tubuh musuh, kemudian
menyemprotkan sekresi pertahanan diri yang dapat melumpuhkan musuh (oily
toxic); kedua, menyemprotkan sekresi pertahanan diri yang mengandung racun ke
permukaan tubuh pemangsa dengan menggunakan labrum; dan ketiga,
mengeluarkan sekresi pertahanan diri yang kental (glue-squirting poison) melalui
fontanel (Prestwitch 1984). Sekresi pertahanan diri yang disemprotkan kasta
prajurit rayap telah menarik perhatian beberapa ahli kimia karena kemampuannya
dalam melumpuhkan musuh dan pemangsa mereka. Beberapa penelitian mengenai
sekresi pertahanan diri kasta prajurit rayap telah dilakukan oleh Prestwich (1984)
pada genus Nasutitermes, Chuah, Goh dan Tho (1989) pada genus Nasutitermes,
Chuah dan Goh (1990) pada genus Hospitalitermes, Goh et al. (1990) pada genus
Laccessititermes, Roseangus dan Traniello (2001) pada genus Zootermopsis,
Lamberty et al. (2001) pada rayap P. spiniger, dan Da Silva et al. (2003) pada
genus Pseudacanthotermes. Hasil penelitian tersebut mengungkapkan bahwa
sekresi pertahanan diri dari fontanel kasta prajurit rayap memiliki senyawa
bioaktif yang berpotensi sebagai pestisida hayati yang mampu mematikan
pemangsa serta menghambat pertumbuhan bakteri dan cendawan.
Sementara itu, Pearce (1997) menyatakan bahwa sekresi pertahanan diri dari
fontanel kasta prajurit rayap mampu menghambat perkembangan dan
sebagai mekanisme pertahanan kimiawi terhadap berbagai jenis cendawan dan
bakteri patogen yang hidup bersama-sama dengan rayap tanah di bawah
permukaan tanah. Beberapa senyawa kimia yang diidentifikasi sebagai anti
predator dan patogen pada rayap tanah Nasutitermes trinervitermes adalah
trinervitene (Prestwich et al. 1976), tetracyclic diterpene pada rayap Longitermes
longipes, spinigerin pada rayap Pseudacanthotermes spiniger,17-O
-Acetoxy-(8,19)β,3α,7α, 9α,14α,17 – hexa hydroxyl trinervitene 2,3,9,14-O-tetrapropionate
pada rayap Hospitalitermes umbrinus, quinone, dan alkana pada rayap
Mastotermitidae (Pearce 1997) serta α-pinena, dan monocyclic lactone pada rayap
Termitidae (Lamberty et al. 2001).
Sementara itu, rayap tanah Coptotermes curvignathus yang penyebarannya
terbatas di daerah Asia Tenggara khususnya Indonesia dan Malaysia
menghasilkan sekresi pertahanan diri dalam jumlah yang lebih banyak dari rayap
tanah genus Hospitalitermes, Nasutitermes, dan Macrotermes. Namun hingga saat
ini pengamatan morfologi dan anatomi saluran penghasil sekresi pertahanan diri
kasta prajurit rayap, karakterisasi, dan pengujian aktivitas biologinya terhadap
semut pemangsa rayap, bakteri dan cendawan belum pernah dilakukan.
Penelitian pengembangan sekresi pertahanan diri kasta prajurit rayap sebagai
penghasil senyawa antimikroba masih sangat terbatas dibandingkan dengan
organisme penghasil senyawa antimikroba lain, seperti bakteri dan cendawan.
Bahkan jika dibandingkan dengan jenis serangga lain seperti; Sarcophaga
peregrina sebagai penghasil antimikroba sapecin (Yamada dan Natori 1993; Rao
1995); Hylophora cecropia sebagai penghasil cecropin; lebah madu (Apis
mellifera) penghasil apidacine (Casteels dan Tempst 1994) dan abaecin (Fujiwara
et. al. 1990); serta ulat sutera Bombyx mori sebagai penghasil lebocin (Hara dan
Yamakawa 1995). Oleh karena itu penelitian pengembangan senyawa antimikroba
dari sekresi pertahanan diri kasta prajurit rayap akan memberikan sumbangan
yang sangat berarti bagi pengembangan ilmu pengetahuan dan teknologi.
Berdasarkan pemikiran tersebut, penelitian mengenai karakterisasi sekresi
pertahanan diri kasta prajurit rayap C. curvignathus, morfologi dan struktur
anatomi saluran penghasil sekresi pertahanan diri, dan uji aktivitas biologinya
Tujuan Penelitian
1. Mengetahui morfologi dan struktur anatomi kelenjar frontal penghasil sekresi
pertahanan diri rayap tanah C. curvignathus.
2. Mengkarakterisasi sekresi pertahanan diri rayap tanah C. curvignathus
3. Mempelajari daya racun sekresi pertahanan diri rayap tanah C. curvignathus
terhadap semut pemangsa rayap, bakteri patogen dan cendawan penyebab
lodoh pada benih Pinus.
4. Mengetahui senyawa bioaktif yang terdapat pada sekresi pertahanan diri rayap
tanah C. curvignathus yang berperan dalam melumpuhkan semut pemangsa
rayap, serta menghambat bakteri patogen dan cendawan penyebab penyakit
lodoh.
Manfaat Penelitian
Manfaat penelitian ini adalah untuk memperoleh informasi ilmiah mengenai
sekresi pertahanan diri rayap tanah C. curvignathus yang diharapkan dapat
menjadi landasan pengetahuan untuk mengembangkan pestisida hayati dalam
mengendalikan semut, menghambat bakteri patogen serta mengatasi serangan
cendawan penyebab penyakit lodoh pada persemaian tanaman kehutanan.
Hipotesis
1. Kelenjar frontal yang menghasilkan sekresi pertahanan diri rayap tanah
C. curvignathus memenuhi hampir seluruh abdomen.
2. Ekstrak sekresi pertahanan diri rayap tanah C. curvignathus dapat mematikan
semut pemangsa rayap.
3. Ekstrak sekresi pertahanan diri rayap tanah C. curvignathus mempunyai
aktivitas antimikroba terhadap bakteri patogen.
4. Ekstrak sekresi pertahanan diri rayap tanah C. curvignathus dapat mencegah
serangan cendawan penyebab lodoh pada benih Pinus merkusii.
5. Senyawa bioaktif yang terdapat pada sekresi pertahanan diri rayap tanah
TINJAUAN PUSTAKA
Sistem Pertahanan Diri Rayap Tanah Coptotermes curvignathus
Rayap tanah telah memainkan peranan yang sangat penting dalam
lingkungan permukiman sebagai organisme pemakan material yang mengandung
lignoselulosa (bahan organik). Akibat aktivitas tersebut terjadi dekomposisi bahan
organik menjadi bahan-bahan anorganik.Rayap merupakan serangga sosial yang
hidup dalam satu koloni dengan organisasi individu yang secara morfologi
dibedakan menjadi bentuk dan kasta yang berlainan. Kasta yang terdapat di dalam
koloni rayap meliputi : kasta pekerja, kasta prajurit dan kasta reproduktif.
Masing-masing kasta melakukan fungsi yang berbeda satu dengan lainnya (Pearce 1997).
Krishna dan Weesner (1969) menyatakan rayap adalah serangga sosial yang
dapat diklasifikasikan ke dalam 6 famili yang meliputi: Mastotermitidae,
Kalotermitidae, Hodotermitidae, Rhinotermitidae, Serritermitidae dan Termitidae.
Rayap tanah Coptotermes termasuk ke dalam famili Rhinotermitidae sub famili
Coptotermitinae. Menurut Nandika et al. (2003), C. curvignathus merupakan
rayap tanah yang paling luas serangannya di Indonesia. Klasifikasi rayap tanah
C.curvignathus sebagai berikut:
Phylum : Arthropoda
Kelas : Insecta
Sub-klass : Pterigota
Ordo : Isoptera
Famili : Rhinotermitidae
Sub-famili : Coptotermitinae
Genus : Coptotermes
Spesies : Coptotermescurvignathus
Thapa (1981) menyatakan kasta prajurit rayap C. curvignathus memiliki
kepala bewarna kuning, antena, labrum dan pronotum kuning pucat. Bentuk
kepala hampir bulat dengan ukuran panjang sedikit lebih besar dari lebarnya,
memiliki fontanel yang lebih lebar. Antena rata-rata terdiri dari 15 segmen;
segmen kedua dan segmen ke empat sama panjangnya. Mandibel berbentuk
mandibel kanan sama sekali rata. Rata-rata panjang kepala tanpa mandibel lebih
kurang 1,56 mm – 1,68 mm. Lebar kepala lebih kurang 1,40 mm – 1,44 mm.
Bagian abdomen ditutupi rambut menyerupai duri, abdomen berwarna putih
kekuning-kuningan.
Menurut Borror dan De Long (1998) rayap hidup dalam kelompok sosial
dengan sistem kasta yang berkembang sempurna. Dalam koloni terdapat serangga
bersayap dan serangga tidak bersayap, ada juga yang hanya mempunyai tonjolan
sayap saja. Sayapnya berjumlah dua pasang yang menempel pada bagian toraks
dan berbentuk seperti selaput, dengan pertulangan sederhana dan reticulate.
Bentuk dan ukuran sayap depan sama dengan sayap belakang, dan oleh karena
itulah ordonya dinamai Isoptera (Iso = sama, ptera = sayap).
Kasta pekerja merupakan anggota yang sangat penting dalam koloni rayap.
Tidak kurang dari 80-90% populasi dalam koloni rayap merupakan
individu-individu kasta pekerja. Kasta pekerja umumnya berwarna pucat dengan kutikula
hanya sedikit mengalami penebalan sehingga tampak menyerupai nimfa. Kasta
reproduktif terdiri dari betina (ratu) yang tugasnya bertelur dan jantan (raja) yang
tugasnya membuahi betina. Kasta ini dibedakan menjadi kasta reproduktif primer
dan kasta reproduktif suplementer atau neoten. Kasta reproduktif primer terdiri
atas serangga-serangga dewasa yang bersayap dan merupakan pendiri koloni.
Menurut Richard dan Davies (1996) neoten muncul segera setelah kasta
reproduktif primer mati atau terpisah karena pemisahan koloni. Neoten dapat
terbentuk beberapa kali dalam jumlah yang besar sesuai dengan perkembangan
koloni. Selanjutnya, neoten menggantikan fungsi kasta reproduktif primer untuk
perkembangan koloni.
Kasta prajurit memiliki bentuk tubuh yang sangat spesifik dengan mandibel
yang berkembang sempurna. Kasta prajurit mampu menyerang musuhnya dengan
mandibel yang dapat menusuk, mengiris, dan menjepit. Peranan kasta prajurit
adalah melindungi koloni terhadap gangguan dari luar, khususnya semut dan
vertebrata predator. Biasanya gigitan kasta prajurit pada tubuh musuhnya sukar
dilepaskan sampai prajurit itu mati sekalipun. Kasta prajurit rayap tanah
C. curvignathus menyerang musuhnya dengan sekresi pertahanan diri yang
2003). Kasta prajurit mudah dikenal karena bentuk kepalanya yang besar dengan
sklerotisasi (penebalan) yang nyata. Anggota dari kasta ini mempunyai mandibel
atau rostrum yang besar dan kuat. Berdasarkan bentuk kasta prajuritnya, rayap
dibedakan atas dua tipe yaitu tipe mandibulate dan tipe nasuti. Pada tipe
mandibulate prajurit-prajuritnya mempunyai mandibel yang kuat dan besar tanpa
rostrum, sedangkan tipe nasuti prajurit-prajuritnya mempunyai rostrum yang
panjang tapi mandibelnya kecil.
Koloni rayap yang berada dalam kondisi bahaya karena serangan predator
(semut, trenggiling, dan lain-lain) akan segera memobilisasi kasta prajurit untuk
menyerang predator. Bentuk morfologi kasta prajurit sangat terspesialisasi untuk
bertahan dan menyerang musuh. Kasta prajurit rayap di Afrika memiliki mandibel
yang sangat tajam sehingga dapat menjepit musuh dan mematahkan tubuh
musuhnya. Sementara kasta prajurit rayap di Amerika Selatan memiliki mandibel
yang berukuran lebih panjang daripada abdomennya. Ketika menyerang musuh,
mereka akan menjepit musuhnya dengan menggunakan mandibel kemudian
mengeluarkan gas beracun untuk melumpuhkan musuh. Pada genus Nasutitermes
dan Coptotermes, kasta prajurit mengeluarkan sekresi pertahahan diri untuk
melumpuhkan musuhnya.
Trowell (2003) telah melakukan penelitian mengenai senyawa bioaktif yang
terdapat pada sekresi pertahanan diri kasta prajurit rayap genus Nasutitermes.
Hasil penelitiannya menyimpulkan bahwa terdapat tiga senyawa antimikroba yang
berpotensi sebagai antibakteri dan antibiotik dari kasta prajurit rayap tanah
Nasutitermes triodiae. Sementara hasil penelitian Lamberty et al. (2001) menye-
butkan terdapat dua senyawa antimikroba yang telah diekstraksi dari sekresi
pertahanan diri kasta prajurit rayap tanah Pseudacanthotermes spiniger, yang
selanjutnya diberi nama termicin dan spinigerin.
Prestwich et al. 1976 melakukan penelitian mengenai senyawa bioaktif yang
terdapat pada sekresi pertahanan diri kasta prajurit rayap tanah Nasutitermes
trinervitermes, dan menemukan bahwa terdapat senyawa kimia yang diidentifika-
si sebagai anti predator dan patogen yaitu trinervitene. Sementara Chuah dan Goh
(1990) menemukan senyawa bioaktif 17-O-Acetoxy-(8,19)β,3α,7α,9α,14α,17 –
kasta prajurit rayap Hospitalitermes umbrinus, dan Pearce (1997) menemukan
senyawa bioaktif quinone dan alkana pada sekresi pertahanan diri kasta prajurit
rayap Mastotermitidae.
Penelitian pengembangan sekresi pertahanan diri kasta prajurit rayap sebagai
penghasil senyawa antimikroba masih sangat terbatas dibandingkan dengan
organisme penghasil senyawa antimikroba lain, seperti bakteri dan cendawan.
Bahkan jika dibandingkan dengan jenis serangga lain seperti: Sarcophaga
peregrina sebagai penghasil antimikroba sapecin (Yamada dan Natori 1993; Rao
1995); Hylophora cecropia sebagai penghasil cecropin; lebah madu (Apis
mellifera) penghasil apidacine (Casteels dan Tempst 1994) dan abaecin (Fujiwara
et al. 1990); serta ulat sutera Bombyx mori sebagai penghasil lebocin (Hara dan
Yamakawa 1995). Oleh karena itu penelitian pengembangan senyawa antimikroba
dari sekresi pertahanan diri kasta prajurit rayap akan memberikan sumbangan
yang sangat berarti bagi pengembangan ilmu pengetahuan dan teknologi.
Antimikroba
Antimikroba adalah senyawa yang dapat menghambat pertumbuhan
mikroba, termasuk di dalamnya adalah antibakteri dan anticendawan. Antibakteri
adalah senyawa biologis atau kimia yang dapat menghambat pertumbuhan dan
aktivitas bakteri (Pelczar dan Chan 1988). Zat antibakteri dapat bersifat
bakterisidal (membunuh bakteri) dan bakteristatik (menghambat pertumbuhan
bakteri) (Frazier dan Westhoff 1988), sedangkan anticendawan adalah senyawa
biologis atau kimia yang dapat menghambat pertumbuhan dan aktivitas cendawan.
Beberapa faktor yang dapat mempengaruhi efektifitas antibakteri meliputi
jenis, jumlah, umur dan lingkungan bakteri; jumlah zat bakteri yang terdapat pada
bahan yang diekstraksi; sifat fisiko kimia substrat (jenis, pH, kadar air dan
senyawa-senyawa lainnya); waktu kontak antara dinding sel dengan zat anti-
bakteri serta suhu lingkungan dimana bakteri tumbuh (Frazier and Westhoff
1988). Beberapa antibakteri hanya mempunyai kemampuan mikrobiostatis
(menghambat pertumbuhan mikroba), sedangkan yang lainnya mempunyai
mikrobiostatis atau mikrobisida bergantung pada konsentrasi antibiotik (Singleton
dan Sainsburry 1978).
Konsentrasi terendah yang diperlukan untuk menghambat pertumbuhan
mikroba disebut konsentrasi hambat tumbuh minimal (KHTM / Minimal
Inhibitory Concentration (MIC)), sedangkan konsentrasi terendah yang tidak
menunjukkan pertumbuhan disebut konsentrasi pembunuhan minimal (KBM /
Minimal Cidal Concentration (MCC)).
Menurut Pelczar dan Chan (1988) ciri-ciri zat antibakteri yang ideal meliputi
substansi mampu membunuh/menghambat bakteri, substansi harus dapat larut
dalam air atau pelarut lain sampai pada taraf yang diperlukan, perubahan yang
terjadi pada substansi antibakteri selama penyimpanan harus seminimal mungkin
dan tidak boleh mengakibatkan kehilangan sifat antibakterinya dengan nyata,
tidak bersifat racun bagi manusia maupun hewan lain, komposisi harus seragam
sehingga bahan aktifnya selalu terdapat pada setiap penggunaan, tidak bereaksi
dengan bahan organik seperti protein atau bahan organik lainnya, menunjukkan
aktivitas yang baik pada suhu kamar atau suhu tubuh, mampu menembus dinding
sel, tidak menimbulkan karat dan warna, mampu menghilangkan bau yang kurang
sedap, mampu bertindak sebagai deterjen (desinfektan), tersedia dalam jumlah
besar dengan harga yang pantas.
Pengukuran adanya kekuatan antibakteri menurut Suriawiria (1978)
dipergunakan metode dari Davis Stout, dengan ketentuan daerah hambatan 20 mm
atau lebih (sangat kuat), daerah hambatan 10 mm – 20 mm (kuat), daerah hambatan 5 mm – 10 mm (sedang), daerah hambatan ≤ 5 mm (lemah). Banyak
faktor dan keadaan dapat mempengaruhi kerja antimikroba, antara lain:
konsentrasi atau intensitas antimikroba, kemasaman atau kebasaan (pH), jumlah
mikroorganisme, temperatur, spesies mikroorganisme dengan kerentanan yang
berbeda, dan adanya bahan organik asing (Pelczar dan Chan 1988). Komponen
antimikroba dapat menyebabkan kerusakan sel mikroba yang menyebabkan
kematian. Kerusakan yang ditimbulkan komponen antimikroba dapat bersifat
mikrosidal (kerusakan tetap) atau mikrostatik (kerusakan yang dapat kembali).
Suatu komponen akan bersifat mikrosidal atau mikrostatik tergantung pada
Bakteri Escherichia coli
Escherichia coli merupakan bakteri gram negatif, tidak mempunyai kapsul,
umumnya mempunyai fimbriae, bersifat motil atau non motil dengan flagella peri-
trikat, berukuran lebar 1 – 1,5 µm dan panjang 2 – 6 µm, bersifat fakultatif
anaerob, tunggal atau berpasangan, mempunyai suhu optimum pertumbuhan 37oC,
tetapi dapat tumbuh pada rentang suhu 15 - 45 oC. Nilai aw optimum adalah 0,96.
Bakteri ini sangat sensitif terhadap panas dan dapat diinaktifkan pada suhu
pasteurisasi atau selama pemasakan makanan (Willshaw et al. 2000 ; Supardi dan
Sukamto 1999). E. coli merupakan bakteri flora normal di dalam saluran
pencernaan hewan dan manusia, sehingga mudah mencemari air. Kontaminasi
bakteri ini pada makanan biasanya berasal dari kontaminasi air yang digunakan.
Dosis yang dapat menimbulkan gejala infeksi E.coli pada makanan berkisar antara
108 – 109 sel. Bahan makanan yang sering terkontaminasi oleh E coli antara lain
daging, ayam, ikan dan makanan hasil laut lainnya, telur dan produk olahannya,
sayuran, buah-buahan, sari buah serta susu (Supardi dan Sukamto 1999). E.coli
K1.1. merupakan bakteri E. colienteropathogenic (EPEC) yang dapat menyebab-
kan infeksi pada usus manusia. Bakteri ini telah memiliki ketahanan yang tinggi
dan bersifat resisten terhadap antibiotik penicilin.
Bakteri Staphylococcus aureus
Staphylococcus aureus termasuk famili Micrococcaceae, merupakan
bakteri Gram positif, berbentuk kokus yang terdapat dalam bentuk tunggal,
berpasangan, berkelompok seperti buah anggur. Kebanyakan galur S. aureus
bersifat patogen dan memproduksi enterotoksin yang tahan panas. Beberapa galur,
terutama yang bersifat patogen memproduksi koagulase, bersifat proteolitik,
lipolitik dan β-hemolitik. Bakteri ini sering terdapat pada pori-pori dan permukaan
kulit, kelenjar keringat dan saluran usus serta dapat menyebabkan intoksikasi dan
kelenjar infeksi bisul, pneumonia, dan mastitis pada hewan (Fardiaz 1983). Suhu
optimum untuk pertumbuhan bakteri S. aureus adalah 35 - 37oC, suhu minimum
6,7 oC dan suhu maksimum 45,5 oC. Bakteri S. aureus dapat tumbuh pada pH 4,0
– 9,8 dengan pH optimum sekitar 7,0 – 7,8. Pertumbuhan pada pH mendekati 9,8
pertumbuhannya (Supardi dan Sukamto 1999). Keracunan pangan stapilokokal
disebabkan oleh Staphylococci (khususnya bakteri S. aureus) yang tumbuh di
dalam bahan pangan dan membentuk enterotoksin sebagai produk metabolitnya.
Gejala-gejala keracunan yang ditimbulkan adalah mual, muntah, kram perut dan
diare. Gejala keracunan ini terjadi antara 1 – 8 jam (biasanya 2 – 4 jam) setelah
mengkonsumsi bahan pangan yang telah terkonta- minasi (Parker 2000).
Cendawan Fusarium oxysporum
Cendawan Fusarium oxysporum termasuk dalam genus Fusarium, famili
Tuberculariaceae, ordo Moniliales, kelas Deuteromycetes yang pada umumnya
memiliki miselia lembut, bersekat dan bercabang (Booth 1971; Dube 1983;
Alexopoulus et al. 1996). Karakteristik cendawan pada medium agar awalnya
miselium yang tumbuh berwarna putih halus seperti kapas dan kemudian
warnanya berubah menjadi ungu. Hifa berdiameter 2–4 μm, mikrokonidia berukuran 4-9 x 2-3 μm dan makro- konidia berukuran 20-29 x 4-5 μm, konidia hialin dengan diameter klamidospora berukuran 5-10 μm (Achmad 1997).
Fusarium merupakan salah satu cendawan penghuni tanah (soil inhabitant) yang
terdiri dari 40 macam spesies. F. oxysporum merupakan penyerbu tanah (soil
invaders) yang terdapat pada tanah-tanah tertentu dimana tersedia tanaman inang
yang cocok untuk kebutuhan hidupnya (Garret 1956 dalam Suharti et al. 1981).
Cendawan Rhizoctonia solani
Rhizoctonia solani merupakan cendawan yang menimbulkan penyakit lodoh
pada tanaman Pinus merkusii, termasuk dalam ’form ordo’ Agonomycetales
‘form-klas’ Deuteromycetes (Alexopoulus et al. 1996). Cendawan R. solani pada
media PDA mula-mula miselianya berwarna putih dan lama kelamaan berubah
menjadi coklat muda sampai tua. Miselia tersebut halus bercabang-cabang
membentuk jala halus dan bersepta. Jarak antar septanya relatif pendek.
Perkembangan miselianya memberikan tanda khas yaitu percabangan tegak lurus
(Von Arx 1981). Karakterisitik cendawan R. solani meliputi hifa vegetatif muda
berinti banyak (multinukleat), berwarna coklat, berdiamater hifa > 6 μm,
terdapat konstriksi (lekukan) pada hifa dan septa terbentuk dekat awal
percabangan hifa, terdapat septa dolipor, membentuk sklerotia yang tidak
beraturan bentuknya, tidak membentuk konidia tetapi membentuk sel-sel
monilioid, tidak terdapat sambungan apit dan tidak membentuk rhizomorf
(Achmad 1997).
Purifikasi dan Identifikasi Kandungan Senyawa Aktif
Metode analisis bahan aktif meliputi metode ekstraksi dan isolasi, metode
pemisahan, metode identifikasi dan analisis hasil (Harborne 1996). Prosedur yang
umum digunakan untuk ekstraksi dan isolasi senyawa aktif adalah pemisahan
berdasarkan kepolaran. Sifat polar pelarut akan menentukan jenis senyawa yang
terekstrak dari suatu bahan. Seringkali untuk mendapat senyawa yang diinginkan
digunakan beberapa pengekstrak secara bertingkat berdasarkan tingkat
kepolarannya. Tingkat kepolaran ini dikenal dengan deret eleutropi pelarut
(Gritter et al. 1991).
Pemisahan dan pemurnian kandungan bahan aktif tumbuhan terutama
dilakukan dengan menggunakan salah satu dari empat teknik kromatografi atau
gabungan teknik tersebut. Keempat teknik kromatografi tersebut adalah :
kromatografi kertas (KKt), kromatografi lapis tipis (KLT), kromatografi gas cair
(KGC) dan kromatografi cair kinerja tinggi (KCKT) (Harborne 1996). Untuk
mendapatkan senyawa murni dalam jumlah banyak maka digunakan kromatografi
kolom preparatif (Hostettmann et al. 1995).
Untuk penampakan hasil biasanya dilakukan revelasi kimia menggunakan
bahan kimia tertentu sedangkan untuk menentukan senyawa aktif yang bermanfaat
untuk tujuan tertentu digunakan metode bioautografi. Metode bioautografi hanya
menampakkan bagian yang aktif menghambat mikrob uji sedangkan bagian yang
tidak aktif tidak dapat dideteksi (Kim et al. 1991). Bioautografi dapat dilakukan
dengan dua cara yaitu secara langsung dan tidak langsung. Metode langsung
dilakukan dengan menaburkan atau menyemprotkan medium agar atau cair yang
telah berisi inokulum biakan bakteri uji diatas plat kromatogram yang berisi hasil
migrasi ekstrak kasar. Apabila senyawa aktif pada kromatogram menghambat
pertumbuhan bakteri uji maka akan tampak satu atau lebih zona bening pada plat
dengan bioautografi, revelasi kimia dapat menunjukkan semua macam kandungan
senyawa yang ada namun tidak dapat memilahkan yang aktif dan yang tidak aktif
(Wallhausser 1969). Selanjutnya setelah pemisahan senyawa aktif diikuti dengan
proses identifikasi. Identifikasi yang lengkap sampai ke dalam golongan senyawa
membutuhkan analisis beberapa sifat atau ciri yang kemudian dibandingkan
dengan data dari pustaka. Sifat yang diukur termasuk titik didih, titik leleh,
putaran optik dan nilai Rf. Tetapi apabila terdapat atau ditemukan data mengenai
senyawa dalam golongan yang sama maka yang perlu ditinjau lebih lanjut adalah
ciri dari senyawa tersebut berupa spektrumnya termasuk spektrum UV, Infra
merah (IM), resonansi magnet ini (RMI) dan spektrum massa (SM) (Harborne
METODE PENELITIAN
Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan pada bulan Juli 2003 sampai bulan Juli 2005 di
Laboratorium Bioteknologi Hewan, Pusat Studi Bioteknologi IPB; Laboratorium
Biologi Hasil Hutan Pusat Studi Ilmu Hayati IPB; serta Laboratorium Zoologi
Fakultas MIPA IPB.
Bahan dan Alat Penelitian
Bahan utama dalam penelitian ini adalah cairan sekresi pertahanan diri kasta
prajurit rayap tanah C. curvignathus. Rayap tanah C. curvignathus berasal dari
Hutan Percobaan Yanlappa Jasinga, Bogor yang telah dipelihara di Laboratorium
Biologi Hasil Hutan, Pusat Studi Ilmu Hayati IPB selama satu tahun (laboratory
reared termites colony). Pemeliharaan rayap dilakukan di dalam bak-bak plastik
berukuran 50 x 60 x 40 cm yang disimpan pada ruang gelap dengan kelembaban
udara berkisar antara 85%-90%.
Bahan kimia untuk ekstraksi sekresi pertahanan rayap tanah C. curvignathus
meliputi etanol, etil asetat, n-heksan, aquabidestilata dan gas nitrogen. Bahan
untuk analisis mikroba yaitu media tumbuh NA (Nutrient Agar), NB (Nutrient
Broth), Bacto Tryptone, Yeast extraxt, NaCl, Agar, NaOH, bakteri S. aureus dan
E. coli enteropatogen (EPEC) K1.1. yang diperoleh dari Laboratorium
Bioteknologi Hewan Pusat Penelitian Bioteknologi IPB. Bahan untuk analisis
cendawan yaitu media tumbuh PDA (Potato Dextrose Agar), cendawan
F. oxysporum dan R. solani yang diperoleh dari benih pinus dan tanah dari
pesemaian pinus PT. Perhutani Pompok Landak Cianjur, benih P. merkusii
diperoleh dari sumber benih di Ponorogo Jawa Timur yang, dipanen pada bulan
Juli 2004, tanah, pasir, clorox, dan jagung. Semut yang digunakan untuk
pengujian toksisitas ekstrak sekresi pertahanan diri rayap berasal dari arboretum
Fakultas Kehutanan IPB spesies O. denticulata. Bahan untuk pembuatan preparat
anatomi kelenjar penghasil sekresi pertahanan diri rayap tanah C. curvignathus
meliputi asam pikrat jenuh, asam asetat glasial, formalin, etanol 95%, Etanol 50%,
Etanol 70%, Etanol 80%, Etanol 90%, Etanol 95%, Etanol 100%, Xylol,
Alat yang digunakan untuk ekstraksi sekresi pertahanan diri rayap tanah
C. curvignathus meliputi alat-alat gelas, pipet pasteur, timbangan analitik,
desikator, dan lemari pendingin. Alat untuk identifikasi komponen senyawa aktif
yang terdapat pada sekresi pertahanan diri rayap tanah C. curvignathus meliputi
Gas Chromatography Mass Spectra (GC-MS). Alat untuk uji antimikroba
meliputi autoklaf, seperangkat peralatan gelas, timbangan analitik, inkubator
37oC, jarum ose, lampu spiritus dan shaker incubator. Alat untuk pembuatan
preparat anatomi kelenjar sekresi pertahanan diri rayap tanah C. curvignathus
mencakup gelas obyek, kaca penutup gelas obyek, dan mikroskop Scanning
Electron (SEM).
Tahapan Penelitian
Penelitian ini dilakukan dalam enam tahap kegiatan sebagai berikut :
Tahap I : Pembuatan preparat anatomi kelenjar frontal penghasil sekresi
pertahanan diri rayap tanah C. curvignathus.
Tahap II : 1. Koleksi sekresi pertahanan diri rayap tanah C. curvignathus.
2. Ekstraksi sekresi pertahanan diri rayap tanah C. curvignathus dengan
n-heksan, etil asetat, etanol dan aquabidestilata
3. Karakterisasi ekstrak sekresi pertahanan diri rayap tanah
C. curvignathus yang meliputi pengukuran pH, viskositas, dan suhu.
Tahap III : Pengujian toksisitas sekresi pertahanan diri rayap tanah
C. curvignathus terhadap semut O. denticulata
Tahap IV : Pengujian aktivitas antibakteri yang meliputi:
1. Perbanyakan kultur bakteri uji
2. Pengujian daya hambat pertumbuhan dengan metode sumur
3. Penentuan nilai konsentrasi daya hambat minimum (MIC)
Tahap V : Pengujian aktivitas anticendawan yang meliputi:
1. Perbanyakan kultur cendawan uji
2. Pengujian daya hambat pertumbuhan cendawan secara in-vitro
3. Uji fitotoksisitas ekstrak sekresi pertahanan diri rayap tanah
C. curvignathus pada benih P. merkusii.
Tahap VI: Penentuan senyawa bioaktif yang terdapat pada ekstrak sekresi
pertahanan diri rayap tanah C. curvignathus yang berperan sebagai
bahan repellen bagi semut pemangsa rayap, antibakteri dan
anticendawan dengan GCMS.
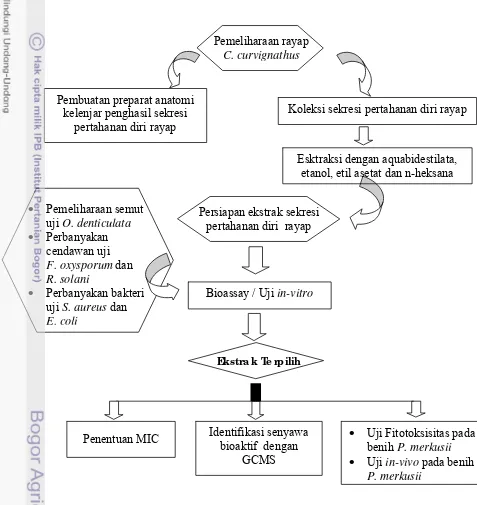
Pembuatan preparat anatomi kelenjar penghasil sekresi
pertahanan diri rayap
Bioassay / Uji in-vitro
Koleksi sekresi pertahanan diri rayap
Esktraksi dengan aquabidestilata, etanol, etil asetat dan n-heksana
Identifikasi senyawa bioaktif dengan
GCMS
Penentuan MIC • Uji Fitotoksisitas pada
benih P. merkusii
• Uji in-vivo pada benih
P. merkusii
Pemeliharaan rayap
C. curvignathus
• Pemeliharaan semut
uji O. denticulata
• Perbanyakan
cendawan uji
F. oxysporum dan
R. solani
• Perbanyakan bakteri
uji S. aureus dan
E. coli
Persiapan ekstrak sekresi pertahanan diri rayap
Ekstra k Te rp ilih
Metode kegiatan penelitian sebagai berikut:
1. Perbanyakan rayap tanah C. curvignathus
Rayap tanah C. curvignathus berasal dari Hutan Percobaan Yanlappa
Jasinga, Bogor yang telah dipelihara di Laboratorium Biologi Hasil Hutan,
Pusat Studi Ilmu Hayati IPB selama satu tahun (Laboratory reared termites
colony). Pemeliharaan rayap tanah C. curvignathus dilakukan di dalam
bak-bak plastik berukuran 50 x 60 x 40 cm yang disimpan pada ruang gelap
dengan kelembaban udara berkisar antara 85%-90%.
2. Pembuatan Preparat Gelas Obyek
Prosedur pembuatan preparat anatomi saluran kelenjar sekresi
pertahanan diri prajurit rayap tanah C. curvignathus sebagai berikut :
a. Rayap kasta prajurit C. curvignathus dicuci dengan NaCl fisiologis
selanjutnya difiksasi dengan larutan bovine selama 18 jam.
b. Spesimen direndam secara berurutan dalam larutan: Etanol 70% - etanol
80% - etanol 95% - etanol 100% (tahap dehidrasi) masing-masing selama
1 jam.
c. Spesimen kemudian direndam dalam campuran larutan etanol dan xylol
(1:1) selama 1 jam – xylol I selama 1 jam dan – xylol II selama 10 menit
(tahap dealkoholisasi).
d. Pada tahap xylol II, ke dalam wadah dimasukkan parafin sedikit demi
sedikit hingga jenuh; kemudian wadah dipindahkan ke dalam inkubator/
termostat pada suhu 57oC.
e. Kemudian berturut-turut dilakukan infiltrasi parafin I – parafin II dan
parafin III masing-masing selama 45 menit.
f. Pembuatan blok parafin (blocking) untuk penyelubungan spesimen.
Parafin murni dipanaskan kemudian dituang pada kotak karton tanpa tutup
yang tidak permanen. Setelah permukaan parafin mulai mengental,
spesimen diletakkan dengan posisi tegak di dalam parafin. Selanjutnya
karton parafin tersebut diletakkan pada permukaan air agar pendinginan
g. Pengirisan dengan mikrotom, dengan ketebalan 8 μm dan menghasilkan
pita-pita yang selanjutnya akan diletakkan pada permukaan gelas obyek
dengan perekat albumin. Gelas obyek kemudian diletakkan diatas pelat
pemanas pada suhu 30oC dan dibiarkan selama 24 jam.
h. Kemudian dilakukan pewarnaan yaitu dengan mencelupkan gelas obyek
secara berurutan ke dalam larutan berikut : Xylol I – Xylol II - Xylol III -
etanol 90% - etanol 80% - etanol 70% - etanol 50% (masing-masing
selama 5 menit) – hematoksilin aquosa– eosin 50% (masing-masing
selama 2 menit) - etanol 70% - etanol 80% - etanol 95% - etanol 100%
(masing-masing selama beberapa celup) – dibersihkan dengan tissu – xylol
I – xylol II (masing-masing selama 5 menit).
i. Gelas obyek selanjutnya dikeringudarakan, kemudian pada bagian
permukaan yang ada preparatnya diberi setetes balsam canada dan
dilekatkan gelas penutup diatasnya.
3. Pembuatan Gambar SEM
Prosedur pembuatan gambar SEM rayap tanah C. curvignathus sebagai
berikut : prajurit rayap tanah C. curvignathus dimasukkan ke dalam gelas kaca
kemudian dilakukan fresh-dry selama 48 jam untuk menghilangkan air dan
lemak yang terdapat di dalam tubuh rayap. Kemudian sampel direkatkan pada
aluminum stubs dan dilapisi dengan emas melalui proses vakum (6-7 Pa)
selama 20 menit dan diamati serta dibuat gambar SEM dengan menggunakan
mikroskop SEM JEOL 5310.
4. Koleksi sekresi pertahanan diri rayap tanah C. curvignathus
Koleksi sekresi pertahanan diri rayap tanah C. curvignathus dilakukan
berdasarkan metode Prestwich et al. (1984) dan Quintana et al. (2003) yang
dimodifikasi. Sekresi pertahanan diri rayap dikeluarkan dari fontanel prajurit
rayap dengan menggunakan pipet pasteur. Untuk setiap pelarut digunakan
cairan sekresi yang diambil dari 4000 ekor rayap. Pelarut untuk ekstraksi
meliputi aquabidestilata, etanol, etil asetat dan n-heksan, dengan demikian
menempel pada pipet pasteur dipindahkan ke dalam botol kaca dan
selanjutnya siap untuk diekstraksi.
5. Ekstraksi sekresi pertahanan diri rayap tanah C. curvignathus
Ekstraksi sekresi pertahanan diri rayap tanah C. curvignathus dilakukan
berdasarkan metode Preswitch et al. (1980) dan Chuah et al. (1990) yang
dimodifikasi. Sebanyak 10 ml aquabidestilata dicampurkan dengan sekresi
pertahanan diri rayap, kemudian dilakukan homogenisasi, dan selanjutnya
pelarut diuapkan dengan cara fresh-dry. Filtrat yang terjadi disimpan di dalam
botol kaca dan selanjutnya disimpan pada suhu –10oC dan siap digunakan
untuk pengujian bioassay.
Pada ekstraksi dengan pelarut organik, sekresi pertahanan diri rayap
dilarutkan ke dalam 10 ml pelarut etanol, kemudian dilakukan homogenisasi.
Selanjutnya pelarut diuapkan dengan ditiup gas nitrogen. Filtrat disimpan
dalam botol kaca dan selanjutnya disimpan pada suhu –10oC. Untuk
mendapatkan ekstrak dengan pelarut etil asetat dan n-heksan, dilakukan
perlakuan yang sama seperti pada perlakuan pelarut etanol.
6. Pengukuran karakteristik fisiko-kimia ekstrak sekresi pertahanan rayap
Karakterisasi fisiko-kimia ekstrak sekresi pertahanan diri rayap meliputi
pengukuran pH, suhu, warna, dan pengukuran viskositas berdasarkan metode
Nandika et al. (1994). Pengukuran viskositas ekstrak sekresi dilakukan dengan
viskometer mikro berdiameter 1 mm, dengan rumus :
1 poise = Berat (kg)
Panjang (m) x Waktu2 (S2)
7. Pengujian toksisitas sekresi pertahanan rayap C. curvignathus terhadap semut O. denticulata
Pengujian toksisitas ekstrak sekresi pertahanan rayap C. curvignathus
dilakukan berdasarkan metode Chen et al. (2002) yang dimodifikasi. Media
pengujian adalah sebuah cawan petri yang disajikan pada Gambar 2. Ekstrak
sekresi rayap sebanyak 200 μl diteteskan pada kertas saring steril yang
berukuran setengah lingkaran, kemudian kertas saring dikeringanginkan. Di
dalam cawan petri diletakkan dua kertas saring, satu kertas saring steril dan
semut O. denticulata diletakkan pada bagian tengah cawan petri. Pengamatan
meliputi waktu kejadian kematian semut pertama kali dan waktu kematian
semut mencapai seratus persen. Sebagai perlakuan kontrol adalah cawan petri
yang diletakkan dua kertas saring steril (tidak mengandung ekstrak sekresi
rayap) kemudian dimasukkan semut O.denticulata pada cawan petri.
Pengujian dilakukan dengan tiga kali ulangan.
Semut O. denticulata diperoleh dari arboretum Fakultas Kehutanan
Institut Pertanian Bogor. Klasifikasi semut O. denticulata sebagai berikut:
Phylum : Arthropoda
Kelas : Insecta
Ordo : Hymenoptera
Famili : Formicidae
Sub-famili : Ponerinae
Genus : Odontoponera
Spesies : Odontoponera denticulata
Gambar 2. Media pengujian toksisitas ekstrak sekresi pertahanan diri rayap
C. curvignathus terhadap Semut O. denticulata
Pengujian perilaku pertahanan diri rayap terhadap semut dilakukan
dengan meletakkan dua ekor semut O. denticulata pada kelompok rayap
berdasarkan metode Collins dan Prestwich (1983). Kelompok rayap diletakkan
pada sebuah cawan petri, yang disajikan pada Gambar 3. Tiga kelompok rayap
digunakan dalam pengujian meliputi kelompok pertama terdiri dari 20 ekor
kasta pekerja dan 20 ekor kasta prajurit, kelompok kedua terdiri dari 50 ekor
kasta pekerja dan 100 ekor kasta prajurit. Pengujian dilakukan dengan tiga
kali ulangan pada setiap kelompok rayap. Pengamatan dilakukan selama enam
jam sejak peletakan semut O. denticulata pada setiap kelompok rayap.
Gambar 3. Media pengujian pertahanan diri rayap tanah C. curvignathus
terhadap semut O. denticulata
8. Pengujian aktivitas antibakteri 8.1 Persiapan kultur bakteri uji
Bakteri yang digunakan adalah biakan murni bakteri Staphyloccus
aureus dan Eschericia coli enteropatogen K1.1. yang diperoleh dari
Laboratorium Bioteknologi Hewan Pusat Penelitian Bioteknologi IPB.
Komposisi medium padat untuk menumbuhkan bakteri terdiri dari : Bacto
Tryptone 1%, yeast extract 0,5 %, NaCl 1% dan Agar 1,5% dan diatur
pada pH 7,0 (netral). Inkubasi dilakukan pada suhu 370C.
8.2 Penentuan fase pertumbuhan akhir (late log phase) bakteri
Tahap ini bertujuan untuk menentukan late log phase bakteri.
Bakteri yang digunakan adalah E. coli dan S. aureus. Penentuannya
dilakukan dengan cara sebagai berikut : satu ose dari agar miring biakan
murni NA diinokulasikan ke dalam lima mililiter NB. Selanjutnya
diinkubasi selama 24 jam. Kultur yang telah 24 jam diambil sebanyak 10 μl dan dinokulasikan kembali ke dalam 10 mililiter NB. Selanjutnya
diinkubasi dan diamati pada jam ke-0, 8, 12, 16 dan 26 jam menggunakan
log phase untuk setiap bakteri dilakukan penghitungan sel menggunakan
alat hemasitometer.
8.3 Persiapan bakteri uji
Hasil late log phase untuk bakteri E.coli dan S. aureus ialah 16 jam.
Pada umur tersebut, jumlah bakteri telah mencapai 108 CFU/ml.
Konsentrasi bakteri yang digunakan untuk pengujian adalah106 CFU/ml.
8.4 Pengujian aktivitas antibakteri
Esktrak sekresi rayap disiapkan pada konsentrasi 40%. Ekstrak
sekresi dalam pelarut n-heksan (EN) diencerkan dengan air steril yang
berisi Tween 80 (0,5%), sedangkan ekstrak sekresi dalam pelarut etanol
(EE), etil asetat (EEA), aquabidestilata (EA) diencerkan dengan air steril
(aquabidestilata). Pengujian aktivitas antibakteri dilakukan menggunakan
difusi sumur berdasarkan Carson dan Riley (1995) sebagai berikut : Dari
persiapan kultur bakteri yang telah dilakukan, dipindahkan secara aseptik
sebanyak 20 μl ke dalam media NA 30 ml. Selanjutnya media dibiarkan
memadat, kemudian dibuat sumur dengan diameter 6 mm. Satu cawan
petri memiliki delapan sumur yang masing-masing diisi dengan EA, EE,
EEA, EN, dan pelarut ekstrak sebagai perlakuan kontrol (aquabidestilata, etanol, etil asetat, n-heksan) masing-masing sebanyak 60 μl. Selanjutnya
cawan petri diinkubasi selama 24 jam pada suhu 370C, Pengamatan zona
hambatan dilakukan dengan mengukur diameter zona bening (milimeter)
yang terbentuk di sekitar sumur. Pengujian dilakukan duplo.
8.5 Penentuan nilai konsentrasi hambat tumbuh minimal bakteri
(MIC / minimum inhibitory concentration)
Nilai MIC adalah konsentrasi terendah yang mampu mematikan
semua bakteri yang diinokulasikan ke dalam medium. Ekstrak yang
digunakan adalah ekstrak etanol, karena menghasilkan penghambatan
pertumbuhan tertinggi. Pengujian dilakukan berdasarkan metode difusi
sumur (Carson dan Riley, 1995). Konsentrasi esktrak etanol yang diuji
meliputi S. aureus dan E. coli. Penghitungan nilai MIC dilakukan
berdasarkan metode Bloomfield (1991), yaitu dengan memplotkan antara
ln Mo (konsentrasi ekstrak) pada sumbu X terhadap nilai kuadrat zona
penghambatan (X2) pada sumbu Y. Perpotongan antara kurva linier
dengan sumbu X merupakan nilai Mt (diperoleh dengan regresi linear).
Besarnya nilai MIC ditetapkan sebagai ¼ x Mt.
9. Pengujian aktivitas anticendawan
9.1 Penyediaan inokulum cendawan
Cendawan patogen penyebab lodoh didapatkan melalui isolasi dari
tanah pesemaian dan benih P. merkusii. Tanah pesemaian didapat dari
pesemaian pinus PT. Perhutani Pompok Landak Cianjur, sedangkan benih
pinus berasal dari Ponorogo Jawa Timur dengan daya berkecambah (DB)
70%.
Isolasi cendawan patogen dari tanah dilakukan dengan metode
pengenceran. Pengenceran yang digunakan adalah 10-2, 10-3, dan 10-4.
Sepuluh gram tanah yang berasal dari pesemaian pinus yang terserang
patogen disuspensikan dalam 90 ml aquadestilata steril sehingga
membentuk pengenceran 10-1. Suspensi tersebut dikocok dan dibiarkan
dalam beberapa menit. Pengenceran selanjutnya dilakukan dengan
mencampur sebanyak 1 ml suspensi pertama dengan 9 ml aquadestilata
steril sehingga membentuk pengenceran 10-2, cara yang sama dilakukan
untuk mendapatkan pengenceran 10-3 dan 10-4. Selanjutnya 0,1 ml
masing-masing suspensi tersebut ditumbuhkan pada media Martin Agar (MA) dan
diinkubasikan pada suhu kamar. Setelah patogen tumbuh, isolat
dimurnikan dan diuji patogenisitasnya.
Isolasi cendawan dari benih dilakukan dengan metode pengujian
kesehatan benih. Metode kesehatan benih yang digunakan adalah metode
blotter yang direkomendasikan oleh ISTA (International Seed Treatment
Association). Metode ini didasarkan pada pertumbuhan kecambah dan
propagul cendawan. Tiga helai kertas merang steril dilembabkan dengan