STUDI Q FEVER PADA TELUR AYAM DI WILAYAH
BOGOR DITINJAU DARI ASPEK KESEHATAN
MASYARAKAT VETERINER
TRIOSO PURNAWARMAN
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa disertasi Studi Q Fever pada Telur Ayam di Wilayah Bogor ditinjau dari Aspek Kesehatan Masyarakat Veteriner adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir disertasi ini.
Bogor, April 2011
ABSTRACT
TRIOSO PURNAWARMAN. Study of Q Fever in Chicken Eggs in Bogor Area : Veterinary Public Health’s Point of View. Under the direction of I WAYAN TEGUH WIBAWAN, FACHRIYAN HASMI PASARIBU and AGUS SETIYONO
Every year, Indonesia imports cattle and meat from Australia. Australia is the first country in the world where Query fever (Q fever) disease in abattoir workers was discovered and it is still endemic. Q fever is a disease that can be transmitted through food (foodborne disease) and it is categorized as zoonoses emerging infectious disease. This disease is caused by Coxiella burnetii (C. burnetii), which is an obligate intracellular pathogen, pleomorphic, resistant to physic-chemistry conditions and potentially used as biological weapons. Transmission to humans occurs through inhalation of dust particles from feces, urine and wool; direct infection from infected animals or tissues such as the rest of abortion, the placenta and the blood; and through the digestive tract from consuming unpasteurized milk and eggs.
This research was aimed (1) to know
C. burnetii was detected serologically and molecularly in Bali cattle, Brahman cross cattle, sheep and goats in the area of Bali and Bogor. Therefore, it is necessary to do a deeper study about its existence on chicken and eggs in Indonesia. This is important because the research results in Japan, Korea and the Philippines in 2003-2004 showed that 4.2% eggs were positive DNA C. burnetii.
the existence of the DNA of C. burnetii in eggs, (2) to know the relationship between the presence of C. burnetii with the characteristics of the farm environment (sanitation, personal hygiene and biosecurity), and (3) to determine the sensitivity and specificity of the nested polymerase chain reaction (nested PCR) method compared with PCR to detect the DNA of C. burnetii.
Qiao modified method for extracting DNA of C. burnetii in egg yolk is capable to produce a high concentration and high level of DNA purity.
Assessment of C. burneti DNA detection in 222 in commercial chicken eggs taken from sector 2 chicken farm and 130 local chicken eggs from sector 4 farm in Bogor area was done. The results shows that there wasn’t any C. burnetii DNA in 352 eggs sample which were tested with nested PCR method. It hadn’t been known the relation between farm environment (sanitation, personal hygiene and biosecurity) and the existence of the DNA of C. burnetii.
The sensitivity of nested PCR method to detect the DNA of C. burnetii reached the limit of detection up to 300 pg or it is 50 times more sensitive than PCR. In addition, PCR and nested PCR has high specificity (conserved) to detect C. burnetii. Two pairs of
primers OMP1-OMP2 and OMP3-OMP4 are highly sensitive and specific of 21 strains C. burnetii and have been used as diagnostic method for Q fever disease in humans.
The results of this study can be used as initial information about the presence of C. burnetii in eggs in Bogor area. In order to determine the infection of C. burnetii in chicken farms, it is necessary to conduct further research, both serological and molecular, in egg-producing regions throughout Indonesia. Further research should be conducted in other poultry eggs such as quail and duck eggs. Besides that, it is necessary to do C. burnetii surveillance in imported cows from Australia so that a guidance control system to face the entry of exotic zoonoses into Indonesia can be compiled.
Key words: Coxiella burnetii, Chicken eggs, sensitivity and specificity, nested polymerase chain reaction.
ditinjau dari Aspek Kesehatan Masyarakat Veteriner. Dibimbing oleh I WAYAN TEGUH WIBAWAN, FACHRIYAN HASMI PASARIBU dan AGUS SETIYONO
Setiap tahun Indonesia mengimpor sapi dan daging dari Australia. Australia merupakan negara pertama ditemukannya penyakit Query fever (Q fever) pada pekerja rumah potong hewan dan sampai sekarang masih bersifat endemik. Q fever merupakan salah satu penyakit yang dapat ditularkan melalui makanan (foodborne disease) dan dikategorikan sebagai emerging infectious disesase yang bersifat zoonosis. Penyakit ini disebabkan oleh Coxiella burnetii (C. burnetii) yang bersifat obligat patogen intraseluler, pleomorfik, tahan terhadap kondisi psikokimia dan berpotensi digunakan sebagai senjata biologis. Penularan ke manusia terjadi melalui inhalasi partikel debu yang berasal dari feses, urin dan wol yang terinfeksi; kontak langsung dari hewan atau jaringan terinfeksi seperti sisa abortus, plasenta dan darah serta melalui saluran pencernaan karena mengkonsumsi susu dan telur yang tidak dipasteurisasi.
Orang yang terinfeksi penyakit Q fever akan memperlihatkan gejala klinis seperti flu (flu like syndrome), pneumonia dan hepatitis. Apabila tidak segera diobati dengan baik sekitar 2-10% akan menjadi endokarditis. Kematian pada kasus kronis dapat mencapai 25-65%, sehingga dari kesehatan masyarakat veteriner perlu mendapatkan perhatian yang serius.
C. burnetii sudah terdeteksi secara serologis dan molekuler pada sapi bali, sapi brahman cross, domba dan kambing di wilayah Bali dan Bogor, maka perlu dilakukan studi lebih mendalam tentang keberadaannya pada ayam dan telur di Indonesia. Hal ini penting karena dari hasil penelitian di Jepang, Korea dan Pilipina pada tahun 2003-2004 menunjukkan 4.2% positif DNA C. burnetii pada telur. Di Indonesia, telur merupakan sumber protein hewani yang mempunyai nilai gizi yang tinggi, harganya terjangkau dan gemar dikonsumsi dalam keadaan mentah atau setengah matang.
Penelitian ini dilakukan untuk (1) mengetahui keberadaan DNA C. burnetii pada telur, (2) mengetahui hubungan keberadaan C. burnetii dengan karakteristik lingkungan peternakan (sanitasi, higiene personal dan biosekuriti), serta (3) mengetahui sensitivitas dan spesifisitas metode nested polymerase chain reaction (nested PCR) dibandingkan dengan PCR untuk mendeteksi DNA C. burnetii.
Modifikasi metode Qiao untuk mengekstraksi DNA C. burnetii pada kuning telur mampu menghasilkan konsentrasi dan tingkat kemurnian DNA yang tinggi.
Kajian dilakukan untuk mendeteksi DNA C. burnetii pada 222 butir telur ayam ras yang diambil dari peternakan ayam sektor 2 dan 130 butir telur ayam lokal dari peternakan sektor 4 di wilayah Bogor. Hasil deteksi menunjukkan tidak ditemukan DNA C. burnetii pada 352 sampel telur yang diuji dengan metode nested PCR dan belum dapat diketahui hubungan antara karakteristik lingkungan (sanitasi, higiene personal dan biosekuriti) dengan keberadaan DNA C. burnetii.
Sensitivitas metode nested PCR untuk mendeteksi DNA C. burnetii mencapai limit deteksi hingga ≥ 300 pg atau 50 kali lebih sensitif dibandingkan PCR. Selain itu PCR dan nested PCR mempunyai spesifisitas yang tinggi (conserved) untuk mendeteksi C. burnetii. Dua pasang primer OMP1-OMP2 dan OMP3-OMP4 sangat sensitif dan spesifik terhadap 21 strain C. burnetii dan sudah digunakan sebagai metode diagnosa untuk penyakit Q fever pada manusia.
maupun molekuler di wilayah-wilayah penghasil telur di seluruh Indonesia dan juga mendeteksi pada telur unggas lainnya seperti telur burung puyuh dan bebek. Disamping itu perlu dilakukan surveilans C. burnetii terhadap sapi-sapi impor asal Australia sehingga dapat disusun pedoman sistim pengendalian menghadapi masuknya penyakit zoonosa baru ke Indonesia.
© Hak Cipta milik IPB, tahun 2011
Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau
menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian,
penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu
masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB.
Dilarang mengumumkan atau memperbanyak sebagian atau seluruh karya tulis dalam
STUDI Q FEVER PADA TELUR AYAM DI WILAYAH
BOGOR DITINJAU DARI ASPEK KESEHATAN
MASYARAKAT VETERINER
TRIOSO PURNAWARMAN
DISERTASI
Sebagai salah satu syarat untuk memperoleh gelar
Doktor pada
Program Studi Sains Veteriner
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Penguji luar komisi pada ujian tertutup : Prof. Dr. drh. Retno D. Soejoedono, MS
Dr. drh. Denny Widaya Lukman, M.Si
Penguji luar komisi pada ujian terbuka : drh. Pudjiatmoko, Ph.D
Prof. Dr. drh. Hj. Mirnawati Sudarwanto
Judul Disertasi
:
Studi Q Fever pada Telur Ayam di Wilayah Bogor ditinjau dari Aspek Kesehatan Masyarakat VeterinerNama : Trioso Purnawarman
NRP : P18600004
Disetujui
Komisi Pembimbing
Ketua
Prof. Dr. drh. I Wayan Teguh Wibawan, MS
Prof. Dr. drh. Fachriyan Hasmi Pasaribu
Anggota Anggota
drh. H. Agus Setiyono, MS, Ph.D
Diketahui
Ketua Program Studi Sains Veteriner Dekan Sekolah Pascasarjana IPB
Prof. drh. Bambang Pontjo P., MS, Ph.D Dr. Ir. Dahrul Syah, M.Sc, Agr
hidayahNya sehingga disertasi ini dapat diselesaikan. Penelitian ini bertujuan untuk
mengetahui keberadaan mikroorganisma patogen pada pangan asal hewan, khususnya
telur yang dapat mempengaruhi keamanan pangan bagi kesehatan masyarakat dengan
topik Q Fever pada Telur Ayam di Wilayah Bogor yang belum pernah diteliti di Indonesia.
Coxiella burnetii (C. burnetii) sebagai penyebab Q fever merupakan salah satu potensi
ancaman besar bagi kesehatan masyarakat veteriner di Indonesia.
Penulis mengucapkan terima kasih yang sebesar-besarnya kepada Prof. Dr. drh.
I Wayan Teguh Wibawan, MS, Prof. Dr. drh. Fachriyan Hasmi Pasaribu dan drh. H. Agus
Setiyono, MS, Ph.D selaku pembimbing yang telah memberi perhatian, semangat serta
dorongan kepada penulis. Kepada Prof. Dr. drh. Hj. Mirnawati Sudarwanto yang telah
membantu memberikan DNA C. burnetii Nine Mile 2 ATCC (NM2) dan masukan
perbaikan metode ekstraksi dalam penelitian ini. Terima kasih juga disampaikan kepada
Dr. Muharam Saepulloh yang telah membantu penelitian dan Dr. Ir. Etih Sudarnika, M.Si
yang memberikan jurnal-jurnal untuk melengkapi disertasi ini. Kepada Prof. drh.
Bambang Pontjo P. MS, Ph.D selaku ketua program studi Sains Veteriner FKH IPB, Prof.
Dr. drh. Retno D. Soejoedono, MS dan Dr. drh. Denny Widaya Lukman, M.Si sebagai
penguji luar komisi pada ujian tertutup serta drh. Pudjiatmoko, Ph.D dan Prof. Dr. drh. Hj.
Mirnawati Sudarwanto sebagai penguji luar komisi pada ujian terbuka. Kepada para
kolega staf pengajar dan laboran di Bagian Kesehatan Masyarakat Veteriner FKH IPB;
staf dan laboran di Laboratorium Terpadu FKH IPB; staf dan laboran di Laboratorium
Terpadu Departemen Ilmu Penyakit Hewan dan Kesehatan Masyarakat Veteriner FKH
IPB; staf dan laboran di Balai Besar Penelitian Veteriner serta para peternak ayam di
wilayah Bogor yang telah membantu penelitian ini. Terima kasih dan penghargaan
penulis sampaikan pula kepada kedua orang tua, mertua, drh. Rosy Roselina, Roby
Raditia Aryoputranto dan Renardi Purnama Putra, atas perhatian, nasehat serta doanya
selama ini.
Semoga tulisan ini dapat bermanfaat sebesar-besarnya bagi kesejahteraan dan
kesehatan masyarakat.
Bogor, April 2011
RIWAYAT HIDUP
Penulis adalah anak ketiga dari empat bersaudara putra Bapak Bambang
Soeletter dan Ibu Sri Hartini serta dilahirkan di Balikpapan pada tanggal 5 Oktober 1962.
Pendidikan dasar sampai menengah atas dijalani di Sekolah Dasar di Palembang
Sumatera Selatan tahun 1968-1974, Sekolah Menengah Pertama Perguruan Cikini
Jakarta tahun 1975-1977 dan Sekolah Menengah Atas Negeri 9 Jakarta tahun
1978-1981. Penulis menyelesaikan studi dokter hewan dari Fakultas Kedokteran Hewan
Institut Pertanian Bogor pada tahun 1986. Pada tahun 1986-1988 penulis bekerja pada
perusahan perunggasan nasional di sektor pembibitan ayam sebagai manajer produksi.
Sejak tahun 1988 diangkat sebagai staf pengajar di Bagian Kesehatan Masyarakat
Veteriner, Departemen Ilmu Penyakit Hewan dan Kesehatan Masyarakat Veteriner FKH
IPB. Penulis melanjutkan pendidikan program Magister Sains (Strata 2) di program
pascasarjana IPB bidang Kesehatan Masyarakat Veteriner (KMV) pada tahun 1990-1994.
Sejak tahun 2000 melanjutkan pendidikan program Doktor (Strata 3) di Sekolah
Pascasarjana IPB bidang Sains Veteriner (SVT).
Penulis aktif dalam berbagai kegiatan organisasi selama menjadi siswa di sekolah
menengah sampai mahasiswa di perguruan tinggi. Setelah lulus dokter hewan bergabung
pada Perhimpunan Dokter Hewan Indonesia dan Perhimpunan Mikrobiologi Indonesia.
Pada tahun 1999-2002 menjadi Sekretaris Jenderal Forum Komunikasi Kesehatan
Masyarakat Veteriner (Forkom Kesmavet) dan tahun 2002-2006 menjadi koordinator
komisi sanitasi lingkungan, Asosiasi Kesehatan Kesehatan Masyarakat Veteriner
(Askesmaveti). Pada tahun 2006 sampai sekarang sebagai anggota panitia teknis 67-03
bidang peternakan dan produk peternakan, Direktorat Jenderal Peternakan dan
Kesehatan Hewan, Kementerian Pertanian, Republik Indonesia serta pada tahun 2010
sampai sekarang sebagai koordinator bidang organisasi Masyarakat Ilmu Perunggasan
Indonesia (MIPI).
Beberapa tulisan yang telah dan akan diterbitkan pada beberapa jurnal nasional
antara lain tingkat kejadian residu formalin pada daging ayam yang dijual di pasar
tradisional di kota Bogor pada Jurnal Medis Veteriner Indonesia serta sensitivitas dan
spesifisitas nested polymerase chain reaction untuk mendeteksi DNA Coxiella burnetii
DAFTAR TABEL.………... xiv
DAFTAR GAMBAR.………
DAFTAR LAMPIRAN………..
xv
xvi
PENDAHULUAN.……… 1
TINJAUAN PUSTAKA
Q Fever.………...
Morfologi dan Karakteristik Coxiella burnetii..……….. Diagnosa Penyakit Q Fever………....
Q Fever pada Hewan.………... Epidemiologi dan Penyebaran Penyakit..………. Patogenesis Q Fever..………. Gejala Klinis.……….
Q Fever pada Manusia.……… Epidemiologi dan Distribusi Penyakit……… Q Fever Sebagai Food-borne Disease………. Gejala Klinis.………. Pengendalian.………...
Q Fever di Indonesia ………...
BAHAN DAN METODE
Waktu dan Tempat Penelitian ………. Tahapan Penelitian ………...
5 5 8 11 11 12 12 13 13 15 16 16 19 20 20
DETEKSI Coxiella burnetii PADA TELUR AYAM RAS DAN LOKAL DI
WILAYAH BOGOR DENGAN METODE NESTED POLYMERASE CHAIN REACTION
Abstrak ………
Abstract ………...
Pendahuluan ……….. Bahan dan Metode ……… Hasil dan Pembahasan ……… Kesimpulan dan Saran ……….
25 25 25 27 31 34
SENSITIVITAS DAN SPESIFISITAS NESTED POLYMERASE CHAIN REACTION UNTUK MENDETEKSI DNA Coxiella burnetii
Abstrak ………
Abstract ………...
Pendahuluan ……….. Bahan dan Metode ……… Hasil dan Pembahasan ……… Kesimpulan ……….
PEMBAHASAN UMUM ……….
KESIMPULAN DAN SARAN
Kesimpulan.………. Saran.………...
DAFTAR PUSTAKA.………...
LAMPIRAN.………..
Halaman
50 50
51
1 Permintaan dan penyediaan daging serta impor sapi bakalan ………..
1
2 Pengobatan Q fever pada manusia……….17
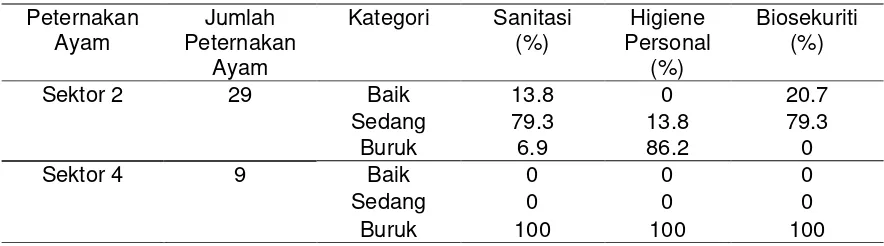
3 Kriteria peternakan ayam………..
33
4 Gambaran sanitasi, higiene personal dan biosekuriti di peternakan ayam
sektor 2 dan sektor 4………..
33
5 Perbandingan sensitivitas PCR dan nested PCR dalam mendeteksi DNA
DAFTAR GAMBAR
Halaman
1 Filogenik C. burnetii berdasarkan analisa sekuen 16S rRNA……….
5
2 C. burnetii dengan mikrograf elektron pada pembesaran 75 000 kali……...
6
3 Antigen fase I dan fase II C. burnetii………..
7
4 Mekanisme infeksi dan gejala penyakit Q fever pada manusia……….
17
5 Tahapan penelitian studi Q fever pada ayam di wilayah Bogor.………
20
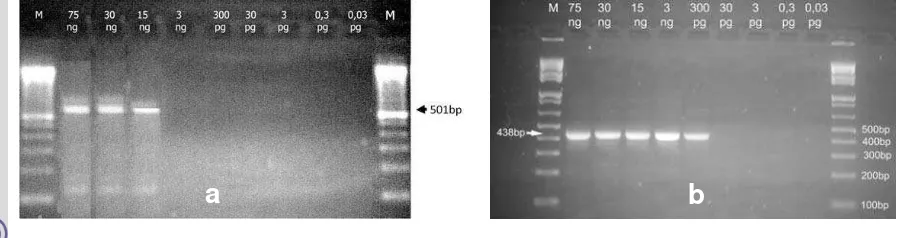
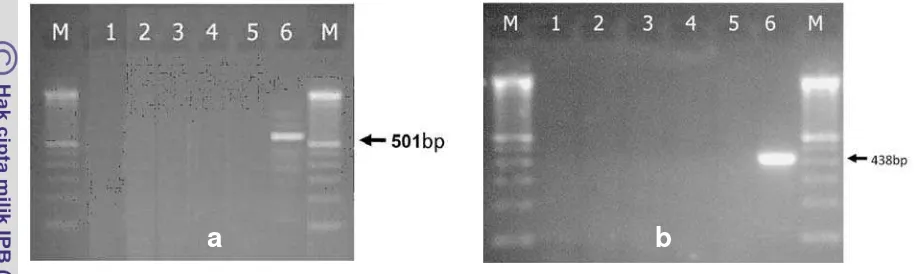
6 Hasil deteksi DNA C. burnetii dengan elektroforesis………...
31
7 Sensitivitas PCR dan nested PCR menggunakan konsentrasi DNA C. burnetii 75 ng/ µl sampai dengan 0.03 pg/µl.………
40
1 Asal sampel telur ayam ras yang berasal dari kabupaten Bogor………..
59
2 Asal sampel telur ayam lokal yang berasal dari kabupaten dankota Bogor...
59
3 Hasil uji nested PCR telur ayam ras yang berasal dari kabupaten Bogor……60
4 Hasil uji nested PCR telur ayam lokal yang berasal dari kabupaten dankota Bogor………..
61
5 Kuesioner untuk peternak………
62
6 Pengelompokan dan pembobotan faktor-faktor yang mempengaruhi
sanitasi, higiene personal dan biosekuriti di peternakan……….
64
7 Skoring (penilaian) faktor-faktor yang mempengaruhi sanitasi, higienePENDAHULUAN
Perkembangan perekonomian Indonesia dewasa ini semakin baik, sehingga permintaan terhadap bahan pangan asal hewan yang aman (safe) dan layak (suitable) juga meningkat. Hal ini dapat dilihat dengan permintaan daging
sapi empat tahun terakhir meningkat sebesar 10.7%, yaitu dari 356 863 ribu ton
pada tahun 2006 menjadi 399 535 pada tahun 2009. Untuk memenuhi
permintaan tersebut, maka impor sapi bakalan meningkat 24.1% dari 218 408
ekor pada tahun 2006 menjadi 271 043 ekor pada tahun 2009. Data
menunjukkan bahwa Indonesia mengimpor sapi rata-rata 650 000 ekor per
tahun yang sebagian besar berasal dari Australia (Apfindo 2010).
Perkembangan permintaan dan penyediaan daging serta impor sapi bakalan
selama empat tahun terakhir disajikan pada Tabel 1.
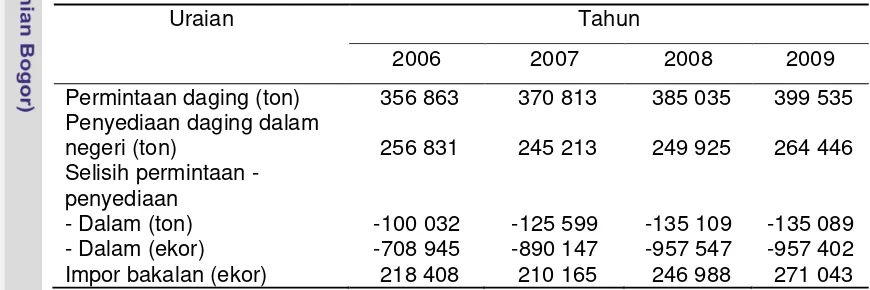
Tabel 1 Permintaan dan penyediaan daging serta impor sapi bakalan (Apfindo 2010)
Uraian Tahun
2006 2007 2008 2009
Permintaan daging (ton) Penyediaan daging dalam negeri (ton)
Selisih permintaan -penyediaan
- Dalam (ton) - Dalam (ekor)
356 863 256 831 -100 032 -708 945 370 813 245 213 -125 599 -890 147 385 035 249 925 -135 109 -957 547 399 535 264 446 -135 089 -957 402 Impor bakalan (ekor) 218 408 210 165 246 988 271 043
Australia merupakan negara asal dan pertama ditemukannya Query fever (Q fever) pada pekerja rumah potong hewan di Brisbane pada tahun 1935 (Acha
dan Szyfres 2003). Sapi bakalan yang di impor dalam jumlah yang banyak, akan
menyebabkan masuknya penyakit baru (eksotik) yang dapat menular pada
hewan dan manusia ke Indonesia.
1977 Q fever termasuk kategori penyakit yang harus dilaporkan (notifiable disease), sedangkan di Amerika Serikat baru di mulai tahun 1999 (CFSPH
2007). Penyakit ini dapat pada manusia ditularkan melalui inhalasi partikel debu
(feses, urin, wol), kontak langsung (plasenta, sisa obortus), makanan (susu, telur)
dan air yang terkontaminasi 1-10 organisme (ID50, yaitu apabila orang terinfeksi
1-10 mikroorganisme Coxiella burnetii, maka 50% dari orang tersebut akan
menunjukkan gejala penyakit) (Acha dan Szyfres 2003; Anonim 2003).
Laporan World Health Organization (WHO) menyatakan bahwa pada
tahun 1955 Q fever pertama kali ditemukan di Indonesia pada 188 serum sapi
yang diperiksa secara serologis positif mengandung antibodi C. burnetii
menggunakan metode cappilary tube agglutination test (CAT) (Kaplan dan
Bertagna 1955). Penelitian berikutnya dilakukan Rumawas (1976) menunjukkan
bahwa dari 323 sampel darah sapi yang diambil dari Bogor, Bandung, Surabaya
dan Semarang ditemukan 4 sampel (1.2%) positif antibodi terhadap Q fever menggunakan metode CAT. Vanpeenen et al. (1978) juga melakukan penelitian
penyakit Q fever pada pekerja di Indonesia secara seroepidemilogi. Hasil
penelitian yang dilakukan Ibrahim et al. (1999) memperoleh 20.8-51.9% positif antibodi terhadap spotted fever, 38% positif murine typhus, tetapi tidak menemukan Q fever pada serum tikus liar menggunakan metode indirect immunoflourescent antibody (IFA) di Jakarta dan Boyolali.
Penelitian selanjutnya dilaporkan Miyashita et al. (2001) pada kasus
pneumonia yang diderita oleh seseorang yang pernah tinggal di Indonesia dan
ditemukan positif terinfeksi C. burnetii. Hasil seroprevalensi Q fever di Bogor
pada domba dan kambing menunjukkan masing-masing sebesar 31.88% dan 20.29% menggunakan metode IFA, sedangkan dengan metode nested polymerase chain reaction (nested PCR) terhadap 245 ekor sapi bali dan brahman cross ditemukan 15 ekor (6.12%) positif DNA C. burnetii serta pada
165 ekor kambing dan domba ditemukan 6 ekor (3.64%) positif DNA C. burnetii
di Bali dan Bogor (Mahatmi 2006).
Penyakit Q fever pada sapi, kambing dan domba sudah ditemukan
di Indonesia, maka kemungkinan penyebaran penyakit ini pada hewan lainnya
termasuk unggas, dapat terjadi. Penularan dari hewan ke hewan, baik antara
3
(Stomoxis sp., Musca sp.) yang bertindak sebagai vektor (Acha dan Szyfres 2003; Maurin dan Raoult 1999; Norlander 2000; Sonenshine et al. 2002).
Penyebaran penyakit Q fever dipermudah akibat penataan wilayah
subsektor peternakan di Indonesia yang masih belum tertata dengan baik. Di
beberapa wilayah di Indonesia, lokasi peternakan sapi, domba dan kambing
berdekatan dengan peternakan unggas, sehingga memudahkan terjadinya
penularan penyakit Q fever melalui kontak langsung, aerosol, maupun melalui
vektor. Penataan peternakan dalam satu wilayah harus tetap memperhatikan sistem pemisahan (zoning) dan jarak antara satu peternakan dengan peternakan lainnya untuk setiap jenis ternak.
Studi seroepidemiologi Q fever menggunakan metode CAT terhadap 25 peternakan ayam di distrik Nainital dan Ajmer, di negara bagian Uttar Pradesh
dan Rajasthan, India, ditemukan 78 sampel (13.24%) positif antibodi Q fever dengan titer 8 sampai 64. Ayam petelur atau layer (umur lebih dari 6 bulan) lebih
tinggi persentase positifnya dibandingkan dengan ayam grower, yaitu 19.74% :
5.55%. Selain itu dilaporkan bahwa pada pekerja peternakan ayam tersebut ditemukan positif antibodi Q fever sebesar 27.52% dengan metode CAT (Rarotra et al. 1978). Hasil penelitian To et al. (1998) menemukan 2% positif titer antibodi C. burnetii menggunakan metode CAT dan 1.1% positif DNA C. burnetii menggunakan metode nested PCR pada ayam di wilayah Fukuoka Jepang. Penelitian yang sama juga dilakukan pada peternakan ayam di Jepang bagian
tengah (Aichi, Shizuoka, Mie dan Gifu), didapatkan 7% positif antibodi IgG terhadap C. burnetii, dengan titer berkisar antara 16 sampai dengan 64 dengan metode IFA, tetapi dengan metode nested PCR tidak ditemukan DNA C. burnetii (Muramatsu et al. 2006).
Hasil penelitian pada telur ayam yang dilakukan di Jepang, Korea dan
Filipina menunjukkan bahwa dari bulan Juli 2003 sampai dengan Juni 2004
didapatkan 179 sampel (4.2%) positif DNA C. burnetii dari 4252 sampel, serta
pada mayones yang dilakukan di Jepang dan Kanada dari bulan Maret 2003
Data tersebut diatas dapat dijadikan dasar untuk melakukan penelitian tentang keberadaan penyakit Q fever di Indonesia, terutama pada ayam dan
bahan pangan asal unggas, khususnya telur. Hal ini penting dilakukan karena
sampai saat ini masih banyak masyarakat Indonesia yang gemar mengkonsumsi
telur mentah atau setengah matang, karena disebabkan masih adanya
kepercayaan bahwa khasiatnya lebih baik bila dimakan dalam keadaan mentah
sebagai pelengkap jamu. Pelacakan keberadaan DNA C. burnetii pada telur
sudah sangat mendesak untuk dilakukan, karena sampai saat ini belum ada studi
atau kajian tentang ada tidaknya mikroorganisme C. burnetii dalam telur,
sehingga penelitian yang dilakukan benar-benar merupakan sesuatu yang baru
di Indonesia.
Penelitian ini bertujuan untuk (1) mengetahui keberadaan DNA C. burnetii pada telur, (2) mengetahui hubungan keberadaan C. burnetii dengan karakteristik
lingkungan peternakan (sanitasi, higiene personal dan biosekuriti), serta (3) mengetahui sensitivitas dan spesifisitas metode nested PCR dibandingkan dengan PCR untuk mendeteksi DNA C. burnetii.
Hipotesis penelitian ini adalah (1) DNA C. burnetii dapat ditemukan pada
telur, (2) terdapat hubungan keberadaan C. burnetii dengan karakteristik
lingkungan (sanitasi, higiene personal dan biosekuriti), serta (3) metode nested
PCR merupakan metode deteksi yang sensitif dan spesifik.
Hasil penelitian ini diharapkan dapat (1) memberikan informasi tentang
keberadaan DNA C. burnetii pada telur, (2) dapat ditetapkan metode uji yang sensitif dan spesifik terhadap C. burnetii sebagai agen penyebab Q fever, serta
(3) dapat digunakan pemerintah sebagai signal awal sistem kewaspadaan dini (SKD), sehingga dapat disusun pedoman cara pengendalian penyakit Q fever di
TINJAUAN PUSTAKA
Q
Fever
Morfologi dan KarakterIstik
Coxiella burnetii
Nama Query fever (Q fever) pertama kali diusulkan tahun 1937 oleh Edward
Holbrook Derrick, setelah adanya gejala demam yang diderita pekerja rumah potong
hewan (RPH) di Brisbane Queensland Australia pada tahun 1935. Pada tahun 1938 Herald Rea Cox dan MacFarlane Burnett menemukan penyebabnya, yaitu Rickettsia burnetii (R. burnetii). Berdasarkan analisa sekuen 16S rRNA R. burnetii yang dilakukan Maurin dan Raoult (1999), secara filogenik dekat dengan Francisella tularensis, Legionella pneumophila, Escherichia coli dan Pseudomonas aeruginosa dalam kelompok famili Proteobacteria subdivisi gamma, sedangkan yang lain subdivisi alpha (Rickettsia rickettsii, Erlichia cheffeensis, Bortonella henseloe, Brucella abortus, Afipia felis), subdivisi beta (Alcaligenes faecalis), subdivisi delta (Campylobacter jejuni) dan subdivisi epsilon (Helicobacter pylori). Tetapi karena mempunyai perbedaan diantara kelompok sub divisi gamma, maka Cornelius B. Philip mengusulkan genus tersendiri menjadi Coxiella burnetii (C. burnetii) yang merupakan penghargaan terhadap Herald Rea Cox dan MacFarlane
Burnett seperti pada Gambar 1 (Singleton dan Sainsbury 2006).
Francisella tularensis
Coxiella burnetii
Legionella pneumophila gamma
Escherichia coli
Pseudomonas aeruginosa
Rickettsia rickettsii
Erlichia cheffeensis
Proteobacteria Bortonella henseloe alpha
Brucella abortus
Afipia felis
Alcaligenes faecalis beta
Campylobacter jejuni delta
Helicobacter pylori epsilon
C. burnetii bersifat obligat patogen intraseluler, termasuk bacterial like organism,
memiliki membran seperti bakteri Gram negatif, namun sulit diamati dengan pewarnaan
Gram. Pewarnaan yang bisa digunakan adalah Gimenez dan Stamp (Maurin dan Raoult 1999; Willems et al. 1998; Zhang et al. 2004).
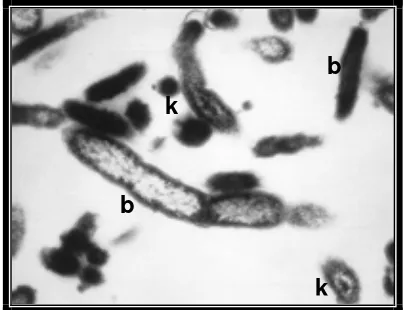
C. burnetii adalah mikroorganisme pleomorfik (bentuknya tidak tetap, batang atau kokoid), berukuran lebar 0.2-0.4 µm dan panjang 0.4-1.0 µm, struktur menyerupai spora (spora like), mempunyai bentuk besar (large form/large cell variant) dan bentuk kecil (small form/small cell variant) seperti dilihat pada Gambar 2 (Fournier et al. 1998; Heinzen et al. 1999; Maurin dan Raoult 1999). C. burnetii dapat bereplikasi menjadi dua kali setiap 20-45 jam di dalam vakuola parasitoforus sel eukariot inang (Angelakis dan Raoult 2010).
Gambar 2 C. burnetii dengan mikrograf elektron pada pembesaran 75 000 kali, bentuk kecil (k); bentuk besar (b) (
k
Fournier et al. 1998).
Bentuk besar adalah bentuk vegetatif yang menginfeksi monosit dan sel
makrofag, sedangkan bentuk kecil terdapat di ekstraseluler dan diduga sebagai bentuk yang infeksius. C. burnetii memiliki 2 bentuk antigen yakni antigen fase I dan fase II.
Antigen fase I ditemukan di alam atau hewan, sedangkan fase II ditemukan setelah passage di telur tertunas atau sel kultur. Antigen fase I lebih patogenik dibandingkan
dengan fase II. Perbedaan antara kedua bentuk fase antigen ini sangat penting di dalam
diagnosa. Antigen fase I mempunyai susunan lipopolisakarida (LPS) yaitu L-vironosa
dihidroksistreptosa dan galaktosamin uronil (1.6) glukosamin, bersifat halus dan berperan
dalam menentukan patogenitasnya, sedangkan pada fase II terlihat kasar dan tidak
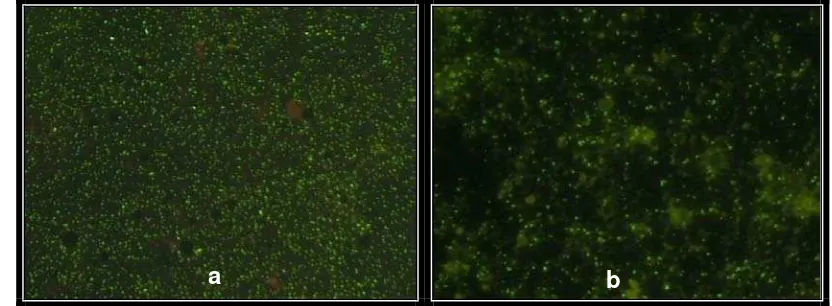
ditemukan rantai sakarida vironosa dan hidroksistreptosa, seperti pada Gambar 3 (Fournier et al. 1998).
b
k
7
Gambar 3 Antigen fase I (a) dan fase II (b) C. burnetii (Fournier et al. 1998).
Coleman et al. (2004) menyatakan bahwa susunan LPS pada mikroorganisme C. burnetii fase I dan fase II berbeda. Berdasarkan analisa electrospray ionization mass spectrometry menunjukkan bahwa pada fase I dan fase II terdapat lipid A yang sama. Lipid A tersebut tidak dapat mengaktifkan toll like receptor 2 (TLR-2) dan TLR-4. Hal ini berbeda dengan lipid A yang berasal dari E. coli yang mampu mengikat TLR-4, sehingga bila ada C. burnetii maka TLR-2 dapat sebagai penentu adanya infeksi dan
akan menghambat pertumbuhan mikroorganisme tersebut di dalam sel inang.
Pada infeksi Q fever akut, antibodi terhadap antigen fase II lebih dominan
dibandingkan dengan terhadap fase I. Namun pada kasus kronik, antibodi terhadap
antigen fase I lebih memegang peran penting. Kedua antibodi ini dapat bertahan hingga berbulan-bulan setelah infeksi (Field et al. 2002; Harris et al. 2000). Zhang et al. (2004) menyatakan bahwa sekuen gen AdaA pada protein membran luar merupakan penanda untuk C. burnetii pada kasus akut serta berhubungan dengan faktor patogenitasnya. Menurut CDC (2005) bahwa pada penderita akut Q fever dapat dideteksi dengan
meningkatnya antibodi IgG fase II serta IgM fase I dan fase II, sedangkan pada kronis Q fever terlihat peningkatan antibodi IgG dan IgA fase I.
Berdasarkan hasil analisa restriction fragment length polymorphism (RFLP) C. burnetii dapat dibagi menjadi 6 grup. Grup I, II, III dihubungkan dengan keganasan
pada hewan, caplak atau isolat yang berasal dari manusia yang terinfeksi ke dalam
kelompok tipe akut, sedangkan grup IV dan V selalu dikaitkan dengan endokarditis pada
manusia yang dikelompokkan dalam tipe kronis. Grup VI merupakan isolat yang
diperoleh dari rodensia yang belum diketahui patogenisitasnya (Colemen et al. 2004). Pada hewan percobaan marmot, infeksi grup I (Nine Mile, African dan Ohio) akan
menunjukkan gejala akut yang jelas, grup V (G dan S) menunjukkan gejala ringan sampai
sedang, serta grup IV (Priscilla dan P) dan V (Dugway) tidak memperlihatkan gejala sama
sekali. Pada tikus infeksi grup I, IV, V dan VI semua menunjukkan gejala klinis yang jelas (Russell-Lodrigue et al. 2009).
Mikroorganisme C. burnetii mempunyai beberapa plasmid, yaitu QpH1, QpRS,
QpDG dan QpDV (Maurin dan Raoult 1999). Plasmid QpH1 ditemukan pada grup I, II
dan III; plasmid QpRS pada grup IV dan V, plasmid QpDG pada grup VI; serta plasmid QpDV pada strain French (Fournier et al. 1998).
Hasil analisa genom C. burnetii Nine Mile fase 1 yang sebesar 1 995 275 pb,
terdapat beberapa gen yang berpotensi dalam proses adesi dan invasi ke dalam sel inang
dan juga mempunyai kemampuan detoksikasi. Ukuran genom dari beberapa strain C. burnetii bervariasi antara 1.5-2.4 Mb (Maurin dan Raoult 1999).
Agen penyebab tahan terhadap kondisi psikokimia, seperti lingkungan panas,
kering dan tahan terhadap beberapa konsentrasi disinfektan, seperti 0.05% hipoklorit,
5% peroksida dan 1:100 larutan lisol serta glutaraldehid, etanol dan gas formaldehid
(CFSPH 2007). Pada bahan pangan asal hewan dan olahannya C. burnetii dapat bertahan hidup 1 bulan pada daging yang disimpan dalam cold storage pada suhu -20 ºC,
42 bulan pada susu segar yang disimpan pada suhu 4-6 ºC dan lebih dari 40 bulan pada
susu skim (CFSPH 2007). Oleh karena itu C. burnetii dapat dikembangkan sebagai senjata biologis yang berpotensi digunakan sebagai ancaman teroris (bioterrorisme) (CDC 2005; Kagawa et al. 2003; Madariaga et al. 2003).
Diagnosa Penyakit Q
fever
Diagnosa yang akurat terhadap penyakit Q fever pada hewan dan manusia masih sulit dilakukan karena infeksi agen penyebab penyakit ini umumnya bersifat subklinis
serta memilki dua fase antigen yang sangat penting dalam peneguhan diagnosa. C. burnetii merupakan bakteri intraseluler yang pada fase akut dapat ditemukan di dalam
darah dan pada fase kronis terakumulasi dalam sel fagosit yang terdapat dalam organ seperti jantung, hati, limpa dan plasenta (Lorenz et al. 1998). Dalam fase akut antibodi
terhadap antigen fase II lebih tinggi dibandingkan dengan fase I dan umumnya dapat
terdeteksi selama minggu kedua sejak terinfeksi, sedangkan pada fase kronis antibodi terhadap antigen fase I bertahan lebih lama (Setiyono et al. 2005).
Metode diagnosa yang tepat harus memperhatikan beberapa faktor, antara lain
sensitivitas, spesifisitas, jumlah sampel yang akan diuji, biaya yang diperlukan dan waktu
9
untuk mendeteksi antigen dalam jumlah sedikit atau respon imun yang kecil, sedangkan
spesifisitas pengujian berkaitan dengan kemampuan untuk membedakan antigen atau respon imun antigen yang sangat erat hubungannya (Fournier et al. 1998).
Beberapa penelitian serodiagnosa memberikan gambaran yang sangat berguna untuk mengetahui seroprevalensi Q fever disuatu daerah secara luas dalam waktu relatif singkat (Setiyono et al. 2008). Metode serodiagnosa yang telah diterapkan untuk pemeriksaan Q fever adalah capilary tube agglutination test (CAT), complement fixation test (CFT), enzyme-linked immunosorbent assay (ELISA) dan indirect immunofluorescent antibody (IFA) (Cetinkaya et al. 2000; Setiyono et al. 2005).
Penggunaan teknik CAT pernah dilakukan di Indonesia terhadap 323 sampel
darah sapi yang diambil dari Bogor, Bandung, Surabaya dan Semarang dan ditemukan 4 sampel (1.2%) positif Q fever (Rumawas 1976). Adesiyun dan Cazabon (1996) mendapatkan 36 sampel (4.8%) positif C. burnetii dari serum darah ayam, sapi, babi,
kerbau, domba dan kambing di beberapa rumah potong di Trinidad. Sementara itu hasil penelitian Richards et al. (2003) mendapatkan 2.1% seropositif Rickettsia dengan metode
ELISA terhadap penduduk di Kepulauan Gag Irian Jaya.
Teknik ELISA dapat digunakan untuk pemeriksaan sampel dalam jumlah banyak,
waktu yang singkat dan mempunyai tingkat sensitivitas yang tinggi tetapi spesifitasnya
rendah. Adapun kekurangan dari teknik ELISA diantaranya sering menimbulkan reaksi
positif palsu. Hal ini disebabkan karena antigen standar yang digunakan umumnya
dipropagasi dalam sel kultur, sehingga ada kemungkinan antibodi dalam serum berikatan
dengan epitop-epitop lain yang ada dipermukaan sel kultur. Reaksi silang yang pernah dilaporkan adalah dengan Microbacterium pneumonia dan Bordetella pertusis (Setiyono et al. 2005; Slaba et al. 2005).
Field et al. (2000) membandingkan dua uji serologis untuk mendiagnosa
Q fever yaitu teknik ELISA dengan IFA. Hasil studi tersebut memperlihatkan bahwa
teknik ELISA memberikan sensitivitas 95% dan spesifisitas 88%, sedangkan
menggunakan IFA sensitivitas 99% dan spesifisitas 98%. Penelitian yang sama juga
dilaporkan Setiyono (2003) bahwa ELISA mempunyai tingkat sensitivitas dan spesifisitas
masing-masing 93.8% dan 83.3%. Teknik ELISA baik digunakan untuk tes skrining
dengan jumlah sampel yang banyak dan spesifisitasnya dapat ditingkatkan dengan mengkombinasi dengan IFA. Hasil penelitian yang dilakukan Kennerman et al. (2010)
menunjukkan 20% seropositif dari 743 domba (42 flok) yang berumur antara 10-24 bulan
Laboratories, Broomfield, CO, USA). Penelitian yang sama juga dilakukan oleh Cekani et al. (2008) dengan teknik ELISA menggunakan Chekit Q fever enzyme immunoassay dan
memperoleh 9.8% seropositif pada domba dan kambing (dari 1085 ekor) serta 7.9%
seropositif pada sapi (dari 571 ekor) di Albania.
Metode IFA merupakan metode yang direkomendasikan oleh banyak peneliti untuk mendapatkan gambaran seroprevalensi Q fever secara cepat dan luas. Hal ini
didasarkan keunggulan metode IFA antara lain cepat, sensitif, relatif murah serta tidak
ditemukan adanya reaksi silang dengan infeksi penyakit lain dan dapat dilakukan untuk
jumlah sampel yang banyak.
Metode IFA digunakan untuk mendiagnosa Q fever fase akut maupun kronis pada
manusia berdasarkan titer immunoglobulin M (IgM), A (IgA) dan G (IgG) yang spesifik
terhadap C. burnetii fase I dan II (Fournier et al. 1998; Setiyono et al. 2005). IgM akan
berespon awal setelah C. burnetii masuk kedalam tubuh, kemudian setelah dua minggu
baru terbentuk IgG dan secara bertahap akan meningkat titernya di dalam darah sampai beberapa bulan dan setelah itu akan menurun (To et al. 1996).
Polymerase chain reaction (PCR) merupakan teknik diagnosa yang paling sensitif dan spesifik saat ini. Nested PCR adalah salah satu aplikasi teknik PCR yang banyak digunakan untuk mendeteksi C. burnetii, walaupun masih mempunyai beberapa kelemahan diantaranya perlu ketelitian yang tinggi dalam pengerjaannya, memerlukan primer yang spesifik dan biayanya relatif mahal (Kato et al. 1998; Zhang et al. 1998).
Penelitian yang dilakukan terhadap 34 ekor domba menggunakan uji serologis
(ELISA dan IFA) serta uji molekuler (PCR) didapatkan 24% positif dengan ELISA, 32%
positif dengan IFA dan 44% positif dengan PCR. Dari 7 ekor domba yang seronegatif,
dilakukan pengujian dengan PCR dan diperoleh hasil positif. Hal ini menunjukkan bahwa PCR mempunyai sensitivitas lebih tinggi dibandingkan uji serologis (Berri et al. 2001).
Perbandingan uji serologis dan molekuler dalam mendiagnosa Q fever fase akut
menunjukkan bahwa apabila serum sampel yang diambil satu sampai dua minggu setelah
infeksi dapat didiagnosa dengan kedua metode uji. Bila diambil pada minggu ke tiga
sampai ke empat sebaiknya menggunakan uji serologis, sedangkan uji molekuler hanya
untuk mengkonfirmasi hasil uji yang seronegatif (Fournier dan Raoult 2003).
Penegakan diagnosa menggunakan satu uji serologis tidak cukup, diperlukan
11
Q
Fever
pada Hewan
Epidemiologi dan Penyebaran Penyakit
Beberapa jenis hewan yang dapat terinfeksi C. burnetii antara lain sapi, kambing,
domba, anjing, kucing, kuda, kerbau, babi, unta, kelinci, reptil, kodok, burung merpati,
kalkun, ayam, bebek, rodensia, ikan dan caplak (Arricau-Bouvery dan Rodolakis 2005; Maurin dan Raoult 1999; Muskens et al. 2007; Parker et al. 2006). Burung dan rodensia merupakan pembawa C. burnetii di alam, sedangkan sapi, kambing dan domba merupakan reservoir utama (Acha dan Szyfres 2003; Kim et al. 2005; Van den Brom dan
Vellema 2009). Di beberapa negara, anjing dan kucing juga merupakan sumber utama
penularan, hal ini sesuai dengan uji serologis yang mendapatkan seropositif pada anjing dan kucing berkisar antara 15-20% (Buhariwalla et al. 1996; Marrie 2000).
Kontaminasi C. burnetii di lingkungan dapat terjadi setelah hewan melahirkan,
terutama melalui cairan kelahiran, plasenta, feses dan urin secara terus menerus.
Kontaminasi tersebut bisa berlangsung beberapa bulan dan dilaporkan pada kambing
lebih lama dibandingkan domba, yaitu selama dua kali masa kebuntingan, oleh karena itu
kambing sering menjadi sumber infeksi ke manusia (Arricau-Bouvery dan Rodolakis 2005; Hatchette et al. 2003). Mikroorganisme C. burnetii berkembangbiak dan tumbuh subur di dalam plasenta dan cairan amnion, sehingga pada hewan bunting infeksi Q fever bersifat
laten (Kloppert et al. 2004).
C. burnetii dilaporkan telah ditemukan pada 40 spesies caplak di dunia, sehingga
caplak merupakan sumber penularan antar hewan di alam, dari hewan liar ke hewan
pelihara dan diantara hewan pelihara melalui feses caplak yang terinhalasi. Disamping itu
penyebaran antar hewan pelihara dapat juga terjadi melalui kontak seksual karena agen
penyebab ditemukan pada semen sapi pejantan (Marrie 2000; Maurin dan Raoult 1999).
Sethi et al. (1978) melakukan penelitian pada ayam petelur leghorn putih umur 6 bulan, dengan menginfeksikan 2 ml larutan 10% membran yolk sac yang mengandung C. burnetii strain Nine Mile melalui oral dan intra peritoneal. Hasil penelitian tersebut
menunjukkan titer antibodi dengan metode CAT mulai meningkat (1:512) pada 13 hari
setelah infeksi dan tertinggi (1:1024) pada 30 hari setelah infeksi, kemudian menurun (<1:8) setelah 90 hari infeksi. Ayam-ayam petelur leghorn putih yang terinfeksi C. burnetii
tidak menunjukkan gejala klinis sama sekali sampai dengan 90 hari. Pada 90 hari setelah
infeksi, C. burnetii tidak ditemukan pada limpa dan hati, tetapi masih dapat diidentifikasi
Patogenesis Q
fever
C. burnetii hidup dan berproliferasi dalam sel inang yaitu lisosom yang bersifat asam. Pada manusia dan hewan target sel utama dari C. burnetii pada monosit atau
sel makrofrag. Jika infeksi terjadi melalui pernafasan maka makrofag alveolar berperan
aktif terhadap terjadinya infeksi akut, sedangkan bila melalui pencernaan, maka sel
kupffer dalam hati yang berperan terhadap infeksi C. burnetii. Bakteri intraseluler
umumnya menggunakan reseptor spesifik pada sel eukariotik seperti integrin untuk dapat menginvasi sel inang, khusus C. burnetii menggunakan reseptor CR-3. Secara alami C. burnetii fase I mempunyai kemampuan yang lemah untuk menempel pada sel inang
melalui monosit ataupun sel makrofag, tetapi mempunyai kemampuan untuk hidup dan
bertahan yang kuat bila sudah menembus dan masuk ke dalam sel-sel tersebut. Hal ini
disebabkan C. burnetii fase I menghambat reseptor CR-3 dan kemudian mengikat monosit melalui kompleks leucocyte response integrin (LRI) dan integrin associated protein (IAP). Sebaliknya fase II lebih mudah masuk ke dalam monosit atau sel makrofag tetapi secara cepat akan dibunuh melalui phagolisosomal pathway (Baca dan Paretsky
1983).
C. burnetii yang masuk ke dalam sel inang secara difusi pasif, akan terperangkap
dalam fagosom yang secara cepat akan berdifusi membentuk fagolisosom. Fagolisosom
akan membentuk vakuola besar yang dinamakan vakuola lisosomal sebagai tempat
persembunyian C. burnetii. C burnetii dapat beradaptasi dalam fagolisosom dan
berkembang baik dalam vakuola parasitoporus yang mempunyai pH 4.7-5.2 (Baca dan
Paretsky 1983). Asam yang terdapat didalam fagolisosom akan mengaktifkan enzim, sehingga sel C. burnetii akan berkembangbiak menjadi bentuk besar (large form/large cell variant) yang resisten setiap 8-12 jam (Maurin dan Raoult 1999).
C. burnetii merupakan bakteri asidofilik yang metabolismenya menjadi aktif bila suasana lingkungannya asam atau dengan adanya perubahan pH menjadi asam.
Perkembangan C. burnetii dapat dihambat dengan cara meningkatkan pH menjadi basa dengan menambahkan chloroquin. Suasana asam diperlukan oleh C. burnetii dalam
mendapatkan nutrisi untuk proses metabolisme seperti pembentukan asam nukleat dan
asam amino (Maurin dan Raoult 1999).
Gejala Klinis
13
ditemukan pada paru-paru, hati, limpa dan darah, sedangkan infeksi kronis tidak
menunjukkan gejala sama sekali (Maurin dan Raoult 1999).
Gejala umum pada ruminansia ditandai dengan anoreksia, rinitis, frekuensi
pernafasan meningkat, abortus, retensio plasenta, plasentitis, endometritis, tidak fertil dan
beberapa ditemukan lahir dalam keadaan lemah, kecil dan mati (Arricau-Bouvery dan
Rodolakis 2005). Pada sapi perah kadang-kadang terlihat pneumonia, sedangkan pada
anak domba terjadi diare dan gangguan pernafasan (Van den Brom dan Vellema 2009).
Di daerah endemik seperti California USA, kejadian abortus pada domba mencapai
18-55% dan sapi 82%, sedangkan di Kanada 0-35% pada domba dan 33-82% pada sapi
(CFSPH 2007). Beberapa peneliti mengatakan bahwa abortus pada domba dan kambing
terjadi pada akhir kebuntingan (Van den Brom dan Vellema 2009).
Q
Fever
pada Manusia
Epidemiologi dan Distribusi Penyakit
Infeksi Q fever pada manusia seringkali berhubungan dengan pekerjaan (occupational disease), seperti peternak, pembeli dan pengunjung yang datang ke
peternakan; dokter hewan; pekerja di peternakan, rumah potong hewan, penyamakan
kulit, pengolahan daging, susu dan wol; peneliti dan pegawai laboratorium serta pekerja di
kebun binatang (Norlander 2000; Van den Brom dan Vellema 2009).
Penularan antar manusia jarang terjadi, tetapi dapat melalui transfusi (darah,
sumsum tulang belakang), saliva dan hubungan seksual. Selain itu dilaporkan bisa tertular selama menangani keguguran dan outopsi pada manusia (Milazzo et al. 2001).
Norlander (2000) melaporkan bahwa insidensi penyakit Q fever di Asia sudah
banyak diketahui, yaitu Thailand, Jepang dan Cina. Di Thailand tahun 2003 dilaporkan
mencapai 1.3% kasus pada manusia (umur 15-62 tahun, atau rata-rata 42 tahun). Di
Amerika Serikat rata-rata 58.4 kasus per tahun dan 67% kasus di California (CFSPH
2007).
Menurut NNDSS (2003) antara tahun 1991-2001 di Australia terjadi 6597 kasus
atau rata-rata 650 kasus per tahun pada manusia. Di Australia selatan pada tahun 1990 hingga Agustus 2001 dilaporkan terdapat 177 kasus Q fever, yaitu 155 (87.6%) kasus
terjadi pada laki-laki dan 147 (83.1%) kasus terjadi pada usia produktif (20-49 tahun).
Dari kasus ini, 90 kasus (50.8%) terjadi pada pekerja di pabrik pengolahan daging, diikuti
oleh 57 kasus (32.2%) pada pekerja yang kontak dengan hewan. Tercatat 17 kasus
berinteraksi dengan pabrik pengolahan daging (pengunjung, penghubung). Sampai saat
ini kasus pada anak-anak belum pernah dilaporkan (CDC 2001). Laporan lain
menyatakan rasio tertular laki-laki:perempuan adalah 75%:25% dan umumnya penderita berusia lebih dari 40 tahun (Maurin dan Raoult 1999). Hasil penelitian Ergas et al. (2006) menyatakan bahwa penyakit Q fever bentuk akut umumnya terjadi pada musim panas pada penderita yang rata-rata berusia 42.7±17.3 tahun dengan perbandingan rasio
laki-laki:perempuan adalah 1.6:1.
Pada bulan Mei 2007 terjadi 182 kasus kejadian pneumonia yang disebabkan
infeksi C. burnetii di Belanda dan kemudian pada tahun 2008 terdapat 1000 kasus pada
manusia dengan gejala seperti demam, lelah, lemah dan berkeringat pada malam hari. Hasil pemeriksaan lebih lanjut ditemukan 65% menderita pneumonia. Infeksi C. burnetii pada manusia tahun 2007 dan 2008 di Belanda dilaporkan disebabkan karena adanya
kasus abortus pada peternakan kambing perah. Adanya kejadian infeksi C. burnetii tersebut, maka sejak tahun 2008 penyakit Q fever pada ruminansia kecil di Belanda wajib dilaporkan (notifiable disease) (Delsing dan Kullberg 2008; Schimmer et al. 2008).
Menurut Rarotra et al. (1978) kasus Q fever juga ditemukan 27.52% positif
antibodi C. burnetii pada pekerja peternakan ayam di India, dan sebanyak 6.38%
memperlihatkan gejala demam. Pada peternakan ayam tersebut secara serologi juga
ditemukan antibodi terhadap C. burnetii. Hal ini menunjukkan bahwa pekerja peternakan ayam beresiko tinggi terhadap infeksi Q fever.
Penelitian yang dilakukan di Australia menyebutkan bahwa 30% mereka yang bekerja di peternakan dan RPH berisiko terserang Q fever. Hal yang sama ditemukan pada 58 orang pekerja pada tiga peternakan domba di Italia yang mempunyai seroprevalensi 45-53% positif antibodi C. burnetii (Marrie 2003).
Tiga orang wisatawan Jepang yang berasal dari wilayah Hyogo, Tottori dan Aichi
merasakan demam, badan pegal dan ngilu pada persendian setelah melakukan
perjalanan inspeksi ke peternakan sapi dan RPH di Australia dan New Zealand selama 11
hari pada bulan September 2001. Hasil pemeriksaan laboratorium ditemukan adanya
gangguan fungsi hati dan trombositonemia, sedangkan dari pemeriksaan serologi dengan
menggunakan IFA maupun ELISA ditemukan peningkatan titer antibodi IgM dan IgG empat kali lipat. Ketiga pasien tersebut didiagnosa Q fever dan sembuh setelah dilakukan pengobatan yang sesuai (Setiyono 2003).
15
imunosupresan karena menderita penyakit tertentu, misalnya AIDS, kanker, limpoma,
tumor, diabetes, hepatitis, gangguan jantung, gangguan ginjal kronis atau penerima
transplan organ.
Q
Fever
sebagai
Food-borne Disease
Transmisi C. burnetii ke manusia terjadi secara aerosal atau inhalasi melalui ’fomite’ atau partikel debu yang terkontaminasi sekret kelahiran yang mengering, jaringan
plasenta, darah, feses dan urin. Selain itu kontak langsung dengan hewan atau jaringan
terinfeksi atau tertular, bulu (wol), kulit, sisa abortus, plasenta, darah, feses, urin serta
melalui saluran pencernaan akibat mengkonsumsi susu dan telur yang tidak dipasteurisasi (Acha dan Szyfres 2003; Anonim 2003; Muramatsu et al. 2006).
Hasil penelitian menyatakan bahwa apabila sapi perah terinfeksi C. burnetii maka mikroorganisme tersebut dapat ditemukan dalam susu (Maurin dan Raoult 1999; Kim et al. 2005). Hal ini merupakan salah satu sumber penularan dari hewan ke manusia (Rodolakis et al. 2009).
Penelitian Hirai et al. (2005) menemukan 131 sampel (53.7%) positif DNA C. burnetii dari 244 sampel susu yang dijual di supermarket di Tokyo menggunakan
metode nested PCR. Di Swiss ditemukan 17 sampel (4.7%) positif DNA C. burnetii dari
359 sampel susu sapi, tetapi tidak ditemukan pada susu domba dan kambing menggunakan metode nested PCR (Fretz et al. 2007).
Sejak burung ditetapkan sebagai salah satu host spectrum dari C. burnetii, maka
apabila ayam terinfeksi dapat membawa agen penyebab ke manusia melalui telur mentah
yang terkontaminasi (Hirai dan To 1998). Sethi et al. (1978) menemukan bahwa C. burnetii dapat diisolasi pada selaput kuning telur dari embrio ayam (chicken embryo
yolk sac). Hasil percobaan pada ayam petelur leghorn putih umur 6 bulan yang diinfeksikan 2 ml larutan 10% membran yolk sac yang mengandung C. burnetii strain Nine Mile secara oral dan intra peritoneal, C. burnetii dapat ditemukan di dalam telur (ditularkan
secara transovarial). Hal yang sama juga dilaporkan Sobeslavsky dan Syrucek (1959)
bahwa C. burnetii dapat ditularkan secara transovarial setelah unggas (Gallus galus domesticus) diinfeksi mikroorganisme tersebut melalui oral.
Penelitian pada telur ayam di Jepang, Korea dan Filipina pada tahun 2003-2004
menemukan 179 sampel (4.2%) positif DNA C. burnetii dari 4252 sampel, serta pada
melakukan penelitian pada 504 sampel telur ayam yang di masuk ke Swiss, dan dilaporkan tidak menemukan DNA C. burnetii pada semua sampel menggunakan metode nested PCR.
Gejala Klinis
Orang yang terserang penyakit Q fever umumnya menunjukkan gejala klinik yang
tidak spesifik atau asymptomatis (60%), spesifik atau symptomatis (38%) dan beberapa
penyakit lainnya (2%), sehingga sulit dibedakan dengan gejala dari penyakit lain. Gejala akut umumnya seperti flu (flue like syndrome), misalnya demam, sakit kepala, berkeringat, menggigil, lelah (fatigue), pegal-pegal, sakit tenggorok, batuk, dada sakit, muntah, diare dan penurunan bobot badan. Penyakit Q fever yang tidak diobati dalam
kurun waktu dua minggu, maka dapat berlanjut menjadi pneumonia (30-50%), radang hati
(hepatitis), infeksi kulit (kudis), hepatomegali, miokarditis, perikarditis, meningoencefalitis,
uveitis, tromboplebitis, artritis, pleuritis dan pankreatitis. Pada wanita hamil yang
terinfeksi C. burnetii akan mengalami keguguran pada semester pertama atau lahir
prematur, bayi dengan bobot badan rendah dan plasentitis pada saat melahirkan
(Arricau-Bouvery dan Rodolakis 2005; CFSPH 2007; Maurin dan Roault 1999). Kematian pada
kasus akut dapat mencapai 1-2% (CDC 2005; CFSPH 2007; Delsing dan Kullberg 2008).
Apabila 6-12 bulan tanpa pengobatan yang efektif, maka 2-10% (1-5%) dari kasus
akut akan menjadi kronis, yaitu endokarditis, infeksi osteoartikular, pneumoni fibrosis, sindrom kelelahan kronis (chronic fatique syndrome) dan masalah kehamilan (Maurin dan Roault 1999; Schimmer et al. 2008). Manifestasi gejala penyakit Q fever pada manusia
sangat bervariasi (lihat pada Gambar 4). Kematian pada penderita kasus kronis bisa
mencapai 25-65% (bila mempunyai faktor imunosupresan dan atau abnormal valvular).
Sindrom kelelahan kronis ditandai dengan sering mengalami kelelahan yang panjang
disertai berkeringat pada malam hari, pegal-pegal, sakit di persendian, gelisah dan waktu
tidur berubah. Sindrom ini terjadi setelah infeksi akut yang berlangsung lebih dari satu
bulan (Arricau-Bouvery dan Rodolakis 2005; CDC 2005; Delsing dan Kullberg 2008). Gambaran darah dari orang yang menderita penyakit Q fever akut ditandai
dengan peningkatan laju endap darah, jumlah sel darah putih cenderung rendah sampai
17
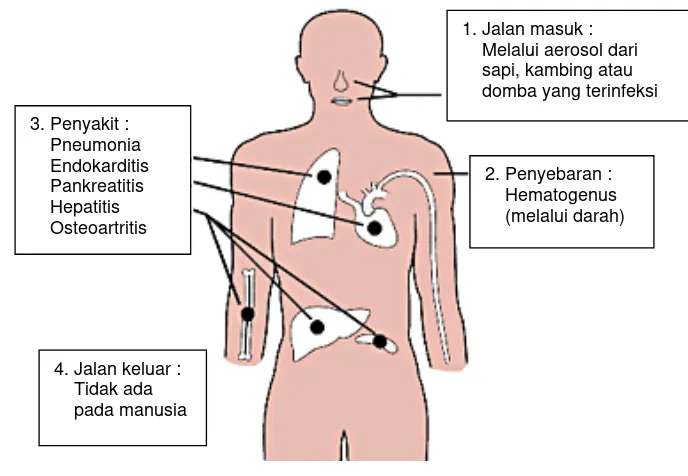
Gambar 4 Mekanisme infeksi dan gejala penyakit Q
fever
pada manusia
(
CDC 2005).Masa inkubasi penyakit Q fever bervariasi mulai 2-5 minggu (1-4 minggu) dan beberapa kasus mencapai lebih dari 6 minggu (Maurin dan Roault 1999; CFSPH 2007; Delsing dan Kullberg 2008). Masa inkubasi dipengaruhi oleh dosis infeksi C. burnetii
(Maurin dan Roault 1999). Dilaporkan bahwa orang yang terinfeksi 1-10 sel mikroorganisme C. burnetii dapat menyebabkan timbulnya gejala klinis (CFSPH 2007).
Pengendalian
NNDSS (2003) melaporkan bahwa sejak tahun 2000-2003 dilakukan upaya pencegahan penyakit ini, yaitu melakukan program vaksinasi Q fever pada pekerja di
Industri pengolahan daging dan RPH, sedangkan pada tahun 2001-2004 dilaksanakan
pada hewan ternak dan pekerja di peternakan (ternak potong dan perah).
Vaksin Q fever (Q Vax) dibuat dengan inaktivasi antigen fase I C. burnetii strain Henzerling yang mengandung antigen kompleks LPS-protein dan disuntikkan secara subkutan dengan dosis tunggal sebesar 30 mikrogram per dosis (Ackland et al. 1994; Waag et al. 2002). Vaksin baru dapat diberikan kepada hewan atau manusia apabila hasil tes serologis tidak ditemukan antibodi terhadap Q fever. Hal ini penting karena vaksinasi Q Vax akan dapat menimbulkan kekebalan awal yang optimum (Anonim 2003).
Studi yang dilakukan di Australia bagian selatan menunjukkan bahwa durasi vaksin 3. Penyakit :
Pneumonia Endokarditis Pankreatitis Hepatitis Osteoartritis
1. Jalan masuk : Melalui aerosol dari sapi, kambing atau domba yang terinfeksi
2. Penyebaran : Hematogenus (melalui darah)
Q Vax dapat memberikan kekebalan pada hewan dan manusia selama lima tahun (Ackland et al. 1994; Waag et al. 2002).
Penelitian yang dilakukan Rodolakis et al. (2009) menunjukkan bahwa pemberian vaksin Q fever fase 1 (Coxevax® CEVA Santé Animale Libourne France) pada sapi perah
dara, efektif dimulai umur 3-4 bulan (vaksinasi pertama) dan kemudian di booster
(vaksinasi kedua) sebelum dilakukan inseminasi buatan untuk memperoleh titer antibodi yang tinggi dan dapat mencegah terjadinya shedding C. burnetii. Pada kejadian penyakit Q fever di Belanda, maka pada akhir tahun 2008 dilakukan pencegahan dengan
memberikan vaksin Coxevax® kepada domba dan kambing yang tidak bunting (Delsing dan Kullberg 2008; Schimmer et al. 2008).
Penyakit Q fever dapat diobati dengan pemberian antibiotik yang sesuai dengan kejadian penyakit, kelompok umur, dosis dan lama pemberian (lihat Tabel 2).
[image:34.612.79.538.367.556.2].
Tabel 2 Pengobatan Q fever pada manusia (Carcopino et al. 2007; Madariaga et al. 2003; Maurin dan Raoult 1999; Nourse et al. 2004; Rolain et al. 2003)
Penyakit Q fever dapat disembuhkan apabila pengobatan dilakukan sedini mungkin (Maurin dan Raoult 1999). Pencegahan penyakit Q fever selain vaksinasi adalah (1) memberikan edukasi pada individu atau kelompok yang berisiko; (2) disposal
(prosedur pemusnahan dengan cara pembakaran dan atau penguburan) dari plasenta, sisa obortus dan fetus; (3) karantina ternak yang akan diimpor; (4) outoclave dan
disinfeksi peralatan laboratorium; (5) pasteurisasi susu pada suhu lebih dari 62.7 °C
selama 30 menit atau 71.6 °C selama 15 detik dan sterilisasi pada suhu 130 °C selama
5 detik serta pesteurisasi telur pada suhu lebih dari 60 °C selama 6.2 menit atau 61.1 °C Kejadian
Penyakit
Kelompok Pengobatan Waktu
Akut
Dewasa
Doksisiklin 200 mg per hari 14 hari Fluoroquinolon 200 mg atau
pefloksasin 400 mg (3 kali per hari)
14-21 hari
Rifamisin 1200 mg per hari 21 hari Wanita hamil Trimetoprim 320 mg atau
sulfametoksazol 1600 mg per hari
> 5 minggu
Anak-anak Doksisiklin 100 mg per hari 10-14 hari
Kronis
Dewasa Doksisiklin 100 mg per hari > 18 bulan Hidroksikloroquin 600 mg per hari
Anak-anak Trimetoprim 160 mg atau
sulfametoksazol 800 mg per hari
19
selama 3.5 menit dapat membunuh mikroorganisme C. burnetii (CFSPH 2007; Marrie
2000; Mine 2008).
Q
Fever
di Indonesia
Beberapa studi, kajian dan penelitian tentang keberadaan Q fever di Indonesia
telah dilakukan sejak tahun 1955 terhadap 188 serum sapi yang diperiksa secara
serologis dan ditemukan positif antibodi C. burnetii menggunakan CAT (Kaplan dan
Bertagna 1955). Penelitian selanjutnya dilakukan oleh Rumawas (1976) pada 323 sampel
darah sapi yang diambil dari Bogor, Bandung, Surabaya dan Semarang dan didapatkan 4 sampel (1.2%) positif antibodi Q fever dengan metode CAT.
Penelitian Miyashita et al. (2001) menemukan infeksi Q fever dari penderita
pneumonia yang pernah tinggal di Indonesia. Hal yang sama juga dilakukan Richards et al. (2003) dan mendapatkan 2.1% seropositif Rickettsia terhadap penduduk di Kepulauan Gag Irian Jaya menggunakan metode ELISA.
Hasil seroprevalensi di Bogor pada domba dan kambing menunjukkan seropositif
masing-masing 31.88% dan 20.29% menggunakan metode IFA, sedangkan penelitian pada sapi bali dan brahman cross ditemukan 6.12% positif DNA C. burnetii serta pada kambing dan domba 3.64% positif DNA C. burnetii menggunakan metode nested PCR di
Bali dan Bogor (Mahatmi 2006).
C. burnetii secara serologis dan molekuler telah ditemukannya pada hewan
ruminansia (domba, kambing, sapi) dan juga manusia, sehingga kemungkinan penularan
kepada hewan lain dan bahan pangan asal hewan (susu, telur) di beberapa wilayah di
Indonesia sudah terjadi. Hal ini didasarkan pada data serologis dan molekuler bahwa C. burnetii sudah ditemukan pada hewan ruminansia di pulau Jawa dan Bali.
Dari segi kesehatan masyarakat veteriner, penyakit Q fever dapat dikelompokkan sebagai emerging atau re-emerging zoonosis yang disebabkan C. burnetii (Vaidya 2008).
Mikrorganisme ini dilaporkan mampu menularkan sejauh 18.3-20 km dari sumber infeksi yang dibawa oleh angin (oerosal transmission), mempunyai dosis infeksi yang rendah (low infectious dose), stabil di lingkungan dan beberapa kondisi psikokimia (stable in the environment) serta berdasarkan estimasi World Health Organization (WHO) apabila 5 kg C. burnetii disebarkan di suatu wilayah dengan populasi penduduk sebesar 5 juta, maka
Waktu dan Tempat Penelitian
Penelitian dilakukan dari bulan Juli 2005 sampai dengan Maret 2010. Sampel
telur diambil dari peternakan ayam petelur komersial ras (sektor 2) sebanyak 222 butir
dan dari peternakan ayam lokal (sektor 4) sebanyak 130 butir di wilayah Bogor.
Pengujian sampel telur dilakukan di Laboratorium Terpadu Fakultas Kedokteran
Hewan IPB dan Unit Pelayanan Mikrobiologi Terpadu (UPMT) Bagian Mikrobiologi Medik
Departemen Ilmu Penyakit Hewan dan Kesmavet FKH IPB. Untuk pengujian sensitivitas
dan spesifisitas metode uji dilakukan di Balai Besar Penelitian Veteriner Bogor.
Tahapan Penelitian
Penelitian ini pada intinya dibagi atas tiga tahap yaitu tahap verifikasi metode ekstraksi DNA Coxiella burnetii (C. burnetii) dari sampel telur dan alat diagnostik nested polymerase chain reaction (nested PCR); tahap pengujian sampel serta pengujian
sensitivitas dan spesifisitas metode. Tahap verifikasi metode ekstraksi DNA C. burnetii
dari kuning telur dengan menggunakan modifikasi metode Qiao (2005). Tahap
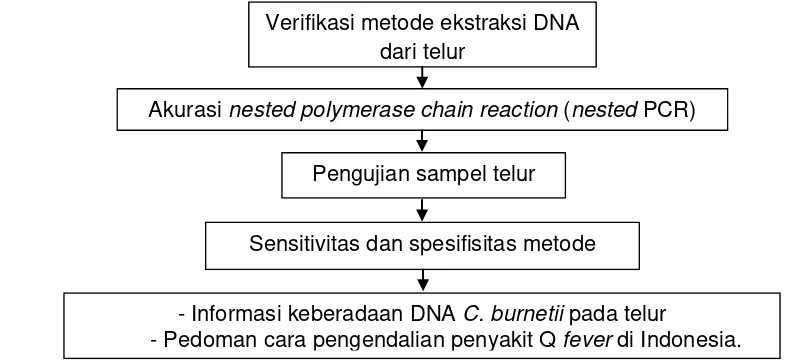
[image:36.612.97.490.517.699.2]selanjutnya melakukan deteksi DNA C. burnetii pada sampel telur yang diambil dari peternakan ayam petelur ras dan lokal dengan metode nested PCR (Zhang et al. 1998). Tahap akhir adalah pengujian sensitivitas dan spesifisitas metode untuk mengetahui batas limit deteksi metode nested PCR yang digunakan. Tahapan penelitian dapat dilihat pada Gambar 5.
Gambar 5 Tahapan penelitian studi Q fever pada ayam di wilayah Bogor. Verifikasi metode ekstraksi DNA
dari telur
Akurasi nested polymerase chain reaction (nested PCR)
Pengujian sampel telur
Sensitivitas dan spesifisitas metode
- Informasi keberadaan DNA C. burnetii pada telur
21
Modifikasi Metode Qiao (2005) untuk Mengekstraksi DNA
C. burnetii
dari
Kuning Telur
Penelitian ini bertujuan untuk mengetahui tingkat konsentrasi dan kemurnian DNA C. burnetii yang diperoleh dari hasil ekstraksi kuning telur menggunakan modifikasi metode Qiao.
Penelitian ini dilakukan dengan mengganti beberapa bahan-bahan untuk ekstraksi seperti PBS (phosphat buffer saline), Tris bufer, Np-40, Tween-20 dan Triton X-100
diganti dengan GenomicprepTM
Larutan hasil ekstrasi diukur konsentrasi dan kemurnian DNA yang diperoleh.
Pengukuran dilakukan dengan cara sebelum digunakan cuvet spektrofotometer dicuci
dengan larutan 1 M NaOH, 1 M HCl dan air milli Q. Larutan DNA dalam mikrotub cell-tissue DNA isolation kit (Amersham Biosciences) yang terdiri dari larutan lisis (cell lysis solution), larutan pengendap protein (protein precipitation solution) dan DNA hydration solution. Modifikasi metode Qiao sudah diverifikasi oleh Prof. Dr. drh. Mirnawati Sudarwanto di Justus Liebig University Gissen
Jerman. Ekstrasi kuning telur dilakukan dengan cara sebelum telur dibuka, kerabang
telur didisinfeksi dengan alkohol 70%. Putih telur dipisahkan dari kuning telur
menggunakan kertas saring steril. 100 µl kuning telur dimasukkan ke dalam mikrotub eppendorf 1.5 ml yang berisi 300 µl larutan lisis (cell lysis solution) dan dihomogenkan
dengan vortex. Tambahkan 5 µl proteinase K (50 mg/ml), dihomogenkan selama 30 detik dan setelah itu diinkubasi 55 ºC dalam waterbath selama 3 jam. Tambahkan 2 µl RNase A solution dan diinkubasi 37 ºC selama 30 menit. Tambahkan 100 µl larutan pengendap protein (protein precipitation solution), dihomogenkan selama 30 detik dan diinkubasi pada temperatur kamar selama 15 menit. Tambahkan 500 µl kloroform
dingin, dihomogenkan 30 detik dan diinkubasi pada temperatur kamar selama 5 menit.
Sentrifus pada 14000 rpm pada suhu 4 ºC selama 5 menit. Sebanyak 300 µl supernatan
(lapisan bening) diambil dan dipindahkan ke mikrotub baru. Tambahkan 500 µl
isopropanol dingin, dibolak-balik sampai terlihat benang-benang putih dan disentrifus
14000 rpm pada suhu 4 ºC selama 5 menit. Supernatan dikeluarkan secara hati-hati
dengan mikropipet. Endapan putih yang diperoleh ditambahkan 500 µl etanol 70% dingin
melalui dinding mikrotub dan disentrifus 14000 rpm pada suhu 4 ºC selama 5 menit.
Supernatan dikeluarkan secara hati-hati dengan mikropipet dan endapan dibiarkan
dikondisikan pada suhu 60 ºC selama 3 menit dan kemudian dihomogenkan agar DNA
terlarut secara merata. Setelah disentrifus beberapa detik diletakkan diatas es. Sebanyak 190 µl hydration solution yang telah ditambahkan dengan 10 µl larutan DNA dimasukkan
ke dalam spektrofotometer. Untuk menghitung konsentrasi DNA maka digunakan rumus :
konsentrasi DNA (µg/ml) = A260 x 50 x 200 (faktor pengenceran), sedangkan tingkat
kemurnian DNA dihitung dengan membagi nilaiOD260 dengan OD280.
Deteksi
C. burnetii
pada Telur dengan Metode
Nested Polymerase Chain
Reaction
(
Nested
PCR)
Penelitian ini bertujuan untuk mengetahui adanya DNA C. burnetii pada telur ayam dengan metode nested PCR.
Larutan DNA yang akan digunakan sebagai sampel merupakan hasil pengukuran
konsentrasi dan kemurnian DNA menggunakan elektroforesis. Primer oligonukeotida
yang digunakan adalah produk (Sigma), yaitu primer OMP1 (5’-AGT AGA AGC ATC CCA
AGC ATT G-3’), OMP2 (5’-TGC CTG CTA GCT GTA ACG ATT G-3’), OMP3 (5’-GAA
GCG CAA CAA GAA GAA CAC-3’) dan OMP4 (5’-TTG GAA GTT ATC ACG CAG TTG-3”), yang didisain dari sekuen nukleotida gen com 1 yang mengkode OMP 27 kD.
Amplifikasi DNA pertama dilakukan dalam volume 30 µl yang berisi 13 µl air milli Q, 10 x PCR bufer 5 µl dengan konsentrasi MgCl2 15 mM (Sigma), 5 µl dNTP 2 mM
(Vivantis), 0.5 µl primer OMP1 100 µM, 0.5 µl primer OMP2 100 µM, 1 µl Taq DNA polymerase (Vivantis) dan 5 µl sampel DNA. Analisis PCR dilakukan berturut-turut, yaitu temperatur 94 °C, 3 menit (pre-denaturasi), 1 putaran, kemudian denaturasi pada temperatur 94 °C, 1 menit, pelekatan (annealing) pada temperatur 54 °C, 1 menit dan pemanjangan (extention) pada temperatur 72 °C, 1 menit selama 36 kali siklus serta
temperatur 72 °C, 4 menit dan hold temperature 4 ºC, 1 putaran dalam DNA thermal cycler. Hasil PCR disimpan pada Amplifikasi kedua yaitu campuran reaksi dan kondisinya
sama dengan amplifikasi pertama kecuali primer dan DNA template. Primers digunakan OMP3 dan OMP4 serta 5 µl produk hasil amplifikasi pertama digunakan sebagai DNA template. Kontrol positif adalah 5 µl dari DNA C. burnetii
Produk amplifikasi PCR dianalisa dengan elektroforesis menggunakan 2% gel
23
agarose direndam dengan 1 x TAE, maka ke dalam sumur dimasukkan sampel, kontrol (positif) dan DNA molecular weight standards (100 pb DNA ladder) yang telah dicampur loading dye dengan perbandingan 1:9. Elektroforesis dijalankan dengan tegangan
100 volt selama 45 menit. Kemudian diwarnai dengan etidium bromida (0.5 µg/ml) selama 30 menit, dilihat hasilnya menggunakan UV illumination pada 320 nm dan dipotret dengan kamera polaroid. Hasil nested PCR dinyatakan positif apabila terlihat adanya
produk yang spesifik dari primer internal (OMP3-OMP4) yang menghasilkan fragmen 438
pb.
Sensitivitas dan Spesifisitas
Nested Polymerase Chain Reaction
(
Nested
PCR) untuk Mendeteksi DNA
C. burnetii
Penelitian ini bertujuan untuk mengetahui tingkat sensitivitas dan spesifisitas
metode nested PCR dibandingkan dengan PCR untuk mendeteksi keberadaan DNA C. burnetii.
Untuk menentukan tingkat optimasi (optimalisasi) nested PCR dan PCR dalam mendeteksi keberadaan DNA C. burnetii, maka pengujian dilakukan dengan mengukur konsentrasi awal DNA menggunakan spektrofotometer. Konsentrasi DNA dibuat menjadi
150 nano gram/µl (ng/µl), sehingga diperoleh konsentrasi akhir dalam reaksi PCR sebesar 75 ng/µl. DNA C. burnetii tersebut diencerkan menjadi 30 ng/µl, 15 ng/µl, 3 ng/µl,
300 piko gram/µl (pg/µl), 30 pg/µl, 3 pg/µl, 0.3 pg/µl dan 0.03 pg/µl. Masing-masing
konsentrasi tersebut diamplifikasi dengan menggunakan dua pasang primer (OMP1-OMP2 dan OMP3-OMP4) untuk nested PCR dan satu pasang primer eksternal
(OMP1-OMP2) untuk PCR.
Untuk mengetahui tingkat spesifitas metode nested PCR, maka dilakukan pendeteksian terhadap bakteri seperti Brucella abortus ATCC 23452, Escherichia coli
ATCC 25922, Pseudomonas aeruginosa ATCC 9027 dan Campylobacter jejuni ATCC 33291. Bakteri-bakteri tersebut merupakan satu kelompok dengan C. burnetii dari famili Proteobacteria.
Untuk primer OMP1-OMP2 dan OMP3-OMP4, amplifikasi pertama dilakukan dalam volume 50 µl yang berisi 13 µl air milli Q, 10 x PCR bufer 5 µl dengan konsentrasi
MgCl2 15 mM (Sigma), 5 µl dNTP 2 mM (Vivantis), 0.5 µl primer OMP1100 µM, 0.5 µl
primer OMP2 100 µM, 1 µl Taq DNA polymerase (Vivantis) dan 25 µl sampel DNA
(5 pg/µl). Analisis PCR dilakukan berturur-turut, yaitu temperatur 94 °C, 3 menit