KAJIAN FILTRASI SARI BUAH NANAS DENGAN
MENGGUNAKAN MEMBRAN SELULOSA ASETAT
Oleh:
FARIDA HURIAWATI
G74102026
PROGRAM STUDI FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Farida Huriawati. G74101029. Kajian Filtrasi Sari Buah Nanas dengan Menggunakan Membran Selulosa Asetat. Dibimbing Oleh: Jajang Juansah, MSi dan Dr. Ki Agus Dahlan.
ABSTRAK
KAJIAN FILTRASI SARI BUAH NANAS DENGAN
MENGGUNAKAN MEMBRAN SELULOSA ASETAT
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
Pada Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Oleh:
Farida Huriawati
G74102026
PROGRAM STUDI FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Kajian Filtrasi Sari Buah Nanas dengan Menggunakan Membran
Selulosa Asetat.
Nama : Farida Huriawati
NRP
: G74102026
Menyetujui,
Pembimbing I Pembimbing II
Jajang Juansah, MSi. Dr. Ki Agus Dahlan
NIP. 132 311 933 NIP. 131 663 021
Mengetahui,
Dekan Fakultas MIPA
Dr. Yonny Koesmaryono, M.S.
NIP. 131 473 999
Riwayat Hidup
Penulis dilahirkan di Ponorogo pada tanggal 21 juli 1983 sebagai putri bungsu dari dua bersaudara pasangan Bapak Kateni dengan Ibu Darmini.
Penulis menyelesaikan pendidikan dasar di SD Negeri Kepatihan 11 Ponorogo pada tahun 1996. Pada tahun yang sama penulis melanjutkan pendidikan di SLTP Negeri 1 Ponorogo sampai tahun 1999, kemudian penulis melanjutkan pendidikan di SMU Negeri 1 Ponorogo sampai tahun 2002, pada tahun 2002 penulis melanjutkan pendidikan S1 jurusan Fisika Fakultas Matematika dan Ilmu Pengetahuan Alam IPB melalui jalur USMI (Undangan Seleksi Masuk IPB).
PRAKATA
Alhamdulillahirrabbil`alamin
Kepada yang senantiasa memberikan hikmah, kemudahan, keajaiban, rizki, hidayah, dan nikmat yang tidak akan pernah terhitung nilainya, sehingga penulis tetap diberikan dan memiliki rasa teguh dan sabar serta semangat dalam menyusun karya ilmiah ini. Karya ilmiah ini telah selesai dilaksanakan pada bulan agustus 2005 -maret 2006, di laboratorium biofisika IPB dan laboratorium kimia analitik IPB dengan judul “ Kajian Filtrasi Sari Buah Nanas dengan Menggunakan Membran Selulosa Asetat ”. penelitian ini dibimbing oleh: Bapak Jajang Juansah, MSi dan Bapak Dr. Ki Agus Dahlan.
Penulis memahami bahwa karya ilmiah ini jauh dari sempurna, tetapi penulis harap semoga skripsi ini bermanfaat bagi perkembangan ilmu pengetahuan.
Pada kesempatan ini penulis ingin mengucapkan rasa terimakasih kepada:
Bapak Jajang Juansah, MSi dan Bapak Dr. Ki Agus Dahlan, selaku Dosen pembimbing yang telah membimbing, mengarahkan, dan senantiasa memberikan motivasi melalui setiap apa yang telah dan pernah diberikan, sehingga tersusunnya karya ilmiah ini. Hibah penelitian SP4.
My family (bapak, ibu dan mas kris), untuk kalianlah kuhaturkan karya ini. Terima kasih atas segala limpahan kasih sayang yang tercurah dan lantunan do`a yang senantiasa diberikan.
Staff dan laboran departemen fisika IPB (Pak Rahmat dan Pak Parman), staff dan laboran kimia analitik departemen kimia IPB (Ibu Enung dan Pak Eman), atas semua bantuan dan kerjasamanya.
Pak Ardian Arif sebagai dosen penguji atas saran dan masukannya . Pak Firman atas semua bantuannya.
My best friends warga BRAVO (ety, dewies, ima, melly, opi, teh ade, teh enda) i love you all sedunia, makasih atas segala bantuan, do`a, semangat dan kebersamaan kalian selama ini.
Teman-teman fisika 39 (isa, ropi, wahyu, fera, cece, neng, eka, reni, leta, laina, rahma, sonny, nono, anam, niko, kofir, ekojambi, arif, luthfan, marwan, tedi, rian, erus, budi, teguh, didit, ananto,ihsan, tio), semoga apa yang pernah kita alami bersama menjadikan kita merasa bagian dari yang lain.
Perpustakaan LSI, Perpustakaan FMIPA, Perpustakaan Departemen Fisika. Serta semua pihak yang tidak dapat penulis sebutkan satu per satu.
Dalam tulisan ini masih terdapat kekurangan, oleh karena itu saran dan kritik membangun sangat penulis harapkan untuk hasil yang lebih baik.
Bogor, Mei 2006
DAFTAR ISI
Halaman
PRAKATA...………..………...vi
DAFTAR ISI………..…………...vii
DAFTAR GAMBAR………...ix
DAFTAR TABEL………...x
DAFTAR LAMPIRAN...xi
PENDAHULUAN Latar Belakang...1
Tujuan Penelitian...1
Manfaat Penelitian...1
Hipotesis...1
Perumusan Masalah...1
TINJAUAN PUST AKA Botani dan Morfologi Nanas………...1
Manfaat Nanas………...2
Jenis Nanas………...2
Tanah dan Iklim Pertumbuhan Nanas………... ...2
Sari Buah Nanas………...3
Membran ………...3
Membran Selulosa Asetat...4
Proses Pemisahan dengan Membran………...5
Filtrasi Membran………...5
Peralatan Filtrasi Membran...5
Fluks Membran………...6
Rejeksi Membran... ...6
Konduktansi Membran...7
Pasteurisasi………...8
Karakteristik Fisik dan pH Kerapatan... ...8
Viskositas...8
Kekeruhan...9
Total Padatan Terlarut... ...9
pH... ...9
BAHAN DAN METODE Waktu Penelitian... ...9
Pembuatan Sari Buah Nanas... ... ...9
Proses Filtrasi Sari Buah Nanas... ...10
Karakterisasi Sari Buah Nanas... ...10
Pengukuran Konduktansi Membran... ... ...10
Prosedur Karakterisasi Pengukuran Kerapatan Sari Buah Nanas... ... ...10
Pengukuran kekentalan Sari Buah Nanas... ... 11
Pengukuran Kekeruhan Sari Buah Nanas... ... ...11
Pengukuran Total Padatan Terlarut Sari Buah Nanas... ... ...11
Pengukuran pH Sari Buah Nanas... ... 11
Analisis Data...11
HASIL DAN PEMBAHASAN Nilai Permeate Membran... ...12
Nilai Fluks Membran………...12
Nilai Rejeksi Membran...13
Karakterisasi Sari Buah Nanas Kerapatan………...13
Kekentalan………...14
Kekeruhan………....15
Total Padatan Terlarut……….. ..16
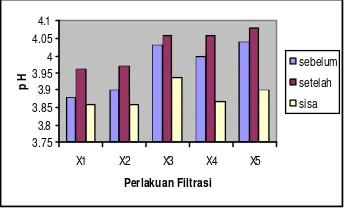
pH………...17
Pengaruh Fouling pada Konduktansi Membran...18
Pengaruh Suhupada Konduktansi Membran...19
Pengaruh Fouling pada Ukuran Pori Membran... 19
KESIMPULAN DAN SARAN... ...19
DAFTAR PUSTAKA ………...20
DAFTAR GAMBAR
Halaman
Gambar 1. Nanas………...……….3
Gambar 2. Struktur Molekul Membran Selulosa Asetat...4
Gambar 3. Morfologi Membran Selulosa Asetat………...…... …...4
Gambar 4. Metode Dead End dan Cross Flow Filtration...5
Gambar 5. Kurva Perubahan Fluks Membran terhadap Waktu………..…….…...6
Gambar 6. Fenomena Fouling………..………...6
Gambar 7. Diagram Alir Pembuatan Sari Buah Nanas...10
Gambar 8. Skema Rangkaian dalam Pengukuran Konduktansi Membran...10
Gambar 9. Volume Permeate Sari Buah Nanas pada Beberapa Perlakuan Filtrasi... 12
Gambar 10. Kurva Hubungan Fluks terhadap Waktu...12
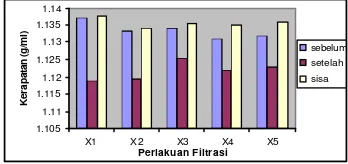
Gambar 11. Kerapatan Sari Buah Nanas pada Beberapa Perlakuan Filtrasi...13
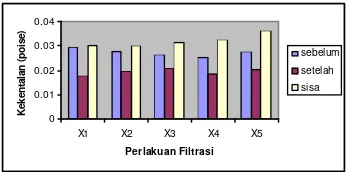
Gambar 12. Kekentalan Sari B uah Nanas pada Beberapa Perlakuan Filtrasi...14
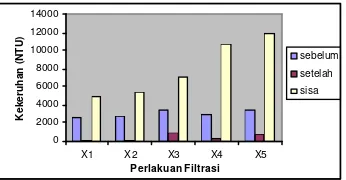
Gambar 13. Kekeruhan Sari Buah Nanas pada Beberapa Perlakuan Filtrasi...15
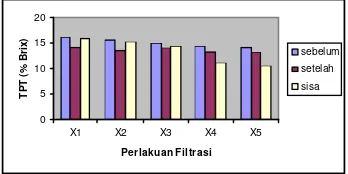
Gambar 14. TPT Sari Buah Nanas pada Beberapa Perlakuan Filtrasi... ...16
DAFTAR TABEL
Halaman
Tabel 1. Nilai Gizi Buah Nanas Segar (per 100 gram )………...2
Tabel 2. Spesifikasi Membran Selulosa Asetat...4
Tabel 3. Pasteurisasi yang Dilakukan terhadap Beberapa Contoh Makanan dan Minuman... ...8
Tabel 4. Nilai Rejeksi Membran...13
Tabel 5. Konduktansi Membran pada Suhu 250C...18
Tabel 6. Konduktansi Membran Bersih pada Beberapa Variasi Suhu...19
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Diagram Alir Penelitian...22
Lampiran 2. Kandungan Mineral dan Vitamin dalam Sari Buah yang Dikal engkan (dalam 100 gram)...23
Lampiran 3. Jenis-Jenis Membran Filtrasi...23
Lampiran 4. Volume Permeate Membran...24
Lampiran 5. Fluks Membran...25
Lampiran 6. Karakt erisasi Fisik Membran...25
Lampiran 7. Rekapitulasi Data Hasil Penelitian...26
Lampiran 8. Konduktansi Membran...28
Lampiran 9. Rekapitulasi Data Ln (G) dan 1/T...30
Lampiran 10. Kurva hubungan Ln (G) dan 1/T...31
Lampiran 11. Jari -jari Pori Membran ...31
Lampiran 12. Persentase Perubahan Karakterisasi Sari Buah Nanas...32
Lampiran 13. Peralatan Penelitian...33
Lampiran 14. Keadaan Sari Buah Nanas pada Proses Filtrasi...35
Lampiran 15. Hasil Pemotretan Membran Selulosa Asetat Sebelum dan Setelah Proses Filtrasi...35
PENDAHULUAN
Latar Belakang
Nanas (Ananas comusus) merup akan salah satu jen is buah tropis yang cukup populer dan banyak digemari oleh masyarakat luas karena rasa dan aromanya yang khas. Walaupun masa panen buah nanas terjadi sepanjang tahun, namun terdapat masa panen raya yang membuat hasil panen nanas berlimpah, sehingga sebagian dari buah nanas terpaksa dijual dengan harga murah atau dibiarkan membusuk di kebun.
Dalam proses industri pangan, buah nanas umumnya diperdagangkan dalam bentuk nanas kaleng, sari buah nanas, dan jelly. Sari buah nanas dapat digunakan sebagai sirup dalam pengalengan buah nanas, juga dapat dikonversi menjadi anggur nanas dan vinegar nanas serta dapat dihasilkan asam sitrat dan kalsium sitrat (Muljohardjo, 1983). Pengolahan melalui proses industri dilakukan dengan tujuan untuk memperpanjang masa simpan dan mempermudah dalam pemasarannya serta untuk meningkatkan nilai ekonomis dari buah nanas.
Teknologi membran buatan sangat bermanfaat dan telah banyak digunakan dalam berbagai bidang aplikasi, seperti pada teknologi industri pangan, biologi, kimia dan kesehatan. Efektivitas kerja membran ditentukan oleh karakteristik dan respon terhadap lingkungannya. Dari segi energi, teknologi membran tergolong teknologi yang hemat energi dan bersih karena saat mengoperasikannya tidak diperlukan energi yang besar. Selain itu juga tidak diperlukan zat -zat kimia pendukung yang menimbulkan masalah baru sehubungan dengan limbah. Membran merupakan pilihan yang tepat untuk keperluan penyaringan, pemisahan dan pemurnian suatu larutan.
Teknologi membran dapat diaplikasikan dalam pengolahan buah-buahan, seperti buah nanas. Namun kajian tentang hal ini masih belum banyak dikemukakan.
Tujuan Penelitian
Penelitian ini dilakukan untuk lebih memahami aplikasi dari teknologi membran yang salah satunya sebagai filter.
Pada penelitian ini digunakan membran selulosa asetat untuk memfilter sari buah nanas hingga dapat dihasilkan sari buah nanas murni.
Selain itu penelitian ini juga bertujuan untuk mengetahui perubahan nilai fluks membran dan nilai konduktansi membran
akibat fouling pada pori-pori membran setelah proses filtrasi serta sifat fisik dan kimia sari buah nanas sebelum, setelah dan sisa proses filtrasi.
Manfaat Penelitian
Manfaat dari penelitian ini adalah untuk pengembangan teknologi membran dalam berbagai bidang aplikasi, terutama dalam industri pangan.
Dapat memberikan informasi tentang fenomena atau karakteristik membran selulosa asetat yang diinteraksikan dengan sari buah nanas.
Hipotesis
• Semakin jernih permeate yang dihasilkan semakin baik kerja membran.
• Semakin besar volume permeate
yang dihasilkan, maka semakin tinggi efektivitas dan efisiensi membran.
• Semakin besar kecepatan pengadukan dan tekanan yang diberikan, maka proses filtrasi akan semakin cepat dan nilai fluksnya akan semakin meningkat.
• Fenomena fouling yang terjadi akan menyebabkan menurunnya nilai fluks membran dan konduktansi membran.
• Fenomena fouling yang terjadi mengakibatkan jari-jari pori membran semakin kecil.
Perumusan Masalah
Masalah utama dalam penelitian ini adal ah bagaimana kecepatan pengadukan dan tekanan mempengaruhi proses filtrasi sari buah nanas.
Sifat fisik dan pH dari hasil filtras i sangat menentukan efektivitas kerja dari membran selulosa asetat. Fenomena fouling
yang terjadi pada pori-pori membran setelah filtrasi mempengaruhi fluks membran dan konduktansi membran.
TINJAUAN PUSTAKA
Botani dan Morfologi Nanas
kumpulan buah yang menjadi satu (Bautista et al, 1983).
Tanaman nanas berasal dari Brazil. Pada saat ini penghasil utama buah nanas adalah Kepulauan Hawai dan daerah penghasil lainnya adalah Taiwan, Malaysia, Australia, Philipina, Thailand, dan beberapa negara di Afrika ( Dull, 1971).
Sistematika buah nanas sesuai dengan taksonominya (Muljohardjo, 1984) adalah sebagai berikut :
Divisio : Spermatofita Sub-divisio : Angiospermae Klasis : Monokotiledoneae Ordo : Farinosae Familia : Bromellaceae Genus : Ananas Spesies : Ananas comusus
Menurut kelompok kerja penulisan buku buah-buahan (BN-LIPI), tanaman nanas berbentuk semak yang mempunyai batang semu dengan tinggi 30-50 cm, daunnya panjang dan pada tepi daun terdapat duri.
Manfaat Nanas
Dalam buah nanas banyak terkandung zat -zat yang berguna bagi tubuh manusia. Zat-zat yang terkandung tersebut antara lain: vitamin C, vitamin A dan mineral.
Nanas banyak mengandung vitamin C yang bermanfaat memelihara kesehatan gigi dan gusi, mempercepat sembuhnya luka-luka, menghindarkan tubuh dari penyakit yang dikenal dengan nama scurvy (skorbut) serta melawan kecenderungan pendarahan pembuluh darah yang halus.
Vitamin A dalam buah nanas sangat baik bagi kesehatan mata. Selain itu, buah nanas mengandung mineral-mineral yang sangat baik untuk nutrisi tubuh. Adapun nilai giz i dari buah nanas tertera pada T abel 1 di bawah ini.
Tabel 1. Nilai Gizi Buah Nanas Segar (per 100 gram)
Zat Gizi Nilai Gizi
Karoten/Vitamin A (S.I) Thiamin/VitaminB1 (mg) Riboflavin/Vitamin B2 (mg) Asam askorbat/Vitamin C (mg) Protein (% berat basah) Karbohidrat (% berat basah) Lemak (% berat basah) Kalsium (mg) Fosfor (mg) Zat Besi (mg) Air (% berat basah)
69 0,04 0,03 13 0,21 7,26 0,11 8 27 0,2 85, 3
Sumber: Direktorat Gizi Departemen Kesehatan RI, 1972.
Jenis Nanas
Terdapat beberapa varietas nanas diantaranya adalah sebagai berikut: Cayenne, Queen, Spanish, Abacaxi, Manipure
(Sulunkhe dan Desai, 1984). Walaupun tanaman nanas memiliki banyak macam dan jenis, namun hanya beberapa jenis saja yang memiliki nilai komersial yang cukup tinggi . Jenis-jenis tersebut diantaranya adalah: varietas Spanish, Queen dan Cayenne
(Muljohardjo, 1983). Ciri dari varietas tersebut adalah (Rismunandar, 1983) :
1. Varietas Spanish
Varietas Spanish memiliki daun yang kecil panjang dan berduri halus sampai kasar. Buahnya bulat, bermata pipih dan besar, serta daging buahnya berwarna putih. Jenis ini cocok dikalengkan atau dikonsumsi segar.
2. Varietas Queen
Varietas Queen memiliki daun yang pendek, berduri tajam dan membengkok ke belakang. Buahnya berbentuk kerucut dan mata buahnya menonjol. Daging buahnya berwarna kuning dan memiliki aroma serta rasa yang manis. Jenis Queen ini yang terkenal adalah Natal Queen dan
Repley Queen. Nanas Palembang dan Bogor termasuk jenis ini.
3. Varietas Cayenne
Jenis ini terdiri dari varietas Smooth Cayenne dan Cayenne Lisse. Smooth Cayenne memiliki daun yang berduri, sedangkan Cayenne Lisse
tidak berduri. Buahnya berbentuk silindris dengan berat 2,3-3,6 kg, daging buahnya berwarna putih kekuningan atau kuning. Penampilan buah bagus dan bermata datar. Jenis
Cayenne tumbuh di Kabupaten Bandung, daerah dataran tinggi Subang dan Pulau Bintan Riau.
Tanah dan Iklim Pertumbuhan Nanas
Sari Buah Nanas
Sari buah (fruit juice) merupakan cairan yang jernih atau hampir jernih yang tidak mengalami proses fermentasi, diperoleh dengan cara pengepresan atau penghancuran buah-buahan yang telah masak dan segar.
Di Indonesia pembuatan sari buah pada umumnya masih dilakukan secara sederhana dan biasanya sari buah tersebut mengandung zat pektin yang menyebabkan cairan sari buah keruh dan terdapat endapan. Pengolahan buah menjadi sari buah selain dapat menghasilkan produk yang lebih awet, juga merupakan minuman yang praktis, rasanya enak dan menyegarkan serta bermanfaat bagi kesehatan tubuh (Winarno, 1997). Kandungan mineral dan vitamin dalam sari buah terdapat dalam Lampiran 2.
Gambar 1. Nanas.
Membran
Secara umum membran dapat didefinisikan sebagai suatu lapisan tipis semipermeabel diantara dua fasa yang berbeda karakter, fasa pertama adalah feed atau larutan pengumpan dan fasa kedua adalah permeate
atau hasil pemisahan. Fungsi utama dari suatu membran ialah sebagai penahan semipermeabel yang dapat melewatkan dan menahan komponen tertentu dalam suatu campuran (Djumali dan Darnoko, 1990). Salah satu fungsi dari membran adalah yang memisahkan materi berdasarkan sifat fisiknya (Hartomo, 1994). Kemampuan pemisahan yang dimiliki membran untuk melewatkan suatu komponen atau molekul diakibatkan oleh adanya perbedaan sifat fisik atau kimia diantaranya tekanan, konsentrasi, potensial listrik dan temperatur (Kurniawan, 2002).
Berdasarkan eksistensinya membran terdiri dari membran alami dan membran sintetik. Membran alami adalah membran pada sistem dan proses kehidupan makhluk hidup. Komponen utama membran alami adalah lipid dan protein. Sedangkan membran sintetik adalah membran buatan, yang dapat terbuat dari bahan alami atau bahan
non-alami. Membran buatan digunakan untuk kepentingan penelitian dan pengujian sifat-sifat membran biologi dan juga untuk kepentingan industri. Kualitas membran buatan diusahakan menyerupai membran alami. Kualitas membran buatan ditentukan oleh sifat -sifatnya. Salah satu contoh dari membran buatan adalah membran selulosa as etat. Membran ini merupakan polimer yang mengandung selulosa asetat. Teknologi membran buatan banyak dimanfaatkan untuk industri kimia dan bahan makanan. Efektivitas kerja membran buatan ditentukan oleh karakteristik dan respon terhadap lingkungan (Juansah, 2002).
Berdasarkan bentuknya membran terdiri dari membran simetri dan asimetri. Membran simetri memiliki struktur pori yang homogen dan relatif sama, ketebalannya antara 10-200 µm. Sedangkan membran asimetrik memiliki ukuran dan kerapatan yang tidak sama. Membran jenis ini memiliki dua lapisan, yaitu lapisan kulit yang tipis dan rapat (skin layer) dengan ketebalan < 0,5 µm serta lapisan pendukung yang berpori dengan ketebalan 50-200 µm (Maryati, 50-2003).
Berdasarkan ukuran pori dikenal membran jenis mikrofiltrasi dengan ukuran pori kisaran mikrometer, ultrafiltrasi dengan ukuran pori kisaran mikrometer sampai nanometer, dan hiperfiltrasi dengan ukuran pori sangat kecil sampai yang tidak memiliki pori sejati (Hartomo, 1994).
Berdasarkan kelistrikannya membran terdiri atas membran bermuatan tetap dan membran bermuatan netral. Membran bermuatan tetap dapat dilalui oleh ion-ion tertentu. Membran bermuatan tetap yang hanya dapat dilalui oleh kation saja disebut membran penukar kation (MPK), sedangkan jika anion saja disebut membran penukar anion (MPA). Selain kedua membran tersebut ada juga membran yang merupakan gabungan keduanya yang disebut Double Fixed Charge Membrane. MPK dan MPA memiliki karakter yang berbeda dan pada aplikasinya dapat digunakan bersamaan. Membran bermuatan tetap ini dapat digunakan dalam proses industri, seperti proses elektrodialisis, fuel cell
daya tahan terhadap tekanan dan suhu, resistivitas dan konduktansi serta karakteristik kelistrikan lainnya (Rakhmanudin, 2005).
Membran Selulosa Asetat
Membran selulosa asetat merupakan membran polimer sintetik. Pada tahun 1960an, Loeb dan Sourirajan
mengembangkan membran selulosa asetat dari bahan polimer selulosa diasetat di Universitas California Los Angeles ( Djumali dan Darnoko, 1990).
Pembuatan membran selulosa asetat dilakukan dengan melarutkan campuran selulosa asetat serbuk, kemudian direaksikan dengan asam anhidrid, memanfaatkan asam cuka (acetid acid) sebagai bahan pelarut dan
perchloric acid atau sulphuric acid sebagai katalisator. Kemudian dicetak menjadi lapisan
film di atas lembaran kaca. Sejumlah kecil pelarut diuapkan, lalu dicelupkan ke air dingin (100C) untuk membentuk membran. Membran yang basah kemudian dicelupkan ke air panas (900C) untuk menguapkan kembali pelarutnya, lalu direndam dalam campuran larutan hidrokarbon, dan selanjutnya dikeringkan di udara terbuka. Struktur molekul dari membran selulosa a setat terdapat pada G ambar 2 di bawah ini.
Gambar 2. Struktur Molekul Membran Selulosa Asetat.
Membran selulosa asetat merupakan membran dengan morfologi as imetrik, seperti terlihat pada G ambar 3. Membran ini termasuk dalam kelompok membran nanofiltrasi yang tidak bermuatan. Membran selulosa asetat dalam filtrasi digunakan untuk menghilangkan koloid, mikroba, pirogen, partikel dengan modul higienis (Hartomo, 1994).
Gambar 3. Morfologi Membran Selulosa A setat.
Membran selulosa asetat memiliki keunggulan dan kelemahan. Keunggulannya antara lain: ideal untuk sampel yang didasari kandungan air, membran selulosa asetat mengikat lebih sedikit protein, ideal untuk media kultur jaringan filtrasi dan sifat sensi tivitas objek biologi , laju alir permeate (fluks) tinggi dan rejeksi garam tinggi, mudah dibuat dan bahan dasar merupakan bahan yang terbarukan, relatif kuat, tidak larut dalam alkohol (Djumali dan Darnoko, 1990). Kelemahannya adalah: kisaran suhu sangat sempit (membran selulosa asetat biasanya dioperasikan tidak lebih dari suhu 300C), kisaran pH yang rendah biasanya antara 3-6 (pada kondisi asam, membran selulosa asetat dilaporkan dapat tahan sampai 4 tahun bila digunakan pada pH 4-5 dan tahan sampai 2 tahun pada pH 6 serta hanya beberapa hari saja bila digunakan pada pH 1 atau 9 kisaran pH yang rendah sering menimbulkan masalah pada waktu pencucian membran, karena larutan pencuci membran biasanya bersifat asam), tidak tahan klorin (klorin merupakan bahan pencuci yang umum digunakan dalam industri pangan membran selulosa asetat dapat teroksidasi oleh klorin konsentrasi bebas tertinggi yang disarankan adalah 1mg/L), dapat mengalami pengerutan dan pengompakan, dapat mengalami biodegradasi, membran yang mudah mengalami perubahan kimia (Djumali dan Darnoko, 1990).
Tabel 2. Spesifikasi Membran Selulosa A setat
Adsorpsi 0,1 µg/cm2 untuk serum
albumin sapi dengan ukuran pori 0,2 µm.
Compatibility atau kesesuain
Stabil pada kisaran pH 4-8, dan mengalami hambatan terhadap banyak alkohol,
hydrocarbon dan minyak. Laju aliran Nilai rata-rata untuk air per
cm2 pada tekanan 1 bar, 22ml/menit untuk 0,2 µm, 69 ml/menit untuk 0,45 µm, 130 ml/menit untuk 0,65 µm dan 200 ml/menit untuk 0,8 µm ukuran pori.
Limits atau keterbatasan
Suhu maksimum, 1800C
Sterilisasi Dengan autoclaving (pada 1210C atau 1340C), dengan radiasi-gamma atau ethylene oxide
Validasi atau pengesahan
Hubungan nilai titik gembung ukuran pori membran 0,2 µm untuk mampu mensterilisasi pada filtrasi telah disahkan oleh Standard Bacteria Challenge Tests
Proses Pemisahan dengan Membran
Proses pemisahan dengan membran terdiri dari beberapa macam, hal ini dapat digolongkan berdasarkan parameter penggeraknya (Kurniawan, 2002), yaitu:
v Proses filtrasi, yaitu proses pemisahan dengan membran dimana tenaga penggeraknya adalah berupa perbedaan tekanan. Ada tiga macam proses filtrasi pada membran yaitu osmosa balik, ultrafiltrasi dan mikrofiltrasi.
v Dialisa, yaitu proses pemisahan dengan membran dimana tenaga penggeraknya berupa perbedaan konsentrasi.
v Elektrodialisa, yaitu proses pemisahan dengan membran dimana tenaga penggeraknya berupa beda potensial listrik.
Filtrasi Membran
Filtrasi adalah salah satu proses pemisahan yang dapat dibedakan menjadi beberapa jenis tergantung pada bahan yang akan dipisahkan serta tingkat pemisahan yang diinginkan (Djumali dan Darnoko, 1990). Filtrasi membran bekerja dengan melewatkan cairan melalui suatu membran tipis yang berbentuk seperti piringan. Filtrasi digunakan untuk memisahkan partikel yang tidak diinginkan.
Secara umum filter dapat digolongkan dalam dua kelompok, yaitu filter dalam (depth filter) dan filter saringan (screen filter). Filter
dalam terbuat dari matriks serat atau butiran yang tersusun secara acak sehingga membentuk suatu massa yang memiliki rongga -rongga. Partikel atau koloid akan terpisah dari cairan karena terperangkap atau terabsorpsi dalam matriks filter. Sedangkan
filter saringan memisahkan partikel -partikel di atas permukaannya seperti halnya saringan. Strukturnya lebih kuat, seragam dan sinambung dengan ukuran pori yang dapat diatur dengan baik pada waktu pembuatannya.
Filter membran termasuk dalam golongan
filter ini. Karena ukuran porinya tertentu filter
ini dapat diklasifikasikan secara absolut atau kuantitatif. Keunggulan lain dari filter
saringan ialah kehilangan bahan karena terserap dalam filter jauh lebih kecil dibandingkan dengan filter dalam (Djumali dan Darnoko, 1990).
Terdapat beberapa membran filtrasi diantaranya: membran mikrofiltrasi, ultrafiltrasi, Reverse Osmosis (RO), elektrolisis, elektrofiltrasi dan dialisis (Taufik
Komara, 2004). Jenis -jenis membran filtrasi ditampilkan pada Lampiran 3.
Filtrasi membran memiliki beberapa keuntungan, antara lain: biaya operasi rendah, merupakan proses pemisahan yang bersih dan relatif sedikit menimbulkan kerusakan pada produk, dapat dilakukan pada suhu kamar dan tidak terjadi perubahan fase komponen (Djumali dan Darnoko, 1990).
Selain keuntungan, filtrasi membran juga mempunyai kelemahan, yaitu terjadinya
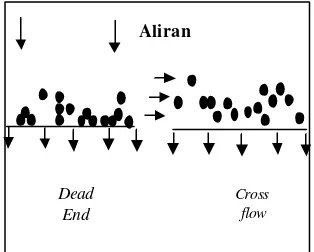
fouling. Fouling merupakan proses terakumulasinya komponen secara permanen akibat filtrasi itu sendiri. Fouling terjadi akibat interaksi yang sangat spesifik secara fisik dan kimia antara berbagai padatan terlarut pada membran (Djumali dan Darnoko, 1990). Kemungkinan terjadinya fouling sangat besar pada metode dead end filtration karena aliran larutan umpan secara vertikal. Peristiwa
fouling dapat dikurangi dengan metode cross flow filtration. Pada metode ini larutan umpan dialirkan secara horizontal.
Gambar 4. Metode Dead End dan Cross Flow Filtration.
Peralatan Filtrasi Membran
Peralatan filtrasi membran tersedia dalam berbagai ukuran, bentuk dan konfigurasi. Setiap jenis memiliki keunggulan dan kelemahan tersendiri. Pemilihan jenis peralatan filtrasi membran tergantung dari sifat larutan dan komponen yang akan diproses.
Peralatan filtrasi membran skala laboratorium biasanya hanya digunakan untuk studi pendahuluan dalam aplikasi membran untuk proses tertentu seperti pemilihan jenis membran, uji permeabilitas komponen-komponen tertentu, studi pengikatan suatu senyawa dengan protein dan sebagainya. Beberapa peralatan filtrasi skala laboratorium antara lain (Djumali dan Darnoko, 1990):
Aliran
Dead End
1. Sel Buntu
Alat ini hanya cocok untuk pemisahan larutan yang sangat encer dengan volume yang sedikit. Tidak ada pengadukan sehingga terjadi polarisasi konsentrasi. Alat ini biasanya digunakan untuk studi pengikat (binding) antara ligan atau mineral dengan protein.
2. Sel Buntu Berpengaduk
Sistem ini memiliki pengaduk megnetik untuk mencegah terjadinya polarisasi konsentrasi. Walaupun demikian karena tidak ada resirkulasi, akumulasi padatan pada permukaan membran lama-lama akan terjadi juga.
3. Sel Bercelah Sempit
Untuk skala laboratorium alat ini merupakan alat terbaik dibandingkan dengan dua alat di atas. Adanya resirkulasi dan aliran silang membuat polarisasi konsentrasi jarang terjadi.
Fluks Membran
Fluks membran adalah volume yang mengalir melalui membran per unit satuan waktu dan luas (Damayanti, 2005). Terdapat beberapa parameter operasi yang mempengaruhi fluks , antara lain tekanan, konsentrasi umpan, temperatur, laju aliran dan turbulensi (Djumali dan Darnoko, 1990).
...(1)
Dimana, J = fluks (L/m2 jam), L= volume
permeate (liter), t = waktu (jam)
Suatu membran dapat dikatakan efektif dan efisien bila membran tersebut mempunyai nilai fluks yang tinggi. Masalah yang timbul ketika membran digunakan dalam proses filtrasi adalah adanya penurunan nilai fluks terhadap w aktu. Hal ini ditunjukkan pada Gambar 5.
Penurunan nilai fluks dalam proses filtrasi dipengaruhi oleh adanya fouling.
Fouling pada membran sangat sulit dihindari dalam proses filtrasi membran. Fouling terjadi akibat adanya molekul-molekul yang terakumulasi pada permukaan membran dan menempati pori-pori membran dan tersumbat di dalamnya. Fenomena fouling ini agak sulit untuk diamati secara langsung, tetapi pengaruh langsung terhadap karakteristik membran bisa diketahui, misalnya penurunan nilai fluks, perubahan nilai konduktansi dan lain sebagainya.
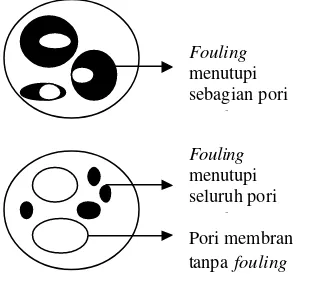
Mekanisme fouling yang terjadi pada pori-pori membr an diilustrasikan pada Gambar 6 di bawah ini.
Gambar 6. Fenomena Fouling.
Rejeksi Membran
Tingkat penolakan membran terhadap suatu komponen dikenal sebagai nilai rejeksi membran. Nilai rejeksi menunjukkan kemampuan suatu membran untuk menahan suatu komponen tertentu agar tidak melewati pori membran (Hartomo, 1994). Dalam penentuan nilai rejeksi membran berkaitan dengan porositas membran. Porositas merupakan perbandingan ukuran pori dengan luasan membran. Semakin kecil ukuran membran, maka porositas yang dihasilkan akan semakin tinggi dan sebaliknya. Jika nilai rejeksi membran menunjuk kan nilai 100% berarti membran mengalami rejeksi sempurna dan sebaliknya jika nilainya 0% menunjukkan larutan dan zat terlarut melewati membran dengan bebas.
…………(2)
Dimana, R = rejeksi membran, CP = konsentrasi komponen referen di dalam
permeate , Cf = konsentrasi komponen referen di dalam feed.
Fouling menutupi sebagian pori membran Fouling menutupi seluruh pori membran Pori membran tanpa fouling
fluks
waktu
Gambar 5. Kurva Perubahan Fluks Membran terhadap Waktu.
Rejeksi membran dapat juga diperoleh dengan persamaan berikut:
…………(3)
Dimana, R = rejeksi membran, ?p = kerapatan
permeate , ?f = kerapatan feed.
Konduktansi Membran
Suatu proses pemisahan dengan menggunakan membran netral ditentukan oleh geometri dan dimensi pori yang dimiliki oleh membran. Geometri dan dimensi pori membran dapat ditentukan dari sifat kelistrikannya. Salah satu sifat listrik yang dimiliki membran adalah konduktivitas. Sifat ini muncul karena adanya interaksi antara ion dengan membran. Besarnya konduktansi membran dapat diperoleh dengan menggunakan pendekatan persamaan:
G = nGP ... ...(4) Dimana, n adalah jumlah pori membran dan GP adalah konduktansi tiap pori dengan asumsi tiap pori-porinya identik.
Nilai GP ditentukan oleh beberapa faktor, diantaranya geometri pori, konsentrasi pori dan mobilitas ionnya. Dengan asumsi bahwa ion di dalam suatu medium dielektrik akan mengalami interaksi elektrostatik dengan membran, maka io n tersebut memiliki energi diri sebesar U. Energi ini merupakan integral dari medan listrik permukaan membran. Maka besarnya energi diri (U) untuk suatu ion dalam medium terbatas dengan konstanta dielektrik yang bervalensi z dan jarak a, adalah:
...(5)
Nilai U sangat bergantung pada . Nilai konstanta dielektrik membran berkisar 3-4 dan untuk larutan adalah 78,5.
Setelah melewati pori membran menyebabkan energi dalam ?U sebagai akibat adanya interaksi dengan membran yang bergantung pada seberapa dekat ion dengan membran.
... ...(6 ) dengan :
b = J ari -jari pori = K onstanta serapan
a = T ergantung konstanta geometri dan dielektrik (pendekatan 0,2)
z = B ilangan valensi ion
= Konstanta dielektrik membran q = Muatan ion
Nilai ?U juga dipengaruhi oleh konsentrasi ion, dengan Co sebagai konsentrasi ion yang jauh dari membran dan C sebagai konsentrasi pada pusat pori membran, maka ? koefisien partisi dari konsentrasi pada keseimbangan dikalkulasikan melalui statistik Boltzmann yaitu:
? = Co/C = exp (-?U/RT) ...(7) Jika P adalah konsentrasi kation dan N menunjukkan konsentrasi anion serta zp dan zn menunjukkan valensinya, maka diperoleh Co yaitu ionic strengh dari larutan:
zp P = zn N = Co ...(8) Nilai GP tiap pori membran terhadap ion yang mengalir diberikan oleh:
...(9)
dengan:
b = Jari-jari pori L = T ebal membran K = Konstanta Boltzmann (1.38662 x 10-23J/K) T = Suhu (Kelvin) R = K onstanta molar gas (0.891441 J/mol K)
Pada suhu yang semakin tinggi nilai G akan semakin membesar, ini berarti pergerakkan ion juga lebih besar. Selain itu koefisien partisi ? akan membesar, dengan demikian energi bebas akibat medan magnet juga membesar (Smith, J.R., K. Dahlan, dan Coster, 1992 dalam Kurniawan, 2002).
Secara eksperimen konduktansi membran dapat ditentukan melalui metode regresi linear dari persamaan:
...(10)
Dimana, A adalah faktor koreksi dan B adalah gradien kurva yang merupakan energi bebas ion. Nilai konduktansi adalah berbanding
ε
ε
0ε
) / 1 ( )ln( G = A + B T
a q z U ε πε 0 2 2 8 = b q z U m ε πε α 0 2 2 4 = ∆
(
)
kTL b D z D z C qGP o p p p n n n
2
2 γ + γ π
terbalik dengan nilai hambatan, hal ini sesuai dengan persamaan:
...(11 )
dimana R = ? L/A. Dalam penelitian ini nilai R diturunkan dari impedansi membran Z melalui persamaan:
...(12 )
dengan ? adalah beda fasa antara tegangan membran dan tegangan referensi yang terbaca pada osiloskop.
...(13 ) dengan:
Vm = Tegangan membran
Vs = Tegangan standar yang diberikan Rs = Hambatan standar yang diberikan dengan frekuensi 1 KHz dan hambatan 1000 ohm, ? = 0 sehingga R = Z dan nilai konduktansi membran adalah
...(14 )
Pasteurisasi
Pasteurisasi merupakan cara pengawetan yang menggunakan suhu pemanasan kurang dari 1000C. Pasteurisasi bertujuan untuk membunuh atau menginaktifkan sel-sel vegetatif dari mikroba, patogen atau pembusuk yang dapat tumbuh pada bahan pangan tersebut.
Pada Tabel 4, menunjukkan pasteurisasi yang dilakukan terhadap beberapa contoh makanan dan minuman. Perlakuan LTLT (Low Temperature Long Time) pada suhu yang relatif rendah dengan waktu yang lebih lama dilakukan pada suhu sekitar 630C-780C dengan lama proses 30 menit. Apabila menggunakan suhu yang lebih tinggi umumnya dilakukan secara cepat. Perlakuan HTST (High Temperature Short Time) dilakukan pada suhu sekitar 800C dengan lama proses sekitar 15 menit.
Tabel 3. Pasteurisasi yang Dilakukan terhadap Beberapa Contoh Makanan dan Minuman
Produk Cara Suhu
(0C)
Waktu (menit)
Susu LTLT 62,8 30 Es krim LTLT 71,1 30 Minuman Anggur HTST 82-85 15 Buah-buahan kering LTLT 65,6-85 30-90 Sari buah anggur
(dalam botol) LTLT 76,7 30 Sari buah karbonasi LTLT 65,6 30
Sumber: Andriani 2002
Karakteristik Fisik dan pH Kerapatan
Salah satu sifat fisik suatu bahan adalah kerapatan, yang didefinisikan sebagai suatu kuantitas dari perbandingan antara massa bahan (m) denga n volume bahan (v) (Tipler, 1994).
V
m
=
ρ
...(15)Keterangan:
m adalah massa benda (kg) dan V adalah volum e (m3). Satuan standar internasional untuk kerapatan adalah kg/m3.
Umumnya kerapatan zat padat dan cairan hampir tidak bergantung terhadap tekanan dan suhu, karena zat padat an cairan hanya mengembang sedikit bila dipanaskan dan menyusut sedikit bila dipengaruhi tekanan eksternal sehingga perubahan volume relatif kecil (Tipler, 1994).
Jika suatu bahan dilarutkan dalam air dan membentuk larutan, maka kerapatannya akan berubah. Kerapatan bervariasi sesuai dengan konsentrasi larutan. Umumnya bahan seperti gula dan garam menjadikan kenaikan kerapatan bahan tetapi kadang-kadang kerapatan juga dapat turun jika dalam larutan terdapat lemak atau alkohol (Dewi, 2002).
Viskositas
Viskositas atau kekentalan dapat dianggap sebagai gesekan internal yang besarnya tertentu pada suatu fluida. Besaran gaya diperlukan untuk menimbulkan kecepatan tertentu yang berhubungan dengan viskositas suatu fluida. Untuk fluida yang berbeda, makin viskos fluida tersebut maka makin besar gaya yang diperlukan. Baik zat cair maupun gas memiliki viskositas. Pada zat cair, viskositas tersebut terutama disebabkan oleh gaya kohesi antar molekul. Sedangkan pada gas, viskositas muncul dari tumbukan antar molekul (Giancoli, 1996).
η
=l
v
A
Fg
/
/
...(16) Keterangan :? : Viskositas (poise) Fg : Gaya geser (dyne) A : Luas permukaan (cm2) ? : Kecepatan aliran (cm/s)
l : Jarak aliran yang diamati terhadap dinding (cm)
θ 2
1 tg Z
R= +
s s m R V V
Z = ×
R
G = 1
Z
Fluida yang berbeda mempunyai viskositas yang berbeda pula. Zat cair memiliki viskositas lebih besar daripada gas (Sears dan Zemansky , 1994).
Untuk memahami perilaku aliran fluida, diperlukan persamaan gerak fluida dalam suatu alat rheological seperti viskometer. Viskometer yang dipergunakan untuk mengukur viskositas ada beberapa jenis antara lain viskometer pipa kapiler dan viskometer bola jatuh (Andriani, 2002) dan viskometer
Ostwald (Saeni, 1989 ).
Kekeruhan
Kekeruhan merupakan suatu ukuran berdasarkan sinar yang dihamburkan atau dibelokkan oleh adanya butir-butir partikel yang terdis persi dalam larutan. Kekeruhan dapat disebabkan oleh bahan -bahan tersuspensi yang bervariasi dari ukuran koloid sampai dispersi kasar, tergantung dari derajat turbulensinya. Penentuan kekeruhan dengan menggunakan metode fotometri disebut
turbidimetri (Saeni, 1989).
Total Padatan Terlarut
Padatan dalam larutan adalah bahan yang masih tetap tinggal sebagai sisa selama penguapan dan pemanasan pada suhu 1030C -1050C (Saeni, 1989). Analisa zat padat terlarut mengukur jumlah zat padat yang larut dalam air. Peny usun utama zat padat terlarut dalam air alami yaitu bikarbonat, kalsium, sulfat, hidrogen, silika, klorin, magnesium, sodium, potasium, nitrogen dan fosfor. Jumlah zat padat terlarut berbeda dengan konduktivitas listrik larutan. Pada jumlah zat padat terlarut, yang diukur adalah jumlah ion dalam air, sedangkan yang diukur dalam konduktivitas listrik adalah kemampuan ion-ion tersebut dalam menghantarkan listrik (Widyasari, 2002).
pH
pH merupakan singkatan dari pondus hydrogenii yang menunjukkan derajat keasaman atau derajat kebasaan dari suatu bahan. pH didefinisikan sebagai negatif logaritma sepuluh konsentrasi ion hidrogen, dapat ditulis sebagai berikut:
pH = -log10 (H+) ...(17) K onsentrasi ion hidrogen yang aktif biasa dinyatakan dengan pH. pH sering digunakan untuk menentukan jenis mikroorganisme yang tumbuh pada suatu produk yang dihasilkan. Setiap
mikroorganisme masing-masing memiliki nilai pH untuk pertumbuhannya, sebagai contoh bakteri paling baik tumbuh pada pH mendekati netral, tetapi beberapa mikroorganisme menyukai suasana asam dan yang lain dapat tumbuh dengan sedikit asam atau dalam suasana basa (Mado na, 2005).
BAHAN DAN METODE
Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Biofisika Departemen Fisika IPB dan Laboratorium Kimia Analitik Departemen Kimia IPB. Penelitian ini mulai pada bulan agustus 2005 sampai maret 2006.
Bahan dan Alat
Bahan utama yang digunakan dalam penelitian ini antara lain adalah membran selulosa asetat 0,2 µm, sari buah nanas dan es batu. Bahan-bahan kimia yang digunakan adalah aquades, larutan buffer pH 4, aseton, dan KCl 1 mM.
Alat yang dipergunakan dalam penelitian ini meliputi: sel buntu berpengaduk, magnetic stirer, pompa udara, manometer, stopwatch, signal generator, multimeter, chamber, resistor1000 ohm, neraca analitik, pipet, gelas ukur, dan cawan plastik. Sedangkan alat-alat yang digunakan untuk karaterisasi fisik dan kimia adalah viskometer bola jatuh (Gilmont), Oakton pH/CON 10 series meter, Digital Refraktometer GMK 701R, piknom eter 25 ml, 2100P turbidimeter, mikrometer skrup, termometer. Alat bantu utama untuk pembuatan sari buah nanas antara lain: pisau, panci email, blender, penyaring berupa kain, kompor, corong, dan botol.
Metode Penelitian
Pembuatan Sari Buah Nanas
a. Pemilihan buah
Buah nanas yang akan diolah menjadi sari buah nanas dipilih yang matang dan sehat. Buah yang sehat ialah buah yang tidak busuk, cacat, pecah dan bebas hama panyakit. Kondisi buah yang mat ang diperlukan agar sari buah nanas yang dihasilkan mempunyai aroma khas buah nanas .
b. Pengupasan dan p encucian
c. Penghancuran atau pengepresan buah Buah yang telah dicuci kemudian dipotong-potong atau dirajang menjadi bagian yang kecil -kecil. Tujuan perajangan ialah untuk memudahkan penghancuran. Penghancuran daging buah dengan menggunakan blender.
d. Penyaringan sari buah
Sari buah yang telah dihancurkan kemudian disaring dengan menggunakan kain.
e. Pasteurisasi
Sari buah dimasukkan ke dalam suatu wadah. Kemudian direbus dalam air panas pada suhu 1000C selama 10 -15 menit.
Buah nanas
?
Pengupasan dan p encucian buah nanas
?
Penghancuran atau pengepresan buah nanas
?
Penyaringan sari buah nanas
?
Pasteurisasi sari buah nanas
?
Sari buah nanas
Gambar 7. Diagram Alir Pembuatan Sari Buah Nanas.
Proses Filtrasi Sari Buah Nanas
Proses filtrasi sari buah nanas dilakukan dalam s istem sel buntu berpengaduk dengan feed sebesar 150 ml. Pada proses ini dilakukan beberapa filtrasi dengan perlakuan berbeda, diantaranya sebagai berikut:
1. Filtrasi sari buah nanas tanpa perlakuan apapun.
2. Filtrasi sari buah nanas dengan memberikan perlakuan pengadukan menggunakan magnetic stirer
dengan variasi kecepatan pengadukan 5 cm/s.
3. Filtrasi sari buah nanas dengan memberikan perlakuan tekanan sebesar 1,021 x 105 Pascal.
4. Filtrasi sari buah nanas dengan memberikan perlakuan pengadukan menggunakan magnetic stirer
dengan variasi kecepatan pengadukan 22 cm/s.
5. Filtrasi sari buah nanas dengan perlakuan kecepatan pengadukan 22 cm/s dan tekanan sebesar 1,021 x 105 Pascal.
Dari proses Filtrasi dilakukan pengukuran volume permeate yang dilewatkan setiap kelipatan 30 menit selama 15 jam. Alat-alat dari proses filtrasi sari buah terdapat pada Lampiran 13.
Karakterisasi Sari Buah Nanas
Pengkarakterisasian s ari buah nanas dilakukan pada sari buah nanas sebelum, setelah dan sisa filtrasi. Karakterisasi yang dilakukan diantaranya adalah kerapatan dengan piknometer 25 ml, kekentalan dengan viskometer bola jatuh (gilmont), kekeruhan dengan turbidimeter 2100P, total padatan terlarut dengan Digital Refraktometer GMK 701R dan pH dengan Oakton pH/CON 10 series meter. Gambar alat -alat karakterisasi ditampilkan pada Lampiran 13.
Pengukuran Konduktansi Membran Pengukuran konduktansi membran
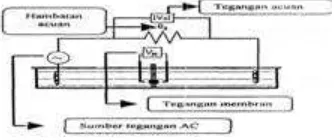
dilakukan pada membran yang bersih dan yang telah dipakai dalam proses filtrasi. Membran tersebut diletakkan pada suatu alat yang disebut chamber yang berisi larutan elektrolit KCl 1 mM dengan empat elektroda yang terpisah. Membran diletakkan di antara dua elektroda yang berdekatan, sinyal ac dengan frekuensi 1 KHz diberikan di antara dua elektroda lainnya yang berjauhan yang sebelumnya dilewatkan pada sebuah resistor 1000 ohm. Selanjutnya data pengukuran tegangan membran dapat diperoleh dengan mengukur beda potensial antara dua elektroda yang mengapit membran. Pengukuran konduktansi membran ini dilakuk an pada beberapa variasi suhu larutan elektrolit KCl 1 mM , yaitu pada suhu 150C, 200C, 250C, 300C, 350C dan 400C. Alat -alat yang digunakan dam pengukuran konduktansi m embran terdapat pada Lampiran 13.
Gambar 8. Skema Rangkaian dalam Pengukuran Konduktansi Membran .
Prosedur Karakterisasi
Pengukuran Kerapatan Sari Buah Nanas
dengan menggunakan aseton, dikeringkan dan ditimbang berat kosongnya. Piknometer diisi dengan sari buah nanas , pengisian dilakukan sampai sari buah nanas dalam piknometer meluap melalui pipa kapiler yang terdapat pada tutupnya. Piknometer dan isinya ditimbang.
Nilai kerapatan sari buah nanas diperoleh dengan menggunakan persamaan :
V
m
m
1−
2=
ρ
... ...(18)Keterangan:
? adalah kerapatan sari buah nanas (g/ml), m1 adalah massa piknometer dan larutan sari buah nanas (g), m2 adalah massa piknometer kosong, dan V adalah volume sari buah nanas (25 ml).
Pengukuran Kekentalan Sari Buah Nanas
Kekentalan sari buah nanas diukur dengan menggunakan viskometer bola jatuh (Gilmont). Sari buah nanas dimasukkan ke dalam viskometer kemudian diukur waktu jatuh bola besi pada jarak 10 cm. Viskositas sari buah nanas (ηs) dengan satuan poise diperoleh menggunakan persamaan berikut :
v k b s s
)
(ρ ρ
η = − ... ...…(19)
keterangan:
k = Konstanta viskometer yaitu 6,39 x 10-3 cm3/s2
?s = Kerapatan sari buah nanas (g/cm3) ?b = Kerapatan bola besi yaitu 7,96 g/cm3 v = Kecepatan bola besi jatuh (cm/s)
Pengukuran Kekeruhan Sari Buah Nanas
Kekeruhan sari buah nanas diukur dengan menggunakan 2100P turbidimeter. Sebelum dipergunakan untuk pengukuran sari buah nanas , turbidimeter harus dikalibrasi terlebih dahulu, yaitu dengan menggunakan
oil khusus dengan nilai kalibrasi 0-1000. Jika nilai kalibrasi sudah berada diantara 0-1000 maka alat sudah dapat digunakan. Sari buah nanas dimasukkan ke dalam gelas turbidimeter, pengisian dilakukan sampai melebihi batas tera putih yang terdapat pada gelas. Setelah itu gelas dimasukkan ke dalam lubang turbidimeter, dan tutup. Nilai kekeruhan dapat diukur dengan menekan tombol read.
Pengukuran Total Padatan Terlarut Sari Buah Nanas
Total padatan terlarut (TPT) sari buah nanas diukur dengan menggunakan Digital Refraktometer GMK 701R. Sebelumnya refraktometer dikalibrasi, tempat sampel ditetesi dengan aquades lalu tekan tombol
meas, jika diperoleh nilai 0,0 berarti refraktometer telah terkalibrasi kemudian dikeringkan dengan tissue. Selanjutnya untuk pengukuran sari buah nanas sama yaitu dengan meneteskan sari buah nanas kemudian menutupnya dengan ligh t cover dan tekan tombol zero dilanjutkan dengan tombol meas.
Pengukuran pH Sari Buah Nanas
Derajat keasaman sari buah nanas diukur dengan menggunakan Oakton pH/Con 10 series meter. Alat pH meter yang akan digunakan sebelumnya dikalibrasi terlebih dahulu dengan menggunakan buffer 4. Elektroda dimasukkan ke dalam larutan
buffer, lalu didiamkan sampai diperoleh nilai yang sesuai dengan larutan buffer yang digunakan. Setelah selesai dikalibrasi elektroda harus dibersihkan dengan aquades
lalu keringkan dengan tissue. Selanjutnya elektroda dicelupkan k e dalam sari buah nanas dan dibiarkan beberapa saat sampai diperoleh nilai pH sari buah nanas yang stabil. Setelah selesai elektroda dibilas dengan aquades dan dikeringkan dengan tissue.
Analisa Data
Faktor-faktor perlakuan yang digunakan dalam proses filtrasi sari buah nanas adalah sebagai berikut :
X1 = Filtrasi t anpa perlakuan X2 = Filtrasi dengan
kecepatan pengadu kan 5 cm/s X3 = Filtrasi dengan tekanan sebesar 1,021 x 105 Pascal
X4 = Filtrasi dengan
kecepatan pengadukan 22 cm/s X5 = Filtrasi dengan kecepatan pengadukan 22 cm/s dan tekanan sebesar
1,021 x 105 Pascal
Persentase perubahan (peningkatan atau penurunan) karakterisasi fisik dan pH sari buah nanas setelah dan sisa proses filtrasi terhadap sari buah nanas sebelum proses filtrasi diperoleh dengan persamaan:
...(20)
100
%
0
0
−
×
Y
Y
Keterangan:
Y0 = K arakterisasi fisik atau pH sari buah nanas sebelum proses filtrasi
Yt = K arakterisasi fisik atau pH sari buah nanas setelah atau sisa proses filtrasi
Y0 – Yt = N egatif, berarti terjadi peningkatan karakterisasi
fisik atau pH sari buah nanas
Y0 – Yt = P ositif, berarti terjadi penurunan karakterisasi
fisik atau pH sari buah nanas
HASIL DAN PEMBAHASAN
Nilai Permeate Membran
Permeate merupakan banyaknya volume larutan yang mampu melewati membran selama proses filtrasi berlangsung. Pada proses filtrasi jumlah dari permeate yang dihasilkan sangat dipengaruhi oleh rancangan atau perlakuan pada proses filtrasi dan sifat dari larutan atau zat yang akan difilter.
Proses filtrasi sari buah nanas dengan
feed sebesar 150 ml menggunakan membran selulosa asetat dengan ukuran pori 0,2 µm dilakukan dengan perlakuan yang berbeda -beda, yaitu: filtrasi sari buah nanas tanpa perlakuan apapun, perlakuan pengadukan menggunakan magnetic stirer dengan variasi kecepatan pengadukan 5 cm/s, perlakuan tekanan sebesar 1,021 x 105 Pascal, perlakuan pengadukan menggunakan magnetic stirer
dengan variasi kecepatan pengadukan 22 cm/s, perlakuan kecepatan pengadukan 22 cm/s dan tekanan sebesar 1,021 x 105 Pascal.
H asil pengamatan menunjukkan jumlah
permeate yang diperoleh dari lima proses filtrasi sari buah nanas dengan berbagai perlakuan yang berbeda selama 15 jam ditunjukkan oleh G ambar 9 dibawah ini.
Gambar 9. Volume Permeate Sari Buah Nanas pada Beberapa Perlakuan Filtrasi.
Dari Gambar 9 terlihat bahwa perlakuan pengadukan dan tekanan pada perlakuan kecepatan pengadukan 22 cm/s dan tekanan
sebesar 1,021 x 105 Pascal memberikan nilai
permeate yang paling tinggi. Hal tersebut disebabkan oleh adanya gaya dorong terhadap
feed dari tekanan yang diberikan dan
difusivitas dari pengadukan yang diberikan terhadap feed. Sedangkan dari perlakuan pengadukan pada variasi kecepatan pengadukan 22 cm/s, mampu menghasilkan
permeate yang lebih besar dibandingkan dengan perlakuan tekanan sebesar 1,021 x 105 Pascal. Pada filtrasi tanpa perlakuan menghasilkan permeate paling rendah yang tidak berbeda jauh dengan filtrasi perlakuan pengadukan pelan. Pada proses filtrasi ini terbentuknya fouling atau polarisasi konsentrasi pada permukaan membran cukup cepat, sehingga cukup rendah permeate yang dihasilkan dibandingkan dengan proses filtrasi dengan perlakuan yang lain.
Nilai Fluks Membran
Fluks membran merupakan banyaknya larutan permeate yang dihasilkan dalam proses filtrasi membran tiap satuan waktu dan luas. Besarnya nilai fluks dari setiap membran berubah dengan bertambahnya waktu filtrasi. Proses filtrasi sari buah nanas dengan feed
sebesar 150 ml menggunakan membran selulosa asetat dengan ukuran pori 0,2 µm dilakukan dengan perlakuan yang berbeda-beda, yaitu: filtrasi sari buah nanas tanpa perlakuan apapun, perlakuan pengadukan menggunakan magnetic stirer dengan variasi kecepatan pengadukan 5 cm/s, perlakuan tekanan sebesar 1,021 x 105 Pascal, perlakuan pengadukan menggunakan magnetic stirer
dengan variasi kecepatan pengadukan 22 cm/s, perlakuan kecepatan pengadukan 22 cm/s dan tekanan sebesar 1,021 x 105 Pascal.
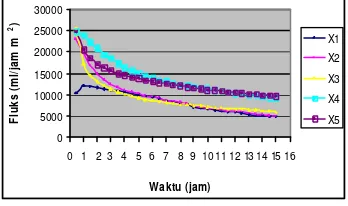
Gambar 10 merupakan kurva hubungan fluks terhadap waktu hasil pengamatan dari lima proses filtrasi sari buah nanas dengan perlakuan yang berbeda-beda selama 15 jam .
Gambar 10. Kurva Hubungan Fluks t erhadap Waktu.
Dari kurva hubungan fluks terhadap waktu dapat dilihat bahwa nilai fluks
0 10 20 30 40 50 60 70 80 90
X1 X2 X3 X4 X5
Perlakuan Filtrasi
Volume Permeate (ml) 0
5000 10000 15000 20000 25000 30000
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16
Waktu (jam)
Fluks (ml/jam m
membran menurun dengan bertambahnya waktu. Pada proses filtrasi dengan perlakuan pengadukan maupun pemberian tekanan memberikan nilai fluks yang lebih besar daripada proses filtrasi tanpa perlakuan apapun. Hal ini dikarenakan pada proses filtrasi dengan perlakuan pengadukan akan meningkatkan difusivitas feed sehingga polarisasi konsentrasi feed dapat dihindari. Selain itu pada filtrasi dengan pengadukan secara tidak langsung dilakukan proses filtrasi dengan metode cross flow filtration, pada metode ini larutan umpan dialirkan secara horizontal, sehingga terbentuknya endapan maupun polarisasi konsentrasi pada permukaan membran dapat dihindari dan
permeate yang dihasilkan menjadi lebih besar. Sedangkan pada proses filtrasi dengan pemberian tekanan akan memberikan gaya dorong lebih besar terhadap feed untuk melewati membran, sehingga akan menghasilkan permeate yang besar.
Pada kurva hubungan fluks terhadap waktu terlihat bahwa pada filtrasi dengan pemberian tekanan sebesar 1,021 x 105 Pascal, perlakuan kecepatan pengadukan 22 cm/s dan tekanan sebesar 1,021 x 105 Pascal penurunan fluks sangat tajam. Hal tersebut dikarenakan adanya udara dari pompa udara yang melewati membran selama proses filtrasi sehingga menghalangi larutan feed untuk melewati membran.
Dengan penurunan nilai fluks ini menunjukkan`adanya peristiwa fouling dalam proses filtrasi membran. Salain itu fouling
dapat terlihat dari perubahan karakteristik fisik membran yang bertambah ketebalan serta massanya (Lampiran 6). Fouling terjadi akibat adanya akumulasi molekul -molekul sari buah nanas pada permukaan m embran dan sebagian terjebak masuk ke dalam pori-pori membran. Peristiwa fouling yang terjadi mengakibatkan terhambatnya aliran feed yang melewati membran dengan kata lain jumlah permeate
yang dihasilkan semakin berkurang dengan bertambahnya waktu filtrasi. Kondisi sari buah nanas sebelum, setelah dan sisa filtrasi ditampilkan pada Lampiran 14. Kondisi membran setelah proses filtrasi ditampilkan pada L ampiran 15.
Nilai Rejeksi Membran
Rejeksi membran merupakan kemampuan membran untuk menahan suatu komponen agar tidak melewati membran. Nilai rejeksi membran tersebut dapat diperoleh dari nisbah konsentrasi terlarut
dalam feed terhadap konsentrasi terlarut dalam
permeate (Persamaan 2).
Pada Tabel 4 menunjukkan nilai rejeksi membran pada beberapa perlakuan filtrasi. Tabel 4. Nilai Rejeksi Membran
Kondisi Membran Rejeksi Membran (%) Membran X1
Membran X2 Membran X3 Membran X4 Membran X5
1,61 1,24 0,77 0,81 0,80
Dari Tabel 4 dapat diartikan bahwa filtrasi dengan perlakuan yang berbeda akan memiliki nilai rejeksi membran yang berbeda pula. Hal tersebut dis ebabkan adanya variasi perlakuan filtrasi seperti penambahan tekanan dan perlakuan pengadukan yang menyebabkan kondisi lingkungan dari setiap filtrasi berbeda-beda.
Filtrasi tanpa perlakuan apapun memberikan nilai rejeksi membran yang terbesar. Hal tersebut dikarenakankan oleh hanya ada gaya gravitasi saja yang memberikan kontribusi terhadap jalannya proses filtrasi. Dapat dilihat juga ternyata perlakuan pengadukan lebih efektif merejeksi daripada perlakuan penambahan tekanan. Hal tersebut dikarenakan perlakuan pengadukan akan meningkatkan difusivitas pada feed, sehingga zat yang kecil dapat melewati membran lebih dulu. Sedangkan pada perlakuan penambahan tekanan memberikan nilai rejeksi membran yang paling rendah, dikarenakan adanya tekanan memberikan gaya dorong tambahan pada feed, sehingga zat-zat dengan ukuran besarpun dapat melewati mem bran.
Karakterisasi Sari Buah Nanas Kerapatan
Pengukuran kerapatan sari buah nanas dilakukan pada sari buah nanas yang belum difilter, telah difilter dan sisa dari proses filtrasi. Hasil pengukuran kerapatan sari buah nanas yang ditunjukkan pada G ambar 11 di bawah ini.
Gambar 11. Kerapatan Sari Buah N anas pada Beberapa Perlakuan Filtrasi.
1.105 1.11 1.115 1.12 1.125 1.13 1.135 1.14
X1 X2 X3 X4 X5
Perlakuan Filtrasi
Kerapatan (g/ml)
Dari tampilan G ambar 11 terlihat bahwa kerapatan sari buah nanas sebelum mengalami proses filtrasi, telah difilter dan sisa dari proses filtrasi memiliki nilai kerapatan yang berbeda-beda.
Dari hasil perhitungan diperoleh data persentase perubahan nilai kerapatan sari buah nanas sebagai berikut, p ada filtrasi tanpa perlakuan, sari buah nanas yang telah difiltrasi mengalami penurunan kerapatan 1,61% dan pada sisa filtrasi meningkat sebesar 0,06% terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas sisa filtrasi mengalami penin gkatan nilai kerapatan sebesar 1,70% terhadap sari buah nanas setelah filtrasi.
Pada filtrasi dengan perlakuan pengadukan menggunakan magnetic stirer
dengan variasi kecepatan pengadukan 5 cm/s , sari buah nanas yang telah difilter mengalami penurunan kerapatan sebesar 1,24% dan sisa filtrasi meningkat kerapatannya 0,07% terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas sisa filtrasi mengalami peningkat an nilai kerapatan sebesar 1,32% terhadap sari buah nanas setelah filtrasi.
Pada filtrasi dengan perlakuan tekanan sebesar 1,021 x 105 Pascal, sari buah nanas yang telah difiltrasi mengalami penurunan kerapatan 0,77% dan pada sisa filtrasi meningkat sebesar 0,14% terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas sisa filtrasi mengalami peningkatan nilai kerapatan sebesar 0,92% terhadap sari buah nanas setelah filtrasi.
Pada filtrasi dengan perlakuan pengadukan menggunakan magnetic stirer
dengan variasi kecepatan pengadukan 22 cm/s, sari buah nanas yang telah difilter mengalami penurunan kerapatan sebesar 0,81% dan sisa fi ltrasi menurun kerapatannya 0,35% terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas si sa filtrasi mengalami peningkatan nilai kerapatan sebesar 1,18% terhadap sari buah nanas setelah filtrasi.
Pada filtrasi dengan perlakuan kecepatan pengadukan 22 cm/s dan tekanan sebesar 1,021 x 105 Pascal, sari buah nanas yang telah difilter mengalami pen urunan kerapatan sebesar 0,80% dan sisa filtrasi menurun kerapatannya 0,38% terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas sisa filtrasi mengalami peningkatan nilai kerapatan sebesar 1,18% terhadap sari buah nanas setelah filtrasi.
Dari data yang diperoleh diketahui bahwa penurunan kerapatan sari buah nanas setelah filtrasi terbesar diperoleh dari filtrasi tanpa perlakuan dan penurunan terkecil dari filtrasi dengan perlakuan tekanan sebesar 1,021 x 105 Pascal. Pada filtrasi dengan perlakuan kecepatan pengadukan 22 cm/s dan tekanan sebesar 1,021 x 105 Pascal sari buah nanas sisa filtrasi mengalami peningkatan kerapatan yang terbesar dan yang paling kecil peningkatan kerapatannya pada filtrasi tanpa perlakuan.
Secara keseluruhan sari buah nanas yang telah mengalami proses filtrasi terjadi penurunan kerapatan yang disebabkan rendahnya jumlah koloid, partikel ataupun padatan -padatan yang terdapat pada sari buah nanas setelah filtrasi. Koloid, padatan-padatan maupun partikel -partikel dengan ukuran lebih besar dari ukuran jari-jari pori membran tidak mampu melewati membran. Sedangkan pada sari buah nanas sisa filtrasi terjadi peningkatan nilai kerapatan yang disebabkan menurunnya zat-zat terlarut dan partikel dengan ukuran yang kecil dalam sari buah nanas yang mampu melewati membran, sehingga yang tertinggal hanyalah zat-zat dengan ukuran yang besar yang tidak mampu melewati membran.
Kekentalan
Kekentalan merupakan salah satu sifat fisik suatu bahan, berikut adalah data kekentalan dari sari buah nanas yang belum difilter, telah difilter dan sisa filtrasi.
Gambar 12. Kekentalan Sari B uah Nanas pada Beberapa Perlakuan Filtrasi.
Gambar 12 menunjukkan bahwa kekentalan sari buah nanas dari lima proses filtrasi dengan perlakuan berbeda. Kekentalan sari buah nanas sebelum mengalami pros es filtrasi, telah difiltrasi dan sisa dari proses filtrasi mengalami perubahan.
Pada filtrasi tanpa perlakuan, sari buah nanas yang telah difiltrasi mengalami penurunan kekentalan 39,73% dan pada sisa filtrasi meningkat sebesar 4,11% terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk
0 0.01 0.02 0.03 0.04
X1 X2 X3 X4 X5
Perlakuan Filtrasi
Kekentalan (poise)
sebelum
setelah
sari buah nanas sisa filtrasi mengalami peningkatan nilai kekentalan sebesar 72,73% terhadap sari buah nanas setelah filtrasi.
Pada filtrasi dengan perlakuan pengadukan menggunakan magnetic stirer
dengan variasi kecepatan pengadukan 5 cm/s, sari buah nanas yang telah difilt er mengalami penurunan kekentalan sebesar 30,32% dan sisa filtrasi menurun kekentalannya 8,30% terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas sisa filtrasi mengalami peningkatan nilai kekentalan sebesar 55,44% terhadap sari buah nanas setelah filtrasi.
Pada filtrasi dengan perlakuan tekanan sebesar 1,021 x 105 Pascal, sari buah nanas yang telah difiltrasi mengalami penurunan kekentalan 21,21% dan pada sisa filtrasi meningkat sebesar 18,18% terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas sisa filtrasi mengalami peningkatan nilai kekentalan sebesar 50,00% terhadap sari buah nanas setelah filtrasi.
Pada filtrasi dengan perlakuan pengadukan menggunakan magnetic stirer
dengan variasi kecepatan pengadukan 22 cm/s, sari buah nanas yang telah difilter mengalami penurunan kekentalan sebesar 26,38% dan sisa filtrasi meningkat kekentalannya 28,34% terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas sisa filtrasi mengalami peningkatan nilai kekentalan sebesar 74,33% terhadap sari buah nanas setelah filtrasi.
Pada filtrasi dengan perlakuan kecepatan pengadukan 22 cm/s dan tekanan sebesar 1,021 x 105 Pascal, sari buah nanas yang telah difilter mengalami penurunan kekentalan sebesar 24,54% dan sisa filtrasi meningkat kekentalannya 31,50% terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas sisa filtrasi mengalami peningkatan nilai kekentalan sebesar 74,27% terhadap sari buah nanas setelah filtrasi.
Dari data yang diperoleh diketahui bahwa penurunan kekentalan sari buah nanas setelah filtrasi terbesar diperoleh dari filtrasi tanpa perlakuan dan penurunan terkecil dari filtrasi dengan perlakuan tekanan sebesar 1,021 x 105 Pascal. Pada filtrasi dengan perlakuan kecepatan pengadukan 22 cm/s dan tekanan sebesar 1,021 x 105 Pascal sari buah nanas sisa filtrasi mengalami peningkatan kekentalan yang terbesar dan yang paling kecil peningkatan kekentalannya pada filtrasi tanp a perlakuan.
Secara keseluruhan sari buah nanas yang telah mengalami proses filtrasi dibandingkan
dengan sari buah nanas sebelum dan sisa filtrasi terjadi penurunan kekentalan yang disebabkan rendahnya jumlah koloid, partikel ataupun padatan-padatan dan m enurunnya total padatan terlarut yang terdapat pada sari buah nanas setelah filtrasi. Sedangkan pada sari buah nanas sisa filtrasi terjadi peningkatan nilai kekentalan sari buah nanas. Hal tersebut disebabkan oleh penurunan atau hilangnya cairan-cairan pelarut dan zat-zat yang terlarut yang memiliki ukuran yang sangat kecil pada sari buah nanas sisa filtrasi.
Kekeruhan
Kekeruhan merupakan banyaknya partikel bahan yang tersuspensi pada suatu larutan. Nilai numerik yang menunjukkan kekeruhan didasarkan pada turut campurnya bahan yang tersuspensi pada jalannya sinar melalui larutan (Sutrisno, 1991). Gambar 13 menunjukkan hasil pengukuran kekeruhan sari buah nanas yang belum difilter, telah difilter dan sisa filtrasi dari lima proses filtrasi dengan variasi perlakuan yang berbeda-beda.
Gambar 13. Kekeruhan Sari B uah Nanas pada Beberapa Perlakuan Filtrasi.
Pada filtrasi tanpa perlakuan, sari buah nanas yang telah difiltrasi mengalami penurunan kekeruhan 97,22% dan pada sisa filtrasi meningkat sebesar 85,52% terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas sisa filtrasi mengalami peningkatan nilai kekeruhan sebesar 6564,88% terhadap sari buah nanas setelah filtrasi.
Pada filtrasi dengan perlakuan pengadukan menggunakan magnet ic stirer
dengan variasi kecepatan pengadukan 5 cm/s, sari buah nanas yang telah difilter mengalami penurunan kekeruhan sebesar 95,63% dan sisa filtrasi menurun kekeruhannya 96,78% terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas sisa filtrasi mengalami peningkatan nilai kekeruhan sebesar 4405,86 % terhadap sari buah nanas setelah filtrasi.
Pada filtrasi dengan perlakuan tekanan sebesar 1,021 x 105 Pascal, sari buah nanas
0 2000 4000 6000 8000 10000 12000 14000
X1 X2 X3 X4 X5
Perlakuan Filtrasi
Kekeruhan (NTU)
sebelum
setelah
yang telah difiltrasi mengalami penurunan kekeruhan 74,46% dan pada sisa filtrasi meningkat sebesar 102,85% terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas sisa filtrasi mengalami peningkatan nilai kekeruhan sebesar 694,20% terhadap sari buah nanas setelah filtrasi.
Pada filtrasi dengan perlakuan pengadukan menggunakan magnetic stirer
dengan variasi kecepatan pengadukan 22 cm/s, sari buah nanas yang telah difilter mengalami penurunan kekeruhan sebesar 90,83% dan sisa filtrasi meningkat kekeruhannya 256,60% terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas sisa filtrasi mengalami peningkatan nilai kekeruhan sebesar 3791,38% terhadap sari buah nanas setelah filtrasi.
Pada filtrasi dengan perlakuan kecepatan pengadukan 22 cm/s dan tekanan sebesar 1,021 x 105 Pascal, sari buah nanas yang telah difilter mengalami penurunan kekeruhan sebesar 77,96% dan sisa filtrasi meningkat kekeruhannya 244,55% terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas sisa filtrasi mengalami peningkatan nilai kekeruhan sebesar 1463,02% terhadap sari buah nanas setelah filtrasi.
Dari data yang diperoleh diketahui bahwa penurunan kekeruhan sari buah nanas setelah filtrasi terbesar diperoleh dari filtrasi tanpa perlakuan dan penurunan terkecil dari filtrasi dengan perlaku an tekanan sebesar 1,021 x 105 Pascal. Pada filtrasi dengan perlakuan kecepatan pengadukan 22 cm/s dan tekanan sebesar 1,021 x 105 Pascal sari buah nanas sisa filtrasi mengalami peningkatan kekeruhan yang terbesar dan yang paling kecil peningkatan kekeruh annya pada filtrasi tanpa perlakuan apapun.
Secara keseluruhan sari buah nanas yang telah mengalami proses filtrasi terjadi penurunan kekeruhan yang disebabkan oleh tidak terlewatkannya koloid, partikel ataupun padatan-padatan pada proses filtrasi sari buah nanas, sehingga sari buah nanas hasil filtrasi memiliki suspensi partikel yang rendah . Sedangkan pada sari buah nanas sisa filtrasi terjadi peningkatan nilai kekeruh an sari buah nanas yang disebabkan tetap tertinggalnya zat -zat, koloid, ataupun partikel yang memiliki ukuran cukup besar selama proses filtrasi pada sari buah nanas sisa filtrasi karena tidak mampu melewati membran. Hal tersebut meningkatkan padatan atau partikel yang tersuspensi pada sari buah nanas sisa filtrasi.
Total Padatan Terlarut
Total padatan terlarut dari sari buah nanas sebelum, setelah dan sisa filtrasi dengan beberapa variasi perlakuan yang berbeda-beda ditampilkan pada Gambar 14 di bawah ini.
Gambar 14. Total Padatan Terlarut (TPT) Sari Buah Nanas pada Beberapa Perlakuan Filtrasi.
Dari hasil pengukuran diperoleh bahwa sari buah nanas yang telah difilter dan sisa dari filtrasi memiliki total padatan terlarut yang lebih rendah dari sari buah nanas yang belum difilter. Dan dari perhitungan diperoleh bahwa p ada filtrasi tanpa perlakuan, sari buah nanas yang telah difiltrasi mengalami penurunan TPT 12,34% dan pada sisa filtrasi menurun sebesar 1,23% terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas sisa filtrasi mengalami peningkatan nilai TPT sebesar 12,68 % terhadap sari buah nanas setelah filtrasi.
Pada filtrasi dengan perlakuan pengadukan menggunakan magnetic stirer
dengan variasi kecepatan pengadukan 5 cm/s, sari buah nanas yang telah difilt er mengalami penurunan TPT sebesar 12,18% dan sisa filtrasi menurun TPT nya sebesar 1,92 % terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas sisa filtrasi mengalami peningkatan nilai TPT sebesar 11,68% terhadap sari buah nanas setelah filtrasi.
Pada filtrasi dengan perlakuan tekanan sebesar 1,021 x 105 Pascal, sari buah nanas yang telah difiltrasi mengalami penurunan TPT 6,00% dan pada sisa filtrasi menurun sebesar 3,33 % terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas sisa filtrasi mengalami peningkatan nilai TPT sebesar 2,84% terhadap sari buah nanas setelah filtrasi.
Pada filtrasi dengan perlakuan pengadukan menggunakan magnetic stirer
dengan variasi kecepatan pengadukan 22 cm/s, sari buah nanas yang telah difilter mengalami penurunan TPT sebesar 7,59% dan sisa filtrasi menurun sebesar 22,76% terhadap sari buah nanas sebelum filtrasi. Sedangkan
0 5 10 15 20
X1 X2 X3 X4 X5
Perlakuan Filtrasi
TPT (% Brix)
sebelum setelah
untuk sari buah nanas sisa filtrasi mengalami penurunan nilai TPT sebesar 16,42% terhadap sari buah nanas setelah filtrasi.
Pada filtrasi dengan perlakuan kecepatan pengadukan 22 cm/s dan tekanan sebesar 1,021 x 105 Pascal, sari buah nanas yang telah difilter mengalami penurunan TPT sebesar 7,69% dan sisa filtrasi menurunkan TPT sebesar 25,87% terhadap sari buah nanas sebelum filtrasi. Sedangkan untuk sari buah nanas sisa filtrasi mengalami penurunan nilai TPT sebesar 19,70% terhadap sari buah nanas setelah filtrasi.
Dari data yang diperoleh diketahui bahwa penurunan TPT sari buah nanas setelah filtrasi terbesar diperoleh dari filtrasi tanpa perlakuan apapun dan penurunan terkecil dari filtrasi dengan perlakuan tekanan sebesar 1,021 x 105 Pascal. Pada filtrasi dengan perlakuan kecepatan pengadukan 22 cm/s dan tekanan sebesar 1,021 x 105 Pascal sari buah