SIFAT-SIFAT MEMBRAN YANG TERBUAT DARI
SARI KULIT BUAH NANAS
MUHAMAD ANDRIANSYAH
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
1
ABSTRAK
MUHAMAD ANDRIANSYAH.
Sifat-Sifat Membran yang Terbuat dari Sari
Kulit Buah Nanas. Dibimbing oleh
SRI MULIJANI
dan
BETTY MARITA
SOEBRATA
.
2
ABSTRACT
MUHAMAD ANDRIANSYAH
. Membrane Properties Made of Pineapple Peel
Waste Extract. Supervised by
SRI MULIJANI
and
BETTY MARITA
SOEBRATA
.
Pineapple processes which have been done nowadays brought a lot of
environmental problems due to enormous pineapple peel waste. Actually, those
waste could be converted into valuable product such as cellulose or
nata de pina
.
Cellulose could be used as membrane which was useful for filtration process.
Nata de pina
was formed through incubation process for five days with the help of
3
Sifat-Sifat Membran yang Terbuat dari
Sari Kulit Buah Nanas
MUHAMAD ANDRIANSYAH
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
4
Judul : Sifat-Sifat Membran yang Terbuat dari Sari Kulit Buah Nanas.
Nama : Muhamad Andriansyah
NIM : G01400061
Disetujui,
Dra. Sri Mulijani, M.S. Betty Marita Soebrata, S.Si., M.Si.
Ketua Anggota
Diketahui,
Dr. Ir. Yonny Koesmaryono, M.S.
Dekan FMIPA
5
PRAKATA
Puji dan syukur Penulis haturkan ke hadirat Allah AWT atas segala rahmat,
dan petunjuk dalam penelitian sehingga tersusunlah karya ilmiah ini. Adapun
penelitian tersebut bertujuan membuat dan mengkarakterisasi membran yang
terbuat dari sari kulit buah nanas, dan dilaksanakan sejak bulan Desember 2004
hingga Juni 2005 di Laboratorium Kimia Anorganik, IPB.
Penulis mengucapkan terima kasih terutama kepada Ibu Dra. Sri Mulijani, M.S.
dan Ibu Betty Marita Soebrata, S.Si., M.Si., sela ku pembimbing yang baik dan
senantiasa menyempatkan waktu untuk berkonsultasi dan selalu memberi
semangat pada Penulis untuk terus berusaha menyelesaikan penelitian ini. Ayah
dan Mamah yang telah banyak berkorban materi, waktu, tenaga, dan juga
senantiasa membantu dengan doa dan semangat untuk suksesnya penelitian ini.
Penulis juga berterima kasih pada Ibu Rini dan Mas Winanda atas bantuannya
dalam analisis fluks air; kepada Bapak Pamulih atas bantuannya dalam analisis
FTIR; dan kepada Ibu Endang atas bantuannya dalam analisis SEM; serta kepada
para laboran di Kimia Anorganik, khususnya kepada Bapak Syawal yang selalu
membantu dalam penelitian ini.
Penulis berterima kasih pula kepada Febry atas kerja samanya dalam
pembuatan
nata de pina
dan rekan-rekan satu penelitian: Tya, Atik, Rene, dan
Nisa; atas diskusi-diskusi yang sangat membantu Penulis dalam menyelesaikan
penelitian ini. Kepada rekan-rekan di Zehn Production: Tasca, Dhea, Abang,
Eddy, dan Safril; yang terus memberi semangat pada Penulis untuk tidak berputus
asa dalam penelitian. Kepada Zendy Fitriana yang selalu mau membantu dan
meluangkan waktu untuk membantu Penulis dalam penelitian. Kepada
rekan-rekan Kimia 37 lainnya, Penulis juga mengucapkan banyak terima kasih. Semoga
Allah SWT membalas semua budi baik kalian.
Akhir kata, semoga karya ilmiah ini dapat bermanfaat.
Bogor, Desember 2005
6
RIWAYAT HIDUP
Penulis dilahirkan di Bogor, Jawa Barat, pada tanggal 31 Agustus 1982 sebagai
anak pertama dari tiga bersaudara sebagai anak pasangan M. Adenan Hamid dan
Tati Kurniasih.
7
DAFTAR ISI
Halaman
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... viii
PENDAHULUAN... 1
TINJAUAN PUSTAKA... 2
Nanas ... 2
Bakteri Pembentuk
Nata
... 2
Definisi Membran ... 3
Klasifikasi Membran ... 3
Karaktersitik Membran ... 4
BAHAN DAN METODE ... 7
Bahan dan Alat ... 7
Metode Penelitian... 7
HASIL DAN PEMBAHASAN ... 8
Nata de Pina
... 8
Analisis Fluks Air ... 9
Kajian Spektrum FTIR Membran ... 11
Analisis Ukuran Pori-Pori ... 12
SIMPULAN DAN SARAN ... 13
Simpulan... 13
Saran ... 13
DAFTAR PUSTAKA ... 13
8
DAFTAR TABEL
Halaman
1 Komposisi Kimia Buah Nanas ... 2
2 Kisaran Fluks dan Tekanan Berbagai Jenis Membran
... 5
3 Nilai Fluks yang Terukur pada Sampel... 10
4 Hasil Analisis dengan FTIR
... 11
DAFTAR GAMBAR
Halaman
1 Prinsip
Cross-Flow Filtration
... 6
2 Prinsip
Dead-End Filtration
... 6
3 Wadah dan Larutan Saat Inkubasi... 8
4
Nata de Pina
Setelah 5 Hari Inkubasi dengan Ketebalan 5 mm ... 8
5
Nata de Pina
yang Telah Dipanen dan Dibersihkan ... 9
6
Nata de Pina
yang Telah Di
press
... 9
7 Hubungan antara waktu dan fluks air pada membran membran 1:4 (sari
kulit nanas dan air) dan gula 5% b/v ... 11
8 Spektrum IR membran membran 1:4 (sari kulit nanas dan air) dan gula
5% b/v ... 12
9 Spektrum IR membran membran 1:1 (sari kulit nanas dan air) dan gula
10% b/v ... 12
10 Spektrum IR Selulosa Asli ... 12
11 Spektrum IR Membran dan Selulosa Asli... 12
12 Permukaan
membran 1:4 (sari kulit nanas dan air) dan gula 5% b/v
dengan perbesaran
1500X ... 12
DAFTAR LAMPIRAN
Halaman
1 Bagan alir metode percobaan ... 16
1
PENDAHULUAN
Nanas merupakan jenis buah yang terkenal baik di Indonesia maupun di belahan dunia lainnya. Selain dikonsumsi sebagai buah segar, nanas juga merupakan salah satu jenis buah–buahan yang diolah menjadi bahan baku untuk industri pengolahan makanan. Hasil pengolahan buah nanas yang sering kita jumpai dalam kehidupan sehari–hari di antaranya sari buah, selai, manisan, dan juga sebagai bahan pelengkap dalam pembuatan makanan. Selain mudah untuk diolah, buah nanas juga memiliki kandungan gizi yang cukup tinggi dan dapat diperoleh dengan harga yang relatif murah.
Produksi nanas di Indonesia mengalami pertumbuhan yang pesat tiap tahunnya. Menurut Sunarjono (2004), produksi buah nanas pada tahun 2000, 2001, dan 2002 masing–masing mencapai 393.299, 494.968, dan 555.588 ton, sedangkan yang mengalami pengolahan lebih lanjut hanya terpakai 53% saja dan sisanya merupakan limbah yang tidak terpakai, sehingga dapat dibayangkan berapa besar limbah yang dihasilkan dari pengolahan buah nanas tersebut. Limbah dari buah nanas terutama kulit buahnya menumpuk dan menimbulkan masalah bagi lingkungan (Susanto et al. 2000). Berdasarkan permasalahan tersebut, maka terdapat suatu peluang untuk memanfaatkan limbah kulit nanas dan mengubahnya menjadi produk yang dapat dimanfaatkan lebih lanjut. Salah satu produk yang dapat diciptakan dari limbah buah nanas ialah nata.
Nata merupakan produk hasil fermentasi dari gula (glukosa) dengan bantuan bakteri
Acetobacter xylinum yang kemudian diubah menjadi selulosa. Menurut Susanto et al.
(2000) pembentukan nata terjadi karena proses pengambilan glu kosa oleh sel–sel A. xylinum. Kemudian glukosa tersebut digabungkan dengan asam lemak membentuk prekursor pada membran sel. Prekursor ini selanjutnya dikeluarkan dalam bentuk ekskresi dan bersama enzim mempolimerisasikan glukosa menjadi selulosa di luar sel. Jenis nata yang dipakai dalam penelitian ini ialah nata de pina yang terbuat dari sari kulit buah nanas. Dilihat dari pencirian nata yang merupakan gabungan dari serat –serat karbon yang menjadi satu membentuk suatu bentuk yang kokoh dan berpori, maka nata memiliki potensi untuk dimanfaatkan sebagai membran selain sebagai makanan kaya serat yang dapat dikonsumsi.
Membran adalah lapisan tipis dari suatu material berpori (porous material) yang dapat digunakan untuk beberapa proses pemisahan (Eryan 2004). Proses pemisahan dengan menggunakan membran merupakan salah satu proses pemisahan yang ekonomis, efektif, dan tidak menimbulkan perubahan pada zat yang dipisahkan baik fisik maupun kimia. Keunggulan membran dibandingkan dengan proses pemisahan yang lain ialah terjadi penghematan energi karena pemisahan dilakukan pada suhu kamar, lebih bersih, dan ramah lingkungan karena tidak menggunakan bahan kimia dan mudah untuk terdegradasi. Selain itu proses penggunaan membran dapat dengan mudah dipasang secara cepat dan tidak membutuhkan ruangan yang luas (Eryan 2004). Keberhasilan teknik pemisahan dengan membran bergantung pada sifat fisik, sifat kimia, sifat mekanis, dan struktur pori.
Pada saat ini teknologi membran telah digunakan secara luas dalam dunia industri. Industri –industri yang menerapkan teknologi membran antara lain: bioindustri, industri makanan dan minuman, farmasi, pengolahan limbah industri, industri kertas , dan lain–lain. Pada umumnya membran dibuat dari polimer alami dan modifikasinya seperti selulosa, dan polimer sintetis seperti polisulfon dan poliamida (Susanto et al. 2000). Selulosa merupakan polisakarida yang terdapat pada tanaman dan merupakan bahan yang dapat digunakan dalam pembuatan membran. Sumber utama selulosa ialah bubur kayu at au kapas, tetapi pertambahan penduduk dan perkembangan teknologi yang semakin pesat mengakibatkan terjadinya peningkatan kebutuhan hidup. Oleh karena itu diperlukan sumber selulosa lain selain kayu, maka dikembangkanlah proses pembuatan selulosa yang berasal dari sari buah–buahan salah satunya ialah nata de pina yang berasal dari sari buah nanas tetapi dalam penelitian ini digunakan sari kulit buah nanas.
Penelitian ini bertujuan membuat dan mengpencirian membran yang berasal dari sari kulit buah nanas. Penelitian ini mengacu pada suatu pemikiran bahwa nata de pina
SIFAT-SIFAT MEMBRAN YANG TERBUAT DARI
SARI KULIT BUAH NANAS
MUHAMAD ANDRIANSYAH
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
1
ABSTRAK
MUHAMAD ANDRIANSYAH.
Sifat-Sifat Membran yang Terbuat dari Sari
Kulit Buah Nanas. Dibimbing oleh
SRI MULIJANI
dan
BETTY MARITA
SOEBRATA
.
2
ABSTRACT
MUHAMAD ANDRIANSYAH
. Membrane Properties Made of Pineapple Peel
Waste Extract. Supervised by
SRI MULIJANI
and
BETTY MARITA
SOEBRATA
.
Pineapple processes which have been done nowadays brought a lot of
environmental problems due to enormous pineapple peel waste. Actually, those
waste could be converted into valuable product such as cellulose or
nata de pina
.
Cellulose could be used as membrane which was useful for filtration process.
Nata de pina
was formed through incubation process for five days with the help of
3
Sifat-Sifat Membran yang Terbuat dari
Sari Kulit Buah Nanas
MUHAMAD ANDRIANSYAH
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
4
Judul : Sifat-Sifat Membran yang Terbuat dari Sari Kulit Buah Nanas.
Nama : Muhamad Andriansyah
NIM : G01400061
Disetujui,
Dra. Sri Mulijani, M.S. Betty Marita Soebrata, S.Si., M.Si.
Ketua Anggota
Diketahui,
Dr. Ir. Yonny Koesmaryono, M.S.
Dekan FMIPA
5
PRAKATA
Puji dan syukur Penulis haturkan ke hadirat Allah AWT atas segala rahmat,
dan petunjuk dalam penelitian sehingga tersusunlah karya ilmiah ini. Adapun
penelitian tersebut bertujuan membuat dan mengkarakterisasi membran yang
terbuat dari sari kulit buah nanas, dan dilaksanakan sejak bulan Desember 2004
hingga Juni 2005 di Laboratorium Kimia Anorganik, IPB.
Penulis mengucapkan terima kasih terutama kepada Ibu Dra. Sri Mulijani, M.S.
dan Ibu Betty Marita Soebrata, S.Si., M.Si., sela ku pembimbing yang baik dan
senantiasa menyempatkan waktu untuk berkonsultasi dan selalu memberi
semangat pada Penulis untuk terus berusaha menyelesaikan penelitian ini. Ayah
dan Mamah yang telah banyak berkorban materi, waktu, tenaga, dan juga
senantiasa membantu dengan doa dan semangat untuk suksesnya penelitian ini.
Penulis juga berterima kasih pada Ibu Rini dan Mas Winanda atas bantuannya
dalam analisis fluks air; kepada Bapak Pamulih atas bantuannya dalam analisis
FTIR; dan kepada Ibu Endang atas bantuannya dalam analisis SEM; serta kepada
para laboran di Kimia Anorganik, khususnya kepada Bapak Syawal yang selalu
membantu dalam penelitian ini.
Penulis berterima kasih pula kepada Febry atas kerja samanya dalam
pembuatan
nata de pina
dan rekan-rekan satu penelitian: Tya, Atik, Rene, dan
Nisa; atas diskusi-diskusi yang sangat membantu Penulis dalam menyelesaikan
penelitian ini. Kepada rekan-rekan di Zehn Production: Tasca, Dhea, Abang,
Eddy, dan Safril; yang terus memberi semangat pada Penulis untuk tidak berputus
asa dalam penelitian. Kepada Zendy Fitriana yang selalu mau membantu dan
meluangkan waktu untuk membantu Penulis dalam penelitian. Kepada
rekan-rekan Kimia 37 lainnya, Penulis juga mengucapkan banyak terima kasih. Semoga
Allah SWT membalas semua budi baik kalian.
Akhir kata, semoga karya ilmiah ini dapat bermanfaat.
Bogor, Desember 2005
6
RIWAYAT HIDUP
Penulis dilahirkan di Bogor, Jawa Barat, pada tanggal 31 Agustus 1982 sebagai
anak pertama dari tiga bersaudara sebagai anak pasangan M. Adenan Hamid dan
Tati Kurniasih.
7
DAFTAR ISI
Halaman
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... viii
PENDAHULUAN... 1
TINJAUAN PUSTAKA... 2
Nanas ... 2
Bakteri Pembentuk
Nata
... 2
Definisi Membran ... 3
Klasifikasi Membran ... 3
Karaktersitik Membran ... 4
BAHAN DAN METODE ... 7
Bahan dan Alat ... 7
Metode Penelitian... 7
HASIL DAN PEMBAHASAN ... 8
Nata de Pina
... 8
Analisis Fluks Air ... 9
Kajian Spektrum FTIR Membran ... 11
Analisis Ukuran Pori-Pori ... 12
SIMPULAN DAN SARAN ... 13
Simpulan... 13
Saran ... 13
DAFTAR PUSTAKA ... 13
8
DAFTAR TABEL
Halaman
1 Komposisi Kimia Buah Nanas ... 2
2 Kisaran Fluks dan Tekanan Berbagai Jenis Membran
... 5
3 Nilai Fluks yang Terukur pada Sampel... 10
4 Hasil Analisis dengan FTIR
... 11
DAFTAR GAMBAR
Halaman
1 Prinsip
Cross-Flow Filtration
... 6
2 Prinsip
Dead-End Filtration
... 6
3 Wadah dan Larutan Saat Inkubasi... 8
4
Nata de Pina
Setelah 5 Hari Inkubasi dengan Ketebalan 5 mm ... 8
5
Nata de Pina
yang Telah Dipanen dan Dibersihkan ... 9
6
Nata de Pina
yang Telah Di
press
... 9
7 Hubungan antara waktu dan fluks air pada membran membran 1:4 (sari
kulit nanas dan air) dan gula 5% b/v ... 11
8 Spektrum IR membran membran 1:4 (sari kulit nanas dan air) dan gula
5% b/v ... 12
9 Spektrum IR membran membran 1:1 (sari kulit nanas dan air) dan gula
10% b/v ... 12
10 Spektrum IR Selulosa Asli ... 12
11 Spektrum IR Membran dan Selulosa Asli... 12
12 Permukaan
membran 1:4 (sari kulit nanas dan air) dan gula 5% b/v
dengan perbesaran
1500X ... 12
DAFTAR LAMPIRAN
Halaman
1 Bagan alir metode percobaan ... 16
1
PENDAHULUAN
Nanas merupakan jenis buah yang terkenal baik di Indonesia maupun di belahan dunia lainnya. Selain dikonsumsi sebagai buah segar, nanas juga merupakan salah satu jenis buah–buahan yang diolah menjadi bahan baku untuk industri pengolahan makanan. Hasil pengolahan buah nanas yang sering kita jumpai dalam kehidupan sehari–hari di antaranya sari buah, selai, manisan, dan juga sebagai bahan pelengkap dalam pembuatan makanan. Selain mudah untuk diolah, buah nanas juga memiliki kandungan gizi yang cukup tinggi dan dapat diperoleh dengan harga yang relatif murah.
Produksi nanas di Indonesia mengalami pertumbuhan yang pesat tiap tahunnya. Menurut Sunarjono (2004), produksi buah nanas pada tahun 2000, 2001, dan 2002 masing–masing mencapai 393.299, 494.968, dan 555.588 ton, sedangkan yang mengalami pengolahan lebih lanjut hanya terpakai 53% saja dan sisanya merupakan limbah yang tidak terpakai, sehingga dapat dibayangkan berapa besar limbah yang dihasilkan dari pengolahan buah nanas tersebut. Limbah dari buah nanas terutama kulit buahnya menumpuk dan menimbulkan masalah bagi lingkungan (Susanto et al. 2000). Berdasarkan permasalahan tersebut, maka terdapat suatu peluang untuk memanfaatkan limbah kulit nanas dan mengubahnya menjadi produk yang dapat dimanfaatkan lebih lanjut. Salah satu produk yang dapat diciptakan dari limbah buah nanas ialah nata.
Nata merupakan produk hasil fermentasi dari gula (glukosa) dengan bantuan bakteri
Acetobacter xylinum yang kemudian diubah menjadi selulosa. Menurut Susanto et al.
(2000) pembentukan nata terjadi karena proses pengambilan glu kosa oleh sel–sel A. xylinum. Kemudian glukosa tersebut digabungkan dengan asam lemak membentuk prekursor pada membran sel. Prekursor ini selanjutnya dikeluarkan dalam bentuk ekskresi dan bersama enzim mempolimerisasikan glukosa menjadi selulosa di luar sel. Jenis nata yang dipakai dalam penelitian ini ialah nata de pina yang terbuat dari sari kulit buah nanas. Dilihat dari pencirian nata yang merupakan gabungan dari serat –serat karbon yang menjadi satu membentuk suatu bentuk yang kokoh dan berpori, maka nata memiliki potensi untuk dimanfaatkan sebagai membran selain sebagai makanan kaya serat yang dapat dikonsumsi.
Membran adalah lapisan tipis dari suatu material berpori (porous material) yang dapat digunakan untuk beberapa proses pemisahan (Eryan 2004). Proses pemisahan dengan menggunakan membran merupakan salah satu proses pemisahan yang ekonomis, efektif, dan tidak menimbulkan perubahan pada zat yang dipisahkan baik fisik maupun kimia. Keunggulan membran dibandingkan dengan proses pemisahan yang lain ialah terjadi penghematan energi karena pemisahan dilakukan pada suhu kamar, lebih bersih, dan ramah lingkungan karena tidak menggunakan bahan kimia dan mudah untuk terdegradasi. Selain itu proses penggunaan membran dapat dengan mudah dipasang secara cepat dan tidak membutuhkan ruangan yang luas (Eryan 2004). Keberhasilan teknik pemisahan dengan membran bergantung pada sifat fisik, sifat kimia, sifat mekanis, dan struktur pori.
Pada saat ini teknologi membran telah digunakan secara luas dalam dunia industri. Industri –industri yang menerapkan teknologi membran antara lain: bioindustri, industri makanan dan minuman, farmasi, pengolahan limbah industri, industri kertas , dan lain–lain. Pada umumnya membran dibuat dari polimer alami dan modifikasinya seperti selulosa, dan polimer sintetis seperti polisulfon dan poliamida (Susanto et al. 2000). Selulosa merupakan polisakarida yang terdapat pada tanaman dan merupakan bahan yang dapat digunakan dalam pembuatan membran. Sumber utama selulosa ialah bubur kayu at au kapas, tetapi pertambahan penduduk dan perkembangan teknologi yang semakin pesat mengakibatkan terjadinya peningkatan kebutuhan hidup. Oleh karena itu diperlukan sumber selulosa lain selain kayu, maka dikembangkanlah proses pembuatan selulosa yang berasal dari sari buah–buahan salah satunya ialah nata de pina yang berasal dari sari buah nanas tetapi dalam penelitian ini digunakan sari kulit buah nanas.
Penelitian ini bertujuan membuat dan mengpencirian membran yang berasal dari sari kulit buah nanas. Penelitian ini mengacu pada suatu pemikiran bahwa nata de pina
TINJAUAN PUSTAKA Nanas
Tanaman nanas telah ada sejak lama di Indonesia. Menurut Morton (1987), tanaman nanas berasal dari Amerika Selatan. Tanaman nanas termasuk dalam suku Plantae dengan sistematika sebagai berikut:
Divisi : Spermatophyta
Kelas : Monocotyledonae
Ordo : Farinosae
Famili : Bromeliaceae
Genus : Ananas
Spesies : Ananas comosus
Tanaman nanas memiliki jenis yang beragam yakni:
Cayenne
Nanas jenis cayenne kulitnya berwarna kuning oranye dan matanya tidak berduri, buahnya berwarna kekuningan, rasanya agak masam dan memiliki kandungan air yang banyak. Jenis ini baik untuk dikalengkan karena mempunyai serat yang kasar, sehingga tidak mudah hancur. Berat buah ini berkisar 0.75–1.50 Kg.
Spanish
Nanas jenis spanish terbagi menjadi dua yakni Red Spanish yang merupakan nanas yang tahan terhadap penyakit dan berumur panjang, berat buah berkisar 0.90–1.80 Kg, daging buah berwarna putih, kulit buah kuat dan kompak sehingga cocok dikirim ke tempat yang jauh dengan pengapalan dalam bentuk segar. Singapore Spanish yang nemiliki berat buah berkisar 1.60–2.30 Kg, kulit buah yang masak berwarna merah oranye, daging buah berwarna kuning, berserat banyak , dan memiliki rasa yang baik sehingga cocok untuk dikalengkan.
Queen
Nanas jenis queen memiliki kulit buah berwarna kuning dan matanya berlekuk dalam. Daging buah berwarna kuning, berat buah berkis ar 1.00–1.50 Kg, rasanya manis , dan enak sehingga cocok untuk dimakan segar. Nanas ini memiliki serat yang halus dan kandungan air yang sedikit.
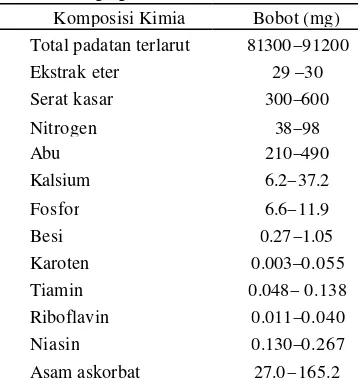
Pada umumnya buah nanas terdiri dari tiga bagian, yaitu kulit, daging, dan hati. Komposisi kimia buah nanas dapat dilihat pada Tabel 1 berikut ini.
Tabel 1 Komposisi kimia per 100000 mg daging buah nanas
Komposisi Kimia Bobot (mg) Total padatan terlarut 81300 –91200 Ekstrak eter 29 –30 Serat kasar 300–600 Nitrogen 38–98 Abu 210–490 Kalsium 6.2–37.2 Fosfor 6.6–11.9 Besi 0.27 –1.05 Karoten 0.003–0.055 Tiamin 0.048– 0.138 Riboflavin 0.011–0.040 Niasin 0.130–0.267 Asam askorbat 27.0 –165.2 Sumber: Morton 1987
Bakteri Pembentuk Nata
Menurut Lapuz et al. (1967), bakteri pertama yang diduga sebagai pembentuk nata
ialah Leuconostoc sp. Tetapi kemudian diketahui bahwa bakteri yang membentuk
nata ialah Acetobacter xylinum.
Bakteri A. xylinum termasuk golongan
Acetobacter yang mempunyai ciri–ciri: gram negatif, obligat aerobik, berbentuk batang, membentuk kapsul, bersifat non motil, dan tidak membentuk spora. Spesies yang telah dikenal antara lain A. aceti, A. orleanensis, A. liquefaciens, dan A. xylinum. Meskipun mempunyai ciri–ciri yang hampir sama dengan spesies lain, namun apabila A. xylinum
ditumbuhkan pada media yang mengandung gula, maka bakteri ini akan merombak gula untuk mensintes is suatu polisakarida yang dikenal dengan selulosa ekstrasel uler.
A. xylinum memiliki sifat sensitif terhadap perubahan sifat fisik dan kimia lingkungannya dan ini akan berpengaruh terhadap nata yang dihasilkan (Lapuz et al., 1967).
3
terbentuk dapat mencapai tebal lebih dari 5 cm dalam waktu satu bulan.
Aktivitas pembentukan nata hanya terjadi pada pH antara 3.50–7.50. Kualitas nata
terbaik dan terbanyak dicapai pada pH 4.5 pada suhu kamar. Terbentuknya pelikel (lapisan tipis nata) mulai dapat dilihat di permukaan setelah 24 jam inkubasi, bersamaan dengan terjadinya proses penjernihan cairan di bawahnya. Jaringan halus transparan yang terbentuk di permukaan membawa sebagian bakteri yang terperangkap di dalamnya. Gas karbondioksida yang dihasilkan secara lambat oleh A. xylinum
mungkin yang menyebabkan pengapungan
nata sehingga terdorong ke permukaan (Susanto et al. 2000).
Definisi Membran
Membran adalah lapisan semipermeabel berupa padatan polimer tipis yang menahan pergerakan bahan tertentu (Scott dan Hughes 1996). Menurut Osada dan Nakagawa (1992), membran merupakan lapisan semipermeabel yang tipis dan dapat digunakan untuk memisahkan dua komponen dengan cara menahan dan melewatkan komponen tertentu melalui pori–pori. Sedangkan menurut Eryan (2004), membran adalah lapisan tipis dari suatu material berpori (porous material) yang dapat digunakan untuk beberapa proses pemisahan.
Klasifikasi Membran
Menurut Mulder (1996) dan Wenten (1999), klasifikasi membran ada beberapa macam yaitu berdasarkan material asal, morfologi, bentuk, dan fungsi.
Berdasarkan Material Asal
Membran bedasarkan material dibagi menjadi dua golongan: membran alamiah yang merupakan membran yang terdapat pada sel tumbuhan, hewan, dan manusia. Membran ini memiliki perbedaan dasar dalam struktur dan fungsi dari membran sintetik. Membran ini berfungsi untuk melindungi isi sel dari pengaruh luar dan membantu proses metabolisme organisme dengan sifat permeabelnya. Sedangkan membran sintesis merupakan membran yang dibuat sesuai dengan kebutuhan dan sifatnya disesuaikan dengan membran alamiah. Membran sintetik dibagi lagi menjadi membran organik dan membran anorganik. Beberapa contoh membran sintetis ada yang terbuat dari
polimer seperti selulosa asetat, selulosa triasetat, polipropilena, polietilena, poliamida, polisulfon, dan polietersulfon, serta ada yang terbuat dari keramik, gelas, dan logam.
Berdasarkan Morfologi
Membran berdasarkan morfologinya dibagi menjadi dua golongan: membran asimetrik dan membran simetrik. Membran asimetrik merupakan suatu membran yang struktur porinya tidak seragam. Membran dengan struktur asimetrik memiliki dua lapisan, yaitu (1) lapisan penyangga atau pendukung yang memiliki ketebalan sebesar 20–100 µm dan memiliki rongga pori makin ke bawah makin besar, (2) lapisan aktif memiliki ketebalan 0.20–1.00 µm, ukuran pori 1.0–10 µm dan memiliki pori yang rapat serta lapisan ini mengadakan kontak langsung dengan larutan.
Membran asimetrik dibagi menjad i dua bagian yaitu membran inversi fase dan membran komposit. Kedua membran ini memiliki perbedaan , yaitu membran inversi fase terdiri dari satu jenis membran dengan perbandingan tertentu. Menurut Scott dan Hughes (1996), membran asimetrik merupakan membran yang menggunakan bahan pendukung bagi lapisan aktif yang berada di atasnya dan berfungsi untuk kebutuhan mekanik.
Membran simetrik merupakan suatu membran yang memiliki struktur pori yang seragam. Pembuatan membran dilakukan pada ruangan tertutup dan jenuh dengan non pelarut. Agar konsentrasi pelarut bisa berlangsung tetap maka penambahan non pelarut dilakukan selambat mungkin sehingga struktur membran yang diperoleh memiliki pori yang seragam dan homogen.
menjadi dua: bentuk lembaran dan silindris berupa tubular dan serat berlubang.
Berdasarkan Bentuk
Bentuk membran dapat dibagi menjadi dua kelompok : membran datar dan tubular. Membran datar memiliki bentuk melebar dan penampang lintang yang besar. Ada beberapa macam membran datar, antara lain: membran datar yang terdiri dari satu lembar, membran datar bersusun yang terdiri dari beberapa lembar yang disusun bertingkat dengan menempatkan pemisah antara dua membran yang berdekatan, dan membran spiral bergulung yang merupakan membran yang disusun bertingkat serta digulung dengan pipa sentral membentuk spiral.
Membran Tubular terdiri dari tiga jenis, antara lain: membran serat berongga (diameter < 0.50 mm), membran kapiler (diameter 0.50– 5.00 mm), dan membran tubular (diameter > 5 mm).
Berdasarkan Fungsi
Ada beberapa macam membran berdasarkan fungsinya, antara lain: membran mikrofiltrasi, ultrafiltrasi, osmosis balik, dialisis, dan elektrodialisis.
Membran mikrofiltrasi merupakan proses pemisahan antar partikel (bakteri, ragi) dan berfungsi untuk menyaring makromolekul > 500.000 g/mol atau partikel berukuran 0.10 – 10.00 µm. Tekanan yang digunakan 0.5 –2.0 atm. Tekanan osmotik diabaikan dan tidak memperhitungkan adanya polarisasi konsentrasi. Membran ini memiliki struktur asimetrik dan simetrik.
Membran ultrafiltrasi merupakan proses pemisahan antar molekul dan berfungsi menyaring makromolekul > 5000 g/mol atau partikel berukuran 0.001–0.100 µ m. Tekanan yang digunakan 1.00–3.00 atm. Tekanan osmotik diabaikan dan tidak memperhitungkan adanya polarisasi konsentrasi. Membran ini memiliki struktur asimetrik.
Membran osmosis balik berfungsi menyaring garam–garam organik > 50 g/mol atau partikel berukuran 0.0001 –0.0010 µm. Tekanan yang digunakan yaitu 8.00–12.00 atm.
Membran dialisis berfungsi memisahkan larutan koloid yang mengandung elektrolit dengan berat molekul kecil. Zat terlarut pada larutan yang konsentrasinya tinggi akan menembus membran ke arah larutan yang konsentrasinya rendah, jadi konsentrasi merupakan gaya pendorong.
Membran elektrodialisis berfungsi memisahkan larutan dengan membran melalui pemberian muatan listrik. Yang menjadi gaya pendorong adalah gaya gerak listrik.
Mallevialle et. al. (1996) menyatakan klasifikasi membran ada empat : berdasarkan bahan pembuatan, morfologi, ada atau tidak adan y a pori dan sifat geometris. Membran berdasarkan bahan pembuatan dibagi menjadi dua golongan yaitu bahan organik dan anorganik. M embran dari bahan organik dibagi lagi menjadi dua bagian antara lain (a) membran alamiah contohnya membran yang terbuat dari selulosa atau turunannya seperti selulosa nitrat dan as etat, dan (b) membran sintesis contohnya polisulfon, poliamida, dan polimer sintesis lainnnya.
Brocks (1983) menyatakan bahwa membran dapat dibedakan berdasarkan ukuran partikel: (1) mikrofilter, memisahkan partikel yang berukuran 10.00–0.10 µm, (2) ultrafilter, memisahkan partikel yang berukuran 0.1–0.01 µm, (3) nanofilter, memisahkan partikel yang berukuran 0.010–0.001 µm , dan (4) osmosis balik, memisahkan partikel yang berukuran 0.0010–0.0001 µm. Berdasarkan gaya penggerak membran dapat d ibedakan menjadi empat yaitu (1) perbedaan suhu, (2) perbedaan konsentrasi, (3) perbedaan tekanan, dan (4) perbedaan potensial kimia.
Pencirian Membran Pencirian, disain, dan segi teknik kimia merupakan beberapa faktor yang harus diperhatikan dalam kinerja membran. Menurut Brocks (1983), Osada dan Nakagawa (1992), dan Wenten (1999), pencirian membran terdiri dari struktur, ukuran pori, dan sifat fisik mekanik serta kimia membran.
Membran ada yang memiliki ukuran pori yang seragam dan ada yang tidak ser agam. Untuk mengetahui ukuran pori suatu membran dapat digunakan alat–alat sebagai berikut: 1 Scanning Electron Microscope (SEM)
merupakan metode yang tepat untuk pencirian membran mikrofiltrasi. Batas resolusi mikroskop electron 0.01 µm (10 nm) dan s ekitar 0.005 µm (5 nm). 2 Tranmission Electron Microscope (TEM)
memiliki energi resolusi yang lebih tinggi daripada SEM.
5
4 Dengan cara melewatkan larutan yang berisi partikel yang ukuran partikelnya sudah diketahui.
Sifat mekanik yang penting dalam pengujian antara lain kekuatan tarik (tensile strength), elongasi, kekuatan lentur, kekuatan patah, dan modulus elastisitas. Beberapa cara yang dapat dilakukan untuk memperbaiki sifat mekanik membran yaitu pemanasan (annealing) dan meningkatkan derajat kristalinitas (Zeman dan Zydney 1996, Wenten 1999, dan Brocks 1983). Derajat kristalinitas adalah benyaknya fasekristalin yang terbentuk dalam polimer. Derajat kristalinitas membran dapat mempengaruhi permeabilitas, selektivitas dan sifat mekanik membran . Semakin besar derajat kristalinitas maka sifat mekanik dari polimer semakin baik.
Sifat kimia yang penting dalam kinerja membran antara lain ketahanan terhadap suhu tinggi dan zat kimia tertentu, sifat hidrofilik atau hidrofobik, ada tidaknya muatan ion atau daya tarik terhadap partikel dalam umpan (Zeman dan Zydney 1996). Brocks (1983) menyatakan bahwa yang perlu diperhatikan adalah kandungan mineral yang terdapat dalam membran dan zat larut yang terdapat dalam larutan yang belum dipisahkan.
Jenis bahan pembuat dan proses pembuatan dapat mempengaruhi pencirian membran itu sendiri. Pada umumnya membran yang terbuat dari selulosa dan turunannya memiliki daya tarik yang besar dibandingkan dengan membran sintetis. Keunggulan membran sintetis adalah tahan terhadap pH umpan. Menurut Zeman dan Zydney (1996), terdapat empat morfologi pori membran, antara lain: sel tutup, sel terbuka, jaringan serat, dan granula.
Nilai fluks dan rejeksi merupakan parameter utama dalam menilai kinerja membran (Wenten 1999 dan Osada dan Nakagawa 1992). Penurunan fluks terjadi karena adanya fouling pada membran tetapi adanya fouling dapat meningkatkan rejeksi, untuk mencegah adanya fouling maka membran harus selalu dibersihkan. Faktor yang mempengaruhi nilai fluks antara lain tekanan transmembran, kecepatan cross–flow .
dan konsentrasi larutan.
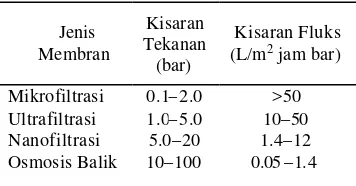
Mulder (1996) menyatakan kisaran fluks dan tekanan berbagai jenis membran dapat dilihat pada Tabel 2.
Tabel 2 Kisaran fluks dan tekanan berbagai jenis membran
Sumber: Mulder (1996)
Filtrasi
Filtrasi adalah pemisahan dengan mengalirkan umpan melalui suatu membran dan molekul yang berukuran lebih besar akan tertahan pada permukaan membran (Gutman 1987). Proses filtrasi dapat pula dikatakan sebagai proses pemisahan dua atau lebih komponen dalam suatu aliran fluida. Proses itu digunakan untuk memisahkan padatan, komponen tidak terlarut , dan partikel lain yang tidak dikehendaki dalam suatu cairan. Proses filtrasi dengan menggunaka n membran sering digunakan untuk memisahkan padatan yang tidak terlarut dalam produk cair. Lapisan media akan menolak padatan tersuspensi dan akan menghasilkan cairan yang jernih (Cheryan 1992).
Proses filtrasi diklasifikasikan berdasarkan ukuran molekul dari komponen yang tertahan oleh media filter. Filtrasi dibagi menjadi dua bagian: filtrasi partikel konvensional (dead– end filtration) dan proses filtrasi membran (cross–flow filtration). Pemisahan partikel besar yang tersuspensi berukuran lebih dari 10 µm dapat menggunakan filtrasi partikel konvensional sedangkan memisahkan zat berukuran kurang dari 10 µm menggunakan filtrasi membran.
Wenten (1999) menyatakan bahwa ada beberapa perbedaan antara filtrasi partikel konvensional dan filtrasi membran:
1 Media filtrasi yang digunakan pada proses konvensional berstruktur terbuka dan tebal, sedangkan pada membran bergantung ukuran pori dan tipis.
2 Tekanan filtrasi membran yang digunakan adalah daya pendorong untuk pemisahan dan pada filtrasi konvensional tekanan digunakan untuk mempercepat proses. 3 Desain proses. Aliran umpan pada filtrasi
konvensional tegak lurus media penyaring dan dilakukan pada sistem terbuka, sedangkan filtrasi membran menggunakan
Jenis Membran Kisaran Tekanan (bar) Kisaran Fluks (L/m2 jam bar)
desain silang atau aliran tangensial dan dilakukan pada sistem t ertutup.
4 Derajat pemisahan. Pada filtrasi konvensional, material yang tersuspensi dapat dipisahkan secara sempurna dari cairan. Filtrasi membran hanya dapat memekatkan mineral yang tertahan dalam jumlah kecil terhadap cairan semula. Menurut Mallevialle et. al. (1996), pada dasarnya operasi pemisahan menggunakan membran adalah memisahkan bagian tertentu dari umpan (feed) menjadi rentetat (larutan yang tidak tersaring) dan permeat (larutan yang telah tersaring). Umpan merupakan larutan yang berisi satu atau lebih campuran molekul atau partikel yang akan dipisahkan. Sesuatu yang melewati pori membran disebut permeat dan rentetat adalah sesuatu yang tidak dapat melewati pori membran.
Zeman dan Zydney (1996) menyatakan prinsip cross–flow filtration pada membran skematis dapat dilihat pada Gambar 1.
Umpan Rentetat Membran Permeat
Gambar 1 Prinsip Cross –Flow Filtration
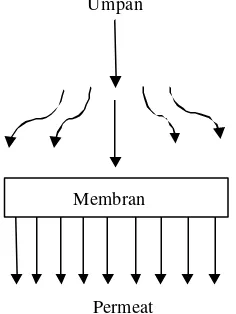
Prinsip dead–end filtration pada membran dapat dilihat Gambar 2.
Umpan
Membran
Permeat
Gambar 2 Prinsip Dead–End Operation
Fouling adalah suatu gejala yang disebabkan oleh deposisi dan akumulasi secara irreversible dari partikel submikron pada permukaan membran atau kristalisasi serta presipitasi dari partikel berukuran kecil pada permukaan atau di dalam membran itu sendiri (Wenten 1999). Menurut Cheryan (1986), fouling merupakan proses terakumulasinya komponen–komponen secara permanen akibat filtrasi itu sendiri. Fouling
membran bergantung pada parameter fisik dan kimia seperti pH, suhu, kekuatan ion, dan interaksi spesifik (ikatan H).
Henry (1988) menyatakan bahwa fouling
disebabkan karena terakumulasinya partikel pada permukaan membran yang semakin lama semakin menumpuk, sehingga mengakibatkan terjadinya penurunan fluks dan perubahan selektivitas. Fouling pada membran disebabkan antara lain lapisan endapan organik (seperti makromolekul, bahan biologis dan sebagainya) dan lapisan endapan anorganik (seperti logam hidroksida dan garam –garam kalsium).
Polarisasi konsentrasi dan fouling dapat membatasi proses pemisahan dengan membran karena keduanya menyebabkan penurunan fluks permeat sehingga menurunkan semua kinerja membran. Penurunan fluks secara berkelanjutan dapat disebabkan oleh fouling partikel–partikel seperti koloid, emulsi, suspensi, makromolekul, garam, dan lain–lain yang menempel pada permukaan membran.
Secara umum ada tiga tipe foulant: partikel, lapisan endapan organik (makromolekul, bahan –bahan biologis, dsb), dan lapisan endapan anorganik (logam hidroksida, garam kalsium dsb) (Mulder 1996).
Beberapa cara yang dapat dilakukan untuk menangani fouling dan polarisasi konsentrasi sebagai berikut (1) perlakuan awal pada larutan umpan. Metode meliputi perlakuan panas, penyesuaian pH, penambahan senyawa kompleks, klorinasi, penyerapan pada karbon aktif , penjernihan kimia, ultrafiltrasi, dan mikrofiltrasi awal, serta (2) sifat –sifat membran.
Pengurangan polarisasi konsentrasi dapat dilakukan dengan menambahkan golakan aliran dekat membran, pencucian berkala, mengurangi tekanan, mengurangi kadar makro terlarut (berat molekul tinggi), mempertinggi suhu , dan memperbesar kelarutan makromolekul.
7
polarisasi konsentrasi. Mulder (1996) dan Wenten (1999), menyatakan metode pencucian ada empat macam, antara lain: 1 Pencucian balik merupakan metode
pencucian yang hanya dapat dilakukan pada membran mikrofiltrasi dan ultrafiltrasi. Teknik pencucian balik merupakan teknik yang umum digunakan untuk penghilangan zat pengotor yang terakumulasi di permukaan membran. Ada dua cara yang dilakukan yaitu pembilasan balik (backflushing) dengan menggunakan permeat dan rangkaian pencucian yang terdiri dari penghembusan udara melalui membran dan pembilasan dengan menggunakan larutan umpan.
2 Pencucian secara mekanik merupakan metode pencucian yang hanya dapat dilakukan pada sistem tubular dengan menggunakan spon.
3 Pencucian secara kimia merupakan metode pencucian yang sangat penting dalam mengurangi fouling. Penambahan zat kimia pada membran dengan jangka waktu tertentu merupakan ciri dari pencucian ini. Adapun bahan kimia yang biasa digunakan untuk pencucian ini antara lain: asam (H3PO4 dan asam sitrat),
basa (NaOH), detergen (alkali dan non– ionik), enzim (protease, amilase, dan lipase), senyawa kompleks (EDTA dan sodium heksametafosfat), desinfektan (H2O2 dan NaOCl), panas , dan gas (etilen
oksida).
4 Pencucian secara elektrik merupakan metode pencucian yang praktis untu k dilakukan karena menggunakan listrik dan susunan modul khusus yang dilengkapi dengan elektroda.
BAHAN DAN METODE Bahan dan Alat
Bahan–bahan yang diperlukan dalam penelitian ini ialah starter (bakteri Acetobacter xylinum) yang diperoleh dari Balai Besar Industri Agro (BBIA) , kulit nanas yng diperoleh dari pedagang buah nanas di Pasar Jambu Dua Bogor, asam asetat glasial, gula pasir, (NH4) 2SO4, dan air.
Alat–alat yang digunakan dalam penelitian ini ialah penghancur Philips HR 2815/A , panci, pisau pemotong, neraca analitik, tempat untuk inkubasi, kertas steril, karet pengikat, termometer, kertas saring, kertas pH, SEM model JSM 5310LV, FTIR model Excalibur
series BIORAD, fluks membran , mesin
hydraulic press (hot press dan cold press) merek GONNO No 023 26 dan 02327, dan alat–alat kaca.
Metode Penelitian Pembuatan n ata de pina
Kulit buah nanas dihancurkan hingga di peroleh sari kulit buah kemudian disaring. Lalu dilakukan pengenceran dengan perbandingan 1:4, 1:2, dan 1:1 (sari kulit nanas dan air) yan g diikuti dengan penambahan gula pasir sebanyak 10% dan 5% b/v (1:4 10%, 1:4 5%, 1:2 10%, 1:2 5%, 1:1 10%, dam 1:4 5%) dan amonium sulfat sebanyak 0,10% b/v sebagai sumber karbon dan nutrisi. Kemudian membran tersebut dijadikan sebagai membrane sample untuk analisis membran selanjutnya.
Sari kulit buah nanas kemudian direbus selama ± 15–20 menit sampai mendidih pada suhu 100 oC. Kemudian didinginkan sampai suhu 28 oC dan diatur pH–nya menjadi 4.5 dengan penambahan asam asetat glasial sebanyak 2% (v/v). Tiap –tiap wadah fermentasi diisi 200ml sari kulit buah dan langsung ditutup dengan kertas steril dan diikat dengan karet pengikat.
Penambahan inokulum sebanyak 10% (v/v) dilakukan apabila medium telah benar– benar dingin dan diinkubasikan selama lima hari pada suhu kamar.
Pencirian membran dengan fluks air Sampel yang telah dipress dibentuk lingkaran dengan diameter 5.80 cm s esuai dengan modul tempat sampel yang berada pada alat penguji fluks tersebut. Sampel yang telah dibentuk ditempatkan dalam modul lalu dijepit. Kemudian modul tersebut dihubungkan dengan selang pengalir umpan, rentetat, permeat, serta selang pengatur tekanan. Kemudian umpan dialirkan dan tekanannya diatur sehingga didapatkan hasil yang diinginkan. Jumlah volume permeat yang dihasilkan dan waktu yang dibutuhkan dicatat. Dari volume dan waktu tersebut dapat diketahui besarnya fluks yang dimiliki oleh sampel.
Pencirian membran dengan FTIR
sampel dianalisis dan spektrum yang terbentuk dicatat.
Pencirian membran dengan SEM
Sampel yang telah dipress dipotong kecil lalu ditempelkan pada tempat sampel. Kemudian sampel ditempatkan dalam seb uah tabung untuk dilapis permukaannya oleh emas (coating) selama 20 menit. Selanjutnya sampel yang telah dilapis tersebut ditempatkan ke dalam SEM dan dicari perbesaran yang paling bagus sehingga terlihat dan diketahui bentuk permukaannya. Setelah didapat gambar yang sesuai lalu gambar tersebut difoto dan disimpan dalam disket. Bagan alir penelitian dapat dilihat lebih jelas pada Lampiran 1.
HASIL DAN PEMBAHASAN
Nata de pina
Nata de pina dibuat berdasarkan prosedur pembuatan nata de coco, hanya berbeda pada bahan baku yang digunakan. Nata de pina
dibuat dari limbah buah nanas yakn i kulit buah nanas yang diperoleh dari pasar Jambu Dua Bogor. Kulit buah nanas dipilih yang masih segar atau belum terlalu lama dikupas dari buahnya. Hal ini sangat penting karena kulit nanas yang masih segar dapat menghasilkan sari kulit yang cukup banyak, lain halnya dengan kulit yang sudah kering atau tidak segar. Selain itu penggunaan bahan yang tidak segar dapat menimbulkan bakteri pengganggu yang dapat mempengaruhi kinerja dari starter dalam membentuk nata
tersebut. Keadaan larutan pada saat diinkubasi dapat dilihat pada Gambar 4.
Nata de pina yang telah terbentuk harus segera dipanen sebab jika dibiarkan terlalu lama akan mengundang tumbuhnya jamur pada permukaan nata tersebut. Jamur apabila dibiarkan terlalu lama akan merusak struktur
nata yang dihasilkan. Perusakan struktur nata
disebabkan akar jamur yang tumbuh ke dalam
nata dapat merusak struktur dan mempengaruhi pori-pori nata yang terbentuk. Setelah dipanen nata tersebut harus segera dibersihkan dan lapisan tipis yang ada dipermukaan nata harus segera dibuang karena lapisan tersebut banyak menmgandung bakteri yang dapat mempengaruhi analisis selanjutnya.
Pada awalnya proses inkubasi berlangsung selama limabelas hari dan dihasilkan nata
dengan ketebalan sekitar 1.50 cm. Nata
dengan ukuran ini ternyata tidak dapat
digunakan karena terlalu tebal untuk dipress
dan hasil setelah dipress tidak terlalu bagus karena penyebaran ketebalannya tidak merata. Untuk selanjutnya digunakanlah nata dengan ukuran setebal 5 mm hasil inkubasi selama lima hari. Keadaan nata pada inkubasi hari ke–5 dapat dilihat pada Gambar 4.
Gambar 3 Wadah dan larutan saat diinkubasi.
Gambar 4 Nata s etelah lima hari inkubasi dengan ketebalan 5 mm.
Nata yang telah diinkubasi selama lima hari dan memiliki ketebalan 5 mm dipanen lalu dicuci dengan air yang mengalir. Pencucian ini ditujukan untuk membersihkan
nata dari larutan dan bakteri yang masih berada pada nata tersebut. Karena pada saat pembuatan larutan menggunakan asam asetat glasial dengan konsentrasi yang tinggi, maka
9
bersifat basa. Proses penetralan berlangsung dengan cara merendam nata dalam larutan basa selama 2 jam. Proses perendaman tidak perlu berlangsung lama karena dikhawatirkan
nata tersebut menjadi basa dan akan menimbulkan bau yang tidak sedap. Setelah direndam selama 2 jam kemudian nata dibilas dengan air dan selanjutnya direndam kembali dalam air selama semalam untuk menghilangkan basa dan mengkondisikan
nata pada kondisi yang netral. Nata selanjutnya dipress dengan mesin hydraulic press untuk mendapatkan suatu lapisan tipis (thin layer) dan menghilangkan air yang masih terdapat pada nata. Lapisan tipis tersebut dinamakan membran selulosa. Nata
yang telah dipanen dan dipress sehingga menjadi sebuah membran selulosa dapat dilihat pada Gambar 5 dan 6.
Gambar 5 Nata yang telah dipanen dan dibersihkan
Gambar 6 Nata yang telah dipress
Analisis fluks air
Membran selulosa yang didapatkan selanjutnya digunakan untuk pengukuran fluks air dengan menggunakan alat fluks membran. Fluks air merupakan parameter yang penting dalam mengpencirian suatu membran. Fluks merupakan nilai dari volume permeat dibagi dengan jumlah luas permukaan, besarnya tekanan dan lamanya waktu yang dibutuhkan oleh umpan untuk melewati membran. Fluks membran yang menggunakan system filtrasi bekerja dengan tekanan sebagai pendorong bukan untuk mempercepat proses seperti yang digunakan pada fluks membran dengan system filtrasi konvendsional. Dari data fluks yang diperoleh dapat diambil kesimpulan pertama jenis dan tipe membran yang diukur.
Alat fluks membran ini sangat sederhana dan tidak terlalu sulit untuk mengoperasikannya. Hal ini dikarenakan fluks membran hanya terdiri dari sebuah pompa yang memiliki tekanan hingga 80 psi. Pompa tersebut tersambung dengan sebuah selang yang berfungsi sebagai saluran umpan, dan dihubungkan dengan sebuah modul berbentuk bulat yang terbuat dari bahan polimer serta bagian dalamnya berlubang dan berfungsi untuk menaruh membran dengan diameter sebesar 5.8 cm. Fluks membran memiliki tiga bagian yang dapat diukur yakni umpan, permeat (air yang terlewatkan oleh membran) dan rentetat (air yang tidak terlewatkan oleh membran). Permeat dapat melewati membran disebabkan permeat terdiri dari partikel– partikel yang berukuran lebih kecil atau sama dengan ukuran pori–pori membran sehingga dapat melewati membran tersebut. Sedangkan rentetat merupakan kebalikan dari permeat. Data tentang permeat dapat digunakan untuk menentukan besarnya fluks yang dimiliki oleh membran tersebut.
Pengukuran fluks membran dilakukan pada membran–membran sampel. Diharapkan dengan pembedaan jenis membran ini dapat diketahui membran mana yang memiliki spesifikasi yang baik dan dapat digunakan lebih jauh lagi khususnya di bidang industri yang ada di Indonesia. Pengukuran dluks sangat penting dalam mengpencirian suatu membran, karena dengan pengukuran ini dapat diketahui sifat awal dari membran khususnya dalam mengetahui jenis filtrasi apa yang dapat dilakukan oleh membran yang diukur tersebut. Fluks yang digunakan menggunakan prinsip cross-flow filtration
untuk mengetahui jenis-jenis filtrasi pada membran yang dinalisis.
Tabel 3 Nilai Rerata Fluks yang Terukur pada Sampel
Tabel 3 merupakan data–data hasil dari pengukuran fluks terhadap berbagai jenis membran . Data tersebut merupakan rerata dari data pengukuran fluks air yang terdapat pada Lampiran 2. Pada pengukuran dengan alat fluks membran parameter yang diperhatikan adalah volume permeat dan waktu laju alir permeat untuk mencapai volume yang diinginkan. Volume permeat yang digunakan pada penelitian ini ialah sebesar 250 ml dan tekanan yang digunakan sebesar 0,35 bar. Besarnya tekanan yang digunakan mengikuti spesifikasi membran yang ada serta mengacu pada tekanan yang dipakai dalam mengp encirian membran dari nata de coco
yang pada dasarnya serupa dengan nata de pina. Hal ini disebabkan oleh proses pembuatan nata de pina memakai metode yang sama dengan pembuatan natade coco. Pada saat tekanan yang digunakan melebihi dari tekanan di atas maka akan menyebabkan membran tersebut menjadi bocor dan rusak sehingga pengukuran yang dilakukan tidak dapat optimal. Dari hasil pengukuran didapatkan waktu alir permeat yang bervariasi. Tetapi dari keseluruhan data yang
diperoleh pada penambahan 10% b/v gula, tidak didapatkan nilai fluks yang baik. Ini ditandai dengan masih besarnya nilai fluks yang terukur. Nilai fluks yang baik yang dapat diterima ialah membran dengan fluks yang kecil yakni pada membran-membran dengan konsentrasi gula 5% b/v. Sementara pada membran dengan konsentrasi gula 10% b/v memiliki nilai fluks diatas 50.000 L/m2jambar. Walaupun nilai fluks yang terukur semakin lama semakin menurun yang merupakan akibat dari gejala fouling. Tetapi tetap saja hal ini tidak bisa dikatakan sebagai hasil yang baik sebab pada pengukuran awal saja waktu yang terukur masih terlalu kecil. Hal ini menandakan bahwa membran tersebut tidak terlalu efektif dalam menyaring partikel yang ada dalam air karena waktu yang dibutuhkan untuk mengalirkan permeat hingga volume 250 ml masih terlalu kecil. Gejala ini dapat disebabkan oleh ukuran pori yang masih terlalu besar sehingga membran dapat dengan mudah untuk melewatkan permeat.
Seperti yang telah dikemukakan sebelumnya bahwa waktu yang paling baik dalam pengukuran fluks air ialah waktu yang paling besar, dan hal tersebut terjadi pada pengukuran membran dengan perbandingan sari kulit nanas. Pada jenis membran itu didapatkan waktu yang besar dibandingkan dengan jenis–jenis membran yang lain dengan lima kali ulangan. Sehingga didapatkan nilai fluks yang relatif kecil pada membran itu dibandingkan dengan membran yang lain. Lamanya waktu alir tersebut disebabkan oleh ukuran pori pada membran 1:4 (sari kulit nanas dan air) dan gula 5% b/v lebih kecil dan lebih rapat dibandingkan dengan membran yang lain, sehingga membran mampu menahan sebagian larutan umpan terutama yang mengandung partikel–partikel besar yang berukuran lebih dari 3 µm dan waktu alir yang terukur pun menjadi lebih besar dibandingkan dengan membran–membran yang lain dan bertambahnya waktu alir pada pada saat pengulangan disebabkan oleh gejala
fouling yang terjadi pada membran.
Gejala fouling merupakan gejala yang disebabkan oleh deposisi dan akumulasi secara irreversible dari partikel submikron pada permukaan membran atau kristalisasi serta presipitasi dari partikel berukuran kecil pada permukaan atau di dalam membran itu sendiri (Wenten, 1999). Menurut Cheryan (1986), fouling merupakan proses terakumulasinya komponen–komponen secara Jenis Membran Fluks Air
( L/m2 jam bar ) 1:4 (sari kulit nanas
dan air) dan konsentrasi gula
10% b/v
61738.24
1:4 (sari kulit nanas dan air) dan konsentrasi gula 5%
b/v
49383.69
1:2 (sari kulit nanas dan air) dan konsentrasi gula
10% b/v
63939.48
1:2 (sari kulit nanas dan air) dan konsentrasi gula 5%
b/v
23183.41
1:1 (sari kulit nanas dan air) dan konsentrasi gula
10% b/v
94769.30
1:1 (sari kulit nanas dan air) dan konsentrasi gula 5%
b/v
11
permanen akibat filtrasi itu sendiri. Hal tersebut disebabkan oleh umpan yang digunakan yakni air mengandung partikel – partikel yang berukuran hampir sama atau lebih besar dari ukuran pori–pori membran sehingga partikel–partikel tersebut akan menumpuk pada permukaan membran dan menghambat kemampuan membran untuk melewatkan larutan umpan sehingga waktu alir permeat menjadi lebih lama. Proses
fouling ini dapat dihilangkan dengan cara memcuci membran sehingga terbebas dari partikel–pertikel yang memenuhi pori–pori membran .
[image:30.612.330.510.523.699.2]Gejala penurunan nilai fluks dapat dilihat pada Gambar 7. Gambar tersebut merupakan kurva hubungan antara waktu dengan fluks air pada membran 1:4 (sari kulit nanas dan air) dan gula 5% b/v. Dari gambar tersebut dapat terlihat bahwa dengan bertambahnya waktu maka akan menurunkan nilai fluks yang terjadi pada membran tersebut. Pada ulangan pertama hingga ketiga pada gambar tersebut tidak terjadi penurunan nilai fluks air yang tajam tetapi pada ulangan keempat dan kelima mulai terjadi penurunan fluks yang signifikan. Hal tersebut berarti membran tersebut telah mulai mengalami gejala fouling yang mengkibatkan berkurangnya keefektifan kinerja membran dalam menyaring larutan umpan sehingga waktu yang dibutuhkan oleh membran untuk melewatkan permeat menjadi semakin besar. Dari analisis awal menggunakan fluks membran, dapat diketahui bahwa membran tersebut merupakan membran mikrofiltrasi setelah membandingkan dengan spesifikasi membran yang ada. Sepeti yang dikemukakan oleh Mulder (1996), membran mikrofiltrasi memiliki kisaran tekanan 0.10-10.00 bar dan kisaran fluks air > 50 L/m2jambar.
Gambar 7 Hubungan antara waktu dan fluks air pada membran membran 1:4 (sari kulit nanas dan air) dan gula 5% b/v.
Kajian Spektrum FTIR Membran Pengukuran fluks membran telah memberikan data–data yang dibutuhkan untuk mengetahui jenis dan pencirian membran yang diukur. Dengan dasar ini maka analisis membran menggunakan FTIR didasarkan pada hasil analisis dengan fluks membran. Sehingga jenis membran yang digunakan dalam analisis FTIR merupakan membran yang memiliki nilai fluks yang kecil, yakni membran 1:4 (sari kulit nanas dan air) dan gula 5% b/v dan nilai fluks yang besar, yakni membran membran 1:1 (sari kulit nanas dan air) dan gula 10% b/v.
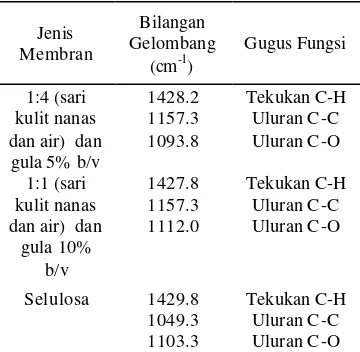
Tabel 4 merupakan gambaran rinci dari puncak-puncak yang ada pada membran-membran yang diukur. Dari tabel di atas dapat dilihat terdapatnya gugus-gugus penyusun suatu selulosa, yakni C-C, C-O, dan C-H. Puncak-puncak yang terbentuk berada pada daerah yang hampir sama atau berdekatan antara membran membran 1:4 (sari kulit nanas dan air) dan gula 5% b/v dan membran 1:1 (sari kulit nanas dan air) dan gula 10% b/v. Hal ini menandakan bahwa kedua membran tersebut memiliki struktur penyusun yang sama. Demikian pula jika dibandingkan dengan spektrum selulosa, akan terdapat puncak-puncak gugus fungsi yang sama dan pada daerah yang hampir sama pula dengan kedua membran yang diukur. Dari data-data yang terukur tersebut dapat dikatakan kedua membran tersebut memiliki struktur yang sama dengan selulosa. Jadi kedua membran tersebut dapat dikatakan sebagai suatu selulosa karena spektrum yang dimilikinya sama dengan selulosa.
Tabel 4 Hasil analisis dengan FTIR
Jenis Membran
Bilangan Gelombang
(cm-1)
Gugus Fungsi
1:4 (sari kulit nanas dan air) dan gula 5% b/v
1428.2 1157.3 1093.8 Tekukan C-H Uluran C-C Uluran C-O 1:1 (sari kulit nanas dan air) dan
gula 10% b/v 1427.8 1157.3 1112.0 Tekukan C-H Uluran C-C Uluran C-O
Selulosa 1429.8 1049.3 1103.3
[image:30.612.136.294.541.632.2]Gambar 8 Spektrum IR membran membran 1:4 (sari kulit nanas dan air) dan gula 5% b/v
Gambar 9 Spektrum IR membran membran 1:1 (sari kulit nanas dan air) dan gula 10% b/v
Gambar 7 dan 8 menunjukkan spektrum IR yang menberikan keterangan tentang gugus apa saja yang berada pada membran. Data-data tentang gugus tersebut dapat dilihat pada Tabel 4. Dari gambar dapat dilihat puncak– puncak gugus fungsi sehingga apabila ketiga gugus tadi digabungkan menurut kaedah IR maka akan tampak suatu senyawa yakni selulosa. Dan apabila dibandingkan dengan spektrum IR selulosa asli, maka akan tampak bentuk spektrum yang sama antara selulosa asli dengan membran yang dianalisis sehingga jelas bahwa membran tersebut merupakan suatu selulosa seperti yang tampak pada Gambar 9 dan 10.
Gambar 10 Spektrum IR selulosa asli
Gambar 11 Spektrum IR membran dan selulosa asli
[image:31.612.131.307.243.339.2]Analisis ukuran pori–pori Pencirian membran selain dengan nilai fluks air dan FTIR, dapat juga dilakukan dengan menggunakan mikroskop elektron SEM. Alat ini sangat berguna sekali untuk mengetahui bentuk permukaan membran dan jumlah serta ukuran pori –pori membran yang dianalisis lebih jauh lagi analisis dengan SEM ini dapat dijadikan pula data pendukung untuk mendukung hipotesis yang digunakan atau data yang telah terukur dari analisis fluks membran sebelumnya. Sebab, dengan menggunakan SEM pula dapat diketahui jenis membran apa yang sedang dianalisis.
[image:31.612.329.505.383.545.2]Gambar 12 Permukaan membran 1:4 (sari kulit nanas dan air) dan gula 5% b/v dengan perbesaran 1500X
[image:31.612.134.310.569.679.2]13
yang lebih besar dari 3.00 µm. Sehingga dapat diketahui bahwa permeat yang terbentuk terdiri dari partikel yang berukuran = 3.00 µm sedangkan rentetat memiliki ukuran partikel = 3.00 µm. Maka dengan membandingkan ukuran pori membran yang dianalisis terhadap spesifikasi membran yang dikemukakan oleh Mulder (1996) dan Wenten (1999) dapat diketahui bahwa membran yang dianalisis merupakan jenis membran mikrofiltrasi sebab kisaran pori–porinya termasuk dalam kisaran pori–pori yang dimi liki oleh membran mikrofiltrasi yakni 0.10- 10.00 µm.
SIMPULAN DAN SARAN Simpulan
Hasil penelitian menunjukkan bahwa membran selulosa dapat dibentuk oleh A. xylinum dalam larutan sari kulit nanas selain dalam larutan air kelapa. Pembuatan membran dapat lebih mudah jika membran tesebut dipress memiliki ketebalan 5 mm yang didapatkan dari hasil inkubasi selama lima hari. Berdasarkan hasil pengukuran fluks air dan SEM dapat diambil kesimpulan bahwa membran yang dianalisis merupakan jenis membran mikrofiltrasi setelah membandingkan hasil yang diperoleh dengan spesifikasi membran yang ada. Berdasarkan analisis gugus fungsi dengan FTIR dapat diketahui bahwa membran tersebut merupakan membran selulosa karena spektrum yang terukur pada membran yang dianalisis serupa dengan spekt rum selulosa asli.
Saran
Modifikasi pada membran seperti asetilasi dan penambahan porogen perlu dilakukan untuk mendapatkan membran yang lebih baik dengan pori–pori yang dapat ditentukan ukuran dan jumlahnya, serta dapat dihasilkan membran dengan spesifikasi yang lebih baik. Selain itu, perlu dilakukan pula analisis TEM dan indeks rejeksi.
DAFTAR PUSTAKA [Anonim ]. 2004. Fourier Transformed
Infra-red Spectroscopy. http://www.wcas-lab.Com/tech/tbftir.html [17 Jun 2004].
Brocks TD. 1983. Membran Filtration: A User’s Guide and Reference Manual. Madison: Science Tech.
Cheryan M. 1986. Ultrafiltration Handbook. Lancester: Technomic.
Eryan. 2004. Pemisahan Gas Dengan Membran Berpori. http://www.eryan @tf.itb.ac.id [1 Des 2004].
Gutman RG. 1987. Membran Filtration, The Rheological of Pressure Driven Cross– Flow Process. England: IOP Publishing Ltd.
Henry JD. 1988. Crossflow Filtration: Recent Development in Separation Science. Cleveland Ohio: CRC Pr.
Lapuz MM, EG Gallerdo, MA Palo. 1967. The nata organism–cultural requirements, characteristics and Identify. Phlippines J. of Sci 96(2): 91-107.
Mallevialle J, Odendaals PE, Wichser MR.
1996. Water Treatment Membran Processes. New York: McGraw -Hill.
Morton JF. 1987. Pineapple, Fruits of Warm Climates. http://www.hort.purdue.edu/ne-wcrop/morton/pineapple.html [29 Juni 2004].
Mulder M. 1996. Basic Principles of Membran Technology. Netherland: Kluwer.
Osada Y, Nakagawa T. 1992. Membran Science and Technology. New York: Marcel Dekker.
Scott K, Hughes R. 1996. Industrial Membran Separation Technology London: Blackie Academic and Proffesionals.
Sudjadi. 1983. Penentuan Struktur Senyawa Organik. Jakarta: Ghalia Indonesia.
Susanto T, R Adhitia, Yunianta. 2000. Pembuatan nata de pina dari kulit nanas kajian dari s umber karbon dan pengenceran medium fermentasi. Jurnal Teknologi Pertanian 1(2):58-66.
Wenten IG. 1996. Teknologi Industrial Membran. Bandung: Departemen Teknik ITB.
Lampiran 1. Bagan alir metode percobaan
Dipotong-potong, dicuci, dihancurkan, lalu disaring
Filtrat
Larutan Sampel
Dididihkan, lalu didinginkan semalam. Ditambahkan asam asetat glasial 2% b/v, serta starter sebanyak 10% v/v.
Diinkubasi selama 5 hari
Nata de Pina
Dipress
Membran
Analisis Fluks Air
Analisis FTIR
Analisis SEM
Diencerkan dengan perbandingan 1:4, 1:2, dan 1:1, lalu ditambahkan gula dengan konsentrasi 10 dan 5%, sert a (NH4)2SO4
17
Lampiran 2. Data Pengukuran Fluks Air Pada Membran
Jenis Membran
Ulangan Tekanan ( bar )
Luas Permukaan
( m2 )
Volume ( L )
Waktu ( jam )
Fluks Air ( L/m2 jam
bar ) 1:4 (sari kulit nanas dan air) dan konsentrasi gula 10% b/v 1 2 3 4 5 0.35 0.35 0.35 0.35 0.35 1.13.10–3 1.13.10–3 1.13.10–3 1.13.10–3 1.13.10–3 0.25 0.25 0.25 0.25 0.25
1.00 x 10–2 1.03 x 10–2 1.03 x 10–2
1.03 x 10–2 1.03 x 10–2
63211.12 61370.02 61370.02 61370.02 61370.02 . 1:4 (sari kulit nanas dan air) dan konsentrasi
gula 5% b/v 1 2 3 4 5 0.35 0.35 0.35 0,.35 0.35 1.13.10–3 1.13.10–3 1.13.10–3 1.13.10–3 1.13.10–3 0.25 0.25 0.25 0.25 0.25
1.28 x 10–2 1.28 x 10–2 1.28 x 10–2 1.28 x 10–2 1.28 x 10–2
49383.69 49383.69 49383.69 49383.69 49383.69 1:2 (sari kulit nanas dan air) dan konsentrasi
gula 10% b/v 1 2 3 4 5 0.35 0.35 0.35 0.35 0.35 1.13.10–3 1.13.10–3 1.13.10–3 1.13.10–3 1.13.10–3 0.25 0.25 0.25 0.25 0.25
9.72 x 10–3 9.72 x 10–3 1.00 x 10–2 1.00 x 10–2 1.00 x 10–2
65032.02 65032.02 63211.12 63211.12 63211.12 1:2 (sari kulit nanas dan air) dan konsentrasi
gula 5% b/v 1 2 3 4 5 0.35 0.35 0.35 0.35 0.35 1.13.10–3 1.13.10–3 1.13.10–3 1.13.10–3 1.13.10–3 0.25 0.25 0.25 0.25 0.25
2.53 x 10–2 2.64 x 10–2 2.72 x 10–2 2.86 x 10–2 2.92 x 10–2
24984.63 23943.60 23239.38 22101.79 21647.64 1:1 (sari kulit nanas dan air) dan konsentrasi
gula 10% b/v 1 2 3 4 5 0.35 0.35 0.35 0.35 0.35 1.13.10–3 1.13.10–3 1.13.10–3 1.13.10–3 1.13.10–3 0.25 0.25 0.25 0.25 0.25
6.67 x 10–3 6.67 x 10–3 6.67 x 10–3 6.67 x 10–3 6.67 x 10–3
94769.30 94769.30 94769.30 94769.30 94769.30 1:1 (sari kulit nanas dan air) dan konsentrasi
gula 5% b/v 1 2 3 4 5 0.35 0.35 0.35 0.35 0.35 1.13.10–3 1.13.10–3 1.13.10–3 1.13.10–3 1.13.10–3 0.25 0.25 0.25 0.25 0.25
9.72 x 10–3 9.72 x 10–3 9.72 x 10–3 1.00 x 10–2 1.00 x 10–2
Contoh Perhiitungan :
Fluks Air = Volume Permeat
( Luas Permukaan x Waktu x Tekanan )
= 0,25 L
(1,13.10–3 m2 x 1,00.10–2 jam x 0,35 bar )
= 63211,12 L/m2 jam bar (Membran A1, Ulangan 1 )
Rerata Fluks Air = Jumlah fluks air dari 5 kali ulangan Jumlah ulangan
= (63211.12 + 61370.02 + 61370.02 + 6137002 + 61370.02) 5