KOMBINASI SPEKTRUM ULTRAVIOLET DAN
MODEL KALIBRASI MULTIVARIAT UNTUK
PENENTUAN SIMULTAN KAFEIN,
VITAMIN B1, B2, DAN B6
YULIA FATMAWATI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Multivariat untuk Penentuan Simultan Kafein, Vitamin B1, B2, dan B6. Dibimbing oleh MOHAMAD RAFI dan UTAMI DYAH SYAFITRI.
Kombinasi spektrum ultraviolet dan model kalibrasi multivariat telah dikembangkan untuk penentuan simultan kadar kafein, vitamin B1, B2, dan B6 dalam contoh minuman berenergi karena mempunyai kriteria cepat, mudah, dan tidak membutuhkan pemisahan terlebih dahulu. Teknik kalibrasi multivariat yang digunakan adalah regresi komponen berganda (principle component regression, PCR) dan kuadrat terkecil parsial (partial least square, PLS).
Kemampuan pendugaan yang lebih baik diberikan oleh PCR yang ditentukan berdasarkan nilai parameter validasi koefisien determinasi (R2) yang tinggi, root mean square error of calibration (RMSEC), dan root mean square error of prediction (RMSEP) yang kecil. Hasil yang diperoleh untuk kafein, vitamin B1, B2, dan B6 menunjukkan nilai RMSEC secara berturut-turut sebesar 0.1572, 0.2184, 0.0979, dan 0.2735. Nilai R2 sebesar 0.9984, 0.7143, 0.9970, dan 0.9822. Sedangkan nilai RMSEP sebesar 0.0991, 0.1168, 0.0782, dan 0.1308. Kadar kafein vitamin B1, B2, dan B6 yang diperoleh dari contoh minuman berenergi dengan PCR adalah 50.0452, 1.5120, 5.2502, dan 5.0045 mg. Berdasarkan evaluasi kinerja analitik pada contoh minuman berenergi, model terbaik juga diberikan oleh PCR karena diperoleh hasil presisi dan akurasi yang lebih baik dibandingkan PLS.
ABSTRACT
YULIA FATMAWATI. Combination of Ultraviolet Spectrum and Multivariate Calibration Models for Simultaneous Determination of Caffeine, B1, B2, and B6-Vitamins. Supervised by MOHAMAD RAFI and UTAMI DYAH SYAFITRI.
Combination of ultraviolet spectrum and multivariate calibration has been developed for simultaneous determination of caffeine, B1, B2, and B6-vitamins contents in energy drinks because it is a fast, easy, and simple method without any pre-separation. The multivariate calibration techniques were used principle component regression(PCR) and partial least square(PLS).
KOMBINASI SPEKTRUM ULTRAVIOLET DAN
MODEL KALIBRASI MULTIVARIAT UNTUK
PENENTUAN SIMULTAN KAFEIN,
VITAMIN B1, B2, DAN B6
YULIA FATMAWATI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
NIM :
G44203004
Menyetujui,
Pembimbing I,
Pembimbing II,
Mohamad Rafi, S.Si
Utami Dyah Syafitri, S.Si. M.Si
NIP 132 321 454
NIP 132 311 922
Mengetahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor,
Dr. drh. Hasim, DEA
NIP 131 578 806
Alhamdulillahi robbil’aalamin, puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya sehingga karya ilmiah ini dapat diselesaikan. Karya ilmiah berjudul Kombinasi Spektrum Ultraviolet dan Model Kalibrasi Multivariat untuk Penentuan Simultan Kafein, Vitamin B1, B2, dan B6 merupakan hasil penelitian yang dilaksanakan mulai bulan Mei sampai Juli 2007 di Laboratorium Kimia Analitik dan Laboratorium Bersama Departemen Kimia FMIPA IPB.
Penulis mengucapkan terima kasih kepada semua pihak yang telah membantu terselesaikannya karya ilmiah ini, di antaranya Mohamad Rafi, S.Si. dan Utami Dyah Syafitri, S.Si. M.Si. selaku pembimbing yang memberikan masukan, pengarahan, dan dorongan selama pelaksanaan penelitian dan penulisan karya ilmiah ini. Terima kasih penulis ucapkan kepada Mama dan Papa tercinta, Kodet, dan Ewink atas segala cinta, kasih sayang, semangat, kesabaran, dan doa yang diberikan. Penghargaan dan terima kasih penulis sampaikan kepada Pusat Studi Biofarmaka LPPM IPB, Om Em, seluruh laboran Kimia Analitik, MbakSiti, dan Mas Heri atas kemudahan yang diberikan kepada penulis.
Ungkapan terima kasih juga disampaikan kepada Riko dan Rahayu yang telah pusing dengan datanya, Elin, Chia, Niken, Wina, Rahma, Max, Ratna, Iqo, dan semua teman-teman Kimia angkatan 40 atas kebersamaan dan semangatnya, serta semua pihak yang telah membantu.
Semoga karya ilmiah ini bermanfaat.
Bogor, Desember 2007
Penulis dilahirkan di Solok, Sumatera Barat pada tanggal 23 Juli 1985 sebagai anak pertama dari pasangan Marion dan Etismawati. Tahun 2003 penulis menyelesaikan studi di SMU Negeri I Gunung Talang. Pada tahun yang sama penulis lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB (USMI) pada Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
DAFTAR ISI
Halaman
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... x
PENDAHULUAN ... 1
TINJAUAN PUSTAKA Kafein ... 1
Vitamin B ... 2
Spektrofotometer Ultraviolet ... 3
Rancangan Fraksional Faktorial ... 3
Kalibrasi Multivariat ... 4
Kriteria Kebaikan Model ... 5
BAHAN DAN METODE Bahan dan Alat ... 6
Metode Penelitian ... 6
Penentuan Panjang Gelombang Maksimum ... 6
Kalibrasi Satu Komponen ... 6
Penentuan Kadar Kafein, VitaminB1, B2, dan B6 dalam Contoh Sintetik ... 6
Penentuan Kadar Kafein, VitaminB1, B2, dan B6 dalam Contoh Minuman ... 7
HASIL DAN PEMBAHASAN Penentuan Panjang Gelombang Maksimum ... 7
Kalibrasi Satu Komponen ... 8
Pembentukan Model dengan PCR dan PLS ... 9
Perbandingan Model antara PCR dan PLS ... 11
Penentuan Kadar Kafein, Vitamin B1, B2, dan B6 dalam Contoh Minuman .. 11
Evaluasi Kinerja Analitik ... 12
SIMPULAN DAN SARAN Simpulan ... 13
Saran ... 13
DAFTAR PUSTAKA ... 13
DAFTAR TABEL
Halaman
1 Prediksi komposisi set kalibrasi ... 6
2 Prediksi komposisi set validasi ... 7
3 Koefisien determinasi dan DLD untuk kafein, vitamin B1, B2, dan B6 ... 10
4 Hasil analisis lima komponen utama PCR ... 10
5 Hasil analisis regresi PLS ... 10
6 Nilai PRESS dan R2 kafein, vitamin B1, B2, dan B6 ... 10
7 Perbandingan parameter kebaikan model validasi kafein, vitamin B1, B2, dan B6 ... 11
8 Korelasi nilai Y sebenarnya dan Y prediksi kafein, vitamin B1, B2 dan B6 ... 11
9 Hasil penentuan simultan kafein, vitamin B1, B2, dan B6 dalam contoh minuman dengan selang kepercayaan 95% ... 12
10 Kandungan Extra Joss® Active B7 ... 12
11 Hasil pengukuran kadar kafein, vitamin B2, dan B6 dengan metode HPLC ... 12
12 Hasi uji presisi dan akurasi kafein, vitamin B1, B2, dan B6 dari contoh minuman berenergi ... 12
DAFTAR GAMBAR
Halaman
1 Struktur kafein ... 22 Struktur tiamin ... 2
3 Struktur riboflavin ... 2
4 Struktur piridoksin ... 3
5 Bagan peralatan Spektrofotometer UV/Vis ... 3
6 Komponen utama prediktor X1, X2, dan X3 (Miller & Miller 2000) ... 4
7 Panjang gelombang maksimum kafein dalam pelarut air deionisasi dengan konsentrasi 8.0 ppm pada daerah 200–400 nm ... 7
9 Panjang gelombang maksimum vitamin B2 dalam pelarut air deionisasi dengan
konsentrasi 2.0 ppm pada daerah 200–400 nm ... 8
10 Panjang gelombang maksimum vitamin B6 dalam pelarut air deionisasi dengan konsentrasi 2.0 ppm pada daerah 200–400 nm... 8
11 Hubungan antara konsentrasi kafein dan absorbans ... 8
12 Hubungan antara konsentrasi vitamin B1 dan absorbans ... 9
13 Hubungan antara konsentrasi vitamin B2 dan absorbans ... 9
14 Hubungan antara konsentrasi vitamin B6 dan absorbans ... 9
DAFTAR LAMPIRAN
Halaman
1 Diagram alir penelitian ... 162 Kurva kalibrasi kafein dari konsentrasi 2.0–62.0 ppm ... 17
3 Kurva kalibrasi vitamin B1 dari konsentrasi 0.2–4.8 ppm ... 17
4 Kurva kalibrasi vitamin B2 dari konsentrasi 1.0–36.0 ppm ... 18
5 Kurva kalibrasi vitamin B6 dari konsentrasi 1.0–52.0 ppm ... 18
6 Hasil analisis komponen utama (PC) (pada delapan PC pertama) ... 19
7 Hasil analisis regresi kafein dengan PC 1, PC2, PC3, PC4, dan PC5 ... 19
8 Hasil analisis regresi vitamin B1 dengan PC 1, PC2, PC3, PC4, dan PC5 ... 20
9 Hasil analisis regresi vitamin B2 dengan PC 1, PC2, PC3, PC4, dan PC5 ... 23
10 Hasil analisis regresi vitamin B6 dengan PC 1, PC2, PC3, PC4, dan PC5 ... 25
11 Perhitungan parameter kebaikan RMSEC dan RMSEP pada PCR ... 27
12 Perhitungan parameter kebaikan RMSEC dan RMSEP pada PLS ... 30
13 Analisis simultan kafein, vitamin B1, B2, dan B6 dalam contoh minuman berenergi ... 33
14 Perhitungan kadar kafein, vitamin B1, B2, dan B6 dalam contoh minuman berenergi dengan PCR dan PLS ... 34
15 Perhitungan uji presisi ... 35
PENDAHULUAN
Kafein, vitamin B1, B2, dan B6 adalah senyawa organik yang banyak terdapat di berbagai jenis sediaan obat, makanan, dan minuman. Salah satu contohnya ialah minuman berenergi yang banyak beredar di pasaran. Kafein banyak digunakan sebagai obat sakit kepala, dan sebagai stimulan pembentukan energi dalam minuman berenergi (Nurachman 2004). Pemberian kafein secara berlebihan dapat menyebabkan gelisah, tremor, insomnia, gugup, hipertensi, kejang, dan mual.
Vitamin B berperan penting dalam metabolisme pembentukan energi yang diperlukan sel-sel otak. Kekurangan atau kelebihan vitamin dapat menyebabkan masalah fisiologi yang serius. Pemberian vitamin B1 yang berlebihan dapat mempengaruhi sistem saraf, kelebihan vitamin B2 sejauh ini tidak menimbulkan efek yang berbahaya, tetapi pemberian vitamin B6 secara berlebihan dapat menimbulkan kerusakan saraf pada kaki dan tangan (ODS 2006). Oleh karena itu, kadar kafein, vitamin B1, B2, dan B6 yang ditambahkan dalam minuman berenergi perlu ditentukan agar tidak menimbulkan efek yang merugikan dan sebagai kendali mutu produk.
Analisis kadar kafein dan vitamin B secara terpisah maupun simultan telah banyak dikembangkan. Salah satunya adalah kromatografi cair kinerja tinggi (HPLC) (Siong & Swan-Choo 1996) yang sangat luas penggunaannya, tetapi selalu membutuhkan preparasi contoh, waktu pengerjaan yang lama, serta peralatan dan bahan relatif mahal. Teknik spektrofotometri ultraviolet-visible (UV-Vis) juga telah dioptimalisasi untuk penentuan simultankadar vitaminB1, B6, dan B12 dalam sirup dan tablet dengan spektrofotometri derivatif ultraviolet (SDUV) menggunakan teknik zero-crossing (Ozgur & Koyuncu 2002). Teknik analisis terpisah kafein juga telah banyak berkembang, seperti penentuan kafein dalam kopi, teh dan kola dengan spektrofotometri derivatif (Alpdogan
et al. 2000) dengan hasil yang cukup baik. Safitri (2007) telah mengembangkan metode cepat penentuan simultan kafein, vitamin B2, dan B6 dalam minuman berenergi dengan teknik zero – crossing. Tetapi hasil yang diperoleh belum memuaskan karena teknik ini hanya dapat digunakan untuk pengukuran simultan kafein dan vitamin B6, tapi tidak dapat digunakan untuk pengukuran simultan kafein, vitamin B2, dan B6. Hal ini
disebabkan karena minuman berenergi memiliki matriks yang berbeda-beda, sehingga teknik SDUV yang telah dikembangkan oleh Safitri (2007) tidak bisa langsung diterapkan. Selain itu, semakin banyak derivatisasi spektrum yang dilakukan, nisbah sinyal terhadap derau (noise) akan menurun sehingga akan menurunkan pula ketelitian dan ketepatannya.
Salah satu solusi yang bisa digunakan untuk penentuan simultan beberapa senyawa dalam contoh adalah dengan teknik kalibrasi multivariat yang merupakan bagian dari kemometrik. Kemometrik pada saat ini merupakan alternatif yang sangat cocok untuk prosedur pemisahan dan deteksi dalam analisis senyawa kimia. Analisis kemometrik dengan teknik regresi komponen utama (principle component regression, PCR) dan kuadrat terkecil parsial (partial least square,
PLS), merupakan teknik kalibrasi multivariat yang bisa digunakan untuk penentuan multikomponen. Teknik PCR dan PLS dapat digunakan untuk menghubungkan spektrum absorpsi dengan konsentrasi kafein, vitamin B1, B2, dan B6 dari minuman berenergi. Keuntungan teknik ini ialah dapat mengeliminasi spektrum pengganggu dalam kuantifikasi contoh, meningkatkan selektivitas, dan tidak memerlukan pemisahan atau prakonsentrasi terlebih dahulu (Lopez-de-Alba et al. 2006).
Oleh karena itu, diperlukan penelitian lebih lanjut untuk penentuan simultan kafein, vitamin B1, B2, dan B6 dari minuman berenergi. Penelitian ini mempelajari dan mengembangkan metode analitik dengan kriteria mudah, murah, dan cepat serta memiliki ketelitian dan ketepatan yang baik. Selain itu, penelitian bertujuan menentukan kadar kafein, vitamin B1, B2, dan B6 secara simultan dengan kombinasi spekrum UV dan model kalibrasi multivariat, juga dibandingkan kebaikan model PCR dan PLS dalam menduga kadar kafein, vitamin B1, B2, dan B6, dan evaluasi kinerja analitik melalui penentuan presisi dan akurasi.
TINJAUAN PUSTAKA
Kafein
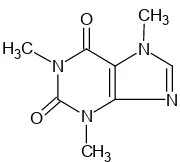
Kafein atau 1,3,7-trimetilxantin merupakan senyawa golongan alkaloid purin (Hesse 2002) dengan rumus molekul C8H10N4O2 (Gambar 1). Senyawa ini
menggumpal, tidak berbau, dan berasa pahit seperti alkaloid pada umumnya. Kafein sukar larut dalam eter, agak sukar larut dalam air dan etanol, serta mudah larut dalam kloroform (Depkes RI 1995).
Kafein dapat menimbulkan perangsangan terhadap susunan saraf pusat (otak), sistem pernapasan, serta sistem pembuluh darah dan jantung. Bahkan senyawa xantin dalam dosis rendah mampu merangsang susunan saraf yang sedang depresi. Lebih jauh, kafein ternyata dapat menetralisasi asam lemak dalam darah. Pada dosis sedang, kafein dapat meningkatkan produksi asam lambung yang berlangsung lama, sehingga memperbesar resiko penyakit lambung, tukak lambung, atau tukak usus halus.
N N N N O CH3 CH3 C H3 O
Gambar 1 Struktur kafein.
Vitamin B
Vitamin B yang esensial bagi nutrisi manusia adalah tiamin (B1), riboflavin (B2), niasin (B3), asam pantotenat (B5), piridoksin (B6), biotin, kobalamin (B12), dan asam folat. Vitamin B larut dalam air, maka kelebihan vitamin B ini akan dieksresikan ke dalam urin dan dengan demikian, jarang tertimbun dalam konsentrasi yang toksik (Murray et al. 1996).
Tiamin (vitamin B1)
Tiamin atau vitamin B1 tersusun dari pirimidin yang dihubungkan oleh jembatan metilena dengan tiazol tersubstitusi (Gambar 2). Tiamin aktif berada dalam bentuk tiamin difosfat (pirofosfat) (Murray et al. 1996). Tiamin adalah senyawa tidak berwarna dengan rumus kimia C12H17N4OS. Senyawa
ini larut dalam air, tetapi tidak larut dalam alkohol dan dapat terdekomposisi jika dipanaskan.
Tiamin terdapat hampir pada semua tanaman dan tubuh hewan yang lazim digunakan sebagai makanan, tetapi kandungan vitamin ini biasanya kecil. Biji-bijian yang tidak digiling sempurna dan daging merupakan sumber tiamin yang baik. Selain itu tiamin juga banyak terdapat pada roti, ginjal, hati, sereal, susu, unggas, makanan laut
(kepiting, ikan, kerang, dan lain-lain), dan telur. N N C H3 N+ S OH CH3 NH2
Gambar 2 Struktur tiamin.
Riboflavin (vitamin B2)
Riboflavin terdiri atas sebuah cincin isoaloksazin heterosiklik yang melekat pada gula alkohol dan ribitol (Gambar 3). Vitamin ini merupakan pigmen berpendar dan berwarna yang relatif stabil terhadap pemanasan, namun akan terurai dengan adanya cahaya (Murray et al. 1996). Senyawa ini memiliki warna kuning atau jingga-kekuningan, sehingga sering digunakan sebagai pewarna makanan.
N N N NH C H3 C H3 OH O O OH OH O H
Gambar 3 Struktur riboflavin.
Vitamin ini berada dalam bentuk aktifnya berupa flavin mononukleotida (FMN) atau flavin adenin dinukleotida (FAD). Seperti halnya vitamin B yang lain, riboflavin juga berperan dalam produksi energi, karena senyawa ini berperan dalam metabolisme lemak, karbohidrat, dan protein. Vitamin B2 juga diperlukan untuk pertumbuhan badan, pembentukan dan respirasi sel darah merah, dan pembentukan antibodi.
Defisiensi vitamin B2 akan menimbulkan berbagai gejala, seperti stomatitis angularis, keilosis, glositis, sebore, dan fotofobia. Sumber alami riboflavin adalah susu, keju, sayuran hijau, hati, ragi, almond, dan kacang-kacangan.
Piridoksin (vitamin B6)
fosfat yang bersesuaian (Gambar 4). Piridoksal fosfat merupakan bentuk utama vitamin B6 yang aktif (Murray et al. 1996). Defisiensi akibat kekurangan vitamin B6 saja jarang terjadi, dan setiap defisiensi biasanya merupakan bagian dari defisiensi umum vitamin B kompleks. Hati, ikan makerel, alpukat, pisang, daging, sayuran, dan telur merupakan sumber vitamin B6 yang baik.
N
OH
CH3 OH
OH
Gambar 4 Struktur piridoksin.
Spektrofotometri Ultraviolet
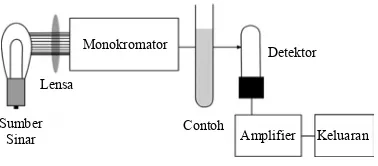
Spektrofotometer sesuai dengan namanya terdiri atas spektrometer dan fotometer (Gambar 5). Spektrometer menghasilkan sinar dari spektrum dengan panjang gelombang tertentu, dan fotometer adalah alat pengukur intensitas cahaya yang yang ditransmisikan atau yang diabsorpsi. Jadi, spektrofotometer digunakan untuk mengukur energi secara relatif jika energi tersebut ditransmisikan, direfleksikan, atau diemisikan sebagai fungsi dari panjang gelombang (Khopkar 1990).
Gambar 5 Bagan peralatan spektrofotometer UV/Vis.
Dasar teknik spektroskopi adalah interaksi antara radiasi elektromagnetik dan bahan yang dianalisis. Analisis dengan spektrofotometri UV didasarkan pada penyerapan energi sinar dengan panjang gelombang tertentu oleh molekul dalam suatu senyawa. Semua molekul dapat menyerap radiasi dalam daerah UV-Vis karena mengandung elektron yang dapat dieksitasikan ke tingkat energi yang lebih tinggi. Besar energi radiasi bergantung pada frekuensi atau panjang gelombang radiasi yang dimiliki.
Hukum Lambert menyatakan bahwa penyerapan sinar tidak bergantung pada intensitas sumber cahaya. Hukum Beer menyatakan bahwa fraksi penyerapan sinar sebanding dengan banyaknya molekul yang menyerap (Sudjadi 1985). Sumber radiasi yang dipancarkan harus memiliki panjang gelombang yang sama untuk penyerapan agar memenuhi hukum Beer.
Cara-cara analisis kuantitatif dengan pengukuran absorbans menggunakan teknik spektrofotometri UV-Vis telah banyak dikembangkan, seperti memakai kurva kalibrasi dari sederet larutan standar, adisi standar, adisi standar titik H, dan teknik derivatif. Kurva kalibrasi menggunakan larutan-larutan standar yang sebaiknya mempunyai komposisi sama dengan komposisi cuplikan yang sebenarnya, dan konsentrasi cuplikan berada di antara konsentrasi-konsentrasi larutan standar (Supriatna 1994).
Metode adisi standar dilakukan dengan menambahkan larutan standar ke dalam larutan cuplikan maupun campuran cuplikan dan standar (Skoog et al. 1998). Metode adisi standar titik H hampir sama dengan adisi standar, yakni juga dilakukan penambahan standar. Hanya saja pengukuran dilakukan pada dua panjang gelombang terpilih, dan konsentrasi contoh bisa langsung diperoleh di titik H tersebut. Sementara itu, dengan teknik derivatif spektrofotometri, spektrum didapat-kan dari plot derivatif pertama atau orde tertinggi absorbans atau transmitans sebagai fungsi panjang gelombang (Skoog et al.
1998).
Rancangan Fraksional Faktorial
Rancangan faktorial merupakan salah satu cara yang digunakan dalam melakukan suatu percobaan untuk melihat efek dari dua faktor atau lebih terhadap hasil yang diperoleh. Dengan menggunakan rancangan faktorial, didefinisikan bahwa setiap percobaan yang dilakukan adalah kombinasi percobaan yang mungkin untuk setiap level dalam faktor yang dicoba (Montgomery 2001).
Untuk percobaan yang memiliki jumlah faktor sedikit, semua kombinasi faktorial desain untuk setiap level dari setiap faktor dapat dilakukan. Namun, untuk percobaan dengan jumlah faktor relatif lebih banyak, jumlah pengamatan yang dilakukan akan sangat besar pula. Jumlah pengamatan yang
Monokromator
Contoh Sumber
Sinar Lensa
sangat besar tersebut dapat dikurangi dengan menggunakan rancangan fraksional faktorial. Sebagai contoh, dalam penelitian ini terdapat empat faktor yang terdiri dari delapan tingkat konsentrasi untuk masing-masing senyawa. Kemudian faktor dan tingkat konsentrasi digunakan sebagai masukan dalam program statistical analysis software
(SAS) 9.1, sehingga terdapat 84 fraksi, yaitu 4096 komposisi. Selanjutnya diperoleh luaran berupa desain percobaan yang telah terfraksionalisasi menjadi 84-2. Luaran ini berupa komposisi 64 campuran set yang terdiri atas 48 komposisi kalibrasi set dan 16 komposisi validasi set.
Kalibrasi Multivariat
Kemometrik adalah seni mengekstraksi informasi kimia dari data yang dihasilkan oleh suatu percobaan kimia (Wold 1995). Kemometrik menyediakan teknik untuk mengurangi data berukuran besar yang diperoleh dari instrumen seperti spektrofotometer (Varmuza 2002). Selanjutnya model ini dapat digunakan untuk menduga contoh yang tidak diketahui.
Kalibrasi multivariat merupakan salah satu bentuk teknik analisis kemometrik yang dapat digunakan untuk menentukan campuran dari beberapa senyawa. Teknik kalibrasi multivariat ini antara lain berupa PCR dan PLS, yang sering digunakan dalam analisis spektrum kuantitatif untuk mendapatkan informasi yang selektif dari data yang tidak selektif (Diaz et al. 1997).
PCR dan PLS memiliki beberapa perbedaan. Pada teknik PCR, hanya informasi dalam matriks X yang digunakan untuk dekomposisi spektrum, sedangkan pada PLS data konsentrasi matriks juga digunakan; jadi bergantung pada X dan Y (Diaz et al. 1997). Pada PCR, dekomposisi spektrum didasarkan pada semua variasi spektrum tanpa memperhatikan konsentrasi contoh.
Teknik-teknik kalibrasi multivariat dengan berbagai kombinasi telah banyak dikembangkan untuk analisis simultan berbagai senyawa dalam campuran, beberapa di antaranya ialah penentuan simultan empat campuran obat farmasi (Cevdet et al. 1998), penentuan piridoksal, piridoksamin, dan asam piridoksat menggunakan fluorimetri dengan variabel spektrum non-linier dan PLS (Berzas
et al. 1998), simultan parasetamol, kafein, dan asam asetilsalisilat dengan spektrofotometri UV dan kombinasi PLS (Medina et al 1999), penentuan Fe, Co, dan Cu dalam medium
misel (Abdollahi et al. 2003), dan penentuan empat senyawa pestisida (Diaz et al. 1997).
Regresi Komponen Utama(PCR)
Ide dari PCR adalah membentuk model antara konsentrasi senyawa dan komponen utama (principle component, PC) pada data matriks (spektrum) (Cevdet et al. 1998). PCR menggunakan regresi untuk mengubah skor dalam konsentrasi (Brereton 2000). Untuk mendapatkan skor yang akan diregresikan dengan konsentrasi dibutuhkan analisis komponen utama (principle component analysis, PCA). PCA merupakan suatu teknik untuk mengurangi jumlah peubah dalam suatu matriks data. Prinsip PCA adalah mencari komponen utama yang merupakan kombinasi linear dari peubah asli (Varmuza 2000).
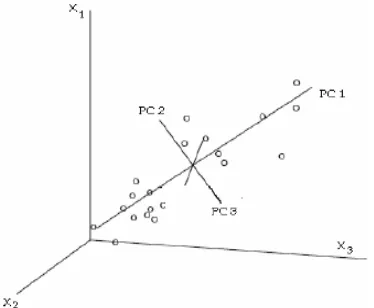
Komponen-komponen utama (PC) tersebut dipilih sedemikian rupa sehingga komponen utama pertama memiliki variasi terbesar dalam set data, sedangkan komponen utama kedua tegak lurus terhadap komponen utama pertama dan memiliki variasi terbesar berikutnya (Miller & Miller 2000). Jika jumlah ragam dari komponen utama satu (PC 1) dan dua (PC 2) lebih besar dari 70%, maka plot skor memperlihatkan visualisasi dua dimensi yang baik (Varmuza 2000). Gambar 6 menggambarkan komponen utama dari peubah X1, X2, dan X3.
Nilai PC yang didapatkan dari PCA kemudian diregresikan secara linear berganda dengan PC sebagai penduga dan konsentrasi sebagai respon. Regresi yang didapat ini menghasilkan matriks koefisien yang apabila dikalikan dengan matriks absorbans menghasilkan matriks konsentrasi.
Gambar 6 Komponen utama prediktor X1,
Kuadrat Terkecil Parsial(PLS)
PLSmerupakan salah satu teknik kalibrasi multivariat yang sangat luas digunakan dalam analisis kuantitatif data spektroskopi dan elektrokimia (Abdollahi et al. 2003). PLS digunakan untuk menduga serangkaian peubah dependen dari peubah independen (penduga) yang jumlahnya sangat banyak, memiliki struktur sistematik linear atau nonlinear, dengan atau tanpa data yang hilang, dan memiliki kolinearitas yang tinggi.
Teknik ini membentuk model dari peubah-peubah yang ada untuk membentuk serangkaian respon dengan menggunakan regresi kuadrat terkecil dalam bentuk matriks (Lindblom 2004). Inti dari PLS adalah untuk menghitung nilai (skor) dari matriks X dan Y
dan untuk membuat model regresi antara nilai-nilai tersebut. Kelebihan dari PLS dibandingkan dengan regresi berganda adalah dalam mengatasi masalah kolinearitas data, peubah penjelas (X) yang banyak, dan juga dapat secara simultan memodelkan beberapa peubah respon (Y) (Wold 1995).
PLS menggambarkan hubungan eksternal dan hubungan internal antara X dan Y. Hubungan eksternal ditulis dengan persamaan berikut:
∑
a h h h=1X= TP'+E = t p' +E (1)
∑
a h h h=1Y = UQ'+F = u q' +F (2)
dengan
X= peubah penjelas
Y= peubah respon
T dan U= vektor skor faktor komponen utama peubah X dan Y
P dan Q= vektor pembobot dari peubah X dan Y
E= matriks sisaan peubah penjelas (X)
F= matriks sisaan peubah respon (Y)
Sedangkan untuk hubungan internal ditulis dengan persamaan berikut:
h h h
u = b t (3)
h h h h h
b =u' t t' t (4)
dengan
h
t dan uh= vektor skor faktor omponen
utama ke-h peubah X dan Y
h
b = koefisien internal
Pendugaan parameter dalam regresi PLS didapatkan melalui model persamaan:
Y = XB + F (5)
dengan
Y= peubah respon
X= peubah penjelas
F= matriks sisaan peubah respon (Y)
B= koefisien regresi PLS
Kriteria Kebaikan Model
Kebaikan suatu model dapat dilihat dari beberapa parameter. Selisih antara nilai aktual dan dugaan dari peubah penjelas (Y) dihitung, dan jumlah kuadrat dari selisih tersebut dikumpulkan untuk mendapatkan nilai
prediction residual error sum of square
(PRESS).
(
)
21
ˆ
n
i i i
PRESS y y
=
=
∑
− (6)dengan:
ŷi = respon dugaan
yi = respon aktual
Selain dari nilai PRESS, kebaikan model juga dilihat dari nilai R2, root mean square error of calibration (RMSEC), dan root mean
square error of prediction (RMSEP). R2
mengindikasikan mutu data antara konsentrasi nyata dan konsentrasi yang diperkirakan. R2
menunjukkan kemampuan suatu metode untuk menghasilkan angka analisis yang proporsi-onal terhadap konsentrasi contoh pada interval konsentrasi tertentu.
RMSEC digunakan untuk menghitung galat dugaan. Dalam model yang memiliki peubah x atau faktor PCR dan PLS yang banyak menyebabkan perbedaan antara RMSEC dan galat dugaan akan menjadi besar (Naes et al. 2002).
RMSEP digunakan untuk data yang dibagi menjadi dua bagian, satu untuk model kalibrasi dan yang lainnya untuk validasi (Naes et al. 2002).
(
)
2 1ˆ
p
N
i i p
i
RMSEP y y N
=
=
∑
− (7)dengan:
ŷi = respon dugaan
yi = respon aktual
Np = jumlah data
menunjukkan nilai ketidaktentuan dalam prosedur perhitungan (Naes et al. 2002).
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah standar kafein diperoleh dari Lab. Kimia Analitik FMIPA IPB, standar vitamin B1, B2, dan B6 diperoleh dari Pusat Studi Biofarmaka LPPM IPB, air deionisasi, dan contoh minuman berenergi Extra Joss® dari PT Bintang Toedjoe yang akan dianalisis.
Alat-alat yang digunakan adalah spektrofotometer UV-Vis Shimadzu 1701 PC dengan perangkat lunak UV Probe versi 2.0, kuvet kuarsa 1 cm, seperangkat komputer, dan alat-alat kaca. Analisis data menggunakan perangkat lunak SAS 9.1 dan Minitab 14.
Metode Penelitian
Penelitian dilakukan dalam beberapa tahap, yaitu penentuan λmaks, penentuan daerah
linear dinamis, pembentukan model kalibrasi dan validasi, penentuan kadar kafein, vitamin B1, B2, dan B6 dalam contoh sintetik dan contoh minuman berenergi, dan evaluasi kinerja metode yang dikembangkan dngan menentukan presisi dan akurasinya (Lampiran 1).
Penentuan Panjang Gelombang Maksimum
Panjang gelombang maksimum (λmaks) tiap
senyawa ditentukan dengan membuat larutan stok 40 ppm untuk masing-masing senyawa. Sebanyak 20 mg kafein, vitamin B1, B2, dan B6 dilarutkan dengan air deionisasi dan ditepatkan dalam labu takar 500 mL. Kemudian sebanyak 10 mL larutan stok kafein, 1 mL larutan stok vitamin B1, dan 5 mL larutan stok vitamin B2 dan B6, diencerkan ke dalam labu takar 50 mL dengan pelarut yang sama. Spektrum absorpsi diukur pada panjang gelombang 200–400 nm dengan interval 0.2 nm dan kecepatan pemayaran medium. λmaks diperoleh dari absorbans
maksimum masing-masing senyawa.
Kalibrasi Satu Komponen
Kalibrasi satu komponen dilakukan dengan membuat variasi konsentrasi tiap senyawa: yaitu 0.10–78.00 ppm untuk kafein, 0.05–6.00
ppm untuk vitamin B1, 0.05–60 ppm untuk vitamin B2, dan 0.05–72.00 ppm untuk vitamin B6. Spektrum absorpsi masing-masing senyawa diukur pada panjang gelombang maksimumnya. Daerah linear dinamis untuk tiap senyawa kemudian ditentukan dengan kurva kalibrasi antara absorbans pada panjang gelombang maksimum dan konsentrasi contoh dengan melihat nilai koefisien korelasi atau koefisien determinansinya.
Penentuan Kadar Kafein, Vitamin B1, B2, dan B6 dalam Contoh Sintetik
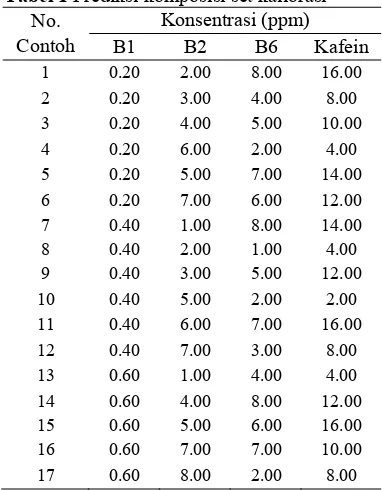
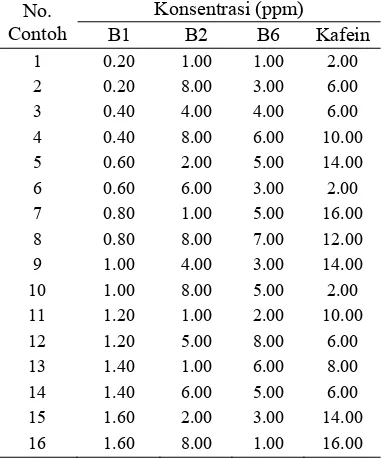
Penentuan kadar kafein, vitamin B1, B2, dan B6 dalam contoh sintetik menggunakan kalibrasi multivariat dilakukan dengan membuat dua set larutan standar. Set kalibrasi mengandung 48 larutan standar (Tabel 1) dan set validasi mengandung 16 larutan standar (Tabel 2).
Konsentrasi tiap senyawa yang berada dalam daerah linear dinamis divariasikan: 2.0–16.0 ppm untuk kafein, 0.2–1.6 ppm untuk vitamin B1, dan 1.0–8.0 ppm untuk vitamin B2 dan B6. Kedua set larutan standar diukur serapannya secara simultan pada panjang gelombang 200–400 nm dengan interval 0.2 nm dan kecepatan pemayaran medium. Data absorbans dari set validasi dan set kalibrasi dikumpulkan dalam 2 matriks yang berbeda. Kemudian konsentrasi dalam set validasi dihitung dengan model kalibrasi multivariat yang diperoleh.
Tabel 1 Prediksi komposisi set kalibrasi No.
Contoh
Konsentrasi (ppm)
B1 B2 B6 Kafein
Lanjutan Tabel 1 Prediksi komposisi set kalibrasi
18 0.60 5.00 1.00 10.00 19 0.80 2.00 4.00 2.00 20 0.80 3.00 8.00 10.00 21 0.80 4.00 1.00 8.00 22 0.80 5.00 3.00 4.00 23 0.80 6.00 6.00 14.00 24 0.80 7.00 2.00 6.00 25 1.00 1.00 7.00 6.00 26 1.00 2.00 2.00 12.00 27 1.00 3.00 6.00 4.00 28 1.00 5.00 1.00 10.00 29 1.00 6.00 8.00 8.00 30 1.00 7.00 4.00 16.00 31 1.20 2.00 7.00 8.00 32 1.20 3.00 3.00 16.00 33 1.20 4.00 6.00 2.00 34 1.20 6.00 1.00 12.00 35 1.20 7.00 5.00 4.00 36 1.20 8.00 4.00 14.00 37 1.40 2.00 3.00 10.00 38 1.40 3.00 7.00 2.00 39 1.40 4.00 2.00 16.00 40 1.40 5.00 4.00 12.00 41 1.40 7.00 1.00 14.00 42 1.40 8.00 8.00 4.00 43 1.60 1.00 3.00 12.00 44 1.60 2.00 6.00 6.00 45 1.60 4.00 7.00 4.00 46 1.60 5.00 5.00 8.00 47 1.60 6.00 4.00 10.00 48 1.60 7.00 8.00 2.00
Tabel 2 Prediksi komposisi set validasi No.
Contoh
Konsentrasi (ppm)
B1 B2 B6 Kafein
1 0.20 1.00 1.00 2.00 2 0.20 8.00 3.00 6.00 3 0.40 4.00 4.00 6.00 4 0.40 8.00 6.00 10.00 5 0.60 2.00 5.00 14.00 6 0.60 6.00 3.00 2.00 7 0.80 1.00 5.00 16.00 8 0.80 8.00 7.00 12.00 9 1.00 4.00 3.00 14.00 10 1.00 8.00 5.00 2.00 11 1.20 1.00 2.00 10.00 12 1.20 5.00 8.00 6.00 13 1.40 1.00 6.00 8.00 14 1.40 6.00 5.00 6.00 15 1.60 2.00 3.00 14.00 16 1.60 8.00 1.00 16.00
Penentuan Kadar Kafein, Vitamin B1, B2, dan B6 dalam Contoh Minuman Berenergi
Contoh minuman berenergi yang akan diukur secara simultan kadar kafein, vitamin B1, B2, dan B6-nya, ditimbang sebanyak 4.0 g. Kemudian contoh dilarutkan dengan air deionisasi dan ditepatkan dalam labu takar 50 mL. Selanjutnya sebanyak 0.625 mL larutan contoh diencerkan ke dalam labu takar 50 mL.
Spektrum contoh diukur dari panjang gelombang 200 sampai 400 nm dengan interval 0.2 nm dan kecepatan pemayaran medium. Data absorbans yang diperoleh kemudian dimasukkan ke dalam persamaan regresi multivariat yang telah didapat dari set kalibrasi untuk mendapatkan konsentrasi contoh dan evaluasi model yang diajukan dari set validasi.
HASIL DAN PEMBAHASAN
Penentuan Panjang Gelombang Maksimum
Panjang gelombang maksimum yang diperoleh dari hasil pengukuran larutan standar kafein, vitamin B1, B2, dan B6 dengan pelarut air deionisasi menggunakan spektrofotometer UV-Vis secara berurutan adalah 272.9, 234.2, 267.0, dan 222.2 nm. Spektrum absorpsi yang diperoleh ditunjukkan berturut-turut pada Gambar 7–10.
Gambar 7 Panjang gelombang maksimum
kafein dalam pelarut air deionisasi dengan konsentrasi 8.0 ppm pada daerah 200–400 nm.
Gambar 8 Panjang gelombang maksimum vitamin B1 dalam pelarut air deionisasi dengan konsentrasi 1.0 ppm pada daerah 200–400 nm.
Gambar 9 Panjang gelombang maksimum
vitamin B2 dalam pelarut air deionisasi dengan konsentrasi 2.0 ppm pada daerah 200–400 nm.
Gambar 10 Panjang gelombang maksimum vitamin B6 dalam pelarut air deionisasi dengan konsentrasi 2.0 ppm pada daerah 200–400 nm.
Kalibrasi Satu Komponen
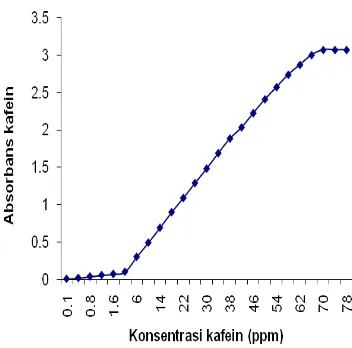
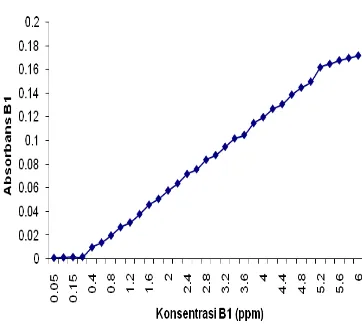
Kalibrasi satu komponen dilakukan untuk memperoleh daerah konsentrasi linear yang dinamis untuk tiap senyawa di panjang gelombang maksimumnya. Gambar 11–14 berturut-turut merupakan kurva yang menunjukkan daerah linear dinamis (DLD) dalam hubungan antara konsentrasi kafein, vitamin B1, B2, dan B6 dan absorbans.
Gambar 11 Hubungan antara konsentrasi
kafein dan absorbans. 234,2 nm
267 nm
Gambar 12 Hubungan antara konsentrasi vitamin B1 dan absorbans.
Gambar 13 Hubungan antara konsentrasi
vitamin B2 dan absorbans.
Gambar 14 Hubungan antara konsentrasi vitamin B6 dan absorbans.
Gambar 11 sampai dengan Gambar 14 juga menunjukkan daerah-daerah saat konsentrasi kafein, vitamin B1, B2, dan B6 tidak lagi memiliki hubungan linear dengan
absorbans. Ketidaklinearan ini disebabkan adanya penyimpangan hukum Lambert-Beer yang disebabkan oleh konsentrasi contoh yang terlalu pekat atau terlalu encer. Konsentrasi yang dipilih adalah yang berada dalam DLD dan memberikan kelinearan yang tinggi (Hwang & Nettleton 2002). Kurva kalibrasi masing-masing senyawa terlampir pada Lampiran 2–5. Konsentrasi yang menunjukkan DLD dan daerah tidak linear ditampilkan pada Tabel 3.
Tabel 3 Koefisien determinasi dan DLD
untuk kafein, vitamin B1, B2, dan B6
Analat R2 DLD (ppm)
Daerah tidak linear (ppm)
Kafein 0.9984 2.0–62.0 0.10–1.60 dan di atas 62.00
Vit. B1 0.9994 0.2–4.8 0.05–0.15 dan di atas 48.00
Vit. B2 0.9992 1.0–36.0 0.05–0.70 dan di atas 36.00
Vit. B6 0.9972 1.0–52.0 0.05–0.70 dan di atas 52.00
Nilai konsentrasi yang termasuk ke dalam DLD digunakan untuk menentukan konsentrasi dalam set kalibrasi dan set validasi contoh sintetik kafein, vitamin B1, B2, dan B6. Pembentukan set kalibrasi dan set validasi terdiri dari delapan tingkat konsentrasi. Delapan tingkat konsentrasi tersebut adalah 2.0–16.0 ppm untuk kafein dengan interval 2 ppm, 0.2–1.6 ppm untuk vitamin B1 dengan interval 0.2 ppm, serta 1.0–6.0 ppm untuk vitamin B2 dan B6 dengan interval 1 ppm.
Pembentukan Model dengan PCR dan PLS
Pemodelan dengan PCR
Model PCR diawali dengan PCA yang menghasilkan nilai loading PC sebanyak jumlah peubah yang dipakai, yaitu 1001 panjang gelombang yang digunakan. Hasil PC yang diperoleh tidak semuanya digunakan, karena tiap PC memberikan proporsi yang berbeda dari seluruh data. Hasil analisis PC ditunjukkan pada Lampiran 6. Nilai PC yang diambil lima, yang cukup mewakili keseluruhan data yang ada. Proporsi dan kumulatif dari kelima PC terdapat pada Tabel 4.
Tabel 4 Hasil analisis lima komponen
utama PCR
PC Nilai
Eigen Proporsi Kumulatif
PC1 2.3181 0.8940 0.8940 PC2 0.1744 0.0670 0.9610 PC3 0.0951 0.0370 0.9980 PC4 0.0038 0.0010 0.9990 PC5 0.0006 0.0000 1.0000
Langkah berikutnya, PC 1, 2, 3, 4, dan 5 diregresikan secara linear berganda dengan konsentrasi kafein, vitamin B1, B2, dan B6 sebagai respon, dan skor PC sebagai penduga, sehingga diperoleh persamaan regresi komponen utama. Persamaan regresi untuk kafein, vitamin B1, B2, dan B6 adalah sebagai berikut:
[kafein] = 0.575 – 2.760 PC1 + 3.830 PC2 – 1.700 PC3 + 4.670 PC4 + 5.440 PC5.
[Vit. B1] = 0.816 + 0.014 PC1– 0.120 PC2 + 0.064 PC3 – 5.710 PC4 – 8.040 PC5.
[Vit. B2] = – 0.116 – 0.466 PC1– 4.250 PC2 – 2.860 PC3 + 2.620 PC4 + 3.330 PC5.
[Vit. B6] = 0.240 – 0.305 PC1– 1.480 PC2 + 7.210 PC3 + 4.270 PC4 – 0.790 PC5.
Sementara hasil analisis lengkap regresi kafein, vitamin B1, B2, dan B6 dengan kelima PC dapat dilihat pada Lampiran 7 – 10.
Pemodelan terhadap PC tersebut dikembalikan lagi ke dalam bentuk absorbans dengan mengalikan koefisien hasil regresi dengan nilai loading pada masing-masing PC sehingga diperoleh persamaan regresi dalam bentuk absorbans. Persamaan regresi tersebut selanjutnya digunakan untuk menduga kadar kafein, vitamin B1, B2, dan B6 dari data set validasi.
Pemodelan dengan PLS
Model PLS juga diawali dengan pembentukan PC. Kemudian dilakukan validasi silang untuk menentukan banyaknya
komponen yang akan digunakan dalam model regresi PLS. Berdasarkan nilai rataan akar PRESS didapatkan nilai minimum sebesar 0.3324 untuk set kalibrasi dan banyaknya komponen yang akan digunakan dalam model, yaitu 5 komponen.
Pemodelan regresi PLS pada tahap selanjutnya dengan menggunakan 5 komponen mampu menjelaskan persentase keragaman peubah penjelas (X) sebesar 99.90% dan 92.22% untuk peubah respon (Y). Hasil analisis PC secara keseluruhan untuk kafein, vitamin B1, B2, dan B6 dengan PLS terdapat pada Tabel 6.
Tabel 5 Hasil analisis regresi PLS
Peubah Kafein Vit. B1
Vit. B2
Vit. B6 Ragam X 99.91 99.90 99.91 99.87 Ragam Y 99.83 72.19 99.78 99.59
n PC 5 5 5 5
Pengolahan dengan PLS juga memberikan konsentrasi dugaan untuk masing-masing senyawa. Konsentrasi dugaan yang didapatkan dari hasil pemodelan 48 set kalibrasi, selanjutnya digunakan untuk menduga kadar kafein, vitamin B1, B2, dan B6 dari 16 campuran set validasi.
Perbandingan Model Antara PCR dan PLS
Ukuran kebaikan model dilihat dari nilai PRESS dan R2. Sedangkan kebaikan validasi model dilihat dari nilai korelasi (r), RMSEP, dan RMSEC dari model tersebut. Hasil R2dan PRESS kafein, vitamin B1, B2, dan B6 ditunjukkan pada Tabel 6, sedangkan parameter kebaikan RMSEC dan RMSEP ditunjukkan pada Tabel 7. Perhitungan kedua parameter kebaikan ini terlampir pada Lampiran 11 untuk PCR dan Lampiran 12 untuk PLS.
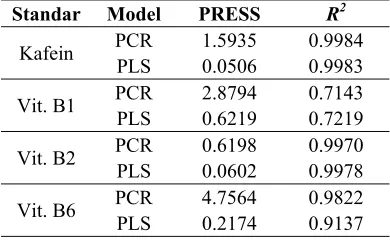
Tabel 6 Nilai PRESS dan R2 kafein, vitamin B1, B2, dan B6
Standar Model PRESS R2
Kafein PCR 1.5935 0.9984 PLS 0.0506 0.9983
Vit. B1 PCR 2.8794 0.7143 PLS 0.6219 0.7219
Vit. B2 PCR 0.6198 0.9970 PLS 0.0602 0.9978
Berdasarkan Tabel 6, nilai PRESS PCR lebih besar dibandingkan dengan PLS, sedangkan nilai R2 kedua model menunjukkan hasil yang cukup baik untuk semua senyawa, kecuali pada vitamin B1. Hal ini disebabkan karena konsentrasi yang digunakan untuk vitamin B1 terlalu rendah (encer) yang dapat memengaruhi serapan saat pengukuran. Besarnya nilai PRESS pada PCR disebabkan karena jumlah galat sisaan dari dugaan pada PCR lebih besar dibandingkan PLS.
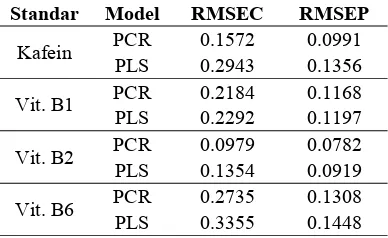
Tabel 7Perbandingan parameter kebaikan
validasi model kafein, vitamin B1, B2, dan B6.
Standar Model RMSEC RMSEP
Kafein PCR 0.1572 0.0991 PLS 0.2943 0.1356
Vit. B1 PCR 0.2184 0.1168 PLS 0.2292 0.1197
Vit. B2 PCR 0.0979 0.0782 PLS 0.1354 0.0919
Vit. B6 PCR 0.2735 0.1308 PLS 0.3355 0.1448
Berdasarkan kriteria kebaikan model di atas, pemilihan model terbaik difokuskan kepada nilai RMSEC dan RMSEP karena keduanya digunakan untuk validasi model. Model yang lebih baik ditunjukkan oleh PCR, karena nilai RMSEC dan RMSEP yang diperoleh pada tiap senyawa lebih kecil dibandingkan dengan PLS.
Nilai RMSEC dan RMSEP yang dihasilkan sangat baik, karena mendekati nol. Evaluasi RMSEP pada kedua model memberikan nilai yang lebih kecil daripada RMSEC sehingga model yang diperoleh sangat baik. Naes et al. (2002) menyatakan bahwa model dugaan yang baik memiliki nilai RMSEP yang rendah dan dapat mengimbangi nilai RMSEC, dan nilai korelasi antara Y
dugaan dengan Y sebenarnya yang tinggi, mendekati 1 (Tabel 8).
Tabel 8 Korelasi nilai Y sebenarnya dengan Y
dugaan untuk kafein, vitamin B1, B2, dan B6
Nilai
korelasi PCR PLS
Kaf vs Kaf^ 0.9990 0.9980
B1 vs B1^ 0.8790 0.8660
B2 vs B2^ 0.9990 0.9980
B6 vs B6^ 0.9930 0.9900 ^ : dugaan
Nilai korelasi menggambarkan hubungan yang proporsional antara dua peubah. Semakin mendekati 1 berarti hubungan antara dua peubah (konsentrasi sebenarnya dengan konsentrasi dugaan) semakin linear. Berdasarkan Tabel 8 terlihat bahwa nilai korelasi ke dua model menunjukkan hubungan yang positif (mendekati 1). Nilai korelasi PCR lebih besar dibandingkan dengan PLS walaupun perbedaan ke dua nilai tersebut tidak signifikan.
Penentuan Kadar Kafein, Vitamin B1, B2, dan B6 dalam Contoh Minuman Berenergi
Kadar kafein, vitamin B1, B2, dan B6 dalam contoh minuman ditunjukkan pada Tabel 9. Spektrum contoh minuman dan contoh perhitungan terlampir pada Lampiran 13 dan 14 . Kadar yang diperoleh PCR tidak jauh berbeda dengan nilai yang tertera pada label minuman (Tabel 10) dan hasil analisis PT Bintang Toedjoe (Tabel 11).
PCR mampu menduga tiga konsentrasi (kafein, vitamin B2, dan B6) dengan baik dibandingkan PLS yang hanya mampu menduga dua konsentrasi saja (Vitamin B1 dan B2). Hal ini dikarenakan kemampuan dari metode PCR dalam mereduksi pengganggu seperti vitamin-vitamin, ion-ion, dan gula yang ada dalam contoh minuman. Selain itu, menurut Chin (2002) untuk penggunaan PLS ukuran contoh tidaklah harus berukuran besar, sedangkan dalam penelitian ini ukuran contoh yang digunakan cukup besar (48 pengamatan dan 1001 peubah untuk masing-masing pengamatan), sehingga menyebabkan pendugaan PLS menjadi kurang baik.
Tabel 10 Kandungan Extra Joss® Active B7 Setiap sachet (4 g) mengandung:
Komponen Jumlah (mg)
Taurin 1000 Ginseng 20 Vitamin B1 1.2
Vitamin B2 5.2 Vitamin B3 20 Vitamin B5 5 Vitamin B6 5 Vitamin B12 1
Inositol 50 Kafein 50 Royal Jelly #
Aspartam # Acesulfame-K # Na-bikarbonat # Asam sitrat #
Pemberi rasa # # Tidak dipublikasikan perusahaan
Tabel 11 Hasil pengukuran kadar kafein, vitamin B2 dan B6 dengan metode HPLC
Contoh Kadar (mg/4 gram)
Kafein 50.1884
Vitamin B2 5.0240 Vitamin B6 4.8881
(Safitri 2007)
Evaluasi Kinerja Analitik
Evaluasi parameter analitik dilakukan untuk melihat ketelitian dan keakuratan metode yang digunakan. Parameter yang dievaluasi hanya presisi dan akurasi saja. Tabel 12 menunjukkan hasil uji presisi dan akurasi yang dilakukan. Perhitungan lengkap untuk uji presisi dan akurasi terlampir pada Lampiran 15 dan 16. Berdasarkan Tabel 12, PCR menunjukkan nilai %SBR dan persentase perolehan kembali yang lebih baik dibandingkan PLS.
Tabel 12 Hasi uji presisi dan akurasi kafein, vitamin B1, B2, dan B6 dari contoh minuman berenergi
Standar %SBR Recovery (%) PCR PLS PCR PLS Kafein 4.00 1.23 100.09 96.56 Vit. B1 2.18 5.24 126.00 125.89 Vit. B2 6.93 15.73 100.97 101.36 Vit. B6 4.96 3.53 100.09 137.45
Uji presisi yang dilakukan adalah keterulangan. Suatu metode dikatakan memiliki nilai presisi yang baik atau ketelitian yang tinggi jika hasil analisis dari serangkaian ulangan memiliki nilai yang tidak jauh berbeda. Nilai presisi ditentukan dari nilai persen simpangan baku relatif (%SBR) enam kali pengukuran.
Berdasarkan kriteria %SBR standar AOAC (1993), dapat diketahui bahwa pengukuran kafein mempunyai kriteria ketelitian yang sedang untuk PCR dan teliti untuk PLS, vitamin B1 mempunyai kriteria ketelitian sedang untuk PCR dan tidak teliti untuk PLS, vitamin B2 memiliki kriteria tidak teliti baik untuk PCR dan PLS, sedangkan vitamin B6 memiliki kriteria ketelitian sedang untuk PCR dan PLS.
Ketidaktelitian yang diperoleh dapat disebabkan oleh sifat dari masing-masing senyawa. Vitamin B1 akan terdekomposisi jika terkena panas, vitamin B6 mudah terdekomposisi oleh basa dan cahaya dalam pH netral dan basa. Vitamin B2 sangat tidak stabil dalam bentuk larutannya. Penentuan spektrum serapan UV untuk vitamin B2 hanya cocok untuk larutan riboflavin murni (Andarwulan & Koswara 1992). Selain itu, vitamin B2 sangat peka terhadap cahaya, sehingga selama pengukuran vitamin B2 dapat terdestruksi sebagian dan kerusakan senyawa ini sebelum pengukuran dimulai dapat memperbesar penyimpangan hasil pengukuran.
Contoh PCR PLS
Batas bawah Bobot (mg) Batas atas Batas bawah Bobot (mg) Batas bawah Kafein 49.9056 50.0452 50.1848 47.7450 48.2799 48.8148 Vit. B1 1.3238 1.5120 1.7002 1.0080 1.5105 2.0130 Vit. B2 5.1656 5.2502 5.3348 4.8299 5.2705 5.7110 Vit. B6 4.7681 5.0045 5.2409 6.3200 6.8727 7.4254
Nilai akurasi dari metode ditunjukkan dengan persentase perolehan kembali
(%recovery). Nilai %recovery yang
diharapkan berdasarkan AOAC (1993) adalah 80–110%. Berdasarkan hasil yang diperoleh, %recovery untuk kafein, vitamin B2, dan B6 yang ditunjukkan PCR lebih besar dari 100%, dan masih berada dalam standar AOAC kecuali untuk vitamin B1. Dengan PLS nilai yang memenuhi standar AOAC hanya untuk kafein dan vitamin B2 saja (lebih besar dari 96%), sedangkan untuk vitamin B1 dan B6 tidak memenuhi standar.
SIMPULAN DAN SARAN
Simpulan
Kombinasi spektrum UV dan model kalibrasi multivariat dapat digunakan untuk menentukan kadar kafein, vitamin B1, B2, dan B6 secara simultan. Model kalibrasi terbaik diberikan oleh PCR, yang ditentukan berdasarkan nilai parameter validasi RMSEC dan RMSEP. Hasil yang diperoleh untuk kafein, vitamin B1, B2, dan B6 menunjukkan nilai RMSEC secara berturut-turut sebesar 0.1572, 0.2184, 0.0979, dan 0.2735. Sedangkan nilai RMSEP sebesar 0.0991, 0.1168, 0.0782, dan 0.1308.
Kadar kafein vitamin B1, B2, dan B6 yang diperoleh dari contoh minuman berenergi dengan PCR adalah 50.0452, 1.5120, 5.2502, dan 5.0045 mg. Sedangkan dengan PLS diperoleh kadar sebesar 48.2799, 1.5105, 5.2705, dan 6.8727mg. Kadar yang diperoleh masih berada dalam selang kepercayaan, dengan interval selang kepercayaan yang lebih sempit diberikan oleh PCR.
Berdasarkan evaluasi kinerja analitik pada contoh minuman berenergi, model terbaik juga diberikan oleh PCR karena diperoleh hasil presisi dan akurasi yang lebih baik dibandingkan PLS.
Saran
Disarankan untuk penggunaan pelarut selain air deionisasi yang dapat menstabilkan vitamin. Selain itu, disarankan adanya optimalisasi terhadap pemilihan panjang gelombang, derivatisasi dan smoothing
terhadap spektrum absorpsi yang didapat, dan evaluasi menyeluruh terhadap parameter analitik dari metode spektrum UV agar diperoleh hasil yang lebih baik.
DAFTAR PUSTAKA
Abdollahi H, Shariat P, Mohammad RK. 2003. Simultaneous spectrophotometric determination of iron, cobalt, and copper by partial least square calibration method in micellar medium. I J P R:207-212.
Alpdogan G, Karabina K, Sungur S. 2002.
Derivative spectrophotometric determination of caffeine in some
beverages. Turk J Chem 26:295-302.
Andarwulan N, Koswara S. 1992. Kimia Vitamin. Jakarta: Rajawali.
[AOAC]. Assosiation Official of Anlytical Chemistry. 1993. Official Methods of Analysis of AOAC International.
Maryland: AOAC International.
Berzas JJ, Murillo JA, Amador-Hernandez J, Gomez MA. 1998. Simultaneous fluorometric determination of pyridoxal, pyridoxamine, and pyridoxic acid by partial least squares using non-linear variable angle synchronous spectra.
Analyst 123:483-488.
Brereton RG. 2000. Introduction to multivariate calibration in analytical chemistry. Analyst 126:2125-2154.
Cevdet D, Demir C, Brereton RG. 1998. Multivariate calibration on designed mixture of four pharmaceutical. Analyst
123:181-189.
Chin WW. 2000. Partial least square for researcher: An overview and presentation of recent advances using PLS approach. University of Houston.
[Depkes RI]. 1995. Farmakope Indonesia. Ed ke-4. Jakarta: Depkes RI
Diaz TG, Guiberteau, Burguillos JMO, Salinas F. 1997. Comparison of chemometric method: derivative ratio spectra and multivariate method (CLS, PCR, and PLS) for the resolution of ternary mixture of pesticides carbofuran carbanyl and phenamifos after their extraction into chloroform. Analyst
Hesse M. 2002. Alkaloids: Nature’s Curse or
Blessing. Zurich: Verlag Helvetica
Chimica Acta.
Hwang JTG, Nettleton D. 2002. Principal components regression with data-chosen components and related Methods.
Analyst 53:899-926.
Khopkar SM. 1990. Konsep Dasar Kimia Analitik. Saptorahardjo A, penerjemah. Jakarta: UI-Pr. Terjemahan dari: Basic Concepts of Analytical Chemistry.
Lindblom T. 2004. Reaction in the system nitro-cellulose/diphenylamine with special reference to the formation of a stabilizing product bonded to nitro-cellulose.
http://www.urn.kb.se/resolve?urn=urn:n bn:se:uu:diva-3989. [30 Sep 2006].
Lopez-de-Alba P, et al. 2006. Simultaneous determination and classification of riboflavin, thiamine, nicotinamide and pyridoxine in pharmaceutical formulations, by UV-visible spectrophotometry and multivariate analysis. J Braz Chem Soc 17:715-722.
Medina AR, Fernandez de Cordova ML, Molina-Diaz A. 1999. Simultaneous determination of paracetamol, caffeine and acetylsalicylic acid by means of FI ultraviolet pls multiphotosensing device.
J Pharm Biomed Anal 21:983-992.
Miller JM, Miller JN. 2000. Statistics and Chemometrics for Analytical Chemistry. Ed ke-4. London: Prentice Hall.
Montgomery DC. 2001. Design and Analysis
of Experimental. Ed ke-5. New York:
Wiley.
Murray RK, Granner DK, Mayes PA, Rodwell VW. 1996. Biokimia Harper. Ed ke-24. Hartono A, penerjemah. Jakarta: Penerbit Buku Kedokteran EGC. Terjemahan dari: Harpers Biochemistry.
Naes T, Isaksson T, Fearn T, Davies T. 2002.
A User-Friendly Guide to Multivariate
Calibration and Classification.
Chichester: NIR Publication.
Nurachman Z. 2004. Minuman Berenergi.
[terhubung berkala].
http:///www.kompas.co.id. [22 Mar 2006]
[ODS] Office of Dietary Supplements. Dietary Supplement Fact Sheet: Vitamin B6. [terhubung berkala]. http:///www.ods.od.nih.gov/factsheets/vit
aminb6. [12 Apr 2006]
Ozgur MU, Koyuncu I. 2002. Determination of ternary mixtures of vitamins (B1, B6, B12) by zero-crossing derivative spectrophotometry. Turk J Chem 26:385-391.
Paradkar MM, Irudayarad J. 2002. Rapid determination of caffeine content in soft drink using FTIR-ATR. Food Chem
78:261-266.
Safitri M. 2007. Metode cepat penentuan simultan kadar kafein, vitamin B2, dan B6 dalam minuman berenergi dengan teknik zero-crossing [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Siong TE, Swan-Choo K. 1996. Simultaneous determination of B-vitamins and ascorbic acid in multi-vitamin preparations by reversed-phase HPLC.
Mal J Nutr 2:176-194.
Skoog DA, Holler FJ, Nieman TA. 1998.
Principle of Instrumental Analysis. Ed ke-5. Philadelphia: Saunders College.
Sudjadi. 1985. Penentuan Struktur Senyawa Organik. Jakarta: Ghalia Indonesia.
Supriatna A. 1994. Kimia Analitik Instrumental. Ed ke-1. Semarang: IKIP Semarang.
Varmuza K. 2002. Applied Chemometrics: From Chemical Data to Relevant Information. 1st Converce on Chemistry. Kairo, Mesir.
Wold S. 1995. Chemometrics; What Do We Want from It?. Chemom Intel Lab Syst
Lampiran 1 Diagram alir penelitian
Penentuan panjang gelombang maksimum
Kalibrasi 1 komponen
Kalibrasi set dan validasi set
Spektrum absorpsi UV pada panjang gelombang
200–400 nm
PCR dan PLS
Sampel minuman berenergi
Spektrum absorpsi UV pada panjang gelombang
200–400 nm Contoh sintetik
R2, PRESS,
Lampiran 2 Kurva kalibrasi kafein dari konsentrasi 2.0 sampai 62.0 ppm.
Lampiran 4 Kurva kalibrasi vitamin B2 dari konsentrasi 1.0 sampai 36.0 ppm
Lampiran 6 Hasil analisis komponen utama (PC) (pada delapan PC pertama)
Principal Component Analysis: 200.0, 200.2, 200.4, 200.6, 200.8, 201.0, 201.2, 201.4
Eigen analysis of the Covariance Matrix
Eigenvalue 2.3181 0.1744 0.0951 0.0038 0.0006 0.0005 0.0002 0.0001 Proportion 0.894 0.067 0.037 0.001 0.000 0.000 0.000 0.000 Cumulative 0.894 0.961 0.998 0.999 1.000 1.000 1.000 1.000
Lampiran 7 Hasil analisis regresi kafein dengan PC1, PC2, PC3, PC4, dan PC5
Regression Analysis: [Kafein] versus PC1, PC2, PC3, PC4, PC5
The regression equation is
[Kafein] = 0.575 - 2.76 PC1 + 3.83 PC2 - 1.70 PC3 + 4.67 PC4 + 5.44 PC5
Predictor Coef SE Coef T P Constant 0.57483 0.09001 6.39 0.000 PC1 -2.75782 0.01610 -171.24 0.000 PC2 3.83086 0.05871 65.25 0.000 PC3 -1.69653 0.07952 -21.33 0.000 PC4 4.6659 0.3999 11.67 0.000 PC5 5.4447 0.9866 5.52 0.000
S = 0.168101 R-Sq = 99.9% R-Sq(adj) = 99.9% PRESS = 1.59354 R-Sq(pred) = 99.84%
Analysis of Variance
Source DF SS MS F P Regression 5 966.48 193.30 6840.43 0.000 Residual Error 42 1.19 0.03
Total 47 967.67
Source DF Seq SS PC1 1 828.61 PC2 1 120.30 PC3 1 12.86 PC4 1 3.85 PC5 1 0.86
Lampiran 8 Hasil analisis regresi vitamin B1 dengan PC1, PC2, PC3, PC4, dan PC5
Regression Analysis: [B1] versus PC1, PC2, PC3, PC4, PC5
The regression equation is
[B1] = 0.816 + 0.0144 PC1 - 0.120 PC2 + 0.064 PC3 - 5.71 PC4 - 8.04 PC5
Predictor Coef SE Coef T P Constant 0.8156 0.1250 6.53 0.000 PC1 0.01444 0.02237 0.65 0.522 PC2 -0.11951 0.08154 -1.47 0.150 PC3 0.0639 0.1104 0.58 0.566 PC4 -5.7067 0.5553 -10.28 0.000 PC5 -8.043 1.370 -5.87 0.000
S = 0.233443 R-Sq = 77.3% R-Sq(adj) = 74.6% PRESS = 2.87943 R-Sq(pred) = 71.43%
Analysis of Variance
Source DF SS MS F P Regression 5 7.7912 1.5582 28.59 0.000 Residual Error 42 2.2888 0.0545
Total 47 10.0800
Source DF Seq SS PC1 1 0.0227 PC2 1 0.1171 PC3 1 0.0183 PC4 1 5.7550 PC5 1 1.8781
Lampiran 9 Hasil analisis regresi vitamin B2 dengan PC1, PC2, PC3, PC4, dan PC5
Regression Analysis: [B2] versus PC1, PC2, PC3, PC4, PC5
The regression equation is
[B2] = - 0.116 - 0.466 PC1 - 4.25 PC2 - 2.86 PC3 + 2.62 PC4 - 3.33 PC5
Predictor Coef SE Coef T P Constant -0.11650 0.05604 -2.08 0.044 PC1 -0.46590 0.01003 -46.46 0.000 PC2 -4.24678 0.03656 -116.17 0.000 PC3 -2.85862 0.04951 -57.74 0.000 PC4 2.6228 0.2490 10.53 0.000 PC5 -3.3350 0.6142 -5.43 0.000
S = 0.104661 R-Sq = 99.8% R-Sq(adj) = 99.8% PRESS = 0.619835 R-Sq(pred) = 99.70%
Analysis of Variance
Source DF SS MS F P Regression 5 209.540 41.908 3825.87 0.000 Residual Error 42 0.460 0.011
Total 47 210.000
Source DF Seq SS PC1 1 23.649 PC2 1 147.836 PC3 1 36.516 PC4 1 1.216 PC5 1 0.323
Lampiran 10 Hasil analisis regresi vitamin B6 dengan PC1, PC2, PC3, PC4, dan PC5
Regression Analysis: [B6] versus PC1, PC2, PC3, PC4, PC5
The regression equation is
[B6] = 0.240 - 0.305 PC1 - 1.48 PC2 + 7.21 PC3 + 4.27 PC4 - 0.79 PC5
Predictor Coef SE Coef T P Constant 0.2399 0.1566 1.53 0.133 PC1 -0.30455 0.02802 -10.87 0.000 PC2 -1.4810 0.1021 -14.50 0.000 PC3 7.2105 0.1383 52.12 0.000 PC4 4.2710 0.6956 6.14 0.000 PC5 -0.794 1.716 -0.46 0.646
S = 0.292433 R-Sq = 98.7% R-Sq(adj) = 98.5% PRESS = 4.75637 R-Sq(pred) = 98.22%
Analysis of Variance
Source DF SS MS F P Regression 5 263.658 52.732 616.62 0.000 Residual Error 42 3.592 0.086
Total 47 267.250
Source DF Seq SS PC1 1 10.105 PC2 1 17.980 PC3 1 232.331 PC4 1 3.224 PC5 1 0.018
Lampiran 11 Perhitungan parameter kebaikan RMSEC dan RMSEP pada PCR
No set
[kafein] (mg/l)
[B1] (mg/l)
[B2] (mg/l)
[B6] (mg/l)
[kafein] dugaan
(mg/l)
[B1] dugaan
(mg/l)
[B2] dugaan
(mg/l)
[B6] dugaan
Lanjutan Lampiran 11 Perhitungan parameter kebaikan RMSEC dan RMSEP pada PCR
V1 2.0 0.2 1.0 1.0 2.2573 0.6355 1.2042 1.3976 V2 6.0 0.2 8.0 3.0 6.2025 0.1881 9.3714 3.3189 V3 6.0 0.4 4.0 4.0 6.0697 0.7283 4.9227 4.4894 V4 10.0 0.4 8.0 6.0 10.1396 0.6219 9.4834 6.6026 V5 14.0 0.6 2.0 5.0 14.0844 0.6428 2.8339 5.4422 V6 2.0 0.6 6.0 3.0 1.6451 1.0163 7.2845 3.6718 V7 16.0 0.8 1.0 5.0 16.4977 1.1581 1.3999 5.6035 V8 12.0 0.8 8.0 7.0 12.2859 1.6165 9.5044 8.0393 V9 14.0 1.0 4.0 3.0 14.1347 1.2615 4.9922 3.5751 V10 2.0 1.0 8.0 5.0 1.2561 1.1448 7.7688 8.6014 V11 10.0 1.2 1.0 2.0 10.2831 0.9369 1.4814 2.1296 V12 6.0 1.2 5.0 8.0 6.0626 1.0404 6.1569 8.5331 V13 8.0 1.4 1.0 6.0 8.0901 1.8546 1.6739 7.1568 V14 6.0 1.4 6.0 5.0 5.8621 0.9196 7.4834 5.2053 V15 14.0 1.6 2.0 3.0 14.462 1.0699 2.8785 3.0545 V16 16.0 1.6 8.0 1.0 16.6446 1.0605 9.5021 1.1868
Perhitungan galat (ê) kafein, vitamin B1, B2, dan B6 PCR
No set ê kafein ê B1 ê B2 ê B6
Lanjutan Perhitungan galat (ê) kafein, vitamin B1, B2, dan B6 PCR
30 0.0448 0.0333 -0.0229 0.1979 31 0.1301 -0.1056 -0.1450 -0.5722 32 0.0465 0.3516 -0.0031 0.0986 33 0.0816 -0.0203 -0.0393 0.3668 34 -0.0776 -0.0707 -0.1079 0.0255 35 -0.0676 0.3067 0.0359 -0.0038 36 -0.0502 -0.1608 -0.1679 -0.0897 37 0.1451 -0.1458 0.2959 0.0186 38 0.3116 -0.0570 0.0022 -0.8829 39 0.0849 -0.2633 0.0859 -0.1639 40 -0.2673 -0.2256 0.0518 -0.3405 41 0.0309 -0.3332 0.1267 -0.3352 42 0.2098 -0.0184 0.2429 -0.5620 43 -0.2299 0.0744 0.0293 0.1065 44 -0.1972 -0.3273 -0.0258 -0.0383 45 0.0276 -0.0852 -0.1790 0.1470 46 -0.0207 -0.3897 -0.0826 0.2201 47 0.1583 0.0740 -0.0458 0.1595 48 -0.1623 -0.1005 -0.0460 0.3503 V1 0.2573 0.4355 0.2042 0.3976 V2 0.2025 -0.0119 1.3714 0.3190 V3 0.0697 0.3283 0.9227 0.4894 V4 0.1396 0.2219 1.4834 0.6026 V5 0.0844 0.0428 0.8340 0.4422 V6 -0.3549 0.4163 1.2845 0.6718 V7 0.4977 0.3581 0.3999 0.6035 V8 0.2859 0.8165 1.5044 1.0393 V9 0.1347 0.2615 0.9922 0.5751 V10 -0.7439 0.1448 -0.2312 3.6014 V11 0.2831 -0.2630 0.4814 0.1296 V12 0.0626 -0.1596 1.1569 0.5331 V13 0.0901 0.4546 0.6739 1.1568 V14 -0.1379 -0.4804 1.4834 0.2053 V15 0.4620 -0.5301 0.8785 0.0545 V16 0.6446 -0.5395 1.5021 0.1868
Contoh perhitungan: ê = [Kafein]dugaan - [Kafein]
= (16.3111– 16.0000) mg/l = 0.3111 mg/l
RMSEC dan RMSEP untuk kafein:
RMSEC =
1
-ê
1 2 in
n i∑
== 0.1572
Lampiran 12 Perhitungan parameter kebaikan RMSEC dan RMSEP pada PLS
No. Set
[kafein] (mg/l)
[B1] (mg/l)
[B2] (mg/l)
[B6] (mg/l)
[kafein]^ (mg/l)
[B1]^ (mg/l)
[B2]^ (mg/l)
[B6]^ (mg/l)
Lanjutan Lampiran 12 Perhitungan parameter kebaikan RMSEC dan RMSEP pada PLS
V1 2.0 0.2 1.0 1.0 2.2785 0.2606 0.9247 0.9857 V2 6.0 0.2 8.0 3.0 6.0778 0.1115 8.0755 2.8683 V3 6.0 0.4 4.0 4.0 6.1392 0.5247 4.1433 3.9305 V4 10.0 0.4 8.0 6.0 10.1092 0.3484 8.1195 5.8179 V5 14.0 0.6 2.0 5.0 13.7929 0.7524 2.0279 5.2670 V6 2.0 0.6 6.0 3.0 1.8282 0.6355 6.3347 2.5623 V7 16.0 0.8 1.0 5.0 15.9342 0.7547 0.7865 5.1125 V8 12.0 0.8 8.0 7.0 12.1974 0.8825 8.1872 6.5866 V9 14.0 1.0 4.0 3.0 13.6787 0.9148 3.9384 3.1824 V10 2.0 1.0 8.0 5.0 1.5180 0.8610 6.9610 6.6795 V11 10.0 1.2 1.0 2.0 9.7997 1.1320 0.9243 1.9484 V12 6.0 1.2 5.0 8.0 6.2496 1.2096 5.3284 7.2185 V13 8.0 1.4 1.0 6.0 8.1940 1.4228 1.2557 5.7929 V14 6.0 1.4 6.0 5.0 6.0335 1.4611 6.3233 4.5052 V15 14.0 1.6 2.0 3.0 14.1194 1.4547 1.9417 3.1088 V16 16.0 1.6 8.0 1.0 16.0496 1.6737 7.7280 1.4337 ^ : dugaan
Perhitungan galat (ê) kafein, vitamin B1, B2, dan B6 PLS
No.
Set ê kafein
ê vitamin B1
ê vitamin B2
ê vitamin B6
Lanjutan Perhitungan galat (ê) kafein, vitamin B1, B2, dan B6 PLS
30 -0.1055 0.0660 0.1081 0.3888 31 -0.2013 0.1240 -0.2631 -0.5352 32 0.1065 0.3806 -0.1036 -0.0113 33 -0.0058 0.0906 0.1234 0.5638 34 -0.2965 0.1496 -0.0086 0.1073 35 0.0755 0.1800 -0.1327 -0.2146 36 -0.2701 0.0789 -0.0526 0.0055 37 0.3902 -0.3109 0.3249 0.1261 38 0.6544 -0.3436 -0.2588 -1.0413 39 0.2950 -0.4100 0.0998 -0.1019 40 -0.0709 -0.3245 -0.0022 -0.3227 41 0.3050 -0.4824 0.0976 -0.2974 42 0.6791 -0.4267 -0.0088 -0.8093 43 0.2430 -0.1292 -0.0754 -0.2230 44 -0.4499 0.0724 0.1581 0.2035 45 0.2169 -0.0550 -0.1793 -0.0231 46 0.1063 -0.2286 -0.0328 0.1032 47 0.4788 -0.0068 -0.0819 -0.1342 48 0.0943 -0.1322 0.0308 0.2135 V1 0.2785 0.0606 -0.0753 -0.0143 V2 0.0778 -0.0885 0.0755 -0.1317 V3 0.1392 0.1247 0.1433 -0.0695 V4 0.1092 -0.0516 0.1195 -0.1822 V5 -0.2071 0.1524 0.0279 0.2670 V6 -0.1718 0.0355 0.3347 -0.4377 V7 -0.0658 -0.0453 -0.2135 0.1125 V8 0.1974 0.0825 0.1872 -0.4134 V9 -0.3213 -0.0852 -0.0616 0.1824 V10 -0.4820 -0.1390 -1.0390 1.6795 V11 -0.2003 -0.0680 -0.0757 -0.0517 V12 0.2496 0.0096 0.3284 -0.7815 V13 0.1940 0.0228 0.2557 -0.2071 V14 0.0335 0.0611 0.3233 -0.4948 V15 0.1194 -0.1453 -0.0583 0.1088 V16 0.0496 0.0737 -0.2720 0.4337
Contoh perhitungan: ê = [Kafein]dugaan - [Kafein]
= (16.3093– 16.0000) mg/l = 0.3093 mg/l
RMSEC dan RMSEP untuk kafein:
RMSEC =
1
-ê
1 2 in
n i∑
== 0.2943
Lampiran 13 Analisis simultan kafein, vitamin B1, B2, dan B6 dalam contoh minuman berenegi
Lampiran 14 Perhitungan presisi dan kadar kafein, vitamin B1, B2, dan B6 dalam contoh minuman berenergi dengan PCR dan PLS
Contoh Ulangan
PCR PLS
Kadar (mg/l) Bobot (mg) Kadar
(mg/l) Bobot (mg)
Kafein
1 11.9867 47.9470 11.9042 47.6168 2 12.1597 48.6389 12.0115 48.0460 3 12.8243 51.2973 12.1264 48.5056 4 12.0553 48.2210 11.9199 47.6796 5 12.8958 51.5834 12.1898 48.7592 6 13.1458 52.5834 12.2682 49.0728
Rerata 12.5113 50.0452 12.0700 48.2799
Vit. B1
1 0.3890 1.5562 0.4053 1.6215 2 0.3782 1.5127 0.3569 1.4274 3 0.3723 1.4892 0.3668 1.4673 4 0.3870 1.5478 0.3932 1.5727 5 0.3710 1.4842 0.3736 1.4943 6 0.3705 1.4821 0.3699 1.4797
Rerata 0.3780 1.5120 0.3776 1.5105
Vit. B2
1 1.1775 4.7098 1.5852 6.3406 2 1.3211 5.2843 1.0704 4.2817 3 1.2317 4.9269 1.1798 4.7192 4 1.4096 5.6383 1.5438 6.1755 5 1.3902 5.5609 1.3094 5.2377 6 1.3453 5.3811 1.2171 4.8685
Rerata 1.3126 5.2502 1.3176 5.2705
Vit. B6
1 1.1987 4.7947 1.7633 7.0531 2 1.2160 4.8639 1.6848 6.7393 3 1.2824 5.1297 1.7503 7.0011 4 1.1805 4.7221 1.7271 6.9083 5 1.2896 5.1583 1.6466 6.5864 6 1.3396 5.3583 1.7369 6.9478
Rerata 1.2511 5.0045 1.7182 6.8727
Contoh perhitungan kafein pada ulangan 1:
Kadar kafein dalam 1000 ml = 11.9867 mg
Kadar kafein dalam 50 ml = mg ml
ml
9867 . 11 1000
50 ×
= 0.5993 mg
Faktor pengenceran =
ml ml
625 . 0
50
= 80
Lampiran 15 Perhitungan uji presisi
Standar Kafein Vit. B1 Vit. B2 Vit. B6
PCR PLS PCR PLS PCR PLS PCR PLS
47.947 47.6168 1.5562 1.6215 4.7098 6.3406 4.7947 7.0531 48.6389 48.046 1.5127 1.4274 5.2843 4.2817 4.8639 6.7393 51.2973 48.5056 1.4892 1.4673 4.9269 4.7192 5.1297 7.0011 48.221 47.6796 1.5478 1.5727 5.6383 6.1755 4.7221 6.9083 51.5834 48.7592 1.4842 1.4943 5.5609 5.2377 5.1583 6.5864 52.5834 49.0728 1.4821 1.4797 5.3811 4.8685 5.3583 6.9478 Rerata 50.0452 48.2799 1.5120 1.5105 5.2502 5.2705 5.0045 6.8727 Standar
deviasi 2.0042 0.5940 0.0329 0.0791 0.3639 0.8256 0.2482 0.1765 %SBR 4.00 1.23 2.18 5.24 6.93 15.73 4.96 3.53
Simpangan Baku Relatif (%SBR) = ×100
x
SB =
100 0452 . 50
0329 .
0 × = 4.00%
Lampiran 16 Perhitungan uji akurasi
Standar Model Standar (mg) % Perolehan
kembali
Label Ditemukan
Kafein
PCR 50.0 50.0452 100.09 PLS 50.0 48.2799 96.56
B1
PCR 1.2 1.5120 126.00
PLS 1.2 1.5105 125.89
B2
PCR 5.2 5.2505 100.97
PLS 5.2 5.2705 101.36
B6
PCR 5.0 5.0045 100.09
PLS 5.0 6.8727 137.45
Recovery = 100%
label kafein standar
ditemukan yang
kafein
standar ×
= 100% mg
00 . 50
mg 0452 .
KOMBINASI SPEKTRUM ULTRAVIOLET DAN
MODEL KALIBRASI MULTIVARIAT UNTUK
PENENTUAN SIMULTAN KAFEIN,
VITAMIN B1, B2, DAN B6
YULIA FATMAWATI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Multivariat untuk Penentuan Simultan Kafein, Vitamin B1, B2, dan B6. Dibimbing oleh MOHAMAD RAFI dan UTAMI DYAH SYAFITRI.
Kombinasi spektrum ultraviolet dan model kalibrasi multivariat telah dikembangkan untuk penentuan simultan kadar kafein, vitamin B1, B2, dan B6 dalam contoh minuman berenergi karena mempunyai kriteria cepat, mudah, dan tidak membutuhkan pemisahan terlebih dahulu. Teknik kalibrasi multivariat yang digunakan adalah regresi komponen berganda (principle component regression, PCR) dan kuadrat terkecil parsial (partial least square, PLS).
Kemampuan pendugaan yang lebih baik diberikan oleh PCR yang ditentukan berdasarkan nilai parameter validasi koefisien determinasi (R2) yang tinggi, root mean square error of calibration (RMSEC), dan root mean square error of prediction (RMSEP) yang kecil. Hasil yang diperoleh untuk kafein, vitamin B1, B2, dan B6 menunjukkan nilai RMSEC secara berturut-turut sebesar 0.1572, 0.2184, 0.0979, dan 0.2735. Nilai R2 sebesar 0.9984, 0.7143, 0.9970, dan 0.9822. Sedangkan nilai RMSEP sebesar 0.0991, 0.1168, 0.0782, dan 0.1308. Kadar kafein vitamin B1, B2, dan B6 yang diperoleh dari contoh minuman berenergi dengan PCR adalah 50.0452, 1.5120, 5.2502, dan 5.0045 mg. Berdasarkan evaluasi kinerja analitik pada contoh minuman berenergi, model terbaik juga diberikan oleh PCR karena diperoleh hasil presisi dan akurasi yang lebih baik dibandingkan PLS.
ABSTRACT
YULIA FATMAWATI. Combination of Ultraviolet Spectrum and Multivariate Calibration Models for Simultaneous Determination of Caffeine, B1, B2, and B6-Vitamins. Supervised by MOHAMAD RAFI and UTAMI DYAH SYAFITRI.
Combination of ultraviolet spectrum and multivariate calibration has been developed for simultaneous determination of caffeine, B1, B2, and B6-vitamins contents in energy drinks because it is a fast, easy, and simple method without any pre-separation. The multivariate calibration techniques were used principle component regression(PCR) and partial least square(PLS).
KOMBINASI SPEKTRUM ULTRAVIOLET DAN
MODEL KALIBRASI MULTIVARIAT UNTUK
PENENTUAN SIMULTAN KAFEIN,
VITAMIN B1, B2, DAN B6
YULIA FATMAWATI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
NIM :
G44203004
Menyetujui,
Pembimbing I,
Pembimbing II,
Mohamad Rafi, S.Si
Utami Dyah Syafitri, S.Si. M.Si
NIP 132 321 454
NIP 132 311 922
Mengetahui:
Dekan Fakultas Mate