RINGKASAN
FEBRI RAHAYU EFTIAH SARI, D14080035. 2013. Karakteristik Kimia dan Mikrobiologi serta Organoleptik Telur Asin dengan Lama Pengovenan yang Berbeda Selama Penyimpanan. Skripsi. Departemen Ilmu Produksi dan Teknologi Peternakan, Fakultas Peternakan, Institut Pertanian Bogor.
Pembimbing Utama : Dr. Ir. Rukmiasih, MS
Pembimbing Anggota : Dr. Ir. Rarah Ratih Adjie Maheswari, DEA
Telur asin yang dihasilkan dari proses perendaman dalam larutan garam biasanya dimasak terlebih dahulu sebelum dijual ke konsumen. Perebusan merupakan metode pemasakan yang sering digunakan pada telur asin, namun daya simpan telur asin dengan metode tersebut tidak berlangsung lama (< 1 bulan), atau jika masih berlangsung lama, hal tersebut lebih disebabkan oleh semakin lamanya waktu pengasinan yang dilakukan, akibatnya rasa putih telur terlampau asin. Salah satu upaya untuk mengatasi hal tersebut adalah dengan mengembangkan metode pemasakan baru seperti kombinasi antara perebusan dan pengovenan. Penelitian ini dilakukan untuk lebih mengetahui perubahan kimia, mikrobiologi, dan organoleptik telur asin yang dioven selama penyimpanan, dan diharapkan pengovenan dapat meningkatkan citarasa telur asin dan mempertahankan kualitasnya selama satu bulan. Penelitian pendahuluan bertujuan untuk menentukan lama pengovenan yang akan digunakan dalam penelitian utama berdasarkan uji ranking hedonik. Penelitian utama bertujuan untuk menganalisis karakteristik kimia, mikrobiologi, dan organoleptik telur asin selama penyimpanan serta memperoleh perlakuan yang terbaik berdasarkan ketiga karakteristik tersebut.
Penelitian utama menggunakan Rancangan Acak Lengkap dengan tiga taraf perlakuan (rebus, rebus dan oven 4 jam, rebus dan oven 6 jam) dan tiga kali ulangan untuk nilai pH, aw, kadar air, dan kadar abu putih telur, serta dua kali ulangan untuk nilai total mikroba. Pengujian karakteristik kimia dan total mikroba dilakukan pada hari ke-0, 15, dan 30; sedangkan karakteristik organoleptik pada hari ke-7 dan 28. Data pengujian nilai pH, aw, kadar air, dan kadar abu putih telur dianalisis sidik ragam dan hasil yang berbeda nyata dilanjutkan dengan uji Tukey. Data pengujian kadar NaCl dianalisis secara deskriptif. Data uji ranking hedonik dianalisis dengan uji Friedman dan hasil yang berbeda nyata dilakukan uji perbandingan berganda. Data uji hedonik dan mutu hedonik dianalisis dengan uji Kruskal Wallis dan hasil yang berbeda nyata dilakukan uji banding rataan ranking.
Hasil penelitian menunjukkan bahwa lama pengovenan berpengaruh (P<0,05) pada kadar air putih telur dan total mikroba (total plate count) sebelum penyimpanan (H0) serta karakteristik organoleptik setelah penyimpanan (H7 dan H28). Karakteristik organoleptik yang dipengaruhi oleh lama pengovenan setelah penyimpanan 7 hari antara lain ranking dan mutu hedonik dari warna putih dan kuning telur, aroma, dan tekstur kuning telur, sedangkan untuk rasa kuning telur lama pengovenan hanya mempengaruhi ranking hedoniknya. Lama pengovenan hanya mempengaruhi nilai hedonik dari warna putih dan kuning telur setelah 28 hari. Kesimpulannya, telur asin yang dioven 6 jam menghasilkan kualitas yang terbaik.
ABSTRACT
Chemical, Microbiology, and Organoleptic Characteristics of Salted Egg Produced by Different Oven Baking Time During Storage
Sari, F. R. E., Rukmiasih and R. R. A. Maheswari
Duck egg is one of poultry products which often be made as salted egg. Nowdays, salted egg can be cooked by different methods, one of them was oven baking method. This main research was aimed to study chemical, microbiology, and organoleptic characteristics of salted duck egg produced by different oven baking time during storage. Salted duck eggs were baked for a duration of four and six hours after boiling (R+O4 and R+O6). Chemical and microbiology characteristics were determined at 0, 15, and 30 days, while organoleptic characteristics were determined at 7 and 28 days. Completely Randomized Design with 3 treatments (boiling (R), R+O4, R+O6) and 3 replications for chemical characteristics or 2 replications for microbiology characteristics was used in this experiment. Data from chemical and microbiology test was analyzed by analysis of variance, while data from organoleptic test was analyzed by Friedman and Kruskal Wallis. The results showed that there were significant differences (P<0.05) in water content of albumen and total plate count of whole egg before storage (0 day), and after storage (7 and 28 days) there were significant differences (P<0.05) in organoleptic characteristics. In conclusion, salted eggs that were oven baked for six hours were the best in this research.
1 PENDAHULUAN
Latar Belakang
Telur merupakan produk ternak unggas yang sering dikonsumsi masyarakat karena harganya murah, kandungan gizinya tinggi, mudah diperoleh, dan dimanfaatkan baik bagian putih telur, kuning telur maupun gabungan keduanya. Jenis telur yang umum digunakan oleh masyarakat untuk membuat telur asin adalah telur itik karena pori-pori kerabang telurnya besar sehingga garam NaCl lebih mudah berpenetrasi ke dalam telur dan kandungan lemaknya tinggi sehingga lebih mudah terbentuk tekstur masir dan berminyak pada kuning telur. Tekstur masir dan berminyak merupakan ciri khas dari telur asin dan menjadi daya tarik bagi konsumen.
Cara sederhana dalam membuat telur asin yaitu dengan merendam telur ke dalam larutan garam. Telur yang diasinkan dengan metode tersebut biasanya mengalami pemasakan terlebih dahulu sebelum dijual ke konsumen. Metode pemasakan yang sering digunakan oleh produsen telur asin adalah perebusan, namun permasalahan yang sering dijumpai adalah daya simpan dari telur asin yang hanya direbus tidak dapat bertahan selama satu bulan dalam suhu ruang, atau jika telur asin tersebut masih bertahan selama satu bulan, hal ini lebih disebabkan oleh semakin lamanya waktu pengasinan yang dilakukan, akibatnya rasa putih telur menjadi sangat asin, sehingga dapat mengurangi citarasa telur asin tersebut karena konsumen tidak menyukai rasa putih telur yang terlampau asin.
2 diharapkan telur asin yang dihasilkan memiliki aroma dan citarasa yang khas serta kualitasnya dapat dipertahankan selama satu bulan dalam suhu ruang.
Tujuan
3 TINJAUAN PUSTAKA
Telur
Telur merupakan salah satu produk unggas yang mengandung protein cukup tinggi sebesar 12%. Telur terutama kaya akan asam amino esensial seperti lisin, triptofan, dan khususnya metionin yang merupakan asam-asam amino esensial terbatas (Yuwanta, 2010). Komposisi asam amino yang lengkap dengan proporsi yang seimbang tersebut menyebabkan protein telur digunakan secara luas sebagai standar dan bilangan nisbah efisiensi protein (NEP) serta dianggap memiliki nilai biologi 100 (Man, 1999).
Pengelompokkan telur berdasarkan bobot minimum yang dijelaskan dalam United States Departement of Agriculture (2000) yakni jumbo (70 gram/butir), besar sekali (63 gram/butir), besar (56 gram/butir), sedang (49 gram/butir), kecil (42 gram/butir), dan kecil sekali (35 gram/butir). Kaewmanee (2010) menyebutkan bah- wa sebutir telur itik tersusun atas 10,87% kerabang, 54,73% putih telur, dan 33,94% kuning telur dengan bentuk struktur telur yang berlapis-lapis (Gambar 1).
Keterangan: (1) Germinal disc (blastoderm), (2) membran yolk, (3) latebra, (4) lapisan yolk terang, (5) lapisan yolk gelap, (6) kalaza, (7) lapisan encer albumen, (8) lapisan kental albumen, (9) pori-pori, (10) kantung udara, (11) membran kerabang, (12) membran dalam telur, (13) permukaan kerabang yang bergabung dengan lapisan mamilari, (14) kutikula, (15) lapisan bunga karang
4 Kerabang Telur
Kerabang telur terdiri atas bagian luar yang ditutupi oleh gelatin (kutikula), garam inorganik, beberapa materi organik dan sedikit air. Rata-rata komposisi protein pada membran kerabang telur ayam sebesar 70%. Bagian kutikula pada kerabang telur diduga mengandung beberapa protein berupa musin (Romanoff dan Romanoff, 1963). Kerabang telur menurut Belitz dan Grosch (2009) terdiri atas kristal kalsium karbonat yang tertanam dalam matriks organik dan kompleks protein-mukopolisakarida dengan perbandingan 50:1, juga sejumlah kecil magnesium karbonat dan fosfat. Suguro et al. (2000) menyebutkan bahwa kandungan kalsium pada kerabang telur sebesar 37,7%. Struktur kerabang telur berdasarkan Belitz dan Grosch (2009) terbagi menjadi empat bagian yakni kutikula, lapisan bersepon (bunga karang), lapisan mamilari, dan pori-pori.
Romanoff dan Romanoff (1963) menyebutkan bahwa ukuran pori-pori besar dan kecil pada permukaan kerabang telur itik masing-masing yaitu 0,036 x 0,031 mm dan 0,014 x 0,012 mm, sedangkan pada permukaan kerabang telur ayam ukuran pori-pori besar dan kecilnya masing-masing yaitu 0,029 x 0,022 mm dan 0,011 x 0,009 mm. Jumlah pori di seluruh bagian kerabang telur bervariasi antara 100-200 pori/cm2, bagian tumpul dari telur memiliki jumlah pori yang lebih banyak serta tebal kerabang yang lebih tipis daripada bagian yang lain. Fungsi pori kerabang telur adalah sebagai tempat pertukaran gas-gas dari dalam dan luar kerabang sehingga membantu respirasi embrio di dalam telur.
Putih Telur (Albumen)
Romanoff dan Romanoff (1963) menyebutkan, bahwa putih telur terdiri atas putih telur encer bagian luar (23,2%) dengan kadar air sebesar 88,8%, putih telur kental (57,3%) dengan kadar air sebesar 87,6%, putih telur encer bagian dalam (16,8%) dengan kadar air sebesar 86,4%, dan khalazaferous (2,7%) dengan kadar air sebesar 84,3%. Bahan penyusun utama dari putih telur adalah air. Kadar air akan mengalami penurunan dari lapisan luar menuju lapisan dalam putih telur.
5 atau ovotransferin (12%), ovomukoid (11%), ovomusin (3,5%), lisosom atau G1 globulin (3,4%), G2 globulin (4%), G3 globulin (4%), ovoflavoprotein (0,8%), ovoglikoprotein (1,0%), ovomakroglobulin (0,5%), ovoinhibitor (1,5%), sistatin (0,05%), dan avidin (0,05%) (Stadelman dan Cotterill, 1995).
Kuning Telur (Yolk)
Kuning telur merupakan emulsi lemak dalam air dengan berat kering sebesar 50% yang terdiri atas 65% lipid, 31% protein, dan 4% karbohidrat, vitamin, dan mineral (Belitz dan Grosch, 2009). Susunan kuning telur dari bagian dalam hingga luar menurut Yuwanta (2010) yakni latebra, kuning telur berwarna putih (white yolk) dan berwarna kuning (yellow yolk) yang tersusun secara konsentris berselang seling, serta membran vitelin. Huopalahti et al. (2007) menyebutkan bagian-bagian dari kuning telur berdasarkan bahan kering yaitu terdiri atas 19%-23% granula dan 77%-81% plasma. Bagian granula terdiri atas 70% high density lipoprotein (HDL), 16% fosvitin, dan 12% low density lipoprotein (LDL), sedangkan bagian plasma terdiri atas LDL sebanyak 85% dan livetin sebanyak 15%.
Bagian granula memiliki ukuran yang seragam dengan diameter 1,0-1,3 µm, sedangkan bagian plasma berupa yolk droplet memiliki ukuran yang bervariasi antara 20-40 µm. Jenis protein yang terdapat pada granula kuning telur yaitu lipovitelin (disusun oleh HDL) dan fosvitin, sedangkan yang terdapat dalam plasma yaitu lipovitelenin (disusun oleh LDL) dan livetin (Belitz dan Grosch, 2009).
Lemak kuning telur menurut Yuwanta (2010) tersusun atas komplek lemak-protein dalam bentuk LDL dan lipovitelin dalam bentuk ikatan bebas. Lemak telur terdiri atas 65% trigliserida, 28,3% fosfolipid, dan 5,2% kolesterol. Stadelman dan Cotterill (1995) menyebutkan bahwa kuning telur merupakan sumber utama karbonil jenuh maupun tak jenuh.
Substansi Aroma
6 diberi pakan dengan kanola akan menghasilkan telur yang berbau amis. Timbulnya bau amis disebabkan oleh terakumulasinya trimetilamin pada kuning telur. Trimetilamin (TMA) terbentuk dari degradasi kolin oleh senyawa mikroba.
Aroma utama yang ditemukan pada putih dan kuning telur yang dimasak adalah sulfur akibat dari penguapan gas H2S (Stadelman dan Cotterill, 1995). Karakteristik aroma dari telur yang dimasak lebih lanjut dijelaskan oleh Warren et al. (1995) yaitu terdapat 32 senyawa volatil yang dapat diidentifikasi dari telur yang dimasak selama 30 menit pada suhu 100 oC melalui analisis volatil extraction. Senyawa volatil tersebut dibagi menjadi 8 kelas yang terdiri atas 10 aldehid, 2 keton, 5 alkohol, 2 alkana, 1 furan, 1 pirazin, 6 senyawa aromatik, dan 6 asam lemak. Di antara senyawa-senyawa tersebut, pirazin merupakan senyawa yang berkontribusi dalam flavor makanan yang dipanggang.
Pengawetan dan Pemasakan Telur
Pengawetan menurut Damayanthi dan Mudjajanto (1995) tidak dapat menaikkan mutu suatu bahan pangan. Pengawetan bertujuan untuk memperlama waktu terjadinya penurunan mutu bahan pangan tersebut.
Prinsip pengawetan telur utuh adalah untuk mencegah terjadinya penguapan air dan terlepasnya CO2 dari dalam telur serta mencegah masuknya mikroba dari luar melalui pori-pori kerabang. Umumnya pengawetan yang dilakukan pada telur dapat dilakukan dalam bentuk pengawetan telur segar dan telur olahan. Pengawetan dalam bentuk telur segar yakni dengan menutup pori-pori kerabang telur. Pengawetan ini dapat dilakukan antara lain dengan pelapisan telur menggunakan minyak, pelapisan dengan bahan kimia (kalsium karbonat, sodium silikat, vaselin, dan parafin), perendaman dalam larutan kapur dan ekstrak nabati. Pengawetan telur segar juga dapat dilakukan dengan menyimpannya dalam lemari es. Pengawetan dalam bentuk telur olahan yakni dengan menambah bahan-bahan yang mampu untuk mengawetkan makanan seperti garam, gula, dan asam (Syariefdan Halid, 1993).
Pengasinan
7 menjadi rendah, (3) garam yang berbentuk larutan dapat mengurangi oksigen terlarut, dan (4) ion Cl dari garam bersifat racun bagi mikroorganisme. Gaman dan Sherrington (1992) menjelaskan bahwa klorin digunakan sebagai desinfektan yang mampu membunuh bakteri dengan reaksi sebagai berikut:
Cl2 + H2O HCl + HOCl. Asam hipoklorat (HOCl) yang terbentuk akan membunuh bakteri dengan cara oksidasi dan kemudian berubah menjadi asam klorida.
Pengasinan menyebabkan terjadinya peningkatan proporsi berat putih telur namun menurunkan proporsi kuning telur. Kadar air baik putih maupun kuning telur menurun secara bertahap seiring meningkatnya kandungan garam dan abu serta lamanya waktu pengasinan (Kaewmanee, 2010).
Pemberian garam menurut Belitz dan Grosch (2009) menimbulkan pengaruh pada kelarutan protein. Pemberian yang terlampau sedikit (konsentrasi rendah) akan meningkatkan kelarutan protein (efek salting in) dengan menekan interaksi protein-protein elektrostatik, sedangkan pemberian garam yang terlampau banyak (konsentrasi tinggi) akan menurunkan kelarutan protein (efek salting out) sebagai hasil dari kecenderungan hidrasi ion garam. Stadelman dan Cotterill (1995) juga menyebutkan bahwa penambahan garam akan meningkatkan koagulasi, beberapa garam menurunkan sejumlah ikatan air pada putih telur.
Pengasinan dengan metode pembalutan cenderung lebih banyak menghasilkan eksudasi minyak pada kuning telur daripada dengan metode perendaman. Kekerasan dan keadhesifan kuning telur juga ditemukan lebih tinggi pada pengasinan metode pembalutan, sedangkan metode perendaman ditemukan lebih tinggi di dalam kemampuan retak, daya elastisitas, kelengketan dan daya kunyah. Kadar air putih telur dari metode perendaman sedikit lebih rendah daripada metode pembalutan, kemungkinan besar hal ini dipengaruhi oleh migrasi air dari putih telur menuju air garam jenuh yang diperantarai dengan proses osmosis (Kaewmanee, 2010).
8
Sumber: Poedjiadi dan Supriyanti (2005)
Proses Termal
Proses termal (pemanasan) menurut Estiasih dan Ahmadi (2011) dapat menyebabkan perubahan pada karakteristik fisik, kimia maupun nutrisi produk pangan. Perubahan yang terjadi bergantung pada intensitas maupun metode pemanasan, bahan baku, serta perlakuan sebelum pemanasan. Perubahan sifat organoleptik juga dapat terjadi pada proses termal. Perubahan tersebut merupakan akumulasi dari berbagai perubahan yang terjadi selama proses seperti denaturasi protein dan restrukturisasi lemak yang menyebabkan perubahan tekstur dan cita rasa produk. Harris dan Karmas (1989) menyebutkan, bahwa pengolahan dapat menyebabkan penyusutan mineral maksimal 3% pada bahan pangan.
Perebusan. Winarno (2008) menyebutkan, perebusan merupakan cara memasak makanan dalam cairan yang sedang mendidih (100 oC). Bahan pangan yang dimasak menggunakan air akan meningkat daya kelarutannya. Hasil penelitian yang dilakukan oleh Wulandari (1999) menunjukkan bahwa lama perebusan yang efektif digunakan untuk tujuan pengawetan adalah selama 15 menit karena menghasilkan penurunan kadar air dan nilai pH yang paling rendah sehingga proses kebusukan dapat diperlambat. Lama perebusan 15 menit menyebabkan protein putih telur yang terdenaturasi lebih sedikit dibandingkan telur yang direbus selama 30 menit. Selain itu penetrasi air rebusan akan lebih rendah bila telur direbus selama 15 menit. Banyaknya protein yang terdenaturasi mampu meningkatkan kadar air dalam putih telur, sehingga menyebabkan proses pembusukan yang ditimbulkan oleh bakteri dan proses kimia lebih dipercepat.
9 liki daya simpan selama 1,5–3 hari. Keretakan kerabang telur yang terjadi pada proses perebusan menurut Brown (2000) dapat dikurangi dengan cold start method yakni memasukkan telur ke panci perebusan yang berisi air dingin lalu dipanaskan.
Pengovenan. Pengovenan adalah proses termal yang menggunakan udara panas. Udara panas tersebut dipindahkan ke bahan makanan melalui tiga cara yakni radiasi, konveksi, dan konduksi (Estiasih dan Ahmadi, 2011). Hasil penelitian Trilaksami et al. (2004) mengenai pengaruh suhu dan lama pengovenan terhadap karakteristik cumi-cumi kertas menunjukkan bahwa suhu mempengaruhi kecerahan produk, semakin tinggi suhu pengovenan menyebabkan semakin rendah nilai kecerahan produk.
Hasil penelitian Ayuza (2011) mengenai pengaruh level suhu pengovenan terhadap kadar protein, kadar air, total koloni bakteri, umur simpan, dan nilai organoleptik telur asin menunjukkan bahwa telur asin yang paling baik adalah telur asin yang dioven selama 6 jam pada suhu 90 oC. Perlakuan telur asin tersebut menghasilkan kadar protein 13,47%, kadar air 54,77%, total koloni bakteri 9,22 x 104 CFU/g dengan umur simpan selama 36,20 hari.
Winarno et al. (1980) menyebutkan jika pemasakan dengan menggunakan udara panas seperti pengovenan dilakukan pada suhu yang terlalu tinggi, maka hal ini dapat mengakibatkan terjadinya “case hardening” yaitu suatu bagian luar (permukaan) dari bahan sudah kering sedangkan bagian sebelah dalamnya masih basah. Hal ini disebabkan oleh suhu yang terlalu tinggi sehingga bagian permukaan cepat mengering dan menjadi keras, serta akan menghambat penguapan selanjutnya dari air yang terdapat di bagian dalam bahan tersebut. Terjadinya “case hardening” dapat menyebabkan mikroba yang ada di bagian dalam bahan yang masih basah dapat berkembang biak sehingga menimbulkan kebusukan, dan membutuhkan waktu yang lebih lama jika bahan akan direhidrasi. Cara mencegah “case hardening” misalnya dengan membuat suhu pengovenan tidak terlalu tinggi.
10 terdiri atas aldehid, keton, berbagai ester, asam, dan alkohol (Estiasih dan Ahmadi, 2011).
Perubahan yang Terjadi selama Pemasakan Denaturasi Protein
Denaturasi merupakan proses yang mengubah struktur molekul tanpa memutuskan ikatan peptida dari protein. Denaturasi dapat disebabkan oleh panas, pH, garam, dan efek permukaan (Man, 1999). Pengertian lain dari denaturasi yang dinyatakan Winarno (2008) yakni modifikasi pada struktur sekunder, tersier, dan kuartener terhadap molekul protein tanpa terjadinya pemecahan ikatan-ikatan kovalen. Struktur primer merupakan susunan asam amino dalam protein yang berbentuk linier. Struktur sekunder merupakan struktur protein yang berbentuk tiga dimensi dengan susunan cabang rantai polipeptida yang saling berdekatan. Struktur tersier merupakan susunan protein yang terdiri atas struktur sekunder yang berbeda bentuknya, sedangkan struktur kuartener merupakan struktur protein yang melibatkan beberapa polipeptida.
Denaturasi secara umum bersifat reversible ketika rantai peptida distabilkan dalam keadaan yang tidak terikat oleh agen denaturasi. Denaturasi yang bersifat irreversible terjadi ketika rantai peptida yang tidak terikat distabilkan oleh interaksinya dengan rantai lain (contohnya protein telur selama perebusan) (Belitz dan Grosch, 2009).
Reaksi Maillard
11 mengubah warna makanan tersebut walaupun secara biologis lisin dalam makanan sudah tidak tersedia.
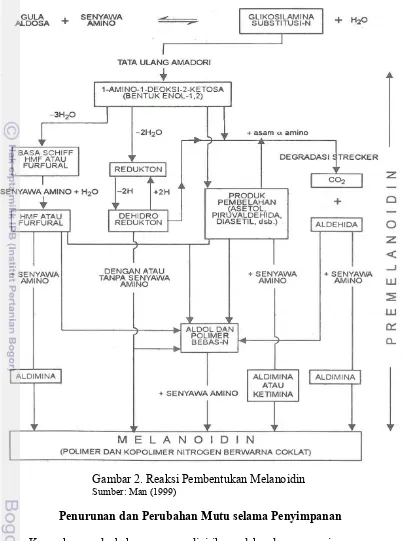
Reaksi Maillard lanjutan dapat terjadi melalui tiga jalur, dua diantaranya dimulai dengan produk amadori, sedangkan yang ketiga dari degradasi Strecker. Reaksi ini akan berakhir dengan pembentukan pigmen berwarna coklat yang disebut melanoidin (Gambar 2). Protein yang telah mengalami reaksi Maillard daya cernanya menurun. Penurunan nilai gizi protein tersebut dapat diuraikan sebagai berikut: (1) lisin dan sistin rusak akibat bereaksi dengan karbonil atau dikarbonil dan aldehid; (2) penurunan availabilitas semua asam amino termasuk leusin (leusin biasanya stabil), karena terbentuknya ikatan silang antar asam-asam amino melalui produk reaksi Maillard; (3) penurunan daya cerna protein karena tercegahnya penetrasi enzim ke dalam substrat (protein) atau karena tertutupinya sisi protein yang dapat diserang enzim dari ikatan silang tersebut (Muchtadi, 1989).
12 Gambar 2. Reaksi Pembentukan Melanoidin
Sumber: Man (1999)
Penurunan dan Perubahan Mutu selama Penyimpanan
13 Perubahan Fisik
Perubahan fisik yang terjadi selama penyimpanan telur utuh diantaranya yaitu berkurangnya berat terutama disebabkan oleh hilangnya air dari putih telur, juga CO2, NH3, N2, dan H2S; pertambahan ukuran ruang udara; penurunan berat jenis; bercak-bercak pada permukaan kulit telur karena penyebaran air yang tidak merata; penurunan jumlah putih telur kental karena serat glikoprotein ovomusin pecah; penambahan ukuran kuning telur karena perpindahan air dari putih telur ke kuning telur sebagai akibat perbedaan tekanan osmosis; perubahan cita rasa; serta kenaikan pH terutama dalam putih telur yang meningkat dari sekitar pH 7 hingga 10 atau 11 sebagai akibat hilangya CO2 (Buckle, 2007).
Penguapan air secara terus menerus melalui kerabang menyebabkan penurunan berat jenis dengan koefisien penurunan harian sekitar 0,0017 g/cm3 (Belitz dan Grosch, 2009). Laju susut air menurut Harris dan Karmas (1989) bergantung pada luas permukaan produk maupun keadaan lingkungannya.
Stadelman dan Cotterill (1995) menyebutkan, kelembaban tidak mempengaruhi kualitas putih dan kuning telur namun berpengaruh besar pada hilangnya bobot telur selama penyimpanan. Kelembaban relatif yang dianjurkan untuk menyimpan telur adalah 75%-80%.
Perubahan Kimia
Nilai pH. Nilai pH merupakan ukuran keasaman atau alkalinitas suatu larutan (Gaman dan Sherrington, 1992). Albumen pada telur segar mengandung bikarbonat dan CO2. Terdapat hubungan antara konsentrasi CO2 bebas dengan pH. Hilangnya CO2 menyebabkan meningkatnya nilai pH pada albumen, nilai pH bergantung pada tekanan parsial dari CO2. Perubahan tekanan CO2 berpengaruh kecil pada pH kuning telur (Stadelman dan Cotterill, 1995). Nilai pH putih telur segar sekitar 7,6-7,9 dan meningkat menjadi 9,7 selama penyimpanan (Belitz dan Grosch, 2009).
14 Kadar Air. Labuza (1980) menjelaskan bahwa kadar air dan aktivitas air (aw) berperan dalam laju dari banyak reaksi kimia dan pertumbuhan mikroba dalam makanan. Kadar air dan aktivitas air akan menurun dengan adanya proses pengeringan. Hal ini menyebabkan cairan menjadi lebih pekat serta beberapa komponen bahan pangan membentuk larutan lewat jenuh dan akhirnya mengendap. Laju reaksi yang meningkat seiring dengan peningkatan konsentrasi dalam larutan menyebabkan naiknya laju penyusutan zat gizi (Harris dan Karmas, 1989).
Air yang terdapat dalam bahan makanan menurut Winarno (2008) umumnya disebut air terikat. Air terikat dibagi menjadi empat tipe menurut derajat keterikatannya. Tipe pertama (1) yaitu molekul air yang terikat pada molekul-molekul lain melalui suatu ikatan hidrogen berenergi besar. Molekul air membentuk hidrat dengan molekul-molekul lain yang mengandung atom O dan N seperti karbohidrat, protein, dan garam. Air tipe ini tidak dapat membeku pada proses pembekuan tetapi sebagian bisa dihilangkan dengan pengeringan biasa. Tipe kedua (2) yakni molekul air yang membentuk ikatan hidrogen dengan molekul air lain di dalam mikrokapiler. Air jenis ini sukar dihilangkan dan penghilangan air tipe ini akan menyebabkan penurunan aktivitas air, jika air tipe ini dihilangkan seluruhnya maka kandungan air bahan berkisar 3%-7%. Tipe ketiga (3) yakni air yang secara fisik terikat dalam jaringan matriks bahan seperti membran kapiler dan serat. Tipe ini disebut juga air bebas, mudah diuapkan dan dapat dimanfaatkan untuk pertumbuhan mikroba. Kandungan air bahan akan berkisar antara 12%-25% jika air tipe ini diuapkan seluruhnya. Tipe keempat (4) yaitu air yang tidak terikat dalam jaringan suatu bahan atau air murni. Contohnya, air yang menempel pada bahan makanan setelah proses pencucian bahan.
Aktivitas Air (aw). Aktivitas air berpengaruh besar terhadap laju dari banyak reaksi kimia dalam makanan dan terhadap laju pertumbuhan mikroba. Kapang dan khamir mulai tumbuh pada kisaran aw 0,7 dan 0,8; sedangkan bakteri tumbuh ketika aw mencapai 0,8 (Man, 1999).
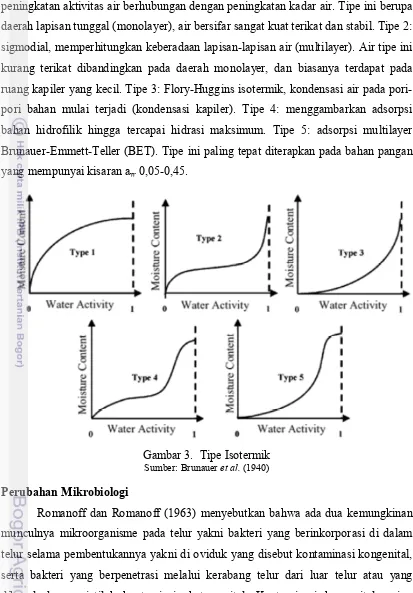
15 peningkatan aktivitas air berhubungan dengan peningkatan kadar air. Tipe ini berupa daerah lapisan tunggal (monolayer), air bersifar sangat kuat terikat dan stabil. Tipe 2: sigmodial, memperhitungkan keberadaan lapisan-lapisan air (multilayer). Air tipe ini kurang terikat dibandingkan pada daerah monolayer, dan biasanya terdapat pada ruang kapiler yang kecil. Tipe 3: Flory-Huggins isotermik, kondensasi air pada pori-pori bahan mulai terjadi (kondensasi kapiler). Tipe 4: menggambarkan adsorpsi bahan hidrofilik hingga tercapai hidrasi maksimum. Tipe 5: adsorpsi multilayer Brunauer-Emmett-Teller (BET). Tipe ini paling tepat diterapkan pada bahan pangan yang mempunyai kisaran aw 0,05-0,45.
Gambar 3. Tipe Isotermik Sumber: Brunauer et al. (1940)
Perubahan Mikrobiologi
16 paratyphi, Staphylococcus aureus, Proteus vulgaris, fluorescent organism, Serratia
marcescens, dan Pseudomonas aeruginosa.
Romanoff dan Romanoff (1963) lebih lanjut menjelaskan bahwa jumlah spora kapang pada kerabang dari telur segar sekitar 200-500 thallus/cm2, jumlah bakteri per kerabang sekitar 35.000 koloni/cm2 ketika diinkubasi pada suhu 37 oC atau 130.000 koloni/cm2 pada 20 oC. Tipe mikroorganisme yang ditemukan pada permukaan kerabang telur antara lain tidak berspora batang (38%), berspora batang (30%), kokus (25%), khamir (4%), dan actinomyces (3%). Biasanya bakteri tidak ditemukan pada kuning telur ataupun putih telur dari 10% telur segar. Tipe mikroorganisme yang sering dijumpai pada telur segar yaitu Basilus dan Mikrokokus. Moats (1980) selanjutnya menyatakan bahwa telur yang tidak mengalami pencucian mengandung kokus gram positif lebih besar daripada yang mengalami pencucian serta mengandung bakteri Aerococcus dan Streptococcus faecalis yang tidak ditemukan pada telur yang mengalami pencucian.
Telur yang dicuci dengan air yang lebih dingin dari telur maka dimungkinkan bakteri akan meresap ke dalam pori-pori kerabang telur. Umumnya, pori-pori pada kerabang telur tahan terhadap penetrasi mikroba karena dilengkapi dengan substansi organik berupa musin dan ketika kering dapat menghambat masuknya bakteri atau kapang. Selaput kerabang (shell membrane) berbentuk jalinan serabut yang memungkinkan berperan sebagai filter bagi mikroorganisme yang berhasil masuk melalui pori-pori kerabang. Albumen juga berperan sebagai barier bagi mikroflora, mikroorganisme yang berhasil melewati kerabang maupun selaputnya dapat mati di dalam putih telur (albumen) sebelum mencapai kuning telur. Kemampuan albumen dalam melindungi kuning telur disebabkan oleh adanya kandungan antibakteri pada albumen tersebut (Romanoff dan Romanoff, 1963).
Harrungton et al. (1974) menyebutkan, bahwa pada telur asin ditemukan Pseudomonas cepacia, Alcaligenes metalcaligenes, A. recti, Micrococcus leutus,
17 tumbuh bila kadar garam pada bahan pangan kurang dari 10%. Persyaratan mutu mikrobiologis telur asin menurut Standar Nasional Indonesia 01-4277-1996 adalah negatif untuk Salmonella dalam satu koloni per 25 gram serta < 10 untuk Staphylococcus aureus dalam satu koloni per gram.
Sel vegetatif bakteri, khamir, dan kapang menurut Effendi (2009) mudah terdestruksi oleh pemanasan sekitar 80 oC, demikian pula spora dari khamir dan kapang. Spora dari bakteri umumnya tahan terhadap pemanasan pada 100 oC selama berjam-jam. Daya tahan terhadap kematian dari mikroorganisme dipengaruhi oleh berbagai faktor antara lain: (1) umur dan kondisi mikroorganisme; (2) komposisi medium seperti kadar air, garam dapur, gula, garam-garam nitrit atau nitrat, lemak, dan zat-zat penghambat pertumbuhan mikroorganisme; (3) nilai pH dan aw medium tumbuh; dan (4) suhu pemanasan. Buckle et al. (2007) menyebutkan, bahwa seringkali organisme tumbuh lebih baik pada bahan pangan yang telah dimasak dibandingkan dengan bahan pangan mentah karena zat-zat gizi tersedia lebih baik dan tekanan persaingan dari mikroorganisme lain telah dikurangi.
Uji Organoleptik
Pengujian organoleptik atau sensori merupakan cara pengujian menggunakan indera manusia sebagai alat utama untuk menilai mutu produk. Penilaian menggunakan alat indera ini meliputi spesifikasi mutu kenampakan, bau, rasa dan konsistensi (tekstur) serta beberapa faktor lain yang diperlukan untuk menilai produk tersebut. Prinsip uji organoleptik adalah menggunakan indera manusia sebagai alat utama untuk menilai mutu produk (Badan Standardisasi Nasional, 2006). Karakteristik sensori seperti tekstur, citarasa, aroma, dan warna dari produk makanan merupakan atribut terpenting bagi konsumen (Theron dan Lues, 2011).
18 dinilai karena mendapat penjelasan atau latihan. Jumlah panelis ini berkisar antara 15-25 orang.
19 MATERI DAN METODE
Lokasi dan Waktu
Penelitian ini dilaksanakan di Laboratorium Terpadu (uji kimia dan mikrobio- logi) dan di bagian Teknologi Hasil Ternak (uji organoleptik), Departemen Ilmu Produksi dan Teknologi Peternakan, Fakultas Peternakan Institut Pertanian Bogor. Penelitian dimulai dari bulan April hingga Juli 2012.
Materi Bahan
Bahan utama dalam penelitian berupa telur itik varietas lokal dengan berat sekitar 50-60 g. Telur itik yang digunakan untuk penelitian pendahuluan berumur 4 hari dan berasal dari Cirebon, sedangkan telur itik yang digunakan untuk penelitian utama berumur 0-1 hari dan berasal dari peternakan rakyat di Ciomas Permai. Bahan yang digunakan dalam proses pengasinan adalah garam dapur.
Bahan-bahan yang digunakan untuk uji kimia antara lain air destilata, larutan K2CrO4 5%, dan AgNO3 0,1 N. Bahan-bahan untuk uji mikrobiologi yaitu larutan NaCl 0,85% steril, spiritus, alkohol 70%, Plate Count Agar (PCA), kapas, aluminium foil, dan label.
Alat
Alat-alat untuk pembuatan telur asin antara lain wadah pengasin (toples), panci, dan oven listrik. Alat untuk uji kimia antara lain timbangan digital 0,0001 g, pH meter, aw meter (Novasina AG), cawan porselen, desikator, tanur, labu erlenmeyer, hot plate dan alat titrasi.
20 Prosedur
Penelitian Pendahuluan
Penilitian pendahuluan bertujuan untuk menentukan lama pengovenan yang akan digunakan dalam penelitian utama melalui uji ranking hedonik.
Penelitian Utama
Penelitian utama bertujuan untuk menganalisis karakteristik kimia, mikrobiologi, dan organoleptik telur asin selama penyimpanan serta memperoleh perlakuan yang terbaik. Langkah-langkah yang dilakukan antara lain:
1. Persiapan Telur Itik
Telur itik yang dipilih memiliki kriteria antara lain berat telur seragam, tidak retak, dan tidak busuk. Tahap selanjutnya telur diteropong (candling) kemudian dicuci dan dibersihkan dengan sabut stainless dan air hangat (35 oC).
2. Pembuatan Larutan Garam
Larutan garam yang digunakan adalah larutan garam dengan konsentrasi 25%. Penentuan konsentrasi tersebut berdasarkan jumlah garam terkecil yang dibutuhkan untuk membuat larutan garam jenuh (Wulandari et al., 2002). Garam ditimbang lalu dilarutkan dalam air mendidih dan didiamkan hingga dingin. Larutan tersebut selanjutnya disaring dengan kain blacu agar diperoleh larutan yang jernih.
3. Perendaman dalam Larutan Garam
Telur disusun di dalam toples kemudian larutan garam dituangkan secara perlahan-lahan ke dalam toples. Perbandingan telur (g) dan larutan garam (ml) yang digunakan untuk merendam adalah 1:2. Bagian atas telur diberi pemberat agar telur tidak mengapung. Perendaman dalam larutan garam dilakukan selama dua belas hari, kemudian telur dikeluarkan dan diletakkan pada suhu ruang selama dua hari (Damayanti, 2008).
4. Perebusan dan Pengovenan
21 5. Penyimpanan
Telur asin disimpan pada suhu ruang (28-30 oC) dengan kelembaban 83% -91% selama 30 hari.
Rancangan dan Analisis Data
Rancangan percobaan pada penelitian utama adalah rancangan acak lengkap (RAL) yang terdiri atas 3 taraf perlakuan yaitu rebus (R), rebus dan oven 4 jam (R+O4), serta rebus dan oven 6 jam (R+O6). Ulangan yang dilakukan sebanyak 3 kali untuk nilai pH, aw, kadar air, dan kadar abu putih telur, serta 2 kali untuk nilai
total plate count. Model matematika yang digunakan dalam penelitian utama sesuai Mattjik dan Sumertajaya (2006) sebagai berikut:
Yij = µ + i + ij
Keterangan: Yij = pengamatan pada perlakuan ke-i dan ulangan ke-j µ = rataan umum
i = pengaruh perlakuan ke-i
ij = pengaruh acak pada perlakuan ke-i dan ulangan ke-j
Analisis Data
Analisis data menggunakan software Minitab 14 dan Statistix 8. Data pengujian kimia (nilai pH, aw, kadar air, serta kadar abu putih telur) dan total mikroba dianalisis dengan sidik ragam, jika hasilnya berbeda nyata dilanjutkan dengan uji Tukey atau Beda Nyata Jujur (Mattjik dan Sumertajaya, 2006). Data pengujian kadar NaCl dianalisis secara deskriptif.
Data pengujian ranking hedonik dianalisis dengan uji Friedman dan jika berbeda nyata dilakukan uji perbandingan berganda. Uji hedonik dan mutu hedonik dianalisis dengan uji Kruskal Wallis dan jika berbeda nyata dilanjutkan dengan uji banding rataan ranking (Gibbons dan Chakraborti, 2003).
Peubah
Pengujian Karakteristik Kimia
22 kandungan air lebih tinggi dan letaknya dekat dengan kerabang telur sehingga lebih mudah terjadi perubahan kimia. Sampel untuk setiap ulangan dan setiap perlakuan berasal dari 2 butir telur yang masing-masing diambil bagian putihnya lalu dikompositkan. Masing-masing pengujian dilakukan secara duplo.
Nilai pH (Accociation of Official Analytical Chemist, 2006). Sampel sebanyak 5 g dihaluskan dan dihomogenkan dengan 5 ml air destilata. Pengukuran dilakukan dengan alat pH-meter yang sebelumnya telah dikalibrasi dengan larutan buffer pada pH 7 dan 4.
Nilai aw. Sampel diambil sesuai dengan kapasitas pengukuran aw meter. Alat aw meter dikalibrasi terlebih dahulu sebelum digunakan. Kalibrasi yang dilakukan yaitu kalibrasi 53, 75, dan 90.
Kadar Air (Accociation of Official Analytical Chemist, 2006). Sampel diambil sebanyak 5 g lalu dimasukkan ke dalam cawan porselen yang telah dikeringkan dan diketahui beratnya. Sampel tersebut kemudian dikeringkan pada oven bersuhu 105 o
C selama 16-18 jam. Cawan dari oven didinginkan dalam desikator dan ditimbang. Kadar air dapat dihitung dengan rumus:
Kadar air (% bb)=berat sampel awal (g) - berat sampel akhir (g)
berat sampel awal (g) x 100%
Kadar Abu (Accociation of Official Analytical Chemist, 2006). Sampel diambil sebanyak 5 gram lalu dimasukkan ke dalam cawan porselen yang telah dikeringkan dan diketahui beratnya. Cawan dan sampel dibakar di atas hot plate hingga sampel tidak berasap lagi, kemudian diletakkan dalam tanur bersuhu 550 oC dan dibiarkan selama 12-18 jam. Kadar abu dapat dihitung dengan rumus:
Kadar abu (% bb) = berat abu (g)
berat sampel awal (g) x 100%
23 titrasi tercapai apabila timbul warna jingga secara persisten. Kadar garam dihitung dengan rumus sebagai berikut:
Kadar garam (NaCl)(% bb)= V x N x 58,4
berat sampel awal (mg)x 100%
Keterangan: V = ml larutan AgNO3 N = normalitas AgNO3 58,4 = berat molekul NaCl
Pengujian Karakteristik Mikrobiologi
Pengujian karakteristik mikrobiologi yang dilakukan adalah pengujian total mikroba atau Total Plate Count (TPC) pada hari ke-0, 15, dan 30. Sampel untuk setiap ulangan dan setiap perlakuan berasal dari 2 butir telur yang masing-masing diambil seluruh bagian isinya lalu dikompositkan.
Pengujian Total Plate Count menurut BAM (Maturin dan Peeler, 2001). Sampel
diambil sebanyak 10 g lalu larutan NaCl fisiologis 0,85% steril ditambahkan sebanyak 90 ml ke dalam wadah steril yang berisi sampel lalu divortex selama 1 hingga 2 menit untuk memperoleh larutan yang homogen. Larutan tersebut merupakan larutan dengan pengenceran 10-1. Sebanyak 1 ml suspensi pengenceran 10-1 dipindahkan dengan pipet steril ke dalam larutan 9 ml NaCl fisiologis untuk mendapatkan pengenceran 10-2 kemudian dibuat pengenceran 10-3 dengan cara yang sama. Tahap selanjutnya 1 ml suspensi dari setiap pengenceran dimasukkan ke dalam cawan petri secara duplo.
Sebanyak 15-20 ml PCA yang sudah didinginkan hingga 45 oC ± 1 oC di- tambahkan pada masing-masing cawan yang sudah berisi suspensi. Homogenisasi campuran dilakukan dengan menggesekkan cawan ke depan dan ke belakang atau dengan membentuk angka delapan lalu didiamkan hingga menjadi padat. Cawan diinkubasi pada temperatur 34-36 oC dengan posisi terbalik selama 24 - 48 jam.
Penghitungan jumlah koloni dilakukan pada setiap seri pengenceran kecuali cawan petri yang berisi koloni menyebar. Kriteria cawan yang dipilih yakni berjumlah 25 – 250 koloni.
24
N= ∑C
[(1 x n1)+(0,1 x n2)x(d)]
Keterangan:
N = total mikroba per ml
∑C = jumlah koloni pada semua cawan
n1 =jumlah cawan yang berisi 25-250 koloni pada pengenceran pertama n2 = jumlah cawan yang berisi 25-250 koloni pada pengenceran kedua
d = angka pengenceran dari cawan yang pertama kali dapat dihitung (berisi 25-250 koloni)
Pengujian Karakteristik Organoleptik
Pengujian karakteristik organoleptik yang dilakukan adalah uji ranking hedonik dan mutu hedonik pada hari ke-7 (H7) serta uji hedonik pada hari ke-28 (H28). Atribut sensori yang dinilai antara lain warna putih dan kuning telur, aroma keseluruhan telur, tekstur putih dan kuning telur, serta rasa putih dan kuning telur.
Uji Organoleptik (Soekarto, 1985). Panelis diberi formulir isian yang dijawab menurut instruksi yang diberikan. Sampel yang disajikan berupa satu butir telur yang dibagi menjadi delapan bagian secara vertikal dan setiap bagian diuji untuk setiap panelis. Panelis yang digunakan adalah panelis agak terlatih berjumlah 15 orang untuk uji ranking dan mutu hedonik dan 20 orang untuk uji hedonik.
Tahapan kegiatan yang dilakukan dalam penelitian utama dapat dilihat pada Gambar 4.
Gambar 4. Diagram Alir Penelitian Utama Pemilihan telur itik Perendaman dalam larutan garam 25%
(12 hari) dan dikeluarkan dari perendaman (2 hari) di suhu ruang
Perebusan (1 jam)
Pengovenan pada suhu 100 o
C selama 0, 4 dan 6 jam ssesuai perlakuan Penyimpanan (T = 28-30
o
C; RH= 83%-91%) Uji kimia dan total
25 HASIL DAN PEMBAHASAN
Penelitian Pendahuluan
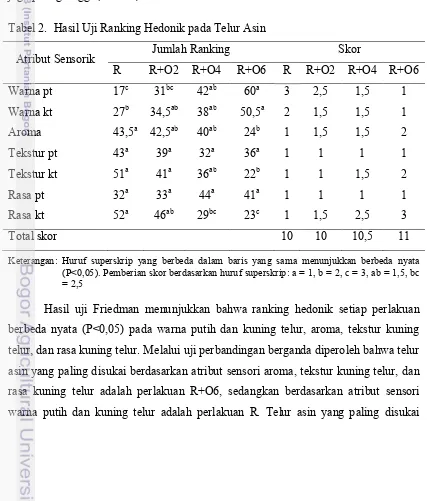
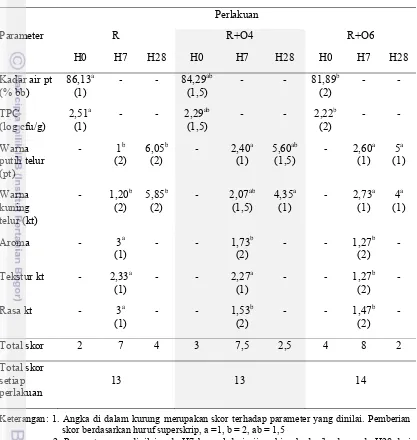
Lamanya pengovenan yang akan digunakan dalam penelitian utama ditentukan melalui uji ranking hedonik pada telur asin dengan perlakuan direbus (R), direbus dan dioven 2 jam (R+O2), direbus dan dioven 4 jam (R+O4), serta direbus dan dioven 6 jam (R+O6). Uji sensori tersebut menggunakan 15 panelis agak terlatih dengan atribut sensori berupa warna putih (pt) dan kuning telur (kt), aroma keseluruhan telur, tekstur putih dan kuning telur, serta rasa putih dan kuning telur. Jumlah ranking terendah pada perlakuan di dalam atribut sensorik yang sama menunjukkan bahwa perlakuan tesebut paling disukai sehingga skor yang diberikan juga paling tinggi (Tabel 2).
Tabel 2. Hasil Uji Ranking Hedonik pada Telur Asin
Atribut Sensorik Jumlah Ranking Skor
R R+O2 R+O4 R+O6 R R+O2 R+O4 R+O6
Warna pt 17c 31bc 42ab 60a 3 2,5 1,5 1
Warna kt 27b 34,5ab 38ab 50,5a 2 1,5 1,5 1
Aroma 43,5a 42,5ab 40ab 24b 1 1,5 1,5 2
Tekstur pt 43a 39a 32a 36a 1 1 1 1
Tekstur kt 51a 41a 36ab 22b 1 1 1,5 2
Rasa pt 32a 33a 44a 41a 1 1 1 1
Rasa kt 52a 46ab 29bc 23c 1 1,5 2,5 3
Total skor 10 10 10,5 11
Keterangan: Huruf superskrip yang berbeda dalam baris yang sama menunjukkan berbeda nyata (P<0,05). Pemberian skor berdasarkan huruf superskrip: a = 1, b = 2, c = 3, ab = 1,5, bc = 2,5
26 berdasarkan seluruh atribut sensorik yaitu telur asin perlakuan rebus dan oven 6 jam (R+O6) dengan total skor tertinggi (11) dan yang paling kurang disukai adalah perlakuan rebus (R) serta rebus dan oven 2 jam (R+O2) dengan total skor terendah (10). Perlakuan yang dipilih untuk penelitian utama adalah perlakuan yang menghasilkan telur asin dengan penilaian disukai (R+O4) hingga paling disukai (R+O6), sedangkan sebagai kontrol dipilih perlakuan R.
Penelitian Utama Karakteristik Kimia pada Putih Telur Asin
Kadar NaCl Putih Telur. Kadar NaCl putih telur hanya diamati sebelum penyimpanan (H0) karena kadar NaCl tidak mengalami perubahan yang signifikan selama penyimpanan (Wulandari, 2002). Kadar NaCl dari putih telur asin pada hari ke-0 dapat dilihat pada Tabel 3.
Tabel 3. Kadar NaCl (% bb) pada Putih Telur Asin
Perlakuan Kadar NaCl (% bb)
Perebusan (R) 3,73 ± 0,01
Perebusan dan oven 4 jam (R+O4) 4,23 ± 0,04
Perebusan dan oven 6 jam (R+O6) 4,83 ± 0,00
27 dengan pengovenan paling lama yaitu 6 jam (R+O6) menghasilkan kadar NaCl paling tinggi, sedangkan pada perlakuan R kadar NaCl paling rendah.
Nilai pH Putih Telur. Ray (2004) menjelaskan bahwa nilai pH adalah konsentrasi ion hidrogen dalam sistem yang diekspresikan sebagai logaritma negatif hidrogen atau konsentrasi proton (–log [H+]). Pengukuran nilai pH perlu dilakukan untuk mengetahui kadar keasaman atau kebasaan serta keamanan dan umur simpan dari suatu produk makanan karena perubahan nilai pH yang signifikan dapat mengubah atribut sensori dari produk makanan tersebut. Rataan nilai pH putih telur asin yang diperoleh selama penyimpanan dapat dilihat pada Gambar 5.
Gambar 5. Nilai pH Putih Telur pada Perlakuan R ( ), R + O4 ( ), dan R + O6
( ) selama Penyimpanan
Hasil sidik ragam menunjukkan bahwa lama pengovenan tidak memberikan pengaruh yang nyata terhadap pH putih telur asin baik sebelum penyimpanan (H0) maupun setelah penyimpanan 15 dan 30 hari (H15 dan H30). Nilai rata-rata pH putih telur asin dari masing-masing perlakuan tergolong basa (pH > 7). Belitz dan Grosch (2009) menyebutkan bahwa nilai pH putih telur segar yang belum mengalami pengasinan sekitar 7,6-7,9, sedangkan nilai pH putih telur asin yang belum dimasak sekitar 7,15-7,99 (Wulandari, 2002). Hal tersebut menunjukkan baik telur itik segar, telur asin yang belum dimasak maupun yang telah dimasak sama-sama memiliki nilai pH putih telur yang tinggi (basa).
Rata-rata nilai pH putih telur setiap perlakuan mengalami penurunan selama penyimpanan, kecuali perlakuan R pada akhir pengamatan (H30). Perubahan nilai
28 pH tersebut sering dihubungkan dengan aktivitas mikroorganisme. Hal ini didukung dengan hasil total mikroba yang cenderung meningkat selama penyimpanan (Gambar 9). Penurunan nilai pH disebabkan oleh peningkatan konsentrasi ion hidrogen yang berasal dari hasil metabolisme mikroorganisme berupa asam. Asam yang terbentuk berasal dari pemecahan karbohidrat atau protein oleh mikroorganisme yang tahan garam seperti Micrococcus dan Pseudomonas. Harrungton et al. (1974) menyebut- kan bahwa Micrococcus leutus dan Pseudomonas cepacia masih ditemukan pada telur asin. Peningkatan nilai pH seperti yang terjadi pada perlakuan R setelah disimpan selama 30 hari juga dipengaruhi oleh mikroorganisme. Buckle et al. (2007) menjelaskan bahwa kapang dan khamir dapat memecah asam yang secara alamiah terdapat dalam bahan makanan sehingga menyebabkan kenaikan nilai pH. Kapang akan menggunakan asam sebagai sumber karbohidratnya dan mengoksidasi asam amino sehingga terbentuk NH3 yang bersifat basa. Fardiaz (1992) menambahkan, beberapa bakteri proteolitik mampu mendegradasi protein menjadi senyawa-senyawa yang bersifat basa seperti amonia selama penyimpanan.
29 Aktivitas air merupakan ukuran ketersediaan air untuk fungsi biologis dan berhubungan dengan kehadiran air pada makanan dalam bentuk bebas (Ray, 2004). Hasil sidik ragam menunjukkan bahwa nilai aktivitas air (aw) tidak berbeda nyata pada ketiga perlakuan telur asin baik sebelum (H0) maupun selama penyimpanan (H15 dan H30). Nilai aw telur asin yang dioven lebih rendah dari telur segar. Ray (2004) menyebutkan bahwa nilai aktivitas air pada telur segar adalah 0,98-0,99. Perubahan nilai aw tersebut disebabkan oleh adanya penambahan garam NaCl dan pemasakan. Winarno (2008) menyebutkan, jika garam dengan konsentrasi tinggi ditambahkan ke dalam suatu larutan protein maka daya larut protein akan berkurang, akibatnya protein akan terpisah sebagai endapan. Peristiwa ini dikenal dengan sebutan salting out, dengan adanya peristiwa tersebut maka nilai aw menjadi turun. Pemasakan turut berperan dalam perubahan nilai aw karena pemasakan menyebabkan sebagian air bebas dari telur menguap sehingga nilai aw menurun.
30 Gambar 6 menunjukkan bahwa penurunan nilai aw putih telur terbesar selama penyimpanan terjadi pada telur asin yang dioven lebih lama (R+O6) walaupun secara statistik lama pengovenan tidak mempengaruhi nilai aw putih telur. Hal tersebut dapat terjadi karena semakin lama waktu pengovenan menyebabkan konsentrasi NaCl yang tertinggal dalam putih telur semakin tinggi sehingga protein globular telur mampu mengikat molekul-molekul air bebas pada putih telur. Pendapat tersebut didukung dengan kadar abu putih telur perlakuan R+O6 lebih tinggi daripada perlakuan R dan R+O4 selama penyimpanan (Gambar 8).
Gambar 6 juga menunjukkan bahwa peningkatan nilai aw ditemukan pada perlakuan R setelah penyimpanan 30 hari (H30). Buckle et al. (2007) menyatakan bahwa peningkatan tersebut disebabkan oleh metabolisme mikroorganisme yang umumnya diikuti dengan pelepasan air sehingga nilai aw akan meningkat.
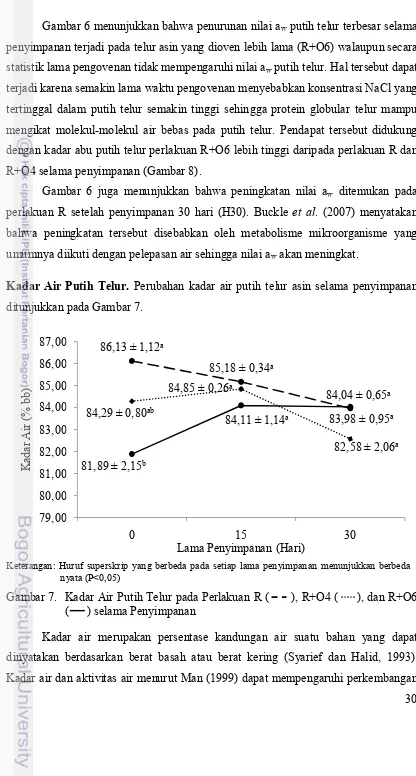
Kadar Air Putih Telur. Perubahan kadar air putih telur asin selama penyimpanan Kadar air dan aktivitas air menurut Man (1999) dapat mempengaruhi perkembangan
86,13 ± 1,12a
31 reaksi pembusukan secara kimia dan mikrobiologi dalam makanan. Hasil sidik ragam menunjukkan bahwa lama pengovenan memberikan pengaruh nyata (P<0,05) pada kadar air putih telur sebelum penyimpanan (H0). Hasil uji Tukey menunjukkan bahwa kadar air putih telur dengan perlakuan rebus dan oven 6 jam (R+O6) berbeda dengan perlakuan yang hanya direbus (R). Semakin lama waktu pengovenan yang dilakukan maka semakin banyak air yang dapat diuapkan dari dalam telur, oleh sebab itu putih telur perlakuan R+O6 mempunyai kadar air yang paling rendah sebelum penyimpanan, diikuti dengan perlakuan R+O4 dan R.
Lama pengovenan tidak memberikan pengaruh nyata pada kadar air putih telur selama penyimpanan 15 dan 30 hari (H15 dan H30). Rata-rata kadar air putih telur mengalami penurunan akibat menguapnya air dari dalam telur selama penyimpanan kecuali perlakuan yang mengalami pengovenan (R+O4, R+O6) setelah disimpan 15 hari. Peningkatan kadar air putih telur terbesar terjadi pada perlakuan R+O6 walaupun secara statistik kadar air putih telur tidak berbeda. Hal tersebut dapat disebabkan oleh waktu pengovenan yang lebih lama menyebabkan denaturasi protein lebih besar dan kadar NaCl yang tertinggal pada putih telur juga lebih banyak. Fennema (1985) menyatakan bahwa salah satu akibat dari denaturasi protein adalah berubahnya daya mengikat air. Umumnya denaturasi protein akan menurunkan daya mengikat air karena interaksi antar protein menjadi lemah sehingga ruang untuk molekul air berkurang, namun dengan adanya NaCl yang juga mampu mendenaturasi protein dan memiliki sifat higroskopis menyebabkan protein globular telur dapat mengikat molekul-molekul air bebas sehingga kadar air putih telur meningkat dan aktivitas airnya menurun. Pendapat tersebut didukung dengan data penurunan aktivitas air terbesar setelah disimpan 15 hari (H15) terdapat pada perlakuan R+O6.
32 penguapan air dipengaruhi oleh diameter dan jumlah pori-pori kulit telur, suhu, kelembaban relatif (RH), dan tekanan udara selama penyimpanan.
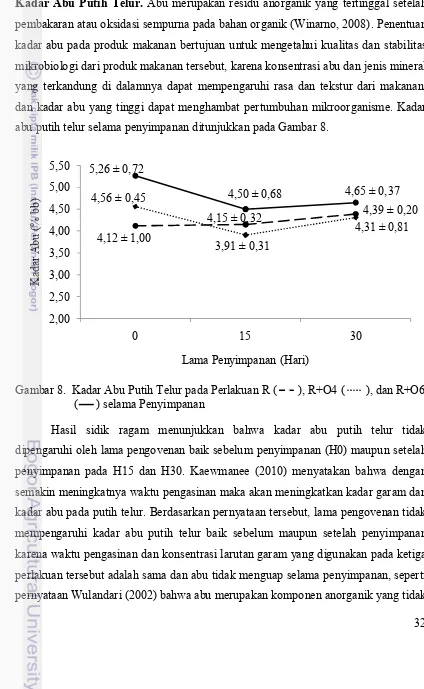
Kadar Abu Putih Telur. Abu merupakan residu anorganik yang tertinggal setelah pembakaran atau oksidasi sempurna pada bahan organik (Winarno, 2008). Penentuan kadar abu pada produk makanan bertujuan untuk mengetahui kualitas dan stabilitas mikrobiologi dari produk makanan tersebut, karena konsentrasi abu dan jenis mineral yang terkandung di dalamnya dapat mempengaruhi rasa dan tekstur dari makanan, dan kadar abu yang tinggi dapat menghambat pertumbuhan mikroorganisme. Kadar abu putih telur selama penyimpanan ditunjukkan pada Gambar 8.
Gambar 8. Kadar Abu Putih Telur pada Perlakuan R ( ), R+O4 ( ), dan R+O6 ( ) selama Penyimpanan
Hasil sidik ragam menunjukkan bahwa kadar abu putih telur tidak dipengaruhi oleh lama pengovenan baik sebelum penyimpanan (H0) maupun setelah penyimpanan pada H15 dan H30. Kaewmanee (2010) menyatakan bahwa dengan semakin meningkatnya waktu pengasinan maka akan meningkatkan kadar garam dan kadar abu pada putih telur. Berdasarkan pernyataan tersebut, lama pengovenan tidak mempengaruhi kadar abu putih telur baik sebelum maupun setelah penyimpanan karena waktu pengasinan dan konsentrasi larutan garam yang digunakan pada ketiga perlakuan tersebut adalah sama dan abu tidak menguap selama penyimpanan, seperti pernyataan Wulandari (2002) bahwa abu merupakan komponen anorganik yang tidak
33 dapat menguap melalui pori-pori kerabang telur, sebab abu yang terdapat pada putih telur akan berikatan dengan protein-protein yang berada dalam putih telur tersebut.
Rata-rata nilai kadar abu putih telur perlakuan R+O4 dan R+O6 mengalami penurunan setelah penyimpanan 15 hari kemudian mengalami peningkatan pada penyimpanan selanjutnya (H30), sedangkan kadar abu putih telur perlakuan R terus mengalami peningkatan selama penyimpanan. Hal tersebut bertolak belakang dengan kadar air putih telur yang diperoleh (Gambar 7). Ersoy dan Ozeren (2009) menyebutkan bahwa kadar abu pada ikan lele yang dipanggang mengalami peningkatan seiring dengan penurunan kadar air pada ikan lele tersebut. Hal ini menunjukkan bahwa kadar abu selalu berkorelasi negatif dengan kadar airnya, karena perhitungan kadar abu ditentukan oleh perbandingan antara berat abu dengan berat sampel awal yang masih mengandung sejumlah air tertentu (Accociation of Official Analytical Chemist, 2006), oleh sebab itu semakin rendah kadar air yang terdapat pada sampel awal maka kadar abu akan semakin tinggi.
Perubahan kadar abu pada putih telur selama penyimpanan juga dapat dihubungkan dengan nilai aktivitas airnya. Kadar abu yang mengandung garam NaCl dapat mempengaruhi protein pada putih telur yang telah terdenaturasi oleh pemasakan untuk masih dapat mengikat molekul-molekul air bebas, sehingga nilai aw putih telur akan turun meskipun kadar airnya meningkat (Gambar 6 dan 7 pada H15). Umumnya peningkatan kadar abu putih telur akan menurunkan nilai aktivitas airnya, karena garam yang terdapat dalam abu bersifat mudah menyerap air (higroskopis).
Karakteristik Mikrobiologi Telur Asin
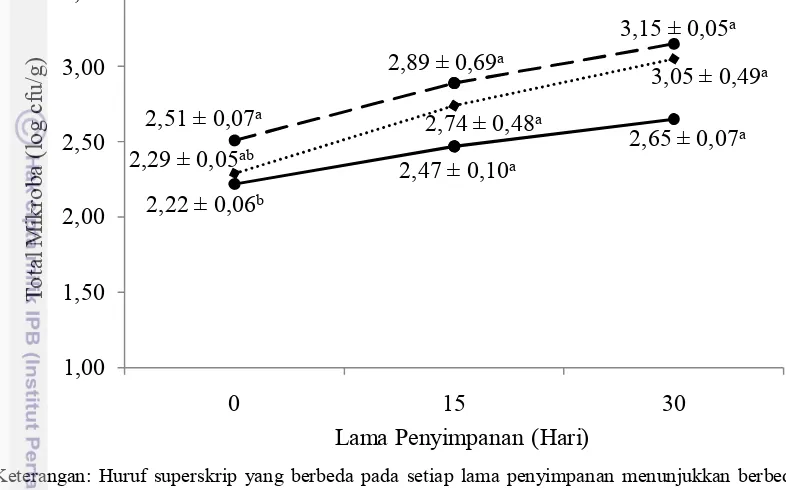
Kerusakan yang terjadi pada produk makanan biasanya disebabkan oleh aktivitas mikroorganisme. Buckle et al. (2007) menyebutkan bahwa pertumbuhan mikroorganisme di dalam makanan dapat menyebabkan perubahan fisik maupun kimia yang tidak diinginkan, sehingga makanan tersebut menjadi tidak layak untuk dikonsumsi. Cepat lambatnya kerusakan bergantung pada total mikroba dalam produk makanan tersebut. Total mikroba telur asin selama penyimpanan ditunjukkan pada Gambar 9.
34 direbus dan dioven selama 6 jam (R+O6), sedangkan total mikroba telur asin yang direbus dan dioven selama 4 jam (R+O4) tidak berbeda dengan R dan R+O6.
Gambar 9. Total Mikroba Telur Asin pada Perlakuan R ( ), R+O4 ( ), R+O6 ( ) selama Penyimpanan
Lama pengovenan berpengaruh pada total mikroba telur asin sebelum penyimpanan karena waktu pengovenan yang lebih lama akan meningkatkan kematian mikroba pembusuk maupun patogen. Mikroorganisme yang masih dimungkinkan untuk tetap hidup dalam telur asin sebelum penyimpanan adalah mikroorganisme dari golongan halofilik (suka dengan kondisi garam), halotoleran (tahan dengan kondisi garam), termofilik (suka dengan kondisi suhu yang tinggi) dan termodurik (tahan dengan kondisi suhu yang tinggi). Buckle et al. (2007) menyebutkan, banyak makanan yang diolah dengan pemanasan mengandung organisme-organisme yang masih hidup seperti spora-spora bakteri termofilik, oleh sebab itu sejumlah mikroorganisme masih ditemukan pada masing-masing perlakuan telur asin.
Lama pengovenan tidak memberikan pengaruh pada total mikroba telur asin selama penyimpanan H15 dan H30, walaupun demikian total mikroba tertinggi selama penyimpanan terdapat pada telur asin perlakuan R yang diikuti dengan
35 perlakuan R+O4 dan R+O6. Gambar 9 menunjukkan bahwa mikroorganisme berada dalam fase pertumbuhan logaritmik selama penyimpanan. Buckle et al. (2007) menyebutkan bahwa sel-sel mikroba dalam fase tersebut akan tumbuh dan membelah diri secara eksponensial hingga mencapai jumlah maksimum. Kecepatan pertumbuhan dalam fase tersebut menurut Fardiaz (1992) sangat dipengaruhi oleh medium tempat tumbuhnya seperti pH dan kandungan nutrien, serta faktor lingkungan seperti suhu dan kelembaban udara.
Suhu (28-30 oC), kelembaban ruang penyimpanan (83%-91%), pH putih telur (7,36-8,13), dan aw putih telur (0,868-0,899) yang tinggi mendukung pertumbuhan bakteri mesofilik, kapang, maupun khamir untuk tumbuh dan berkembang biak dalam telur asin selama penyimpanan. Estiasih dan Ahmadi (2009) menjelaskan bahwa mikroba pembusuk memiliki peluang lebih besar untuk tumbuh dan berkembang biak pada nilai pH yang lebih besar dari 4,6. Aktivitas air (aw) minimal menurut Jay (2000) untuk pertumbuhan bakteri adalah 0,9, khamir 0,88, kapang 0,80, dan bakteri halofilik 0,75. Golongan bakteri lebih menyukai kondisi bahan pangan yang mengandung protein dan berasam rendah (pH>4,5), sedangkan kapang dan khamir lebih menyukai bahan pangan yang mengandung karbohidrat dan gula serta berasam tinggi (pH<4,5) (Syarief dan Halid, 1993). Pernyataan tersebut menunjukkan bahwa golongan bakteri lebih mudah untuk tumbuh dan berkembang dalam telur asin selama penyimpanan daripada kapang dan khamir, karena komposisi protein pada telur asin lebih besar daripada karbohidrat berdasarkan Poedjiadi dan Supriyanti (2005).
Batas maksimum angka lempeng total (total plate count) pada telur segar berdasarkan SNI 7388:2009 adalah 105 koloni/g atau 5 log cfu/g. Mengacu pada standar tersebut, maka total mikroba telur asin perlakuan R, R+O4, dan R+O6 yang diperoleh selama penyimpanan 30 hari termasuk rendah sehingga masih aman untuk dikonsumsi. Rendahnya total mikroba dapat disebabkan oleh jumlah mikroba awal (sebelum telur diasinkan) yang rendah, faktor pengasinan dan pemasakan.
36 akibatnya pertumbuhan mikroorganisme aerobik dapat terhambat selama pengasinan. Perebusan dan pengovenan selama ≥ 1 jam juga dapat menyeleksi mikroorganisme yang dapat bertahan dalam telur asin, sehingga total mikroba sebelum penyimpanan (H0) cenderung rendah terutama perlakuan yang dioven lebih lama (R+O6) dan jumlahnya tetap berada di bawah batas maksimal TPC (SNI 7388:2009) selama penyimpanan 30 hari di suhu ruang.
Karakteristik Organoleptik Telur Asin
Penilaian organoleptik (evaluasi sensori) dilakukan dalam dua tahap, yakni tahap pertama yang bertujuan untuk mengetahui urutan penerimaan serta mutu dari telur asin setelah penyimpanan 7 hari (H7) melalui uji ranking dan mutu hedonik, serta tahap kedua yang bermaksud untuk mengetahui daya terima telur asin setelah penyimpanan 28 hari (H28) melalui uji hedonik.
Evaluasi Sensori Tahap Pertama
Hasil uji ranking hedonik dan mutu hedonik dalam evaluasi sensori tahap pertama ditunjukkan pada Gambar 10 dan 11.
Gambar 10. Rataan Nilai Ranking Hedonik Telur Asin pada Parameter Warna Putih Telur (pt), Warna Kuning Telur (kt), Aroma, Tekstur pt, Tekstur kt, Rasa pt, dan Rasa kt dengan Jumlah Panelis (n) =15; = Perlakuan R, = Perlakuan R+O4, = Perlakuan R+O6 dengan Skala 1 (Paling Di- sukai) hingga 3 (Paling Kurang Disukai)
b b
warna pt warna kt aroma tekstur pt tekstur kt rasa pt rasa kt
R
37 Gambar 11. Rataan Nilai Mutu Hedonik Telur Asin pada Parameter Warna Putih
Telur (pt), Warna Kuning Telur (kt), Aroma, Tekstur pt, Tekstur kt, Rasa pt, dan Rasa kt dengan Jumlah Panelis (n) =15; = Perlakuan R, = Perlakuan R+O4, = Perlakuan R+O6
Warna Putih Telur. Warna merupakan salah satu karakteristik penting yang menjadi referensi konsumen dalam memilih suatu produk makanan. Nilai rata-rata ranking hedonik untuk warna putih telur asin rebus (R) sebesar 1,00 ± 0,00, telur asin rebus dan oven 4 jam (R+O4) sebesar 2,40 ± 0,51, serta telur asin rebus dan oven 6 jam (R+O6) sebesar 2,60 ± 0,51. Hasil uji Friedman menunjukkan bahwa terdapat perbedaan yang nyata (P<0,05) pada warna putih telur asin. Warna putih telur asin yang paling disukai berdasarkan uji perbandingan berganda adalah warna putih telur perlakuan R, sedangkan yang paling kurang disukai adalah perlakuan R+O4 dan R+O6. Penilaian tersebut berhubungan dengan nilai mutu hedonik yang diberikan.
c c
warna pt warna kt aroma tekstur pt tekstur kt rasa pt rasa kt
M
1. Huruf yang berbeda pada setiap atribut sensorik menunjukkan berbeda nyata (P<0,05) 2. Nilai mutu hedonik dan deskripsinya
38 Nilai rata-rata mutu hedonik dari masing-masing perlakuan telur asin yaitu 1,00 ± 0,00 untuk perlakuan R, 2,13 ± 0,35 untuk perlakuan R+O4, dan 3,13 ± 0,63 untuk perlakuan R+O6. Warna putih telur dari ketiga perlakuan tersebut dapat dilihat pada Gambar 12.
Gambar 12. Warna Putih Telur Asin dengan Perlakuan Rebus (R), Rebus dan Oven 4 Jam (R+O4), serta Rebus dan Oven 6 Jam (R+O6)
Hasil uji Kruskal Wallis menunjukkan bahwa lama pengovenan berpengaruh (P<0,05) terhadap warna putih telur asin. Hasil uji banding rataan ranking menunjukkan bahwa warna putih telur R berbeda dengan R+O4 dan R+O6, dengan deskripsi mutu hedonik masing-masing perlakuan yaitu putih (R), putih kekuningan (R+O4), dan kuning kecoklatan (R+O6). Perbedaan tersebut disebabkan oleh kecepatan reaksi Maillard yang bervariasi pada masing-masing perlakuan. Reaksi Maillard pada perlakuan R berlangsung lebih lambat dan diduga berada pada tahap awal, sehingga warna putih telur belum berubah. Muchtadi (1989) menjelaskan bahwa senyawa Amadori yang terbentuk dari reaksi awal Maillard merupakan bentuk utama lisin terikat dalam makanan yang masih belum mengubah warna makanan tersebut.
Reaksi Maillard pada produk makanan menurut Simpson (2012) dan Man (1999) dapat terjadi karena adanya reaksi antara gula pereduksi dan protein yang didukung oleh faktor lingkungan seperti suhu, aktivitas air, pH dan komposisi kimia dari produk makanan tersebut. Reaksi Maillard dapat berlangsung lebih lambat dalam proses perebusan karena terjadi penyerapan air rebusan melalui pori-pori kerabang telur, sehingga air tersebut akan melarutkan protein dan gula-gula pereduksi yang berperan sebagai reaktan dalam reaksi Maillard. Pernyataan tersebut didukung oleh Fellow (2000) yang menyebutkan bahwa semakin tinggi kadar air
39 bahan makanan maka laju reaksi Maillard semakin turun karena kadar air yang tinggi mampu melarutkan zat-zat yang akan bereaksi dalam reaksi Maillard. Man (1999) menambahkan bahwa reaksi Maillard akan cepat terjadi dengan semakin meningkatnya aw dan mencapai laju maksimum pada aw 0,6 hingga 0,7. Lewat rentang tersebut laju reaksi akan mengalami penurunan kembali.
Pengovenan yang lebih lama menyebabkan perubahan warna putih telur lebih jelas terlihat. Hal ini disebabkan oleh adanya pengurangan kadar air yang lebih besar, sehingga zat-zat yang akan bereaksi dalam reaksi Maillard lebih terkonsentrasi dan reaksi Maillard berlangsung lebih cepat. Intensitas warna kecoklatan yang dihasilkan dari reaksi Maillard tidak selalu sama pada setiap telur meskipun lama pengovenan yang dilakukan sama, karena setiap telur memiliki ketebalan dan jumlah pori-pori kerabang yang berbeda sehingga kecepatan panas dari proses pengovenan yang diterima oleh bagian putih telur juga berbeda.
Reaksi Maillard yang terjadi pada produk makanan dapat menjadi suatu hal yang diinginkan atau sebaliknya tergantung aspek yang dilihat (Man, 1999). Warna putih telur yang paling disukai panelis adalah perlakuan R karena warnanya masih putih, oleh sebab itu reaksi Maillard tidak diharapkan terjadi pada telur asin jika dilihat dari aspek warna putih telur.
Warna Kuning Telur. Nilai rata-rata warna kuning telur dari uji ranking hedonik yaitu 1,20 ± 0,41 (R), 2,07 ± 0,70 (R+O4), dan 2,73 ± 0,46 (R+O6). Hasil uji Friedman menunjukkan bahwa terdapat perbedaan yang nyata (P<0,05) pada warna kuning telur. Warna kuning telur perlakuan R paling disukai sedangkan perlakuan R+O6 paling kurang disukai (Gambar 10). Penilaian tersebut berhubungan dengan mutu hedonik yang diberikan.
40 Maillard, akibatnya warna kuning telur menjadi kecoklatan. Trilaksami et al. (2004) menyebutkan bahwa kecerahan dari suatu produk makanan akan berkurang dengan semakin tingginya suhu dan lama pengovenan.
Sama halnya dengan warna putih telur, reaksi Maillard juga tidak diharapkan terjadi pada telur asin jika dilihat dari aspek warna kuning telur, karena panelis paling menyukai warna kuning telur yang cerah (perlakuan R). Pernyataan ini didukung oleh Soekarto (1985) bahwa warna cerah atau mencolok dari suatu bahan makanan dapat memberi kesan yang menarik sehinggga lebih disukai oleh konsumen.
Gambar 13. Warna Kuning Telur Asin dengan Perlakuan Rebus (R), Rebus dan Oven 4 Jam (R+O4), serta Rebus dan Oven 6 Jam (R+O6)
Aroma. Aroma atau bau dapat timbul karena adanya reseptor khas dalam sel olfaktori yang akan menangkap molekul senyawa bau dengan bentuk dan ukuran yang sesuai sehingga timbul impuls yang menyatakan mutu bau tersebut (Winarno, 2008). Nilai rata-rata ranking hedonik untuk aroma telur asin yaitu 3,00 ± 0,00 (R), 1,73 ± 0,46 (R+O4), dan 1,27 ± 0,46 (R+O6).
Hasil uji Friedman menunjukkan bahwa terdapat perbedaan yang nyata (P<0,05) pada aroma telur asin. Aroma telur asin yang mengalami pengovenan (R+O4 dan R+O6) paling disukai daripada yang hanya mengalami perebusan (R). Hal ini dapat terjadi karena timbulnya aroma khas pada telur asin yang dioven. Smith dan Hui (2004) menyatakan bahwa reaksi Maillard akan menimbulkan citarasa, warna dan aroma yang khas pada produk hasil pemanggangan. Fellow (2000) menambahkan, aroma yang terbentuk selama pemanggangan tergantung dari kombinasi lemak, asam amino, gula yang ada pada bahan makanan, suhu dan kadar air bahan, serta lama waktu pemanasan.
41 Nilai rata-rata dari uji mutu hedonik terhadap aroma telur asin adalah 3,27 ± 0,80 (R), 2,27 ± 0,88 (R+O4), dan 2,07 ± 0,88 (R+O6). Hasil uji Kruskal Wallis menunjukkan bahwa lama pengovenan berpengaruh (P<0,05) terhadap aroma telur asin. Hasil uji banding rataan ranking menunjukkan bahwa aroma telur asin perlakuan R berbeda dengan perlakuan R+O4 dan R+O6, sedangkan perlakuan R+O4 memiliki mutu hedonik yang sama dengan R+O6. Deskripsi mutu hedonik masing-masing perlakuan yaitu kurang amis (R) dan tidak amis (R+O4 dan R+O6).
Aroma yang timbul pada telur asin yang direbus (R) berasal dari senyawa sulfur, hal ini sesuai dengan pernyataan Stadelman dan Cotterill (1995) bahwa aroma utama pada telur yang dimasak adalah sulfur, sedangkan aroma khas pada telur asin yang mengalami pengovenan (R+O4 dan R+O6) berasal dari senyawa pirazin (Warren et al., 1995). Berbeda dengan warna putih dan kuning telur, reaksi Maillard diharapkan terjadi pada telur asin jika dilihat dari aspek aroma, sebab aroma telur menjadi tidak amis dan beraroma khas pemanggangan.
Tekstur Putih Telur. Tekstur menurut Fellow (2000) paling banyak ditentukan oleh kadar air, lemak, tipe dan jumlah karbohidrat, serta protein yang terdapat pada bahan makanan. Tekstur suatu bahan makanan menurut Lawless dan Heymann (1998) digunakan oleh konsumen sebagai indikator dari kualitas makanan (food quality) dan dapat diketahui melalui indra penglihatan, sentuhan, serta pendengaran. Nilai rata-rata tekstur putih telur yang diperoleh dari uji ranking hedonik (Gambar 10) yaitu 1,67 ± 0,82 (R), 1,87 ± 0,74 (R+O4), dan 2,47 ± 0,74 (R+O6). Hasil uji Friedman menunjukkan bahwa tidak terdapat perbedaan yang nyata pada tekstur putih telur, artinya tidak ada tekstur putih telur yang paling disukai maupun yang paling kurang disukai.
42 Tekstur Kuning Telur. Nilai rata-rata tekstur kuning telur dari uji ranking hedonik yaitu 2,33 ± 0,82 (R), 2,27 ± 0,59 (R+O4), dan 1,27 ± 0,46 (R+O6). Hasil uji Friedman menunjukkan bahwa terdapat perbedaan yang nyata (P<0,05) pada tekstur kuning telur asin. Tekstur kuning telur yang paling disukai berdasarkan uji perbandingan berganda adalah perlakuan R+O6. Penilaian tersebut berhubungan dengan nilai mutu hedonik yang diberikan.
Nilai rata-rata mutu hedonik pada tekstur kuning telur yakni 3,00 ± 0,85 (R), 3,53 ± 0,52 (R+O4), dan 4,13 ± 0,74 (R+O6). Hasil uji Kruskal Wallis menunjukkan bahwa lama pengovenan berpengaruh (P<0,05) pada tekstur kuning telur. Melalui uji banding rataan ranking diperoleh bahwa tekstur kuning telur R berbeda dengan R+O6, sedangkan tekstur kuning telur R+O4 tidak dapat dibedakan dengan R dan R+O6. Deskripsi mutu hedonik masing-masing perlakuan yaitu kurang masir (R), kurang masir hingga masir (R+O4), dan masir (R+O6). Tekstur kuning telur perlakuan R+O6 lebih masir dari perlakuan R, karena waktu pengovenan yang lebih lama menyebabkan denaturasi protein dan penguapan air dari kuning telur lebih besar terjadi. Protein kuning telur yang berikatan dengan lemak (lipoprotein) telah terdenaturasi akibat penambahan NaCl sebelum dilakukan pemasakan, akibatnya protein akan terlepas dari lemaknya dan saling menyatu. Waktu pengovenan yang lebih lama semakin membantu penggabungan protein tersebut sehingga ukuran granula polihedral semakin besar dan dengan semakin banyaknya air yang diuapkan menyebabkan pemadatan granula dalam kuning telur semakin kuat dan batas antar granula semakin jelas terlihat. Hal tersebut menyebabkan tekstur kuning telur R+O6 lebih masir.