SISTEM PENGOLAHAN AIR YANG BERBEDA PADA
PEMBENIHAN GURAMI DENGAN MEDIA BERSALINITAS
3 PPT DAN FITOREMEDIATOR
Lemna perpusilla
ALEXANDER BURHANI MARDA
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa tesis berjudul Sistem Pengolahan Air yang Berbeda pada Pembenihan Gurami dengan Media Bersalinitas 3 ppt dan Fitoremediator Lemna perpusilla adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Agustus 2015
Alexander Burhani Marda
RINGKASAN
ALEXANDER BURHANI MARDA. Sistem Pengolahan Air yang Berbeda pada Pembenihan Gurami dengan Media Bersalinitas 3 ppt dan Fitoremediator Lemna perpusilla. Dibimbing oleh KUKUH NIRMALA, ENANG HARRIS DAN EDDY SUPRIYONO
Salah satu penyebab terbesar penurunan kualitas air dalam kegiatan budidaya adalah sisa pakan yang tidak termakan, feses dan buangan organik dari ikan. Sisa pakan dan feses yang terbuang ke perairan merupakan potensi cemaran organik berupa N dan P yang dapat mempengaruhi tingkat kesuburan dan kelayakan kualitas air bagi ikan budidaya.
Beberapa cara telah dilakukan untuk memperbaiki kualitas air diantaranya dengan menggunakan filtrasi, penambahan aerasi dan menggunakan media tanaman atau yang biasa dikenal fitoremediasi. Filtrasi merupakan suatu teknologi untuk menahan maupun menyaring partikel-partikel fisik pada air. Penambahan aerasi merupakan salah satu cara untuk meningkatkan kelarutan oksigen sehingga dapat mereduksi dan mendukung perubahan ammonia dan nitrit di perairan. Penambahan tanaman merupakan salah satu cara untuk mengurangi kandungan limbah anorganik yang dapat memutus perubahan reaksi kimia dari ammonia menjadi nitrit. Penelitian ini bertujuan menganalisis kemampuan L. perpusilla
dalam menyerap unsur hara limbah nitrogen dan fosfat pada sistem pengolahan air yang berbeda, serta menganalisis derajat kelangsungan hidup (DKH), laju pertumbuhan harian (LPH).
Penelitian ini menggunakan 12 akuarium dengan ukuran 50 cm x 33 cm x 50 cm. Ikan ditebar dengan kepadatan 150 ekor/49.5 L dan dipelihara selama 30 hari. Rancangan percobaan yang dilakukan adalah Rancangan Acak Lengkap (RAL) dengan 3 kali ulangan. Perlakuan terdiri atas: A (L. perpusilladan salinitas 3 ppt), B (L. perpusilla, salinitas 3 ppt dan filter), C (L. perpusilla, salinitas 3 ppt dan aerasi) dan D (L. perpusilla, salinitas 3 ppt, aerasi dan filter).
Hasil penelitian setelah dilakukan pengujian secara statistik menunjukkan bahwa pengurangan limbah organik N oleh L. perpusilla tidak berbeda nyata disetiap perlakuan pada H 30 (0.07 g N - 0.11 g N) yang merupakan hari terakhir penelitian. Begitu juga dengan nilai P pada akhir pemeliharan menunjukkan tidak berbeda nyata disetiap perlakuan (0.00 g P - 0.01 g P). Derajat kelangsungan hidup ikan gurami tertinggi pada perlakuan C (L. perpusilla, salinitas 3 ppt dan aerasi) yaitu 95.0% dan terendah pada perlakuan A (L. perpusilla dan salinitas) yaitu 40.0%. Laju pertumbuhan harian ikan gurami selama masa pemeliharaan tidak berbeda nyata. Hal ini karena media yang digunakan diberikan salinitas hingga 3 ppt.
Berdasarkan penelitian ini didapatkan bahwa penambahan salinitas 3 ppt,L. perpusilla, aerasi dan filter pada media pemeliharaan dapat menyerap limbah organik N dan P serta dapat digunakan untuk sistem pengolahan air akuakultur. Sehingga mampu menurunkan kandungan limbah organik, meningkatkan laju pertumbuhan harian dan derajat kelangsungan hidup.
SUMMARY
ALEXANDER BURHANI MARDA. Water Management System in Different Gouramy Hatcheries using 3 ppt Salinity Media and Phytoremediator Lemna perpusilla. Supervised by KUKUH NIRMALA, ENANG HARRIS and EDDY SUPRIYONO
Some of the biggest causes of water quality degradation in aquaculture activities are unconsumed feed, feces and organic effluent. Unconsumed feed and feces discharged into coastal water can be considered as potential organic contamination source in the form N and P that can affect the level of fertility and the feasibility of water quality for fish farming.
Several methods have been used to improve water quality such as filtration, media addition of aeration and use of plant or commonly known as phytoremediation. Filtration is a technology to withstand physical or particle filter in the water. The addition of aeration is one way to increase the solubility of oxygen in order to reduce and support changes in ammonia and nitrite in the water. The addition of plants is another way to reduce the amount of organic waste that can hamper the chemical reaction of ammonia to nitrite. This study aims to analyze the ability of L. perpusilla to absorb nutrients nitrogen and phosphates in different waste water treatment systems and also to analyze the survival and growth.
This study uses 12 aquariums with a size of 50 cm x 33 cm x 50 cm. Fish stocked at a density of 150 fish / 49.5 L and maintained for 30 days. The experimental design was conducted completely randomized design (CRD) with three replications. The treatment consists of: A (L. perpusillaand 3 ppt salinity), B (L. perpusilla, 3 ppt salinity and filter), C (L. perpusilla, 3 ppt salinity and aeration) and D (L. perpusilla, 3 ppt salinity , aeration and filter).
Results of the study after statistical testing showed that the reduction of organic waste N byL. perpusillanot significantly different from each treatment at H 30 (0.07 g N– 0.11 g N) which is the last day of the study. So is the value of P at the end of maintenance showed no significant difference in each treatment (0.00 g P - 0:01 g P). The degree of survival of carp highest in treatment C (L. perpusilla, 3 ppt salinity and aeration) is 95.0% and the lowest in treatment A (L. perpusilla
and salinity) is 40.0%. Carp daily growth rate during the maintenance period are not significantly different. This is because the medium used is given up to 3 ppt salinity.
Based on this study it was found that the addition of 3 ppt salinity, L. perpusilla, aeration and filter media maintenance can absorb organic wastes N and P, and can be used for aquaculture water treatment systems. So as to reduce the content of organic waste, increase the daily growth rate and degree of viability.
© Hak Cipta Milik IPB. Tahun 2015
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan,
penelitian, penulisan karya ilmiah, penyusunan laporanp penulisan kritik, atau tinjauan suatu masalah;danpengutipan tersebut tidak merugikan kepentingan IPB
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Ilmu Akuakultur
SISTEM PENGOLAHAN AIR YANG BERBEDA PADA
PEMBENIHAN GURAMI DENGAN MEDIA BERSALINITAS
3 PPT DAN FITOREMEDIATOR
Lemna perpusilla
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2015
Judul Tesis : Sistem Pengolahan Air yang Berbeda pada Pembenihan Gurami dengan Media Bersalinitas 3 ppt dan Fitoremediator Lemna perpusilla
Nama : Alexander Burhani Marda
NIM : C151114061
Disetujui oleh
Komisi Pembimbing
Dr Ir Kukuh Nirmala, MSc Ketua
Prof Dr Ir Enang Harris, MS Anggota
Dr Ir Eddy Supriyono, MSc Anggota
Diketahui oleh
Ketua Program Studi Ilmu Akuakultur
Dr Ir Widanarni, MSi
Dekan Sekolah Pascasarjana
Dr Ir Dahrul Syah, MSc Agr
PRAKATA
Segala puji bagi Allah SWT yang telah memberikan rahmat dan hidayah-Nya. sehingga karya ilmiah ini dapat terselesaikan. Tema yang dipilih dalam penelitian ini adalah Sistem Pengolahan Air yang Berbeda pada Pembenihan Gurami dengan Media Bersalinitas 3 ppt dan FitoremediatorLemna perpusilla.
Penulis menyampaikan terima kasih kepada Bapak Dr Ir Kukuh Nirmala, MSc, Bapak Prof Dr Ir Enang Harris, MS dan Bapak Dr Ir Eddy Supriyono, MSc atas bimbingan dan motivasi yang telah diberikan, serta Ibu Dr Ir Dinar Tri Soelistyowati, DEA yang telah banyak memberi saran. Di samping itu penghargaan dan terima kasih juga penulis sampaikan kepada keluarga dan rekan akuakultur atas segala doa dan bantuannya.
Akhir kata penyusun berharap semoga karya ilmiah ini dapat bermanfaat bagi semua pihak yang membutuhkan.
Bogor, Agustus 2015
DAFTAR ISI
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 2
Tujuan Penelitian 3
Manfaat Penelitian 4
METODE 4
Tempat dan Waktu Penelitian 4
Persiapan Wadah dan Media Pemeliharaan 4
Hewan Uji 4
Tanaman Uji 5
Filter dan Aerasi 5
Prosedur Penelitian 5
Parameter Uji 6
Analisis Data 7
HASIL DAN PEMBAHASAN 7
Hasil 7
Pembahasan 14
SIMPULAN DAN SARAN 18
Simpulan 18
Saran 18
DAFTAR PUSTAKA 19
LAMPIRAN 22
DAFTAR GAMBAR
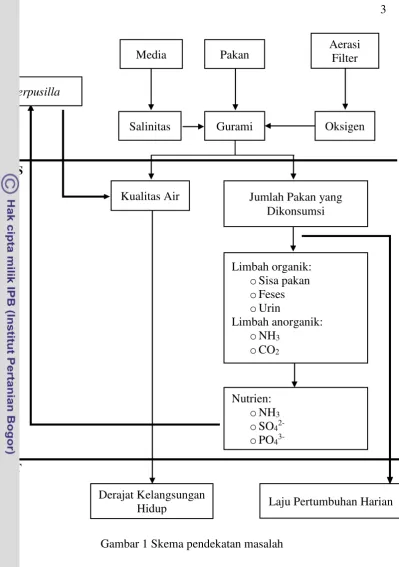
1 Skema pendekatan masalah 3
2 Presentase derajat kelangsungan hidup (DKH) ikan gurami pada media
pemeliharaan selama 30 hari 8
3 Laju pertumbuhan harian (LPH) ikan gurami pada media pemeliharaan
selama 30 hari. 8
4 Efisiensi pemberian pakan (EPP) pada media pemeliharaan selama 30 hari. 9
5 Ammonia pada media pemeliharaan selama 30 hari. 9
6 Nitrit pada media pemeliharaan selama 30 hari. 10
7. Nitrat pada media pemeliharaan selama 30 hari. 10
8. Total suspended solid(TSS) pada media pemeliharaan selama 30 hari. 11 9. Dissolved oxygen(DO) pada media pemeliharaan selama 30 hari. 11 10.Biological oxygen demand(BOD) pada media pemeliharaan selama 30 hari.12 11.Total organic matter(TOM) pada media pemeliharaan selama 30 hari. 12
12. pH pada media pemeliharaan selama 30 hari. 13
13. Kandungan nitrogen padaL. perpusillaselama 30 hari. 13
14. Kandungan fosfor padaL. perpusillaselama 30 hari. 14
DAFTAR LAMPIRAN
1. Desain akuarium penelitian selama 30 hari masa penelitian 22
2. Output tabel ANOVA analisis ragam DKH pada media pemeliharaan selama
30 hari dengan menggunakan SPSS 18.0. 22
3. Output tabel uji lanjut Duncan DKH pada media pemeliharaan selama 30
hariL. perpusilladengan SPSS 18.0. 22
4. Output tabel ANOVA analisis ragam LPH pada media pemeliharaan selama
30 hari dengan menggunakan SPSS 18.0. 22
5. Output tabel uji lanjut Duncan LPH pada media pemeliharaan selama 30 hari
L. perpusilladengan SPSS 18.0. 22
6. Output tabel ANOVA analisis ragam EPP pada media pemeliharaan selama
30 hari dengan menggunakan SPSS 18.0. 23
7. Output tabel uji lanjut Duncan EPP pada media pemeliharaan selama 30 hari
L. perpusilladengan SPSS 18.0. 23
8. Output tabel ANOVA analisis ragam ammonia pada media pemeliharaan
selama 30 hari dengan menggunakan SPSS 18.0. 22
9. Output tabel uji lanjut Duncan ammonia pada media pemeliharaan selama
30 hariL. perpusilladengan SPSS 18.0. 24
10. Output tabel ANOVA analisis ragam nitrit pada media pemeliharaan selama
30 hari dengan menggunakan SPSS 18.0. 24
11. Output tabel uji lanjut Duncan nitrit pada media pemeliharaan selama 30
hariL. perpusilladengan SPSS 18.0. 24
12. Output tabel ANOVA analisis ragam nitrat pada media pemeliharaan
selama 30 hari dengan menggunakan SPSS 18.0. 24
13. Output tabel uji lanjut Duncan nitrat pada media pemeliharaan selama 30
14. Output tabel ANOVA analisis ragam DO pada media pemeliharaan selama
30 hari dengan menggunakan SPSS 18.0. 25
15. Output tabel uji lanjut Duncan DO pada media pemeliharaan selama 30 hari
L. perpusilladengan SPSS 18.0. 25
16. Output tabel ANOVA analisis ragam BOD pada media pemeliharaan
selama 30 hari dengan menggunakan SPSS 18.0. 25
17. Output tabel uji lanjut Duncan BOD pada media pemeliharaan selama 30
hariL. perpusilladengan SPSS 18.0. 26
18. Output tabel ANOVA analisis ragam TOM pada media pemeliharaan
selama 30 hari dengan menggunakan SPSS 18.0. 26
19. Output tabel uji lanjut Duncan TOM pada media pemeliharaan selama 30
hariL. perpusilladengan SPSS 18.0. 26
20. Output tabel ANOVA analisis ragam pH pada media pemeliharaan selama
30 hari dengan menggunakan SPSS 18.0. 26
21. Output tabel uji lanjut Duncan pH pada media pemeliharaan selama 30 hari
L. perpusilladengan SPSS 18.0. 27
22. Output tabel ANOVA analisis ragam N yang diserap oleh L. perpusilla
dengan menggunakan SPSS 18.0. 27
23. Output tabel uji lanjut Duncan pengaruh penambahan filter dan aerasi pada media 3 ppt terhadap parameter jumlah N yang diserapL. perpusilladengan
SPSS 18.0. 27
24. Output tabel ANOVA analisis ragam P yang diserap oleh L. perpusilla
dengan menggunakan SPSS 18.0. 28
25. Output tabel uji lanjut Duncan pengaruh penambahan filter dan aerasi pada media 3 ppt terhadap parameter jumlah P yang diserapL. perpusilladengan
1 PENDAHULUAN
Latar Belakang
Kualitas air merupakan salah satu faktor yang paling berpengaruh dalam kegiatan budidaya ikan. Pengaruh kualitas air terbesar terdapat pada budidaya air tawar, namun perairan air tawar saat ini mengalami penurunan. Salah satu penyebab terbesar penurunan kualitas air dalam kegiatan budidaya adalah sisa pakan yang tidak termakan, feses dan buangan organik dari ikan. Sisa pakan dan feses yang terbuang keperairan merupakan potensi cemaran organik berupa N dan P yang dapat mempengaruhi tingkat kesuburan dan kelayakan kualitas air bagi kehidupan ikan budidaya. Beban limbah organik N dan P yang dari sistem budidaya menjadi salah satu aspek penting dalam kegiatan budidaya (Yosmaniar 2010). Salah satu perairan Indonesia yang terlah mengalami penurunan kualiatas air adalah waduk cirata. Menurut Komarawidjajaet al. (2005) perairan pada waduk cirata mengalami peningkatan nitrogen (N) >500 mg L-1dan pospor (P) >20. Nilai tersebut melebihi dari baku mutu kualitas air. Baku mutu kualitas air untuk budidaya air tawar memiliki nilai N 10, P 0.2 yang termasuk dalam kelas dua dan N 20, P 1 untuk kelas tiga (Peraturan Pemerintah 2001).
Beberapa cara telah dilakukan untuk memperbaiki kualitas air diantaranya dengan menggunakan filtrasi, penambahan aerasi dan menggunakan media tanaman atau yang biasa dikenal fitoremidiasi. Filtrasi merupakan suatu teknologi untuk menahan maupun menyaring partikel-partikel fisik pada air. Salah satu cara filtrasi yang telah digunakan adalah slow sand filter pada tambak ikan bandeng (Febriwahyudi dan Hadi 2011) menggunakan media pasir. Namun penggunaan filter ini hanya bersifat fisik tidak bisa menyaring secara kimiawi. Selain itu juga filtrasi dapat menggunakan biota air seperti kijing (Molleda 2007) dan tanaman air. Penambahan aerasi merupakan salah satu cara untuk meningkatkan kelarutan oksigen sehingga dapat mereduksi dan mendukung perubahan ammonia dan nitrit di perairan. Kebutuhan akan oksigen pada setiap proses tersebut berbeda, untuk merubah ammonia menjadi nitrit membutuhkan oksigen sebesar 1.5 mg L-1. dan
untuk merubah nitrit menjadi nitrat membutuhkan oksigen sebesar 0.5 mg L-1. Apabila hanya menggunakan aerasi saja maka kebutuhan oksigen tidak cukup, oleh karena itu perlu penambahan oksigen lain salah satunya dengan menggunakan agen fitoremediasi.
Fitoremediasi adalah penggunaan tanaman dan bagian-bagiannya untuk dekontaminasi limbah dan masalah-masalah pencemaran lingkungan baik secara
ex-situmenggunakan kolam buatan atauin-situ(langsung di lapangan) pada tanah atau daerah yang terkontaminasi limbah (Subroto 1996). Fitoremediasi dapat menggunakan tanaman air seperti Lemna(Chenget al. 2002; Ozengin dan Elmaci 2007; Ferdoushiet al. 2008; Amalia 2014), kayu apu (Hermawatiet al. 2005; Indah
et al. 2014), Hydrilla verticilata (Sumiyati et al. 2009) dan eceng gondok (Hardyanti dan Suparni 2007; Indahet al. 2014). Diantara tanaman yang prospektif untuk digunakan sebagai agen fitoremediasi limbah organik untuk perairan adalah
Lemna perpusilla.
2
menyerap nitrogen sebesar 3.36 g m2-1hari-1dan fosfor sebesar 0.20 g m2-1hari-1di
perairan (Cheng et al. 2002), menghilangkan total COD sebesar 73-84%, total nitrogen sebesar 83-87% dan total fosfor sebesar 70-85% (Ozengin dan Elmaci 2007). KapasitasL. perpusillasebanyak 44.1% dapat mereduksi nitrogen dan fosfat (Amalia 2014). Dari banyak jenis Lemna, yang paling mendominasi di daerah perairan Indonesia adalahL. perpusilla.L. perpusillamemiliki kemampuan untuk menangani perairan secara biologis, tetapi belum banyak diketahui oleh para pembudidaya. Pembudidaya ikan hanya menganggapL. perpusilla sebagai pakan tambahan yang dapat diberikan pada ikan terutama ikan herbivora bukan sebagai agen fitoremediator yang dapat menangani limbah perairan.
Ikan gurami (Osphronemus gourami) merupakan salah satu ikan yang memiliki nilai ekonomis penting. Ikan gurami memiliki harga yang cukup menjanjikan sebagai ikan konsumsi masyarakat. Namun, dalam kegiatan budidaya ikan gurami memiliki laju pertumbuhan yang relatif lama dibandingkan dengan ikan air tawar lainnya. Salah satu cara untuk mempercepat laju pertumbuhan ikan gurami adalah dengan meningkatkan salinitas pemeliharaan ikan gurami (Dewi 2006; Rasmawan 2009; Nirmala dan Rasmawan. 2010).
Perubahan salinitas berdampak pada laju pertumbuhan ikan, serta fungsi fisiologis ikan. Ikan akan mempertahankan isoosmotiknya dengan cara osmoregulasi yang merupakan upaya ikan untuk mengontrol keseimbangan air dan ion antara tubuh dengan lingkungannya atau suatu proses pengaturan tekanan osmose (Fujaya 2004) sehingga proses fisiologis tubuh berjalan secara normal. Pemeliharaan ikan gurami dengan salinitas 3 ppt menghasilkan laju pertumbuhan dan tingkat kelangsungan hidup lebih tinggi dibandingkan dengan air yang tidak bersalinitas (Rasmawan 2009; Nirmalaet al. 2010).
Pengolahan sistem air yang berbeda dengan menambahkan filter dan aerasi serta adanya tanaman berupaL. perpusilladapat mengurangi limbah organik berupa N dan P, sehingga derajat kelangsungan hidup (DKH) dan laju pertumbuhan harian (LPH) ikan gurami meningkat.
Perumusan Masalah
Sisa pakan sertaurinedanfecesyang terbuang ke perairan merupakan sumber potensi cemaran organik berupa nitrogen (N) dan fosfor (P) yang dapat mempengaruhi tingkat kesuburan dan kelayakan kualitas air bagi kehidupan ikan budidaya. Pakan yang diberikan selama masa budidaya juga berpotensi mengurangi kualitas perairan.
3
Tujuan Penelitian
Tujuan dari penelitian ini adalah sebagai berikut:
1. Menganalisis kemampuan L. perpusilla dalam menyerap unsur hara limbah organik pada media bersalinitas 3 ppt.
2. Menganalisis derajat kelangsungan hidup (DKH), laju pertumbuhan harian (LPH) ikan gurami.
Gambar 1 Skema pendekatan masalah
L. perpusilla
Pakan Media
Gurami Oksigen
Laju Pertumbuhan Harian Nutrien:
oNH3 oSO4 2-oPO4 3-Salinitas
Limbah organik: oSisa pakan
oFeses oUrin
Limbah anorganik: oNH3
oCO2
Jumlah Pakan yang Dikonsumsi Kualitas Air
Derajat Kelangsungan Hidup
Aerasi Filter
INPUT
PROSES
4
Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi mengenai kemampuan Lemna perpusilla, aerasi dan filter bagi perairan budidaya dalam pengurangan limbah organik pada sistem pengolahan air.
2 METODE
Tempat dan Waktu Penelitian
Penelitian dilaksanakan pada bulan November hingga Desember 2014 di Laboratorium Lingkungan Akuakultur 3, Departemen Budidaya Perairan. Institut Pertanian Bogor. Analisis nitrogen dan fosfor dilakukan di Laboratorium Nutrisi Ikan Departemen Budidaya Perairan Institut Pertanian Bogor. Uji kualitas air dilakukan di Laboratorium Lingkungan Departemen Budidaya Perairan, Institut Pertanian Bogor.
Persiapan Wadah dan Media Pemeliharaan
Wadah yang digunakan dalam penelitian berupa akuarium yang berukuran 50 cm x 33 cm x 50 cm sebanyak 15 buah. Akuarium terlebih dahulu dicuci dengan deterjen dan dikeringkan. Selanjutnya akuarium didesinfeksi dengan klorin 30 ppm selama 24 jam, kemudian dibersihkan kembali. Akuarium yang telah didesinfeksi diisi dengan air tawar sebanyak 49.5 L pada 3 akuarium dan air dengan bersalinitas 3 ppt pada 12 akuarium. Media pemeliharaan ikan gurami menggunakan air bersalinitas 0 ppt dan 3 ppt yang berasal dari proses penambahan garam grosok dengan perbandingan 1:1 antara garam (g) dengan air (L). Air berasal dari Laboratorium Lingkungan 3 Akuakultur yang terlebih dahulu ditampung dalam tandon dan diendapkan. Air untuk tandon 3 ppt diisi sebanyak 135.83 L, kemudian ditambahkan garam grosok hingga mencapai 3 ppt sebanyak 407.49 g.
Hewan Uji
5
Tanaman Uji
Tanaman yang digunakan dalam penelitian ini adalah Lemna perpusilla
yang berasal dari Lembaga Ilmu Pengetahuan (LIPI) Cibinong. Kepadatan L. perpusilla pada media pemeliharan selama masa penelitian adalah 30% dari luas media pemeliharaan ikan.L. perpusillaterlebih dahulu dibudidaya untuk mencapai biomassa yang diinginkan dalam penelitian. Pupuk yang digunakan pada media budidaya berasal dari pembakaran sekam padi yang diaduk dengan kotoran ayam. Pemberian pupuk hanya sekali dengan ketinggian air yang digunakan adalah 20 cm.
Filter dan Aerasi
Filter yang digunakan adalah filter dengan menggunakan kapas filter sebagai media penyaringannya. Penggunaan kapas filter diharapkan dapat mengurangi kekeruhan air dan kandungan N dan P pada media penelitian. Penggunaan aerasi hanya satu titik untuk beberapa media penelitian, sedangkan beberapa diantaranya lagi tidak ada penambahan aerasi (Lampiran 1).
Prosedur Penelitian
Ikan yang didatangkan terlebih dahulu di aklimatisasi di dalam akuarium kaca berukuran 50 x 33 x 30 cm yang dilengkapi dengan aerasi filter selama 7 hari. Setelah itu beberapa ikan dipindahkan ke akuarium stok lainnya untuk proses aklimatisasi. Aklimatisasi menggunakan air bersalinitas secara bertahap hingga 3 ppt. Proses penambahan salinitas menggunakan garam grosok dengan perbandingan 1:1. Salinitas ditingkatkan perhari hingga mencapai 3 ppt pada hari ke-3. Selama proses aklimatisasi tersebut, ikan diberi pakan secara at satiation
sebanyak dua kali sehari. Setelah itu ikan dipindahkan ke wadah penelitian yang akan digunakan.
Penelitian ini menggunakan rancangan acak lengkap (RAL) yang terdiri atas 5 perlakuan dengan 3 ulangan. Adapun perlakuan yang digunakan adalah sebagai berikut.
Perlakuan A :L. perpusilladan salinitas 3 ppt. Perlakuan B :L. perpusilla, salinitas 3 ppt dan filter. Perlakuan C :L. perpusilla, salinitas 3 ppt dan aerasi. Perlakuan D :L. perpusilla, salinitas 3 ppt, aerasi dan filter.
Pakan yang digunakan adalah pakan komersil. Pemberian pakan dilakukan sebanyak dua kali sehari yaitu pada pukul 07:00 WIB dan pukul 16:00 WIB secara
6
Parameter Uji
1. Jumlah Nitrogen dan Fosfor dalam BiomassaLemna perpusilla
Pengukuran nitrogen dan fosfor pada biomassa L. perpusilla
dilakukan setiap 10 hari sekali, dengan cara sebagai berikut: 1. Menimbang biomassaL. perpusilla.
2. Mengukur kadar nitrogen dan fosfat padaL. perpusilla.
3. Menghitung jumlah nitrogen dan fosfatL. perpusilladengan persamaan sebagai berikut:
Keterangan:
N dan PL. perpusilla = Jumlah nitrogen dan fosfor dalam biomassa L. perpusilla(g)
N dan P = Kadar nitrogen dan fosfor dalamL. perpusilla(%)
BiomassaL. perpusilla = BiomassaL. perpusillasetiap 10 hari (g)
2. Derajat Kelangsungan Hidup (%)
Derajat kelangsungan hidup dihitung berdasarkan persamaan berikut.
Keterangan:
DKH = Derajat kelangsungan hidup (%)
Nt = Jumlah ikan pada akhir penelitian (ekor)
No = Jumlah ikan pada awal penelitian (ekor)
3. Laju Pertumbuhan Harian
Laju pertumbuhan harian (LPH) dihitung dengan menggunakan rumus (Huisman 1987):
Keterangan:
LPH = Laju pertumbuhan harian (%)
Wo = Bobot rata-rata ikan pada awal pemeliharaan (gram) Wt = Bobot rata-rata ikan pada akhir pemeliharaan (gram) t = Periode pemeliharaan (hari)
DKH = Nt
No
x 100% 100
N dan PL. perpusilla=N dan P x biomassaL. perpusilla
Wt
Wo 1
7
4. Efisiensi Pemberian Pakan (EPP)
Efisiensi pemberian pakan dihitung berdasarkan persamaan Zonneveld et al. (1991).
Keterangan:
EPP = Efisiensi pemberian pakan (%) Pa = Jumlah pakan yang dikonsumsi (g) Bt = Bobot biomassa ikan pada hari ke-t (g) Bo = Bobot biomassa ikan pada awal tebar (g) Bm = Bobot biomassa ikan mati (g)
5. Analisis Kualitas Air
Analisis kualitas fisika dan kimia air meliputi suhu, pH, ammonia, nitrit, nitrat, biological oxygen demand (BOD), total organic matter (TOM), total suspended solid (TSS) dandissolved oxygen(DO). Pengukuran suhu, pH dan DO dilakukan setiap hari, sedangkan ammonia, nitrit, nitrat, BOD dan (TOM) diukur setiap 10 hari sekali selama masa pemeliharaan.
Analisis Data
Data yang diperoleh dari hasil penelitian ditabulasi dan dianalisis menggunakan program Microsoft Excel 2013 dan SPSS 18.0 yang meliputi Analisis Ragam (ANOVA) dan uji F pada selang kepercayaan 95%. Apabila berpengaruh nyata maka akan diuji lanjut dengan menggunakan uji Duncan. Selanjutnya data disajikan dalam bentuk tabel dan grafik.
3 HASIL DAN PEMBAHASAN
Hasil
Derajat Kelangsungan Hidup (DKH)
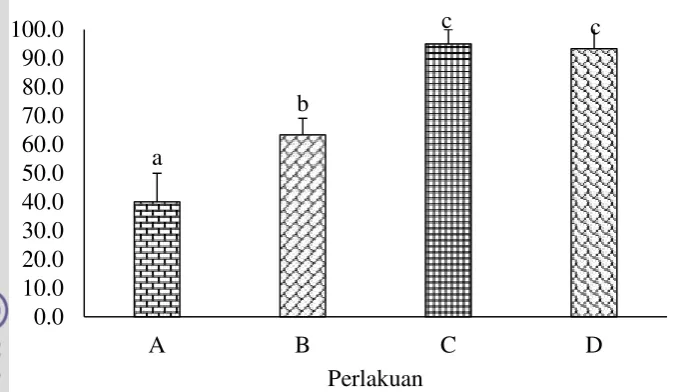
Hasil analisis ragam (ANOVA) menunjukkan bahwa faktor penambahanL. perpusilla, salinitas 3 ppt, aerasi dan filter memberikan pengaruh nyata terhadap nilai DKH. Hasil pengukuran nilai DKH pada media pemeliharaan dapat dilihat pada Gambar 2. Perolehan nilai DKH terendah ada pada perlakuan A yaitu 40.0±10.00%. Sementara itu, perolehan tertinggi ada pada perlakuan C dan D.
8
Ket: A (L. perpusilladan salinitas 3 ppt), B (L. perpusilla, salinitas 3 ppt dan filter), C (L. perpusilla, salinitas 3 ppt dan aerasi) dan D (L. perpusilla, salinitas 3 ppt, aerasi dan filter). Huruf yang berbeda menunjukkan hasil yang berbeda nyata (p<0.05)
Gambar 2 Presentase derajat kelangsungan hidup (DKH) ikan gurami pada media pemeliharaan selama 30 hari.
Laju Pertumbuhan Harian (LPH)
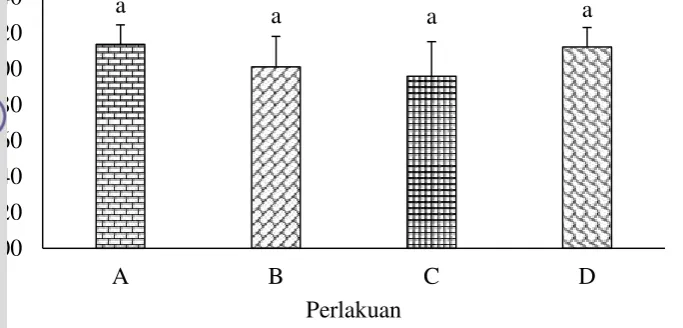
Hasil analisis ragam (ANOVA) menunjukkan bahwa faktor penambahanL. perpusilla, salinitas 3 ppt, aerasi dan filter memberikan pengaruh nyata terhadap nilai LPH. Hasil pengukuran nilai LPH pada media pemeliharaan dapat dilihat pada Gambar 3. Hasil uji statistik menyatakan bahwa, nilai LPH pada setiap perlakuan tidak berbeda nyata.
Ket: A (L. perpusilladan salinitas 3 ppt), B (L. perpusilla, salinitas 3 ppt dan filter), C (L. perpusilla, salinitas 3 ppt dan aerasi) dan D (L. perpusilla, salinitas 3 ppt, aerasi dan filter). Huruf yang berbeda menunjukkan hasil yang berbeda nyata (p<0.05)
9
Efisiensi Pemberian Pakan (EPP)
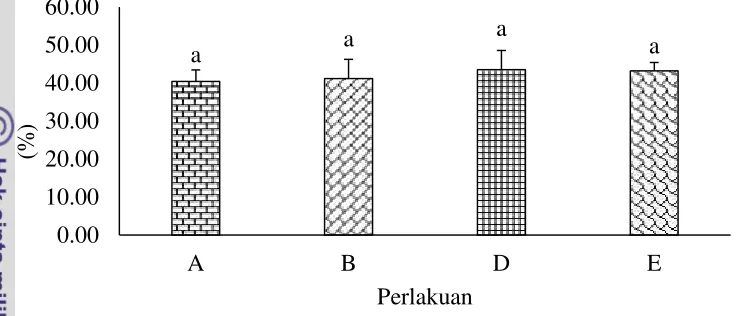
Hasil analisis ragam (ANOVA) menunjukkan bahwa faktor penambahanL. perpusilla, salinitas 3 ppt, aerasi dan filter memberikan pengaruh nyata terhadap efisiensi pemberian pakan. Hasil pengukuran efisiensi pakan pada media pemeliharaan dapat dilihat pada Gambar 4. Hasil uji statistik menyatakan bahwa, nilai EPP pada setiap perlakuan tidak berbeda nyata.
Ket: A (L. perpusilladan salinitas 3 ppt), B (L. perpusilla, salinitas 3 ppt dan filter), C (L. perpusilla, salinitas 3 ppt dan aerasi) dan D (L. perpusilla, salinitas 3 ppt, aerasi dan filter). Huruf yang berbeda menunjukkan hasil yang berbeda nyata (p<0.05)
Gambar 4 Efisiensi pemberian pakan (EPP) ikan gurami pada media pemeliharaan selama 30 hari.
Ammonia
Hasil analisis ragam (ANOVA) menunjukkan bahwa faktor penambahanL. perpusilla, salinitas 3 ppt, aerasi dan filter memberikan pengaruh nyata terhadap nilai ammonia. Hasil pengukuran nilai ammonia pada media pemeliharaan dapat dilihat pada Gambar 5. Perolehan nilai ammonia terendah ada pada perlakuan A dan C. Sementara itu, perolehan tertinggi ada pada perlakuan B dan D.
Ket: A (L. perpusilladan salinitas 3 ppt), B (L. perpusilla, salinitas 3 ppt dan filter), C (L. perpusilla, salinitas 3 ppt dan aerasi) dan D (L. perpusilla, salinitas 3 ppt, aerasi dan filter). Huruf yang berbeda menunjukkan hasil yang berbeda nyata (p<0.05)
Gambar 5 Ammonia pada media pemeliharaan selama 30 hari.
10
Nitrit
Hasil analisis ragam (ANOVA) menunjukkan bahwa faktor penambahanL. perpusilla, salinitas 3 ppt, aerasi dan filter memberikan pengaruh nyata terhadap nilai nitrit. Hasil pengukuran nilai nitrit pada media pemeliharaan dapat dilihat pada Gambar 6. Hasil uji statistik menyatakan bahwa, nilai EPP pada setiap perlakuan tidak berbeda nyata.
Ket: A (L. perpusilladan salinitas 3 ppt), B (L. perpusilla, salinitas 3 ppt dan filter), C (L. perpusilla, salinitas 3 ppt dan aerasi) dan D (L. perpusilla, salinitas 3 ppt, aerasi dan filter). Huruf yang berbeda menunjukkan hasil yang berbeda nyata (p<0.05)
Gambar 6 Nitrit pada media pemeliharaan selama 30 hari.
Nitrat
Hasil analisis ragam (ANOVA) menunjukkan bahwa faktor penambahanL. perpusilla, salinitas 3 ppt, aerasi dan filter memberikan pengaruh nyata terhadap nilai nitrat. Hasil pengukuran nilai nitrat pada media pemeliharaan dapat dilihat pada Gambar 7. Perolehan nilai nitrat terendah ada pada perlakuan A yaitu 0.34±0.041 mg L-1, sedangkan perolehan tertinggi ada pada perlakuan D yaitu 1.15±0.095 mg L-1.
Ket: A (L. perpusilladan salinitas 3 ppt), B (L. perpusilla, salinitas 3 ppt dan filter), C (L. perpusilla, salinitas 3 ppt dan aerasi) dan D (L. perpusilla, salinitas 3 ppt, aerasi dan filter). Huruf yang berbeda menunjukkan hasil yang berbeda nyata (p<0.05)
Gambar 7 Nitrat pada media pemeliharaan selama 30 hari.
11
Total Suspended Solid(TSS)
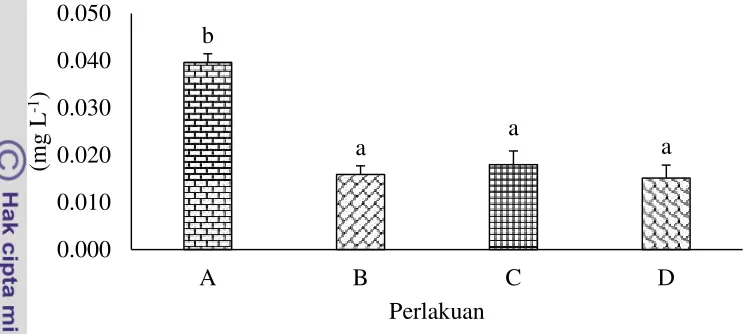
Hasil analisis ragam (ANOVA) menunjukkan bahwa faktor penambahanL. perpusilla, salinitas 3 ppt, aerasi dan filter memberikan pengaruh nyata terhadap nilai TSS. Hasil pengukuran nilai TSS pada media pemeliharaan dapat dilihat pada Gambar 8. Perolehan tertinggi ada pada perlakuan A yaitu 0.040±0.003 mg L-1.
Ket: A (L. perpusilladan salinitas 3 ppt), B (L. perpusilla, salinitas 3 ppt dan filter), C (L. perpusilla, salinitas 3 ppt dan aerasi) dan D (L. perpusilla, salinitas 3 ppt, aerasi dan filter). Huruf yang berbeda menunjukkan hasil yang berbeda nyata (p<0.05)
Gambar 8Total suspended solid(TSS) pada media pemeliharaan selama 30 hari.
Dissolved Oxygen(DO)
Hasil analisis ragam (ANOVA) menunjukkan bahwa faktor penambahanL. perpusilla, salinitas 3 ppt, aerasi dan filter memberikan pengaruh nyata nilai DO pada media pemeliharaan selama 30 hari. Hasil pengukuran nilai DO pada media pemeliharaan dapat dilihat pada Gambar 9. Perolehan nilai DO terendah ada pada perlakuan A yaitu 4.89±0.135 mg L-1.
Ket: A (L. perpusilladan salinitas 3 ppt), B (L. perpusilla, salinitas 3 ppt dan filter), C (L. perpusilla, salinitas 3 ppt dan aerasi) dan D (L. perpusilla, salinitas 3 ppt, aerasi dan filter). Huruf yang berbeda menunjukkan hasil yang berbeda nyata (p<0.05)
12
Biological Oxygen Demand(BOD)
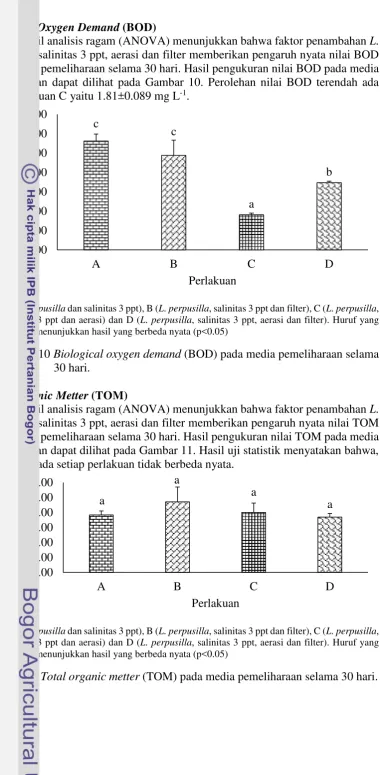
Hasil analisis ragam (ANOVA) menunjukkan bahwa faktor penambahanL. perpusilla, salinitas 3 ppt, aerasi dan filter memberikan pengaruh nyata nilai BOD pada media pemeliharaan selama 30 hari. Hasil pengukuran nilai BOD pada media pemeliharaan dapat dilihat pada Gambar 10. Perolehan nilai BOD terendah ada pada perlakuan C yaitu 1.81±0.089 mg L-1.
Ket: A (L. perpusilladan salinitas 3 ppt), B (L. perpusilla, salinitas 3 ppt dan filter), C (L. perpusilla, salinitas 3 ppt dan aerasi) dan D (L. perpusilla, salinitas 3 ppt, aerasi dan filter). Huruf yang berbeda menunjukkan hasil yang berbeda nyata (p<0.05)
Gambar 10Biological oxygen demand(BOD) pada media pemeliharaan selama 30 hari.
Total Organic Metter(TOM)
Hasil analisis ragam (ANOVA) menunjukkan bahwa faktor penambahanL. perpusilla, salinitas 3 ppt, aerasi dan filter memberikan pengaruh nyata nilai TOM pada media pemeliharaan selama 30 hari. Hasil pengukuran nilai TOM pada media pemeliharaan dapat dilihat pada Gambar 11. Hasil uji statistik menyatakan bahwa, nilai EPP pada setiap perlakuan tidak berbeda nyata.
Ket: A (L. perpusilladan salinitas 3 ppt), B (L. perpusilla, salinitas 3 ppt dan filter), C (L. perpusilla, salinitas 3 ppt dan aerasi) dan D (L. perpusilla, salinitas 3 ppt, aerasi dan filter). Huruf yang berbeda menunjukkan hasil yang berbeda nyata (p<0.05)
13
pH
Hasil analisis ragam (ANOVA) menunjukkan bahwa faktor penambahanL. perpusilla, salinitas 3 ppt, aerasi dan filter tidak memberikan pengaruh nyata terhadap nilai pH. Hasil pengukuran nilai pH pada media pemeliharaan dapat dilihat pada Gambar 12. Perolehan nilai pH terendah ada pada perlakuan C dan D. Perolehan tertinggi ada pada perlakuan A dan B.
Ket: A (L. perpusilladan salinitas 3 ppt), B (L. perpusilla, salinitas 3 ppt dan filter), C (L. perpusilla, salinitas 3 ppt dan aerasi) dan D (L. perpusilla, salinitas 3 ppt, aerasi dan filter). Huruf yang berbeda menunjukkan hasil yang berbeda nyata (p<0.05)
Gambar 12 pH pada media pemeliharaan selama 30 hari.
Kandungan NitrogenL. perpusilla
Hasil analisis ragam (ANOVA) menunjukkan bahwa faktor penambahanL. perpusilla, salinitas 3 ppt, aerasi dan filter memberikan pengaruh pada kemampuan
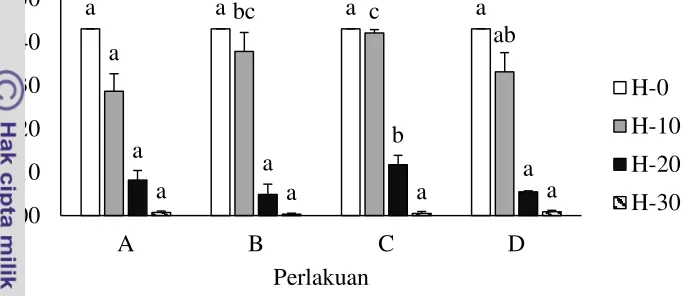
L. perpusilla dalam menyerap nitrogen pada media 3 ppt. Hasil pengukuran nitrogen pada L. perpusilla dapat dilihat pada Gambar 13. Kemampuan L. perpusillamengalami penurunan dari H 0 hingga H 20. Hasil statistik menyatakan bahwa nilai nitrogen pada H 20 berbeda nyata. Pada H 30, nilai nitrogen pada L. perpusilla kembali meningkat, namun tidak terlihat berbeda nyata pada setiap perlakuan.
Ket: A (L. perpusilladan salinitas 3 ppt), B (L. perpusilla, salinitas 3 ppt dan filter), C (L. perpusilla, salinitas 3 ppt dan aerasi) dan D (L. perpusilla, salinitas 3 ppt, aerasi dan filter). Huruf yang berbeda menunjukkan hasil yang berbeda nyata (p<0.05)
Gambar 13 Kandungan nitrogen padaL. perpusillaselama 30 hari.
14
Kandungan FosforL. perpusilla
Hasil analisis ragam (ANOVA) menunjukkan bahwa faktor penambahanL. perpusilla, salinitas 3 ppt, aerasi dan filter memberikan pengaruh pada kemampuan
L. perpusilla dalam menyerap fosfor pada media 3 ppt. Hasil pengukuran fosfor pada L. perpusilla dapat dilihat pada Gambar 14. Kemampuan L. perpusilla
mengalami penurunan dari H 0 hingga H 30. Pada akhir penelitian, hasil statistik menyatakan bahwa nilai fosfor tidak berbeda nyata pada setiap perlakuan.
Ket: A (L. perpusilladan salinitas 3 ppt), B (L. perpusilla, salinitas 3 ppt dan filter), C (L. perpusilla, salinitas 3 ppt dan aerasi) dan D (L. perpusilla, salinitas 3 ppt, aerasi dan filter). Huruf yang berbeda menunjukkan hasil yang berbeda nyata (p<0.05)
Gambar 14 Kandungan fosfor padaL. perpusillaselama 30 hari.
Pembahasan
PemanfaatanL. perpusilladengan menggunakan aerasi, filter dan salinitas bertujuan menyerap limbah di perairan agar mengurangi beban cemar pada media budidaya untuk mendukung kelangsungan hidup ikan. Hasil analisis terhadap derajat kelangsungan hidup (DKH) dapat dilihat pada Gambar 2. Perlakuan C dan D merupakan perlakuan yang baik pada hasil DKH dibandingkan dengan perlakuan A dan B. Tingginya nilai DKH pada perlakuan C (L. perpusilla, salinitas dan aerasi) dan perlakuan D (L. perpusilla, salinitas aerasi dan filter) dipengaruhi oleh adanya penambahan aerasi. Aerasi dibantu dengan bakteri mampu mepercepat proses perombakan ion organik menjadi ion anorganik sehingga dapat dimanfaatkan dengan baik oleh L. perpusilla. Proses perombakan dari ammonia menjadi nitrit membutuhkan 1.5 mg L-1oksigen, sedangkan proses perombakan dari nitrit menjadi nitrat membutuhkan 0.5 mg L-1 oksigen. Penambahan aerasi merupakan faktor penting mengingat adanya penambahan salinitas dapat mengurangi kandungan oksigen terlarut (DO) pada media pemeliharaan. Penambahan salinitas berfungsi untuk mempercepat laju pertumbuhan harian (LPH) ikan gurami, hal ini sesuai pada penelitian sebelumnya yang menyatakan bahwa pemeliharaan ikan gurami dengan salinitas 3 ppt menghasilkan laju pertumbuhan dan tingkat kelangsungan hidup lebih tinggi dibandingkan dengan air yang tidak bersalinitas (Rasmawan 2009; Nirmala dan Rasmawan 2010). Menurut Sticney (1979) dalam Nirmalaet al. (2005) ikan yang dipelihara dalam media bersalinitas dengan konsentrasi yang sama didalam tubuhnya (isoosmotik) akan lebih banyak menggunakan energi untuk
15
pertumbuhannya dan lebih sedikit untuk osmoregulasinya. Selain itu kondisi isoosmotik menyebabkan energi tersimpan didalam tubuh karena berkurangnya energi yang terpakai untuk proses osmosis (Holliday 1969; Nirmala et al. 2005). Hal ini sesuai dengan hasil perhitungan statistik yaitu nilai LPH ikan gurami selama masa penelitian tidak berbeda nyata (Gambar 3).
Salinitas 3 ppt pada media, menjadikan ikan gurami berada dalam kondisi isoosmotik. Kondisi isoosmotik berpengaruh terhadap penggunaan energi pada ikan gurami. Pada media tanpa salinitas, ikan gurami membutuhkan 3-5% energi untuk melakukan osmoregulasi disetiap waktunya. Penambahan salinitas 3 ppt mengakibatkan kondisi ikan dan media pemeliharaan menjadi isoosmotik, sehingga ikan gurami dapat menyimpan 3-5% energi atau mengalihkan energi tersebut ke dalam proses pertumbuhan. Berkurangnya penggunaan energi pada proses osmoregulasi juga berdampak terhadap efisiensi pemberian pakan (EPP). Berdasarkan penambahan salinitas 3 ppt pada setiap media pemeliharaan dan di uji secara statisik, nilai EPP ikan gurami tidak berbeda nyata (Gambar 4).
Kualitas air merupakan salah satu faktor yang mempengaruhi derajat kelangsungan hidup dan laju pertumbuhan harian ikan gurami. Ammonia merupakan salah satu faktor menurunnya kualitas air. Berdasarkan Boyd (1982) amonia dalam bentuk tidak terionisasi (NH3) bersifat toksik bagi ikan. Nilai
ammonia media pemeliharaan termasuk dalam batas aman 0.18 mg L-1 - 0.36 mg L-1. Boyd (1990) kadar ammonia <1 mg L-1 masih layak untuk budidaya ikan.
Affiati dan Lim (1986) dalam Haryati (1995) pertumbuhan benih ikan gurami masih baik pada kadar amonia <0.12 mg L-1, sedangkan nilai dari Peraturan Pemerintah (2001) kadar ammonia pada perikanan yaitu 0.5 mg L-1dan pada ikan yang rentan terhadap ammonia kadar ammonia≤0.02 mg L-1. Perlakuan A dan C berbeda nyata terhadap perlakuan B dan D (Lampiran 9). Penambahan salinitas memberikan proses ionisasi terhadap ammonia. Kadar ammonia yang terionisasi memberikan reaksi pertukaran ion Na+ yang memacu proses homeostasis atau regulasi lingkungan osmotik internal ikan menjadi lebih baik. Ammonia yang ada di dalam tubuh ikan akan keluar ke lingkungan melalui pertukaran dengan Na+(Wedemeyer 1996). Hal tersebut sesuai dengan pernyataan Yuwono dan Purnama (2001) salah satu fungsi homeostasis yang terpenting pada organisme hidup adalah regulasi lingkungan osmotik internal yang tepat, mekanisme pengaturan keseimbangan cairan tubuh inilah yang merupakan fungsi osmoregulasi. Rendahnya nilai ammonia pada perlakuan A dan C (Gambar 4) dipengaruhi oleh persentase DKH serta adanya penambahan aerasi pada media. Rendahnya persentasi DKH pada perlakuan A dikarenakan tidak adanya penambahan perlakuan selain adanya L. perpusilla dan salinitas 3 ppt pada media. Hal ini mempengaruhi kadar ammonia yang berasal dari sisa pakan yang tidak termakan, feses, urin dan ammonia (NH3)
yang dikeluarkan oleh ikan, sehingga ikan mengalami kematian. Kematian ikan akan mengurangi sumber ammonia pada media pemeliharaan.
16
dengan nitrifikasi yang mengkonversi nitrogen ammonium (N-NH4) menjadi nitrit
(N-N2) dengan bantuan bakteri nitrosomonas (Widayat et al. 2010). Rendahnya
kandungan nitrit pada media bersalinitas dikarenakan proses nitrifikasi bakteri yang berjalan dengan baik (Harsitoningrumet al. 2012). Namun bakteri nitrifikasi akan mulai berkurang kemampuannya seiring dengan meningkatnya salinitas. Kandungan nitrit yang tinggi pada suatu media budidaya akan sangat membahayakan bagi ikan. Hal ini terjadi dikarenakan nitrit mampu mengoksidasi ion ferrous (Fe2) menjadi ion ferric (Fe3+) di dalam haemoglobin (Hb) pada tubuh
ikan. Sehingga, mengubah haemoglobin (Hb) menjadi methaemoglobin (MetHb) di dalam darah yang dapat menyebabkan kematian (Jensen 1992).
Nitrat bisa menyebabkan terjadinyabloomingalga yang akan menurunkan kadar oksigen terlarut di air (Hallberg 1989). Tingginya nilai nitrat pada perlakuan D (Gambar 7) dikarenakan aerasi dan filter memberikan pengaruh terhadap kandungan oksigen yang bisa dimanfaatkan oleh bakteri nitrobacter. Proses perubahan nitrit menjadi nitrat membutuhkan bakteri nitrobacter dan oksigen. Oksigen diperlukan dalam proses oksidasi berbagai senyawa kimia dan respirasi berbagai organisme perairan (Dahuriet al. 2004). Banyaknya bakteri nitrobacter
menghasilkan nitrat pada perlakuan D masih dalam batas aman, karena kandungan DO pada perlakuan D tetap tercukupi akibat dari penambahan aerasi dan filter.
Total Suspended Solid(TSS) yang diperoleh dalam masa penelitian berasal dari sisa pakan yang tidak termakan yang terdegradasi,fecesdari ikan gurami dan sebagian dari L. perpusilla yang mati. TSS dipengaruhi oleh pergerakan dan penyerapan air dari filter dan aerasi. Hal ini dibuktikan pada perlakuan A (L. perpusilladan salinitas 3 ppt) memiliki nilai TSS paling tinggi sebesar 0.04 mg L
-1(Gambar 8) dibandingkan dengan perlakuan lain yang terdapat aerasi dan filter.
Penggunaan filter memberikan hasil yang lebih baik, hal ini terjadi karena faktor yang menyebabkan TSS tertahan pada kapas filter, sedangkan pada penambahan aerasi, beberapa faktor penyebab TSS terangkat dan menempel ke sisi akuarium yang disebabkan oleh pecahan gelembung udara. Hal ini juga dibuktikan pada penelitian Anwari et al. (2011) penggunaan aerasi selama 120 menit dapat menurunkan kandungan TSS pada media air. Hal ini menunjukkan bahwa pemberianL. perpusilla, filter dan aerasi berpengaruh terhadap pengurangan nilai TSS.
Dissolved Oxygen(DO) yang terdapat di dalam air yang dinyatakan dalam milligram per liter (mg L-1). Oksigen di perairan berasal dari proses fotosintesis dari fitoplankton atau jenis tumbuhan air dan melalui proses difusi dari udara (APHA 1989). Kandungan DO pada penelitian ini berkisar antara 4.89-6.37 mg L-1
(Gambar 9). Hasil uji statistik menyatakan bahwa perlakuan B tidak berbeda nyata terhadap perlakuan A, C dan D. Namun perlakuan A berbeda nyata terhadap perlakuan C dan D (Lampiran 15). Penggunaan aerasi dan filter menghasilkan DO yang tinggi pada media pemeliharaan. Hal tersebut diperlukan mengingat salinitas yang terdapat pada perlakuan mempengaruhi kandungan DO selama pemeliharaaan. Semakin tinggi salinitas maka kandungan DO pada perairan semakin rendah (Indrayanaet al. 2014).
17
antara 1.81-5.62 mg L-1(Gambar 10). Apabila mengacu pada baku mutu Peraturan
Pemerintah Nomor 82 Tahun 2001, kandungan BOD pada penelitian ini masuk kedalam kelas 1, 2 dan 3. Perlakuan C merupakan perlakuan dengan nilai BOD terendah 1.80±0.100 mg L-1dan termasuk kedalam kelas 1 yaitu nilai BOD≤2. Hal ini mengartikan bahwa nilai BOD pada perlakuan C memiliki kandungan yang bagus pada media pemeliharaan. Semakin besar kandungan BOD pada suatu media mengartikan bahwa kandungan bahan organik pada media semakin banyak. Hal ini akan meningkatkan kebutuhan DO bagi mikroba untuk mengurai bahan organik menjadi CO2+ H2O + energi. Hal ini menjadikan media pemeliharaan toksik bagi
ikan, namun penentuan nilai BOD pada perairan yang mengandung toksik cenderung kurang cocok dilaksanakan, karena bahan–bahan toksik tersebut dapat menghambat atau mematikan mikroba yang menjadi pelaku dekomposisi bahan organik
Total Organic Matter(TOM) pada penelitian ini berasal penumpukan yang diakibatkan dari matinya L. perpusilla dan tidak termakannya pakan yang diberikan. Kandungan TOM pada media pemeliharaan berkisar antara 7.38-9.42 mg L-1. Gambar 11 memperlihatkan kandungan TOM setelah dilakukan uji statistik tidak berbeda nyata pada setiap perlakuan (Lampiran 19).
Nilai pH selama masa pemeliharaan didapatkan sebesar 6.69-7.26 (Gambar 12). Nilai pH ini dipengaruhi oleh aktivitas biologis fotosintesis dan respirasi dari
L. perpusilla serta keberadaan ion-ion wadah pemeliharaan. Perubahan pH juga mempengaruhi pertumbuhan dan aktivitas biologis pada L. perpusilla dan ikan gurami. Nilai pH yang tinggi akan meningkatkan persentase dari ammonia yang tidak terionisasi dan meningkatkan kecepatan pengendapan fosfat di perairan (Boyd 1990).
L. perpusilla menyerap nitrogen (N) dan fosfor (P) dalam bentuk ion anorganik di dalam air limbah budidaya sebagai sumber nutrisi untuk mendukung pertumbuhannya. Pada penelitian ini kemampuanL. perpusilladalam menyerap N dan P selama masa pemeliharaan 30 hari mengalami penurunan (Gambar 13 dan Gambar 14). Penurunan terjadi terdiri dari beberapa faktor, beberapa diantaranya ketidakmampuanL. perpusillaberadaptasi pada media bersalinitas 3 ppt, N dan P masih dalam bentuk senyawa organik dan sedikitnya sumber N dan P yang masuk ke dalam media pemeliharaan.
Penambahan salinitas 3 ppt menjadi penyebab berkurangnya kemampuanL. perpusilla dalam menyerap ion anorganik N dan P. Hal ini terjadi karena L. perpusilla secara alamiah tumbuh pada media tidak bersalinitas (tawar). Penambahan salinitas akan menarik kandungan air pada tanaman, terutama pada bagian akar dan sel tanaman. Tingginya salinitas pada media membuat sel tanaman mengalami hypertonic yang mengakibatkan plasmolyzed, sehingga kandungan air pada sel tanaman akan keluar dan ion-ion seperti Na Cl banyak masuk kedalam sel, sehingga sel mengalami pengkerutan, mengurangi pertumbuhan dan perkembangan. Nielsen et al. (2003) salinitas dapat mempengaruhi berkurangnya pertumbuhan dan perkembagan dari akar dan daun pada tumbuhan air. Salinitas yang tinggi secara signifikan akan menghambat pertumbuhan, mengurangi kemampuan akar sehingga akar menipis.
18
difermentasikan dengan kotoran ayam. Kandungan N berkurang secara drastis pada H-10. Hasil uji statistik memperlihatkan pada H-20 memiliki hasil yang berbeda nyata. Pada H-30, kandungan N yang terserap oleh L. perpusilla mengalami peningkatan yang tidak berbeda nyata. N dan P yang berasal dari sisa pakan dan feses masih dalam bentuk senyawa organik. Senyawa organik tidak dapat langsung diserap oleh L. perpusilla. Besarnya ukuran N dan P organik tidak dapat diserap secara langsung oleh L. perpusilla, hal ini dikarenakan akar pada L. perpusilla
berukuran kecil, sehingga hanya dapat menyerap N dan P dalam bentuk anorganik (ion).
Sedikitnya sumber N dan P pada media pemeliharaan turut mempengaruhi rendahya kandungan N dan P pada L. perpusilla. Sumber N dan P hanya mengandalkan dari sisa pakan yang tidak termakan oleh ikan, feses dan NH3pada
insang. Sedikitnya sumber N dan P maka perkembangan bakteri untuk merombak N dan P organik menjadi N dan P anorganik semakin lama. Secara umum bakteri nitrosmonas mulai merombak N pada ammonia menjadi N pada nitrit, hal ini ini akan membutuhkan waktu yang lama jika kandungan ammonia pada media juga sedikit. Hal tersebut juga akan berpengaruh terhadap perombakan nitrit menjadi nitrat. Lambatnya proses perombakan maka kandungan nitrat yang dapat diserap olehL. perpusillasemakin sedikit.
4 SIMPULAN DAN SARAN
Simpulan
L. perpusillatidak dapat bertahan dengan baik pada salinitas 3 ppt, sehingga mempengaruhi kemampuanL. perpusilla dalam menyerap unsur hara fan limbah organik pada media pemeliharaan. Hal ini terlihat berkurangannya kandungan N dan P padaL. perpusilladari awal hingga akhir penelitian. Perlakuan C merupakan perlakuan terbaik dari nilai derajat kelangsungan hidup (DKH) pada ikan gurami selama masa penelitian. Meski tidak berbeda nyata dengan perlakuan D, namun perlakuan C dapat menghemat nilai produksi dari segi penggunaan listrik karena hanya menggunakan aerasi.
Saran
19
DAFTAR PUSTAKA
Amalia F. 2014. Kapasitas fitoremidiator Lemna perpusilla dalam mereduksi limbah nitrogen danfosfat pada sistem resirkulasi budidaya ikan lele (Clarias gariepinus). [Tesis]. Bogor: Institut Pertanian Bogor.
Anwari F, Muslim GR, Hadi A, Mirwan A. 2011. Studi penurunan kadar BOD. COD, TSS dan pH limbah pabrik tahu menggunakan metode aerasi bertingkat. Prestasi. 1 (1). Hlm 1-7.
APHA. 1989. Standard Methods for The Examnation of Water and Wastewater. Washington. DC 20005.
Boyd CE. 1982. Water Quality Management in Pond Fish Culture. International Center for Aquaculture Agricultural Experiment Station. Auburn University. Auburn. Alabama.
Boyd CE. 1990. Water Quality in Ponds for Aquaculture. Auburn. AL: Auburn University/Alabama Agricultural Experiment Station.
Cheng J, Landesman L, Bergmann BA, Classen JJ, Howard JW, Yamamoto YT. 2002. Nutrient removal from Swine lagoon liquid by Lemna minor 8627. Transactions of The Asae. Vol. 45(4): 1003–1010.
Dahuri R, Rais J, Ginting SP, Sitepu MJ. 2004. Pengelolaan Sumberdaya Wilayah Pesisir dan Laut Secara Terpadu. Edisi revisi. PT. Pradnya Paramita, Jakarta. Dewi ES. 2006.Pengaruhsalinitas0,3,6,9dan12 ppt terhadap pertumbuhandan
kelangsungan hidup benih ikan gurami(Ospronemus gouramy)ukuran 3-6 cm. [Skripsi]. Bogor: Institut Pertanian Bogor.
Febriwahyudi CT, Hadi W. 2011. Resirkulasi air tambak bandeng dengan slow sand filter. [Tugas Akhir]. Institut Teknologi Sepuluh Nopember.
Ferdoushi Z, Haque F, Khan S, Haque M. 2008. The effects of two aquatic floating macrophytesc (Lemna and Azolla) as bifilters of nitrogen and phosphate in fish pond.Turkish Journal of Fisheries and Aquatic Sciences8: 253-258.
Fujaya Y. 2004. Fisiologi Ikan Dasar Pengenmbangan Teknologi Perikanan. Rineka Cipta. Hal 75.
Hallberg GR. 1989. Nitrate in groundwater in the United States. IN: Nitrogen management and Groundwater Protection. Elsevier. Amsterdam. pp. 35-74. Hardyanti N, Suparni SR. 2007. Fitoremidiasi phospat dengan pemanfaatan
enceng gondok (Eichhornia erassipes) (studi kasus pada limbah cair industri kecil laundry).Jurnal PRESIPITASI2 (1). ISSN 1907-187X.
Harsitoningrum M, Sudarno, Istirokhatun T. 2012. Pengaruh fluktuasi salinitas terhadap nitrifikasi oleh bakteri yang diambil pada estuari sungai banjir kanal barat-Semarang.Jurnal Teknik Lingkungan2 (1): 1-8.
Haryati. 1995. Pengaruh Penggantian Artemia Salina dengan Daphnia sp. Terhadap Pertumbuhan dan DKH Benih Ikan Gurami Osphronemus gouramyLacepede. Program Pascasarjana Institut Pertanian Bogor.
Hermawati E, Wiryanto, Solichatun. 2005. Fitoremediasi limbah detergen menggunakan kayu apu (Pistia stratiotesL.) dan genjer (Limnocharis flavaL.). Bio SMART. Vol. 7. 116 (2). 115-124.
20
Huisman EA. 1987. The principles of fish culture production. Department of Aquaculture.Wageningen University.Netherland.
Indah LS, Hendrarto B, Soedarsono P. 2014. Kemampuan enceng gondok
(Eichhornia sp.) dan kayu apu (Pistia sp.) dalam menurunkan bahan organik limbah industri tahu (skala laboratorium). Diponegoro Journal of Maquares
3(1): 1-6.
Indrayana R, Yusuf M, Rifai A. 2014. Pengaruh arus permukaan terhadap sebaran kualitas air di perairan Genuk Semarang.Jurnal Oseanografi. 3 (4) : 651–659. Jensen FB. 1992. Influence of haemoglobin conformat ion, nitrite and eicosanoids on K+ transport across the carp red blood cell membrane. Journal of Experimental Biology171: 349-371.
Komarawidjaja W, Sukimin S, Arman E. 2005. Status kualitas air waduk Cirata dan dampaknya terhadap pertumbuhan ikan budidaya.Jurnal Teknologi Lingkungan P3TL-B PPT6 (1): 268-273.
Molleda MI. 2007. Water quality in Recirculating Aquaculture System for Arctic Charr(Salvelinus alpinusL.)Culture. División de Cultivos Marinos. Centro de Investigaciones Pesqueras (CIP) 5ta Ave y 246. Barlovento, Santa Fe, Ciudad de la Habana, Cuba.
Nielsen DL, Brock MA, Rees GN, Baldwin DS. 2003.Effect of increasing salinity on freshwater ecosystem in Australia.Australian Journal of Botany51: 655-665. Nirmala K, Lesmono DP, Djokosetiyanto D. 2005. Pengaruh Teknik Adaptasi Salinitas Terhadap Kelangsungan Hidup Dan Pertumbuhan Benih Ikan Patin.
Pangasiussp.Jurnal Akuakultur Indonesia4 (1): 25–30.
Nirmala K, Rasmawan. 2010. Kinerja pertumbuhan ikan gurami (Osphronemus goramy Lac.) yang dipelihara pada media bersalinitas dengan paparan medan listrik.Jurnal Akuakultur Indonesia9 (1): 46–55.
Ozengin N, Elmaci A. 2007. Performance of Duckweed (Lemna minor L.) on different types of wastewater treatment. Journal of Environmental Biology 28 (2) 307-314.
Peraturan Pemerintah. 2001. Pengelolaan kualitas air dan pengendalian pencemaran air.
Rasmawan. 2009. Kinerja pertumbuhan ikan gurami (Osphronemus goramy Lac.) yang dipelihara pada media bersalinitas dengan paparan medan listrik. [Skripsi]. Program Studi Teknologi dan Manajemen Akuakultur. Fakultas Perikanan dan Ilmu Kelautan Institut Pertanian Bogor.
Subroto MA. 1996. Fitoremediasi, dalam: Prosiding Pelatihan dan Lokakarya Peranan Bioremediasi dalam Pengelolaan Lingkungan. Cibinong. 24-25 Juni 1996.
Sugiharto. 1987.Dasar-dasar pengelolaan air limbah. UI Press. Jakarta.
Sumiyati S, Handayani DS, Hartanto W. 2009. Pemanfaatan hydrilla (Hydrilla verticillain) untuk menurunkan logam tembaga (Cu) dalam limbah elektroplating studi kasus: industri kerajinan perak kelurahan citraan kota gede. 7 (2). ISSN 1907-187X.
Wedemeyer. GA. 1996. Physiology of fish in intensive culture systems. Chapman & Hall. New York. 232 pp.
21
biofiltrasi menggunakan media plastik tipe sarang tawon. Jurnal Akuakultur Indonesia6 (1): 64-76.
Yosmaniar. 2010. Hubungan Konversi Pakan dengan Beban Limbah Hara N dan
P yang Dibuang ke Air Pemeliharaan. Prosiding Forum Inovasi Teknologi Akuakultur. 681-688.
Yuwono E, Purnama S. 2001. Fisiologi Hewan I. Departemen Pendidikan Nasional. Universitas Jenderal Soedirman. Fakultas Biologi. Purwokerto.
22
Lampiran 1. Desain akuarium penelitian selama 30 hari masa penelitian.
Keterangan :
Perlakuan A :L. perpusilladan salinitas 3 ppt. Perlakuan B :L. perpusilla, salinitas 3 ppt dan filter. Perlakuan C :L. perpusilla, salinitas 3 ppt dan aerasi. Perlakuan D :L. perpusilla, salinitas 3 ppt, aerasi dan filter.
Lampiran 2. Output tabel ANOVA analisis ragam DKH pada media pemeliharaan selama 30 hari dengan menggunakan SPSS 18.0.
Sum of Squares df Mean Square F Sig.
Between Groups 6239.583 3 2079.861 28.524 0.000
Within Groups 583.333 8 72.917
Total 6822.917 11
Lampiran 3. Output tabel uji lanjut Duncan DKH pada media pemeliharaan selama 30 hariL. perpusilladengan SPSS 18.0.
Perlakuan N Subset for alpha = 0.05
1 2 3
Duncan
A (L+S) 3,00 40,00
B (L+S+F) 3,00 63,33
D (L+S+F + A) 3,00 93,33
C (L+S+A) 3,00 95,00
Sig. 1,00 1,00 0,82
Nilai pada kolom yang sama menunjukkan bahwa setiap perlakuan tidak berbeda nyata
Lampiran 4. Output tabel ANOVA analisis ragam LPH pada media pemeliharaan selama 30 hari dengan menggunakan SPSS 18.0.
Sum of Squares df Mean Square F Sig.
Between Groups 0,590 3 0,197 1,501 0,287
Within Groups 1,048 8 0,131
23
Lampiran 5. Output tabel uji lanjut Duncan LPH pada media pemeliharaan selama 30 hariL. perpusilladengan SPSS 18.0.
Perlakuan N Subset for alpha = 0.05
1
Duncan
D (L+S+F + A) 3,00 4,36
A (L+S) 3,00 4,72
C (L+S+A) 3,00 4,80
B (L+S+F) 3,00 4,97
Sig. 0,09
Nilai pada kolom yang sama menunjukkan bahwa setiap perlakuan tidak berbeda nyata
Lampiran 6. Output tabel ANOVA analisis ragam EPP pada media pemeliharaan selama 30 hari dengan menggunakan SPSS 18.0.
Sum of Squares df Mean Square F Sig.
Between Groups 20,187 3 6,729 0,414 0,748
Within Groups 130,176 8 16,272
Total 150,362 11
Lampiran 7. Output tabel uji lanjut Duncan EPP pada media pemeliharaan selama 30 hariL. perpusilladengan SPSS 18.0.
Perlakuan N Subset for alpha = 0.05
1
Duncan
A (L+S) 3,00 40,44
B (L+S+F) 3,00 41,16
D (L+S+F + A) 3,00 43,19
C (L+S+A) 3,00 43,48
Sig. 0,41
Nilai pada kolom yang sama menunjukkan bahwa setiap perlakuan tidak berbeda nyata
Lampiran 8. Output tabel ANOVA analisis ragam ammonia pada media pemeliharaan selama 30 hari dengan menggunakan SPSS 18.0.
Sum of Squares df Mean Square F Sig.
Between Groups 0,069 3 0,023 8,103 0,008
Within Groups 0,023 8 0,003
24
Lampiran 9. Output tabel uji lanjut Duncan ammonia pada media pemeliharaan selama 30 hariL. perpusilladengan SPSS 18.0.
Perlakuan N Subset for alpha = 0.05
1 2
Duncan
C (L+S+A) 3,00 0,18
A (L+S) 3,00 0,23
B (L+S+F) 3,00 0,35
D (L+S+F + A) 3,00 0,36
Sig. 0,23 0,84
Nilai pada kolom yang sama menunjukkan bahwa setiap perlakuan tidak berbeda nyata
Lampiran 10. Output tabel ANOVA analisis ragam nitrit pada media pemeliharaan selama 30 hari dengan menggunakan SPSS 18.0.
Sum of Squares df Mean Square F Sig.
Between Groups 0,067 3 0,022 1,025 0,431
Within Groups 0,175 8 0,022
Total 0,242 11
Lampiran 11. Output tabel uji lanjut Duncan nitrit pada media pemeliharaan selama 30 hariL. perpusilladengan SPSS 18.0.
Perlakuan N Subset for alpha = 0.05
1
Duncan
C (L+S+A) 3,00 0,96
B (L+S+F) 3,00 1,01
D (L+S+F + A) 3,00 1,12
A (L+S) 3,00 1,14
Sig. 0,21
Nilai pada kolom yang sama menunjukkan bahwa setiap perlakuan tidak berbeda nyata
Lampiran 12. Output tabel ANOVA analisis ragam nitrat pada media pemeliharaan selama 30 hari dengan menggunakan SPSS 18.0.
Sum of Squares df Mean Square F Sig.
Between Groups 0,987 3 0,329 26,245 0,000
Within Groups 0,100 8 0,013
25
Lampiran 13. Output tabel uji lanjut Duncan nitrat pada media pemeliharaan selama 30 hariL. perpusilladengan SPSS 18.0.
Perlakuan N Subset for alpha = 0.05
1 2 3
Duncan
A (L+S) 3,00 0,34
C (L+S+A) 3,00 0,74
B (L+S+F) 3,00 0,81
D (L+S+F + A) 3,00 1,15
Sig. 1,00 0,45 1,00
Nilai pada kolom yang sama menunjukkan bahwa setiap perlakuan tidak berbeda nyata
Lampiran 14. Output tabel ANOVA analisis ragam DO pada media pemeliharaan selama 30 hari dengan menggunakan SPSS 18.0.
Sum of Squares df Mean Square F Sig.
Between Groups 4,564 3 1,521 6,013 0,019
Within Groups 2,024 8 0,253
Total 6,588 11
Lampiran 15. Output tabel uji lanjut Duncan DO pada media pemeliharaan selama 30 hariL. perpusilladengan SPSS 18.0.
Perlakuan N Subset for alpha = 0.05
1 2
Duncan
A (L+S) 3,00 4,89
B (L+S+F) 3,00 5,45 5,45
C (L+S+A) 3,00 6,31
D (L+S+F + A) 3,00 6,37
Sig. 0,21 0,07
Nilai pada kolom yang sama menunjukkan bahwa setiap perlakuan tidak berbeda nyata
Lampiran 16. Output tabel ANOVA analisis ragam BOD pada media pemeliharaan selama 30 hari dengan menggunakan SPSS 18.0.
Sum of Squares df Mean Square F Sig.
Between Groups 25,520 3 8,507 44,450 0,000
Within Groups 1,531 8 0,191
26
Lampiran 17. Output tabel uji lanjut Duncan BOD pada media pemeliharaan selama 30 hariL. perpusilladengan SPSS 18.0.
Perlakuan N Subset for alpha = 0.05
1 2 3
Duncan
C (L+S+A) 3,00 1,80
D (L+S+F + A) 3,00 3,47
B (L+S+F) 3,00 4,88
A (L+S) 3,00 5,62
Sig. 1,00 1,00 0,07
Nilai pada kolom yang sama menunjukkan bahwa setiap perlakuan tidak berbeda nyata
Lampiran 18. Output tabel ANOVA analisis ragam TOM pada media pemeliharaan selama 30 hari dengan menggunakan SPSS 18.0.
Sum of Squares df Mean Square F Sig.
Between Groups 7,313 3 2,438 1,630 0,258
Within Groups 11,962 8 1,495
Total 19,274 11
Lampiran 19. Output tabel uji lanjut Duncan TOM pada media pemeliharaan selama 30 hariL. perpusilladengan SPSS 18.0.
Perlakuan N Subset for alpha = 0.05
1
Duncan
D (L+S+F + A) 3,00 7,38
A (L+S) 3,00 7,68
C (L+S+A) 3,00 8,01
B (L+S+F) 3,00 9,42
Sig. 0,09
Nilai pada kolom yang sama menunjukkan bahwa setiap perlakuan tidak berbeda nyata
Lampiran 20. Output tabel ANOVA analisis ragam pH pada media pemeliharaan selama 30 hari dengan menggunakan SPSS 18.0.
Sum of Squares df Mean Square F Sig.
Between Groups 0,661 3 0,220 2,784 0,110
Within Groups 0,634 8 0,079
27
Lampiran 21. Output tabel uji lanjut Duncan pH pada media pemeliharaan selama 30 hariL. perpusilladengan SPSS 18.0.
Perlakuan N Subset for alpha = 0.05
1 2
Duncan
C (L+S+A) 3,00 6,69
D (L+S+F + A) 3,00 6,95 6,95
A (L+S) 3,00 7,25
B (L+S+F) 3,00 7,25
Sig. 0,28 0,25
Nilai pada kolom yang sama menunjukkan bahwa setiap perlakuan tidak berbeda nyata
Lampiran 22. Output tabel ANOVA analisis ragam N yang diserap olehL. perpusilladengan menggunakan SPSS 18.0.
Sum of Squares df Mean Square F Sig.
Corrected Model 0.001a 3 0.000 0.008 0.999
Intercept 0.695 1 0.695 18.044 0.001
Perlakuan 0.001 3 0.000 0.008 0.999
Error 0.462 12 0.39
Total 1.159 16
Corrected Total 0.463 15
Lampiran 23. Output tabel uji lanjut Duncan pH pada media pemeliharaan selama 30 hariL. perpusilladengan SPSS 18.0.
Perlakuan N Subset for alpha = 0.05
1
Duncan
C (L+S+A) 4.00 0.1978
D (L+S+F + A) 4.00 0.2064
B (L+S+F) 4.00 0.2102
A (L+S) 4.00 0.2194
Sig. 0,888
28
Lampiran 24. Output tabel ANOVA analisis ragam N yang diserap olehL. perpusilladengan menggunakan SPSS 18.0.
Sum of Squares df Mean Square F Sig.
Corrected Model 0.005a 3 0.002 0.035 0.991
Intercept 0.753 1 0.753 17.288 0.001
Perlakuan 0.005 3 0.002 0.035 0.991
Error 0.522 12 0.044
Total 1.279 16
Corrected Total 0.527 15
Lampiran 25. Output tabel uji lanjut Duncan pH pada media pemeliharaan selama 30 hariL. perpusilladengan SPSS 18.0.
Perlakuan N Subset for alpha = 0.05
1
Duncan
A (L+S) 4.00 0.2025
D (L+S+F + A) 4.00 0.2050
B (L+S+F) 4.00 0.2150
C (L+S+A) 4.00 0.2450
Sig. 0.794
29
RIWAYAT HIDUP
Penulis dilahirkan di Medan pada tanggal 17 Juli 1989 sebagai anak pertama dari empat bersaudara oleh pasangan Thosin Burhani dan Tengku Mardatillah. Penulis menyelesaikan pendidikan sekolah menengah atas di Madrasah Aliyah Al-Zaytun tahun 2007. Pada Tahun yang sama penulis lulus seleksi masuk melalui jalur SPMB pada Universitas Padjadjaran dan memilih Program Studi Perikanan, Fakultas Perikanan dan Ilmu Kelautan. Pendidikan sarjana penulis selesaikan tahun 2011. Pada tahun 2012 penulis mendapatkan kesempatan untuk menempuh pendidikan magister ke Sekolah Pascasarjana IPB, program studi Ilmu Akuakultur. Karya ilmiah ini sedang dalam proses untuk publikasi pada Jurnal Ilmu Akuakultur Indonesia pada tahun 2015 dengan judul Efektivitas Fitoremediator