ABSTRACT
EVALUATION OF PRECIPITATION PROCESS CONDITIONS TOWARDS THE PHYSICOCHEMICAL PROPERTIES OF ITTARA
TAPIOCA
By
DESY SILVIANTI
One method to improve the characteristics of starch is by means of a starch modification. Modifications may occur due to spontaneous fermentation by microorganism which hidrolyze the starch, degrade the amylose and amylopectin, destroy the structure and integrity of the starch granules, causing changes in the characteristics of tapioca produced by ITTARA. The processing of tapioca cottage industry (ITTARA) is still using simple mechanical technology, so that the processing takes place in a relatively longer time, especially in the precipitation stage which aims to separate the starch from the water. Precipitation is one of the stages of cassava processing into starch in ITTARA which lasts for 15 to 24 hours so as allow microorganisms to grow and live on starch deposition and conduct the spontaneous fermentation. The purpose of this research is to determine the effect of precipitation time on the tapioca physicochemical properties of ITTARA PD Semangat Jaya at every level of tapioca quality.
of precipitation time of tapioca starch slurry on flour pH, water content and degree of white of tapioca ITTARA but long precipitation lowers the pH of the filtrate, starch content, amylose contentof tapioca ITTARA at any level of quality. Long precipitation increases the ash content, change the shape and size of ITTARA tapioca granules at every level of quality observed.
ABSTRAK
EVALUASI KONDISI PROSES PENGENDAPAN TERHADAP
SIFAT FISIKOKIMIA TAPIOKA ITTARA
Oleh
DESY SILVIANTI
Salah satu metode untuk memperbaiki karakteristik pati adalah dengan cara modifikasi pati. Modifikasi juga dapat terjadi akibat adanya fermentasi spontan oleh mikroorganisme yang mengidrolisis pati, mendegradasi amilosa dan amilopektin, merusak struktur dan integritas granula pati, sehingga menyebabkan perubahan karakteristik tapioka yang dihasilkan ITTARA. Proses pengolahan tapioka Industri Rakyat (ITTARA) masih menggunakan teknologi mekanik sederhana, sehingga proses pengolahan berlangsung dalam waktu yang cukup lama terutama pada tahap pengendapan yang bertujuan memisahkan pati dari bagian air. Pengendapan merupakan salah satu tahap pengolahan ubi kayu menjaditapiokadi ITTARA berlangsungselama 15 sampai 24 jam, sehingga memungkinkan mikroorganisme untuk tumbuh dan hidup pada endapan pati sehingga terjadi fermentasi spontan. Tujuan penelitian ini untuk mengetahui pengaruh lama pengendapan terhadap sifat fisikokimia tapioka ITTARA PDSemangat Jaya pada setiap tingkat kualitas tapioka.
Penelitian ini menggunakan Rancangan Acak Kelompok Lengkap dengan faktor tunggal 3 ulangan. Faktor tunggal yang diuji berupa lama pengendapan yaitu 0, 10, 15, 20 dan 25 jam. Pengamatan dilakukan pada tiga jenis kualitas tapioka ITTARA PD Semangat Jaya yaitu tapioka kualitas I, II dan III. Parameter yang diamati adalah pH filtrate, pH tepung, derajat putih, kadar air, kadar abu, kadar pati, kadar amilosa dan amilopektin. Data diuji normalitas dengan
RIWAYAT HIDUP
Penulis dilahirkan di Bandung pada tanggal 17 Desember 1976, sebagai anak kedua dari lima bersaudara dari pasangan Bapak Drs. Hi. M. Yunus HS dan Ibu Hj. Etty Djuhaeti, A.Md. Penulis telah menikah dengan Yudiansyah, SP., pada tanggal 31 Mei 2003 dan dikaruniai tiga orang anak yang bernama Nur Intan Khairunnisa, Nur Laily Hijrianti dan M. Ikram Rasyad.
Penulis menyelesaikan pendidikan Taman Kanak-kanak di TK Pertiwi Way Jepara pada tahun 1983, Sekolah Dasar Negeri1Way Jepara pada tahun 1989, Sekolah Menengah Pertama di SMPN 1 Way Jepara pada tahun 1992, dan Sekolah Menengah Atas di SMANegeri 1 Way Jepara pada tahun 1995.
Pada bulan Juli tahun 1995, penulis diterima sebagai mahasiswa Jurusan Teknologi Hasil Pertanian, Fakultas Pertanian, Universitas Lampung dan menyelesaikan program sarjana pada bulan Desember 1999 dan sejak bulan Desember 2003 penulis di terima sebagai PNS di lingkungan Kementerian Perindustrian RI sebagai staf pengajar pada SMK-SMTI Bandar Lampung.
SANWACANA
Alhamdulillahi rabbil’aalamiin, puji dan syukur penulis ucapkan ke hadirat Allah SWT, karena atas berkat dan kuasa-Nya penulis dapat menyelesaikan penulisan tesis ini. Dengan selesainya tesis ini, penulis mengucapkan terima kasih kepada : 1. Bapak Prof. Dr. Ir. Udin Hasanudin, M.T., selaku pembimbing pertama dan
pembimbing akademik atas bimbingannya dalam proses penyelesaian pendidikan S2 dan penulisan tesis ini.
2. Ibu Ir. Siti Nurdjanah, M.Sc. Ph.D., selaku pembimbing kedua atas saran, bimbingan dan masukannya dalam penyelesaian penelitian dan penyelesaian tesis ini;
3. Ibu Ir. Neti Yuliana, M.Si., Ph.D. selaku dosen penguji yang telah banyak memberikan pengarahan, saran dan kritikan dalam menyelesaikan skripsi ini; 4. Bapak/Ibu dosen pengajar, staf administrasi dan pranata laboratorium di
Program Studi Magister Teknologi Industri Pertanian Universitas Lampung 5. Bapak Drs. Heri Purnomo, M.Pd., selaku kepala sekolah beserta dewan
guru/staf SMK-SMTI Bandar Lampung yang selalu mendukung dan memotivasi selama ini
6. Buyahku “Drs.Hi. M. Yunus H.S.” dan Ummi-ku “Etty Djuhaeti, A.Md.” atas
xiii
7. Suamiku “Yudiansyah, S.P”, atas cinta kasih, pengertian dan kesabarannya
hingga penulis mampu menyelesaikan pendidikan dan penulisan tesis ini. Anak-anakku: Intan, Lily dan Ikram, yang selalu memberi keceriaan membuat hidupku lebih berwarna atas pengertian dan pengorbanan waktunya 8. Saudara-saudaraku : Gusti Irma-Junjungan Ali, Kanjeng Irfan-Sumber Meilia,
Tengku Dedy-Semuhun Febri, dan Adek Dina-Rajo Aris, atas supportnya dan siap selalu berbagi dalam suka dan duka.
9. Teman-teman sejawat SMTI yang selalu memberi bantuan dan hiburan : Aprilia, Kinung, Pirma, Miranti, Yani, Tria, Arum, Fetty, Kristin, Rani dan
Senior’s ku; Yuk Leli, Mbak Isti, ‘Te Teti, Kak Nur, Atu Fifi, mbak Neni,
pak Hamim, Ummi Atiek, Bu Ocha, yang selalu memotivasi penulis selama bekerja dan kuliah, terimakasih telah banyak membantu.
10. Teman-teman angkatan 2012 MTIP : Yuliza, Sucihati, Rini, Andre, Aji, Eci, Anjar, bu Nurul, Ardi, Nouval, atas . dan atas persahabatan yang luar biasa serta adik-adikku : Fizzaria, Mia, Billi, Mutia, Arlinda, Amel atas bantuan dan kerjasamanya ;
11. Mas Joko, Mbak Yanti, Mas Midi, Mas Hanafi terimakasih telah membantu penulis selama menyelesaikan penelitian ini;
Penulis berharap semoga Allah SWT membalas kebaikan mereka.
Bandar Lampung, Desember 2014 Penulis
DAFTAR ISI
Halaman
DAFTAR ISI...ii
DAFTAR TABEL ...v
DAFTAR GAMBAR ...ix
I. PENDAHULUAN...1
A. Latar Belakang dan Masalah ...1
B. Tujuan Penelitian ...3
C. Kerangka Pemikiran ...3
D. Hipotesis ...5
II. TINJAUAN PUSTAKA...6
A. Ubi Jayu ...6
B. Pati ...10
C. Sifat Fisikokimia Pati ...12
D. Tapioka...14
E. Ekstraksi Tapioka ...16
1. Pemarutan ... 17
2. Pengendapan ... 18
3. Pengeringan ... 19
F. Fermentasi dan Modifikasi Tepung Ubi kayu ... 20
III. BAHAN DAN METODE...26
A. Tempat dan Waktu Penelitian ...26
C. Metode Penelitian ...27
D. Pelaksanaan Penelitian ...28
E. Pengamatan ...29
1. Derajat Keasaman (pH) Filtrat dan Tapioka...29
2. Bentuk Granula Pati...30
3. Sifat Amilograf ...30
4. Derajat Putih ...31
5. Kadar Air ...31
6. Kadar Abu...32
7. Kadar Pati ...32
8. Kadar Amilosa dan Amilopektin ...34
IV. HASIL DAN PEMBAHASAN...37
A. pH Filtrat ...39
B. pH Tapioka ...42
C. Bentuk Granula Pati ...44
D. Sifat Amilograf ...47
E. Derajat Putih ...50
F. Kadar Air ...52
G. Kadar Abu ...55
H. Kadar Pati...57
I. Kadar Amilosa dan Amilopektin ...59
V.KESIMPULAN DAN SARAN...63
A. Kesimpulan ...63
B. Saran ...63
DAFTAR PUSTAKA...64
DAFTAR TABEL
Tabel Halaman
1. Komposisi kimia tapioka dalam 100 gram bahan...15
2. Syaratmututapiokaberdasarkansni 3451:2011 ...16
3. Hasil pengamatan fisikokimia tapioca ITTARA kualitasI (Kw I), kualitas II (Kw II), dan kualitas III (Kw III) pada berbagai waktu pengendapan...40
4. Pengamatan derajat putih tapioca kualitas I (Kw I), kualitas II (Kw II), dan kualitas III (Kw III) pada berbagai waktu pengendapan menggunakan Whiteness meter...49
5. Kadar pH filtrat kualitas I ... 70
6. Uji normalitas (Lilliefors test) pH filtrate kualitas I ...70
7. Uji kehomogenan (kesamaan) ragam (Bartlett's test)...71
8. Analisis ragam pH filtrat kualitas I ...71
9. Uji BNT pH filtrate kualitas I ...72
10. Kadar pH filtrat kualitas II ...72
11. Uji normalitas (lilliefors test) pH filtrate kualitas II ...73
12. Uji kehomogenan (kesamaan) ragam(Bartlett's test)...73
13. Analisis ragam pH filtrate kualitas II...74
14. Uji BNT pH filtrate kualitas II...74
16. Uji normalitas (Lilliefors test) pH filtrate kualitas III...75
17. Uji kehomogenan (kesamaan) ragam (Bartlett's test)...76
18. Analisis ragam pH filtrate kualitas III...76
19. Uji BNT pH filtrat kualitas III ...77
20. Kadar pH tapioka kualitas I ...77
21. Uji normalitas (Lilliefors test) pH tapioka kualitas I ...78
22. Uji kehomogenan (kesamaan) ragam (Bartlett's test)...78
23. Analisis ragam pH tapioka kualitas I ...79
24. Uji BNT pH tapioka kualitas I ...79
25. Kadar pH tapioka kualitas I ...80
26. Uji normalitas (Lilliefors test) pH tapioka kualitas II ...80
27. Uji kehomogenan (kesamaan) ragam (Bartlett's test)...81
28. Analisis ragam pH tapioka kualitas II...81
29. Uji BNT pH tapioka kualitas II...82
30. Kadar pH tapioka kualitas III...82
31. Uji normalitas (Lilliefors Test) ph tapioka kualitas III ...83
32. Uji kehomogenan (kesamaan) ragam (Bartlett's test)...83
33. Analisis ragam pH tapioka kualitas III ...84
34. Uji BNT pH tapioka kualitas III...84
35. Kadar air tapioka kualitas I ...85
36. Uji normalitas (Lilliefors test) kadar air tapioka kualitas I ...85
37. Uji kehomogenan (kesamaan) ragam (Bartlett's test)...86
38. Analisis ragam kadar air tapioka kualitasI...86
40. Kadar air tapioka kualitas I ...87
41. Uji normalitas (Lilliefors test) kadar air tapioka kualitas II...88
42. Uji kehomogenan (kesamaan) ragam (Bartlett's test)...88
43. Analisis ragam kadar air tapioka kualitas II...89
44. Uji BNT kadar air tapioka kualitas II...89
45. Kadar air tapioka kualitas III. ...90
46. Uji normalitas (Lilliefors test) kadar air tapioka kualitas III ...90
47. Uji kehomogenan (kesamaan) ragam(Bartlett's test)...91
48. Analisis ragam kadar air tapioka kualitas III ...91
49. Uji BNT kadar air tapioka kualitas III ...92
50. Kadar abu tapioka kualitas I ...92
51. Uji normalitas (Lilliefors test) kadar abu tapioka kualitas I...93
52. Uji kehomogenan (kesamaan) ragam (Bartlett's test)...93
53. Analisis ragam kadar abu tapioka kualitas I ...94
54. Uji BNT kadar abu tapioka kualitas I ...94
55. Kadar abu tapioka kualitas II ...95
56. Uji normalitas (Lilliefors test) kadar abu tapioka kualitas II ...95
57. Uji kehomogenan (kesamaan) ragam(Bartlett's test)...96
58. Analisis ragam kadar abu tapioka kualitas II ...96
59. Uji BNT kadar abu tapioka kualitas II ...97
60. Kadar abu tapioka kualitas III...97
61. Uji normalitas (Lilliefors test) kadar abu tapioka kualitas III...98
62. Uji kehomogenan (kesamaan) ragam (Bartlett's test)...98
64. Uji BNT kadar abu tapioka kualitas III...99
65. Kadar pati tapioka kualitas I ...100
66. Uji normalitas (Lilliefors test) kadar pati tapioka kualitas I ... 100
67. Uji kehomogenan (kesamaan) ragam (Bartlett's test)... 101
68. Analisis ragam kadar pati tapioka kualitas I ... 102
69. Uji BNT kadar pati tapioka kualitas I ... 103
70. Kadar pati tapioka kualitasII ...103
71. Uji normalitas (Lilliefors test) kadar pati tapioka kualitas II... 104
72. Uji kehomogenan (kesamaan) ragam (Bartlett's test)... 104
73. Analisis ragam kadar pati tapioka kualitas II... 105
74. Uji BNT kadar pati tapioka kualitas II... 105
75. Kadar pati tapioka kualitas III...106
76. Uji normalitas (Lilliefors test) kadar pati tapioka kualitas III... 106
77. Uji kehomogenan (kesamaan) ragam (Bartlett's test)... 107
78. Analisis ragam kadar pati tapioka kualitas III ... 107
79. Uji BNT kadar pati tapioka kualitas III ... 108
80. Kadar amilosa tapioka kualitas I ... 108
81. Uji normalitas (Lilliefors test) kadar amilosa tapioka kualitas I... 109
82. Uji kehomogenan (kesamaan) ragam (Bartlett's test)... 109
83. Analisis ragam kadar amilosa tapioka kualitas I... 110
84. Uji BNT kadar amilosa tapioka kualitas I... 110
85. Kadar amilosa tapioka kualitas II ...111
86. Uji normalitas (Lilliefors test) kadar amilosa tapioka kualitas II... 111
88. Analisis ragam kadar amilosa tapioka kualitas II ... 112
89. Uji BNT kadar amilosa tapioka kualitas II ... 113
90. Kadar amilosa tapioka kualitas III ...113
91. Uji normalitas (Lilliefors test) kadar amilosa tapioka kualitas III ...114
92. Uji kehomogenan (kesamaan) ragam (Bartlett's test)...114
93. Analisis ragam kadar amilosa tapioka kualitas III ...115
94. Uji BNT kadar amilosa tapioka kualitas III ...115
95. Kadar amilopektin tapioka kualitas I ...116
96. Uji normalitas (Lilliefors test) kadar amilopektin tapioka kualitas I ... 116
97. Uji kehomogenan (kesamaan) ragam (Bartlett's test)...117
98. Analisis ragam kadar amilopektin tapioka kualitas I ...117
99. Uji BNT kadar amilopektin tapioka kualitas I. ... 118
100.Kadar amilopektin tapioca kualitas II. ... 118
101.Uji normalitas (Lilliefors test) kadar amilopektin tapioka kualitas II ... 119
102.Uji kehomogenan (kesamaan) ragam (Bartlett's test) ...119
103.Analisis ragam kadar amilopektin tapioka kualitas II...120
104.Uji BNT kadar amilopektin tapioka kualitas II...120
105.Kadar amilopektin tapioca kualitas III...121
106. Uji normalitas (lilliefors test) kadar amilopektin tapioka kualitas III... 121
107.Uji kehomogenan (kesamaan) ragam (Bartlett's test)...122
108.Analisis ragam kadar amilopektin tapioka kualitas III ...122
109.Uji BNT kadar amilopektin tapioka kualitas III ...123
110.Sifat amilograf tapioca kualitas I menggunakan Brabender ...124
ix
DAFTAR GAMBAR
Gambar Halaman
1. Pohon industry pengolahan ubi kayu menjadi berbagai produk turunannya ... 9 2. Struktur amilosa ... 11
3. Struktur amilopektin ... 11
4. Diagram alir proses pengolahan tapioka di skala kecil (dimodifikasi) ... 18 5. Pelaksaan penelitian... 28 6. Bak pengendapan di PD Semangat Jaya ... 38 7. Ph filtrate bubur pati tapioka kualitas I (Kw I), tapioka kualitas II (Kw II) dan tapioka kualitas III (Kw III) pada berbagai waktu pengendapan ... 41 8. pH tepung tapioka kualitas I (Kw I), tapioka kualitas II (Kw II) dan tapioka
kualitas III (Kw III) pada berbagai waktu pengendapan... 42 9. Granula tapioka kualitas I (Kw I), tapioka kualitas II (Kw II) dan tapioka
kualitas III(Kw III) pada berbagai waktu pengendapan... 46 10. Kadar air tapioka kualitas I (Kw I), tapioka kualitas II (Kw II) dan tapioka
kualitas III(Kw III) pada berbagai waktu pengendapan... 53 11. Kadar abu tapioca kualitas I (Kw I), tapioca kualitas II (Kw II) dan tapioca
kualitas III(Kw III) pada berbagai waktu pengendapan... 56 12. Kadar pati tapioca kualitas I (Kw I), tapioca kualitas II (Kw II) dan tapioca
kualitas III(Kw III) pada berbagai waktu pengendapan... 58 13. Kadar amilosa tapioca kualitas I (Kw I), tapioca kualitas II (Kw II) dan
tapioca kualitas III (Kw III) pada berbagai waktu pengendapan ... 61 14. Kadar amilopektin tapioca kualitas I (Kw I), tapioca kualitas II (Kw II)
x
16. Kurva standar glukosa ... 125
17. Pengambilan bubur pati di bak pengendapan PD. Semangat Jaya ... 126
18. Bak pengendapan bubur pati berkapasitas 20 L ... 126
19. Pengeringan endapan pati di dalam oven suhu 60oC selama 5 jam ... 127
20. Tapioka yang telah dikeringkan pada berbagai lama pengendapan ... 127
21. Pengukuran absorbansi pada analisis kadar amilosa ... 128
22. Brabender micro viscoamylograph tapioca kualitas I pengendapan 0 jam ... 129
23. Brabender micro viscoamylograph tapioca kualitas I pengendapan 0 jam ... 130
24. Brabender micro viscoamylograph tapioca kualitas I pengendapan 10 jam ... 131
25. Brabender micro viscoamylograph tapioca kualitas I pengendapan 10 jam ... 132
26. Brabender micro viscoamylograph tapioca kualitas I pengendapan 15 jam ... 133
27. Brabender micro viscoamylograph tapioca kualitas I pengendapan 15 jam ... 134
28. Brabender micro viscoamylograph tapioca kualitas I pengendapan 20 jam ... 135
29. Brabender micro viscoamylograph tapioca kualitas I pengendapan 20 jam ... 136
30. Brabender micro viscoamylograph tapioca kualitas I pengendapan 25 jam ... 137
31. Brabender micro viscoamylograph tapioca kualitas I pengendapan 25 jam ... 138
32. Brabender micro viscoamylograph tapioca kualitas II pengendapan 0 jam ... 139
xi
34. Brabender micro viscoamylograph tapioca kualitas II pengendapan 10 jam ... 141 35. Brabender micro viscoamylograph tapioca kualitas II pengendapan 10 jam ... 142 36. Brabender micro viscoamylograph tapioca kualitas II pengendapan 15 jam ... 143 37. Brabender micro viscoamylograph tapioca kualitas II pengendapan 15 jam ... 144 38. Brabender micro viscoamylograph tapioca kualitas II pengendapan 20 jam ... 145 39. Brabender micro viscoamylographtapiokakualitas IIpengendapan20
jam………...146
40. Brabender micro viscoamylograph tapioca kualitas II pengendapan 25 jam ... 147 41. Brabender micro viscoamylograph tapioca kualitas II pengendapan 25 jam ... 148 42. Brabender micro viscoamylograph tapioca kualitas III pengendapan 0 jam
... 149 43. Brabender micro viscoamylograph tapioca kualitas III pengendapan 0 jam
... 150 44. Brabender micro viscoamylograph tapioca kualitas III pengendapan 10 jam
... 151 45. Brabender micro viscoamylograph tapioca kualitas III pengendapan 10 jam
... 152 46. Brabender micro viscoamylograph tapioca kualitas III pengendapan 15 jam
... 153 47. Brabender micro viscoamylograph tapioca kualitas III pengendapan 15 jam
... 154 48. Brabender micro viscoamylograph tapioca kualitas III pengendapan 20 jam
... 155 49. Brabender micro viscoamylograph tapioca kualitas III pengendapan 20 jam
xii
1
I. PENDAHULUAN
A. Latar Belakang dan Masalah
Permintaan tapioka di Indonesia cenderung terus meningkat. Peningkatan permintaan tersebut karena terjadi peningkatan jumlah industri makanan dan non-makanan yang menggunakan bahan baku tapioka dan juga peningkatan konsumsi rumah tangga. Konsumsi rumah tangga tapioka menurut data BPS (2012) meningkat dari 1,825 kg/kapita/tahun pada tahun 2008 menjadi 2,770 kg/kapita/tahun pada tahun 2011. Peningkatan konsumsi tapioka dalam negeri berbanding terbalik dengan produksi tapioka yang hanya mampu memenuhi kebutuhan beberapa wilayah di Indonesia, sehingga diperlukan impor tapioka untuk memenuhi kebutuhan tapioka dalam negeri. Menurut BPS (2013), impor tapioka Indonesia pada tahun 2012 mencapai 2 juta ton per tahun.
2
mendorong lahirnya lebih dari 70 industri tapioka yang ada di Provinsi Lampung dengan skala produksi dan tingkatan teknologi yang beragam yaitu mekanik sederhana, semi modern, danfull otomatic.
Salah satu industri yang mengolah ubi kayu menjadi tapioka dengan teknologi mekanik sederhana adalah Industri tapioka rakyat (ITTARA). Salah satu ITTARA yang masih bertahan dan berproduksi dengan baik di Provinsi Lampung adalah PD Semangat Jaya yang berlokasi di Kecamatan Negeri Katon Kabupaten Pesawaran. ITTARA ini masih menggunakan teknologi mekanik sederhana, sebagian proses produksi menggunakan mesin penggerak untuk melakukan pemarutan dan pengepresan, proses pemisahan pati dilakukan dengan pengendapan bubur singkong dan proses pengeringan mengandalkan bantuan sinar matahari. Teknologi proses produksi yang dimulai dari proses penerimaan bahan baku, pembersihan, pemotongan, pemarutan, penyaringan, pengendapan, pengeringan, pengayakan, pengemasan dan penggudangan ini diduga dapat mempengaruhi kualitas tapioka ITTARA.
3
mikroorganisme untuk hidup pada endapan pati sehingga diduga akan menyebabkan terjadinya fermentasi spontan yang mengarah pada modifikasi pati sehingga dapat mempengaruhi sifat fisikokimia tapioka yang dihasilkan ITTARA. Selama ini data karakteristik tapioka yang dihasilkan oleh ITTARA belum banyak dilaporkan. Oleh karena itu dalam penelitian ini dikaji apakah waktu pengendapan pati sebagai salah satu tahap pengolahan ubi kayu menjadi tapioka berpengaruh terhadap sifat fisikokimia tapioka yang dihasilkan ITTARA PD Semangat Jaya.
B. Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui pengaruh lama pengendapan terhadap sifat fisikokimia tapioka ITTARA PD Semangat Jaya pada setiap tingkat kualitas tapioka.
C. Kerangka Pemikiran
4
tapioka yaitu dengan melakukan modifikasi pati. Pati yang termodifikasi adalah pati yang telah mengalami perlakuan enzimatis, fisik atau kimia, sehingga merubah satu atau lebih dari sifat asalnya, seperti suhu awal gelatinisasi, ketahanan terhadap pemanasan, dan kecenderungan retrogradasi. Perubahan yang terjadi dapat terjadi pada level molekular dengan atau tanpa mengubah penampakan dari granula patinya (Moorthy, 2004).
Hasil pengamatan terhadap tapioka ITTARA dan tapioka yang ada di pasaran diketahui terdapat beberapa perbedaan atribut sensori seperti warna dan aroma. Tapioka yang ada dipasaran mempunyai warna lebih putih dibandingkan tapiokaITTARA (putih agak kekuningan). Aroma tapioka ITTARA juga lebih asam dibandingkan tapioka yang ada dipasaran. Perbedaan tersebut merupakan indikator terjadinya modifikasi pati selama proses pengendapan. Modifikasi dapat terjadi akibat adanya fermentasi spontan oleh mikroorganisme yang hidup pada endapan tapioka, sehingga menyebabkan perombakan struktur pati. Semakin lama waktu pengendapan menyebabkan proses fermentasi berlangsung semakin lama sehingga diduga mempengaruhi karakteristik tapioka yang dihasilkan.
bak-5
bak pengendapan. Proses fermentasi secara spontan oleh berbagai mikroba yang mungkin tumbuh dapat menyebabkan perubahan karakteristik dari tapioka yang dihasilkan, seperti naiknya visKositas, kemampuan gelasi, daya rehidrasi, dan kemampuan melarut (Pusparaniet al., 2014).
Fermentasi merupakan suatu aktivitas mikroorganisme terhadap senyawa molekul organic komplek menjadi molekul-molekul yang lebih sederhana, sehingga mempengaruhi sifat fungsional bahan tersebut. Selain itu fermentasi juga dapat menghidrolisis pati menjadi gula sederhana, mendegradasi amilosa dan amilopektin, merusak struktur dan integritas granula pati, sehingga merubah sifat pati alami. Menurut Zubaidah dan Irawati (2013), fermentasi asam laktat akan menghasilkan enzim yang berperan dalam pemutusan ikatan rantai cabang amilopektin dan rantai lurus amilosa, sehingga mempengaruhi rasio amilosa dan amilopektin dan kemudian akan mempengaruhi sifat fisikokimia pati seperti pH, derajat putih, kadar amilosa dan amilopektin,serta sifat amilograf pati. Oleh karena itu dalam penelitian ini dilakukan pengamatan pengaruh waktu pengendapan pati terhadap sifat fisikokimia tapioka yang dihasilkan pada setiap tingkatan kualitas tapioka di PD Semangat Jaya.
D. Hipotesis
6
II. TINJAUAN PUSTAKA
A. Ubi Kayu
Ubi kayu mempunyai banyak nama daerah diantaranya adalah ketela pohon, singkong, ubi jenderal, ubi inggris, telo puhung, kasape, bodin, telo jenderal (Jawa), sampeu, huwi dangdeur, huwi jenderal (Sunda), kasbek (Ambon), dan ubi prancis (Padang).Ubi kayu merupakan komoditi perdagangan yang mempunyai nilai ekonomis tinggi.Ubi kayu merupakan sumber bahan makanan ketiga di Indonesia setelah padi dan jagung yang potensial untuk dikembangkan terutama dipropinsi Lampung.Luas areal ubi kayu di Indonesia mencapai 915.459 Ha dengan luas panen 1.259.152 Ha dan produksi rata-rata mencapai 15,5 ton per Ha.Lampung yang merupakan sentra utama ubi kayu nasional mempunyai luas areal penanaman ubi kayu 298.989 Ha, Jawa Timur luas areal 240.493 Ha, Jawa Tengah 215.574 Ha, dan Jawa Barat 114.853 Ha.
Tanaman ubi kayu dalam sistematika (taksonomi) tumbuhan dilkasifikasikan sebagai berikut :
Kingdom :Plantae(tumbuh-tumbuhan) Divisio :Magnoliophyta
7
Famili :Euphorbiaceae
Genus :Manihot
Spesies :Manihot esculentaCrantz
Ubi kayu (Manihot esculenta) adalah tanaman dikotil berumah satu yang ditanam untuk dimanfaatkan patinya yang terkandung didalam akar lumbung (umbi) karena daya cernanya yang baik.Ubi berkembang dari penebalan sekunder akar serabut adventif.Bentuk umbi bermacam-macam dan kebanyakan berbentuk silinder dan meruncing, beberapa diantaranya bercabang.Bagian umbi yang mengecil dan berkayu menghubungkan ubi dengan batang.Daging bagian dalam berwarna putih dan ada juga yang berwarna kuning (Rukmana, 1997).Bagian dalam ubi kayu merupakan pembuluh xylem yang diselubungi oleh lapisan kambium, oleh karena itu bagian dalam ubi kayu keras meskipun banyak mengandung air.Pada bagian luar umbi, dibawah kulit terdapat lapisan gabus yaitu sel-sel yang mati (tidak berfungsi dalam sistem metabolisme).Baik kulit luar maupun sel-sel gabus berfungsi bagian dalam umbi (Heddy dan Kurniati, 1994).
Sebagai komoditi pertanian ubi kayu termasuk komoditas yang mudah rusak setelah dipanen.Setelah ubi kayu dipanen, jaringan sel ubi kayu masih hidup dan terus melakukan respirasi oleh sebab itu ubi kayu tidak mempunyai waktu simpan yang lama.Dalam jangka waktu 2-3 hari apabila tidak segera diproses atau dikonsumsi ubi kayu akan mengalami warna berubah menjadi kecoklatan atau kebiruan dan menimbulkan rasa tidak enak hingga akhirnya menjadi busuk yang disebabkan oleh aktivitas enzim yang terdapat didalam lendirnya (Wargionoet al.,
8
Umbi ubi kayu akan segera mengalami perubahan mutu setelah umbi dipotong dari tanaman. Perubahan mutu tersebut disebabkan perubahan komponen organik karena berlangsungnya proses biokimia atau disebabkan faktor-faktor lain yang mempengaruhinya. Akibat luka pada kedua ujung umbi dan luka lain yang mungkin terjadi waktu dipanen adalah pangkal utama percepatan kerusakan terutama kerusakan fisiologis dan mikrobiologis. Kerusakan umbi yang khas pada ubi kayu adalah kepoyoan. Kepoyoan mulai terlihat setelah umbi dipanen lewat 24 jam dan biasanya mulai dari bagian luka di kedua ujung atau luka lainnya terus menjalar ke bagian tengah umbi.
Umbi yang poyo ditandai oleh perubahan warna dari putih ke warna kehitaman atau bergaris-garis tipis hitam kebiruan. Kepoyoan bukan hanya akan menurunkan mutu cita rasa ubi kayu, tetapi juga mengurangi kadar patinya. Penurunan kadar pati tersebut disebabkan karena granula pati yang terkandung didalam umbi sebagian besar terdegradasi, sehingga banyak mengandung komponen-komponen non pati pada umbi tersebut. Hal ini tentu saja akan merugikan jika ubi kayu akan diambil patinya sebagai bahan baku dalam berbagai industri (Anonimous, 2007).
9
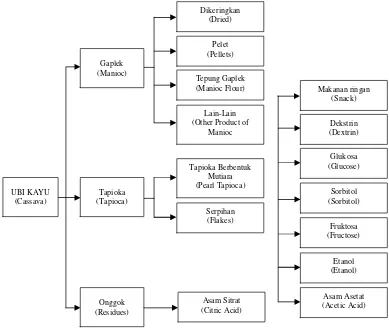
yang tidak beracun mengandung asam sianida kurang dari 50 mg/Kg ubi segar, akan tetapi yang beracun dapat sampai 250 mg/kg bahkan lebih. Ubi kayu dapat digunakan sebagai bahan baku pembuatan gula cair (High Fructose Syrup, glucose syrup), tapioka, modified starch dan alkohol. Pemanfaatan ubi menjadi berbagai produk seperti terlihat pada Gambar 1.
Gambar 1.Pohon industri pengolahan ubi kayu menjadi berbagai produk turunannya.Sumber : Wijanaet al.(2011)
Ubi kayu segar mengandung 35-40% bahan kering dan 90% diantaranya adalah karbohidrat. Ubi kayu dapat menghasilkan 150 kkal/100g bobot segar. Ubi kayu juga merupakan sumber vitamin C yang baik, mengandung 30-35 mg/100g bobot segar, dan biasanya rendah kandungan serat (1,4%) dan lemaknya (0,3%).
10
B. Pati
Pati merupakan komponen karbohidrat utama dalam ubi kayu.Kadar pati tertinggi dihasilkan setelah ubi kayu berumur 12 bulan. Pati terdapat dalam jumlah 64 sampai 72% dari total karbohidrat, sedangkan amilosa sejumlah 17 sampai 20% dari pati. Pati merupakan karbohidrat yang tersedia dalam jumlah besar sebagai makanan cadangan dalam tanaman, terdapat sebagai granula dalam plastisida sel dan terpisah dari sitoplasma (Wijandi, 1976) .
Pati merupakan homopolimer glukosa dengan ikatan α-glikosidik, yang banyak
terdapat pada tumbuhan terutama biji-bijian, umbi-umbian.Berbagai macam pati tidak sama sifatnya,tergantung dari panjang rantai atom karbonnya, serta lurus atau bercabang (Koswara, 2006; Pudjihastuti, 2011).Bentuk asli pati alamiadalah butiran-butiran kecil yang sering disebut granula.Bentuk dan ukuran granula merupakan karakteristik setiap jenis pati, karena itu digunakan untuk identifikasi.Pati tersusun paling sedikit oleh tiga komponen utama yaitu amilosa, amilopektin dan material antara seperti protein dan lemak.
Amilosa mempunyai struktur lurus yang didominasi dengan ikatan
11
Gambar 2. Struktur amilosa Sumber : Taggart (2004)
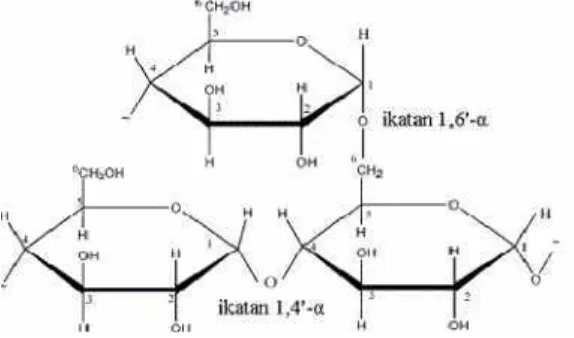
Amilopektin mempunyai titik percabangan dengan ikatan α-(1,6)-D-glukosa
disampingikatan α-(1,4)-D-glukosa pada rantai lurusnya, dan memiliki bobot
molekul yang besar. Amilopektinjuga dapat membentuk kristal, tetapi tidak sereaktif amilosa karena adanya rantaipercabangan yang menghalangi terbentuknya kristal (Taggart, 2004). Pati alami biasanya mengandung amilopektin lebihbanyak daripada amilosa (Flach, 1993). Struktur amilopektin disajikan pada Gambar 3.
12
C. Sifat Fisikokimia Pati
Pati merupakan polisakarida yang tidak mempunyai rasa manis dan merupakan jenis karbohidrat yang paling sering digunakan sebagai sumber energi dalam bentuk makanan pokok serta dalam bentuk jenis makanan lain. Dalam keadaan murni pati bewarna putih, tidak berbau dan tidak berasa (Winarno, 1997). Pati didalam tanaman dapat merupakan energi cadangan. Pati ubi kayu sangat cepat dikenal dan telah digunakan secara permanen dalam beberapa industri yang menggunakan pati, sedangkan jenis pati yang lain kurang mendapat tempat penting karena sifat pati ubi kayu yang unik. Pati ini dengan cepat akan tergelatinisasi oleh pemanasan dengan air dan larutannya setelah pendinginan secara komparatif tetap cair. Selanjutnya, larutan tersebut secara relatif lebih stabil dalam hal bahwa larutan tersebut tidak cepat memisah kembali ke bentuk yang tidak larut (insoluble form).
13
akan lebih baik bila dibandingkan dengan ukuran granula pati yang besar(Muhlis, 2003).
Bentuk butir pati secara fisik berupa semi kristal yang terdiri dari unit kristal dan unit amorf. Unit kristal lebih tahan terhadap perlakuan asam kuat dan enzim, sedangkan unit amorf sifatnya labil terhadap asam kuat dan enzim (Sajilata et al.,
2006). Perbandingan antara bagian amorf dan bagian kristalin serta jumlah ikatan cabang dalam setiap granula pati sangat menentukan kecepatan hidrolisis. Semakin tinggi bagian amorf dalam granula semakin mudah butiran pati tersebut terhidrolisis karena ikatan antar molekul pada bagian amorf tidak begitu kuat. Sebaliknya pada bagian kristalin ikatan antar molekul sangat kuat, sehingga lebih sukar untuk dihidrolisis (Sajilataet al.,2006).
14
Suhu padasaat granula pati pecah disebut suhu gelatinisasi dan besarnya berbeda tergantung pada jenis pati dankonsentrasinya (Winarno, 1991).Pengembangan granula pati disebabkan oleh molekul-molekul air yang melakukan penetrasi ke dalam granula dan terperangkap dalam susunan molekul-molekul amilosa dan amilopektin. Granula pati yang kaya akan amilosa mempunyai kemampuan untuk mengkristal lebih besar yang disebabkan oleh lebih intensifnya ikatan hidrogen.
D. Tapioka
Tapioka merupakan hasil ekstraksi pati ubi kayu (Manihot utilissima POHL.) yang mengalami pencucian sempurna dan dilanjutkan dengan pengeringan. Di Indonesia ubi kayu merupakan hasil pertanian pangan kedua terbesar setelah padi. Ubi kayu merupakan hasil produk pertanian yang potensinya tinggi sebagai sumber karbohidrat untuk bahan pangan dan industri (Rukmana, 1997).
15
Kandungan utamatapioka adalah karbohidrat dan memiliki sedikit protein dan lemak. Komposisi kimia tapioka dapat dilihat pada Tabel 1.
Tabel1. Komposisi kimia tapioka dalam 100 gram bahan
Komponen Jumlah (gram) Sumber : Direktorat Gizi Departemen Kesehatan RI, 2004.
Dalam Standar Nasional Indonesia (SNI), nilai pH tapioka tidak dipersyaratkan. Namun demikian, beberapa institusi mensyaratkan nilai pH untuk mengetahui mutu tapioka berkaitan dengan proses pengolahan. Salah satu pengolahan tapioka yang berkaitan dengan pH adalah pada proses pembentukan pasta. Menurut Winarno (2002), pembentukan gel optimum terjadi pada pH 4-7. Bila pH terlalu tinggi, pembentukan pasta makin cepattercapai tetapi cepat turun lagi.Sebaliknya bila pH terlalu rendah, pembentukan pasta menjadi lambat dan viscositasnya akan turun bila proses pemanasan dilanjutkan. The Tapioca Institute of America (TIA) menetapkan standar pH tapioka sekitar 4.5-6.6 (Radley, 1976).Syarat mutu tapioka sesuai SNI dapat dilihat pada Tabel 2.
16
Tabel 2.Syarat mutu tapioka berdasarkan SNI 3451:2011
No Kriteria Uji Satuan Persyaratan
6 Derajat Putih (MgO = 100) - Min.91
7 Derajat Asam mL NaOH 1 N/
100 gr
Maks.4 8 Cemaran Logam
8.1 Kadmium (Cd) Mg/kg Maks. 0,2
8.2 Timbal (Pb) Mg/kg Maks. 0,25
8.3 Timah (Sn) Mg/kg Maks. 40
8.4 Merkuri (Hg) Mg/kg Maks. 0,05
9 Cemaran Arsen (As) Mg/kg Maks. 0,5
Sumber : Badan Standarisasi Nasional, 2011.
E. Ekstraksi Tapioka
Tapioka berbentuk butiran atau granula yang banyak terdapat dalam sel umbi ubi kayu.Dengan cara memisahkan komponen granula pati inti dari komponen lainnya maka akan diperoleh tapioka.Perbedaan proses pembuatan tapioka industri besar biasanya dilakukan dengan menggunakan alat-alat atau mesin-mesin canggih berbeda dengan industri rumah tangga ataupun industri rakyat dimana proses dilakukan secara tradisional dengan menggunakan alat-alat yang sederhana.
17
pemurnian, pengeringan, pengayakan, pengemasan, dan penggudangan. Proses pengolahan tapioka di industri skala kecil pada umumnya dapat dilihat pada Gambar4.Secara garis besar ada empat tahapan yang harus dilakukan dalam proses ekstraksitapiokayaitu : 1) Tahap pemecahan sel dan pemisahan butiran pati dari unsur lain yang tidak larut, melalui kegiatan pengupasan, pencucian, pemarutan dan penyaringan; 2) Tahap pengambilan pati dengan penambahan air, termasuk juga perlakuan ini adalah proses pengendapan dan pencucian; 3) Tahap pembuangan atau penghilangan air. Untuk membantu kegiatan ini bisa dilakukan dengan pengeringan melalui panas dan pemusingan; 4)Tahap terakhir adalah melakukan penepungan agar diperoleh tepung yang dikehendaki. Kegiatan pembuatan tapiokaseperti terlihat pada Gambar 4.
1. Pemarutan
18
saringan ampas tertahan, sementara air yang mengandung pati ditampung dalam wadah pengendapan (Wijanaet al., 2011).
Gambar 4.Diagram alir proses pengolahan tapioka di skala kecil (dimodifikasi) Sumber :Wijanaet al.(2011)
Pengupasan kulit
Pencucian Umbi
Pemarutan
Pencucian
Penyaringan + air
Pengendapan Pati
Penjemuran
Penggilingan
Pengayakan Ubi Kayu
Onggok
Air buangan Air buangan
Kulit dan kotoran
Air
Air
19
2. Pengendapan
Pengendapan dimaksudkan memisahkan pati murni dari bagian lain seperti ampas dan unsur-unsur lainnya.Proses pengendapan masih terdapat butiran pati termasuk protein, lemak dan komponen lain yang stabil dan kompleks, sehinggaakan sulit memisahkan butiran pati dengan komponen lainnya. Bahkan butiran ini terdapat berbagai senyawa sehingga dapat menimbulkan bau yang khas.Senyawa alkohol dan asam organik merupakan komponen yang mempunyai aroma khas.Untuk menghindari bau dan perubahan yang tidak diinginkan, pengendapan diusahakan secepat mungkin. Untuk mempercepat pengendapan sering ditambahkan senyawa kimia tertentu seperti asam sulfat, alumunium sulfat, sulfur dioksida dan chlorin. Disamping membantu pengendapan, senyawa-senyawa tersebut juga dapat membantu proses pemutihan dari tepung yang akandiperoleh dan bersifat sebagai senyawa antimikroba untuk memperpanjang masa simpan tapioka.
3. Pengeringan
20
penghancuran ini masih berupa tepung kasar sedangkan yang kita butuhkan adalah tepung halus, untuk itu perlu diayak atau disaring.
Ayakan atau saringan sering kali dipasang bersamaan dengan saat penghancuran, dengan demikian hasilnya segera bisa diperoleh.Sementara butiran yang masih kasar dimasukkan lagi kedalam rol guna penggilingan, kemudian dilakukan penyaringan kembali.Pada penyaringan berikutnya akan diperoleh tapioka yang cukup halus dan segera dipaket/ dibungkus. Sebanyak 1.000 kg ubi kayu segaryang diolah akan dihasilkan 230-250 kg tapioka, 280-300 kg ampas (onggok) dan ±25 Kg meniran.
F. Fermentasi dan Modifikasi Tepung Ubi Kayu
Pada awalnya fermentasi diartikan sebagai pemecahan gula menjadi alkohol dan CO2.Kemudian pengertian tersebut berkembang sehingga pemecahan laktosa menjadi asam laktat oleh Streptococcus lactis dalam suasana anaerobik (kurang oksigen) juga diartikan sebagai fermentasi.
21
rasa dan bau alkohol; ketela pohon dan ketan akan menghasilkan bau alkohol dan asam (tape); serta susu akan menghasilkan bau dan rasa asam.
Berdasarkan penambahan starter (kultur mikroorganisme), fermentasi dibedakan atas dua jenis, yakni fermentasi spontan dan fermentasi tidak spontan. Fermentasi spontan adalah fermentasi yang berjalan alami, tanpa penambahan starter, misalnya fermentasi sayuran (acar/pikel, sauerkraut dari irisan kubis), terasi, dan lain-lain.Fermentasi tidak spontan adalah fermentasi yang berlangsung dengan penambahan starter/ragi, misalnya tempe, yoghurt, roti, dan lain-lain. Fermentasi ditujukan untuk memperbanyak jumlah mikroorganisme dan menggiatkan metabolismenya dalam makanan.Jenis mikroorganisme yang digunakan terbatas dan disesuaikan dengan produk akhir yang dikehendaki. Zat gizi lain juga dipecah menghasilkan CO2dan lain-lain.Hasil fermentasi tergantung pada jenis bahan pangan (substrat), jenis mikroorganisme, dan lingkungan.
Beberapa mikrobaberperan dalam fermentasi pangan antara lainbakteri asam laktat. Bakteri asam laktat adalah kelompok bakteri gram positif yang berbentuk batang atau bulat, katalase negatif, tidak membentuk spora, pada umumnya tidak motil tetapi ada beberapa yang motil, suhu pertumbuhan antara 20-40oC.Sifat-sifat khusus bakteri asam laktat adalah mampu tumbuh pada kadar gula, alkohol dan garam yang tinggi, tumbuh pada pH 3,8-8,0 serta memfermentasi berbagai monosakarida dan disakarida (Stamer, 1979).
22
(1) Obligat homofermentatif, artinya gula gula hanya bias difermentasi melalui jalur glikolisis, dan tidak bias mengkonsumsi pentose. Hampir seluruh produk yang dihasilkan oleh kelompok bakteri ini berupa asam laktat, contoh :L.acidophillus, L.delbruckii, L.helveticus.
(2) obligat heterofermentatif, artinya hanya jalur 6-phosphogluconate/phosphoketolase yang dapat digunakan untuk memfermentasi glukosa dengan hasil produk akhir berupa asam laktat, ethanol, asetat dan CO2.
(3) fakultatif heterofermentatif, artinya bisa melalui kedua jalur sebelumnya baik glikolisis maupun jalur 6-phosphogluconate/phosphoketolase. Kelompok ini mengkonsumsi heksosa dan pentose, contohnya L.casei, L.plantarum, L.curvatus dan L.sake(Salimen dan Wright, 1993).
Klasifikasi bakteri asam laktat pada tingkat genera didasarkan pada morfologi, model fermentasi gula, suhu pertumbuhan, kemampuan untuk tumbuh pada konsentrasi garam tinggi dan toleransi pada kondisi asam atau basa.Beberapa genera bakteri asam laktat meliputi Lactobacillus Spp., Lactococcus Spp., Leuconostoc Spp., Pedioccocus Spp., Aerococcus Spp., Enterococcus Spp.,
Carnobacterium Spp., Vagococcus Spp., dan Tetra genococcus Spp (Stamer, 1979).
23
manitol dan CO2.(Buchanan dan Gibons, 1986).Proses fermentasi yang umum dari tipe ini :
C6H2O6 CH3CHOHCHOH + CO2+C2H5OH
Glukosa Asam laktat Ethanol
Bakteri homofermentatif sering digunakan dalam pengawetan makanan karena jumlah asam yang tinggi dalam makanan dapat menghambat pertumbuhan bakteri lain.Bakteri asam laktat bersifat homofermentatif, misalnya Streptococcus faecalis, Streptococcus liquifaciens, Pediococcus cereviseae dan Lactobacillus
plantarum (Salminen dan Wrigth, 1993).Pada fermentasi heterofermentatif, senyawa-senyawa lain yang diproduksi seperti CO2, sedikit asam-asam volatil, alkohol dan ester. Pembentukan asam selama proses fermentasi akan mengakibatkan kondisi substrat semakin asam. Bakteri asam laktat tidak hanya berfungsi menurunkan pH media, tetapi juga menghasilkan antibiotik yang disebut bakteriosin, sehingga dapat menghambat pertumbuhan bakteri pembusuk.Selain itu, bakteri asam laktat juga memproduksi H2O2 dan produksi senyawa pembentuk aroma spesifik (Sudarmadji, 1989).
24
Selama proses fermentasi senyawa polifenol menjadi tidak aktif dalam pH yang rendah, dikarenakan senyawa polifenol memiliki sifat cenderung asam dan dapat melepaskan ion H+dari gugus OH, sehingga larut dalam air (Kartikaet al., 2004). Sebagian mikroorganisme yang tumbuh selama perendaman mempunyai kemampuan untuk menurunkan kadar pH akibat hasil metabolisme selama proses fermentasi dengan menghidrolisis karbohidrat sederhana menjadi asam, sehingga kandungan fenol menurun dan terdegradasi oleh enzim yang dikeluarkan oleh mikroorganisme yang tumbuh dengan cara merusak cincin aromatik senyawa fenol. Dalam proses degradasi fenol selanjutnya, mikroorganisme memanfaatkan fenol sebagai sumber karbon dan energi (Ferhan et al., 2002). Fenol terdegradasi
menjadi CO 2 dan H 2 O (Udiharto, 2002) sehingga reaksi pencoklatan dapat
dihindari.Reaksi browning enzimatis akan berjalan selama ada enzim (enzim PPO), substrat dan lingkungan yang sesuai. Kecil kemungkinan terjadi browning
enzimatis selama proses pengolahan karena enzim terhambat karena pH rendah dan fenol telah terdegradasi.
25
26
III. METODE PENELITIAN
A. Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Analisa Hasil Pertanian dan Laboratorium Limbah Jurusan Teknologi Hasil Pertanian Universitas Lampung dandi PD Semangat Jaya Kecamatan Negeri Katon Kabupaten Pesawaran. Penelitian dilaksanakan pada bulan Januari 2014 sampai April 2014.
B. BahandanAlat
Bahan yang digunakan dalam penelitian ini adalah tiga jenis tapioka basah yaitu tapioka kualitas 1, tapioka kualitas 2, dan tapioka kualitas 3, produksi ITTARA PD Semangat Jaya Kecamatan Negeri Katon Kabupaten Pesawaran.Bahan-bahankimia,sepertiHCl 25%, NaOH 45%, glukosa, fenol 5%, etanol, CH3COOH 1 N dan larutan Iod.
27
kaca preparat dan gelas penutup, erlenmeyer, pipet tetes, pipet gondok, gelas ukur merk Pyrex,Brabender visco amylograph,sentrifusemerk Hsiangtai.
C. MetodePenelitian
Penelitian dilakukan dalam dua bagian yaitu : 1. Observasi Lapang
Pengambilan data lapangan, yaitu semua data dan informasi, fakta petunjuk dan indikasi yang didapat dari hasil penyelidikan dan wawancara secara langsung di lapangan.Data digunakan untuk mendapatkan gambaran kondisi terkini di ITTARA PD Semangat Jaya meliputi jumlah produksi, kegiatan di industri, fasilitas dan proses pengolahan yang diterapkan.
2. Penelitian Laboratorium
28
perbedaan sifat kimia dan fisiologis tapioka pada setiap perlakuan waktu pengendapan.
D. PelaksanaanPenelitian
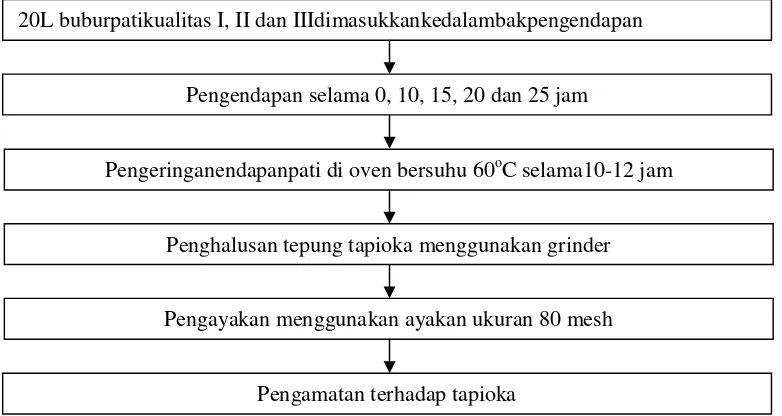
Penelitian dimulai dengan mengambil sampel bubur pati dari bak pengendapan di ITTARA PD Semangat Jaya pada jarak dari titik inlet yang berbeda, yaitu 0-30 meter sebagai pati tingkat kualitas I (G1), 30-60 meter kedua sebagai pati tingkat kualitasII (G2), dan 60-90 meter ketiga sebagai pati tingkat kualitasIII (G3). Selanjutnya sebanyak 20 L bubur pati tersebut diendapkan di dalam bak-bak plastik dengan masing-masing waktu yang berbeda yaitu 10 jam (P1), 15 jam (P2), 20 jam (P3), dan 25 jam (P4), sebagai control pengendapan 0 jam (P0). Pati yang didapat dikeringkan dengan menggunakan cabinet dryer dengan suhu 60oC selama 10-12 jam, kemudian dihaluskan dengan menggunakan grinder, diayak menggunakan ayakan yang berukuran 80 mesh kemudian dilakukan pengamatan. Diagram alir pelaksanaan penelitian disajikan pada Gambar 5.
Gambar 5. Pelaksanaan penelitian
20L buburpatikualitas I, II dan IIIdimasukkankedalambakpengendapan
Pengendapan selama 0, 10, 15, 20 dan 25 jam
Pengeringanendapanpati di oven bersuhu 60oC selama10-12 jam
Penghalusan tepung tapioka menggunakan grinder
Pengayakan menggunakan ayakan ukuran 80 mesh
29
E. Pengamatan
Pengamatan dilakukan pada saat proses pengendapan dan pengamatan setelah pati dikeringkan. Pengamatan terhadap nilai pH larutan dilakukan selama proses pengendapan, sedangkan pengamatan yang dilakukan setelah tapioka dikeringkan meliputi sifat fisik dan sifat kimia tapioka. Sifat fisik yaitu bentuk granula pati,sifat amilograf, derajatputih, dan nilai pH. Sifat kimia meliputi kadar air, kadar abu, kadar pati, dan kadar amilosa-amilopektin.
1. Derajat Keasaman (pH) Larutan dan Tapioka
Pengukuran nilai pH menggunakan metode dalam AOAC (1990) yaitu dengan menggunakanMettler Toledo MP220 pH meter. Pengukuran pH filtrat dilakukan pada awal waktu pengendapan (0 jam) dan pada akhir waktu pengendapan (10 jam, 15 jam, 20 jam, dan 25 jam). Sebanyak 25 melarutan filtrat dimasukkan dalam gelas piala 50 ml. Pengukuran nilai pH tepung menggunakan metode AOAC (1990). Sampel ditimbang sebanyak 5 gr dan dimasukkan ke dalam 10 ml aquades lalu dikocok sampai homogen.
30
2. Bentuk granula pati
Analisa granula pati dilakukan secara mikroskopis dengan Microscope binocular
merk Olympus. Tepungseberat0,5 gram ditempatkan pada slide, kemudian diberi setetes air dan diamati dibawah mikroskop dengan perbesaran sampai 400 kali. Dilakukan sebanyak dua kali per sampel.
3. Sifat Amilograf
Sifat amilografi tapioca diukur dengan menggunakan alat Brabender viscoamilograph OHG Duisburg Type 800121. Sampel ditimbang sebanyak 45 g, lalu dimasukkan ke dalam botol gelas yang volumenya 500 ml dan ditambahkan aquades sebanyak 450 ml. Kemudian campuran air dan pati dipindahkan ke dalam mangkuk amilograf yang telah terpasang pada alat Brabender viscoamilograph.
31
4. DerajatPutih
Derajat putih diukur dengan menggunakan alat Kett Electric laboratory C-100-3
Whitenessmeter. Sebelum digunakan alat dikalibrasi dengan standar derajat putih yaitu BaSO4, yang memiliki derajat putih 100%. Setelah dikalibrasi, derajat putih sampel dapat diukur dengan memasukkan sejumlah sampel dalam wadah sampel yang tersedia sampai benar-benar padat, kemudian wadah ditutup. Wadah yang telah berisi sampel dimasukkan kedalam tempat pengukuran lalu nilai derajat putih akan keluar pada layar (A). Derajat putih diukur dengan cara sebagai berikut :
5. Kadar air
Kadar air (AOAC, 1995) bahan pangan ditetapkan dengan tapioka ditimbang sebanyak 1-2 g dalam cawan yang telah diketahui beratnya. Kemudian sampel dikeringkan dalam oven pada suhu 100-105˚C selama 3-5 jam tergantung bahannya dan didinginkan dalam eksikator dan ditimbang. Sampel tersebut dipanaskan lagi dalam oven 30 menit, didinginkan dalam desikator dan ditimbang; perlakuan ini diulangi sampai tercapai berat konstan (selisih penimbangan berturut-turut kurang dari 0,2 mg). Pengurangan berat merupakan banyaknya air dalam bahan.
DP (%) = A x 100%
32
6. Kadar Abu
Kadar abu (AOAC, 1995) bahan pangan ditetapkan dengan menimbang sisa mineral hasil pembakaran bahan organikpadasuhu 550°C.Sejumlah 3-5 gram sampel ditimbang dan dimasukkan ke dalam cawan porselin yang telah dikeringkandandiketahuiberatnya. Kemudian cawan dan sampel tersebut dibakar dengan pemanas listrik dalam ruang asap sampai sampel tidak berasap dan diabukan pada tanur pengabuan pada suhu 550°C sampai dihasilkan abu yang berwarna abu-abu terang atau bobotnya telah konstan. Selanjutnya kembali didinginkan di desikator dan ditimbang segera setelah mencapai suhu ruang. Kadar abu sampel dapat dihitung dengan menggunakan rumus sebagai berikut : bobotsampel (g)
7. Kadar Pati
Analisis kadar pati dilakukan berdasarkan metode AOAC (1984).Sebanyak 2 gram tapioka dimasukkan kedalam Erlenmeyer, lalu ditambah aquades sampai volume 50 ml, kemudian disentrifius selama 15 menit dengan kecepatan 3000 rpm. Suspensi disaring dengan kertas saring, dan endapannya dicuci dengan
% Kadar Air =Beratawal (Beratbotoltimbang + Berat sample)–Beratakhir x 100% Berat sample
33
aquades sampai diperoleh filtrat sebanyak 250 ml. Endapan dipindahkan secara kuantitatif dari ketas saring Whatman no 42 kedalam Erlenmeyer 500 ml dengan pencucian menggunakan 200 ml aquades kemudian ditambahkan HCl 25% sebanyak 20 ml, dihidrolisis dengan dibawah pendingin balik selama 1,5 jam dan didinginkan. Selanjutnya dinetralkan dengan NaOH 45% dan dilakukan pengenceran sampai volumenya 500 ml, lalu disaring dengan kertas saring.
Sebelum penentuan kadar pati sampel, terlebih dahulu dibuat kurva standar dengan membuat larutan glukosa standar (10 mg glukosa anhidrat/100 ml air). Larutan glukosa standar tersebut dilakukan 6 pengenceran, sehingga diperoleh larutan glukosa dengan konsentrasi : 2,4, 6, 8, dan 10 mg/ 100 ml. Sebanyak 7 buah tabung reaksi bersih, masing-masing diisi dengan 1 mllarutan glukosa standar tersebut diatas. Satu tabung diisi dengan aquades sebagai blangko. Kemudian ke dalam tabung reaksi ditambahkan fenol 5% sebanyak 1 ml, dan ditambahkan asam sulfat pekat sebanyak 5 ml.Panaskan dengan penangas air pada suhu 30oC selama 20 menit. Kurva standar dibuat dengan cara menghubungkan antara konsentrasi glukosa dengan OD (Optical Density). Optical Density masing-masing larutan tersebutdibaca pada panjang gelombang 490 nm. Penentuan kadar pati sampel dilakukan seperti cara penentuan kurva standar glukosa. Jumlah kadar pati ditentukan berdasarkan OD larutan contoh dan kurva standar dan dihitung berdasarkan rumus berikut :
34
Keterangan :
A = Glukosa yang diperoleh dari kurva standar(mg/100ml) B = Volume sampel (ml)
C = Konsentrasi pengenceran larutan sampel D = berat sampel (gr)
0,9 = faktor penentu kadar pati
8. Kadar AmilosadanAmilopektin
Pengukuran kadar amilosa dilakukan secara iodometri berdasarkan reaksi antara amilosa dengan senyawa iod yang menghasilkan warna biru (Yuan, 2007).
PersiapanlarutanIod
Sebanyak 2 gram larutan Kalium Iodida (KI) dilarutkan ke dalam 50 ml air suling dalam gelas piala 100 ml, kemudian 0,2 gram Iodin dimasukkan dan dikocok dengan alat pengocok sampai larut. Larutan dipindahkan ke dalam labu ukur 100 ml, kemudian ditambahkan air suling sampai volume 100 ml, dikocok kembali sampai merata, sehingga diperoleh larutan I-KI 2%.
Pembuatan kurva standar amilosa
35
dalam labu takar 100 ml. Gel ditambahkan dengan aquades dan dikocok, kemudian ditepatkan hingga 100 ml dengan aquades.
Larutan diatas diambil kemudian dengan menggunakan pipet masing-masing sebanyak 1, 2, 3, 4, dan 5 ml lalu dimasukkan dalam labu takar 100 ml dan diasamkan dengan asam asetat 1 N sebanyak 0,2, 0,4, 0,6, 0,8 dan 1,0 ml. Ke dalam masing-masing labu takar ditambahkan 2 ml larutan iod 2% dan aquades sampai tanda tera. Larutan digoyang-goyang secara manual hingga merata dan dibiarkan selama 20 menit, kemudian diukur serapannya dengan spektrofotometer UV-Vis pada panjang gelombang 620 nm, dibuat kurva hubungan antara kadar amilosa dengan serapannya.
36
Keterangan :
A = Konsentrasi amilosa sampel yang diperoleh dari kurva standar (mg/100ml) B = Faktor konversi
C = Nilai konstanta sampel (100) D = Nilai konstanta - kadar air
Kadar amilopektin dihitung berdasarkan selisih antara kadar pati dan amilosa.
Kadar Amilosa (%) = x 100%
D C x B A x
V. KESIMPULAN
A. Kesimpulan
1. Lama pengendapan bubur pati tapioca tidak berpengaruh terhadap pH tepung, kadar air dan derajat putih tapioka ITTARA pada setiap tingkat kualitas yang diamati.
2. Lama pengendapan menurunkan pH filtrat, kadar pati,kadar amilosa dan amilopektin tapioka ITTARA pada setiap tingkat kualitas.
3. Lama pengendapan meningkatkan kadar abu, mempengaruhi sifat amilograf, merubah bentuk dan ukuran granula tapioka ITTARA pada setiap tingkat kualitas.
B. Saran
64
DAFTAR PUSTAKA
Aini. N., H. Purwiyatno, R. M. Tiendan. A. Nuri. 2010. Hubungan Antara Waktu Fermentasi Grits Jagung dengan Sifat Gelatinisasi Tepung Jagung Putih yang Dipengaruhi Ukuran Partikel. Jurnal Teknologi dan Industri Pangan. 21(1):18-23.
Anggraeni, P.Y. dan S.S. Yuwono. 2014. Pengaruh Fermentasi Alami Pada Chips Ubi Jalar (Ipomoea batatas) Terhadap Sifat Fisik Tepung Ubi Jalar Terfermentasi. Jurnal Pangan dan Agroindustri. 2(2):59-69. Anonim. 2007. Penanganan dan Pengolahan Ubi Kayu Modul 6. Digital Library.
Puslata Universitas Terbuka. Banten. 9 Februari 2008. Http://www. pustaka.ut.ac.id.
Anonim. 2010. Struktur Pati. http://kuliahpangan77.Wordpress.com / 2010 /04/14/telur/. Diakses pada tanggal 15 Agustus 2014.
AOAC. 1995. Official Methods of Analysis of The Association of Analytical
Chemist. Washington, DC.
Arisandi, F. 2010. Perubahan Granula dari Pati MOCAL (Modified Cassava Flour) sebagai Akibat Fermentasi Spontan. Jurnal Litbang Pertanian
23 (4):149.
Ayu, D.C. dan S.Y. Sudarminto. 2014. Pengaruh Suhu Blancing dan Lama Perendaman Terhadap Sifat Fisik Kimia Tepung Kimpul
(Xanthosomasagittifolium). Jurnal Pangan dan Agroindustri.
2(2):110-120.
Badan Pusat Statistik. 2011. Statistik Indonesia. http://www.bps.go.id. Jakarta. Diakses pada tanggal 11 September 2013.
Badan Pusat Statistik. 2012. Statistik Indonesia. http://www.bps.go.id. Jakarta . Diakses pada tanggal 11 September 2013.
65
Buchanan, R.E. and N.E. Gibbons. 1986. Bergey’s Manual of Systematic Bacteriology. William and Wilkin Baltimore. London.
Charles, A.L., Y.H. Chang, W.C. Ko, K. Sriroth, T.C. Huang. 2005. Influence of Amylopectin Structure and Amylose Content on The Gelling Properties of Five Cultivars of Cassava Starches. Jurnal Agric Food Chem 53 (7):2717-2725.
Departemen Kesehatan. 2004. Komposisi Zat Gizi Pangan Indonesia. DepartemanKesehatan RI:Direktorat Bina Gizi Masyarakat dan Pusat Penelitian dan Pengembangan Gizi.
Eliasson A.C, M.Gudmundsson. 1996. Starch: Physicochemical and Functional Aspects. Di dalam. Eliasson AC, editor.Carbohydrates in Food. New York: Marcel Dekker
Efendi, P.J. 2010. Kajian Karakteristik Fisik Mocaf (Modified Cassava Flour) dari Ubi Kayu (Manihotesculenta Crantz) Varietas Malang-I dan Varietas Mentega dengan Perlakuan Lama Fermentasi. Skripsi .Universitas Sebelas Maret. Surakarta.
Emanual, F. 2005. Karakteristik dan Modifikasi Pati. Teknologi Pati dan Gula. Hibah Penulisan Buku Ajar Tenaga Akademik Universitas Hasanuddin Makassar.
Epriliati, I., P. Hariyani, dan A. Apriyantono. 2002. Kajian Karakteristik dan Sifat Fungsional Pati Gayam (Inocarpus Edulis Forst). Jurnal Teknologi dan Industri Pangan. 13(2):32-40.
Febriyanti, T. 1990. Studi Karakteristik Fisik, Kimia, dan Fungsional Beberapa Varietas Tepung Singkong. Skripsi. IPB. Bogor.
Ferhan, M., Z. Ahmed, S. Riazuddin, M.I. RajokadanM. Khalik. 2002. Estimation and Removal Of Phenol In Pharmatical Industrial Effluents from Paracetamol an Aspirin Manufacturing Units. Journal of Biological Science. 2(9) : 587-590.
Flach, M. 1993. Problems and Prospects of Sago Palm Development.Sago Palm 1: 8-17.
Heddy, S., W. Hadi and M. Kurniati. 1994. Pengantar Produksi Tanaman dan Penanganan Pasca Panen. PT. Raja Grafindo Persada. Jakarta. 139-148.
66
Kostinek, M., I. Specht., V.A. Edward, C.Pinto, M. Egounlety, C.Sossa, S. Mbugua, C. Dortu, P. Thonart, L. Taljaard, M. Mengu, C.M.A.P. Franz and W.H. Holzapfel. 2007. Characterisation and biochemical properties of predominant lactic acid bacteria from fermenting cassava for selection as starter cultures. International Journal of Food Microbiology. 114:342–351.
Lay, W.G. 1989. Mikrobiologi. Buku Ajar Dasar-dasar Mikrobiologi. IPB Press. Bogor.
Medikasari, S.Nurdjanah, N. Yuliana dan N. Lintang.C.S. 2009. Sifat Amilografi Pasta Pati Sukun Termodifikasi Menggunakan Sodium Tripolifosfat.
Jurnal Teknologi Industri dan Hasil Pertanian. 14(2): 173-177.
Maryani, N. 2010. Studi Pembuatan Mie Kering Berbahan Baku Tepung Singkong dan MOCAL (modified cassava flour). Jurnal Sains Terapan. Institut Pertanian Bogor. Bogor.
Meyer,H. 1985. Food Chemistry. Reinhold Publishing Corporation. New York. Moorthy, S.N. 2004. Tropical Sources of Starch. In: Ann CE (ed). Starch in
Food: Structure, Function and Application. Florida: CRC Pr.
Muchtadi, T.P. dan Sugiyono. 1992. Ilmu Pengetahuan Bahan Pangan. Departemen Pendidikan dan Kebudayaan Dirjen Pendidikan Tinggi PAU Pangan dan Gizi. IPB.
Nazhrah. 2013. Pengaruh Proses Fisik dan Proses Kimia Terhadap Produksi Pati Resisten Pada Empat Varietas Ubi Kayu (Manihotesculenta). Skripsi. Universitas Sumatera Utara. Medan.
Ocloo.F.C.K, G. Otoo, R.M. Nkasah, T. Mahami, S. Odonkor and E. T. Quayson. 2011. Functional and Physicochemical Characteristics of Starch Obtained from Gamma-Irradiated Sweet Potato (Ipomeabatatas L.)
Jurnal of Agriculture and Food Technology. 1(7) : 116-122.
Oghenejoboh, K.M. 2012. Effects of Starch Fermentation on the Shelf-Lifeof Cassava Starch Based Adhesive. British Biotechnology Journal. 2(4): 257-268.
Ottaway, P.B. 1999. The Technology of Vitamins in Food. Aspen Publisher, Inc. Garthersburg. Marryland.
67
Pusparani.T dan S. Y. Sudarminta. 2014. Pengaruh Fermentasi Alami Chips Ubi Jalar Terhadap Sifat Fisik Tepung Ubi Jalar. Jurnal Pangan dan Agroindustri. Vol2(4):137-147.
Pomeranz. 1985. Functional Properties of Food Component. Academic Press, Inc.
Radley, J.A. 1976. Starch Production Technology. London: Applied Science. Rahman. 2007. Mempelajari Karakteristik Kimia dan Fisik Tepung Tapioka dan
MOCAL (Modified Cassava Flour) sebagai Penyalut Kacang pada Produk Kacang Salut. Skripsi. Institut Pertanian Bogor. Bogor.
Rachman, I.D. 2012. Studi Pembuatan “Tapioca Fermented Flour” (TFF) dengan Fermentasi Alami dan Penambahan Inokulum. Jurusan Teknologi Pertanian. FakultasPertanian. Universitas Hasanuddin. Makassar.
Rasulu, H. S. Yuwono,. Dan J.Kusnadi. 2012. Karakteristik Tepung Ubi Kayu Terfermentasi sebagai Bahan Pembuatan Sagukasbi. Jurnal Teknologi Pertanian. 13(1):1-7.
Richana, N. dan Widaningrum. 2009. Penggunaan Tepung dan Pasta dari beberapa varietas Ubi Jalar sebagai Bahan Baku Mi. Jurnal Pascapanen:43-52.
Rukmana RH. 1997. Ubi Kayu,Budidaya dan PascaPanen. Kanisius. Jakarta. 54 hal.
Sahlin P. 1999. Fermentation as a Method of Food Processing Production of Organic Acids , pH Developmentand Microbila Growth in Fermenting Cereals. Tesis. Lund Institute of Technology. Lund University.
Sajilata, M.G., R. S. Singhai and P. R. Kulkarni. 2006. Resistant Starch, Compreherensive Reviews In Food Science and Food Safety. Institute Of Food Technologist. Matunga, Mumbai. India. 5: 1-7.
Salim, Emil, 2011. Tepung Tapioka Solusi Atasi Ketergantungan Impor Terigu. Andi Offset: Yogyakarta.
Salminen, S. and A. V. Wright. 1993. Lactid Acid Bacteria. Marcel Dekker, Inc. New York.
68
Stamer, J. R. 1979. The Lactid Acid Bacteria. Microbes of Diversity. Food Technol. (1) : 60-65.
Stanier, R.Y., M. Doudorrf, and E.A. Adelberg. 1963. The Microbial World. Prentice-Hall Inc. Westport. Cennecticut.
Subagio, A. 2006. Ubi Kayu :Substitusi Berbagai Tepung-tepungan. Food Review Indonesia, April 2006:18-22.
Sudarmadji, S,R. Kasmidjo, Sardjono, D. Wibowo, S.Margino, dan E.S. Rahayu. 1989. Mikrobiologi Pangan. PAU Pangan dan Gizi Universitas Gadjah Mada. Yogyakarta.
Sunarti, T.C. dan P.D.Sari. 2012. Sour Cassava Starch Production by Spontaneous Fermentation. Institut Pertanian Bogor.
Swinkles, J.M. 1985. Source of Starch, Its Chemistry and Physics. In: Van Beynum, G.M.AA. and Roels, J.A. (eds). Starch Conversion Technology. Marcell Dekker, Inc. New York and Basel, p:295-360. Syamsir, E, P. Haryadi, D. Fardiat, N. Andar wulan dan F. Kusnandar. 2011.
Karakterisasi Tapioka Dari Lima Varietas Ubi Kayu (Manihot Utilisima Crantz) Asal Lampung. Jurnal Agrotek. 5 (1):93-105.
Taggart, P. 2004. Starch as an Ingredients : Manufacture and Applications. In: Ann CE (ed). Starch in Food : Structure, Function, and Application.
Florida: CRC Pr.
Tjokro Adikoesoemo, P.S. 1986. HFS dan Industri Ubi Kayu Lainnya. PT. Gramedia. Jakarta.
Udiharto, M. 2002. Degradasi Senyawa Karbon dan Fenol Dalam Air Buangan dari Suatu Lapangan Migas Pada Kondisi Statis. Proceeding : Seminar Nasional Teknologi Pengolahan Limbah dan Pemulihan Kerusakan Lingkungan-BPPT. BPPT. Jakarta : 176-186.
Vogel, R.F., M.A. Ehrman, and M.G. Ganzle, 2002. Development and Potential of Starter Lactobacilli Resulting from Exploration of the Sour Dough Ecosystem. Antonie van Leewwnhoek, 81 (1-4): 631-638.
Wargiono., J. Saraswati, J. Pasaribu, and Sutoro. 1990. Pengkajian dan Pengembangan Teknologi Pra dan Pascapanen Ubi Kayu 2. Prosiding Seminar Nasional UPT.EPG Lampung.
69
Wijana.S., N.Irnia dan N.Ika. 2011. Analisis Kelayakan Teknis dan Finansial Produksi Tapioka dari Bahan Baku Gaplek pada Skala Industri Kecil Menengah (Studi Kasus di Sentra Industri Tapioka Kabupaten Kediri, Jawa Timur). Jurnal Teknologi Pertanian. 12(2):130-137.
Wijandi, S. 1976. Ilmu Pengetahuan Bahan Umbi-umbian. Departemen Teknologi Hasil Pertanian Institut Pertanian Bogor. Bogor.
Winarno, F.G. 1983. Enzim Pangan. PT Gramedia Pustaka Utama. Jakarta. Winarno, F.G. 1991. Kimia Pangan dan Gizi.PT GramediaPustakaUtama.
Jakarta.
Winarno, F.G. 2002. Kimia Pangan. PT Gramedia Pustaka Utama. Jakarta. Yuan, Y., L. Zhang., Y. Dai and J. Yu. 2007. Physicochemical Properties Of
Starch Obtained From Dioscorea Nipponica Makino Comparison With Other Tuber Starches. J. Food Engineering. 82 : 436-442.
Yudi, A. 2011. Proses Fermentasi Pati Singkong Mentah oleh Lactobacillus plantarum B9(Kajian Jenis dan Konsentrasi Sumber Nitrogen). Skripsi. Universitas Brawijaya. Malang.
Zubaidah, E. dan N. Irawati. 2013. Pengaruh Penambahan Kultur (Aspergillus niger, Lactobacillus plantarum) dan Lama Fermentasi terhadap Karakteristik Mocaf. Jurnal Teknologi dan Hasil Pertanian. 11(3):43-46.