ABSTRACT
POTENTION TEST OF PAPAYA (Carica papaya L.) LEAVES EXTRACT AS LARVACIDE FOR Aedes aegypti MOSQUITO LARVAE INSTARS III
By
Anggia Putri Saraswati
Aedes aegypti is dengue fever vector mosquito which still be a public health problem in Indonesia. Chemical insecticides are the most commonly used as larvacide to control and eradicate Aedes aegypti. However, the long use of chemical larvicides can caused resistance for these vectors. Dangers of using chemical larvicides can be minimized by using natural larvicides, one of the plants is leaves of papaya plant (Carica papaya L.) which is known contains flavonoids and saponins that have potentially as larvicides. This research objective was to know about potention of papaya leaves extract as larvacide for Aedes aegypti, also to know about Lethal Concentration value (LC50 and LC90) and Lethal Time value (LT50 and LT90). The experiment research using a completely randomized design was conducted with five levels of concentration of the extract , which is 0.2 % ; 0.4 % ; 0.6 % ; 0.8 % ; and 1 % with 4 times repetition at each concentration. Then, was observed number of larvae that die every 5 , 10 , 20 , 40 , 60 , 120 , 240 , 480 , 1440 , 2880, and 4320 minutes . Hypothesis test of one-way ANOVA resulted p value (sig) = 0.002 because of p<0.05 accordingly larvicides potention in each concentration are different. In the post hoc Tukey analysis was known effective concentration than controls (0%) was 1%. Probit analysis result showed that LC50 value was 1,0% in 1440 minutes ; 0,8% in 2880 and 4320 minutes, as well as LT50 value obtained was 2278.73 minutes at a concentration of 1.0 %. While the LC90 and LT90 values in this study was not obtained . The results showed that papaya leaves extract is potential as larvicides for Aedes aegypti mosquito.
ABSTRAK
UJI POTENSI EKSTRAK DAUN PEPAYA (Carica papaya L.) SEBAGAI LARVASIDA TERHADAP LARVA NYAMUK Aedes aegypti INSTAR III
Oleh
Anggia Putri Saraswati
Aedes aegypti merupakan vektor penyakit Demam Berdarah Dengue (DBD) yang masih menjadi masalah kesehatan masyarakat di Indonesia. Upaya pengendalian dan pemberantasan Aedes aegypti saat ini banyak dilakukan, salah satunya dengan menggunakan larvasida kimiawi. Tetapi penggunaan larvasida kimiawi secara berkelanjutan menimbulkan resistensi pada nyamuk vektor. Diketahui daun tanaman pepaya (Carica papaya L.) mengandung flavonoid dan saponin yang berpotensi sebagai larvasida. Telah dilakukan penelitian yang bertujuan untuk mengetahui potensi dari ekstrak daun pepaya (Carica papaya L.), mengetahui nilai Lethal Concentration (LC50 dan LC90) dan Lethal Time (LT50dan LT90). Penelitian eksperimen yang menggunakan rancangan acak lengkap ini dilakukan dengan enam konsentrasi ekstrak, yaitu 0% sebagai kontrol; 0,2%; 0,4%; 0,6%; 0,8%; dan 1% dengan 4 kali pengulangan di setiap konsentrasi. Kemudian dilakukan pengamatan terhadap jumlah larva yang mati setiap 5, 10, 20, 40, 60, 120, 240, 480, 1440, 2880, dan 4320 menit. Dari hasil Uji ANOVA yang diuji lanjut dengan Uji BNT diketahui konsentrasi yang paling efektif dibandingkan kontrol (0%) adalah 0,6%. Dari analisis probit diperoleh nilai LC50 sebesar 0,8%, sedangkan untuk nilai LC90 sebesar 1,3%. Nilai LT50 dan LT90 dari penelitian ini adalah 2.278,73 (37,97 jam) dan 15.820,22 (263,67 jam). Kesimpulan dari penelitian ini adalah ekstrak daun pepaya (Carica papaya L.) berpotensi sebagai larvasida terhadap larva Aedes aegypti instar III, dan konsentrasi ekstrak yang paling efektif adalah konsentrasi sebesar 0,6%.
Uji Potensi Ekstrak Daun Pepaya (Carica papaya L.) sebagai Larvasida terhadap Larva Nyamuk Aedes aegypti Instar III
(Skripsi)
Oleh
ANGGIA PUTRI SARASWATI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
RIWAYAT HIDUP
Anggia Putri Saraswati dilahirkan di Pringsewu
pada tanggal 13 Februari 1993, anak pertama dari pasangan Bapak Drs. Januri dan Ibu Sri Rahayu, S.H. Penulis mengawali pendidikan pertama di
Taman Kanak-kanak Kartika II-31 pada tahun 1997.
Tahun 1998 penulis melanjutkan pendidikan di Sekolah Dasar Kartika II-6
Bandar Lampung. Setelah itu melanjutkan pendidikan di SMPN 9 Bandar Lampung pada tahun 2004 dan SMAN 14 Bandar Lampung pada tahun 2007. Tahun 2010 penulis terdaftar sebagai mahasiswa Jurusan Biologi Fakultas
Matematika dan Ilmu Pengetahuan Alam Universitas Lampung melalui jalur Ujian Mandiri.
Selama menjadi mahasiswa, penulis aktif dalam organisasi kampus, yaitu menjadi pengurus Himpunan Mahasiswa Biologi (HIMBIO) sebagai Anggota
Pada tahun 2013 penulis melaksanakan Kerja Praktik di Balai Besar Penelitian
dan Pengembangan Vektor dan Reservoir Penyakit Salatiga Jawa Tengah selama 40 hari dengan judul “ Kemampuan Predasi Mesocyclops aspericornis Betina terhadap Larva Aedes aegypti di Laboratorium Balai Besar Penelitian dan Pengembangan Vektor dan Reservoir Penyakit Salatiga Jawa Tengah ”.
Pada tahun 2014 untuk mencapai gelar Sarjana Biologi (S.Si.), penulis
melaksanakan penelitian dan menyelesaikan tugas akhirnya dalam bentuk
skripsi yang berjudul “ Uji Potensi Ekstrak Daun Pepaya (Carica papaya L.)
Karya sederhana ini
ku persembahkan untuk
keluargaku,
para pendidikku,
sahabat-sahabatku,
“Dan bahwasanya setiap manusia itu tiada akan
memperoleh (hasil) selain apa yang telah di
usahakanya”
(QS.An-Najm-39)
“
Gagal di dalam kemuliaan itu lebih baik,
ketimbang menang di dalam rasa kehinaan dan kecurangan”
SANWACANA
Assalamualaikum Wr. Wb.
Alhamdulillah, puji syukur penulis haturkan kepada Allah SWT yang tidak
pernah berhenti mencurahkan kasih sayang, kesabaran, serta rahmat-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul “Uji Potensi Ekstrak Daun Pepaya (Carica papaya L.) sebagai Larvasida terhadap Larva Nyamuk Aedes aegypti Instar III”.
Penulis telah banyak menerima bantuan dan bimbingan dari berbagai pihak dalam penyusunan skripsi ini. Untuk itu penulis ingin menyampaikan rasa
terima kasih kepada:
1. Ibu Dra. Endah Setyaningrum, M.Biomed. selaku Pembimbing Satu
yang telah dengan sabar membimbing dan meluangkan waktunya untuk memberikan ide, nasihat, kritik, dan saran selama penulisan skripsi ini. 2. Ibu Dra. Ellyzarti, M.Sc. selaku Pembimbing Dua yang telah dengan
3. Bapak Tugiyono, Ph.D. selaku Pembahas yang telah banyak
membimbing dan meluangkan waktu untuk memberikan masukan-masukan yang bermanfaat dalam penulisan skripsi ini.
4. Bapak Prof. Suharso, Ph.D. selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung.
5. Ibu Dra. Nuning Nurcahyani, M.Sc. selaku Ketua Jurusan Biologi
FMIPA Universitas Lampung yang telah memberikan dukungan dan motivasi serta memberikan izin kepada penulis untuk melakukan
penelitian dan penyusunan skripsi.
6. Ibu Elly L. Rustiati, M.Sc. selaku Pembimbing Akademik.
7. Bapak dan Ibu dosen yang telah membekali penulis dengan berbagai ilmu pengetahuan, serta segenap karyawan di Jurusan Biologi FMIPA Universitas Lampung atas bimbingan dan bantuannya kepada penulis.
8. Ibuku tercinta yang tiada henti memberikan kasih sayang, dukungan, nasihat, dan doanya selama ini.
9. Adikku M. Prama Yudha yang selalu memberikan semangat dan doa.
10. Sahabat-sahabat terbaikku Biologi 2010, Arinjani D.H., Dewi Chusniasih, Ismalia Husna, Meita Mahardianti, Rika Erviana, Rodi
Astuti, Septina Maulida dan Yunita Lestari yang telah memberikan semangat, keceriaan, dan bantuannya selama ini.
11. Teman seperjuangan, Ismalia Husna, terima kasih atas bantuan dan
motivasinya hingga skripsi ini dapat terselesaikan.
12. Teman-teman Kerja Praktik, Yunita Lestari, Ismalia Husna, dan Sasono
13. Teman-teman KKN-Tematik Desa Mulyosari, Ridho Hasyanah, Fani
Pangaribuan, Indah Aprianti, Wayan Diatniti, Cinthya C.D.I., Febrina J.D., Obby Chandra, Julian F., Andrew Charlos A., M. Kafi. Terima
kasih atas kebersamaannya selama ini.
14. Teman-teman Biologi angkatan 2010, kakak tingkat, dan adik tingkat di Jurusan Biologi terima kasih atas dukungan dan kebersamaannya.
15. Semua pihak yang tidak dapat penulis sebutkan satu persatu yang telah membantu terselesaikannya skripsi ini.
Akhir kata penulis menyadari bahwa skripsi ini masih jauh dari
kesempurnaan, akan tetapi sedikit harapan semoga skripsi ini bermanfaat bagi kita semua.
Wassalamualaikum Wr. Wb. Bandar Lampung, 20 Mei 2014
Penulis
DAFTAR ISI
IV. HASIL PENGAMATAN DAN PEMBAHASAN ... 31
A. Hasil Pengamatan ... 31
1. Uji Larvasida ... 31
2. Lethal Concentration 50% (LC50) dan 90% (LC90) ... 35
3. Lethal Time 50% (LT50) dan 90% (LT90) ... 38
B. Pembahasan ... 39
1. Uji Larvasida ... 39
2. Lethal Concentration 50% (LC50) dan 90% (LC90) ... 43
3. Lethal Time 50% (LT50) dan 90% (LT90) ... 44
V. KESIMPULAN ... 47
A. Simpulan ... 47
B. Saran ... 48
DAFTAR PUSTAKA ... 48
LAMPIRAN ... 53
Lampiran 1 ... 53
Lampiran 2 ... 54
Lampiran 3 ... 55
Lampiran 4 ... 56
DAFTAR TABEL
Tabel Halaman
1. Persentase rata-rata kematian larva Aedes aegypti pada berbagai
konsentrasi ekstrak daun pepaya (Carica papaya L.) ... 32 2. Hasil Analisis dengan ANOVA……….. 34 3. Rata – rata Jumlah Kematian Larva Aedes aegypti Setelah Diberi
Ekstrak Daun Pepaya (Carica papaya L.) ... 34 4. Persentase Rata-rata Nilai LC50 dan LC90 Larva Aedes aegypti…..… 36 5. Nilai LT50 dan LC90 kematian larva Ae. aegypti………... 38 6. Jumah Kematian Larva Aedes aegypti Setelah Diberi Ekstrak
Daun Pepaya (Carica papaya L.)………..….. 54 7. Uji BNT Terhadap Larva Aedes aegypti Setelah Diberi Ekstrak
Daun Pepaya……….... 57
8. Uji BNT Terhadap Larva Aedes aegypti Berdasarkan Lamanya
Waktu Kontak dengan Ekstrak Daun Pepaya……… 57 9. Uji BNT Terhadap Larva Instar III Aedes aegypti Berdasarkan
Interaksi Antara Konsentrasi Ekstrak Daun Kemangi Hutan dan
DAFTAR GAMBAR
Gambar Halaman
Gambar 1. Tanaman Pepaya………..…….. ………. 10
Gambar 2. Daun Tanaman pepaya……………… ……….. 12
Gambar 3. Nyamuk Aedes aegypti ………... 16
Gambar 4. Telur Larva Aedes. aegypti……….………...…………. 19
Gambar 5. Larva Aedes aegypti ……… 20
Gambar 6. Pupa Aedes aegypti……… ………… 21
Gambar 7. Respon konsentrasi ekstrak daun pepaya terhadap kematian larva uji dalam 4320 menit (72 jam)……….. 33
Gambar 8. Nilai LC50 Ekstrak Daun Pepaya dari menit pengamatan ke-480 sampai menit ke-4320………...…………. 37 Gambar 9. Nilai LC90 Ekstrak Daun Pepaya dari menit Pengamatan ke-480 sampai menit ke-4320……….... 37
Gambar 10. Nilai LT50 pada setiap konsentrasi……… 39
Gambar 11. Daun Pepaya yang Telah Dikering-anginkan……….. 66
Gambar 12. Cacahan Daun Pepaya yang Direndam dalam Etanol 96%... 66
Gambar 13. Proses Penyaringan Hasil Rendaman Daun Pepaya…………. 67
Gambar 14. Rotary evaporator yang Digunakan untuk Menguapkan Pelarut Etanol Ekstrak Daun Pepaya……... 67
Gambar 15. Proses Pengenceran Ekstrak Daun Pepaya……….. 68
Gambar 17. Penetasan Telur Aedes aegypti dalam Media Air………. 69 Gambar 18. Konsentrasi Ekstrak Daun Pepaya yang Digunakan
dalam Uji Sesungguhnya………. 69 Gambar 19. Pengambilan Larva Aedes aegypti yang Mati……….. 70 Gambar 20. Larva Aedes aegypti yang telah Terpapar
I. PENDAHULUAN
A. Latar Belakang
Indonesia merupakan salah satu negara yang beriklim tropis, dimana negara dengan iklim tropis ini hanya memiliki dua musim, yaitu musim penghujan
dan musim kemarau. Pergantian musim yang terjadi sangat berpengaruh terhadap perkembangbiakan nyamuk, terutama saat pergantian musim
kemarau ke musim penghujan. Di Indonesia banyak hidup berbagai jenis nyamuk yang berbahaya seperti nyamuk Aedes aegypti, Aedes albopictus, Aedes scutellaris, Aedes polymensiensis, Anopheles sp. dan lain-lain. Nyamuk yang paling berbahaya dan banyak ditemukan disekitaran lingkungan masyarakat adalah nyamuk Aedes aegypti (Nuryadin, 2010).
Nyamuk Aedes aegypti merupakan nyamuk penyebab penyakit demam berdarah dengue (DBD) yang masih menjadi masalah kesehatan masyarakat
di Indonesia. Jumlah penderita DBD dari tahun ke tahun terus meningkat dan penyebarannya pun semakin meluas karena cepatnya proses penularan, serta
2
Aedes aegypti mendapatkan virus dengue sewaktu menggigit atau menghisap darah orang yang sakit DBD, kemudian kembali menggigit orang yang sehat sehingga orang tersebut tertular (Depkes RI, 2007).
Beragam cara telah dilakukan untuk memberantas nyamuk penyebab penyakit demam berdarah ini, diantaranya dengan menggunakan insektisida kimiawi
seperti temephos (abate). Namun penggunaan insektisida kimiawi secara terus-menerus akan menimbulkan dampak kontaminasi residu dalam air.
Selain itu penggunaan insektisida kimiawi memerlukan biaya yang cukup besar, serta dapat menimbulkan resistensi pada berbagai spesies nyamuk
vektor penyakit (Panghiyangani et al, 2012). Di berbagai negara seperti Bolivia, Argentina, Brazil, Karibia , Kuba, Thailand, bahkan Indonesia dilaporkan telah terjadi resistensi larva Aedes aegypti terhadap temephos (Raharjo, 2006).
Cara pengendalian secara biologi juga telah banyak dilakukan, contohnya
dengan menggunakan berbagai agen pengendali hayati seperti : Mesocyclops aspericornis, Romanomermis iyengari, dan Bacillus thuringiensis. Upaya lain yang dapat dilakukan adalah dengan cara pengelolaan lingkungan, seperti mengubur kaleng-kaleng bekas, menguras dan menutup penampungan air, atau dengan pemasangan kelambu(Panghiyangani et al, 2012).
Penggunaan insektisida dalam memberantas nyamuk vektor dinilai lebih
3
yang ditimbulkan sangat cepat. Salah satu solusi pemecahan masalah yang
ditimbulkan akibat penggunaan insektisida kimiawi adalah dengan menggunakan insektisida nabati. Hal ini dikarenakan aplikasi insektisida
nabati pada umumnya tidak menyebabkan resistensi nyamuk vektor dan tidak menimbulkan residu sehingga aman bagi kesehatan manusia
(Hamijaya dan Asikin, 2005).
Menurut Subiyakto (2005), insektisida nabati dapat dibuat dari beberapa
bagian tanaman, yakni berupa akar, umbi, batang, daun, biji dan buah dengan teknologi sederhana, seperti berupa larutan hasil perasan, perendaman,
ekstrak, dan rebusan. Salah satu tanaman yang dapat dijadikan insektisida nabati adalah tanaman pepaya (Carica papaya L.). Daun pada tanaman pepaya memiliki kandungan bahan aktif seperti enzim papain, alkaloid
karpaina, flavonoid, pseudokarpaina, glikosid, karposid, saponin, sakarosa, dekstrosa, dan levulosa (Dalimarta dan Hembing, 1994). Bahan aktif yang terkandung pada daun pepaya tersebut dapat mempengaruhi beberapa
aktifitas fisik serangga, seperti penghambatan aktifitas makan, pernapasan, pertumbuhan dan perkembangan, serta kematian atau mortalitas serangga
(Dadang dan Prijono, 2008).
Penelitian yang dilakukan Alboneh (2012) memberikan hasil bahwa ekstrak
4
nyamuk dewasa sehingga dapat menyebabkan kematian. Hasil penelitian
menunjukkan bahwa ekstrak etanol daun pepaya dengan metode elektrik pada konsentrasi 25% memiliki efek insektisida yang lebih besar jika dibandingkan
dengan konsentrasi 20% dan 15%.
Berdasarkan hasil penelitian Utomo et. al (2010), zat papain yang terkandung dalam tanaman papaya berperan dalam proses pemecahan jaringan ikat (proteolitik) dan juga apabila masuk ke dalam tubuh larva nyamuk Aedes aegypti akan menyebabkan terhambatnya hormon pertumbuhan. Selain itu, alkaloid karpaina yang terkandung juga bersifat toksik terhadap larva Aedes aegypti. Disebutkan juga dalam hasil penelitiannya bahwa dosis serbuk biji pepaya yang paling efektif adalah 200 mg/100 ml karena dapat membunuh 100 % larva Aedes aegypti setelah pemaparan 24 jam.
Penelitian lain yang dilakukan oleh Wicaksana tahun (2012), menyebutkan bahwa air perasan buah pepaya (Caricapapaya L.) dengan metode elektrik mempunyai efek sebagai insektisida nyamuk dewasa Culex sp. dan dengan konsentrasi 70% dapat mengakibatkan kematian nyamuk Culex sp. dewasa hingga 97%. Diketahui juga jika semakin tinggi konsentrasi yang digunakan maka makin tinggi pula tingkat kematian nyamuk.
Krishna et. al.( 2008) mengemukakan bahwa bagian tanaman buah pepaya seperti akar, daun, buah , dan biji mengandung bahan aktif yang dapat
5
nyamuk Aedes aegypti adalah dengan cara membunuh larvanya, sehingga dapat memutus siklus hidup nyamuk tersebut (Nurhasanah, 2001). Berdasarkan hal-hal tersebut, peneliti tertarik melakukan penelitian untuk
menguji potensi ekstrak etanol daun pepaya (Carica papaya L.) sebagai larvasida terhadap larva nyamuk Aedes aegypti instar III.
B. Tujuan Penelitian
1. Penelitian ini bertujuan untuk mengetahui potensi ekstrak daun pepaya (Carica papaya L.) sebagai larvasida terhadap larva nyamuk Aedes aegypti instar III.
2. Mengetahui Lethal Concentration 50% (LC50) dan Lethal Concentration 90% (LC90) ekstrak daun pepaya (Carica papaya L.) sebagai larvasida terhadap larva nyamuk Aedes aegypti instar III.
3. Mengetahui Lethal Time 50% (LT50) dan Lethal Time 90% (LT90) ekstrak daun pepaya (Carica papaya L.) sebagai larvasida terhadap larva nyamuk Aedes aegypti instar III.
C. Manfaat Penelitian
Adapun manfaat dari penelitian ini adalah
6
2. Memberikan informasi ilmiah bagi peneliti mengenai potensi ekstrak
daun papaya (Carica papaya L.) sebagai larvasida terhadap larva nyamuk Aedes aegypti dan dapat mengembangkan wawasan ilmu bagi peneliti. 3. Memberikan informasi bagi masyarakat bahwa ekstrak daun papaya
(Carica papaya L.) dapat digunakan sebagai larvasida dalam usaha menurunkan angka kejadian Demam Berdarah Dengue (DBD) di
Indonesia.
D. Kerangka Pikir
Indonesia yang beriklim tropis sering kali mengalami pergantian musim yang sangat berpengaruh terhadap perkembangbiakan nyamuk, terutama saat pergantian musim kemarau ke musim penghujan. Di Indonesia banyak hidup
berbagai jenis nyamuk yang berbahaya, salah satunya nyamuk Aedes aegypti. Aedes aegypti merupakan nyamuk penyebab penyakit demam berdarah dengue (DBD) yang masih menjadi masalah kesehatan masyarakat di
Indonesia. Melalui gigitannya, nyamuk Aedes aegypti menularkan virus dengue penyebab penyakit DBD.
Penggunaan insektisida kimiawi sebagai salah satu upaya pengendalian vektor penyebab DBD secara terus-menerus dapat menimbulkan dampak
7
sebagai solusi pemecahan masalah yang ditimbulkan oleh insektisida
kimiawi, karena insektisida nabati aman bagi kesehatan manusia.
Berdasarkan beberapa hasil penelitian, ekstrak daun pepaya (Carica papaya L.) dapat dijadikan sebagai insektisida nabati karena memiliki kandungan bahan aktif seperti enzim papain, alkaloid karpaina, dan flavonoid, yang dapat
mempengaruhi beberapa aktifitas fisik serangga, seperti penghambatan aktifitas makan, pernapasan, pertumbuhan dan perkembangan, serta kematian
serangga. Belum ada penelitian tentang ekstrak etanol daun pepaya (Carica papaya L.) sebagai larvasida terhadap larva nyamuk Aedes aegypti instar III. Digunakan larva Aedes aegypti instar III karena pada fase ini intensitas makan larva lebih tinggi sehingga larva lebih sering membuka mulut dan juga karena ukuran tubuhnya yang besar sehingga mudah untuk diamati.
Pembuatan ekstrak daun pepaya dilakukan dengan metode maserasi, yaitu dengan merendam cacahan daun pepaya yang sudah dikeringkan dengan cara
diangin-anginkan sebanyak 300 gram dengan 2,5 L pelarut etanol 96% selama 24 jam. Kemudian hasil rendaman disaring dan dipekatkan. Untuk
mendapatkan tingkat konsentrasi yang paling efektif, maka dibuatlah pengenceran dengan akuades dengan konsentrasi yaitu 0% sebagai kontrol, 0,2%; 0,4%; 0,6%; 0,8%; dan 1% (konsentrasi ditentukan berdasarkan uji
8
Kemudian dilakukan pengamatan hingga 72 jam setelah diberikan
pemaparan, lama waktu pengamatan disesuaikan dengan kriteria WHO tahun 2005. Pengamatan dilakukan dengan menghitung dan mencatat jumlah larva
yang mati, untuk kemudian dihitung presentase rata-rata kematian larva pada setiap kelompok perlakuan. Data yang telah diperoleh lalu dianalisis dengan menggunakan analisis ANOVA dan analisis probit.
E. Hipotesis
1. Semakin tinggi konsentrasi ekstrak daun pepaya (Carica papaya L.) yang diberikan akan menimbulkan kematian yang tinggi pada larva nyamuk Aedes aegypti instar III.
2. Nilai LC50 dan LC90 ekstrak daun pepaya (Carica papaya L.) sebagai larvasida terhadap larva Aedes aegypti terjadi pada konsentrasi di atas 0,2%.
II. TINJAUAN PUSTAKA
A. Pepaya (Carica papaya L.)
1. Klasifikasi Tanaman Pepaya
Klasifikasi tanaman pepaya adalah sebagai berikut (Yuniarti, 2008):
Regnum : Plantae
Divisi : Spermatophyta Class : Dicotyledoneae
Ordo : Cistales Family : Caricaceae Genus : Carica
Species : Carica Papaya L.
2. Karakteristik Tanaman Pepaya
Pepaya (Carica papayaL.) merupakan tanaman yang berasal dari Amerika Tengah. Pepaya dapat tumbuh dengan baik di daerah yang
10
disebarluaskan ke berbagai penjuru dunia. Negara penghasil pepaya
antara lain Costa Rica, Republik Dominika, Puerto Riko, dan lain-lain. Brazil, India, dan Indonesia merupakan penghasil pepaya yang cukup
besar (Warisno, 2003).
Haryoto (1998) mengatakan bahwa tanaman papaya (Carica papaya L.) baru dikenal secara umum sekitar tahun 1930 di Indonesia, khususnya
dikawasan Pulau Jawa. Tanaman pepaya ini sangat mudah tumbuh di berbagai cuaca. Menurut Warisno (2003), tanaman pepaya merupakan
herba menahun, dan termasuk semak yang berbentuk pohon. Batang, daun, bahkan buah pepaya bergetah, tumbuh tegak, dan tingginya dapat mencapai2,5-10 m. Batang pepaya tak berkayu, bulat, berongga, dan
tangkai di bagian atas terkadang dapat bercabang (Gambar 1). Pepaya dapat hidup pada ketinggian tempat 1 m-1.000 m dari permukaan laut
dan pada kisaran suhu 22°C-26°C.
11
Dalimartha dan Hembing (1994) mengatakan bahwa pada tanaman
pepaya daunnya berkumpul di ujung batang dan ujung percabangan, tangkainya bulat silindris, juga berongga, panjang 25-100 cm. Helaian
daun bulat telur dengan diameter 25-75 cm, daun berbagi menjari, ujung daun runcing, pangkal berbentuk jantung, warna permukaan atas hijau tua, permukaan bawah warnanya hijau muda, tulang daun menonjol di
permukaan bawah daun. Bunga jantan berkumpul dalam tandan,
mahkota berbentuk terompet, warna bunganya putih kekuningan. Pepaya
memiliki bermacam-macam bentuk, warna, dan rasa. Pepaya muda memiliki biji yang berwarna putih sedangkan yang sudah matang
berwarna hitam. Tanaman ini dapat berbuah sepanjang tahun dimulai pada umur 6-7 bulan dan mulai berkurang setelah berumur 4 tahun.
3. Kandungan Kimia Daun Pepaya
Dari beberapa kandungan yang ada pada daun pepaya tersebut yang diduga memiliki potensi sebagai larvasida adalah enzim
papain, saponin, flavonoid, dan tanin (Priyono, 2007).
a. Enzim Papain
Enzim papain adalah enzim proteolitik yang berperan dalam
12
ikatan peptida dalam protein sehingga protein akan menjadi terputus
(Nani dan Dian, 1996).
Enzim papain dapat banyak ditemukan pada daun pepaya (Gambar 2). Walaupun dalam dosis yang rendah, dan apabila enzim papain masuk ke dalam tubuh larva nyamuk Aedes aegypti akan
menimbulkan reaksi kimia dalam proses metabolisme tubuh yang dapat menyebabkan terhambatnya hormon pertumbuhan. Bahkan
akibat dari ketidakmampuan larva untuk tumbuh akibatnya dapat menyebabkan kematian pada larva (Nani dan Dian, 1996).
Gambar 2. Daun tanaman pepaya ( Sumber : Koleksi Pribadi )
b. Flavonoid
13
flavonoid yaitu memiliki bau yang sangat tajam, rasanya yang pahit,
dapat larut dalam air dan pelarut organik, dan juga mudah terurai pada temperatur tinggi. Dinata (2008), mengatakan bahwa flavonoid
merupakan senyawa yang dapat bersifat menghambat makan serangga. Flavonoid berfungsi sebagai inhibitor pernapasan sehingga menghambat sistem pernapasan nyamuk yang dapat
mengakibatkan nyamuk Aedes aegypti mati (Dinata, 2008). Bagi tumbuhan pepaya itu sendiri flavonoid memiliki peran sebagai
pengatur kerja antimikroba dan antivirus.
c. Saponin
Senyawa lainpada daun pepaya yang memiliki peran sebagai
insektisida dan larvasida adalah saponin. Saponin merupakan senyawa terpenoid yang memiliki aktifitas mengikat sterol bebas dalam sistem pencernaan, sehingga dengan menurunnya jumlah
sterol bebas akan mempengaruhi proses pergantian kulit pada serangga (Dinata, 2009).
Saponin terdapat pada seluruh bagian tanaman pepaya seperti akar, daun, batang, dan bunga. Senyawa aktif pada saponin
14
permukaan sehingga dapat merusak membran sel serangga
(Mulyana, 2002).
d. Tanin
Tanin merupakan salah satu senyawa yang termasuk ke dalam
golongan polifenol yang terdapat dalam tanaman pepaya.
Mekanisme kerja senyawa tanin adalah dengan mengaktifkan sistem
lisis sel karena aktifnya enzim proteolitik pada sel tubuh serangga yang terpapar tanin (Harborne , 1987).
Menurut Harborne (1987), senyawa kompleks yang dihasilkan dari interaksi tanin dengan protein tersebut bersifat racun atau toksik
yang dapat berperan dalam menghambat pertumbuhan dan
mengurangi nafsu makan serangga melalui penghambatan aktivitas enzim pencernaan.
Tanin mempunyai rasa yang sepat dan memiliki kemampuan
menyamak kulit. Tanin terdapat luas dalam tumbuhan berpembuluh, dalam angiospermae terdapat khusus dalam jaringan kayu.
Umumnya tumbuhan yang mengandung tanin dihindari oleh hewan
pemakan tumbuhan karena rasanya yang sepat. Salah satu fungsi tanin dalam tumbuhan adalah sebagai penolak hewan herbivore dan
15
B. Nyamuk Aedes aegypti
1. Klasifikasi Aedes aegypti
Klasifikasi Aedes aegypti adalah sebagai berikut (Boror dkk, 1989):
Kingdom : Animalia Phylum : Arthropoda
Class : Insecta Ordo : Diptera
Family : Culicidae Genus : Aedes
Species : Aedes aegypti
2. Morfologi Nyamuk Aedes aegypti
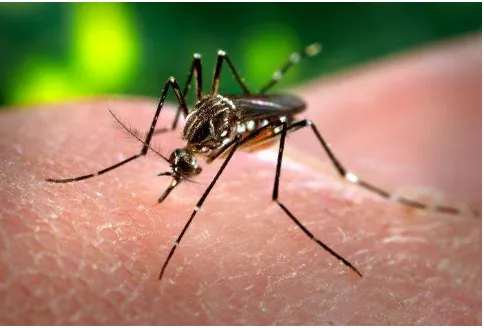
Aedes aegypti dewasa mempunyai ukuran tubuh yang kecil, mempunyai warna dasar tubuh yang hitam dengan bintik-bintik putih pada beberapa
bagian badannya, terutama pada kakinya (Gambar 3). Aedes aegypti dikenal dari bentuk morfologinya yang khas, yaitu terdapat dua garis melengkung vertikal di bagian kiri dan kanan mesonotum
16
Gambar 3. Nyamuk Aedes aegypti ( Sumber : Aditya, 2010)
Alat tusuk atau yang disebut proboscis terdapat dibagian kepala. Proboscis pada Aedes aegypti memiliki permukaan yang halus serta panjang dan langsing. Proboscis pada nyamuk betina berfungsi sebagai alat penghisap darah, sedangkan pada nyamuk jantan untuk menghisap nektar pada bunga dan sari buah-buahan. Pada sisi kanan proboscis
nyamuk terdapat palpus sebagai alat peraba (Ridadet al, 1999). Ukuran palpus ini lebih pendek daripada proboscisnya (Aradilla, 2009). Antena nyamuk jantan lebih lebat daripada nyamuk betina, disebut plumose. Sedangkan pada nyamuk betina antenanya jumlahnya lebih sedikit, disebut pilose.
Mesonotum (sebagian thorax yang tampak) diliputi bulu-bulu halus. Pada mesonotum terdapat skutelum, yang membentuk tiga lobi (tiga
17
yang terdiri dari coxae, trochanter, femur, tibia, dan lima tarsus yang
berakhir sebagai cakar (Aradilla, 2009).
Aedes aegypti mempunyai abdomen yang panjang dan langsing. Bagian abdomen terdiri dari 10 ruas, dimana dua ruas terakhir berubah menjadi alat kelamin, yang mana pada nyamuk jantan disebut hypopigidium dan pada betina disebut cerci.
3. Perilaku Aedes aegypti
Penularan penyakit dilakukan oleh nyamuk betina karena hanya nyamuk betina yang menghisap darah. Nyamuk betina memperoleh asupan protein yang diperlukannya dari darah, serta untuk memproduksi dan
mematangkan telurnya (Womack, 1993). Sedangkan nyamuk jantan memperoleh energinya dari nektar bunga, sari buah, ataupun tumbuhan. Nyamuk Aedes aegypti bersifat diurnal atau aktif pada pagi hingga sore hari.
18
4. Siklus Hidup Aedes aegypti
Nyamuk Aedes aegypti mengalami metamorfosis yang sempurna (holometabola), terdiri dari telur, larva, pupa, dan nyamuk dewasa
(Nurmaini, 2003).
a. Stadium Telur
Menurut Womack (1993), telur Aedes aegypti berwarna hitam dan berbentuk elips, mempunyai dinding yang bergaris-garis dan membentuk bangunan yang menyerupai gambaran kain kasa,
memiliki panjang 0,80 mm, dan berat 0,0010-0,015 mg (Gambar 4).
Seekor nyamuk betina dapat meletakkan rata-rata sebanyak 100 telur tiap kali bertelur pada permukaan air bersih secara individual,
terpisah satu dengan yang lain, dan menempel pada dinding tempat perindukkannya (Djakaria, 2000).
Telur Aedes aegypti tahan pada keadaan kering, dan pada kondisi normal telur yang terendam air akan menetas dalam waktu satu
hingga dua hari. Beberapa faktor dapat mempengaruhi daya tetas telur, diantaranya suhu, pH, air perindukan, cahaya, serta
19
Gambar 4. Telur Aedes aegypti
( Sumber : Center for Disease Control Public Health Image Library )
b. Stadium Larva
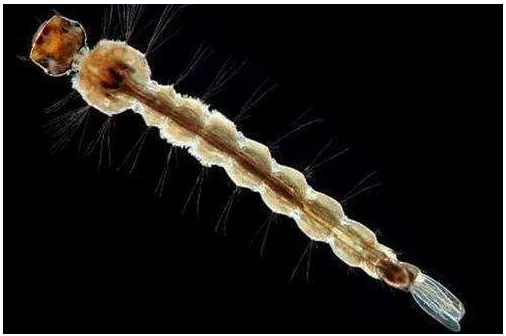
Larva Aedes aegypti membentuk sudut 450 pada bidang permukaan air saat beristirahat. Larva Aedes aegypti berbentuk silindris terdiri dari caput yang berbentuk globuler, thorax, dan abdomen yang
terdiri dari 8 segmen. Bagian caput terdapat bulu sikat yang digunakan untuk mencari makan. Pada abdomen segmen ke-8 terdapat siphon sebagai alat pernafasan (Gambar 5).
Terdapat empat tahapan dalam perkembangan larva yang disebut instar. Perkembangan dari instar I ke instar IV memerlukan waktu
sekitar 5-8 hari. Setelah mencapai instar IV, larva berubah menjadi pupa dan larva memasuki masa dorman. Pupa bertahan selama dua
20
Gambar 5. Larva Aedes aegypti
( Sumber : Center for Disease Control Public Health Image Library )
c. Stadium Pupa
Pada stadium pupa terjadi perubahan bentuk, yaitu cephalothorax
yang menjadi lebih besar daripada abdomen. Larva yang memasuki tahap pupa memiliki bentuk tubuh yang membengkok seperti tanda koma. Dalam pertumbuhannya terjadi proses pembentukan sayap,
kaki, dan alat kelamin (Depkes RI, 2007).
Pupa sangat sensitif jika terkena getaran atau gangguan, pupa akan menyelam dengan cepat untuk kemudian kembali lagi ke permukaan
21
Gambar 6. Pupa Aedes aegypti
( Sumber : Center for Disease Control Public Health Image Library )
d. Nyamuk Dewasa
Nyamuk jantan keluar terlebih dahulu dari kepompong, kemudian disusul dengan nyamuk betina, dan nyamuk jantan akan tetap tinggal
dekat sarang sampai nyamuk betina keluar dari kepompong. Setelah nyamuk betina keluar dari kepompong maka nyamuk jantan akan langsung mengawini nyamuk betina sebelum mencari darah. Selama
hidupnya, nyamuk betina hanya sekali mengalami perkawinan (Nurmaini, 2003).
Nyamuk dewasa setelah keluar dari kepompong memiliki tiga bagian, yaitu kepala (caput), dada (thorax), dan perut (abdomen).
Fase akuatik berlangsung selama 8-12 hari, dimana stadium larva selama 6-8 hari dan stadium pupa (kepompong) berlangsung 2-4
22
nyamuk dewasa membutuhkan waktu 10-14 hari. Umur nyamuk
Aedes aegypti dewasa dapat mencapai 2-3 bulan (Ridadet al, 1999).
5. Pengendalian Aedes aegypti
a. Pengelolaan Lingkungan
Upaya yang dapat dilakukan untuk pengendalian nyamuk vektor
adalah dengan cara pengelolaan lingkungan sehingga lingkungan menjadi tidak kondusif sebagai habitat perkembangbiakan nyamuk Aedes aegypti, seperti mengubur kaleng-kaleng bekas, menguras dan menutup penampungan air (Panghiyanganiet al, 2012).
b. Pengendalian Secara Fisik
Pengendalian secara fisik adalah pengendalian untuk menghilangkan
perindukan vektor (Anggraeni, 2010). Beberapa diantaranya yaitu : 1. Pakaian pelindung, dengan menggunakan pakaian yang cukup
tebal atau longgar, yang dapat melindungi tangan dan kaki agar terhindar dari gigitan nyamuk.
2. Perlindungan diri dengan menggunakan raket listrik untuk
perlindungan diri dari nyamuk. Bahan penolak serangga yang alami banyak juga digunakan untuk perlindungan diri seperti
23
3. Kelambu dan gorden yang banyak digunakan masyarakat untuk
menghindari dari gigitan nyamuk.
4. Pemasangan kawat kasa yang dipasang pada ventilasi rumah
dapat menghalangi nyamuk dewasa masuk kedalam rumah (Anggraeni, 2010).
c. Pengendalian Secara Biologis
Menurut Anggraeni (2010), pengendalian biologis dapat dilakukan dengan menyebarkan musuh alami seperti parasit dan predator di
daerah terjangkit atau daerah endemis, diantaranya seperti : 1. Berbagai jenis ikan pemakan larva dapat membantu program
pengendalian larva nyamuk vektor, seperti ikan nila merah
(Oreochromis niloticus), nila hitam (Tilapia nikotika), ikan mas (Cyprinus carpio), dan lain-lain.
2. Pengendalian vektor dengan bakteri Bacillus thuringiensis yang memproduksi toksin yang terdapat dalam bentuk kristal yang sangat beracun.
3. Toxorhynchites sp. adalah salah satu dari beberapa jenis nyamuk yang tidak mengisap darah mamalia. Larva nyamuk ini
memangsa larva nyamuk yang berukuran lebih kecil.
24
tersebut keluar dengan jalan menyobek dinding tubuh inang
sehingga menyebabkan kematian inang tersebut.
d. Pengendalian Secara Kimiawi
Pemberantasan secara kimiawi yaitu pengendalian DBD dengan
menggunakan bahan kimia, menurut Depkes RI (2007) dapat ditempuh dengan beberapa teknik, yaitu:
1. Pengasapan (fogging), yaitu suatu teknik untuk mengurangi penularan penyakit DBD sampai batas waktu tertentu dengan
menggunakan senyawa kimia malathion dan fenthion.
2. Pemberantasan larva nyamuk dengan larvasida kimiawi yang diberikan pada tempat perkembangbiakan larva vektor DBD
seperti pada penampungan air, maka larvasida harus efektif pada dosis rendah, tidak bersifat racun bagi manusia/mamalia, tidak menyebabkan perubahan rasa, warna dan bau, dan efektivitasnya
lama, seperti temephos (abate).
C. Ekstraksi
Ekstraksi merupakan pembuatan sediaan sari pekat tumbuh-tumbuhan
25
Proses awal pembuatan ekstrak adalah tahapan pembuatan serbuk simplisia
kering, kemudian dengan peralatan tertentu sampai derajat kehalusan tertentu. Kemudian dilakukan perendaman dengan pelarut yang sesuai. Cairan pelarut
dalam proses pembuatan ekstrak adalah pelarut yang baik bagi senyawa aktif yang terkandung dalam bahan yang akan di buat ekstraknya, dengan demikian senyawa tersebut dapat terpisah dari bahan dan dari senyawa kandungan yang
lain. Senyawa aktif akan larut dalam pelarut organik karena adanya
perbedaan konsentrasi antara di dalam dan di luar sel, mengakibatkan difusi
pelarut organik yang mengandung zat aktif keluar sel dan proses ini akan terus berlangsung hingga terjadi keseimbangan (Depkes RI, 1986).
Flavonoid merupakan salah satu dari beberapa senyawa aktif yang berperan sebagai larvasida pada daun pepaya, flavonoid dapat larut dengan baik pada
pelarut polar seperti akuades, etanol, dan methanol. Etanol dipertimbangkan sebagai cairan penyari karena lebih selektif, kapang dan kuman sulit tumbuh dalam etanol 20% ke atas, tidak beracun, netral, etanol dapat bercampur
III. METODE PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini dilakukan di Laboratorium Zoologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung pada bulan
Januari 2014. Ekstraksi daun pepaya (Carica papaya L.) dilakukan di Laboratorium Kimia Organik Jurusan Kimia Fakultas Matematika dan Ilmu
Pengetahuan Alam Universitas Lampung.
B. Alat dan Bahan
1. Alat
Alat-alat yang digunakan dalam penelitian diantaranya gelas ukur untuk mengukur jumlah hasil ekstraksi, bejana kaca untuk tempat pembuatan
ekstrak, labu ukur untuk pengenceran ekstrak, pengaduk untuk
27
tempat pengamatan, pipet larva berbahan plastik untuk memindahkan
larva, saringan larva, pipet tetes, kertas label, alat tulis, kertas tisu, counter, dan stopwatch sebagai alat pencatat waktu pengamatan.
2. Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah daun pepaya yang dikering-anginkan dan kemudian dihancurkan sebanyak 300 gram,
larva nyamuk Aedes aegypti instar III sebagai larva uji, etanol 96% sebagai pelarut sebanyak 2,5 L, akuades sebagai pengencer ekstrak
daun pepaya, dan dog food sebagai pakan larva.
C. Rancangan Penelitian
Metode yang digunakan dalam penelitian ini adalah eksperimental laboratorium dengan Rancangan Acak Lengkap (RAL) dan dengan
perlakuan tunggal yang menggunakan 6 jenis konsentrasi yaitu 0% sebagai kontrol; 0,2%; 0,4%; 0,6%; 0,8%; dan 1% yang ditentukan berdasarkan
hasil dari uji pendahuluan, serta dilakukan 4 kali pengulangan.
D. Prosedur Penelitian
28
1. Tahap Persiapan
a. Preparasi Bahan Uji
Telur nyamuk Aedes aegypti yang digunakan dalam penelitian ini diperoleh dari Loka Penelitian dan Pengembangan Pemberantasan Penyakit Bersumber Binatang (P2B2) Ciamis Jawa Barat.
b. Rearing Larva
Telur kemudian ditetaskan dalam nampan plastik yang berisi air bersih untuk pemeliharaan larva nyamuk. Telur menetas dalam
waktu 2 hari dan setelah menetas diberi makan berupa dog food. Dalam waktu kurang lebih 4 hari, larva nyamuk tumbuh mencapai instar III.
c. Pembuatan Ekstrak Daun Pepaya
Pembuatan ekstrak daun papaya (Carica papaya L.) menggunakan metode maserasi dan dengan pelarut berupa etanol 96%. Daun pepaya tua dikeringkan dengan cara diangin-anginkan dalam ruangan, dan tidak dengan dijemur dibawah terik matahari karena
dapat menghilangkan senyawa aktif yang terkandung di dalam daun pepaya. Kemudian daun pepaya kering dihancurkan dengan cara
29
karena etanol merupakan pelarut yang bersifat polar sehingga
senyawa aktif seperti flavonoid dalam daun pepaya yang juga
bersifat polar dapat larut dengan baik. Rendaman tersebut kemudian
disaring dengan kertas saring untuk mendapatkan ekstrak yang diinginkan. Ekstrak yang sudah disaring kemudian dipekatkan dengan dengan alat vacuum rotary evaporator sehingga diperoleh ekstrak daun pepaya dengan konsentrasi 100% (Depkes RI, 1986). Hasil ekstraksi kemudian diencerkan dengan akuades sebanyak
enam konsentrasi yaitu 0% sebagai kontrol; 0,2%; 0,4%; 0,6%; 0,8%; dan1% (konsentrasi ditentukan berdasarkan hasil dari uji
pendahuluan yang telah dilakukan sebelumnya).
2. Tahap Penelitian
Ekstrak daun papaya (Carica papaya L.) dengan konsentrasi 0%
sebagaikontrol; 0,2%; 0,4%; 0,6%; 0,8%; dan 1% dimasukkan ke dalam
30
E. Pengamatan
Menurut WHO (2005), setiap perlakuan diamati pada 11 interval waktu yaitu
pada menit 5, 10, 20, 40, 60, 120, 240, 480, ke-1440, ke-2880, dan ke-4320 setelah diberi perlakuan dengan menghitung jumlah larva yang mati disetiap interval waktu pengamatan tersebut. Dan
jumlah larva yang mati di setiap menitnya dikalkulasikan.
F. Analisis Data
Hasil pengamatan yang diperoleh dianalisa dengan menggunakan ANOVA, agar dapat mengetahui adanya perbedaan rata-rata kematian larva nyamuk di setiap perlakuan yang diberikan. Kemudian dilakukan uji lanjut dengan BNT
(Beda Nyata Terkecil) karena ada perbedaan kematian larva nyamuk pada setiap perlakuan.
IV. HASIL PENGAMATAN DAN PEMBAHASAN
A. Hasil Pengamatan
1. Uji Larvasida
Penelitian dengan pemberian ekstrak daun pepaya (Carica papaya L.) terhadap larva Aedes aegypti instar III yang dilakukan selama tiga hari pengamatan dengan berbagai konsentrasi yaitu 0% sebagai kontrol; 0,2% ; 0,4% ; 0,6% ; 0,8% ; dan 1,0% berpotensi sebagai larvasida terhadap larva nyamuk Aedes aegypti. Terjadi peningkatan kematian larva uji seiring dengan meningkatnya waktu pajanan dan konsentrasi ekstrak daun pepaya yang diberikan. Kematian larva Aedes aegypti dimulai pada menit ke-480 pada konsentrasi 0,2% dengan rata-rata kematian sebesar 1,25%
32
Tabel 1. Persentase rata-rata kematian larva Aedes aegypti pada berbagai konsentrasi ekstrak daun pepaya (Carica papaya L.)
Konsen- trasi (%)
Persentase Rata-rata Kematian Larva (%) pada menit ke-
Rata-rata
Keterangan : Jumlah larva Aedes aegypti yang digunakan sebanyak 20 ekor per perlakuan
Pada Tabel 1 terlihat bahwa tidak dijumpai kematian larva Aedes aegypti pada konsentrasi 0% ekstrak daun pepaya hingga menit ke-4320 (72 jam), sedangkan jumlah kematian larva uji tertinggi dijumpai pada
konsentrasi 1% dengan nilai rerata mencapai 60,00%. Kematian larva uji terjadi mulai dari menit ke-480 yaitu pada konsentrasi 0,2% dan 1,0%.
Dari hasil pengamatan dapat diketahui bahwa adanya korelasi antara besar konsentrasi dengan daya bunuh yang ditimbulkan. Hal ini dapat
dilihat dari besarnya nilai r yaitu 0,967 (Gambar 7). Berdasarkan nilai r yang diperoleh dapat disimpulkan bahwa semakin tinggi konsentrasi
33
Gambar 7. Respon konsentrasi ekstrak daun pepaya terhadap kematian larva uji dalam 4320 menit (72 jam)
Selanjutnya untuk mengetahui perbedaan pengaruh pemberian
konsentrasi ekstrak daun pepaya terhadap kematian larva Aedes aegypti, dilakukan uji statistik terhadap data pengamatan yang telah diperoleh. Pada uji statistik diperlukan uji normalitas terlebih dahulu untuk
menentukan sebaran data tersebut normal atau tidak, dan pada uji normalitas diperoleh nilai p > 0,05 yang berarti sebaran data tersebut normal. Selanjutnyakarena sebaran data normal dapat dilakukan uji
dengan menggunakan ANOVA untuk mengetahui perbedaan rata-rata kematian larva nyamuk Aedes aegypti yang terjadi di setiap perlakuan. Uji ANOVA hanya dilakukan pada menit pengamatan yang telah dijumpai adanya kematian larva uji, yaitu dimulai dari menit ke-480. Hasil analisis dengan menggunakan ANOVA dapat dilihat pada Tabel 2.
34
Tabel 2. Hasil Analisis dengan ANOVA
Sumber
Keterangan :** = berbeda sangat nyata
Dari Tabel 2 terlihat bahwa F hitung > F tabel sehingga dapat diketahui bahwa besar konsentrasi ekstrak daun pepaya (Carica papaya L.) dan lamanya waktu pemaparan berpengaruh terhadap kematian larva uji, oleh sebab itu analisis dilanjutkan dengan menggunakan Uji BNT (Beda
Nyata Terkecil).
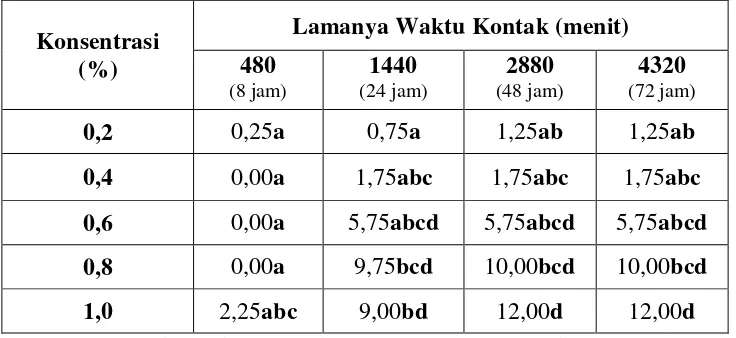
Tabel 3. Rata – rata Jumlah Kematian Larva Aedes aegypti Setelah Diberi Ekstrak Daun Pepaya (Carica papaya L.)
Konsentrasi (%)
Lamanya Waktu Kontak (menit) 480
35
Pada Tabel 3 dapat dilihat bahwa terjadi kematian larva uji tertinggi pada
konsentrasi ekstrak 1,0%, tetapi berdasarkan hasil analisis di atas menunjukkan kematian larva uji pada konsentrasi ekstrak 1,0% tidak
berbeda nyata dengan konsentrasi 0,6% dan 0,8%, sedangkan konsentrasi 0,6% ; 0,8% dan 1,0% berbeda nyata dengan konsentrasi ekstrak 0,2% dan 0,4%. Berdasarkan hasil dari analisis ANOVA, konsentrasi 0,6%
merupakan konsentrasi ekstrak daun pepaya yang paling efektif bagi larva Aedes aegypti jika dibandingkan dengan konsentrasi lainnya.
Hasil pengamatan menunjukkan bahwa kematian larva Aedes aegypti baru mulai dijumpai pada menit pengamatan ke-480, sehingga analisis hanya dilakukan dari menit pengamatan ke-480. Tabel 3
memperlihatkan bahwa pada menit pengamatan ke-2880 dan ke-4320
tidak terjadi peningkatan rata-rata kematian larva Aedes aegypti yang bermakna dengan menit pengamatan lainnya, sehingga dapat dikatakan ekstrak daun pepaya efektif jika digunakan sebagai larvasida dalam
waktu 1440 menit (24 jam).
2. Lethal Concentration 50% (LC50) dan 90% (LC90)
Lethal Concentration merupakan suatu ukuran untuk mengukur daya toksisitas pada suatu jenis insektisida, yang ditentukan berdasarkan jumlah kematian larva uji pada setiap konsentrasi. Nilai LC50 merupakan
36
yang diuji, sedangkan nilai LC90 merupakan konsentrasi yang dibutuhkan
untuk membunuh 90% dari jumlah larva yang di uji. Analisis dilakukan hanya pada waktu pengamatan yang telah dijumpai adanya kematian larva
uji, yaitu dimulai pada menit ke-480. Hasil analisis probit untuk LC50 dan LC90 dapat dilihat dalam Tabel 4 berikut :
Tabel 4. Persentase Rata-rata Nilai LC50 dan LC90 Larva Aedes aegypti
No Waktu (menit)
Nilai LC50 (%)
Batas Kepercayaan 95% Nilai LC90 (%)
Batas Kepercayaan 95%
Minimum Maksimum Minimum Maksimum
1 480 1,2 1,1 2,5 1,5 1,2 3,8
2 1440 0,9 0,8 1,2 1,4 1,2 2,1
3 2880 0,8 0,6 1,0 1,3 1,1 2,1
4 4320 0,8 0,6 1,0 1,3 1,1 2,1
Pada Tabel 4 dapat dilihat bahwa nilai LC50 pada menit ke-480 sebesar
1,2% dan pada menit ke-4320 sebesar 0,8%. Hal ini menunjukkan bahwa terjadi penurunan konsentrasi yang dibutuhkan seiring dengan semakin
lamanya waktu pajanan. Hal yang sama juga terjadi pada nilai LC90, pada menit ke-480 sebesar 1,5% dan pada menit-4320 sebesar 1,3%.
Berdasarkan konsentrasi yang digunakan, yaitu 0%; 0,2%; 0,4%; 0,6%; 0,8%; dan 1% maka efektifitas ekstrak daun pepaya sebagai larvasida
37
Penurunan nilai LC50 seiring dengan meningkatnya lama waktu pajanan
hanya terjadi hingga menit ke-2880 yang dapat dilihat pada Gambar 8.
Gambar 8. Nilai LC50Ekstrak Daun Pepaya dari menit pengamatan ke-480sampai menit ke-4320
Penurunan nilai LC90 seiring dengan meningkatnya lama waktu pajanan hingga menit ke-2880 dapat dilihat pada Gambar 9.
38
3. Lethal Time 50% (LT50) dan 90% (LT90)
Nilai LT50 merupakan waktu yang dibutuhkan untuk membunuh 50% dari jumlah larva yang di uji pada konsentrasi tertentu, sedangkan nilai LT90 merupakan waktu yang dibutuhkan untuk membunuh 90% dari jumlah
larva yang di uji pada konsentrasi tertentu. Nilai LT50 dan LT90 diperoleh dengan menggunakan program analisis Probit. Hasil analisis probit untuk
LT50 dapat dilihat pada Tabel 5 berikut :
Tabel 5.Nilai LT50 dan LT90 kematian larva Ae. aegypti
No Konsentrasi
Nilai LT50 (jam)
Batas Kepercayaan 95% Nilai LT90 (jam)
Batas Kepercayaan 95%
Minimum Maksimum Minimum Maksimum
1 0,2% 8.616,4 11,9 61.010,1 53.723,1 49.057,3 58.832,5
2 0,4% 1.536,1 47,3 49.888,2 39.565,8 59,553 26.286,3
3 0,6% 177,7 59,3 532,5 3.383,5 149,3 76.682,1
4 0,8% 49,4 35,9 67,8 583,1 127,9 2.656,9
5 1,0% 37,9 30,3 47,6 263,7 137,3 506,5
Pada Tabel di atas dapat dilihat bahwa nilai LT50 yang diperoleh pada
konsentrasi ekstrak 0,2% ; 0,4% ; dan 0,6% melebihi batas waktu pengamatan yaitu 4320 menit (72 jam), sedangkan untuk nilai LT90 pada semua konsentrasi tidak dapat ditentukan karena melebihi batas waktu
39
Gambar 10. Nilai LT50 pada setiap konsentrasi
B. Pembahasan
1. Uji Larvasida
Uji potensi ekstrak daun pepaya ini merupakan pengujian untuk
mengetahui pengaruh senyawa kimia yang terkandung dalam daun pepaya terhadap kematian larva Aedes aegypti instar III dengan berbagai
konsentrasidan dilakukan pengamatan hingga 72 jam. Sebelumnya telah dilakukan uji pendahuluan selama 24 jam untuk mengetahui rentang
40
yang telah dilakukan menunjukkan nilai persentase rerata kematian larva
uji tertinggi yaitu sebesar 97,5% pada konsentrasi ekstrak 1,0%.
Berdasarkan hasil dari uji pendahuluan tersebut maka digunakan
konsentrasi ekstrak daun pepaya sebesar 0% sebagai kontrol; 0,2% ; 0,4% ; 0,6% ; 0,8% ; dan 1,0% di dalam uji sesungguhnya. Penentuan
konsentrasi ekstrak daun pepaya yang digunakan dalam uji sesungguhnya sesuai dengan WHO Guidelines for Laboratory and Field Testing of Mosquito Larvicides (2005) dengan persentase konsentrasi maksimal penelitian larvasida yang digunakan sebesar 1%.
Berdasarkan Tabel 1 dapat diketahui bahwa pada konsentrasi 0%
(kontrol) tidak dijumpai adanya kematian larva Aedes aegypti, sedangkan pada masing-masing kelompok perlakuan yang diberi ekstrak
menunjukkan adanya kematian larva uji. Hasil penelitian ini menunjukkan bahwa rata-rata kematian tertinggi terdapat pada
konsentrasi 1,0% yaitu 48 ekor (60%) dan rata-rata kematian terendah terdapat pada konsentrasi 0,2% yaitu sebanyak 5 ekor (6,25%). Hal
tersebut menunjukkan bahwa tingginya angka kematian larva uji bergantung pada besar konsentrasi ekstrak yang diberikan dan lamanya waktu pemaparan (Riyanti, 2005).
Hasil uji ANOVA menunjukkan bahwa pada konsentrasi ekstrak 0,6% ;
41
0,4%. Berdasarkan hasil dari analisis ANOVA, konsentrasi 0,6%
merupakan konsentrasi ekstrak daun pepaya yang paling efektif bagi larva Aedes aegypti jika dibandingkan dengan konsentrasi 0,8% dan 1,0%, karena ketiga konsentrasi tersebut berdasarkan hasil uji BNT tidak menunjukkan perbedaan jumlah kematian larva yang nyata. Hal ini menunjukkan bahwa ekstrak daun pepaya dengan konsentrasi 0,6%
sudah memiliki daya bunuh yang tinggi terhadap larva Aedes aegypti instar III. Tingginya angka kematian larva uji pada konsentrasi ekstrak
0,6% disebabkan oleh banyaknya jumlah senyawa aktif yang kontak langsung dengan larva uji selama waktu pengamatan.
Pada ekstrak daun pepaya, senyawa aktif seperti flavonoid yang
merupakan racun pernapasan masuk ke dalam tubuh larva melalui sistem
pernapasan yang kemudian akan menimbulkan gangguan pada syaraf dan kerusakan sistem pernapasan, sehingga mengakibatkan larva tidak dapat bernapas dan akhirnya menyebabkan kematian pada larva
(Robinson, 1995).
Senyawa aktif lain pada daun pepaya yang berperan sebagai larvasida adalah saponin yang berfungsi sebagai racun perut atau racun pencernaan. Cara kerja dari saponin adalah menurunkan tegangan permukaan selaput
mukosa traktus digestivus larva sehingga menjadi korosif. Saponin juga menyebabkan kerusakan pada jaringan epitelium pada usus tengah larva
42
diedarkan melalui haemolimfe, terhambatnya proses absorpsi sari-sari
makanan mengakibatkan proses pertumbuhan pada larva terhambat dan akhirnya menyebabkan kematian pada larva (Dinata, 2009).
Selain itu menurut Priyono (2007), senyawa tanin merupakan racun kontak yang mengakibatkan aktifnya sistem lisis sel karena enzim
proteolitik pada sel tubuh larva. Senyawa tanin yang terkandung dalam ekstrak daun pepaya diduga menurunkan aktifitas enzim pencernaan
seperti amilase dan protease, sehingga penyerapan protein dapat terganggu dan mengakibatkan kematian pada larva karena adanya
gangguan penyerapan nutrisi dan menurunnya laju pertumbuhan pada larva (Harborne, 1987).
Fungsi kandungan senyawa aktif seperti flavonoid, saponin, dan tanin juga dapat dilihat darihasil penelitian yang dilakukan oleh Wardani et al. (2010) mengenai kandungan zat aktif daun tembelekan terhadap kematian
larva Aedes aegypti. Berdasarkan hasil penelitian tersebut ekstrak daun tembelekan mengandung alkaloid dan saponin yang bertindak sebagai
racun pencernaan dan flavonoid sebagai racun pernapasan.
Berdasarkan hasil penelitian lain yang dilakukan oleh Lianawati (2008),
43
lain yang terkandung seperti minyak atsiri dan flavonoid bekerja sebagai
racun pernapasan, serta saponin yang bekerja sebagai racun perut.
2. Lethal Concentration 50% (LC50) dan 90% (LC90)
Nilai LC50 yang diperoleh dari hasil analisis menunjukkan bahwa terjadi
penurunan jumlah konsentrasi yang dibutuhkan untuk membunuh 50% larva uji seiring dengan semakin lamanya waktu pajanan yang diberikan,
karena walaupun dengan jumlah konsentrasi yang rendah akan tetap menimbulkan kematian terhadap larva uji jika larva lebih lama terpapar
oleh racun yang dikandung ekstrak daun pepaya tersebut. Penelitian lain yang dilakukan oleh Wulandari et al. (2012) mengenai potensi getah buah pepaya (Carica papaya L.) terhadap mortalitas larva nyamuk Aedes albopictus didapatkan nilai LC50 yang juga semakin menurun seiring dengan bertambahnya waktu pajanan. Pada penelitian tersebut didapatkan nilai LC50 sebesar 26,30 ppm pada menit ke-1440 dan 9,12 ppm pada
menit ke-5760.
Pada Gambar 8 nilai LC50 pada menit ke-5 hingga menit ke-480 berada di atas nilai standar WHO yaitu 1% (batas standar konsentrasi larvasida), sehingga pada rentang waktu 5 hingga 480 menit ekstrak daun pepaya
yang digunakan dalam penelitian ini belum cukup efektif membunuh 50% larva uji. Tetapi pada menit pengamatan berikutnya diperoleh nilai LC50
44
pepaya efektif untuk membunuh 50% larva uji. Pada hasil penelitian yang
dilakukan oleh Ariyati (2013) mengenai efektifitas ekstrak kulit batang pepaya (Carica papaya L.) sebagai larvasida nyamuk Aedes aegypti ditemui nilai LC50 yang juga di bawah nilai standar WHO yaitu sebesar 0,8%.
Nilai LC90 yang diperoleh dari penelitian ini memperlihatkan bahwa untuk membunuh 90% larva uji dibutuhkan konsentrasi ekstrak daun pepaya di
atas 1,0% (Gambar 9) atau dengan kata lain konsentrasi yang digunakan dalam penelitian ini masih belum efektif jika digunakan sebagai larvasida
karena kematian yang ditimbulkan belum mencapai 90% dari total larva uji yang digunakan. Hal tersebut sesuai dengan hasil penelitian yang dilakukan oleh Nopitasari (2013) mengenai uji aktifitas ekstrak n-heksana
biji langsat (Lansium domesticum Cor.) sebagai larvasida Aedes aegypti yang menunjukkan bahwa nilai LC90 berada pada konsentrasi ekstrak sebesar 4% dan 5% (di atas nilai standar WHO).
3. Lethal Time 50% (LT50) dan 90% (LT90)
Nilai LT50 pada Tabel 5 menunjukkan bahwa semakin tinggi konsentrasi ekstrak daun pepaya yang diberikan maka semakin sedikit juga waktu
yang diperlukan untuk membunuh 50% larva Aedes aegypti. Hasil dari analisis Probit menunjukkan bahwa pada konsentrasi ekstrak 0,2% ; 0,4%
45
jam), sehingga pada konsentrasi tersebut dapat dikatakan bahwa ekstrak
daun pepaya belum dapat membunuh 50% dari larva uji yang digunakan. Tetapi nilai LT50 yang diperoleh pada konsentrasi ekstrak 0,8% dan 1,0%
lebih rendah dari batas waktu pengamatan yaitu 49,40 jam untuk konsentrasi 0,8% dan 37,97 jam untuk konsentrasi 1,0%.
Terjadinya penurunan nilai LT50 pada konsentrasi ekstrak 0,8% dan 1,0% dikarenakan besarnya konsentrasi yang diberikan terhadap larva uji
menyebabkan efek toksik pada ekstrak daun pepaya semakin besar pula sehingga hanya dibutuhkan waktu yang sedikit untuk membunuh 50%
larva uji. Hal ini menunjukkan bahwa konsentrasi ekstrak daun pepaya yang paling cepat menyebabkan kematian pada larva uji adalah 0,8% dan 1,0%.
Nilai LT50 tersebut serupa dengan hasil penelitian yang dilakukan oleh Hidayatulloh (2013) mengenai efektifitas pemberian ekstrak akar
kecombrang (Etlingera elatior) terhadap larva Aedes aegypti instar III dimana persentase konsentrasi maksimal penelitian larvasida yang
digunakan adalah dibawah 1,0%. Nilai LT50 yang diperoleh dari penelitian tersebut adalah sebesar 380,88 menit (6,34 jam) untuk konsentrasi 0,75% dan 151,81 menit (2,53 jam) untuk konsentrasi 1,0%.
Hasil berbeda ditemukan pada nilai LT90 yang menunjukkan semua
46
dibuktikan dengan nilai LT90 (Tabel 5) yang melebihi batas waktu
pengamatan (72 jam). Besarnya konsentrasi ekstrak daun pepaya yang diberikan tidak mampu mengakibatkan kematian 90% dari jumlah larva
DAFTAR PUSTAKA
Aditya, D. 2010. Mengenal Makhluk yang Bernama “Nyamuk”. http://dhony aditya .wordpress.com/2010/11/26/mengenal-makhluk-yang-bernama-nyamuk/. Diakses tanggal 22 November 2013.Pukul 14.34 WIB. Alboneh, F. H. 2012. Uji Potensi Ekstrak Etanol Daun Pepaya (Carica papaya)
Sebagai Insektisida Terhadap Nyamuk Aedes Sp dengan Metode listrik.(Skripsi). Fakultas Kedokteran Universitas Brawijaya. Malang. Ansel, H.C. 2005. Pengantar Bentuk Sediaan Farmasi. Edisi Keempat. UI Press.
Jakarta
Anggraeni, D.S. 2010. Stop Demam Berdarah Dengue. Bogor
Aradilla, A.S. 2009.Uji Efektifitas Larvasida Ekstrak Etanol Daun Mimba (Azadira chtaindica) terhadap Larva Aedes aegypti.(Skripsi). Fakultas Kedokteran Universitas Diponegoro. Semarang.
Ariyati, Tutik. 2013. Efektifitas Ekstrak Kulit Batang Pepaya (Carica papaya L.) sebagai Larvasida Nyamuk Aedes aegypti. Tesis.Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Jember. Jember.
Borror, D.J., Tripelhorn,C.A., Johnson, N.F. 1989. An introduction to the study of insects. Saunders College Publishing. USA.
Chahaya, I. 2003. Pemberantasan Vektor Demam Berdarah di Indonesia. USU digital library.
DadangdanPrijono D. 2008.Insektisida Nabati :Prinsip, Pemanfaatan, dan
Pengembangan. Departemen Proteksi Tanaman. Institut Pertanian Bogor. Bogor.
Dalimarta, S danHembing, W. 1994.Tanaman Berkhasiat Obat di Indonesia jilid ke-3.PustakaKartini. Jakarta.
49
Depkes RI. 2007.Aedes aegypti Vampir Mini yang Mematikan. Badan Penelitian dan Pengembangan Kesehatan Depkes RI. Jakarta. Inside (Inspirasidan Ide) Litbangkes P2B2.Vol 2.
Dinata, A. 2009.Mengatasi DBD dengan Kulit Jengkol .www.miqra indonesia .blogspot.com. Diakses tanggal 22 November 2013.Pukul 11.23 WIB. Dinata.2008.Lawan Alzheimer dengan Flavonoid. http://cybermed.cbn.net.id/cbprtl
/common/banner.aspx?x=cybermed&id=18. Diakses tanggal 21 November2013.Pukul 17.23 WIB.
Djakaria. 2000. Vektor penyakit virus, riketsia, spiroketa dan bakteri. Parasitologi Kedokteran. Edisi Ketiga. Balai Penerbit FKUI. Jakarta: 235-237.
Dzulkarnain, B. 1996.Tinjauan Hasil Penelitian Tanaman Obat di Berbagai Institusi. Dit.Jen POM, Dep.Kes RI. Jakarta. hal. 26. Hamijaya, M.Z. dan Asikin, A. 2005. Teknologi ”Indiggenous” dalam
mengendalikan hama padi di Kalimantan Selatan. Dalam Simposium Nasional, Ketahanan dan Keamanan Pangan pada Era Otonomi dan Globalisasi. Bogor.
Haryoto. 1998. Membuat Saus Pepaya. Fakultas Kedokteran Universitas Brawijaya. JakaElektrik Kanisius. Malang
Harborne, J.B. 1987. Metode Fitokimia. ITB. Bandung.
Hidayatulloh, N. 2013.Efektifitas Pemberian Ekstrak Ethanol 70% Akar
Kecombrang (Etlingeraelatior) terhadap Larva Instar III Aedes aegypti sebagai Biolarvasida Potensial.(Skripsi). Fakultas Kedokteran
Universitas Lampung. Lampung.
Ismatullah, Ahmad. 2014. Uji Efektifitas Larvasida Ekstrak Daun Binahong (Anreder acordifolia (Ten.) Steenis) terhadap Larva Aedes aegypti instar III. (Skripsi). Fakultas Kedokteran Universitas Lampung. Lampung. Krishna, K.L., Paridhavi, M., Patel, J.A. 2008.Review on Nutrional, Medicinal,
and Pharmacological Properties of Papaya (Carica papaya L.). Natural Product Radiance Vol7(4), p.364-73.
Linda. 2009. Carica papaya. http://herselfshoustongarden.com/2009/08/papaya-tree-carica-papaya.html/papaya-tree.Diaksestanggal 22 November 2013.Pukul 13.09 WIB.
Listiawati, Y. 2010. Uji Efek Antipiretik Ekstrak Etanol Daun Legundi (Vitex trifolia Linn) pada Kelinci yang Diinduksi Vaksin Dpt-Hb.
50
Lianawati H. 2008. Uji Efikasi Daun Pare (Momordica charantia Linnaeus) TerhadapKematian Larva Nyamuk Aedes aegypti Linnaeus. FKM UNDIP. Semarang.
Muhaeni,Dina. 2007.Pengendalian Larva Anopheles aconitus Sebagai Vektor Malaria Dengan Air Rendaman Gadung.(Skripsi). Fakultas Biologi Universitas Jenderal Soedirman. Purwokerto.
Mulyana. 2002. Ekstraksi senyawa Aktif Alkaloid, Kuinon, Saponin dari Tumbuhan Kecubung sebagai Larvasida dan Insektisida terhadap Nyamuk Aedes aegypti. (Skripsi). Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor. Bogor.
Nani S. dan Dian S. 1996.Tinjauan Hasil Penelitian Tanaman Obat di Berbagai Institut III. Jakarta.
Nopitasari.2013. Uji Aktifitas Ekstrak n-Heksana Biji Langsat (Lansium
domesticum Cor.) sebagai Larvasida Aedes aegypti. (Skripsi). Fakultas Kedokteran. Universitas Tanjungpura. Pontianak.
Nurhasanah,S.2001.Efek Mematikan Ekstrak Biji Sirsak (Annona muricata)
Terhadap Larva Aedes aegypti. Fakultas Kedokteran. Universitas Sebelas Maret. Surakarta.
Nurmaini. 2003. Identifikasi, Vektor Dan Binatang Pengganggu Serta
Pengendalian Anopheles Aconictus Secara Sederhana. USU. Medan Nuryadin, A. 2010.Makalah Demam Berdarah Dengue
. http://www.adinnagrak.blogspot.com/2013/11/makalah-demam-berdarah-dengue-latar.html.Diaksestanggal 19 November 2013.Pukul 20.34 WIB
Panghiyangani R., Marlinae L., Yuliana, Fauzi R., Noor D., danAnggriyani W.P., 2012. Potential of Turmeric Rhizome Essential Oils Against
Aedes aegypti Larvae. Universa Medicina. Vol 31, no. 1 Priyono.2007. Enzim Papain dari Pepaya (Carica papaya).
http://priyonoscience.blogspot.com/2009/07enzim-papainpepaya. html, diaksestanggal 20 November 2013. Pukul 21.09 WIB
Raharjo, B. 2006.Uji kerentanan Aedes aegypti dari Surabaya, Palembang serta Beberapa wilayah di Bandung terhadap Temephos. Institut Teknologi Bandung. Bandung.
Ridad A., Ochadian H., Natadisastra D. 1999. Bunga Rampai Entomologi Medik. Edisi ke 2.Bagian Parasitologi Fakultas Kedokteran Universitas
51
Riyanti, H. 2005. Toksikologi Limbah Cair Kelapa Sawit terhadap Ikan Nila (Aeromonas Sp). (Skripsi). FKIP Universitas Riau.Pekanbaru.
Robinson, T. 1995. Kandungan Organik Tumbuhan Tinggi. ITB Press. Bandung. Soedarto, D.T.M.H. 1992. Atlas Entomologi Kedokteran. EGC. Surabaya
Subiyakto. 2005. Pestisida Nabati: Pembuatan dan Pemanfaatannya. Penerbit Kanisius. Cetakan I. ISBN 979-21-1004-6.58 hlm.
Utomo M., Amaliah S., Suryati F.A. 2010. Daya Bunuh Bahan Nabati Serbuk Biji Papaya terhadap Kematian Larva Aedes aegypti Isolat
Laboratorium B2P2VRP Salatiga. Salatiga.p152-158. Warisno. 2003. Budidaya Pepaya. Penerbit Kanisius. Yogyakarta.
Wardani, R.S., Mifbakhudin, Kiky Y. 2010. Pengaruh Konsentrasi Ekstrak Daun Tembelekan (Lantana camara) terhadap Kematian Larva Aedes aegypti. Universitas Muhammadiyah Semarang.Vol 6, no.2.
Wicaksana W, P. 2012. Uji Potensi Air Perasan Buah Pepaya (Carica
papaya L.) Sebagai Insektisida Pada Nyamuk Culex sp. Dengan Metode Elektrik. (Skripsi). Fakultas Kedokteran Universitas Brawijaya. Malang Wijana dan Ngurah.1982. Beberapa Karakter Aedes aegypti Sebagai Vektor
Demam Berdarah Dengue. Fakultas Kedokteran Universitas Udayana. Bali
Womack, M., 1993.The yellow fever mosquito, Aedesaegypti. Wing Beats. Vol5(4):4
World Health Organization. 1999. Regional Office for South-East Asia, New Delhi. Guidelines for Treatment of Dengue Fever/Dengue Hemmorhagic Fever in Small Hospitals.
Wulandari, Sri. Arnentis. Sri R. 2012. Potensi Getah Buah Pepaya (Carica papaya L) terhadap Mortalitas Larva Nyamuk Aedes albopictus.Universitas Riau. Pekanbaru.Vol9 , no.1. p66-76.