ANALISIS LOGAM ALUMINIUM (Al) DAN CALSIUM (Ca) PADA
PROSES AIR TIRTANADI DENGAN MENGGUNAKAN GAS
PEMBAKAR YANG BERBEDA DENGAN METODE
SPEKTROFOTOMETRI SERAPAN ATOM
TESIS
Oleh
ELLIWATI HASIBUAN 097006003/KIM
FAKULTAS MATEMATIK DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
JUDUL TESIS :ANALISIS LOGAM ALUMINIUM (Al) DAN
CALSIUM (Ca) PADA PROSES AIR TIRTANADI
DENGAN MENGGUNAKAN GAS PEMBAKAR
YANG BERBEDA DENGAN METODE SPEKTRO
FOTO METRI SERAPAN ATOM
Nama Mahasiswa : Elliwati Hasibuan Nomor Pokok : 097006003
Program Studi : Kimia
Menyetujui Komisi Pembimbing
(Prof. Dr. Zul Alfian, MSc) (Prof. Dr. Harry Agusnar, MSc, M. Phil.)
Ketua Anggota
Ketua Program Studi, Dekan
Tanggal lulus : 20 Juni 2011
Telah diuji pada
Tanggal : 20 Juni 2011
PANITIA PENGGUJI TESIS
Ketua : Prof. Dr. Zul Alfian, MSc
Anggota : 1. Prof. Dr. Harry Agusnar, MSc, M. Phil.) 2. Prof. Basuki Wirjosentono, MS, PhD 3. Prof. Dr. Harlem Marpaung, MSc 4. Dr. Hamonangan Nainggolan, Msc
ANALISIS LOGAM ALUMINIUM (Al) DAN CALSIUM (Ca) PADA
PROSES AIR TIRTANADI DENGAN MENGGUNAKAN GAS
PEMBAKAR YANG BERBEDA DENGAN METODE
SPEKTROFOTOMETRI SERAPAN ATOM
TESIS
Diajukan Sebagai Salah Satu Syarat untuk Memperoleh Gelar Magister Sains Dalam Program Studi Ilmu Kimia pada Fakultas Matematik dan Ilmu
Pengetahuan Alam Universitas SumateraUtara
Oleh
ELLIWATI HASIBUAN 097006003/KIM
FAKULTAS MATEMATIK DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERNYATAAN
ANALISIS LOGAM ALUMINIUM (Al) DAN CALSIUM (Ca) PADA
PROSES AIR TIRTANADI DENGAN MENGGUNAKAN GAS
PEMBAKAR YANG BERBEDA DENGAN METODE
SPEKTROFOTOMETRI SERAPAN ATOM
TESIS
Dengan ini saya menyatakan bahwa dalam tesis ini tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan disuatu Perguruan Tinggi dan sepanjang pengetahuan saya tidak terdapat karya atau pendapat yang pernah ditulis atau diterbitkan oleh orang lain kecuali secara tertulis diacu dalam naskah dan disebutkan sumbernya dalam daftar pustaka.
Medan, 20 Juni 2011 Penulis
ANALISIS LOGAM ALUMINIUM (Al) DAN CALSIUM (Ca)
PADA PROSES AIR TIRTANADI DENGAN MENGGUNAKAN GAS
PEMBAKAR YANG BERBEDA DENGAN METODE
SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Telah dilakukan penelitian analisis logam Aluminium (Al) dan Calsium (Ca) pada air PDAM TIRTANADI dari Sunggal Medan dengan menggunakan gas pembakar yang berbeda dengan metode Spektrofotometri Serapan Atom. Sampel air diambil dari dua tempat yaitu : Air flokulasi dan Air reservoir. Sampel dianalisa sekali sebulan selama 3 bulan. Hasil penelitian análisis kadar Aluminium (Al) dalam air flokulasi adalah : 0.3338 ± 0.0089 mg/L dalam air reservoir dengan Nitrous-Asetilen adalah Al 0.1810 ± 0.0099 mg/L. Pengukuran kadar logam Ca dengan metode SSA menggunakan gas Asetilen-Udara dibandingkan dengan Nitrous-Asetilen hasil pengukuran kadar Ca dengan Asetilen-Udara adalah: untuk air flokulasi 5.3884 ± 0.0023 mg/L dan 1.9467 ± 0.0009 mg/L, untuk air reservoir 3.9046 ± 0.0012 mg/L dan dengan Nitrous-Asetilen Ca 1.5479 ± 0.0003 mg/L. Untuk análisis logam Ca yang terbaik digunakan gas pembakar Asetilen-Udara. Untuk logam Al dimana Asetilen-Udara tidak dapat ditentukan tapi digunakan gas pembakar Nitrous-Asetilen. Air dari proses pengolahan pada air PDAM TIRTANADI dari Sunggal Medan memenuhi syarat kesehatan untuk diminum berdasarkan Parameter untuk logam Al dan Ca sesuai PEMENKES RI No. 492/Menkes/Per/IV/2010.
ANALYSIS OF ALUMINIUM AND CALSIUM IN THE PDAM TIRTANADI PROSCESS BY USING SPECTRTROFOTOMETRE ABSORPTION METHOD
WITH DIFFERENT GAS
ABSTRACT
The Analysis of Aluminum and Calcium in the PDAM Sunggal Medan water that is floculation water and after floculation water has been carried out by using Spectrophotometre Absorption method with air-acetylene gas and nitrous-acetylene. The results of analysis of Al was 0.338 ± 0.005 mg/L floculation water and 0.1810 ± 0.0005 mg/L for water after floculation with nitrous-acetylene. The results of analysis of Ca was 5.3884 ± 0.0023 mg /L for floculation water and 1.9467 ± 0.0009 mg /L for water after floculation with air-acetylene gas, whereas with nitrous-acetylene was of 1.5479 ± 0.0003 mg/L. The analysis of Aluminium was achieved by using nitrous-acetylene and did not give result with air-nitrous-acetylene. The rersult show the concentraction of Ca and Al in the PDAM Tirtanadi Sunggal Medan is fulfalled the requirement of the PERMENKES No. 492/Menkes/Per/IV/2010.
KATA PENGANTAR
Puji dan syukur penulis panjatkan kehadirat Allah SWT yang memberi limpahan rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan tesis ini.
Dengan selesainya tesis ini, penulis mengucapkan terimakasih yang sebesar-besarnya kepada : Rektor Universitas Sumatera Utara, Bapak Prof. Dr. dr. Syahril Pasaribu DMTH, MSc, CTM SpA(K), atas kesempatan dan fasilitas yang diberikan kepada penulis untuk menyelesaikan Program Magister, Dekan FMIPA Dr. Sutarman, MSc. Dan ketua Program Studi Kimia, Bapak Prof. Basuki Wirjosentono, MS, PhD. Atas kesempatan yang telah diberikan kepada penulis untuk menjadi mahasiswa Program Mangister pada Sekolah Pascasarjana Universitas Sumatera Utara.
Terima kasih yang sebesar-besarnya dan penghargaan yang setinggi-tingginya kepada :
1. Bapak Prof. Dr. Zul Alfian, MSc. Selaku Dosen Pembimbing Utama dan Bapak Prof. Dr. Harry Agusnar, MSc, M. Phil. Selaku Anggota Komisi Pembimbing yang setiap saat dengan penuh perhatian dan selalu menyediakan waktu untuk memberikan bimbingan, saran dan motivasi sehingga tesis ini dapat penulis selesaikan.
2. Bapak Prof. Basuki Wirjosentono, MS, PhD. Bapak Prof. Dr. Harlem Marpaung, MSc Bapak Dr. Hamonangan Nainggolan, MSc. Selaku dosen pembanding yang banyak memberikan saran dan masukan dalam penulisan tesis ini.
3. Alm. Ibunda F. Siregar, Alm Ayahanda K. Hasibuan, BA serta saudara/saudari Alm. Abang Ir. Parhimpunan Raja. Indra Hasibuan, Alm. Haris Hasibuan, SH dan Kakak Dra. Ida Lumongga Hasibuan, Apt, MHum dan adek-adek Ir. Muhammad Abduh MP Hasibuan, Muhammad Ali Ansyari Hasibuan, SH, SpN, Netty Mutiara Hasibuan ST, Ibrahim Isnan Hasibuan, ST atas doa serta dukungannya baik moril maupun material.
Matematik dan Ilmu Pengetahuan Alam.
5. Bapak dan Ibu Dosen serta pegawai Sekolah Pascasarjana, Program Studi Kimia yang telah memberikan ilmu dan motivasi bagi penulis.
6. Bapak Ketua Departemen Kimia Fakultas Kedokteran USU dr. Simon Marpaung, M.Kes dan Bapak Dekan Fakultas Kedokteran USU Prof. Gontar A. Siregar, SpPD. KGEH yang memberikan rekomendasi kepada saya untuk mengikut Program Mangister Ilmu Kimia di Sekolah Pasca Sarjana Universitas Sumatera Utara atas izin dan bantuannya saya ucapkan terimakasih.
7. Teman-teman mahasiswa angkatan 2009, Zulhan Efendi Sinaga, Elly Suryani Harahap, Ahmad Afifullah Ritonga, Hendri Faisal, Sumatera Tarigan, Haposan Manalu, Lintong Pane, Cut Wira dan angkatan 2010 Ridwan Harahap Fakultas Matematik dan Ilmu Pengetahuan Alam/ Program Studi Kimia yang telah banyak memberikan bantuan moril dan dorongan kepada penulis. Penulis menyadari bahwa tesis ini masih banyak kekurangan dan masih jauh dari sempurna, oleh karena itu penulis sangat mengharapkan kritik dan saran yang sifatnya membangun dari pihak pembaca untuk kesempurnaan bagi penelitian dan kemajuan ilmu amin.
Medan, 20 Juni 2011
RIWAYAT HIDUP
Penulis dilahirkan di Sipirok, Kecamatan Sipirok, Kabupaten Tapanuli Selatan pada tanggal 17 Oktober 1962, sebagai anak ke empat dari K.Hasibuan BA, dan F.Siregar.
Penulis menjalani pendidikan SD Negeri 7 Sipirok tamat Tahun 1974, SMP Negeri 1 Sipirok tamat Tahun 1977, SMA Negeri 2 Medan tamat Tahun 1981.
Kemudian melanjutkan pendidikan pada Program D3 Pendidikan Kimia Analis Universitas Sumatera Utara tamat Tahun 1985.
Pada Thn 1991 penulis bekerja di Kantor Gubernur di Biro Pembangunan Daerah sebagai tenaga honor sampai Tahun 1999. Dan Tahun 2000 diangkat sebagai Laboran di Fakultas Kedokteran USU dan Asisten di Laboratorium Kimia FK USU.
Pada Tahun 2001 penulis melanjutkan pendidikan S1 di Kimia Nondik di Universitas Negeri Medan tamat Tahun 2004. Pada Tahun 2004 s/d 2009 penulis menjadi Dosen Luar biasa di Fakultas Keperawatan Universitas Sumatera Utara.
Pada Tahun 2005 penulis menjadi Dosen Luar biasa di Fakultas Kedokteran Gigi USU sampai sekarang. Pada Tahun 2007 sampai 2008 Dosen di STIKES TAKASIMA Medan. Pada Tahun 2008 penulis menjadi Dosen Luar biasa di Fakultas Kedokteran USU.
DAFTAR ISI
Halaman
ABSTRAK i
ABSTRACT ii
KATA PENGANTAR iii
RIWAYAT HIDUP v
DAFTAR ISI vi
DAFTAR TABEL ix
DAFTAR GAMBAR xi
DAFTAR LAMPIRAN ix
BAB 1 PENDAHULUAN 1
1.1. Latar belakang 2
1.2. Permasalahan 3
1.3. Pembatasan masalah 3
1.4.Tujuan Penelitian 3
1.5. Manfaat penelitian 3
1.6. Lokasi Penelitian 3
1.7. Metodologi Penelitian 3
BAB 2 Tinjauan Pustaka 4
2.1. Logam 4
2.2. Aluminium (Al) 4
2.3. Calsium 5
2.4. Spektrofotometer Serapan Atom (SSA) 6
2.5. Instrumentasi Spektrofotometer Serapan Atom (SSA) 6
2.6. Peralatan Spektrofotometer Serapan Atom (SSA) 7
2.6.1. Sumber radiasi 7
2.6.3. Systim pembakar 8
2.6.4. Monokromator 8
2.6.5. Detektor 8
2.6.6. Read Out 8
2.7. Sistim Atomisasi 9
2.7.1. Jenis-jenis nyala yang digunakan 10
2.7.2. Gas pembakar 11
2.8. Kegunaan Spektrofotometer Serapan Atom (SSA) 12 2.9. Faktor-faktor gangguan dalam Spektrofotometer Serapan Atom (SSA) 12
2.10. Atomisasi sampel 13
BAB 3 METODE DAN BAHAN PENELITIAN 14
3.1. Alat-alat yang digunakan 14
3.1.1. Alat-alat yang digunakan 14
3.1.2. Bahan-bahan yang digunakan 14
3.2. Cara pengambilan sampel 15
3.3. Prosedur kerja 15
3.3.1. Persiapan pengawetan sampel contoh uji dengan Asam Nitrat 15
3.3.2. Persiapan contoh uji/preparasi sampel dengan larutan HNO3 15
3.3.3. Persiapan contoh uji/preparasi sampel 15
3.3.4. Pembuatan larutan standar Aluminium 100 mg/L 16
3.3.5. Pembuatan larutan standar Aluminium 10 mg/L 16 3.3.6. Pembuatan larutan Seri Standar Aluminium 16
3.3.7. Pembuatan larutan standar Kalsium 100 mg/L 16
3.3.8. Pembuatan larutan Kalsium 10 mg/L 16
3.3.9. Pembuatan larutan Seri Standar Kalsium 16
3.3.10. Pembuatan Pembuatan kurva standar Kalsium dan penentuan kadar Kalsium Pada sampel 16
3.3.11. Pembuatan Pembuatan kurva standar Aluminiumum dan penentuan kadar Aluminium Pada sampel 16
3.4. Bagan penelitian 18
3.4.1. Pembuatan kurva kalibrasi Ca menggunakan SSA 18
3.4.2. Persiapan dan pengawetan contoh uji 19
3.4.3. Pembuatan kurva kalibrasi Aluminium 20
3.4.4. Persiapan dan pengwetan contoh uji Al 21
BAB 4 HASIL PENELITIAN 22
4.1. Hasil penelitian 22
4.1.1. Pengukuran kadar Aluminium 22
4.1.2. Penurunan garis regresi dengan Metode Least 23
4.1.3. Perhitungan koefisien korelasi 25
4.1.4. Penentuan kadar Aluminium Nitrous-Asetilen 25
4.1.5. Pengukuran kadar Calsium (Ca) 27
4.1.6 Penentuan kadar Ca nyala Asetilen-Udara 28
4.1.7. Penentuan kadar Ca nyala Nitrous-Asetilen 33 4.2. Pembahasan 36
BAB 5 KESIMPULAN 39
5.1. Kesimpulan 39
5.2. Saran 39
DAFTAR TABEL
Nomor Judul Halaman
1. Tabel 1.1.Campuran gas pembakar yang digunakan dalam analisis logam 11 2. Tabel 4.1 kondisi SSA Merek Shimadzu tipe AA-6300 22 3. Tabel 4.2. Data absorbansi larutan seri standar Al nyala Nitrous-Asetilen 22 4. Tabel 4.3. Hasil pengukuran absorbasi Logam Al dalam sampel air flokulasi Secara SSA nyala Nitrous Asetilen 23 5. Tabel 4.4. Penurunan persamaan garis regresi metode Least Square untuk
Al nyala Nitrous-Asetilen 24
6. Tabel 4.5. Hasil pengukuran kadar logam Al dalam sampel air flokulasi
Secara SSA Dengan Nitrous-Asetilena 26
7. Tabel 4.6. Hasil pengukuran absorbansi Logam Al dalam sampel air reservoir
secara SSA nyala Nitrous-Asetilen 26
8. Tabel 4.7. Hasil pengukuran kadar logam Al dalam sampel air reservoir
secara SSA Dengan Ntrous-Asetilen 26
9. Tabel 4.8. Tabel kondisi SSA Merek Shimadzu tipe AA 6300 27 10. Tabel 4.9.Data absorbansi larutan seri standar Asetilen-Udara 27 11. Tabel 4.10 Hasil pengukuran Absorbansi Logam Ca dalam sampel air
flokulasi Secara SSA nyala Asetilen-Udara 28 12. Tabel 4.11. Hasil pengukuran kadar logam dalam sampel air bak penjernih
(flokulasi) Secara SSA dengan Nitrous-Asetilen 29 13. Tabel 4.12. Hasil pengukuran absorbansi logam Ca dalam sampel reservoir
secara SSA nyala Asetilen-Udara 30
14. Tabel 4.13. Hasil pengukuran kadar logam Ca dalam sampel reservoir secara
SSA nyala Asetilen-Udara 31
15. Tabel 4.14. Kondisi alat SSA Merk Shimadzu tipe AA-6300 pada
pengukuran konsentrasi Ca 31
16. Tabel 4.15. Hasil Data absorbansi larutan seri standar Calsium 32 17. Tabel 4.16. Hasil pengukuran absorbansi logam Ca dalam sampel flokulasi 32 secara SSA nyala Nitrous-Asetilen
18. Tabel 4.17. Hasil pengukuran kadar logam Ca dalam sampel flockulasi
secara SSA nyala Nitrous-Asetilen 34
19. Tabel 4.18. Hasil pengukuran absorbansi logam Ca dalam sampel reservoir
secara SSA nyala Nitrous-Asetilen 34
20. Tabel 4.19 Hasil pengukuran kadar logam Ca dalam sampel air reservoir secara
DAFTAR GAMBAR
Nomor Judul Halaman
1. Gambar 2.1 Sistimatis ringkas dari alat Spektrofotometri Serapan atom 6 2. Gambar 2.2. Spektrofotometri Serapan Atom 10 3. Gambar 2.3. Tungku Spektrofotometri Serapan Atom 10 4. Gambar 4.1. Kurva kalibrasi larutan seri standar Aluminium (Al) dengan nyala
Nitrous-Asetilen 23
5. Gambar 4.2. Kurva kalibrasi larutan seri standar Calsium dengan nyala
Asetilen-Udara 28
6. Gambar 4.4. Kurva kalibrasi larutan seri standar Calsium dengan nyala
DAFTAR LAMPIRAN
Nomor Judul Halaman
ANALISIS LOGAM ALUMINIUM (Al) DAN CALSIUM (Ca)
PADA PROSES AIR TIRTANADI DENGAN MENGGUNAKAN GAS
PEMBAKAR YANG BERBEDA DENGAN METODE
SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Telah dilakukan penelitian analisis logam Aluminium (Al) dan Calsium (Ca) pada air PDAM TIRTANADI dari Sunggal Medan dengan menggunakan gas pembakar yang berbeda dengan metode Spektrofotometri Serapan Atom. Sampel air diambil dari dua tempat yaitu : Air flokulasi dan Air reservoir. Sampel dianalisa sekali sebulan selama 3 bulan. Hasil penelitian análisis kadar Aluminium (Al) dalam air flokulasi adalah : 0.3338 ± 0.0089 mg/L dalam air reservoir dengan Nitrous-Asetilen adalah Al 0.1810 ± 0.0099 mg/L. Pengukuran kadar logam Ca dengan metode SSA menggunakan gas Asetilen-Udara dibandingkan dengan Nitrous-Asetilen hasil pengukuran kadar Ca dengan Asetilen-Udara adalah: untuk air flokulasi 5.3884 ± 0.0023 mg/L dan 1.9467 ± 0.0009 mg/L, untuk air reservoir 3.9046 ± 0.0012 mg/L dan dengan Nitrous-Asetilen Ca 1.5479 ± 0.0003 mg/L. Untuk análisis logam Ca yang terbaik digunakan gas pembakar Asetilen-Udara. Untuk logam Al dimana Asetilen-Udara tidak dapat ditentukan tapi digunakan gas pembakar Nitrous-Asetilen. Air dari proses pengolahan pada air PDAM TIRTANADI dari Sunggal Medan memenuhi syarat kesehatan untuk diminum berdasarkan Parameter untuk logam Al dan Ca sesuai PEMENKES RI No. 492/Menkes/Per/IV/2010.
ANALYSIS OF ALUMINIUM AND CALSIUM IN THE PDAM TIRTANADI PROSCESS BY USING SPECTRTROFOTOMETRE ABSORPTION METHOD
WITH DIFFERENT GAS
ABSTRACT
The Analysis of Aluminum and Calcium in the PDAM Sunggal Medan water that is floculation water and after floculation water has been carried out by using Spectrophotometre Absorption method with air-acetylene gas and nitrous-acetylene. The results of analysis of Al was 0.338 ± 0.005 mg/L floculation water and 0.1810 ± 0.0005 mg/L for water after floculation with nitrous-acetylene. The results of analysis of Ca was 5.3884 ± 0.0023 mg /L for floculation water and 1.9467 ± 0.0009 mg /L for water after floculation with air-acetylene gas, whereas with nitrous-acetylene was of 1.5479 ± 0.0003 mg/L. The analysis of Aluminium was achieved by using nitrous-acetylene and did not give result with air-nitrous-acetylene. The rersult show the concentraction of Ca and Al in the PDAM Tirtanadi Sunggal Medan is fulfalled the requirement of the PERMENKES No. 492/Menkes/Per/IV/2010.
BAB 1
PENDAHULUAN
1.1. Latar Belakang
Spektrofotometri Serapan Atom (SSA) di dalam beberapa dekade menjadi salah satu cara yang paling luas digunakan untuk teknik analisa logam (Kennedy, J. H.1984 ). SSA digunakan untuk analisis kuantitatif unsur-unsur logam dalam jumlah sekelumit (trace) dan sangat kelumit (ultratrace). Cara analisis ini memberikan kadar total unsur logam dalam suatu sampel dan tidak tergantung pada bentuk molekul dari logam sampel tersebut (Rohman, A. 2007). Sampai saat ini telah digunakan untuk mendeteksi (menganalisa) hampir keseluruhan unsur-unsur logam yang terdapat di dalam sistim berkala unsur (sistim periodik unsur). Metode SSA digunakan untuk menganalisis sampel yang terdapat di dalam bahan-bahan biologi, pertanian, makanan dan minuman, air, tanah, pupuk, besi baja dan juga bahan-bahan pencemar lingkungan. Pada tahun terakhir ini sesuai kemajuan Iptek alat SSA semakin sensitive dan canggih dan dapat digabungkan dengan komputer dalam pengelolaan datanya. Investasi besar dalam peralatan-peralatan seperti SSA amat penting dalam menunjang kemampuan laboratorium. Sebagai metode analisa yang popular untuk analisa logam disamping sederhana ia juga selektif dan sangat sensitip (K. Kacaribu, 2008).
Beberapa unsur logam sangat dibutuhkan oleh makluk hidup untuk mempertahankan kehidupannya. Tetapi ada juga yang memberikan dampak buruk logam berat biasanya menimbulkan efek-efek khusus pada makluk hidup. Dapat dikatakan secara umum bahwa semua logam berat dapat menjadi bahan racun bagi makluk hidup. Namun demikian meski semua logam berat dapat mengakibatkan keracunan atas makluk hidup, meskipun sebagian logam-logam berat tersebut tetap dibutuhkan makluk hidup. Kebutuhan tersebut berada dalam jumlah yang sangat sedikit (Palar, 2008).
Logam berat jika sudah terserap kedalam tubuh akan menumpuk akumulatif) hingga nantinya dibuang melalui proses pembuangan. Hal serupa juga terjadi apabila suatu lingkungan terutama perairan telah terkontaminasi logam berat maka proses pembersihannya akan sulit sekali dilakukan (Putra, A.Johan. 2006).
Adanya banyak variasi nyala yang dipakai betahun-tahun untuk spektrometri atom. Sumber yang paling banyak digunakan adalah campuran asetilen-udara dan Nitrous-Asetilen.
a. Nyala Asetilen-udara (Udara-C2H2)
Nyala dapat digunakan pada hampir semua atom dan mempunyai suhu maximumnya 2.300oC.
b. Nyala Nitrous oksida asetilen (N2O- C2H2)
Nyala ini mempunyai temperatur tinggi suhu maximumnya 2.955 oC.
Air alami banyak mengandung logam-logam dalam jumlah kecil dan jumlah ini semakin besar bila menerima asupan dari aktivitas manusia. Dalam penelitian ini dianalisis logam Ca dan Al yang diolah pada pengolahan air minum PDAM TIRTANADI dari Sunggal Medan. Mengingat atom-atom akan menyerap cahaya pada panjang gelombang tertentu, tergantung pada sifat logamnya. Nyala yang diperlukan untuk penetapan logam Calsium menyerap panjang gelombangnya 422,7 nm, dan untuk Aluminium 309,3 nm (Rohman, A. 2007) jauh berbeda maka timbul keinginan untuk menganalisis Ca dan Al dengan metode SSA menggunakan gas pembakar Asetilen-Udara dan Nitrous-Asetilen.
Dilaboratorium gas pembakar yang tersedia biasanya terbatas dan yang sering tersedia adalah gas Asetilen-Udara untuk digunakan dalam análisis logam.
1.2. Permasalahan
1. Bagai mana efisiensi gas pembakar Asetilen-Udara dibandingkan dengan Gas pembakar Nitrous-Asetilen pada logam Aluminium dan Calsium.
2. Apakah analisa kadar logam Aluminium (Al) dan Calsium (Ca) di PDAM Tirtanadi dari Sunggal Medan memenuhi stándar air Permenkes,bila menggunakan Asetilen-Udara atau gas Nitrous-Asetilen.
1.3. Pembatasan masalah
1. Penentuan análisis logam Aluminium (Al) dan Ca dengan gas pembakar Asetilen- Udara dan Nitrous-Asetilen.
2. Menganalisis kadar Aluminium (Al) dan Calsium (Ca) pada proses air minum PDAM Tirtanadi yang berasal dari Sunggal Medan dengan menggunakan metode Spektrofotometri Serapan Atom.
3. Analisa kwantitatip yang digunakan dengan SSA, setelah diperoleh gas pembakar yang efisiensi, maka dilakukan pemeriksaan terhadap logam Aluminium dan Calsium pada air PDAM Tirtanadi di Sunggal Medan apakah masih sesuai dengan Permenkes.
1.4. Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah :
Untuk mengetahui análisis logam Aluminium (Al) dan Calsium (Ca) pada proses air PDAM Tirtanadi dari Sunggal Medan dengan gas pembakar yang berbeda.
1.5. Manfaat Penelitian
Dari hasil penelitian ini diharapkan dapat memberikan informasi bahwa dalam pengukuran logam Aluminium (Al) dan Calsium (Ca) dapat dipilih gas yang paling efektif digunakan pada analisa SSA.
1.6. LokasiPenelitian
1. Laboratorium Kimia Analitik FMIPA Universitas Sumatera Utara 2. Lokasi pengambilan sampel air PDAM Tirtanadi di Sunggal Medan. 1.7. Metodologi Penelitian
1. Penelitian ini merupakan eksperimen laboratorium
2. Sampel yang digunakan adalah dari proses pengolahan air minum PDAM Tirtanadi dari Sunggal Medan yang berasal dari :
1. Air dari bak penjernih (flokulasi) 2. Air olahan (Reservoir)
BAB 2
TINJAUAN PUSTAKA 2. 1. Logam
Dalam kehidupan sehari-hari, kita tidak terpisah dari benda-benda yang bersifat
logam. Benda ini kita gunakan sebagai alat perlengkapan rumah tangga seperti sendok,
garpu,pisau dan lain-lain sampai pada tingkat perhiasan mewah yang tidak dapat dimiliki
oleh semua orang seperti emas, perak dan lain-lain. Secara gamlang dalam konotasi
keseharian kita beranggapan bahwa logam diidentikkan dengan besi. Logam tersebut
padat keras berat dan sulit dibentuk (Palar, 2008).
Logam berat adalah unsur logam dengan molekul tinggi. Dalam kadar yang
rendah sekalipun logam berat umumnya sudah beracun bagi tumbuhan dan hewan,
termasuk manusia. (Notohadiprawiro,T.1993)
Logam berat ini dapat menimbulkan efek kesehatan bagi manusia tergantung
bagian mana logam berat terikat dalam tubuh.
Lebih jauh lagi, logam berat ini akan bertindak sebagai penyebab alergi, bagi beberapa
orang karsinogen bagi manusia. Jalur masuknya adalah melalui kulit, pernapasan dan
pencernaan.
Logam berat jika sudah terserap kedalam tubuh akan menumpuk hingga nantinya
dibuang melalui proses ekskresi. Hal serupa juga terjadi apabila suatu lingkungan
terutama perairan telah terkontaminasi (tercemar) logam berat maka proses
pembersihannya akan sulit sekali dilakukan. Kontaminasi logam berat ini dapat berasal
dari faktor alam seperti kegiatan gunung berapi dan kebakaran hutan atau factor manusia
seperti pembakaran minyak bumi, pertambangan, peleburan, proses industry, kegiatan
pertanian, peternakan dan kehutanan, serta limbah buangan termasuk sampah rumah
tangga. (Putra.J.A.2006).
2.2. Aluminium
Aluminium merupakan logam yang paling banyak di dunia, ditemukan dalam
tanah, dalam air dan udara. Sekitar 8 % kerak bumi terdiri dari Aluminium. Elemen
ini adalah elemen paling berlimpah yang secara alami terdapat di udara, tanah dan air.
hanya ke suplai air tapi juga kebanyakan makanan dan obat yang diproses (Tony
Sarvinder Singh,2006). Terlalu banyak asupan aluminium dapat memberikan efek
negative yang dapat merusak otak (menyebabkan Alzheimer), menyebabkan kerusakkan
DNA, disfungsi ginjal, serta diduga dapat memicu kanker payudara. Sumber
alumunium yang bisa dikhawatirkan antara lain kandungannya di dalam obat-obatan,
seperti antacids, aspirin, obat anti diarrhea, bedak bayi dan lipstick. Selain itu agar
waspada terhadap alat masak yang terbuat dari bahan aluminium karena alat ini
dapat bereaksi kimia bila terkena asam cuka, Asam tomat, asam jawa, asam jeruk dan
sebagainya.
Aluminium terakumulasi di berbagai jaringan di dalam tubuh, termasuk otak, ginjal, hati,
paru-paru, dan tiroid. Aluminium bersaing dengan kalsium dalam proses absorpsi
sehingga dapat mengakibatkan mineralisasi tulang berkurang.
Pada bayi hal ini menghambat pertumbuhan. Hal ini juga mengganggu penyerapan
fosfor, seng dan selenium oleh tubuh. Potensi bahaya dari keracunan Alumunium
antara lain: dapat menyebabkan kerusakan otak, luka usus dan lambung, penyakit
gastrointestinal, Parkinson's Disease, masalah kulit, retardasi mental pada bayi,
gangguan belajar pada anak, penyakit hati, sakit kepala, mual mulas, sembelit,
kurangnya energy dan perut kembung (Suara media, 2011).
2.3. Calsium (Ca)
Kalsium adalah logam metalik, unsur kelima terbanyak di kerak bumi. Unsur ini
merupakan bahan baku utama dedaunan, tulang belulang, gigi dan kerang dan kulit
telur. Kalsium tidak pernah ditemukan di alam tanpa terkombinasi dengan unsur
lainnya. Ia banyak terdapat sebagai batu kapur, gipsum, dan fluorite. Apatite merupakan
flurofosfat atau klorofosfat kalsium (Mohsin,Y.2006).
Kalsium terdapat sebanyak 99 % dalam tulang kerangka dan sisanya dalam cairan antar
sel dan plasma. Kalsium mengatur permeabilitas membrane sel bagi K dan Na dan
mengaktivasi banyak enzim, seperti pembekuan darah. Defesiensi kalsium menyebabkan
lunaknya tulang serta mudah terangsangnya syaraf otot dengan akibat kejang. Dalam
kebanyakan kasus kekurangan disebabkan oleh defisiensi vitamin D dan terlambatnya
Kalsium diperlukan sebagai bahan gizi untuk tanaman tinggkat tinggi dan sebagai
mikronutrien untuk sejumlah ganggang. Walaupun kalsium merupakan mineral yang
dibutuhkan manusia dan hewan, jumlah yang ditemukan dalam air tidaklah cukup. Disisi
lain kalsium merupakan konstituen utama dalam air sadah (Montgomery, J. M. 1985).
2.4. Spektrofotometri Serapan Atom (SSA)
Teknik Analisis spektrofotometri termasuk salah satu teknik analisis instrumental
disamping teknik kromatografi dan elektrolisis kimia. Teknik tersebut memanfaatkan
fenomena interaksi materi dengan gelombang elektromagnetik seperti sinar-X,
ultraviolet, cahaya tanpak dan inframerah. Fenomena interaksi bersifat spesifik baik
absorbsi maupun emisi. Interaksi tersebut menghasilkan signal-signal yang disadap
sebagai analisa kualitatif dan kuantitatif. Contoh teknik absorbsi atom (SSA) yang
merupakan alat ampuh dalam analisis logam (K. Kacaribu, 2008)
SSA adalah metoda analisis yang berdasarkan pada pengukuran radiasi cahaya
yang diserap atom bebas. Analisis menggunakan alat SSA ini memiliki keuntungan dari
hasil analisisnya yang sangat peka, teliti dan cepat, pengerjaannya relatip sederhana serta
tidak perlu dilakukan pemisahan unsur logam dalam pelaksanaannya.
Analisis SSA yang didasarkan pada penyerapan energi radiasi dari sumber nyala
atom-atom yang berada pada tingkat energi dasar. Komponen-komponen utama yang
menyusun SSA adalah sumber cahaya, atomizer, monokromator, detector, dan
penampilan data (Anderson,1987). Penggunaan SSA dalam menganalisa kandungan
logam-logam, dikarenakan dengan metode SSA unsur-unsur dengan energi eksitasi
rendah.
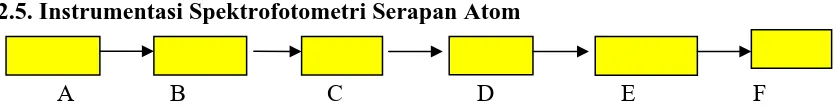
2.5. Instrumentasi Spektrofotometri Serapan Atom
A B C D E F
Gambar 2.1. Sistematis Ringkas dari Alat Spektrofotometri Serapan Atom
Keterangan :
A. Lampu Katoda Berongga
dari unsur logam yang akan dianalisa (setiap logam memiliki lampu khusus untuk
logam tersebut)
B. Chopper
Mengatur sinar yang dipancarkan
C. Tungku
Tempat pembakaran (untuk memecahkan larutan sampel pada tetesan halus dan
meleburkannya kedalam nyala untuk diatomkan).
D. Monokromator
Mendispersi sinar yang ditransmisikan oleh atom.
E. Detector
Mengukur sinar yang ditranmisikan dan memberikan signal sebagai respon terhadap
terhadap sinar yang diterima.
F. Meter bacaan nilai absorbansi
Gunanya untuk membaca nilai absorbansi (Haris, 1978).
2.6. Peralatan SSA 2.6.1. Sumber radiasi
Sumber radiasi yang digunakan harus memancarkan spektrum atom dari unsur
yang ditentukan. Spektrum atom yang dipancarkan harus terdiri dari garis tajam yang
mempunyai setengah lebar yang sama dengan garis serapan yang dibutuhkan oleh
atom-atom dalam contoh. Sumber sinar lazim dipakai adalah lampu katoda berongga (hallow
chatoda lamp). Untuk penetapan apa saja yang diminta, lampu katoda berongga yang
digunakan mempunyai sebuah katoda pemancar yang terbuat dari unsur yang sama
(Basset dkk 1994).
2.6.2. Nyala
Nyala digunakan untuk mengubah sampel berupa padatan atau cairan menjadi
bentuk uap atomnya, dan juga berfungsi untuk atomisasi. Untuk spektroskopi nyala suatu
persyaratan yang penting adalah bahwa nyala dipakai hendaknya menghasilkan
dalam keadaan dasar maupun dalam keadaan tereksitasi, dipengaruhi oleh komposisi
nyala.
Komposisi nyala asetilen – udara sangat baik digunakan untuk lebih dari tiga
puluh unsur sedangkan komposisi nyala propana –udara disukai untuk logam yang
mudah diubah menjadi uap atomik. Untuk logam seperti Aluminium (Al) dan Titanium
(Ti) yang membentuk oksida refraktori temperatur tinggi dari nyala Nitrous-asetilen
sangat perlu dan sensitivitas dijumpai bila nyala kaya akan asetilen.
2.6.3. Sistim pembakar –pengabut (nebulizer)
Tujuan sistim pembakar- pengabut adalah untuk mengubah larutan uji menjadi
atom-atom dalam bentuk gas. Fungsi pengabut adalah menghasilkan kabut atau aerosol
larutan uji. Larutan yang akan dikabutkan ditarik ke dalam pipa kapiler oleh aksi
semprotan udara yang ditiupkan melalui ujung kapiler, diperlakukan aliran gas
bertekanan tinggi untuk menghasilkan aerosol yang halus. (Basset dkk,1994)
2.6.4. Monokromator
Dalam spektroskopi serapan atom fungsi monokromator adalah untuk
memisahkan garis resonansi dari semua garis yang tak diserap yang dipancarkan oleh
sumber radiasi. Dalam kebanyakan instrumen komersial digunakan kisi difraksi
karena sebaran yang dilakukan oleh kisi seragam dari pada yang dilakukan oleh
prisma dan akibatnya instrumen kisi dapat memelihara daya pisah yang lebih
tinggi sepanjang jangka panjang gelombang yang lebih besar (Braun, RD, 1982).
2.6.5. Detektor
Detektor pada spektrofotometer absorbsi serapan atom berfungsi mengubah
intensitas radiasi yang datang menjadi arus listrik. Pada SSA yang umum
dipakai sebagai detektor adalah tabung penggandaan foton (PMT = Photo
Multiplier Tube Detector) (Mulja, 1977).
Read out merupakan system pencatatana hasil. Hasil pembacaan dapat berupa
angka atau kurva dari suatu recorder yang menggambarkan absorbansi atau
intensitas emisi (Braun, R.D, 1982).
2.7. Sistim Atomisasi A. Sistim Atomisasi nyala
Setiap alat SSA mencakup dua komponen utama sistim introduksi sampel dan
sumber (source) atomisasi. Untuk kebanyakan instrument sumber atomisasi ini adalah
nyala dan sampel di introduksikan dalam bentuk larutan. Sampel masuk ke nyala dalam
bentuk aerosol. Aerosol biasanya dihasilkan oleh Nebulizer (pengabut) yang
dihubungkan ke nyala oleh ruang penyemprot (chamber spray).
Proses atomisasi adalah proses pengubahan sample dalam bentuk larutan
menjadi spesies atom dalam nyala.
Secara ideal fungsi dari sistim atomisasi (source) adalah :
1. Mengubah sembarang jenis sampel menjadi uap atom fasa–gas dengan sedikit
perlakuan atau tampa perlakuan awal.
2. Melakukan seperti poin 1 untuk semua elemen (unsur) dalam sampel pada
semua level konsentrasi.
3. Agar diperoleh kondisi operasi yang identik untuk setiap elemen dalam sampel.
4. Mendapatkan sinyal analitik sebagai fungsi sederhana dari konsentrasi tiap-tiap
elemen yakni agar gangguan dan pengaruh media sampel menjadi minimal.
5. Memberikan analisis yang teliti dan tepat.
6. Pengoperasian yang murah
7. Memudahkan operasi.
B. Sistim Atomisasi dengan Tungku
Sistim nyala api ini lebih dikenal dengan nama GFAAS. GFAAS dapat
mengatasi kelemahan dari sistim nyala seperti, sensivitas, jumlah sampel dan penyiapan
sampel.
Ada tiga tahap atomisasi dengan tungku yaitu ;
a. Tahap pengeringan atau penguapan larutan
c. Tahap atomisasi
Gambar 2.2. Spektrofotometri Serapan Atom dan alat-alat gelas yang digunakan
dalam analisis.
Gambar 2.3. Tungku Spektrofotometri Serapan Atom
2.7.1. Jenis-jenis nyala yang Digunakan
Nyala api utama yang digunakan untuk penyerapan atom dan spektrometri emisi
yang tercantum dalam Tabel 1.1. bersama-sama dengan suhu maksimal akan terbakar.
Api yang paling banyak digunakan untuk penyerapan atom adalah nyala asetilen-udara
dan nitrous oksida - asetilen. Suhu tinggi api yang terakhir ini tidak diperlukan dan
bahkan mungkin merugikan bagi banyak kasus dalam penyerapan atom karena akan
menyebabkan ionisasi dari atom gas. Namun, sangat berguna bagi elemen-elemen
yang cenderung untuk membentuk oksida panas-stabil di udara-asetilen api (yang
"unsur tahan api"). Udara-asetilena dan api hidrokarbon lainnya menyerap sebagian
besar radiasi pada panjang gelombang di bawah 200 nm, dan api udara argon-hidrogen
2.7.2. Gas Pembakar
Pada SSA dipakai dua macam gas pembakar yang bersifat oksidasi dan tahan
bakar. Gas pengoksidasi contohnya udara, udara (dan O2) atau campuran O2 + N2O.
Sedangkan bahan bakar adalah gas alam, propana, butana, asetilen dan H2 atau asetilen.
Gas pembakar dapat merupakan campuran seperti :
- Udara dengan asetilen (terbanyak) dipakai
- N2O dengan asetilen (Mulja, M. Suharman. 1995)
Tabel 1.1. Campuran gas pembakar yang digunakan dalam analisis logam menggunakan metode SAA nyala
Gas campuran nyala Kecepatan maximum nyala
Cm/detik
Dalam spektrometri emisi nyala api, api panas diperlukan untuk analisis sejumlah besar
unsur, dan baik oksigen-asetilen ("asetilin") api atau api nitro oksida-asetilen digunakan.
Nyala api asetilen memiliki kecepatan pembakaran tinggi. (Cristian G. D. 1980).
Kebanyakan metode SSA menggunakan sistim gabungan ini diantara nyala dan bahan
bakar dimana system ini berfungsi, setelah larutan sampel diuapkan. Nyala yang paling
banyak digunakan serapan atom adalah udara-Asetilen yang mempunyai suhu
Pengesanan yang tempat diperlukan dalam menentukan gas dan udara tersebut
untuk mendapatkan gas-udara dan seterusnya memberi pengulangan penentuan yang
memuaskan.
2.8. Kegunaan Spektrofotometri Serapan Atom (SSA)
Metode SSA telah diperkenalkan oleh A.Walsh tahun 1955 dan mengalami
perkembangan yang sangat pesat. Sampai saat ini telah digunakan untuk mendeteksi
(menganalisa) hamper keseluruh unsur-unsur logam yang terdapat di tabel priodik
unsur. Metode Atomic Absorbtion Spectrofotometric banyak digunakan untuk
menganalisis sampel yang terdapat didalam bentuk bahan-bahan pencemar lingkungan
(Zul Alfian 2009). Pada tahun terakhir ini SSA semakin sensitif, canggih dan dapat
digabungkan dengan computer dalam pengolahan datanya. Investasi besar dalam
peralatan-peralatan seperti SSA amat penting dalam menunjang misi laboratirium. Maka
pemanfaatanya bergantung pada kemampuan sumber daya manusia, seperti kemampuan
pemahaman teori dasar, spectrum aplikasi, ketelusuran metode analisis yang disyaratkan
pada SNI 19-17025-2000.
2.9. Faktor-faktor gangguan dalam SSA
Gangguan diartikan sebagai suatu factor kimia atau fisika yang akan
mempengaruhi jumlah atom untuk analit pada keadaan standar (ground state) sehingga
akan menyebabkan bertambah atau berkurangnya bacaan nilai serapan atom unsur yang
dianalisis.
Ada beberapa gangguan dalam menggunakan SSA:
a. Suhu yang sesuai, suhu gas pembakar harus sesuai dengan suhu unsur yang akan
dianalisis.
b. Konsentrasi sampel tidak boleh melebihi kesensitifan dari alat detector SSA.
Ini akan menyebabkan gangguan terhadap garis spectrum dan mengakibatkan
kerusakan pada alat detector SSA.
c. Pengaruh peguapan pelarut dan bahan larutan jangan sampai menurunkan suhu nyala
Memang selain dengan metode SSA, unsur-unsur dengan energi eksitasi rendah dapat
juga dianalis dengan fotometri nyala, tetapi untuk unsur-unsur dengan ekstasi tinggi
hanya dapat dilakukan dengan fotometri nyala. Untuk analisis dengan garis spectrum
resonansi antara 400-800 nm, fotometri nyala sangat berguna, sedangkan antara 200-300
nm metode SSA lebih baik dari fotometri nyala (Kopkar, S.M, 1990).
2.10.Atomisasi menggunakan nyala dapat menganalisis seluruh logam-logam yang terdapat dalam sistim priodik
Proses yang menghasilkan atom-atom bebas (atomisasi) dalam analisis SSA ada
beberapa cara yaitu:
1. Atomisasi Dengan Nyala
Dalam analisis kuantitatif Metode SSA atomisasi dengan nyala, sampel harus disiapkan
berupa larutan. Beberapa cara melarut sampel :
a. Sampel langsung dilarutkan dalam pelarut yang sesuai
b. Sampel dilarutkan dalam asam
c. Sampel terlebih dahulu dilebur dengan pelarut suatu basa (alkali), kemudian hasil
peleburan itu dilarutkan dengan asam.
2. Atomisasi Tanpa Nyala
Dengan teknik tanpa nyala diperoleh sensitivitas pengukuran yang lebih tinggi
dibandingkan teknik nyala. Cara atomisasi tanpa nyala ini adalah hasil perkembangan
yang lebih maju, meliputi atomisasi generasi uap dan atomisasi dengan tungku suhu
tinggi.
3. Atomisasi dengan cara ini terbatas untuk unsur As,Se, Sb,dan Hg
Dengan cara biasa unsur-unsur ini tidak memberikan hasil yang baik. As,Se dan Sb biasa
direduksi menjadi hidrida dalam bentuk gas. Reduktor umum dipakai yaitu SnCl2 atau
NaBH4. Khusus untuk Hg dengan cara ini tidak dibutuhkan pembentukan uap hidrida.
Dengan metode ini Hg mempunyai sensitifitas 0.001 g/ml akan memberikan ketelitian
2000 kali lebih tinggi dari pada penetapan Hg dalam nyala asetilen. Bagai manapun
atomisasi tanpa nyala hanya dapat dilakukan untuk logam-logam dengan temperatur
BAB 3
METODE DAN BAHAN PENELITIAN
3.1. Alat-alat dan bahan
3.1.1. Alat-alat yang digunakan
- Spektrofotometri Serapan Atom AA-6300 Shimadzu
- Lampu hallow katoda
- Lampu katoda
- Erlemeyer 250 ml
- Pipet ukur 5 ml; 10 ml; 15 ml;
- PH meter WlkLAB
- Labu ukur 50 ml Pyrex
- Gelas Beaker Pyrex
- Pemanas listrik
- Labu semprot
- Kertas saring ukuran 0.45 µm
3.1.2. Bahan-bahan yang digunakan
- Akuadest
- Asam Nitrat (HNNO3) p
- Larutan induk Aluminium 1000 mg/L E.Merck
- Larutan induk Kalsium 1000 mg/L E.Merck
- Gas Asetilen
- Gas Nitro Oksida
- Asam klorida (HCl) (1+1)
- Sampel air minum PDAM Titanadi dari Sunggal Medan
- Lantan klorida (LaCl3) (50 g/L)
3.2. Cara pengambilan sampel
Pengambilan sampel memakai teknik sampel sesaat sampel yang diambil secara
langsung dari badan air yang sedang dipantau (G. Alaerts1987). Sampel ini hanya
menggambarkan karakteristik air pada saat pengambilan sampel ( Ehsa 2011).
Pada penelitian ini sebagai populasi air flokulasi dan air olahan (reservoir).
Air flokulasi yaitu air dalam bak setelah penambahan tawas Al2(SO4)3. Air olahan
(reservoir) yaitu air yang mau didistribusikan ke pelanggan.
3.3. Prosedur kerja
3.3.1 Persiapan dan pengawetan contoh uji dengan asam nitrat (HNO3) p
Contoh uji tidak dapat segera dianalisa, maka contoh uji diawetkan dengan
penambahan asam nitrat (HNO)3 p sampai pH kurang dari 2 dengan waktu penyimpanan
maksimal 6 bulan (SNI 06-6989.56-2005).
3.3.2. Persiapan contoh uji/preparasi sampel dengan larutan HNO3 p
a. Sebanyak 100 ml contoh uji/sampel yang sudah dikocok sampai homogen diambil, lalu
dimasukkan kedalam erlenmeyer.
b. Kemudian ditambahkan 5 ml HNO3 p
c. Selanjutnya dipanaskan di pemanas listrik sampai larutan contoh uji hampir kering
d.Setelah didinginkan beberapa saat lalu ditambahkan 50 ml aquadest,kemudian
dimasukkan kedalam labu ukur 100 ml melelui kertas saring dan ditepatkan 100 ml
dengan akuadest.
3.3.3 Persiapan contoh uji /preparasi sampel
Uji gas Asetilen-Udara:
a. Sebanyak 100 ml contoh uji/sampel yang sudah dikocok sampai homogen diambil lalu
dimasukkan kedalam erlemeyer.
b. kemudian ditambahkan 2 mL asam klorida (1+1)
c. Selanjutnya dipanaskan dipemanas listrik sampai lalrutan contoh uji hampir kering
d. Lalu tambahkan 1 mL Lantan Klorida
e. Setelah didinginkan beberapa saat dipindahkan kedalam labu ukur 100 ml
melalui kertas saring dan ditambahkan aquadest sampai tanda batas 100 mL.
f. Diukur serapannya dengan SSA menggunakan gas asetlen-udara.
3.3.4. Pembuatan larutan stándar Aluminium 100 mg/L
Sebanyak 5 ml larutan induk Aluminium 1000 mg/L dimasukkan kedalam labu
takar 50 ml lalu diencerkan dengan aquades sampai garis tanda dan dihomogenkan.
3.3.5. Pembuatan Larutan Standar Alumunium 10 mg/L
Sebanyak 5 ml larutan standar Aluminium 100 mg/L dimasukkan kedalam labu
takar 50 ml lalu diencerkan dengan aquades sampai garis tanda dan
dihomogenkan.
3.3.6. Pembuatan larutan Seri Standar Aluminium 0.0; 1; 2; 3; 4; 5 mg/L
Sebanyak 0.0; 5; 10; 15; 20; dan 25 ml larutan Aluminium 10 mg/L
dimasukkan kedalam labu takar 50 ml lalu diencerkan dengan aquades sampai garis
tanda dan dihomogenkan.
3.3.7. Pembuatan larutan standar Kalsium 100 mg/L
Sebanyak 5 ml larutan induk Kalsium 1000 mg/L dimasukkan kedalam labu takar 50 ml
lalu diencerkan dengan aquades sampai garis tanda dan dihomogenkan.
3.3.8. Pembuatan Larutan Standar Kalsium 10 mg/L
Sebanyak 5 ml larutan standar Kalsium 100 mg/L dimasukkan kedalam labu takar 50 ml
lalu diencerkan dengan aquades sampai garis tanda dan dihomogenkan.
3.3.9 Pembuatan larutan Seri Standar Kalsium 0.0; 0.5; 1; 1.5; 2; 2.5; 3; mg/L
Sebanyak 0,0; 0.25; 5; 7.5; 10; dan 12.5 ml larutan Kalsium 10 mg/L dimasukkan
kedalam labu takar 50 ml lalu diencerkan dengan aquades sampai garis tanda dan
dihomogenkan.
3.3.10. Pembuatan Kurva Standar Kalsium dan Penentuan Kadar Kalsium pada Sampel
Larutan blanko diukur absorbansinya dengan menggunakan Spektrofotometer Serapan
Atom pada spesifik 422.7 nm. Perlakuan dilakukan sebanyak 3 kali. Dilakukan hal
yang sama untuk larutan seri standar kalsium 0.0; 0.5; 1; 1.5; 2; 2.5; 3; mg/L dan
larutan sampel.
3.3.11. Pembuatan Kurva Standar Aluminium dan Penentuan Kadar Aluminium pada sampel
Larutan blanko diukur absorbansinya dengan menggunakan Spektrofotometer Serapan
yang sama untuk larutan seri standar Aluminium 0,0; 1; 2; 3; 4; 5 mg/L dan larutan
sampel.
3.3.12. Preparasi Sampel
Sebanyak 100 ml sampel dimasukkan kedalam gelas beaker. Ditambahkan HNO3 pekat
hingga pH 2-5 lalu diencerkan dengan larutan pengencer sampai garis tanda dan diaduk
3.4. Bagan Penelitian
3.4.1. Pembuatan Kurva Kalibrasi Calsium (Ca) menggunakan SSA Nyala
Larutan standar logam
Calsium (Ca) 1000 mg/L
Sebanyak 5 ml dimasukkan Kedalam labu ukur 50 ml
Ditambah akuadest tepat tanda batas
Ditambah akuades tepat tanda batas
Ditambah akuades tepat tanda batas
Diatur keasamaan pH 3 Dioptimalkan alat SSA
Mengukur larutan standar Calsium (Ca) dengan Nyala pada 422,7 nm
Buat kurva kalibrasi
Pengukuran absorbansi sampel
Lar standar logam Calsium (Ca) 100 mg/L
Sebanyak 5 ml masukkan Kedalam labu ukur 50 ml
Lar standar logam Calsium (Ca) 10 mg/L
0 ml, 2,5 ml, 5 ml, 7,5 ml, 10 ml, 12,5 ml, Masing-masing kedalam Labu ukur 50 ml
Larutan standar Ca konsentrasi 0, 0,5, 1, 1,5,2, 2,5, 3 mg/L
3.4.2. Persiapan dan Pengawetan Contoh uji Ca (SNI 06-6989.56-2005)
Ditambah HNO3 (p) hingga pH 3
Ditambah 2 ml asam klorida (1 + 1 )
Dipanaskan hingga hampir kering
1 ml Lantan Clorida
Dimasukkan ke labu ukur 100 ml dengan cara
disaring dan + air suling hingga tanda tera
Diukur absorbansinya dengan Spektrofotometer
Serapan Atom pada spesifik 422,7 nm untuk
Calsium Sampel air
Awetan sampel
Diambil 100 ml sampel air dikocok hingga homogen
Sampel air mengandung Ca
3.4.3. Pembuatan Kurva Kalibrasi Aluminium (Al) menggunakan SSA Nyala (SNI 06-6989.34-2005)
Larutan standar Aluminium 1000 mg/L
Ditambah akuadest tepat tanda batas
Sebanyak 5 ml dimasukkan Kedalam labu ukur 50 ml
Ditambah akuades tepat tanda batas
Ditambah akuades tepat tanda batas
Diatur keasamaan pH 3
Dioptimalkan alat SSA
Mengukur larutan standar Aluminium (Al) dengan Nyala pada 309,3 nm
Buat kurva kalibrasi
Pengukuran absorbansi sampel Larutan standar Al konsentrasi
0, 1, 2, 3, 4, 5 mg/L
Hasil Sebanyak 5 ml masukkan
Lar standar logam Aluminium (Al) 10 mg/L
0 ml, 5 ml, 10 ml, 15 ml, 20 ml, 25 ml Masing-masing kedalam Labu ukur 50 ml
3.4.4. Persiapan dan Pengawetan Contoh uji Aluminium (Al) (SNI 06-6989.56-2005)
Ditambah HNO3 (p) hingga pH 3
Ditambah 2 ml asam klorida (1 + 1 )
Dipanaskan hingga hampir kering
Saring
Dioptimalkan alat SSA
Diukur absorbansinya dengan Spektrofotometer Serapan Atom pada spesifik 309,3 nm untuk Aluminium
Awetan sampel
Sebanyak 100 ml sampel
Dimasukkan ke labu ukur 100 ml + air suling sampai tanda batas
Sampel air mengandung Al
BAB 4
HASIL PENELITIAN
4.1. Hasil Penelitian
4.1.1. Pengukuran Kandungan Aluminium (Al)
Kondisi alat Spektrofotometer Serapan Atom (SSA) pada pengukuran
konsentrasi Aluminium dapat dilihat pada table 4.1.
Tabel 4.1. Kondisi alat SSA Merek Shimadzu tipe AA-6300 pada
pengukuran konsentrasi Aluminium
No Parameter Spesifikasi metode nyala
1.
Tabel 4.2. Data absorbansi larutan seri standar Aluminium
Gambar 4.1. Kurva kalibrasi larutan seri standar Aluminium dengan Nyala Nitrous-Asetilen.
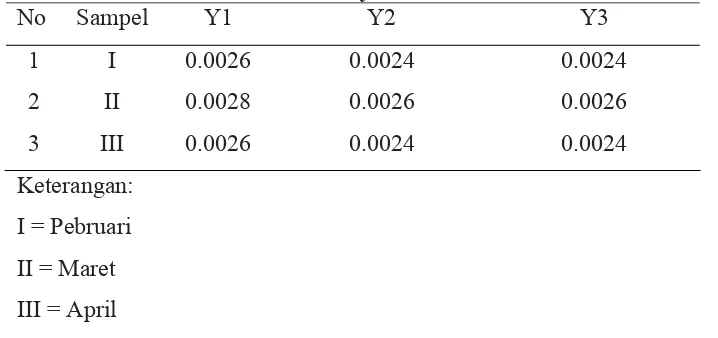
Tabel 4.3. Hasil pengukuran Absorbansi Logam Al dalam sampel air flokulasi secara SSA nyala Nitrous Asetilen
No Sampel Y1 Y2 Y3
1 I 0.0026 0.0024 0.0024
2 II 0.0028 0.0026 0.0026
3 III 0.0026 0.0024 0.0024
Keterangan:
I = Pebruari
II = Maret
III = April
4.1.2. Penurunan garis regresi dengan Metode Least Square
Hasil pengukuran absorbansi seri larutan standar Al pada table 4.2 diplotkan
terhadap konsentrasi larutan standar sehingga diperoleh suatu kurva kalibrasi berupa
garis linier. Persamaan garis regresi untuk kurva kalibrasi ini dapat diturunkan dengan
Tabel 4.4. Penurunan persamaan garis regresi dengan metode Least Square untuk Aluminium nyala Nirous-Asetilen
No Xi Yi Xi‐X Yi‐Y Xi‐X2 Yi‐Y2 (Xi‐x)(Yi‐y)
1 0 0 ‐2.5 ‐0.0185 6.25 0.0003 0.0463
2 1 0.0074 ‐1.5 ‐0.0111 2.25 0.0001 0.0167
3 2 0.0152 ‐0.5 ‐0.0033 0.25 0.0000 0.0017
4 3 0.0215 0.5 0.0029 0.25 0.0000 0.0015
5 4 0.03 1.5 0.0115 2.25 0.0001 0.0172
6 5 0.0371 2.5 0.0186 6.25 0.0003 0.0464
Σ 15 0.1112 0 0 17.5 0.0009 0.1298
Keterangan : Xi = konsentrasi
Yi = Absorbansi
X = ∑ xi = 15 = 2.5 n 6
Y =∑ yi = 0.1112 = 0.018533 n 6
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan garis :
Y = ax + b
dimana a = slope
b = intersep
Selanjutnya harga slope dapat ditentukan dengan menggunakan metode Least Square
sebagai berikut :
a = ∑ (xi-x)(yi-y) ∑ (xi-x)2
b = y-ax
Dengan mensubtitusikan harga-harga yang tercantum pada table 4.4 di atas maka
diperoleh persamaan :
a = 0.1298 = 0,0074 17.5
b = - 0.0000
4.1.3. Perhitungan Koefisien Korelasi
Koefisien korelasi (r) dapat ditentukan sebagai berikut ;
∑{ ( Xi - X)(Yi-Y)}
r =
√{ (∑ Xi – X )2 (∑Yi-Y)2}
= 0.1298 √( 17.5)( 0.0009)
r = 0.9995
4.1.4. Penentuan kadar Al nyala Nitrous-Asetilen
Kadar Al dapat ditentukan dengan menggunakan metode kurva kalibrasi dengan
mensubtitusikan nilai Y (absorbansi) yang diperoleh dari hasil pengukuran terhadap garis
regresi dan kurva kalibrasi Y = 0.0074x + 0.0000 sehingga diperoleh konsentrasi Al.
Untuk sampel bak penjernih (flokulasi) diperoleh diperoleh nilai absorbansi :
Untuk sampel I
Y1 = 0.0026
Y2 = 0.0024
Y3 = 0.0024
Y =0.0074x + 0.0000
X = Y + 0.0000
0,0074
Untuk Y = 0.0026
X1 = 0.0026 + 0.0000
0.0074
= 0.3518
X2 = 0.3248
X3 = 0.3248
X = 0.3338
(X1-X)2 = (0.3518 - 0.3338 ) 2 = 0.0003
(X2-X)2= (0.3248 - 0.3338 ) 2 = 0.0000
(X3-X)2= (0.3248 - 0.3338 ) 2 = 0.0000
Maka S = ∑(Xi – X)2 = 0.0003 = 0.0155
n-1 2
Didapat harga Sx = S = 0.0155 √ n √ 3
= 0.0089
Dari data hasil pengukuran kadar Aluminium dalam air flokulasi (bak penjernih) sampel
I ialah sebesar : 0.3338 ± 0.089 mg/L, data selengkapnya pada table 4.5.
Tabel 4.5. Hasil pengukuran kadar logam Al dalam sampel air flokulasi secara SSA dengan Nitrous-Asetilen
No Sampel X1 X2 X3 Kadar mg/L
1 I 0.3518 0.3248 0.3248 0.3338 ± 0.0089 mg/L
2 II 0.3788 0.3515 0.3518 0.3608 ± 0.0089 mg/L
3 III 0.3383 0.3248 0.3248 0.3383 ± 0.0089 mg/L
Tabel 4.6. Hasil pengukuran absorbansi logam Al dalam sampel air reservoir secara SSA dengan Nitrous-Asetilen
No Sampel Y1 Y2 Y3
1 I 0.0014 0.0012 0.0014
2 II 0.0015 0.0012 0.0012
3 III 0.0014 0.0014 0.0012
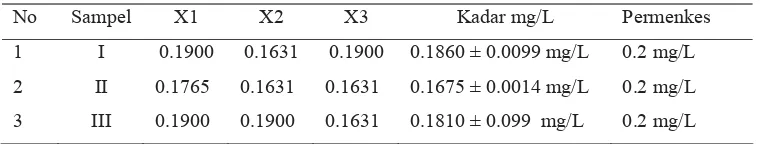
Tabel 4.7. Hasil pengukuran kadar logam Al dalam sampel air reservoir secara SSA dengan Nitrous-Asetilen
No Sampel X1 X2 X3 Kadar mg/L Permenkes
1 I 0.1900 0.1631 0.1900 0.1860 ± 0.0099 mg/L 0.2 mg/L
2 II 0.1765 0.1631 0.1631 0.1675 ± 0.0014 mg/L 0.2 mg/L
4.1.5. Pengukuran Kadar Calsium ( Ca)
Kondisi alat Spektrofotometer Serapan Atom (SSA) pada pengukuran konsentrasi
Calsium dapat dilihat pada table 4.8
Gambar. 4.2. Kurva kalibrasi larutan seri standar Calsium dengan nyala Asetilen-Udara.
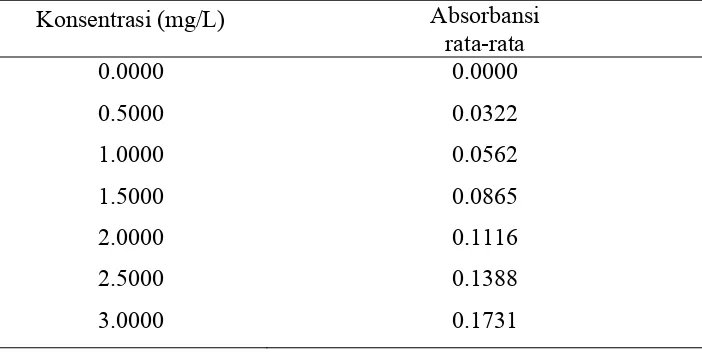
Tabel 4.10. Hasil pengukuran Absorbansi Logam Ca dalam sampel air flokulasi secara SSA nyala Asetilen-udara
No Sampel Y1 Y2 Y3
1 I 0.3046 0.3042 0.3042
2 II 0.3048 0.3046 0.3046
3 III 0.3038 0.3037 0.3035
4.1.6. Penentuan kadar Ca nyala Asetilen-Udara
Kadar Ca dapat ditentukan dengan menggunakan metode kurva kalibrasi dengan
mensubtitusikan nilai Y (absorbansi) yang diperoleh dari hasil pengukuran terhadap garis
regresi dan kurva kalibrasi Y = 0.0563X + 0.0011 sehingga diperoleh konsentrasi Ca.
Untuk sampel bak penjernihan (flokulasi) diperoleh nilai absorbansi :
Y1 = 0.3046
Y2 = 0.3042
Y3 = 0.3042
Dengan mensubtitusikan nilai Y (absorbansi) kepersamaan regresi :
X = y - 0.0011
0.0563
Untuk y = 0,3046
X1 = 0.3046 – 0.0011
0.0563
= 5.3931
X2 = 5.3860
X3 = 5.3860
X = 5.3884
Dengan demikian kadar Calsium bak penjernih (flokulasi) pada sampel I adalah :
X =∑ xi = 5. 3884 mg/L
n
(X1-X)2 = ( 5.3931 - 5. 3884)2 = 0.0000
(X2-X)2= (5.3860 - 5. 3884) 2 = 0.0000
(X3-X)2= (5.3860 - 5. 3884) 2 = 0.0000
∑(Xi – X)2 = 0.0000
Maka S = ∑(Xi – X)2 = 0,0000= 0.0041
n-1 2
Didapat harga Sx = S = 0.0041 √ n √ 3
= 0.0023
Dari data hasil pengukuran kadar Calsium dari bak penjernih (flokulasi) sampel I
sebesar : 5. 3884 ± 0.0023 mg/L, data selengkapnya pada table 4.11.
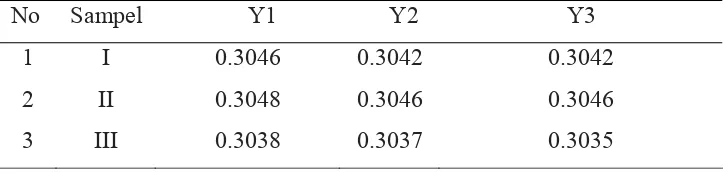
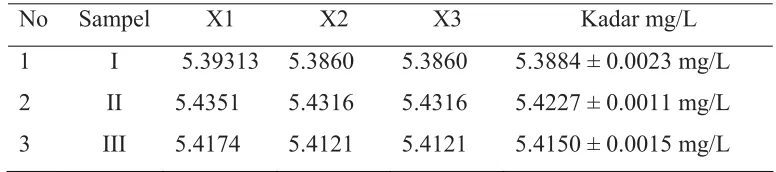
Tabel 4.11. Hasil pengukuran kadar logam Ca dalam sampel air flokulasi secara SSA dengan Asetilen-udara
No Sampel X1 X2 X3 Kadar mg/L
1 I 5.39313 5.3860 5.3860 5.3884 ± 0.0023 mg/L
2 II 5.4351 5.4316 5.4316 5.4227 ± 0.0011 mg/L
3 III 5.4174 5.4121 5.4121 5.4150 ± 0.0015 mg/L
reservoir secara SSA nyala Asetilen-udara
No Sampel Y1 Y2 Y3
1 I 0.2190 0.2188 0.2184
2 II 0.2188 0.2186 0.2186
3 III 0.2188 0.2184 0.2184
Untuk sampel air jernih (air reservoir) diperoleh nilai absorbansi :
Y1 = 0.2190
Y2 = 0.2188
Y3 = 0.2184
Dengan mensubtitusikan nilai Y (absorbansi) kepersamaan regresi :
Y = 0.0563X + 0.0011
X = y - 0.0011
0.0563
Untuk Y = 0.2190
X1 = 0.2190 - 0.0011
0.0563
= 3.8721
X2 = 0.2188 - 0.0011 = 3.8544 0.0563
X3 = 0.2184 - 0.0011 0.0563
= 3.8615
Dengan demikian kadar Calsium (Ca) air jernih (air reservoir) pada sampel I :
X =∑ xi = 3.8625 mg/L n
(X1-X)2 = (0.2190 - 5.3919)2 = 0.0000
(X2-X)2= (0.2188 - 5.3919) 2 = 0.0000
(X3-X)2= (0.2144 - 5.3919) 2 = 0.0000
Maka S = ∑(Xi – X)2 = 0.0000 = 0.0000
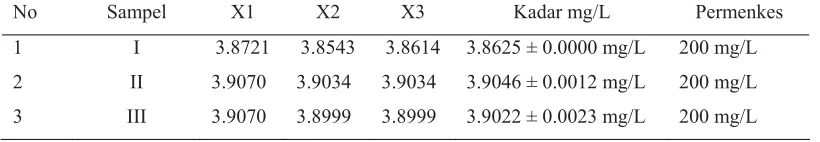
Tabel 4.13. Hasil pengukuran kadar logam Ca dalam sampel air reservoir secara SSA dengan Asetilen-udara
No Sampel X1 X2 X3 Kadar mg/L Permenkes
1 I 3.8721 3.8543 3.8614 3.8625 ± 0.0000 mg/L 200 mg/L
2 II 3.9070 3.9034 3.9034 3.9046 ± 0.0012 mg/L 200 mg/L
3 III 3.9070 3.8999 3.8999 3.9022 ± 0.0023 mg/L 200 mg/L
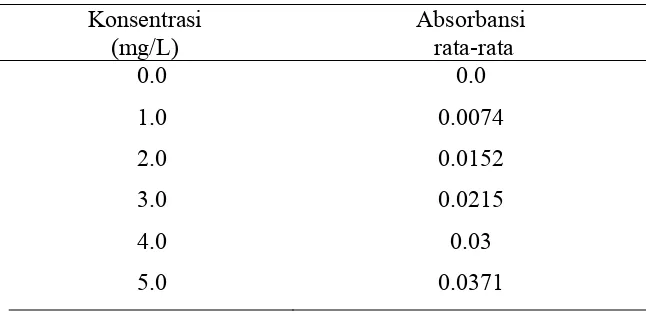
Tabel 4.14. Kondisi alat SSA Merek Shimadzu tipe AA-6300 pada penmgukuran konsentrasi Calsium (Ca)
Konsentrasi (mg/L)
Absorbansi rata-rata
0.0 0.0
0.5 0.0993
1.0 0.1986
1.5 0.3045
2.0 0.4325
2.5 0.5306
3.0 0.6363
Gambar 4.4. Kurva kalibrasi larutan standar Ca dengan nyala Nirous-
Asetilen
Tabel 4.16. Hasil pengukuran Absorbansi Logam Ca dalam sampel air flokulasi secara SSA nyala Nitrous Asetilen
No Sampel Y1 Y2 Y3
1 I 0.4108 0.4106 0.4104
2 II 0.4056 0.4054 0.4054
3 III 0.4054 0.4052 0.4052
Untuk sampel I bak penjernih (flokulasi) diperoleh nilai absorbansi :
Y1 = 0.4108
Y2 = 0.4106
Y3 = 0.4104
Dengan mensubtitusikan nilai Y (absorbansi) kepersamaan regresi :
Y = 0.2147x+ (- 0.0073)
X = y + (-0.0073)
0.2147
Untuk y = 0.4108
X1 = 0.4108 + 0.0073
0.2147
= 1.9477
X2 = 1.9467
X3 = 1.9458
X = 1.9467
Dengan demikian kadar Calsium (Ca) pada sampel I bak penjernih (flokulasi) :
X =∑ xi = 1.9467 mg/L n
(X1-X)2 = (1,9476 -1.9467)2 = 0.0000
(X2-X)2= (1.9467 -1.9467) 2 = 0.0000
(X3-X)2= (1.9458 -1.9467) 2 = 0.0000
∑(Xi – X)2 = 0.0000
Maka S = ∑(Xi – X)2 = 0.0000 = 0.0000
n-1 2
Dari data hasil pengukuran kadar Calsium dari bak penjernih (flokulasi) sampel I
sebesar: 1.9467 ± 0.0000 mg/L data selengkapnya pada tabel 4.17
No Sampel X1 X2 X3 Kadar mg/L Permenkes
1 I 1.9467 1.9467 1.9458 1.9467 ± 0.0000 mg/L 200 mg/L
2 II 1.9234 1.9225 1.9225 1.9228 ± 0.0002 mg/L 200 mg/L
3 III 1.9234 1.9215 1.9215 1.9222 ± 0.0006 mg/L 200 mg/L
Tabel 4.18. Hasil pengukuran Absorbansi Logam Ca dalam sampel air reservoir secara SSA nyala Nitrous Asetilen
No Sampel Y1 Y2 Y3
1 I 0.3252 0.3250 0.3250
2 II 0.3250 0.3248 0.3248
3 III 0.3252 0.3250 0.3250
Untuk sampel air jernih (air reservoir) diperoleh nilai absorbansi :
Y1 = 0.3252
Y2 = 0.3250
Y3 = 0.3250
Dengan mensubtitusikan nilai Y (absorbansi) kepersamaan regresi :
Y = 0.2147X + (‐ 0.0075)
X = Y + (- 0.0075) 0.2147
Untuk Y = 0.3250
X1 = 0.3250 + (0.0075)
0.2147 =1.5496
X2 = 1.5487
X3 = 1.5487
X = 1.5490
Dengan demikian kadar Calsium (Ca) air jernih (air reservoir) pada sampel I :
X =∑ xi = 1.5490 mg/L n
(X1-X)2 = (1.5496 - 1.549)2 = 0.0000
(X3-X)2= (1.5487- 1.5490)2 = 0.0000
∑ = 0.0000
Maka S = ∑(Xi – X)2 = 0.0000 = 0.0000
n-1 2
Didapat harga Sx = S = 0.0000 = 0.0000 √ n √ 3
Dari data hasil pengukuran kadar Calsium dari air jernih (air reservoir) sampel I
sebesar : 1.54902 ± 0.0000 mg/L, data selengkapnya pada table 4.19
Tabel 4.19. Hasil pengukuran kadar logam Ca dalam sampel air reservoir secara SSA dengan Nitrous –Asetilen
No Sampel X1 X2 X3 Kadar mg/L Permenkes
1 I 1.5489 1.5479 1.5479 1.5483 ± 0.0000 mg/L 200 mg/L
2 II 1.5479 1.5471 1.5471 1.5472 ± 0.0003 mg/L 200 mg/L
3 III 1.5489 1.5479 1.5479 1.5483 ± 0.0003 mg/L 200 mg/L
4.2. Pembahasan
Teknik Analisis spektrofotometri termasuk salah satu teknik analisis Instrumental
disamping teknik kromatografi dan elektrolisis kimia. Teknik tersebut memanfaatkan
fenomena interaksi materi dengan gelombang elektromagnetik seperti sinar-X,
ultraviolet, cahaya tanpak dan inframerah. Fenomena interaksi bersifat spesifik
baik absorbsi maupun emisi. Interaksi tersebut menghasilkan signal-signal yang
disadap sebagai analisa kualitatif dan kuantitatif. Contoh teknik absorbsi atom (SSA)
yang merupakan alat ampuh dalam analisis logam (K. Kacaribu, 2008).
SSA adalah metoda analisis yang berdasarkan pada pengukuran radiasi cahaya
yang diserap atom bebas. Analisis menggunakan alat SSA ini memiliki keuntungan
dari hasil analisisnya yang sangat peka, teliti dan cepat, pengerjaannya relatip
sederhana serta tidak perlu dilakukan pemisahan unsur logam dalam pelaksanaannya.
Analisis SSA yang didasarkan pada penyerapan energi radiasi dari sumber Nyala
menyusun SSA adalah sumber cahaya, atomizer, monokromator, detector,dan
penampilan data Anderson, 1987). Penggunaan SSA dalam menganalisa kandungan
logam-logam, dikarenakan dengan metode SSA unsur-unsur dengan energi eksitasi
rendah.
Metode SSA mendasarkan pada prinsip absorbsi cahaya oleh atom. Atom-atom
akan menyerap cahaya pada panjang gelombang tertentu, tergantung pada sifat
unsurnya. Sebagai contoh,Calsium menyerap pada 422,7 nm, Aluminium menyerap pada
309,3 nm. Cahaya pada panjang gelombang ini mempunyai cukup energi untuk
mengubah tingkat elektronik suatu atom yang mana transisi elektronik suatu atom
bersifat spesifik. Dengan menyerap suatu energi, maka atom akan memperoleh
energi sehingga suatu atom pada keadaan dasar dapat ditingkatkan energinya
ketingkat eksitasi (Rohman, A. 2007).
Dalam penentuan kwalitatif logam menggunakan metode Spektrofotometri Serapan
Atom, zat yang dianalisis dalam bentuk larutan diaspirasikan kedalam spektorfotometer
sehingga akan terjadi penguapan pelarut dan unsur yang ditentukan (analit) akan
terdissosiasi membentuk atom-atom bebas. Pembentukan atom-atom yang disebut
proses atomisasi ini dari oksida logam memerlukan temperatur yang berbeda yang
bergantung kepada kekuatan yang diperlukan untuk peruraiannya menjadi atom-atom
bebas. Aluminium termasuk logam yang mempunyai oksida yang sukar terurai dalam
pemanasan artinya diperlukan pemenasan yang lebih tinggi dibanding dengan Calsium
yang lebih mudah terurai menjadi atom-atom.
Dalam peneletian ini penentuan Al dengan Asetilen-Udara tidak diperoleh oleh
karena itu adalah keharusan untuk menggunakan Nitrous-Asetilen. Jadi dalam
laboratorium pengadaan gas pembakar harus dilakukan sesuai dengan unsur yang
dianalisis. Diharapkan pengadaan bahan bakar tersedia secara komersial.
Pemantauan dan penentuan kadar Al dalam air minum perlu dilakukan dengan teliti
karena kadar yang berlebih dari batas yang diperbolehkan oleh permenkes harus
dipenuhi. Untuk menjaga kesehatan konsumen karena dalam proses penghilangan logam
berat dalam proses ini menggunakan tawas yang mengandung Al juga, maka limbah
Dari hasil penggunaan gas pembakar Asetilen-udara dan Nitrous-Asetilen untuk
menganalisis logam Al yang mengguap pada suhu ± 2955 oC menunjukkan bahwa pada
temparatur itu hasil atomisasinya optimum. Sedangkan pada Asetilen-Udara pada suhu ±
2300oC logam Al tidak teratomisasi karena suhunya kurang tinggi untuk terjadinya
proses atomisasi.
Dari hasil penggunaan gas pembakar Asetilen-udara pada suhu ± 2300oC untuk
menganalisis logam Ca mengguap pada suhu ± 2300oC menunjukkan hasil yang proses
atomisasi lebih optimum dibandingkan Nitrous-Asetilen proses atomisasi pada suhu ±
2955 oC. Sementara itu proses untuk gas pembakar Nitrous-Asetilen kurang optimum,
dibawah suhu tersebut. karena suhu ± 2955 oC sebagian dari logam Ca telah menguap
dan bacaan SSA menjadi rendah.
Dari hasil penelitian yang telah dilakukan seperti terlihat pada tabel 4.5 dan 4.7
dan 4.11 dan 4.13 analisis untuk penentuan kadar logam Ca dan Al pada proses air
PDAM TIRTANADI dari Sunggal Medan dengan metode SSA yang menggunakan
(Asetilen-Udara dan Nitrous-Asetilen) dapat digunakan untuk logam Ca dapat
menggunakan kedua gas tersebut. Untuk logam Al hanya dapat ditentukan dengan
metode SSA yang menggunakan gas Nitrous-Asetilen karena suhunya tinggi 2955oC.
Penambahan larutan tawas (Al2SO4)3 dalam bak penjernih (flokulasi) sangat
mempengaruhi kadar logam Aluminium pada pengolahan air di PDAM Tirtanadi di
SunggalMedan. Karena proses flokulasi yang terjadi di clarifier dapat memplok
logam-logam yang bercampur dengan lumpur halus sehingga mengendap maka kadar
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
1. Untuk menganalisis logam Al digunakan gas pembakar Nitrous-Asetilen,
sedangkan untuk Ca dapat menggunakan Asetilen-Udara dan Nitrous-Asetilen.
Dan gas terbaik untuk analisis logam Ca adalah Asetilen-Udara.
2. Kadar Aluminium (Al) dalam air flokulasi adalah : 0.3338 ± 0.0089 mg/L, dalam
air reservoir dengan Nitrous-Asetilen adalah (Al) 0.1860 ± .0099 mg/L. Dan
kadar Calsium menggunakan Asetilen-Udara adalah: untuk air flokulasi
5.3884 ± 0.0023 mg/L dan 1.9467 ± 0.0009 mg/L, untuk air reservoir 3.9046 ±
0.0012 mg/L dan dengan Nitrous-Asetilen Ca 1.5479 ± 0.0003 mg/L hasil ini
memenuhi syarat air minum berdasarkan PERMENKES RI No.492/Menkes/Per/
IV/ 2010.
5.2. Saran
Disarankan untuk peneliti berikutnya untuk menganalisis logam-logam lain
seperti Sn dengan gas Asetilen-Udara dan Nitrous-Asetilen dari sumber dan dari
hasil pengolahan air yang digunakan sebelum perlakuan sehingga dengan demikian