W0 = Berat mula – mula evaporator (miligram) D = Density/massa jenis (gram/cm3)
A = Area/luas daerah yang terpapar korosi (inch atau cm2 pada rumus ke 2)
T = Time/waktu terpaparnya evaporator terhadap korosi (jam)
W1 = Berat setelah 8 hari kerja evaporator (milligram)
W = Weight Loss/kehilangan berat = W0 – W1 (milligram)
Karat akibat korosi yang tampak pada permukaan dalam evaporator.
Diagram Desain Penelitian / Design of Experiment (DoE)
Faktor yang dapat dikendalikan : - Tekanan pada evaporator (vakum) - Bahan dan desain pada evaporator - Suhu pada evaporator
- Kosentrasi garam pada air laut
- Banyaknya/jumlah air laut dalam lingkungan kerja - Aerasi (dalam lingkungan tertutup)
Faktor yang tidak dapat dikendalikan : - Suhu lingkungan (suhu luar evaporator) - Aliran air laut dari tangki menuju evaporator
- Sisa brine (endapan garam) yang tertinggal dalam evaporator
INPUT OUTPUT
Eeq_cat (Potensial kesetimbangan katoda) = Volt i0_cat (Pertukaran massa jenis arus pada katoda) = A/m2 A_cat (Slope Tafel pada katoda) = Volt
Eeq_an (Potensial kesetimbangan anoda) = Volt i0_an(Pertukaran massa jenis arus pada anoda) = A/m2 A_an(Slope Tafel pada anoda) = Volt
ilim_an(Nilai batas arus) = A/m2 M(Massa molar rata-rata) = g/mol
r(Massa jenis) = kg/m3
- Laju korosi yang terjadi pada permukaan material
- Bentuk deformasi pada permukaan material melalui penggambaran (plot) Tafel
- Arah distribusi arus potensial dari proses korosi
Diagram Desain Penelitian / Design of Experiment (DoE)
Faktor yang dapat dikendalikan: - Suhu pada evaporator (statis) - Konduktivitas elektrolit (air laut) - Logam anoda dan katoda yang bereaksi - Potensial kesetimbangan reaksi
- Waktu pemaparan logam dalam elektrolit - Salinitas elektrolit (air laut)
Faktor yang tidak dapat dikendalikan / diabaikan: - Pengaruh sisa garam yang tertinggal pada permukaan - Pengaruh permukaan pengelasan
INPUT OUTPUT
1
2
3 4
DAFTAR PUSTAKA
Ali MT, Fath HES, Armstrong PR. A comprehensive techno-economical review of indirect solar desalination. Renew Sustain Energy Rev 2011;15:4187-99.
Chattoraj, Indranil. Journal of Fundamentals of Corrosion & Its Prevention. National Metallurgical Laboratory, Jamshedpur 831007.2005.
Higgins, Lindley A. dan Mobley, R. Keith. Maintenance Engineering Handbook. Sixth Edition. Mc Graw-Hill. USA. 2002.
Jones, Denny A. Principles and Prevention of Corrosion. Second Edition. Macmiliian Publishing Company. New York. 1992.
Ketut Astawa, Made Sucipta, dan I Putri Gede Artha Negara..Analisa Performansi Destilasi Air Laut Tenaga Surya Menggunakan Penyerap Radiasi Surya Tipe Bergelombang Bebahan Dasar Beton. Jurnal Ilmiah Teknik Mesin Universitas Udayana. April 2011.
Kalogirou S. Seawater desalination using renewable energy sources. Prog Energy Combust Sci 2005;31:242-81.
M.K., Satria Nova dan Nisbah, Nurul M.Analisis Pengaruh Salinitas dan Suhu Air Laut Terhadap Laju Korosi Baja A36 pada Pengelasan SMAW. Jurnal Teknik ITS.September 2012.
Sharon, H. dan Reddy, K.S. Journal of Renewable and Sustainable Energy Reviews.Heat Transfer and Thermal Power Laboratory, Department Mechnical Engineering, Indian Institute of Technology, Madras, Chemnal, 600036, India. 2013
(http://en.wikipedia.org/wiki/Corrosion)
(http://en.wikipedia.org/wiki/Water_distribution_on_Earth)
(http://www.unwater.org/statistics_use.html)
BAB 3
METODOLOGI PENELITIAN
Untuk mengamati dan memprediksi fenomena terbentuknya korosi dapat dilakukan dengan membangun kaidah numerik yang akan mensimulasikan laju korosi evaporator dalam sistem desalinasi air laut dari hasil pengujian secara eksperimental yang telah dilakukan. Dalam penelitian ini kedua kaidah tersebut akan ditinjau sehingga validasi pertumbuhan dan laju korosi dapat dilakukan dengan mengolah hasil dari kedua kaidah. Untuk itu langkah awal yang perlu dilakukan adalah mengidentifikasi desain parameter dari objek korosi yang akan diteliti.
3.1 Desain Parameter Penelitian (Design Of Experiment)
Dalam mendesain parameter, hal utama yang dilakukan adalah mengidentifikasi parameter input (masukan) dan output (hasil) serta parameter desain yang mengendalikan korelasi antara parameter input maupun output.
Proses fenomena pertumbuhan korosi yang terjadi pada evaporator sistem desalinasi ditandai dengan berkurangnya berat akhir dibandingkan dengan berat awal / mula – mula evaporator, perubahan berat ini diakibatkan utamanya oleh air laut yang memiliki kandungan garam sehingga terjadilah reaksi kimia antara logam evaporator (logam yang dipakai pada percobaan adalah logam paduan stainless steel) dengan garam yang akan menghasilkan korosi dalam bentuk karat.
Akhirnya, hasil dari korosi berupa berkurangnya berat evaporator dan terbentuknya karat pada permukaan evaporator akibat korosi menjadi parameter
output. Untuk ringkasnya, desain parameter dirangkum dalam Diagram Desain
Penelitian yang telah dilampirkan pada halaman selanjutnya.
Reaksi kimia serta perubahan fisik (mekanik) yang terjadi pada evaporator dapat dilihat pada tabel 3.1, gambar 3.1 dan 3.2 dibawah ini:
Tabel 3.1 Tabel Desain Parameter Penelitian (Dokumen Penulis) Reaksi
Kimiawi Fe3++ 3 H2O Fe(OH)3+ 3 H+
Reaksi Fisik
Keadaan fisik sebelum
penelitan
Keadaan fisik setelah
penelitian
Berat awal evaporator adalah
Berat akhir evaporator menjadi yang diakibatkan oleh
korosi
Permukaan logam evaporator yang masih mengkilap (gambar
3.1)
Permukaan logam evaporator telah terbentuk karat dan tertinggal brine/endapan
garam (gambar 3.2)
Gambar 3.2 Permukaan Evaporator Setelah 8 Hari Penelitian (Dokumen Penulis)
3.1.1 Komponen dan Fungsi
Tabel komponen dan fungsi memaparkan detail bagian penelitian mana yang difokuskan untuk dilakukan peninjauan, hal ini mencakup komponen apa sajakah yang diteliti, fungsi dari komponen dalam sistem, perubahan fenomena fisik yang dialami komponen, parameter yang ditinjau dalam komponen serta menetapkan rumus empirik yang digunakan dalam membahas perubahan parameter yang dialami komponen.
Tabel 3.2 Tabel Komponen dan Fungsi (Dokumen Penulis)
3.1.2 Data Pengukuran Eksperimental
Tabel ini berisi hal/parameter yang akan diteliti dalam penelitian dan hasil yang akan didapat dalam eksperimen. Tabel 3.3 merupakan rangkuman mengenai parameter apa sajakah yang digunakan atau diteliti dari eksperimen.
Tabel 3.3 Tabel Data Pengukuran Eksperimental (Dokumen Penulis) Komponen yang diteliti Fungsi komponen Fenomena perubahan fisik Rumus empirik yang digunakan Parameter yang diukur Evaporator Sebagai tempat perubahaan fasa
air laut menjadi uap Perubahan berat akibat terjadinya korosi Atau Berat awal dan akhir evaporator
Parameter Input Parameter Output
Parameter
Desain
Berat mula
– mula evaporator
(W0)
Luas daerah spesimen (A) Waktu terpaparnya spesimen terhadap korosi (T) Berat akhir evaporator
(W1)
Kehilangan
Berat (W)
[W1– W0]
Laju korosi
(MPY)
... mg (miligram)
... inchi ... cm2
3.2 Perhitungan Laju Korosi dengan Simulasi
Perhitungan laju korosi dengan simulasi aplikasi dilakukan dengan tujuan membandingkan data perhitungan hasil secara teoritis dengan hasil komputasi sehingga didapatkan ralat (beda) perhitungan penelitian dengan hasil simulasi. Perhitungan simulasi menggunakan aplikasi COMSOL MULTIPHYSICS 5.0 untuk menunjukkan deformasi pada permukaan evaporator
akibat terjadinya korosi galvanis yang membentuk pit (lubang) dengan berbasis metode polarisai. Deformasi timbul akibat adanya reaksi kimia besi dengan stainless steel dengan media elektrolit berupa air laut dengan waktu pemaparan selama 64 jam.
3.2.1 Identifikasi Parameter
Secara komputasi pembangunan model dan pengujian dilakukan untuk identifikasi deformasi yang terjadi pada evaporator. Pada saat evaporator terpapar dengan media elektrolit berupa air laut hal maka simulasi akan menghasilakan deformasi yang disebabkan oleh korosi dengan menggunakan software COMSOL 5.0.
Data – data yang diperlukan untuk komputasional didapat dari hasil penelitian dan standar parameter yang dikeluarkan oleh NACE dan aplikasi COMSOL dalam bentuk jurnal ilmiah, data – data yang diambil untuk komputasi yaitu sebagai berikut :
1. Data potensial korosi besi
2. Data konduktivitas elektrolit (air laut)
3. Data massa jenis arus reaksi elektroda pada anoda dan katoda
3.2.2 Variabel Yang Diamati
Sesuai dengan performansi evaporator secara eksperimen, variabel tertentu menjadi fokus perhatian yang perlu dikondisikan untuk pengolahan data guna mendapatkan hasil yang mendekati sempurna. Adapun variabel yang diamati dalam studi eksperimental maupun simulasi numerik ini adalah sebagai berikut :
Secara eksperimental :
Laju korosi yang terbentuk pada permukaan evaporator yang terpapar dengan media elektrolit berupa air laut selama 80 jam
Secara simulasi numerik :
1. Deformasi permukaan evaporator yang diakibatkan oleh korosi galvanis disebabkan adanya reaksi kimia antara
2. Laju korosi permukaan evaporator berupa deformasi akibat korosi galvanis
3. Massa jenis arus reaksi dan distribusi potensial pada elektrolit 3.2.3 Parameter Fluida
Parameter fluida yang digunakan pada saat melakukan komputasi adalah air laut dengan sifat – sifat fisik seperti tabel 3.4 di bawah
Tabel 3.4 Tabel Data Sifat Fisik Air Laut (Dokumen Penulis)
Nomor Parameter Keterangan
1 Jenis Fluida Air Laut
2 Tekanan Fluida 6 cmHg
3.2.4 Design of Eksperiment Simulasi (DoE Simulasi)
Untuk mengidentifikasi gejala korosi pada evaporator perlu dibangun model eksperimental dari permukaan evaporator itu sendiri, Komponen yang disimulasi adalah permukaan evaporator dalam keadaan terpapar media elektrolit (air laut). Gambar 3.3 merupakan gambar yang digunakan untuk mensimulasi pengaruh dan laju deformasi dan DoE simulasi akan disertakan pada halaman berikutnya.
Gambar 3.3 Penjelasan Daerah – Daerah Simulasi (Dokumen Penulis) Berdasarkan DoE simulasi diatas maka dapat dijelaskan bahwa pada saat sistem desalinasi bekerja maka terdapat beberapa parameter yang mempengaruhi laju korosi pada evaporator seperti: laju potensial anoda dan katoda, salinitas dan konduktivitas media elektrolit serta temperatur dan tekanan dalam evaporator sendiri.
Pada saat evaporator bekerja permukaan stainless steel evaporator yang kehilangan lapisan pelindung (pasivitas) akan terjadi reaksi antara unsur besi(Fe) dengan elektron dan air yang terkandung dalam media elektrolit sehingga menyebabkan korosi, hal ini diperparah dengan adanya korosi galvanis antara permukaan evaporator yang belum berkorosi dengan yang telah berkorosi ditambah dengan kondisi lingkungan sistem yang memiliki temperatur dan tekanan cukup tinggi sehingga mempercepat timbulnya korosi dan laju korosi.
Permukaan Stainless Steel Permukaan Besi
Parameter kondisi akan menentukan laju korosi yang timbul dan deformasi yang tejadi pada permukaan yang mengalami korosi dan membandingkan dengan permukaan yang tidak terkena korosi.
3.2.5 Kerangka Konsep Pemodelan Numerik
Adapun kerangka konsep pemodelan numerik ini yang dapat dilihat pada bagian berikut :
\
3.2.6 Setup Komputasi
Proses pre-processing merupakan proses yang dilakukan sebelum pengujian (simulasi). Proses ini mencakup pembuatan model, penentuan parameter, penentuan anoda katoda sampai dengan pembuatan mesh (meshing). 1. Pembuatan Model
Pembuatan model permukaan evaporator dalam simulasi ini dilakukan dalam 2 dimensi. Komponen evaporator tidak perlu dibangun dalam bentuk 3 dimensi dikarenakan simulasi dilakukan dalam hitungan per jam sehingga hasil korosi yang terbentuk sangatlah kecil, oleh karena itu simulasi dengan model 2
Permasalahan
1. Fenomena korosi pada evaporator sistem desalinasi air laut
Pengamatan
1. Membangun simulasi korosi pada evaporator
2. Membangun simulasi deformasi permukaan evaporator
Parameter Kontrol 1. Bahan evaporator 2. Media elektrolit 3. Keadaan lingkungan kerja sistem
Alat simulasi 1. Personal computer 2. Aplikasi COMSOL
Hasil
1. Simulasi laju korosi pada evaporator 2. Simulasi bentuk deformasi yang terjadi
dimensi akan memberikan hasil yang lebih baik dan jelas daripada hasil 3 dimensi. Model dibuat dengan aplikasi COMSOL dan disertakan sebagi berikut. (ukuran dalam bentuk milimeter untuk memperjelas hasil simulasi). Model gambar 2 dimensi disertakan dalam gambar 3.4 berikut.
Gambar 3.4 Model Simulasi 2 Dimensi (Dokumen Penulis) 2. Menentukan anoda,katoda dan media elektrolit (domain)
Computational domain merupakan bidang batas simulasi.Domain
komputasi terbagi atas 3 elemen, yaitu anoda yang merupakan bagian terkorosi (besi), katoda yang merupakan bagian yang tidak mengalami korosi (stainless steel) dan media elektrolit. Gambar domain dijelaskan pada gambar 3.5, 3.6 dan 3.7 sebagai berikut:
Gambar 3.6 Domain Katoda (Stainless Steel) (Dokumen Penulis)
Gambar 3.7 Domain Anoda (Besi) (Dokumen Penulis) 3. Pembuatan Mesh
diatur secara otomatis dengan element size normal (0.001 mm). Bentuk mesh dapat dilihat pada gambar 3.8 berikut:
Gambar 3.8 Meshing Model Simulasi (Dokumen Penulis) 4. Menginput Parameter Simulasi
Pada bagian ini diinput data parameter dari reaksi kimia (korosi) yang terjadi Parameter yang udara yang diinput adalah Potensial kesetimbangan katoda, pertukaran massa jenis arus pada katoda, slope Tafel pada katoda, potensial kesetimbangan anoda, pertukaran massa jenis arus pada anoda, slope Tafel pada anoda, nilai batas arus, massa molar rata-rata dan massa jenis. Data parameter diperoleh dari jurnal NACE, COMSOL, eksperiment terdahulu dan perhitungan manual. Gambar 3.9 adalah input parameter yang dirunjukkan sebagai berikut:
5. Menginput Konduktivitas Elektrolit dalam Media Elektrolit
Pada bagian ini diinput nilai konduktivitas elektrolit pada media elektrolit untuk menentukan seberapa baiknya media elektrolit mampu menghantarkan arus listrik/elektrolit, pengaturan lainnya digunakan pengaturan default.Gambar 3.10 menunjukkan input nilai konduktivitas elektrolit air laut.
Gambar 3.10 Input Nilai Konduktivitas Elektrolit dalam Media Elektrolit (Dokumen Penulis)
6. Menginput Temperatur Kerja Sistem
Pada bagian ini diinput nilai temperatur pada permukaan anoda dan katoda ketika terjadi korosi.Temperatur mempengaruhi laju korosi, semakin tinggi korosi maka umumnya laju korosi semakin besar, terutama pada stainless steel (304) yang akan kehilangan lapisan pasivitas diatas temperatur kerja 50oC (343 Kelvin). Gambar input temperatur ditunjukkan oleh gambar 3.11 sebagai berikut:
Gambar 3.11 Input Nilai Temperatur Kerja Sistem (Dokumen Penulis) 7. Mendefinisikan Parameter Waktu Kerja Sistem
Gambar 3.12 Paraneter Waktu Simulasi (Dokumen Penulis) 3.2.7 Diagram Alir Simulasi
Secara garis besar, proses simulasi akan dilaksanakan seperti yang ditunjukkan pada Gambar 3.13 sebagai berikut:
Gambar 3.13 Diagram Alir Simulasi Ya
Tidak
Pembuatan geometri di COMSOL
Proses meshing
Pendefinisian Parameter
Pendefinisian Kondisi Kerja dan Media Elektrolit
Menginput waktu simulasi sebagai definisi studi deformasi dan laju korosi yang berhubungan dengan waktu
MULAI
Mendapatkan hasil Simulasi
3.3 Kelengkapan Penelitian
3.3.1 Waktu dan Tempat
Pengujian dilakukan di Medan, Sumatera Utara pada Jalan Tridharma, Universitas Sumatera Utara, Gedung J20 (Gedung Magister Teknik Mesin Fakultas Teknik Universitas Sumatera Utara) selama lebih kurang 6 bulan.
3.3.2 Alat dan Bahan
3.3.2.1 Alat
Alat yang dipakai dalam penelitian ini terdiri dari: 1. Tangki Air Laut, Konsentrat Garam, dan Air Bersih
Tangki yang berfungsi sebagai penampung air laut, konsentrat garam dan air bersih yang dipasang di bawah 10 meter dari evaporator dan kondensor agar pengvakuman dapat berlangsung. Tangki yang akan digunakan mempunyai volume masing-masing 20 liter. Gambar 3.14 menunjukkan tangki air laut yang dipakai pada penelitian ini.
Gambar 3.14 Tangki Air Laut (Sumber: Dokumen Penulis)
2. Evaporator
pemanasan dengan bantuan pemanas elektrik (heater) dan termokopel sebagai pengatur temperatur, hal mendasar yang membedakan evaporator yang digunakan pada sistem ini adalah aplikasi keadaan/kondisi vakum dan keseimbangan tekanan volume dalam sistem desalinasi. Evaporator terletak pada ketinggian 10,34 meter diatas permukaan tanah. Posisi evaporator diletakkan demikian agar kondisi vakum natural dapat terbentuk sehingga air laut dapat naik sendiri tanpa bantuan pompa ke evaporator melalui aplikasi keseimbangan volume dalam sistem, dimana tinggi 10,34 meter merupakan tinggi minimum (untuk media air PAM) agar kesetimbangan terjadi untuk media air laut ketinggian kesetimbangan evaporator yang diperlukan agak rendah yaitu 10,06 meter sehingga air laut tetap dapat terhisap naik dengan posisi evaporator yang demikian, evaporator mampu menghisap dan menghasilkan air bersih sebesar 1,2 liter dalam 1 hari kerja (8 jam) menggunakan mekanisme kerja diatas. Gambar 3.15 menunjukkan gambar evaporator yag digunakan dalam penelitian. Spesifikasi evaporator yang akan digunakan adalah sebagai berikut :
Material : Paduan stainless-steel Tipe ANSI-304; dengan mur dan skrup pengunci tutup evaporator terbuat dari Stainless-Steel Tipe ANSI-304. Agar tidak adanya udara yang keluar antara celah tutup evaporator dengan dengan badan eveporator maka dibuat sebuah lapisan kedap udara dengan material karet
packing.
Ketebalan bahan : 5,8 mm Diameter evaporator : 50 cm Tinggi tangki evaporator : 15 cm Tinggi kerucut penutup : 12 cm
3. Kondensor
Kondensor pada sistem ini berbentuk tabung yang dimiringkan dan di sepanjang tabung terdapat sirip (fin) yang berfungsi mempercepat proses kondensasi di kondensor. Semakin cepat proses kondensasi, semakin cepat pula air bersih yang dihasilkan. Gambar 3.16 merupakan gambar kondensor secara keseluruhan yang dipakai dalam penelitian. Spesifikasi kondensor yang digunakan adalah sebagai berikut :
Material : Tembaga
Panjang Tabung : 0.5 m Ketebalan Tabung : : 0.25 cm Diameter Tabung : 4 inci
Untuk sirip (fin) yang dipasang di permukaan luar tabung memilki spesifikasi sebagai berikut:
Jumlah fin : 10 buah Diameter fin : 25.4 cm Ketebalan fin : 0.0635 cm Jarak antar fin : 4 cm
Gambar 3.16 Kondensor (Sumber: Dokumen Penulis)
4. Tube in Tube Heat Exchanger
sehingga konsentrat garam yang tidak mendidih akan dialirkan ke tangki konsentrat garam. Oleh karena temperatur konsentrat garam masih relatif tinggi saat dipanaskan di evaporator, maka sebelum dialirkan ke tangki konsentrat garam, terlebih dahulu konsentrat garam akan dialirkan ke tube in tube heat exchanger untuk mengalirkan sebagian kalor terhadap air laut yang mengalir di pipa dalam.Sehingga pemanasan di evaporator dapat berlangsung dengan cepat. Gambar 3.17 menunjukkan bangun dari tube heat exchanger yang dipakai pada penelitian.Spesifikasi tube in tube heat exchanger adalah sebagai berikut :
Material pipa luar : PVC Material pipa dalam : Tembaga Diameter pipa luar : 2.54 cm Diameter pipa dalam : 1.27 cm
Gambar 3.17 Tube in Tube Heat Exchanger (Sumber: Dokumen Penulis)
5. Manometer
Gambar 3.18 Manometer (Sumber: Dokumen Penulis)
6 Timbangan digital
Timbangan digital digunakan untuk mengukur berat evaporator sebelum maupun setelah pemaparan terhadap air laut. Timbangan digital dengan kemampuan menimbang berat sampai dua angka dibelakang koma ditunjukkan oleh gambar 3.19.
3.2.2.2 Bahan
Bahan yang digunakan dalam penelitian ini adalah air laut yang memiliki temperatur awal 25oC dan konsentrasi garam 3.5%.
Gambar 3.19 merupakan sketsa dari sistem yang merupakan gabungan dari alat – alat penelitian yang ditunjukkan sebagai berikut:
Gambar 3.20 Sistem Desalinasi Air Laut (Sumber: Dokumen Penulis) 3.3.3 Prosedur Penelitian
Prosedur penelitian dilakukan dengan langkah-langkah sebagai berikut : 1. Pemasangan alat dan isolasi hingga menjadi sistem desalinasi vakum 2. Mengukur berat mula-mula evaporator
3. Pengecekan kevakuman sistem
4. Kalibrasi alat ukur yang digunakan saat pengujian 5. Mengisi air laut pada tangki air laut
6. Membiarkan sistem desalinasi berkerja selama 10 hari 7. Mencatat berat evaporator untuk data perhitungan laju korosi
8. Menghitung laju korosi dalam evaporator dengan bahan stainless – steel berdasarkan data eksperimental
11.Menentukan langkah perawatan/pencegahan berdasarkan data yang didapat
Untuk lebih ringkasnya prosedur penelitan yang dilakukan dapat dilihat melalui diagram alir pada gambar 3.20. yang dilampirkan pada halaman selanjutnya.
3.3.4 Jadwal Pelaksaan Penelitian / Schedule
Berikut akan disertakan estimasi jadwal penelitian mulai dari perancangan desain sistem alat desalinasi sampai selesainya sidang tugas akhir. Jadwal penelitian dilampirkan pada bagian lampiran penulisan.
3.3.5 Estimasi Biaya Penelitian
Estimasi biaya penelitian diperlukan untuk rencana kedepan dari penelitian, apakah sebagai harga dasar produk apabila sistem desalinasi penelitian ingin diproduksi ataupun sebagai catatan biaya dasar apabila ingin dilakukan pengembangan/penelitian sistem lebih lanjut.
Gambar 3.21. Bagan Alir Penelitian Secara Keseluruhan Mulai
Pengukuran berat mula – mula evaporator
Pemasangan Alat dan Isolasi
Apakah unit desalinasi telah mencapai kondisi vakum?
Pengisian Air Laut pada Tangki Air Laut
Membiarkan sistem desalinasi berkerja selama 10 hari
Mengukur berat evaporator setelah 10 hari
Menghitung laju korosi yang terjadi dalam evaporator dengan metode weight loss
Selesai
Melakukan perhitungan laju korosi dengan simulasi dengan metode polarisasi
Melakukan validasi data dengan membandingkan kedua metode perhitungan
Menentukan tindakan perawatan/pencegahan yang dilakukan Apakah data telah valid
(dapat diterima)? TIDAK
TIDAK
YA
BAB 4
HASIL DAN PEMBAHASAN
4.1 Input dan Output Eksperimntal
Dalam membangun Design Of Experimental (DOE), terdapat parameter input dan parameter output. Adapun parameter-parameter yang ditunjukkan oleh tabel 4.1 sebagai berikut :
Tabel 4.1 Tabel Input dan Output Secara Eksperimental (Dokumen Penulis)
4.2 Hasil Laju Korosi Evaporator Dalam Eksperimental
Berikut akan dipaparkan hasil perhitungan laju korosi penelitian dengan metode weight-loss. Data – data yang didapat akan dikumpulkan,dianalisa dan dirangkum hasilnya melalui tabel data pengukuran yang terdapat pada tabel 4.2. Setelah perangkuman data selesai maka metode perhitungan akan dijelaskan satu – persatu, dari pembuktian pengambilan data input sampai dengan penjelasan perhitungan hasil parameter desain berupa laju korosi pada evaporator didapat, adapun kondisi batas pada evaporator yaitu:
- Tekanan vakum pada kondisi bekerjanya evaporator - Bahan evaporator adalah logam stainless – steel 304 Komponen
Parameter
Input Output
Evaporator
Berat Mula – Mula (W0) = miligram
Luas Daerah Spesimen (A) = inchi/cm2
Waktu Terpaparnya Spesimen terhadap Korosi (T) = jam
Berat Akhir Evaporator (W1) = miligram
- Media elektrolit berupa air laut dengan kadar garam 3.5% per liter - Temperatur kerja dianggap statis pada temperatur 50oC\
Tabel 4.2 Tabel Hasil Perhitungan Laju Korosi Secara Eksperimental (Dokumen Penulis)
Data berat mula – mula dan berat akhir evaporator diambil dari hasil penimbangan menggunakan timbangan digital dengan kemampuan menimbang berat sampai dua angka dibelakang koma. Validasi data berat ditunjukkan oleh foto yang terdapat pada gambar 4.1 yang diambil pada waktu penimbangan sebelum dan sesudah penelitian dilakukan. Data kehilangan berat (W) merupakan hasil pengurangan berat awal evaporator dengan berat akhir evaporator.
Parameter Input Parameter Output Parameter Desain
Berat mula –
mula
evaporator
(W0)
Luas daerah spesimen (A) Waktu terpaparny a spesimen terhadap korosi (T) Berat akhir evaporator
(W1)
Kehilangan
Berat (W)
[W1– W0]
Gambar 4.1 Berat Evaporator Sebelum (Kiri) dan Sesudah (Kanan) (Dokumen Penulis)
Luas daerah spesimen merupakan luas daerah (permukaan) evaporator yang bersinggungan/melakukan kontak dengan media elektrolit (air laut) sehingga luas daerah spesimen perhitungan dapat ditulis sebagai rumus berikut :
Gambar 4.2 Evaporator dalam kondisi tertutup (Dokumen Penerbit)
Gambar 4.3 Evaporator dalam kondisi terbuka (Dokumen Penerbit)
Dengan catatan bahwa tinggi air dalam evaporator adalah 9 centimeter yang menjadi tinggi tabung evaporator dalam perhitungan luas permukaan yang mengalami korosi. Penjabaran perhitungan luas dijelaskan sebagai berikut :
1. Luas Alas dan Dinding Evaporator
Diketahui diameter eveporator adalah 48 centimeter dengan tinggi evaporator yang terpapar dalam media elektrolit adalah 9 centimeter. Dikarenakan evaporator berbentuk silinder /tabung tanpa tutup maka digunakan rumus luas selimut tabung + rumus luas lingkaran alas pada tabung.
Luas Evaporator = π r2+ 2 π r t
Sehingga : L = 3.14 x (24)2 + 2 x 3.14 x 24 x 9 = 1808.64 + 1356.48
2. Luas Heater
Diketahui diameter heater adalah 0.5 centimeter dengan panjang heater 240 centimeter. Sama seperti evaporator, heater juga berupa
silinder/tabung tetapi tanpa tutup dan alas sehingga rumus yang dipakai hanya rumus selimut tabung.
Luas Heater = 2 π r t
Sehingga : L = 2 x 3.14 x 0.25 x 240 = 376,80 cm2
3. Luas Lubang Pipa Inlet
Lubang pipa inlet setengah inci berbentuk lingkaran dan terdapat pada alas evaporator, perhitungan luas lubang ini menggunakan rumus lingkaran.
Luas lubang pipa = π r2
Sehingga : L = 3.14 x (1.27)2 = 5.06 cm2
4. Luas Permukaan Spesimen
Maka luas permukaan/daerah spesimen yang terpapar dalam media elektrolit adalah sebagai berikut:
Luas keseluruhan = 3156.12 + 376,80 – 5.06 cm2 = 3536.86 cm2 (548.21 inchi)
Kehilangan berat evaporator didapat dari perbedaan hasil mula – mula evaporator dan hasil akhir evaporator setelah terpapar media elektrolit dan mengalami korosi, kehilangan berat (weight loss) dihitung dalam miligram dan dirumuskan sebagai berikut:
W = W1 – W0
Sehingga : W = 33.410.000 - 33.200.000 miligram = 210.000 miligram
Setelah mendapatkan hasil diatas maka kita dapat mencari laju korosi yang dialami oleh evaporator dalam lingkungan kerja yang telah ditetapkan dengan metode weight-loss. Metode ini akan menghasilkan laju korosi dalam satuan mils/tahun atau mm/tahun sehingga kita dapat mengetahui apakah bahan yang digunakan dalam katergori baik atau buruk apabila dipaparkan dalam lingkungan kerja tertentu. Perhitungan laju korosi dengan metode weight-loss ditunjukkan sebagai berikut:
atau
Dimana :
W adalah Weight Loss/kehilangan berat (miligram) D adalah Density/massa jenis (gram/cm3)
A adalah Luas daerah yang terpapar korosi (inch atau cm2 pada rumus ke 2)
T adalah Time/waktu terpaparnya evaporator terhadap korosi (jam) MPY adalah laju korosi per tahun (mils/tahun atau mm/tahun)
Dalam mm/tahun :
Sehingga hasil laju korosi eksperimental yang didapatkan dengan metode perhitungan weight-loss adalah 10.12 mm/tahun (398.03 mils/tahun), apabila merujuk kepada tabel nilai resistensi korosi (tabel 2.2, bab 2) maka dapat dilihat bahwa penggunaan material stainless steel dalam kondisi kerja yang telah ditentukan berada pada batas unacceptable (tidak dapat diterima ) sehingga material stainless steel-304 tidak cocok dipakai dalam evaporator sistem desalinasi air laut. Laju korosi yang terlampau tinggi akan menyebabkan failure dalam waktu yang dekat, dikarenakan deformasi permukaan alas maupun dinding evaporator yang terbentuk mengarah pada terbentuknya crack akibat korosi. 4.3 Hasil Laju Korosi Evaporator Dalam Simulasi
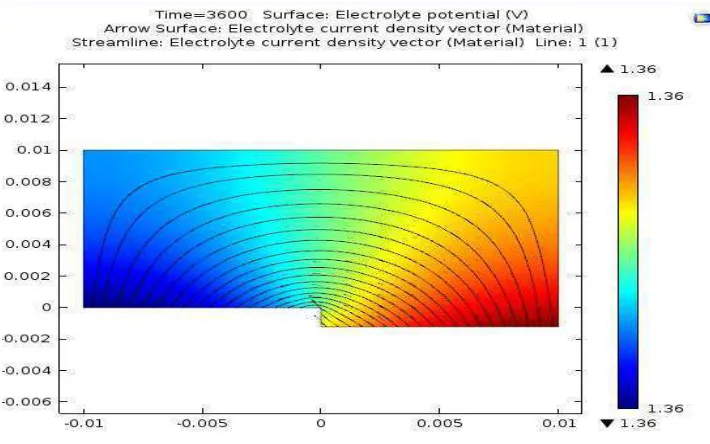
Pada tahap ini terlihat hasil yang ingin didapatkan dari proses simulasi. Untuk penelitian ini hasil yang ingin didapat dari simulasi adalah deformasi dan nilai laju korosi. Dapat dilihat pada gambar 4.4, 4.5 dan 4.6 bahwa deformasi yang dialami oleh anoda (besi) dibandingkan dengan katoda (stainless steel). Terlihat pada hasil simulasi bahwa laju korosi yang timbul per jam adalah 0.0011 mm/jam (ditunjukkan oleh gambar 4.5) sehingga deformasi akibat
korosi yang timbul pada 8 jam pengujian (1 hari pengujian) adalah 0,0088
mm yang ditunjukkan oleh gambar 4.6. Penunjukkan arah potensial dan
4.5 merupakan pembesaran dari gambar 4.4 agar pembaca dapat melihat hasil korosi yang terjadi dengan lebih jelas. Perlu diingat karena pemodelan awal pada permukaan anoda (yang berkorosi) telah didesain dengan permukaan yang memiliki kedalaman 1x10^-4 lebih dalam daripada permukaan anoda maka hasil laju korosi yang didapat akan dikurangi kedalaman awalnya.
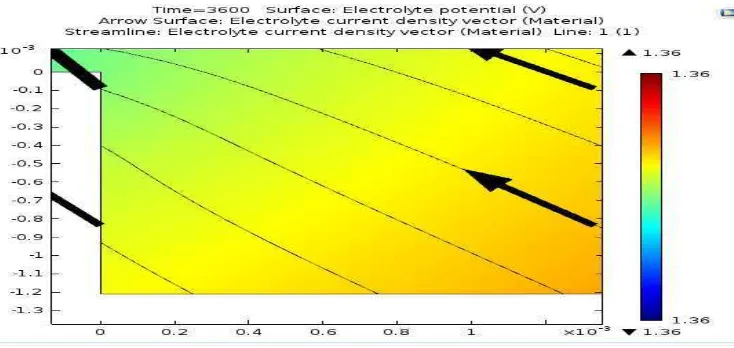
[image:33.595.132.487.508.730.2]Kontur/ warna merah menunjukkan batas daerah anoda (daerah yang berkorosi) dengan nilai batas elektrolit potensial yang lebih tinggi sedangkan daerah dengan warna biru menunjukkan daerah katoda (daerah yang tidak berkorosi) dengan nilai batas elektrolit potensial yang lebih rendah, semakin “biru” warna daerah pada hasil simulasi maka daerah tersebut tidak mengalami korosi dan menerima elektron dari hasil perbedaan potensial elektrolit, demikian sebaliknya semakin “merah” suatu daerah semakin daerah itu mengalami korosi dan cenderung melepaskan elektron. Panah hitam yang tampak pada gambar menunjukkan arah perpindahan elektron dari bagian anoda ke bagian katoda. Perpindahan elektron dari permukaan anoda ke katoda diakibatkan adanya reaksi korosi galvanisasi, dimana material – material berdekatan cenderung akan melakukan pertukaran elektron akibat reaksi galvanis natural kedua material, dimana material yang memiliki seri galvanis lebih rendah (dalam hal ini permukaan besi) akan melakukan pelepasan elektron lebih lanjut menuju material dengan seri galvanis yang lebih tinggi (permukaan stainless steel).
Gambar 4.5 Laju Korosi Selama 1 Jam (Dokumen Penulis)
Gambar 4.6 Deformasi dan Laju Korosi Selama 1 Hari Pengujian (8 Jam) (Dokumen Penulis)
lingkungan luar. Tidak hanya mereka ikut menyumbangkan terjadinya korosi karena bersifat konduktif secara alamiah namun mereka juga memiliki sifat menghancurkan sifat pasifitas dari logam dengan cara berikatan dengan lapisan oksida pada permukaan logam. Serangan yang ditimbulkan oleh anion ini bersifat lokalisasi sehingga lebih berbahaya dari deformasi yang disebabkan uniform
corrosion karena lubang yang terbentuk mampu melubangi permukaan logam
secara terpusat
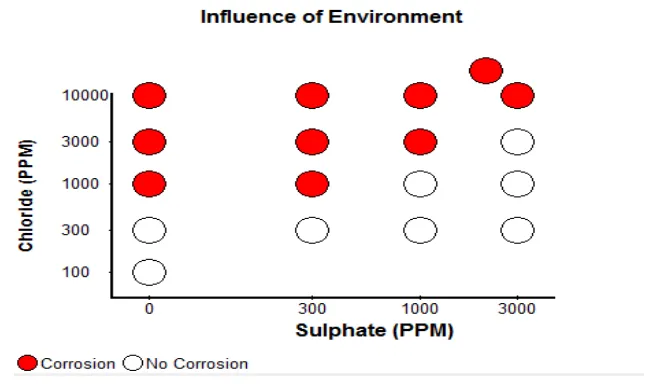
Apabila dibandingkan dengan agresifitas ion klorida, maka ion sulfat (SO42-) pada umumnya lebih tidak agresif dalam menyebabkan gejala korosi. Akan tetapi, mereka dapat dikonversikan menjadi ion sulfida yang sangat korosif oleh Sulphate Reducing Bacteria (SRB). Jumlah kandungan klorida dan sulfat untuk menyebabkan korosi pada suatu sistem berbeda-beda tergantung dengan keadaan lingkungan, material yang berkorosi, temperatur dan faktor lainnya. . (Adler Flitton, M. K. and E. Escalante. 2003. “Simulated Service Testing in Soil,”
American Society of Metals Handbook, Volume 13A: Corrosion:
Fundamentals, Testing and Protection, sub-section S-3c, American Society for
[image:35.595.147.474.454.646.2]Metals International, Metals Park, Ohio)
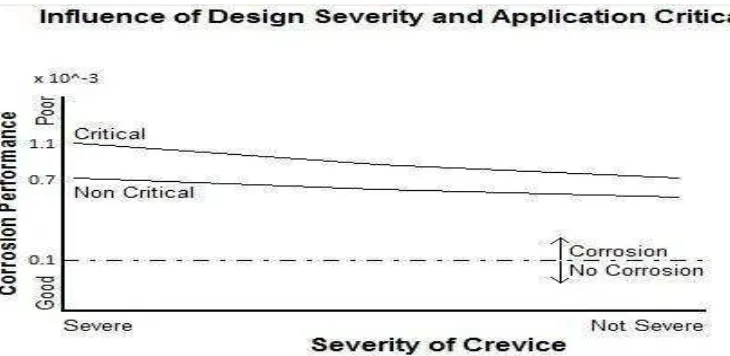
Gambar 4.8 Grafik Pengaruh Laju Korosi Terhadap Tingkat Kerusakan Retakan (Dokumen Penulis)
4.4 Validasi Data
Sebagai validasi data, peneliti membandingkan hasil perhitungan laju korosi secara eksperimental dengan metode weight-loss (kehilangan berat) dengan hasil perhitungan secara simulasi yang menggunakan metode polarisasi, dimana untuk kemudiannya pembuktian validasi dihitung dalam perbedaan hasil yang ditunjukkan dalam bentuk persen ralat.
Sebelum menghitung ralat antara kedua metode yang digunakan hasil yang didapat harus disamakan dalam satu haisl yang sama satuan yang sama) sebelum dicari persen ralat/perbedaan hasil perhitungan. Hasil ini akan dirangkum pada tabel 4.3 sebagai berikut untuk mempermudah penunjukkan perbedaan antara perhitungan simulasi dengan eksperimental.
Tabel 4.3 Tabel Hasil Laju Korosi dari Eksperiment dan Simulasi (Dokumen Penulis)
Satuan hasil perhitungan
Hasil Laju Korosi Dari Penelitian
(Eksperimental) Dari Simulasi (Numerikal)
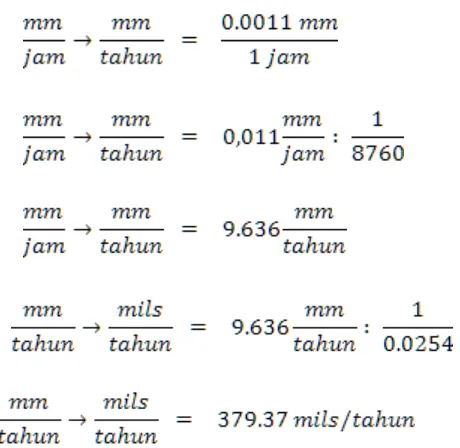
mm/jam 0.001155 0.0011
mm/tahun 10.12 9.636
Perhitungan Pengubahan Satuan Eksperimental:
Perhitungan Pengubahan Satuan Numerikal:
[image:38.595.207.437.266.490.2]Selain itu penulis juga membuat statistik perbandingan perubahan laju korosi dari awal terbentuknya korosi sampai akhir penelitian selesai dilakukan yang didapatkan dari simulasi dan eksperimental , penunjukkan data akan digambarkan dalam bentuk diagram garis scatter untuk memperjelas nilai ralat yang terjadi pada setiap jam pertumbuhan laju korosi yang ditunjukkan oleh tabel 4.4 seperti berikut:
Tabel 4.4 Perbandingan Kenaikan Laju Korosi Per-Jam Secara Eksperimental dan Simulasi (Dokumen Penulis)
Jam ke - Laju Korosi
Eksperimental
Laju Korosi Simulasi
1 0,001155 0,0011
3 0,003465 0,0033
4 0,00462 0,0044
5 0,005775 0,0055
6 0,00693 0,0066
7 0,008085 0,0077
8 0,00924 0,0088
9 0,010395 0,0099
10 0,01155 0,011
11 0,012705 0,0121
12 0,01386 0,0132
13 0,015015 0,0143
14 0,01617 0,0154
15 0,017325 0,0165
16 0,01848 0,0176
17 0,019635 0,0187
18 0,02079 0,0198
19 0,021945 0,0209
20 0,0231 0,022
21 0,024255 0,0231
22 0,02541 0,0242
23 0,026565 0,0253
24 0,02772 0,0264
25 0,028875 0,0275
26 0,03003 0,0286
27 0,031185 0,0297
28 0,03234 0,0308
29 0,033495 0,0319
30 0,03465 0,033
31 0,035805 0,0341
32 0,03696 0,0352
33 0,038115 0,0363
34 0,03927 0,0374
35 0,040425 0,0385
37 0,042735 0,0407
38 0,04389 0,0418
39 0,045045 0,0429
40 0,0462 0,044
41 0,047355 0,0451
42 0,04851 0,0462
43 0,049665 0,0473
44 0,05082 0,0484
45 0,051975 0,0495
46 0,05313 0,0506
47 0,054285 0,0517
48 0,05544 0,0528
49 0,056595 0,0539
50 0,05775 0,055
51 0,058905 0,0561
52 0,06006 0,0572
53 0,061215 0,0583
54 0,06237 0,0594
55 0,063525 0,0605
56 0,06468 0,0616
57 0,065835 0,0627
58 0,06699 0,0638
59 0,068145 0,0649
60 0,0693 0,066
61 0,070455 0,0671
62 0,07161 0,0682
63 0,072765 0,0693
64 0,07392 0,0704
Gambar 4.9 Grafik Statistik Perbandingan Laju Korosi Eksperimental dan Simulasi (Dokumen Penulis)
Maka nilai persen ralat yang didapatkan adalah sebagai berikut: Persen Ralat Satuan mm/jam
Persen Ralat Satuan mm/tahun
Persen Ralat Satuan mils/tahun
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil simulasi dan pengujian eksperimen yang telah dilakukan dan ditunjukkan pada bab sebelumnya, maka kesimpulan dari hasil penelitian ini yaitu:
1. Dari hasil identifikasi ditemukan bahwa fenomena laju korosi dapat diukur pada sistem evaporator dengan kondisi kerja yang telah ditentukan. Metode perhitungan weight-loss dan metode polarisasi dapat digunakan untuk mencari nilai laju korosi yang terjadi dalam evaporator.
2. Penggunaan bahan stainless-steel jenis 304 (SAE 304) tidak dapat digunakan sebagai bahan pembuatan evaporator akibat tingginya nilai laju korosi yang akan menyebabkan evaporator mengalami failure dalam waktu yang singkat.
3. Pola pemeliharaan yang paling efektif pada evaporator (sebagai APK) pada sistem desalinasi air laut adalah dengan pemilihan bahan pembuatan evaporator yang tepat dan pencegahan korosi dilakukan dengan metode pengorbanan anoda (proteksi katoda) secara berkala.
4. Berdasarkan hasil eksperimental dan perhitungan dengan menggunakan metode weight-loss didapatkan bahwa laju korosi yang terjadi pada evaporator adalah 10.12 milimeter/tahun.
pitting (lubang) yang akan kemudian akan mengakibatkan
stress-corrosion cracking dan kedepannya akan mengakibatkan failure pada
evaporator akibat cracking (retak).
6. Dari hasil uji laju korosi secara komputasional dan eksperimental, didapatkan nilai laju korosi evaporator yang mendekati namun masih terjadinya perbedaan nilai laju korosi dalam deviasi yang dapat ditoleransi.
5.2 Saran
1. Untuk peneliti selanjutnya, disarankan untuk melakukan penelitian dalam waktu yang lebih lama untuk mengetahui awal mula titik crack (retak) yang terjadi akibat terjadinya korosi.
2. Melakukan simulasi dengan menghitung faktor – faktor yang mendekati keadaan sebenarnya (eksperimental).
BAB 2
TINJAUAN PUSTAKA
2.1 Teori Dasar Desalinasi
Air asin merupakan larutan yang mengandung beberapa jenis zat terlarut seperti garam-garam, yang jumlahnya rata-rata 3 sampai 4,5 % (sedang air payau dibawah 3% diatas 0,05%). Dengan desalinasi maka air tawar dipisahkan dari air asin. Karena "desalinasi adalah proses pemisahan yang digunakan untuk mengurangi kandungan garam terlarut dari air asin dan juga air payau hingga level tertentu sehingga air dapat digunakan sebagai air bersih". Proses desalinasi melibatkan tiga aliran cairan, yaitu umpan berupa air asin (misalnya air laut) ataupun air payau, produk bersalinitas rendah, dan konsentrat bersalinitas tinggi. Produk proses desalinasi umumnya merupakan air dengan kandungan garam terlarut kurang dari 500 mg/l, yang dapat digunakan untuk keperluan industri, pertanian, dan domestik (kebutuhan air yang digunakan pada tempat-tempat hunian pribadi untuk memenuhi keperluan sehari-hari). Hasil sampingan dari proses desalinasi adalah brine. Brine adalah larutan garam berkonsentrasi tinggi (lebih dari 35000 mg/l garam terlarut). Metoda yang digunakan pada proses pengolahan air ini disebut desalinasi air asin.
Terdapat beberapa cara dan metode desalinasi diantaranya yang tradisonal adalah dengan menggunakan metode vacuum distillation. Prinsipnya yaitu dengan memanaskan air laut untuk menghasilkan uap air, yang selanjutnya dikondensasi untuk menghasilkan air bersih. Cara yang paling umum adalah menggunakan metode osmosis terbalik (reverse osmosis atau RO). Osmosis terbalik dianggap yang paling efektif dalam melakukan desalinasi dalam skala besar. Prinsip kerja metode ini adalah dengan mendesak air laut melewati membran-membran semi-permeabel untuk menyaring kandungan garamnya.
Sistem vakum disini dimaksudkan untuk menurunkan titik penguapan sehingga air laut menguap pada temperatur yang lebih rendah dan hasil distilasi yang didapat lebih banyak dengan energi panas yang lebih sedikit (lebih efisien) serta untuk menarik lebih cepat (flowrate meningkat) dari wadah air laut ke dalam sisi ruang pemanas atau ruang evaporator sistem desalinasi.
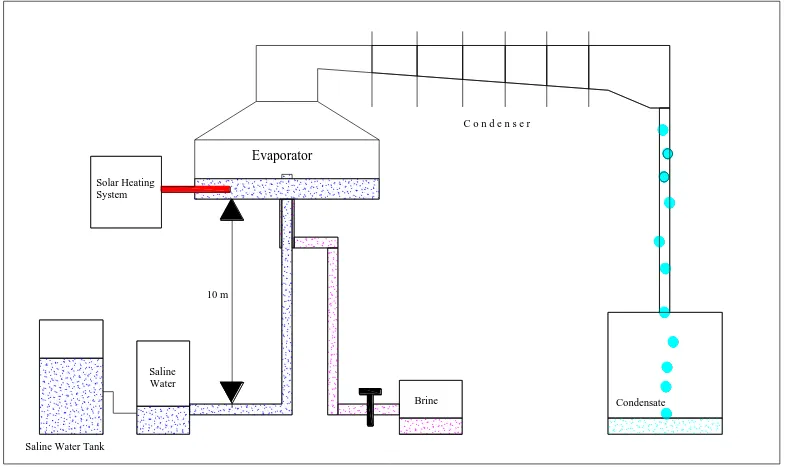
Konsep dari sistem ini adalah memanfaatkan ruang vakum yang dibentuk secara alami untuk dapat mengevaporasikan sejumlah air laut pada tekanan yang lebih rendah dengan suplai energi panas yang lebih sedikit dibanding dengan teknik konvensional. Tekanan atmosfer akan sama dengan tekanan hidrostatis yang dibentuk dengan pipa air setinggi 10 meter. Jadi, jika ketinggian pipa lebih dari 10 meter dan ditutup dari bagian atas dengan air, dan air dibiarkan jatuh kebawah akibat gravitasi, air akan jatuh pada ketinggian sekitar 10 meter, dan membentuk ruang vakum diatasnya. Gambar 2.1 menunjukkan desalinasi sistem vakum. Selain desalinasi sistem vakum, masih banyak jenis lain sistem desalinasi bertenaga surya. (Ketut,dkk.2011)
Condensate Brine
Saline Water
Saline Water Tank Solar Heating System
Evaporator
C o n d e n s e r
[image:45.595.117.510.396.630.2]10 m
Gambar 2.1. Desalinasi Sistem Vakum Natural
2.2 Korosi
antara logam dengan lingkungannya. Atom logam yang berada di alam ditemukan dalam bentuk mineral yang merupakan gabungan dari beberapa zat – zat kimia. Jumlah energi yang sama untuk mendapatkan logam dari mineral dikeluarkan kembali dalam reaksi kimiawi dalam pembentukan korosi. Korosi akan mengembalikan logam ke keadaan mineral yang mirip atau bahkan sama dengan keadaan ketika mineral logam ditambang, sehingga korosi sendiri juga dapat diartikan sebagai proses kebalikan dari extractive metallurgy (J.H.Payer, W.K
Boyd, D.B. Dippold, dan W.H Fisher. Mater, Perform)
Banyak material non-logam, seperti keramik, terdiri atas logam yang reakrivitas kimia-nya telah terpenuhi dari formasi ikatan – ikatan atom dengan ion lain contohnya seperti ion oksida dengan silika. Oleh karena itu, material tersebut tidak akan bereaksi dan lebih cenderung mengalami degradasi dengan faktor kekuatan mekanikal maupun temperatur daripada korosi. Material lain seperti polimer dan gelas, cenderung tidak mengalami reaksi kimia dengan lingkungannya, dan istilah korosi lebih mengarah ke degradasi, namun penggunaan polymer sebagai pelapis material logam yang kemudian mengalami kegagalan melalui degradasi digolongkan sebagai pengaruh korosi.
Korosi dapat menyebabkan adanya retakan maupun lubang dalam suatu permukaan logam, oleh karena korosi merupakan proses difusi yang mempengaruhi permukaan, metode pencegahan adalah dengan menggunakan pasivitas ataupun pelapisan yang tergantung pada kondisi lingkungan pengoperasian sebuah sistem.
2.2.1 Proses Terjadinya Korosi
Hampir semua proses korosi logam meliputi perpindahan muatan elektron dalam fasa aqueous. Sehingga, perlunya pembahasan tentang sifat
electrochemical untuk memahami proses terjadinya korosi.
2.2.1.1 Reaksi Elektrochemical
Berikut akan diberikan contoh korosi antara logam zinc dengan asam klorida yang dituliskan reaksinya sebagai berikut:
Zinc akan bereaksi dengan asam klorida dan membentuk larutan zinc klorida dan mengeluarkan hidrogen pada permukaannya, bentuk ion dari persamaan diatas adalah sebagai berikut:
Zn + 2H+ + 2Cl- ======> Zn2+ + 2Cl- +H2 (2)
Dengan mengeliminasi Cl dari kedua sisi akan didapatkan: Zn + 2H+ ========> Zn2+ + H2 (3)
Sehingga, reaksi korosi yang sama akan muncul pada asam klorida dan reaksi (2) dapat dipisahkan sebagai berikut:
Zn =====> Zn2+ + 2e- reaksi anoda (3) 2H+ ======> 2e- + H2 reaksi katoda (4)
Reaksi (3) didefinisikan sebagai reaksi anoda, merupakan reaksi oksidasi dimana elektron valensi zinc bertambah dari 0 menjadi +2. Melepaskan elektron, e, sedangkan reaksi (4), didefinisikan sebagai reaksi katoda, adalah reaksi reduksi dimana kondisi oksidasi hidrogen berkurang dari +1 menjadi 0, mengabsorbsi sebuah elektron.
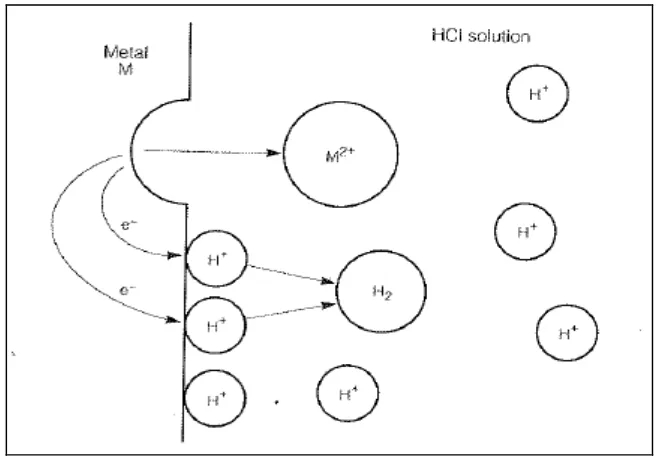
Reaksi komposit yang melibatkan pertukaran muatan atau pertukarn elektron akan ditunjukkan pada gambar 2.2. Logam yang larut dalam reaksi (3) akan melepaskan elektron kedalam kumpulan logam yang akan bermigrasi ke permukaan yang kemudian bereaksi dengan H+ dalam larutan untuk membentuk H2 dalam reaksi (4). Air diperlukan sebagai pengangkut ion seperti Zn2+ dan H+ yang dinamakan elektrolit.
Gambar 2.2 Diagram skematis dari kelarutan logam Mg (Principles and
Prevention of Corrotion, 2nd ed., halaman 6)
Inilah yang menjadi basis untuk menggunakan proteksi katoda sebagai perlindungan pada korosi jalur pipa, pengeboran minyak laut lepas, sampai pada logam yang digunakan pada evaporator.
2.2.1.2 Polarisasi
Reaksi electrochemical seperti yang terjadi pada (3) dan (4) hanya terjadi pada tingkatan tetap (taraf reaksi tetap). Jika elektron pada reaksi (4) diberlakukan, maka potensial pada permukaan akan menjadi lebih negatif, menunjukkan bahwa kelebihan elektron dengan muatan negatif berakumulasi pada permukaan logam/larutan menunggu untuk terjadinya reaksi sebagai hasil dari reaksi yang tidak mampu mengakomodasikan seluruh elektron. Perubahan potensial negatif ini dinamakan sebagai polarisasi katoda, begitu pula yang terjadi pada reaksi (3) ketika kehilangan efisiensi elektron pada logam dilepaskan pada permukaan yang akan menghasilkan perubahan potensial positif yang dinamakan polarisasi anoda. Ketika defisiensi menjadi lebih besar, polarisasi anoda akan berperan sebagai gaya penggerak terjadinya korosi oleh reaksi anoda (3).
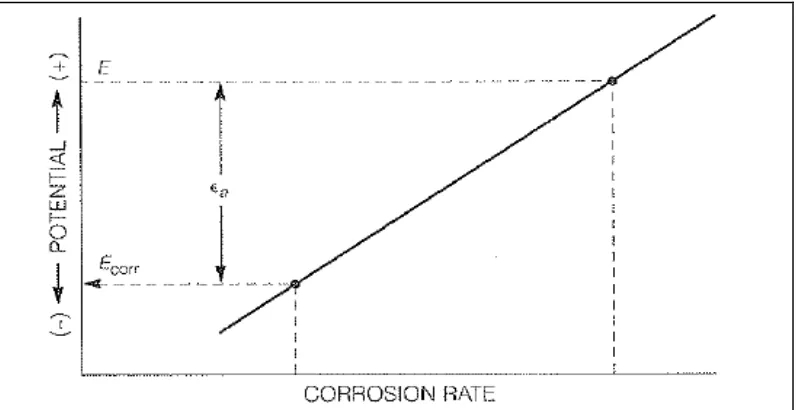
kecepatan dimana elektron dapat bertukar dari reaksi katoda dan anoda yang ada. Ketika potensial permukaan meningkat dari Ecorr menuju E, maka laju reaksi
anoda atau laju korosi akan meningkat, seperti yang ditunjukkan gambar 2.3. Polarisasi anoda didefinisikan sebagai εa = E – Ecorr. Tanpa adanya polarisasi,
[image:49.595.115.513.189.394.2]reaksi akan menimbulkan laju korosi yang sangat tinggi.
Gambar 2.3 Skema Pertambahan Laju Korosi pada Polarisasi (Principles and
Prevention of Corrotion, 2nd ed., halaman 8)
2.2.1.3 Pasivitas
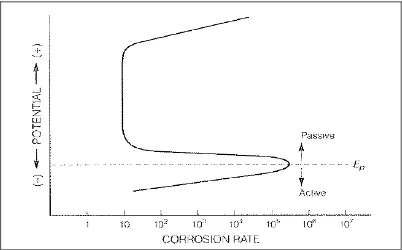
Untuk kebanyakan logam , termasuk kobalt, besi, nikel, krom,stainless steel dan titanium, laju korosi akan menurun setelah melewati potensial batas, εp, seperti ditunjukkan pada gambar 2.4. Ketahanan korosi diatas batas ini, meskipun adanya gaya korosi yang tinggi (polarisasi anoda yang tinggi) disebut dengan pasivitas. Dibawah εp laju korosi logam kembali meningkat dengan perbedaan laju korosi antara batas dapat mencapai 103 sampai 106 kali. Pasivitas terjadi karena adanya pembentukan lapisan tipis oksida hidrasi, yang bertindak sebagai pelindung untuk reaksi pelarutan anoda. Kebanyakan logam memiliki range pasivitas tersendiri, sebagai contohnya stainless-steel type 304 akan memiliki pasivitas pada air laut aerasi namun tidak di air laut yang tidak ber-aerasi.
stainless-steel. Akan tetapi, pasivitas bukanlah tanpa masalah, lapisan yang diciptakan oleh pasivitas cenderung tipis (berkisar 10μm) sehingga apabila lapisan tersebut mengalami breakdown maka pembentukan korosi berupa pitting, crevice sampai cracking dapat terjadi tanpa dapat terdeteksi. (Jones, Denny A. Principles
[image:50.595.113.515.209.459.2]and Prevention of Corrotion. 2nd Ed. 1992)
Gambar 2.4 Pasivitas pada Potensial Oxidasi Diatas εp (Principles and Prevention
of Corrotion, 2nd ed., halaman 10)
2.2.1.4 Korosi Dalam Kajian Mekanikal
Dari segi perubahan fisik yang dialami material ketika mengalami
korosi, kebanyakan mekanisme korosi telah memiliki kaidah/karakteristik masing
– masing yang telah ditetapkan, contohnya reaksi batangan besi (Fe) dengan gas oksigen (O2) serta air (H2O) yang paling umum dijumpai dalam kehidupan sehari
– hari akan menghasilkan karat besi (Fe2O3), hal ini telah ditetapkan bentuk – bentuk fasa korosi melalui kecendrungan ikatan – ikatan atom yang merupakan sifat kimiawi suatu bahan, bukanlah dari sifat mekanis suatu bahan.
Namun kajian mekanikal dapat terlihat dan dihubungkan dalam segi perubahan energi dalam proses terbentuknya korosi, Gejala korosi timbul secara alami, dimana pengaruhnya dialami oleh hampir semua zat dan diatur oleh perubahan-perubahan energi. Sesuai dengan hukum thermodinamika yaitu: - Keseimbangan Termodinamika Pertama: Energi tidak dapat diciptakan dan dimusnahkan.
- Keseimbangan Ternodinamika Kedua: Semua perubahan spontan terjadi disertai pelepasan energi bebas dari sistem ke lingkungan sekitar pada temperatur dan tekanan konstan.
Hukum thermodinamika ke – 0 merupakan prinsip dasar untuk pengukuran temperatur. Hukum thermodinamika ke – 0 dapat terpenuhi apabila terjadi tiga keseimbangan sekaligus yaitu :
- Keseimbangan Termal : setelah semua suhu sama pada setiap titik.
- Keseimbangan Mekanik : setelah tidak ada lagi gerakan, ekspansi atau kontraksi.
- Keseimbangan Kimia : setelah semua reaksi kimia berlangsung.
Pernyataan pertama atau hukum pertama thermodinamika sangat penting dalam pengkajian perubahan-perubahan yang terjadi ketika logam mengalami korosi. Pernyataan kedua atau hukum kedua thermodinamika menyatakan ketika korosi berlangsung secara alami, proses yang terjadi bersifat spontan dan disertai pelepasan energi bebas. Dalam keadaan yang sebebas-bebasnya, alam akan meminimumkan energi, dan dengan korosilah alam meminimumkan energi logam-logam.
Sebuah konsep yang menjelaskan laju reaksi-reaksi korosi adalah teori keadaan peralihan (Transition State Theory), yang persamaannya :
A + B = C + D
Persamaan diatas merupakan bentuk ringkasan pernyataan, ‘Dua zat A dan B, yang dikenal sebagai reaktan, saling berinteraksi sedemikian rupa untuk
membentuk dua zat baru yaitu C dan D yang merupakan hasil reaksi’. Agar dapat menghasilkan zat-zat baru A dan B bukan hanya harus saling sentuh melainkan juga harus terpadu secara fisik, untuk membentuk suatu zat antara AB. Hal ini terjadi dalam waktu yang singkat dan jika reaktan-reaktan memiliki energi cukup dan orientasi keduanya untuk berpadu tepat. AB merupakan keadaan peralihan, dimana reorganisasi keadaan peralihan ini yang kemudian secara langsung menghasilkan C dan D.
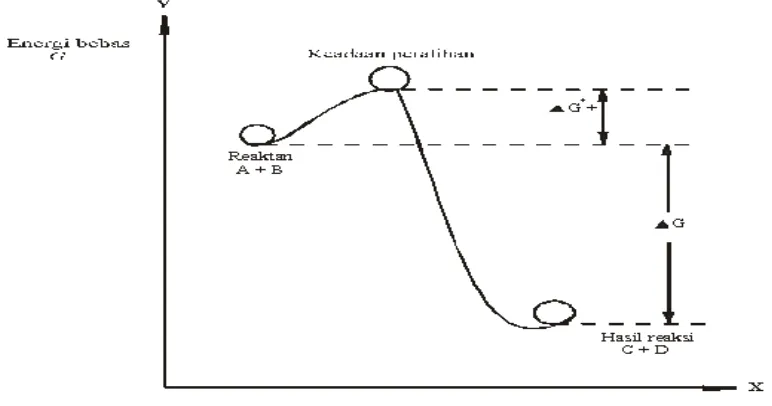
Profil energi merupakan sebuah diagram yang berguna untuk menggambarkan perubahan-perubahan energi bebas yang berlangsung selama reaksi (gambar 2.5). Sumbu Y dalam diagram merupakan energi bebas, perubahan
energi ditulis dengan ∆G, dengan kesepakatan bahwa huruf delta capital (∆)
menyatakan ‘perubahan’. Sumbu X digunakan untuk koordinat reaksi dan dapat
[image:52.595.119.505.498.701.2]dianggap menyatakan kearah mana proses bergerak maju.
Dari gambar di atas menyatakan bahwa keadaan peralihan harus mempunyai energi bebas lebih tinggi dibanding jumlah energi-energi bebas pada masing-masing zat asal, yaitu A dan B. Pada umumnya, jumlah ini dinyatakan
dengan simbol ∆G+. Karena gambar diatas merupakan reaksi spontan maka energi-energi hasil reaksi, C dan D harus lebih rendah dari energi-energi reaktan,
A dan B, dengan selisih sebesar ∆G. Begitu terbentuk, keadaan peralihan dapat
berubah kembali menjadi reaktan atau terus berubah menjadi hasil reaksi.
[image:53.595.202.475.358.616.2]Logam-logam dalam keadaan tidak bergabung dengan bahan lainnya, biasanya memiliki tingkat energi tinggi. Hal ini dijelaskan pada gambar 2.6 menggunakan profil energi untuk menggambarkan perubahan-perubahan thermodinamika yang dialami suatu atom logam, logam bila berdiri sendiri disebut atom logam, dan sesudah bergabung lagi disebut hasil korosi.
Gambar 2.6. Profil Energi Termodinamika untuk Logam dan Senyawanya (http://ismantoalpha.blogspot.co.id/2009/12/macam-macam-korosi.html)
Terakhir, pembahasan terbentuknya melalui gaya – gaya mekanis (seperti gaya tensile maupun gaya kompresi) tidak memiliki pengaruh yang signifikan atau bahkan tidak berpengaruh pada korosi dari material. Gaya kompresi tidak menyebabkan keretakan, dan pada kenyataannya gaya kompresi melalui teknik
shot-peening digunakan untuk menurunkan kemungkinan material logam
mengalami fatik, keretakan dari pengaruh Stress-Corrosion-Cracking (SCC). Akan tetapi gabungan dari gaya tensile dan pengaruh lingkungan korosi yang spesifik dapat menyebabkan kegagalan tiba-tiba melalui cracking pada struktur logam.
2.2.2 Jenis – Jenis Korosi pada Material Logam
Terdapat beberapa bentuk korosi yang ditunjukkan secara skematis di gambar 2.7 dan diurutkan sebagai berikut, yang selanjutnya akan dibahas satu persatu secara singkat:
A. Korosi yang dapat terlihat dan diidentifikasi secara langsung, meliputi 1. Uniform Corrosion
2. Galvanic Corrosion 3. Crevice Corrosion 4. Pitting Corrosion 5. Hydrogen Damage
B. Korosi yang memerlukan identifikasi tambahan atau alat Bantu, meliputi 6. Erosion Corrosion
7. Cavitation
8. Fretting Corrosion 9. Intergranullar Corrosion
C. Korosi yang memerlukan mikroskopi untuk identifikasinya, meliputi 10. Exfolation
11. Dealloying
12. Corrosion Fatigue
Uniform Corrosion merupakan korosi umum yang dialami sebagian besar
logam. Namun dampaknya bentuk korosi lainnya bersifat lebih berpusat, lebih susah dideteksi dan lebih merusak meskipun tidak menkomsumsi/mengenai seluruh material. Hydrogen damage lebih mengacu pada hasil metalurgi, tetapi tetap dibahas akibat frekuensi kejadiannya (Chattoraj, Indrianil.Jurnal
[image:55.595.117.549.224.691.2]Fundamentals of Corrosion & Its Prevention.)
Gambar 2.7 Rangkuman Skema Jenis – Jenis Bentuk Korosi (Principles and
2.2.2.1 Uniform Corrosion
Apabila kerusakan permukaan logam bersifat merata/sejajar maka kerusakan dapat digolongkan kedalam uniform corrosion. Untuk dapat terjadinya
uniform corrosion, lingkungan korosif / reaksi harus dapat terjadi / bereaksi
dengan keseluruhan bagian dalam permukaan logam, ditambah logam itu sendiri harus merata baik secara metalurginya maupun komposisinya. Contoh yang paling mendasar dari korosi jenis ini adalah korosi yang disebabkan oleh atmosfer, contoh lainnya seperti korosi yang terjadi pada baja yang dicelupkan dalam larutan asam. Korosi jenis ini lebih dipilih dalam pandangan teknis apabila dibandingkan dengan korosi lokal/pemusatan lainnya karena dapat diprediksi sehingga dapat dijadikan sebuah faktor dalam perencanaan. Gambar 2.8 menunjukkan permukaan struktur baja bangunan yang telah mengalami uniform
[image:56.595.148.475.371.567.2]corrosion.
Gambar 2.8 Uniform Corrosion pada Struktur Baja (corrosion.ksc.nasa.gov)
2.2.2.2 Galvanic Corrosion
Ketika dua logam didekatkan/dipasang dengan kehadiran elektrolit korosif, salah satu diantara logam tersebut akan mengalami korosi dan yang lain akan terlindung dari korosi itu sendiri. Ketika dua logam yang memiliki potensial korosi, Ecorr, berbeda maka salah satu logam dengan muatan positif atau muatan
campuran seperti stainless steel maupun nikel berada dalam kondisi pasivitas aktif (diatas εp).
[image:57.595.190.433.309.757.2]Gambar 2.9 akan menunjukkan contoh galvanic corrosion diantara logam baja karbon yang dilas dengan sebuah stainless steel. Flens dari pipa baja tersebut akan mengalami korosi di sekitar sambungan las. Semakin menjauh dari las, maka korosi semakin susah terjadi akibat adanya resistensi pada jalur elektrolit, sehingga konduktivitas elektrolit hanya terjadi pada daerah keci di sambungan.
Tabel 2.1 Tabel Seri Galvanic Dalam Air Laut (Principles and Prevention of
Gambar 2.9 Proses Galvanisasi Stainless Steel dan Baja Karbon
(engineering.stackexchange.com)
2.2.2.3 Crevice Corrosion
Crevice corrosion adalah korosi berpusat yang terjadi dalam tempat
tertutup (crevice, lubang), yang dimana akses dari fluida yang bekerja dari lingkungan sangatlah terbatas. Formasi dari sel aerasi yang berbeda akan menimbulkan korosi didalam lubang tersebut. Contoh dari crevice sendiri adalah jarak antara bagian, bagian bawah dari gasket atau seal, didalam retakan, atau ruang yang dipenuhi dengan kotoran maupun sludge.
Korosi ini dipengaruhi oleh jenis crevice (metal atau metal-nonmetal), geometri crevice (bentuk, ukuran permukaan) dan faktor metalurgi serta lingkungan. Pemaparan suatu logam terhadap korosi ini telah ditentukan melalui prosedur standard ASTM dengan acuan temperatur batas crevice
corrosion sebagai indikator pengurutan ketahanan material. Korosi stainless-steel
Gambar 2.10 Crevice Corrosion pada Stainless Steel 316 di APK Sistem Desalinasi Air Laut (Crevice Corrosion .Corrosionclinic.com. 2012)
2.2.2.4. Pitting Corrosion
Kondisi tertentu, seperti konsentrasi oksigen yang rendah atau konsentrasi kloridayang akan membentuk anion, dapat mempengaruhi kemampuan sebuah logam untuk membentuk kembali lapisan pasivitasnya. Pada kasus terparah, keseluruhan permukaan akan tetap terlindungi namun fluktuasi terpusat pada sebuah titik akan mengalami degradasi lapisan oksida hingga mencapai titk batas, korosi pada kondisi berikut dapat menyebabkan munculnya lubang korosi
(corrosion pits), Meskipun lubang korosi hanya terbentuk pada keadaan yang
berukuran jauh lebih besar. Korosi jenis ini umum dijumpai pada logam passivasi, dan dapat dicegah dengan pengendalian lingkungan disekitar logam. Gambar 2.11 menunjukkan lubang (pit) yang dihasilkan akibat pitting corrosion dan Gambar 2.12 menunjukkan bentuk lubang (pit) yang mungkin terbentuk dalam pitting
[image:60.595.124.500.188.329.2]corrosion.
Gambar 2.11 Pitting dan Crevice Corrosion dalam Material Stainless Steel yang Terpapar Larutan Besi Klorida (www.nap.edu)
Gambar 2.12 Skema Penjalaran Lubang (Pit) pada Pitting Corrosion
(Wikipedia.org)
2.2.2.5 Environmental Induced Corrosion
Korosi yang disebabkan oleh faktor lingkungan ini meliputi tiga jenis korosi, yaitu Stress Corrosion Cracking (SCC), Corrosion Fatigue Cracking (CFC), dan Hidrogen-Induced Cracking (HIC).
[image:60.595.163.462.397.520.2]klorida panas. kuningan terhadap larutan ammonia, dan baja karbon terhadap nitrat dimana hal tersebut ditunjukkan oleh gambar 2.13.
CFC terjadi dalam siklus tekanan dalam lingkungan korosif. Kerentanan terhadap dan laju korosi dari keretakan fatik tanpa korosi biasanya bertambah karena adanya kehadiran lingkungan korosif. Baik logam maupun paduan dapat terpapar oleh korosi jenis ini, tanpa adanya lingkungan spesifik. Beach marks secara makroskopis biasanya dapat disaksikan ketika produk korosi diakumulasikan pada jalur keretakan. Akan tetapi, beach marks juga dapat terjadi apabila terdapat perbedaan pada deformasi mikroplastik ketika penjalaran keretakan terganggu, dan beach marks (yang ditunjukkan gambar 2.14) yang muncul dengan indikasi korosi yang sedikit atau tidak ada sama sekali.
[image:61.595.197.428.498.657.2]HIC yang menyebabkan keretakan terjadi ketika difusi hidrogen dalam lattice logam mengalami evolusi hidrogen yang memproduksi atom hidrogen pada permukaan selama korosi electroplating, pembersihan atau proteksi katoda. Keretakan HIC diakselarasi oleh polarisasi katoda.HIC cenderung bersifat lebih dominan dibandingkan SCC pada karbon, logam baja paduan rendah, stainless steels, paduan aluminium, dan paduan titanium. HIC juga berkontribusi terhadap hilangnya umur fatik pada paduan logam kekuatan tinggi, dimana biasanya dipakai dalam pesawat terbang.
Gambar 2.14 Beach Marks dalam Corrosion Fatigue Cracking (Principles and
Prevention of Corrotion, 2nd ed., halaman 18)
2.2.2.6 Hydrogen Damage
Serangan hidrogen adalah reaksi dari hidrogen dengan karbida dalam baja yang membentuk metana, sehingga menyebabkan dekarburisasi, kehampaan, dan tonjolan permukaan. Tonjolan hidrogen yang ditunjukkan oleh gambar 2.15 atau keretakan hidrogen yang lebih kecil dapat terlihat ketika kekosongan yang berisi hidrogen meledakpada permukaan material. Kekosongan terjadi ketika atom hidrogen berpindah dari permukaan material menuju ke bagian dalam material dimana kemudian hidrogen berkumpuldan membentuk tekanan internal untuk merobek dan mendeformasi logam secara lokal.
Formasi hidrat merapuhkan logam reaktif seperti titanium, zink, magnesium, tantalum, niobium, vanadium, uranium dan thorium.
Gambar 2.15 Tonjolan Hidrogen dalam Baja Karbon AISI 1020 (Principles and
[image:62.595.214.424.546.707.2]2.2.2.7 Intergranullar Corrosion
Ketidak murnian reaktif dapat memisahkan atom logam atau elemen yang mengalami pasivitas seperti kromium dapat habis ketika berada dalam batas grain (grain boundaries). Sebagai hasilnya, batas grain atau tempat yang bersangkutan biasanya memiliki tingkat ketahanan korosi yang lebih rendah, korosi yang terjadi pada batas grain dapat menjadi lebih parah sehingga dapat mengakibatkan grain terjatuh dari permukaan, hal inilah yang disebut dengan intergranullar corrosion (IGC) yang biasanya juga banyak dijumpai pada sistem logam paduan.
[image:63.595.158.467.372.576.2]Contoh bentuk IGC yang terjadi pada stainless steel jenis austenitik (ditunjukkan oleh gambar 2.16) dimana perlakuan panas akan menghabiskan batas grain kromium oleh reaksi metalurgi dengan karbon. Dimana struktru akan rentan terhadap korosi IGC, pada range temperatur 425 sampai 815oC (800 sampai 1500oF), kromium karbida (Cr23C6) akan menguap pada batas grain dan menghabiskan jumlah kromium pada daerah disekitar struktur.
Gambar 2.16 Intergranullar Corrosion pada Permukaan Stainless Steel Austentik yang Dilihat Menggunakan Mikroskopi (Principles and Prevention of Corrotion,
2nd ed., halaman 21)
2.2.2.8 Dealloying dan Dezincification
Sebuah elemen logam paduan yang aktif (bernilai negatif secara
electrochemical) yang mengalami pemecahan element secara luas cenderung
dengan dezincification, adalah contoh yang umum dijumpai. Zinc lebih aktif daripada tembaga dalam tabel galvanisasi dan siap meluluhkan kuningan, meninggalkan hasil korosi tembaga yang memiliki sifat mekanikal yang lemah.
Dezincification dapat secara mudah dikenali dengan warna merah dan cenderung
[image:64.595.192.432.292.455.2]muncul dan terjadi dibawah lapisan dan kerusakan yang terjadi cenderung tiba-tiba dan tidak dapat diprediksi seperti yang ditunjukkan oleh gambar 2.17. Masalah umum lainnya yang dijumpai adalah penggunaan tembaga sebagai komponen umum dalam suatu bangunan/struktru yang memiliki sifat lebih mulia apabila dibandingkan dengan material lain seperti nikel, silicon, dan aluminium yang kemudian luluh akibat korosi dezincification.
Gambar 2.17 Proses Dezincification dalam Kuningan (met-tech.com)
2.2.2.9 Erosion-Corrosion dan Fretting
Kombinasi dari fluida korosif dan kecepatan aliran yang tinggi akan menghasilkan korosi erosion-corrosion. Fluida yang stagnant atau berjalan-lambat akan menyebabkan laju korosi yang rendah sampai menengah, akan tetapi gerakan fluida yang cepat akan secara fisik mengkorosi dan menghilangkan lapisan protektif korosi, sehingga akan menunjukkan logam reaktif dibagian bawah lapisan. Pasir dan kotoran tambahan akan mempercepat korosi dan mempercepat serangan erosion-corrosion. Logam paduan yang memiliki kekuatan rendah dan bergantung pada lapsisan pelindung biasanya mengalami korosi jenis ini. Serangan korosi biasanya mengikuti arah dari aliran dan turbulensi disekitar permukaan logam. Erosion – corrosion merupakan jenis korosi yang umum
Kavitasi merupakan kasus khusus dari erosion-corrosion. Ini terjadi ketika kecepatan fluida sangat tinggi dan reduksi tekanan dalam aliran cukup untuk menguapkan air menjadi gelembung yang kemudian akan meledak pada permukaan logam. Ledakan tersebut akan memproduksi tekanan ekstrim yang menganggu permukaan lapisan dan bahkan dapat memecahkan partikel logam itu sendiri. Bentuk dari serangan ini berupa lubang kasar yang pada akhirnya berujung pada penetrasi logam itu sendiri. Kavitasi biasanya terjadi pada blade turbin, impeller pompa, propeller kapal dan pipa air dimana perubahan tekanan secara besar berada. Gambar 2.18 menunjukkan deformasi akibat
erosion-corrosion yang terjadi pada joint pipa kapal.
Fretting merupakan bentuk lain dari korosi erosion-corrosion, akan tetapi
terjadi pada fasa uap. Erosi terjadi akibat gerakan kecil, biasanya dari vibrasi, diantara logam yang berkorosi dan permukaan padat dibawah tekanan. Gerakan tersebut akan menyebabkan lapisan oksida di permukaan terlepas, dan kembali menunjukkan logam reaktif sama seperti jenis erosion-corrosion lainnya. Fretting biasanya ditunjukkan dengan warna merah dari besi oksida yang diproduksi pada permukaan baja seperti yang ditunjukkan oleh gambar 2.19.(Jones, Denny A.
[image:65.595.173.452.497.682.2]Principles and Prevention of Corrotion. 2nd Ed. 1992)
Gambar 2.19 Fretting Corrosion pada Baja (www.pbclinear.com)