PEMERIKSAAN DAN PENETAPAN KADAR ZAT PEWARNA
RHODAMIN B PADA SAUS DAN KERUPUK
DI KOTA MEDAN
SKRIPSI
OLEH: KAKARIAWATY
NIM : 071524033
PROGRAM EKSTENSI JURUSAN FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PEMERIKSAAN DAN PENETAPAN KADAR ZAT PEWARNA
RHODAMIN B PADA SAUS DAN KERUPUK
DI KOTA MEDAN
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk mencapai gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH: KAKARIAWATY
NIM : 071524033
PROGRAM EKSTENSI JURUSAN FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PEMERIKSAAN DAN PENETAPAN KADAR ZAT PEWARNA
RHODAMIN B PADA SAUS DAN KERUPUK
DI KOTA MEDAN
OLEH: KAKARIAWATY
NIM : 071524033
Dipertahankan di hadapan Panitia Penguji Fakultas Farmasi
Universitas Sumatera Utara Pada tanggal: Februari 2010
Pembimbing I, Panitia Penguji,
Drs. Immanuel Meliala, M.Si, Apt. Prof. Dr. rer.nat. Effendy De Lux Putra, SU., Apt. NIP. 195001261983031002 NIP.195306191983031001
Pembimbing II, Drs. Immanuel Meliala, M.Si, Apt. NIP. 195001261983031002
Prof. Dr.Jansen Silalahi, M.App.Sc.,Apt.
NIP. 195006071979031001 Drs. Muchlisyam, M.Si., Apt. NIP. 195006221980021001
Drs. Maralaut Batubara, M.Phill., Apt. NIP. 195101311976031003
Dekan,
KATA PENGANTAR
Puji dan syukur penulis ucapkan kehadirat Tuhan Yang Maha Kuasa atas
berkat dan karunia-Nya yang telah memberikan pengetahuan, kekuatam dan
kebijakan dalam penyelesaian skripsi ini untuk memenuhi syarat guna mancapai
gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
Tujuan dari penelitian ini adalah untuk mengetahui apakah pada saus dan
kerupuk menggunakan zat pewarna Rhodamin B dan kadar Rhodamin B yang
terdapat pada pada saus dan kerupuk. Melalui penelitian ini diketahui bahwa pada
sampel kerupuk mengandung rhodamin B yang masih digunakan sebagai
pewarna. Rhodamin B dapat menyebabkan iritasi saluran pernafasan, iritasi kulit,
iritasi pada mata, iritasi pada saluran pencernaan, keracunan dan gangguan hati
Penulis juga menyampaikan terimakasih yang sebesar-besarnya kepada
Bapak Drs. Immanuel Meliala, M.Si., Apt., dan Prof. Dr. Jansen Silalahi, M.App.
Sc,.Apt yang telah membimbing penulis dengan penuh kesabaran hingga
selesainya penyusunan skripsi ini. Ucapan terimakasih juga disampaikan kepada
Dekan Fakultas Farmasi Universitas Sumatera Utara, Prof. Dr. Sumadio
Hadisahputra, Apt., yang telah memberikan fasilitas selama masa pendidikan dan
juga kepada Almarhum Bapak Drs. Ubaidillah M., Apt., selaku dosen wali yang
telah memberi bimbingan dan dorongan kepada penulis selama perkuliahan.
Pada kesempatan ini penulis menyampaikan terimakasih dan penghargaan
yang tulus kepada Ibunda tercinta Chao Soek Hoei dan seluruh keluarga atas doa,
dorongan dan pengorbanan baik moril maupun material dalam penyelesaian
skripsi ini dan tidak lupa juga penulis menyampaikan terimakasih kepada
yang namanya tidak dapat ditulis satu persatu, yang telah banyak membantu
penulis dalam proses penelitian hingga selesainya penulisan skripsi ini
Medan, Februari 2010 Penulis,
ABSTRAK
Walaupun Rhodamin B dilarang digunakan di dalam makanan dan minuman, tetapi ternyata masih ditemukan dalam beberapa produk makanan dan minuman seperti saus, es dan kerupuk. Tujuan penelitian ini adalah untuk melakukan pemeriksaan dan penetapan kadar rhodamin B didalam saus dan kerupuk. Ada empat puluh sampel yang diperiksa yaitu sampel saus cabai (saus cabai bermerek 9 macam dan saus cabai tidak bermerek 6 macam), saus tomat (saus tomat bermerek 7 macam dan saus tomat tidak bermerek 8 macam) dan kerupuk (kerupuk bermerek 4 macam dan kerupuk tidak bermerek 6 macam). Pemeriksaan kualitatif Rhodamin B dilakukan dengan kromatografi lapis tipis (KLT) dan spektrofotometer sinar tampak. Secara kromatografi lapis tipis (KLT) menggunakan pengembang butanol, asam asetat glacial dan aquades (40:10:24) yang menghasilkan noda bewarna merah muda jika dilihat secara visual dan memberikan fluoresensi kuning jika dilihat dibawah sinar UV 254nm. Secara
spektrofotometer sinar tampak diukur serapan maksimumnya pada panjang gelombang 450-750nm. Penetapan kadar dilakukan secara spektrofotometri sinar tampak pada panjang gelombang 557nm.
Hasil penelitian menunjukkan bahwa 5% sampel yang diperiksa ternyata mengandung Rhodamin B (dua dari empat puluh sampel). Kadar Rhodamin B pada sampel yang diperiksa adalah 65,5763mcg/g untuk sampel II (kerupuk bulat) dan 7,1416mcg/g untuk sampel IV (kerupuk batang). Dari penelitian ini diketahui bahwa Rhodamin B masih digunakan sebagai pewarna pada kerupuk.
Kata kunci: Saus, Kerupuk, Rhodamin B, Penetapan Kadar, Kromatografi Lapis
ABSTRACT
Although banned Rhodamin B used in the food and drink, but it is still found in some food and beverage products such as sauces, ice and crackers. The objective of this research was to examine and quantitative analysis Rhodamin B of sauce and crackers. There were forty samples examined a sample of chili sauce (chili sauce branded 9 kinds and of not branded chili sauce 6 kinds), ketchup (tomato sauce 7 branded and not branded ketchup 8 kinds) and crackers (4 kinds of branded crackers and cracker 6 kinds of branded not). The Qualitative identification of Rhodamin B have been done with Thin Layer Chromatography (KLT) and visible Spectrophotometer. In Thin Layer Chromatography (KLT) using developer butanol, glacial acetic acid and aquades (40:10:24). It has been given the pink bold if it seen visually and given yellow fluorescence if seen in UV spectrum 254nm. In visible spectrophotometer is measured at its maximum absorption wavelength 450-750nm. Quantitative analysis was be done by visible
spectrophotometry maximum wavelength 557nm.
The results show that 5% out of the analysis samples contain Rhodamin B (two samples out of forty). Rhodamin B levels in the samples examined was 65.5763 mcg/g for sample II (round crackers) and 7.1416 mcg/g for sample IV (crackers sticks). From this research that known Rhodamin B is still used as a dye in crackers.
Keywords: Sauce, Crackers, Rhodamin B, Quantitative Analysis, Thin Layer
DAFTAR ISI
Halaman
JUDUL ………... HALAMAN JUDUL ………. LEMBAR PENGESAHAN ……….. KATA PENGANTAR ……….. ABSTRAK ………. ABSTRACT ………... DAFTAR ISI ………. DAFTAR TABEL ………. DAFTAR GAMBAR ………. DAFTAR LAMPIRAN ………. BAB I PENDAHULUAN ………...
1.1Latar Belakang ………
1.2Perumusan Masalah ………...
1.3Hipotesis ………...
1.4Tujuan Penelitian ………
1.5Manfaat Penelitian ………..
BAB II TINJAUAN PUSTAKA ……… 2.1 Bahan Tambahan Pangan ………...
2.2 Bahan Pewarna ...
2.3 Rhodamin B ...
2.4 Pemeriksaan Kualitatif dan Kuantitatif Rhodamin B ...
2.4.2 Metode Spektrofotometer Sinar Tampak ...
2.5 Perolehan Kembali ...
2.6 Batas Deteksi dan Batas Kuantitatif ...
BAB III METODOLOGI PENELITIAN……… 3.1 Alat-alat ………..
3.2 Bahan-bahan ………...
3.3 Metode Pengambilan Sampel ……….
3.4 Prosedur Kerja ………
3.4.1 Pemeriksaan Kualitatif Rhodamin B ………..
3.4.1.1 Metode Spektrofotometer Sinar Tampak …………...
3.4.1.2 Metode Kromatografi Lapis Tipis ……….
3.4.2 Penetapan Kadar Rhodamin B ………
3.4.2.1 Pembuatan Larutan Baku Rhodamin B ……….
3.4.2.1.1 Pembuatan Larutan Induk Baku I ………..
3.4.2.1.2 Pembuatan Larutan Induk Baku II ……….
3.4.2.2 Penentuan Panjang Gelombang Maksimum ………..
3.4.2.3 Penentuan Waktu Kerja ……….
3.4.2.4 Kurva Kalibrasi Larutan Rhodamin B ………...
3.4.2.5 Penetapan Kadar Rhodamin B pada Sampel ……….
3.5 Uji Validasi Metode Analisis ………...
3.5.1 Penentuan Uji Perolehan Kembali ………..
3.5.2 Penentuan Batas Deteksi dan Batas Kuantitatif ………..
BAB IV HASIL DAN PEMBAHASAN……….. 4.1Pemeriksaan Kualitatif Rhodamin B pada sampel………...
4.2Penetapan Kadar ………..
4.2.1Panjang Gelombang Maksimum Larutan Rhodamin B……....
4.2.2Waktu Kerja Larutan Rhodamin B ………..
4.2.3Kurva Kalibrasi Larutan Rhodamin B ……….
4.2.4Kadar Rhodamin B pada sampel ……….
4.2.5Uji Validasi Metode Analisis ………...
BAB V KESIMPULAN DAN SARAN ……….
5.1Kesimpulan ………
5.2Saran ……….
DAFTAR PUSTAKA ……… LAMPIRAN ………..
29
29
30
30
31
32
34 34
34
DAFTAR TABEL
Halaman
Tabel 1. Bahan Pewarna Sintetis yang diizinkan di Indonesia ……… Tabel 2. Zat Pewarna Alami bagi Makanan dan Minuman yang diizinkan di
Indonesia ………...
Tabel 3. Barang Pewarna Sintetis yang di larang di Indonesia ………... Tabel 4. Hasil pemeriksaan kualitatif Rhodamin B pada sampel dengan menggunakan Kromatografi Lapis Tipis (KLT) dan
Spektrofotometer Sinar Tampak ………..
Tabel 5. Kadar Rhodamin B pada sampel ……….. 5
5
6
27
DAFTAR GAMBAR
Halaman
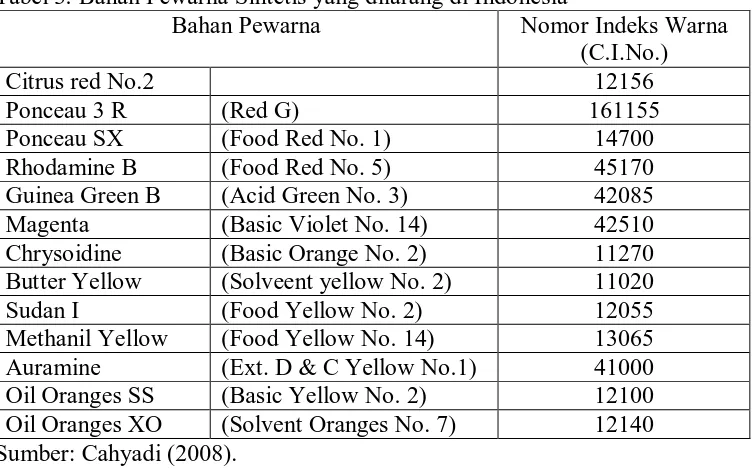
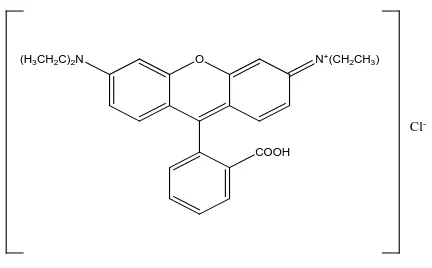
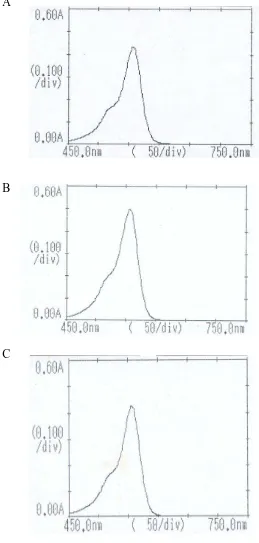
Gambar 1. Rumus Bangun Rhodamin B ……… Gambar 2. A adalah Kurva Absorbansi Larutan Rhodamin B. B dan C adalah Kurva Absorbansi sampel kerupuk bulat sampel kerupuk batang yang mengandung Rhodamin B yang diukur secara
spektrofotometer sinar tampak pada panjang gelombang 450nm-
750nm ………..
Gambar 3. Kromatogram Hasil Uji Kualitatif Rhodamin B pada Sampel ….... Gambar 4. Kromatogram Hasil Uji Kualitatif Rhodamin B pada Sampel dengan penambahan baku Rhodamin B ……… Gambar 5. Kurva Kalibrasi Larutan Rhodamin B dengan pelarut HCl 0,1N pada panjang gelombang 557nm secara Spektrofotometri Sinar Tampak ………
7
24
25
26
31
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Perhitungan Harga Rf ………... Lampiran 2. Kurva Absorbansi Larutan Rhodamin B secara Spektrofotometri Sinar Tampak pada Panjang Gelombang 450nm-750nm ……….
Lampiran 3. Kurva Absorbansi sampel II (kerupuk bulat) yang mengandung Rhodamin B secara spektrofotometer sinar tampak pada panjang
gelombang 450nm-750nm ………
Lampiran 4. Kurva Absorbansi sampel IV (kerupuk batang) yang
mengandung Rhodamin B secara spektrofotometer sinar tampak
pada panjang gelombang 450nm-750nm ………..
Lampiran 5. Data Pengukuran Waktu Kerja Larutan Rhodamin B ………….. Lampiran 6. Data dan Kurva Kalibrasi Larutan Rhodamin B pada Panjang Gelombang 557 nm ………...
Lampiran 7. Perhitungan Persamaan Regresi ………... Lampiran 8. Contoh Perhitungan Kadar Rhodamin B pada Sampel ………… Lampiran 9. Analisa Data Statistik untuk Menghitung Kadar Rhodamin B dalam kerupuk Bulat ……….
Lampiran 10. Analisa Data Statistik untuk Menghitung Kadar Rhodamin B dalam Kerupuk Batang ………...
Lampiran 11. Hasil Analisa Kadar Rhodamin dalam Sampel ……….. Lampiran 12. Perhitungan Perolehan Kembali (%) Kadar Rhodamin B Sampel ………
37
38
39
40
41
42
43
44
45
48
50
Lampiran 13. Perhitungan Batas Deteksi dan Batas Kuantitatif ………... Lampiran 14. Kromatogram Hasil Uji Kualitatif Rhodamin B pada Sampel ... Lampiran 15. Kromatogram Hasil Uji Kualitatif Rhodamin B pada sampel yang dilihat dibawah Sinar UV 254nm ………...
Lampiran 16. Kromatogram Hasil Uji Kualitatif Rhodamin B pada Sampel dengan penambahan baku Rhodamin B ………..
Lampiran 17. Kromatogram Hasil Uji Kualitatif Rhodamin B pada sampel dengan penambahan baku Rhodamin B yang dilihat dibawah
Sinar UV 254nm ……….
Lampiran 18. Surat Sertifikasi Bahan Baku POM ……… Lampiran 19. Sampel Saus Cabai dan Saus Tomat ……….. Lampiran 20. Sampel Kerupuk ………. Lampiran 21. Alat Spektrofotometer UVmini-1240 dan Neraca Analitik …… Lampiran 22. Nilai Distribusi t ……….
52
53
54
55
56
57
58
59
60
ABSTRAK
Walaupun Rhodamin B dilarang digunakan di dalam makanan dan minuman, tetapi ternyata masih ditemukan dalam beberapa produk makanan dan minuman seperti saus, es dan kerupuk. Tujuan penelitian ini adalah untuk melakukan pemeriksaan dan penetapan kadar rhodamin B didalam saus dan kerupuk. Ada empat puluh sampel yang diperiksa yaitu sampel saus cabai (saus cabai bermerek 9 macam dan saus cabai tidak bermerek 6 macam), saus tomat (saus tomat bermerek 7 macam dan saus tomat tidak bermerek 8 macam) dan kerupuk (kerupuk bermerek 4 macam dan kerupuk tidak bermerek 6 macam). Pemeriksaan kualitatif Rhodamin B dilakukan dengan kromatografi lapis tipis (KLT) dan spektrofotometer sinar tampak. Secara kromatografi lapis tipis (KLT) menggunakan pengembang butanol, asam asetat glacial dan aquades (40:10:24) yang menghasilkan noda bewarna merah muda jika dilihat secara visual dan memberikan fluoresensi kuning jika dilihat dibawah sinar UV 254nm. Secara
spektrofotometer sinar tampak diukur serapan maksimumnya pada panjang gelombang 450-750nm. Penetapan kadar dilakukan secara spektrofotometri sinar tampak pada panjang gelombang 557nm.
Hasil penelitian menunjukkan bahwa 5% sampel yang diperiksa ternyata mengandung Rhodamin B (dua dari empat puluh sampel). Kadar Rhodamin B pada sampel yang diperiksa adalah 65,5763mcg/g untuk sampel II (kerupuk bulat) dan 7,1416mcg/g untuk sampel IV (kerupuk batang). Dari penelitian ini diketahui bahwa Rhodamin B masih digunakan sebagai pewarna pada kerupuk.
Kata kunci: Saus, Kerupuk, Rhodamin B, Penetapan Kadar, Kromatografi Lapis
ABSTRACT
Although banned Rhodamin B used in the food and drink, but it is still found in some food and beverage products such as sauces, ice and crackers. The objective of this research was to examine and quantitative analysis Rhodamin B of sauce and crackers. There were forty samples examined a sample of chili sauce (chili sauce branded 9 kinds and of not branded chili sauce 6 kinds), ketchup (tomato sauce 7 branded and not branded ketchup 8 kinds) and crackers (4 kinds of branded crackers and cracker 6 kinds of branded not). The Qualitative identification of Rhodamin B have been done with Thin Layer Chromatography (KLT) and visible Spectrophotometer. In Thin Layer Chromatography (KLT) using developer butanol, glacial acetic acid and aquades (40:10:24). It has been given the pink bold if it seen visually and given yellow fluorescence if seen in UV spectrum 254nm. In visible spectrophotometer is measured at its maximum absorption wavelength 450-750nm. Quantitative analysis was be done by visible
spectrophotometry maximum wavelength 557nm.
The results show that 5% out of the analysis samples contain Rhodamin B (two samples out of forty). Rhodamin B levels in the samples examined was 65.5763 mcg/g for sample II (round crackers) and 7.1416 mcg/g for sample IV (crackers sticks). From this research that known Rhodamin B is still used as a dye in crackers.
Keywords: Sauce, Crackers, Rhodamin B, Quantitative Analysis, Thin Layer
BAB I PENDAHULUAN
1.1Latar Belakang
Menurut Peraturan Pemerintah RI No.28, Tahun 2004, Rhodamin B
merupakan zat warna tambahan yang dilarang penggunaannya dalam
produk-produk pangan. Rhodamin B merupakan zat warna sintetik yang umum digunakan
sebagai pewarna tekstil. (Djalil, dkk., 2005). Rhodamin B dapat menyebabkan
iritasi saluran pernafasan, iritasi kulit, iritasi pada mata, iritasi pada saluran
pencernaan, keracunan dan gangguan hati (Trestiati, 2003). Zat warna rhodamin B
walaupun telah dilarang penggunaannya tetapi masih ada produsen yang sengaja
menambahkan zat warna rhodamin B pada produknya karena harga zat pewarna
untuk pangan lebih mahal jika dibandingkan dengan zat pewarna tekstil dan kulit
biasanya warna dari zat pewarna tekstil dan kulit lebih menarik dibanding dengan
zat pewarna untuk makanan. Pemberian zat pewarna berbahaya dalam bahan
makanan dan minuman juga disebabkan karena ketidaktahuan tentang zat pewarna
apa saja yang diperbolehkan dan yang tidak diperbolehkan untuk ditambahkan
pada makanan. Masyarakat kurang mengetahui bahwa pewarna tekstil yang
digunakan dalam makanan dapat menimbulkan gangguan kesehatan tubuh yang
dalam jangka panjang dapat menyebabkan penyakit seperti kanker dan tumor pada
organ tubuh manusia (Judarwanto, 2006).
Beberapa pedagang karena ketidaktahuannya telah menggunakan beberapa
bahan pewarna yang dilarang untuk pangan, seperti Rhodamin B yang ditemukan
pada produk sirup jajanan, kerupuk, saus dan terasi merah. Dari hasil penelitian
terdapat 5 sampel yang positif mengandung zat warna yang dilarang oleh
pemerintah, yaitu Rhodamin B pada produk sirup jajanan, kerupuk dan terasi
merah (Cahyadi, 2008).
Oleh karena itu, penelitian dilakukan dengan tujuan untuk mengetahui
apakah pada saus dan kerupuk menggunakan zat pewarna Rhodamin B dan kadar
Rhodamin B yang terdapat pada pada saus dan kerupuk. Pemeriksaan Rhodamin
B dilakukan dengan metode Kromatografi Lapis Tipis (KLT) dan metode
Spektrofotometer Sinar Tampak. Identifikasi dengan Kromatografi Lapis Tipis
(KLT), Rhodamin B akan memberikan fluoresensi kuning jika dilihat dibawah
sinar UV 254 nm dan berwarna merah jambu jika dilihat secara visual (Ditjen
POM, 1997). Secara spektrofotometer sinar tampak diukur serapan maksimumnya
pada panjang gelombang 450-750nm. Penetapan kadar rhodamin B dengan
metode spektrofotometri sinar tampak (BPOM, 2006).
1.2Perumusan Masalah
1. Apakah Rhodamin B masih digunakan sebagai zat pewarna pada saus dan
kerupuk di Kota Medan?
2. Berapakah kadar Rhodamin B yang terdapat didalam saus dan kerupuk di
Kota Medan?
1.3Hipotesis
1. Pada saus dan kerupuk yang ada di Kota Medan mengandung zat pewarna
Rhodamin B.
2. Rhodamin B dalam saus dan kerupuk yang ada di Kota Medan terdapat
Tujuan Penelitian
Tujuan dari penelitian adalah untuk:
1. Mengetahui apakah Rhodamin B masih digunakan sebagai zat pewarna pada saus dan kerupuk di Kota Medan.
2. Menentukan kadar Rhodamin B yang terdapat pada saus dan kerupuk di Kota Medan
Manfaat Penelitian
Memberikan informasi kepada masyarakat dan instansi terkait tentang
adanya zat warna berbahaya yang masih digunakan sebagai zat pewarna pada
BAB II
TINJAUAN PUSTAKA
2.1 Bahan Tambahan Pangan
Bahan tambahan pangan adalah bahan yang biasanya tidak digunakan
sebagai makanan dan biasanya bukan merupakan komponen khas makanan,
mempunyai atau tidak mempunyai nilai gizi, yang dengan sengaja ditambahkan ke
dalam makanan untuk maksud teknologi pada pembuatan, pengolahan, penyiapan,
perlakuan, pengepakan, pengemasan dan penyimpanan, pengangkutan makanan
untuk menghasilkan suatu makanan yang lebih baik atau mempengaruhi sifat khas
makanan tersebut (Cahyadi, 2008).
Menurut Peraturan Menteri Kesehatan R.I. No. 329/Menkes/PER/XII/76,
yang dimaksud dengan aditif makanan adalah bahan yang ditambahkan dan
dicampurkan sewaktu pengolahan makanan untuk meningkatkan mutu (Winarno,
2002). Tujuan penggunaan bahan tambahan pangan adalah dapat meningkatkan
atau mempertahankan nilai gizi dan kualitas daya simpan. Bahan tambahan
pangan yang digunakan hanya dapat dibenarkan apabila, tidak digunakan untuk
menyembunyikan atau menutupi penggunaan bahan yang salah atau yang tidak
memenuhi persyaratan dan tidak digunakan untuk menyembunyikan cara kerja
yang bertentangan dengan cara produksi yang baik untuk pangan serta tidak
digunakan untuk menyembunyikan kerusakan bahan pangan (BPOM, 2003).
Bahan Tambahan Pangan (BTP) dikelompokkan berdasarkan tujuan
penggunaanya di dalam pangan. Bahan Tambahan Pangan (BTP) yang sering
2.2 Bahan Pewarna
Zat pewarna dibagi menjadi dua kelompok yaitu certified color dan
uncertified color. Certified color merupakan zat pewarna sintetik yang diijinkan
penggunaannya dalam makanan (Tabel 1). Uncertified color adalah zat pewarna
yang berasal dari bahan alami (Tabel 2) (Winarno, 2004). Beberapa zat pewarna
sintetik yang dilarang penggunaannya dalam makanan adalah Rhodamin B,
Sudan-I, Metanil Yellow, dan Ponceau 3R (Tabel 3).
Penambahan bahan pewarna pangan dilakukan untuk beberapa tujuan,
yaitu untuk memberi kesan menarik bagi konsumen, menyeragamkan warna
makanan, menutupi perubahan warna selama proses pengolahan dan mengatasi
perubahan warna selama penyimpanan (BPOM, 2003)
Tabel 1. Bahan Pewarna Sintesis yang diizinkan di Indonesia
Pewarna Nomor Indeks
Warna (C.I.No.)
Batas Maksimum Penggunaan Amaran Amaranth: CI Food Red 9 16185 Secukupnya Biru berlian Brilliant blue FCF : CI 42090 Secukupnya Eritrosin Food red 2
Eritrosin : CI
45430 Secukupnya
Hijau FCF Food red 14 Fast green FCF : CI
42053 Secukupnya
Hijau S Food green 3 Green S : CI. Food
44090 Secukupnya
Indigotin Green 4
Indigotin : CI.Food
73015 Secukupnya
Ponceau 4R Blue I
Ponceau 4R : CI
16255 Secukupnya
Kuning Food red 7 74005 Secukupnya
Kuinelin Quineline yellow CI. Food yellow 13
15980 Secukupnya
Kuning FCF Sunset yellow FCF CI. Food yellow 3
- Secukupnya
Riboflavina Riboflavina 19140 Secukupnya
Tartrazine Tartrazine Secukupnya
Tabel 2. Zat Pewarna Alami bagi Makanan dan Minuman yang Diijinkan di Indonesia
Warna Nama Nomor Indeks Nama
Merah Alkanat 75520
Merah Cochineal red ( karmin ) 75470
Kuning Annato 75120
Kuning Karoten 75130
Kuning Kurkumin 75300
Kuning Safron 75100
Hijau Klorofil 75810
Biru Ultramarin 77007
Coklat Karamel -
Hitam Carbon black 77266
Hitam Besi oksida 77499
Putih Titanium dioksida 77891
Sumber: Winarno (2004)
Tabel 3. Bahan Pewarna Sintetis yang dilarang di Indonesia
Bahan Pewarna Nomor Indeks Warna (C.I.No.)
Citrus red No.2 12156
Ponceau 3 R (Red G) 161155
Ponceau SX (Food Red No. 1) 14700
Rhodamine B (Food Red No. 5) 45170
Guinea Green B (Acid Green No. 3) 42085 Magenta (Basic Violet No. 14) 42510 Chrysoidine (Basic Orange No. 2) 11270 Butter Yellow (Solveent yellow No. 2) 11020
Sudan I (Food Yellow No. 2) 12055
Methanil Yellow (Food Yellow No. 14) 13065 Auramine (Ext. D & C Yellow No.1) 41000 Oil Oranges SS (Basic Yellow No. 2) 12100 Oil Oranges XO (Solvent Oranges No. 7) 12140 Sumber: Cahyadi (2008).
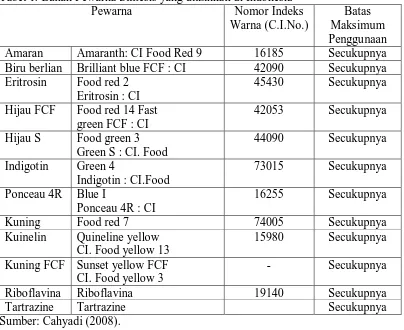
2.3 Rhodamin B
Rhodamin B merupakan zat warna sintetik yang umum digunakan sebagai
pewarna tekstil. (Djalil, dkk., 2005). Nama lazim dari rhodamin B adalah
tetraethylrhodamine; D&C Red No. 19; rhodamine B chloride dengan rumus
O
COOH
(H3CH2C)2N N+(CH2CH3)
Cl
-Gambar 1. Rumus Bangun Rhodamin B
Pemerian : Hablur Hijau atau serbuk ungu kemerahan dan berfluoresensi.
Rhodamin B sangat mudah larut dalam air dan dalam alkohol; sukar larut dalam
asam encer dan dalam larutan alkali. Rhodamin B digunakan sebagai pewarna
untuk sutra, katun, wol, nilon, serat asetat, kertas, tinta dan pernis, sabun, pewarna
kayu, bulu, kulit dan pewarna untuk keramik China (Budavari, 1996).
Penggunaan Rhodamin B pada makanan dan minuman dalam waktu lama
(kronis) akan mengakibatkan kanker dan gangguan fungsi hati. Namun demikian,
bila terpapar Rhodamin B dalam jumlah besar maka dalam waktu singkat akan
terjadi gejala akut keracunan Rhodamin B. Bila Rhodamin B tersebut masuk
melalui makanan akan mengakibatkan iritasi pada saluran pencernaan dan
mengakibatkan gejala keracunan dengan urine yang berwarna merah maupun
merah muda.. Selain melalui makanan dan minuman, Rhodamin B juga dapat
mengakibatkan gangguan kesehatan, jika terhirup akan terjadi iritasi pada saluran
pernafasan. Mata yang terkena Rhodamin B juga akan mengalami iritasi yang
ditandai dengan mata kemerahan dan timbunan cairan atau udem pada mata.Jika
terpapar pada bibir dapat menyebabkan bibir akan pecah-pecah, kering, gatal,
2.4 Pemeriksaan Kualitatif dan Kuantitatif Rhodamin B
Analisis Kualitatif Rhodamin B dapat dilakukan dengan beberapa cara
seperti Kromatografi Lapis Tipis (KLT) dan Spektrofotometer Sinar Tampak,
untuk analisis kuantitatif Rhodamin B dilakukan secara Spektrofotometer Sinar
Tampak.
2.4.1 Metode Kromatografi Lapis Tipis (KLT)
Kromatogafi Lapis Tipis (KLT) adalah metode kromatografi cair yang
paling sederhana. Kromatografi Lapis Tipis (KLT) yang dapat dipakai dengan dua
tujuan. Pertama, digunakan untuk uji identifikasi senyawa baku. Untuk
meyakinkan identifikasi dapat dilakukan dengna menggunakan lebih dari 1 fase
gerak dan jenis semprot. Teknik spiking dengan menggunakan senyawa baku
yang telah diketahui sangat dianjurkan untuk lebih memantapkan pengambilan
keputusan identifikasi senyawa. Kedua digunakan untuk analisis kuantitatif
dengan KLT. Pertama bercak diukur langsung pada lempeng dengan
menggunakan ukuran luas atau densitometri. Cara kedua adalah dengan mengerok
bercak lalu menetapkan kadar senyawa yang terdapat dalam bercak tersebut
dengan metode analisis lain, misalkan dengan metode spektrofotometri (Rohman,
2007).
Analisis kualitatif Rhodamin B dengan menggunakan metode
Kromatografi Lapis Tipis (BPOM, 2000) dengan prinsip membandingkan harga
Rf, jika dilihat secara visual berwarna merah jambu dan jika dilihat dibawah sinar
Faktor–faktor yang mempengaruhi gerakan noda dalam kromatografi
lapisan tipis yang juga mempengaruhi harga Rf:
a. Struktur kimia dari senyawa yang sedang dipisahkan
b. Sifat dari penyerap dan derajat aktifitasnya
c. Tebal dan kerataan dari lapisan penyerap
d. Pelarut dan derajat kemurnian fase gerak
e. Derajat kejenuhan dari uap dalam bejana pengembangan yang digunakan
f. Teknik percobaan
g. Jumlah cuplikan yang digunakan
h. Suhu
i. Kesetimbangan (Hardjono, 1985).
2.4.2 Metode Spektrofotometri Sinar Tampak
Analisis kualitatif dan kuantitatif Rhodamin B dapat dilakukan dengan
metode spektrofotometer sinar tampak (BPOM, 2006). Untuk analisis kualitatif
Rhodamin B dengan menggunakan spektrofotometer sinar tampak yaitu dengan
membandingkan kurva absorbansi yang diukur secara spektrofotometer sinar
tampak pada panjang gelombang 450-750nm (kenkel, 1994) dan untuk analisis
kuantitatif dengan spektrofotometer sinar tampak dengan mengukur
absorbansinya kemudian kadar Rhodamin B dalam sampel dapat dihitung dengan
menggunakan kurva kalibrasi dengan persamaan regresi y = ax + b.
Spektrofotometri Sinar Tampak adalah pengukuran absorbansi energi
cahaya oleh suatu sistem kimia pada suatu panjang gelombang tertentu (Day,
2002). Spektrum UV-Vis mempunyai bentuk yang lebar dan hanya sedikit
spektrum ini sangat berguna untuk pengukuran secara kuantitatif. Konsentrasi dari
analit di dalam larutan bisa ditentukan dengan mengukur absorban pada panjang
gelombang tertentu dengan menggunakan hukum Lambert-Beer (Darchriyanus,
2004; Rohman, 2007). Sinar ultraviolet mempunyai panjang gelombang antara
200-400 nm, dan sinar tampak mempunyai panjang gelombang 400-750 nm
(Darchriyanus, 2004; Ditjen POM, 1995).
Hukum Lambert-Beer (Beer’s Law) adalah hubungan linieritas antara
absorban dengan konsentrasi larutan analit (Darchriyanus, 2004). Menurut
Rohman (2007) dan Day (2002), Hukum Lambert-Beer menyatakan bahwa
intensitas yang diteruskan oleh larutan zat penyerap berbanding lurus dengan tebal
dan konsentrasi larutan dan berbanding terbalik dengan transmitan.
Panjang gelombang yang digunakan untuk analisis kuantitatif adalan
panjang gelombang yang mempunyai absorbansi maksimal, dilakukan dengan
membuat kurva hubungan antara absorbansi dengan panjang gelombang dari suatu
larutan baku pada konsentrasi tertentu.
Ada beberapa alasan mengapa harus menggunakan panjang gelombang maksimal,
yaitu :
1. Pada panjang gelombang maksimal, kepekaannya juga maksimal karena pada
panjang gelombang maksimal tersebut, perubahan absorbansi untuk setiap
satuan konsentrasi adalah yang paling besar.
2. Disekitar panjang gelombang maksimal, bentuk kurva absorbansi datar dan
3. Jika dilakukan pengukuran ulang maka kesalahan yang disebabkan oleh
pemasangan ulang panjang gelombang akan kecil sekali, ketika digunakan
panjang gelombang maksimal.
Ada beberapa tahapan yang harus dilakukan dalam analisis dengan
spektrofotometri ultraviolet dan cahaya tampak yaitu:
1. Penentuan Panjang Gelombang Serapan Maksimum
Panjang gelombang yang digunakan untuk analisis kuantitatif adalah panjang
gelombang dimana terjadi absorbansi maksimum. Untuk memperoleh panjang
gelombang maksimum dapat diperoleh dengan membuat kurva hubungan antara
absorbansi dengan panjang gelombang dari suatu larutan baku dengan konsentrasi
tertentu.
2. Waktu kerja (operating time)
Tujuannya ialah untuk mengetahui waktu pengukuran yang stabil. Waktu
kerja ditentukan dengan mengukur hubungan antara waktu pengukuran dengan
absorbansi larutan.
3. Pembuatan Kurva Kalibrasi
Dilakukan dengan membuat seri larutan baku dalam berbagai konsentrasi
kemudian absorbansi tiap konsentrasi diukur lalu dibuat kurva yang merupakan
hubungan antara absorbansi dengan konsentrasi. Kurva kalibrasi yang lurus
menandakan bahwa hukum Lambert-Beer terpenuhi.
4. Pembacaan absorbansi sampel
Absorbansi yang terbaca pada spektrofotometer hendaknya terletak antara 0,2
disebabkan karena kisaran nilai absorbansi tersebut kesalahan fotometrik yang
terjadi adalah paling minimal.
5. Perhitungan Kadar
Perhitungan kadar dapat dilakukan dengan metode regresi yaitu dengan
menggunakan persamaan garis regresi yang didasarkan pada harga serapan dan
larutan standar yang dibuat dalam beberapa konsentrasi, paling sedikit
menggunakan 5 rentang konsentrasi yang meningkat yang dapat memberikan
serapan linier, kemudian di plot menghasilkan suatu kurva kalibrasi, konsentrasi
suatu sampel dapat dihitung berdasarkan kurva tersebut (Rohman, 2007).
Rumus perhitungan kadar rhodamin B:
Bs Fp V X
K = . .
Keterangan K = Kadar total rhodamin B dalam sampel (mcg/g) X = Kadar rhodamin B sesudah pengenceran V = Volume sampel (ml)
Fp = Faktor pengenceran Bs = Berat sampel
2.5 Perolehan Kembali
Persen perolehan kembali digunakan untuk menyatakan kecermatan.
Kecermatan merupakan ukuran yang menunjukkan derajat kedekatan hasil
analisis dengan kadar analit sebenarnya. Kecermatan dapat ditentukan dengan dua
cara yaitu metode simulasi (spiked-placebo recovery) dan metode penambahan
baku (standard addition method). Dalam metode simulasi, sejumlah analit bahan
murni pembanding kimia ditambahkan ke dalam campuran bahan pembawa
sediaan farmasi (plasebo) lalu campuran tersebut dianalisis dan hasilnya
dilakukan dengan menambahkan sejumlah analit dengan konsentrasi tertentu pada
sampel yang diperiksa lalu dianalisis lagi dengan metode tersebut (WHO, 1992).
Menurut WHO (1992), perolehan kembali dapat dihitung dengan rumus
sebagai berikut : Uji perolehan kembali (%) =
A C
CA CF
*
− x 100%
Keterangan : CF = Konsentrasi sampel yang diperoleh setelah
penambahan larutan baku.
CA = Konsentrasi sampel sebelum penambahan larutan
baku.
C*A = Konsentrasi larutan baku yang ditambahkan.
Batas Deteksi dan Batas Kuantitatif
Batas Deteksi adalah konsentrasi analit terendah dalam sampel yang masih
dapat dideteksi. Batas Deteksi dapat diperoleh dari kalibrasi standar yang diukur
sebanyak 6 sampai 10 kali (Gandjar, 2007;Satiadarma, 2004).
Batas deteksi dapat dihitung dengan rumus.
Batas Deteksi = slope
SD x 3
Batas Kuantitatif adalah kuantitatif terkecil analit dalam sampel yang
masih dapat diukur dalam kondisi percobaan yang sama dan masih memenuhi
criteria cermat dan seksama (WHO,1992).
Batas kuantitatif dapat dihitung dengan rumus.
Batas Kuantitatif = slope
BAB III
METODOLOGI PENELITIAN
Metode penelitian yang dilakukan adalah penelitian deskriptif yaitu untuk
memeriksa zat pewarna Rhodamin B dan untuk mengetahui kadar Rhodamin B
dalam saus dan kerupuk. Penelitian dilakukan di Laboratorium Kimia Farmasi
Kualitatif Fakultas Farmasi USU.
3.1 Alat-Alat
Alat-alat yang digunakan terdiri dari spektrofotometer UV Mini-1240
(Shimadzu) yang dihubungkan dengan printer Epson LQ 300, neraca analitis
(Vibra), bejana, lampu UV 254 nm, benang wool, plat KLT, pipet totol, kertas
saring, pro pipet, penangas air dan alat-alat gelas seperti labu tentukur, pipet
volume, gelas ukur, beaker glass, erlenmeyer, corong, cawan penguap dan batang
pengaduk.
3.2 Bahan-Bahan
Bahan pereaksi yang digunakan adalah HCl 0,1 N, Larutan Amonia 2%,
NaOH 10%, NaOH 0,5%, Aquades, Eter, Asam asetat 6%, Larutan Amonia 10%,
Butanol dan Asam asetat glacial. Pembuatan HCl 0,1N yaitu dengan
mengencerkan 8,3ml asam klorida pekat 37% v/v dengan air suling dalam labu
tentukur 1000 ml (Ditjen POM, 1979). Pembuatan NaOH 10 % dengan
melarutkan 10 gram natrium hidroksida dalam 100 ml air suling bebas CO2.
Pembuatan NaOH 0,5 % dengan melarutkan 5 gram natrium hidroksida dalam
3.3 Metode Pengambilan Sampel
Pengambilan sampel dilakukan secara purposif yaitu didasarkan pada
produk yang beredar dipasaran baik yang bermerek dan yang tidak bermerek.
Pengambilan sampel didasarkan atas pertimbangan bahwa sampel yang diambil
dapat mewakili seluruh populasi sampel yang beredar di kota Medan dan sampel
yang dianalisis dianggap sebagai sampel yang representatif (Sudjana, 1996).
Sampel yang diperiksa adalah saus (cabai dan tomat) dan kerupuk. Sampel
saus cabai yang bermerek (9 botol) dan yang tidak bermerek (5 botol) dan saus
tomat yang bermerek (7 botol) dan yang tidak bermerek (8 botol). Kerupuk
bermerek 4 macam dan kerupuk tidak bermerek 6 macam.
3.4 Prosedur Kerja
3.4.1 Pemeriksaan Kualitatif Rhodamin B
Pemeriksaan Kualitatif Rhodamin B pada sampel menggunakan metode
Spektrofotometer Sinar Tampak dan Kromatografi Lapis Tipis (KLT).
3.4.1.1 Metode Spektofotometer Sinar Tampak
Metode Spektofotometer Sinar Tampak berdasarkan prosedur dari BPOM,
2006. Prinsip dari metode ini adalah dengan membandingkan kurva absorbansi
yang diukur dengan spektofotometer sinar tampak pada panjang gelombang
450-750nm.
Pembuatan Larutan Baku Pembanding dan Larutan Uji
Larutan baku pembanding dibuat dengan cara melarutkan baku
pembanding Rhodamin B dengan HCl 0,1N (Larutan A) dan larutan uji dibuat
dengan menimbang sejumlah ± 15-20 gram sampel yang telah dihomogenkan,
dengan 100 ml larutan amonia 2% dan didiamkan semalam sehingga semua
pewarna larut. Larutan disaring dan diuapkan diatas penangas air hingga kering.
Pewarna dilarutkan secara kuantitatif dengan 30 ml, dimasukkan kedalam corong
pisah 250 ml, ditambahkan 6 ml larutan natrium hidroksida 10%. Lalu diekstraksi
dengan 30 ml dietil eter. Ekstrak eter dipisahkan dan dicuci dengan larutan
natrium hidroksida 0,5%. Ekstrak eter diekstraksi tiga kali, tiap kalinya dengan 10
ml asam klorida 0,1N hingga lapisan eter tidak berwarna lagi, lapisan dibuang,
ekstrak asam klorida 0,1N ditampung dalam labu tentukur 50 ml dan ditambahkan
asan klorida 0,1 N sampai tanda (Larutan B). Masing-masing larutan A dan B
diukur secara spektofotometer UV-Visibel pada panjang gelombang
450nm-750nm.
3.4.1.2Metode Kromatografi Lapis Tipis
Metode Kromatografi Lapis Tipis (KLT) berdasarkan prosedur dari
BPOM, 2000. Prinsip dari metode KLT adalah dengan membandingkan harga Rf
dan bila dilihat secara visual berwarna merah jambu dan dibawah sinar UV
254nm berfluoresensi kuning. Dari prosedur ini terlebih dahulu dibuat larutan
sampel, larutan sampel yang ditambah dengan baku pembanding dan larutan baku
pembanding kemudian di identifikasi dengan kromatografi lapis tipis.
1. Larutan Sampel
a. Timbang sampel masing 30 gram larutkan/suspensikan
masing-masing sampel dalam 50 ml aquades kemudian tambahkan asam asetat 6
%, masukkan benang wool dan panaskan diatas penangas sambil
b. Jika larutan masih berwarna dapat ditambahkan lagi benang wool sambil
dipanasi sampai semua warnanya terserap dan larutan menjadi tidak
berwarna. Benang wool yang berwarna cuci berulang-ulang dengan
aquades hingga bersih.
c. Benang wool yang telah bersih dimasukkan ke dalam cawan penguap,
tambahkan larutan ammonia 10 % secukupnya, dipanaskan diatas
penangas air hingga warna benang wool luntur.
d. Larutan berwarna yang dperoleh dikumpulkan dalam cawan porselin dan
diuapkan diatas penangas air hingga kering dan dilarutkan dalam 2ml air.
2. Larutan Sampel yang ditambah Baku Pembanding
a. Timbang sampel masing-masing 30 gram larutkan masing-masing sampel
dalam 50 ml aquades dan tambahkan 50 mg Rhodamin B pada
masing-masing sampel,
b. Kemudian dibuat perlakuan yang sama dengan larutan sampel.
3. Larutan Baku Pembanding
Dibuat dengan cara menimbang 50 mg Rhodamin B kemudian dilarutkan
dalam 100 ml aquades.
4. Identifikasi dengan Kromatografi Lapis Tipis a. Sediakan Plat Pra Lapis GF 254
b. Penjenuhan Chamber
Chamber dilapisi dengan kertas saring lalu tuang eluen (butanol : asam
asetat glasial : aquades dengan perbandingan 40 : 10: 24) kemudian tutup
rapat dan dibiarkan sampai jenuh yang ditandai dengan eluen naik sampai
c. Penotolan
1. Larutan sampel ditotolkan pada garis penotolan plat yang berjarak 2
cm dari tepi plat menggunakan pipet kapiler yang telah dibilas dengan
aquades, penotolan dilakukan dengan tegak lurus.
2. Larutan sampel yang ditambah dengan baku pembanding ditotolkan
pada garis penotolan yang berjarak 2 cm dari titik penotolan sampel
menggunakan pipet kapiler yang telah dibilas dengan aquades,
penotolan dilakukan dengan tegak lurus.
3. Larutan baku pembanding ditotolkan pada garis penotolan yang
berjarak 2 cm dari titik penotolan sampel dengan menggunakan pipet
kapiler yang telah dibilas dengan aquades, penotolan dilakukan dengan
tegak lurus.
d. Proses Perambatan
Plat pra lapis yang telah ditotolkan dengan sampel dimasukkan ke dalam
chamber yang telah jenuh dengan eluen, kemudian chamber ditutup dan
dibiarkan beberapa saat sampai eluen naik sampai batas atas plat pra lapis.
Angkat plat pra lapis kemudian keringkan dengan alat pengering.
e. Identifikasi Bercak
Letakkan plat pra lapis dibawah lampu UV dengan panjang gelombang
254nm, tandai bercak.
f. Menghitung Harga Rf
Dari bercak yang diperoleh dapat dihitung harga Rf.
3.4.2 Penetapan Kadar Rhodamin B
Penetapan Kadar Rhodamin B pada sampel menggunakan prosedur dari
BPOM, 2006. Prosedur ini dimulai dengan pembuatan larutan baku rhodamin B,
penentuan panjang gelombang, penentuan waktu kerja, kurva kalibrasi larutan
rhodamin B dan penetapan kadar Rhodamin B pada sampel.
3.4.2.1 Pembuatan Larutan Baku Rhodamin B 3.4.2.1.1 Pembuatan Larutan Induk Baku I
Ditimbang dengan seksama 50 mg BPFI Rhodamin B kemudian
dimasukkan kedalam labu ukur 50 ml, larutkan dengan HCl hingga larut
kemudian diencerkan dengan HCl sampai garis tanda.
Konsentrasi larutan induk baku I = ml mg
50 50
x 1000mcg/ml = 1000mcg/ml
3.4.2.1.2 Pembuatan Larutan Induk Baku II
Dipipet 2,5 ml larutan induk baku I dengan menggunakan pipet volum,
dimasukkan kedalam labu ukur 50 ml kemudian diencerkan dengan HCl sampai
garis tanda.
Konsentrasi larutan induk baku I = ml
ml
50 5 , 2
x 1000mcg/ml = 50mcg/ml
3.4.2.2 Penentuan Panjang Gelombang Maksimum
Dipipet 2 ml dari larutan induk baku II Rhodamin B dimasukkan kedalam
labu ukur 50 ml kemudian diencerkan dengan HCl sampai garis tanda (kadar
2mcg/ml), ukur serapan pada panjang gelombang 450-750nm, sebagai blanko
3.4.2.3Penentuan Waktu Kerja
Dipipet 2,5 ml larutan induk baku II dan dimasukkan ke dalam labu ukur
50 ml (konsentrasi 2,5 ppm), kemudian diencerkan dengan HCl sampai garis
tanda. Diukur pada panjang gelombang maksimum dan akan diperoleh absorban
selama 30 menit, sebagai blanko digunakan HCl 0,1N.
3.4.2.4 Kurva Kalibrasi Larutan Rhodamin B
Dari larutan induk baku II dipipet sebanyak 1ml, 1,5ml, 2ml, 2,5ml dan 3
ml. Masing-masing dimasukkan kedalam labu ukur 50 ml kemudian diencerkan
dengan HCl 0,1N sampai garis tanda. Sehingga diperoleh larutan dengan
konsentrasi 1mcg/ml, 1,5mcg/ml, 2mcg/ml, 2,5mcg/ml dan 3mcg/ml. Kemudian
diukur serapannya pada panjang gelombang 557nm dan sebagai blanko digunakan
HCl 0,1N akan diperoleh kurva konsentrasi vs absorban.
3.4.2.5 Penetapan Kadar Rhodamin B pada Sampel
Diisolasi Rhodamin B dari sampel, prosedur kerjanya sama dengan
pembuatan larutan sampel (dilihat pada 2.4.1.2). Rhodamin B yang telah diisolasi
dari sampel disaring dan 10-20% filtrat pertama dibuang, filtrat selanjutnya
ditampung dan diukur serapannya pada panjang gelombang 557nm dan sebagai
blanko digunakan HCl 0,1 N. Kadar Rhodamin B dalam sampel dapat dihitung
dengan menggunakan kurva kalibrasi dengan persamaan regresi y = ax + b.
Rumus Perhitungan Kadar Rhodamin B.
Bs Fp V X
K = . .
Keterangan K = Kadar total rhodamin B dalam sampel (mcg/g) X = Kadar rhodamin B sesudah pengenceran V = Volume sampel (ml)
3.5 Uji Validasi Metode Analisis
Validasi dilakukan untuk menjamin bahwa metode analisis yang dilakukan
akurat, spesifik, reprodusibel dan tahan pada kisaran analit yang akan dianalisis.
Uji validasi yang digunakan yaitu uji akurasi dengan parameter uji perolehan
kembali, batas deteksi dan batas kuantitatif.
3.5.1 Penentuan Uji Perolehan Kembali
Uji perolehan kembali dilakukan dengan menambahkan larutan baku
Rhodamin B dengan konsentrasi 50 ppm sebanyak 1 ml kedalam sampel
kemudian dianalisis dengan perlakuan yang sama pada sampel.
Menurut WHO (1992), perolehan kembali dapat dihitung dengan rumus
sebagai berikut : Uji perolehan kembali (%) =
A C
CA CF
*
− x 100%
Keterangan : CF = Konsentrasi sampel yang diperoleh setelah
penambahan larutan baku.
CA = Konsentrasi sampel sebelum penambahan larutan
baku.
C*A = Konsentrasi larutan baku yang ditambahkan.
3.5.2 Penentuan Batas Deteksi dan Batas Kuantitatif
Batas Deteksi adalah konsentrasi analit terendah dalam sampel yang masih
dapat dideteksi. Batas Deteksi dapat diperoleh dari kalibrasi standar yang diukur
sebanyak 6 sampai 10 kali (Gandjar, 2007;Satiadarma, 2004).
Batas deteksi dapat dihitung dengan rumus sebagai berikut :
Batas Deteksi = slope
Batas Kuantitatif adalah kuantitatif terkecil analit dalam sampel yang
masih dapat diukur dalam kondisi percobaan yang sama dan masih memenuhi
criteria cermat dan seksama (WHO,1992).
Batas kuantitatif dapat dihitung dengan rumus :
Batas Kuantitatif = slope
BAB IV
HASIL DAN PEMBAHASAN
4.1 Pemeriksaan Kualitatif Rhodamin B pada Sampel
Pada penelitian ini dilakukan pemeriksaan kualitatif dan kuantitatif
Rhodamin B pada sampel. Sebelum dilakukan pemeriksaan secara kuantitatif
maka perlu dilakukan pemeriksaaan secara kualitatif untuk mengetahui ada
tidaknya rhodamin B pada sampel. Pemeriksaan kualitatif rhodamin B pada
sampel menggunakan metode Spektrofotometer Sinar Tampak dan Kromatografi
Lapis Tipis (KLT). Berdasarkan hasil pemeriksaan kualitatif rhodamin B dengan
menggunakan spektrofotometer sinar tampak maka diperoleh kurva absorbansi
seperti pada Gambar 2.
Identifikasi spektrofotometer sinar tampak yaitu dengan membandingkan
kurva absorbansi pada panjang gelombang 450-750nm (Kenkel, 1994). Dari
gambar 2 dapat dilihat bahwa sampel mempunyai kurva absorbansi yang sama
dengan kurva absorbansi baku pembanding rhodamin B maka dapat disimpulkan
bahwa sampel positif mengandung rhodamin B. Kurva absorbansi larutan baku
pembanding dengan sampel kerupuk yang mengandung Rhodamin B dapat dilihat
A
B
C
[image:40.595.147.406.90.633.2]Selain identifikasi dengan spektrofotometer sinar tampak juga digunakan
identifikasi dengan kromatografi lapis tipis. Identifikasi dengan kromatografi lapis
tipis yaitu dengan membandingkan harga Rf dan apabila dilihat secara visual
berwarna merah jambu dan jika dilihat dibawah sinar UV 254nm berfluoresensi
kuning, gambar kromatogram dapat dilihat pada Gambar 3 dan 4.
[image:41.595.148.475.226.531.2]B ST STM ST+R SC SCM SC+R KM KB(I) KB(II)
Gambar 3. Kromatogram hasil uji kualitatif rhodamin B pada sampel
Keterangan : B = Baku pembanding ST = Sampel saos tomat
STM = Sampel saos tomat bermerek
ST+R = Sampel saos tomat + baku pembanding SC = Sampel saos cabai
SCM = Sampel saos cabai bermerek
SC+R = Sampel saos cabai + baku pembanding KM = Kerupuk bermerek
Dari gambar 3 dapat dilihat bahwa ada satu noda (sampel KM) yang
mempunyai warna yang hampir sama dengan warna noda Rhodamin B, tetapi
noda tersebut bukan Rhodamin B karena apabila dilihat dibawah sinar UV 254nm,
noda tersebut tidak berfluoresensi memberikan warna kuning.
Selain itu, untuk mengidentifikasi suatu senyawa dapat dilakukan dengan
melihat harga Rf-nya. Identifikasi sahih dilakukan jika senyawa yang dianalisis
dibandingkan dengan senyawa pembanding dan dengan campuran yang terdiri
atas senyawa yang dianalisis dan senyawa pembanding (cara spiking) pada lapisan
yang sama (Gritter, 1991) dapat dilihat pada Gambar 3.
B KB(II) KB(II)+R KB(I) KB(I)+R
Gambar 4. Kromatogram Hasil Uji Kualitatif Rhodamin B pada Sampel dengan penambahan baku Rhodamin B
Keterangan : B = Baku pembanding
KB (I) = Sampel Kerupuk Bulat yang mengandung Rhodamin B
KB (I) + R = Sampel Kerupuk Bulat yang mengandung Rhodamin B + Baku pembanding
KB (II) = Sampel Kerupuk Batang yang mengandung Rhodamin B
[image:42.595.177.422.324.591.2]Dari gambar diatas dapat dilihat bahwa ada 2 sampel yang memberikan
harga Rf yang berdekatan dengan pembandingnya. Sampel II (kerupuk bulat),
harga Rfnya 0,835 dan harga Rf dari campuran sampel dan baku pembanding
adalah 0,841 sedangkan pada sampel IV(kerupuk batang), harga Rf nya 0,841 dan
harga Rf dari campuran sampel dan pembanding adalah 0,841. Jadi dapat
disimpulkan bahwa sampel kerupuk bulat dan sampel kerupuk batang positif
mengandung Rhodamin B (Perhitungan Harga Rf pada Lampiran 1 halaman 37).
Data dari hasil pemeriksaan kualitatif rhodamin B secara spektrofotometer
[image:43.595.114.527.372.717.2]dan kromatografi lapis tipis pada sampel diperoleh data seperti ditunjukkan pada
Tabel 4.
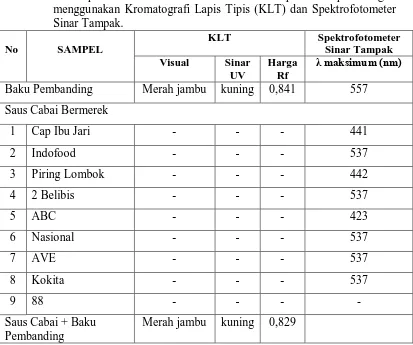
Tabel 4. Hasil pemeriksaan kualitatif Rhodamin B pada sampel dengan menggunakan Kromatografi Lapis Tipis (KLT) dan Spektrofotometer Sinar Tampak.
No SAMPEL
KLT Spektrofotometer
Sinar Tampak
Visual Sinar
UV
Harga Rf
λ maksimum (nm)
Baku Pembanding Merah jambu kuning 0,841 557 Saus Cabai Bermerek
1 Cap Ibu Jari - - - 441
2 Indofood - - - 537
3 Piring Lombok - - - 442
4 2 Belibis - - - 537
5 ABC - - - 423
6 Nasional - - - 537
7 AVE - - - 537
8 Kokita - - - 537
9 88 - - - -
Saus Cabai + Baku Pembanding
Tabel 4. (lanjutan)
Saus Tomat Bermerek
10 Heinz - - - 537
11 ABC - - - 537
12 Carrefour - - - 537
13 Del Monte - - - -
14 Indofood - - - 537
15 Prima - - - -
16 Xo Xing - - - -
Saus Tomat+ Baku Pembanding
Merah jambu kuning 0,817
Saus Cabai tidak Bermerek
17 Sampel I - - - 509
18 Sampel II - - - -
19 Sampel III - - - -
20 Sampel IV - - - 482
Tabel 4. (lanjutan)
21 Sampel V - - - 466
22 Sampel VI - - - 487
Saus Tomat tidak Bermerek
23 Sampel I - - - 481
24 Sampel II - - - 487
25 Sampel III - - - 490
26 Sampel IV - - - 486
27 Sampel V - - - 466
28 Sampel VI - - - 500
29 Sampel VII - - - 537
30 Sampel VIII - - - -
Kerupuk Bermerek
31 Cap Bintang - - - -
32 Cap Ikan Mas Koki - - - -
[image:44.595.114.529.96.695.2] [image:44.595.113.530.113.763.2]Tabel 4. (lanjutam)
34 Cap Aneka - - - -
Kerupuk tidak Bermerek
35 Sampel I (ikan) - - -
36 Sampel II (bulat) Merah jambu kuning 0,835 556 Sampel II (bulat) +
Rhodamin B
Merah jambu kuning 0,841
37 Sampel III (kerucut)
- - - -
38 Sampel IV (batang) Merah jambu kuning 0,841 556 Sampel IV (batang) +
Rhodamin B
Merah jambu kuning 0,841
39 Sampel V (bulat kecil)
- - - -
40 Sampel VI (bulat besar)
- - - -
Keterangan : (-) = negatif
Dari tabel diatas dapat dilihat bahwa ada 2 sampel yang memberikan hasil
positif karena mempunyai harga Rf yang berdekatan dengan harga Rf baku
pembanding dan jika diamati secara visual berwarna merah jambu dan diamati
dibawah sinar UV berfluoresensi kuning (dapat dilihat pada Gambar 2).
(Kromatogram Hasil Uji Kualitatif Rhodamin B pada Sampel pada Lampiran 14
halaman 53). Suatu senyawa yang mengandung Rhodamin B akan mudah diamati.
Secara visual akan memberikan warna merah jambu dan jika dilihat dibawah sinar
UV akan berfluoresensi memberikan warna kuning (Ditjen POM, 2001).
4.2 Penetapan Kadar
4.2.1 Panjang Gelombang Maksimum Larutan Rhodamin B
Penentuan panjang gelombang maksimum larutan Rhodamin B dilakukan
pada konsentrasi 2,5 ppm dengan rentang panjang gelombang 450-750 nm. Hal ini
[image:45.595.112.529.99.360.2]itu pengukuran dilakukan pada rentang tersebut karena pada panjang gelombang
maksimum kepekaannya juga maksimum dan disekitar panjang gelombang
maksimum bentuk kurva absorbansi datar dan pada kondisi tersebut hukum
Lambert-Beer akan terpenuhi (Rohman, 2007). Kurva Serapan larutan Rhodamin
B dapat dilihat pada Gambar 2 A.
Hasil penentuan panjang gelombang maksimum larutan Rhodamin B
dengan konsentrasi 2,5 ppm, diperoleh λ maksimum pada 557nm. Panjang
gelombang maksimum yang diperoleh ini berbeda dengan yang terdapat dalam
sertifikat pengujian Badan POM yaitu 554nm Perbedaan panjang gelombang
sebesar 3nm masih dalam batas toleransi yang diperkenankan menurut Farmakope
Indonesia Edisi IV (1995) yaitu lebih kurang 3 nm. Hal ini berarti bahwa panjang
gelombang ini dapat diterima untuk analisis Rhodamin B pada sampel.
4.2.2 Waktu Kerja Larutan Rhodamin B
Pada penentuan waktu kerja larutan baku Rhodamin B diperoleh waktu
pengukuran yang stabil dimulai dari menit ke-10 sampai menit ke-22 (Data
pengamatan pada Lampiran 5, halaman 41). Dari data waktu kerja, tidak diperoleh
data yang mempunyai kesamaan angka 4 desimal. Sehingga yang diambil sebagai
waktu kerja yang terbaik adalah data yang mempunyai kesamaan angka 3 desimal
dan angka ke 4 desimalnya berdekatan satu sama lain.
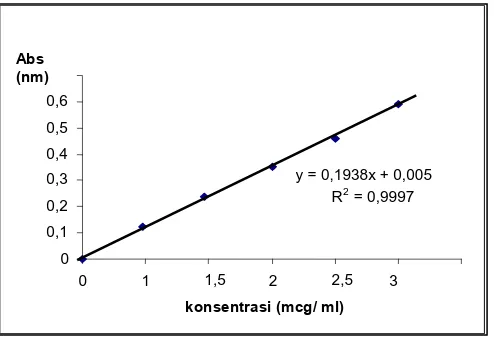
4.2.3 Kurva Kalibrasi Larutan Rhodamin B
Pembuatan kurva kalibrasi larutan Rhodamin B dilakukan dengan
membuat larutan dengan berbagai konsentrasi pengukuran yaitu 1 ppm, 1,5 ppm,
y = 0,1938x + 0,005 R2 = 0,9997
0 0,1 0,2 0,3 0,4 0,5 0,6
0 1 1,5 2 2,5 3
konsentrasi (mcg/ ml) Abs
(nm)
557nm. Kurva kalibrasi Larutan Rhodamin B dapat dilihat pada Gambar 5 (Data
[image:47.595.158.405.144.315.2]dan Gambar pada Lampiran 6, halaman 41).
Gambar 5. Kurva Kalibrasi Larutan Rhodamin B dengan pelarut HCl 0,1N pada panjang gelombang 557nm secara Spektrofotometri Sinar Tampak
Dari hasil perhitungan persamaan regrasi kurva kalibrasi diatas diperoleh
persamaan garis y = 0,1938x + 0,005 dengan koefisien korelasi (r) sebesar 0,9997.
Dari hasil tersebut dapat dikatakan bahwa terdapat korelasi yang positif antara
kadar dan serapan. Artinya, dengan meningkatnya konsentrasi maka absorbansi
juga akan meningkat. Hal ini berarti terdapat 99,99 % data yang memiliki
hubungan linier (Sudjana, 2002).
4.2.4. Kadar Rhodamin B pada sampel
Dari sampel saus dan kerupuk yg telah di identifikasi dengan kromatografi
lapis lipis dan spektofotometer sinar tampak terdapat 2 sampel kerupuk yang
positif mengandung Rhodamin B, sehingga dilakukan penetapan kadar. Penetapan
kadar Rhodamin B yang terdapat pada sampel kerupuk yang positif dilakukan
dengan menggunakan spektrofotometri sinar tampak. Hasil penetapan kadar
analisa statistik dan analisa kadar Rhodamin B dalam sampel dapat dilihat pada
Lampiran 8, 9, 10 dan 11, halaman 44-50).
Tabel 5. Kadar Rhodamin B pada sampel
No Sampel Kadar Rhodamin B
(mcg/g)
Standar Deviasi (SD)
1 Sampel II (kerupuk bulat)
65,5763 0,0072
2 Sampel IV (kerupuk batang)
7,1416 0,0167
Dari tabel diatas dapat dilihat bahwa kadar Rhodamin B dalam kedua
kerupuk cukup besar. Hal ini sangat membahayakan masyarakat yang
mengkonsumsi kerupuk. Karena semakin besar kemungkinan Rhodamin ini
masuk ke dalam tubuh dan memberikan efek toksik (Budavari, 1996).
Rhodamin B merupakan zat pewarna sintetik yang berbahaya. Sering
disalahgunakan untuk mewarnai berbagai makanan dan minuman. Apabila
Rhodamin B digunakan sebagai pewarna makanan dapat menimbulkan iritasi pada
saluran pencernaan dan menimbulkan gejala keracunan dan air seni berwarna atau
merah muda.
4.2.5 Uji Validasi Metode Analisis
Pada penelitian ini dilakukan juga uji validasi metode dengan maksud
untuk melihat kebenaran metode yang digunakan. Salah satu uji validasi tersebut
adalah uji perolehan kembali. Dalam hal ini uji perolehan kembali dilakukan pada
sampel kerupuk bulat, dimana sejumlah larutan baku yang sudah diketahui
konsentrasinya ditambahkan ke dalam sampel kerupuk yang sudah diketahui
kadarnya. Hasil perolehan kembali yaitu 93,72%. (Hasil dan perhitungan pada
Rentang rata-rata hasil uji perolehan kembali yang diizinkan untuk 1 ppm
unit yang diperiksa adalah 80-110% (WHO, 1992). Dari hasil yang diperoleh
menunjukkan bahwa persen perolehan kembali dapat diterima dan dapat
disimpulkan bahwa metode yang dilakukan cukup akurat.
Selain itu juga dilakukan parameter uji validasi yang lain yaitu batas
deteksi dan batas kuantitasi. Batas deteksi dan kuantitasi yang diperoleh dari
penelitian ini adalah berturut-turut 0,2043 mcg/ml dan 0,6811 mcg/ml (Hasil
perhitungan pada Lampiran 13, halaman 52).
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari hasil pemeriksaan yang telah dilakukan maka dapat disimpulkan
bahwa 5% dari sampel yang diperiksa ternyata mengandung Rhodamin B (dua
sampel dari empat puluh sampel). Dari hasil penelitian diperoleh kadar Rhodamin
B pada sampel II (kerupuk bulat) sebesar 65,5763mcg/g dan pada sampel IV
(kerupuk batang) sebesar 7,1416mcg/g.
5.2 Saran
a. Untuk peneliti selanjutnya, diharapkan untuk memeriksa zat warna tekstil
lain yang dilarang digunakan pada makanan.
b. Disarankan kepada Badan Pengawas Obat-Obatan dan Makanan untuk
DAFTAR PUSTAKA
BPOM. (2003). Bahan Tambahan Pangan. Direktorat SPKP, Deputi III. Jakarta. Hal: 9.
Cahyadi, W. (2008). Analisis dan Aspek Kesehatan Bahan Tambahan Pangan. Edisi kedua. Penerbit Bumi Aksara. Jakarta. Hal: 1-2, 61-65.
Dachriyanus, (2004). Analisis Struktur Senyawa Organik Secara Spektroskopi. Penerbit Andalas University Press. Jakarta. Hal: 1-3.
Day, R.A & Underwood, A.L. (1999). Analisis Kimia Kuantitatif. Penerjemah: Pudjaatmaka, A.H. Edisi kelima, Penerbit Erlangga. Jakarta. Hal: 393.
Ditjen POM. (1979). Farmakope Indonesia. Edisi Ketiga. Departemen Kesehatan RI. Jakarta. Hal:712.
Ditjen POM. (1995). Farmakope Indonesia. Edisi Keempat. Departemen Kesehatan RI. Jakarta, Hal: 1176.
Ditjen POM. (2000). Metode Analisis PPOM. Jakarta: Departemen Kesehatan RI.
Ditjen POM. (2006). Metode Analisis PPOM. Jakarta: Departemen Kesehatan RI.
Gandjar, I.G dan Rohman, A. (2007). Kimia Farmasi Analisis. Cetakan Kedua, Penerbit Pustaka Pelajar. Jakarta. Hal: 120.
Gritter, R.J., dan James, M.R. (1991). Pengantar Kromatografi. Terbitan Kedua. Bandung: Penerbit ITB. Hal: 107, 133.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Majalah Ilmu Kefarmasian. Vol.I No.3. Hal: 117-133.
Holme,J.D. and Peck,H. (1983). Analitycal Biochemistry. Departement of Biological Sciences Sheffield City Polytecnic. London. New York. Hal: 39.
Satiadarma, K. (2004). Asas Pengembangan Prosedur Analisis. Edisi Pertama. Penerbit Airlangga University Press. Surabaya. Hal: 47
Stahl, E. (1985). Analisis Obat secara Kromatografi dan Mikroskopi. Penerbit ITB Bandung. Hal: 3.
Sudjana. (2002). Metode Statistika. Edisi Statistika. Edisi Keenam. Penerbit Tarsito, Bandung. Hal: 168, 371.
Suyanti. (2007). Membuat Aneka Olahan Cabai. Penerbit Penebar Swadaya, Jakarta. Hal: 48.
WHO. (1992). Validation of Analytical Procedures Used in Examination of Pharmaceutical materials. WHO Technical Report Series. No. 823. Hal: 117.
Lampiran 1. Perhitungan Harga Rf
Harga Rf =
Jarak yang digerakkan oel pelarut dari titik asal Jarak yang digerakkan oleh senyawa dari titik asal
Plat A
Jarak yang digerakkan oleh pelarut dari titik asal = 1,5cm
Harga Rf untuk baku pembanding = 14,3/17 = 0,841
Harga Rf untuk sampel saus tomat + baku pembanding = 13,9/17 = 0,0817
Harga Rf untuk sampel saus cabai + baku pembanding = 14,1/17 = 0,829
Harga Rf untuk sampel kerupuk bulat = 14,2/17 = 0,835
Harga Rf untuk sampel kerupuk batang = 14,2/17 = 0,835
Plat B
Jarak yang digerakkan oleh pelarut dari titik asal = 1,5cm
Harga Rf untuk baku pembanding = 14,3/17 = 0,841
Harga Rf untuk sampel kerupuk batang = 14,2/17 = 0,835
Harga Rf untuk sampel kerupuk batang + Rhodamin B = 14,3/17 = 0,841
Harga Rf untuk sampel kerupuk bulat = 14,3/17 = 0,841
Lampiran 5. Data Pengukuran Waktu Kerja Larutan Rhodamin B
y = 0,1938x + 0,005 R2 = 0,9997
0 0,1 0,2 0,3 0,4 0,5 0,6
0 1 1,5 2 2,5 3
konsentrasi (mcg/ ml) Abs
(nm)
Lampiran 6. Data dan Kurva Kalibrasi Larutan Rhodamin B pada Panjang Gelombang 557 nm
No Konsentrasi
(mcg/ml) Absorbansi
1 0,000 0,000
2 1,000 0,188
3 1,500 0,278
4 2,000 0,381
5 2,500 0,479
6 3,000 0,582
Lampiran 7. Perhitungan Persamaan Regresi
No Konsentrasi
(mcg/ml) Absorbansi
1 0,000 0,000
2 1,000 0,188
3 1,500 0,278
4 2,000 0,381
5 2,500 0,479
6 3,000 1,582
a
( )
∑
∑ ∑
( )
∑
∑
− −
= 2 2
x n x xy n y x
(
)(
) (
)
(
10,000) (
622,500)
4,310 6 1,908 10,000 2 − − = 0,1938 =b= y−ax
005 , 0 ) 667 , 1 ( 1938 , 0 318 , 0 − = − =
Maka persamaan garis regresinya adalah: y = 0,1938 x – 0,005
r =
] / ) ( ) ][( / ) ( ) [( / ) )( ( 2 2 2 2 n y y n x x n y x xy Σ − Σ Σ − ∑ ∑ Σ − Σ = ] 6 / ) 908 , 1 ( ) 857 , 0 ][( 6 / ) 000 , 10 ( ) 500 , 22 [( 6 / ) 908 , 1 )( 000 , 10 ( 3105 , 4 2 2 − − − = 1308 , 1 1305 , 1 = 0,9997
No x y x2 y2 xy
1 0,000 0,000 0,000 0,000 0,000
2 1,000 0,188 1,000 0,035 0,188
3 1,500 0,278 2,250 0,077 0,417
4 2,000 0,381 4,000 0,145 0,762
5 2,500 0,479 6,250 0,229 1,197
6 3,000 0,582 9,000 0,338 1,746
∑ 10,000 1,908 22,500 0,824 4,310
x = 1,667 y= 0,318 x2
Lampiran 8. Contoh Perhitungan Kadar Rhodamin B pada Sampel
Berat sampel yang ditimbang = 19,315 gram
Serapan (y) = 0,4957
Persamaan regresi y = 0,1938 - 0,0050
Kadar Rhodamin (x) 0,4957 = 0,1938 X - 0,0050
X =
0,1938 0,4957-0,0050
X = 2,5330 mcg/ml
Rumus Perhitungan Kadar Rhodamin B. K = Bs
X.V.Fp
Keterangan K = Kadar total Rhodamin B dalam sampel (mcg/g) X = Kadar Rhodamin B sesudah pengenceran V = Volume sampel (ml)
Fp = Faktor Pengenceran Bs = Berat sampel
Kadar Total Rhodamin B =
19,315 2,5330x50x10
= 65,5708 mcg/g
Kadar Rhodamin pada sampel yang lain dapat dihitung dengan cara yang sama seperti contoh diatas.
Lampiran 9. Analisa Data Statistik untuk Menghitung Kadar Rhodamin B dalam kerupuk Bulat
No Berat
(gram) Absorbansi
X
(Kadar) X −X
(
)
2
X X −
1 19,315 0,4957 65,5708 0,0382 0,00145
2 19,276 0,4948 65,6836 0,0510 0,00260
3 19,358 0,4966 65,5439 0,0113 0,00012
4 19,450 0,4978 65,3933 -0,1393 0,01940
5 19,452 0,4989 65,5331 0,0005 0,00000025
6 19,319 0,4958 65,5711 0,0385 0,00148
X =65,5326
∑
(
X −X)
2=0,0250SD =
(
)
1 2 − −
∑
n X X = 1 6 0,0250 − = 0,0707Pada interval kepercayaan 95% dengan nilai α = 0,05 dan dk = 5 diperoleh nilai
t
tabel =2,5706. Data diterima jikat
hitung<t
tabelt
hitung=n SD X X / −
t
hitung data 1 = 1,3263t
hitung data 2 = 1,7708t
hitung data 3 = 0,3923t
hitung data 4 = 4,8368 (data ditolak)t
hitung data 5 = 0,0173Karena ada data yang
t
hitung >t
tabel maka data itu dihitung kembali dengan carayang sama tanpa mengikutsertakan data yang thitung > t tabel.
No Berat
(gram) Absorbansi
X
(Kadar) X −X
(
)
2
X X −
1 19,315 0,4957 65,5708 0,0103 0,000106
2 19,276 0,4948 65,6836 0,0231 0,000533
3 19,358 0,4966 65,5439 -0,0166 0,000275
5 19,452 0,4989 65,5331 -0,0274 0,000750
6 19,319 0,4958 65,5711 0,0106 0,000112
X = 65,5605
∑
(
X −X)
2=0,001776SD =
(
)
1 2 − −
∑
n X X = 1 5 0,001776 − = 0,0210Pada interval kepercayaan 95% dengan nilai α = 0,05 dan dk = 4 diperoleh nilai
t
tabel =2,7765. Data diterima jikat
hitung <t
tabelt
hitung =n SD X X / −
t
hitung data 1 = 1,1075t
hitung data 2 = 2,4838t
hitung data 3 = 1,7849t
hitung data 5 = 2,9462 (data ditolak)Karena ada data yang
t
hitung >t
tabel maka data itu dihitung kembali dengan carayang sama tanpa mengikutsertakan data yang thitung > t tabel.
No Berat
(gram) Absorbansi
X
(Kadar) X −X
(
)
2
X X −
1 19,315 0,4957 65,5708 0,0035 0,0000122
2 19,276 0,4948 65,6836 0,0163 0,000265
3 19,358 0,4966 65,5439 -0,0234 0,000547
6 19,319 0,4958 65,5711 0,0038 0,0000144
X = 65,5673
∑
(
X −X)
2=0,000838SD =
(
)
1 2 − −
∑
n X X = 1 4 0,000838 − = 0,0167Pada interval kepercayaan 95% dengan nilai α = 0,05 dan dk = 3 diperoleh nilai
t
tabel =3,1824. Data diterima jika thitung <t
tabelt
hitung =n SD X X / −
t
hitung data 1 = 0,4216t
hitung data 2 = 1,9638t
hitung data 3 = 2,8190t
hitung data 6 = 0,4578Semua data diterima maka :
Kadar Rhodamin B (μ) = X ± ( t x SD/ n )
= 65,5763 ± ( 3,1824 x 0,00964)
Lampiran 10. Analisa Data Statistik untuk Menghitung Kadar Rhodamin B dalam Kerupuk Batang
No Berat
(gram) Absorbansi
X
(Kadar) X −X
(
)
2
X X −
1 15,168 0,4242 7,1337 0,0086 0,0000739
2 15,196 0,4249 7,1324 0,0099 0,0000980
3 15,210 0,4257 7,1393 -0,003 0,000009
4 15,189 0,4253 7,1423 -0,0001 0,00000001
5 15,199 0,4261 7,1511 0,0088 0,0000774
6 15,205 0,4265 7,1552 0,0129 0,000166
X =7,1433
∑
(
X −X)
2=0,0004243SD =
(
)
1 2 − −
∑
n X X = 1 6 0,0004243 − = 0,00921Pada interval kepercayaan 95% dengan nilai α = 0,05 dan dk = 5 diperoleh nilai
t
tabel =2,5706. Data diterima jikat
hitung <t
tabelt
hitung =