EFEKTIFITAS PROSES ELEKTROKOAGULASI TERHADAP
PENURUNAN KADAR BESI AIR SUMUR
SKRIPSI
YESA YEMIMA BR SEMBIRING
100802073
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
EFEKTIFITAS PROSES ELEKTROKOAGULASI TERHADAP
PENURUNAN KADAR BESI AIR SUMUR
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
YESA YEMIMA BR SEMBIRING
100802073
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
PERSETUJUAN
Judul :Efektifitas Proses Elektrokoagulasi Terhadap
Penurunan Kadar Besi Air Sumur
Kategori :Seminar Hasil
Nama :Yesa Yemima Br Sembiring
Nomor Induk Mahasiswa :100802073
Program Studi :Sarjana (S1) Kimia
Departemen :Kimia
Fakultas :Matematika dan Ilmu Pengetahuan Alam
Universitas Sumatera Utara
:Disetujui di Medan, Mei 2015
Komisi Pembimbing :
Pembimbing 2, Pembimbing 1,
Dr. Hamonangan Nainggolan, M.Sc Dra.Saur Lumban Raja, M.Si
NIP. 195606241983031002 NIP. 195506231986012002
Disetujui Oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
EFEKTIFITAS PROSES ELEKTROKOAGULASI TERHADAP
PENURUNAN KADAR BESI AIR SUMUR
SKRIPSI
S
aya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.Medan, Mei 2015
PENGHARGAAN
Puji dan syukur penulis ucapkan kepada Tuhan Yang Maha Esa atas berkat dan rahmatNya begitu besar sehingga penulis mampu untuk menyelesaikan tugas akhir ini dengan baik.
Dengan segala kerendahan hati penulis mengucapkan terima kasih yang sebesar-besarnya kepada Ibu Dra. Saur Lumban Raja, M.Si selaku pembimbing I dan Bapak Dr. Hamonangan Nainggolan, M.Sc selaku pembimbing 2 yang telah banyak memberikan arahan selama penyusunan skripsi ini. Terimakasih juga kepada Bapak Prof. Dr. Seri Bima Sembiring, M.Sc selaku Ketua Bidang Kimia Anorganik FMIPA USU dan Bapak Dr. Nimpan Bangun, M.Sc selaku Kepala Laboratorium Kimia Anorganik FMIPA USU yang telah memberikan saran-saran kepada penulis. Terima kasih kepada ibu Dr. Rumondang Bulan, MS dan bapak Albert Pasaribu, M.Sc selaku ketua dan sekretaris Departemen Kimia FMIPA-USU Medan dan seluruh dosen FMIPA-FMIPA-USU yang telah membimbing penulis selama perkuliahan.
Penulis juga mengucapkan terima kasih yang sedalam-dalamnya kepada orang tua saya Atasen Sembiring dan Sehtamalem br Bangun serta Ibu Tina Nainggolan dan Bapak Johnny Seragih yang telah mendoakan, memberikan semangat dan dukungan kepada penulis juga kepada adik-adikku Jusak Bin Berit Sembiring, Jeremia Sembiring dan Benyamin Sembiring. Penulis juga mengucapkan terima kasih kepada Cell Group Leader dan seluruh teman-teman di Bethel dan Harvest serta seluruh teman-teman seperjuangan stambuk 2010.
Penulis menyadari bahwa skripsi ini jauh dari kesempurnaan dan kiranya dapat memberikan manfaat terhadap kemajuan ilmu pengetahuan terutama dalam bidang kimia.
EFEKTIFITAS PROSES ELEKTROKOAGULASI TERHADAP
PENURUNAN KADAR BESI AIR SUMUR
ABSTRAK
Telah dilakukan penelitian dalam air sumur tentang efektifitas proses elektrokoagulasi terhadap penurunan kadar besi. Dalam penelitian ini penurunan kadar besi dilakukan dengan tiga tahap yaitu filtrasi, elektrokoagulasi dan elektrokoagulasi yang disertai dengan filtrasi, dimana proses elektrokoagulasi dilakukan dengan variasi waktu 15, 30, 45 dan 60 menit menggunakan elektroda aluminium. Filtratnya ditambahkan dengan asam nitrat yang bertujuan untuk menghilangkan zat-zat pengganggu yang terdapat dalam sampel dengan bantuan pemanas listrik. Logam Fe dianalisa dengan Spektrofotometer Serapan Atom (SSA). Hasil analisa diperoleh waktu elektrokoagulasi optimum adalah 45 menit, dengan persentasi penurunan kadar Fe yaitu 78,68% dengan kadar Fe : 0,2182 mg/L, selanjutnya proses elektrokoagulasi disertai dengan penyaringan dan diperoleh persentasi penurunan kadar Fe yaitu 85,02% dengan kadar Fe : 0,1533 mg/L. Dari hasil tersebut diperoleh bahwa proses penyaringan (filtrasi) juga berpengaruh pada penurunan kadar logam Fe. Kadar besi yang diperoleh dari hasil penelitian tersebut sudah memenuhi KEPMENKES RI No. 907/MENKES/VII/2002.
Kata kunci : Air Sumur, Elektrokoagulasi, Filtrasi
THE EFFECTIVENESS OF THE ELECTROCOAGULATION
PROCESS TO DECREASE THE IRON CONTENT OF
WATER WELL
ABSTRACT
Research in the well water on the effectiveness of the process of electrolysis to decrease iron levels. In this study, a decrease in the levels of iron carried out in three stages, namely filtration, electrocoagulation and electrocoagulation were accompanied by filtration, where the electrocoagulation process is done with the variation of time 15, 30, 45 and 60 minutes using aluminum electrodes. The filtrate was added with nitric acid which aims to eliminate nuisance substances contained in the sample with the aid of an electric heater. Fe was analyzed by Atomic Absorption Spectrophotometer (AAS). The results of the analysis, the optimum electrolysis time is 45 minutes, with the percentage decrease in Fe content is 78.68% with Fe content: 0.2182 mg / L, further electrocoagulation process is accompanied by filtration and obtained the percentage reduction is 85.02% Fe content with content Fe: 0.1533 mg / L. From the results obtained that the screening process (filtration) also affects the reduction of Fe metal content. Iron content obtained from the results of these studies has met KEPMENKES RI No. 907/MENKES/VII/2002.
DAFTAR ISI
Bab 1. PENDAHULUAN 1.1. Latar Belakang 1
Bab 2. TINJAUAN PUSTAKA 2.1. Air 5
2.2. Sumur Gali 6
2.3. Logam Besi (Fe) 7
2.3.1. Sifat Logam Besi 7
2.3.2. Logam Besi Dalam Air 7 2.3.3. Akibat Kelebihan Konsentrasi Besi Terlarut 9 2.4. Sel Elektrokimia 10
2.7.2. Instrumentasi Spektrofotometer Serapan Atom (SSA) 19
2.7.3. Gangguan pada SSA dan Cara Mengatasinya 21
Bab 3. METODE PENELITIAN 3.1. Alat 22
3.3. Prosedur Penelitian 23
Bab 4. HASIL DAN PEMBAHASAN 4.1. Hasil Penelitian 31
4.1.1. Pengukuran Kadar Besi dari Hasil 31
DAFTAR TABEL
Nomor Judul Halaman
Tabel
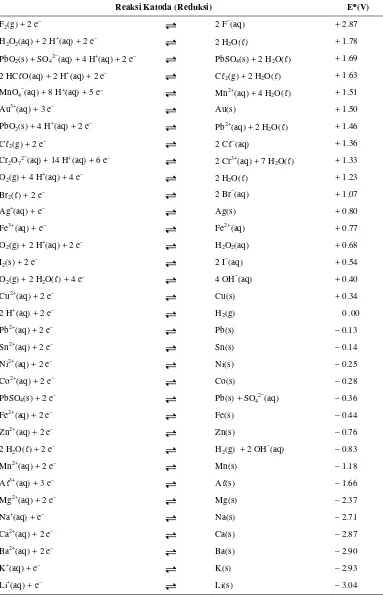
2.1. Potensial Reduksi Standar 12
4.1. Data Absorbansi dari Larutan Seri Standar Besi 31
4.2. Penurunan Persamaan Garis Regresi untuk Penentuan 32 Konsentrasi Besi
4.3. Konsentrasi Awal Logam Besi di dalam Air Sumur 34
4.4. Konsentrasi dan Persentasi Penurunan Logam Besi Hasil 35 Filtrasi Air Sumur
4.5. Konsentrasi dan Persentasi Penurunan Logam Besi Hasil 35 Elektrokoagulasi Air Sumur dengan Variasi Waktu
DAFTAR GAMBAR
Nomor Judul Halaman
Gambar
2.1. Prinsip dari Proses Elektrokoagulasi 13
2.2. Interaksi dalam Proses Elektrokoagulasi 14
2.3. Sistem Peralatan Spektrofotometer Serapan Atom 19
3.4.1. Rangkaian Alat Elektrokoagulasi 26
DAFTAR LAMPIRAN
Nomor Judul Halaman
Lampiran
1. Persyaratan Kualitas Air Minum Menurut 45
KEPMENKES RI No. 907 / MENKES / VII / 2002
2. Alat yang Digunakan Saat Proses Elektrokoagulasi 53
3. Air Sumur Sebelum dan Sesudah Proses Elektrokoagulasi 54
EFEKTIFITAS PROSES ELEKTROKOAGULASI TERHADAP
PENURUNAN KADAR BESI AIR SUMUR
ABSTRAK
Telah dilakukan penelitian dalam air sumur tentang efektifitas proses elektrokoagulasi terhadap penurunan kadar besi. Dalam penelitian ini penurunan kadar besi dilakukan dengan tiga tahap yaitu filtrasi, elektrokoagulasi dan elektrokoagulasi yang disertai dengan filtrasi, dimana proses elektrokoagulasi dilakukan dengan variasi waktu 15, 30, 45 dan 60 menit menggunakan elektroda aluminium. Filtratnya ditambahkan dengan asam nitrat yang bertujuan untuk menghilangkan zat-zat pengganggu yang terdapat dalam sampel dengan bantuan pemanas listrik. Logam Fe dianalisa dengan Spektrofotometer Serapan Atom (SSA). Hasil analisa diperoleh waktu elektrokoagulasi optimum adalah 45 menit, dengan persentasi penurunan kadar Fe yaitu 78,68% dengan kadar Fe : 0,2182 mg/L, selanjutnya proses elektrokoagulasi disertai dengan penyaringan dan diperoleh persentasi penurunan kadar Fe yaitu 85,02% dengan kadar Fe : 0,1533 mg/L. Dari hasil tersebut diperoleh bahwa proses penyaringan (filtrasi) juga berpengaruh pada penurunan kadar logam Fe. Kadar besi yang diperoleh dari hasil penelitian tersebut sudah memenuhi KEPMENKES RI No. 907/MENKES/VII/2002.
Kata kunci : Air Sumur, Elektrokoagulasi, Filtrasi
THE EFFECTIVENESS OF THE ELECTROCOAGULATION
PROCESS TO DECREASE THE IRON CONTENT OF
WATER WELL
ABSTRACT
Research in the well water on the effectiveness of the process of electrolysis to decrease iron levels. In this study, a decrease in the levels of iron carried out in three stages, namely filtration, electrocoagulation and electrocoagulation were accompanied by filtration, where the electrocoagulation process is done with the variation of time 15, 30, 45 and 60 minutes using aluminum electrodes. The filtrate was added with nitric acid which aims to eliminate nuisance substances contained in the sample with the aid of an electric heater. Fe was analyzed by Atomic Absorption Spectrophotometer (AAS). The results of the analysis, the optimum electrolysis time is 45 minutes, with the percentage decrease in Fe content is 78.68% with Fe content: 0.2182 mg / L, further electrocoagulation process is accompanied by filtration and obtained the percentage reduction is 85.02% Fe content with content Fe: 0.1533 mg / L. From the results obtained that the screening process (filtration) also affects the reduction of Fe metal content. Iron content obtained from the results of these studies has met KEPMENKES RI No. 907/MENKES/VII/2002.
BAB 1
PENDAHULUAN
1.1.Latar Belakang
Air merupakan salah satu sumber daya yang penting bagi manusia, karena seluruh
kegiatan manusia sangat berkaitan erat dengan ketersediaan air. Berkurangnya
ketersediaan air bersih merupakan salah satu masalah yang dihadapi banyak
negara termasuk Indonesia, seiring dengan pertambahan penduduk dan aktivitas
manusia yang semakin beragam (Heriani,E., 2014).
Menurut Peraturan Menteri Kesehatan Nomor :
907/MENKES/SK/VII/2002, air bersih adalah air yang digunakan untuk
keperluan sehari-hari yang kualitasnya memenuhi syarat kesehatan yang meliputi
persyaratan mikrobiologi, fisika, kimia, dan radioaktif. Adapun beberapa
parameter kadar maksimum yang diperbolehkan secara kimia anorganik : air raksa
0,001 mg/L, arsen 0,05 mg/L, besi 1,0 mg/L, fluorida 1,5 mg/L, kadnium 0,005
mg/L, kesadahan (CaCO3) 500 mg/L, selenium 0,01 mg/L, seng 15 mg/L, timbal
0,05 mg/L dan pH 6,5-9,0.
Belawan merupakan suatu kawasan industri dan sarana pelabuhan terbesar
di Kota Medan (Juanta,P., 2014). Sebagian kecil masyarakat yang tinggal di
Kecamatan Medan Belawan, masih ada menggunakan air sumur gali untuk
memenuhi kebutuhan air bersih dan air minum walaupun keadaan air sumur gali
pada daerah tersebut memiliki warna yang keruh. Hal ini dikarenakan
keberadaan sarana Perusahaan Daerah Air Minum (PDAM) pada daerah tersebut
Mineral yang sering berada dalam air dengan jumlah besar adalah
kandungan Fe. Apabila Fe tersebut berada dalam jumlah yang banyak akan
muncul berbagai gangguan lingkungan. Unsur besi (Fe) yang berlebih
menimbulkan noda-noda pada peralatan dan bahan pakaian yang berwarna putih.
Unsur Fe dapat menimbulkan bau, warna dan koloid pada air minum
(Widowati,W dkk., 2008).
Menurunkan kadar Fe dalam air sumur dapat dilakukan dengan
menggunakan metode elektrokoagulasi. Elektrokoagulasi adalah proses
penggumpalan dan pengendapan partikel-partikel halus dalam air menggunakan
energi listrik. Elektrokoagulasi membutuhkan peralatan yang sederhana dan
mudah dioperasikan. Proses elektrokoagulasi dilakukan pada bejana elektrolisis
yang didalamnya terdapat dua penghantar listrik yang disebut elektroda, yang
tercelup dalam larutan elektrolit. Elektrokoagulasi bukan merupakan teknologi
baru, dimana teknologi ini ditemukan lebih dari seratus tahun dan merupakan
pengolahan air bersih yang cukup besar di London (Nainggolan,H., 2004).
Telah banyak dilakukan penelitian mengenai metode elektrokoagulasi ini,
seperti; Muhammad Ridwan Harahap (2008) telah meneliti penurunan kadar
logam seng pada air limbah PT. Industri Karet Nusantara, Sofia Novita (2012)
telah melakukan penelitian mengenai pengaruh variasi kuat arus listrik dan waktu
pengadukan untuk penjernihan air baku PDAM Tirtanadi IPA Sunggal dan M.
Adib Fadli dkk (2011) melakukan penelitian mengenai penyisihan kadar COD,
BOD dan warna pada limbah cair industri batik, menggunakan tiga plat elektroda
yaitu aluminium (Al), besi (Fe), dan seng (Zn), yang paling efektif digunakan
untuk menurunkan konsentrasi COD, BOD dan warna dalam limbah cair industri
batik adalah plat elektroda aluminium.
Dalam hal ini, penulis tertarik untuk melakukan penelitian mengenai
pengolahan air bersih khususnya penurunan kadar logam Fe dari air sumur dengan
menggunakan metode elektrokoagulasi dimana plat elektoda yang digunakan
I.2. Permasalahan
Bagaimana pengaruh metode elektrokoagulasi dalam proses pengolahan air bersih
khususnya penurunan kadar logam Fe pada air sumur tanpa penambahan zat
koagulan.
I.3. Pembatasan Masalah
Dalam penelitian ini objek masalah dibatasi sebagai berikut :
1. Air sumur yang digunakan berasal dari daerah Jl. Pulau Halmahera,
Lingkungan 10, Kec.Medan Belawan, KM 20.5.
2. Elektroda yang digunakan adalah elektroda aluminium.
3. Proses elektrokoagulasi dilakukan dengan variasi waktu.
4. Parameter yang di analisa merupakan kandungan kadar logam Fe.
5. Pengujian dilakukan sebelum dan sesudah proses elektrokoagulasi dengan
variasi waktu.
I.4. Tujuan Penelitian
Yang menjadi tujuan dari penelitian ini adalah :
1. Untuk mengetahui proses pengolahan air bersih khususnya penurunan
kadar logam Fe pada air sumur dengan menggunakan metode
elektrokoagulasi.
2. Untuk mengetahui waktu optimum elektrokoagulasi yang digunakan,
sehingga menghasilkan air dengan kadar Fe yang memenuhi syarat air
I.5. Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan informasi bahwa metode
elektrokoagulasi dapat digunakan sebagai pengolahan air bersih khususnya
sebagai penurunan kadar logam Fe pada air sumur.
I.6. Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Analitik FMIPA Universitas Sumatera
Utara. Analisis kadar logam dilakukan di Badan Riset dan Penelitian
(BARISTAN) Medan.
Air sumur diambil dari Daerah Belawan, Kec.Medan Labuhan, Kel.Pekan
Labuhan, KM 20.5
1.7. Metodologi Penelitian
Penelitian ini merupakan penelitian eksperimental laboratorium. Sampel yang
digunakan diambil dari air sumur Belawan. Dalam penelitian ini penurunan kadar
besi dilakukan dengan tiga tahap yaitu filtrasi, elektrokoagulasi dan
elektrokoagulasi yang disertai dengan filtrasi, dimana proses elektrokoagulasi
dilakukan dengan variasi waktu 15, 30, 45 dan 60 menit menggunakan elektroda
aluminium. Filtratnya ditambahkan dengan asam nitrat yang bertujuan untuk
menghilangkan zat-zat pengganggu yang terdapat dalam sampel dengan bantuan
pemanas listrik. Selanjutnya dianalisa kadar logam Fe dengan Spektrofotometri
BAB 2
TINJAUAN PUSTAKA
2.1. Air
Air merupakan sumber daya alam yang sangat penting untuk kehidupan setiap
mahluk hidup di bumi ini. Oleh sebab itu diperlukan sumber air yang mampu
menyediakan air yang baik dari segi kualitas dan kuantitas. Pertumbuhan
penduduk yang begitu pesat, mengakibatkan sumber daya air di dunia menjadi
salah satu kekayaan yang sangat penting. Air merupakan hal pokok bagi konsumsi
dan sanitasi umat manusia, untuk produksi barang industri, serta untuk produksi
makanan, kain dan sebagainya. Namun air tidak tersebar secara merata di atas
permukaan bumi akan tetapi bervariasi (Suripin, M., 2001)
Air di permukaan bumi ini terdiri atas 97% air asin di lautan, 2% masih
berupa es, 0,0009% berupa danau, 0,00009% merupakan air tawar di sungai dan
sisanya merupakan air permukaan yang dapat dimanfaatkan untuk kebutuhan
hiidup manusia, tumbuhan dan hewan yang hidup di daratan. Oleh sebab itu, air
merupakan barang langka yang paling dominan dibutuhkan di permukaan bumi
ini (Nugroho,A., 2006).
Menurut Peraturan Menteri Kesehatan RI No.907/MEN.KES/SK/VII/2002
tanggal 29 Juli 2002 tentang Syarat-Syarat dan Pengawasan Kualitas Air, air
minum adalah air yang melalui proses pengolahan yang memenuhi syarat
kesehatan dan dapat langsung diminum. Persyaratan kesehatan air minum yaitu
2.2. Sumur Gali
Sumur gali adalah satu sarana yang paling umum digunakan oleh masyarakat
kecil untuk mengambil air tanah dangkal dan dipergunakan sebagai sumber air
bersih. Air tanah dangkal adalah air yang paling mudah terkontaminansi oleh
rembesan yang berasal dari sarana pembuangan air kotor, jamban dan kotoran
hewan. Sumur gali umumnya dibuat untuk mengambil air tanah bebas sehingga
sangat dipengaruhi oleh musim (Ompusunggu,H., 2009).
Sumur gali menyediakan air yang berasal dari lapisan tanah yang relatif
dekat dari permukaan tanah, oleh karena itu dengan mudah terkena kontaminasi
melalui rembesan. Umumnya rembesan berasal dari tempat buangan kotoran
manusia kakus/jamban dan hewan, juga dari limbah sumur itu sendiri, baik karena
lantainya maupun saluran air limbahnya yang tidak kedap air (Entjang,I., 2000).
Keadaan konstruksi dan cara pengambilan air sumur pun dapat merupakan
sumber kontaminasi, misalnya sumur dengan konstruksi terbuka dan pengambilan
air dengan timba. Sumur dianggap mempunyai tingkat perlindungan sanitasi yang
baik, bila tidak terdapat kontak langsung antara manusia dengan air di dalam
sumur (Entjang,I., 2000).
Cara pengambilan air tanah yang paling tua dan sederhana adalah dengan
membuat sumur gali dengan kedalaman lebih rendah dari posisi permukaan air
tanah. Jumlah air yang dapat diambil dari sumur gali biasanya terbatas, dan air
yang diambil adalah air dangkal. Untuk pengambilan air yang lebih besar
diperlukan luas dan kedalaman galian yang lebih besar. Kedalaman sumur gali
tergantung lapisan tanah, ketinggian dari permukaan air laut, dan ada tidaknya air
bebas di bawah lapisan tanah. Sumur gali biasanya dibuat dengan kedalaman tidak
lebih dari 5-8 meter di bawah permukaan tanah. Cara ini cocok untuk daerah
pantai dimana air tanah berada di atas air asin (Gabriel,J.F., 2001).
2.3. Logam Besi (Fe)
2.3.1. Sifat-Sifat Logam Besi
Besi (Fe) merupakan logam transisi dan memiliki nomor atom 26. Bilangan
oksidasi Fe adalah +3 dan +2. Fe memiliki berat atom 55,845 g/mol, titik leleh
1.5380 C, dan titik didih 2.8610 C. Fe menempati urutan sepuluh besar sebagai
unsur di bumi. Fe menyusun 5-5,6 dari kerak bumi dan menyusun 35 % dari
massa bumi. Konsentrasi tertinggi terdapat pada lapisan dalam dari inti bumi dan
sejumlah kecil terdapat di lapisan terluar kerak bumi. Beberapa tempat di bumi
bisa mengandung Fe mencapai 70%. Logam Fe ditemukan dalam inti bumi berupa
hematit. Fe hampir tidak dapat ditemukan sebagai unsur bebas. Fe diperoleh
dalam bentuk tidak murni sehingga harus melalui reaksi reduksi guna
mendapatkan Fe murni. Fe ditemukan terutama sebagai mineral hematit (Fe2O3);
magnetit (Fe3O4); mineral lain yang merupakan sumber Fe adalah limonit
[FeO(OH)nH2O], siderit (FeCO3), dan takonit (Widowati,W dkk., 2008).
Logam besi memiliki warna putih keperakan, yang kukuh dan liat. Asam
klorida encer atau pekat dan asam sulfat encer dapat melarutkan besi.
Fe(s) + 2HCl(aq)→ Fe2+(aq) + 2Cl-(aq) + H2↑(g)
2Fe(s) + 3H2SO4(aq) + 6H+(aq) → 2Fe3+(aq) + 3SO2↑(g) +6H2O(l)
Dengan asam nitrat encer dingin, terbentuk ion besi (II) dan amonia :
4Fe(s) + 10H+(aq) + NO-3(aq) → 4Fe2+(aq) + NH4+(aq) + 3H2O(l)
Asam nitrat pekat yang panas dapat melarutkan besi dengan membentuk gas
nitrogen oksida dan ion besi (III) :
Fe(s) + HNO3(aq) + 3H+(aq) → Fe3+(aq) + NO↑(g) + 2H2O(l) (Svehla,G.,1979)
2.3.2. Logam Besi Dalam Air
Mineral yang sering berada dalam air dengan jumlah besar adalah kandungan Fe.
Apabila Fe tersebut berada dalam jumlah yang banyak akan muncul berbagai
aktivitas industri. Besi dalam air tanah bisa berbentuk Fe(II) dan Fe(III) terlarut
(Widowati,W dkk., 2008). Pada umumnya, besi yang ada di dalam air dapat
bersifat :
a. terlarut sebagai Fe2+ (ferro) atau Fe3+ (ferri) ;
b. tersuspensi sebagai butir koloidal (diameter < 1 mikrometer) atau lebih
besar ;
c. tergabung dengan zat organis atau zat padat yang inorganis (seperti tanah liat)
(Nainggolan,H., 2011).
Perairan yang mengandung besi tidak diinginkan untuk keperluan rumah
tangga, karena dapat menyebabkan bekas karat pada pakaian, porselin dan
alat-alat lainnya serta menimbulkan rasa yang tidak enak untuk air minum. Besi (II)
sebagai ion berhidrat dapat larut, merupakan jenis besi yang terdapat dalam air
tanah, karena air tanah tidak berhubungan dengan oksigen dari atmosfer,
konsumsi oksigen bahan organik dalam media mikroorganisme akan
menghasilkan keadaan reduksi dalam air tanah. Oleh karena itu, besi dengan
bilangan oksidasi rendah yaitu Fe(II) umumnya ditemukan dalam air tanah
dibandingkan Fe(III). Secara umum Fe(II) terdapat dalam air tanah berkisar antara
1,0-10 mg/L, dalam kondisi tidak ada oksigen air tanah mengandung Fe(II) jernih
tetapi saat mengalami oksidasi oleh oksigen yang berasal dari atmosfer ion ferro
akan berubah menjadi ion ferri (Effendi, 2003).
Kadar besi pada perairan yang mendapat cukup aerasi (aerob) hampir tidak
pernah lebih dari 0,3 mg/l, kadar besi pada perairan alami berkisar 0,05-0,2 mg/l.
Pada air tanah dengan kadar oksigen yang rendah, kadar besi dapat mencapai 10-
100 mg/l. Kadar besi >1,0 mg/l dianggap membahayakan kehidupan organisme
akuatik. Air yang diperuntukkan untuk air minum sebaiknya memiliki kadar besi
2.3.3. Akibat Kelebihan Konsentrasi Besi Terlarut
Apabila kosentrasi besi terlarut dalam air melebihi batas, akan menyebabkan
berbagai masalah, diantaranya :
1. Gangguan teknis
Endapan Fe(OH) bersifat korosif dapat mengendap pada saluran pipa, sehingga
mengakibatkan clogging dan mengotori bak/wastafel/kloset.
2. Gangguan fisik
Gangguan fisik yang ditimbulkan oleh adanya besi terlarut dalam air adalah
timbulnya warna, bau dan rasa. Air akan terasa tidak enak bila konsentrasi besi
terlarutnya > 1,0 mg/L karena dapat menyebabkan air berbau seperti telur busuk.
3. Gangguan kesehatan
Senyawa besi dalam jumlah kecil di dalam tubuh manusia berfungsi sebagai
pembentuk sel-sel darah merah, dimana tubuh memerlukan 7–35 mg/hari yang
sebagian diperoleh dari air.
Namun zat Fe yang berlebih pada tubuh dapat menimbulkan masalah bagi
kesehatan, beberapa diantaranya yaitu :
a. Air minum yang mengandung besi cenderung menimbulkan rasa mual
apabila dikonsumsi.
b. Kadar Fe yang besar dapat merusak dinding usus. Kematian sering kali
disebabkan oleh rusaknya dinding usus ini.
c. Kadar Fe > 1 mg/L akan menyebabkan terjadinya iritasi pada mata dan
kulit.
d. Hemokromatesis primer besi akibat dari penyerapan Fe dalam jumlah
berlebih di dalam tubuh. Feritin berada dalam keadaan jenuh akan besi
sehingga kelebihan mineral ini akan disimpan dalam bentuk kompleks
dengan mineral lain yaitu hemosiderin. Akibatnya terjadilah sirosis hati
dan kerusakan pankreas sehingga menimbulkan diabetes (Widowati,W
2.4. Sel Elektrokimia
Sel elektrokimia adalah sel yang menghasilkan transfer bentuk energi listrik
menjadi energi kimia atau sebaliknya, melalui saling interaksi antara arus listrik
dan reaksi redoks (Hiskia,A.,1992).
Reaksi redoks merupakan akibat dari aliran arus listrik yang diberikan dan
berlangsung pada bagian yang disebut elektroda. Pertemuan antara dua fase
dengan komposisi yang berlainan akan menyebabkan perbedaaan potensial antara
dua fase tersebut, sehingga terjadi pemisahan muatan listrik. Transfortasi muatan
listrik antar fase dapat terjadi pada fase elektrolit dan fase elektroda. Elektroda
adalah fase tempat muatan listrik dibawa oleh gerakan elektron. Sedangkan
elektrolit adalah fase tempat muatan listrik dibawa oleh gerakan ion – ion
(Hiskia,A.,1992).
Secara umum sel elektrokimia didefinisikan sebagai 2 elektroda yang
dipisahkan oleh paling sedikit satu fase elektrolit. Elektroda tempat terjadinya
oksidasi disebut anoda dan elektroda tempat terjadinya reduksi disebut katoda.
Oksidasi yaitu suatu perubahan kimia, jika :
a.Suatu zat memberikan atau melepaskan elektron
b.Suatu unsur mengalami pertambahan bilangan oksidasi atau tingkat oksidasi
c.Terjadi pada anoda atau elektroda positif suatu sel elektrokimia
Reduksi ialah suatu perubahan kimia, jika :
a.Suatu zat menangkap atau menerima elektron
b.Suatu unsur mengalami pengurangan bilangan oksidasi atau tingkat oksidasi
c.Terjadi pada katoda atau elektroda negatif suatu sel elektrokimia
2.5. Potensial Elektroda
Suatu reaksi reduksi dapat menimbulkan potensial listrik tertentu yang disebut
potensial elektroda (E0). Makin mudah suatu unsur mengalami reduksi, makin
besar E0 yang ditimbulkannya. Terdapat perbedaan potensial antara dua elektroda
pada kondisi ada arus ataupun tidak ada arus. Dengan membuat potensial
elektroda lebih negatif, energi elektron akan meningkat dan akan mencapai tingkat
yang cukup untuk mengisi keadaan kosong pada spesi dalam elektrolit. Dalam hal
ini terjadi aliran elektron dari elektroda ke larutan sehingga menimbulkan arus
reduksi. Sedangkan dengan membuat potensial elektroda lebih positif, energi
elektroda dapat direndahkan. Beberapa titik elektron dalam larutan elektrolit akan
mencari energi yang lebih sesuai pada elektroda dan menyebabkan terjadinya
perpindahan elektron dari larutan elektrolit ke elektroda sehingga menimbulkan
arus oksidasi (Putra,M., 2000).
Harga E0 yang dipakai adalah harga E0 relatif yang dibandingkan terhadap
suatu elektroda standar sehingga disebut harga E0 yaitu potensial elektroda
standar. Sebagai standar dalam menentukan E0 adalah elektroda hidrogen. Gas
hidrogen murni dialirkan pada elektroda platina yang bersentuhan dengan larutan
asam (H+). Pada permukaan platina terdapat kesetimbangan :
2H+ + 2e H2
Harga E0 pada reaksi ini ditetapkan 0 Volt. Harga E0 dari semua reaksi reduksi
adalah harga yang dibandingkan terhadap E0 Hidrogen ( Putra,M., 2000).
Berdasarkan harga E0 yang tercantum dalam daftar, disusun suatu deret
unsur yang disebut deret potensial logam (deret volta) mulai dari
unsur-unsur yang memiliki E0 terkecil sampai kepada unsur yang memiliki E0 terbesar
(Putra,M., 2000).
Reaksi katoda atau reduksi ditunjukkan dalam tabel 2.1. Dalam hal ini,
apabila elektroda bertindak sebagai anoda dan menjalani oksidasi, maka reaksinya
Tabel 2.1. Potensial Reduksi Standar (Keenan,C.W., 1999)
Reaksi Katoda (Reduksi) E°(V)
2.6. Elekrokoagulasi
Elektrokoagulasi adalah proses penggumpalan dan pengendapan partikel-partikel
halus dalam air menggunakan energi listrik. Proses elektrokoagulasi dilakukan
pada bejana elektrolisis yang didalamnya terdapat dua penghantar arus listrik
searah yang disebut elektroda, yang tercelup dalam larutan limbah sebagai
elektrolit.
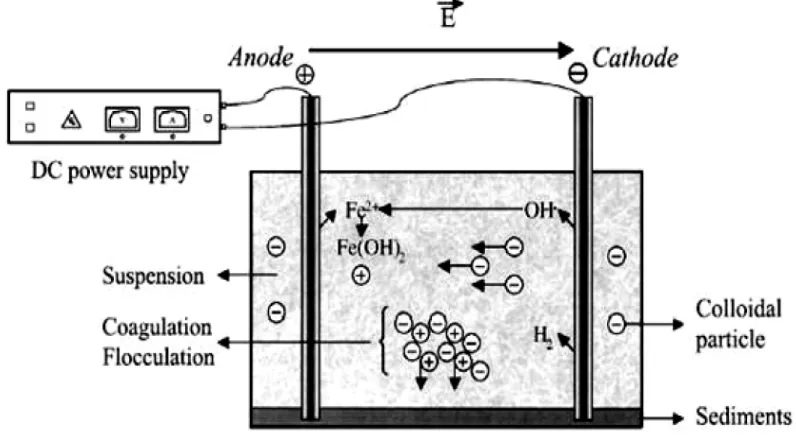
Gambar 2.1 Prinsip dari Proses Elektrokoagulasi (Ni’am,M.F., 2007)
Apabila dalam suatu larutan elektrolit ditempatkan dua elektroda dan
dialiri arus listrik searah, maka akan terjadi peristiwa elektrokimia yaitu gejala
dekomposisi elektrolit, yaitu ion positif (kation) bergerak ke katoda dan menerima
elektron yang di reduksi dan ion negatif (anion) bergerak ke anoda
danmenyerahkan elektron yang dioksidasi. Sehingga membentuk flok yang
mampu mengikat kontaminan dan partikel-partikel dalam limbah (Sutrisno.T.,
1987).
Elektrokoagulasi dikenal juga sebagai elektrolisis gelombang pendek.
air. Itu dapat digunakan menjadi sebuah uji nyata dengan proses yang sangat
efektif untuk pemindahan bahan pengkontaminasi di dalam air. Proses ini dapat
mengurangi lebih dari 99% kation logam berat. Pada dasarnya sebuah elektroda
logam akan teroksidasi dari logam M menjadi kation (M+). Selanjutnya, air akan
direduksi menjadi gas hidrogen dan ion hidroksil (OH). Elektrokoagulasi ini
dikenal sebagai reaksi in situ kation logam (Holt,P.K. et al, 2006).
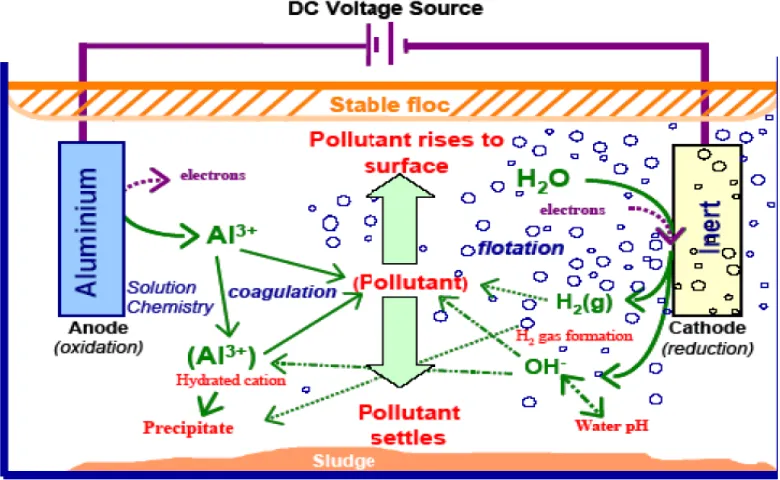
Gambar 2.2. Interaksi Dalam Proses Elektrokoagulasi (Holt,P.K. et al, 2006).
Interaksi yang terjadi dalam larutan :
a. Migrasi menuju muatan elektroda yang berlawanan (elektroporesis) dan
netralisasi muatan.
b. Kation atau ion hidroksil membentuk sebuah endapan dengan pengotor.
c. Interaksi kation logam dengan OH- membentuk sebuah hidroksida, dengan sifat
adsorpsi yang tinggi selanjutnya berikatan dengan pollutan (bridge
coagulation).
d. Senyawa hidroksida yang terbentuk membentuk gumpalan (flok) yang lebih
besar .
f. Sesudah flok terjadi, gas H2 membantu Flotasi dengan membawa polutan
kelapisan buih flok di permukaan cairan (Holt,P.K. et al, 2006).
Reaksi yang terjadi pada proses ini adalah :
a. Reaksi pada Katoda
Reaksi pada katoda adalah reduksi terhadap kation, jadi yang diperhatikan hanya
kation saja.
1.Jika larutan mengandung ion- ion logam alkali, ion – ion logam alkali tanah, ion
Al3+ dan ion Mg2+, maka ion – ion logam ini tidak dapat direduksi larutan. Yang
akan mengalami reduksi adalah pelarut (air) dan terbentuk gas hidrogen (H2) pada
katoda. Reaksi yang terjadi di katoda tergantung pada pH air yang diolah. Pada
kondisi netral atau basa, gas hidrogen terjadi dengan reaksi :
2H2O(l) + 2e− → 2OH−(aq) + H2(g) E0 = -0,83 V
Dari daftar E0 diketahui bahwa reduksi terhadap air lebih mudah berlangsung dari
pada reduksi terhadap ion – ion diatas.
2.Sedangkan pada kondisi asam, reaksi pembentukan gas hidrogen adalah sebagai
berikut :
2H+(aq) + 2e−→ H2(g) E0 = 0,00 V
3.Jika larutan mengandung ion – ion lain, maka ion – ion logam ini akan direduksi
menjadi masing – masing logamnya dan logam yang terbentuk itu diendapkan
pada permukaan bidang katoda (Holt,P.K. et al, 2006).
Contoh :
Fe2+(aq) + 2e− → Fe(s) E0 = -0,44 V
Mn2+(aq) + 2e− → Mn(s) E0 = -1,18 V
b.Reaksi pada Anoda
Elektroda pada anoda, elektrodanya diketahui dioksidasi (bereaksi) diubah
menjadi ionnya.
Contoh :
Al(s) → Al3+(aq) + 3e− E0 = +1,66 V
Dalam sistem elektrokimia dengan anoda terbuat dari aluminium, beberapa
kemungkinan reaksi elektroda dapat terjadi sebagai berikut :
Anoda :
Flokulasi adalah penggabungan dari partikel-partikel hasil koagulasi menjadi
partikel yang lebih besar dan mempunyai kecepatan mengendap yang lebih besar,
dengan cara pengadukan lambat. Dalam hal ini proses koagulasi harus diikuti
flokulasi yaitu penggumpalan koloid terkoagulasi sehingga membentuk flok yang
mudah terendapkan atau transportasi partikel tidak stabil, sehingga kontak antar
partikel dapat terjadi (Sutrisno,T., 1987).
Koloid yang tidak stabil cenderung untuk menggumpal, walaupun
kecepatan penggumpalannya sangat lambat. Kecepatan penggumpalan ini
ditentukan oleh banyaknya kontak antar partikel koloid dan efektifitas kontak
yang terjadi karena:
a. Gerak Brown (perikinetik)
b. Gradien kecepatan dalam media suspensi (ortokinetik) yang bergantung pada
temperatur, kecepatan aliran air, jumlah partikel koloid, konsentrasi dan ukuran
2.6.2. Koagulasi
Koagulasi adalah proses destabilisasi partikel – partikel koloid. Partikel – partikel
tersebut membentuk lapisan secara kimia yang kemudian diikuti dengan flokulasi.
Zat – zat kimia yang digunakan untuk mendestabilkan partikel koloid disebut
dengan koagulan. Koagulan yang paling umum dan paling sering digunakan
adalah alum (aluminium sulfat) dan garam – garam besi. Karakteristik dari kation
multivalensi adalah mempunyai kemampuan menarik koagulan ke muatan partikel
koloid (Proste,R.L., 1997).
Pada dasarnya proses koagulasi dapat dilakukan dengan dua cara, yaitu
cara kimia dan cara fisika. Koagulasi cara kimia yaitu proses penjernihan air
dilakukan dengan memberikan penambahan bahan kimia sebagai koagulan
berbentuk garam (aluminium sulfat) untuk mempercepat terjadinya pembentukan
flok yang dapat diendapkan. Sedangkan koagulasi secara fisika yang sering
dinamakan dengan elektrokoagulasi merupakan metode pengolahan air secara
elektrokimia dimana pada anoda terjadi pelepasan koagulan aktif berupa ion
logam (biasanya aluminium atau besi) ke dalam larutan, sedangkan pada katoda
terjadi reaksi elektrolisis berupa pelepasan gas hidrogen (Holt,P.K. et al, 2006).
2.6.3. Kelebihan Elektrokoagulasi
Adapun kelebihan dari elektrokoagulasi yaitu :
a. Elektrokoagulasi memerlukan peralatan sederhana dan mudah untuk
dioperasikan.
b. Elektrokoagulasi lebih cepat mereduksi kandungan partikel-partikel koloid
yang paling kecil, hal ini disebabkan pengaplikasian listrik kedalam air akan
mempercepat pergerakan partikel-partikel koloid didalam air dengan demikian
akan memudahkan proses.
c. Gelembung-gelembung gas yang dihasilkan pada proses elektrokoagulasi ini
d. Dapat memberikan efisiensi proses yang cukup tinggi untuk berbagai kondisi,
dikarenakan tidak dipengaruhi temperatur.
e. Tidak diperlukan pengaturan pH.
f. Tanpa menggunakan bahan kimia tambahan.
g. Endapan yang terbentuk dari proses elektrokoagulasi lebih mudah dipisahkan
dari air.
h. Dapat memindahkan partikel – partikel koloid yang lebih kecil.
I. Dapat diatur arus listriknya (Purwaningsih,I., 2008).
2.6.4. Kekurangan Elektrokoagulasi
Selain kelebihan, elektrokoagulasi juga memiliki beberapa kekurangan yaitu :
a. Tidak dapat digunakan untuk mengolah cairan yang mempunyai sifat elektrolit
kuat dikarenakan akan terjadi hubungan singkat antar elektroda.
b. Besarnya reduksi logam berat dalam cairan dipengaruhi oleh besar kecilnya
arus voltase listrik searah pada elektroda, luas sempitnya bidang kontak
elektroda dan jarak antar elektroda.
c. Elektrodanya dapat terlarut sehingga dapat mengakibatkan terjadinya oksidasi.
d. Penggunaan listrik yang mungkin mahal.
e. Batangan anoda yang mudah mengalami korosi sehingga harus selalu diganti
(Purwaningsih,I., 2008).
2.7. Spektrofotometer Serapan Atom (SSA)
Spektrofotometri Serapan Atom (SSA) adalah spektrofotometri atom yang lebih
melibatkan pada proses penyerapan panjang gelombang yang dipancarkan oleh
suatu unsur atom yang dilewatkan melalui gas pembakar. Dalam beberapa tahun
terakhir ini, SSA telah menjadi salah satu teknik analisis yang banyak digunakan.
Pada kenyataannya, dapat kita katakan bahwa SSA digunakan untuk menganalisa
2.7.1. Prinsip Spektrofotometer Serapan Atom (SSA)
Prinsip dasar spektrofotometer serapan atom dimana jika suatu larutan yang
mengandung suatu senyawa logam dihembuskan kedalam suatu nyala (misalnya
asitilena yang terbakar di udara), dapat terbentuk uap yang mengandung atom –
atom logam itu. Beberapa atom logam dalam gas ini dapat dieksitasi ke tingkat
energi yang lebih tinggi yang cukup tinggi untuk memungkinkan pemancaran
radiasi yang karakteristik dari logam tersebut. Tetapi jumlah jauh lebih besar dari
atom logam bentuk gas itu normalnya tetap berada dalam keadaan tak tereksitasi
atau dengan perkataan lain dalam keadaan dasar. Atom – atom kedaan dasar ini
mampu menyerap energi cahaya yang panjang gelombang resonansinya khas
untuknya, yang pada umumnya adalah panjang gelombang radiasi yang akan
dipancarkan atom – atom itu bila tereksitasi dari keadaan dasar. Jadi jika cahaya
dengan panjang gelombang resonansi itu dilewatkan nyala yang mengandung
atom – atom yang bersangkutan, maka sebagian cahaya itu akan diserap dan jauh
penyerapan akan berbanding lurus dengan banyaknya atom keadaan dasar yang
berada dalam keadaan nyala (Mulja,J.C., 1991) .
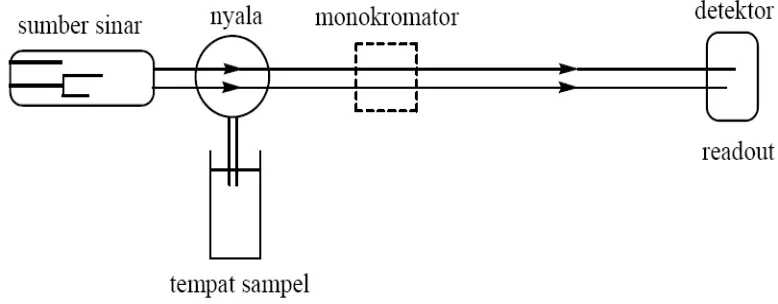
2.7.2. Instrumentasi Spektrofotometer Serapan Atom
Sistem peralatan spektrofotometer serapan atom dapat dilihat pada gambar berikut
ini:
1. Sumber sinar
Sumber sinar yang lazim dipakai adalah lampu katoda berongga. Lampu ini terdiri
atas tabung kaca tertutup yang mengandung suatu katoda dan anoda. katoda
sendiri berbentuk silinder berongga yang terbuat dari logam atau dilapisi dengan
logam tertentu. Tabung logam ini diisi dengan gas mulia (neon atau argon)
dengan tekanan rendah (Rohman,A., 2007).
2. Tempat sampel
Dalam analisis, sampel yang akan dianalisis harus diuraikan menjadi atom-atom
yang masih dalam keadaan atas. Ada beberapa macam alat yang dapat digunakan
untuk mengubah suatu sampel menjadi uap atom-atom yaitu dengan nyala dan
tanpa nyala.
a. Nyala (Flame)
Nyala digunakan untuk mengubah sampel yang berupa padatan atau cairan
menjadi bentuk uap atomnya, dan juga berfungsi untuk atomisasi
b. Tanpa Nyala (Flameless)
Pengatoman dapat dilakukan dalam tungku dari grafit, kemudian tabung
tersebut dipanaskan dengan system elektris dengan cara melewatkan arus
listrik grafit.. Akibat pemanasan ini, maka zat yang akan dianalisis
berubah menjadi atom-atom netral. (Rohman,A., 2007).
3. Monokromator
Monokromator memisahkan, mengisolasi, dan mengontrol intensitas dari radiasi
energi yang mencapai detector.(Haswell,S.J., 1991).
4. Detektor
Detektor pada spektrofotometer serapan atom berfungsi mengubah intensitas
radiasi yang akan datang menjadi arus listrik. Pada spektrofotometer serapan atom
yang umum dipakai sebagai detektor adalah tabung penggandaan foton
5. Readout
Sistem pencatat yang digunakan pada instrument SSA berfungsi untuk mengubah
sinyal yang diterima melalui bentuk digital, berarti system pencatat menengah
atau mengurangi kesalahan dalam pembacaan skala dan sebagainya, serta
menyeragamkan tampilnya data, yaitu dalam satuan absorbansi (Haswell,S.J.,
1991).
2.7.3. Gangguan Pada SSA dan Cara Mengatasinya
Sampel dalam bentuk molekul karena disosiasi yang tidak sempurna akan
cenderung mengabsorpsi radiasi dari sumber radiasi. Demikian juga terjadinya
ionisasi atom akan menjadi sumber kesalahan pada SSA oleh karena spektrum
radiasi oleh ion jauh berbeda dengan spektrum absorpsi atom netral yang memang
akan ditentukan (Mulja,J.C., 1991).
Ada beberapa cara untuk mengurangi gangguan kimia pada SSA yaitu:
1. Menaikkan temperatur nyala agar mempermudah penguraian untuk itu dipakai
gas pembakar campuran C2H2 + N2O yang memberikan nyala dengan
temperatur yang tinggi.
2. Menambahkan elemen pengikat gugus atom penyangga, sehingga terikat kuat
akan tetapi atom yang ditentukan bebas sebagai atom netral. Misalnya,
penentuan logam yang terikat sebagai garam, dengan penambahan logam, yang
lainnya akan terjadi ikatan lebih kuat dengan anion pengganggu.
3. Pengeluaran unsur pengganggu dari matriks sampel dengan cara eksitasi.
BAB 3
METODE PENELITIAN
3.1. Alat
Gelas Beaker 1000 mL Pyrex
Gelas Ukur 50 mL Pyrex
Adaptor 3-13,8 V/10A Super
Kabel Tembaga
Stowatch
Lempengan Aluminium
Hotplate Stirer Cimarec
Pipet Tetes
Penjepit Buaya
Spektrofotometer Serapan Atom Varian AA 240 FS
Selang Infus
Labu Takar 100 mL Pyrex
pH meter
3.2. Bahan
Air Sumur
Ijuk
Kerikil
Pasir
HNO3 (p) p.a. E’Merck
3.3. Prosedur Penelitian
3.3.1. Pembuatan Larutan Standar Logam Besi
3.3.1.1. Pembuatan Larutan Standar Logam Besi 100 mg/L
Sebanyak 10 mL larutan induk logam besi 1000 mg/L dimasukkan ke dalam labu
takar 100 mL lalu diencerkan dengan akuades sampai garis batas dan diaduk
sampai homogen.
3.3.1.2. Pembuatan Larutan Standar Logam Besi 10 mg/L
Sebanyak 10 mL larutan induk logam besi 100 mg/L dimasukkan ke dalam labu
takar 100 mL lalu diencerkan dengan akuades sampai garis batas dan diaduk
sampai homogen.
3.3.1.3. Pembuatan Larutan Standar Logam Besi 1 mg/L
Sebanyak 10 mL larutan induk logam besi 10 mg/L dimasukkan ke dalam labu
takar 100 mL lalu diencerkan dengan akuades sampai garis batas dan diaduk
sampai homogen.
3.3.1.4. Pembuatan Larutaan Seri Standar Logam Besi
Sebanyak 25 mL; 50 mL; 75 mL; 100 mL; dan 125 mL larutan induk logam besi
1 mg/L dimasukkan ke dalam 5 buah labu takar 100 mL lalu kemudian
diencerkan dengan akuades sampai garis tanda dan diaduk hingga homogen
sehingga diperoleh larutan seri standar logam besi 0,25 mg/L; 0,50 mg/L; 0,75
3.3.1.5. Pembuatan Kurva Kalibrasi Logam Besi
Larutan seri standar logam besi 0,25 mg/L diukur absorbansinya pada panjang
gelombang 248,3 nm. Perlakuan hal yang sama dilakukan terhadap larutan seri
standar 0,50 mg/L; 0,75 mg/L; 1,00 mg/L; dan 1,25 mg/L. (SNI 06-6989-5-2004)
3.3.2. Perlakuan Terhadap Sampel
a. Sebanyak 1 L sampel dimasukkan ke dalam gelas Beaker, kemudian
dialirkan ke dalam wadah yang berisikan pasir, ijuk dan kerikil. Sebanyak
100 mL filtratnya dimasukkan kedalam gelas Beaker sebanyak 100 mL,
ditambahkan 5 mL HNO3 (p) dan diuapkan hingga sampel hampir habis.
Selanjutnya ditambahkan 50 mL aquadest dan dibuat pH sampai 3.
Kemudian dimasukkan kedalam labu takar 100 mL. Lalu diencerkan
dengan aquadest hingga garis batas dan dihomogenkan. Selanjutnya
dianalisa logam Fe dengan Spektrofotometer Serapan Atom (SSA).
b. Sebanyak 1 L sampel dimasukkan ke dalam gelas beaker,
dielektrokoagulasi selama 15 menit kemudian didiamkan selama ±30
menit lalu dimasukkan sebanyak 100 mL ke dalam gelas Beaker kemudian
ditambahkan 5 mL HNO3 (p) dan diuapkan hingga sampel hampir habis.
Selanjutnya ditambahkan 50 mL aquadest dan dibuat pH sampai 3.
Kemudian dimasukkan ke dalam labu takar 100 mL. Lalu diencerkan
dengan aquadest hingga garis batas dan dihomogenkan. Selanjutnya
dianalisa logam Fe dengan Spektrofotometer Serapan Atom (SSA) . Hal
c. Sebanyak 1 L sampel dimasukkan ke dalam gelas Beaker,
dilektrokoagulasi selama 15 menit kemudian didiamkan selama ±30 menit
dan dialirkan ke dalam wadah yang berisikan pasir, ijuk dan kerikil.
Sebanyak 100 mL filtratnya dimasukkan ke dalam gelas Beaker lalu
ditambahkan 5 mL HNO3 (p) dan diuapkan hingga sampel hampir habis.
Selanjutnya ditambahkan 50 mL aquadest dan dibuat pH sampai 3.
Kemudian dimasukkan ke dalam labu takar 100 mL. Lalu diencerkan
dengan aquadest hingga garis batas dan dihomogenkan. Selanjutnya
dianalisa logam Fe dengan Spektrofotometer Serapan Atom (SSA). Hal
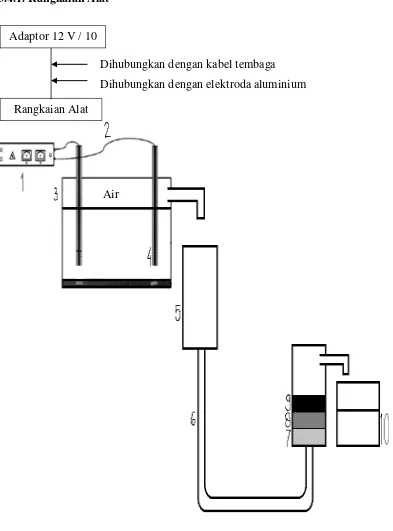
3.4. Bagan Penelitian 3.4.1. Rangkaian Alat
Dihubungkan dengan kabel tembaga
Dihubungkan dengan elektroda aluminium
Air
Gambar 3.4.1 Rangkaian alat elektrokoagulasi Rangkaian Alat
Keterangan:
1. Sumber tegangan
2. Kabel tembaga
3. Wadah + Air
4. Elektroda
5. Wadah
6. Selang
7. Pasir
8. Ijuk
9. Kerikil
3.4.2. Air Sumur dengan Penyaringan
Dialirkan ke dalam wadah yang berisikan
pasir, ijuk dan kerikil
Dimasukkan kedalam gelas
Beaker sebanyak 100 mL
Ditambahkan 5 mL HNO3 (p)
Diuapkan hingga sampel hampir
habis
Ditambahkan 50 mL aquadest
Dibuat pH sampai 3
Dimasukkan kedalam labu takar
100 mL
Diencerkan dengan aquadest
hingga garis batas
Dihomogenkan
Dianalisa kadar logam Fe dengan
Spektrofotometer Serapan Atom
(SSA)
1L Air Sumur
Filtrat Filtrat
3.4.3. Elektrokoagulasi Air Sumur tanpa Penyaringan
Dimasukkan ke dalam gelas Beaker
Dielektrokoagulasi* selama 15 menit
Didiamkan selama ±30 menit
Dimasukkan kedalam gelas Beaker
sebanyak 100 mL
Ditambahkan 5 mL HNO3 (p)
Diuapkan hingga sampel hampir habis
Ditambahkan 50 mL aquadest
Dibuat pH sampai 3
Dimasukkan kedalam labu takar 100 mL
Diencerkan dengan aquadest hingga garis
batas
Dihomogenkan
Dianalisa kadar logam Fe dengan
Spektrofotometer Serapan Atom (SSA)
*Catatan: dilakukan hal yang sama untuk variasi waktu 30, 45 dan 60 menit. 1L Air Sumur
3.4.4. Elektrokoagulasi Air Sumur dengan Penyaringan
Dimasukkan ke dalam gelas Beaker
Dielektrokoagulasi* selama 15 menit
Didiamkan selama ±30 menit
Dialirkan ke dalam wadah yang berisikan
pasir, ijuk dan kerikil
Dimasukkan kedalam gelas
Beaker sebanyak 100 mL
Ditambahkan 5 mL HNO3 (p)
Diuapkan hingga sampel hampir
habis
Ditambahkan 50 mL aquadest
Dibuat pH sampai 3
Dimasukkan kedalam labu takar
100 mL
Diencerkan dengan aquadest
hingga garis batas
Dihomogenkan
Dianalisa kadar logam Fe dengan
Spektrofotometer Serapan Atom
(SSA)
*Catatan: dilakukan hal yang sama untuk variasi waktu 30, 45 dan 60 menit. 1L Air Sumur
Residu Filtrat
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
4.1.1. Pengukuran Kadar Besi dari Hasil Elektrokoagulasi Air Sumur
Kurva kalibrasi larutan standar untuk penentuan kandungan logam besi (Fe)
dalam air sumur dilakukan dengan membuat larutan standar Fe dengan berbagai
konsentrasi yaitu 0,25; 0,50; 0,75; 1,0; 1,25 mg/L dan diukur intensitasnya dengan
alat SSA. Data intensitas untuk larutan standar Fe dapat dilihat pada Tabel 4.1 di
bawah ini.
Tabel 4.1. Data Absorbansi dari Larutan Seri Standar Besi
Konsentrasi (ppm) Absorbansi(nm)
0,2500
4.1.1.1. Penurunan Persamaan Garis Regresi
Hasil pengukuran absorbansi seri larutan standar besi pada tabel 4.1 diplotkan
terhadap konsentrasi larutan standar sehingga diperoleh suatu kurva kalibrasi
berupa garis linear yang diturunkan dengan metode Least Square dengan
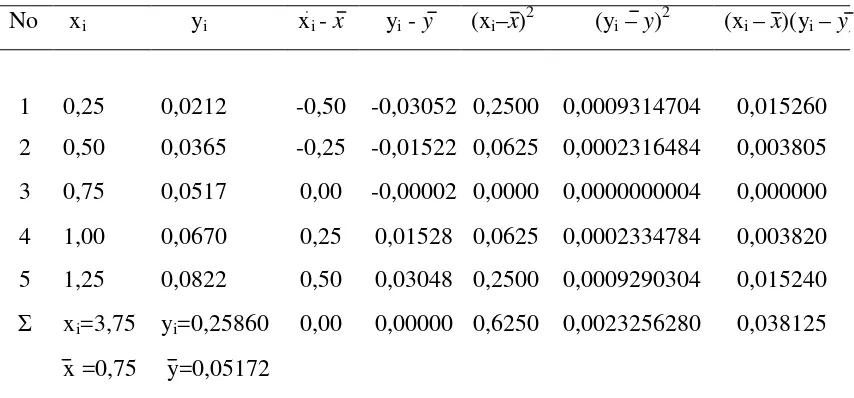
Tabel 4.2. Penurunan Persamaan Garis Regresi untuk Penentuan Konsentrasi Besi
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan
garis :
y = ax + b
Dimana : a = slope
b = intersept
Selanjutnya harga slope dapat ditentukan dengan menggunakan metode Least
Square sebagai berikut :
a = ∑(xi−x�)(yi−y�)
∑(xi−x) 2
=0,038125
0,6250
= 0,061
Harga intersept (b) diperoleh melalui substitusi harga (a) ke persamaan berikut :
Sehingga diperoleh harga intersept (b) = 0,0034
Maka persamaan garis regresi adalah:
y = 0,061x + 0,006
4.1.1.2. Menghitung Koefisien Korelasi (R)
R = ∑(xi−x)�yi− y�
Sehingga diperoleh harga koefisien korelasi (R) = 0,9999
Setelah diperoleh persamaan garis regresi dan koefisien relasi (R) pada
pengukuran larutan standar maka absorbansi dari larutan standar Fe diplotkan
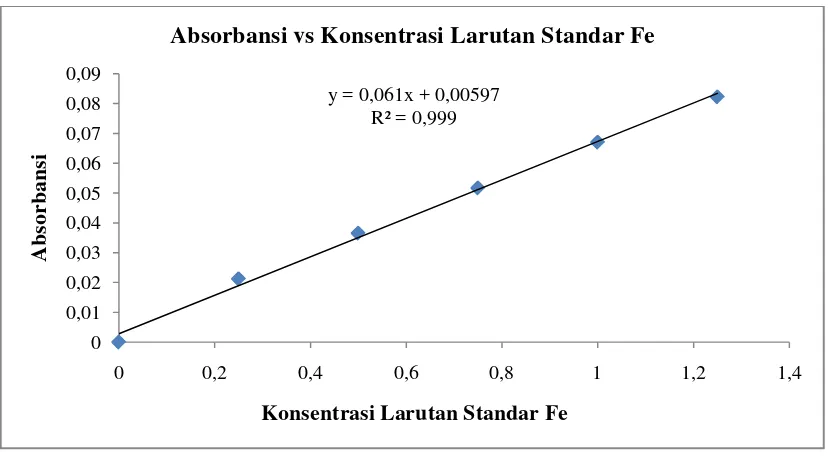
Gambar 4.1. Kurva Kalibrasi Larutan Standar Fe
4.1.1.3. Penentuan Konsentrasi Besi (Fe)
Konsentrasi Fe dapat ditentukan dengan menggunakan metode kurva kalibrasi
dengan mensubstitusikan nilai y (absorbansi) yang diperoleh dari hasil
pengukuran terhadap garis regresi dan kurva kalibrasi y = 0,061x + 0,00597
sehingga diperoleh konsentrasi besi (Fe).
Tabel 4.3. Konsentrasi Awal Logam Besi di dalam Air Sumur
Absorbansi (nm) Konsentrasi (ppm)
0,0684 1,0235
4.1.1.4. Penentuan Persentasi Penurunan Konsentrasi Besi (Fe)
Persentasi penurunan konsentrasi logam besi (Fe) dapat ditentukan dengan
formula berikut ini :
Konsentrasi awal logam Fe−Konsentrasi akhir logam Fe
Konsentrasi awal logam Fe ×100%
Penentuan persentasi penurunan konsentrasi besi (Fe) ini dilakukan dalam
tiga variasi, yaitu penentuan besi (Fe) dari hasil filtrasi, penentuan besi (Fe) dari
hasil elektrokoagulasi air sumur dan penentuan besi (Fe) dari hasil
elektrokoagulasi dan filtrasi air sumur.
y = 0,061x + 0,00597
Hasil perhitungan dari persentasi penurunan konsentrasi logam besi (Fe)
hasil filtrasi air sumur dapat dilihat pada Tabel 4.4. dibawah ini.
Tabel 4.4. Konsentrasi dan Persentasi Penurunan Logam Besi Hasil Filtrasi Air
Sumur
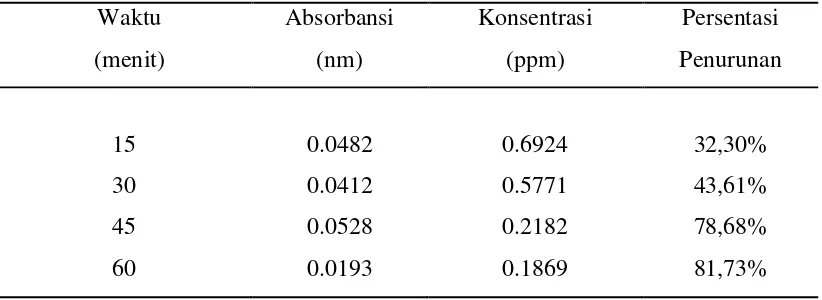
Hasil perhitungan dari persentasi penurunan konsentrasi logam besi (Fe)
hasil elektrokoagulasi air sumur dapat dilihat pada Tabel 4.5. dibawah ini.
Tabel 4.5. Konsentrasi dan Persentasi Penurunan Logam Besi Hasil
Elektrokoagulasi Air Sumur dengan Variasi Waktu
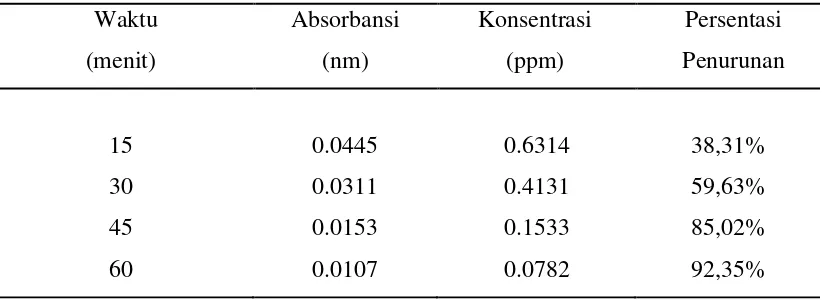
Tabel 4.6. Konsentrasi dan Persentasi Penurunan Logam Besi Hasil
Elektrokoagulasi dan Filtrasi Air Sumur dengan Variasi Waktu
Waktu
(menit)
Absorbansi
(nm)
Konsentrasi
(ppm)
Persentasi
Penurunan
15 0.0445 0.6314 38,31%
30 0.0311 0.4131 59,63%
45 0.0153 0.1533 85,02%
4.2. Pembahasan
Pengolahan air sumur yang hanya dilakukan dengan elektrokoagulasi masih
kurang efesien. Untuk itu perlu dilakukan elektrokoagulasi yang dibantu dengan
penyaringan untuk mendapatkan hasil air yang jernih.
Prinsip dasar dari elektrokoagulasi ini merupakan reaksi reduksi dan
oksidasi (redoks). Dalam suatu sel elektrokoagulasi, peristiwa oksidasi terjadi di
elektroda (+) yaitu anoda dan sekaligus berfungsi sebagai koagulan, sedangkan
reduksi dan pengendapan terjadi di elektroda (-) yaitu katoda. Yang terlibat reaksi
dalam elektrokoagulasi selain elektroda adalah air yang diolah yang berfungsi
sebagai larutan elektrolit.
Proses elektrokoagulasi ini dilakukan pada bejana elektrolisis yang di
dalamnya terdapat dua penghantar arus listrik searah yaitu elektroda berupa plat
aluminium , yang tercelup dalam 1L air sumur sebagai elektrolit. Penelitian ini
dilakukan menggunakan tegangan 12 V dan arus 10A.
Apabila dalam suatu elektrolit ditempatkan dua elektroda dan dialiri arus
listrik searah, maka akan terjadi peristiwa elektrokimia yaitu gejala dekomposisi
elektrolit, yaitu ion positif (kation) bergerak ke katoda dan menerima elektron
yang direduksi dan ion negatif (anion) bergerak ke anoda dan menyerahkan
elektron yang dioksidasi.
Menurut Holt, 2006 adapun reaksi yang terjadi apabila kedua elektroda
merupakan plat aluminium adalah sebagai berikut :
1. Katoda yang berupa plat aluminium akan mereduksi air membentuk gas
hidrogen sebagai gelembung – gelembung gas.
2H2O(l) + 2e− → 2OH−(aq) + H2(g) E0 = -0,83 V
2. Anoda yang berupa plat aluminium akan mengalami oksidasi menjadi ionnya
Elektroda aluminium akan melarutkan ion Al3+ ke dalam air dan akan
bereaksi dengan air (hidrolisa) sebelum terjadi prespitat Al(OH)3. Kemudian Al3+
akan membentuk hidroksida yang mempunyai sifat – sifat adsorpsi yang tinggi.
Al3+ + 3H2O → Al(OH)3 + 3H+
Dengan terbentuknya Al(OH)3 hasil hidrolisa dari Al3+ yang bermuatan
positif maka koloid dari senyawa besi dan partikel lainnya yang bermuatan lebih
rendah akan tertarik oleh ion Al3+ dan membentuk senyawa yang bersifat netral.
Ini berarti proses destabilisasi muatan. Dalam kondisi ini presipitat Al(OH)3 akan
berfungsi sebagai inti dari pembentukan flok dimana akan membentuk flok-flok
yang lebih besar bersama dengan partikel koloid lainnya bersifat stabil dan
mengandung lebih sedikit air yang terikat. Evolusi gas hidrogen membantu dalam
pencampuran dan karenanya membantu flokulasi. Flok yang terbentuk akibat
terjadinya destabilisasi partikel koloid akan mengalami flotasi, mengambang dan
memadat di permukaan air oleh gelembung udara (gas H2) yang terbentuk pada
plat elektroda.
2H2O(l) + 2e− → 2OH−(aq) + H2(g) E0 = -0,83 V
Semakin lama waktu yang digunakan untuk mengaliri arus listrik dalam
proses elektrokoagulasi, maka persentase penurunan kekeruhan juga menjadi
semakin meningkat, sehingga air yang dihasilkan akan menjadi semakin jernih
karena semakin besar waktu yang digunakan pada saat proses elektrokoagulasi,
maka akan semakin banyak ion Alumunium (Al3+) yang dilepaskan. Pada prinsip
kerjanya, ion – ion alumunium inilah yang berperan aktif sebagai koagulan yang
mengikat partikel – partikel koloid dalam air. Setelah ion alumunium berikatan
dengan partikel – partikel pengganggu tersebut, maka keduanya akan membentuk
suatu flok. Semakin lama flok – flok tersebut akan bergabung dengan flok lainnya
sehingga membentuk flok yang lebih besar. Pada air hasil elektrokoagulasi,
terdapat dua jenis flok yang terbentuk. Flok pertama adalah flok yang mengendap
pada dasar wadah dan flok kedua adalah flok yang berada pada permukaan air
hasil penjernihan. Adapun flok yang mengendap pada dasar wadah merupakan
flok – flok yang berukuran besar sehingga pada saat air di diamkan maka flok
tersebut akan bersedimentasi pada dasar wadah. Sedangkan flok yang terdapat
katoda yang mengangkat flok yang masih melayang pada air menuju permukaan
air. Adapun peristiwa ini dikenal dengan flotasi. Flotasi adalah peristiwa
terangkatnya flok – flok yang terbentuk pada proses elektrokoagulasi oleh gas
hydrogen yang dihasilkan katoda menuju permukaan air. Keberadaan kedua jenis
flok yang terbentuk merupakan salah satu kelebihan dari penjernihan air dengan
proses elektrokoagulasi, karena dengan adanya flok yang terdapat pada
permukaan air akan mempermudah proses pemisahan air hasil penjernihan dengan
flok yang terbentuk.
Selanjutnya, air hasil elektrokoagulasi ini dialirkan ke dalam bejana
filtrasi. Hal ini dapat menurunkan konsentrasi logam, senyawa organik dan
partikel lainnya didalam air sumur.
Penyaringan yang dilakukan setelah elektrokoagulasi dilakukan dari
bawah ke atas dimaksudkan agar tekanan air pada waktu melewati bejana filtrasi
sama diseluruh permukaannya. Dengan sistem penyaringan seperti ini diharapkan
flok–flok yang halus akan benar-benar tertahan dan tertinggal dibawah. Tidak
seperti penyaringan pada umumnya yang dilakukan dari atas ke bawah, tekanan di
tempat jatuhnya air tentu akan lebih besar, hal ini bisa menyebabkan pecahnya
flok yang telah terbentuk.
Pada penelitian ini dilakukan proses destruksi dengan HNO3 (p) terhadap
air sumur hasil elektrokoagulasi yang bertujuan untuk memutuskan ikatan unsur
logam dengan komponen lain di dalam air sehingga logam tersebut berada dalam
keadaan bebas sehingga mudah untuk dianalisis dengan Spektrofotometer Serapan
Atom.
Dari hasil penelitian ini didapatkan bahwa waktu optimum
elektrokoagulasi dalam pengurangan kadar Fe selama 45 menit, dimana kadar besi
yang di peroleh sudah memenuhi syarat air bersih KEPMENKES RI No.
907/MENKES/VII/2002, dengan persentasi penurunan kadar Fe yaitu 78,68%
dengan kadar Fe : 0,2182 mg/L, selanjutnya proses elektrokoagulasi disertai
dengan penyaringan dan diperoleh persentasi penurunan kadar Fe yaitu 85,02%
Dari hasil tersebut diperoleh bahwa proses penyaringan (filtrasi) juga
berpengaruh pada penurunan kadar logam Fe. Pada waktu 60 menit sebenarnya
kadar Fe yang diperoleh semakin rendah, tetapi untuk menghemat penggunaan
waktu dan arus listrik yang digunakan maka waktu optimum elektrokoagulasi
selama 45 menit.
Hasil analisis Spektrofotometer Serapan Atom terhadap konsentrasi besi
menunjukkan bahwa pada waktu optimum selama 45 menit elektrokoagulasi air
sumur dengan penyaringan lebih baik dibandingkan dengan elektrokoagulasi
tanpa penyaringan dengan masing – masing persentasi penurunan adalah 85,02%
dan 78,68%. Hal ini dikarenakan penyaringan juga berpengaruh pada penurunan
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
1. Metode elektrokoagulasi dapat digunakan dalam proses pengolahan air bersih
khususnya penurunan kadar logam Fe pada air sumur.
2. Waktu optimum elektrokoagulasi dalam penurunan kadar Fe di dapat selama 45
menit dimana kadar Fe yang diperoleh sudah memenuhi syarat air bersih menurut
KEPMENKES RI No. 907/MENKES/VII/2002.
5.2. Saran
Diharapkan agar peneliti selanjutnya menguji parameter – parameter lain yang
sesuai dengan persyaratan air bersih berdasarkan KEPMENKES RI No.
DAFTAR PUSTAKA
Adib, M. F. 2011. Penyisihan Kadar COD, BOD Dan Warna Pada Limbah Cair
Industri Batik Dengan Metode Elektrokoagulasi.
Effendi, H. 2003. Telaah Kualitas Air Bagi Pengelolaan Sumber Daya dan
Lingkungan Perairan. Cetakan Kelima. Kanisius. Yogyakarta.
Entjang, I. 2000. Ilmu Kesehatan Masyarakat. PT.Citra Adtya Bakti. Bandung.
Gabriel, J.F. 2001. Fisika Lingkungan. Hipokrates. Jakarta.
Haswell, S.J. 1991. Atomic Absorption Spectrometry. Elsevier. Amsterdam.
Heriani, E. 2014. Studi Pendahuluan Pengolahan Air Payau Menjadi Air Bersih
Dengan Metode Kombinasi Elektrokoagulasi Dan Adsorpsi Menggunakan
Karbosil. Bandar Lampung
Hiskia, A. 1992. Kimia Unsur dan Radiokimia. Citra Aditya Bakti. Bandung
Holt, P.K. Barton, G.W., and Mitchel, C.A. 2006. Electrocoagulation as a
Wastewater Treatment. The University of Sydney. New South Wales.
Juanta, P. 2014. Pendeteksian Intrusi Air Laut dan Analisis Kandungan Air pada
Sumur Bor dengan Metode Konduktivitas Listrik di Daerah Belawan.
[Skripsi]. Medan: Universitas Negeri Medan, Program Sarjana.
Keenan, C.W. 1999. Ilmu Kimia Untuk Universitas. Edisi keenam. Erlangga.
Jakarta.
Kennedy, J.H. 1990. Analytical Chemistry Principples. Second Edition. Saunders
College Publishing. USA.
Mulja, J.C dan Miller, J.N. 1991. Statistika Untuk Kimia Analitik. Edisi kedua.
Terjemahan Suroso. Bandung : Penerbit ITB.
Nainggolan, H. 2011. Pengolahan Limbah Cair Industri Perkebunan dan Air
Gambut menjadi Air Bersih. USU Press. Medan.
Ni’am, M.F. Othman, F., Sohaili, J., Fauzia, Z. 2007. Removal of COD And
Turbidity to Improve Wastewater Quality Using Electrocoagulation
Technique. The Malaysian Journal of Analytical Sciences. Volume 1.
Nugroho, A. 2006. Bioindikator Kualitas Air. Penerbit Universitas Trisakti.
Jakarta.
Novita, S. 2012. Pengaruh Variasi Kuat Arus Listrik dan Waktu Pengadukan pada
Proses Elektrokoagulasi untuk Penjernihan Air Baku PDAM Tirtanadi IPA
Sunggal. [Skripsi]. Medan: Universitas Sumatera Utara, Program Sarjana.
Ompusunggu, H. 2009. Analisa Kandungan Nitrat Air Sumur Gali Masyarakat di
Sekitar Tempat Pembuangan Akhir (TPA) Sampah di Desa Namo Bintang
Kecamatan Pancur Batu. [Skripsi]. Medan: Universitas Sumatera Utara,
Program Sarjana.
Peraturan Menteri Kesehatan Republik Indonesia. 2002. PERMENKES RI NO
907/MENKES/SK/VII/2002 Syarat – Syarat dan Pengawasan Kualitas Air
Minum.
Proste, R.L. 1997. Theory and Practice of Water and Wastewater Treatment. John
Wiley and Sons. New York.
Putra, M.H. 2000. Efektifitas Dan Efesiensi Proses Elektrokoagulasi Untuk
Penurunan Kekeruhan Air Sumur Dangkal Guna Meningkatkan Kualitas
Air Minum. [Tesis]. Medan: Universitas Sumatera Utara, Program Pasca
Sarjana.
Purwaningsih, I. 2008. Pengolahan Limbah Cair Industri Batik CV. Batik Indah
Raradjonggrang Yogyakarta dengan Metode Elektrokoagulasi Ditinjau
dari Parameter Chemycal Oxygen Demand (COD) dan Warna. UII.
Yogyakarta.
Ridwan, M.H. 2008. Penurunan Kadar Logam Seng Pada Air Limbah PT. Industri
Karet Nusantara Dengan Metode Elektrokoagulasi. [Skripsi]. Medan:
Universitas Sumatera Utara.
Rohman, A. 2007. Kimia Farmasi. Cetakan Pertama. Yogyakarta. Pustaka Pelajar.
Suripin, M. 2001. Pelestarian Sumber Daya Tanah dan Air. Penerbit Andi.
Yogyakarta.
Sutrisno, T. 1987. Teknologi Penyediaan Air Bersih. Penerbit Rineka Cipta.
Jakarta.
Svehla, G. 1979. Buku Teks Analisis Anorganik Kualitatif Makro dan Semimikro.
Widowati, W., Sastiono, A., dan Jusuf, R.R. 2008. Efek Toksik Logam.
Pencegahan dan Penanggulangan Pencemaran. Penerbit Andi Yogyakarta.
Lampiran 1. Persyaratan Kualitas Air Minum Menurut KEPMENKES RI No.907/MENKES / VII / 2002
Lampiran 2. Alat yang Digunakan Saat Proses Elektrokoagulasi
Rangkaian Alat Elektrokoagulasi Rangkaian Alat Filtrasi
Lampiran 3. Air Gambut Sebelum dan Sesudah Proses Elektrokoagulasi
Air Sumur Sebelum di Elektrokoagulasi Air Sesudah di Elektrokoaguasi