UNIVERSITAS DIPONEGORO
PENGARUH KONSENTRASI
CHEMICAL OXYGEN DEMAND
(COD) DAN pH TERHADAP KINERJA
GRANULAR ACTIVATED
CARBON DUAL CHAMBER MICROBIAL FUEL CELLS
(GAC-DCMFCs)
TUGAS AKHIR
ESTUNING MUGI RAHAJENG
21080110130045
FAKULTAS TEKNIK
PROGRAM STUDI TEKNIK LINGKUNGAN
SEMARANG
UNIVERSITAS DIPONEGORO
PENGARUH KONSENTRASI
CHEMICAL OXYGEN DEMAND
(COD) DAN pH TERHADAP KINERJA
GRANULAR ACTIVATED
CARBON DUAL CHAMBER MICROBIAL FUEL CELLS
(GAC-DCMFCs)
TUGAS AKHIR
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Strata 1 (S1)
ESTUNING MUGI RAHAJENG
21080110130045
FAKULTAS TEKNIK
PROGRAM STUDI TEKNIK LINGKUNGAN
ii
Skripsi ini adalah hasil karya saya sendiri,
dan semua sumber baik yang dikutip maupun yang dirujuk telah saya nyatakan dengan benar.
NAMA : Estuning Mugi Rahajeng NIM : 21080110130045
Tanda Tangan :
v bawah ini :
Nama : Estuning Mugi Rahajeng
NIM : 21080110130045
Jurusan/Program Studi : Teknik Lingkungan
Fakultas : Teknik
Jenis Karya : Skripsi
Demi pengembangan ilmu pengetahuan, menyetujui untuk memberikan kepada Universitas Diponegoro Hak Bebas Royalti Noneksklusif (Non-exclusive Royalty Free Right) atas karya ilmiah saya yang berjudul :
“Pengaruh Konsentrasi Chemical Oxygen Demand (COD) Dan pH Terhadap Kinerja Granular Activated Carbon Dual Chamber Microbial Fuel Cells
(GAC-DCMFCs)” beserta perangkat yang ada (jika diperlukan). Dengan Hak Bebas Royalti/ Noneksklusif ini Universitas Diponegoro berhak menyimpan, mengalihmedia/ formatkan, mengelola dalam bentuk pangkalan data (database), merawat dan mempublikasikan tugas akhir saya selama tetap mencantumkan nama saya sebagai penulis/pencipta dan sebagai pemilik Hak Cipta.
Demikian pernyataan ini saya buat dengan sebenarnya.
Dibuat di : Semarang Pada Tanggal : Desember, 2014
Yang menyatakan
vi
Demand (COD) dan pH Terhadap Kinerja Granular Activated Carbon Dual Chamber Microbial Fuel Cells (GAC-DMFCs)”.
Microbial Fuel Cells (MFCs) merupakan sebuah sistem yang langsung mengonversi energi kimia yang terdapat pada substrat bio-convertible menjadi energi listrik, menggunakan katalis berupa bakteri. Pengolahan dengan menggunakan reaktor ini tidak hanya dapat menurunkan parameter pencemar dalam air limbah akan tetapi sekaligus bisa dijadikan sumber energi alternatif karena elektron yang dihasilkan dari mekanisme bakteri akan ditangkap oleh elektroda yang berada di dalam reaktor. Tujuan penelitian tugas akhir ini adalah menganalisis pengaruh konsentasi COD dan pH dan menentukan konsentrasi COD dan pH optimum terhadap kinerja GAC-DCMFCs.
Akhir kata, semoga Laporan Tugas Akhir ini bermanfaat bagi semua pembaca terutama mahasiswa sehingga turut berperan serta dalam menjaga kelestarian lingkungan.
Semarang, Desember 2014
vii terimakasih banyak penulis tujukan kepada :
1. Allah SWT, Tuhanku Yang Maha Esa. Tidak ada alasan untuk tidak selalu mengucap syukur pada-Mu.
2. Ibu Sukani, Bapak Aris Mulyanto, dan Mas Sinung Mugi Aji, keluargaku yang selalu mendukung dan setia mendoakan untuk kesuksesanku.
3. Bapak Dr. Ir. Syafrudin, CES, MT selaku ketua program studi Teknik Lingkungan Universitas Diponegoro.
4. Ir. Dwi Siwi Handayani, MSi selaku dosen wali dan kordinator mata kuliah tugas akhir yang telah membantu kelancaran administrasi penyelesaian tugas akhir.
5. Ibu Sri Sumiyati, ST. MSi dan Bapak Ganjar Samudro, ST. MT selaku pembimbing I dan II Tugas Akhir yang telah memberikan bimbingan dan dukungan untuk penulis dalam pelaksanaan Tugas Akhir.
6. Bapak Dr. Haryono Setiyo Huboyo, ST, MT dan Bapak Wiharyanto Oktiawan, ST, MT selaku penguji I dan II sidang Tugas Akhir.
7. Teman-teman satu tim MFCs yang saya sayangi Amelia Fitriani, Agustin Wijayanti, Nurul Ulfia, Mei Ekowati, Lintang Iradati, Mazlani Firdausya Rohim, serta khusus untuk Bimastyaji Surya Ramadan dan Maulana Khafid Arrohman yang juga telah bersedia mengajak saya menjadi teman satu tim SEC (Super Enviro Club) selama 3 tahun, sungguh pengalaman luar biasa. Terimakasih kawan.
8. Aris Nurhidayah, Agustin Wijayanti, dan Devi Nur Vidyautami, ST yang menjadi sahabat baik sejak maba. Terimakasih dukungan dan doanya. 9. Muhamad Hibban yang selalu mendukung dan membantu penulis dalam
viii
11.Seluruh teman-teman Teknik Lingkungan angkatan 2010 atas dukungan, semangat dan doanya dari awal hingga saat ini, sampai jumpa lagi pada tahun 2020 di Jepang.
12.Mas Purwono dan Mas Ryan yang setia direpotkan selama penulis melakukan penelitian di laboratorium TL
13.Mas Dayat, Ibu Anik, Mbak Silvy, Pak Adi, Mas Habibi, Mas Budi, dan staff admin lainnya yang telah membantu penulis dalam meberikan kelancaran proses administrasi tugas akhir.
14.Kepada semua orang-orang yang turut membantu penulis selama proses penelitian tugas akhir ini berlangsung yang tidak dapat disebutkan satu persatu namanya.
Semarang , Desember 2014
ix
Estuning Mugi Rahajeng*); Sri Sumiyati*); Ganjar Samudro *) *)
Program Studi Teknik Lingkungan Undip, Jl. Prof. H. Sudarto, SH Tembalang – Semarang
ABSTRAK
Microbial Fuel Cells adalah alat untuk mengonversi energi kimia menjadi energi listrik dengan bantuan reaksi katalis dari mikroorganisme. Kinerja MFCs dapat dipengaruhi oleh konsentasi COD dan pH. Pada penelitian ini, digunakan variasi kedua variabel tersebut, yaitu konsentrasi COD sebesar 400, 800,1200 mg/L dan pH 6, 7, 8. Sistem MFCs ini dilengkapi dengan penggunaan granular activated carbon (GAC) sebagai media perlekatan bakteri di ruang anoda. Hasil penelitian menunjukkan bahwa jumlah COD yang disisihkan meningkat ketika konsentrasi meningkat. Untuk power density, terjadi peningkatan sebesar 132,0 dan 245,0 mW/m2 ketika konsentrasi COD 400 dan 800 mg/L. Tetapi ketika konsentrasi COD 1200 mg/L, power density menurun menjadi 206,0 mW/m2. Kondisi optimum untuk COD 400 dan 800 mg/L berada pada pH 7, sedangkan COD 1200 mg/L berada pada pH 8 yang mampu menyisihkan COD dan memproduksi listrik lebih baik.
x
Estuning Mugi Rahajeng*); Sri Sumiyati*); Ganjar Samudro *) *)
Department of Environmental Engineering Undip, Jl. Prof. H. Sudarto, SH
Tembalang – Semarang
ABSTRACT
Microbial Fuel Cells are devices to convert chemical energy into
electrical energy by the catalytic reaction of microorganisms. MFCs performance
can be affected by the COD and pH. In this study, variations of these two
variables are used; the COD concentration of 400, 800, 1200 mg/L and pH 6, 7,
8. This system is accompanied by granular activated carbon (GAC) as an
attachment media of bacteria in the anode chamber. The result showed that the
amount of COD removed increasing as the concentration increased. For power
density, increased by 132,0 and 245,0 mW/m2 when the COD concentrations are
400 and 800 mg / L. However, when the COD concentration is 1200 mg/L power
density decreased to 206,0 mW/m2. The optimum conditions for the COD of 400
and 800 mg/L were at pH 7, whereas for the COD of 1200 mg/L were at pH 8
which capable of removing COD and produce electricity better.
xi
HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI... ... v
KATA PENGANTAR... ... vi
HALAMAN PERSEMBAHAN ... vii
ABSTRAK... ... ix
DAFTAR ISI .. ... xi
DAFTAR GAMBAR ... xiv
DAFTAR TABEL ... xvi
DAFTAR SINGKATAN DAN ISTILAH ... xvii
BAB I PENDAHULUAN
1.1 Latar Belakang ... I-1 1.2 Identifikasi Masalah ... I-2 1.3 Pembatasan Masalah ... I-3 1.4 Perumusan Masalah... I-3 1.5 Tujuan Penelitian... I-3 1.6 Manfaat Penelitian... I-3
BAB II TINJAUAN PUSTAKA
xii
2.3 Granular Activated CarbonDual Chamber MFCs (GAC-DCMFCs) ... II-8 2.4 Air Buangan sebagai Bahan Baku MFCs ... II-10 2.5 Proses Pengolahan Biologi Secara Anaerob ... II-10 2.6 Biofilter Tercelup (Biofilm) ... II-11 2.7 Proses Pengolahan Biologi dengan Biakan Melekat ... II-12 2.8 Mekanisme Biofilm dalam Mentransfer Elektron ... II-13 2.9 Tahapan Penelitian ... II-15 2.10 Kapasitas Adsorpsi ... II-16 2.11 Power Density ... II-18 2.11.1 Kuat Arus Listrik ... II-19 2.11.2 Tegangan Listrik ... II-19 2.11.3 Coulombic Efficiency (CE)... II-20 2.12 Penelitian Terdahulu ... II-20 2.13 Hipotesis Penelitian ... II-22 2.14 Variabel Bebas dan Terikat ... II-23 2.25 Kerangka Pemikiran Penelitian ... II-23
BAB III METODELOGI PENELITIAN
xiii
3.7 Diagram Alir Penelitian ...III-21
BAB IV HASIL DAN PEMBAHASAN
4.1 Uji Karakteristik Limbah Cair Domestik ... IV-1 4.2 Kemampuan Adsorpsi... ... IV-2 4.2.1 Penentuan Isotherm Percobaan Batch ... IV-3 4.3 Pengoperasian Reaktor MFCs ... IV-7 4.3.1 Seeding dan Aklimatisasi ... IV-7 4.3.2 Tahap Running ... IV-13 4.3.2.1 Pengaruh Konsentrasi COD dan pH terhadap Kinerja
GAC-DCMFCs ... IV-14 4.3.2.2 Menentukan Konsentrasi COD dan pH Optiimum
terhadap Kinerja GAC-DCMFCs... IV-15 4.4 pH Effluent GAC-DCMFCs ... IV-26 4.5 Kesimpulan Hasil Uji Hipotesis ... IV-28
BAB V KESIMPULAN DAN SARAN
5.1 Kesimpulan... V-1 5.2 Saran... ... V-2 DAFTAR PUSTAKA
LAMPIRAN A: Data Penelitian
xiv
Gambar 2.3 Transfer Kontak Langsung antara Protein Redox-Aktif di Permukaan Sel Luar ...
II-14
Gambar 2.4 Transfer Elektron melalui Mediator Elektron Terlarut ...II-14 Gambar 2.5 Transfer Elektron menggunakan Nanowires ...II-15 Gambar 2.6 Kerangka Pikir Penelitian ...II-24 Gambar 3.1 Skematik Reaktor GAC-DCMFCs ...III-6 Gambar 3.2 Tampak Depan Rangkaian Reaktor GAC-DCMFCs ...III-6 Gambar 3.3 Tampak Depan Reaktor GAC-DCMFCs ...III-7 Gambar 3.4 Tampak Samping dan Atas Rangkaian Reaktor GAC-DCMFCs
...III-7 Gambar 3.5 Diagram Alir Proses Pembuatan Limbah Artifisial ...III-10 Gambar 3.6 Diagram Alir Proses Pembuatan Jembatan Garam ...III-11 Gambar 3.7 Diagram Alir Proses Preparasi Elektroda ...III-16 Gambar 3.8 Diagram Alir Proses Preparasi GAC...III-16 Gambar 3.9 Diagram Alir Proses Pembuatan Larutan Penyangga ...III-17 Gambar 3.10 Skema Penelitian Taap Seeding dan Aklimatisasi ...III-19 Gambar 3.11 Skema Penelitian Taap Running ...III-20 Gambar 3.12 Diagram Alir Metode Penelitian ...III-22 Gambar 4.1 Kurva Isoterm Freundlich ...IV-3 Gambar 4.2 Kurva Isoterm Langmuir ...IV-4 Gambar 4.3 Kurva Isoterm BET ...IV-5 Gambar 4.4 Penyisihan COD 400, 800, dan 1200 mg/L pada Tahap Seeding
dan Aklimatisasi
.... IV-8
Gambar 4.5 Power Density COD 400, 800, dan 1200 mg/L pada
xv
Gambar 4.8 A. Penyisihan Konsentrasi COD 1200 mg/L; B. Power
xvi
xvii
Adsorpsi Fluida terikat kepada suatu padatan dan akhirnya membentuk suatu lapisan tipis
Aklimatisasi Upaya adaptasi dari suatu organisme terhadap suatu lingkungan baru yang akan dimasukinya Anaerobik Kondisi tanpa udara (oksigen)
Artifisial Buatan
Batch Proses produksi yang berlangsung secara tidak kontinyu
Biofilm Bakteri yang melekat di suatu permukaan dan diselimuti oleh pelekat karbohidrat yang dikeluarkan oleh bakteri.
BOD Biological Oxygen Demand
Buffer Larutan yang digunakan untuk mempertahankan
nilai pH tertentu agar tidak banyak berubah selama reaksi kimia berlangsung
CH3COOH Asam asetat
CH4 Gas metan
COD Chemical Oxygen Demand
DCMFCs Dual Chamber Microbial Fuel Cells Dependent Variable Variabel bebas
Dual Chamber Bilik ganda
GAC Granular Activated Carbon
GAC-DCMFCs Granular Activated Carbon Microbial Fuel Cells
Hidrolisis Reaksi kimia yang memecah molekul air (H2O)
menjadi kation hidrogen (H+) dan anion hidroksida (OH−) melalui suatu proses kimia
Independent Variable Variabel terikat
KMnO4 Kalium Permanganat
xviii
pH Derajat keasaman
Running Tahap pengoperasian reaktor
Salt bridge Jembatan garam
Seeding Pembiakan bakteri
Sloughing Lepasnya film dari media
I-1 BAB I PENDAHULUAN
1.1 Latar Belakang
Seiring dengan kemajuan zaman, kebutuhan manusia akan suatu hal semakin meningkat. Hal ini dibuktikan dengan meningkatnya pula limbah yang dihasilkan tiap harinya. Kegiatan sehari-hari seperti MCK merupakan kontribusi besar dalam menurunnya kualitas lingkungan. Air limbah juga dapat berasal dari kegiatan non domestik, seperti dari kegiatan pertanian, perdagangan, dan industri. Dengan menggunakan teknologi pengolahan yang tepat, diharapkan air limbah dapat tertangani dengan baik. Menurut Sami (2012: 2), sasaran pengolahan air adalah untuk mengurangi BOD, COD, partikel tercampur, membunuh organisme pathogen, menghilangkan bahan nutrisi, komponen beracun yang tidak dapat didegradasikan agar konsentrasi yang ada menjadi rendah.
Beberapa teknologi pengolahan air limbah yang dapat digunakan antara lain adalah UASB dan anaerobic digestion yang dioperasikan secara anaerobik, serta
trickling filter, RBC, oxidation ditch, dll yang dioperasikan secara aerobik. Setiap jenis teknologi pengolahan air limbah mempunyai keunggulan dan kelemahannya masing-masing, oleh karena itu dalam hal pemilihan jenis teknologi tersebut perlu diperhatikan aspek operasional, ekonomis, lingkungan, dan manfaatnya secara keseluruhan. Salah satu teknologi yang memenuhi aspek-aspek diatas adalah
menjadi sumber karbon untuk microbial fuel cells, dan energi listrik yang dihasilkan cukup untuk digunakan dalam pengolahan air limbah berikutnya dan ini berarti mengurangi konsumsi energi (Li, 2007: 1).
Dalam pengoperasian MFCs, konsentrasi COD dan pH merupakan variabel yang menjadi faktor operasional sistem. Konsentrasi COD yang tinggi membuat mikroorganisme mensintesis lebih enzim dengan mempertahankan kemampuan menghilangkan COD dalam beberapa waktu, oleh karena itu mikroorganisme mampu menurunkan COD pada tingkat konsentrasi tinggi sehingga meningkatkan intensitas maksimum yang dihasilkan dari sistem MFCs. Dalam penelitian yang dilakukan oleh Campo, et al. (2012), bertambahnya konsentrasi COD meningkatkan aktivitas mikroorganisme sehingga meningkatkan produksi arus listrik. Peningkatan produksi listrik juga dipengaruhi oleh operasional pH. Pada MFCs dual chamber, kuat arus tertinggi dicapai pada pH netral antara 6,5 sampai 8 (Behera and Ghangrekar, 2009: 5114). Selain mengatur sistem MFCs dalam kondisi COD dan pH yang optimum, kinerja MFC dapat ditingkatkan dengan menggunakan granular activated carbon (GAC) berfungsi sebagai media lekat. MFCs yang menggunakan GAC sebagai media lekat dapat disebut sebagai
Granular Activated Carbon Dual Chamber Microbial Fuel Cells (GAC-DCMFCs). Dalam konteks ini, tujuan dari penelitian yang akan dilakukan adalah pengoperasian MFCs dengan media lekat GAC ketika COD dan pH digunakan sebagai variabel. Berdasarkan penelitian yang pernah dilakukan, variasi COD dan pH dapat mempengaruhi performa MFCs, semakin besar COD yang diolah dan pH yang optimum maka kinerja MFCs semakin baik.
1.2 Identifikasi Masalah
Identifikasi masalah pada penelitian ini adalah:
1. Tingginya konsentrasi organik yang ada di dalam air limbah akan menyebabkan masalah bagi lingkungan sehingga memerlukan pengolahan yang tepat.
1.3 Pembatasan Masalah
Pembatasan masalah pada penelitian ini adalah:
1. Konsentrasi COD yang rendah maupun tinggi dapat menyebabkan perubahan produksi listrik dan penyisihan COD di dalam reaktor GAC-DCMFCs.
2. pH dapat menyebabkan perubahan produksi listrik dan penyisihan COD di dalam reaktor GAC-DCMFCs.
1.4 Perumusan Masalah
Perumusan masalah pada penelitian ini adalah:
1. Bagaimana pengaruh konsentrasi COD dan pH terhadap kinerja GAC-DCMFCs?
2. Berapakah konsentrasi COD dan pH optimum pada GAC-DCMFCs?
1.5 Tujuan Penelitian
Tujuan penelitian ini adalah:
1. Menganalisis pengaruh konsentasi COD dan pH terhadap kinerja GAC-DCMFCs.
2. Menentukan konsentrasi COD dan pH optimum terhadap kinerja GAC-DCMFCs.
1.6 Manfaat penelitian
Manfaat yang diharapkan dalam penelitian ini antara lain adalah: A. Bagi Pembaca
1. Menambah pengetahuan dan wawasan mengenai pengolahan limbah dengan menggunakan Microbial Fuel Cells.
B. Bagi Penulis
1. Menambah pengetahuan mengenai pengolahan limbah dengan menggunakan Microbial Fuel Cells.
I-1 BAB II
TINJAUAN PUSTAKA
2.1 Microbial Fuel Cells (MFCs)
Pada dasarnya, berbagai bentuk bahan organik dapat digunakan sebagai substrat dalam microbial fuel cells, seperti glukosa (Liu dan Logan, 2004), asetat (Logan et al., 2007), asam amino (Logan et al., 2005) dan air limbah dari manusia dan hewan (Liu et al., 2004). Secara umum mekanisme prosesnya adalah substrat dioksidasi oleh bakteri menghasilkan elektron dan proton pada anoda.Elektron ditransfer memalui sirkuit eksternal, sedangkan proton didifusikan melalui larutan menuju katoda. Pada katoda, reakasi elektron dan proton terhadap oksigen akan menghasilkan air (H2O) (Cheng et al., 2006).
2.1.1 Keuntungan Microbial Fuel Cells
2.1.2 Prinsip Kerja Microbial Fuel Cells
Prinsip kerja MFCs adalah memanfaatkan mikroba yang melakukan metabolisme terhadap medium di anoda untuk mengkatalisis pengubahan materi organik menjadi energi listrik dengan mentransfer elektron dari anoda melalui kabel dan menghasilkan arus ke katoda. Transfer elektron dari anoda diterima oleh ion kompleks di katoda yang memiliki elektron bebas. Dalam MFCs, yang dapat digunakan sebagai donor elektron adalah zat hasil metabolisme mikroba atau elektron yang dilepaskan mikroba saat melakukan metabolismenya. Zat hasil metabolisme mikroba umumnya merupakan senyawa yang mengandung hidrogen, seperti etanol, metanol, atau gas metana. Senyawa ini dapat digunakan sebagai sumber hidrogen melalui serangkaian proses untuk memproduksi elektron dan menghasilkan arus listrik. Setiap aktivitas metabolisme yang dilakukan mikroba umumnya melibatkan pelepasan elektron bebas ke medium. Elektron ini dapat dimanfaatkan langsung pada anoda dalam MFCs untuk menghasilkan arus listrik (Novitasari, 2011: 7).
Secara umum mekanismenya adalah substrat dioksidasi oleh bakteri menghasilkan elektron dan proton pada anoda. Elektron ditransfer melalui sirkuit eksternal, sedangkan proton didifusikan melalui separator membran menuju katoda. Pada katoda, reaksi elektron dan proton terhadap oksigen akan menghasilkan air (Cheng et al., 2006).
2.1.3 Perkembangan Teknologi Microbial Fuel Cells
dari skala laboratorium dan untuk memproduksi bioenergi pada skala yang lebih besar. Penelitian yang dilakukan oleh ilmuwan Amerika di Penn State akhir tahun 2005 lalu mungkin menambah satu bidang lagi kontribusi bakteri terhadap kehidupan manusia. Adalah MFCs, suatu sistem yang ditemukan dengan menggunakan bantuan tenaga listrik untuk menghasilkan hidrogen dan air bersih dari air limbah rumah tangga, pertanian maupun industri. Dr. Bruce Logan, profesor peliti dan penemunya Ramanathan Ramnarayan mengatakan, proses MFCs tidak dibatasi biomassa karbohidrat yang ada pada substrat sebagai penghasil hidrogen seperti pada proses fermentasi biasa. Walaupun MFCs telah ada sebelumnya, Logan mengatakan, MFC yang baru ini sedikit berbeda dengan pendahulunya. Pada MFCs baru, ketika bakteri “memakan” substrat, bakteri mentransfer elektron pada anoda. Bakteri juga melepaskan proton yang kemudian larut. Elektron pada anoda bermigrasi melalui kabel menuju katoda, dimana dengan bantuan secara elektrokimia akan terjadi kombinasi dengan proton membentuk gas hidrogen. Pada saat pertama didemonstrasikan, gas hidrogen benar-benar dapat ditangkap dan dapat dijadikan sebagai bahan bakar yang dapat diperbarui serta ramah lingkungan.
2.1.4 Bakteri di Microbial Fuel Cells
Telah diketahui selama hampir seratus tahun bahwa bakteri bisa menghasilkan listrik (Logan, 2006: 512) tetapi hanya dalam beberapa tahun terakhir, kemampuan ini menjadi lebih populer di laboratorium. Dalam MFCs, bakteri tertentu yang disebut exoelectrogens dapat mengoksidasi bahan organik dan mentransfer elektron ke anoda serta menghasilkan arus listrik (Logan 2006: 512). Banyak mikroorganisme memiliki kemampuan untuk mentransfer elektron yang berasal dari metabolisme bahan organik untuk anoda. Sedimen laut, tanah, air limbah, sedimen air tawar dan lumpur aktif adalah sumber yang kaya untuk mikroorganisme ini, seperti Escherichia coli, Geobacter sulfurreducens,
Shewanella oneidensis, Shewanella putrefaciens (Du et al., 2007: 467)
2.1.5 Komponen MFCs
Sebuah MFCs terdiri dari sebuah ruang anodik dan ruang katodik yang dipisahkan oleh membran maupun jembatan garam. Tabel 2.1. menunjukkan ringkasan komponen MFCs dan bahan yang digunakan untuk membangunnya (Logan, 2007: 61).
Tabel 2.1
Material Komponen Microbial Fuel Cells
Bahan Material Keterangan
Anoda Graphite, graphite felt, carbon paper,
carbon-cloth, Pt, Pt black, reticulated
vitreous carbon (RVC)
Harus ada
Katoda Graphite, graphite felt, carbon paper,
carbon-cloth, Pt, Pt black, RVC
Harus ada
Ruang anoda Glass, polycarbonate, plexiglas Harus ada
Ruang katoda Glass, polycarbonate, plexiglas Harus ada
Sistem pertukaran
ion
Proton exchange membrane: Nafion, Ultrex,
polyethylene.poly
(styrene-co-divinylbenzene); salt bridge, porcelain
septum, atau solely electrolyte
Bahan Material Keterangan
Katalis Elektroda Pt, Pt black, MnO2, Fe
3+,
polyaniline,
electron mediator immobilized on anode
Opsional
Sumber: Du et al., 2007
2.2 Faktor Operasional MFCs 2.2.1 Substrat dalam MFCs
Dalam kultur campuran, sulit untuk menganalisis apakah substrat yang terbaik karena proses metabolisme yang berbeda setiap spesies (Liu, 2007). Beberapa penelitian tentang substrat yang telah dilakukan diantaranya mengunakan substrat asetat (Logan, et al., 2007), glukosa (Catal et al., 2008a),
2.2.2 pH
pH adalah derajat keasaman yang digunakan untuk menyatakan tingkat keasaman atau kebasaan yang dimiliki oleh suatu larutan. pH merupakan faktor kritis untuk semua proses berbasis mikroba. Pada MFCs, pH tidak hanya mempengaruhi metablisme dan pertumbuhan bakteri tapi juga terhadap transfer proton dan reaksi katoda sehingga mempengaruhi performa MFCs. Sebagian besar MFCs beroperasi pada pH mendekati netral untuk menjaga kondisi pertumbuhan optimal komunitas mikroba yang terlibat dalam pembentukan listrik (Liu, 2008; Kristin, 2012). Menurut Budhi dkk (1999: V-159), derajat keasaman kultur medium sangat berpengaruh terhadap populasi mikroba. Bakteri penghasil metana sangat sensitif terhadap perubahan pH. Pada rentang pH 6-8, laju produksi gas metana berkisar antara l-4 ml/hari. Penambahan larutan penyangga diperlukan untuk mempertahankan pH sekitar 7 agar pertumbuhan bakteri penghasil metana tidak terhambat. Kapasitas penyangga dalam reaktor ditunjukkan dengan adanya alkalinitas.
2.2.3 Temperatur
Kinetika bakeri, transfer massa proton melalui elektrolit dan laju reaksi okisgen pada katoda menetukan performa MFCs dan semua tergantung pada temperatur. Biasanya konstanta reaksi biokimia mengganda setiap kenaikan temperatur 10°C sampai tercapai temperatur optimal. Sebagian besar studi MFCs dilakukan pada temperature 28-35°C (Liu et al., 2008: 277). Dalam penelitian (Patil et al., 2010: 16) dijelaskan bahwa temperatur tidak hanya berpengaruh kepada pertumbuhan bakteri tetapi juga berpengaruh dalam produksi listrik. Secara umum, produksi listrik meningkat sesuai dengan suhu lingkungannya. Hal ini sudah di observasi dalam penelitian bahwa dalam peningkatan suhu dari 30 - 40 oC meningkatkan produksi listrik hingga 80 % (Liu et al., 2010: 2165).
2.2.4 Hydraulic Retention Time ( HRT)
penurunan kadar COD/BOD dan pembentukan daya pada MFCs (Liu, 2008; Kristin 2012: 12).
2.2.5 Arsitektur Reaktor MFCs
Secara umum, desain reaktor MFCs dan pemilihan material sangat penting dan berpengaruh terhadap perfoma MFCs. Faktor utama dalam desain MFCs terdiri dari desain reaktor, jarak elektroda, tipe dan jenis separator, jumlah rasio dari elektroda (luas dan volume) , jenis elektroda dan pemilihan katalis, larutan maupun bio katoda (Borole et al., 2011: 4816)
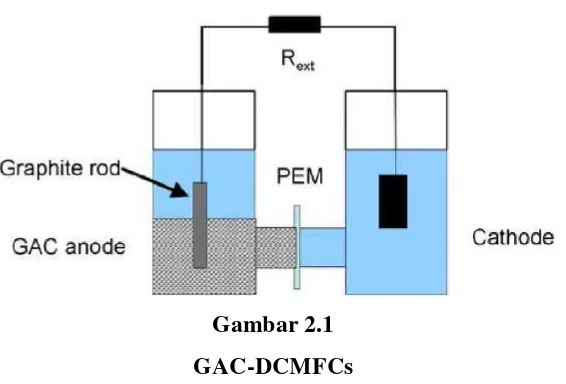
2.3 Granular Activated Carbon Dual Chamber MFCs (GAC-DCMFCs) MFCs dua kompartemen biasanya dijalankan dalam modus batch dengan media kimia tertentu seperti glukosa atau larutan asetat untuk menghasilkan energi. MFCs dua kompartemen saat ini hanya digunakan di laboratorium. Komponennya memiliki ruang anodik dan ruang katodik yang dihubungkan oleh PEM, atau kadang-kadang jembatan garam untuk memungkinkan proton bergerak melintasi ke katoda sementara mencegah difusi oksigen ke anoda. Kompartemen ini dapat dibuat dalam berbagai bentuk praktis (Du et al., 2007: 6).
Karbon aktif granular (GAC), media filter yang umum digunakan dalam proses pengolahan air limbah, merupakan bahan yang murah dan tahan lama dengan luas permukaan yang tinggi (minimal 1000 m2 /g), yang bisa meningkatkan adhesi bakteri dan dapat digunakan sebagai bahan anoda yang cocok di MFCs (Jiang, 2009: 31). Filter GAC telah digunakan selama 20 tahun untuk menghilangkan bahan organik terlarut oleh adsorpsi. Baru-baru ini, telah diketahui bahwa selain mengadsorpsi bahan organik, GAC juga merupakan bahan yang baik untuk pengembangan bakteri yang menempel. Granular Activated Carbon Dual Chamber MFCs merupakan modifikasi dari dual chamber MFCs dengan tambahan GAC di ruang anoda seperti desain penelitian Jiang et al.
Gambar 2.1 GAC-DCMFCs
Sumber: Jiang et al. (2009: 32)
Menurut Liu (2012), manfaat penggunaan GAC adalah kemampuannya untuk menyerap senyawa organik beracun yang mungkin menghambat mikroorganisme yang terlibat dalam sistem anaerobik di MFCs. GAC dapat memberikan luas area tinggi untuk perlekatan mikroba. Sifat tambahan dari GAC adalah konduktivitas listrik yang tinggi dan kemungkinan bahwa hal itu dapat berfungsi sebagai akseptor elektron. GAC adalah salah satu jenis elektroda yang efektif dalam MFCs karena mikroorganisme dapat mentransfer elektron ke GAC yang berfungsi sebagai elektroda di anoda. Produksi arus dalam MFCs dapat dibatasi oleh jumlah luas permukaan anoda tersedia untuk pembentukan biofilm, dan lambatnya kinetika degradasi substrat.
Gambar 2.2
2.4 Air Buangan sebagai Bahan Baku MFCs
Air buangan merupakan sisa buangan hasil suatu proses yang sudah tidak dipergunakan lagi, baik berupa sisa industri, rumah tangga, peternakan, pertanian, dan sebagainya. Dalam sistem MFCs, mikroba yang terdapat secara alami dalam air buangan dimanfaatkan untuk memproduksi energi listrik melalui reaksi yang memungkinkan terjadinya transpor elektron dari permukaan sel ke anoda. Energi listrik yang dihasilkan oleh konsorsium mikroba dalam sampel air buangan tanpa perlakuan khusus mungkin tidak cukup besar untuk dapat dimanfaatkan. Oleh karena itu, untuk meningkatkan perolehan energi listrik, akan dilakukan pengukuran secara seri dan optimasi terhadap sampel. Optimasi bertujuan untuk meningkatkan produksi energi listrik oleh konsorsium mikroba. Upaya ini juga diharapkan dapat menurunkan kadar pencemar pada sampel air buangan yang digunakan (Sitorus, 2010: 12).
2.5 Proses Pengolahan Biologi Secara Anaerob
Menurut Budhi dkk (1999: V-159), proses fermentasi anaerob pada dasarnya adalah proses pengubahan senyawa organik menjadi metana dan karbondioksida, tanpa kehadiran oksigen. Mengingat pengolahan ini tidak membutuhkan oksigen, secara otomatis dapat mengurangi kebutuhan energi, manjaga kestabilan efluen yang dihasilkan, produksi lumpur yang rendah, kebutuhan nutrisi rendah, dan menghasilkan biogas yang dapat dimanfaatkan (Grady dan Lim, 1980). Berikut ini tahapan dekomposisi seyawa organik secara anaerob menurut Menurut Budhi dkk(1999: V-159):
dan alkohol. Kemudian bakteri asetogenik menghidrolisis zat hasil fermentasi menjadi asam asetat, hidrogen, dan karbondioksida.
3. Proses pembentukan metana terutama berasal dari asam asetat, tetapi ada juga yang berasal dari hidrogen dan karbondioksida. Ada dua bakteri yang berperan, yaitu bakteri metana asetoklasik dan bakteri metana pengonsumsi hidrogen. Bakteri metana asetoklasik mengubah asam asetat menjadi metana dan karbondioksida. Bakteri ini mampu mengendalikan nilai pH proses fermentasi dengan jalan mengonsumsi asam asetat membentuk karbondioksida. Bakteri pengonsumsi hidrogen mengubah hidrogen bersama-sama dengan karbondioksida menjadi metana dan air.
2.6 Biofilter Tercelup (Biofilm)
Biofilm yang dikenal sebagai kumpulan lendir adalah kumpulan komunitas mikroba yang melekat secara bertahap membentuk endapan di atas permukaan dari operator (pembawa) yang akan mengakibatkan efisiensi limbah (pembawa) akan turun (Hui Huang dkk, 2014 : 2).
limbah sama dengan yang terjadi di lingkungan alami. Mikroorganisme yang ada pada biofilm akan mendegradasi senyawa organik yang ada di dalam air. Lapisan biofilm yang semakin tebal akan mengakibatkan berkurangnya difusi oksigen ke lapisan biofilm yang dibawahnya (Herlambang dan Said, 2010: 3)
Menurut Monroe (2007), ada 5 tahap pembentukan biofilm yaitu:
1. Pelekatan awal: mikrooganisme melekat pada permukaan suatu benda dan dapat diperantarai oleh fili (rambut halus sel) contohnya pada P.aeruginosa. 2. Pelekatan permanen: mikrooganisme melekat dengan bantuan eksopolisakarida
(EPS).
3. Maturasi I: proses pematangan biofilm tahap awal.
4. Maturasi II: proses pematangan biofilm tahap akhir, mikroorganisme siap untuk menyebar.
5. Dispersi: Sebagian mikroorganisme akan menyebar dan berkolonisasi di tempat lain.
2.7 Proses Pengolahan Biologi dengan Biakan Melekat
Proses biologis dengan biakan melekat yakni proses pengolahan limbah dimana mikroorganisme yang digunakan dibiakkan pada suatu media sehingga mikroorganisme tersebut melekat pada permukaan media. Proses ini disebut juga proses film mikrobiologis atau proses biofilm (Said, 2000: 101). Sistem pengolahan limbah dengan biakan melekat adalah sistem yang menggunakan reaktor dimana air limbah dikontakkan dengan film mikrobiologis yang dilekatkan pada permukaan media. Pada proses biakan melekat, mikroorganisme bertanggungjawab untuk mengubah materi organik atau nutrien dengan cara melekat pada packing material inert. Proses biakan melekat dapat dioperasikan pada proses aerob dan anaerob.
menghilangkan kekeruhan dan menjernihkan air. Pada umumnya proses biofilm dirancang untuk mengubah dan menghilangkan polutan organik dan senyawa ammonia (Said, 2000: 101).
Tabel 2.2
Keunggulan dan Kelemahan Proses Biakan Melekat
Keunggulan
Pengoperasian mudah
Lumpur yang dihasilkan sedikit
Mampu mengolah berbagai konsentrasi limbah Tahan terhadap fluktuasi debit dan konsentrasi Tahan terhadap penurunan suhu
Memerlukan lahan sedikit Estetis
Tidak ada masalah pada pengendapan lumpur Kemampuan pengolahan lebih efektif
Kelemahan
Menimbulkan bau
Padatan hasil sloughing tidak dapat dikontrol
Biayanya lebih besar dibanding pengolahan dengan lumpur aktif
Sumber: Said (2000: 102)
2.8 Mekanisme Biofilm dalam Mentransfer Elektron
Transfer elektron ekstraselular didefinisikan sebagai proses di mana elektron yang dilepaskan pada oksidasi donor elektron ditransfer keluar dari mikroorganisme menuju akseptor elektron ekstraselular. Menurut Leang et al., (2010: 4080), tiga mekanisme di mana elektron ditransfer dari mikroorganisme menuju anoda antara lain:
a) Transfer Elektron melalui Kontak Langsung antara Protein Redox-Aktif di Permukaan Sel Luar
biofilm, sedangkan OmcB berpartisipasi dalam transfer elektron dari biofilm ke anoda (Leang et al, 2010: 4080; Lovley, 2012: 396).
Gambar 2.3
Transfer Elektron melalui Kontak Langsung antara Protein Redox-Aktif di Permukaan Sel Luar
Sumber: Lovley, 2012
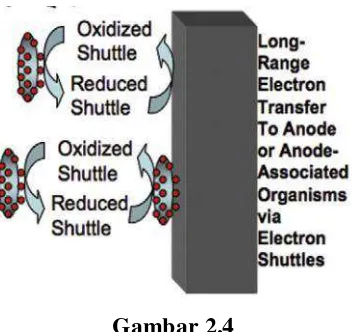
b) Transfer Elektron melalui Elektron Mediator Terlarut
Mediator elektron menyediakan sarana untuk mengantar elektron dari bagian dalam mikroorganisme menuju anoda. Mediator ini dapat diberikan secara eksternal untuk memudahkan transfer elektron (mediator eksogen), maupun diproduksi sendiri oleh mikroorganisme (mediator endogen).
Gambar 2.4
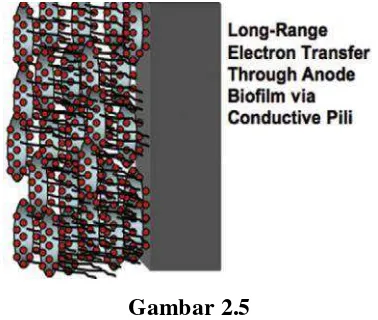
c) Konduksi Elektron menggunakan Nanowires
Nanowire ini dapat mendorong transfer elektron jangka panjang di biofilm multilayer setebal kira-kira 40-50 μm, dan juga bertindak sebagai komponen struktural pembentukan biofilm (Reguera et al., 2006).
Gambar 2.5
Konduksi Elektron menggunakan Nanowires Sumber: Lovley, 2012
2.9 Tahapan Penelitian 1. Seeding dan Aklimatisasi
Seeding atau pembenihan bertujuan untuk menumbuhkan dan mengembangbiakkan mikroorganisme di dalam substrat yang akan diolah
(Syafila, 2000: 243), sedangkan proses aklimatisasi dilakukan untuk mendapatkan
suatu kultur mikroorganisme yang stabil dan dapat beradaptasi dengan air
buangan. Proses aklimatisasi dilakukan dalam dua tahap, yaitu dengan konsentrasi air limbah sebesar 50% dan 100% untuk menghindari shock loading
(Himawan, 2012: 4). Apabila aklimatisasi berhasil yang ditandai dengan penurunan COD mencapai angka penurunan yang stabil (Fauzia, 2012: 32)
2. Running
berbeda dengan sistem sebelumnya yaitu dengan sistem kontinyu (Septyana, 2014: IV-6).
2.10 Kapasitas Adsorpsi
Isoterm adsorpsi adalah adsorpsi yang menggambarkan hubungan antara zat yang teradsorpsi oleh adsorben dengan tekanan atau konsentrasi pada keadaan kesetimbangan dan temperatur konstan. Persamaan yang sering digunakan untuk menggambarkan data percobaan isoterm telah dikembangkan oleh 1) Freundlich, 2) Langmuir, dan 3) Brunauer, Emmett, dan Teller (Isoterm BET) (Tchobanoglous et al., 1991:318).
Dalam sistem cair, isoterm adsorpsi menyatakan variasi adsorben dan adsorbat yang terjadi pada suhu konstan. Pada kondisi kesetimbangan terjadi distribusi larutan antara fasa cair dan fasa padat.Rasio dari distribusi tersebut merupakan fungsi konsentrasi dan larutan. Pada umumnya jumlah material yang diserap per satuan berat dari adsorben bertambah seiring dengan bertambahnya konsentrasi walaupun hal itu tidak selalu berbanding lurus.
1. Isotherm Freundlich
Bila diasumsikan bahwa volume cairan tidak mengalami perubahan selama proses adsorpsi berlangsung, pelarut sedikit sekali atau bahkan tidak terjerap dan volume adsorben tidak mengalami perubahan, maka akan berlaku persamaan empiris sebagai berikut:
q = k. Cn1
Keterangan:
q = konsentrasi maksimum adsorbat dalam adsorben dalam keadaan setimbang (gram/gram)
k dan n = konstanta dimana nilainya tergantung pada temperatur, jenis adsorben dan jenis unsur yang akan diserap (Sawyer, 2003)
C = konsentrasi zat terlarut pada saat setimbang (mg/l)
Log q = log K + 1 nlog C
2. Isotherm Langmuir
Langmuir menganggap permukaan suatu zat padat tediri dari ruang elementer yang masing-masing dapat mengadsorpsi suatu molekul gas. Langmuir mengandaikan bahwa semua ruang elementer tersebut adalah identik atau sama dalam afinitasnya untuk molekul gas dan adanya molekul ruang yang ada di dekatnya. Isotherm Langmuir mengasumsikan bahwa satu adsorbat mengikat satu bagian pada adsorben dan seluruh permukaan pada adsoerben mempunyai afinitas yag sama terhadap adsorbat (Sawyer, 2003). Pada isoterm Langmuir, adsorpsi terbatas pada lapisan tunggal dari molekul-molekul terlarut terlarut adsorbat tidak bebas berpindah ke permukaan.Model isotherm tersebut dikembangkan
berdasarkan serapan atau adsorpsi oleh “lapisan pertama” (monolayer) gas oleh fasa padat, kemudian diperluas untuk digunakan untuk digunakan pada adsorpsi zat terlarut oleh adsorbat padat dengan adsorpsi monolayer dan permukaan yang homogen (Kurniawan, 2005: 9).
Persamaan Langmuir ini didasarkan oleh kesetimbangan antara kondensasi dan evaporasi (penguapan) dari molekl yang terserap dengan memertimbangan lapisan jerap monokuler. Dari pernyataan di atas diperoleh persamaan Langmuir seperti di bawah ini (Sawyer, 2003):
q = qm
Kads. C 1 + Kads. C Keterangan :
q = konsentrasi adsorbat terjerap (massa adsorbat/ massa adsorben) biasanya disebut adsorption density (F)
qm = kapasitas maksimum adsorben
Kads = ukuran afinitas adsorat pada adsorben C = konsentrasi zat terlarut pada saat setimbang
1 ersamaan isotherm Brunnauer-Emmet-Teller (BET). Persamaan ini digunakan dengan asumsi untuk mendeskripsikan adsorpsi multilayer (Sundstrom, 1979). Selain itu asumsi pada model persamaan BET adalah:
1. Molekul terserap tidak berpindah ke permukaan
2. Entalpi adsorpsi konstan pada setiap molekul di setiap lapisan
3. Semua molekul di luar lapisan pertam amemiliki energi yang sama untuk adsorpsi
4. Untuk memulai pada lapisan yang lain lapisan sebelumnya tidak harus penuh
Berdasarkan asumsi diatas, bentuk persamaan BET adalah:
=
− 1 + −1 /
Keterangan :
Co = Konstanta awal larutan
kB = Konstanta (tergantung pada energi adsorpsi)
Persamaan tersebut dapat diubah menjadi persamaan linier menjadi persamaan seperti dibawah ini (Sundstrom, 1979).
− = dihasilkan melalui pengukuran menggunakan digital multimeter dan analog mikroampere. Dari data kuat arus dan tegangan, dapat diperoleh nilai power density (mW/m2), yaitu daya per satuan luas permukaan elektroda. Power density
� � mWm 2 = I mA X V(volt ) A(m2)
2.11.1 Kuat Arus Listrik
Menurut Utomo (2013), Kuat arus listrik ialah banyaknya muatan listrik yang mengalir tiap detik melalui suatu penghantar. Simbol kuat arus adalah I. Satuan kuat arus listrik ialah Ampere yang diambil dari nama seorang ilmuwan Perancis yaitu: Andrey Marie Ampere (1775 –1836). Misalkan bahwa dalam waktu t detik mengalir muatan listrik sebesar q coulomb dalam suatu penghantar berpenampang A, maka dirumuskan:
= atau q = I . t
Satuan = = ( ). Satuan lain untuk kuat arus misalnya
miliampere (mA) dan mikroampere (µA), dengan konversi 1 mA = 10-3A dan µA 10-6A. Sedangkan kuat arus untuk setiap satuan luas penampang dinamakan kerapatan arus. Rapat arus dinyatakan dengan:
= A/m2
Jumlah muatan adalah n x electron-elektron yang berpindah atau q = n. e Sehingga berlaku pula n .e = I .t
2.11.2 Tegangan Listrik
Tegangan listrik (kadang disebut sebagai voltase) adalah perbedaan potensial listrik antara dua titik dalam rangkaian listrik, dan dinyatakan dalam satuan volt. Besaran ini mengukur energi potensial dari sebuah medan listrik yang mengakibatkan adanya aliran listrik dalam sebuah konduktor listrik. (Wikipedia.com, 2014).
mengalirkan arus dinamakan gaya gerak listrik (ggl) yang diberi symbol ε. Satuan ggl adalah volt (V) (Utomo, 2013).
Beda potensial antara titik A dan B di luar sumber tegangan disebut tegangan jepit atau tegangan terpakai, dinyatakan dengan simbol VAB. Satuan beda potensial ialah volt. Konversi lain yang sering dipakai adalah satuan milivolt (mV). Dimana 1 mV = 10-3volt. Dua titik mempunyai beda potensial 1 volt, bila sumber arus mengeluarkan energi sebesar 1 joule untuk setiap coulnmb muatan yang dipindahkannya A ke B. Jika energi yang dikeluarkan sumber tegangan = W joule, muatan yang dipindahkan dari A ke B = q coulomb, maka beda potensial antara A dan B
= dalam Volt. Jadi 1 Volt = 1
2.11.3 Coulombic Efficiency (CE)
Coulombic Efficiency (CE) merupakan parameter penting untuk mengevaluasi kinerja MFCs. CE didefinisikan sebagai rasio dari muatan yang sebenarnya dihasilkan dengan muatan teoritis saat substrat sudah benar-benar dikonversi menjadi listrik. Perhitungan ini didasarkan pada persamaan dibawah ini mana I adalah arus, ∆COD adalah perubahan COD dalam larutan anoda, v adalah volume ruang anoda, 4 adalah mol elektron yang ditransfer ketika 1 mol oksigen teroksidasi, 32 g/mol adalah berat molekul oksigen dan F adalah konstanta Faraday (Jiang, 2009: 33).
2.12 Penelitian Terdahulu
Tabel 2.3
Penelitian Terdahulu Microbial Fuel Cells
Nama Judul Metode Kesimpulan
Dari arti katanya, hipotesis memang berasal dari 2 penggalan kata “hypo”
yang artinya “di bawah” dan “thesa” yang artinya “kebenaran”. Jadi hipotesis yang kemudian cara menulisnya disesuaikan dengan ejaan bahasa Indonesia menjadi hipotesa, dan berkembang menjadi hipotesis (Arikunto, 2010: 110).
H0: Terdapat hubungan yang positif antara COD dan pH dalam mempengaruhi efisiensi penurunan COD dan produksi listrik yang dihasilkan dalam reaktor GAC-DCMFCs
H1: Tidak ada hubungan yang positif antara COD dan pH dalam mempengaruhi efisiensi penurunan COD dan produksi listrik yang dihasilkan dalam reaktor GAC-DCMFCs
2.14 Variabel Bebas dan Terikat
Variabel bebas merupakan variabel yang mempengaruhi atau yang menjadi sebab perubahannya atau timbulnya variable dependent/ varibel terikat (Sugiyono, 2008). Variabel ini dapat diberi masukan, dimanipulasi. Variabel ini dianggap dapat menyebabkan, mengakibatkan atau mempengaruhi hasil tersebut. (Tahir, 201:,33). Sedangkan variabel terikat atau variabel dependen adalah tipe variabel yang dijelaskan atau dipengaruhi oleh variabel independen (Sangadji, 2010). Variabel ini adalah hasil atau akibat dari bagaimana variabel bebas dimanipulasi.
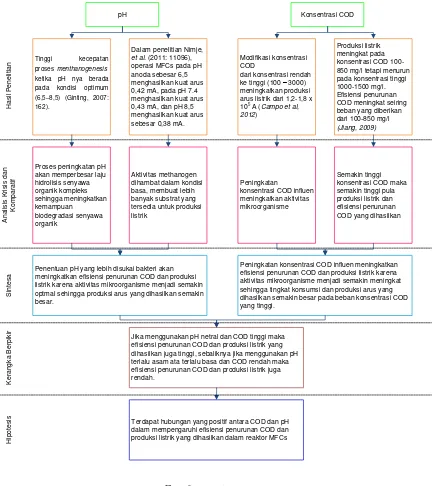
2.15 Kerangka Pikir Penelitian
pH
Tinggi kecepatan proses menthanogenesis
ketika pH nya berada pada kondisi optimum (6,5–8,5) (Ginting, 2007: arus listrik dari 1,2-1,8 x 105
Penentuan pH yang lebih disukai bakteri akan meningkatkan efisiensi penurunan COD dan produksi listrik karena aktivitas mikroorganisme menjadi semakin optmal sehingga produksi arus yang dihasilkan semakin besar.
Peningkatan konsentrasi COD influen meningkatkan efisiensi penurunan COD dan produksi listrik karena aktivitas mikroorganisme menjadi semakin meningkat sehingga tingkat konsumsi dan produksi arus yang dihasilkan semakin besar pada beban konsentrasi COD yang tinggi.
Jika menggunakan pH netral dan COD tinggi maka efisiensi penurunan COD dan produksi listrik yang dihasilkan juga tinggi, sebaliknya jika menggunakan pH terlalu asam ata terlalu basa dan COD rendah maka efisiensi penurunan COD dan produksi listrik juga rendah.
Terdapat hubungan yang positif antara COD dan pH dalam mempengaruhi efisiensi penurunan COD dan produksi listrik yang dihasilkan dalam reaktor MFCs
H
Meningkatnya aktivitas manusia, berbanding lurus dengan buangan (limbah) yang dihasilkan dari kegiatan sehari - hari. Adanya limbah tersebut berpotensi dapat menurunkan kualitas lingkungan. Untuk itu perlu adanya
III-1 BAB III
METODOLOGI PENELITIAN
3.1. Tujuan Operasional Penelitian
Dalam melakukan kegiatan penelitian, diperlukan suatu perumusan tujuan operasional penelitian. Tujuan operasional merupakan keterangan secara lengkap beserta data-data yang dibutuhkan untuk mendukung penelitian ketahap selanjutnya. Penelitian ini bertujuan untuk menjelaskan pengaruh variasi konsentrasi COD dan pH dalam kinerja GAC-DCMFCs. Untuk mempermudah penyampaian tujuan operasional dapat dilihat pada tabel di bawah ini. Tujuan yang hendak dicapai dari penelitian ini adalah:
Tabel 3.1
Tujuan Operasional Penelitian
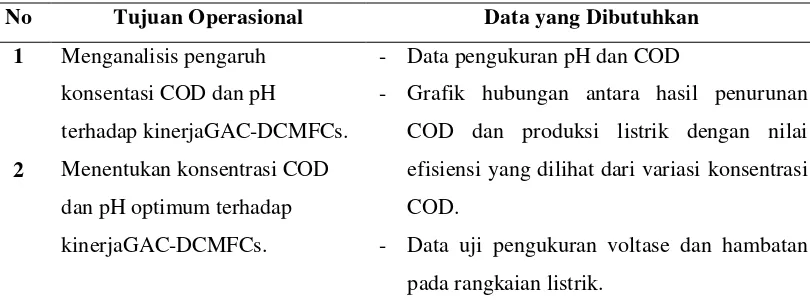
No Tujuan Operasional Data yang Dibutuhkan
1 Menganalisis pengaruh
konsentasi COD dan pH
terhadap kinerjaGAC-DCMFCs.
- Data pengukuran pH dan COD
- Grafik hubungan antara hasil penurunan
COD dan produksi listrik dengan nilai
efisiensi yang dilihat dari variasi konsentrasi
COD.
- Data uji pengukuran voltase dan hambatan
pada rangkaian listrik.
2 Menentukan konsentrasi COD
dan pH optimum terhadap
kinerjaGAC-DCMFCs.
3.2. Tempat dan Waktu Pelaksanaan Penelitian
3.3. Variabel Penelitian
Ada beberapa variabel yang digunakan dalam penelitian ini yaitu variabel bebas dan terikat. Berikut ini penjelasannya:
a. Variabel Bebas
Variabel bebas dalam penelitian ini adalah konsentrasi COD awal dan pH karena dianggap yang menyebabkan perubahan efisiensi dari COD dan jumlah produksi listrik yang dihasilkan.
b. Variabel Terikat
Pada penelitian ini yang menjadi variabel terikat adalah kinerja reaktor (penyisihan COD dan produksi listrik) yang akan dipengaruhi oleh adanya COD dan pH.
3.4. Teknik Pengumpulan Data
Pada tahap ini dilakukan proses pengumpulan data yang akan dibutuhkan untuk mengetahui tingkat penurunan kandungan COD dan produksi listrik yang optimum dari reaktor Microbial Fuel Cells. Data hasil dari penelitian ini bersifat kuantitatif yang merupakan hasil pengukuran dari analisis laboratorium.
3.4.1. Sumber Data a. Data Primer
Data-data primer yang dibutuhkan yaitu data COD inlet dan outlet, voltase, kuat arus, pH, dan suhu.
b. Data Sekunder
3.4.2. Sumber Pengumpulan Data a. Data Primer
Sumber pengumpulan data primer yaitu bersumber pada place dan paper.
Place merupakan data yang berasal dari sampel ke 9 reaktor dan paper berarti berasal dari hasil laboratorium.
b. Data Sekunder
Pengumpulan data sekunder ini bersumber dari paper yaitu buku dan jurnal dengan metode pengumpulan data dan/ didokumentasikan. Selebihnya data sekunder diperoleh dari hasil diskusi maupun bimbingan dosen dan narasumber terkait lainnya.
3.4.3. Metode Pengumpulan Data a. Data Primer
Proses pengumpulan data primer ini menggunakan tes yaitu uji laboratorium sehingga alat penggumpul datanya adalah alat-alat laboratorium. b. Data Sekunder
Pengumpulan data skunder ini bersumber dari paper yaitu buku dan jurnal dengan metode pengumpulan data dan didokumentasikan.
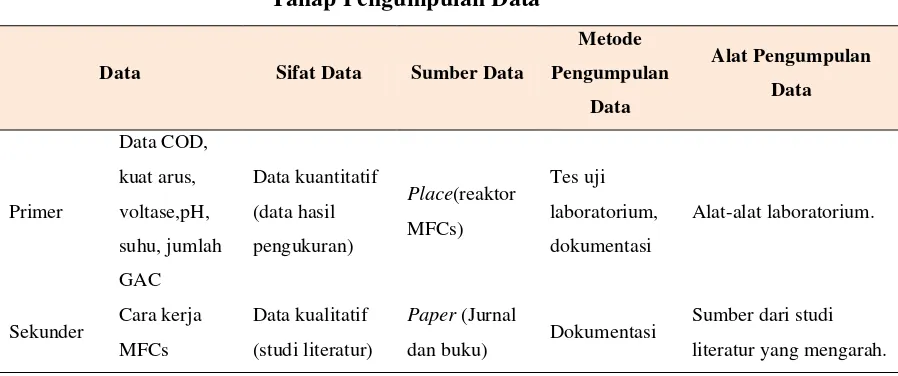
Tabel 3.2 menggambarkan tahapan pengumpulan data penelitian agar lebih jelas.
3.5. Alat dan Bahan
Dalam proses penelitian ini, alat dan bahan yang digunakan sebagai bahan aklimatisasi, analisis COD, pengukuran kuat arus, voltase serta reaktor penelitian adalah sebagai berikut.
A. Alat
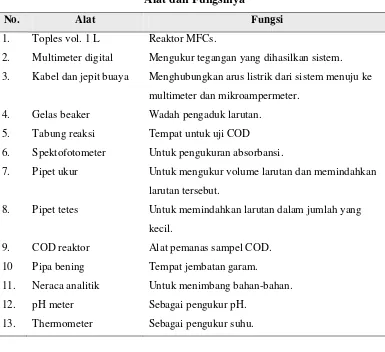
Alat yang digunakan untuk penelitian ini adalah sebagai berikut : Tabel 3.3
Alat dan Fungsinya
No. Alat Fungsi
1. Toples vol. 1 L Reaktor MFCs.
2. Multimeter digital Mengukur tegangan yang dihasilkan sistem.
3. Kabel dan jepit buaya Menghubungkan arus listrik dari sistem menuju ke
multimeter dan mikroampermeter.
4. Gelas beaker Wadah pengaduk larutan.
5. Tabung reaksi Tempat untuk uji COD
6. Spektofotometer Untuk pengukuran absorbansi.
7. Pipet ukur Untuk mengukur volume larutan dan memindahkan
larutan tersebut.
8. Pipet tetes Untuk memindahkan larutan dalam jumlah yang
kecil.
9. COD reaktor Alat pemanas sampel COD.
10 Pipa bening Tempat jembatan garam.
11. Neraca analitik Untuk menimbang bahan-bahan.
12. pH meter Sebagai pengukur pH.
13. Thermometer Sebagai pengukur suhu.
B. Bahan
Tabel 3.4 Bahan dan Fungsinya
No Bahan Fungsi
1. CH3COOH Bahan limbah artifisial
2. Glucose Monohydrate
3. Elektroda karbon baterai Elektroda penghantar listrik
4. Solution digestion (K2Cr2O7 + HgSO4) dan
pereaksi asam sulfat (H2SO4 + Ag2SO4)
Reagen COD
5. Aquadest Sebagai larutan pengencer
6. Agar dan NaCl Sebagai bahan jembatan garam
7. KMnO4 Sebagai larutan elektrolit di katoda
8. HCl 1 M Sebagai bahan preparasi elektroda
9. NaOH 1M Sebagai bahan preparasi elektroda
10. GAC Sebagai media lekat bakteri
3.6. Prosedur Penelitian
Pada penelitian ini terbagai menjadi tiga tahapan yaitu tahap persiapan, tahap pelaksanaan penelitian dan tahap analisis data.
3.6.1. Tahap Persiapan
Pada tahap ini dilakukan persiapan alat-alat yang akan digunakan dalam penelitian. Tahapan persiapan meliputi pembuatan reaktor, pembuatan limbah artifisial, pembuatan jembatan garam, preparasi elektroda, GAC, pembuatan larutan elektrolit dan persiapan alat dan bahan.
1. Pembuatan reaktor
Reaktor GAC-DCMFCs di buat berjumlah 9 pasang (ruang anoda-katoda), seluruh reaktor di buat duplikasinya. Desain reaktor adalah sebagai berikut:
V= 600 mL (Jiang dan Li, 2009).
Td= 10 jam = 600 menit (Jiang dan Li, 2009).
= �
� =
600
600 � = 1 / �
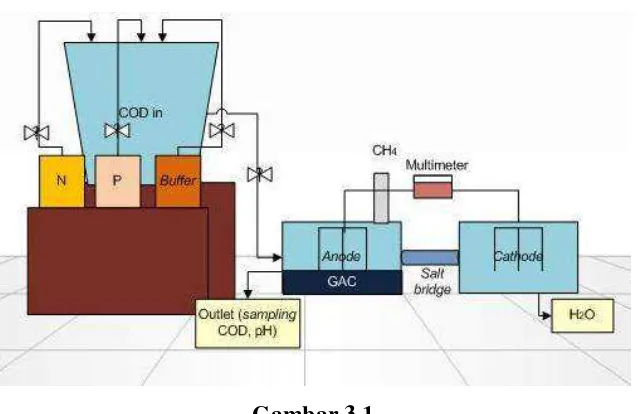
Gambar 3.1
Skematik Reaktor GAC-DCMFCs
Gambar 3.2
Gambar 3.3
Tampak Depan Reaktor GAC-DCMFCs
Gambar 3.4
Tabel 3.5
Keterangan Gambar 3.2. dan 3.3
No. Keterangan Fungsi
1 Bak inlet (limbah + nutrisi)
Bak penampung limbah yang akan di olah.
2 Buffer pH Larutan penyangga (HCl/ NaOH) yang digunakan untuk mempertahankan nilai pH.
3 Selang inlet Alat untuk menyalurkan limbah ke ruang anoda. 4 Tutup toples Mengondisikan ruangan anoda dalam suasana
anaerob.
5 Kabel Penyambung elektroda ke jepit buaya
6 Outlet gas Tempat pengukuran gas pada waktu tertentu. 7 Multimeter Alat untuk mengukur produksi listrik.
8 Elektroda graphite rod
Sebagai penghantar listrik, berjumlah masing-masing 5 buah pada ruang anoda dan katoda.
9 Selang outlet anoda Alat untuk menyalurkan limbah setelah pengolahan menuju outlet anoda.
10 Outlet anoda Tempat pengambilan sampel pH, COD. 11 Thermometer Alat untuk mengukur suhu setiap hari.
12 GAC Sebagai media lekat bakteri, terletak di ruang anoda sebanyak 300 gram.
13 Jembatan garam Media pentransfer proton, penghubung ruang anoda dan katoda.
14 Selang outlet katoda Alat untuk menyalurkan air menuju outlet anoda.
pada waktu-waktu yang telah direncanakan. Pada ruang katoda (aerobik) terdapat saluran outlet tempat keluarnya H2O. Ruang anoda dan katoda dihubungkan dengan sebuah jembatan garam. Kedua ruangan tersebut dilengkapi oleh elektroda yang terhubung dengan kabel menggunakan penjepit buaya, tetapi terdapat perbedaan didalam ruang anoda yang dilakukan penambahan GAC sebagai media lekat bakteri. Listrik yang dihasilkan oleh sistem dapat diukur menggunakan multimeter.
2. Pembuatan limbah artifisial
Limbah yang digunakan adalah limbah artifisial menggunakan asetat pro analis berupa asam asetat glasial dan glukosa monohidrat. COD yang terkandung di dalam limbah mempengaruhi hasil dari produksi listrik, sebagai sumber karbon untuk produksi listrik serta tujuan pengolahan air limbah. Asam asetat sangat mudah digunakan oleh mikroorganisme untuk menghasilkan energi karena memiliki rantai karbon yang paling rendah, (Du et al, 2007). Glukosa juga menjadi salah satu substrat yang paling digunakan dalam MFCs karena menghasilkan power density yang lebih besar daripada substrat yang lain walaupun glukosa memiliki couloumbic efficiency paling rendah karena glukosa merupakan substrat yang dapat difermentasi sehingga elektron yang dihasilkan lebih banyak digunakan untuk proses metanogenesis dan fermentasi (Lee et al, Du et al, 2007).
Mulai
Diagram Alir Proses Pembuatan Limbah Artifisial
Untuk membuat limbah artifisial mula-mula menyiapkan asam asetat dan glukosa dengan jumlah yang telah ditentukan dan dilakukan pengenceran masing-masing hingga mencapai volume 100 mL. Kemudian kedua larutan dicampur, maka didapatkan air limbah sebanyak 200 mL. Untuk mendapatkan volume limbah yang lebih besar, komposisi bahan pembuat air limbah artifisial ditambahkan sesuai kelipatannya. Setelah itu dilakukan pengaturan pH hingga mencapai suasana netral menggunakan larutan penyangga NaOH 5M (Jung, et al.,2011). Ketika pH sudah netral, sampel diambil sebanyak 2,5 mL dan dilakukan pengenceran sesuai kebutuhan konsentrasi COD (400 mg/L 1 kali, 800 mg/L 2 kali, 1200 mg/L 3 kali pengenceran). Setelah diencerkan, sampel dipipet ke tabung reaksi sebanyak 2,5 ml lalu ditambahkan 1,5 mL digestion solution dan 3,5 mL pereaksi asam sulfat. Sampel yang telah dibuat, dipanaskan di COD reaktor selama 2 jam dengan temperatur 150 °C. Selanjutnya sampel yang telah dipanaskan, didiamkan beberapa saat untuk menghilangkan panas dan bisa dilakukan analisis menggunankan spektrofotometer dengan panjang gelombang 600 nm (SNI 6989.2:2009).
pengolahan biologis yang optimum adalah 100:5:1 (Gray, 2004) sehingga pada penelitian ini, digunakan rasio tersebut.
Tabel 3.6 dalam 200 mL air limbah artifisial.
Massa KNO3 yang ditambahkan sebagai unsur N
Massa KNO3 =
Massa KH2PO4 yang ditambahkan sebagai unsur P
ditentukan dengan cara titrasi atau dengan bantuan spektrofotometer. Nilai COD teoritis dari senyawa tertentu dapat dihitung dari pertimbangan stoikiometri. Jika nilai teoritis ini sesuai dengan nilai eksperimental, disimpulkan bahwa oksidasi bahan organik selesai. Teoritis COD dari senyawa dengan rumus C struktural dapat ditentukan dari dua persamaan redoks yang menggambarkan reaksi oksidasi keseluruhan.
Setelah persamaan (1.1a) dan (1.1b) digabung maka menjadi:
CxHyOz + ¼·(4x+y-2z)·O2 → x·CO2 + y/2·H2O (1.1) Dari persamaan (1.1) dapat diketahui bahwa teori COD (atau kebutuhan oksigen teoritis) 1 mol senyawa CxHyOz berjumlah ¼ · (4x + y-2z) mol O2. Mengetahui bahwa massa molar CxHyOz dapat dinyatakan sebagai (12x+y+16z) g.mol-12 dan massa molar oksigen adalah 32 gram, dapat disimpulkan bahwa
1. Selama menguji COD bahan organik benar-benar teroksidasi, dan 2. Ketepatan dan kemampuan pengujian akurat.
Tabel 3.7
Nilai COD Teoritis per Unit Massa
Sumber: www.wastewaterhandbook.com
Perhitungan COD glukosa:
Nilai COD secara teoritis untuk 1 kg glukosa (C6H12O6) adalah Dari persamaan (1.2) dan diketahui bahwa x=6, y=12, dan z=6, maka CODt = 8.( (4.6)+(12)-(2.6))/ ((12.6)+(12)+(16.6))
= 192/180
= 1,067 mg COD/ mg C6H12O6 = 1,067 kg COD/ kg C6H12O6
Perhitungan COD asam asetat:
CODt = 8. ((4.2)+(4)-(2.2))/ ((12.2)+(4)+(16.2)) = 64/60
= 1,067 mg COD/ mg CH3COOH = 1,067 kg COD/ kg CH3COOH
Konversi COD ke metan
Satu mol metan membutuhkan 2 mol oksigen untuk mengoksidasinya menjadi karbondioksida dan air. Maka, satu gram metan yang diproduksi sama dengan penyisihan 4 gram COD. Reaksiya adalah (Rabaey et al, 2005):
CH4 + 2O2 → CO2 + 2H2O
3. Pembuatan jembatan garam
Jembatan garam dibuat dengan menggunakan agar pro analis 15 gram (Nair, 2013) dan ditambahkan dengan NaCl dengan konsentrasi tertentu. Pembuatan salt bridges dilakukan dengan menggunakan larutan NaCl 1M karena memiliki nilai produksi listrik yang tinggi dalam penelitian Kumar et al, (2012). Berikut ini perhitungan dalam preparasi NaCl 1 Molar dalam 250 ml:
Massa NaCl adalah = 58,45
4 = 14,6125 � �
Jadi dalam Preparasi Jembatan Garam NaCl 1 Molar dibutuhkan massa NaCl sebanyak 14,6125 gram. Adapun langkah pembuatan jembatan garam dapat dijelaskan di diagram alir di bawah ini:
Pengambilan air
Diagram Alir Proses Pembuatan Jembatan Garam
4. Persiapan elektroda karbon baterai
Mempersiapkan
Diagram Alir Proses Preparasi Elektroda
5. Persiapan media lekat GAC
Media lekat GAC digunakan untuk meningkatkan performa dalam menurunkan konsentrasi COD serta media perlekatan bakteri. Dalam preparasinya digunakan HCl dan NaOH 1 M yang diketahui dapat meningkatkan power density dan luas mikropori GAC (Wang et al., 2013). Mula-mula GAC direndam dalam larutan HCl 1M selama dua hari, lalu dibilas dengan air. Selanjutnya GAC direndam dalam larutan NaOH 1 M selama dua hari, dan dibilas kembali menggunakan air. Setelah dibilas, GAC dijemur dibawah sinar matahari, dan siap untuk digunakan. Untuk lebih jelasnya langkah dalam preparasi GAC dapat dilihat pada diagram alir berikut:
Merendam GAC
Diagram Alir Proses Preparasi GAC
6. Persiapan larutan elektolit KMnO4
Dalam penelitian ini digunakan larutan elektrolit KMnO4 dengan fungsi sebagai penerima donor proton dari cathode chamber. Dalam penelitian ini larutan KMnO4 digunakan dengan konsentrasi 0,15 M (Ardhianto, 2014).
Diketahui MR KMNO4= 158
7. Persiapan larutan penyangga (buffer)
Larutan penyangga, dapar atau buffer adalah larutan yang digunakan untuk mempertahankan nilai pH tertentu sesuai kebutuhan eksperimen agar tidak banyak berubah selama reaksi kimia berlangsung. Sifat yang khas dari larutan penyangga ini adalah pH-nya hanya berubah sedikit dengan pemberian sedikit asam kuat atau basa kuat.
Untuk membuat larutan penyangga, mula-mula menyiapkan pH meter yang sudah dikalibrasi untuk meningkatkan akurasi pengukurannya. Setelah itu, pH air limbah diukur. Lalu diteteskan larutan penyangga asam HCl 5 M untuk menurunkan pH, ataupun basa NaOH 5 M untuk meningkatkan pH (Jung, et al.,2011). Secara skematik langkah-langkah pembuatan larutan penyangga dapat dilihat pada gambar berikut ini:
Menyiapkan pH
Diagram Alir Proses Pembuatan Larutan Penyangga
8. Uji Batch Adsorpsi
Prosedur penelitian proses batch dilakukan seperti berikut (Panduan Praktikum Satuan Proses ITS, 2002):
1. GAC ditimbang dengan variasi berat yang telah ditentukan yaitu sebanyak 0, 100, 150, dan 250 gram kedalam 4 buah wadah dengan volume kerja 600 mL. Membuat air limbah artifisial dengan konsentrasi tertentu, lalu diuji COD.
2. 600 ml air limbah artifisial masing-masing dimasukkan kedalam wadah yang telah berisi GAC.
3. Dilakukan proses pengadukan dengan jartest selama 60 menit dengan kecepatan konstan yakni 90 rpm.
4. Sampel didiamkan selama 15 menit, kemudian diuji konsentrasi COD. 5. Menganalisis nilai COD pada seluruh sampel.
3.6.2. Tahapan Pelaksanaan Penelitian dan Pengambilan Data
Tahapan penelitian ini dimulai dari proses pengembang biakan bakteri, tahap aklimatisasi, pengoperasian reaktor GAC-DCMFCs dan pengambilan data.
1. Seeding dan aklimatisasi
3 hari Seeding dan Aklimatisasi
COD 800 mg/L + nutrisi
COD 400 mg/L + nutrisi COD 1200 mg/L + nutrisi
pH 7
Skema Penelitian Tahap Seeding dan Aklimatisasi
2. Pengoperasian Reaktor (Running)
Tahap running atau pengoperasian reaktor dimulai setelah tahap aklimatisasi menunjukkan COD removal secara stasioner. Berikut skema penelitian pada tahap running:
Running
COD 800 mg/L + nutrisi COD 1200 mg/L + nutrisi COD 400 mg/L + nutrisi
Kesembilan reaktor GAC-DCMFCs, dialiri oleh limbah artifisial dengan variasi konsentrasi COD 400, 800, dan 1200 mg/L serta ditambahkan unsur C, N, P dengan rasio 100: 5: 1 sebagai nutrisi untuk bakteri (Gray, 2004). Ketiga variasi COD tersebut di variasikan pula pH nya masing-masing 6, 7, dan 8 (Behera and
3.6.3. Teknik Analisis Data
Data yang telah dikumpulkan kemudian dianalisis dan hasil analisis tersebut dimasukan kedalam bab 4. Tujuan analisis data ini adalah untuk menyusun dan menganalisis data yang sudah diperoleh dari penelitian.
Adapun hal yang dianalisis adalah:
1. Pengaruh konsentasi COD dan pH terhadap kinerja GAC-DCMFCs. 2. Konsentrasi COD dan pH optimum terhadap kinerja GAC-DCMFCs. Hal diatas dapat dianalisis dengan mengetahui:
a. Hasil pengukuran COD selama running
b. Hasil pengukuran pH, suhu selama running
c. Hasil pengukuran voltase, kuat arus, dan hambatan selama running
3.7. Diagram Alir Penelitian
Mulai - Bahan untuk seeding bakteri - Bahan untuk analisis lab.
3.. Persipan Limbah Buatan - Pembuatan limbah artifisial menggunakan asam asetat
Seeding danAklimatisasi 1. Penurunan COD stasioner
Pengoperasian Reaktor
GAC-DCMFCs 1. Variabel Bebas- Konsentrasi COD awal - pH
Sesuai dengan diagram alir penelitian diatas, dapat dijelaskan bahwa sebelum dilakukan penelitian, penulis terlebih dahulu melakukan studi literatur untuk menguatkan hipotesis dari latar belakang masalah yang teah diambil sebelumnya. Setelah didapatkan beberapa studi literatur yang mendukung, penulis melakukan uji pendahuluan yaitu uji karakteristik air limbah, dalam hal ini karena air limbah yang digunakan adalah air limbah artifisial maka uji karakteristik air limbah diganti dengan pembuatan air limbah artifisial dengan bahan asam asetat.
C:N:P adalah 100:5:1 (Gray, 2004), dan bahan untuk tahap seeding. Tahap
seeding dan aklimatisasi dilaksanakan selama 14 hari dengan menggunakan substrat limbah artifisial dengan variasi pH 6, 7, 8. Ketika penurunan COD sudah stasioner dilanjutkan ke tahap running yaitu selama 35 hari. Pada tahap running
IV-1 BAB IV
HASIL DAN PEMBAHASAN
4.1 Uji Karakteristik Limbah Cair
Sebelum dilakukan pengoperasian reaktor MFCs, perlu dilakukan penelitian pendahuluan berupa uji karakteristik limbah cair domestik. Tujuan dari uji karakteristik ini adalah untuk menentukan berapa variasi konsentrasi yang akan digunakan sebagai susbstrat di sistem MFCs. Peneliti melakukan studi literatur terlebih dahulu selanjutnya melaksanakan uji karakteristik air limbah dengan mengambil sampel di lapangan. Sumber – sumber air limbah merupakan
grey water yang berasal dari perumahan A dan perumahan B, serta yang terakhir adalah air limbah tahu. Berikut adalah hasil uji karakteristik air limbah yang dapat dilihat pada tabel 4.1; 4.2; dan 4.3:
Tabel 4.1
Hasil Uji Karakteristik Grey Water Perumahan A No. Parameter Satuan Hasil Uji Baku Mutu
1. COD mg/l 381.7 10 mg/l**
2. pH - 7,34 6-9*
Keterangan:
* : Kepmen LH No. 112 Tahun 2003 ** : PP No. 82 Tahun 2001 Golongan I
Tabel 4.2
Hasil Uji Karakteristik Grey Water Perumahan B No. Parameter Satuan Hasil Uji Baku Mutu
1. COD mg/l 889.5 10 mg/l**
2. pH 7,12 6-9*
Keterangan:
Tabel 4.3
Hasil Uji Karakteristik Limbah Tahu
No. Parameter Satuan Hasil Uji Baku Mutu
Untuk mengetahui kemampuan adsorben GAC dalam mengadsorpsi COD yang terdapat dalam air limbah artifisial, maka dilakukan uji batch. Mula-mula GAC ditimbang dengan variasi berat yang telah ditentukan yaitu sebanyak 0, 100, 150, dan 200 gram kedalam 4 buah wadah dengan volume kerja 600 mL. Pemilihan variasi jumlah GAC tersebut dengan pertimbangan kesesuaian volume reaktor MFC dengan berat GAC per butirnya sehingga memerlukan variasi jumlah yang cukup besar. Selanjutnya dibuat limbah artifisial dengan nilai COD sekitar 800 mg/L. Air limbah artifisial selanjutnya dituangkan ke dalam wadah yang telah berisi GAC, lalu dilakukan pengadukan menggunankan alat jartest sebagai dengan kecepatan 90 rpm selama 60 menit. Setelah 15 menit, seluruh sampel diuji nilai CODnya dengan data yang disajikan pada tabel 4.4:
Tabel 4.4