PENETAPAN HARGA pKa DERIVAT ASAM ARIL ASETAT (Diklofenak, Ibuprofen dan Ketoprofen)
SECARA SPEKTROFOTOMETRI UV
SKRIPSI
Oleh:
HELVI DELIANA NIM: 060824052
FAKULTAS FARMASI
KATA PENGANTAR
Puji dan syukur kehadirat Allah yang Maha Kuasa yang telah
melimpahkan rahmat, karunia dan ridho-Nya, sehingga penulis dapat
menyelesaikan skripsi ini yang diajukan sebagai salah satu syarat dalam
memperoleh gelar sarjana farmasi pada Fakultas Farmasi Universitas Sumatera
Utara.
Penulis juga tidak lupa mengucapkan terima kasih dan penghargaan yang
tulus kepada orang tua tercinta, ayahnda Kasnan dan Ibunda Faizah, serta
adik-adikku dan seluruh keluarga atas doa, kasih sayang, dorongan semangat dan
pengorbanan baik moril maupun materil dalam menyelesaikan skripsi ini.
Ucapan terima kasih serta penghargaan juga ditujukan kepada:
1. Bapak Dekan dan para Pembantu Dekan Fakultas Farmasi Universitas
Sumatera Utara.
2. Bapak Drs. Isma’il, MSi, Apt dan Bapak Drs. Fathur Rahman Harun, MSi.,
Apt, yang telah membimbing dengan penuh kesabaran, tulus dan ikhlas selama
penelitian dan penulisan skripsi ini berlangsung.
3. Bapak Panitia Penguji atas segala arahan dan masukan yang sangat berarti
dalam penyempurnaan skripsi ini.
4. Ibu Dra. Marline Nainggolan MS., Apt., sebagai penasehat akademik atas
segala bimbingan selama proses perkuliahan.
5. Kepala dan para staf Laboratorium Kimia Kuantitatif atas seluruh fasilitas yang
6. Sahabat-sahabat penulis rekan-rekan mahasiswa farmasi ekstensi stambuk
2006, serta seluruh pihak yang telah memberikan bantuan, motivasi, dan
inspirasi bagi penulis selama masa perkuliahan sampai penyusunan skripsi ini.
Semoga Allah SWT memberikan balasan yang berlipat ganda atas jasa-jasa besar
mereka.
Penulis menyadari bahwa tulisan ini masih jauh dari kesempurnaan
sehingga membutuhkan banyak masukan dan kritikan. Namun penulis berharap
semoga skripsi ini dapat menjadi sumbangan berarti bagi ilmu pengetahuan
khususnya di bidang farmasi.
Medan, Januari 2009
Penulis,
ABSTRAK
Harga pKa yang diperoleh dari suatu senyawa dapat berbeda-beda,
tergantung metode yang digunakan pada penentuan harga pKa tersebut. Menurut
Moffat A.C. et al (2004), harga pKa dari derivat asam aril asetat; diklofenak 4,2;
ibuprofen 4,4 dan 5,2; dan ketoprofen 4,5 yang ditentukan dengan menggunakan
metode Spektrofotometri Ultraviolet multi panjang gelombang atau dengan istilah
Dip-Probe Spectroscopy (D-PAS), metode ini telah divalidasi dengan akurasi
yang tinggi. Dan menurut Foye (1996) harga pKa dari derivat asam aril aseat;
diklofenak belum diketahui; ibuprofen 5,2; dan ketoprofen 5,94, harga pKa ini
ditentukan dengan metode yang umum digunakan yaitu titrasi potensiometri dan
spektrofotometri.
Telah dilakukan penetapan harga pKa dari derivat asam aril asetat
(diklofenak, ibuprofen, ketoprofen) yang diproduksi oleh PT. Indofarma. Sampel
ditentukan secara spektrofotometri ultraviolet, dengan cara dilarutkan dalam
alkohol kemudian diencerkan dalam larutan NaOH 0,2 N, HCl 0,2 N dan larutan
dapar fosfat berbagai variasi pH., lalu diukur pada panjang gelombang 230 – 300
nm dengan alat spektrofotometer ultraviolet.
Hasil penetapan harga pKa diperoleh bahwa harga pKa rata-rata dari
diklofenak 4,75 dengan standar deviasi (SD) = 0,41; ibuprofen 5,32 dengan
standar deviasi (SD) = 0,17 dan ketoprofen 5,75 dengan standar deviasi (SD) =
0,35. Hasil pengujian statistik menunjukkan bahwa harga pKa rata-rata dari
bahan baku Diklofenak, Ibuprofen dan Ketoprofen tidak menunjukkan perbedaan
ABSTRACT
The pKa values have goten of the compounds can be different, suspinding
to the methode used on determinition of that pKa values. Based on Moffat A.C. et
al (2004), pKa values of derivate aryl acetic acid: diclofenac 4,2; ibuprofen 4,4
and 5,2; and ketoprofen 4,5 are determined by used UV multiwavelength
Spectrophotometric methode termed Dip-Probe Spectroscopy (or D-PAS), this
methode has been validated with high accuracy. And based on Foye (1996) pKa
values of derivate aryl acetic acid; not yet knowed for diclofenac; ibuprofen 5,2;
and ketoprofen 5,94, this pKa values determined by generally methode used that
are titration potentimetric and spectrophotometric.
Determining pKa values of derivate aryl acetic acid (diclofenac, ibuprofen,
ketoprofen) produced by PT. Indofarma. The sample determined by UV
spectrophotometric with dissolved in alcohol then diluted in NaOH 0,2 N, HCl 0,2
N solution and dapar phospat solution in various pH variation, then measured by
using UV spectrophotometric at wavelength 230-300 nm.
The result determined pKa values have goten that the range of average
pKa values of diclofenac 4,765 with standard deviation (SD) = 0,41; ibuprofen
5,32 with standard deviation (SD) = 0,17; and ketoprofen 5,75 with standard
deviation (SD) = 0,35. The result of statistical analysis showed that the range of
average pKa values of component part standard diclofenac, ibuprofen and
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
ABSTRAK ... iii
ABSTRACT ... iv
DAFTAR ISI ... v
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN ... x
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian... 3
BAB II METODOLOGI PENELITIAN ... 4
2.1 Alat – alat ... 4
2.2 Bahan – bahan ... 4
2.3 Prosedur ... 4
2.3.1 Pelaksanaan Penelitian ... 4
2.3.2 Pengambilan Sampel ... 4
2.3.3 Pembuatan Pereaksi ... 5
2.3.3.2 Pembuatan Larutan Dapar pH 4,2 – 6,2 ... 5
2.3.4 Penentuan serapan maksimum ... 6
2.3.5 Pembuatan larutan induk baku ... 7
2.3.6 Penetapan harga pKa sampel secara spektrofotometri ultraviolet .. 7
2.3.7 Analisa Data Secara Statistik ... 10
BAB III HASIL DAN PEMBAHASAN ... 11
3.1 Hasil Penentuan Konsentrasi ... 11
3.2 Hasil Penentuan Serapan Maksimum. ... 11
3.3 Penentuan Serapan Sampel dari Panjang Gelombang 230 – 300 nm ... 15
3.4 Hasil Pengukuran Serapan Sampel Dan Larutan Dapar Dengan Berbagai Variasi pH ... 27
3.5 Penetapan Harga pKa ... 28
BAB IV KESIMPULAN DAN SARAN ... 31
4.1 Kesimpulan ... 31
4.2 Saran ... 31
DAFTAR TABEL
Halaman
Tabel 1 Data serapan diklofenak baku dalam larutan NaOH 0,2 N
dengan konsentrasi 68 ppm ... 15
Tabel 2 Data serapan diklofenak baku dalam larutan HCl 0,2 N dengan
konsentrasi 68 ppm ... 15
Tabel 3 Data serapan diklofenak baku dalam larutan dapar pH 5,8
dengan konsentrasi 68 ppm ... 16
Tabel 4 Data serapan diklofenak baku dalam larutan dapar pH 5,4
dengan konsentrasi 68 ppm ... 16
Tabel 5 Data serapan diklofenak baku dalam larutan dapar pH 4,8
dengan konsentrasi 68 ppm ... 17
Tabel 6 Data serapan diklofenak baku dalam larutan dapar pH 4,2
dengan konsentrasi 68 ppm ... 17
Tabel 7 Data serapan ibuprofen baku dalam larutan NaOH 0,2 N
dengan konsentrasi 1640 ppm ... 19
Tabel 8 Data serapan ibuprofen baku dalam larutan HCl 0,2 N dengan
konsentrasi 1640 ppm ... 19
Tabel 9 Data serapan ibuprofen baku dalam larutan dapar pH 6,2
Tabel 10 Data serapan ibuprofen baku dalam larutan dapar pH 5,8
dengan konsentrasi 1640 ppm ... 20
Tabel 11 Data serapan ibuprofen baku dalam larutan dapar pH 5,4
dengan konsentrasi 1640 ppm ... 21
Tabel 12 Data serapan ibuprofen baku dalam larutan dapar pH 4,8
dengan konsentrasi 1640 ppm ... 21
Tabel 13 Data serapan ketoprofen baku dalam larutan NaOH 0,2 N
dengan konsentrasi 20 ppm ... 23
Tabel 14 Data serapan ketoprofen baku dalam larutan HCl 0,2 N dengan
konsentrasi 20 ppm ... 23
Tabel 15 Data serapan ketoprofen baku dalam larutan dapar pH 6,2
dengan konsentrasi 20 ppm ... 24
Tabel 16 Data serapan ketoprofen baku dalam larutan dapar pH 5,8
dengan konsentrasi 20 ppm ... 24
Tabel 17 Data serapan ketoprofen baku dalam larutan dapar pH 5,4
dengan konsentrasi 20 ppm ... 25
Tabel 18 Data serapan ketoprofen baku dalam larutan dapar pH 4,8
dengan konsentrasi 20 ppm ... 25
DAFTAR GAMBAR
Halaman
Gambar 1 Kurva serapan diklofenak dengan konsentrasi 13,6 ppm dan
panjang gelombang maksimum secara spektrofotometri
ultraviolet ... 12
Gambar 2 Kurva serapan Ibuprofen dengan konsentrasi 244 ppm dan
panjang gelombang maksimum secara spektrofotometri
ultraviolet ... 13
Gambar 3 . Kurva serapan ketoprofen dengan konsentrasi 6 ppm dan
panjang gelombang maksimum secara spektrofotometri
ultraviolet ... 14
Gambar 4 Kurva serapan diklofenak dengan konsentrasi 68 ppm dalam
berbagai suasana secara spektrofotometri ultraviolet ... 18
Gambar 5 Kurva serapan ibuprofen dengan konsentrasi 1640 ppm dalam
berbagai suasana secara spektrofotometri ultraviolet ... 22
Gambar 6 Kurva serapan ketoprofen dengan konsentrasi 20 ppm dalam
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Hasil perhitungan harga pKa Diklofenak secara
spektrofotometri ultraviolet ... 34
Lampiran 2 Hasil perhitungan harga pKa Ibuprofen secara spektrofotometri ultraviolet ... 36
Lampiran 3 Hasil perhitungan harga pKa Ketoprofen secara spektrofotometri ultraviolet ... 38
Lampiran 4 .. Analisa data Statistik harga pKa dari Diklofenak ... 40
Lampiran 5 Analisa data Statistik harga pKa dari Ibuprofen ... 41
Lampiran 6 Analisa data Statistik harga pKa dari Ketoprofen ... 42
Lampiran 7 Gambar alat ... 43
ABSTRAK
Harga pKa yang diperoleh dari suatu senyawa dapat berbeda-beda,
tergantung metode yang digunakan pada penentuan harga pKa tersebut. Menurut
Moffat A.C. et al (2004), harga pKa dari derivat asam aril asetat; diklofenak 4,2;
ibuprofen 4,4 dan 5,2; dan ketoprofen 4,5 yang ditentukan dengan menggunakan
metode Spektrofotometri Ultraviolet multi panjang gelombang atau dengan istilah
Dip-Probe Spectroscopy (D-PAS), metode ini telah divalidasi dengan akurasi
yang tinggi. Dan menurut Foye (1996) harga pKa dari derivat asam aril aseat;
diklofenak belum diketahui; ibuprofen 5,2; dan ketoprofen 5,94, harga pKa ini
ditentukan dengan metode yang umum digunakan yaitu titrasi potensiometri dan
spektrofotometri.
Telah dilakukan penetapan harga pKa dari derivat asam aril asetat
(diklofenak, ibuprofen, ketoprofen) yang diproduksi oleh PT. Indofarma. Sampel
ditentukan secara spektrofotometri ultraviolet, dengan cara dilarutkan dalam
alkohol kemudian diencerkan dalam larutan NaOH 0,2 N, HCl 0,2 N dan larutan
dapar fosfat berbagai variasi pH., lalu diukur pada panjang gelombang 230 – 300
nm dengan alat spektrofotometer ultraviolet.
Hasil penetapan harga pKa diperoleh bahwa harga pKa rata-rata dari
diklofenak 4,75 dengan standar deviasi (SD) = 0,41; ibuprofen 5,32 dengan
standar deviasi (SD) = 0,17 dan ketoprofen 5,75 dengan standar deviasi (SD) =
0,35. Hasil pengujian statistik menunjukkan bahwa harga pKa rata-rata dari
bahan baku Diklofenak, Ibuprofen dan Ketoprofen tidak menunjukkan perbedaan
ABSTRACT
The pKa values have goten of the compounds can be different, suspinding
to the methode used on determinition of that pKa values. Based on Moffat A.C. et
al (2004), pKa values of derivate aryl acetic acid: diclofenac 4,2; ibuprofen 4,4
and 5,2; and ketoprofen 4,5 are determined by used UV multiwavelength
Spectrophotometric methode termed Dip-Probe Spectroscopy (or D-PAS), this
methode has been validated with high accuracy. And based on Foye (1996) pKa
values of derivate aryl acetic acid; not yet knowed for diclofenac; ibuprofen 5,2;
and ketoprofen 5,94, this pKa values determined by generally methode used that
are titration potentimetric and spectrophotometric.
Determining pKa values of derivate aryl acetic acid (diclofenac, ibuprofen,
ketoprofen) produced by PT. Indofarma. The sample determined by UV
spectrophotometric with dissolved in alcohol then diluted in NaOH 0,2 N, HCl 0,2
N solution and dapar phospat solution in various pH variation, then measured by
using UV spectrophotometric at wavelength 230-300 nm.
The result determined pKa values have goten that the range of average
pKa values of diclofenac 4,765 with standard deviation (SD) = 0,41; ibuprofen
5,32 with standard deviation (SD) = 0,17; and ketoprofen 5,75 with standard
deviation (SD) = 0,35. The result of statistical analysis showed that the range of
average pKa values of component part standard diclofenac, ibuprofen and
BAB I PENDAHULUAN 1.1.Latar Belakang
Sifat fisika molekul organik seperti pKa ,efek sterik dan koefisien partisi
berhubungan erat dengan bidang farmasi. Sifat fisika molekul obat dan juga
reaksi-reaksi degradasi suatu obat memegang peranan yang penting dalam
mendesain metode analis. Bentuk molekul obat ada yang sederhana dan ada yang
sangat kompleks yang mengandung beberapa gugus fungsional (Rohman, 2007).
Gabungan beberapa gugus fungsional dalam satu molekul obat akan
menentukan secara keseluruhan sifat-sifat molekul obat tersebut. Ionisasi molekul
obat merupakan hal yang penting karena terkait dengan absorbsi obat dan
distribusinya dalam jaringan-jaringan tubuh. Nilai pKa suatu molekul terkait
dengan formulasi sediaan obat dan juga dalam desain metode analis untuk
keperluan penentuan kadarnya (Rohman, 2007).
Jadi harga pKa dapat digunakan untuk membandingkan kekuatan relatif
senyawa asam lemah maupun basa lemah dan juga dapat digunakan
bersama-sama dengan tetapan fisikokimia lain, termasuk data kelarutan dan koefisien
partisi, untuk berbagai jenis penerapan analitik, peracikan, dan penelitian (Foye,
1996).
Turunan asam aril asetat mempunyai aktivitas antiradang dan analgesik
yang tinggi, dan terutama digunakan sebagai antirematik (Siswandono&Sukardjo,
1995). Obat ini secara umum digunakan luas pada pengobatan rematoid dan
Semuanya diabsorbsi dengan baik pada pemberian per-oral dan hampir semuanya
terikat dengan albumin serum (Mycek, 2001).
Menurut Moffat A.C. et al (2004), harga pKa dari derivat asam aril asetat;
diklofenak 4,2; ibuprofen 4,4 dan 5,2; dan ketoprofen 4,5 yang ditentukan dengan
menggunakan metode Spektrofotometri Ultraviolet multi panjang gelombang atau
dengan istilah Dip-Probe Spectroscopy (D-PAS), metode ini telah divalidasi
dengan akurasi yang tinggi. Dan menurut Foye (1996) harga pKa dari derivat
asam aril aseat; diklofenak belum diketahui; ibuprofen 5,2; dan ketoprofen 5,94,
harga pKa ini ditentukan dengan metode yang umum digunakan yaitu titrasi
pot ensiometri dan spektrofotometri.
Selain metode diatas, harga pKa dapat juga ditentukan dengan
menggunakan tetapan σ Hammett yaitu berdasarkan gugus penarik elektron yang
tersubstitusi pada cincin aromatik, dengan cara ini diperoleh harga pKa untuk
ibuprofen 4,57; ketoprofen 4,53 sedangkan untuk diklofenak belum diketahui
(Siswandono&Soekardjo, 1998). Harga pKa yang diperoleh dari suatu senyawa
dapat berbeda-beda, tergantung metode yang digunakan pada penentuan harga
pKa tersebut (Foye, 1996).
Berdasarkan hal tersebut diatas, peneliti tertarik untuk melakukan
penelitian penetapan harga pKa dari derivat asam aril asetat yaitu Diklofenak,
Ibuprofen, Ketoprofen secara spektrofotometri ultraviolet. Pemilihan senyawa ini
berdasarkan khasiatnya sebagai anti rematik yang banyak digunakan serta
1.2 Perumusan Masalah
Apakah harga pKa dari derivat asam aril asetat (Diklofenak, Ibuprofen,
Ketoprofen) yang diperoleh berbeda dengan harga pKa yang terdapat dalam
literatur?
1.3 Hipotesis
Harga pKa dari derivat asam aril asetat (Diklofenak, Ibuprofen,
Ketoprofen) yang diperoleh berbeda dengan harga pKa yang terdapat dalam
literatur.
1.4 Tujuan
Untuk menentukan harga pKa dari derivat asam aril asetat (Diklofenak,
Ibuprofen ,Ketoprofen) secara spektrofotometri ultraviolet.
1.5 Manfaat
Diharapkan penelitian ini berguna dalam menentukan harga pKa dari
BAB II
TINJAUAN PUSTAKA 2.1 Uraian Umum
a. Diklofenak
Rumus Bangun :
Rumus Molekul : C14H11Cl2NO
Rumus bangun :
2
Sinonim : 2-[(2,6-Dichlorophenyl)amino]benzenacetic acid
Berat : 296,2
Pemerian : Serbuk kristal, putih atau agak kekuningan, agak higroskopis
Kelarutan : Praktis tidak larut dalam air; larut dalam alkohol; agak mudah
larut dalam aseton; sangat mudah larut dalam metil alkohol
Sinonim : α methyl-4-(2-Methylprophyl)benzenacetic acid
Berat : 206,3
Pemerian : Serbuk hablur, putih hingga hampir putih; berbau khas lemah.
Kelarutan : Praktis tidak larut dalam air; sangat mudah larut dalam etanol;
dalam metanol dalam aseton dan dalam klorofom; sukar larut
dalam etil asetat.
c. ketoprofen
Rumus Bangun :
Rumus Molekul : C16H14O3
Sinonim : 3-Benzoyl-α-methyl benzenacetic acid
Berat : 254,3
Pemerian : Serbuk hablur, putih atau hampir putih, tidak atau hampir
tidak berbau..
Kelarutan : Mudah larut dalam etanol, dalam kloroform dan dalam eter;
2.2 Analgetika Non Narkotik
Analgetik non narkotik digunakan untuk mengurangi rasa sakit yang
ringan sampai berat, sehingga sering disebut analgetik ringan, juga untuk
menrunkan suhu badan pada keadaan panas badan yang tinggi dan sebagai
antiradang untuk pengobatan rematik. Analgetika non narkotik bekerja pada
perifer dan sentral sistem saraf pusat. Obat ini mengadakan potensiasi dengan
obat-obat penekan saraf pusat.
Mekanisme Kerja 1. Analgesik
Analgetika non narkotika menimbulkan efek analgesik dengan menghambat
secara langsung dan selektif enzim-enzim pada sistem saraf pusat yang
mengkatalis biosintesis prostaglandin, seperti siklooksigenase sehingga mencegah
sensitasi reseptor rasa sakit oleh mediator-mediator rasa sakit, seperti bradikinin,
histamin serotonin, protasiklin, prostaglandin, ion-ion hidrogen dan kalium, yang
dapat merangsang rasa sakit secara mekanis atau kimiawi.
2. Antipiretik
Analgetika non narkotika menimbulkan efek antipiretik dengan meningkat
eliminasi panas, pada penderita dengan suhu badan tinggi, dengan cara
menimbulkan dilatasi buluh darah perifer dan mobilisasi air sehingga terjadi
pengenceran darah dan pengeluaran keringat. Pengaruh obat pada suhu badan
normal relatif kecil. Penurunan suhu tersebut adalah hasil kerja obat pada sistem
3. Antiradang
Keradangan timbul karena pengaktifan fosfolipase A2, enzim yang menyebabkan
pelepasan asam arakidonat,yang kemudian diubah menjadi prostaglandin oleh
prostaglandin sintetase. Analgetik non narkotik menimbulkan efek antiradang
melalui beberapa kemungkinan, antara lain adalah menghambat biosinteis dan
pengluaran prostaglandin dengan cara memblok secara terpulihkan enzim
siklooksigenase sehingga menurunkan gejala keradangan. Mekanisme yang lain
adalah menghambat enzim-enzim yang terlibat pada biosintesis mukopolisakarida
dan glikoprotein, meningkatkan pergantian jaringan kolagen dengan memperbaiki
jaringan penghubung dan mencegah pengeluaran enzim-enzim lisosom melalui
stabilisasi membran yang terkena radang. Analgetika non narkotik efektif untu
mengurangi keradangan tetapi tidak dapat mencegah kerusakan jaringan pada
penderita artritis.
Berdasarkan struktur kimianya obat antiradang bukan steroid dibagi
menjadi tujuh kelompok yaitu turunan salisilat, turunan 5-pirazolidindion, turunan
N-arilantranilat, turunan asam arilasetat, turunan heteroarilasetat, turunan
oksikam, dan turunan lain-lain.
TURUNAN ASAM ARILASETAT
Turunan ini mempunyai aktivitas antiradang analgesik yang tinggi, dan terutama
digunakan sebagai antirematik.
Contoh turunan asam arilasetat :
1. Diklofenak Na (Voltaren, Neurofenac) dan diklofenak K (Cataflam),
mempunyai aktivitas antirematik, antiradang dan analgesik-antipiretik,
berbagai keadaan rematik dan kelainan degeneratif pada sistem otot
rangka.
Diklofenak diserap secara cepat dan sempurna didalam lambung, kadar
plasma tertinggi dicapai 2 jam setelah pemberian oral, dengan waktu paruh
antara 6-15 jam.
Dosis : 25-50 mg 3 kali sehari
2. Ibuprofen (Brufen, Ifen, Motrin), mempunyai aktivitas antirematik,
antiradang dan analgesik-antipiretik, digunakan terutama untuk
mengurangi rasa nyeri akibat keradangan pada berbagai kondisi rematik
dan artritis.
Ibuprofen diserap dengan cepat dalam saluran cerna, kadar serum tertinggi
terjadi dalam 1-2 jam setelah pemberian oral, dengan waktu paruh 1,8-2
jam.
Dosis : 400 mg 3-4 kali sehari.
3. Ketoprofen (Profenid), mempunyai aktivitas antiradang dan
analgesik-antipiretik, digunakan terutama untuk mengurangi rasa nyeri akibat
keradangan pada berbagai keadaan rematik dan kelainan degeneratif pada
sistem otot rangka.
Ketoprofen diserap secara cepat dan sempurna dalam saluran cerna, kadar
plasma tertinggi dicapai dalam 0,5-1 jam setelah pemberian oral, dengan
waktu paruh 2-3 jam.
2.2 Hubungan struktur-aktivitas turunan asam arilasetat
Turunan asam ariasetat secara umum mempunyai gambaran struktur
sebagai berikut :
b. Mempunyai gugus karbonil atau ekivalennya seperti asam enolat,
sulfonamida yang terpisah oleh satu atom C dari inti aromatik datar.
Pemisahan dengan lebih dari sau atom C, misal pada turunan asam
propionat atau butirat, akan menurunkan aktivitas.
c. Adanya gugus α-metil pada rantai samping asetat dapat meningkatkan
aktivitas antiradangnya.
Contoh : ibufenak, tidak mempunyai gugus α-metil dan bersifat
hepatotoksik,turunan α-metilnya (ibuprofen) mempunyai aktivitas antir α
-metildang yang lebih tinggi dibanding ibufenak.
Makin panjang jumlah atom C aktivitasnya makin menurun.
d. Adanya α-substitusi menyebabkan senyawa bersifat optis-aktif dan
kadang-kadang isomer satu lebih aktif dibanding yang lain. Konfigurasi
yang aktif adalah bentuk isomer S.
Contoh : S( + )-ibuprofen lebih aktif disbanding isomer ( - ), sedang
isomer ( + ) dan ( - )-fenoprofen mempunyai aktivitas yang sama.
e. Mempunyai gugus hidrofob yang terikat pada atom C inti aromatikpada
posisi meta atau para dari gugus asetat.
f. Turunan ester dan amida juga mempunyai aktivitas antiradang secara in
vivo dihidrolisis menjadi bentuk asamnya. Demikian pula untuk turunan
alkohol dan aldehida, secara in vivo dioksidasi menjadi gugus karboksil.
2.3 Mekanisme Reaksi Diklofenak Ibuprofen dan Ketoprofen a. Diklofenak
b. Ibuprofen
a. Ketoprofen
3HC C
2.4 Sintesis Prostaglandin
PERU BAH AN ARAK H I DON AT
ASPI RI N I NDOMETASI N
I BUBRUFEN 2O2 AA SIKLOOKSIGENASE
OH O
O(O)H
O
O
PROSTAGLANDIN ENDOPEOCID H2 (G2) {PGH2{PGG2}]
PROSTASIKLIN SINTESIS
DENGAN PENATAAN ULANG
O PENATAAN ULANG TROMBOKSAN PENATAAN ULANG TROMBOKSAN
SINTESIS
OH O
O(O)H
+
2HC C
C O
O H
H
HYROXHEPTADECATRIONIKACID (HHT)
MALONALDEHID
1. SINTESIS PGE2 2. SINTESIS PGD2 3. SINTESIS PGF 2
OH O
O(O)H
O
O
1. PGE2 ; R1=O, R2 = α OH, H 2. PGD2 ; R1 = α OH, H, R2 = O 3. PGF2; R1 = R2 = αΟΗ, Η
2.3 Sifat Kimia Fisika dan Aktivitas Biologis
Salah satu sifat kimia fisika yang berhubungan dengan aktivitas biologis
dan penting dalam rancangan obat antara lain adalah ionisasi. Untuk dapat
menimbulkan aktivitas biologis, pada umumnya obat dalam bentuk tidak
terionisasi, tetapi adapula yang aktif dalam bentuk ionnya. Ionisasi sangat penting
dalam hubungannya dengan proses transpor obat dan interaksi obat-reseptor.
1. Obat Yang Aktif Dalam Bentuk Tidak Terionisasi
Sebagian besar obat yang bersifat asam atau basa lemah, bentuk tidak
terionisasinya dapat memberikan efek biologis. Hal ini dimungkinkan bila kerja
obat terjadi di membran sel atau didalam sel. Obat modern sebagian besar bersifat
elektrolit lemah, yaitu asam atau basa lemah, dan derajat ionisasi atau bentuk
Hubungan antara pKa dan fraksi obat terionisasi dan yang tidak terionisasi
dari obat yang bersifat asam dan basa lemah, dinyatakan melalui persamaan
Henderson-Hasselbach sebagai berikut :
Untuk asam lemah :
pKa = pH + log Cu/Ci
Cu : fraksi asam yang tidak terionisasi
Ci : fraksi asam terionisasi
Contoh :
RCOOH RCOO- + H+
pKa = pH + log (RCOOH) / (RCOO-) (H+
RNH
)
Untuk basa lemah :
pKa = pH + log Cu/Ci
Cu : fraksi basa yang tidak terionisasi
Ci : fraksi basa terionisasi
Contoh :
3+ RNH2 + H+
pKa = pH + log (RNH3+) / (RNH2
Pada obat yang bersifat asam lemah, dengan meningkatnya pH, sifat
ionisasi bertambah besar, bentuk tidak terionisasi berambah kecil, sehingga
jumlah obat yang menembus membran biologis semakin kecil. Akibatnya, )
Perubahan pH dapat berpengaruh terhadap sifat kelarutan dan koefisien
partisi obat. Garam dari asam atau basa lemah, bentuk tidak terionisasinya mudah
diabsorbsi oleh saluran cerna, dan aktivitas biologis sesuai dengan kadar obat
kemungkinan obat untuk berinteraksi dengan reseptor semakin rendah dan
aktivitas biologisnya semakin menurun.
Pada obat yang bersifat basa lemah, dengan meningkatnya pH, sifat
ionisasi bertambah kecil, bentuk tidak terionisasinya semakin besar, sehingga
jumlah obat yang menembus membran biologis bertambah besar pula. Akibatnya,
kemungkinan obat untuk berinteraksi dengan reseptor bertambah besar dan
aktivitas biologisnya semakin meningkat.
2. Obat Yang Aktif Dalam Bentuk Ion
Beberapa senyawa menunjukkan aktivitas biologis yang makin meningkat
bila derajat ionisasinya meningkat. Karena kesulitan bentuk ion untuk menembus
membran biologis diduga bahwa senyawa tipe ini memberikan efek biologis
diluar sel.
Bell dan Robin ( 1942), mengatakan bahwa aktivitas antibakteri turunan
sulfonamida mncapai maksimum bila mempunyai pKa 6-8. Pada pKa tersebut
sulfonamida terionisasi ± 50 %. Pada pKa 3-5, sulfonamida terionisasi sempurna,
dan bentuk ionisasi ini tidak dapat menembus membran sehingga aktivitas
antibakterinya rendah.
Bila kadar bentuk ion kurang lebih sama dengan kadar bentuk molekul
(pKa 6-8), aktivitas antibakterinya akan maksimal. Pada pKa 9-11, penurunan
pKa meningkatkan jumlah sulfonamida yang terionisasi, jumlah senyawa yang
menembus membran kecil, sehingga aktivitas antibakterinya rendah.
Harga pKa senyawa kimia yang terionisasi lemah merupakan ukuran yang
mudah dalam hal kecenderungannya melepaskan atau menarik proton dalam
larutan air. Secara tepat, pKa adalah logaritma negatif Ka yang secara matematika
tidak praktis atau tetapan disosiasi asam. Makin kuat senyawa asam, makin rendah
pKa-nya dan makin besar ionisasinya dalam air. Makin kuat senyawa basa, makin
tinggi pKa asam yang bersangkutan, dan makin besar ionisasinya dalam air.
Jadi harga pKa dapat digunakan untuk membandingkan kekuatan relatif
senyawa asam lemah maupun basa lemah. Harga pKa senyawa obat sering
digunakan bersama-sama dengan tetapan fisikokimia lain, termasuk data kelarutan
dan koefisien partisi, untuk berbagai jenis penerapan analitik, klinik, peracikan,
dan penelitian. Misalnya, diketahui bahwa yang menghasilkan efek farmakologi
hanyalah beberapa jenis obat yang terionisasi atau yang mempunyai
angka-banding tertentu antara yang terionisasi dan yang tidak teionisasi.
Suatu senyawa dapat mempunyai beberapa harga pKa, tergantung pada
jumlah gugus fungsi yang dapat terionisasi. Senyawa itu digolongkan sebagai
amfoter jika mempunyai substituen ionisasi asam (pemberi proton) maupun basa
(penerima proton), misalnya tetrasiklindan semua asam amino.
Harga pKa gugus pengionisasi terentu dapat sangat dipengaruhi oleh
adanya substituen kimia lain yang mengionisasi atau tidak mengionisasi dan
memberi dan menarik electron dalam sutau sistem resonansi atau induksi.
Penafsiran dasar-dasar kimia organik yang tepat dapat diterapkan dengan
memakai harga pKa senyawa yang telah pasti untuk memperkirakan pKa analog
2.7 SPEKTROFOTOMETRI
Spektrofotometri ultraviolet adalah salah satu cara analisa spektroskopik
yang memakai sumber radiasi elektromagnetik dekat (190-380) dengan memakai
instrumen spektrofotometer(Mulja dan Suharman, 1995).
Gugus fungsi yang menyerap radiasi didaerah ultraviolet dan daerah
tampak disebut kromofor dan hampir semua kromofor mempunyai ikatan tak
jenuh. Pada kromofor jenis ini transisi terjadi dari π → π*, yang menyerap pada λ
max kecil dari 200 nm (tidak terkonjugasi), isalnya pada >C=C< dan -C≡C-.
Kromofor ini merupakan tipe transisi dari sistem mengandung elektron π pada
orbital molekulnya. Untuk senyawa yang mempunyai sistem konjugasi, perbedaan
energi antara keadaan dasar dan keadaan tereksitasi menjadi lebih kecil sehingga
penyerapan terjadi pada panjang gelombang yang lebih besar (Noerdin, 1985;
Dachriyanus, 2004).
Gugus fungsi seperti –OH, -NH2, dan Cl yang mempunyai elektron
valensi bukan ikatan disebut auksokrom yang tidak menyerap radiasi pada
panjang gelombang yang lebih besar dari 200 nm, tetapi menyerap kuat pada
daerah ultraviolet jauh. Bila suatu auksokrom terikat pada suatu kromofor, maka
pita serapan kromofor bergeser ke panjang gelombang yang lebih panjang (efek
batokrom) dengan intensitas yang lebih kuat. Efek hipsokrom adalah suatu
pergeseran pita serapan ke panjang gelombang yang lebhh pendek, yag sering kali
terjadi bila muatan positif dimasukkan ke dalam molekul (Noerdin, 1985;
BAB III
METODOLOGI PENELITIAN 3.1 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah spektrofotometer
ultraviolet (Shimadzu 1240), pH meter (Hanna), neraca analitik (Vibra), alat-alat
gelas, pompa karet.
Bahan-bahan
Bahan-bahan yang digunakan dalam penelitian ini kecuali dinyatakan lain
berkualitas E. Merck, asam klorida, natrium hidroksida, kalium dihidrogen fosfat,
etanol 96 %; diklofenak (Indofarma), ibuprofen (Indofarma), ketoprofen
(Indofarma); aquadest (Lab Kimia Farmasi Kuantitatif).
3.3 Prosedur
3.3.1 Pelaksanaan Penelitian
Penelitian dilakukan di Laboratorium Kimia Farmasi Kuantitatif Fakultas
Farmasi USU.
3.3.2 Pengambilan Sampel
Metode pengambilan sampel dilakukan dengan cara sampling purposif
yang dikenal juga dengan sampling pertimbangan dimana sampel ditentukan atas
dasar pertimbangan bahwa sampel yang tidak terambil mempunyai karakteristik
3.3.3 Pembuatan Pereaksi
3.3.3.1 Pembuatan Larutan Asam Klorida 0,2 N
Diencerkan 20 ml HCl 35 % dengan air suling dalam labu tentukur sampai
volume 1000 ml (Ditjen POM, 1979)
3.3.3.2 Pembuatan Larutan Dapar pH 4,2 – 6,2 (Ditjen POM, 1979) Pembuatan larutan A (Kalium Dihidrogen Fosfat 0,2 M)
Sejumlah 27,218 gram Kalium dihidrogen fosfat dilarutkan dalam air
bebas CO2 hingga 1000 ml. (Ditjen POM, 1979)
Pembuatan larutan B (Natrium Hidroksida 0,2N)
Sejumlah 8 gram natrium hidroksida dilarutkan dalam air bebas CO2
hingga 1000 ml (Ditjen POM, 1979)
Pembuatan dapar 200 ml
Sejumlah larutan A ditambah sejumlah larutan B dengan volume tertentu,
diencerkan dengan air suling bebas CO2 sampai 200 ml. Kemudian pH diukur
dengan pH meter, apabila larutan terlalu asam ditambah tetes demi tetes larutan B
sampai pH yang dikehendaki. Sebaliknya apabila larutan terlalu basa ditambahkan
larutan A tetes demi tetes sampai pH yang dikehendaki.
Perbandingan larutan A dan B yang digunakan untuk membuat larutan
dapar 200 ml yaitu : pH 4,2 : 50,0 ml larutan A ditambah 0,4 ml larutan B
pH 4,8 : 50,0 ml larutan A ditambah 1,1 ml larutan B
pH 5,0 : 50,0 ml larutan A ditambah 2,1 ml larutan B
3.3.4 Pembuatan Natrium Diklofenak menjadi Diklofenak
Ke dalam beker glas dimasukkan sejumlah Natrium Diklofenak, kemudian
dilarutkan dengan aquadest hingga larut. Tambahkan sedikit demi sedikit larutan
HCl 0,2 N hingga terbentuk endapan putih, lalu tambahkan lagi sampai tidak
terbentuk endapan. Endapan yang terbentuk lalu disaring dan dibilas dengan
aquadest. Kemudian endapan dimasukkan ke dalam crush porselen dan
dikeringkan dalam oven pada suhu ± 110 º C selama 1 jam.
3.3.5 Penentuan Serapan Maksimum a. Diklofenak
Ditimbang seksama sejumlah 34 mg diklofenak baku, dimasukkan dalam
labu tentukur 100 ml, dilarutkan dengan NaOH 0,1 N dan dicukupkan
volumenya sampai garis tanda sehingga diperoleh konsentrasi 340 ppm
(larutan induk baku)
Dipipet 2 ml dari larutan induk baku, dimasukkan ke dalam labu tentukur
50 ml, dicukupkan dengan NaOH 0,1 N sampai garis tanda sehingga
konsentrasinya menjadi 13,6 ppm. Kemudian diukur serapannya pada panjang
gelombang 200 – 400 nm. (gambar 1 hal:12)
b. Ibuprofen
Ditimbang seksama sejumlah 610 mg diklofenak baku, dimasukkan dalam
labu tentukur 100 ml, dilarutkan dengan NaOH 0,1 N dan dicukupkan
volumenya sampai garis tanda sehingga diperoleh konsentrasi 6100 ppm
Dipipet 2 ml dari larutan induk baku, dimasukkan ke dalam labu tentukur
50 ml, dicukupkan dengan NaOH 0,1 N sampai garis tanda sehingga
konsentrasinya menjadi 244 ppm. Kemudian diukur serapannya pada panjang
gelombang 200 – 400 nm. (gambar 2 hal:13)
c. Ketoprofen
Ditimbang seksama sejumlah 15 mg diklofenak baku, dimasukkan dalam
labu tentukur 100 ml, dilarutkan dengan NaOH 0,1 N dan dicukupkan
volumenya sampai garis tanda sehingga diperoleh konsentrasi 150 ppm
(larutan induk baku)
Dipipet 2 ml dari larutan induk baku, dimasukkan ke dalam labu tentukur
50 ml, dicukupkan dengan NaOH 0,1 N sampai garis tanda sehingga
konsentrasinya menjadi 6 ppm. Kemudian diukur serapannya pada panjang
gelombang 200 – 400 nm. (gambar 3 hal:14)
3.3.6 Pembuatan Larutan Induk Baku a. Diklofenak
Ditimbang seksama sejumlah 34 mg diklofenak baku dimasukkan ke
dalam labu takar 250 ml (136 ppm), dilarutkan dengan etanol 96 % kemudian
ditambahkan sedikit demi sedikit sampai garis tanda.
b. Ibuprofen
Ditimbang seksama sejumlah 820 mg ibuprofen baku dimasukkan ke
dalam labu takar 250 ml (3280 ppm), dilarutkan dengan etanol 96 % kemudian
c. Ketoprofen
Ditimbang seksama sejumlah 10 mg ketoprofen baku dimasukkan ke
dalam labu takar 250 ml (40 ppm), dilarutkan dengan etanol 96 % kemudian
ditambahkan sedikit demi sedikit sampai garis tanda.
3.3.7 Penetapan Harga Pka Sampel Secara Spektrofotometri Ultraviolet a. Diklofenak
• Dipipet 25 ml larutan induk baku dimasukkan ke dalam labu tentukur 50
ml. Kemudian diencerkan dengan larutan NaOH 0,2 N.(68 ppm)
• Dipipet 25 ml larutan induk baku dimasukkan ke dalam labu tentukur 50
ml. Kemudian diencerkan dengan larutan HCl 0,2 N.
• Dipipet 25 ml larutan induk baku dimasukkan ke dalam labu tentukur 50
ml. Kemudian diencerkan dengan larutan dapar fosfat pH 5,8.
• Dipipet 25 ml larutan induk baku dimasukkan ke dalam labu tentukur 50
ml. Kemudian diencerkan dengan larutan dapar fosfat pH 5,4.
• Dipipet 25 ml larutan induk baku dimasukkan ke dalam labu tentukur 50
ml. Kemudian diencerkan dengan larutan dapar fosfat pH 4,8.
• Dipipet 25 ml larutan induk baku dimasukkan ke dalam labu tentukur 50
ml. Kemudian diencerkan dengan larutan dapar fosfat pH 4,2
• Diukur pH nya dengan pH meter dan dicatat (sebagai dasar perhitungan).
• Kemudian diukur resapannya dari λ 230 sampai 300 nm. (gambar 4 hal:18)
b. Ibuprofen
• Dipipet 25 ml larutan induk baku dimasukkan ke dalam labu tentukur 50
• Dipipet 25 ml larutan induk baku dimasukkan ke dalam labu tentukur 50
ml. Kemudian diencerkan dengan larutan HCl 0,2 N.
• Dipipet 25 ml larutan induk baku dimasukkan ke dalam labu tentukur 50
ml. Kemudian diencerkan dengan larutan dapar fosfat pH 6,2.
• Dipipet 25 ml larutan induk baku dimasukkan ke dalam labu tentukur 50
ml. Kemudian diencerkan dengan larutan dapar fosfat pH 5,8.
• Dipipet 25 ml larutan induk baku dimasukkan ke dalam labu tentukur 50
ml. Kemudian diencerkan dengan larutan dapar fosfat pH 5,4.
• Dipipet 25 ml larutan induk baku dimasukkan ke dalam labu tentukur 50
ml. Kemudian diencerkan dengan larutan dapar fosfat pH 4,8
• Diukur pH nya dengan pH meter dan dicatat (sebagai dasar perhitungan).
• Kemudian diukur resapannya dari λ 230 sampai 300 nm. (gambar 5 hal:22)
c. Ketoprofen
• Dipipet 25 ml larutan induk baku dimasukkan ke dalam labu tentukur 50
ml. Kemudian diencerkan dengan larutan NaOH 0,2 N.(20 ppm)
• Dipipet 25 ml larutan induk baku dimasukkan ke dalam labu tentukur 50
ml. Kemudian diencerkan dengan larutan HCl 0,2 N.
• Dipipet 25 ml larutan induk baku dimasukkan ke dalam labu tentukur 50
ml. Kemudian diencerkan dengan larutan dapar fosfat pH 6,2.
• Dipipet 25 ml larutan induk baku dimasukkan ke dalam labu tentukur 50
ml. Kemudian diencerkan dengan larutan dapar fosfat pH 5,8.
• Dipipet 25 ml larutan induk baku dimasukkan ke dalam labu tentukur 50
ml. Kemudian diencerkan dengan larutan dapar fosfat pH 4,8.
• Diukur pH nya dengan pH meter dan dicatat (sebagai dasar perhitungan).
• Kemudian diukur resapannya dari λ 230 sampai 300 nm. (gambar 6 hal 26)
Dihitung harga pKa masing-masing dengan rumus :
HA buffer
buffer A
A A
A A pKa
pH
− − +
= −
log
dimana :
AA- = absorbansi anion
AHA = absorbansi asam bebas
A buffer = absorbansi campuran anion dan molekul asam bebas
2.3.7 Analisa Data Secara Statistik
Untuk menghitung standar deviasi digunakan rumus :
1
2
− −
=
∑
−
n x x SD
Keterangan:
SD = standar deviasi; x = pKa sampel; x = pKa rata-rata sampel; −
n = jumlah perlakuan
Untuk menghitung t hitung
(
)
n
SD
x
x
t
hitung=
−
digunakan rumus ;
Dimana:
x = pKa sampel; −
x = pKa rata-rata sampel; SD = Standar deviasi;
n = jumlah perlakuan
Dengan dasar penolakan data adalah : t hitung > t tabel atau t hitung < -t tabel dan
BAB III
HASIL DAN PEMBAHASAN 3.1 Hasil Penentuan Konsentrasi
Untuk mengetahui konsentrasi pengukuran yang terbaik perlu dilakukan
orientasi terhadap kurva serapan dari masing-masing sampel. Konsentrasi yang
diinginkan yaitu konsentrasi yang dapat menunjukkan perbedaan absorbansi yang
besar antara larutan sampel dalam suasana basa dan suasana asam.
Dari hasil orientasi untuk membuat kurva serapan dari ketiga sampel yaitu
diklofenak, ibuprofen, dan ketoprofen yang dapat menunjukkan perbedaan
absorbansi yang besar antara larutan sampel dalam suasana basa dan suasana
asam, diperoleh absorbansi diklofenak pada konsentrasi 68 ppm; ibuprofen 1640
ppm; dan ketoprofen 20 ppm.
3.2 Hasil Penentuan Serapan Maksimum
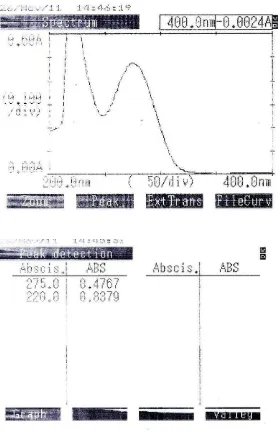
Menurut Moffat A.C. et al (2004), diklofenak memberikan serapan
maksimum pada panjang gelombang 275 nm dalam pelarut NaOH 0,1 N dengan
A11 = 351b. Dari hasil pengukuran panjang gelombang maksimum diklofenak
baku dalam pelarut NaOH 0,1 N secara spektrofotometri ultraviolet diperoleh
Gambar 1. Kurva serapan diklofenak dengan konsentrasi 13,6 ppm dan panjang
gelombang maksimum secara spektrofotometri ultraviolet
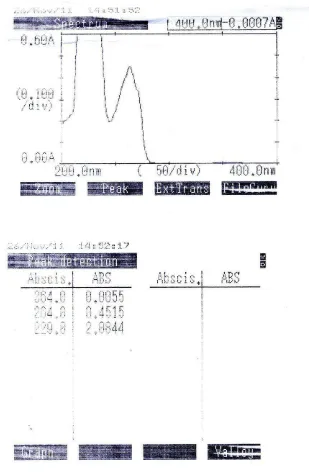
Ibuprofen memberikan serapan maksimum pada panjang gelombang 265
nm dalam pelarut NaOH 0,1 N dengan A11 = 18,5a. Dan menurut USP XXII
ibuprofen memberikan serapan maksimum pada panjang gelombang 264 nm dan
Dari hasil pengukuran panjang gelombang maksimum ibuprofen baku
dalam pelarut NaOH 0,1 N secara spektrofotometri ultraviolet diperoleh serapan
maksimum pada panjang gelombang 264 nm seperti (gambar 2)
Gambar 2. Kurva serapan Ibuprofen dengan konsentrasi 244 ppm dan panjang
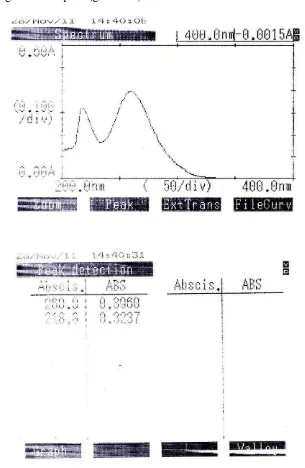
Ketoprofen memberikan serapan maksimum pada panjang gelombang 262
nm dalam pelarut NaOH 0,1 N dengan A11 = 647a. Dari hasil pengukuran panjang
gelombang maksimum ketoprofen baku dalam pelarut NaOH 0,1 N secara
spektrofotometri ultraviolet diperoleh serapan maksimum pada panjang
Dari hasil pengukuran serapan maksimum dalam pelarut NaOH 0,1 N
secara spektrofotometri ultraviolet pada masing-masing sampel diperoleh bahwa
serapan maksimum ini memenuhi persyaratan serapan maksimum yaitu lebih
kurang 2 nm dari λ maksimum yang terdapat dalam literatur (FI edisi IV. 1995).
3.3 Penentuan Serapan Sampel dari Panjang Gelombang 230 – 300 nm b. diklofenak
Tabel 1. Data serapan diklofenak baku dalam larutan NaOH 0,2 N dengan
konsentrasi 68 ppm
Tabel 2. Data serapan diklofenak baku dalam larutan HCl 0,2 N dengan
Tabel 3. Data serapan diklofenak baku dalam larutan dapar pH 5,8 dengan
konsentrasi 68 ppm
Tabel 4. Data serapan diklofenak baku dalam larutan dapar pH 5,4 dengan
Tabel 5. Data serapan diklofenak baku dalam larutan dapar pH 4,8 dengan
konsentrasi 68 ppm
Tabel 6. Data serapan diklofenak baku dalam larutan dapar pH 4,2 dengan
0.8 1.2 1.6 2 2.4
240 245 250 255 260 265 270 275 280 285 290 295 300
panjang gelombang (nm)
a
b
s
o
r
b
a
n
s
i
Series1 Series2 Series3 Series4 Series5 Series6
Gambar 4. Kurva serapan diklofenak dengan konsentrasi 68 ppm dalam berbagai
suasana secara spektrofotometri ultraviolet
Keterangan : series 1 dalam NaOH 0,2 N
series 2 dalam HCl 0,2 N
series 3 dalam dapar pH 5,8
c. Ibuprofen
Tabel 7. Data serapan ibuprofen baku dalam larutan NaOH 0,2 N dengan
konsentrasi 1640 ppm
Tabel 8. Data serapan ibuprofen baku dalam larutan HCl 0,2 N dengan
konsentrasi 1640 ppm
Tabel 9. Data serapan ibuprofen baku dalam larutan dapar pH 6,2 dengan
konsentrasi 1640 ppm
Tabel 10. Data serapan ibuprofen baku dalam larutan dapar pH 5,8 dengan
Tabel 11. Data serapan ibuprofen baku dalam larutan dapar pH 5,4 dengan
konsentrasi 1640 ppm
Tabel 12. Data serapan ibuprofen baku dalam larutan dapar pH 4,8 dengan
0 0.5 1 1.5 2
240 245 250 255 260 265 270 275 280 285 290 295 300
panjang gelom bang (nm )
a
b
s
o
rb
a
n
s
i
Series1 Series2 Series3 Series4 Series5 Series6
Gambar 5. Kurva serapan ibuprofen dengan konsentrasi 1640 ppm dalam
berbagai suasana secara spektrofotometri ultraviolet
Keterangan : series 1 dalam NaOH 0,2 N
series 2 dalam HCl 0,2 N
series 3 dalam dapar pH 6,2
series 4 dalam dapar pH 5,8
d. Ketoprofen
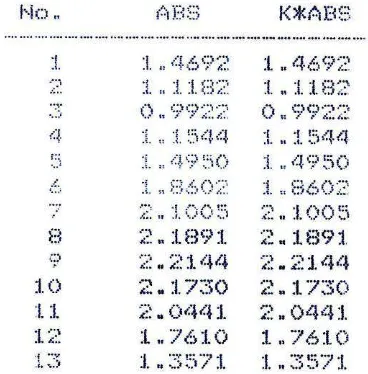
Tabel 13. Data serapan ketoprofen baku dalam larutan NaOH 0,2 N dengan
konsentrasi 20 ppm
Tabel 14. Data serapan ketoprofen baku dalam larutan HCl 0,2 N dengan
Tabel 15. Data serapan ketoprofen baku dalam larutan dapar pH 6,2 dengan
konsentrasi 20 ppm
Tabel 16. Data serapan ketoprofen baku dalam larutan dapar pH 5,8 dengan
Tabel 17. Data serapan ketoprofen baku dalam larutan dapar pH 5,4 dengan
konsentrasi 20 ppm
Tabel 18. Data serapan ketoprofen baku dalam larutan dapar pH 4,8 dengan
0.2 0.4 0.6 0.8 1 1.2 1.4
220 225 230 235 240 245 250 255 260 265 270 275 280 285 290 295
panjang gelombang (nm)
a
b
s
o
r
b
a
n
s
i
Series1 Series2 Series3 Series4 Series5 Series6
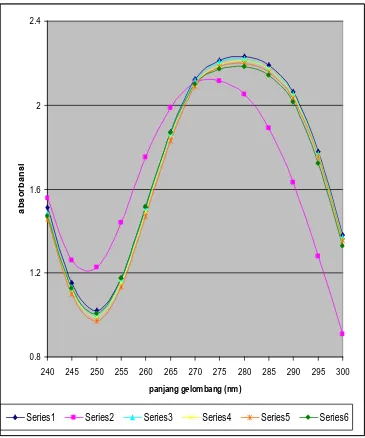
Gambar 6. Kurva serapan ketoprofen dengan konsentrasi 20 ppm dalam berbagai
suasana secara spektrofotometri ultraviolet
Keterangan : series 1 dalam NaOH 0,2 N
series 2 dalam HCl 0,2 N
series 3 dalam dapar pH 6,2
series 4 dalam dapar pH 5,8
3.4 Hasil Pengukuran Serapan Sampel dalam Larutan NaOH 0,2 N, Larutan HCl 0,2 N dan Larutan Dapar Dengan Berbagai Variasi pH
a. diklofenak
Larutan dapar dengan berbagai variasi pH setelah ditambah dengan larutan
diklofenak sama banyak dan diukur pHnya dengan pH meter diperoleh pH
larutan dengan serapan sebagai berikut :
NaOH 0,2 N dengan absorbansi 1,7798
HCl 0,2 N dengan absorbansi 1,2799
Dapar pH 5,8 menjadi 6,8 dengan absorbansi 1,7672
Dapar pH 5,4 menjadi 6,4 dengan absorbansi 1,761
Dapar pH 4,8 menjadi 5,8 dengan absorbansi 1,755
Dapar pH 4,2 menjadi 5,2 dengan absorbansi 1,723
b. Ibuprofen
Larutan dapar dengan berbagai variasi pH setelah ditambah dengan larutan
ibuprofen sama banyak dan diukur pHnya dengan pH meter diperoleh pH
larutan dengan serapan sebagai berikut :
NaOH 0,2 N dengan absorbansi 2,0620
HCl 0,2 N dengan absorbansi 1,8270
Dapar pH 6,2 menjadi 5,9 dengan absorbansi 1,9943
Dapar pH 5,8 menjadi 5,3 dengan absorbansi 1,9355
Dapar pH 5,4 menjadi 4,8 dengan absorbansi 1,8799
c. Ketoprofen
Larutan dapar dengan berbagai variasi pH setelah ditambah dengan larutan
ketoprofen sama banyak dan diukur pHnya dengan pH meter diperoleh pH
larutan dengan serapan sebagai berikut :
NaOH 0,2 N dengan absorbansi 1,0331
HCl 0,2 N dengan absorbansi 1,2562
Dapar pH 6,2 menjadi 7,2 dengan absorbansi 1,0435
Dapar pH 5,8 menjadi 6,9 dengan absorbansi 1,056
Dapar pH 5,4 menjadi 6,4 dengan absorbansi 1,0745
Dapar pH 4,8 menjadi 5,8 dengan absorbansi 1,0873
Dari hasil data serapan sampel dalam berbagai suasana diperoleh bahwa
titik isobestik pada diklofenak terjadi pada panjang gelombang 270 nm; ibupofen
pada panjang gelombang 250 nm dan ketoprofen pada panjang gelombang 230
nm. Titik isobestik adalah panjang gelombang dimana absorbsitivitas molar dari
asam dan basa sama. Sebagai dasar untuk menghitung harga pKa digunakan
absorbansi pada daerah setelah titik isobestik ini (Willard, 1981).
3.5 Penetapan Harga pKa
Dari hasil penetapan harga pKa diklofenak, ibuprofen dan ketoprofen
dengan menggunakan metode Spektrofotometri Ultraviolet, diperoleh harga pKa
rata-rata dari diklofenak 4,765 dengan standar deviasi (SD) = 0,41; ibuprofen 5,32
dengan standar deviasi (SD) = 0,17; dan ketoprofen 5,75 dengan standar deviasi
Tabel 19. Data harga pka dari diklofenak, ibuprofen dan ketoprofen
Dari tabel diatas diperoleh bahwa harga pKa yang tertinggi berturut-turut
ketoprofen, ibuprofen dan yang paling rendah diklofenak. Menurut Moffat et al
(2004) harga pKa untuk ketoprofen yaitu 4,5 dan menurut Foye (1996) 5,94.
Sedangkan dari hasil penelitian diperoleh yaitu 5,75. Harga pKa ini mendekati
harga pKa yang terdapat pada Foye. Hal ini disebabkan karena berdasarkan
pengaruh induksi dan resonansi, pada gugus ketoprofen terdapat gugus C=O pada
posisi meta dengan induksi negatif (I-) resonansi negatif (R-), tetapi karena
pengaruh cincin benzen pada gugus C=O yang memberikan elektron secara
bersama sehingga harga pKa mendekati netral.
Untuk ibuprofen harga pKanya ada 2 yaitu 4,4 dan 5,2 (Moffat et al.
2004) dan 5,2 (Foye. 1996). Hasil yang diperoleh yaitu 5,32 yang bila
dibandingkan dengan moffat dan foye perbedaannya tidak terlalu jauh. Karena
berdasarkan pengaruh induksi dan resonansi, pada ibuprofen terdapat gugus CH2
pada posisi para, resonansi terjadi karena hiperkonjugasi pada CH3 dan CH pada
benzen lebih elektronegatif dibandingkan CH2 sehingga memberikan (R+, I+).
Sedangkan untuk diklofenak menurut Moffat et al (2004) harga pKanya
yaitu 4,2 dan menurut Foye (1996) harga pKanya belum ditentukan. Hasil yang
diperoleh yaitu 4,75 yang bila dibandingkan dengan moffat perbedaannya tidak
terlalu jauh. Karena berdasarkan pengaruh induksi dan resonansi, pada gugus
diklofenak terdapat gugus NH yang memberikan (I-) dan (R+), dengan adanya
atom H dari gugus NH pada posisi orto dan atom OH dari gugus COOH terjadi
jembatan hidrogen yang menyebabkan diklofenak makin asam dan pKa semakin
turun. Adanya Cl juga menyebabkan penurunan pH, hal ini karena apabila suatu
senyawa ditambah gugus penarik elektron akan menaikkan sifat keasamannya.
Apabila (R+, I+) dan (R+, I-) maka pemberi elektron dan harga pKa
meningkat, dan apabila (R-, I-) maka penarik elektron dan harga pKa menurun.
Harga pKa gugus pengionisasi tertentu dapat dipengaruhi oleh adanya substituen
kimia lain yang mengionisasi atau tidak mengionisasi dan memberi atau menarik
elektron dalam suatu sistem resonansi dan induksi (Foye, 1996).
Perbedaan harga pKa yang diperoleh dengan harga pKa teori dipengaruhi
oleh adanya pelarut organik yaitu alkohol, biasanya mengganggu kesetimbangan
ionisasi dalam air. Untuk asam, kesetimbangan didesak kekiri dengan
menguntungkan pelarutan bentuk yang tidak terionisasi. Efek pada penentuan
harga pKa dalam sistem pelarut organik biasanya terlihat sebagai harga yang lebih
BAB IV
KESIMPULAN DAN SARAN 4.1 Kesimpulan
Hasil penelitian diperoleh bahwa harga pKa dari bahan baku Diklofenak,
Ibuprofen dan Ketoprofen dengan menggunakan metode Spektrofotometri
Ultraviolet yaitu harga pKa rata-rata dari diklofenak 4,75 dengan standar deviasi
(SD) = 0,41; ibuprofen 5,32 dengan standar deviasi (SD) = 0,17 dan ketoprofen
5,75 dengan standar deviasi (SD) = 0,35.
4.2 Saran
Disarankan agar peneliti selanjutnya dapat menetapkan harga pKa sediaan
DAFTAR PUSTAKA
Anonim, (1988). Petunjuk Praktikum QSAR, Mid Career Training in
Pharmacochemistry. A joint project between Fakultas Farmasi Universitas
Gajah Mada, Yogyakarta and the Departement of Pharmacochemistry,
Vrije Universiteit. Amsterdam, the Netherlands. Hand out Period 2.Hal 1-5
Anonim, (1990). USP XXII NF XVII Pharmacopeia The National Formulasi.
Marck Printing Company, Easton, PA, 8042
Ditjen POM. (1979). Farmakope Indonesia. Edisi ketiga. Departemen Kesehatan
RI. Jakarta. Hal. 744-748 dan 753-755.
Ditjen POM. (1995). Farmakope Indonesia. Edisi keempat. Departemen
Kesehatan RI. Jakarta. Hal. 1066.
Foye William O. (1990). Principles of Medicinal Chemistry. Reprinted. London.
LEA & FEBIGER/PHILADELPIA. Hal. 866-867.
Foye William O. (1996). Prinsip-prinsip Kimia Medisinal. Jilid II edisi kedua.
Gadjah Mada University Press. Yogyakarta. Hal. 1809-1811.
Moffat A.C. et. al. (2004). Clarke’s analysis of drugs and poisons. In
Pharmaceuticals body fluids and postmortem material. Third edition.
London-Chicago. PhP Pharmaceutical Press. Hal. 552 dan 904-905
Mycek, Mary J. (2001). Farmakologi Ulasan Bergambar. Edisi kedua. Widya
Medika. Jakarta. Hal. 411
Siswandono dan Soekarjo, B. (1995). Kimia Medisinal. Cetakan Pertama. Penerbit
Airlangga University Press. Surabaya. Hal. 550-552
Siswandono dan Soekarjo, B. (1998). Prinsip-Prinsip Rancangan Obat. Cetakan
Pertama. Penerbit Airlangga University Press. Surabaya. Hal. 202
Sudjana. (1992). Metode Statistik. Edisi kelima. Penerbit Tarsito Bandung. Hal.
145-147
Willard H. Hobart, (1981). Instrumental Methods of Analysis. 7th edition.
Lampiran 1. Hasil perhitungan harga pKa Diklofenak secara spektrofotometri
ultraviolet pada λ analitik 295
HA
1. pH dapar 5,8 menjadi 6,8 dengan absorbansi 1,7672
= absorbansi dalam larutan HCl 0,2 N yaitu 1,2799 AHA = absorbansi dalam larutan NaOH 0,2 N yaitu 1,7798
A buffer = absorbansi dalam larutan dapar
22
2. pH dapar 5,4 menjadi 6,4 dengan absorbansi 1,761
3. pH dapar 4,8 menjadi 5,8 dengan absorbansi 1,755
4. pH dapar 4,2 menjadi 5,2 dengan absorbansi 1,723
31
Lampiran 2. Hasil perhitungan harga pKa Ibuprofen secara spektrofotometri
ultraviolet pada λ analitik 265 nm
HA
1. pH dapar 6,2 menjadi 5,9 dengan absorbansi 1,9943
= absorbansi dalam larutan HCl 0,2 N yaitu 1,827 AHA = absorbansi dalam larutan NaOH 0,2 N yaitu 2,062
A buffer = absorbansi dalam larutan dapar
3. pH dapar 5,4 menjadi 4,8 dengan absorbansi 1,8799
Lampiran 3. Hasil perhitungan harga pKa Ketoprofen secara spektrofotometri
ultraviolet pada λ analitik 250 nm
HA
1. pH dapar 6,2 menjadi 7,2 dengan absorbansi 1,0453
= absorbansi dalam larutan HCl 0,2 N yaitu 1,2562 AHA = absorbansi dalam larutan NaOH 0,2 N yaitu 1,0331
A buffer = absorbansi dalam larutan dapar
3. pH dapar 5,4 menjadi 6,4 dengan absorbansi 1,0745
4. pH dapar 4,8 menjadi 5,8 dengan absorbansi 1,0873
31
Lampiran 4. Analisa data Statistik harga pKa dari Diklofenak
Standar Deviasi 0,41
Lampiran 5. Analisa data Statistik harga pKa dari Ibuprofen
Standar deviasi 0,17
3
Lampiran 6. Analisa data Statistik harga pKa dari Ketoprofen
Standar deviasi 0,35
Lampiran 7. Gambar alat
a. Spektrofotometer Ultraviolet (Shimadzu mini 1240)
b. pH meter (Hanna)