i SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh
Yoki Christian Andrianto NIM: 068114163
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
PARASETAMOL DAN IBUPROFEN SECARA SPEKTROFOTOMETRI UV DENGAN APLIKASI METODE PANJANG GELOMBANG
BERGANDA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh
Yoki Christian Andrianto NIM: 068114163
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
v
Satu-satunya Sahabat, Guru, dan Bapaku yang hanya karena kemurahan-Nya saja aku bisa menjalani dan melewati semua ini. Kepada Papa dan Mamaku tercinta, yang selalu sabar menghadapi
polah tingkahku, terima kasih atas cinta kasihnya dan pelajaran berharga dalam hidupku, serta atas doa restunya sehingga aku bisa
menjadi lebih baik.
Cicikku, cik nana yang selalu menjadi teman, kakak sekaligus kadang menjadi sainganku, yang tak pernah lelah mendukung aku dalam
segala hal.
Untuk mbak yuli yang sejak kecil selalu menjaga dan merawat, dan tidak pernah berhenti mendukungku.
Untuk peri kecilku Winda yang selalu ada dan mendukungku setiap saat.
Serta sahabat-sahabatku ”ngapak team”, yang selalu ada buat mendukungku.
Almamaterku
viii
Banyak obat yang menggunakan macam-macam zat aktif, nalge obat nalgesic. Sehingga muncul kesulitan untuk menganalisis kadar masing-masing komponen. Oleh karena itu diperlukan suatu metode untuk menganalisis masing-masing komponen tersebut, misalnya untuk menganalisis kadar campuran parasetamol dan ibuprofen dalam tablet.
Metode yang dipakai adalah metode spektrofotometri UV dengan aplikasi panjang gelombang berganda untuk analisis campuran, sehingga tidak perlu memisahkan masing-masing komponen. Namun, sebelum digunakan untuk aplikasi maka sebelumnya metode ini harus diketahui validasi metodenya, kemudian dilihat akurasi dan presisinya.
Hasil penelitian metode ini menunjukkan bahwa nilai range recovery yang diperoleh untuk parasetamol dan ibuprofen adalah 90,3%-99,6% dan 92,8%-101,5%. Dan nilai %CV yang diperoleh untuk parasetamol dan ibuprofen adalah 0,555% dan 0,329%. Nilai standard recovery dan %CV yang dipakai adalah 90-107% dan <2%. Nilai recovery dan nilai %CV dari parasetamol dan ibuprofen masuk dalam range standard, sehingga dapat disimpulkan bahwa metode ini memiliki akurasi yang baik dan presisi yang baik.
Kata kunci: spektofotometri UV, parasetamol, ibuprofen, analisis campuran, panjang gelombang berganda
ix
The method used is the method of UV spectrophotometry with multiple wavelength applications for the analysis of the mixture, so no need to separate each component. However, before being used for the previous application of this method to know the validity of the method, by looking at the accuracy (recovery value) and precision (% CV).
The results of the study range recovery values obtained for paracetamol and ibuprofen were 90.3% -99.6% and 92.8% -101.5%. Value% CV obtained for paracetamol and ibuprofen was 0.555% and 0.329%. This shows the method of UV spectrophotometry with multiple wavelength applications have accuracy and good precision
.
Keywords: spektofotometri UV, paracetamol, ibuprofen, a mixture of analysis, multiple wavelength
x
Puji syukur ke hadirat Tuhan Yang Maha Esa karena atas limpahan berkatnya penulis mampu menyelesaikan skripsi dengan judul Validasi Metode Penetapan Kadar Campuran Parasetamol dan Ibuprofen secara Spektrofotometri UV dengan Aplikasi Panjang Gelombang Berganda. Penyusunan skripsi ini sebagai syarat untuk memperoleh gelar Sarjana Farmasi Program Studi Ilmu Farmasi Universitas Sanata Dharma. Segala usaha dan upaya dalam penyusunan skripsi ini tidak lepas dari bantuan dan kerja sama berbagai pihak. Oleh karena itu penulis ingin mengucapkan terima kasih yang sebesar-besarnya kepada:
1. Ibu Rita Suhadi, M.Si., Apt selaku dekan Fakultas Farmasi Universitas Sanata Dharma.
2. Ibu Christine Patramurti, M.Si., Apt selaku dosen pembimbing yang telah meluangkan waktunya untuk memberikan bimbingan, pengarahan dan saran dari mulai penyusunan proposal sampai skripsi ini selesai.
3. Ibu Dra. M M Yetty Tjandrawati, M. Si selaku dosen penguji yang telah memberikan kritik dan saran kepada penulis sehingga skripsi penulis menjadi lebih baik.
4. Bapak Jeffry Julianus, M. Si selaku dosen penguji yang telah memberikan kritik dan saran yang diberikan kepada penulis.
5. Ibu Yunita Linawati sebagai dosen pembimbing akademik.
xi
9. P.T. Konimex yang telah memberikan bantuan bahan baku ibuprofen.
10. Keluarga besarku yang telah memberikan kesempatan dan kepercayaan yang sangat berharga ini.
11. Aang sebagai teman satu tim dalam pengerjaan penelitian skripsi ini, terima kasih atas kerjasama dan kebersamaan kita.
12. Buat mas bimo, sebagai laboran Lab kimia instrumental, teman futsal, dan seorang sahabat terima kasih atas bantuan dan waktu yang telah disediakan selama mengerjakan penelitian ini, mas Parlan, dan mas Kunto, terima kasih atas segala bantuannya.
13. Pungki, michele, angel, boim dan toni, teman seperjuangan dalam pengerjaan penelitian ini.
14. Buat teman-teman kos Wisma Manunggal yang selalu setia mendukung dan menemani penulis dalam suka dan duka.
15. Buat temen-temen kelas C dan FST A, terima kasih atas persahabatan yang indah yang telah kita jalani, semoga persahabatan ini kekal selamanya.
16. Buat Anton, Yakob, Jimbonk, Pungky, dan temen Ngapak team kalian adalah bagian terbaik dalam hidupku.
17. Dan semua pihak yang tidak dapat disebutkan satu persatu yang telah membantu penulis.
xiii
HALAMAN PERSETUJUAN PEMBIMBING... iii
HALAMAN PENGESAHAN... iv
HALAMAN PERSEMBAHAN... v
HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI... vi
PERNYATAAN KEASLIAN KARYA... vii
INTISARI... viii
ABSTRACT... ix
KATA PENGANTAR... x
DAFTAR ISI... xiii
DAFTAR TABEL... xvi
DAFTAR GAMBAR... xvii
DAFTAR LAMPIRAN... xix
BAB I PENGANTAR... 1 A. Latar Belakang... 1 1. Permasalahan... 3 2. Keaslian Penelitian... 3 3. Manfaat Penelitian... 3 B. Tujuan... 4
BAB II PENELAAHAN PUSTAKA... 5
xiv
C. Spektrofotometri... 7
1. Tinjauan spektrofotometri secara umum... 7
2. Dasar analisis kuantitatif spektrofotometri UV... 10
3. Pemilihan pelarut... 12
D. Analisis Multikomponen Secara Spektrofotometri UV... 13
E. Validitas metode Analisis Instrumental... 17
F. Landasan Teori... 20
G. Hipotesis... 21
BAB III METODOLOGI PENELITIAN... 22
A. Jenis dan Rancangan Penelitian... 22
B. Variabel Penelitian... 22
C. Definisi Operasional... 22
D. Bahan Penelitian... 23
E. Alat Penelitian... 23
F. Tata Cara Penelitian... 23
1. Pembuatan larutan baku parasetamol dan ibuprofen... 23
2. Penentuan panjang gelombang penelitian... 24
3. Penentuan harga serapan jenis... 24
4. Penetapan kadar parasetamol dan ibuprofen dalam sampel... 25
G. Analisis Hasil... 26
xv D. Penetapan Kadar Parasetamol dan
Ibuprofen Dalam Sampel... 39
BAB V KESIMPULAN DAN SARAN... 42
A. Kesimpulan... 42
B. Saran... 42
DAFTAR PUSTAKA... 43
LAMPIRAN... 44
xvi
I. Pemilihan pelarut dalam spektrofotometri UV... 12
II. Kriteria rentang recovery yang diterima... 18
III. Kriteria KV yang dapat diterima... 19
IV. Data perhitungan serapan jenis parasetamol replikasi I... 35
V. Data perhitungan serapan jenis parasetamol replikasi II... 36
VI. Data perhitungan serapan jenis parasetamol replikasi III... 36
VII. Data perhitungan serapan jenis ibuprofen replikasi I... 36
VIII. Data perhitungan serapan jenis ibuprofen replikasi II... 37
IX. Data perhitungan serapan jenis ibuprofen replikasi III... 37
X. Data hasil perhitungan kadar, recovery, dan %CV………... 40
XI. Data penimbangan parasetamol untuk larutan baku... 46
XII. Data penimbangan ibuprofen untuk larutan baku... 46
XIII. Data penimbangan parasetamol dan ibuprofen untuk larutan sampel... 46
XIV. Data perhitugan serapan jenis parasetamol replikasi pertama... 53
XV. Data perhitugan serapan jenis parasetamol replikasi kedua... 53
XVI. Data perhitugan serapan jenis parasetamol replikasi ketiga... 54
XVII. Data perhitugan serapan jenis ibuprofen replikasi pertama... 54
XVIII. Data perhitugan serapan jenis ibuprofen replikasi kedua... 55
XIX. Data perhitugan serapan jenis ibuprofen replikasi ketiga... 55
XX. Data serapan larutan sampel... 58
xvii
III. Diagram tingkat energi elektronik... 8
IV. Spektra serapan senyawa X dan Y, tak ada tumpang tindih pada dua panjang gelombang... 13
V. Spektra serapan senyawa X dan Y, tumpang tindih satu cara... 14
VI. Spektra tumpang tindih dari dua komponen dan spektra serapan campuran dua komponen... 15
VII. Spektra serapan parasetamol konsentrasi rendah... 28
VIII. Spektra serapan parasetamol konsentrasi tengah... 29
IX. Spektra serapan parasetamol konsentrasi tinggi... 29
X. Spektra serapan ibuprofen konsentrasi rendah... 29
XI. Spektra serapan ibuprofen konsentrasi tengah... 29
XII. Spektra serapan ibuprofen konsentrasi tinggi... 29
XIII. Struktur kromofor dan auksokrom Parasetamol... 31
XIV. Struktur kromofor Ibuprofen... 32
XV. Spektra tumpang tindih parasetamol dan ibuprofen... 31
XVI. Spektra sampel campuran parasetamol dan ibuprofen... 39
XVII. Spektra parasetamol konsentrasi rendah... 50
XVIII. Spektra parasetamol konsentrasi tengah... 50
XIX. Spektra parasetamol konsentrasi tinggi... 50
xviii
XXII. Spektra ibuprofen konsentrasi tinggi... 51 XXIII. Spektra tumpang tindih parasetamol-ibuprofen
perbandingan konsentrasi 7:4... 52 XXIV. Spektra campuran Parasetamol dan Ibuprofen……….. 52
xix
Lampiran 3 : Skema kerja dan contoh perhitungan kadar
parasetamol-ibuprofen... 47 Lampiran 4 : Spektra parasetamol-ibuprofen konsentrasi
rendah, sedang, tinggi... 50 Lampiran 5 : Spektra tumpang tindih dan campuran
parasetamol-ibuprofen... 52 Lampiran 6 : Perhitungan serapan jenis parasetamol-ibuprofen... 53 Lampiran 7 : Data perhitungan kadar parasetamol-ibuprofen... 56 Lampiran 8 : Perhitungan Recovery dan %CV
1
PENDAHULUAN
A. Latar Belakang
Saat ini banyak dijumpai suatu sediaan obat, misal sediaan tablet yang mengandung lebih dari satu macam zat aktif. Kebanyakan tablet mengandung satu macam zat aktif saja dan bahan eksipien. Adanya lebih dari satu macam zat aktif ini biasanya ditujukan untuk mendapatkan efek yang lebih baik, dimana kegunaan zat aktif yang satu mendukung kegunaan zat aktif yang lainnya. Kriteria sediaan obat yang baik adalah apabila obat tersebut mengandung bahan-bahan yang sesuai dengan komposisi. Sehingga diharapkan dengan komposisi yang tepat efek obat yang diperoleh juga maksimal. Contoh sediaan tablet yang mengandung lebih dari satu macam zat aktif adalah tablet analgesik yang mengandung campuran ibuprofen dan parasetamol. Parasetamol dan ibuprofen dipilih atas dasar kedua macam zat tersebut banyak dijumpai dalam sediaan obat yang dijual secara bebas, sehingga perlu dilakukan penelitian tentang penetapan kadarnya untuk menjamin kualitas sediaan obat. Namun, dengan adanya lebih dari satu macam zat aktif dalam satu sediaan obat, menimbulkan kesulitan dalam penetapan kadarnya.
Menurut Farmakope edisi IV, penetapan kadar parasetamol dan ibuprofen ini dapat dilakukan dengan metode spektrofotometri UV. Metode spektrofotometri UV digunakan untuk menganalisis senyawa tunggal. Dengan adanya modifikasi metode spektrofotometri UV, maka metode ini dapat digunakan untuk analisis multikomponen. Metode analisis yang dibutuhkan di
bagian kontrol kualitas industri obat dalam rangka pengawasan mutu obat adalah metode analisis yang cepat dan memenuhi persyaratan kesahihan suatu metode. Dengan modifikasi tersebut maka penetapan kadar campuran parasetamol dan ibuprofen dapat ditetapkan secara simultan atau secara bersama-sama dan dengan waktu yang singkat. Oleh karena itu, pengembangan metode analisis parasetamol dan ibuprofen perlu dilakukan.
Dalam pengembangan metode analisis ini perlu mempertimbangkan sifat fisika kimia parasetamol dan ibuprofen. Parasetamol dan ibuprofen mempunyai kelarutan yang hampir sama, salah satunya adalah mudah larut dalam metanol. Selain itu, parasetamol dan ibuprofen dapat menyerap radiasi elektromagnetik UV dengan serapan maksimal pada panjang gelombang yang berdekatan yaitu 244 nm untuk serapan parasetamol dan 221 nm untuk serapan ibuprofen. Dari data panjang gelombang maksimum kedua senyawa yang memiliki selisih yang kecil menunjukkan bahwa kurva serapan parasetamol dan ibuprofen mengalami tumpang tindih secara keseluruhan. Berdasarkan sifat tersebut, metode penetapan kadar yang dapat dikembangkan adalah metode analisis multikomponen yang lebih praktis secara spektrofotometri UV dengan prinsip persamaan regresi berganda melalui perhitungan operasi matriks dengan metode pengamatan pada panjang gelombang berganda. Pada metode ini tidak diperlukan proses pemisahan komponen zat aktif karena kadar parasetamol dan ibuprofen dapat ditetapkan secara bersama-sama.
Penetapan kadar campuran parasetamol dan ibuprofen dengan metode spektrofotometri UV ini belum pernah dilakukan, sehingga sebelum diaplikasikan metode ini harus divalidasi terlebih dahulu.
Validasi metode dapat diartikan sebagai suatu prosedur yang digunakan untuk membuktikan bahwa metode analisis tersebut memberikan hasil seperti yang diharapkan dengan kecermatan dan ketelitian yang memadai. Parameter yang digunakan untuk validasi metode ini adalah akurasi dan presisi. Parameter yang dipakai adalah akurasi dan presisi karena dengan penilaian dari kedua parameter ini sudah cukup mewakili untuk menilai validitas metode spektrofotometri UV ini.
1. Permasalahan
Apakah campuran parasetamol dan ibuprofen yang ditetapkan kadarnya secara spektrofotometri UV dengan aplikasi panjang gelombang berganda mempunyai akurasi dan presisi yang baik?
2. Kesahihan Penelitian
Sejauh pengetahuan penulis, penelitian mengenai analisis multikomponen secara spektrofotometri UV terhadap campuran parasetamol dan ibuprofen dengan aplikasi panjang gelombang berganda belum pernah dilakukan. 3. Manfaat penelitian
a. Manfaat metodologis. Penelitian ini diharapkan dapat memberikan tambahan wawasan terhadap perkembangan analisis multikomponen secara spektrofotometri UV dengan aplikasi metode panjang gelombang berganda, khususnya untuk campuran parasetamol dan ibuprofen.
b. Manfaat praktis. Penelitian dapat digunakan sebagai metode alternatif untuk analisis multikomponen campuran parasetamol dan ibuprofen secara spektrofotometri UV dengan aplikasi metode panjang gelombang berganda.
B. Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui akurasi dan presisi metode penetapan kadar campuran parasetamol dan ibuprofen secara spektrofotometri UV dengan aplikasi metode panjang gelombang berganda.
BAB II
PENELAAHAN PUSTAKA
A. Parasetamol
Sinonim lain dari parasetamol adalah asetaminofen;
p-Hidroksiasetanilida; p-asetamidofenol; N-asetil-p-aminofenol; C6H9NO2, dengan
berat molekul 151,16 (Anonim, 1995). Rumus bangun dari parasetamol adalah sebagai berikut
O
N H
OH
Parasetamol mengandung tidak kurang dari 98,0% dan tidak lebih dari 101,0% C6H9NO2. Pemerian dari parasetamol adalah berupa serbuk hablur, putih,
tidak berbau, rasa sedikit pahit. Parasetamol ini memiliki kelarutan dalam air panas, dalam natrium hidroksida 1N, dan mudah larut dalam metanol, etanol. Parasetamol dapat menyerap panjang gelombang pada 244 nm (Anonim, 1995).
Parasetamol atau asetaminofen adalah obat analgesik dan antipiretik yang populer dan digunakan untuk meredakan sakit kepala, sengal-sengal dan sakit ringan, dan demam. Digunakan dalam sebagian besar resep obat analgesik salesma dan flu. Berbeda dengan obat analgesik yang lain seperti aspirin dan ibuprofen, parasetamol tidak memiliki sifat antiradang. Jadi parasetamol tidak
tergolong dalam obat jenis Non Steroid Anti Imuno Deficiency (NSAID). Dalam dosis normal yaitu 4 gram perhari, parasetamol tidak menyakiti permukaan dalam perut atau mengganggu gumpalan darah, ginjal atau duktus arteriosus pada janin (Anonim, 2000).
B. Ibuprofen
Sinonim lain dari ibuprofen adalah 2-(p-Isobutilfenil)asam propionat, C13H18O2, dengan berat molekul 206,28. Rumus bangun dari ibuprofen adalah
sebagai berikut:
O HO
Ibuprofen mengandung tidak kurang dari 97,0% dan tidak lebih dari 103,0% C13H18O2 dihitung terhadap zat anhidrat. Pemerian dari ibuprofen ini
adalah berupa serbuk hablur, putih, hingga hampir putih, berbau khas lemah. Kelarutan dari ibuprofen ini yaitu praktis tidak larut dalam air, sangat mudah larut dalam etanol, dalam metanol, dalam aseton, dan dalam kloroform, sukar larut dalam etil asetat. Serapan maksimal dari ibuprofen pada panjang gelombang 221 nm (Anonim, 1995).
Ibuprofen adalah sejenis obat yang tergolong dalam kelompok antiperadangan non-steroid dan digunakan untuk mengurangi rasa sakit akibat
artritis. Ibuprofen juga tergolong dalam kelompok analgesik dan antipiretik. Obat ini dijual dengan merk dagang advil, motrin, nuprin, dan brufen. Dosis normal untuk ibuprofen adalah 1,2 gram sehari (Anonim, 2000).
C. Spektrofotometri 1. Tinjauan spektrofotometri secara umum
Teknik spektroskopik adalah suatu teknik analisis fisika kimia yang mengamati tentang interaksi atom atau molekul dengan radiasi elektromagnetik. Pada prinsipnya interaksi radiasi elektromagnetik dengan molekul akan menghasilkan satu atau dua dari tiga kejadian yang mungkin terjadi. Ketiga macam kejadian yang mungkin terjadi adalah hamburan (scattering), absorpsi
(absorption), dan emisi (emision) radiasi elektromagnetik oleh atom atau molekul
yang diamati (Mulja & Suharman, 1995).
Spektrofotometri UV adalah teknik analisis spektroskopik yang memakai sumber radiasi elektromagnetik ultraviolet dekat (190-380 nm) dengan memakai instrumen spektrofotometer.
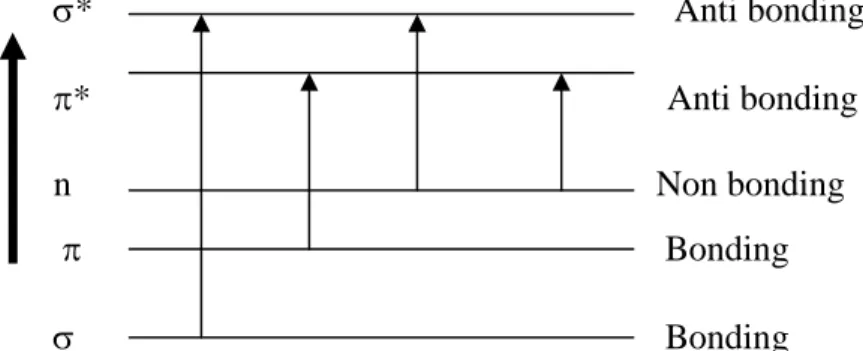
Apabila pada suatu molekul dikenakan radiasi elektromagnetik maka akan terjadi eksitasi ke tingkat energi yang lebih tinggi yang dikenal sebagai orbital elektron ”anti-bonding” (Mulja & Suharman, 1995). Diagram tingkat energi elektron pada keadaan dasar dan keadaan tereksitasi ditunjukkan pada gambar:
* Anti bonding
* Anti bonding
n Non bonding
Bonding
Bonding
Gambar 3. Diagram tingkat energi elektronik (Mulja dan Suharman, 1995) Absorpsi sinar ultraviolet oleh suatu atom atau molekul M dapat dianggap melalui dua proses. Proses pertama adalah eksitasi yang ditunjukkan oleh pesamaan: M + hv M*
Ketika suatu radiasi foton melewati molekul, absorpsi dapat terjadi jika energi foton tersebut sesuai dengan perbedaan energi diantara ground state dan satu tingkat energi yang lebih tinggi dari molekul tersebut. Pada keadaan ini energi dari foton ditransfer kepada molekul tersebut dan mengubahnya ke tingkat energi yang lebih tinggi yang disebut excited state M*. Proses terakhir adalah relaksasi. Setelah suatu periode singkat, molekul berrelaksasi ke tempat aslinya atau ground state dengan mentransfer kelebihan energinya ke atom atau molekul lain pada medium tersebut. Proses ini menyebabkan peningkatan temperatur lingkungan sementara. Ini dapat digambarkan dengan persamaan sebagai berikut:
M* M + Energi (Skoog, 1994)
Absorpsi sinar UV dalam suatu molekul disebabkan karena adanya elektron yang bertanggung jawab terhadap absorpsi sinar tersebut. Dua tipe elektron yang bertanggung jawab terhadap absorpsi radiasi UV dalam molekul yaitu elektron terbagi yang berpartisipasi langsung dalam pembentukkan ikatan
dan yang tergabung dengan lebih dari satu atom, dan elektron luar tak terbagi yang banyak terlokalisasi pada atom seperti oksigen, halogen, sulfur, dan nitrogen (Skoog, 1994).
Aplikasi spektroskopi serapan untuk senyawa organik didasarkan pada transisi n atau π ke π*karena energi yang dibutuhkan untuk proses ini membawa puncak absorpsi ke daerah spektra 200-700 nm. Kedua transisi ini membutuhkan gugus tidak jenuh yang memberikan orbital π (Skoog, 1994).
Transisi π-π* ini menunjukkan pergeseran merah (geseran batokromik) dengan adanya substitusi gugus-gugus yang memberi atau menarik elektron (Sastrohamidjojo, 1991).
Senyawa organik pada umumnya mempunyai gugusan atom yang dapat mengabsorpsi radiasi UV disebut sebagai kromofor (Mulja & Suharman, 1995). Pusat serapan sinar ultraviolet ada pada kromofor (Skoog, 1985). Kromofor merupakan suatu gugus kovalen tidak jenuh yang bertanggung jawab untuk serapan elektronik. Sebagai contoh C-C, C-O, dan NO2 (Silverstein, Bassler,
Morrill, 1974).
Pada senyawa organik dikenal pula auksokrom, yakni gugus fungsional yang mempunyai elektron bebas seperti –OH, O-NH2, dan OCH3 yang
memberikan transisi (nσ*) (Mulja & Suharman, 1995). Apabila auksokrom terikat pada suatu kromofor maka akan merubah baik panjang gelombang dan intensitas dari serapan (Silverstein, Bassler, Morrill, 1974). Auksokrom akan menggeser puncak serapan kearah panjang gelombang yang lebih panjang
(geseran merah/ red shift/ geseran batokromik) dengan disertai peningkatan intensitas (efek hiperkromik) (Skoog, 1985).
Geseran batokromik adalah geseran dari serapan ke panjang gelombang yang lebih panjang karena sisipan atau pengaruh pelarut (geseran merah/red shift). Geseran hipsokromik adalah geseran dari serapan ke panjang gelombang yang lebih pendek karena gugus ganti atau pengaruh pelarut (geseran biru/blue shift).
Efek hiperkromik adalah suatu kenaikan di dalam intensitas serapan akibat adanya gugus ganti atau pengaruh pelarut. Sedangkan efek hipokromik adalah suatu penurunan di dalam intensitas serapan karena pengaruh pelarut. 2. Dasar analisis kuantitatif spektrofotometri UV
Spektrofotometri UV dapat digunakan untuk analisa kualitatif dan kuantitatif. Kemampuan suatu senyawa dalam mengabsorpsi sinar UV digunakan sebagai dasar pengukuran kualitatif dan kuantitatif (Skoog, 1994). Setiap molekul analit mampu mengabsorpsi radiasi elektromagnetik pada panjang gelombang karakteristik (Silverstein, Bassler, Morrill, 1974).
Dalam studi kuantitatif, berkas radiasi yang ditransmisikan diukur. Radiasi yang diserap oleh sampel ditetapkan dengan membandingkan intensitas sinar yang ditransmisikan ketika tidak ada senyawa yang mengabsorpsi.
Apabila suatu radiasi elektromagnetik dikenakan pada suatu larutan dengan intensitas radiasi semula (Io) maka sebagian radiasi tersebut akan
diteruskan (It), dipantulkan (Ir), dan diabsorpsi (Ia), sehingga:
Hukum Lambert. Hukum ini menyatakan bahwa bila cahaya monokromatik melewati medium tembus cahaya, laju berkurangnya intensitas oleh bertambahnya ketebalan, berbanding lurus dengan intensitas cahaya. Ini setara dengan menyatakan bahwa intensitas cahaya yang dipancarkan berkurang secara eksponensial dengan bertambahnya medium yang menyerap.
Hukum Beer. Beer mengkaji efek konsentrasi penyusun yang berwarna dalam larutan, terhadap transmisi maupun absorbsi cahaya. Beer menemukan hubungan yang sama antara transmisi dan konsentrasi seperti yang dikemukakan oleh Lambert antara transmisi dan ketebalan lapisan, yakni intensitas berkas cahaya monokromatik berkurang secara eksponensial dengan bertambahnya konsentrasi zat penyerap secara linier.
Menurut Mulja dan Suharman (1995), dari kedua hukum tersebut dapat diperoleh suatu persamaan matematik yang menggambarkan hubungan antara transmitan atau absorban terhadap konsentrasi zat yang dianalisis dan tebal larutan yang mengabsorbsi sebagai:
T It Io 10 a.b.c A log 1 T a.b.c dimana: T = persen transmitan
Io = intensitas radiasi yang datang It = intensitas radiasi yang diteruskan a = absorbansi molar
b = tebal kuvet c = konsentrasi
Jika c dinyatakan mol dm-3 dan b dalam sentimeter, maka a diberi lambang dan disebut koefisien absorbsi molar (Silverstein et al., 1991; Basset et
al., 1994).
3. Pemilihan pelarut
Spektrofotometri UV-Vis dapat melakukan penentuan terhadap sampel yang berupa larutan, gas atau uap. Menurut Mulja dan Suharman, untuk sampel yang berupa larutan perlu diperhatikan beberapa persyaratan pelarut yang dipakai, antara lain:
a. Pelarut yang dipakai tidak mengandung sistem ikatan rangkap terkonjugasi pada struktur molekulnya dan tidak berwarna
b. Tidak terjadi interaksi dengan molekul senyawa yang dianalisis c. Kemurniaannya harus tinggi atau derajat untuk analisis.
Pada umumnya pelarut yang sering digunakan dalam analisis spektrofotometri UV-Vis adalah air, etanol, sikloheksan, dan isopropanol. Namun demikian perlu diperhatikan absorpsi pelarut yang dipakai pada daerah UV-Vis (penggal UV = UV cut off) (Mulja dan Suharman, 1995).
Tabel I. Pelarut untuk daerah ultraviolet dan daerah tampak (Day and Underwood, 1996)
Jenis pelarut UV cut off (nm) Jenis pelarut UV cut off (nm)
Air Metanol Sikloheksana Heksana Dietil eter p-Dioksan Etanol 190 210 210 210 220 220 220 Kloroform Karbon tetraklorida Benzena Toluena Piridina Aseton Karbon disulfida 250 265 280 285 305 330 380
D. Analisis Multikomponen dengan Spektrofotometri UV
Analisis kuantitatif campuran dua komponen merupakan teknik pengembangan analisis kuantitatif komponen tunggal. Prinsip pelaksanaanya adalah mencari absorban atau beda absorban tiap-tiap komponen yang memberikan korelasi yang linier terhadap konsentrasi, sehingga akan dapat dihitung masing-masing kadar campuran zat tersebut secara serentak atau salah satu komponen dalam campurannya dengan komponen yang lainnya (Mulja dan Suharman, 1995).
1. Kemungkinan I
Spektra tidak tumpang tindih, atau sekurangnya dimungkinkan untuk menemukan suatu panjang gelombang dimana X menyerap dan Y tidak, serta panjang gelombang serupa untuk mengukur Y. Situasi kemungkinan I dapat dilihat pada gambar 4. Konstituen X dan Y semata-mata diukur masing-masing pada panjang gelombang1dan2(Day and Underwood, 1996).
X Y a b s o r b a n 1 2 Panjang gelombang
Gambar 4. Spektra absorpsi senyawa X dan Y (tidak ada tumpang tindih pada dua panjang gelombang yang digunakan) (Day and Underwood, 1996)
2. Kemungkinan II
Tumpang tindih satu-cara dari spektra: seperti ditunjukkan pada gambar 5, Y tidak mengganggu pengukuran X pada 1, tetapi X memang menyerap
cukup banyak bersama-sama Y pada 2. Pendekatan soal ini pada prinsipnya
sederhana. Konsentrasi X ditetapkan langsung dari absorbans larutan pada 1.
Kemudian absorbans yang disumbangkan oleh larutan X pada 2 dihitung dari
absortifitas molar X pada 2, yang telah diketahui sebelumnya. Sumbangan ini
dikurangkan dari absorbans terukur larutan pada 2 sehingga akan diperoleh
absorban yang disebabkan oleh Y; konsentrasi Y kemudian dapat diukur dengan cara yang umum (Day and Underwood, 1996). Spektra kemungkinan dua dapat dilihat pada gambar 5.
X Y a b s o r b a n 1 2 Panjang gelombang
Gambar 5. Spektra serapan senyawa X dan Y. Tumpang tindih satu cara: X dapat diukur tanpa gangguan Y, namun X mengganggu pengukuran Y (Day and Underwood, 1996)
3. Kemungkinan III
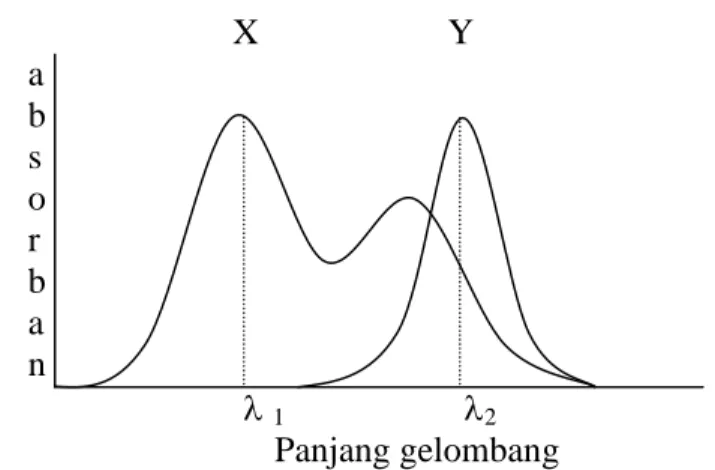
Tumpang tindih dua cara dari spektra: bila tidak dapat ditemukan panjang gelombang di mana X atau Y menyerap secara eksklusif, seperti yang ditunjukkan pada gambar 6:
X Y a b s o r b a n 1 2 Panjang gelombang
Gambar 6. Spektra serapan senyawa X dan Y. Tumpang tindih dua cara: tidak ada panjang gelombang dimana salah satu komponen dapat diukur tanpa gangguan oleh yang lain (Day and Underwood, 1996)
Spektra saling tumpang tindih dari dua komponen X dan Y, pada absorbansi maksimum dari komponen X pada 1, komponen Y juga mempunyai
absorbansi tersendiri. Demikian juga pada absorbansi maksimum senyawa Y pada 2, komponen X juga mempunyai absorbansi tersendiri. Spektrum serapan dari
campuran X dan Y merupakan jumlah dari dua kurva individu. Sehingga dapat ditulis persamaan – persamaan absorbansi total pada setiap panjang gelombang sebagai berikut:
Pada1:
AX(1)= aX(1) . b . cX dan AY(1)= aY(1) . b . cY
Absorbansi campuran pada1: Ac(1)= AX(1)+AY(1)
= aX(1). b. cX+ aY(1). b . cY (1)
pada2:
AX(2)= aX(2) . b . cX dan AY(2)= aY(2). b . cY
Absorbansi campuran pada2:
Ac(2)= AX(2)+AY(2)
dimana:
Ac(1)dan Ac(2) = absorbansi – absorbansi campuran yang teramati dari
campuran pada panjang gelombang1dan2
AX(1)dan AX(2) = absorbansi – absorbansi komponen X dalam
campuran pada panjang gelombang1dan2
AY(1)dan AY(2) = absorbansi – absorbansi komponen X dalam
campuran pada panjang gelombang1dan2
aX(1), aX(2), aY(1), aY(2) = serapan molar dari komponen X dan Y pada
panjang gelombang1dan2
cXdan cY = konsentrasi komponen X dan Y dalam campuran
(Pescok, 1986)
Serapan – serapan molar ditentukan pengukuran terhadap larutan murni X dan Y pada kedua panjang gelombang tersebut. Jadi untuk dua konsentrasi X dan Y yang tidak diketahui diperoleh dengan menyelesaikan dua persamaan (1) dan (2) secara bersama dengan pengukuran Ac pada dua panjang gelombang yang berbeda (Pescok, 1986).
Penggunaan teknik persamaan simultan memerlukan beberapa persyaratan agar diperoleh hasil yang memuaskan, antara lain harga selisih panjang gelombang maksimum masing – masing komponen harus relatif besar (Zainuddin, 1999) atau harga rasio serapan jenis antar komponen pada panjang gelombang maksimum cukup besar. Pada campuran multikomponen yang ada, terutama pada sediaan farmasi syarat tersebut akan sulit terpenuhi. Untuk mengatasi hal tersebut, telah diperkenalkan analisis multikomponen menggunakan prinsip persamaan regresi berganda (multiple regression) melalui perhitungan matriks dengan metode pengamatan beberapa panjang gelombang (multiple
wavelength) (Zainuddin,1999).
Jika suatu campuran bikomponen diamati serapannya pada multi panjang gelombang 1, 2, 3, 4, …..j, maka akan diperoleh j persamaan yaitu:
Ac1= a1x.cx+ a1y.cy Ac2= a2x.cx+ a2y.cy Ac3= a3x.cx+ a3y.cy . . . . . . . . Acj= ajx.cx+ ajy.cy Dimana:
Ac1, Ac2, Ac3, …Acj = serapan campurak pada panjang gelombang 1, 2, 3, ... j.
a1x, a2x, a3x, …ajx = serapan jenis senyawa X pada panjang gelombang 1, 2, 3, j
a1y, a2y, a3y, …ajy = serapan jenis senyawa Y pada panjang gelombang 1, 2, 3, j
cx = konsenttrasi senyawa X
cy = konsentrasi senyawa Y
Jika masing – masing disusun dalam persamaan matriks [:] maka akan didapat persamaan matriks sebagai berikut:
Ac
a
ij x c
imDari persamaan matriks tersebut maka dapat ditentukan harga c1 dan c2 secara bersamaan, dengan persamaan matriks:
c
a x a
1
1x a
x Ac
Perhitungan tersebut akan valid jika pengukuran serapan dilakukan pada multi panjang gelombang dengan jumlah melebihi komponen dan dikenal dengan istilah over-determained system (Zainuddin cit Massart, 1999).
E. Validitas Metode Analisis Instrumental
Kesahihan metode analisis diartikan sebagai suatu prosedur yang digunakan untuk membuktikan bahwa metode analisis tersebut memberikan hasil seperti yang diharapkan dengan kecermatan dan ketelitian yang memadai.
Pedoman kesahihan metode analisis didukung oleh parameter-parameter berikut ini:
1. Akurasi
Akurasi atau kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil analis dengan kadar analit yang sebenarnya. Range nilai %
recovery analit yang dapat diterima adalah 90-110%. Range tersebut bersifat
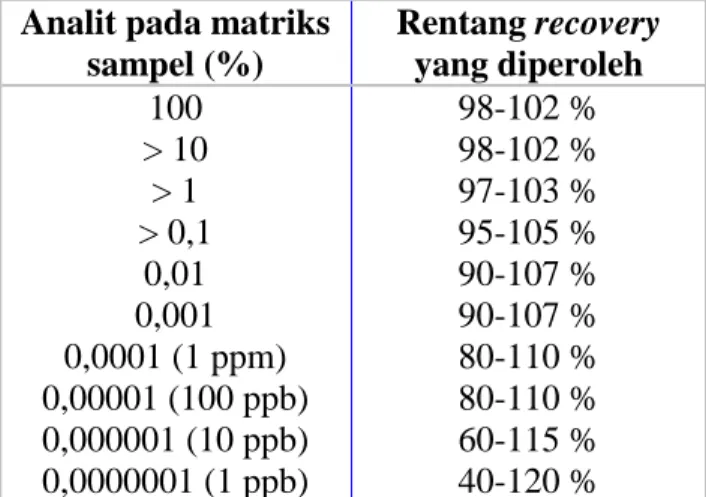
fleksibel tergantung dari kondisi analit yang diperiksa, jumlah sampel dan kondisi laboratorium. Akurasi dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan (Harmita, 2004).
Tabel II. Kriteria rentang recovery yang dapat diterima (Harmita, 2004) Analit pada matriks
sampel (%) Rentang recovery yang diperoleh 100 > 10 > 1 > 0,1 0,01 0,001 0,0001 (1 ppm) 0,00001 (100 ppb) 0,000001 (10 ppb) 0,0000001 (1 ppb) 98-102 % 98-102 % 97-103 % 95-105 % 90-107 % 90-107 % 80-110 % 80-110 % 60-115 % 40-120 % 2. Presisi
Presisi atau keseksamaan adalah ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual, diukur melalui penyebaran hasil individual dari rata – rata jika prosedur diterapkan secara berulang pada sampel – sampel yang diambil dari campuran yang homogen (Harmita, 2004). Presisi biasanya dinyatakan dalam koefisien variasi (KV). Suatu metode dapat dinyatakan memiliki presisi yang baik apabila memiliki KV < 2 % tetapi kriteria ini fleksibel
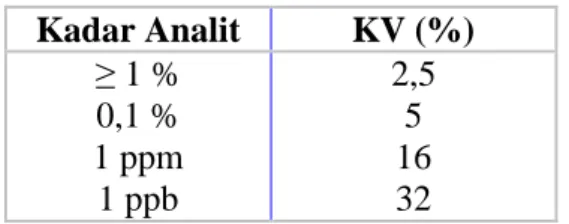
tergantung dari kondisi analit yang diperiksa, jumlah sampel dan kondisi laboratorium. Berikut ketentuan nilai KV yang dapat diterima (Harmita, 2004) :
Tabel III. Kriteria KV yang dapat diterima Kadar Analit KV (%) ≥ 1 % 0,1 % 1 ppm 1 ppb 2,5 5 16 32 3. Keterulangan
Suatu metode analisis harus dapat diulang terhadap sampel yang sama dengan prosedur yang sama dan hasil yang memenuhi persyaratan statistik secara umum
4. Sensitivitas
LOD (Limit Of Detection) adalah suatu parameter untuk penentuan suatu sampel dengan kadar yang terkecil akan tetapi masih memberikan tanggap detector yang berbeda dengan pembanding atau tanpa sampel. Sedangkan LOQ
(Limit Of Quantitation) adalah kadar terkecil dari sampel yang dapat dianalisis
dengan hasil penentuan kuantitatif yang menunjukkan akurasi dan presisi yang memadai
5. Selektivitas
Diharapkan detektor instrument hanya memberikan tanggapan terhadap sinyal molekul yang spesifik atau tertentu
6. Kemantapan
Idealnya metode analisis akan memberikan hasil sama kalau sampelnya sama walaupun pengerjaannya dengan merk instrument yang berbeda, waktu, dan tempat yang berbeda pula.
F. Landasan Teori
Penetapan kadar parasetamol dan ibuprofen dapat dilakukan secara spektrofotometri UV. Parasetamol mempunyai serapan maksimal pada panjang gelombang 244 nm. Ibuprofen mempunyai serapan maksimal pada 221 nm. Kedua zat ini larut dalam pelarut yang sama yaitu metanol sehingga dapat ditetapkan kadarnya secara bersama-sama. Kedua senyawa tersebut mempunyai selisih panjang gelombang yang tidak terlalu besar sehingga kurva serapan masing-masing komponen saling tumpang tindih secara keseluruhan maka dapat dilakukan analisis multikomponen secara spektrofotometri UV dengan aplikasi panjang gelombang berganda yang berkembang dari teknik persamaan simultan.
Metode spektrofotometri UV dengan modifikasi metode panjang gelombang berganda dapat digunakan untuk analisis campuran parasetamol dan ibuprofen. Untuk mengetahui ketelitian dan ketepatan dari metode spektrofotometri UV yang akan digunakan untuk penetapan kadar campuran parasetamol dan ibuprofen, metode spektrofotometri UV ini harus divalidasi terlebih dahulu. Parameter yang digunakan untuk validasi metode adalah akurasi dan presisi. Metode spektrofotometri UV ini memiliki akurasi dan presisi yang
baik maka metode ini dapat diaplikasikan untuk menetapkan kadar campuran parasetamol dan ibuprofen dalam tablet.
G. Hipotesis
Metode spektrofotometri UV dengan aplikasi panjang gelombang berganda untuk penetapan kadar campuran parasetamol dan ibuprofen memiliki akurasi dan presisi yang baik.
BAB III
METODOLOGI PENELITIAN
A. Jenis Dan Rancangan Penelitian
Penelitian ini adalah penelitian non eksperimental deskriptif karena tidak ada subjek uji yang dimanipulasi atau dikenai perlakuan.
B. Variabel Penelitian
1. Variabel bebas dalam penelitian ini adalah panjang gelombang yang digunakan (variable continuous)
2. Variabel tergantung dalam penelitian ini adalah kadar campuran parasetamol dan ibuprofen yang digunakan untuk analisis hasil validasi (variable
continuous)
3. Variabel pengacau terkendali dalam penelitian ini adalah pelarut yang digunakan.
C. Definisi Operasional
1. Analisis multikomponen secara spektrofotometri UV adalah analisis kuantitatif suatu komponen zat dalam campuran dengan menggunakan teknik analisis spektroskopik yang memakai sumber radiasi elektromagnetik ultraviolet.
2. Campuran Parasetamol dan ibuprofen adalah campuran antara parasetamol dan ibuprofen dengan perbandingan 7:4.
3. Panjang gelombang pengamatan adalah metode pengamatan yang dilakukan pada 5 panjang gelombang yang berbeda.
D. Bahan Penelitian
Bahan-bahan yang digunakan dalam penelitian ini adalah parasetamol mutu working standar (No. COA 0920032), ibuprofen mutu working standar (No. COA 50909135) dari PT. KONIMEX, pelarut yang digunakan adalah metanol pro analisis.
E. Alat Penelitian
Alat-alat yang dipergunakan dalam penelitian ini adalah spektrofotometer UV-Vis (OPTIMA SP3000F), neraca analitik, micropipet 1000µL, kuvet, dan alat-alat gelas yang biasa digunakan di Laboratorium analisis..
F. Tata Cara Penelitian 1. Pembuatan larutan baku Parasetamol
Sebanyak 10 mg parasetamol ditimbang kurang lebih seksama dan dilarutkan dalam metanol hingga 10,0 ml. Ambil 1,0 ml larutan tersebut encerkan dengan aquadest hingga 10,0 ml. Dari larutan tadi dibuat larutan dengan seri kadar 0,4; 0,5; 0,7; 0,8; 1,0; 1,1 mg/100ml, yakni dengan mengencerkan 0,4; 0,5; 0,7; 0,8; 1,0; 1,1 ml dalam aquadest hingga 10,0 ml.
2. Pembuatan larutan baku Ibuprofen
Sebanyak 10 mg ibuprofen ditimbang seksama dan dilarutkan dalam metanol hingga 10,0 ml. Ambil 1,0 ml larutan tersebut encerkan dengan aquadest hingga 10,0 ml. Dari larutan tadi dibuat larutan dengan seri kadar 0,6; 0,8; 1,0; 1,1; 1,2; 1,4 mg/100ml, yakni dengan mengencerkan 0,6; 0,8; 1,0; 1,1; 1,2; 1,4 ml dalam aquadest hingga 10,0 ml.
3. Penentuan panjang gelombang
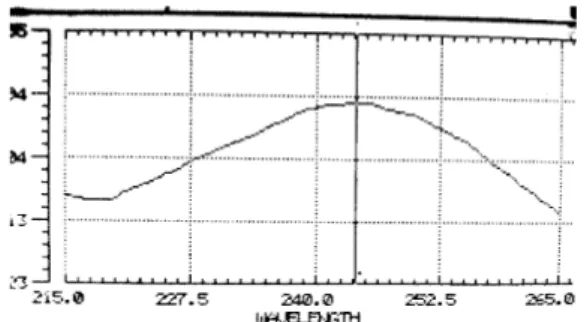
Dari seri kadar yang telah diperoleh pada penetapan rentang kadar parasetamol-ibuprofen, masing-masing diambil satu seri kadar yaitu konsentrasi tengah dan dilakukan pengukuran absorbansi kedua larutan pada rentang panjang gelombang 215-265nm, sehingga dapat diketahui absorbansi masing-masing larutan pada berbagai panjang gelombang.
Dibuat spektrum serapan antara panjang gelombang lawan absorbansi. Menentukan 5 panjang gelombang pada daerah tumpang tindih dari kedua spektrum serapan yang diperoleh. Panjang gelombang yang diperoleh digunakan untuk mengukur absorbansi larutan baku parasetamol-ibuprofen.
4. Penentuan harga Serapan Jenis
Larutan baku parasetamol dan ibuprofen yang telah dibuat, diukur absorbansinya pada multi panjang gelombang yang telah ditentukan. Harga serapan jenis kedua senyawa ditentukan dengan menggunakan metode regresi linear yang dioperasikan pada data konsentrasi dan absorbansi masing-masing senyawa pada setiap panjang gelombang pengukuran.
Dari persamaan regresi yang diperoleh, y = bx + a , y adalah harga serapan (A), b adalah koefisien regresi yang menunjukkan harga serapan jenis (a), x adalah kadar (mg/100ml), sedangkan a adalah konstanta.
5. Pengamatan absorbansi larutan sampel
a. Pembuatan sampel campuran parasetamol-ibuprofen. Dibuat larutan baku parasetamol dan ibuprofen dengan menimbang masing-masing sebanyak 10 mg, kemudian dilarutkan dalam 10 ml metanol, sebanyak 5 replikasi. Dari tiap replikasi larutan baku parasetamol dan ibuprofen masing-masing diambil 1,05 ml dan 0,6 ml, campur, tambah aquadest sampai 10 ml Sebanyak 1,0 ml dari larutan tersebut diencerkan dengan aquadest hingga 10,0 ml. Larutan ini diukur pada 5 panjang gelombang yang diperoleh pada prosedur di atas. Absorbansi hasil pengukuran ini lalu disebut sebagai absorbansi campuran.
b. Perhitungan kadar parasetamol-ibuprofen dalam campuran. Perhitungan kadar masing-masing komponen dalam campuran dilakukan atas dasar absorbansi campuran (Ac) dan serapan jenis tiap komponen pada multi panjang gelombang yang telah diketahui dari hasil pengukuran dengan menggunakan persamaan matriks:
G. Analisis Hasil
Analisis hasil dilakukan untuk mengetahui validitas metode yang digunakan dalam penelitian. Parameter yang diukur:
1. Akurasi
Penilaian akurasi berdasarkan perolehan kembali (recovery). Nilai
recovery dihitung dari kadar yang terukur atau kadar hasil dibandingkan dengan
kadar yang sebenarnya dikalikan 100%. Akurasi dikatakan baik jika recovery berada dalam rentang 90-110%. Recovery dapat dirumuskan sebagai berikut:
Recovery = Kadar hasil
2. Presisi
Penentuan presisi berdasarkan harga koefisien variasi (KV) atau
Coefficient of Variation (CV). Jika CV lebih kecil dari 2%, maka dinilai
mempunyai presisi yang baik. Koefisien variasi (CV) diperoleh dengan rumus: CV = Standar deviasi kadar hasil
X 100% Kadar sebenarnya
Harga rerata kadar hasil
X 100%
Recovery =
BAB IV
HASIL DAN PEMBAHASAN
Penetapan kadar campuran parasetamol dan ibuprofen dalam sampel dengan menggunakan metode spektrofotometri UV dengan aplikasi panjang gelombang berganda belum pernah dilakukan sebelumnya sehingga sebelum dialikasikan maka metode ini harus divalidasi terlebih dahulu. Langkah-langkah yang harus dilakukan, sebagai berikut:
A. Pembuatan larutan baku Parasetamol dan Ibuprofen
Larutan baku parasetamol dan ibuprofen dengan seri konsentrasi tertentu dibuat dengan cara melarutkan masing-masing bahan parasetamol dan ibuprofen tersebut kedalam pelarut yang sesuai. Pelarut yang sesuai untuk melarutkan kedua bahan tersebut adalah metanol. Metanol digunakan sebagai pelarut karena parasetamol dan ibuprofen sangat mudah larut di dalam metanol. Metanol yang dipakai adalah metanol pro analisis. Selain itu juga, diketahui metanol memiliki serapan pada panjang gelombang dibawah 210 nm, sehingga metanol akan meneruskan atau tidak akan menyerap sinar dengan panjang gelombang diatas 210 nm, akibatnya metanol tidak akan mengganggu spektrum serapan dari parasetamol dan ibuprofen, karena metanol tidak memberikan serapan pada panjang gelombang diatas 210 nm.
Larutan baku parasetamol dan ibuprofen dengan berbagai konsentrasi diukur serapannya untuk menentukan serapan jenis parasetamol dan ibuprofen pada tiap panjang gelombang yang digunakan dalam penelitian. Larutan baku yang diperoleh terlebih dahulu diukur serapannya pada panjang gelombang
maksimum masing-masing larutan. Rentang serapan yang diperbolehkan untuk larutan baku adalah serapan antara 0,2-0,8 pada panjang gelombang dimana serapannya maksimal karena pembacaan serapan pada rentang tersebut memberikan prosentase kesalahan analisis yang masih dapat diterima yaitu (0,5-1,0%).
Berdasarkan hasil pengukuran serapannya, larutan parasetamol dengan konsentrasi 0,4; 0,5; 0,7; 0,8; 1,0; 1,1 mg% dan larutan ibuprofen dengan konsentrasi 0,6; 0.8; 1,0; 1,1; 1,2; 1,4 mg% dapat memberikan serapan dalam rentang 0,2-0,8. Untuk melihat rentang serapannya adalah dengan melakukan pengukuran pada panjang gelombang maksimum dari masing-masing komponen dengan 3 seri konsentrasi yaitu konsentrasi rendah, sedang, tinggi. Dipilih 3 konsentrasi ini karena dengan menganalisa serapan pada konsentrasi rendah, tengah, tinggi dapat mewakili konsentrasi-konsentrasi lain dalam seri larutan baku. Bila serapan pada konsentrasi rendah, tengah, tinggi dari senyawa sudah memberikan serapan yang baik, maka dapat dipastikan seri konsentrasi lainnya juga dapat memberikan serapan yang baik juga. Dari hasil pengukuran diperoleh spektrum dari parasetamol dan ibuprofen pada 3 seri konsentrasi yaitu sebagai berikut :
Gambar 8. Spektrum parasetamol konsentrasi tengah 0,7 mg% Abs 0,482
Gambar 9. Spektrum parasetamol konsentrasi tinggi 1,1 mg% Abs 0,676
Gambar 10. Spektrum ibuprofen konsentrasi rendah 0,6 mg% Abs 0,345
Gambar 11. Spektrum ibuprofen konsentrasi tengah 1,0 mg% Abs 0,469
Secara teoritis serapan maksimum untuk parasetamol adalah 244 nm, pada penelitian didapatkan serapan maksimum larutan parasetamol dalam metanol adalah sama dengan panjang gelombang teoritis, yaitu 244 nm. Untuk serapan maksimal ibuprofen secara teoritis adalah 221 nm, pada penelitian didapat serapan maksimal ibuprofen adalah 223 nm. Terjadi pergeseran yang disebabkan oleh perbedaan pelarut, secara teori pelarut yang digunakan adalah metanol, pada penelitian pelarut yang digunakan adalah metanol-aquadest, sehingga hal ini berakibat pada pergeseran serapan maksimal ibuprofen. Adanya komponen pelarut polar yaitu aquadest menyebabkan pergeseran panjang gelombang yang lebih tinggi karena dengan pelarut polar akan menyebabkan transisi elektron bebas semakin mudah terjadi, sehingga panjang gelombang serapannya bergeser lebih besar. Pergeseran panjang gelombang yang dikenal adalah pergeseran bathokromik dan pergeseran hipokromik, untuk pergeseran pada serapan ibuprofen adalah pergeseran batokromik, yaitu pergeseran ke arah panjang gelombang yang lebih besar.
Dilihat dari kurva serapan dari larutan baku parasetamol dan ibuprofen, maka kurva serapan dari kedua senyawa memiliki bentuk kurva yang berbeda, yaitu puncak kurva dari ibuprofen berada pada panjang gelombang yang lebih kecil dari parasetamol, yaitu pada 223 nm. Kurva serapan parasetamol memberikan puncak serapan pada panjang gelombang 244 nm. Meski bentuk kurva dari parasetamol dan ibuprofen berbeda, tapi kedua senyawa memberikan bentuk kurva serapan yang konsisten atau mirip pada konsentrasi rendah, tengah, tinggi. Perbedaan bentuk dan puncak kurva dari parasetamol dan ibuprofen
disebabkan karena perbedaan bentuk struktur dari kedua senyawa. Kedua senyawa sama-sama memiliki ikatan kromofor yang sama panjang sehingga mereka dapat memiliki serapan di daerah UV, tapi hal yang membedakan adalah adanya gugus auksokrom pada struktur parasetamol sedangkan pada struktur ibuprofen hanya memiliki ikatan kromofor dan tidak memiliki auksokrom. Auksokrom ini membantu untuk meningkatkan intensitas serapan dari suatu senyawa sehingga panjang gelombang yang akan diserap juga makin besar, seperti pada parasetamol. Oleh karena itu, maka kurva parasetamol memiliki puncak serapan pada panjang gelombang yang lebih besar. Struktur sistem kromofor dan auksokrom dari parasetamol dan ibuprofen yaitu:
Gambar 13. Struktur kromofor dan auksokrom parasetamol
Gambar 14. Struktur kromofor ibuprofen
Keterangan = : kromofor --- : auksokrom
. Larutan baku parasetamol dan ibuprofen ini dibuat dalam 6 seri konsentrasi karena dalam penelitian ini ada 5 panjang gelombang sehingga akan
didapat 30 data yang merupakan jumlah minimal untuk mendapatkan data dengan karakteristik populasi yang terdistribusi normal.
B. Penentuan Panjang Gelombang Penelitian
Setelah didapat spektrum serapan dari masing-masing komponen, maka spektrum ini kemudian digunakan untuk menentukan panjang gelombang penelitian yang digunakan. Pembacaan spektrum serapan ini dilakukan pada rentang panjang gelombang 215-265 nm, karena pada rentang panjang gelombang ini parasetamol dan ibuprofen tumpang tindih secara keseluruhan. Penentuan dilakukan dengan menggabungkan 2 spektrum tersebut kemudian dicari 5 titik sebagai panjang gelombang yang akan digunakan. Spektrum yang dipilih adalah spektrum parasetamol konsentrasi tinggi dan spektrum ibuprofen konsentrasi rendah, karena mewakili perbandingan konsentrasi parasetamol dan ibuprofen yaitu 7:4
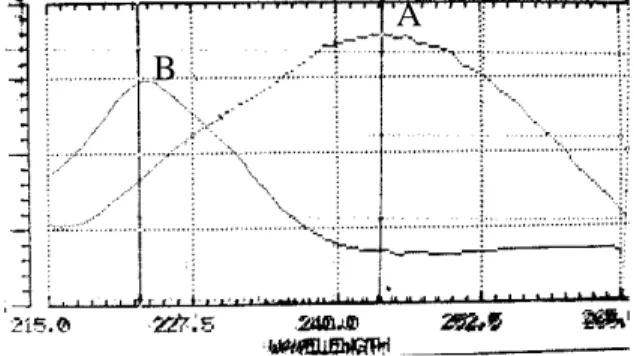
Spektrum overlapping dari spektrum parasetamol dan ibuprofen dapat dilihat sebagai berikut:
Gambar 15. Spektrum tumpang tindih parasetamol dan ibuprofen perbandingan konsentrasi 7:4
Keterangan = A : Spektrum serapan parasetamol B : Spektrum serapan ibuprofen
A B
Berdasarkan kurva serapan tersebut maka dapat ditentukan 5 panjang gelombang yang akan digunakan. Lima panjang gelombang yang digunakan adalah 223 nm pada panjang gelombang ini adalah serapan maksimal dari ibuprofen dan parasetamol masih memberikan serapan pada panjang gelombang ini, 225 nm, pada panjang gelombang ini parasetamol masih memberikan serapan dan ibuprofen juga masih memberikan serapan yang cukup besar meski konsentrasinya lebih kecil, 227 nm, pada panjang gelombang ini serapan parasetamol cukup besar dan ibuprofen masih memberikan serapan yang cukup besar, 230 nm, panjang gelombang ini merupakan titik potong kedua kurva serapan parasetamol dan ibuprofen, 235 nm, pada panjang gelombang ini serapan parasetamol cukup besar dan ibuprofen masih memberikan serapan.
Jadi lima panjang gelombang yang digunakan untuk pengukuran pada penelitian ini adalah 223 nm, 225 nm, 227nm, 230 nm, dan 235 nm.
C. Penentuan Serapan Jenis
Harga serapan jenis merupakan nilai yang menunjukkan seberapa besar kontribusi serapan suatu senyawa terhadap serapan dari campuran senyawa pada suatu panjang gelombang.
Penentuan harga serapan jenis ini dilakukan dengan mengukur serapan masing-masing larutan baku baik parasetamol dan ibuprofen pada panjang gelombang 223, 225, 227, 230, 235 nm. Penentuan harga serapan jenis ini harus mematuhi persamaan dalam hukum Beer yaitu:
A = abc
Dimana A = serapan a = serapan jenis b = tebal kuvet c = konsentrasi
Namun pada saat pengukuran serapan larutan parasetamol dan ibuprofen dapat terjadi gangguan instrumen yang berupa derau atau noise (e). Adanya derau atau noise ini menurut hukum Beer:
A = abc + e
Apabila ketebalan kuvet (b) adalah 1 cm maka persamaan tersebut menjadi:
A = ac + e
Dalam penelitian ini penentuan harga serapan jenis dilakukan dengan mengoperasikan data serapan pada tiap panjang gelombang terhadap konsentrasi larutan dalam persamaan regresi linier yang analog dengan persamaan dalam hukum Beer. Persamaan regresi linier adalah:
Y = bx + a
Pada persamaan regresi linier tersebut, y menunjukkan serapan (A), b menunjukkan serapan jenis (a), x adalah konsentrasi (c) dalam mg%, sedangkan a adalah derau atau noise (e) yang dapat diabaikan.
Harga noise sangat kecil sehingga berada disekitar garis lurus A = ac pada hukum Beer dengan demikian noise dapat diabaikan. Secara matematika harga noise diasumsikan mempunyai distribusi normal dengan variansi konstan
dan nilai tengah sama dengan nol. Untuk memperkecil derau atau noise maka harga koefisien relasi yang dipilih adalah harga koefisien relasi yang mendekati satu sehingga korelasi antara konsentrasi dan serapan benar-benar atau mendekati linier.
Derau atau noise ini tidak disebabkan oleh materi yang dianalisis akan tetapi disebabkan oleh gangguan instrumen seperti rangkaian elektronik, getaran selama alat sedang bekerja, variansi temperatur dan sebagainya.
Setelah dilakukan pengukuran serapan masing-masing larutan pada panjang gelombang penelitian dengan replikasi sebanyak 3 kali, ternyata harga serapan jenis antar replikasi hampir sama. Ini menunjukkan bahwa serapan jenis pada tiap panjang gelombang memang serapan jenis dari parasetamol dan ibuprofen. Hasil pengamatan serapan dan harga serapan jenis parasetamol dan ibuprofen adalah sebagai berikut:
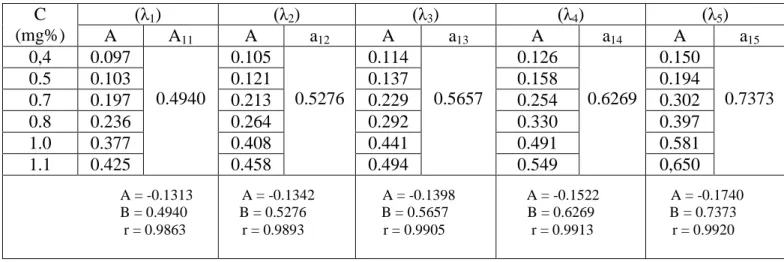
Tabel IV. Data perhitungan serapan jenis Parasetamol Replikasi I C (mg%) (λ1) (λ2) (λ3) (λ4) (λ5) A A11 A a12 A a13 A a14 A a15 0,4 0.097 0.4940 0.105 0.5276 0.114 0.5657 0.126 0.6269 0.150 0.7373 0.5 0.103 0.121 0.137 0.158 0.194 0.7 0.197 0.213 0.229 0.254 0.302 0.8 0.236 0.264 0.292 0.330 0.397 1.0 0.377 0.408 0.441 0.491 0.581 1.1 0.425 0.458 0.494 0.549 0,650 A = -0.1313 A = -0.1342 A = -0.1398 A = -0.1522 A = -0.1740 B = 0.4940 B = 0.5276 B = 0.5657 B = 0.6269 B = 0.7373 r = 0.9863 r = 0.9893 r = 0.9905 r = 0.9913 r = 0.9920
Tabel V. Data perhitungan serapan jenis Parasetamol Replikasi II C (mg%) (λ1) (λ2) (λ3) (λ4) (λ5) A a11 A a12 A a13 A a14 A a15 0,4 0.091 0.3483 0.105 0.3908 0.119 0.4317 0.139 0.4704 0.176 0.5447 0.5 0.115 0.130 0.141 0.162 0.197 0.7 0.167 0.195 0.226 0.251 0.310 0.8 0.213 0.239 0.269 0.299 0.361 1.0 0.281 0.328 0.367 0.417 0.511 1.1 0.339 0.376 0.414 0.454 0,528
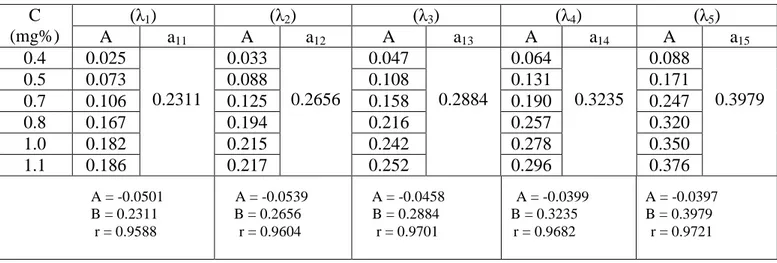
Tabel VI. Data perhitungan serapan jenis Parasetamol Replikasi III C (mg%) (λ1) (λ2) (λ3) (λ4) (λ5) A a11 A a12 A a13 A a14 A a15 0.4 0.025 0.2311 0.033 0.2656 0.047 0.2884 0.064 0.3235 0.088 0.3979 0.5 0.073 0.088 0.108 0.131 0.171 0.7 0.106 0.125 0.158 0.190 0.247 0.8 0.167 0.194 0.216 0.257 0.320 1.0 0.182 0.215 0.242 0.278 0.350 1.1 0.186 0.217 0.252 0.296 0.376
Tabel VII. Data perhitungan serapan jenis Ibuprofen Replikasi I C (mg%) (λ1) (λ2) (λ3) (λ4) (λ5) A A21 A A22 A A23 A A24 A A25 0.6 0.239 0.4854 0.235 0.4684 0.222 0.4321 0.168 0.3235 0.065 0.1588 0.8 0.338 0.331 0.311 0.235 0.097 1.0 0.498 0.492 0.464 0.355 0.160 1.1 0.503 0.497 0.469 0.360 0.167 1.2 0.552 0.539 0.503 0.379 0.170 1.4 0.613 0.597 0.555 0.416 0,184 A = -0.0501 A = -0.0539 A = -0.0458 A = -0.0399 A = -0.0397 B = 0.2311 B = 0.2656 B = 0.2884 B = 0.3235 B = 0.3979 r = 0.9588 r = 0.9604 r = 0.9701 r = 0.9682 r = 0.9721 A = -0.0602 A = -0.0643 A = -0.0678 A = -0.0658 A = -0.0613 B = 0.3483 B = 0.3908 B = 0.4317 B = 0.4704 B = 0.5447 r = 0.9918 r = 0.9951 r = 0.9968 r = 0.9953 r = 0.9924 A = -0.0333 A = -0.0277 A = -0.0186 A = -0.0101 A = -0.0209 B = 0.4824 B = 0.4684 B = 0.4321 B = 0.3235 B = 0.1588 r = 0.9805 r = 0.9768 r = 0.9729 r = 0.9656 r = 0.9489
Tabel VIII. Data perhitungan serapan jenis Ibuprofen Replikasi II C (mg %) (λ1) (λ2) (λ3) (λ4) (λ5) A A21 A A22 A A23 A A24 A A25 0.6 0.142 0.2535 0.140 0.2514 0.132 0.2361 0.093 0.1754 0.022 0.0625 0.8 0.219 0.215 0.200 0.139 0.037 1.0 0.263 0.258 0.237 0.163 0.054 1.1 0.293 0.288 0.270 0.201 0.063 1.2 0.326 0.316 0.296 0.211 0.065 1.4 0.340 0.339 0.318 0.229 0.069
Tabel IX. Data perhitungan serapan jenis Ibuprofen Replikasi III C (mg %) (λ1) (λ2) (λ3) (λ4) (λ5) A A21 A A22 A A23 A A24 A A25 0.6 0.116 0.3602 0.115 0.3533 0.106 0.3359 0.070 0.2340 0.012 0.1174 0.8 0.143 0.149 0.144 0.098 0.019 1.0 0.212 0.218 0.208 0.117 0.041 1.1 0.279 0.276 0.259 0.142 0.064 1.2 0.351 0.345 0.325 0.230 0.083 1.4 0.375 0.367 0.350 0.245 0.097
Nilai serapan jenis yang dipakai adalah nilai serapan jenis dari parasetamol dan ibuprofen pada replikasi II. Pemilihan nilai serapan jenis ini dapat ditentukan berdasarkan harga r hitung. Nilai r hitung dibandingkan dengan nilai r tabel dengan taraf kepercayaan 95% dengan df 4 yaitu 0,811. Berdasarkan
Keterangan:
a11= serapan jenis parasetamol pada 223 nm a21= serapan jenis ibuprofen pada 223 nm a12= serapan jenis parasetamol pada 225 nm a22= serapan jenis ibuprofen pada 225 nm a13= serapan jenis parasetamol pada 227 nm a23= serapan jenis ibuprofen pada 227 nm a14= serapan jenis parasetamol pada 230 nm a24= serapan jenis ibuprofen pada 230 nm a15= serapan jenis parasetamol pada 235 nm a25= serapan jenis ibuprofen pada 235 nm
A = 0.0061 A = 0.0037 A = 0.0022 A = -0.0057 A = -0.0119 B = 0.2535 B = 0.2514 B = 0.2361 B = 0.1754 B = 0.0625 r = 0.9792 r = 0.9853 r = 0.9868 r = 0.9825 r = 0.9670 A = -0.1182 A = -0.1161 A = -0.1099 A = -0.0876 A = -0.0667 B = 0. 3602 B = 0. 3533 B = 0. 3359 B = 0. 2340 B = 0. 1174 r = 0.9743 r = 0.9715 r = 0.9793 r = 0.9332 r = 0.9735
data tersebut terlihat bahwa nilai r hitung parasetamol dan ibuprofen pada replikasi II lebih besar dari nilai r tabel. Ini berarti bahwa persamaan tersebut mempunyai linearitas yang baik, karena nilai r hitung semakin mendekati 1. Dasar lain dalam memilih nilai serapan jenis yang akan digunakan dapat dilihat dari nilai a dari persamaan, nilai a ini melambangkan noise atau pengganggu. Dalam suatu penelitian harga noise yang diterima adalah semakin mendekati 0, karena menunjukkan bahwa hasil penelitian ini dapat dipercaya. Nilai a dari parasetamol ataupun ibuprofen pada replikasi II memberikan hasil yang baik, yaitu nilai a nya semakin mendekati 0, meskipun untuk nilai a dari parasetamol dan ibuprofen replikasi 2 bukan nilai a yang terkecil. Hal pertama yang harus diperhatikan adalah melihat nilai r nya. Nilai r diterima bila lebih besar dari nilai r tabel, dan nilai r yang semakin mendekati 1.
Berdasarkan pada penilaian tersebut maka nilai serapan jenis yang digunakan untuk parasetamol dan ibuprofen adalah nilai serapan jenis pada replikasi kedua, didukung dengan nilai a dan r yang baik
Dari data harga serapan jenis parasetamol dan ibuprofen, nilai serapan jenis prasetamol pada panjang gelombang 223, 225, 227, 230, 235 nm, memiliki nilai yang lebih besar daripada nilai serapan jenis ibuprofen pada ke-5 panjang gelombang tersebut. Hal ini menunjukkan bahwa kontribusi serapan parasetamol dalam campuran lebih besar dari kontribusi serapan ibuprofen dalam campuran. Hal ini dikarenakan konsentrasi parasetamol dalam campuran lebih besar dari pada konsentrasi ibuprofen (7:4). Data serapan jenis yang diperoleh ini kemudian
digunakan untuk menetapkan kadar parasetamol dan ibuprofen dalam campuran dengan perhitungan matriks.
D. Penentuan Kadar Parasetamol dan Ibuprofen
Sampel campuran yang digunakan dalam penelitian ini terdiri dari parasetamol dan ibuprofen dengan perbandingan komposisi 7:4. Perbandingan komposisi ini didasarkan pada komposisi masing-masing zat dalam sediaan yang telah beredar di pasaran. Larutan sampel dibuat sebanyak lima replikasi, dengan tujuan agar data yang diperoleh lebih akurat dan representatif. Kemudian larutan tersebut diukur serapannya pada kelima panjang gelombang yaitu 223, 225, 227, 230, 235 nm.
Dari hasil pengukuran spektrum sampel campuran diperoleh bentuk spektrum sebagai berikut:
Gambar 16. Spektrum sampel campuran parasetamol & ibuprofen
Dari bentuk spektrum campuran parasetamol dan ibuprofen berbeda dengan bentuk spektrum tumpang tindih (gambar 15), karena spektrum campuran merupakan gabungan dari 2 senyawa dalam satu larutan, sehingga tidak dapat diperoleh bentuk spektrum yang sama dengan bentuk spektrum overlapping, karena pada spektrum overlapping bukan merupakan gabungan spektrum
parasetamol dan ibuprofen, tapi merupakan tumpang tindih dari spektrum masing-masing larutan. Pada spektrum campuran, parasetamol dan ibuprofen terdapat dalam satu larutan sehingga spektrum yang diperoleh merupakan spektrum dari campuran parasetamol dan ibuprofen, bukan gabungan dari 2 spektrum. Oleh karena itu spektrum yang dihasilkan berbeda dengan spektrum overlapping.
Data serapan larutan sampel campuran parasetamol dan ibuprofen yang didapat digunakan untuk mengukur kadar masing-masing campuran, dengan cara memasukkan data yang tersedia pada rumus perhitungan matriks. Kemudian dari perhitungan akan diperoleh kadar masing-masing komponen campuran. Sehingga dapat dihitung nilai recovery dan %CV nya.
Tabel X. Data hasil perhitungan kadar, recovery, dan % CV Nomor sampel Parasetamol Ibuprofen Kadar terukur (mg%) Kadar teoritis (mg%) Recovery (%) Kadar terukur (mg%) Kadar teoritis (mg%) Recovery (%) 1 1.0249 1.05 97.610 0.6074 0.654 92.875 2 1.0161 1.1235 90.441 0.6085 0.6 101.417 3 1.0094 1.1025 91.556 0.6038 0.642 94.049 4 1.0154 1.1235 90.378 0.6067 0.63 96.302 5 1.0140 1.0185 99.558 0.6044 0.624 96.859 Rerata recovery % CV 93.9086 Rerata recovery % CV 96.3004 0.555 0.329
Recovery digunakan untuk menentukan akurasi suatu metode analisis
sedangkan % CV digunakan untuk menentukan presisi suatu metode analisis. Akurasi suatu metode analisis untuk bahan obat dengan kadar kecil dikategorikan baik apabila nilai range recovery nya antara 90-107%, karena kadar analit yang diperoleh 0,0105 mg/ml dan 0,006 mg/ml, jadi range recovery yang
dipakai 90-107%. Sedangkan suatu metode analisis dikatakan mempunyai presisi yang baik apabila % CV < 2%.
Berdasarkan data tersebut range nilai recovery parasetamol dan ibuprofen adalah 90,3%-99,6% dan 92,8%-101,5%. Dan nilai % CV untuk parasetamol dan ibuprofen adalah 0,555% dan 0,329%. Nilai range recovery parasetamol dan ibuprofen masuk dalam range 90-107%, sehingga dapat dikatakan metode ini memiliki akurasi yang baik. Nilai % CV dari parasetamol dan ibuprofen juga masuk dalam range <2%, sehingga dapat dikatakan metode ini juga memiliki presisi yang baik. Dari data tersebut dapat disimpulkan bahwa metode penetapan kadar campuran parasetamol dan ibuprofen dengan spektrofotometri UV dengan panjang gelombang berganda memiliki akurasi dan presisi yang baik.
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Penetapan kadar campuran Parasetamol dan Ibuprofen secara spektrofotometri UV dengan aplikasi metode panjang gelombang berganda memiliki akurasi dan presisi yang baik.
B. Saran
1. Perlu dilakukan penelitian lebih lanjut untuk mengaplikasikan metode penetapan kadar capuran parasetamol dan ibuprofen dalam sediaan obat, misal tablet.
2. Perlu dilakukan penelitian lebih lanjut tentang penetapan kadar campuran parasetamol dan ibuprofen dengan metode yang lain.
DAFTAR PUSTAKA
Anonim, 1989, The Merck Index, 11thED, 6688, 6987, Merck & Co, New Jersey Anonim, 1995, Farmakope Indonesia IV, 643, 489, Departemen Kesehatan
Republik Indonesia, Jakarta
Anonim, 2000, IONI (Informatorium Obat Nasional Indonesia), 183, 355, Departemen Kesehatan Republik Indonesia & Dirjen POM, Jakarta
Day, R. A., Underwood, A. L., 1980, Quantitative Analysis, 3rd Ed, 355-391,
Prentice Hall Ltd, New Delhi
Day, R. A., Underwood, A. L., 1996, Kimia Analisis Kuantitatif, Edisi V, 382-415, Erlangga, Jakarta
Mulja, M., Suharman, 1995, Analisis Instrumental, 1-59, Airlangga University Press, Surabaya
Mulja, M., Hanwar, D., 2003, Prinsip-prinsip Cara Berlaboratorium yang Baik (Good Laboratory Practice), Majalah Farmasi Airlangga, vol.III, No. 2 Nurkhayati, Tri, 2000, Analisis Multikomponen Secara Spektrofotometri UV
Campuran Oktil Metoksisinamat Dan Oksibenzon Dengan Aplikasi Metode Panjang Gelombang Berganda, Skripsi, Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta
Pescok, R., L., Shields, L. D., 1976, Modern Methodes of Chemical Analysis, 2nd Ed., 115-239, John Willey & Sons, New York
Sastrohamidjojo, H., 1991, Spektroskopi, 1-43, Liberty, Yogyakarta
Silvesterstein, R. M., Bassler, G. C., Morril, T. C., 1974, Spectrometric
Identification of Organic Compound, 3rd Ed, 231-252, John Willey & Sons, Toronto
Skoog, D. A., 1985, Principle of Instrumental Analysis, 3rdEd, 113-213, Saunders College Publishing, Philadelphia
Skoog, West, Holler, 1994, Analitical Chemistry (An Introduction), 6th Ed, 383-432, Sounders College Publishing, Philadelphia
Zainuddin, M., 1994, Pengaruh Rasio Harga Serapan Jenis Terhadap Akurasi Hasil Analisis Spektrofotometri Dengan Teknik Persamaan Simultan,
Zainuddin, M., 1999(a), Pengaruh Selisih Panjang Gelombang Maksimum Antar Komponen Terhadap Akurai Kuantitatif Campuran Bikomponen Secara Spektrofotometri Dengan Teknik Persamaan Simultan, J. MIPA 4 (1) Zainuddin, M., 1999 (b), Aplikasi Metode Panjang Gelombang Berganda Pada
Analisis Multikomponen Secara Spektrofotometri Terhadap Campuran Fenilbutazon dan Metampiron, Majalah Farmasi Indonesia, 10(4). 217-223
Lampiran 1. Sertifikat bahan Sertifikat Parasetamol
Lampiran 2. Data Penimbangan
Tabel XI. Data penimbangan Parasetamol untuk larutan baku
NO Keterangan Bobot parasetamol
(gram)
1 Replikasi 1 0,01
2 Replikasi 2 0,0106
3 Replikasi 3 0,0095
Tabel XII. Data penimbangan Ibuprofen untuk larutan baku
Tabel XIII. Data penimbangan Parasetamol dan Ibuprofen untuk larutan sampel
NO Keterangan Bobot Parasetamol(gram) Bobot Ibuprofen(gram) 1 Replikasi I 0,0100 0,0109 2 Replikasi II 0,0107 0,0100 3 Replikasi III 0,0105 0,0107 4 Replikasi IV 0,0107 0,0105 5 Replikasi V 0,0097 0,0104
NO Keterangan Bobot ibuprofen
(gram)
1 Replikasi 1 0,0094
2 Replikasi 2 0,0098
Lampiran 3. Skema Kerja dan contoh perhitungan kadar parasetamol dan ibuprofen dalam campuran.
Timbang 10 mg parasetamol dan ibuprofen
Larutkan 10 mg parasetamol dan ibuprofen dalam 10ml metanol p.a
Dari masing-masing larutan, ambil 1,06 ml dari larutan parasetamol dan 0,6 ml dari larutan ibuprofen
Campur kedua larutan dan add aquadest sampai 10 ml (larutan A)
Ambil 1ml dari larutan campuran add aquadest sampai 10 ml (larutan B)
Larutan B diukur pada 5 panjang gelombang penelitian
Lakukan replikasi sebanyak 5 kali
Perhitungan kadar campuran parasetamol dan ibuprofen dalam Larutan B berdasarkan serapan campuran menggunakan persamaan matriks sebagai berikut :
a. Contoh perhitungan kadar teoritis parasetamol dan ibuprofen: Sampel untuk replikasi pertama
Serbuk ibuprofen yang tertimbang: 0,0109 gram
larutan stok campuran dibuat dengan mengambil 1,05 ml dan 0,6 ml dari larutan baku parasetamol dan larutan baku ibuprofen, larutkan dalam 10 ml aquadest. Kadar parasetamol dan ibuprofen dalam campuran tersebut:
parasetamol 1,05ml = 1,05 mg/10 ml = 0,105 mg/ml ibuprofen 0,6 ml = o,6 mg/10 ml = 0,06 mg/ml
larutan yang diukur dibuat dengan mengambil 1 ml dari larutan stok dan add aquadest sampai 10 ml. Sehingga kadar parasetamol dan ibuprofen :
Kadar parasetamol = c1x v1= c2x v2 0.105 ml x 10mg/10ml = 10 ml x X mg/ml X mg/ml = 0.0105 x FP 100X X mg/ml = 1.05mg/ml Kadar ibuprofen = c1x v1= c2x v2 0.06 ml x 10.9mg/10ml = 10 ml x X mg/ml X mg/ml = 0.00654 x FP 100 kali X mg/ml = 0.654mg/ml
Jadi kadar teoritis dari parasetamol dan ibuprofen adalah 1,05 mg/ml dan 0,654 mg/ml
b. contoh perhitungan kadar percobaan parasetamol dan ibuprofen Replikasi 1 = 0.3483 0.3908 0.4317 0.4704 0.5447 0.2535 0.2514 0.2361 0.1754 0.0625 0.3488 0.2535 0.3913 0.2514 0.4322 0.2361 0.4709 0.1754 0.5447 0.0625 -1 X 0.3483 0.3908 0.4317 0.4704 0.5447 0.2535 0.2514 0.2361 0.1754 0.0625 0.531 0.546 0.572 0.587 0.601 1.0249 0.6074 C1 C2 C1 C2 =
Keterangan C1= kadar parasetamol
C2 = kadar ibuprofen
Jadi kadar percobaan parasetamol dan ibuprofen dalam campuran 1,0249 mg/ml dan 0,6074 mg/ml
Lampiran 4. Spektrum Parasetamol dan Ibuprofen konsentrasi rendah, tengah, dan tinggi
Gambar 17. Spektrum parasetamol konsentrasi rendah
Gambar 18. Spektrum parasetamol konsentrasi tengah
Gambar 20. Spektrum ibuprofen konsentrasi rendah
Gambar 21. Spektrum ibuprofen konsentrasi tengah
Lampiran 5. Spektra tumpang tindih dan spektra campuran parasetamol-ibuprofen
Gambar 23. Spektra tumpang tindih parasetamol dan ibuprofen perbandingan konsentrasi 7:4
Lampiran 6. Perhitungan Serapan Jenis Parasetamol dan Ibuprofen Tabel XIV. Data perhitungan serapan jenis Parasetamol Replikasi I C (mg%) (λ1) (λ2) (λ3) (λ4) (λ5) A A11 A a12 A a13 A a14 A a15 0,4 0.097 0.4940 0.105 0.5276 0.114 0.5657 0.126 0.6269 0.150 0.7373 0.5 0.103 0.121 0.137 0.158 0.194 0.7 0.197 0.213 0.229 0.254 0.302 0.8 0.236 0.264 0.292 0.330 0.397 1.0 0.377 0.408 0.441 0.491 0.581 1.1 0.425 0.458 0.494 0.549 0,650
Tabel XV. Data perhitungan serapan jenis Parasetamol Replikasi II C (mg%) (λ1) (λ2) (λ3) (λ4) (λ5) A a11 A a12 A a13 A a14 A a15 0.4 0.091 0.3483 0.105 0.3908 0.119 0.4317 0.139 0.4704 0.176 0.5447 0.5 0.115 0.130 0.141 0.162 0.197 0.7 0.167 0.195 0.226 0.251 0.310 0.8 0.213 0.239 0.269 0.299 0.361 1.0 0.281 0.328 0.367 0.417 0.511 1.1 0.339 0.376 0.414 0.454 0.528 A = -0.1313 A = -0.1342 A = -0.1398 A = -0.1522 A = -0.1740 B = 0.4940 B = 0.5276 B = 0.5657 B = 0.6269 B = 0.7373 r = 0.9863 r = 0.9893 r = 0.9905 r = 0.9913 r = 0.9920 A = -0.0602 A = -0.0643 A = -0.0678 A = -0.0658 A = -0.0613 B = 0.3483 B = 0.3908 B = 0.4317 B = 0.4704 B = 0.5447 r = 0.9918 r = 0.9951 r = 0.9968 r = 0.9953 r = 0.9924