Lampiran 1. Gambar sediaan tablet B
Lampiran 2. Daftar spesifikasi sediaan tablet B
Nama Produk : Bodrex®
Produksi : Tempo Scan Pacific Nomor Registrasi : DBL8522700810A1 Nomor Bet : 100045
Tanggal Kadaluarsa : September 2020
Lampiran 3. Alat-alat
Gambar 2. Spektrofotometer UV-Visible (Shimadzu UV 1800)
Gambar 3. Neraca analitik (Mettler Toledo)
Lampiran 4. Perhitungan pembuatan HCl 0,1 N HCl pekat = 37% setara dengan 12 N
V1 x N1 = V2 x N2
Lampiran 5. Bagan alir pembuatan larutan induk baku dan serapan maksimum parasetamol
ditimbang sebanyak 50 mg
dimasukkan ke dalam labu tentukur
50 ml
dilarutkan dan dicukupkan dengan pelarut HCl 0,1 N
dipipet 5 ml
dimasukkan ke dalam labu tentukur 50 ml
dicukupkan dengan pelarut HCl 0,1 N
dipipet 0,65 ml
dimasukkan ke dalam labu tentukur 10 ml dicukupkan dengan pelarut HCl 0,1 N
diukur serapan pada panjang gelombang 200-400 nm
Panjang gelombang parasetamol 243,8 nm
Lampiran 6. Bagan alir pembuatan larutan induk baku dan serapan maksimum kafein
ditimbang sebanyak 50 mg
dimasukkan ke dalam labu tentukur 50 ml dilarutkan dan dicukupkan dengan pelarut HCl 0,1 N
dipipet 5 ml
dimasukkan ke dalam labu tentukur 50 ml dicukupkan dengan pelarut HCl 0,1 N
dipipet 0,86 ml
dimasukkan ke dalam labu tentukur 10 ml dicukupkan dengan pelarut HCl 0,1 N
diukur serapan pada panjang gelombang 200 - 400 nm
Baku Kafein
LIB I Kafein 1000 μg/ml
Kafein 8,6 μg/ml
Panjang gelombang kafein 271 nm
Lampiran 7. Bagan alir pembuatan dan pengukuran serapan larutan standar parasetamol
dipipet masing-masing sebanyak 0,3 ml; 0,45 ml; 0,65 ml; 0,75 ml dan 0,9 ml
dimasukkan masing-masing ke dalam labu tentukur 10 ml
diencerkan dengan pelarut HCl 0,1 N Larutan Standar Parasetamol
(3,0 µg/ml; 4,5 µg/ml; 6,5 µg/ml; 7,5 µg/ml dan 9,0 µg/ml)
Data Kalibrasi Parasetamol LIB II Parasetamol 100 μg/ml
Lampiran 8. Bagan alir pembuatan dan pengukuran serapan larutan standar kafein
dipipet masing-masing sebanyak 0,4 ml; 0,6 ml; 0,86 ml; 1,0 ml dan 1,2 ml
dimasukkan masing-masing ke dalam labu tentukur 10 ml
diencerkan dengan pelarut HCl 0,1 N
Larutan Standar Kafein (4,0 µg/ml; 6,0 µg/ml; 8,6 µg/ml;
10,0 µg/ml dan 12,0 µg/ml)
Data Kalibrasi Kafein LIB II Kafein 100 μg/ml
Lampiran 9. Bagan alir penentuan panjang gelombang analisis parasetamol dan kafein
Kafein (8,6 μg/ml) Parasetamol (6,5 μg/ml)
diukur serapan dari masing-masing parasetamol dan kafein pada panjang gelombang 200 - 400 nm
ditumpang tindihkan spektrum serapan masing-masing komponen
ditentukan 5 panjang gelombang analisis diambil panjang gelombang pada spektrum serapan komponen mulai memberikan serapan sampai hampir tidak memberikan serapan
Lampiran 10. Bagan alir pembuatan larutan baku campuran parasetamol dan kafein
Kedua larutan dicampurkan ke dalam labu tentukur 10 ml dicukupkan dengan pelarut HCl 0,1 N
Diambil dari larutan tersebut 1 ml dimasukkan ke dalam labu tentukur 10 ml dicukupkan dengan pelarut HCl 0,1 N
Larutan diukur pada panjang gelombang 200-400 nm
Dilakukan pengulangan sebanyak 6 kali
Kafein = 10 mg Parasetamol = 10 mg
Dimasukkan ke dalam labu tentukur 10 ml Dilarutkan dan dicukupkan dengan pelarut HCl 0,1 N Larutan Parasetamol
(1000 µg/ml)
Dimasukkan ke dalam labu tentukur 10 ml Dilarutkan dan dicukupkan dengan pelarut HCl 0,1 N Larutan Kafein
(1000 µg/ml)
Lampiran 11. Bagan alir penentuan kadar parasetamol dan kafein dalam sediaan tablet B
ditimbang (berat 20 tablet = 16,542 g)
digerus dalam lumpang sampai halus dan homogen
ditimbang setara 10 mg parasetamol (penimbangan dilakukan sebanyak 6 kali pengulangan)
dihitung kesetaraan kafein yang terkandung di dalamnya
dimasukkan ke dalam labu tentukur 50 ml dilarutkan dengan pelarut HCl 0,1 N
dihomogenkan dengan sonikator selama 15 menit disaring
dibuang 10 ml filtrat pertama ditampung filtrat selanjutnya dipipet 1,58 ml
dimasukkan ke dalam labu tentukur 50 ml
dipipet 4,03 ml larutan kafein dengan konsentrasi 100 µg/ml
dimasukkan ke dalam labu tentukur 50 ml di atas dicukupkan dengan pelarut HCl 0,1 N
diukur pada 5 titik panjang gelombang
dihitung Nilai Absorbansi
Kadar 20 tablet
Lampiran 14. Perhitungan kadar teoritis dari campuran baku parasetamol dan kafein
Pengulangan 1 (penimbangan parasetamol dan kafein masing-masing 10,0 mg) Kadar parasetamol:
Pengulangan 2 (penimbangan parasetamol dan kafein masing-masing 10,1 mg) Kadar parasetamol:
Lampiran 14. (Lanjutan)
Pengulangan 4 (penimbangan parasetamol dan kafein masing-masing 10,0 mg) Kadar parasetamol:
Pengulangan 5 (penimbangan parasetamol dan kafein masing-masing 10,3 mg) Kadar parasetamol:
Lampiran 15. Data penimbangan baku parasetamol dan kafein, serta kadar teoritis dari parasetamol dan kafein
Pengulangan Penimbangan (mg)
Kadar Teoritis Parasetamol
(µg/ml)
Kadar Teoritis Kafein (µg/ml)
1 10,0 6,50 8,60
2 10,1 6,56 8,68
3 10,1 6,56 8,68
4 10,0 6,50 8,60
5 10,3 6,69 8,85
Lampiran 16. Data penimbangan dan serapan dari tablet B
Replikasi Penimbangan (mg)
Serapan pada Panjang Gelombang
223 nm 243,8 nm 258 nm 262 nm 271 nm
1 14,2 0,496 0,540 0,569 0,578 0,569
2 14,2 0,502 0,542 0,570 0,579 0,569
3 13,8 0,497 0,537 0,565 0,576 0,568
4 13,7 0,497 0,537 0,564 0,575 0,569
5 14,1 0,499 0,541 0,569 0,579 0,569
Lampiran 17. Perhitungan kadar teoritis dari parasetamol dan kafein dalam tablet B
Berat 20 tablet = 16542 mg
Berat setara parasetamol = 10 mg (Pemilihan 10 mg adalah agar tahap pengenceran tidak banyak sehingga dapat mengurangi kesalahan pengerjaan)
Dengan kesetaraan parasetamol 10 mg, maka dihitung berat serbuk yang ditimbang: Serbuk yang Ditimbang = x Berat 20 tablet
Serbuk yang Ditimbang = x 16542 mg Serbuk yang Ditimbang = 13,79 mg
Sehingga secara teoritis, dalam serbuk 13,79 mg yang ditimbang terdapat kesetaraan parasetamol sebesar 10 mg.
1. Serbuk yang Ditimbang = 14,2 mg
Serbuk yang Ditimbang = x Berat 20 tablet
14,2 mg =
x 16542 mg
Berat Setara Parasetamol = 10,3011 mg
Konsentrasi Parasetamol dan Kafein dalam Labu 50 ml: Parasetamol =
x 1000 = 206,022 µg/ml
Kafein:
=
Konsentrasi Kafein = 17,1685 µg/ml
Volume Parasetamol dan Kafein yang diambil untuk dilakukan pengenceran dalam labu 50 ml:
V1 x C1 = V2 x C2
Lampiran 17. (Lanjutan)
Konsentrasi Parasetamol dan Kafein setelah dilakukan pengenceran untuk diukur:
Konsentrasi Kafein yang akan ditambahkan (Metode Adisi Standar): Konsentrasi Kafein = 8,6 µg/ml – 0,5426 µg/ml
= 8,0574 µg/ml
Dibuat larutan kafein baku dengan konsentrasi 100 µg/ml: Kafein = x 1000 = 100 µg/ml
Volume kafein yang diambil untuk diadisi: V1 x C1 = V2 x C2
V1 x 100 µg/ml = 50 ml x 8,0574 µg/ml V1 = 4,03 ml
Konsentrasi kafein dalam volume yang diambil untuk diadisi: V1 x C1 = V2 x C2
4,03 x 100 µg/ml = 50 ml x C2 C2 = 8,06 µg/ml
Lampiran 17. (Lanjutan)
2. Serbuk yang Ditimbang = 14,2 mg
Serbuk yang Ditimbang = x Berat 20 tablet
14,2 mg =
x 16542 mg
Berat Setara Parasetamol = 10,3011 mg
Konsentrasi Parasetamol dan Kafein dalam Labu 50 ml: Parasetamol =
x 1000 = 206,022 µg/ml
Kafein:
=
Konsentrasi Kafein = 17,1685 µg/ml
Volume Parasetamol dan Kafein yang diambil untuk dilakukan pengenceran dalam labu 50 ml:
V1 x C1 = V2 x C2
V1 x 206,022 µg/ml = 50 ml x 6,5 µg/ml V1 = 1,58 ml
Konsentrasi Parasetamol dan Kafein setelah dilakukan pengenceran untuk diukur:
Parasetamol:
V1 x C1 = V2 x C2 1,58 ml x 206,022 µg/ml = 50 ml x C2
C2 = 6,5102 µg/ml Kafein:
V1 x C1 = V2 x C2 1,58 ml x 17,1685 µg/ml = 50 ml x C2
Lampiran 17. (Lanjutan)
Konsentrasi Kafein yang akan ditambahkan (Metode Adisi Standar): Konsentrasi Kafein = 8,6 µg/ml – 0,5426 µg/ml
= 8,0574 µg/ml
Dibuat larutan kafein baku dengan konsentrasi 100 µg/ml: Kafein = x 1000 = 100 µg/ml
Volume kafein yang diambil untuk diadisi: V1 x C1 = V2 x C2
V1 x 100 µg/ml = 50 ml x 8,0574 µg/ml V1 = 4,03 ml
Konsentrasi kafein dalam volume yang diambil untuk diadisi: V1 x C1 = V2 x C2
4,03 x 100 µg/ml = 50 ml x C2 C2 = 8,06 µg/ml
Konsentrasi kafein yang diukur = 0,5426 µg/ml + 8,06 µg/ml = 8,6026 µg/ml
3. Serbuk yang Ditimbang = 13,8 mg
Serbuk yang Ditimbang = x Berat 20 tablet
13,8 mg =
x 16542 mg
Berat Setara Parasetamol = 10,0109 mg
Lampiran 17. (Lanjutan) Kafein:
=
Konsentrasi Kafein = 16,6848 µg/ml
Volume Parasetamol dan Kafein yang diambil untuk dilakukan pengenceran dalam labu 50 ml:
V1 x C1 = V2 x C2
V1 x 200,218 µg/ml = 50 ml x 6,5 µg/ml V1 = 1,62 ml
Konsentrasi Parasetamol dan Kafein setelah dilakukan pengenceran untuk diukur:
Parasetamol:
V1 x C1 = V2 x C2 1,62 ml x 200,218 µg/ml = 50 ml x C2
C2 = 6,4871 µg/ml Kafein:
V1 x C1 = V2 x C2 1,62 ml x 16,6848 µg/ml = 50 ml x C2
C2 = 0,5406 µg/ml
Konsentrasi Kafein yang akan ditambahkan (Metode Adisi Standar): Konsentrasi Kafein = 8,6 µg/ml – 0,5406 µg/ml
= 8,0594 µg/ml
Lampiran 17. (Lanjutan)
Volume kafein yang diambil untuk diadisi: V1 x C1 = V2 x C2
V1 x 100 µg/ml = 50 ml x 8,0594 µg/ml V1 = 4,03 ml
Konsentrasi kafein dalam volume yang diambil untuk diadisi: V1 x C1 = V2 x C2
4,03 x 100 µg/ml = 50 ml x C2 C2 = 8,06 µg/ml
Konsentrasi kafein yang diukur = 0,5406 µg/ml + 8,06 µg/ml = 8,6006 µg/ml
4. Serbuk yang Ditimbang = 13,7 mg
Serbuk yang Ditimbang = x Berat 20 tablet
13,7 mg =
x 16542 mg
Berat Setara Parasetamol = 9,9383 mg
Konsentrasi Parasetamol dan Kafein dalam Labu 50 ml: Parasetamol =
x 1000 = 198,766 µg/ml
Kafein:
=
Konsentrasi Kafein = 16,5638 µg/ml
Volume Parasetamol dan Kafein yang diambil untuk dilakukan pengenceran dalam labu 50 ml:
V1 x C1 = V2 x C2
Lampiran 17. (Lanjutan)
Konsentrasi Parasetamol dan Kafein setelah dilakukan pengenceran untuk diukur:
Konsentrasi Kafein yang akan ditambahkan (Metode Adisi Standar): Konsentrasi Kafein = 8,6 µg/ml – 0,5399 µg/ml
= 8,0601 µg/ml
Dibuat larutan kafein baku dengan konsentrasi 100 µg/ml: Kafein = x 1000 = 100 µg/ml
Volume kafein yang diambil untuk diadisi: V1 x C1 = V2 x C2
V1 x 100 µg/ml = 50 ml x 8,0601 µg/ml V1 = 4,03 ml
Konsentrasi kafein dalam volume yang diambil untuk diadisi: V1 x C1 = V2 x C2
4,03 x 100 µg/ml = 50 ml x C2 C2 = 8,06 µg/ml
Lampiran 17. (Lanjutan)
5. Serbuk yang Ditimbang = 14,1 mg
Serbuk yang Ditimbang = x Berat 20 tablet
14,1 mg =
x 16542 mg
Berat Setara Parasetamol = 10,2285 mg
Konsentrasi Parasetamol dan Kafein dalam Labu 50 ml: Parasetamol =
x 1000 = 204,570 µg/ml
Kafein:
=
Konsentrasi Kafein = 17,0475 µg/ml
Volume Parasetamol dan Kafein yang diambil untuk dilakukan pengenceran dalam labu 50 ml:
V1 x C1 = V2 x C2
V1 x 204,570 µg/ml = 50 ml x 6,5 µg/ml V1 = 1,59 ml
Konsentrasi Parasetamol dan Kafein setelah dilakukan pengenceran untuk diukur:
Parasetamol:
V1 x C1 = V2 x C2 1,59 ml x 204,570 µg/ml = 50 ml x C2
C2 = 6,5053 µg/ml Kafein:
V1 x C1 = V2 x C2 1,59 ml x 17,0475 µg/ml = 50 ml x C2
Lampiran 17. (Lanjutan)
Konsentrasi Kafein yang akan ditambahkan (Metode Adisi Standar): Konsentrasi Kafein = 8,6 µg/ml – 0,5421 µg/ml
= 8,0579 µg/ml
Dibuat larutan kafein baku dengan konsentrasi 100 µg/ml: Kafein = x 1000 = 100 µg/ml
Volume kafein yang diambil untuk diadisi: V1 x C1 = V2 x C2
V1 x 100 µg/ml = 50 ml x 8,0579 µg/ml V1 = 4,03 ml
Konsentrasi kafein dalam volume yang diambil untuk diadisi: V1 x C1 = V2 x C2
4,03 x 100 µg/ml = 50 ml x C2 C2 = 8,06 µg/ml
Konsentrasi kafein yang diukur = 0,5421 µg/ml + 8,06 µg/ml = 8,6021 µg/ml
6. Serbuk yang Ditimbang = 14,1 mg
Serbuk yang Ditimbang = x Berat 20 tablet
14,1 mg =
x 16542 mg
Berat Setara Parasetamol = 10,2285 mg
Lampiran 17. (Lampiran) Kafein:
=
Konsentrasi Kafein = 17,0475 µg/ml
Volume Parasetamol dan Kafein yang diambil untuk dilakukan pengenceran dalam labu 50 ml:
V1 x C1 = V2 x C2
V1 x 204,570 µg/ml = 50 ml x 6,5 µg/ml V1 = 1,59 ml
Konsentrasi Parasetamol dan Kafein setelah dilakukan pengenceran untuk diukur:
Parasetamol:
V1 x C1 = V2 x C2 1,59 ml x 204,570 µg/ml = 50 ml x C2
C2 = 6,5053 µg/ml Kafein:
V1 x C1 = V2 x C2 1,59 ml x 17,0475 µg/ml = 50 ml x C2
C2 = 0,5421 µg/ml
Konsentrasi Kafein yang akan ditambahkan (Metode Adisi Standar): Konsentrasi Kafein = 8,6 µg/ml – 0,5421 µg/ml
= 8,0579 µg/ml
Lampiran 17. (Lanjutan)
Volume kafein yang diambil untuk diadisi: V1 x C1 = V2 x C2
V1 x 100 µg/ml = 50 ml x 8,0579 µg/ml V1 = 4,03 ml
Konsentrasi kafein dalam volume yang diambil untuk diadisi: V1 x C1 = V2 x C2
4,03 x 100 µg/ml = 50 ml x C2 C2 = 8,06 µg/ml
Lampiran 18. Perhitungan kadar parasetamol dan kafein dengan operasi matriks Pengulangan 1
- X
=
Pengulangan 2
- X
=
Pengulangan 3
- X
=
Pengulangan 4
- X
=
Pengulangan 5
- X
=
Pengulangan 6
- X
Lampiran 19. Perhitungan kadar akurasi dari hasil matriks parasetamol dan kafein
Pengulangan 1 Parasetamol = x 100,31% = 91,94%
Kafein = x 100,06% = 97,98%
Pengulangan 2 Parasetamol = x 100,31% = 92,68%
Kafein = x 100,06% = 97,61%
Pengulangan 3 Parasetamol = x 100,31% = 91,83%
Kafein = x 100,06% = 98,28%
Pengulangan 4 Parasetamol = x 100,31% = 91,66%
Kafein = x 100,06% = 97,95%
Pengulangan 5 Parasetamol = x 100,31% = 92,34%
Kafein = x 100,06% = 98,27%
Pengulangan 6 Parasetamol = x 100,31% = 92,13%
Kafein = x 100,06% = 98,53%
Lampiran 20. Perhitungan statistik kadar parasetamol dan kafein pada sediaan tablet B
1. Kadar Parasetamol
No. (X)
Kadar Akurasi dari hasil matriks (%)
X - (X - )2
1. 91,94 -0,16 0,0256
2. 92,68 0,58 0,3364
3. 91,83 -0,27 0,0729
4. 91,66 -0,44 0,1936
5. 92,34 0,24 0,0576
6. 92,13 0,03 0,0009
= 92,10 (X - )2 = 0,6870
SD = = = = 0,3707
Uji statistik pada taraf kepercayaan 95% maka nilai α = 0,05 ; dk = n-1 = 6-1 = 5 Diperoleh ttabel = (1 – ½ α); dk
= (1 – 0,025); 5 = 0,975; 5 = 2,5706
Dasar penerimaan data jika t hitung≤ t tabel.
t hitung =
t hitung 1 = = 0,6437 (diterima)
t hitung 2 = = 2,3334 (diterima)
Lampiran 20. (Lanjutan)
t hitung 4 = = 1,7701 (diterima)
t hitung 5 = = 0,9656 (diterima)
t hitung 6 = = 0,1207 (diterima)
Lampiran 20. (Lanjutan)
Dasar penerimaan data jika t hitung≤ t tabel
t hitung =
t hitung 1 = = 0,5168 (diterima)
t hitung 2 = = 2,1103 (diterima)
t hitung 3 = = 0,7752 (diterima)
t hitung 4 = = 0,6459 (diterima)
t hitung 5 = = 0,7321 (diterima)
t hitung 6 = = 1,8519 (diterima)
Semua data diterima, maka kadar kafein sebenarnya untuk α = 0,05; dk = 5 adalah:
μ = ± ttabel x
Lampiran 21. Perhitungan koefisien variasi (% KV) parasetamol dan kafein dalam sediaan tablet B
% KV =
x 100%
Lampiran 22. Spektrum serapan campuran baku parasetamol dan kafein
nm .
200,00 250,00 300,00 350,00 400,00
Ab
s.
1,500
1,000
0,500
Lampiran 22. (Lanjutan)
nm .
200,00 250,00 300,00 350,00 400,00
Ab
s.
1,500
1,000
0,500
Lampiran 23. Spektrum serapan sampel sediaan tablet B
nm .
200,00 250,00 300,00 350,00 400,00
Ab
s.
1,500
1,000
0,500
Lampiran 23. (Lanjutan)
nm .
200,00 250,00 300,00 350,00 400,00
Ab
s.
1,500
1,000
0,500
DAFTAR PUSTAKA
Andrianto, Y. C. (2009). Validasi Metode Penetapan Kadar Campuran Parasetamol dan Ibuprofen Secara Spektrofotometri UV dengan Aplikasi Panjang Gelombang Berganda. Skripsi. Yogyakarta: Fakultas Farmasi Universitas Sanata Dharma. Halaman 1-3, 23-26.
Bliesner, D. M. (2006). Validating Chromatographic Methods: A Practical Guide. New Jersey: John Wiley and Sons, Inc. Halaman 1.
Day, R. A., dan Underwood, A. L. (1986). Quantitative Analysis. Edisi Kelima. Penerjemah: Pudjaatmaka, A. H. (2002). Analisis Kimia Kuantitatif. Edisi Kelima. Jakarta: Penerbit Erlangga. Halaman 413-415.
Ditjen POM RI. (1979). Farmakope Indonesia. Edisi Ketiga. Jakarta: Departemen Kesehatan RI. Halaman 649.
Ditjen BKAK. (2014). Farmakope Indonesia. Edisi Kelima. Jakarta: Kementerian Kesehatan RI. Halaman 998, 1028.
Ermer, J., dan McB., J. H. M. (2005). Method Validation in Pharmaceutical Analysis: A Guide to Best Practice. Weinheim: Wiley-VCH. Halaman 63, 80, 86.
Gandjar, I. G., dan Rohman, A. (2012). Analisis Obat secara Spektrofotometri dan Kromatografi. Cetakan Pertama. Yogyakarta: Pustaka Pelajar. Halaman 65, 81, 91-92, 262, 482-483.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Majalah Ilmu Kefarmasian. 1(3): 121-135.
Holina, P. (2009). Penetapan Kadar Tablet Parasetamol Produksi PT. Kimia Farma (Persero) Tbk Plant Medan Secara Nitrimetri. Tugas Akhir. Medan: Fakultas Farmasi Universitas Sumatera Utara. Halaman 23.
Huber, L. (2007). Validation and Qualification in Analytical Laboratories. Edisi Kedua. New York: Informa Healthcare USA, Inc. Halaman 125-126. Khopkar, S. M. (1985). Basic Concepts of Analytical Chemistry. Penerjemah:
Saptorahardjo, A., dan Nurhadi, A. (1990). Konsep Dasar Kimia Analitik. Cetakan Pertama. Jakarta: UI-Press. Halaman 215.
Moffat, A. C., Osselton, M. D., dan Widdop, B. (2011). Clarke’s Analysis of Drugs and Poisons. Edisi Keempat. London: Pharmaceutical Press. Halaman 507, 1028, 1856.
Munson, J. W. (1984). Pharmaceutical Analysis: Modern Methods. Part B. Penerjenah: Harjana. (1991). Analisis Farmasi: Metode Modern. Parwa B. Surabaya: Airlangga University Press. Halaman 334.
Pane, R. K. (2010). Penetapan Kadar Parasetamol, Kafein dan Asetosal dalam Sediaan Oral Secara Simultan dengan Metode Kromatografi Cair Kinerja Tinggi (KCKT). Skripsi. Medan: Fakultas Farmasi Universitas Sumatera Utara. Halaman 42.
Rohman, A. (2007). Kimia Farmasi Analisis. Cetakan Pertama. Yogyakarta: Pustaka Pelajar. Halaman 226-232,240-243, 262.
Rosita, N. (2015). Uji Validasi Metode Zero Crossing Spektrofotometri Derivatif Pada Penetapan Kadar Kafein dan Parasetamol dalam Sediaan Tablet. Skripsi. Medan: Fakultas Farmasi Universitas Sumatera Utara. Halaman 49.
Satiadarma, K., Mulja, H. M., Tjahjono, D. H., dan Kartasasmita, R. E. (2004). Asas Pengembangan Prosedur Analisis. Edisi Pertama. Surabaya: Airlangga University Press. Halaman 46-49, 88-91, 97.
Sinaga, S. (2006). Analisa Kadar Kafein dalam Minuman Berenergi yang Beredar di Kota Medan Tahun 2006. Skripsi. Medan: Fakultas Kesehatan Masyarakat Universitas Sumatera Utara. Halaman 22-23.
Sudjana. (2005). Metode Statistika. Bandung: Penerbit Tarsito. Halaman 93, 145, 201, 225.
Tan, H. T., dan Rahardja, K. (2007). Obat-Obat Penting Khasiat, Penggunaan, dan Efek-Efek Sampingnya. Edisi Keenam. Jakarta: PT. Elex Media Komputindo Kelompok Gramedia. Halaman 318, 373-374.
USP 30 NF 25. (2007). The United State Pharmacopoeia 30 and The National Formulary 25. Edisi Ketiga puluh. Halaman 1272.
Watson, D. G. (2005). Pharmaceutical Analysis: A Textbook for Pharmacy Students and Pharmaceutical Chemists. Edisi Kedua. Penerjemah: Syarief, W. R. (2007). Analisis Farmasi: Buku Ajar Untuk Mahasiswa Farmasi dan Praktisi Kimia Farmasi. Edisi Kedua. Jakarta: EGC. Halaman 107.
Wulandari, F. (2008). Penetapan Kadar Campuran Parasetamol dan Kofein dalam Sediaan Tablet yang Beredar dengan Metoda Spektrofotometri UV Multikomponen. Skripsi. Padang: Fakultas Farmasi Universitas Andalas. Halaman 34.
Zainuddin, M. (1999). Aplikasi Metode Panjang Gelombang Berganda Pada Analisis Multikomponen Secara Spektrofotometri Terhadap Campuran
BAB III
METODE PENELITIAN
3.1 Jenis Penelitian
Penelitian ini termasuk jenis penelitian eksperimental, dilakukan secara spektrofotometri dengan metode panjang gelombang berganda yang merupakan pengembangan dari metode spektrofotometri multikomponen terhadap analisa campuran dua zat aktif, yaitu parasetamol dan kafein pada sediaan tablet.
3.2 Tempat dan Waktu Penelitian
Penelitian ini dilakukan pada bulan Februari sampai dengan April 2016 di Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara.
3.3 Alat
Alat-alat yang digunakan dalam penelitian ini adalah spektrofotometer UV-Visible, Personal Computer (PC) yang dilengkapi software UV Probe 2.42
(UV-1800 Shimadzu), neraca analitik (Mettler Toledo), sonikator (Branson 1510), kuvet, alat-alat gelas, lumpang dan alu serta alat-alat lainnya yang diperlukan dalam penyiapan sampel. Gambar beberapa alat di atas dapat dilihat pada Lampiran 3 halaman 41.
3.4 Bahan
3.5 Pengambilan Sampel
Metode pengambilan sampel dilakukan secara purposif, yaitu ditentukan atas dasar pertimbangan bahwa sampel yang diambil mempunyai karakteristik yang sama dengan yang diteliti (Sudjana, 2005). Pengambilan sampel ditentukan tanpa membandingkan sampel antara satu tempat dengan tempat yang lain, karena pengambilan sampel dianggap homogen. Sampel yang digunakan dalam penelitian ini adalah tablet B yang mengandung parasetamol 600 mg dan kafein 50 mg. Gambar sediaan dan daftar spesifikasi sediaan tablet dapat dilihat pada Lampiran 1 dan 2 halaman 39 dan 40.
3.6 Prosedur Penelitian
3.6.1 Pembuatan pelarut HCl 0,1 N
Diencerkan 8,3 ml HCl 37% (v/v) dengan 1 Liter akuades (Ditjen POM RI,
1979). Perhitungan pembuatan pelarut dapat dilihat pada Lampiran 4 halaman 42.
3.6.2 Pembuatan larutan induk baku (LIB) parasetamol
3.6.3 Pembuatan larutan induk baku kafein
Ditimbang dengan seksama 50 mg baku pembanding kafein BPFI, kemudian dimasukkan ke dalam labu tentukur 50 ml, dilarutkan dengan HCl 0,1 N hingga larut, dicukupkan volume dengan HCl 0,1 N sampai garis tanda sehingga didapatkan larutan dengan konsentrasi 1000 μg/ml (LIB I). Dari larutan LIB I dipipet 5 ml dimasukkan ke dalam labu tentukur 50 ml, dicukupkan dengan HCl 0,1 N sampai garis tanda sehingga didapatkan larutan dengan konsentrasi 100 μg/ml (LIB II). Bagan alir prosedur penelitian dapat dilihat pada Lampiran 6 halaman 44.
3.6.4 Pembuatan spektrum serapan maksimum parasetamol
Diambil sebanyak 0,65 ml dari LIB II parasetamol (konsentrasi = 100
μg/ml) kemudian dimasukkan ke dalam labu tentukur 10 ml. Selanjutnya larutan diencerkan dengan pelarut HCl 0,1 N sampai garis tanda, lalu dikocok sampai homogen untuk memperoleh larutan parasetamol dengan konsentrasi 6,5 μg/ml. Diukur serapannya pada panjang gelombang 200-400 nm. Bagan alir prosedur penelitian dapat dilihat pada Lampiran 5 halaman 43.
3.6.5 Pembuatan spektrum serapan maksimum kafein
3.6.6 Pembuatan larutan standar parasetamol
Diambil sebanyak 0,3 ml; 0,45 ml; 0,65 ml; 0,75 ml; dan 0,9 ml dari LIB II parasetamol, kemudian masing-masing dimasukkan ke dalam 5 labu tentukur 10 ml. Diencerkan dengan pelarut HCl 0,1 N untuk membuat larutan standar parasetamol dengan konsentrasi 3,0 μg/ml; 4,5 µg/ml; 6,5 μg/ml; 7,5 µg/ml; dan 9,0 μg/ml. Bagan alir prosedur penelitian dapat dilihat pada Lampiran 7 halaman 45.
3.6.7 Pembuatan larutan standar kafein
Diambil sebanyak 0,4 ml; 0,6 ml; 0,86 ml; 1,0 ml; dan 1,2 ml dari LIB II kafein, kemudian masing-masing dimasukkan ke dalam 5 labu tentukur 10 ml. Diencerkan dengan pelarut HCl 0,1 N untuk membuat larutan standar kafein dengan konsentrasi 4,0 μg/ml; 6,0 µ g/ml; 8,6 μg/ml; 10,0 µg/ml; dan 12,0 μg/ml. Bagan alir prosedur penelitian dapat dilihat pada Lampiran 8 halaman 46.
3.6.8 Penentuan serapan larutan standar
Larutan standar parasetamol dengan konsentrasi 3,0 μg/ml; 4,5 µg/ml; 6,5 μg/ml; 7,5 µg/ml; dan 9,0 μg/ml dan larutan standar kafein dengan konsentrasi 4,0 μg/ml; 6,0 µ g/ml; 8,6 μg/ml; 10,0 µg/ml; dan 12,0 μg/ml yang masing-masing telah dibuat enam kali perulangan, diukur serapannya pada panjang gelombang 200-400 nm. Nilai serapan kedua senyawa ditentukan dengan menggunakan persamaan regresi yang dioperasikan pada data konsentrasi dan absorbansi masing-masing komponen pada setiap panjang gelombang pengukuran.
Dari persamaan regresi yang diperoleh: y = ax + b Keterangan:
3.6.9 Penentuan panjang gelombang analisis dari tumpang tindih spektrum Dibuat larutan parasetamol dengan konsentrasi 6,5 μg/ml dan larutan kafein dengan konsentrasi 8,6 μg/ml, kemudian kedua larutan ini diukur serapannya masing-masing pada panjang gelombang 200-400 nm. Selanjutnya, spektrum serapan dari masing-masing komponen ditumpang tindihkan, pembacaan spektrum ini dilakukan pada rentang panjang gelombang 215-300 nm, karena pada rentang panjang gelombang ini parasetamol dan kafein tumpang tindih secara keseluruhan. Kemudian dipilih 5 titik sebagai panjang gelombang yang akan digunakan, pemilihan panjang gelombang diambil dari spektrum serapan komponen mulai memberikan serapan sampai hampir tidak memberikan serapan. Bagan alir prosedur penelitian dapat dilihat pada Lampiran 9 halaman 47.
3.6.11 Penentuan kadar parasetamol dan kafein dalam tablet
Ditimbang 20 tablet dan digerus dalam lumpang sampai halus dan homogen. Selanjutnya ditimbang seksama sejumlah serbuk setara dengan 10 mg parasetamol (penimbangan dilakukan sebanyak 6 kali pengulangan), dihitung kesetaraan kafein yang terkandung di dalamnya. Dimasukkan ke dalam labu tentukur 50 ml dan dilarutkan dengan pelarut HCl 0,1 N sampai garis tanda, dihomogenkan dengan sonikator selama 15 menit. Larutan tersebut kemudian disaring, lebih kurang 10 ml filtrat pertama dibuang, filtrat selanjutnya ditampung. Kemudian dipipet 1,58 ml larutan filtrat, dimasukkan ke dalam labu tentukur 50 ml.
Kemudian ditambahkan 4,03 ml larutan kafein (konsentrasi = 100 µg/ml), dimasukkan ke dalam labu tentukur 50 ml yang di dalamnya terdapat 1,58 ml filtrat, lalu dicukupkan dengan pelarut HCl 0,1 N sampai garis tanda sehingga diperoleh larutan yang di dalamnya terdapat parasetamol dengan konsentrasi 6,5 µg/ml dan kafein dengan konsentrasi 8,6 µg/ml. Diukur serapan pada panjang gelombang yang telah ditentukan. Bagan alir prosedur penelitian dapat dilihat pada Lampiran 11 halaman 49.
Menurut Harmita (2004), dalam metode adisi standar (penambahan bahan baku), sejumlah sampel yang dianalisis ditambah analit dengan kadar yang diperlukan dari kadar analit yang diperkirakan, dicampur dan dianalisis kembali. Selisih kedua hasil dibandingkan dengan kadar yang sebenarnya.
% Kadar sampel = x 100 % Keterangan:
Ca = konsentrasi perolehan sampel setelah penambahan baku Cb = konsentrasi baku yang ditambahkan
3.6.12 Perhitungan kadar parasetamol dan kafein dalam campuran.
Perhitungan kadar masing-masing komponen dalam campuran dilakukan atas dasar serapan campuran (Ac) dan serapan tiap komponen pada multi panjang gelombang yang telah diketahui dari hasil pengukuran dengan menggunakan persamaan matriks:
[c] = [[a] x [a1]]-1 x [a] x Ac] Keterangan :
[c] = konsentrasi komponen dari campuran
[a] = matriks serapan senyawa penyusun campuran
[a1] = transpose matriks serapan senyawa penyusun campuran [[a] x [a1]]-1 = invers matriks dikali transpose matriks serapan senyawa
penyusun campuran
[Ac] = matriks nilai serapan sampel 3.6.13 Analisis Hasil
Analisis hasil dilakukan untuk mengetahui validitas metode yang digunakan dalam penelitian, berikut parameter yang diukur:
a. Akurasi
Nilai akurasi dihitung dari hasil matriks kadar yang diperoleh dibandingkan dengan kadar teoritis dikalikan % kadar sertifikat analisis. Akurasi dikatakan baik jika berada dalam rentang 90,0-110,0% (Andrianto, 2009).
Akurasi dari hasil matriks diperoleh dengan rumus:
Akurasi dari hasil matriks = x % kadar sertifikat analisis
b. Uji Presisi
Penentuan presisi berdasarkan nilai koefisian variasi (KV) atau Coefficient of variation (CV). Jika KV lebih kecil dari 2% maka dinilai mempunyai presisi
Koefisien variasi diperoleh dengan rumus:
KV =
x 100%
c. Analisis Data Penetapan Kadar Secara Statistik
Data perhitungan kadar parasetamol dan kafein dianalisis secara statistik dengan menggunakan uji ttabel distribusi t dapat dilihat pada Lampiran 20 halaman 71 dan 72.
Rumus yang digunakan adalah :
SD =
Untuk mencari t hitung digunakan rumus: thitung =
Data diterima jika thitung < ttabel pada interval kepercayaan 95% dengan nilai
α = 0,05. Keterangan :
SD = standard deviation / simpangan baku x = kadar dalam satu perlakuan
x = kadar rata-rata dalam satu sampel n = jumlah perlakuan
α = tingkat kepercayaan
Menurut Sudjana (2005), untuk menghitung kadar parasetamol dan kafein sebenarnya dalam sampel secara statistik dapat digunakan rumus:
μ = ± ttabel x Keterangan :
SD = standard deviation / simpangan baku x = kadar rata-rata dalam satu sampel n = jumlah perlakuan
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Penentuan Spektrum Serapan Maksimum
Berdasarkan hasil penelitian, diperoleh panjang gelombang maksimum parasetamol (konsentrasi 6,5 μg/ml) pada 243,8 nm dan kafein (konsentrasi
8,6 μg/ml) pada 271 nm.
Spektrum serapan maksimum parasetamol dan kafein masing-masing dapat dilihat pada Gambar 4.1 dan 4.2.
nm .
200.00 250.00 300.00 350.00 400.00
Ab
s.
0.800
0.600
0.400
0.200
pada suasana asam (A11 = 668a) terletak pada 245 nm, sedangkan untuk kafein pada suasana asam (A11 = 504a) terletak pada 273 nm (Moffat, dkk., 2011).
Berdasarkan teori dengan hasil yang diperoleh, perbedaan panjang gelombang maksimum masing-masing parasetamol dan kafein tidak kurang dan tidak lebih dari 2 nm. Dalam hal ini, panjang gelombang maksimum masing-masing komponen telah memenuhi syarat (Moffat, dkk., 2011).
4.2 Spektrum Serapan dalam Berbagai Konsentrasi
Spektrum serapan parasetamol dan kafein dalam berbagai konsentrasi dapat dilihat pada Gambar 4.3 dan Gambar 4.4.
n m .
2 0 0 ,0 0 2 5 0 ,0 0 3 0 0 ,0 0 3 5 0 ,0 0 4 0 0 ,0 0
Ab
s.
0 ,8 0 0
0 ,6 0 0
0 ,4 0 0
0 ,2 0 0
spektrum dari masing-masing zat, sehingga bisa dikatakan pengggunaan pelarut HCl 0,1 N stabil terhadap parasetamol maupun kafein.
Metode spektrofotometri biasa tidak dapat dilakukan untuk menetapkan kadar parasetamol dan kafein dalam campuran karena spektrum parasetamol dan kafein saling tumpang tindih dan serapan pada panjang gelombang dalam spektrum campuran tidak menggambarkan besar konsentrasi zat tersebut dalam campurannya. Berbeda dengan spektrofotometri metode panjang gelombang berganda, metode ini memungkinkan untuk menetapkan kadar suatu zat dalam campuran zat tersebut dengan zat lainnya, dengan syarat masing-masing komponen masih memiliki serapan pada panjang gelombang yang ditentukan (Andrianto, 2009).
4.3 Penentuan Panjang Gelombang Analisis
Spetrum tumpang tindih serapan maksimum parasetamol dan kafein dapat dilihat pada Gambar 4.5.
nm .
200.00 250.00 300.00 350.00 400.00
Ab
s.
0.800
0.600
0.400
0.200
6,5 µg/ml dan kafein konsentrasi 8,6 µg/ml. Pembacaan spektrum serapan ini dilakukan pada rentang panjang gelombang 215-300 nm, karena pada rentang panjang gelombang ini parasetamol dan kafein tumpang tindih secara keseluruhan.
Pada penelitian ini, dipilih 5 titik panjang gelombang yang akan digunakan dalam penetapan kadar parasetamol dan kafein dalam sediaan tablet karena larutan baku parasetamol dan kafein dibuat dalam 6 seri konsentrasi sehingga akan didapat 30 data yang merupakan jumlah minimal untuk mendapatkan data dengan karakteristik populasi yang terdistribusi normal (Zainuddin, 1999). Spektrum yang dipilih adalah dari spektrum serapan parasetamol konsentrasi 6,5 µ g/ml dan kafein konsentrasi 8,6 µg/ml. Lima titik panjang gelombang yang akan digunakan dapat dilihat pada Gambar 4.6.
nm .
200.00 250.00 300.00 350.00 400.00
Ab
s.
0.800
0.600
0.400
0.200
gelombang 262 nm kafein memberikan serapan yang cukup besar sedangkan parasetamol mulai menurun. Pada panjang gelombang 271 nm merupakan serapan maksimum kafein.
4.4 Hasil Penentuan Serapan pada Lima Panjang Gelombang
Harga serapan merupakan nilai yang menunjukkan seberapa besar konstribusi serapan suatu senyawa terhadap serapan dari campuran senyawa pada panjang gelombang (Andrianto, 2009).
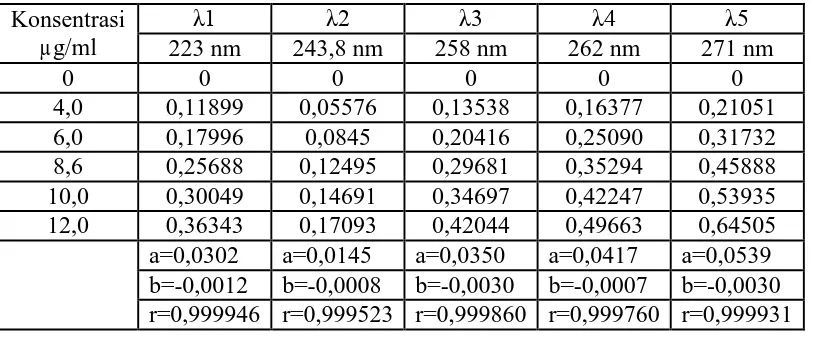
Penentuan harga serapan ini dilakukan dengan mengukur serapan masing-masing larutan baku parasetamol dan kafein pada panjang gelombang 223 nm; 243,8 nm; 258 nm; 262 nm; dan 271 nm. Data perhitungan serapan parasetamol dan kafein dapat dilihat pada Tabel 4.1 dan 4.2.
Tabel 4.1 Data Perhitungan Serapan Parasetamol
Tabel 4.2 Data Perhitungan Serapan Kafein Konsentrasi a=0,0424 a=0,0693 a=0,0444 a=0,0343 a=0,0186 b=0,0009 b=0,0014 b=0,0008 b=0,0006 b=0,0009 r=0,999627 r=0,999871 r=0,999766 r=0,999766 r=0,999667
Nilai serapan (a) yang dipakai adalah nilai serapan dari parasetamol dan kafein pada pengulangan 6. Pemilihan nilai serapan (a) dapat ditentukan berdasarkan harga r hitung. Nilai r hitung dibandingkan dengan nilai r tabel dengan taraf kepercayaan 95% dengan df 4 yaitu 0,8114. Berdasarkan data tersebut terlihat bahwa nilai r hitung parasetamol dan kafein pada pengulangan 6 lebih besar dari nilai r tabel. Ini berarti bahwa persamaan tersebut mempunyai linearitas yang baik, karena nilai r hitung mendekati 1.
Data serapan jenis yang diperoleh ini kemudian digunakan untuk menetapkan kadar parasetamol dan kafein dalam campuran dengan perhitungan matriks. Data perhitungan serapan parasetamol dan kafein pengulangan 1 sampai pengulangan 6 masing-masing dapat dilihat pada Lampiran 12 halaman 50 dan Lampiran 13 halaman 52.
4.5 Hasil Spektrum Serapan Campuran Baku Parasetamol dan Kafein
Spektrum tumpang tindih serapan campuran baku parasetamol dan kafein dapat dilihat pada Gambar 4.7.
n m .
2 0 0 .0 0 2 5 0 .0 0 3 0 0 .0 0 3 5 0 .0 0 4 0 0 .0 0
Ab
s.
1 .5 0 0
1 .0 0 0
0 .5 0 0
dari parasetamol dan kafein, hal ini dikarenakan spektrum campuran merupakan kombinasi dari spektrum zat yang menyusunnya.
4.6 Hasil Penentuan Kadar Parasetamol dan Kafein pada Sediaan Tablet Spektrum tumpang tindih serapan sampel sediaan tablet B dapat dilihat pada Gambar 4.8.
nm .
200,00 250,00 300,00 350,00 400,00
Ab
s.
1,500
1,000
0,500
rumus perhitungan matriks. Kemudian dari perhitungan akan diperoleh kadar masing-masing komponen campurannya, kemudian dihitung akurasi dari hasil matriks dan koefisien variasinya (% KV). Data konsentrasi, kadar dan koefisien variasi (% KV) parasetamol dan kafein dalam sediaan tablet B dapat dilihat pada Tabel 4.3.
Tabel 4.3 Data Konsentrasi, Kadar dan Koefisien Variasi (% KV) Parasetamol dan Kafein dalam Sediaan Tablet B
Hasil penetapan kadar parasetamol dan kafein dalam sediaan tablet B dapat dilihat pada Tabel 4.4.
Tabel 4.4 Hasil Penetapan Kadar Parasetamol dan Kafein dalam Sediaan Tablet B
No Obat Tablet B Kandungan di
Kadar parasetamol dan kafein pada sediaan tablet Bmemenuhi persyaratan menurut USP 30 NF 25 (2007) yaitu untuk sediaan tablet parasetamol dan kafein
No
Rata-rata dari akurasi hasil matriks 92,10 Rata-rata dari akurasi hasil matriks
98,10
yaitu tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket.
Diperoleh rentang kadar akurasi dari hasil matriks untuk masing-masing parasetamol dan kafein adalah 91,71%-92,49% dan 97,76%-98,44%. Koefisien variasi (% KV) untuk masing-masing parasetamol dan kafein adalah 0,40% dan 0,33%. Nilai rentang kadar akurasi parasetamol dan kafein memiliki akurasi yang baik karena berada pada rentang 90%-110% dan juga memiliki presisi yang baik karena % KV parasetamol dan kafein termasuk <2%.
Perhitungan kadar teoritis dari parasetamol dan kafein dalam tablet B dapat dilihat pada Lampiran 17 halaman 58. Perhitungan kadar parasetamol dan kafein dengan operasi matriks dapat dilihat pada Lampiran 18 halaman 69. Perhitungan kadar akurasi dari hasil matriks parasetamol dan kafein dapat dilihat pada Lampiran 19 halaman 70. Perhitungan statistik kadar parasetamol dan kafein pada sediaan tablet B dapat dilihat pada Lampiran 20 halaman 71. Perhitungan koefisien variasi (% KV) parasetamol dan kafein dapat dilihat pada Lampiran 21 halaman 74.
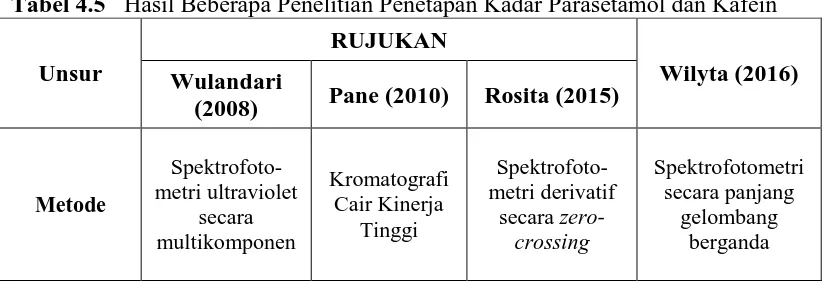
4.7 Hasil Beberapa Penelitian Penetapan Kadar Parasetamol dan Kafein Hasil beberapa penelitian penetapan kadar parasetamol dan kafein dapat dilihat pada Tabel 4.5.
BAB V
KESIMPULAN DAN SARAN 5.1 Kesimpulan
Berdasarkan penelitian yang dilakukan, maka dapat disimpulkan:
a. Metode panjang gelombang berganda secara spektrofotometri dapat digunakan dalam penetapan kadar parasetamol dan kafein dalam sediaan tablet dengan menggunakan pelarut HCl 0,1 N.
b. Kadar parasetamol dan kafein dalam sediaan tablet yang ditentukan dengan metode panjang gelombang berganda secara spektrofotometri memenuhi persyaratan yang tercantum dalam USP 30 NF 25 (2007) dengan persentase kadar sebesar 92,10% ± 0,39% dan 98,10% ± 0,34% masing-masing untuk parasetamol dan kafein.
5.2 Saran
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Bahan 2.1.1 Parasetamol
Menurut Ditjen BKAK (2014), uraian mengenai parasetamol adalah sebagai berikut:
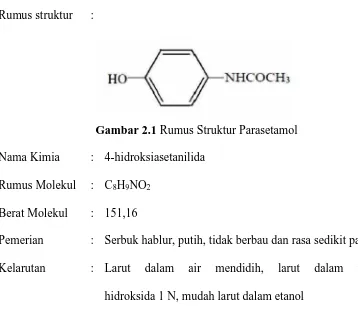
Rumus struktur :
Gambar 2.1 Rumus Struktur Parasetamol Nama Kimia : 4-hidroksiasetanilida
Rumus Molekul : C8H9NO2 Berat Molekul : 151,16
Pemerian : Serbuk hablur, putih, tidak berbau dan rasa sedikit pahit
Kelarutan : Larut dalam air mendidih, larut dalam natrium hidroksida 1 N, mudah larut dalam etanol
Parasetamol merupakan metabolit dari fenasetin, memiliki khasiat analgetik antipiretik tanpa aktivitas antiradang, memiliki waktu paruh (t1/2) 1-4 jam. Dewasa ini pada umumnya dianggap sebagai zat antinyeri yang paling aman, juga untuk pengobatan swamedikasi (pengobatan mandiri). Efek analgetiknya dapat diperkuat oleh kafein hingga 50%. Pada dosis tinggi mengakibatkan nekrosis hati yang tidak reversibel. Dosis yang berlebihan (overdose) dapat menimbulkan mual dan
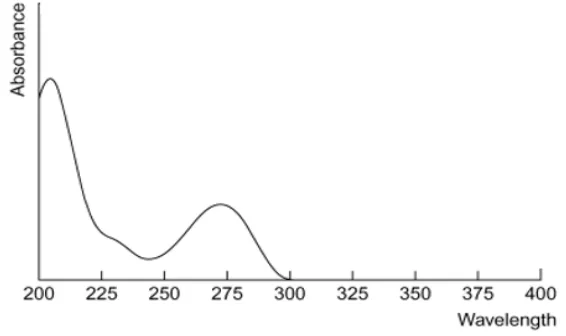
Menurut Moffat, dkk. (2011), pada pelarut asam, parasetamol memiliki panjang gelombang maksimum sebesar 245 nm (A11 = 668a). Pada pelarut basa,
parasetamol memiliki panjang gelombang maksimum sebesar 257 nm (A11 = 715a). Spektrum parasetamol dapat dilihat pada Gambar 2.2.
Gambar 2.2 Spektrum Parasetamol (Moffat, dkk., 2011) 2.1.2 Kafein
Menurut Ditjen BKAK (2014), uraian mengenai kafein adalah sebagai berikut:
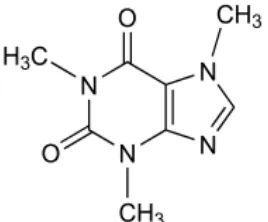
Rumus Struktur :
Gambar 2.3 Rumus Struktur Kafein Nama Kimia : 1,3,7–trimetilxantine
Pemerian : Serbuk putih, bentuk jarum mengkilat, biasanya menggumpal, tidak berbau, rasa pahit, larutan bersifat netral terhadap kertas lakmus, bentuk hidratnya mengembang di udara
Kelarutan : Agak sukar larut dalam air dan dalam etanol, mudah larut dalam kloroform, sukar larut dalam eter
Secara alami, kafein banyak terdapat dalam kopi, kakao dan daun teh. Kafein memiliki efek menghilangkan rasa letih, lapar dan mengantuk, serta meningkatkan daya konsentrasi. Kafein memiliki waktu paruh (t1/2) 3-5 jam. Kafein sering dikombinasi dengan parasetamol guna memperkuat efek analgetiknya. Penggunaan kafein secara berlebihan dapat menyebabkan ketergantungan (Tan dan Rahardja, 2007)
Menurut Moffat, dkk. (2011), pada pelarut asam, kafein memiliki panjang gelombang maksimum sebesar 273 nm (A11 = 504a). Pada pelarut basa, kafein tidak memberikan serapan. Spektrum kafein dapat dilihat pada Gambar 2.4.
2.2 Spektrofotometri Ultraviolet-Visibel (UV-Vis) 2.2.1 Pengertian spektrofotometri ultraviolet-visibel
Spekrofotometri ultraviolet-visibel merupakan salah satu teknik analisis spektrofotometri yang menggunakan sumber radiasi elektromagnetik sinar ultraviolet dan sinar tampak (visibel) dengan memakai instrumen spektrofotometer (Gandjar dan Rohman, 2012). Spektrofotometer digunakan untuk mengukur energi secara relatif jika energi tersebut ditransmisikan, direfleksikan, atau diemisikan sebagai fungsi dari panjang gelombang (Khopkar, 1985). Sinar ultraviolet memiliki panjang gelombang antara 200-400 nm, sedangkan sinar tampak memiliki panjang gelombang antara 400-800 nm (Moffat, dkk., 2011).
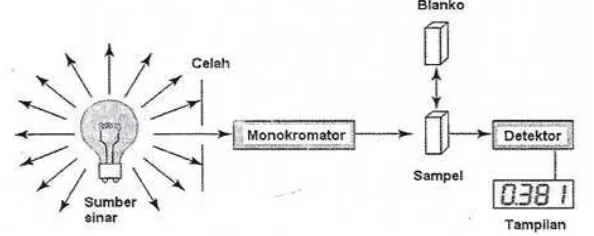
2.2.2 Instrumensasi spektrofotometer ultraviolet-visibel
Spektrofotometer adalah alat yang terdiri dari spektrometer dan fotometer. Spektrometer menghasilkan sinar dari spektrum dengan panjang gelombang tertentu dan fotometer adalah alat pengukur intensitas cahaya yang ditransmisikan atau yang diabsorpsi (Khopkar, 1985). Biasanya spektrofotometer telah mempunyai software untuk mengolah data yang dapat dioperasikan melalui komputer yang telah terhubung dengan spektrofotometer (Moffat, dkk., 2011). Diagram spektrofotometer ultraviolet-visibel dapat dilihat pada Gambar 2.5.
Menurut Rohman (2007) dan Satiadarma, dkk. (2004), komponen spektrofotometer ultraviolet-visibel adalah sebagai berikut:
a. Sumber sinar atau lampu: lampu deuterium digunakan untuk daerah ultraviolet pada panjang gelombang dari 200-400 nm, sementara lampu halogen kuarsa atau lampu tungsten digunakan untuk daerah visibel pada panjang gelombang antara 400-800 nm.
b. Monokromotor: digunakan untuk memperoleh sumber sinar yang monokromatis.
c. Optik-optik: dapat didesain untuk memecah sumber sinar melewati dua kompartemen.
d. Detektor: digunakan sebagai alat yang menerima sinyal dalam bentuk radiasi elektromagnetik, mengubah, dan meneruskannya dalam bentuk sinyal listrik ke rangkaian sistem penguat elektronika.
Sinar ultraviolet dan sinar tampak memberikan energi yang cukup untuk terjadinya transisi elektron (Rohman, 2007). Elektron yang energinya tertinggi dalam molekul, berada dalam tingkat energi elektron dasar, terdapat dalam orbital
δ, π, atau n, masing-masing mempunyai keadaan tereksitasi sesuai dengan energi
elektron terendah (Satiadarma, dkk., 2004).
Penyerapan sinar ultraviolet dan sinar tampak dibatasi oleh sejumlah gugus fungsional (yang disebut dengan kromofor) yang mengandung elektron valensi dengan tingkat energi eksitasi yang relatif rendah. Elektron yang terlibat pada penyerapan sinar ultraviolet dan sinar tampak ini ada tiga, yaitu elektron sigma, elektron phi, dan elektron bukan ikatan (non bonding electron) (Rohman, 2007). Diagram tingkat energi elektronik dapat dilihat pada Gambar 2.6.
Gambar 2.6 Diagram Tingkat Energi Elektronik (Rohman, 2007)
Menurut Rohman (2007), transisi-transisi elektronik yang terjadi di antara tingkat-tingkat energi di dalam suatu molekul ada empat yaitu:
1. Transisi δ→δ*
Energi yang diperlukan untuk transisi ini besarnya sesuai dengan energi sinar yang frekuensinya terletak di antara ultraviolet vakum (kurang dari 180 nm). Jenis transisi ini terjadi pada daerah ultraviolet vakum sehingga kurang begitu bermanfaat untuk analisis dengan cara spektrofotometri ultraviolet-visibel.
δ* anti ikatan sigma
π* anti ikatan phi n elektron non ikatan
π ikatan phi
2. Transisi n→δ*
Jenis transisi ini terjadi pada senyawa organik jenuh yang mengandung atom-atom yang memiliki elektron bukan ikatan (elektron n). Energi yang diperlukan untuk transisi jenis ini lebih kecil dibandingkan
transisi δ→δ* sehingga sinar yang diserap pun mempunyai panjang
gelombang lebih panjang, yakni sekitar 150-250 nm. Kebanyakan transisi ini terjadi pada panjang gelombang kurang dari 200 nm.
3. Transisi n→π* dan transisi π→π*
Untuk memungkinkan terjadinya transisi ini, maka molekul organik harus mempunyai gugus fungsional yang tidak jenuh sehingga ikatan rangkap dalam gugus tersebut memberikan orbital phi yang diperlukan. Jenis transisi ini merupakan transisi yang paling cocok untuk analisis dengan panjang gelombang 200-700 nm, dan panjang gelombang ini secara teknis dapat diaplikasikan pada spektrofotometer ultraviolet-visibel.
2.2.4 Hukum Lambert-Beer
Hukum Lambert-Beer menyatakan bahwa intensitas yang diteruskan oleh
larutan zat penyerap berbanding lurus dengan tebal dan konsentrasi larutan (Rohman, 2007). Hukum Lambert-Beer umumnya dikenal dengan persamaan sebagai berikut:
A = a.b.c (g/liter) atau A = ε.b.c (mol/liter) atau A = A11.b.c (g/100 ml) Keterangan: A = absorbansi c = konsentrasi
2.2.5 Kegunaan spektrofotometri ultraviolet-visibel
Metode spektrofotometri memiliki beberapa keuntungan antara lain kepekaan yang tinggi, ketelitian yang baik, mudah dilakukan, cepat pengerjaannya, dan dapat digunakan untuk menentukan senyawa campuran (Munson, 1984). Data spektrum ultraviolet-visibel secara tersendiri dapat digunakan untuk identifikasi kualitatif obat, tetapi sangat terbatas karena rentang daerah radiasi yang relatif sempit hanya dapat menghasilkan sedikit sekali puncak absorpsi. Penggunaan utama spektrofotometri ultraviolet-visibel adalah dalam analisis kuantitatif. Apabila dalam alur radiasi spektrofotometer terdapat senyawa yang mengabsorpsi radiasi, akan terjadi pengurangan kekuatan radiasi yang mencapai detektor (Satiadarma, dkk., 2004; Rohman, 2007).
2.3 Analisis Multikomponen dengan Spektrofotometri Ultraviolet-Visibel
Analisis kuantitatif campuran dua komponen merupakan teknik pengembangan analisis kuantitatif komponen tunggal. Prinsip pelaksanaannya adalah mencari absorban atau beda absorban tiap-tiap komponen yang memberikan korelasi yang linier terhadap konsentrasi, sehingga akan dapat dihitung masing-masing kadar campuran zat tersebut secara serentak atau salah satu komponen komponen dalam campurannya dengan komponen lainnya (Mulja dan Suharman, 1995).
Menurut Day dan Underwood (1986), terdapat beberapa kemungkinan yang terjadi pada spektrum absorban dua komponen.
Kemungkinan I
λ1 dan λ2. Gambar spektrum absorban senyawa X dan Y dapat dilihat pada Gambar 2.7.
Gambar 2.7 Spektrum Absorban Senyawa X dan Y Kemungkinan II
Terjadi tumpang tindih satu cara dimana Y tidak mengganggu pengukuran X pada λ1, tetapi X mengganggu pengukuran Y karena X memang menyerap cukup banyak bersama-sama Y pada λ2. Spektrum absorban senyawa X dan Y, spektrum X bertumpang tindih pada spektrum Y dapat dilihat pada Gambar 2.8.
Gambar 2.8 Spektrum Absorban Senyawa X dan Y, Spektrum X Bertumpang Tindih pada Spektrum Y
Kemungkinan III
Gambar 2.9 Spektrum Absorban Senyawa X dan Y Saling Tumpang Tindih
Menurut Andrianto (2009), pada penetapan kadar campuran multikomponen sulit dilakukan, sehingga untuk mengatasi hal tersebut diperkenalkan analisis multikomponen menggunakan prinsip persamaan regresi berganda melalui perhitungan matriks dengan metode pengamatan beberapa panjang gelombang berganda (multiple wavelength).
2.4 Validasi Metode
Validasi metode adalah suatu proses yang menunjukkan bahwa prosedur analitik telah sesuai dengan penggunaan yang dikehendaki. Proses validasi metode untuk prosedur analitik dimulai dengan pengumpulan data validasi oleh pelaksana guna mendukung prosedur analitiknya (Bliesner, 2006).
Hasil validasi metode dapat digunakan untuk memutuskan kualitas, reabilitas, dan konsistensi dari hasil analisis (Huber, 2007). Adapun karakteristik dalam validasi metode menurut USP 30 NF 25 (2007) yaitu akurasi, presisi, spesifisitas, batas deteksi, batas kuantitasi, linieritas, rentang, dan kekasaran/ketahanan.
2.4.1 Akurasi
perolehan kembali (% recovery). Akurasi merupakan ukuran ketepatan prosedur analisis (Satiadarma, dkk., 2004).
2.4.2 Presisi
Presisi adalah ukuran keterulangan metode analisis, termasuk di antaranya kemampuan instrumen dalam melakukan hasil analisis yang reprodusibel. Presisi dinyatakan sebagai standar deviasi relatif atau koefisien variasi. Keterulangan dilakukan dengan cara menganalisis sampel yang sama oleh analis yang sama menggunakan instrumen yang sama dalam periode waktu yang singkat. Syarat koefisien variasi bernilai kurang dari 2% (Satiadarma, dkk., 2004).
2.4.3 Spesifisitas
Spesifisitas adalah suatu ukuran seberapa mampu metode tersebut mengukur analit saja dengan adanya senyawa-senyawa lain yang terkandung di dalam sampel (Watson, 2005). Secara umum, spesifisitas dapat ditunjukkan oleh minimalnya gangguan oleh senyawa lain terhadap hasil analisis. Pendekatan tidak langsung adalah lewat pengamatan karakteristik akurasi dari metode tersebut. Bila akurasi metode telah dapat diterima maka metode tersebut otomatis telah masuk kriteria sebagai metode yang spesifik (Ermer dan McB. Miller, 2005).
2.4.4 Batas deteksi dan batas kuantifikasi
Batas deteksi didefinisikan sebagai konsentrasi analit terendah dalam sampel yang masih dapat dideteksi, meskipun tidak dapat dikuantifikasi. Batas deteksi merupakan batas uji yang spesifik menyatakan apakah analit di atas atau di bawah nilai tertentu (Rohman, 2007). Menurut Harmita (2004), batas deteksi dapat dihitung dengan rumus sebagai berikut:
Batas kuantifikasi didefinisikan sebagai konsentrasi analit terendah dalam sampel yang dapat ditentukan dengan presisi dan akurasi yang dapat diterima pada kondisi operasional metode yang digunakan (Rohman, 2007). Menurut Harmita (2004), batas kuantifikasi dapat dihitung dengan rumus sebagai berikut:
Batas kuantifikasi = 2.4.5 Linieritas
Linieritas menunjukkan kemampuan suatu metode analisis untuk memperoleh hasil pengujian yang sesuai dengan kisaran konsentrasi analit tertentu. Hal ini dapat dilakukan dengan cara membuat kurva kalibrasi dari beberapa set larutan baku yang telah diketahui konsentrasinya. Persamaan garis yang digunakan pada kurva kalibrasi diperoleh dari persamaan y = ax + b. Persaman ini akan menghasilkan koefisien korelasi (r). Koefisien korelasi inilah yang digunakan untuk mengetahui linieritas suatu metode analisis (Satiadarma, dkk., 2004).
2.4.6 Rentang
Rentang adalah interval antara batas konsentrasi tertinggi dan terendah analit yang terbukti dapat ditentukan menggunakan prosedur analisis, dengan presisi, akurasi, dan linieritas yang baik. Rentang biasanya dinyatakan dalam satuan yang sama dengan hasil uji (Satiadarma, dkk., 2004).
2.4.7 Kekasaran dan ketahanan
BAB I PENDAHULUAN 1.1 Latar Belakang
Sediaan farmasi yang beredar di pasaran kebanyakan berupa campuran berbagai zat berkhasiat. Campuran ini bertujuan untuk meningkatkan efek terapi dan kemudahan dalam pemakaian. Salah satu campuran zat aktif yang sering digunakan adalah obat analgesik. Analgesik merupakan obat yang meredakan rasa nyeri tanpa mengakibatkan kehilangan kesadaran. Kombinasi analgesik yang banyak ditemukan adalah parasetamol dengan kafein (Tan dan Rahardja, 2007). Parasetamol dan kafein dipilih atas dasar kedua macam zat tersebut banyak dijumpai dalam sediaan obat yang dijual secara bebas, sehingga perlu diadakan penelitian tentang penetapan kadarnya untuk menjamin kualitas sediaan obat. Namun, dengan adanya lebih dari satu macam zat aktif dalam satu sediaan obat, menimbulkan kesulitan dalam penetapan kadarnya.
Penetapan kadar parasetamol dan kafein dalam bentuk tunggal dapat ditetapkan dengan metode spektrofotometri ultraviolet, dalam larutan asam parasetamol memiliki serapan maksimum pada panjang gelombang 245 nm (A11 = 668a), sedangkan kafein pada panjang gelombang 273 nm (A11 = 504a)
Beberapa penelitian mengenai penetapan kadar parasetamol dan kafein dalam sediaan tablet telah banyak dilakukan sebelumnya dengan beberapa metode, antara lain dengan metode spektrofotometri ultraviolet mutikomponen (Wulandari, 2008), metode Kromatografi Cair Kinerja Tinggi (KCKT) (Pane, 2010) dan metode zero crossing spektrofotometri derivatif (Rosita, 2015).
Metode spektrofotometri ultraviolet digunakan untuk menganalisis senyawa tunggal, tetapi dengan melakukan modifikasi pada metode, spektrofotometri ultraviolet dapat digunakan untuk analisis multikomponen. Dengan modifikasi tersebut, Andrianto (2009) telah melakukan penetapan kadar campuran parasetamol dan ibuprofen menggunakan metode panjang gelombang berganda.
Pada metode panjang gelombang berganda, penentuan lima panjang gelombang analisis diperoleh dengan menumpang tindihkan spektrum serapan maksimum masing-masing komponen, selanjutnya penetapan kadar dilakukan dengan prinsip persamaan regresi melalui perhitungan operasi matriks. Pada metode ini tidak diperlukan proses pemisahan komponen zat aktif karena kadar parasetamol dan kafein dapat ditetapkan secara bersama-sama tanpa harus dipisahkan, dengan waktu yang singkat dengan alat dan biaya yang relatif lebih murah (Andrianto, 2009).
yaitu mengandung parasetamol dan kafein tidak kurang dari 90,0% dan tidak lebih dari 110,0 % dari jumlah yang tertera pada etiket.
Dalam penetapan kadar campuran beberapa zat dengan metode panjang gelombang berganda juga harus memenuhi persyaratan validasi. Parameter yang dipakai adalah uji akurasi (ketepatan) dan uji presisi (ketelitian) dengan koefisien variasi (% KV) karena penilaian dari kedua parameter ini sudah cukup mewakili
untuk menilai validitas dari metode panjang gelombang berganda (Andrianto, 2009).
Di pasaran, perbandingan parasetamol dan kafein dalam tablet sebesar 12:1 sehingga dalam penetapan kadar campurannya perlu dilakukan metode adisi terhadap kafein. Berdasarkan hal tersebut maka penulis tertarik untuk melakukan penetapan kadar parasetamol dan kafein dalam sediaan tablet dengan metode panjang gelombang berganda secara spektrofotometri.
1.2 Perumusan Masalah
Berdasarkan latar belakang di atas, maka dibuat perumusan masalah sebagai berikut:
1. Apakah metode panjang gelombang berganda secara spektrofotometri dapat digunakan dalam penetapan kadar parasetamol dan kafein dalam sediaan tablet?
1.3 Hipotesis
Berdasarkan perumusan masalah diatas, maka dibuat hipotesis sebagai berikut:
1. Metode panjang gelombang berganda secara spektrofotometri dapat digunakan dalam penetapan kadar parasetamol dan kafein dalam sediaan tablet.
2. Kadar parasetamol dan kafein dalam sediaan tablet yang ditentukan dengan metode panjang gelombang berganda secara spektrofotometri memenuhi persyaratan yang tercantum dalam USP 30 NF 25 (2007).
1.4 Tujuan Penelitian
Tujuan dilakukannya penelitian ini adalah:
1. Untuk mengetahui apakah metode panjang gelombang berganda secara spektrofotometri dapat digunakan dalam penetapan kadar parasetamol dan kafein dalam sediaan tablet.
2. Untuk mengetahui apakah kadar parasetamol dan kafein dalam sediaan tablet yang ditentukan dengan metode panjang gelombang berganda secara
spektrofotometri memenuhi persyaratan yang tercantum pada USP 30 NF 25 (2007).
1.5 Manfaat Penelitian
APLIKASI METODE PANJANG GELOMBANG BERGANDA SECARA SPEKTROFOTOMETRI TERHADAP PENETAPAN KADAR
PARASETAMOL DAN KAFEIN DALAM SEDIAAN TABLET ABSTRAK
Latar Belakang: Berbagai sediaan obat yang terdapat di pasaran mengkombinasikan dua atau lebih zat aktif dalam satu sediaan, seperti obat analgesik. Sehingga muncul kesulitan untuk menganalisis kadar masing-masing komponen. Oleh karena itu diperlukan suatu metode untuk menganalisis masing-masing komponen tersebut, misalnya untuk menganalisis kadar campuran parasetamol dan kafein dalam sediaan tablet.
Tujuan Penelitian: Untuk menetapkan kadar campuran parasetamol dan kafein dalam sediaan tablet secara spektroktrofotometri ultraviolet dengan metode panjang gelombang berganda.
Metode: Pengambilan sampel secara purposif terhadap sediaan tablet B. Penetapan kadar parasetamol dan kafein secara spektrofotometri ultraviolet dengan metode panjang gelombang berganda, menggunakan pelarut HCl 0,1 N. Hasil: Hasil penelitian menunjukkan bahwa kadar parasetamol yang diperoleh dalam tablet B sebesar 92,10% ± 0,39% dan untuk kafein diperoleh 98,10% ± 0,34%. Dapat disimpulkan bahwa hasil penetapan kadar campuran parasetamol dan kafein dalam tablet memenuhi persyaratan sesuai dengan persyaratan yang tertera pada United States Pharmacopoeia (USP 30 NF 25, 2007). %KV parasetamol sebesar 0,40% dan kafein sebesar 0,33%.
Kesimpulan: Berdasarkan hasil penelitian yang dilakukan maka metode spektrofotometri ultraviolet dengan panjang gelombang berganda dapat digunakan untuk melakukan penetapan kadar campuran parasetamol dan kafein dalam sediaan tablet.
APPLICATION OF MULTIPLE WAVELENGTH METHOD BY SPECTROPHOTOMETRY FOR DETERMINATION OF
PARACETAMOL AND CAFFEINE IN TABLET ABSTRACT
Background: Many drugs that available in the market combine two or more active substance, such as analgesics. Hence the difficulty to analyze the levels of each component. Therefore, we need a method to analyze each of these components, for example, to analyze the levels of a mixture of paracetamol and caffeine in tablets.
Research Purpose: The purpose of this research is to determine the levels of paracetamol and caffeine in tablet using spectrophotometry ultraviolet with multiple wavelength method.
Method: The method of research was done by purposive sampling to tablet B. Determination of paracetamol and caffeine using spectrophotometry ultraviolet with multiple wavelength method, in the HCl 0.1 N solvent.
Result: The results of research was exhibited that paracetamol in tablet B are 92.10% ± 0.39% and caffeine are 98.10% ± 0.34%. Therefore, it can be concluded that the determination of paracetamol and caffeine in tablet meets the requirements of the United States Pharmacopoeia (USP 30 NF 25, 2007). %CV of paracetamol are 0.40% and caffeine are 0.33%.
Conclusion: Based on the result of researchs that spectrophotometry ultraviolet with multiple wavelength method can be used to determine the levels of paracetamol and caffeine in tablet.
APLIKASI METODE PANJANG GELOMBANG BERGANDA
SECARA SPEKTROFOTOMETRI TERHADAP
PENETAPAN KADAR PARASETAMOL DAN
KAFEIN DALAM SEDIAAN TABLET
SKRIPSI
OLEH:
KANGGA SRI WILYTA
NIM 121501094
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
APLIKASI METODE PANJANG GELOMBANG BERGANDA
SECARA SPEKTROFOTOMETRI TERHADAP
PENETAPAN KADAR PARASETAMOL DAN
KAFEIN DALAM SEDIAAN TABLET
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
KANGGA SRI WILYTA
NIM 121501094
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
PENGESAHAN SKRIPSI
APLIKASI METODE PANJANG GELOMBANG BERGANDA SECARA SPEKTROFOTOMETRI TERHADAP PENETAPAN KADAR
PARASETAMOL DAN KAFEIN DALAM SEDIAAN TABLET OLEH:
KANGGA SRI WILYTA NIM 121501094
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 18 Agustus 2016
Medan, Oktober 2016
Prof. Dr. Muchlisyam, M.Si., Apt. NIP 195006221980021001
Pembimbing II
Dra. Tuty Roida Pardede, M.Si., Apt. NIP 195401101980032001
Panitia Penguji,
Prof. Dr. Siti Morin Sinaga, M.Sc., Apt. NIP 195008281976032002
Prof. Dr. Muchlisyam, M.Si., Apt.
NIP 195006221980021001
Dra. Sudarmi, M.Si., Apt. NIP 195409101983032001
KATA PENGANTAR
Puji syukur ke hadirat Tuhan Yang Maha Esa karena atas limpahan berkat dan kasihNya, penulis dapat menjalani masa perkuliahan dan penelitian hingga menyelesaikan penyusunan skripsi dengan baik. Adapun judul skripsi ini adalah “Aplikasi Metode Panjang Gelombang Berganda secara Spektrofotometri Terhadap Penetapan Kadar Parasetamol dan Kafein dalam Sediaan Tablet”. Skripsi ini merupakan salah satu syarat guna memperoleh gelar Sarjana Farmasi dari Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini penulis ingin menyampaikan rasa terima kasih yang tulus kepada Ibu Dr. Universitas Sumatera Utara yang telah memberikan fasilitas sehingga penulis dapat menyelesaikan pendidikan demi memperoleh gelar sarjana farmasi. Bapak Prof. Dr. Muchlisyam, M.Si., Apt., dan Ibu Dra. Tuty Roida Pardede, M.Si., Apt., selaku dosen pembimbing yang telah meluangkan waktunya untuk memberikan bimbingan, pengarahan, saran dan motivasi selama penelitian sampai penyusunan skripsi ini selesai, juga kepada Ibu Prof. Dr. Siti Morin Sinaga, M.Sc., Apt., Ibu Dra. Sudarmi, M.Si., Apt., dan Ibu Sri Yuliasmi, M.Si., Apt., selaku dosen penguji yang telah memberikan kritik, saran dan arahan kepada penulis demi kesempurnaan skripsi ini.
hingga penyelesaian skripsi ini. Untuk teman-teman seperjuangan di Laboratorium Penelitian, khususnya Cindy Febriani yang telah sangat membantu dan mengajarkan banyak hal selama penelitian, untuk sahabat-sahabat: Derianty, Lany, Sylvia, Shena, Nugraha, Romy, Michael dan teman-teman stambuk 2012 lainnya yang tidak dapat penulis sebutkan satu-persatu namanya, terima kasih telah banyak memberikan bantuan, dukungan dan motivasi dalam menyelesaikan penulisan skripsi ini.
Penulis menyadari bahwa skripsi ini masih memiliki banyak kekurangan, oleh sebab itu dengan segala kerendahan hati penulis bersedia menerima kritik dan saran yang membangun untuk kesempurnaan skripsi ini. Akhir kata, penulis berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, Agustus 2016 Penulis,
SURAT PERNYATAAN Saya yang bertanda tangan di bawah ini,
Nama : Kangga Sri Wilyta
Nomor Induk Mahasiswa : 121501094
Program Studi : S-1 Farmasi Reguler
Judul Skripsi : Aplikasi Metode Panjang Gelombang Berganda secara Spektrofotometri terhadap Penetapan Kadar Parasetamol dan Kafein dalam Sediaan Tablet Dengan ini menyatakan bahwa skripsi ini ditulis berdasarkan data dari hasil pekerjaan yang saya lakukan sendiri, dan belum pernah diajukan oleh orang lain untuk memperoleh gelar kesarjanaan di Perguruan Tinggi dan bukan plagiat karena kutipan yang ditulis telah disebutkan sumbernya di dalam daftar pustaka. Apabila dikemudian hari ada pengaduan dari pihak lain karena di dalam skripsi ini ditemukan plagiat karena kesalahan saya sendiri, maka saya bersedia menerima sanksi apapun oleh Program Studi Farmasi Fakultas Farmasi Universitas Utara, dan bukan menjadi tanggung jawab pembimbing.
Demikianlah surat pernyataan ini saya perbuat dengan sebenarnya untuk dapat digunakan jika diperlukan sebagaimana mestinya.
Medan, Agustus 2016 Yang membuat pernyataan,