DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2013
LENA ELVIRA ROSA
PENENTUAN KUERSETIN DALAM BAWANG DAYAK
(Eleutherine palmifolia) DENGAN
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Penentuan Kuersetin
dalam Bawang Dayak (Eleutherine palmifolia) dengan Kromatografi Cair Kinerja
Tinggi adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Mei 2013
Lena Elvira Rosa
ABSTRAK
LENA ELVIRA ROSA. Penentuan Kuersetin dalam Bawang Dayak (Eleutherine
palmifolia) dengan Kromatografi Cair Kinerja Tinggi. Dibimbing oleh DEDEN
SAPRUDIN dan EDY DJAUHARI PURWAKUSUMAH.
Eleutherine palmifolia yang dikenal dengan nama bawang dayak atau bawang sabrang adalah tanaman obat yang banyak digunakan dalam mengobati berbagai penyakit seperti diabetes, hipertensi, dan menurunkan kolesterol. Penelitian ini bertujuan menentukan besarnya kandungan kuersetin dalam bawang dayak dan mendapatkan kinerja analisis penentuan kuersetin pada bawang dayak dengan metode kromatografi cair kinerja tinggi (KCKT). Untuk meyakinkan bahwa metode analisis KCKT dapat digunakan sesuai dengan tujuan yang diinginkan maka metode tersebut divalidasi. Parameter-parameter validasi yang diuji meliputi linearitas, limit deteksi, limit kuantifikasi, dan ketelitian. Linearitas pada konsentrasi 0.5, 2.5, 10, dan 20 mg/L memiliki koefisien korelasi sebesar 0.9992. Limit deteksi metode ini adalah sebesar 0.0482 mg/L dan limit kuantifikasi sebesar 0.1460 mg/L. Ketelitian yang diperoleh dari metode ini ialah 13.41%. Rerata kadar kuersetin yang diperoleh adalah 0.2943%. Jumlah kuersetin yang cukup tinggi membuat bawang dayak berpotensi sebagai obat.
Kata kunci: bawang dayak, bawang sabrang, Eleutherine palmifolia, kromatografi
cair kinerja tinggi, kuersetin
ABSTRACT
LENA ELVIRA ROSA. Determination of Quercetin in Bawang Dayak
(Eleutherine palmifolia) Using High-Performance Liquid Chromatography. Supervised by DEDEN SAPRUDIN dan EDY DJAUHARI PURWAKUSUMAH.
Eleutherine palmifolia known as bawang dayak or bawang sabrang is widely used as herbal medicine to treat various diseases, including diabetes, hypertension and lowering cholesterol. The objectives of this research are to
determine content of quercetin in bawang dayak and to analyze the performance
of determination method of quercetin in bawang dayak using high-performance
liquid chromatography (HPLC). To ensure that HPLC method can be used for the intended purpose then the method has to be validated. Parameters determined on method validation were linearity, limit of detection, limit of quantification, and precision. The linearity in the concentrations of 0.5, 2.5, 10, and 20 mg/L showed correlation coefficient of 0.9992. The limit of detection was 0.0482 mg/L and the limit of quantification was 0.1460 mg/L. The precision of this method was
13.41%. The average concentration quercetin in bawang dayak was 0.2943%. The
number of quercetin that is high enough make bawang dayak potential as a
medicine.
Keywords: bawangdayak, bawang sabrang, Eleutherine palmifolia,
PENENTUAN KUERSETIN DALAM BAWANG DAYAK
(Eleutherine palmifolia) DENGAN
KROMATOGRAFI CAIR KINERJA TINGGI
LENA ELVIRA ROSA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul Skripsi : Penentuan Kuersetin dalam Bawang Dayak (Eleutherine palmifolia) dengan Kromatografi Cair Kinerja Tinggi
Nama : Lena Elvira Rosa
NIM : G44080102
Disetujui oleh
Dr. Deden Saprudin, MSi Pembimbing I
Drs. Edy Djauhari PK., MSi Pembimbing II
Diketahui oleh
Prof. Dr. Ir. Tun Tedja Irawadi, MS Ketua Departemen
PRAKATA
Puji dan syukur kehadirat Allah SWT yang telah melimpahkan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul
“Penentuan Kuersetin dalam Bawang Dayak (Eleutherine palmifolia) dengan
Kromatografi Cair Kinerja Tinggi”.Penulis mengucapkan terima kasih kepada
Bapak Dr. Deden Saprudin, MSi. dan Bapak Drs. Edy Djauhari PK., MSi selaku pembimbing yang senantiasa memberikan saran dan kritik yang membangun
kepada penulis selama melakukan penelitian. Kepada Genksi Foundation yang
telah memberikan beasiswa kepada penulis selama perkuliahan dan penelitian penulis mengucapkan terima kasih. Kepada Laboratorium Bersama penulis mengucapkan teima kasih atas bantuannya dalam keringanan biaya penelitian. Ucapan terima kasih penulis sampaikan pula kepada Pak Eman Suherman, Bu Nunung Nuryanti, Pak Kosasih, Pak Edi Suhendar, dan Mas Eko, atas bantuan yang diberikan selama penulis melaksanakan penelitian.
Penulis juga mengucapkan terima kasih kepada Almarhumah Bunda, Almarhum Ayah, Kak Lusi, Bang Amir dan Ndung yang telah mendukung penulis dengan doa dan kasih sayangnya. Selain itu, penulis juga mengucapkan terima kasih kepada Septhia, Kiki, Ani, dan Nia atas bantuan dan dorongannya selama penelitian. Penulis berharap karya ilmiah ini dapat bermanfaat bagi perkembangan ilmu pengetahuan.
Bogor, Mei 2013
DAFTAR ISI
DAFTAR TABEL vii
DAFTAR GAMBAR vii
DAFTAR LAMPIRAN vii
PENDAHULUAN 1
METODE 2
Bahan dan Alat 2
Prosedur Penelitian 2
HASIL DAN PEMBAHASAN 4
Penentuan Kadar Air dan Kadar Abu 4
Hasil Ekstraksi Kuersetin 4
Hasil Analisis Ekstrak Bawang Dayak dengan KCKT 5
Metode Validasi 6
SIMPULAN DAN SARAN 9
Simpulan 9
Saran 9
DAFTAR PUSTAKA 10
DAFTAR TABEL
1. Hasil pencarian eluen terbaik 6
2. Hasil pengujian linearitas 7
3. Hasil pengujian ketelitian 8
DAFTAR GAMBAR
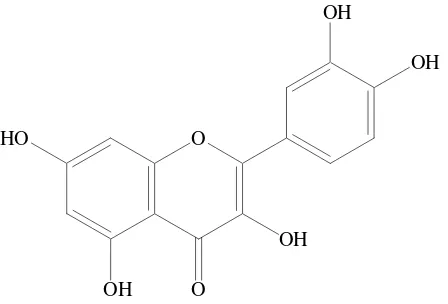
1 Struktur kuersetin 5
2 Kurva standar kuersetin rerata 7
DAFTAR LAMPIRAN
1 Diagram alir penelitian 12
2 Kadar air umbi bawang dayak 13
3 Kadar abu umbi bawang dayak 14
4 Pencarian eluen terbaik 15
5 Uji linearitas 18
6 Penentuan limit deteksi dan limit kuantifikasi 23
1
PENDAHULUAN
Indonesia merupakan negara yang cukup berlimpah dengan hasil alamnya. Banyak diantara jenis tanaman yang tumbuh di Indonesia dapat digunakan untuk tujuan pengobatan. Tanaman yang dipercaya sebagai tanaman obat oleh masyarakat sebagian besar belum diketahui dengan pasti kandungan kimia dan khasiat. Kondisi ini menuntut adanya penelitian-penelitian yang mengarah pada penemuan kandungan kimia dan khasiat dari berbagai macam tanaman obat yang ada di Indonesia. Banyaknya penelitian yang telah dilakukan dan terbuktinya khasiat dari tanaman obat membuat penggunaan dan permintaan terhadap tanaman obat semakin meningkat.
Salah satu tanaman yang dipercaya berkhasiat dan digunakan sebagai obat
oleh masyarakat Indonesia adalah umbi bawang dayak (Eleutherine palmifolia)
yang termasuk dalam suku Iridaceae. Tanaman ini dapat tumbuh hampir di setiap daerah di Indonesia seperti di Kalimantan, Jawa, dan Sumatera. Tanaman ini banyak digunakan oleh masyarakat pedalaman sebagai obat/ramuan tradisional. Bahkan di Tanah Grogot, Kabupaten Paser, Provinsi Kalimantan Timur, bersama tanaman herbal lain bawang dayak diproduksi dalam bentuk kapsul tanpa bahan pengawet untuk mengatasi berbagai penyakit (Muchroni 2010).
Masyarakat Dayak sebagai konsumen terbanyak tanaman ini menuturkan bahwa bawang dayak sering digunakan sebagai obat kanker payudara dan penambah stamina. Selain itu, oleh masyarakat lain umbinya dipercaya bermanfaat sebagai antiemetik,radang usus, disenteri, penyakit kuning, luka, bisul,
diabetes melitus, hipertensi, dan menurunkan kolesterol (Arung et al. 2009).Hasil
uji yang telah dilakukan menunjukkan bahwa tanaman bawang dayak memiliki hampir semua kandungan fitokimia, antara lain alkaloid, glikosida, flavonoid, fenolik dan steroid (Anne 2011).
Penelitian Rosfianita (2010) mengungkapkan kandungan terdapat flavonoid golongan flavonol pada bawang dayak. Sebagian besar tanaman obat mengandung banyak senyawa flavonoid (Farnsworth 1966). Jenis flavonoid yang banyak terdapat pada tanaman adalah kuersetin, mirisetin, dan kaemferol. Pada penelitian Miean dan Suhaila (2008) jenis flavonoid yang paling banyak terdapat dalam daun bawang adalah flavonoid jenis kuersetin. Berdasarkan penelitian tersebut, dimungkinkan bahwa pada bawang dayak jenis flavonoid yang paling banyak adalah kuersetin. Kuersetin merupakan senyawa golongan flavonol yang paling banyak terdapat dalam tanaman dan juga paling aktif (Furhman dan Aviram 2002). Banyak tanaman obat menunjukkan khasiatnya yang baik seiring dengan tingginya kandungan kuersetin. Khasiat bawang dayak yang banyak dipercaya sebagai antikanker dan penyakit lainnya dimungkinkan karena tingginya kadar kuersetin dalam bawang dayak.
Penelitian ini dilakukan untuk mengetahui besarnya kandungan
2
BAHAN DAN METODE
Bahandan Alat
Bahan-bahan yang digunakan antara lain sampel bawang dayak dari kebun
Biofarmaka Bogor, metanol, asetonitril, HCl, KH2PO4, H3PO4, dan standar
kuersetin. Alat-alat yang digunakan antara lain oven, tanur, eksikator, neraca
analitik, dan KCKT Shimadzu LC-20Akolom C-18 phase; Develosil ODS-UG-3
yang memiliki dimensi panjang 75 mm dan diameter dalam 4.6 mm. Fase gerak
yang digunakan adalah metanol dan H3PO40.5% secara isokratik dengan laju alir
0.9 mL/menit. Detektor yang digunakan adalah detektor ultraviolet (UV) pada panjang gelombang 370 nm.
Metode
Tahapan penelitian yang dilakukan meliputi preparasi sampel bawang dayak, penentuan kadar air dan kadar abu, hidrolisis bawang dayak, dan kemudian penentuan flavonoid pada ekstrak bawang dayak dengan KCKT (Lampiran 1).
Preparasi Umbi Bawang Dayak
Umbi bawang dayak segar dibersihkan dari kotoran dengan mencucinya dengan air bersih, lalu ditiriskan. Sampel dirajang tipis dan dikering-anginkan di udara terbuka terlindung dari sinar matahari langsung. Sampel dianggap kering bila sudah rapuh (hancur jika diremas) kemudian sampel digiling sampai menjadi serbuk.
Penentuan Kadar Air (AOAC 2007)
Cawan porselen dikeringkan di dalam oven bersuhu 105 °C selama 60 menit. Selanjutnya cawan didinginkan dalam eksikator selama 30 menit dan ditimbang bobot kosongnya. Sebanyak 2 g serbuk umbi bawang dayak dimasukkan ke dalam cawan dan dikeringkan di dalam oven selama 5 jam pada suhu 105 °C. Setelah itu, cawan didinginkan dalam eksikator sekitar 30 menit dan ditimbang, demikian seterusnya sampai diperoleh bobot konstan. Penentuan kadar air dilakukan 3 kali ulangan (triplo).
Kadar air (%) = – × 100%
Keterangan:
A = bobot bahan sebelum dikeringkan (g) B = bobot bahan setelah dikeringkan (g)
Penentuan Kadar Abu (AOAC 2007)
3
kemudian dibakar dalam tanur pada suhu 600 °C sampai diperoleh abu. Cawan berisi abu didinginkan dalam eksikator dan ditimbang.
Kadar abu (%) = × 100%
Keterangan:
A = bobot contoh awal (g)
B = bobot abu (g)
Hidrolisis Bawang Dayak (Nuutila et al. 2002)
Ekstraksi sekaligus hidrolisis flavonoid dilakukan dengan menambahkan ke dalam100 mg serbuk umbi bawang dayak sebanyak10mL HCl 1.2 M dalam methanol 50% kemudian direfluks pada 35 °C selama 16 jam. Hidrolisis dilakukan 3 kali ulangan. Ekstrak didinginkan pada suhu ruang, lalu sebanyak 10
mL disonikasi,dan disaring menggunakan filter 0.45 μm sebelum diinjeksikan ke
KCKT.
Analisis Kuersetin dengan KCKT (Hertog et al. 1992)
Pencarian Eluen Terbaik. Eluen yang diujiialah campuran asetonitril dan
KH2PO4 0.025 M dengan nisbah, meliputi 3:1, 5:3, 1:2, dan 2:3 secara
isokratik.Perubahan konsentrasi KH2PO4juga dilakukan, yaitu menjadi 1.67 × 10
-3
M dan 1.00× 10-3M dengan nisbah asetonitril danKH2PO4 sebesar 1:3 secara
isokratik. Secara gradien diujikan dengannisbah asetonitril denganKH2PO40.025
M 1:3 pada menit 0-10 menit dan asetonitril denganKH2PO40.025 M 1:1 pada
menit 10-20. Selain itu, digunakan juga eluen campuran metanol dengan asam fosfat 0.5% 80:20.
Pembuatan Larutan Standar. Larutan stok standar kuersetin 500
μg/mLdisiapkan dengan melarutkan 5 mg standar kuersetindalam 10mL metanol.
Larutan standar yang digunakan dalam penelitian ini terdiri atas 4 konsentrasi,
yaitu 0.5, 2.5, 10, dan 20 μg/mL, dibuat dengan mengencerkan larutan
stok.Larutan standar disaring menggunakan filter 0.45 μm sebelum diinjeksikan
ke KCKT.
Pembuatan Kurva Standar. Larutan standar dengan konsentrasi 0.5, 2.5,
10, dan 20 μg/mL diinjeksikan ke. KCKT. Luas puncak kromatogram standar yang diperoleh dari berbagai konsentrasi tersebut kemudian dialur ke dalam 1 grafik. Persamaan garis yang dihasilkan akan digunakan pada perhitungan limit
deteksi dan limit kuantifikasi.
Pengukuran Kadar Kuersetin. Larutan ekstrak bawang dayak hasil hidrolisis diukur kadar kuersetinnya dengan menggunakan KCKT. Kadar kuersetin ditentukan berdasarkan kurva standar yang merupakan hubungan antara konsentrasi standar dan luas puncak kuersetin.
Validasi Metode (Bae et al. 2012)
Parameter-parameter yang diukur adalah limit deteksi, limit kuantifikasi, linearitas, dan ketelitian.
4
Linearitas. Larutan standar kuersetin dengan konsentrasi 0.5, 2.5, 10, dan
20 μg/mL diinjeksikan ke dalam KCKT masing-masing sebanyak 3 kali.
Ketelitian. Larutan ekstrak bawang dayak, diinjeksikan sebanyak 5 kali.
HASIL DAN PEMBAHASAN
Penentuan Kadar Air dan Kadar Abu
Kandungan air di dalam suatu bahan merupakan faktor yang memengaruhi pertumbuhan bakteri dan mikroorganisme. Kadar air rerata umbi bawang dayak adalah 10.13%, yang menunjukkan bahwa dalam 100 gram sampel bawang dayak terkandung 10.13 g air yang terikat secara fisi dan dapat hilang oleh pemanasan pada suhu sekitar 105 °C. Data pengukuran tersaji pada Lampiran 2. Menurut Winarno (1992), kadar air minimum agar bakteri tidak tumbuh adalah 10%. Kadar air simplisia umbi bawang dayak yang diperoleh lebih besar dari 10% maka tidak dapat disimpan dalam jangka waktu yang lama.
Kadar air juga dapat dipakai untuk menentukan kadar zat aktif berdasarkan bobot keringnya. Jumlah air yang terkandung pada suatu bahan bergantung pada perlakuan yang telah dialami bahan tersebut dan kelembapan udara tempat penyimpanan. Bahan yang sama jika dianalisis pada waktu yang berbeda dapat menghasilkan kadar zat aktifnya karena kelembapa berubah. Jika kadar air bahan diketahui, maka bobot keringnya tetap. Jadi, apabila zat aktif bahan tidak rusak dan bahan juga tidak mengalami perubahan selain kadar airnya, maka kadar zat aktif akan konstan nilainya (Harjadi 1986).
Penentuan kadar abu dilakukan untuk menentukan kandungan bahan-bahan anorganik atau mineral dalam suatu bahan, kemurnian serta kebersihan bahan. Kadar abu rerata yang diperoleh sebesar 3.20% (Lampiran 3).
Hasil Ekstraksi Kuersetin
Aglikon flavonoid dalam tumbuhan umumnya terikat pada gula dan terdapat dalam beberapa bentuk kombinasi glikosida. Untuk penentuan kuersetin pada bawang dayak, residu gula harus terlebih dulu diputus dari aglikon dengan cara hidrolisis. Ekstraksi sekaligus hidrolisis flavonoid dilakukan dengan metode
refluks menggunakan pelarut metanol 50%. Hertog etal.(1992) melaporkan bahwa
5
Gambar 1 Struktur kuersetin
Menurut Nuutila et al. (2002), kondisi optimum hidrolisis untuk
menghasilkan kuersetin adalah pada suhu 35 °C dalam waktu 16 jam pada kondisi ini, kuersetin dalam bawang dayak tidak rusak dan terekstraksi secara maksimum. Jumlah kuersetin meningkat dengan semakin lama waktu hidrolisis, namun dapat pula terjadi degradasi kuersetin. Penelitian Lombard (2005) menunjukkan bahwa kuersetin glukosida dalam bawang relatif stabil terhadap suhu dan juga waktu hidrolisis. Penambahan HCl 1.2 M berfungsi menghidrolisis ikatan glikosidik pada flavonoid glikosida sehingga akan terpecah menjadi aglikon (flavonoid tanpa
gula terikat). HCl dipilih karena lebih efisien dibandingkan dengan H2SO4
(Hertog etal. 1992).
Hasil Analisis Ekstrak Bawang Dayak dengan KCKT
Fase gerak yang digunakan pada awal penelitian adalah asetonitril 25%
dalam KH2PO4 0025 M secara isokratik dengan laju alir 0.9 mL/menit. Eluen
tersebut tidak menghasilkan profil kromatogram yang baik, puncak kuersetin
melebar dan berekor.Hal ini dikarenakan KH2PO4 bersifat kurang polar sehingga
kurang baik mengalirkan kuersetin dan membuat puncak menjadi berekor. Kromatogram yang tidak cukup baik membuat pencarian eluen terbaik harus dilakukan untuk analisis ini.
Pencarian eluen terbaik dilakukan dengan menggunakan berbagai komposisi
eluenasetonitril dalam KH2PO4 0.025 M (Tabel 1). Penggunaan eluen yang
sama,tetapidengan nisbah asetonitril dan KH2PO4 0.025 Myang berbanding
terbalik dengan kondisi awal, (3:1) menghasilkan kromatogram dengan waktu retensi kuersetin terlalu cepat (Lampiran 4a).Agar kuersetin tidak terlalu cepat
keluar, nisbah asetonitril:KH2PO40.025 Mdiubah menjadi 1:1 dan 5:3. Kuersetin
bersifat polar, maka komposisi pelarut KH2PO40025 Mditambah agar eluen lebih
6
Tabel 1Pencarian eluen terbaik
Eluen Puncak yang dihasilkan Keterangan
Asetonitril:KH2PO40.025 M (3:1) Waktu retensi terlalu cepat Lampiran 4a
Asetonitril:KH2PO4 0.025 M (1:1) Waktu retensi terlalu cepat Lampiran 4b
Asetonitril:KH2PO4 0.025 M (5:3) Waktu retensi terlalu cepat Lampiran 4c
Asetonitril:KH2PO4 0.025 M (2:3) Berekor dan membelah Lampiran 4d
Asetonitril:KH2PO4 0.025 M (1:2) Berekor dan membelah Lampiran 4e
Asetonitril:KH2PO4(gradien) Berekor dan membelah Lampiran 4f
Asetonitril:KH2PO4 1.67 ×10-3 (1:3) Berekor dan membelah Lampiran 4g
Asetonitril:KH2PO4 1.00 × 10-3 (1:3) Berekor dan membelah Lampiran 4h
Metanol:Asam fosfat 0.5% (80:20) Tidak berekor Lampiran 4i
Pengujian campuran eluen asetonitril dan KH2PO4 dengan nisbah 2:3 dan
1:2 didasarlanpada selisih komposisi asetonitril dan KH2PO4yang tidak berbeda
jauh sehingga diharapkan dapat menghasilkan waktu retensi yang tidak terlalu cepat dan puncak yang tidak berekor tetapi, kromatogram yang didapatkan menunjukkan puncak yang berekor dan membelah menjadi beberapa puncak (Lampiran 4d dan 4e). Perubahan nisbah eluen dari isokratik menjadi gradien tetap menghasilkan puncak yang berekor(Lampiran 4f). Perubahan konsentrasi
KH2PO4juga dilakukan, tetapi puncak yang dihasilkan semakin membelah
(Lampiran 4g dan 4h). Berdasarkan hasil analisis dapat disimpulkan bahwa eluen
campuran asetonitril dengan KH2PO4 tidak cukup baik digunakan untuk analisis
kuersetin. Selanjutnya analisis dilakukan dengan menggunakan eluen metanol dan asam fosfat 0.5% (80:20) dan laju alir 0.9 mL/menit. Eluen ini memberikan kromatogram (Lampiran 4i) dengan puncak yang cukup baik sehingga dipilih sebagai eluen untuk analisis selanjutnya.
Validasi Metode Penentuan Kadar Kuersetin dengan KCKT
Validasi metode analisis merupakan proses untuk menunjukkan bahwa prosedur analisis sesuai dengan tujuan yang diharapkan. Validasi metode adalah proses penetapan dan evaluasi unjuk kerja sebuah metode analisis sesuai cara-cara yang ditentukan oleh konsensus bersama organisasi internasional. Validasi metode yang dilakukan pada penelitian ini meliputi pengujian linearitas, limit deteksi, limit kuantifikasi, dan ketelitian.
Linearitas
Linearitas adalah kemampuan metode analisis untuk mendapatkan hasil uji yang proporsional terhadap konsentrasi analit. Linearitas metode penentuan kadar kuersetin dengan KCKT ditentukan dengan cara membuat kurva hubungan antara
konsentrasi standar pada sumbu x dan luas area pada sumbu y. Konsentrasi
standar kuersetin yang digunakan adalah 0.5, 2.5, 10, dan 20 mg/L sebanyak 3
kali ulangan. Linearitas dinyatakan dalam koefisien korelasi (r). Koefisien
korelasi adalah kemampuan dari metode analisis untuk menghasilkan angka analisis yang proporsional terhadap konsentrasi analit dalam contoh pada interval konsentrasi tertentu (Wahyuni 2006). Berdasarkan hasil pengujian diperoleh data
yang disajikan pada Tabel 2 sehingga menghasilkan kurva standar rerata nilai r
7
lebih besar dari 0.9900. Nilai r ini menunjukkan bahwa kurva memiliki kelinieran
yang tinggi, artinya dengan meningkatnya konsentrasi kuersetin maka luas puncak juga akan mengalami peningkatan yang linier.
Tabel 2 Hasil pegujian linearitas Konsentrasi
(ppm)
Luas Area (mAU*s)
Rerata SD RSD
Ulangan 1 Ulangan 2 Ulangan 3
0.5 45.1670 45.2620 45.0350 45.15467 0.114001 0.0025
2.5 156.1970 156.0450 153.9870 155.4097 1.234407 0.0079
10 626.1690 630.3570 625.1750 627.2337 2.750167 0.0044
20 1189.0720 1184.1740 1173.0080 1182.0850 8.233287 0.0070
Keterangan : SD : standar deviasi RSD : simpangan baku relatif
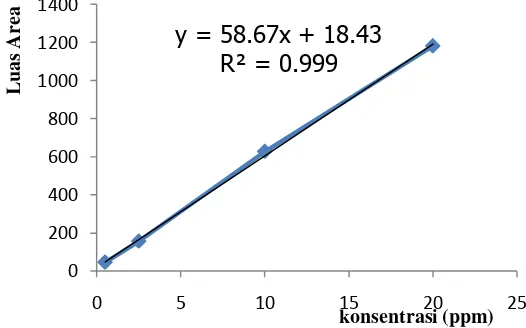
Gambar 2 Kurva standar kuersetin
Persamaan regresi linear untuk kurva standar rerata adalah y = 58.671x +
18.438(Gambar 2). Nilai kemiringan garis kurva menyatakan sensitivitas suatu metode. Nilai kemiringan garis yang besar menunjukkan bahwa perubahan konsentrasi yang kecil sangat berpengaruh terhadap sinyal detektor yang dihasilkan. Metode dengan nilai kemiringan seperti ini dapat dikatakan mempunyai sensitivitas yang sangat baik (Chan 2004).
Limit Deteksi dan Limit Kuantifikasi
Limit deteksi dan limit kuantifikasi diperoleh berdasarkan persamaan regresi linear kurva standar rerata hasil penentuan uji linearitas. Limit deteksi ditentukan untuk mengetahui konsentrasi analit terendah yang menghasilkan respons yang masih dapat dideteksi oleh sistem. Limit deteksi metode ini sebesar 0.0482 mg/L. Nilai ini menunjukkan bahwa sinyal antara kuersetin dengan derau dapat dibedakan pada konsentrasi terendah 0.0482 mg/L. Apabila nilai konsentrasi kuersetin dibawah 0.0482 mg/L maka instrumen tidak dapat mendeteksi keberadaan sinyal tersebut.
8
Limit kuantifikasi ditentukan untuk mengetahui konsentrasi analit terendah yang terdapat dalam sampel yang dapat diukur secara tepat dan teliti. Nilai limit kuantifikasi berdasarkan hasil uji sebesar 0.1460 mg/L. Konsentrasi analit yang terukur di bawah nilai ini memberikan ketelitian dan ketepatan yang kurang baik. Perhitungan limit deteksi dan limit kuantifikasi disajikan pada Lampiran 6.
Ketelitian
Ketelitian suatu metode analisis merupakan ukuran yang menunjukkan tingkat kesesuaian atau kedekatan setiap hasil analisis yang dilakukan berulang pada sampel yang homogen pada kondisi analisis yang sama. Ketelitian yang dilakukan adalah kedapatulangan karena dilakukan oleh operator, instrumen, peralatan, dan laboratorium yang sama. Kedapatulangan dapat digunakan untuk mengetahui adanya galat acak yang berasal dari preparsi contoh, seperti penimbangan, ekstraksi contoh, pembuatan larutan, penyaringan, dan kondisi instrumen KCKT yang digunakan.
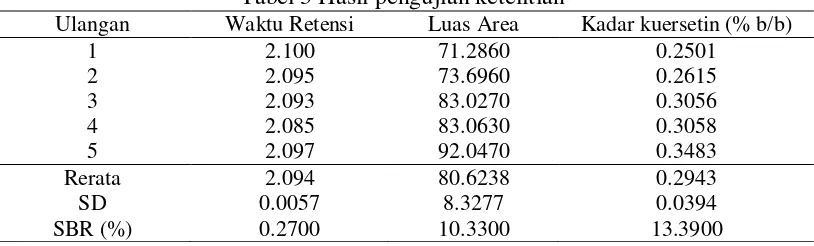
Tabel 3 Hasil pengujian ketelitian
Ulangan Waktu Retensi Luas Area Kadar kuersetin (% b/b)
1 2.100 71.2860 0.2501
Ketelitian dapat diketahui dengan menghitung simpangan baku relatif (SBR)
dari lima kali pengukuran. Data pengukuran ketelitian pada sampel disajikan pada
Tabel 3. Nilai SBR yang dihasilkan sebesar 13.39%. Menurut ICH (1995) nilai
SBR harus lebih kecil atau sama dengan 2.0%. Akan tetapi kondisi ini sangat
bergantung pada konsentrasi analit yang diperiksa, jumlah sampel, dan kondisi
laboratorium. Nilai SBR di atas 2% pada hasil penelitian menunjukkan bahwa
terdapat galat acak yang berasal dari penyiapan larutan yang sangat memengaruhi hasil analisis secara nyata. Galat acak terbesar diduga dari proses hidrolisis dan
kondisi KCKT. Metode ini berdasarkan nilai SBR yang diperoleh termasuk tidak
cukup teliti, artinya setiap hasil analisis yang dilakukan secara berulang memiliki nilai kedapatulangan yang cukup berbeda jauh. Perhitungan ketelitian dapat dilihat pada Lampiran 7.
Pengukuran Kadar Kuersetin dalam Bawang Dayak
9
standar merupakan metode dengan penambahan sejumlah standar ke dalam analit (Harvey 2000). Hasil analisis terhadap pengukuran konsentrasi kuersetin menunjukkan bahwa bawang dayak memiliki konsentrasi kuersetin rerata
0.2943% (b/b). Kenikir merupakan tanaman yang diidentifikasi memiliki
konsentrasi kuersetin terbesar pada peneltian yang dilakukan oleh Nuri et al
(2010), yaitu sebesar 0.4399%. Miean dan Mohamed (2001), melakukan penelitian terhadap kandungan flavonoid (myrisetin, kuersetin, kaempferol, luteolin, dan apigenin) pada 62 jenis tanaman pangan daerah tropis. Berdasarkan hasil yang diperoleh, kandungan kuersetin pada ke-62 jenis tanaman tersebut tidaklah sebanyak pada kenikir dan juga bawang dayak. Kandungan kuersetin pada penelitian tersebut terbanyak ditemukan pada daun bawang, yaitu sebanyak 0.1497% (b/b).
Banyak tanaman obat menunjukkan khasiatnya yang baik seiring dengan tingginya kandungan kuersetin. Kuersetin telah terbukti memiliki aktivitas sebagai anti peradangan karena langsung menghambat penyebab utama dari proses peradangan tersebut. Kuersetin juga memiliki aktivitas anti tumor. Selain itu, kuersetin memiliki pengaruh yang positif dalam membantu untuk mencegah kanker, prostatitis, gangguan jantung, katarak, dan gangguan pernafasan, seperti
bronkitis dan asma (Gusdinar et al. 2009). Tingginya kadar kuersetin yang
terdapat dalam bawang dayak membuat bawang dayak memiliki kemampuan sebagai anti peradangan dan anti tumor yang dapat dimanfaatkan sebagai alternatif tanaman obat.
SIMPULAN DAN SARAN
Simpulan
Metode penentuan kadar kuersetin dengan metode Kromatografi cair kinerja
tinggi mempunyai linearitas yang baik dengan persamaan kurva standar rerata y =
58.671x + 18.438dan r = 0.9992. Limit deteksi dan kuantifikasi berturut-turut
adalah 0.0482 mg/L dan 0.1460 mg/L. Metode ini mempunyai ketelitian yang tidak cukup teliti dengan nilai %SBR sebesar 13.39%. Konsentrasi kuersetin pada
bawang dayak sebesar 0.2943% (b/b) sehingga dapat digunakan sebagai tanaman
obat dengan kadar kuersetin yang cukup tinggi.
Saran
10
DAFTAR PUSTAKA
Anne A. 2011. Bawang dayak, obat herbal pengusir kanker [internet]. [diunduh 18 Nov 2011]. Tersedia dari: http://www.anneahira.com/bawang-dayak.htm.
[AOAC] Association of Official Analytical Chemist. 2007. Official Methods of
Analysis of AOAC International. Washington DC (US): AOAC.
Arung ET, Kusuma IW, Christy OE, Shimizu K, Kondo R. 2009. Evaluation of
medicinal plants from Central Kalimantan for antimelanogenesis. J Nat Med.
63:473-480. doi:10.1007/s11418-009-0351-7.
[ASEAN] Association of South East AsianNations. 1996. Good
ManufacturingPractice Guidelines. Ed ke-3. Jakarta (ID): ASEAN.
Bae H, Jayaprakasha GK, John J, Bhimanagouda S. 2012. Extraction efficiency
and validation of an HPLC method for flavonoid analysis in peppers. Food
Chemistry. 130: 751-758. doi:10.1016/j.foodchem.2011.07.041.
Chan CC. 2004. Potency method validation. Di dalam: Chan CC, Lee YC, Lam H,
Zhang XM, editor. Analytical MethodValidation and Instrument
PerformanceVerification. New Jersey (US): J Wiley.
Fajiriah S, Darmawan A, Sundowo A, Artanti N. 2007. Isolasi Senyawa
Antioksidan dari Ekstrak Etilasetat Daun Benalu Dendrophthoe pentandra
yang Tumbuh pada Inang Lobi-lobi. Jakarta (ID): Lembaga Ilmu Pengetahun Indonesia. hlm. 17-20. doi:22-67-1-PB.
Farnsworth NR. 1996. Biological and phytochemical screening of plants. Journal
of Pharmaceutical Sciences. 55: 259-260,
262,264-266.doi:10.1002/jps.2600550302.
Furhaman B, Aviram M. 2002. Polyphenols and flavonoids protect LDL against atherogenic modifications. Di dalam : Cadenas E dan L. Packer, editor.
Handbook of Antioxidants, Second Edition. New York (US): Marcel Dekker Inc.
Gusdinar, Rina H, Kartasasmita RE, Adnyana IK. 2009. Sintesis kuersetin terklorinasi dan aktivitas perlindungan terhadap tukak lambung. Majalah Farmasi Indonesia (4) 163-169.
Harjadi W. 1986. Ilmu Kimia Analitik Dasar. Jakarta (ID): Gramedia.
Harvey D. 2000. Modern Analytical Chemistry. New York (US): McGraw Hill.
Hertog MGL, Hollman PCH, Venema DP. 1992. Optimatization of a quantitative HPLC determination of potentially anticarcinogenic flavonoids in
vegetables and fruits. J. Agric. Food.Chem. 40: 1591-1598.
doi:10.1021/jf00021a023.
[ICH] International Conference on Harmonization. 1995. Validation ofAnalytical
Procedurs: Definitions andTerminology. [internet]. [diunduh10 Feb2007]. Tersedia dari: http://www.ich.org.
Lombard K, Peffley E, Geoffriau E, Thompson L, Herring A. 2005. Quercetin in
onion (Alliumcepa L.) after heat-treatment simulating home preparation.
Journal of Food Composition and Analysis. 18: 571 – 581. doi:10.1016/j.jfca.2004.03.027.
Miean KH, S Mohamed. 2001. Flavonoid (myricetin, quercetin, kaempferol,
luteolin, and apigenin) content of edible tropical plant. J. Agric. Food. Chem.
11
Muchroni A. 2010. Bawang dayak [internet]. [diacu 18 Nov 2011]. Tersedia dari: evisyari.wordpress.com/2009 /05/22/bawang-dayak/.
Nuutila AM, Kammiovirta K, Oksman KM. 2002. Comparison of methods for the hydrolysis of flavonoids and phenolic acids from onion and spinach for
HPLC analysis. Food Chemistry. 76 : 519–525.
doi:10.1016/S0308-8146(01)00305-3.
Nuri A, Ratna B, Diny AS, Bradley B, Hanny W. 2010. Flavonoid content and
antioxidant activity of vegetables from Indonesia. Food Chemistry. 121 :
1231–1235.doi:10.1016/j.foodchem.2010.01.033
Rosfianita MN. 2011. Isolasi dan Karakterisasi Senyawa Flavonoid Umbi dari
Tumbuhan Bawang Sabrang(Eleutherine palmifolia (L.) Merr). [skripsi].
Medan (ID): Universitas Sumatera Utara.
Sri Wahyuni. 2006. Perbandingan Sistem Ekstraksi dan Validasi Penentuan Xantorrhizol dari Temulawak secara Kromatografi Cair Kinerja Tinggi. [skripsi]. Bogor (ID): Institut Pertanian Bogor.
12
Lampiran 1Diagram alir penelitian
13
Lampiran 2Kadar air umbi Bawang Dayak
Ulangan
14
Lampiran 3 Kadar abu umbi Bawang Dayak
Ulangan
Contoh perhitungan :
15
Lampiran 4Kromatogram kuersetin dengan berbagai jenis eluen
(a) Kromatogram kuersetin dengan eluen asetonitril:KH2PO4 0.025 M(3:1)
(b) Kromatogram kuersetin dengan eluen asetonitril:KH2PO4 0.025 M(1:1)
(c) Kromatogram kuersetin dengan eluen asetonitril:KH2PO4 0.025 M(5:3)
0.0 2.5 5.0 7.5 10.0 12.5 15.0 17.5 20.0 22.5 m in
Detector A:370nm
/2
Detector A:370nm
/1
Detector A:370nm
16
Lanjutan Lampiran 4
(d) Kromatogram kuersetin dengan eluen asetonitril:KH2PO4 0.025 M(2:3)
(e) Kromatogram kuersetin dengan eluen asetonitril:KH2PO4 0.025 M(1:2)
(f) Kromatogram kuersetin dengan eluen asetonitril:KH2PO4 0.025 M(gradien)
0.0 2.5 5.0 7.5 10.0 12.5 15.0 m in
Detector A:370nm
/4
Detector A:370nm
17
Lanjutan Lampiran 4
(g) Kromatogram kuersetin dengan eluen asetonitril:KH2PO4 1.67 × 10-3M (1:3)
(h) Kromatogram kuersetin dengan eluen asetonitril:KH2PO4 1.00 × 10-3M (1:3)
(i) Kromatogram kuersetin dengan eluen metanol:asam fosfat 0.5% (80 : 20)
0 .0 2 .5 5 .0 7 .5 1 0 .0 1 2 .5 1 5 .0 1 7 .5 m in
Detector A:370nm
18
Lampiran 5 Uji Linearitas
Kromatogram standar kuersetin 0.5 ppm ulangan 1
Kromatogram standar kuersetin0.5 ppm ulangan 2
19
Lanjutan Lampiran 5
Kromatogram standar kuersetin2.5 ppm ulangan 1
Kromatogram standar kuersetin2.5 ppm ulangan 2
Kromatogram standar kuersetin2.5 ppm ulangan 3
20
Lanjutan Lampiran 5
Kromatogram standar kuersetin10 ppm ulangan 1
Kromatogram standar kuersetin10 ppm ulangan 2
Kromatogram standar kuersetin10 ppm ulangan 3
21
Lanjutan Lampiran 5
Kromatogram standar kuersetin20 ppm ulangan 1
Kromatogram standar kuersetin20 ppm ulangan 2
Kromatogram standar kuersetin20 ppm ulangan 3
22
Lanjutan Lampiran 5
Konsentrasi (ppm)
Luas Area (mAU*s)
23
Lampiran 6 Penentuan limit deteksi dan limit kuantifikasi
Ulangan Nilai
a b r
1 58.9930 17.4550 0.9994
2 58.7800 19.0270 0.9990
3 58.2390 18.8310 0.9990
Rerata 58.6707 18.4377 0.9991
SD 0.38877 0.8566 0.0002
Limit Deteksi 0.0482
Limit Kuantifikasi 0.1460
ket : nilai a (slope), b (intercept), dan r (koefisien korelasi) dari masing-masing persamaan kurva kalibrasi.
Berdasarkan persamaan y = 58.671x + 18.438
Limit deteksi = 3.3 ×σ
= 3.3 ×0.8566
58.6707
= 0.0482
Limit kuantitasi = 10 ×σ
= 10 ×0.8566
58.6707
= 0.1460 Keterangan:
σ : simpangan baku intersep dari kurva standar
24
Lampiran 7 Uji ketelitian
Kromatogram sampel ulangan 1
Kromatogram sampel ulangan 2
Kromatogram sampel ulangan 3
0.0 1.0 2.0 3.0 4.0 5.0 6.0 7.0 8.0 9.0 m in
Detector A Ch1:370nm
1
Detector A Ch1:370nm
1
Detector A Ch1:370nm
25
Lanjutan Lampiran 7
Kromatogram sampel ulangan 4
Kromatogram sampel ulangan 5
Ulangan Waktu
Retensi
- Persamaan linier
y = 58.671x + 18.438 x = konsentrasi (ppm) y = Luas Area
Detector A Ch1:370nm
1
Detector A Ch1:370nm
26
Lanjutan Lampiran 7
Konsentrasi kuersetin sebenarnya = konsentrasi kuersetin ×faktor pengenceran
= 0.9007 ×25
1
= 22.5175 mg/L
Bobot kuersetin = konsentrasi kuersetin sebenarnya × volume larutan
= 22.5175 mg/L× 0.0100 L
- Rerata Kadar kuersetin
n
X = ∑i=1 Xi / n
= 0.2501+ 0.2615+ 0.3056+ 0.3058+ 0.3483
5 = 0.2943%
- Standar Deviasi kadar kuersetin
�� = (xi-x ) 2
n - 1 = 0.0394
- Simpangan baku Relatif
SBR= ��
x × 100 =
0.0394
27
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 12 Desember 1990 dari M. Panggabean (Alm) dan Hamidah Hamjah (Almh). Penulis adalah putri kedua dari dua bersaudara. Tahun 2008, penulis lulus dari SMA Negeri 2 Bekasi dan pada tahun yang sama penulis lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui jalur Seleksi Nasional Mahasiswa Baru Perguruan Tinggi Negeri (SNMPTN) dan diterima di Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, penulis menjadi asisten praktikum Kimia Tingkat Persiapan Bersama (TPB) pada tahun 2009-2012, asisten Praktikum Kimia Analitik Ekstensi pada tahun 2010/2011, serta asisten Kimia Bahan Alam Ekstensi pada tahun ajaran 2011/2012. Penulis juga aktif dalam organisasi Ikatan Mahasiswa Kimia (Imasika) tahun ajaran 2010/2011 dan juga 2011/2012 serta
kepanitiaan lainnya. Bulan Juli-Agustus 2011 penulis berkesempatan
melaksanakan kegiatan Praktik Lapangan di Pusat Penelitian dan Pengembangan Keteknikan Kehutanan dan Pengolahan Hasil Hutan dengan judul laporan
“Pembuatan Biodiesel dari Minyak Biji Bintaro (Cerbera manghas) dengan