STUDI PERBANDINGAN PEMANFAATAN JERUK NIPIS,
ASAM CUKA, DAN ASAM JAWA DALAM PENGIKATAN
PLUMBUM (Pb) PADA CUMI-CUMI
DI PERAIRAN BELAWAN
SKRIPSI
OLEH:
STEPHANIE DEBORA NIM 060804047
FAKULTAS FARMASI
STUDI PERBANDINGAN PEMANFAATAN JERUK NIPIS,
ASAM CUKA, DAN ASAM JAWA DALAM PENGIKATAN
PLUMBUM (Pb) PADA CUMI-CUMI
DI PERAIRAN BELAWAN
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
STEPHANIE DEBORA NIM 060804047
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
STUDI PERBANDINGAN PEMANFAATAN JERUK NIPIS,
ASAM CUKA, DAN ASAM JAWA DALAM PENGIKATAN
PLUMBUM (Pb) PADA CUMI-CUMI
DI PERAIRAN BELAWAN
OLEH:
STEPHANIE DEBORA NIM 060804047
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sumatera Utara Pada tanggal: Agustus 2010
Pembimbing I, Panitia Penguji,
Drs. Maralaut Batubara, M.Phill., Apt. Drs. Chairul Azhar Dalimunthe, M.Sc., Apt. NIP 195101311976031003 NIP 194907061980021001
Pembimbing II, Drs. Maralaut Batubara, M.Phill., Apt. NIP 195101311976031003
Drs. Muchlisyam, M.Si., Apt. Dra. Tuty Roida Pardede, M.Si., Apt. NIP 195006221980021001 NIP 195401101980032001
Drs. Immanuel S. Meliala, M.Si., Apt. NIP 195001261983031002
Dekan,
KATA PENGANTAR Salam damai sejahtera,
Puji syukur pada Tuhan Yesus Kristus atas berkat anugerah dan kasih
setia-Nya, hingga penulis dapat menjalani masa perkuliahan dan penelitian hingga
akhirnya menyelesaikan penyusunan skripsi ini untuk mencapai gelar Sarjana
Farmasi di Fakultas Farmasi di Fakultas Farmasi Universitas Sumatera Utara.
Ucapan terima kasih yang tulus tiada terhingga penulis sampaikan kepada
kedua orangtua tercinta, Ayahanda D.L. Gultom dan Ibunda Dj. R. Sinaga, juga
kepada kakakku Emma Novica Gultom, dan adikku Arian Ardianto Gultom, juga
seseorang yang kukasihi, bang Adolf King Simatupang, beserta seluruh keluarga
besar yang senantiasa memberikan motivasi, dukungan, perhatian, semangat, dan
doa kepada penulis selama perkuliahan hingga penyelesaian skripsi ini.
Penulis juga mengucapkan terima kasih yang sebesar-besarnya kepada
Bapak Drs. Maralaut Batubara, M.Phill., Apt. dan Bapak Drs. Muchlisyam,
M.Si., Apt., selaku dosen pembimbing yang telah membimbing penulis dengan
penuh kesabaran, ketulusan, dan keikhlasan selama melakukan penelitian hingga
selesainya penulisan skripsi ini.
Ucapan terimakasih juga disampaikan kepada:
1. Dekan Fakultas Farmasi USU, Prof. Dr. Sumadio Hadisahputra, Apt., yang
telah memberikan bantuan dan fasilitas selama masa pendidikan.
2. Bapak Drs. Chairul Azhar Dalimunthe, M.Sc., Apt., Ibu Dra. Tuty Roida
Pardede, M.Si., Apt., dan Bapak Drs. Immanuel S. Meliala, M.Si., Apt.,
sebagai tim penguji yang sangat banyak memberikan masukan dan saran
3. Bapak Drs. Salim Usman, M.Si, Apt., selaku dosen wali serta seluruh dosen
staf pengajar Fakultas Farmasi yang telah banyak membimbing dan mendidik
penulis selama masa perkuliahan hingga selesai.
4. Ibu Dra. Masfria, M.S., Apt., selaku Kepala Laboratorium Kimia Farmasi
Kualitatif dan Bapak Drs. Maralaut Batubara, M.Phill., Apt., selaku Kepala
Laboratorium Kimia Bahan Makanan yang telah membantu dan menyediakan
fasilitas kepada penulis selama melakukan penelitian.
5. Sahabat-sahabat terbaikku, “Christian Pharmacy ’06”, yaitu Lia, Apri, Dina,
Abeth, Ruth, Mastin, Deni, Leli, Wati, Wina, Cyan, Jandri, Roni, Jhon,
Gokman, teman-teman seperjuangan Farmasi ’06, kakak dan abang senior
Farmasi, adik-adik junior Farmasi, serta semua pihak yang tidak dapat
disebutkan satu persatu yang telah banyak membantu penulis hingga
selesainya penulisan skripsi ini.
Semoga Tuhan Yesus memberikan balasan yang berlipat ganda atas segala
kebaikan dan bantuan yang telah diberikan kepada penulis.
Akhir kata penulis menyadari bahwa tulisan ini masih belum sempurna.
Untuk itu penulis mengharapkan kritik dan saran yang membangun. Semoga
skripsi ini dapat memberikan sumbangan yang bermanfaat bagi ilmu pengetahuan
khususnya bidang farmasi.
Medan, Agustus 2010
Penulis,
Studi Perbandingan Pemanfaatan Jeruk Nipis, Asam Cuka, dan Asam Jawa dalam Pengikatan Plumbum (Pb)
pada Cumi-Cumi di Perairan Belawan
Abstrak
Cumi-cumi di perairan Belawan dinyatakan telah tercemar oleh logam
berat plumbum (Pb). Untuk mengatasi dampak toksik dari logam berat ini,
diperlukan upaya untuk menurunkan kadar plumbum (Pb) dalam cumi-cumi.
Tujuan penelitian ini adalah untuk memeriksa pengaruh berbagai larutan
perendam sebagai upaya menurunkan kandungan logam berat Pb. Penetapan
kadar dilakukan sebelum dan sesudah perendaman dengan menggunakan jeruk
nipis, asam cuka, dan asam jawa.
Kandungan Pb pada cumi-cumi ditetapkan dengan analisis kualitatif dan
kuantitatif. Analisis kualitatif dilakukan dengan pereaksi ditizon 0,005% pada pH
7 dimana akan terbentuk warna merah tua. Sedangkan analisis kuantitatif
dilakukan dengan metode Spektrofotometri Serapan Atom Elektrotermal pada
panjang gelombang 217, 0 nm.
Hasil analisis menunjukkan kadar Pb setelah dilakukan perendaman
dengan menggunakan jeruk nipis selama 30 menit dan 60 menit mengalami
penurunan masing-masing sebesar 72,06% dan 70,61% untuk metode destruksi
basah dan 74,47% dan 74,04% untuk metode destruksi kering, dengan asam cuka
selama 30 menit dan 60 menit mengalami penurunan masing-masing sebesar
75,00% dan 75,06% untuk metode destruksi basah dan 76,99% dan 77,31% untuk
metode destruksi kering, dan dengan asam jawa selama 30 menit dan 60 menit
mengalami penurunan masing-masing sebesar 71,92 % dan 72,47 % untuk metode
destruksi basah dan 74,71 % dan 74,47 % untuk metode destruksi kering.
Perendaman cumi-cumi dalam jeruk nipis, asam cuka, maupun asam jawa
efektif menurunkan kadar logam timbal (Pb) dalam cumi-cumi yang berasal dari
perairan Belawan.
Comparative Study of Utilization of Lime, Acetic Acid, and Tamarind for Bind Plumbum (Pb) content
in squids from Belawan Waters
Abstract
Squids in the waters of Belawan obviously have been contaminated by
heavy metals plumbum (Pb). To keep down the toxic effects of this heavy metals,
it’s necessary do the efforts to reduce levels of plumbum (Pb) in squids. The
purpose of this study was to examine the effect of various soaking solution as the
effort to reduce Pb heavy metals content. Assay is carried out before and after
soaking by using lime, acetic acid, and tamarind.
Determination of Pb was done by qualitative and quantitative analysis. The
qualitative analysis by using dithizon 0.005% at pH 7 which will be formed deep
red colour. While the quantitative analysis was done by using Electrothermal
Atomic Absorption Spectrophotometry method at wavelengths of 217, 0 nm.
The results show levels of lead after soaking by using lime for 30 minutes
and 60 minutes respectively decreased by 72.06% and 70.61% for the wet
digestion method and 74.47% and 74.04% for the dry ashing method, with acetic
acid for 30 minutes and 60 minutes respectively decreased by 75.00% and 75.06%
for the wet digestion method and 76.99% and 77.31% for dry ashing method, and
tamarind for 30 minutes and 60 minutes respectively decreased by 71.92% and
72.47% for the wet digestion method and 74.71% and 74.47% for dry ashing
method.
Thus soaking squid in lime, acetic acid, and tamarind are effectively
reduce levels of lead (Pb) in the squid from Belawan waters.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Cumi-cumi ... 5
2.2 Pencemaran laut ... 6
2.3 Timbal (Pb) ... 6
2.4 Uraian Jeruk Nipis ... 7
2.5 Asam Cuka ... 8
2.7 Pengikatan Logam ... 9
2.8 Metode destruksi ... 10
2.8.1 Destruksi Basah ... 10
2.8.2 Destruksi Kering ... 11
2.9 Spektrofotometri Serapan Atom ... 11
2.10 Validasi Metode Analisis ... 13
2.10.1 Kecermatan (accuracy) ... 13
2.10.2 Keseksamaan (precision) ... 14
2.10.3 Batas Deteksi ... 14
2.10.4 Batas Kuantitasi ... 14
BAB III METODOLOGI PENELITIAN ... . 15
3.1 Lokasi Penelitian ... 15
3.2 Bahan-bahan ... 15
3.2.1 Sampel ... 15
3.2.2 Pereaksi ... 15
3.3 Alat-alat ... 16
3.4 Pembuatan Pereaksi ... 16
3.5 Prosedur Penelitian ... 17
3.5.1 Pengambilan Sampel ... 17
3.5.2 Penyiapan Sampel ... 17
3.5.3 Proses Destruksi ... 18
3.5.3.1 Proses Destruksi Kering ... 18
3.5.3.2 Proses Destruksi Basah ... 18
3.5.5 Analisis Kuantitatif ... 19
3.5.5.1 Penentuan Panjang Gelombang Maksimum ... 19
3.5.5.2 Penentuan Linieritas Kurva Kalibrasi Logam Plumbum (Pb) ... 19
3.5.5.3 Penentuan Kadar Plumbum (Pb) dalam Cumi-cumi ... 20
3.5.5.4 Uji Perolehan Kembali ... 20
3.5.5.4.1 Pembuatan Larutan Standar ... 20
3.5.5.4.2 Prosedur Uji Perolehan Kembali ... 21
. 3.5.5.5 Analisis Data Secara Statistik ... 21
3.5.5.6 Penentuan Batas Deteksi dan Batas Kuantitasi ... 22
3.5.6 Bagan Penyiapan Sampel ... 24
3.5.7 Bagan Destruksi Kering ... 26
3.5.8 Bagan Destruksi Basah ... 27
BAB IV HASIL DAN PEMBAHASAN ... 28
4.1 Hasil Uji Kualitatif ... 28
4.2 Hasil Uji Kuantitatif ... 29
4.2.1 Kurva Kalibrasi Logam Plumbum (Pb) ... 29
4.2.2 Analisis Kadar Plumbum (Pb) dalam Cumi-cumi ... 30
4.2.3 Hasil Penurunan Kadar Plumbum (Pb) Setelah Perendaman dalam Air Perasan Jeruk Nipis, Asam Cuka, dan Larutan Asam Jawa ... 31
4.2.4.1 Analisis Beda Nilai Rata-rata Penurunan Kadar Plumbum (Pb) pada Cumi-cumi dengan
Perendaman dalam Jeruk Nipis,
Asam Cuka, dan Asam Jawa ... 34
4.2.4.2 Analisis Beda Nilai Rata-rata Kadar Plumbum (Pb) pada Cumi-cumi dengan Perbedaan Waktu Perendaman ... 35
4.2.4.3 Analisis Beda Nilai Rata-rata Kadar Plumbum (Pb) pada Cumi-cumi antara Metode Destruksi Basah dan Metode Destruksi Kering ... 36
4.2.5 Uji Perolehan kembali ... 37
4.2.6 Batas Deteksi dan Batas Kuantitasi ... 37
BAB V KESIMPULAN DAN SARAN ... 39
5.1 Kesimpulan ... 39
5.2 Saran ... 39
DAFTAR PUSTAKA ... . 41
DAFTAR TABEL Halaman
Tabel 1. Hasil Uji Kualitatif Logam Plumbum (Pb)
dengan Pereaksi Dithizon 0,005%b/v ... 28
Tabel 2. Data Kadar Logam Plumbum (Pb) ... 30
Tabel 3. Persen Penurunan Kadar Plumbum (Pb)
Setelah Perendaman dalam Air Perasan Jeruk Nipis,
Asam Cuka, dan Larutan Asam Jawa ... 31
Tabel 4. Kadar Plumbum (Pb) pada Cumi-cumi setelah Perendaman dalam Jeruk Nipis, Asam Cuka, dan Asam Jawa
Selama 30 menit dan 60 menit ... 35
Tabel 5. Persen Uji Perolehan Kembali (Recovery)
DAFTAR GAMBAR
Halaman
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Data Hasil Pengukuran Absorbansi Larutan Standar
Plumbum (Pb) ... 44
Lampiran 2. Contoh Perhitungan Persamaan Regresi Plumbum (Pb) ... 45
Lampiran 3. Hasil Analisis Plumbum (Pb) dalam Cumi-cumi ... 46
Lampiran 4. Contoh Perhitungan Kadar Plumbum (Pb) dalam Cumi-cumi ... 51
Lampiran 5. Perhitungan Statistik Kadar Plumbum (Pb) pada Cumi-cumi ... 52
Lampiran 6. Pengujian Beda Nilai Rata-rata Kadar Plumbum (Pb) pada Cumi-cumi dengan Perendaman dalam Jeruk Nipis, Asam Cuka, dan Asam Jawa ... 68
Lampiran 7. Data Hasil Uji Perolehan Kembali Plumbum (Pb) pada Cumi-cumi ... 70
Lampiran 8. Contoh Perhitungan Uji Perolehan Kembali Plumbum (Pb) dalam Cumi-cumi ... 71
Lampiran 9. Perhitungan Batas Deteksi dan Batas Kuantitasi Plumbum (Pb) ... 72
Lampiran 10. Gambar Hasil Analisa Kualitatif Logam Plumbum (Pb) dengan Pereaksi Ditizon 0,005% b/v ... 73
Lampiran 11. Gambar Perairan Belawan ... 75
Lampiran 12. Gambar Cumi-cumi ... 75
Lampiran 13. Gambar Buah Jeruk Nipis ... 76
Lampiran 14. Gambar Asam Cuka ... 76
Lampiran 15. Gambar Asam Jawa ... 76
Lampiran 16. Gambar Alat Spektrofotometer Serapan Atom Graphite Furnace ... 77
Lampiran 18. Daftar Nilai Distribusi-t ... 78
Lampiran 19. Daftar Nilai Distribusi F
pada tingkat 5% dengan α= 0,05 ... 78
Lampiran 20. Hasil pengukuran Pb dalam Sampel ... 79
Lampiran 21. Hasil pengukuran Pb dalam Sampel
secara Destruksi Basah ... 82
Lampiran 22. Hasil pengukuran Pb dalam Sampel
secara Destruksi Kering ... 83
Lampiran 23. Hasil pengukuran Pb dalam Sampel Setelah Ditambahkan
Studi Perbandingan Pemanfaatan Jeruk Nipis, Asam Cuka, dan Asam Jawa dalam Pengikatan Plumbum (Pb)
pada Cumi-Cumi di Perairan Belawan
Abstrak
Cumi-cumi di perairan Belawan dinyatakan telah tercemar oleh logam
berat plumbum (Pb). Untuk mengatasi dampak toksik dari logam berat ini,
diperlukan upaya untuk menurunkan kadar plumbum (Pb) dalam cumi-cumi.
Tujuan penelitian ini adalah untuk memeriksa pengaruh berbagai larutan
perendam sebagai upaya menurunkan kandungan logam berat Pb. Penetapan
kadar dilakukan sebelum dan sesudah perendaman dengan menggunakan jeruk
nipis, asam cuka, dan asam jawa.
Kandungan Pb pada cumi-cumi ditetapkan dengan analisis kualitatif dan
kuantitatif. Analisis kualitatif dilakukan dengan pereaksi ditizon 0,005% pada pH
7 dimana akan terbentuk warna merah tua. Sedangkan analisis kuantitatif
dilakukan dengan metode Spektrofotometri Serapan Atom Elektrotermal pada
panjang gelombang 217, 0 nm.
Hasil analisis menunjukkan kadar Pb setelah dilakukan perendaman
dengan menggunakan jeruk nipis selama 30 menit dan 60 menit mengalami
penurunan masing-masing sebesar 72,06% dan 70,61% untuk metode destruksi
basah dan 74,47% dan 74,04% untuk metode destruksi kering, dengan asam cuka
selama 30 menit dan 60 menit mengalami penurunan masing-masing sebesar
75,00% dan 75,06% untuk metode destruksi basah dan 76,99% dan 77,31% untuk
metode destruksi kering, dan dengan asam jawa selama 30 menit dan 60 menit
mengalami penurunan masing-masing sebesar 71,92 % dan 72,47 % untuk metode
destruksi basah dan 74,71 % dan 74,47 % untuk metode destruksi kering.
Perendaman cumi-cumi dalam jeruk nipis, asam cuka, maupun asam jawa
efektif menurunkan kadar logam timbal (Pb) dalam cumi-cumi yang berasal dari
perairan Belawan.
Comparative Study of Utilization of Lime, Acetic Acid, and Tamarind for Bind Plumbum (Pb) content
in squids from Belawan Waters
Abstract
Squids in the waters of Belawan obviously have been contaminated by
heavy metals plumbum (Pb). To keep down the toxic effects of this heavy metals,
it’s necessary do the efforts to reduce levels of plumbum (Pb) in squids. The
purpose of this study was to examine the effect of various soaking solution as the
effort to reduce Pb heavy metals content. Assay is carried out before and after
soaking by using lime, acetic acid, and tamarind.
Determination of Pb was done by qualitative and quantitative analysis. The
qualitative analysis by using dithizon 0.005% at pH 7 which will be formed deep
red colour. While the quantitative analysis was done by using Electrothermal
Atomic Absorption Spectrophotometry method at wavelengths of 217, 0 nm.
The results show levels of lead after soaking by using lime for 30 minutes
and 60 minutes respectively decreased by 72.06% and 70.61% for the wet
digestion method and 74.47% and 74.04% for the dry ashing method, with acetic
acid for 30 minutes and 60 minutes respectively decreased by 75.00% and 75.06%
for the wet digestion method and 76.99% and 77.31% for dry ashing method, and
tamarind for 30 minutes and 60 minutes respectively decreased by 71.92% and
72.47% for the wet digestion method and 74.71% and 74.47% for dry ashing
method.
Thus soaking squid in lime, acetic acid, and tamarind are effectively
reduce levels of lead (Pb) in the squid from Belawan waters.
BAB I PENDAHULUAN
1.1. Latar Belakang
Perairan laut Belawan dinyatakan telah tercemar oleh logam berat. PT.
Pelabuhan Indonesia I melaporkan bahwa logam Pb, Cd, dan Hg yang merupakan
logam berat yang toksik dalam perairan Belawan telah melewati ambang batas
(Laporan Pemantau Pelindo I, 2004). Pada air laut di lautan lepas kontaminasi
logam biasanya terjadi secara langsung dari atmosfer atau karena tumpahan
minyak dari kapal tanker yang melewatinya, juga berasal dari pertambangan,
peleburan logam, dan jenis industri lainnya (Darmono, 2001).
Cumi-cumi yang termasuk dalam kelas Cephalopoda merupakan
kelompok yang tertinggi tingkat evolusinya di antara mollusca. Tubuh simetri
bilateral, dengan sebuah kaki yang terbagi menjadi lengan-lengan yang dilengkapi
alat penghisap dan sistem saraf yang berkembang baik terpusatkan di kepala.
Cumi-cumi mempunyai pandangan mata yang sangat bagus, berenang dengan
cepat, dan dapat merayap di dasar atau berenang di dekat dasar (Romimohtarto,
2001). Berdasarkan pola hidupnya tersebut, yaitu habitat maupun faktor
makanannya, cumi-cumi dapat dijadikan sebagai salah satu bioindikator yang
digunakan untuk mengetahui besarnya pencemaran yang terjadi dalam lingkungan
habitatnya.
Penelitian sebelumya telah menyatakan bahwa cumi-cumi sebagai salah
satu biota laut yang berasal dari perairan laut Belawan telah tercemar logam
plumbum (Pb) (Mariadi, 2007). Padahal kita ketahui bawa cumi-cumi merupakan
diperdagangkan di banyak pasar di Indonesia dan mempunyai nilai ekonomi
(Romimohtarto,2001).
Logam Pb merupakan salah satu logam yang banyak dimanfaatkan dalam
kehidupan manusia dibanding logam toksik lainnya dikarenakan logam ini
memiliki sifat-sifat yang khusus, seperti sifatnya yang lunak, tahan terhadap
korosi, titik lebur rendah, serta bahan isolator yang baik (Palar, 2008). Di
antaranya digunakan pada industri baterai, kabel, penyepuhan, pestisida, antiletup
pada bensin, zat penyusun solder, dan sebagai formulasi penyambung pipa
(Widowati,2008). Akibatnya buangan (limbah) dari industri tersebut akan jatuh
pada jalur-jalur perairan seperti anak-anak sungai, kemudian akan dibawa terus
menuju lautan, sehingga akan merusak serta mencemari lingkungan perairan yang
dimasukinya (Palar, 2008).
Meskipun jumlah Pb yang diserap oleh tubuh hanya sedikit, logam ini
ternyata menjadi sangat berbahaya karena dapat merusak perkembangan otak pada
anak-anak, menyebabkan penyumbatan sel-sel darah merah, anemia, dan
mempengaruhi anggota tubuh lainnya (Purnomo, 2009). Proses masuknya Pb ke
dalam tubuh dapat melalui beberapa jalur, yaitu melalui makanan dan minuman,
udara dan perembesan atau penetrasi pada selaput atau lapisan kulit (Palar, 2008).
Logam Pb yang telah masuk ke dalam tubuh dapat mengikat gugus aktif
yang esensial bagi tubuh. Namun dengan adanya suatu senyawa kimia tertentu
yang mampu berikatan dengan suatu logam dan membentuk kompleks, maka
dampak toksik logam dapat dihindarkan (Pudjiadi, 2000). Senyawa kimia ini
mempunyai gugus karboksilat dan hidroksil sehingga dapat dimanfaatkan sebagai
chelating agent (Manahan, 1977).
Beberapa penelitian mengenai pengikatan logam telah dilakukan antara
lain dengan menggunakan jeruk nipis pada udang windu (Armanda, 2009), asam
jawa pada ikan tongkol (Permata, 2009), serta asam cuka pada kerang bulu
(Pertiwi, 2008).
Berdasarkan uraian di atas, peneliti tertarik untuk melakukan penelitian
perbandingan penurunan kadar logam berat Pb pada cumi-cumi dengan
penambahan jeruk nipis, asam cuka dan asam jawa dengan perbedaan waktu
perendaman. Selain itu, pengolahan sampel dilakukan dengan dua metode, yaitu
metode destruksi basah dan destruksi kering. Hal ini dimaksudkan agar diketahui
metode mana yang lebih efisien dalam penetapan kadar logam. Dari penelitian ini
diharapkan dapat ditemukan perlakuan yang paling baik dalam upaya penurunan
kadar Pb dalam cumi-cumi dengan menggunakan jeruk nipis, asam jawa, dan
asam asetat yaitu dengan cara mudah, sederhana dan efektif sehingga dapat
disosialisasikan kepada masyarakat umum khususnya ibu rumah tangga dan
penjual seafood sehingga dampak pemaparan logam berat Pb dapat hindari.
1.2 Perumusan Masalah
1. Apakah ada perbedaan penurunan kadar plumbum (Pb) pada cumi-cumi
dengan menggunakan jeruk nipis, asam cuka, dan asam jawa ?
2. Apakah proses destruksi mempengaruhi penetapan kadar plumbum (Pb)
pada cumi-cumi ?
3. Apakah perbedaan waktu perendaman memberikan pengaruh yang
1.3 Hipotesis Ho diterima jika:
1. Penurunan kadar plumbum (Pb) pada cumi-cumi dengan menggunakan
larutan jeruk nipis, asam cuka, dan asam jawa tidak berbeda.
2. Proses destruksi tidak mempengaruhi kadar plumbum (Pb) pada
cumi-cumi.
3. Perbedaan waktu perendaman memberikan pengaruh yang berbeda
terhadap penurunan kadar plumbum (Pb) dalam cumi-cumi.
1.4 Tujuan Penelitian
1. Melakukan penurunan kadar plumbum (Pb) dalam cumi-cumi dengan
mempergunakan jeruk nipis, asam cuka, dan asam jawa.
2. Melakukan proses destruksi kering dan destruksi basah terhadap sampel
hasil perendaman dengan jeruk nipis, asam cuka, dan asam jawa.
3. Melakukan penurunan kadar plumbum (Pb) setelah perendaman dalam
larutan jeruk nipis, asam cuka, dan asam jawa dengan waktu perendaman
yang berbeda.
1.5 Manfaat Penelitian
Hasil penelitian ini dapat dimanfaatkan oleh masyarakat untuk
menurunkan kadar logam berat dalam proses pengolahan makanan, terutama
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Cumi-cumi (Anonim, 2005) Klasifikasi Ilmiah
Kerajaan : Animalia
Filum : Mollusca
Kelas : Cephalopoda
Subkelas : Coleoidea
Ordo : Teuthoidea
Famili : Loliginidae
Genus : Loligo
Spesies : Loligo pealii
Nama Daerah : Cumi-cumi
Bentuk cumi-cumi umumnya memanjang dan ditutupi oleh mantel yang
mempunyai dua sirip segitiga, dapat tetap bergerak dalam satu tempat atau
bergerak mundur atau maju hanya dengan mengubah arah sifon. Hewan ini
memiliki delapan lengan dan dua tentakel panjang yang pada bagian ujungnya
dilengkapi dengan mangkuk penghisap yang bertangkai. Alat ini dapat dengan
cepat mengarah ke mangsa untuk dapat ditangkap. Hewan ini pada umumnya
memakan ikan-ikan kecil. Pada bagian bawah kulitnya terdapat sebuah cangkang
yang ringan dan transparan berbentuk pena yang terbuat dari kitin (Castro, 2005).
Ukuran cumi-cumi dewasa bervariasi dari ukuran kecil yaitu sekitar 13 cm
panjangnya, atau yang lebih panjang lagi sekitar 0,5 hingga 1 meter, hingga
Architeuthis. Hewan ini dapat mencapai panjang hingga 18 m dan berat hingga
4,4 ton. Sedangkan tentakelnya dapat mencapai panjang hingga 10 meter dan
diameter tubuhnya kira-kira 3,5 meter. Biasanya hewan ini hidup pada laut dengan
kedalaman 300-600 meter (Webber, 1991).
2.2 Pencemaran laut
Salah satu kontaminan kimia dari lautan di dunia ini adalah logam,
terutama yang diklasifikasikan sebagai logam berat. Sangat sedikit dari beberapa
logam yang diperlukan sebagai nutrisi penting bagi tubuh makhluk hidup, dan
apabila kelebihan justru dapat bersifat racun (Castro, 2005).
Salah satu logam berat yang sangat mengganggu yang dibawa ke laut
sebagai polutan beracun adalah logam timbal. Timbal adalah salah satu logam
yang paling luas tersebar. Timbal adalah racun bagi manusia, menyebabkan
gangguan saraf dan bahkan kematian. Sumber utama pencemaran laut yang
menghasilkan timbal adalah sisa pembuangan dari kendaraan laut berbahan bakar
timbal. Logam ini dapat sampai ke air melalui hujan dan debu. Timbal juga dapat
ditemukan dari berbagai macam produk, seperti cat dan keramik, yang akhirnya
terbawa ke laut (Castro, 2005).
2.3 Timbal (Pb)
Timbal (Pb) adalah logam lunak berwarna abu-abu kebiruan mengkilat,
memiliki titik lebur rendah dan mudah dibentuk. Logam ini dapat digunakan
untuk melapisi logam agar tidak timbul perkaratan. Timbal meleleh pada suhu
328o C dan mendidih pada suhu 1740o C (Widowati, 2008). Timbal larut dalam
Logam Pb digunakan dalam industri baterai, kabel, penyepuhan, pestisida,
sebagai zat antiletup pada bensin, zat penyusun patri atau solder, dan sebagai
formulasi penyambung pipa sehingga memungkinkan terjadinya kontak antara air
rumah tangga dengan Pb (Widowati,2008).
Timbal bersifat toksik pada manusia, intoksikasi terjadi melalui jalur oral,
lewat makanan, minuman, pernafasan, lewat kulit, lewat mata, dan lewat
parenteral. Orang dewasa mengabsorpsi Pb sebesar 5-15 % dari keseluruhan Pb
yang dicerna, sedangkan anak-anak mengabsorpsi Pb lebih besar, yaitu 41,5 %.
Toksisitas Pb berpengaruh terhadap biosintesa hem, sistem kardiovaskuler,
respirasi, syaraf, gastrointestinal, urinaria, endokrin, reproduksi, dan berperan
sebagai kofaktor dalam proses karsinogenesis (Widowati, 2008).
Sebagian kecil Pb dieksresikan lewat urin atau feses karena sebagian
terikat oleh protein. Sedangkan sebagian lagi terakumulasi dalam ginjal, hati,
kuku, jaringan lemak, dan rambut. Tingkat ekskresi Pb melalui sistem urinaria
adalah sebesar 76%, gastrointestinal 16%, dan rambut, kuku, serta keringat
sebesar 8% (Widowati, 2008).
2.4 Uraian Jeruk Nipis (Adina, 2008) Kerajaan : Plantae
Divisi : Spermatophyta
Subdivisi : Angiospermae
Kelas : Dicotyledonae
Ordo : Rutales
Famili : Rutaceae
Spesies : Citrus aurantiifolia Swingle
Sinonim : Limonia aurantifolia Christm., Limon spinosum Mill., Citrus
limonia Osbeck, Citrus lima Luman, Citrus spinosissima
G.F.W. Meyer, Citrus acida Roxb., Citrus aurantium
Sekuesteran adalah bahan tambahan makanan yang dapat mengikat ion
logam yang ada dalam makanan. Sekuesteran dapat mengikat logam dalam bentuk
ikatan kompleks sehingga dapat mengalahkan sifat dan pengaruh jelek logam
tersebut dalam bahan. Ligan atau sekuesteran dapat berupa senyawa organik
seperti asam sitrat (Meronda, 2008).
Asam sitrat merupakan asam organik lemah yang ditemukan pada daun
dan buah tumbuhan genus Citrus (jeruk-jerukan). Ion sitrat dapat bereaksi dengan
banyak ion logam membentuk garam sitrat (Anonim, 2010).
2.5 Asam Cuka
Upaya menghilangkan atau menurunkan kadar logam berat dalam biota
laut yaitu dengan menggunakan chelating agent. Salah satu penelitian
membuktikan bahwa penggunaan chelating agent yaitu asam asetat mampu
menurunkan kadar Pb pada biota laut (Agustini, 2008).
Larutan asam cuka merupakan larutan yang yang digunakan sebagai bahan
tambahan makanan yaitu sebagai pengasam, pengawet, dan juga penyedap
makanan yang mempunyai kemampuan mengikat logam sehingga dapat
menurunkan kadar logam berat pada biota laut sebelum pengolahan menjadi
2.6 Asam Jawa (Anonim, 2009) Kerajaan : Plantae
Divisi : Magnoliophyta
Kelas : Magnoliopsida
Ordo : Fabales
Famili : Fabaceae (Leguminosae)
Genus : Tamarindus
Spesies : Tamarindus indica Linn
Buah polong asam jawa mengandung senyawa kimia antara lain asam
appel, asam sitrat, asam tartrat, asam suksinat, pektin, dan gula invert (Anonim,
2009).
Kegunaan buah asam jawa antara lain digunakan dalam aneka bahan
masakan atau bumbu, memberikan rasa asam atau untuk menghilangkan bau amis
ikan, sebagai bahan sirup, selai, gula-gula, dan jamu. Sedangkan khasiat dari asam
jawa ialah dapat mengobati penyakit seperti asma, batuk, demam, sakit panas,
reumatik, sakit perut, alergi/biduran, sariawan, luka, eksim, bisul, bengkak
disengat lipan/lebah, serta gigitan ular berbisa (Anonim, 2009).
2.7 Pengikatan Logam
Logam-logam pada umumnya dapat membentuk ikatan dengan
bahan-bahan organik alam maupun bahan-bahan-bahan-bahan organik buatan. Proses pembentukan
ikatan tersebut dapat terjadi melalui pembentukan garam organik dengan gugus
karboksilat seperti misalnya asam sitrat, tartrat, dan lain-lain. Di samping itu,
logam dapat berikatan dengan atom-atom yang mempunyai elektron bebas dalam
Senyawa kimia tertentu yang mampu membentuk ikatan koordinasi
dengan logam melalui dua atau lebih atom disebut chelating agent (chelator).
Senyawa yang dibentuk oleh chelator dan logam disebut khelat (Anonim, 2009).
2.8 Metode destruksi
Untuk menentukan kandungan mineral bahan harus dihancurkan atau
didestruksi dulu. Cara yang biasa dilakukan yaitu pengabuan kering (dry ashing)
dan pengabuan basah (wet digestion). Pemilihan cara tersebut tergantung pada
sifat zat organik dalam bahan, mineral yang akan dianalisa serta sensitivitas cara
yang digunakan (Apriantono, 1989).
2.8.1 Destruksi Basah
Teknik destruksi basah adalah dengan memanaskan sampel organik
dengan penambahan asam mineral pengoksidasi atau campuran dari asam-asam
mineral tersebut. Penambahan asam mineral pengoksidasi dan pemanasan dapat
mengoksidasi sampel secara sempurna, sehingga menghasilkan ion logam dalam
larutan asam sebagai sampel anorganik untuk dianalisis selanjutnya. Destruksi
basah biasanya menggunakan H2SO4, HNO3, dan HClO4 atau campuran dari
ketiga asam tersebut (Anderson, 1987).
Pengabuan basah memberikan benerapa keuntungan. Suhu yang digunakan
tidak dapat melebihi titik didih larutan dan pada umumnya karbon lebih cepat
hancur daripada menggunakan cara pengabuan kering. Cara pengabuan basah
pada prinsipnya adalah penggunaan asam nitrat untuk mendestruksi zat organik
pada suhu rendah dengan maksud menghindari kehilangan mineral akibat
2.8.2 Destruksi Kering
Destruksi basah merupakan sebuah prosedur dimana sampel yang telah
diketahui beratnya diletakkan pada sebuah krus, lalu ke sebuah tanur yang
dipanaskan pada suhu tertentu. Krus umumya terbuat dari platinum dan juga
tersedia krus yang terbuat dari perselen, silika, besi, dan nikel (Chapple, 1991).
Perhatian harus diberikan pada saat melakukan destruksi kering karena ada
tiga kemungkinan sumber kehilangan unsur tertentu seperti:
- Kehilangan mekanis pada saat pengeringan sampel, misalnya jika sampel
dikeringkan dengan sangat cepat, tejadi kehilangan zat dari krus. Dengan
demikian untuk mencegah hal ini terjadi, diperlukan proses pengeringan yang
relatif lambat
- Kehilangan zat pada saat penguapan sampel dalam tanur. Logam yang
memiliki titik uap yang rendah seperti Sb, Cr, Mo, Fe, Mg, Al, dll yang mana
akan mudah lepas saat pengabuan pada suhu 550o C.
- Penyerapan zat ke dalam krus dapat saja terjadi, kecuali pada wadah platinum.
Hal terburuk dapat terjadi apabila sampel mengandung logam halida atau
senyawa fospat (Chapple, 1991).
2.9 Spektrofotometri Serapan Atom
Spektrofotometri Serapan Atom digunakan untuk analisis kuantitatif
unsur-unsur logam dalam jumlah sekelumit (trace) dan sangat sekelumit (ultratrace).
Cara analisis ini memberikan kadar total unsur logam dalam suatu sampel dan
tidak tergantung pada bentuk molekul dari logam dalam sampel tersebut. Cara ini
cocok untuk analisis kelumit logam karena mempunyai kepekaan yang tinggi,
Metode spektrofotometri serapan atom berprinsip pada absorpsi energi
cahaya oleh atom- netral pada panjang gelombang tertentu tergantung pada sifat
unsurnya. Dengan menyerap suatu energi, maka atom akan memeperoleh energi
sehingga suatu atom pada keadaan dasar dapat ditingkatkan energinya ke tingkat
eksitasi (Khopkar, 1990).
Spektrofotometri Serapan Atom Elektrotermal pertama kali diperkenalkan
pada awal tahun 1970. Secara umum alat ini memiliki tingkat kesensitivan yang
tinggi karena seluruh sampel diatomisasi dalam periode yang singkat. Sensitivitas
dan batas deteksinya ialah 20 hingga 1000 kali lebih baik dibandingkan dengan
metode flame emission spectrophotometry (Berg, 1985). Selain itu volume sampel
yang dibutuhkan relatif sedikit, yaitu biasanya ± 0,5-10 μL. Sedangkan peralatan
yang dibutuhkan pada analisis elektrotermal ini adalah sama dengan peralatan
pada metode absorpsi nyala. Sebagian besar instrumen didesain secara modern
sehingga perubahan tipe atomisasi ke tipe lain merupakan persoalan yang relatif
mudah (Skoog, 1988).
Keuntungan dari penggunaan grafit furnis ini yaitu (Chapple, 1991):
- Sensitivitas yang tinggi
- Hanya membutuhkan volume sampel yang sedikit
- Penggunaan sampel yang efisien (tanpa pembuangan)
- Mencapai batas deteksi yang rendah
- Sebagian besar sampel dapat dianalisis dengan atau tanpa perlakuan.
Spektrofotometri Serapan Atom Elektrotermal didasari oleh prinsip yang
sama dengan Spektrofotometri Serapan Atom dengan nyala tetapi dilengkapi alat
burner. Penetapan kadar yaitu dengan cara pemanasan sampel terbagi dalam tiga
tahap, yaitu (Berg, 1985):
- pertama, pemanasan dengan suhu rendah pada tube untuk mengeringkan
sampel
- kedua, atau disebut dengan tahap pengarangan, menghancurkan bahan organik
dan menguapkan komponen matriks lainnya pada suhu medium
- terakhir, pemanasan dengan suhu tinggi pada tube atau pemijaran dengan
menggunakan gas inert sehingga terjadi atomisasi.
2.10 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap
parameter tertentu berdasarkan percobaan laboratorium untuk membuktikan
bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya. Beberapa
parameter analisis yang harus dipertimbangkan dalam validasi metode analisis
diuraikan dan didefinisikan sebagaimana cara penentuannya (Harmita, 2004).
Validasi dilakukan untuk menjamin bahwa metode analisis yang dilakukan akurat,
spesifik, reprodusibel, dan tahan pada kisaran analit yang akan dianalisis
(Rohman, 2007). Beberapa parameter validasi diuraikan di bawah ini:
2.10.1 Kecermatan (accuracy)
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil
analis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai
persen perolehan kembali (recovery) analit yang ditambahkan (Harmita, 2004).
Keterangan:
Cr = konsentrasi sampel yang diperoleh setelah penambahan larutan baku
Ca = konssentrasi sampel sebelum penambahan larutan baku
C = konsentrasi larutan baku yg ditambahkan
2.10.2 Keseksamaan (precision)
Keseksamaan adalah ukuran yang menunjukkan derajat kesesuaian antara
hasil uji individual, diukur melalui penyebaran hasil individual dari rata-rata jika
prosedur diterapkan secara berulang pada sampel-sampel yang diambil dari
campuran yang homogen (Harmita, 2004).
2.10.3 Batas Deteksi
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan. Batas ini dapat diperoleh
dari kalibrasi standar yang diukur sebanyak 6 sampai 10 kali. Batas deteksi dapat
dihitung dengan rumus sebagai berikut (Harmita, 2004):
Batas deteksi =
Keterangan: SB = simpangan baku
2.10.4 Batas Kuantitasi
Batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang
masih dapat memenuhi kriteria cermat dan seksama. Batas ini dapat diperoleh dari
kalibrasi standar yang diukur sebanyak 6 sampai 10 kali. Batas kuantitasi dapat
dihitung dengan rumus sebagai berikut (Harmita, 2004):
Batas kuantitasi =
BAB III
METODOLOGI PENELITIAN
Penelitian ini merupakan penelitian laboratorium eksperimental dengan
rancangan pre-test dan post-test untuk menganalisis perbedaan penurunan kadar
logam Pb dalam cumi-cumi (Loligo pealii) dengan metode destruksi basah dan
kering, serta dengan perbedaan waktu perendaman menggunakan asam jeruk
nipis, asam cuka, dan asam jawa.
3.1 Lokasi Penelitian
Penelitian dilakukan di empat lokasi yaitu penyiapan preparasi dilakukan
di Laboratorium Kimia Bahan Makanan Fakultas Farmasi dan Laboratorium
Kimia Farmasi Kualitatif Fakultas Farmasi, pengabuan sampel dilakukan di
Laboratorium Penelitian Fakultas MIPA, dan pengukuran kadar dengan
Spektrofotometer Serapan Atom dilakukan di salah satu perusahaan di Kawasan
Industri Medan (KIM).
3.2 Bahan-Bahan 3.2.1 Sampel
Sampel yang diperiksa dalam penelitian ini adalah cumi-cumi (Loligo
pealii) yang berasal dari perairan laut Belawan.
3.2.2 Pereaksi
Bahan yang digunakan semua pro analisis keluaran E. Merck, kecuali
disebutkan lain, yaitu asam nitrat 65%, ditizon 98%, amonium hidroksida 25%,
kristal kalium sianida, larutan standar timbal 1000 ppm, kloroform, dan air suling
3.3 Alat-alat
Alat- alat yang digunakan yaitu spektrofotometer serapan atom Graphite
Furnace (GBC Avanta G-GF 3000), lemari asam, hot plate (Favorit), neraca
analitik (AND GF-200), tanur (Ney M-525 Series II), pH indikator universal (E.
Merck), krus porselen 100 ml, blender, pisau stainless steel, spatula, botol kaca
100 ml, dan alat- alat gelas.
3.4 Pembuatan Pereaksi 1. Larutan HNO3 5N
Larutan HNO3 65% b/v sebanyak 350 ml diencerkan dengan air suling
hingga 1000 ml (Ditjen POM, 1979).
2. Larutan Ditizon 0,005% b/v
Difeniltiokarbazen (ditizon) sebanyak 5 mg dilarutkan dalam 100 ml
kloroform (Vogel, 1990).
3. Larutan NH4OH 1N
NH4OH 25% b/b sebanyak 7,4 ml diencerkan dalam 100 ml air suling
(Ditjen POM, 1995).
4. Air perasan Jeruk Nipis
Empat buah jeruk nipis diperas, lalu diencerkan dalam 400 ml air.
5. Larutan Asam Cuka 5 %
Asam cuka 15 % sebanyak 200 ml diencerkan dalam 600 ml air.
6. Larutan Asam Jawa
3.5 Prosedur Penelitian 3.5.1 Pengambilan sampel
Populasi penelitian adalah cumi-cumi yang dijual di daerah Pantai
Belawan. Pengambilan sampel dilakukan di TPI (Tempat Penampungan Ikan)
Bagan Deli-Belawan.
Metode pengambilan sampel dilakukan secara sampling purposif yang
dikenal juga sebagai sampling pertimbangan dimana pengambilan sampel
ditentukan berdasarkan asumsi bahwa semua jenis cumi-cumi yang dijual di
daerah Pantai Belawan adalah homogen tercemar logam berat timbal (Sudjana,
2005).
3.5.2 Penyiapan Sampel
Sampel berupa cumi-cumi segar yang dibuang cangkangnya. Kemudian
dicuci bersih dan ditimbang sebanyak 4 kg dan dibagi menjadi dua bagian. Bagian
pertama sebanyak 1 kg dan bagian kedua sebanyak 3 kg.
Bagian pertama (1 kg) ditiriskan selama 15 menit, kemudian diblender
hingga halus. Bagian kedua (3 kg) dibagi menjadi tiga bagian. Masing-masing
sebanyak 1 kg. Bagian pertama direndam dalam larutan jeruk nipis, bagian kedua
direndam dalam larutan asam cuka, dan bagian ketiga direndam dalam larutan
asam jawa.
Setelah perendaman selama 30 menit, masing-masing sampel yang telah
direndam dengan berbagai larutan asam tadi diambil sebanyak 500 gram, dicuci
bersih, lalu ditiriskan selama 15 menit. Setelah itu diblender hingga halus. Pada
waktu perendaman, setiap 5 menit sampel diaduk-aduk yang bertujuan agar
yang sama terhadap masing-masing sisa 500 gram setelah perendaman selama 60
menit.
3.5.3 Proses Destruksi
3.5.3.1 Proses Destruksi Kering
Sampel cumi-cumi yang telah dihaluskan untuk setiap perlakuan
ditimbang ± 25 gram di dalam krus porselen, lalu dipanaskan di atas hot plate
untuk menguapkan kandungan air yang terdapat pada cumi-cumi sampai kering
dan mengarang. Diabukan di tanur dengan temperatur awal 25o C dan
perlahan-lahan temperatur dinaikkan menjadi 500o C. Pengabuan dilakukan selama 12 jam.
Tanur dimatikan, dibiarkan menjadi dingin. Krus porselen dikeluarkan dari dalam
tanur.
Hasil pengabuan dilarutkan dalam 10 ml HNO3 5N, kemudian dipanaskan
di atas penangas air selama 30 menit. Lalu dimasukkan ke dalam labu tentukur
25 ml. Dibilas krus dan corong dengan air suling. Kemudian dicukupkan
volumenya dengan air suling hingga garis tanda. Kemudian disaring
menggunakan kertas saring Whatman no.42 dengan membuang 2 ml larutan
pertama hasil penyaringan. Larutan hasil destruksi ini digunakan untuk uji
kualitatif dan uji kuantitatif logam plumbum (Pb) (Chapple, 1991).
3.5.3.2 Proses Destruksi Basah
Sampel cumi-cumi yang telah dihaluskan untuk setiap perlakuan
ditimbang ± 25 gram di dalam erlenmeyer. Selanjutnya ditambahkan HNO3 pekat
sebanyak 25 ml hingga sampel terendam. Lalu didiamkan selama 24 jam dengan
tujuan agar dapat mempercepat proses destruksi yang dilakukan. Setelah 24 jam,
kuning muda jernih. Kemudian dipindahkan ke dalam labu tentukur 100 ml dan
bilas tempat larutan hasil destruksi dengan air suling. Hasil pembilasan disatukan
dengan larutan sebelumnya dalam labu tentukur dan ditepatkan dengan air suling
hingga garis tanda. Kemudian disaring menggunakan kertas saring Whatman
no.42 dengan membuang 2 ml larutan pertama hasil penyaringan. Larutan hasil
destruksi ini digunakan untuk uji kualitatif dan uji kuantitatif logam plumbum
(Pb) (Darmono, 1995).
3.5.4 Analisis Kualitatif
Ke dalam tabung reaksi dimasukkan 2 ml larutan sampel hasil destruksi
kering dan destruksi basah, diatur pH 7 dengan penambahan ammonium
hidroksida 1N, dimasukkan kalium sianida, ditambahkan 2 ml larutan dithizon
0,005%, dikocok kuat, dibiarkan larutan memisah. Terbentuk warna merah tua
berarti sampel mengandung Pb (Vogel, 1990).
3.5.5 Analisis Kuantitatif
3.5.5.1 Penentuan Panjang Gelombang maksimum
Penentuan panjang gelombang maksimum dilakukan berdasarkan penggunaan lampu katoda berongga Pb yaitu super lamp current 5 mA, setelah itu
dilakukan pengaturan dengan komputer sehingga diperoleh panjang gelombang
absorbsi maksimum untuk logam plumbum (Pb) 217 nm (Chapple, 1991).
3.5.5.2 Penentuan Linieritas Kurva Kalibrasi Logam Plumbum (Pb)
Larutan standar plumbum (Pb) (1000 mcg/ml) dipipet sebanyak 10 ml,
dimasukkan ke dalam labu tentukur 100 ml, kemudian ditambahkan 10 ml HNO3
Larutan standar plumbum (Pb) (100 mcg/ml) dipipet sebanyak 10 ml,
dimasukkan ke dalam labu tentukur 100 ml, kemudian ditambahkan 10 ml HNO3
5N, ditepatkan sampai garis tanda dengan air suling (konsentrasi 10 mcg/ml).
Larutan kerja logam plumbum (Pb) dibuat dengan memipet 0; 0,5; 1; 2; 3;
dan 4 ml larutan baku 10 mcg/ml, dimasukkan ke dalam labu tentukur 100 ml,
ditambahkan 10 ml HNO3 5N kemudian ditepatkan sampai garis tanda dengan air
suling (larutan kerja ini mengandung 0; 50; 100; 200; 300; 400 mcg/l) dan diukur
pada panjang gelombang 217 nm (hasil dapat dilihat pada Lampiran 1).
3.5.5.3 Penentuan Kadar Plumbum (Pb) dalam Cumi-cumi
Larutan sampel yang telah didestruksi kering maupun yang telah
didestruksi basah diukur absorbansinya dengan spektrofotometer serapan atom
pada panjang gelombang 217 nm.
Nilai absorbansi yang diperoleh berada dalam rentang kurva kalibrasi
larutan baku plumbum (Pb). Konsentrasi plumbum (Pb) dalam sampel dalam unit
ppb (mcg/l) ditentukan berdasarkan persamaan linier dari kurva kalibrasi.
Kadar logam plumbum (Pb) dalam sampel dapat dihitung dengan cara
sebagai berikut:
Kadar logam (mg/kg) =
Berat sampel (gr)x 10-3
(
konsentrasi logam (mcg/ml)x 10-3)
x volume (ml)Hasil dapat dilihat pada Lampiran 3 dan contoh perhitungan kadar logam
pada Lampiran 4.
3.5.5.4 Uji Perolehan Kembali
3.5.5.4.1 Pembuatan Larutan Standar
Larutan standar plumbum (Pb) (1000 mcg/ml) dipipet sebanyak 10 ml,
HNO3 5N, ditepatkan sampai garis tanda dengan air suling (konsentrasi 100
mcg/ml).
Larutan standar plumbum (Pb) (100 mcg/ml) dipipet sebanyak 10 ml,
dimasukkan larutan ke dalam labu tentukur 100 ml, kemudian ditambahkan 10 ml
HNO3 5N, ditepatkan sampai garis tanda dengan air suling (konsentrasi 10
mcg/ml).
Larutan standar plumbum (Pb) (10 mcg/ml) dipipet sebanyak 10 ml,
dimasukkan larutan ke dalam labu tentukur 100 ml, kemudian ditambahkan 10 ml
HNO3 5N, ditepatkan sampai garis tanda dengan air suling (konsentrasi 1
mcg/ml).
3.5.5.4.2 Prosedur Uji Perolehan Kembali
Uji perolehan kembali dilakukan dengan cara menentukan kadar logam
dalam sampel, selanjutnya dilakukan penentuan kadar logam dalam sampel
setelah penambahan larutan standar yang jumlahnya diketahui dengan pasti.
Larutan standar yang ditambahkan yaitu 1 ml larutan standar plumbum (Pb)
(konsentrasi 1 mcg/ml).
Uji perolehan kembali dilakukan terhadap sampel yang sama dan
dianalisis dengan cara yang sama dengan pengerjaan sampel awal (hasil dapat
dilihat pada lampiran 7 dan 8).
Persen recovery dapat dihitung dengan persamaan berikut:
n ditambahka yang
baku am jumlah
awal sampel dalam
am jumlah
sampel dalam
am total
kadar
log
log
log −
x 100%
3.5.5.5 Analisis Data Secara Statistik
(Pb) dalam cumi-cumi sebelum dan sesudah perendaman (hasil dapat dilihat pada
lampiran 5).
Adapun metode statistik untuk menentukan kandungan logam berat
plumbum (Pb) dalam cumi-cumi dianalisis dengan metode standar deviasi dengan
rumus:
SD =
( )
1 -n
X -Xi 2
∑
Keterangan : Xi = kadar sampel
= kadar rata-rata sampel
n = jumlah perlakuan
Untuk mencari t hitung digunakan rumus (Sudjana, 2005):
t hitung =
n SD
X Xi
/
−
dan untuk menentukan kadar logam di dalam sampel dengan interval kepercayaan
95%, α = 0,05, dk = n-1, dapat digunakan rumus:
Kadar Logam =
µ
= ± (t(α/2, dk) x SD / )Keterangan : = kadar rata-rata sampel
SD = Standar Deviasi
dk = derajat kebebasan (dk = n-1)
α = interval kepercayaan
n = jumlah perlakuan
3.5.5.6 Penentuan Batas Deteksi dan Batas Kuantitasi
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
kriteria cermat dan seksama.
Batas deteksi dan batas kuantitasi ini dapat diperoleh dari kalibrasi standar
yang diukur sebanyak 6 sampai 10 kali, (hasil dapat dilihat pada lampiran 9) dan
dapat dihitung dengan rumus sebagai berikut (Harmita, 2004):
Batas deteksi = slope
SB x 3
Batas kuantitasi = slope
SB x 10
Keterangan: SB = Simpangan Baku
Simpangan Baku =
(
)
2
2
− −
∑
n Yi
3.5.6 Bagan Penyiapan Sampel 1000 gram cumi-cumi dicuci bersih direndam dalam 4 buah jeruk nipis yang diencerkan dalam 400 ml air
dicuci bersih
direndam dalam campuran 150 g asam jawa dan 500 ml air setelah 30 menit
ditimbang 500 gram
500 g 500 g Cumi-cumi 4000 g
setelah 30 menit ditimbang 500 gram
dicuci bersih
direndam dalam 200 ml asam cuka 15% yang diencerkan dalam 600 ml air
setelah 30 menit ditimbang 500 gram
Keterangan:
Ck = Sampel tanpa perendaman
Ca1 = Sampel dengan perendaman dalam larutan jeruk nipis selama 30 menit
Ca2 = Sampel dengan perendaman dalam larutan jeruk nipis selama 60 menit
Cb1 = Sampel dengan perendaman dalam asam cuka selama 30 menit
Cb2 = Sampel dengan perendaman dalam asam cuka selama 60 menit
Cc1 = Sampel dengan perendaman dalam larutan asam jawa selama 30 menit
3.5.7 Bagan Destruksi Kering
Sampel yang telah dihaluskan
dimasukkan ke dalam krus porselen
ditimbang ± 25 gram
dipanaskan di atas hot plate
Sampel yang telah kering dan mengarang
diabukan di tanur selama 12 jam
dibiarkan dingin pada desikator
Abu
dilarutkan dalam HNO3 5N
dipanaskan di atas penangas air
dimasukkan ke dalam labu tentukur 25 ml
dibilas sisa residu pada krus porselen dengan air suling
ditepatkan volumenya hingga garis tanda dengan air suling
25 ml larutan sampel
Hasil
diukur pada panjang gelombang 217, 0 nm
3.5.8 Bagan Destruksi Basah
Sampel yang telah dihaluskan
ditimbang ± 25 gram di dalam erlenmeyer
ditambah 25 ml HNO3(p)
didiamkan selama 24 jam
Sampel + HNO3(p)
didestruksi selama 2 jam
disaring dengan kertas saring
Whatman No.42 ke dalam botol didinginkan
ditepatkan dengan air suling
hingga garis tanda
100 ml larutan sampel
diukur pada panjang gelombang 217, 0 nm
Hasil
dipindahkan ke dalam labu tentukur
100 ml
dibilas tempat larutan hasil destruksi
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Uji Kualitatif
Untuk mengidentifikasi bahwa sampel telah tercemar logam berat,
dilakukan reaksi kualitatif dengan menggunakan pereaksi ditizon 0,005% b/v.
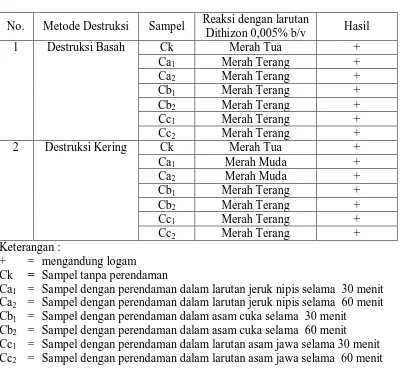
[image:45.595.114.514.273.647.2]Hasil reaksi dapat dilihat pada tabel berikut :
Tabel 1. Hasil Uji Kualitatif Logam Pb dengan Pereaksi Ditizon 0,005% b/v
No. Metode Destruksi Sampel Reaksi dengan larutan
Dithizon 0,005% b/v Hasil
1 Destruksi Basah Ck Merah Tua +
Ca1 Merah Terang +
Ca2 Merah Terang +
Cb1 Merah Terang +
Cb2 Merah Terang +
Cc1 Merah Terang +
Cc2 Merah Terang +
2 Destruksi Kering Ck Merah Tua +
Ca1 Merah Muda +
Ca2 Merah Muda +
Cb1 Merah Terang +
Cb2 Merah Terang +
Cc1 Merah Terang +
Cc2 Merah Terang +
Keterangan :
+ = mengandung logam Ck = Sampel tanpa perendaman
Ca1 = Sampel dengan perendaman dalam larutan jeruk nipis selama 30 menit
Ca2 = Sampel dengan perendaman dalam larutan jeruk nipis selama 60 menit
Cb1 = Sampel dengan perendaman dalam asam cuka selama 30 menit
Cb2 = Sampel dengan perendaman dalam asam cuka selama 60 menit
Cc1 = Sampel dengan perendaman dalam larutan asam jawa selama 30 menit
Cc2 = Sampel dengan perendaman dalam larutan asam jawa selama 60 menit
Tabel di atas menunjukkan adanya logam berat timbal (Pb) yang terdapat
dalam cumi-cumi melalui reaksi dengan ditizon 0,005 % pada pH 7 dengan
memberikan warna merah tua pada larutan sampel tanpa perendaman dan warna
dalam jeruk nipis, asam cuka, dan asam jawa selama 30 menit dan 60 menit.
Perubahan warna ini menunjukkan bahwa setelah perendaman dalam jeruk nipis,
asam cuka, maupun asam jawa, jumlah logam plumbum (Pb) telah berkurang
dibandingkan dengan sampel tanpa perendaman (Fries, 1977).
4.2 Hasil Uji Kuantitatif
4.2.1 Kurva Kalibrasi Logam Plumbum (Pb)
Kurva kalibrasi logam Pb diperoleh dengan cara mengukur absorbansi dari
larutan standar logam tersebut. Dari pengukuran kurva kalibrasi untuk logam Pb
diperoleh persamaan garis regresi yaitu: Y = 0,002208X + 0,063104. Data hasil
pengukuran absorbansi larutan standar logam Pb dapat dilihat pada Lampiran 1.
Contoh perhitungan persamaan regresi dapat dilihat pada Lampiran 2.
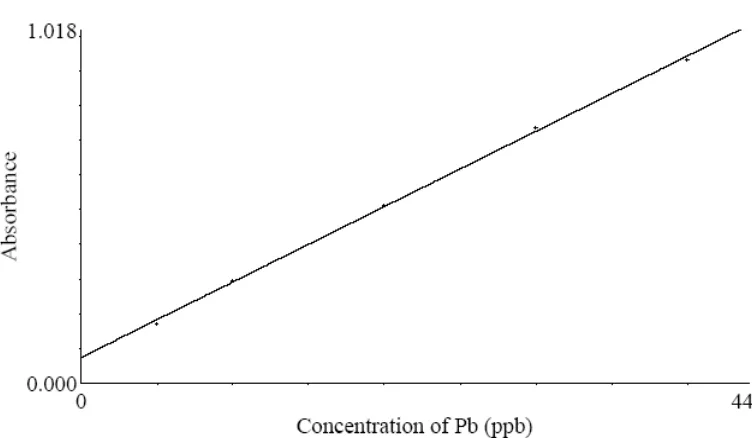
Kurva kalibrasi larutan standar Pb dapat dilihat pada gambar 1 dibawah
[image:46.595.113.489.440.659.2]ini:
Berdasarkan kurva diatas diperoleh hubungan yang linier antara
konsentrasi dengan serapan (absorbansi) dengan nilai koefisien korelasi (r)
sebesar 0,99942. Nilai r ini menunjukkan hubungan korelasi yang positif antara
konsentrasi dan absorbansi (Rohman, 2007).
4.2.2 Analisis Kadar Plumbum (Pb) dalam Cumi-cumi
Penentuan kadar logam Timbal (Pb) dilakukan secara Spektrofotometri
Serapan Atom. Konsentrasi logam Pb dalam sampel ditentukan berdasarkan
persamaan garis regresi linier kurva kalibrasi larutan standar. Data dan
perhitungan dapat dilihat pada Lampiran 3 dan Lampiran 4.
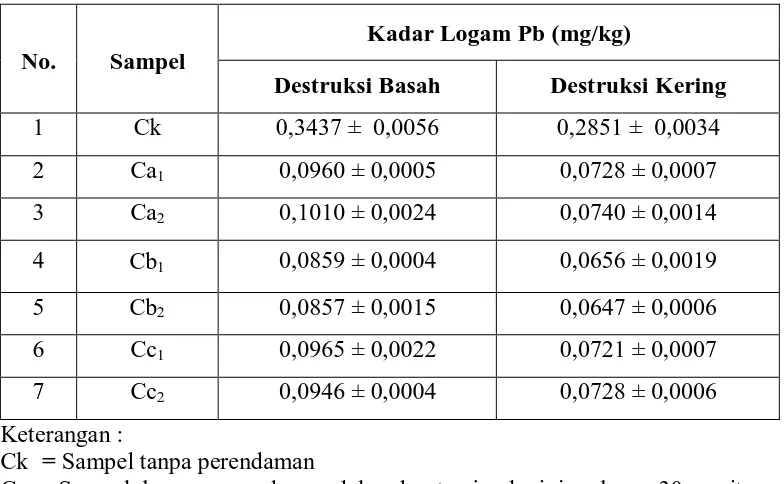
Hasil analisa kuantitatif logam Timbal (Pb) dapat dilihat pada Tabel 2.
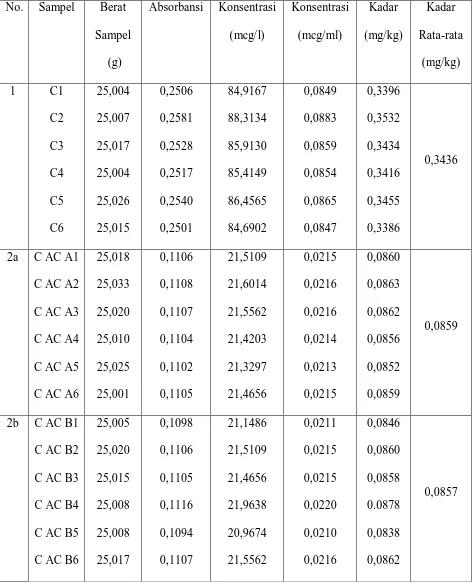
[image:47.595.113.505.414.656.2]Perhitungan dapat dilihat pada Lampiran 5.
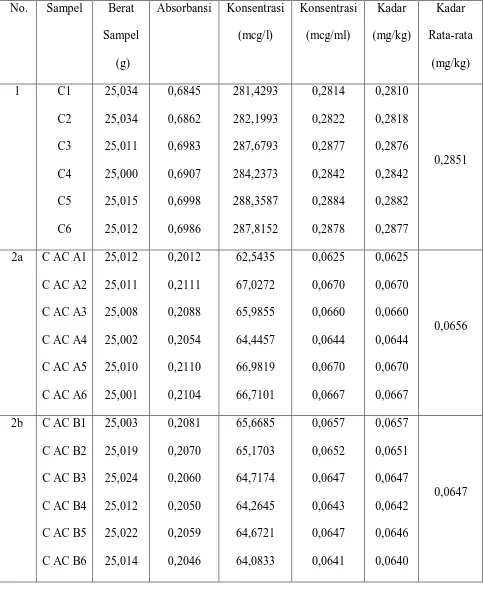
Tabel 2. Data Kadar Logam Plumbum (Pb)
No. Sampel
Kadar Logam Pb (mg/kg)
Destruksi Basah Destruksi Kering
1 Ck 0,3437 ± 0,0056 0,2851 ± 0,0034
2 Ca1 0,0960 ± 0,0005 0,0728 ± 0,0007
3 Ca2 0,1010 ± 0,0024 0,0740 ± 0,0014
4 Cb1 0,0859 ± 0,0004 0,0656 ± 0,0019
5 Cb2 0,0857 ± 0,0015 0,0647 ± 0,0006
6 Cc1 0,0965 ± 0,0022 0,0721 ± 0,0007
7 Cc2 0,0946 ± 0,0004 0,0728 ± 0,0006
Keterangan :
Ck = Sampel tanpa perendaman
Ca1 = Sampel dengan perendaman dalam larutan jeruk nipis selama 30 menit
Ca2 = Sampel dengan perendaman dalam larutan jeruk nipis selama 60 menit
Cb1 = Sampel dengan perendaman dalam asam cuka selama 30 menit
Cb2 = Sampel dengan perendaman dalam asam cuka selama 60 menit
Cc1 = Sampel dengan perendaman dalam larutan asam jawa selama 30 menit
4.2.3 Hasil Penurunan Kadar Plumbum (Pb) Setelah Perendaman dalam Air Perasan Jeruk Nipis, Asam Cuka, dan Larutan Asam Jawa
Dari hasil perhitungan secara statistik diperoleh kadar rata-rata plumbum
dalam cumi-cumi. Berdasarkan kadar rata-rata tersebut diperoleh penurunan kadar
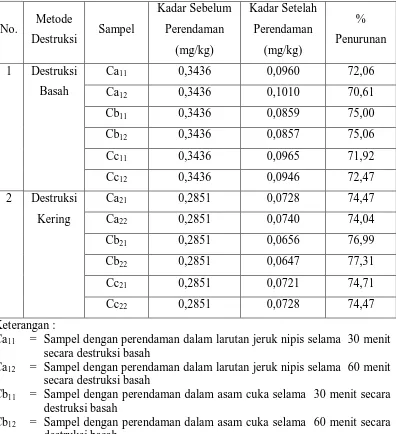
plumbum yang dapat dilihat pada tabel 3. Perhitungan persentase penurunan
dihitung terhadap kadar awal.
Tabel 3. Persen Penurunan Kadar Plumbum (Pb) Setelah Perendaman dalam Air Perasan Jeruk Nipis, Asam Cuka, dan Larutan Asam Jawa
No. Metode
Destruksi Sampel
Kadar Sebelum
Perendaman
(mg/kg)
Kadar Setelah
Perendaman
(mg/kg)
%
Penurunan
1 Destruksi
Basah
Ca11 0,3436 0,0960 72,06
Ca12 0,3436 0,1010 70,61
Cb11 0,3436 0,0859 75,00
Cb12 0,3436 0,0857 75,06
Cc11 0,3436 0,0965 71,92
Cc12 0,3436 0,0946 72,47
2 Destruksi
Kering
Ca21 0,2851 0,0728 74,47
Ca22 0,2851 0,0740 74,04
Cb21 0,2851 0,0656 76,99
Cb22 0,2851 0,0647 77,31
Cc21 0,2851 0,0721 74,71
Cc22 0,2851 0,0728 74,47
Keterangan :
Ca11 = Sampel dengan perendaman dalam larutan jeruk nipis selama 30 menit
secara destruksi basah
Ca12 = Sampel dengan perendaman dalam larutan jeruk nipis selama 60 menit
secara destruksi basah
Cb11 = Sampel dengan perendaman dalam asam cuka selama 30 menit secara
destruksi basah
Cb12 = Sampel dengan perendaman dalam asam cuka selama 60 menit secara
destruksi basah
Cc11 = Sampel dengan perendaman dalam larutan asam jawa selama 30 menit
[image:48.595.119.515.277.711.2]Cc12 = Sampel dengan perendaman dalam larutan asam jawa selama 60 menit
secara destruksi basah
Ca21 = Sampel dengan perendaman dalam larutan jeruk nipis selama 30 menit
secara destruksi kering
Ca22 = Sampel dengan perendaman dalam larutan jeruk nipis selama 60 menit
secara destruksi kering
Cb21 = Sampel dengan perendaman dalam asam cuka selama 30 menit secara
destruksi kering
Cb22 = Sampel dengan perendaman dalam asam cuka selama 60 menit secara
destruksi kering
Cc21 = Sampel dengan perendaman dalam larutan asam jawa selama 30 menit
secara destruksi kering
Cc22 = Sampel dengan perendaman dalam larutan asam jawa selama 60 menit
secara destruksi kering
Berdasarkan tabel 2 tersebut, kadar rata-rata logam Timbal (Pb) tanpa
perendaman dengan metode destruksi basah adalah 0,3437 ± 0,0056 mg/kg dan
dengan metode destruksi kering adalah 0,2851 ± 0,0034 mg/kg. Jika dikaitkan
dengan ketentuan FAO/WHO yg menyatakan bahwa kadar plumbum yang
diperbolehkan dalam tubuh hewan laut yang dapat dikonsumsi manusia adalah
tidak lebih dari 1 ppm (Agustini, 2008), maka kadar plumbum dalam cumi-cumi
yang berasal dari perairan Belawan belum melebihi batas maksimum yang
diperbolehkan.
Dari perhitungan tersebut diperoleh kesimpulan bahwa terjadi penurunan
kadar timbal (Pb) pada cumi-cumi setelah perendaman dalam larutan jeruk nipis,
asam cuka, maupun asam jawa.
Berdasarkan penelitian yang dilakukan dapat dinyatakan bahwa buah jeruk
nipis, asam cuka, dan larutan asam jawa memiliki kemampuan yang cukup efektif
untuk menurunkan kadar logam berat plumbum (Pb). Hal ini disebabkan adanya
berbagai macam senyawa organik yang mengandung gugus karboksilat dan
hidroksil yang terdapat pada jeruk nipis, asam cuka, dan asam jawa yang
Dengan demikian, ada berbagai macam cara yang dapat dilakukan oleh
masyarakat untuk menurunkan kadar logam dari makanan yang berasal dari laut
yaitu dengan cara melakukan perendaman terlebih dahulu dalam larutan jeruk
nipis, perendaman dalam asam cuka 5%, atau bisa juga dengan perendaman dalam
larutan asam jawa.
4.2.4 Pengujian Beda Nilai Rata-rata Kadar Plumbum (Pb) pada Cumi-cumi dengan Perendaman dalam Jeruk Nipis, Asam Cuka, dan Asam Jawa
Dilakukan uji beda nilai rata-rata secara statistik pada taraf kepercayaan
[image:50.595.116.512.397.609.2]95%. Uji yang dilakukan adalah uji F dan uji T yang hasilnya dapat dilihat pada
tabel di bawah ini.
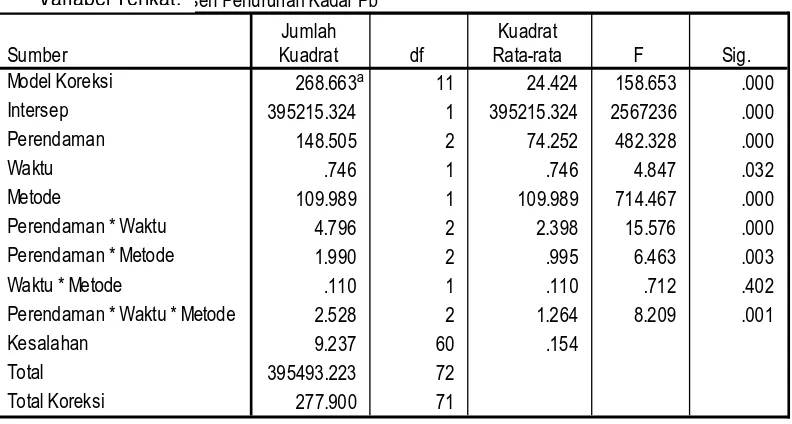
Dari tabel diperoleh F hitung untuk faktor perendaman adalah 482,328 dan
F tabel sebesar 3,1504, dimana F hitung > F tabel. Hal ini menunjukkan bahwa
perendaman mempengaruhi penurunan kadar Plumbum (Pb) cumi-cumi.
Tes Pengaruh masing-masing Subjek
Dependent Variable: Persen Penurunan Kadar Pb
268.663a 11 24.424 158.653 .000 395215.324 1 395215.324 2567236 .000 148.505 2 74.252 482.328 .000 .746 1 .746 4.847 .032 109.989 1 109.989 714.467 .000 4.796 2 2.398 15.576 .000 1.990 2 .995 6.463 .003 .110 1 .110 .712 .402 2.528 2 1.264 8.209 .001 9.237 60 .154
395493.223 72 277.900 71 Sumber
Model Koreksi Intersep Perendaman Waktu Metode
Perendaman * Waktu Perendaman * Metode Waktu * Metode
Perendaman * Waktu * Metode Kesalahan
Total Total Koreksi
Jumlah
Kuadrat df
Kuadrat
Rata-rata F Sig.
R Kuadrat = .967 a.
Selain itu dari tabel diperoleh F hitung untuk faktor perbedaan waktu
adalah 4,847 dan F tabel sebesar 4,0012, dimana F hitung > F tabel. Hal ini
menunjukkan bahwa perendaman dengan waktu 30 menit mempengaruhi
penurunan kadar Plumbum (Pb) cumi-cumi. Hal ini juga dapat dilihat dari
rata-rata kadar timbal pada cumi-cumi sebelum perendaman adalah lebih tinggi
daripada kadar cumi-cumi setelah perendaman selama 30 menit dengan air
perasan jeruk nipis, asam cuka, atau larutan asam jawa.
Kemudian, dari tabel diperoleh F hitung untuk faktor metode destruksi
adalah 714,467 dan F tabel sebesar 4,0012, dimana F hitung > F tabel. Hal ini
menunjukkan bahwa proses destruksi mempengaruhi kadar Plumbum (Pb) dalam
cumi-cumi.
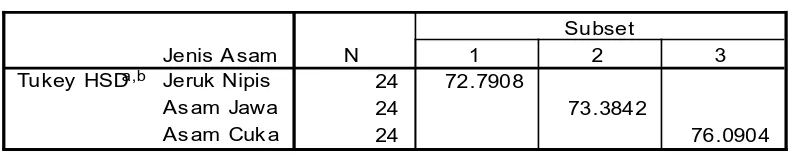
[image:51.595.115.510.453.531.2]4.2.4.1Analisis Beda Nilai Rata-rata Penurunan Kadar Plumbum (Pb) pada Cumi-cumi dengan Perendaman dalam Jeruk Nipis, Asam Cuka, dan Asam Jawa
Tabel di atas bertujuan untuk mencari atau menguji kelompok mana yang
tidak berbeda atau tidak memiliki perbedaan yang signifikan dengan kelompok
lainnya. Dari tabel di atas dapat dilihat bahwa penurunan kadar plumbum (Pb)
pada perendaman cumi-cumi dalam jeruk nipis berbeda dengan perendaman
dalam asam jawa serta berbeda pula dengan perendaman dalam asam cuka.
Dengan demikian dapat disimpulkan bahwa penurunan kadar plumbum (Pb) pada
Pe rse n Pe nuruna n Kada r Pb
24 72.7908
24 73.3842
24 76.0904
Jenis A sam Jeruk Nipis As am Jawa As am Cuk a Tukey HSDa,b
N 1 2 3
Subset
Jumlah Sampel Rata-rata = 24. 000. a.
masing-masing perendaman dalam asam jeruk nipis, asam cuka, dan asam jawa
memiliki perbedaan yang signifikan.
Dari tabel di atas dapat dilihat bahwa yang paling baik dalam mengikat
plumbum (Pb) pada cumi-cumi adalah asam cuka. Hal ini disebabkan karena asam
cuka merupakan asam organik sintetik yang murni. Sedangkan asam jawa dan
jeruk nipis merupakan asam organik dari bahan alam yang tidak kita ketahui
kandungan pengotornya sehingga dapat mengurangi efektifitas kandungan asam
jawa dan jeruk nipis dalam mengikat plumbum (Pb) pada cumi-cumi.
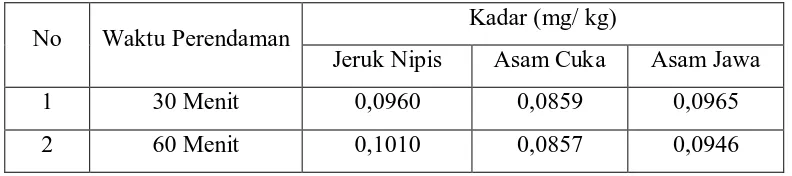
[image:52.595.118.514.401.489.2]4.2.4.2 Analisis Beda Nilai Rata-rata Kadar Plumbum (Pb) pada Cumi-cumi dengan Perbedaan Waktu Perendaman
Tabel 4. Perbedaan Kadar Plumbum (Pb) pada Cumi-cumi Setelah Perendaman dalam Jeruk Nipis, Asam Cuka, dan Asam Jawa Selama 30 menit dan 60 menit
No Waktu Perendaman Kadar (mg/ kg)
Jeruk Nipis Asam Cuka Asam Jawa
1 30 Menit 0,0960 0,0859 0,0965
2 60 Menit 0,1010 0,0857 0,0946
Dari tabel di atas dapat dilihat bahwa penurunan kadar Pb dengan
perendaman selama 30 menit ternyata tidak berbeda jauh dengan penurunan kadar
Pb dengan perendaman selama 60 menit. Maka dapat disimpulkan bahwa tidak
terdapat perbedaan yang signifikan antara waktu perendaman 30 menit dan waktu
perendaman 60 menit terhadap penurunan kadar plumbum (Pb) dalam
cumi-cumi. Hal ini berarti bahwa kemampuan pengikatan dari ketiga asam tersebut
hanya maksimal pada menit ke 30. Meskipun waktu perendaman diperpanjang,
4.2.4.2.1 Analisis Beda Nilai Rata-rata Kadar Plumbum (Pb) pada Cumi-cumi antara Metode Destruksi Basah dan Metode Destruksi Kering
Dari tabel di atas dapat dilihat bahwa dengan taraf signifikansi 0,05,
t-hitung yang diperoleh sebesar 13,843 dan nilai t tabel sebesar 2,019541, dimana
t-hitung > t-tabel. Hal ini menunjukkan bahwa terdapat perbedaan yang
signifikan antara metode destruksi basah dan destruksi kering.
Besarnya nilai probabilitas atau signifikansi adalah 0,00 lebih kecil dari
0,05. Hal ini menunjukkan ada perbedaan yang signifikan antara metode destruksi
basah dan destruksi kering.
Secara teknis, bila ditinjau dari metode destruksi, destruksi basah lebih
efektif dalam menentukan kadar logam Pb dibandingkan dengan metode destruksi
kering. Dapat dilihat pada tabel bahwa selisih kadar Pb yang diperoleh antara
destruksi basah dan destruksi kering adalah cukup bermakna yaitu sekitar 23,48
%. Hal ini terjadi karena pada metode destruksi kering lebih banyak terjadi
kehilangan logam Pb pada proses destruksi, diantaranya proses penguapan air dan
pengarangan di atas hot plate, pengabuan dengan menggunakan suhu tinggi
hingga 500o C dan waktu pemanasan yang sangat lama, serta pemanasan larutan
sampel. Sementara diketahui bahwa logam Pb mulai melebur pada suhu
327,46°C. Sedangkan pada metode destruksi basah hanya mengalami satu kali
proses pemanasan larutan sampel pada suhu rendah pada waktu pemanasan yang
relatif singkat.
Hasil Ana lisis pe rbandingan: T-Test (Pa ired Sa mples Test)
.0280190 .0131174 .0020241 .0239314 .0321067 13.843 41 .000 Destruksi Basah
-Destruksi Kering Var 1
Rata-rata Std. Devias i
Std. Error
Rata-rata Lower Upper Perbedaan pada Interval Keperc ayaan
95% Perbedaan Antarvariabel
t df
Dengan demikian, metode yang lebih baik untuk penetapan kadar logam
pada sampel adalah metode destruksi basah karena menunjukkan hasil
pengukuran logam yang lebih tinggi dibandingkan secara destruksi kering.
Padahal kedua metode tersebut sama-sama mempengaruhi kadar logam Pb yang
terkandung di dalamnya. Jadi, proses destruksi mempengaruhi kadar logam Pb
dalam cumi-cumi yang diperiksa.
4.2.5 Uji Perolehan kembali
Hasil Uji Perolehan kembali logam timbal (Pb) dalam cumi-cumi setelah
penambahan larutan standar timbal (Pb) dapat dilihat pada lampiran 7. Contoh
perhitungan persen recovery logam dalam sampel dapat dilihat pada lampiran 8.
Persen uji perolehan kembali timbal (Pb) dalam cumi-cumi dapat dilihat
pada tabel 9.
Tabel 5. Persen Uji Perolehan Kembali Plumbum (Pb) dalam Cumi-cumi No Logam yang dianalisa Recovery rata-rata(%)
1. Pb 72,05 %
Berdasarkan tabel di atas, dapat dilihat bahwa rata-rata hasil uji perolehan
kembali untuk logam timbal (Pb) adalah 72,05 %. Persen recovery tersebut
menunjukkan ketepatan kerja pada saat pemeriksaan kadar Pb dalam sampel
(Ermer, 2005).
4.2.6 Batas Deteksi dan Batas Kuantitasi
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan. Sedangkan batas kuantitasi
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
[image:54.595.120.500.442.488.2]dilakukan, maka diperoleh batas deteksi (LOD) untuk logam timbal adalah 0,0176
mcg/ml. Sedangkan untuk batas kuantitasi (LOQ) untuk logam timbal yaitu
BAB V
KESIMPULAN DAN SARAN
5.1Kesimpulan
Dari hasil pemeriksaan sebelum dan sesudah perendaman dalam asam
yang berbeda (jeruk nipis, asam cuka, dan asam jawa) dapat disimpulkan bahwa:
- Jeruk nipis, asam cuka, maupun asam jawa memiliki kemampuan untuk
menurunkan kadar plumbum (Pb). Penurunan kadar plumbum (Pb) pada
masing-masing perendaman dalam jeruk nipis, asam cuka, dan asam jawa
memiliki perbedaan yang signifikan. Yang paling baik dalam menurunkan
plumbum (Pb) pada cumi-cumi adalah asam cuka, diikuti dengan asam jawa,
dan jeruk nipis.
- Perbedaan waktu perendaman selama 30 menit dan 60 menit tidak memberikan
pengaruh yang berbeda terhadap penurunan kadar plumbum (Pb) dalam
cumi-cumi.
- Proses destruksi mempengaruhi kadar plumbum (Pb) pada cumi-cumi.
Destruksi basah lebih efektif digunakan dalam menentukan kadar logam Pb
dibandingkan dengan metode destruksi kering.
5.2Saran
- Disarankan kepada peneliti selanjutnya untuk melakukan pemeriksaan
penurunan kadar plumbum (Pb) pada cumi-cumi dengan menggunakan jenis
asam lainnya, seperti jeruk purut, jeruk lemon, jeruk bali, dan sebagainya.
- Disarankan kepada peneliti selanjutnya untuk melihat perbedaan penurunan
kadar plumbum (Pb) dengan memvariasikan berat asam dengan waktu
- Disarankan kepada masyarakat agar melakukan perendaman dengan
menggunakan asam cuka 5% sebelum mengolah makanan laut agar dapat