PENDUGAAN pH AIR HUJAN BERDASARKAN KONSENTRASI GAS SO2
DENGAN PENDEKATAN HUKUM HENRY : DISTRIBUSI SPASIAL & TEMPORAL DI KOTA BANDUNG
OLEH : JULIANA ANGGRAINI
G24103003
DEPARTEMEN GEOFISIKA DAN METEOROLOGI FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
PENDUGAAN pH AIR HUJAN BERDASARKAN KONSENTRASI GAS SO2
DENGAN PENDEKATAN HUKUM HENRY : DISTRIBUSI SPASIAL & TEMPORAL DI KOTA BANDUNG
JULIANA ANGGRAINI G24103003
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Program Study Meteorologi
DEPARTEMEN GEOFISIKA DAN METEOROLOGI FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
LEMBAR PENGESAHAN
Judul Penelitian : Pendugaan pH Air Hujan Berdasarkan Konsentrasi Gas SO2 dengan Pendekatan Hukum Henry : Distribusi Spasial & Temporal di Kota Bandung
Nama : Juliana Anggraini
NRP : G24103003
Menyetujui
Pembimbing I, Pembimbing II,
Dr. Imam Santosa M.S Dr. Eng. Esrom Hamonangan NIP : 130804894 NIP : 770000139
Mengetahui
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor
Dr. Drh. Hasim, DEA NIP : 131578806
RINGKASAN
JULIANA ANGGRAINI. Pendugaan pH Air Hujan Berdasarkan Konsentrasi Gas SO2
dengan Pendekatan Hukum Henry : Distribusi Spasial & Temporal di Kota Bandung. Dibimbing oleh : IMAM SANTOSA dan ESROM HAMONANGAN.
Hujan asam atau lebih tepatnya presipitasi asam, adalah istilah yang digunakan untuk mendeskripsikan curah hujan yang memiliki pH di bawah 5,6. Hujan asam merupakan masalah lingkungan yang serius karena dapat menyebabkan korositas pada bangunan/gedung atau bersifat korosif terhadap bahan bangunan, merusak tanaman dan hasil produksinya dan merusak kehidupan biota di danau-danau/aliran sungai, sehingga hujan asam perlu diprediksi, dan dikontrol.
Nilai pH air hujan adalah suatu indikator terjadinya hujan asam, sehingga nilainya perlu diketahui. Salah satu pendekatan yang dapat digunakan untuk menduga pH air hujan adalah Hukum Henry karena hukum Henry membantu untuk memperkirakan jumlah tiap-tiap gas yang akan masuk ke dalam larutan, namun karena setiap gas memiliki daya kelarutan yang berbeda-beda dan hal ini juga mempengaruhi lajunya, maka konstanta kesetimbangan dalam hukum Henry harus disertakan dalam perhitungan. Dalam penelitian ini hanya digunakan satu parameter polutan, yaitu SO2 sehingga konstanta yang dihitung hanya konstanta hukum Henry untuk gas tersebut.
Hasil penelitian menunjukkan bahwa gas SO2 memberikan pengaruh yang signifikan terhadap pengasaman air hujan, hal ini terbukti dengan konsentrasi sebesar 30µg/m3 sekalipun dapat menurunkan pH sebesar 0.0983, namun nilai pH yang didapat lebih tinggi daripada pH terukur yaitu berkisar antara 5,6 - 6 di Stasiun Ariagraha, Tirtalega dan Batununggal, sedangkan pH di stasiun Dago dan Cisaranten lebih rendah yaitu antara 5,2 – 5,4. Perbandingan nilai pH antara musim hujan dan musim kering di setiap stasiun tidak terlalu besar, yaitu sekitar 0.01-0.09 kecuali untuk stasiun Cisaranten, yaitu 0.10-0.33. Hal ini disebabkan nilai pH hanya diduga berdasarkan konsentrasi gas SO2, sedangkan polutan yang berkontribusi terhadap pengasaman air hujan bukan hanya SO2 tetapi juga NOx dan CO2. Perbedaan nilai pH di beberapa stasiun disebabkan faktor lokasi.
Distribusi angin rata-rata pada musim hujan dan musim kering masing-masing adalah ke arah Barat dan ke arah Timur sehingga diperkirakan pada musim hujan gas-gas SO2 ini akan terbawa ke daerah Dago (kecamatan Coblong), Kecamatan Bandung Wetan, Kecamatan Kiara condong, Kecamatan Cicendo, Kecamatan Andir dan Kecamatan Babakan Ciparay, sementara pada musim kering diperkirakan distribusi gas SO2 akan menuju Kecamatan Cicadas, Kecamatan Ujung Berung (Cisaranten Wetan), Kecamatan Cibiru, Kecamatan Rancasari (Ariagraha) dan Kecamatan Margacinta, sehingga diperkirakan pH air hujan di daerah-daerah ini akan menurun
KATA PENGANTAR
Alhamdulliah, puji syukur penulis panjatkan kehadirat Allah SWT karena atas izin dan karunia-Nya laporan penelitian ini dapat diselesaikan. Judul yang dipilih dalam penelitian ini adalah Pendugaan pH Air Hujan Berdasarkan Konsentrasi Gas SO2 dengan Pendekatan
Hukum Henry : Distribusi Spasial & Temporal di Kota Bandung. Laporan penelitian ini tidak akan terselesaikan tanpa bantuan dan dukungan dari berbagai pihak, oleh karena itu penulis menghaturkan ucapan terima kasih sebanyak-banyaknya kepada :
1. Bapak Dr. Imam Santosa M.S, dan Bapak Dr. Eng. Esrom Hamonangan selaku pembimbing penulis dalam menjalankan penelitian,
2. Ibu Ana Turyanti yang telah banyak memberi masukan, bantuan dan bimbingan privat kepada penulis sehingga penulis dapat menyelesaikan penelitian ini, maaf ya bu sering merepotkan.. 3. Bapak Luki, Bapak Jamal, Ibu Rita dan Ibu Medi di AQMS Pusarpedal, Serpong yang telah
membantu penulis selama melakukan penelitian di Pusarpedal
4. Kak Adib dan Pak Khariri di Bagian Pencemaran Udara BMG untuk data kualitas air hujannya..
5. Ibu Andrea di BPLHD Bandung atas data polutannya.
6. Papa, Mama, Bro Andi, Ayu, Bebi, Jaka dan De’ Wani, atas doa dan cinta serta kasih sayangnya, yang memberikan motivasi tiada terkira untuk selalu berbuat dan memberi yang terbaik, Hope I can make all your wish come true.. hope I can make you proud of me.. hope you always happy..
7. Seluruh Keluargaku dimanapun berada, terima kasih untuk kepercayaan dan doanya, semoga penulis dapat menjadi apa yang kalian harapkan..
8. Keluarga Bapak Nanang , thank you for all the helps,,
9. Temen-temen seperjuangan di LabMet, Let’s keep up fighting guys! All u need is the hands, legs, eyes, brain which is work more harder than before and the heart which always pray.. and the most important, always believe you can do whatever you want! Always believe you can do it!
10. Nanik, Nunun, Nonik, you guys rock and keep this bond forever... Ayu, Puji n Dimi, terima kasih buat semangat n doanya, Latief dan Ucup, terima kasih buat petanya..., Yeti dan Ida terima kasih sudah bersedia datang ke latihan seminarku yang aneh.. (hehe..), Ria “shasya”
sang sekretaris, Jurick sang “jurick”, Iqo yang lagi berjuang, Ponco, Mia, Yuni dan Tria,
where are you guys? QQ, Dicka dan Budi, ganbatte ne’ tinggal sedikit lagi niy!! LabMet
harus “cuci gudang secepatnya!!”. Tri, Mamat, Kolay, Rifky, Shandy, Wiranto, Bonang,
Kulu, Manto, Congky, Dwi, Bismi, Mega, Dhada dan Harry.. Thanx ya buat semua yang sudah kalian lakukan.. hope our bond never break and keep our friendship forever.. Love u all..
11. AIDA komik n rental, thanx for keep me healthy, happy, rilex n poor!!
12. Komputerku yang dengan setia menemaniku mengerjakan penelitian, yang telah mengalami berbagai penderitaan mulai dari kena virus sampai nge-hang tiba-tiba, terima kasih sudah nemenin aku mengerjakan semua pekerjaanku baik yang jelas maupun yang tidak jelas..
13. Dicky Fajar Anugrah, terima kasih untuk semua doa, semangat, perhatian, dan selalu ada sebagai tempat bersandar di saat penulis lelah,
Last but not least, semoga laporan penelitian ini dapat bermanfaat bagi ilmu pengetahuan dan bagi siapapun yang membacanya.
Bogor, Mei 2008
RIWAYAT HIDUP
DAFTAR ISI
LEMBAR PENGESAHAN... i
RINGKASAN... ii
PRAKATA... ... iii
RIWAYAT HIDUP... iv
DAFTAR ISI... v
DAFTAR GAMBAR... vi
DAFTAR TABEL... vii
DAFTAR LAMPIRAN... vii
1. PENDAHULUAN 1.1 Latar Belakang... 1
1.2 Tujuan... 1
2. TINJAUAN PUSTAKA 2.1 Atmosfer... 2
2.1.1 Komposisi Atmosfer... 2
2.1.2 Polusi Udara... 2
2.1.3 Pengaruh Kondisi Meteorologi terhadap Dispersi... 2
2.2 Hujan Asam... 3
2.2.1 Definisi Hujan Asam... 3
2.2.2 Proses Pembentukan Hujan Asam... 3
2.2.3 Efek Hujan Asam... 3
2.3 Sulfur Dioksida... 3
2.4 Tingkat Kelarutan Gas... 4
2.4.1 Kelarutan Gas berdasarkan Suhu... 4
2.4.2 Kelarutan Gas berdasarkan Tekanan... 4
2.5 Kesetimbangan Penyerapan dan Hukum Henry... 5
2.6 Gambaran Umum Kota Bandung... 5
2.6.1 Kondisi Geografis Kota Bandung... 5
2.6.2 Kondisi Iklim Kota Bandung... 7
2.6.3 Kondisi Geologi dan Fisiografi... 7
2.6.4 Transportasi... 7
2.6.5 Industri... 7
2.6.6 Air Quality Monitoring System... 8
3. METODOLOGI 3.1 Waktu dan Tempat Penelitian... 10
3.2 Bahan... 10
3.3 Alat... 10
3.4 Asumsi... 10
3.5 Metode... 10
3.5.1 Pendugaan Nilai pH... 10
3.5.2 Kesetimbangan Kimia Fase Cair... 10
3.5.3 Distribusi Spasial dan Temporal Deposisi Asam... 12
4. HASIL DAN PEMBAHASAN 4.1 Kondisi umum Daerah Kajian... 13
4.2 Suhu Udara dan Konstanta Hukum Henry... 14
4.3 Curah Hujan... 14
4.4 Arah dan Kecepatan Angin... 15
4.5 Konsentrasi Gas SO2... 18
4.6 Pendugaan pH Air Hujan... 19
4.7 Distribusi pH Air Hujan... 21
4.8 Distribusi Gas SO2 dan pH... 23
5. KESIMPULAN DAN SARAN 5.1 Kesimpulan ... 28
5.2 Saran... 28
DAFTAR GAMBAR
Gambar 1. Proses Pembentukan Deposisi Asam... 3
Gambar 2. Kelarutan Gas Berdasarkan Suhu... 4
Gambar 3. Batas Administrasi Kecamatan Kota Bandung... 6
Gambar 4. Peta Kemiringan Lahan Kota Bandung... 6
Gambar 5. Rute Angkutan Kota Bandung... ... 8
Gambar 6. Sebaran Lokasi Industri Kota Bandung... ... 9
Gambar 7. Peta Lokasi Stasiun Pemantau Otomatis dan Data Display……..…... 13
Gambar 8. Peta Kontur Ketinggian Stasiun Pemantauan Kualitas Udara Bandung... 13
Gambar 9. Kelarutan SO2 dalam Air Versus Suhu... 14
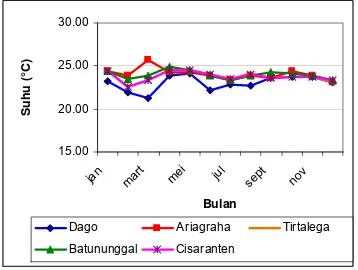
Gambar 10. Grafik Suhu Udara di Stasiun Kualitas Udara Bandung... 15
Gambar 11. Grafik Curah Hujan Kota Bandung... 15
Gambar 12. Arah dan Kecepatan Angin Musim Hujan Dago... 16
Gambar 13. Arah dan Kecepatan Angin Musim Kering Dago... 16
Gambar 14. Arah dan Kecepatan Angin Musim Hujan Ariagraha... 17
Gambar 15. Arah dan Kecepatan Angin Musim Kering Ariagraha... 17
Gambar 16. Arah dan Kecepatan Angin Musim Hujan Tirtalega ... 17
Gambar 17. Arah dan Kecepatan Angin Musim Kering Tirtalega ... 17
Gambar 18. Arah dan Kecepatan Angin Musim Hujan Batununggal... 17
Gambar 19. Arah dan Kecepatan Angin Musim Kering Batununggal... 17
Gambar 20. Arah dan Kecepatan Angin Musim Hujan Cisaranten... 17
Gambar 21. Arah dan Kecepatan Angin Musim Kering Cisaranten... 17
Gambar 22. Grafik Konsentrasi SO2 Musim Kering... 19
Gambar 23. Grafik Konsentrasi SO2 Musim Hujan... ... 19
Gambar 24. Peta Distribusi SO2 Musim Kering... ... 19
Gambar 25 Peta Distribusi SO2 Musim Hujan... ... ... ... 19
Gambar 26. Grafik pH Dugaan Musim Hujan... 20
Gambar 27. Grafik pH Dugaan Musim Kering... 20
Gambar 28. Grafik pH Terukur Stasiun Cuaca BMG Bandung... ... 21
Gambar 29. Peta Distribusi pH Mingguan Musim Hujan Minggu I... 22
Gambar 30. Peta Distribusi pH Mingguan Musim Hujan Minggu II... 22
Gambar 31. Peta Distribusi pH Mingguan Musim Hujan Minggu III... 22
Gambar 32. Peta Distribusi pH Mingguan Musim Hujan Minggu IV... 22
Gambar 33. Peta Distribusi pH Mingguan Musim Hujan Minggu I... 23
Gambar 34. Peta Distribusi pH Mingguan Musim Hujan Minggu II... 23
Gambar 35. Peta Distribusi pH Mingguan Musim Hujan Minggu III... 23
Gambar 36. Peta Distribusi pH Mingguan Musim Hujan Minggu IV... 23
Gambar 37. Distribusi Gas SO2 Musim Hujan Dago………... 25
Gambar 38. Distribusi Gas SO2 Musim Kering Dago………... 26
Gambar 39. Distribusi Gas SO2 Musim Hujan Ariagraha…………... 26
Gambar 40. Distribusi Gas SO2 Musim Kering Ariagraha …..……... 26
Gambar 41. Distribusi Gas SO2 Musim Hujan Tirtalega…..……... 26
Gambar 42. Distribusi Gas SO2 Musim Kering Tirtalega …..……... 26
Gambar 43. Distribusi Gas SO2 Musim Hujan Batununggal …..……... 26
Gambar 44. Distribusi Gas SO2 Musim Kering Batununggal …..…... 26
Gambar 45. Distribusi Gas SO2 Musim Hujan Cisaranten …..……... 26
DAFTAR TABEL
Tabel 1. Koefisien Hukum Henry dari Gas-Gas Atmosfer yang Terlarut Dalam Air………. 5
Tabel 2. Jumlah Kendaraan Bermotor (Umum dan Pribadi)……….. 7
Tabel 3. Jumlah Industri Non-Formal Kota Bandung………...………….. 8
Tabel 4. Lokasi Stasiun Pengukuran Kualitas Udara Bandung………...…………. 14
Tabel 5. Persentase Perolehan Data (Jumlah Hari Pengamatan) di Stasiun Pemantauan Otomatis Bandung ……….………... 19
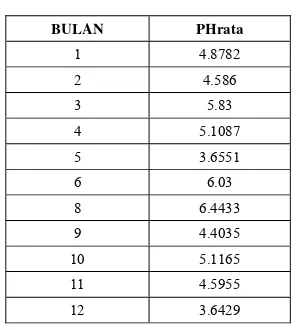
Tabel 6. pH Terukur Tahun 2003………...………….. 20
Tabel 7. pH Dugaan Mingguan Musim Hujan 2003………..………. 20
Tabel 8. pH Dugaan Mingguan Musim Kering 2003…………..…..…………....…………. 20
DAFTAR LAMPIRAN Lampiran 1. Pembentukan Partikel Ammonium Sulfat ……... 31
Lampiran 2. Siklus Sulfur di Atmosfer ………... 32
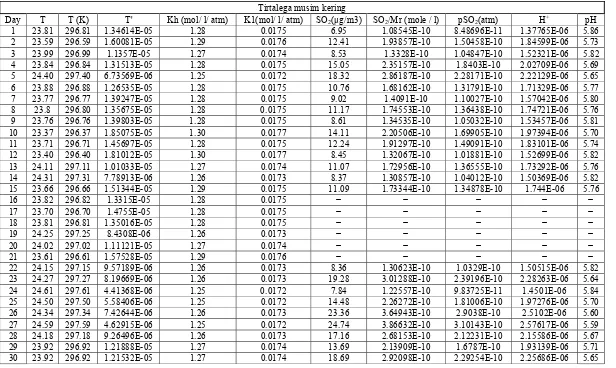
Lampiran 3. Tabel Konsentrasi Gas SO2 di Lima Stasiun Pengukuran Kualitas Udara Kota Bandung ………...…………... 33
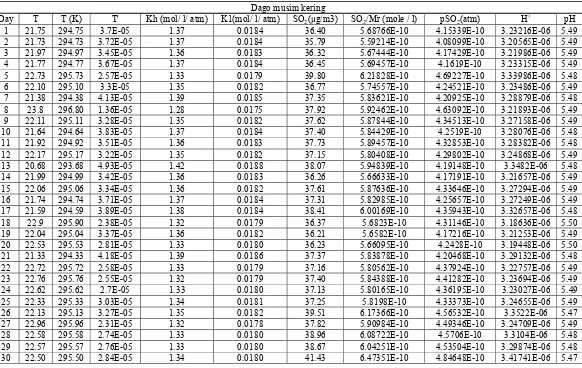
Lampiran 4. Tabel pH Dugaan Stasiun Dago Pada Musim Hujan ………...……... 34
Lampiran 5. Tabel pH Dugaan Stasiun Dago Pada Musim Kering………... 35
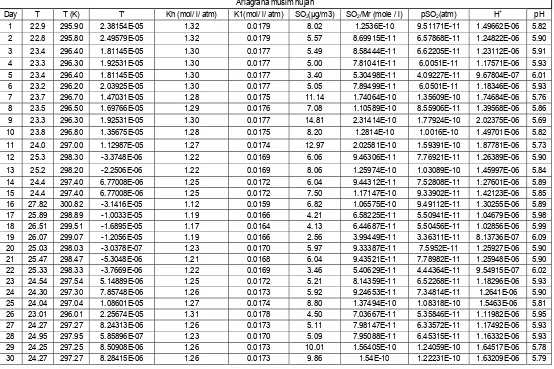
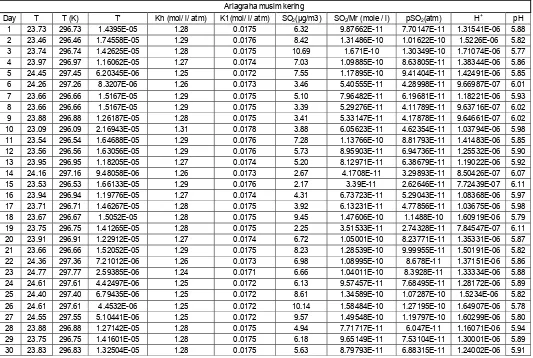
Lampiran 6. Tabel pH Dugaan Stasiun Ariagraha Pada Musim Hujan ..…………... 36
Lampiran 7. Tabel pH Dugaan Stasiun Ariagraha Pada Musim Kering …………... 37
Lampiran 8. Tabel pH Dugaan Stasiun Tirtalega Pada Musim Hujan ………... 38
Lampiran 9. Tabel pH Dugaan Stasiun Tirtalega Pada Musim Kering... 39
Lampiran 10. Tabel pH Dugaan Stasiun Batununggal Pada Musim Hujan... 40
Lampiran 11. Tabel pH Dugaan Stasiun Batununggal Pada Musim Kering... 41
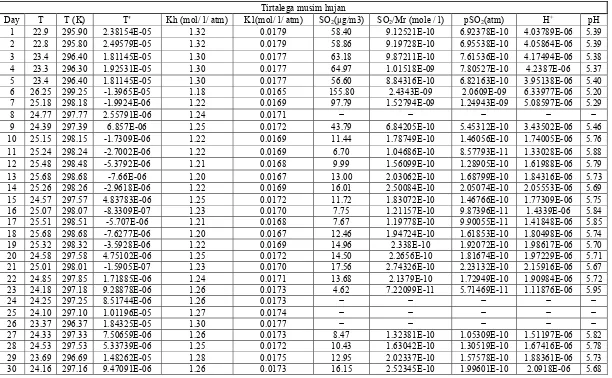
Lampiran 12. Tabel pH Dugaan Stasiun Cisaranten Pada Musim Hujan... 42
Lampiran 13. Tabel pH Dugaan Stasiun Cisaranten Pada Musim Kering... 43
I. PENDAHULUAN 1.1 Latar Belakang
Topik seputar kimia air hujan, termasuk diantaranya hujan asam, kian mendapat perhatian khusus dan merupakan suatu topik utama dalam isu lingkungan. Hujan asam merupakan masalah lingkungan yang serius karena dapat menyebabkan korositas pada bangunan/gedung atau bersifat korosif terhadap bahan bangunan, merusak tanaman dan hasil produksinya dan merusak kehidupan biota di danau-danau/aliran sungai, sehingga hujan asam perlu diprediksi, dan dikontrol.
Hujan dikatakan bersifat asam apabila memiliki pH di bawah 5,6. Batas rata-rata pH air hujan adalah 5,6 dan merupakan nilai yang dianggap normal atau hujan alami seperti yang telah disepakati secara internasional oleh badan dunia WMO (BMG, 2003). Air hujan alami bersifat asam karena besarnya konsentrasi CO2 di udara, yang apabila bereaksi dengan uap air akan membentuk asam.
Penambahan gas SO2 di atmosfer dapat menambah keasaman air hujan, karena walaupun konsentrasinya di udara lebih kecil daripada CO2, namun kelarutan dan konstanta kesetimbangan SO2 lebih besar daripada CO2. Selain itu H2SO3 merupakan asam yang lebih kuat daripada H2CO3 sehingga dalam konsentrasi yang kecil sekalipun SO2 mempengaruhi keasaman air hujan (Brimblecombe, 1986). Hal ini didukung oleh hasil penelitian Nurhayati dan Hara (2000) yang menyatakan bahwa ion SO4
2-
merupakan kontributor yang memiliki pengaruh dalam pengasaman air hujan di Indonesia.
Nilai pH air hujan merupakan salah satu indikator terjadinya hujan asam, sehingga nilai ini perlu diketahui. Analisa mengenai tingkat konsentrasi unsur-unsur kimia yang terlarut dalam air hujan, termasuk derajat keasamannya (pH) telah dilakukan oleh BMG yaitu dengan melakukan pengukuran air hujan di beberapa kota di Indonesia dan menganalisisnya, namun jumlah stasiun pemantau kualitas air hujan hanya satu untuk setiap kota dan umumnya terletak pada daerah rural sehingga kurang mewakili kondisi sebenarnya di lapang. Selain itu metode sampling dilakukan seminggu sekali, sehingga dikhawatirkan akan mempengaruhi nilai pH air hujan karena kemungkinan air hujan yang tertampung bukan merupakan air pada hujan pertama melainkan beberapa kejadian hujan. Akumulasi dari partikel debu yang tercampur dalam air hujan
selama waktu sampling juga dapat mempengaruhi pH.
Berdasarkan hasil penelitian Tuti Budiwati et al (2005) beberapa kota besar di Indonesia telah mengalami hujan asam. Hal ini diindikasikan dengan pH air hujan yang rendah, yaitu berkisar antara 4,5 – 5,0. Salah satu kota yang telah mengalami hujan asam adalah kota Bandung. Bandung adalah salah satu kota yang mengalami perkembangan dalam segala bidang. Semakin pesatnya kemajuan ekonomi mendorong semakin bertambahnya kebutuhan akan transportasi. Perkembangan pusat bisnis dan industri memacu penggunaan bahan bakar dan emisi. Selain itu topografi Bandung yang unik ikut mempengaruhi potensi polusi udara di kota ini. Topografi dapat mengubah arah dan kecepatan angin secara tiba-tiba dan profil kota besar yang cukup kasap merupakan peredam energi kinetik dan melemahkan angin, sehingga dengan kombinasi yang dimiliki kota Bandung, menyebabkan potensi polusi udara di kota ini cukup tinggi. Konsekuensi peningkatan polutan-polutan di atmosfer inilah yang dapat menyebabkan terjadinya hujan asam.
Untuk memudahkan analisa kualitas air hujan diperlukan suatu pendekatan yang dapat menduga pH air hujan secara langsung. Salah satu pendekatan yang dapat digunakan adalah Hukum Henry dan kesetimbangan fase cair, yang menyatakan bahwa pada saat kesetimbangan tekanan parsial gas di atas suatu campuran sama dengan konsentrasi gas dalam campuran tersebut (Brimblecombe, 1986). Hukum Henry telah banyak digunakan di negara lain baik sebagai metode perhitungan maupun dalam bentuk software sebagai pendekatan dalam memprediksi jumlah gas yang terlarut dalam air hujan atau droplet awan dan pH air hujan.
1.2 Tujuan
1. Menduga pH air hujan di beberapa stasiun pengukuran kualitas udara kota Bandung berdasarkan konsentrasi SO2 dengan menggunakan pendekatan hukum Henry.
PENDUGAAN pH AIR HUJAN BERDASARKAN KONSENTRASI GAS SO2
DENGAN PENDEKATAN HUKUM HENRY : DISTRIBUSI SPASIAL & TEMPORAL DI KOTA BANDUNG
OLEH : JULIANA ANGGRAINI
G24103003
DEPARTEMEN GEOFISIKA DAN METEOROLOGI FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
PENDUGAAN pH AIR HUJAN BERDASARKAN KONSENTRASI GAS SO2
DENGAN PENDEKATAN HUKUM HENRY : DISTRIBUSI SPASIAL & TEMPORAL DI KOTA BANDUNG
JULIANA ANGGRAINI G24103003
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Program Study Meteorologi
DEPARTEMEN GEOFISIKA DAN METEOROLOGI FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
LEMBAR PENGESAHAN
Judul Penelitian : Pendugaan pH Air Hujan Berdasarkan Konsentrasi Gas SO2 dengan Pendekatan Hukum Henry : Distribusi Spasial & Temporal di Kota Bandung
Nama : Juliana Anggraini
NRP : G24103003
Menyetujui
Pembimbing I, Pembimbing II,
Dr. Imam Santosa M.S Dr. Eng. Esrom Hamonangan NIP : 130804894 NIP : 770000139
Mengetahui
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor
Dr. Drh. Hasim, DEA NIP : 131578806
RINGKASAN
JULIANA ANGGRAINI. Pendugaan pH Air Hujan Berdasarkan Konsentrasi Gas SO2
dengan Pendekatan Hukum Henry : Distribusi Spasial & Temporal di Kota Bandung. Dibimbing oleh : IMAM SANTOSA dan ESROM HAMONANGAN.
Hujan asam atau lebih tepatnya presipitasi asam, adalah istilah yang digunakan untuk mendeskripsikan curah hujan yang memiliki pH di bawah 5,6. Hujan asam merupakan masalah lingkungan yang serius karena dapat menyebabkan korositas pada bangunan/gedung atau bersifat korosif terhadap bahan bangunan, merusak tanaman dan hasil produksinya dan merusak kehidupan biota di danau-danau/aliran sungai, sehingga hujan asam perlu diprediksi, dan dikontrol.
Nilai pH air hujan adalah suatu indikator terjadinya hujan asam, sehingga nilainya perlu diketahui. Salah satu pendekatan yang dapat digunakan untuk menduga pH air hujan adalah Hukum Henry karena hukum Henry membantu untuk memperkirakan jumlah tiap-tiap gas yang akan masuk ke dalam larutan, namun karena setiap gas memiliki daya kelarutan yang berbeda-beda dan hal ini juga mempengaruhi lajunya, maka konstanta kesetimbangan dalam hukum Henry harus disertakan dalam perhitungan. Dalam penelitian ini hanya digunakan satu parameter polutan, yaitu SO2 sehingga konstanta yang dihitung hanya konstanta hukum Henry untuk gas tersebut.
Hasil penelitian menunjukkan bahwa gas SO2 memberikan pengaruh yang signifikan terhadap pengasaman air hujan, hal ini terbukti dengan konsentrasi sebesar 30µg/m3 sekalipun dapat menurunkan pH sebesar 0.0983, namun nilai pH yang didapat lebih tinggi daripada pH terukur yaitu berkisar antara 5,6 - 6 di Stasiun Ariagraha, Tirtalega dan Batununggal, sedangkan pH di stasiun Dago dan Cisaranten lebih rendah yaitu antara 5,2 – 5,4. Perbandingan nilai pH antara musim hujan dan musim kering di setiap stasiun tidak terlalu besar, yaitu sekitar 0.01-0.09 kecuali untuk stasiun Cisaranten, yaitu 0.10-0.33. Hal ini disebabkan nilai pH hanya diduga berdasarkan konsentrasi gas SO2, sedangkan polutan yang berkontribusi terhadap pengasaman air hujan bukan hanya SO2 tetapi juga NOx dan CO2. Perbedaan nilai pH di beberapa stasiun disebabkan faktor lokasi.
Distribusi angin rata-rata pada musim hujan dan musim kering masing-masing adalah ke arah Barat dan ke arah Timur sehingga diperkirakan pada musim hujan gas-gas SO2 ini akan terbawa ke daerah Dago (kecamatan Coblong), Kecamatan Bandung Wetan, Kecamatan Kiara condong, Kecamatan Cicendo, Kecamatan Andir dan Kecamatan Babakan Ciparay, sementara pada musim kering diperkirakan distribusi gas SO2 akan menuju Kecamatan Cicadas, Kecamatan Ujung Berung (Cisaranten Wetan), Kecamatan Cibiru, Kecamatan Rancasari (Ariagraha) dan Kecamatan Margacinta, sehingga diperkirakan pH air hujan di daerah-daerah ini akan menurun
KATA PENGANTAR
Alhamdulliah, puji syukur penulis panjatkan kehadirat Allah SWT karena atas izin dan karunia-Nya laporan penelitian ini dapat diselesaikan. Judul yang dipilih dalam penelitian ini adalah Pendugaan pH Air Hujan Berdasarkan Konsentrasi Gas SO2 dengan Pendekatan
Hukum Henry : Distribusi Spasial & Temporal di Kota Bandung. Laporan penelitian ini tidak akan terselesaikan tanpa bantuan dan dukungan dari berbagai pihak, oleh karena itu penulis menghaturkan ucapan terima kasih sebanyak-banyaknya kepada :
1. Bapak Dr. Imam Santosa M.S, dan Bapak Dr. Eng. Esrom Hamonangan selaku pembimbing penulis dalam menjalankan penelitian,
2. Ibu Ana Turyanti yang telah banyak memberi masukan, bantuan dan bimbingan privat kepada penulis sehingga penulis dapat menyelesaikan penelitian ini, maaf ya bu sering merepotkan.. 3. Bapak Luki, Bapak Jamal, Ibu Rita dan Ibu Medi di AQMS Pusarpedal, Serpong yang telah
membantu penulis selama melakukan penelitian di Pusarpedal
4. Kak Adib dan Pak Khariri di Bagian Pencemaran Udara BMG untuk data kualitas air hujannya..
5. Ibu Andrea di BPLHD Bandung atas data polutannya.
6. Papa, Mama, Bro Andi, Ayu, Bebi, Jaka dan De’ Wani, atas doa dan cinta serta kasih sayangnya, yang memberikan motivasi tiada terkira untuk selalu berbuat dan memberi yang terbaik, Hope I can make all your wish come true.. hope I can make you proud of me.. hope you always happy..
7. Seluruh Keluargaku dimanapun berada, terima kasih untuk kepercayaan dan doanya, semoga penulis dapat menjadi apa yang kalian harapkan..
8. Keluarga Bapak Nanang , thank you for all the helps,,
9. Temen-temen seperjuangan di LabMet, Let’s keep up fighting guys! All u need is the hands, legs, eyes, brain which is work more harder than before and the heart which always pray.. and the most important, always believe you can do whatever you want! Always believe you can do it!
10. Nanik, Nunun, Nonik, you guys rock and keep this bond forever... Ayu, Puji n Dimi, terima kasih buat semangat n doanya, Latief dan Ucup, terima kasih buat petanya..., Yeti dan Ida terima kasih sudah bersedia datang ke latihan seminarku yang aneh.. (hehe..), Ria “shasya”
sang sekretaris, Jurick sang “jurick”, Iqo yang lagi berjuang, Ponco, Mia, Yuni dan Tria,
where are you guys? QQ, Dicka dan Budi, ganbatte ne’ tinggal sedikit lagi niy!! LabMet
harus “cuci gudang secepatnya!!”. Tri, Mamat, Kolay, Rifky, Shandy, Wiranto, Bonang,
Kulu, Manto, Congky, Dwi, Bismi, Mega, Dhada dan Harry.. Thanx ya buat semua yang sudah kalian lakukan.. hope our bond never break and keep our friendship forever.. Love u all..
11. AIDA komik n rental, thanx for keep me healthy, happy, rilex n poor!!
12. Komputerku yang dengan setia menemaniku mengerjakan penelitian, yang telah mengalami berbagai penderitaan mulai dari kena virus sampai nge-hang tiba-tiba, terima kasih sudah nemenin aku mengerjakan semua pekerjaanku baik yang jelas maupun yang tidak jelas..
13. Dicky Fajar Anugrah, terima kasih untuk semua doa, semangat, perhatian, dan selalu ada sebagai tempat bersandar di saat penulis lelah,
Last but not least, semoga laporan penelitian ini dapat bermanfaat bagi ilmu pengetahuan dan bagi siapapun yang membacanya.
Bogor, Mei 2008
RIWAYAT HIDUP
DAFTAR ISI
LEMBAR PENGESAHAN... i
RINGKASAN... ii
PRAKATA... ... iii
RIWAYAT HIDUP... iv
DAFTAR ISI... v
DAFTAR GAMBAR... vi
DAFTAR TABEL... vii
DAFTAR LAMPIRAN... vii
1. PENDAHULUAN 1.1 Latar Belakang... 1
1.2 Tujuan... 1
2. TINJAUAN PUSTAKA 2.1 Atmosfer... 2
2.1.1 Komposisi Atmosfer... 2
2.1.2 Polusi Udara... 2
2.1.3 Pengaruh Kondisi Meteorologi terhadap Dispersi... 2
2.2 Hujan Asam... 3
2.2.1 Definisi Hujan Asam... 3
2.2.2 Proses Pembentukan Hujan Asam... 3
2.2.3 Efek Hujan Asam... 3
2.3 Sulfur Dioksida... 3
2.4 Tingkat Kelarutan Gas... 4
2.4.1 Kelarutan Gas berdasarkan Suhu... 4
2.4.2 Kelarutan Gas berdasarkan Tekanan... 4
2.5 Kesetimbangan Penyerapan dan Hukum Henry... 5
2.6 Gambaran Umum Kota Bandung... 5
2.6.1 Kondisi Geografis Kota Bandung... 5
2.6.2 Kondisi Iklim Kota Bandung... 7
2.6.3 Kondisi Geologi dan Fisiografi... 7
2.6.4 Transportasi... 7
2.6.5 Industri... 7
2.6.6 Air Quality Monitoring System... 8
3. METODOLOGI 3.1 Waktu dan Tempat Penelitian... 10
3.2 Bahan... 10
3.3 Alat... 10
3.4 Asumsi... 10
3.5 Metode... 10
3.5.1 Pendugaan Nilai pH... 10
3.5.2 Kesetimbangan Kimia Fase Cair... 10
3.5.3 Distribusi Spasial dan Temporal Deposisi Asam... 12
4. HASIL DAN PEMBAHASAN 4.1 Kondisi umum Daerah Kajian... 13
4.2 Suhu Udara dan Konstanta Hukum Henry... 14
4.3 Curah Hujan... 14
4.4 Arah dan Kecepatan Angin... 15
4.5 Konsentrasi Gas SO2... 18
4.6 Pendugaan pH Air Hujan... 19
4.7 Distribusi pH Air Hujan... 21
4.8 Distribusi Gas SO2 dan pH... 23
5. KESIMPULAN DAN SARAN 5.1 Kesimpulan ... 28
5.2 Saran... 28
DAFTAR GAMBAR
Gambar 1. Proses Pembentukan Deposisi Asam... 3
Gambar 2. Kelarutan Gas Berdasarkan Suhu... 4
Gambar 3. Batas Administrasi Kecamatan Kota Bandung... 6
Gambar 4. Peta Kemiringan Lahan Kota Bandung... 6
Gambar 5. Rute Angkutan Kota Bandung... ... 8
Gambar 6. Sebaran Lokasi Industri Kota Bandung... ... 9
Gambar 7. Peta Lokasi Stasiun Pemantau Otomatis dan Data Display……..…... 13
Gambar 8. Peta Kontur Ketinggian Stasiun Pemantauan Kualitas Udara Bandung... 13
Gambar 9. Kelarutan SO2 dalam Air Versus Suhu... 14
Gambar 10. Grafik Suhu Udara di Stasiun Kualitas Udara Bandung... 15
Gambar 11. Grafik Curah Hujan Kota Bandung... 15
Gambar 12. Arah dan Kecepatan Angin Musim Hujan Dago... 16
Gambar 13. Arah dan Kecepatan Angin Musim Kering Dago... 16
Gambar 14. Arah dan Kecepatan Angin Musim Hujan Ariagraha... 17
Gambar 15. Arah dan Kecepatan Angin Musim Kering Ariagraha... 17
Gambar 16. Arah dan Kecepatan Angin Musim Hujan Tirtalega ... 17
Gambar 17. Arah dan Kecepatan Angin Musim Kering Tirtalega ... 17
Gambar 18. Arah dan Kecepatan Angin Musim Hujan Batununggal... 17
Gambar 19. Arah dan Kecepatan Angin Musim Kering Batununggal... 17
Gambar 20. Arah dan Kecepatan Angin Musim Hujan Cisaranten... 17
Gambar 21. Arah dan Kecepatan Angin Musim Kering Cisaranten... 17
Gambar 22. Grafik Konsentrasi SO2 Musim Kering... 19
Gambar 23. Grafik Konsentrasi SO2 Musim Hujan... ... 19
Gambar 24. Peta Distribusi SO2 Musim Kering... ... 19
Gambar 25 Peta Distribusi SO2 Musim Hujan... ... ... ... 19
Gambar 26. Grafik pH Dugaan Musim Hujan... 20
Gambar 27. Grafik pH Dugaan Musim Kering... 20
Gambar 28. Grafik pH Terukur Stasiun Cuaca BMG Bandung... ... 21
Gambar 29. Peta Distribusi pH Mingguan Musim Hujan Minggu I... 22
Gambar 30. Peta Distribusi pH Mingguan Musim Hujan Minggu II... 22
Gambar 31. Peta Distribusi pH Mingguan Musim Hujan Minggu III... 22
Gambar 32. Peta Distribusi pH Mingguan Musim Hujan Minggu IV... 22
Gambar 33. Peta Distribusi pH Mingguan Musim Hujan Minggu I... 23
Gambar 34. Peta Distribusi pH Mingguan Musim Hujan Minggu II... 23
Gambar 35. Peta Distribusi pH Mingguan Musim Hujan Minggu III... 23
Gambar 36. Peta Distribusi pH Mingguan Musim Hujan Minggu IV... 23
Gambar 37. Distribusi Gas SO2 Musim Hujan Dago………... 25
Gambar 38. Distribusi Gas SO2 Musim Kering Dago………... 26
Gambar 39. Distribusi Gas SO2 Musim Hujan Ariagraha…………... 26
Gambar 40. Distribusi Gas SO2 Musim Kering Ariagraha …..……... 26
Gambar 41. Distribusi Gas SO2 Musim Hujan Tirtalega…..……... 26
Gambar 42. Distribusi Gas SO2 Musim Kering Tirtalega …..……... 26
Gambar 43. Distribusi Gas SO2 Musim Hujan Batununggal …..……... 26
Gambar 44. Distribusi Gas SO2 Musim Kering Batununggal …..…... 26
Gambar 45. Distribusi Gas SO2 Musim Hujan Cisaranten …..……... 26
DAFTAR TABEL
Tabel 1. Koefisien Hukum Henry dari Gas-Gas Atmosfer yang Terlarut Dalam Air………. 5
Tabel 2. Jumlah Kendaraan Bermotor (Umum dan Pribadi)……….. 7
Tabel 3. Jumlah Industri Non-Formal Kota Bandung………...………….. 8
Tabel 4. Lokasi Stasiun Pengukuran Kualitas Udara Bandung………...…………. 14
Tabel 5. Persentase Perolehan Data (Jumlah Hari Pengamatan) di Stasiun Pemantauan Otomatis Bandung ……….………... 19
Tabel 6. pH Terukur Tahun 2003………...………….. 20
Tabel 7. pH Dugaan Mingguan Musim Hujan 2003………..………. 20
Tabel 8. pH Dugaan Mingguan Musim Kering 2003…………..…..…………....…………. 20
DAFTAR LAMPIRAN Lampiran 1. Pembentukan Partikel Ammonium Sulfat ……... 31
Lampiran 2. Siklus Sulfur di Atmosfer ………... 32
Lampiran 3. Tabel Konsentrasi Gas SO2 di Lima Stasiun Pengukuran Kualitas Udara Kota Bandung ………...…………... 33
Lampiran 4. Tabel pH Dugaan Stasiun Dago Pada Musim Hujan ………...……... 34
Lampiran 5. Tabel pH Dugaan Stasiun Dago Pada Musim Kering………... 35
Lampiran 6. Tabel pH Dugaan Stasiun Ariagraha Pada Musim Hujan ..…………... 36
Lampiran 7. Tabel pH Dugaan Stasiun Ariagraha Pada Musim Kering …………... 37
Lampiran 8. Tabel pH Dugaan Stasiun Tirtalega Pada Musim Hujan ………... 38
Lampiran 9. Tabel pH Dugaan Stasiun Tirtalega Pada Musim Kering... 39
Lampiran 10. Tabel pH Dugaan Stasiun Batununggal Pada Musim Hujan... 40
Lampiran 11. Tabel pH Dugaan Stasiun Batununggal Pada Musim Kering... 41
Lampiran 12. Tabel pH Dugaan Stasiun Cisaranten Pada Musim Hujan... 42
Lampiran 13. Tabel pH Dugaan Stasiun Cisaranten Pada Musim Kering... 43
I. PENDAHULUAN 1.1 Latar Belakang
Topik seputar kimia air hujan, termasuk diantaranya hujan asam, kian mendapat perhatian khusus dan merupakan suatu topik utama dalam isu lingkungan. Hujan asam merupakan masalah lingkungan yang serius karena dapat menyebabkan korositas pada bangunan/gedung atau bersifat korosif terhadap bahan bangunan, merusak tanaman dan hasil produksinya dan merusak kehidupan biota di danau-danau/aliran sungai, sehingga hujan asam perlu diprediksi, dan dikontrol.
Hujan dikatakan bersifat asam apabila memiliki pH di bawah 5,6. Batas rata-rata pH air hujan adalah 5,6 dan merupakan nilai yang dianggap normal atau hujan alami seperti yang telah disepakati secara internasional oleh badan dunia WMO (BMG, 2003). Air hujan alami bersifat asam karena besarnya konsentrasi CO2 di udara, yang apabila bereaksi dengan uap air akan membentuk asam.
Penambahan gas SO2 di atmosfer dapat menambah keasaman air hujan, karena walaupun konsentrasinya di udara lebih kecil daripada CO2, namun kelarutan dan konstanta kesetimbangan SO2 lebih besar daripada CO2. Selain itu H2SO3 merupakan asam yang lebih kuat daripada H2CO3 sehingga dalam konsentrasi yang kecil sekalipun SO2 mempengaruhi keasaman air hujan (Brimblecombe, 1986). Hal ini didukung oleh hasil penelitian Nurhayati dan Hara (2000) yang menyatakan bahwa ion SO4
2-
merupakan kontributor yang memiliki pengaruh dalam pengasaman air hujan di Indonesia.
Nilai pH air hujan merupakan salah satu indikator terjadinya hujan asam, sehingga nilai ini perlu diketahui. Analisa mengenai tingkat konsentrasi unsur-unsur kimia yang terlarut dalam air hujan, termasuk derajat keasamannya (pH) telah dilakukan oleh BMG yaitu dengan melakukan pengukuran air hujan di beberapa kota di Indonesia dan menganalisisnya, namun jumlah stasiun pemantau kualitas air hujan hanya satu untuk setiap kota dan umumnya terletak pada daerah rural sehingga kurang mewakili kondisi sebenarnya di lapang. Selain itu metode sampling dilakukan seminggu sekali, sehingga dikhawatirkan akan mempengaruhi nilai pH air hujan karena kemungkinan air hujan yang tertampung bukan merupakan air pada hujan pertama melainkan beberapa kejadian hujan. Akumulasi dari partikel debu yang tercampur dalam air hujan
selama waktu sampling juga dapat mempengaruhi pH.
Berdasarkan hasil penelitian Tuti Budiwati et al (2005) beberapa kota besar di Indonesia telah mengalami hujan asam. Hal ini diindikasikan dengan pH air hujan yang rendah, yaitu berkisar antara 4,5 – 5,0. Salah satu kota yang telah mengalami hujan asam adalah kota Bandung. Bandung adalah salah satu kota yang mengalami perkembangan dalam segala bidang. Semakin pesatnya kemajuan ekonomi mendorong semakin bertambahnya kebutuhan akan transportasi. Perkembangan pusat bisnis dan industri memacu penggunaan bahan bakar dan emisi. Selain itu topografi Bandung yang unik ikut mempengaruhi potensi polusi udara di kota ini. Topografi dapat mengubah arah dan kecepatan angin secara tiba-tiba dan profil kota besar yang cukup kasap merupakan peredam energi kinetik dan melemahkan angin, sehingga dengan kombinasi yang dimiliki kota Bandung, menyebabkan potensi polusi udara di kota ini cukup tinggi. Konsekuensi peningkatan polutan-polutan di atmosfer inilah yang dapat menyebabkan terjadinya hujan asam.
Untuk memudahkan analisa kualitas air hujan diperlukan suatu pendekatan yang dapat menduga pH air hujan secara langsung. Salah satu pendekatan yang dapat digunakan adalah Hukum Henry dan kesetimbangan fase cair, yang menyatakan bahwa pada saat kesetimbangan tekanan parsial gas di atas suatu campuran sama dengan konsentrasi gas dalam campuran tersebut (Brimblecombe, 1986). Hukum Henry telah banyak digunakan di negara lain baik sebagai metode perhitungan maupun dalam bentuk software sebagai pendekatan dalam memprediksi jumlah gas yang terlarut dalam air hujan atau droplet awan dan pH air hujan.
1.2 Tujuan
1. Menduga pH air hujan di beberapa stasiun pengukuran kualitas udara kota Bandung berdasarkan konsentrasi SO2 dengan menggunakan pendekatan hukum Henry.
2. TINJAUAN PUSTAKA 2.1 Atmosfer
2.1.1 Komposisi Atmosfer
Udara merupakan campuran beberapa macam gas yang perbandingannya tidak tetap, tergantung pada keadaan suhu udara, tekanan udara dan lingkungan sekitarnya. Udara adalah atmosfer yang berada di sekeliling bumi yang fungsinya sangat penting bagi kehidupan makhluk hidup. Gas-gas yang berada di permukaan bumi ada yang memiliki konsentrasi yang sama (permanent gases) sedangkan sebagian lagi konsentrasinya berbeda menurut waktu dan tempatnya
(variable gases). Perubahan konsentrasi
gas-gas ini terjadi karena penggunaannya oleh makhluk hidup atau karena perubahan kondisi alam.
2.1.2 Polusi Udara
Polusi udara adalah kondisi atmosfer dengan kandungan substansi yang sudah melebihi batas normal, yang dapat menimbulkan pengaruh pada hewan, tumbuhan, bahan bangunan dan manusia (Seinfield, 1986). Substansi tersebut adalah unsur kimia alami atau antropogenik hasil aktivitas manusia atau senyawa yang terbentuk di udara, berupa gas, butir cairan atau partikel padat yang bersifat membahayakan maupun aman.
Pada beberapa daerah perkotaan, kendaraan bermotor menghasilkan 85% dari seluruh pencemaran udara yang terjadi (Siregar, 2005). Kendaraan bermotor merupakan sumber pencemar bergerak yang menghasilkan CO, hidrokarbon yang tidak terbakar sempurna, NOx, SOx dan partikel. SOx, khususnya belerang dioksida (SO2) dan belerang trioksida (SO3) yang merupakan senyawa gas berbau tidak sedap, yang banyak dijumpai di kawasan industri yang menggunakan batu bara dan kokas sebagai bahan bakar dan sumber energi utamanya.
2.1.3 Pengaruh Kondisi Meteorologi terhadap Dispersi
2.1.3.1 Stabilitas Atmosfer
Kondisi stabilitas atmosfer terbagi menjadi dua, yaitu stabilitas statis dan stabilitas dinamis (Stull dalam Turyanti, 2005). Stabilitas dinamis ditentukan oleh faktor
buoyancy (daya apung udara akibat pemanasan
dari radiasi matahari) dan wind shears (gesekan yang terjadi antara dua lapisan atmosfer dengan arah angin berbeda), sedangkan stabilitas statis hanya
mempertimbangkan faktor buoyancy. secara umum stabilitas statis terdiri dari tiga kondisi kestabilan, yaitu stabil, tidak stabil dan netral.
Menurut Prawirowardoyo (1986), kondisi stabil adalah kondisi yang terjadi pada saat suhu paket udara lebih kecil daripada suhu udara lingkungan sehingga massa udaranya menjadi lebih besar dan menyebabkan paket tersebut tidak dapat bergerak vertikal ke atas namun akan kembali ke ketinggian semula. Hal ini menyebabkan paket tersebut cenderung stabil di tempatnya. Kondisi stabil biasanya terjadi pada malam hari.
Kondisi tidak stabil terjadi saat suhu paket udara lebih tinggi daripada suhu udara lingkungannya sehingga massa dan tekanan udaranya menjadi rendah dan menyebabkan paket akan mengembang secara vertikal. Kondisi tidak stabil biasanya terjadi pada siang hari akibat pemanasan radiasi matahari yang tinggi.
Kondisi netral terjadi jika suhu paket udara sama dengan suhu udara lingkungan, sehingga suhu keduanya akan sama pada ketinggian yang sama. kondisi ini biasa terjadi pada siang ataupun malam.
Menurut Oke (1978) pergerakan vertikal polutan di boundary layer (lapisan perbatas), secara umum dikendalikan oleh stabilitas udara. Konveksi bebas dan ketebalan lapisan percampuran berperan penting dalam mendifusikan material ke dalam volume yang lebih besar dan membuat suatu batas atas terhadap dimensi vertikal dari volume tersebut. Jika dilihat dari sudut pandang konvektif, kondisi terbaik untuk terjadinya dispersi polutan adalah pada saat kondisi tidak stabil yang kuat dan lapisan percampuran yang tebal, sebaliknya kondisi terburuk untuk terjadinya dispersi polutan adalah pada saat terjadi inversi suhu dan lapisan perbatas stabil. Inversi terjadi saat udara yang hangat dikelilingi oleh udara yang dingin.
2.1.3.2 Kecepatan Angin dan Topografi Angin horizontal memainkan peranan penting dalam transport dan pengenceran polutan. Seiring dengan peningkatan kecepatan angin, volume pergerakan udara oleh suatu sumber dalam suatu periode waktu juga akan meningkat.
yang lebih besar, dan konsentrasi di sekitar daerah tujuan akan menjadi lebih rendah. Perubahan besar dalam arah angin dapat terjadi dalam periode waktu yang singkat.
Topografi dapat berdampak secara mikro dan skala meso pada daerah titik dan daerah sumber. Pegunungan menyebabkan aliran udara lokal yang disebabkan oleh peningkatan kekasapan permukaan sehingga menurunkan kecepatan angin. Sebagai tambahan, pegunungan dan perbukitan membentuk barrier terhadap pergerakan udara.
2.2 Hujan Asam 2.2.1 Definisi Hujan Asam
Hujan asam merupakan istilah umum untuk menggambarkan turunnya asam dari atmosfer ke bumi. Sebenarnya turunnya asam dari atmosfer ke bumi bukan hanya dalam kondisi "basah" tetapi juga "kering". Sehingga dikenal pula dengan istilah deposisi (penurunan/pengendapan) basah dan deposisi kering. Masalah deposisi asam terjadi di lapisan atmosfer terendah, yaitu di troposfer.
Deposisi basah mengacu pada hujan asam, kabut dan salju. Ketika hujan asam ini mengenai tanah, dapat berdampak buruk bagi tumbuhan dan hewan, tergantung dari konsentrasi asamnya, kandungan kimia tanah, buffering capacity (kemampuan air atau tanah untuk menahan perubahan pH), dan jenis tumbuhan/hewan yang terkena.
Deposisi kering mengacu pada gas dan partikel yang mengandung asam. Sekitar 50% keasaman di atmosfer jatuh kembali ke bumi melalui deposisi kering. Kemudian angin membawa gas dan partikel asam tersebut mengenai bangunan, mobil, rumah dan pohon. Ketika hujan turun, partikel asam yang menempel di bangunan atau pohon tersebut akan terbilas, menghasilkan air permukaan (run off ) yang asam.
2.2.2 Proses Pembentukan Hujan Asam Emisi sulfur dan nitrogen yang berasal dari bahan bakar fosil merupakan penyebab utama timbulnya deposisi asam. Ketika kedua unsur polutan bercampur dengan uap air di udara, terbentuklah asam sulfur dan nitrat (H2SO4 dan HNO3).
Seperti halnya asam hidroklorik (yang berasal dari gas HCl yang diproduksi oleh industri berat) dan asam karbonat, di dalam air H2SO4 dan HNO3 akan terurai menjadi ion H
+ dan ion-ion Cl-, CO32-, SO42- dan NO3-. Penambahan ion H+ dan ion-ion negatif ini akan menurunkan nilai pH, yang dipakai
sebagai indikasi tingkat keasaman suatu sampel air hujan.
Secara sederhana, reaksi pembentukan hujan asam adalah sebagai berikut:
Gambar 1. Proses Pembentukan Deposisi Asam
Sumber : Environmental Protection Agency, 2006
2.2.3 Efek Hujan Asam
Hujan asam berdampak langsung pada lingkungan seperti perubahan pH tanah yang menyebabkan perubahan pola adsorption
dan desorpstion sehingga terjadi perubahan
nutrisi pada run off permukaan maupun dari infiltrsi air ke dalam tanah. Hujan asam dapat menurukan laju pertumbuhan tanaman, pertumbuhan tanaman pertanian dan pertumbuhan tanaman hutan. Hujan asam dapat mempercepat pelapukan dan erosi logam, bahan bangunan dan monument-monumen. salah satu dampak yang paling penting adalah hujan asam dapat mengubah kualitas air permukaan dan meracuni spesies perairain.
2.3 Sulfur Dioksida (SO2)
Gas penyebab utama terjadinya hujan asam adalah gas SO2, yang umumnya diemisikan sebagai hasil pembakaran bahan bakar fosil (minyak dan batu bara).
ppm (BMG, 2003). Sumber Buangan Sulfat lainnya adalah :
• Hasil pencucian mineral
(GIPS:CaSO4.2H2O)
• Oksidasi mineral sulfida (PIRIT: FeS2) • Industri deterjen
• Limbah domestik
Pembakaran 1000 kg bahan bakar minyak dapat menghasilkan 60 kg SO2 di atmosfer. Gas SO2 tidak dapat terbakar namun sangat mudah larut dalam air pada suhu ruang sedangkan SO3 tidak reaktif. SO2 larut dalam uap air untuk membentuk asam, dan berinteraksi dengan gas-gas dan partikel lain di udara untuk membentuk sulfat dan produk lain yang dapat membahayakan manusia dan lingkungan. Lebih dari 65% SO2 dilepaskan ke udara atau lebih dari 13 juta ton per tahun, yang berasal dari alat elektronik, khususnya yang menggunakan batu bara. Siklus Sulfur dapat dilihat pada lampiran 1.
Gas SO2 yang dilepaskan dapat dioksidasi oleh OH untuk membentuk H2SO4, Gas ini menjadi higroskopik (kemampuan menyerap air) dan menjadi reaktif dan menyerap H2O dan uap NH3 secara cepat untuk membentuk aerosol NH4HSO4 dan (NH4)2SO4. Hal ini ditunjukkan pada lampiran 2.
Sumber pelenyap senyawa sulfur adalah
rainout dan washout. Rainout adalah proses di
dalam awan melalui aerosol higroskopis dari senyawa sulfur yang bertindak sebagai inti kondensasi dan melalui mekanisme tangkapan dan penggabungan menjadi tetes hujan dan jatuh ke permukaan tanah. Washout adalah proses penangkapan aerosol oleh tetes air hujan yang jatuh, yang meliputi proses yang terjadi di bawah awan.
2.4 Tingkat Kelarutan Gas
Kelarutan suatu gas dalam droplet air hujan merupakan salah satu kontrol yang paling penting dalam kimia air hujan. Kelarutan suatu gas dalam air hujan secara umum dijelaskan oleh suatu persamaan yang dikenal sebagai Hukum Henry, yang menyatakan bahwa pada saat kesetimbangan, tekanan parsial suatu gas dalam larutan sebanding dengan konsentrasi gas dalam larutan tersebut. Dalam mempelajari kimia atmosfer penting untuk mengasumsikan hubungan antara konsentrasi dalam fase gas dan fase cair berada dalam bentuk kesetimbangan.
( )g
A
( )aqA
=
Kondisi gas yang bereaksi dalam air sedikit rumit sehingga hukum Henry hanya menghitung disolusi yang sederhana bukan hidrolisis berikutnya.
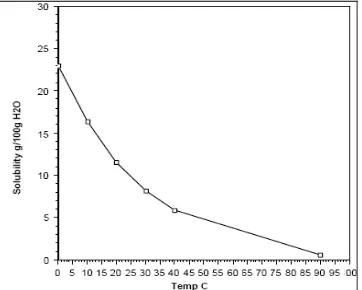
2.4.1 Kelarutan Gas berdasarkan Suhu. Variasi kelarutan gas dengan suhu dapat terlihat dari gambar 8. Seiring dengan peningkatan suhu, kelarutan gas menurun secara perlahan seperti ditunjukkan oleh penurunan trend dalam grafik (Ophardt, 2003).
Larutan lebih banyak berada pada suhu yang lebih rendah dan sangat sedikit yang berada pada suhu yang tinggi.
Sifat kelarutan gas dengan suhu sangat mirip dengan sifat tekanan uap yang meningkat seiring dengan peningkatan suhu. Peningkatan suhu menyebabkan peningkatan energi kinetic. Energi kinetik yang lebih besar menyebabkan lebih banyak gerakan molekul yang memecah ikatan intermolekul dan keluar dari padatan.
Gambar 2. Kelarutan Gas Berdasarkan Suhu (Sumber : virtual chembook, 2003)
2.4.2 Kelarutan Gas berdasarkan Tekanan. Kelarutan suatu gas akan meningkat seiring dengan peningkatan tekanan. Peningkatan tekanan akan menyebabkan molekul-molekul gas dipaksa masuk ke dalam larutan (Ophardt, 2003).
dalam larutan, tetapi setiap gas memiliki daya kelarutan yang berbeda-beda dan hal ini juga mempengaruhi lajunya. Sehingga konstanta kesetimbangan dalam hukum henry harus disertakan dalam perhitungan.
2.5 Kesetimbangan Penyerapan dan Hukum Henry
Penyerapan suatu jenis gas dalam air dapat ditampilkan dalam bentuk :
A (g) + H2O ↔ A.H2O A (g) ↔ A (aq)
Dimana A.H2O dan A (aq) merupakan dua cara penulisan yang berbeda dari gas A dalam keadaan terlarut. Kesetimbangan antara gas A dalam fase gas dengan gas A dalam keadaan terlarut dapat ditunjukkan dalam bentuk konstanta kesetimbangan penyerapan, KA,
[
. 2]
[
−1 −1]
= moleL atm
p O H A K A A
Satuan konvensional tersebut merupakan koefisien hukum Henry, HA
[
A.H2O]
=HApADimana PA merupakantekanan parsial gas A dalam fase gas dan [A.H2O] adalah konsentrasi dari gas A terlarut dalam larutan. Satuan umum koefisien hukum Henry HA adalah [mole l-1 atm-1], sehingga terlihat bahwa KA dan HA adalah identik. Satuan mole l-1 secara umum ditulis sebagai M.
Jika kedua konsentrasi dalam bentuk gas maupun cair dari gas A ditunjukkan dalam sebuah basis molar maka persamaan dapat ditulis sebagai :
[
]
( )
[
]
A AA A
A
H
RT
H
RT
P
P
H
g
A
O
H
.
A
2=
=
&
&
Dimana ĤA merupakan bentuk koefisien hukum Henry yang tidak berdimensi. Untuk mengubah HA menjadi ĤA gunakan R = 0.082 atm M-1 K-1.
Tabel 1 memberikan koefisien hukum Henry dari beberapa gas atmosfer di udara pada suhu 298 K. Nilai yang diberikan dalam tabel tersebut hanya menggambarkan kelarutan gas secara fisik, yaitu hanya kesetimbangan A (g) + H2O ↔ A . H2O. Beberapa jenis gas dalam tabel, sekali terlarut akan berada dalam kesetimbangan asam-basa atau bereaksi dengan air. Suatu jenis gas yang memiliki koefisien hukum Henry yang besar ( > 103 ), secara esensial akan diserap sempurna oleh air.
Tabel 1. Koefisien Hukum Henry dari Gas-Gas Atmosfer yang Terlarut dalam Air
Gas H, M atm-1 (298 K)
O2 1.3 x10
-3
NO 1.9 x10
-3
C2H4 4.9 x10
-3
O3d 9.4 x10-3
NO2 b
1 x 10-2
N2O 2.5 x 10
-2
CO2c 3.4 x 10-2
SO2c 1.24
HNO2c 49
NH3 b
62
HCl 2.5 x 103
HCHOf 6.3 x 103
H2O2 7.1 x 104e
HNO3 c
2.1 x 105
a
diadaptasi dari Schwartz (1983) dan Martin (1984a)
b
NO2 yang terlarut bereaksi dengan air
c
Jenis gas ini berpartisipasi dalam kesetimbangan asam-basa yang tidak terlihat dalam nilai H yang diberikan.
d
ozon sebenarnya terlarut dalam air (Roth dan Sullivan, 1981). Untuk tujuan ini hanya akan digunakan koefisien hukum Henry yang ditampilkan disini dan sebagai fungsi dari temperature. Koefisien hukum Henry dari Roth dan Sullivan adalah H = 3.84 x 107
[OH
-]0.035
exp(-2428/T) [atm mole fraction-1
], didefinisikan oleh PA = HAxA
e
pengukuran koefisien hukum Henry terbaru adalah yang dilakukan oleh Yoshizumi et al (1984) yang mendapatkan nilai koefisien HH2O2 = 1.42 x 105 pada
suhu 293 K.
f
HCHO eksis dalam larutan secara umum dalam bentuk gem-diol: HCHO + H2O ↔ H2C(OH)2. koefisien hukum
Henry yang diberikan dalam table berlaku untuk HCHO dan H2C(OH)2.
2.6 Gambaran Umum Kota Bandung 2.6.1 Kondisi Geografis Kota Bandung.
total luas Kota Bandung, (berdasar luasan peta penggunaan lahan Kota Bandung oleh Bappeda Kota Bandung) yang terlihat hijau kira-kira 35% (4% tegalan, 25% sawah, 4,65% kebun, taman kota 0.63%).
Kota Bandung terdiri dari 26 Kecamatan dengan batas-batas administratif sebagai berikut (gambar 3):
• Sebelah utara : Kota Lembang dan Cisarua
• Sebelah barat : Kota Padalarang dan
Cimahi
• Sebelah selatan : Kota Dayeuhkolot dan Buah Batu
• Sebelah timur : Kota Cileunyi
Lokasi Kota Bandung cukup strategis, dilihat dari segi komunikasi, perekonomian maupun keamanan. Hal tersebut disebabkan :
1) Kota Bandung terletak pada pertemuan poros jalan raya :
a. Barat - Timur yang memudahkan
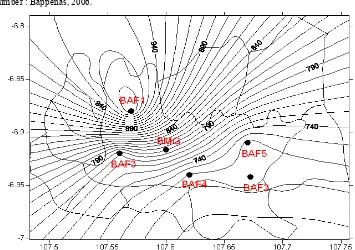
Gambar 3. Batas Administrasi Kecamatan Kota Bandung Sumber : Bappenas, 2006.
hubungan dengan Ibukota Negara b. Utara - Selatan yang memudahkan
lalu lintas ke daerah perkebunan (Subang dan Pangalengan).
2). Letak yang tidak terisolasi dan dengan komunikasi yang baik akan memudahkan aparat keamanan untuk bergerak kesetiap penjuru (Pemerintah Kota Bandung, 2007).
Bentang alam kota bandung mempunyai kemiringan lahan ke arah selatan dan berbukit di bagian utara sehingga berbentuk menyerupai cekungan (Gambar 4).
Kota Bandung bagian utara memiliki ketinggian sekitar 1225 m dpl dan memiliki kemiringan yang cukup curam (diatas 8%), bagian tengah kota Bandung memiliki ketinggian rata-rata 675 m dpl, sedangkan bagian selatan memiliki ketinggian sekitar 750 m dpl dengan kemiringan lahan yang relatif datar.
2.6.2 Kondisi Iklim Kota Bandung
Iklim kota Bandung dicirikan dengan udara lembab yang panas, curah hujan yang tinggi dan kecepatan angin yang sedang. Suhu minimum rata-rata adalah 18°C dan suhu maksimum rata-rata mencapai 30°C. Dari aspek klimatologi, Kabupaten Bandung termasuk dalam tipe iklim B1 (Pemerintah Kota bandung, 2007).
2.6.3 Kondisi Geologi dan Fisiografi
Jenis batuan yang terdapat di kota Bandung terdiri dari tufa pasir dan tufa berbatu apung. Jenis tanah di bagian utara dan selatan kota Bandung berbeda. Jenis tanah di bagian utara umumnya andosol yaitu tanah yang mengandung bahan organik lebih dari 1% dan kejenuhan basa (NH4OAc) lebih dari 50%, sedangkan di bagian selatan serta timur tersebar tanah alluvial kelabu bahan endapan liat yaitu tanah yang berasal dari endapan baru berlapis-lapis dengan bahan organik yang jumlahnya tidak teratur dengan kedalaman dan memiliki kandungan pasir kurang dari 60%, sedangkan di bagian tengah dan barat tersebar tanah latosol.
Sungai-sungai yang melewati Kota Bandung umumnya bersumber di Kecamatan Lembang (Kabupaten Bandung). Sungai besar yang mengalir di tengah kota adalah Sungai Cikapundung, dan di bagian timur kota mengalir Sungai Cidurian. Keadaan drainase di Bandung bagian utara cukup baik, sedangkan di Bandung bagian selatan kurang baik.
Penggunaan lahan yang dominan (tahun 2001) adalah perumahan (64,68%) dan
pertanian lahan kering (27.61%). Penggunaan lainnya adalah industri (3,81%), fasilitas sosial dan perdagangan (Pemerintah Kota Bandung, 2007).
2.6.4 Transportasi
Sistem transportasi memegang peranan penting dalam pengendalian pencemaran udara perkotaan. Makin banyak volume kendaraan yang beroperasi di jalan, makin banyak jumlah emisi gas buang total. Volume pergerakan orang dan kendaraan yang tinggi antara Kota Bandung dan wilayah sekitarnya (Kabupaten Bandung dan Kota Cimahi) telah memberikan kontribusi yang signifikan pada kepadatan lalu lintas di pusat-pusat Kota Bandung.
Kepadatan kendaraan di Bandung cukup tinggi, seperti di jalan Merdeka jumlah kendaraan pribadi yang melintas perjam sekitar 1814, motor 1384, truk 57, angkutan umum sekitar 63. sementara di jalan Asia Afrika kendaraan yang melintas per jam sekitar 1313, motor 1002, truk 42 dan angkutan umum sekitar 32 (Utama dalam Turyanti, 2005)
Kondisi emisi kendaraan bermotor sangat dipengaruhi oleh kualitas bahan bakar dan kondisi pembakaran dalam mesin. Antara tahun 2000 – 2003 jumlah kendaraan bermotor di Kota Bandung bertambah rata-rata 8% per tahun; dengan komposisi sepeda motor terbesar, yaitu sekitar 59% pada 2003.
Tabel 2. Jumlah Kendaraan Bermotor (Umum dan Pribadi)
No Jenis Kendaraan
Jumlah Kendaraan (Unit) 2001 2002 2003
1 Sepeda Motor 283.936 324.366 344.132
2 Penumpang Mobil 164.035 175.333 181.115
3 Barang Mobil 43.455 45.648 46.758
4 Bus Besar 1.263 1.276 1.276
5 Bus Sedang 70 70 70
6 UmumBukan 1.974 2.105 2.151
7 Kendaraan Khusus 263 261 260
Sumber: Bappenas, 2006.
2.6.5 Industri
Jumlah industri di kota Bandung sangat banyak yang mencakup industri formal dan non- formal. Industri formal di Bandung mencakup industri logam, tekstil, kimia pupl dan kertas, elektronika serta agro dan hasil hutan.
No Jenis Industri 2001 2002 2003
1 Kimia 500 895 974
2 Bahan
bangunan 149 456 496
3 Pangan 2278 1185 1289
4 Sandang 2203 1898 2067 5 Barang dari
kulit 834 481 523
6 Barang dari
logam 619 1100 1197 7 Elektronik 100 497 541
8 Kraum 189 715 778
Sumber : Dinas Perindustrian dan Perdagangan Kota Bandung, 2006
2.6.6 Air Quality Monitoring System Jaringan pemantau kualitas udara ambien (Air Quality Monitoring System – AQMS) adalah jaringan pemantauan udara ambien otomatis yang diselenggarakan oleh KLH dan pemerintah 10 kota di Indonesia, yaitu DKI Jakarta, Semarang, Surabaya, Bandung, Pontianak, Palangkaraya, Jambi, Pekanbaru,
Terdapat beberapa stasiun pemantau tetap (fixed station), stasiun bergerak (mobile
station) dan beberapa papan display di setiap
kota tersebut.
Stasiun pemantau mengukur secara kontinu parameter-parameter PM10, SO2, NOx, CO, dan O3, serta parameter meteorologi lokal yaitu arah dan kecepatan angin, temperatur, kelembaban udara, dan radiasi
global. Konsentrasi setiap pencemar yang
diukur di stasiun pemantau dicatat dalam satuan microgram per meter kubik (μg/m3) kecuali CO yang dicatat dalam milligram per meter kubik (mg/m3). Data konsentrasi tersebut kemudian dikonversikan ke dalam Indeks Standar Pencemar Udara (ISPU) melalui perhitungan yang ditetapkan dalam Keputusan Kepala BAPEDAL No. KEP- 107/KABAPEDAL/11/1997. Konversi data pemantauan ke nilai indeks yang kualitatif dan tidak berdimensi tersebut dimaksudkan untuk memudahkan masyarakat menterjemahkan hasil pemantauan kualitas udara ambien. Kategori ISPU terdiri atas 5 kategori, yaitu baik, sedang, tidak sehat dan berbahaya. Saat ini Kota Bandung mempunyai 5 stasiun pemantau udara ambien tetap, 1 stasiun bergerak, dan 5 papan display yang beroperasi sejak tahun 2001. Stasiun-stasiun tetap terletak di Dago Pakar (BAF1), perumahan Arya Graha (BAF2), Tirtalega (BAF3), perumahan Batununggal Indah (BAF4), dan Cisaranten Wetan (BAF5). Lima data display terpasang di Bundaran Cibiru, Taman Tegalega, Alun-alun, Jl. Setiabudi, dan Pintu Tol Pasteur.
Sumber : Bappenas, 2006.
3. METODOLOGI 3.1 Waktu dan Tempat Penelitian.
Penelitian ini dilaksanakan mulai bulan Mei 2007 sampai bulan Januari 2008 di Laboratorium AQMS PUSARPEDAL, Serpong dan Laboratorium Meteorologi Departemen Geofisika dan Meteorologi IPB Bogor.
3.2 Bahan :
• Data polutan udara SO2 di lima stasiun pengukuran kualitas udara Kota Bandung tahun 2003 (AQMS PUSARPEDAL)
• Data curah hujan harian kota Bandung tahun 2003 (BMG)
• Data cuaca (suhu, arah dan kecepatan angin) di lima stasiun pengukuran kualitas udara Kota Bandung tahun 2003 (AQMS PUSARPEDAL)
• Data cuaca (suhu, arah dan kecepatan angin) (BMG)
• Data pH air hujan terukur Kota Bandung (BMG)
3.3 Alat :
• Microsoft Office Word dan Excell
• Software Surface Mapping System
• Software Windrose
3.4 Asumsi
Asumsi yang digunakan dalam penelitian ini adalah :
1. Curah hujan terjadi secara uniform dan kontinu di seluruh daerah kajian. 2. Gas yang bereaksi dalam air cukup
rumit sehingga pendekatan Hukum Henry hanya menghitung untuk pemisahan yang sederhana bukan hidrolisis berikutnya.
3. Konsentrasi dalam fase gas dan cair berada dalam bentuk kesetimbangan.
3.5 Metode :
3.5.1 Pendugaan Nilai pH
Nilai pH air hujan dapat diperkirakan dengan menggunakan data konsentrasi polutan SO2, dengan menggunakan persamaan berdasarkan hukum Henry dan kesetimbangan kimia fase cair (Brimblecombe, 1986).
3.5.2 Kesetimbangan Kimia Fase Cair Pada disolusi dalam air sejumlah zat akan berdisosiasi menjadi ion. Disosiasi ini adalah reaksi timbal balik yang mencapai kesetimbangan dengan cepat (Seinfield, 1986).
Air sendiri akan terionisasi dan membentuk ion hidrogen, H+, dan ion hidroksida, OH-, yang ditunjukkan dalam reaksi sebagai berikut :
− +
+
⇔
H
OH
O
H
2Sehingga pada saat kesetimbangan akan diperoleh:
[ ][
]
[
H O]
OH H K w 2 ' − + =
dimana K′w = 1.82 x 10-16 M pada suhu 298 K. Konsentrasi molekul H2O sangat besar (sekitar 55.5), dan ion yang terbentuk sangat sedikit, sehingga [H2O] sebenarnya konstan. konsentrasi molar dari air murni dapat digabungkan menjadi konstanta kesetimbangan yaitu :
[ ][
+ −]
= H OH
KW
dimana Kw = K′w[H2O] = 1 x 10 -14
M2 pada suhu 298 K Untuk air murni, setiap molekul air berdisosiasi menghasilkan satu ion hydrogen dan satu ion hidroksida, sehingga [H+] = [OH -], sehingga pada suhu 298 K, [H+] = [OH-] = 1 x 10-7 M. total konsentrasi ion dalam air murni hanya 0.2 μM dibandingkan dengan 55,5 M untuk air murni itu sendiri. Sehingga secara kasar terdapat 300 juta molekul air untuk tiap ion dalam air murni. Sebagai hasilnya, air murni diketahui merupakan elektrolit yang sangat lemah dan hanya memiliki konduktivitas listrik yang sangat kecil.
pH air dapat dihitung dengan menggunakan persamaan :
[ ]
+−
=
H
pH
log
sehingga terlihat bahwa pH air murni pada suhu 298 K adalah 7.0.
Sulfur Dioksida / Kesetimbangan Air Pada saat proses disolusi terjadi, SO2 terhidrolisis sehingga molekul SO2 akan berkombinasi dengan molekul air dan membentuk satu molekul SO2.H2O yang merepresentasikan konsentrasi gas SO2 yang terlarut dalam air. Sulfur dioksida terlarut, SO2.H2O, berdisosiasi dua kali untuk membentuk ion sulfit dan ion bisulfit.
Konstanta kesetimbangan untuk ketiga reaksi di atas adalah :
[
]
2 2 2 2. SO SO hs p O H SO HK = =
[H+] [HSO3-] Ks1=
[SO2 . H2O]
[H+] [SO32-] Ks2 =
[HSO3
-]
(Sumber : Seinfield, 1986)
dimana Khs adalah konstanta kesetimbangan untuk hidrolisis SO2, dan Ks1 serta Ks2 adalah konstanta kesetimbangan disosiasi pertama dan kedua untuk SO2 terlarut. Terlihat bahwa konstanta disosiasi kedua sangat kecil bila dibandingkan dengan konstanta disosiasi pertama sehingga pengaruhnya terhadap pH sangat kecil dan dapat diabaikan.
Terlihat dari reaksi tersebut bahwa konsentrasi air cair telah bergabung ke dalam konstanta hidrolisis dan bahwa Khs identik dengan koefisien hukum Henry untuk SO2, yaitu KSO2, sehingga konsentrasi gas dalam larutan
diberikan oleh persamaan :
[SO2 . H2O] = KhsPSO2
Ks1 [SO2 . H2O] KhsKsiPSO2
[HSO3-] = =
[H+] [H+]
Ks2[HSO3-] KhsKsiKs2PSO2
[SO32-] = =
[H+] [H+]2
(Sumber : Seinfield, 1986)
Dari ketiga persamaan tersebut maka hubungan elektronetralitas (hubungan konsentrasi ion dalam larutan) dari ion-ion tersebut dapat ditentukan, yaitu :
[ ] [ ]
+ = − +[
−] [
+ 2−]
3 3 2SO HSOOH H
(Sumber : Seinfield, 1986)
Jika sumber ion hidrogen dalam sistem hanya berasal dari disosiasi gas SO2, sehingga [HSO3-] =[H+], maka dapat digunakan persamaan sebagai berikut :
[
HSO3]
=[ ]
H = KHK′pSO2+ −
dimana :
KH = Konstanta hukum Henry
K′ = Konstanta disosiasi pertama hukum Henry (2.7 x 10-2 pada suhu 15°C dan 1.7 x 10-2 pada T =298 K).
pSO2 = Tekanan parsial gas SO2.
(Sumber : Brimblecombe, 1986)
Tekanan parsial adalah kontribusi tekanan total dalam campuran yang dibuat oleh salah satu komponen dalam campuran pada kondisi kesetimbangan. Tekanan parsial gas SO2 dapat dicari dengan menggunakan persamaan berikut :
C
K
pSO
2=
H×
dimana :
pSO2 =Tekanan parsial gas SO2 (atm)
KH =Konstanta hukum Henry (mol L-1 atm-1)
C =Konsentrasi gas dalam
larutan (μg/m3)
Satuan tekanan parsial gas SO2 adalah atm, sehingga konsentrasi gas SO2 harus dikonversi ke dalam mol/L, yaitu :
L mol g mol m g mol g m g Mr C 9 3 3 3 10 10 / / = − × = − =μ
Sehingga persamaan (16) akan menjadi :
(
C)
K
pSO H 9
2 10
−
× =
Konstanta hukum Henry dapat berubah tergantung suhu, konstanta hukum Henry akan semakin besar seiring dengan penurunan suhu. Cara sederhana untuk menjelaskan hukum Henry sebagai fungsi suhu adalah sebagai berikut : ⎥ ⎦ ⎤ ⎢ ⎣ ⎡ ⎟ ⎠ ⎞ ⎜ ⎝ ⎛ − ⎟ ⎠ ⎞ ⎜ ⎝ ⎛ Δ− = Θ Θ T T R H so K
KH H exp ln 1 1
dimana :
KHӨ = Koefisien hukum Henry dalam kondisi standar (TӨ = 298,15 K) = 1.2 M/atm.
TӨ = Suhu kondisi standar = 298.15
(-ΔsolnH/R) = Entalpi campuran yang disini merupakan temperature
dependence = -d ln KH/d (1/T) = 2900 K.
(Sumber : Sander, 1999)
sehingga konstanta disosiasi pertama hukum Henry juga dapat ditentukan berdasarkan persamaan tersebut. ⎥ ⎦ ⎤ ⎢ ⎣ ⎡ ⎟ ⎠ ⎞ ⎜ ⎝ ⎛ − ⎟ ⎠ ⎞ ⎜ ⎝ ⎛ Δ− ′ = ′ Θ Θ T T R H so K
K exp ln 1 1
dimana :
K′′θ = Konstanta disosiasi
pertama hukum Henry dalam kondisi standar
(-ΔsolnH/R) = Entalpi campuran yang
disini merupakan
temperature dependence = -d
ln KH/d (1/T) = 2090 K. (Sumber : Sander, 1999)
3.5.3 Distribusi Spasial dan Temporal Deposisi Asam.
Distribusi arah angin, pH, dan SO2 untuk masing-masing lokasi didekati dengan pemetaan menggunakan Software Surface
Mapping System dan Windrose. Hal ini
dimaksudkan untuk menduga distribusi spasial dan distribusi temporal, baik periode mingguan atau bulanan. Software surface mapping
system digunakan untuk melihat
kecenderungan konsentrasi gas SO2 tertinggi atau nilai pH yang terendah di setiap stasiun kajian, sedangkan Windrose digunakan untuk melihat distribusi gas SO2 dan arah angin sehingga diketahui ke arah mana gas akan terbawa yang akan menyebabkan pH di daerah tujuan angin akan menurun.
Surfer adalah salah satu perangkat lunak yang digunakan dalm pembuatan peta kontur dan pemodelan tiga dimensi yang berdasarkan pada grid. Grid adalah serangkaian garis vertikal dan horizontal yang dalam surfer berbentuk segiempat dan digunakan sebagai dasar pembentuk kontur dan surface tiga dimensi (Budiyanto, 2005).
Pembuatan peta kontur ataupun model tiga dimensi dalam surfer diawali dengan pembuatan data tabular XYZ. Data XYZ selajutnya diinterpolasikan dalam sebuah file grid. Proses kedua ini sering disebut dengan istilah gridding. Proses gridding menghasilkan sebuah file grid. File grid digunakan sebagai dasar pembuatan peta kontur dan model tiga dimensi.
Gridding menentukan prosedur interpolasi dari pembuatan file grid. Dalam
penelitian ini metode yang digunakan adalah
Kriging. Metode ini digunakan karena Kriging
adalah metode yang fleksibel dan dapat digunakan ke sebagian besar data. Kemampuan menerima berbagai data menjadikan metode ini sebagai metode yang efektif.
Data polutan di lima stasiun pengukuran pada tahun 2003 tidak kontinu dan data lengkap hanya pada bulan Januari dan Juni sehingga analisa distribusi spasial dan temporal SO2, angina dan pH air hujan dugaan akan dibagi ke dalam musim kering (bulan Juni) dan musim hujan (bulan Januari).
Gambar 7. Peta Lokasi Stasiun Pemantau Otomatis dan Data Display Sumber : Bappenas, 2006.
4. HASIL DAN PEMBAHASAN 4.1 Kondisi Umum Daerah Kajian
Stasiun pemantauan kualitas udara (fix station) yang terdapat di Bandung ada lima stasiun dan masing-masing mewakili daerah dataran tinggi, pemukiman padat penduduk, daerah padat lalu lintas, daerah perumahan
industri dan daerah padat industri yaitu, Dago (BAF1), Ariagraha (BAF2), Tirtalega (BAF3), Batununggal (BAF4) dan Cisaranten Wetan (BAF5). Kelima stasiun ini terletak pada koordinat dan ketinggian yang berbeda, yang disajikan dalam Tabel 4.
[image:32.612.138.493.442.692.2]Tabel 4. Lokasi Stasiun Pengukuran Kualitas Udara Bandung
Stasiun Latitude Longitude Altitude (mdpl) BAF1 107.57 -6.88 982
BAF2 107.67 -6.94 719
BAF3 107.56 -6.92 771
BAF4 107.62 -6.94 718
BAF5 107.67 -6.91 715
Dari tabel terlihat bahwa stasiun Dago merupakan satu-satunya stasiun yang terletak di daerah dataran tinggi sebelah utara Bandung, sedangkan ke empat stasiun lainnya terletak pada daerah dengan topografi relatif datar. Ariagraha dan Batununggal terletak di Selatan Bandung, Cisaranten Wetan di bagian Timur Bandung sedangkan Tirtalega di bagian Barat yang merupakan daerah dengan topografi paling rendah.. Secara umum seluruh stasiun pemantauan kualitas udara Kota bandung terletak pada cekungan Bandung (gambar 7 dan 8).
Topografi Kota Bandung yang seperti cekungan dan relatif rumit ini menyebabkan dispersi/transpor zat-zat pencemar dalam bentuk gas, partikel, dan aerosol ke atmosfer terhambat atau daya pengenceran udara berkurang. Kemampuan udara untuk mendispersikan zat-zat pencemar sangat ditentukan oleh topografi dan stratigrafi daerah dan faktor meteorologi (kecepat