TERHADAP MIKROBA
PATOGEN PANGAN
ASRIANI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Saya menyatakan dengan sebenar-benarnya bahwa segala pernyataan dalam disertasi saya yang berjudul
KAJIAN EFEK SINERGI ANTIMIKROBA METABOLIT BAKTERI ASAM LAKTAT DAN MONOASILGLISEROL MINYAK KELAPA TERHADAP
MIKROBA PATOGEN PANGAN
adalah karya saya sendiri dengan pembimbingan komisi pembimbing dan belum pernah diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal dari atau dikutip dari karya yang diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka.
Bogor, November 2006
Asriani
and Monoacylglycerol of Coconut Oil Mixture on Food Pathogen Microbes. Under the Supervision of: BETTY SRI LAKSMI JENIE, SEDARNAWATI YASNI, and IDWAN SUDIRMAN.
Synergistic effect of two or more kinds of antimicrobial substances usually expressed higher activity than the cumulative given by both or more antimicrobial substances. The organic acid and monolaurin have been reported to show synergism as antimicrobials in food. The lactic acid bacteria (BAL) are known as organic acid producer, mainly lactic acid, while the monoacylglycerol (MAG) of coconut oil known having antimicrobial properties due to its short and medium chains of fatty acids, especially lauric acid.
Study on the synergic effect of antimicrobial activity of BAL metabolites and MAG of coconut oil mixture had been conducted using six strains of BAL i.e.
Lactobacillus brevis, Lb. acidophilus, Lb. plantarum pi28a, Lb. plantarum sa28k, Lb. plantarum kik and Lb. coryneformis. The aims of the studies were: (1) to obtain BAL which have the highest synergic antimicrobial effect with MAG; (2) to obtain the optimum ratio of BAL and MAG and its MIC (minimum inhibitory concentration) for the test bacteria; (3) to analyze the mechanism of action of BAL-MAG mixture on bacterial cells; (4) to evaluate the stability of the combined BAL-MAG in different pH and heating temperatures and times.
The isolates of BAL which have effect synergic with MAG and the optimum ratio of BAL and MAG were conducted by using well diffusion method, while the MIC (minimum inhibitory concentration) for the test bacteria conducted by using contact method. The action mechanism of BAL-MAG on protein and nucleic acid leakages were observed by using Spectrophotometer, K+ and Ca2+ leakages with Atomic Absorbtion Spectrophotometer, and the morphology of cells were observed by using SEM (Scanning Electron Microscope). The evaluation of stability of the combined BAL-MAG of coconut oil were conducted on pH 4, 5, 6, and 7, on room temperature of 80, 100, and 121 oC as long as 10, 20, and 30 minutes by using well diffusion. The application on food system (tofu) were conducted by soaking in 2 and 4 MIC concentrations.
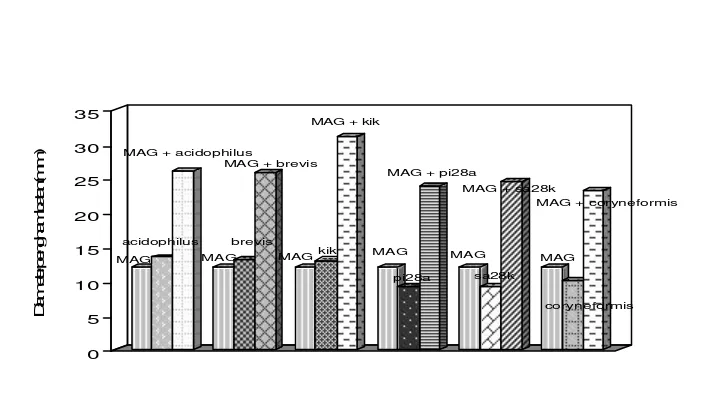
Among the BAL studies, Lb. plantarum kik showed the highest synergic effect with MAG against Listeria monocytogenes. The optimum ratio of BAL metabolites - MAG mixture were found at 5:3. Combination of Lb. plantarum kik – MAG could inhibit the growth of all bacteria tasted with the highest activity showed against Listeria monocytogenes was 30,66 mm in diameter of inhibition zone; and the lowest activity against Escherichia coli was 20.20 mm.
The MIC values found out were 1,2%, 1,4%, 2,5% and 3% for Listeria monocytogenes, Bacillus cereus, Salmonella Typhimurium and Escherichia coli,
Ca2+ was higher than K+. The effect of the mixture on the cell morphology of L. monocytogenes and Salmonella Typhimurium observed Under SEM (Scanning Electron Microscopo) caused some degree of cell damage according to the concentration applied. In general, the higher the concentration applied, the more were the cell damage occurred.
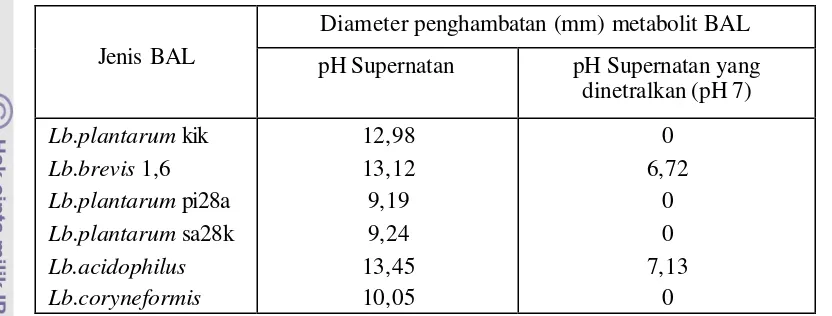
Stability of the mixture Lb. plantarum kik metabolite-MAG was affected by different pH and heating temperature and time. At pH 4-7, the antibacterial activity of the mixture and individual MAG were quite stabil, except for the individual Lb. plantarum
kik did not show antibacterial activity at pH 7.
The mixture still showed bacterial activity after heating at 75 and 100 oC for 10, 20, and 30 minutes, whereas at 121 oC, bacterial activity only showed on heating for 10 minutes, either for individual substances or the mixture. Application of the metabolite of
Lb. plantarum kik metabolite-MAG on soybean curd as food system model at the concentration of 4 MIC could extend the shelf life long as 6 days at room temperature.
Key words: Antimicrobial synergistic effect, lactic acid bacteria (LAB), monoacylglycerol (MAG), food pathogen microbes.
ASRIANI. Kajian Efek Sinergi Antimikroba Campuran Metabolit Bakteri Asam Laktat dan Monoasilgliserol Minyak Kelapa Terhadap Mikroba Patogen Pangan. Dibawah bimbingan BETTYSRI LAKSMI JENIE, SEDARNAWATI YASNI dan IDWAN SUDIRMAN.
Efek sinergi suatu senyawa antimikroba didefinisikan sebagai efek yang dihasilkan oleh campuran dari dua jenis atau lebih antimikroba yang akan memberikan pengaruh yang lebih besar dari jumlah efek kumulatif campuran kedua antimikroba tersebut. Asam organik dan monolaurin telah dilaporkan memiliki sifat sinergi dalam penggunaannya sebagai bahan antimikroba dalam bahan pangan. Bakteri asam laktat merupakan salah satu jenis bakteri yang dikenal sebagai penghasil asam organik terutama asam laktat, sedangkan monoasilgliserol dari minyak kelapa diketahui memiliki sifat antibakteri dan antikapang karena mengandung asam-asam lemak rantai pendek dan menengah terutama asam laurat.
Kajian efek sinergi antimikroba campuran metabolit BAL dan MAG minyak kelapa telah dilakukan dengan menggunakan enam isolat BAL, yaitu: Lb. brevis, Lb. acidophilus, Lb. plantarum pi28a, Lb. plantarum sa28k, Lb. plantarum kik dan Lb. coryneformis. Tujuan penelitian ini adalah: (1) untuk memperoleh BAL yang memiliki efek sinergi tertinggi dengan MAG minyak kelapa; (2) untuk memperoleh rasio optimal dari campuran metabolit BAL-MAG minyak kelapa dan MIC untuk uji bakteri; (3) untuk menguji stabilitas campuran metabolit BAL-MAG minyak kelapa terhadap perbedaan pH, pemanasan dan waktu, serta aplikasinya pada sistem pangan tahu.
Isolat bakteri asam laktat yang diseleksi adalah Lb. brevis, Lb. acidophilus, Lb. plantarum pi28a, Lb. plantarum sa28k, Lb. coryneformis dan Lb. plantarum kik. Pengujian aktivitas antibakteri dari campuran metabolit BAL-MAG minyak kelapa dilakukan terhadap 4 jenis bakteri yaitu Listeria monocytogenes, Bacillus cereus,
Salmonella Typhimurium, dan Escherichia coli serta Aspergillus flavus.
Seleksi BAL yang bersinergi dengan MAG minyak kelapa dan penentuan rasio metabolit BAL-MAG dilakukan dengan menggunakan metode difusi sumur, sedangkan penentuan nilai MIC dilakukan dengan metode kontak. Pengamatan terhadap mekanisme kerja dari campuran metabolit BAL-MAG minyak kelapa terhadap kebocoran protein dan asam nukleat dengan spektrofotometer, kebocoran ion Ca2+ dan ion K+ dengan AAS (Atomic Absorption Spektrofotometer), serta morfologi sel dengan SEM (Scanning Electron Microscope). Pengujian stabilitas campuran metabolit BAL-MAG minyak kelapa dilakukan pada pH 4, 5, 6, dan 7 serta suhu 80, 100 dan 121 oC selama 10, 20 dan 30 menit dengan metode difusi sumur. Aplikasi terhadap sistem pangan tahu dilakukan dengan perendaman pada konsentrasi 2 dan 4 MIC.
2,5% dan 3% berturut-turut untuk L. monocytogenes, B. cereus, S. Typhimurium dan E. coli. Campuran metabolit Lb. plantarum kik-MAG minyak kelapa juga menunjukkan sinergi aktivitas antikapang yang cukup baik dengan mereduksi berat miselia Aspergillus flavus sebesar (0,86-2,75 mg/ml) dari pada penggunaan secara tunggal (0,35-1,54 mg/ml) pada konsentrasi 5-20%.
Semakin tinggi konsentrasi campuran metabolit Lb. plantarum kik-MAG minyak kelapa maka kebocoran sel makin parah, dimana kebocoran protein lebih tinggi dari pada asam nukleat. Demikian halnya dengan kebocoran ion Ca2+ lebih besar dari pada ion K+. Pengamatan dengan SEM menunjukkan metabolit Lb. plantarum kik -MAG minyak kelapa menyebabkan perubahan morfologi sel Listeria monocytogenes dan Salmonella
Typhimurium pada tingkat kerusakan yang bervariasi, seperti terjadinya pembengkakan sel diikuti dengan pengkerutan pada sel L. monocytogenes dan terhambatnya gangguan pada pembentukan septa dan terbentuknya lubang pada permukaan sel S.Typhimurium
Stabilitas dari campuran metabolit Lb. plantarum kik-MAG minyak kelapa dipengaruhi oleh pH, dan pemanasan. Aktivitas antibakteri pada pH 4-7 cukup stabil kecuali pada penggunaan tunggal dari metabolit Lb. plantarum kik, yaitu pada pH 7 tidak menunjukkan aktivitas antibakteri.
Campuran metabolit Lb. plantarum kik-MAG minyak kelapa masih menunjukkan aktivitas antibakteri pada pemanasan 75 dan 100 oC selama 10, 20 dan 30 menit, sedangkan pada suhu 121 oC aktivitas antibakteri hanya diperlihatkan selama pemanasan 10 menit baik terhadap penggunaan tunggal dari metabolit Lb. plantarum kik dan MAG minyak kelapa maupun campurannya. Aplikasi metabolit Lb. plantarum kik-MAG minyak kelapa pada tahu sebagai model sistem pangan dengan konsentrasi 2 MIC mampu bertahan selama 4 hari dibandingkan kontrol (1 hari), sedangkan pada konsentrasi 4 MIC dapat bertahan selama 6 hari pada suhu ruang dengan sifat organoleptik (warna, bau dan tekstur) yang masih diterima oleh panelis.
Kata kunci : Efek sinergi antimikroba, bakteri asam laktat (BAL), monoasilgliserol (MAG), mikroba patogen pangan.
PRAKATA ...
Bakteri Asam Laktat………... Metabolit Hasil Produksi Bakteri Asam Laktat ....………. Monoasilgliserol……….. Sifat Antimikroba Monoasilgliserol Minyak Kelapa……….. Mikroba Patogen pada Bahan Pangan ………... Mekanisme Kerja Senyawa Antimikroba………... Daftar Pustaka ……… ………... 3 METODOLOGI UMUM
Tempat dan Waktu ……….……….... Bahan dan Alat ……....………... Metodologi Penelitian ...………...…….. Daftar Pustaka.……… 4 EFEK SINERGI ANTIBAKTERI BEBERAPA CAMPURAN
METABOLIT BAL DENGAN M AG MINYAK KELAPA
DALAM MENGHAMBAT PERTUMBUHAN Listeria
monocytogenes
5 AKTIVITAS ANTIMIKROBA CAMPURAN METABOLIT Lb.plantarum kik-MAG MINYAK KELAPA TERHADAP MIKROBA PATOGEN PANGAN
Abstrak………....
6 MEKANISME KERJA ANTIBAKTERI CAMPURAN
METABOLIT Lb. plantarum kik-MAG MINYAK KELAPA TERHADAP BAKTERI PATOGEN PANGAN
Abstrak……… Pendahuluan ………... Metodologi……….. Hasil dan Pembahasan… ……… Kesimpulan………... Daftar Pustaka………... 7 STABILITAS AKTIVITAS ANTIMIKROBA METABOLIT Lb. plantarum kik-MAG MINYAK KELAPA SERTA APLIKASINYA PADA PRODUK TAHU
8 PEMBAHASAN UMUM ………...
2.1
2.2
2.3 2.4
4.1
4.2
5.1
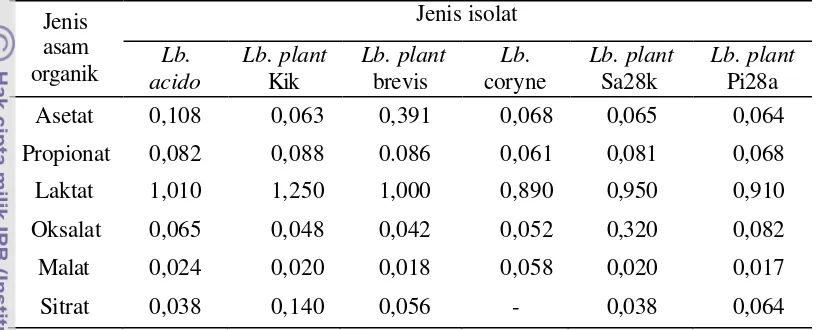
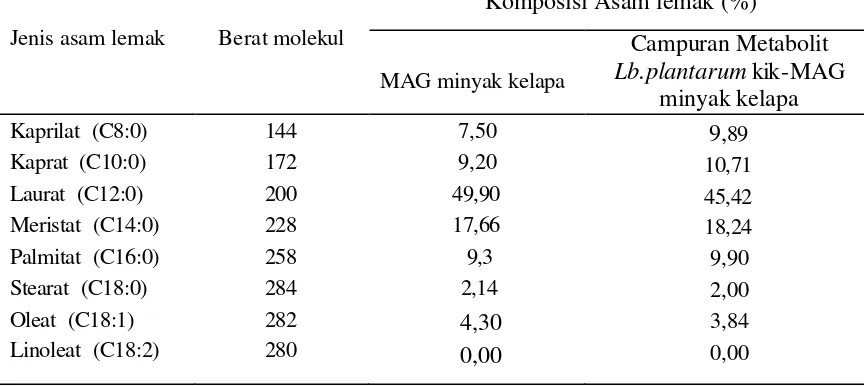
Aktivitas antibakteri dari monolaurin dan bahan pengawet pangan lainnya………..……… Aktivitas antikapang dari monolaurin dan bahan pengawet pangan lain...………... Komposisi asam lemak beberapa jenis minyak nabati ... Penurunan massa sel (%) kapang dan khamir pada beberapa jenis antimikroba pada konsentrasi 1%... Kandungan asam-asam organik (%) berbagai metabolit isolat BAL hasil pengujian dengan HPLC ... Diameter penghambatan dari beberapa metabolit BAL pada pH Supernatan dan pH supernatan yang dinetralkan ... Kandungan asam-asam lemak pada MAG minyak kelapa serta campuran metabolit Lb. plantarum kik-MAG minyak kelapa ...
12
12 13
15
55
56
69
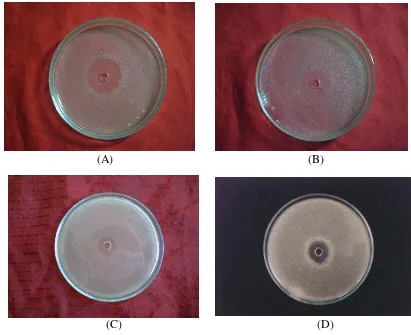
Hal Struktur dinding sel bakteri Gram positif dan Gram negatif (Kightley R, 2006)…………... Bagan alir pelaksanaan penelitian ... Diameter penghambatan MAG minyak kelapa dalam berbagai konsentrasi alkohol ... Diameter penghambatan penggunaan tunggal metabolit (1) coryneformis; (2) sa28k; (3) MAG; (4) pi28a; (5) kik; (6) acidophilus; (7) brevis terhadap L. monocytogenes ... Diameter penghambatan penggunaan campuran metabolit (1) kik+MAG; (2) pi28a+MAG; (3) coryneformis + MAG; (4) acidophilus + MAG; (5) sa28k + MAG; (6) brevis + MAG terhadap L. monocytogenes ... Aktivitas antibakteri MAG minyak kelapa dan metabolit BAL serta Campuran metabolit BAL-MAG minyak kelapa terhadap L. monocytogenes ... Aktivitas antibakteri campuran metabolit Lb.plantarum kik- MAG minyak kelapa pada berbagai rasio terhadap L.monocytogenes…… Aktivitas antibakteri campuran metabolit Lb.plantarum kik-MAG terhadap beberapa bakteri patogen ... Diameter penghambatan campuran metabolit Lb.plantarum kik-MAG terhadap (A) L.monocytogenes; (B) B.cereus; (C) E.coli dan (D) S.Typhimurium ... Nilai MIC metabolit Lb.plantarum kik-MAG minyak kelapa terhadap beberapa bakteri patogen ... Berat kering miselia kapang Aspergillus flavus (mg/ml) yang diberi metabolit Lb. plantarum kik,MAG dan campuran metabolit
6.2a
Pengaruh dosis campuran metabolit Lb. plantarum kik-MAG minyak kelapa terhadap kebocoran ion-ion logam dari sel B. cereus ... Pengaruh dosis campuran metabolit Lb. plantarum kik-MAG minyak kelapa terhadap kebocoran ion-ion logam dari sel S. Typhimurium... Bentuk sel normal L. monocytogenes (20.000 X)... Pengaruh campuran metabolit Lb. plantarum kik-MAG pada dosis 1 MIC terhadap morfologi sel L. monocytogenes (20000X) .. Pengaruh campuran metabolit Lb. plantarum kik-MAG Minyak kelapa pada konsentrasi 2 MIC terhadap morfologi sel L. monocytogenes (20.000X) ... Bentuk sel normal S. Typhimurium (15.000 X) ... Pengaruh campuran metabolit BAL-MAG pada dosis 1 MIC terhadap morfologi sel S. Typhimurium (15.000X) ... Pengaruh campuran metabolit BAL-MAG pada dosis 2 MIC terhadap morfologi sel Salmonela Typhimurium(15.000X) ... Pengaruh pH terhadap aktivitas antibakteri campuran metabolit
Lb. Plantarum kik-MAG minyak kelapa ... Pengaruh pH terhadap aktivitas antibakteri metabolit Lb. plantarum kik... Pengaruh pH terhadap aktivitas antibakteri MAG minyak kelapa ... Pengaruh suhu dan lama pemanasan terhadap aktivitas antibakteri campuran metabolit Lb.plantarum kik -MAG minyak kelapa ... Pengaruh suhu (oC) dan lama pemanasan terhadap aktivitas antibakteri metabolit Lb. plantarum kik ... Pengaruh suhu dan lama pemanasan terhadap aktivitas antibakteri MAG minyak kelapa ... Pengaruh konsentrasi campuran metabolit Lb. plantarum kik-MAG minyak kelapa pada berbagai MIC terhadap penurunan total mikroba (log CFU/g) pada tahu yang disimpan sampai hari ke-6 ... Pengaruh konsentrasi campuran metabolit Lb. plantarum kik- MAG minyak kelapa pada berbagai MIC terhadap skor panelis terhadap warna tahu yang disimpan sampai hari ke-6 ... Pengaruh konsentrasi campuran metabolit Lb. plantarum kik-MAG minyak kelapa pada berbagai MIC terhadap skor
7.4b
7.4c
Pengaruh konsentrasi campuran metabolit Lb. plantarum kik-MAG minyak kelapa pada berbagai MIC terhadap skor penerimaan panelis tekstur tahu yang di simpan sampai hari ke 6 ..
Kesadaran masyarakat terhadap kesehatan semakin meningkat sementara
masyarakat dihadapkan pada tuntutan kebutuhan pangan yang praktis, mudah
diolah, siap saji dan tahan lama tanpa bahan pengawet sintetik, serta tetap bermutu dan aman dikonsumsi. Oleh karena itu diperlukan penerapan teknologi rintangan
(hurdle) dengan menggunakan bahan pengawet alami.
Bakteri asam laktat (BAL) telah diketahui menghasilkan senyawa
antimikroba berupa asam organik (asam laktat, asam asetat, asam format) diasetil,
hidrogen peroksida, karbon dioksida dan bakteriosin. Berbagai jenis BAL yang bersifat antimikroba telah berhasil diisolasi dari berbagai jenis makanan Indonesia
diantaranya Lie (1996); Idawati (1996); Solihati (1996) dan Jenie et al. (2000) . Potensi BAL sebagai bahan pengawet pangan nabati maupun hewani telah
diteliti oleh beberapa peneliti. Jenie et al. ( 2000) melaporkan bahwa penggunaan BAL pada ikan peda kering mampu mereduksi pertumbuhan Staphylococcus aureus dan Bacillus cereus sebesar tiga unit log (log cycle). Smith et al. (2005) melaporkan kemampuan dari bakteri asam laktat dalam mereduksi E. coli O157:H7 sebesar 2,5 unit log dan Salmonella 3 unit log pada daging sapi selama penyimpanan 12 hari pada suhu penyimpanan 5 oC. Selanjutnya dijelaskan bahwa efek penghambatan dari BAL disebabkan adanya produksi asam organik, hidrogen
peroksida maupun bakteriosin yang semuanya diketahui memiliki efek
antimikroba.
BAL selain diketahui memiliki sifat antibakteri yang cukup luas juga
memiliki sifat antikapang. Sifat antikapang BAL tersebut oleh beberapa peneliti
dilaporkan terdapat dalam suspensi BAL, sedangkan dalam supernatan pada
konsentrasi tertentu sifat antikapang tersebut tidak terlihat. Hal ini dilaporkan oleh
Gourama dan Bullerman (1995) bahwa suspensi sel BAL (L. acidophilus, L. bulgaricus dan L. plantarum) mampu menghambat pertumbuhan kapang dan produksi aflatoksin Aspergillus flavus, sedangkan supernatan bebas selnya tidak mampu menghambat pertumbuhan kapang, tetapi mampu menghambat produksi
efek penghambatan dari L. acidopihilus; Lactobacillus delbrueki subsp. Lactis dan Lactococcus lactis subsp. lactis terhadap kapang P. commune dan P. roqueforti. Dengan demikian potensi BAL sebagai antikapang umumnya lebih rendah dari
sifat antibakterinya. Hal lain yang juga masih menjadi kendala di dalam
penggunaan asam organik dari BAL ini adalah rasanya yang asam sehingga akan
membatasi aplikasinya pada bahan-bahan pangan. Salah satu upaya untuk
mengatasi hal ini, adalah dengan mengkombinasikan metabolit BAL sebagai sumber asam organik dengan antimikroba lain yang juga bersifat sebagai
antimikroba alami (antibakteri dan antikapang) seperti monoasilglisero l (MAG)
dari minyak kelapa. Dengan cara ini diharapkan tidak hanya rasa asam dari
metabolit BAL tersebut dapat direduksi tetapi juga aktivitas antimikrobanya
menjadi efektif, dan peluang penggunaan antimikroba alami menjadi luas.
Selain itu, penggunaan MAG minyak kelapa dan metabolit BAL sebagai
senyawa antimikroba akan menguntungkan karena akan diperoleh senyawa
antimikroba yang relatif aman serta mudah diperoleh, dan secara organoleptik
dapat diterima.
Monoasilgliserol (MAG) minyak kelapa yang pada awalnya hanya dikenal
sebagai bahan pengemulsi pangan ternyata dapat berperan sebagai bahan pengawet pangan dan sifat ini tidak dimiliki oleh MAG dari minyak nabati lain (Wang et al. 1993). Perbedaan ini terutama oleh adanya asam lemak jenuh rantai pendek dan
menengah, sedangkan minyak nabati lain didominasi oleh asam lemak tidak jenuh
dan asam lemak jenuh rantai panjang. Jenis MAG minyak kelapa yang telah
ditemukan bersifat antimikroba khususnya untuk bakteri dan kapang adalah
monolaurin, monokaprilin, monokaprat, monomeristin dan monoasilgliserol.
Outara et al. (1998) melaporkan bahwa penggunaan monolaurin menunjukkan penghambatan yang besar terhadap L. curvatus, B. thermosphacta dan L. sake (Gram positif), sedangkan terhadap bakteri P. flourescens, E. coli dan S. Typhimurium (Gram negatif), tidak menunjukkan penghambatan sampai dengan konsentrasi 2500 µg/ml. Hal yang sama juga ditemukan oleh Lee et al. (2002) menggunakan gliserol laurat diperoleh penghambatan yang tinggi terhadap B. cereus dan S. aureus, sedangkan terhadap E. coli O:157:O7 dan S. enteritidis tidak menunjukkan aktivitas penghambatan sampai pada pemberian konsentrasi 1000
ppm. Kabara (1993) melaporkan bahwa monokaprilin dan monolaurin memiliki
Fo r m a t t e d : English ( U. S. )
Fo r m a t t e d : Sw edish ( Sw eden)
Fo r m a t t e d : Fon t color: Au t o, Sw edish ( Sw eden)
kemampuan yang lebih besar dalam menghambat pertumbuhan bakteri, kapang dan khamir dibanding dengan asam sorbat yang merupakan asam organik dan banyak
digunakan sebagai pengawet pangan.
Monolaurin dalam bahan pangan diduga kuat memiliki efek sinergi dengan
asam-asam organik seperti asam atau garam laktat, asam atau garam sitrat maupun
asam atau garam sorbat. Hal ini didasarkan pada penelitian Oh dan Marshall (1994)
yang menemukan penurunan jumlah sel L. monocytogenes sebesar 0,5 unit log yang diberi monolaurin sebesar 0,72 mM dan 1 unit log pada pemberian 1,44 mM
asam laktat. Bila monolaurin dan asam laktat dicampur mampu menurunkan
sebesar 2 unit log pada produk udang yang disimpan pada suhu refrigerator 4 oC selama penyimpanan 20 hari. Efek sinergi dari asam organik dengan monolaurin
dijelaskan oleh Blaszyk et al. (1998) disebabkan oleh kemampuan dari asam organik (asam lemah) dalam merusak atau mengganggu kestabilan dinding sel dan
diperkuat oleh monolaurin yang mampu mempengaruhi struktur membran sel,
kondisi ini yang menyebabkan sel lisis dan akhirnya mempercepat kematian sel
mikroba. Selanjutnya dijelaskan Davidson dan Branen (1994) bahwa asam organik
dan monolaurin secara bersama-sama merusak membran dengan memperbesar pori
membran, hal ini akan meningkatkan efektivitas dari monolaurin dalam mengganggu aktivitas enzim-enzim terutama yang berperan dalam respirasi
akibatnya ATP tidak terbentuk dan pada gilirannya sel mengalami lisis yang diikuti
dengan kematian sel.
Efek sinergi antimikroba monolaurin dengan asam organik telah dilaporkan
oleh peneliti sebelumnya, namun belum ditemukan publikasi yang melaporkan efek
sinergi dari asam-asam organik maupun minyak atsiri dengan MAG minyak kelapa.
Campuran metabolit BAL dan MAG minyak kelapa diharapkan dapat melengkapi
sifat antimikroba, baik monolaurin sebagai komponen utama dari MAG minyak
kelapa yang diketahui memiliki aktivitas tinggi terhadap bakteri Gram positif dan
kapang sedangkan asam organik dari supernatan metabolit BAL terhadap Gram
negatif serta rasa asam yang menjadi faktor pembatas dalam penggunaannya
Tujuan Penelitian
Penelitian ini bertujuan untuk :
1. Menyeleksi beberapa isolat bakteri asam laktat yang mempunyai kemampuan
bersinergi dengan monoasilgliserol minyak kelapa dan penentuan rasio
metabolit BAL-MAG minyak kelapa yang maksimum dalam menghambat
pertumbuhan bakteri patogen (L. monocytogenes).
2. Mempelajari aktivitas campuran metabolit BAL-MAG minyak kelapa terhadap
berbagai mikroba patogen dan penentuan nilai MIC (Minimum Inhibition Concentration) terhadap bakteri L. monocytogenes, B. cereus, E. coli dan S. Typhimurium.
3. Mengkaji mekanisme kerja antibakteri campuran metabolit BAL-MAG melalui pengamatan kebocoran sel bakteri dan perubahan morfologi sel menggunakan
SEM (Scanning Electron Microscope).
4. Menentukan stabilitas antibakteri campuran metabolit BAL-MAG terhadap
pH, pemanasan dan sistem pangan.
Manfaat Penelitian
Secara umum manfaat penelitian ini adalah dalam rangka pengembangan
ilmu pangan terutama dalam bidang mikrobiologi pangan, dan secara khusus
penelitian ini dilaksanakan untuk memperoleh informasi ilmiah tentang efek sinergi
dari metabolit beberapa bakteri asam laktat dengan monoasilgliserol minyak kelapa
dan aktivitasnya terhadap mikroba patogen guna meningkatan keamanan pangan
serta me mperoleh bahan pengawet alami sebagai pengganti bahan antimikroba
sintetik yang diketahui dapat menimbulkan berbagai masalah terutama di bidang
Hipotesis
1. Campuran metabolit BAL – MAG minyak kelapa akan memberikan efek
sinergi dalam mengh ambat pertumbuhan bakteri uji.
2. Efek sinergi campuran metabolit BAL dengan MAG minyak kelapa akan
meningkat dengan meningkatnya rasio campuran metabolit BAL-MAG dan
mencapai maksimum atau mendekati maksimum pada rasio campuran metabolit BAL-MAG minyak ke lapa yang sesuai.
3. Aktivitas antimikroba campuran metabolit BAL-MAG minyak kelapa berbeda
untuk setiap jenis mikroba.
4. Campuran metabolit BAL-MAG minyak kelapa menyebabkan kebocoran
protein dan asam nukleat serta menimbulkan perubahan morfologi pada sel bakteri patogen.
5. Stabilitas antibakteri campuran metabolit BAL-MAG dipengaruhi oleh pH,
pemanasan dan sistem pangan.
Bakteri Asam Laktat
Bakteri asam laktat (BAL) erat kaitannya dengan proses fermentasi pangan,
dan saat ini telah berkembang dalam industri fermentasi pangan. Stiles dan
Holzapel (1997) menyatakan bahwa bakteri asam laktat (BAL) memiliki sifat Gram
positif, tidak membentuk spora dan dapat berbentuk koki, kokobasili atau batang.
Pada umumnya bakteri asam laktat bersifat katalase negatif, non motil atau sedikit
motil, mikroaerofilik sampai anaerob, toleran terhadap asam, kemoorganotrofik dan
membutuhkan suhu mesofilik (Salminen dan Von Wright 2004 ). Lebih lanjut
dinyatakan oleh Jay (1996) bakteri asam laktat bersifat mesofilik dan termofilik,
beberapa dapat tumbuh pada suhu 5 oC dan tertinggi 45 oC, dapat bertahan pada pH
3,2 dan pada pH yang lebih tinggi 9,6, beberapa hanya dapat tumbuh pada kisaran
pH yang sempit (pH 4,0–4,5). Bakteri ini termasuk mikroorganisme GRAS
(Generally Recognized as Safe) atau golongan mikroorganisme yang aman
ditambahkan dalam makanan karena sifatnya tidak toksik dan tidak menghasilkan
toksin, yang dikenal dengan sebutan “food grade microorganism“, yaitu
mikroorganisme yang tidak beresiko terhadap kesehatan (Alakomi et al. 2000).
Peran utama bakteri asam laktat adalah sebagai kultur starter produk-produk
yang melibatkan proses fermentasi untuk memperoleh produk akhir dengan tingkat
konsistensi yang tinggi. Selain menghasilkan produk akhir yang konsisten, bakteri
asam laktat ternyata juga memiliki efek mengawetkan pada produk fermentasi yang
diinginkan. Untuk tujuan pengawetan, dibutuhkan produksi massa sel yang tinggi,
tahan selama pembekuan dan pengeringan, serta stabil selama penyimpanan.
Disamping itu kultur harus mampu tumbuh pesat, tidak rentan terhadap phage,
toleran terhadap garam dan stabil secara genetika (Jenie et al. 1996b).
Pada dasarnya penggunaan bakteri asam laktat dalam makanan ditujukan
untuk memperpanjang masa simpan, meningkatkan kualitas dan menghambat
pertumbuhan mikroorganisme patogen dan pembusuk. Efek mengawetkan dan daya
hambat dari bakteri asam laktat berkaitan dengan substansi antimikrobanya.
Menurut Leverentz et al. (2006) bakteri asam laktat merupakan salah satu
patogen dalam bahan pangan karena mampu menurunkan pH dan menghasilkan
bakteriosin.
Jenie et al. (2001) melaporkan bahwa bakteri asam laktat memiliki aktivitas
antimikroba dengan memproduksi metabolit berupa produksi asam organik (asam
laktat, asam format, dan asam asetat), diasetil, hidrogen peroksida, karbondioksida,
bakteriosin dan juga komponen-komponen antimikroba yang bersifat antagonistik
dengan spektrum yang luas terhadap mikroorganisme. Disamping itu Pitt et al.
(2000) menyatakan bahwa selama proses fermentasi, bakteri asam laktat akan
menghasilkan metabolit- metabolit yang menimbulkan perubahan rasa dan bentuk
makanan serta menghambat pertumbuhan bakteri patogen dan pembusuk.
Pembentukan asam pada produk metabolisme BAL akan menurunkan nilai
pH, dan mengakibatkan mikroba patogen dan perusak yang umumnya tidak tahan
suasana asam akan terhambat. Akumulasi produk akhir asam mengakibatkan
turunnya pH dan akan menghambat pertumbuhan bakteri Gram positif maupun
bakteri Gram negatif. Kultur bakteri asam laktat dapat diisolasi dari berbagai
produk-produk bahan pangan seperti pada produk sayuran (pikel, sauerkraut, sawi
asin), produk fermentasi ikan (peda, bekasam, kecap ikan, silase, terasi dan
sebagainya ), produk-produk daging, dan produk susu (yoghurt, susu asam keju ).
Berdasarkan cara kerjanya terhadap glukosa, BAL dibagi menjadi dua
golongan, yaitu homofermentatif yang mampu memfermentasi glukosa menjadi
asam laktat sebagai produk utamanya, dan pada kelompok heterofermentatif yang
mampu memfermentasi glukosa menjadi asam laktat dan senyawa lain, seperti
asam asetat, CO2, diasetil, bakteriosin dan etanol (Jay 1998).
Metabolit Hasil Produksi Bakteri Asam Laktat
Senyawa antimikroba merupakan senyawa kimia atau biologi yang dapat
menghambat pertumbuhan dan aktivitas mikroba, dan senyawa tersebut sering
digolongkan sebagai bahan pengawet. Bakteri asam laktat menghasilkan beberapa
senyawa antimikroba. Senyawa antimikroba ini ada yang bersifat bakterisidal
(membunuh bakteri), bakteriostatik (menghambat pertumbuhan bakteri), fungisidal
(membunuh kapang dan khamir) dan fungistatik (menghambat pertumbuhan
Komponen senyawa antimikroba yang terdapat dalam BAL disamping
berfungsi sebagai antibakteri juga berfungsi sebagai antimikotik. Menurut Gourama
dan Bullerman (1995) sifat antimikotik ini disebabkan oleh adanya senyawa
polipeptida dan metabolit dari bakteri asam laktat dengan berat molekul rendah
yang dapat menghambat pertumbuhan kapang serta dapat pula menghambat sintesis
aflatoksin. Jenis kapang yang dapat dihambat adalah Aspergillus parasiticus, A.
fumigatus, Rhizopus sp dan lain–lain. Stilles et al. (2002) dalam Magnusson (2003)
menemukan adanya efek penghambatan dari Lactobacillus sanfrancisco CBI yang
menghasilkan metabolit yang mengandung asam propionat, asam butirat dan
valerat terhadap beberapa jenis kapang diantaranya Penicillium spp, Aspergillus
spp, Fusarium spp, dan Monilla spp. Cabo et al. (2002) melaporkan temuannya
bahwa bakteri asam laktat dari L. plantarum dan L. casei subsp. casei sangat efektif
dalam menghambat P. commune dan P. roqueforti dan kurang efektif terhadap
Aspergillus parasiticus, Aspergillus flavus dan Fusarium avenaceum tetapi dapat
mengendalikan produksi aflatoksin dari Aspergillus flavus.
Efektivitas antimikroba dalam mengawetkan bahan makanan adalah dengan
cara mengendalikan pertumbuhan mikroorganisme atau secara langsung
memusnahkan seluruh atau sebagian mikroorganisme (Brannen dan Davidson
1993). Frazier et al. (1987) mengemukakan bahwa kemampuan suatu senyawa
antimikroba di dalam menghambat atau membunuh mikroba sangat ditentukan oleh
(1) konsentrasi senyawa antimikroba, (2) jenis, jumlah, umur dan latar belakang
kehidupan mikroorganisme, (3) Suhu dan waktu kontak, serta (4) sifat fisik dan
kimia media (pH, kadar air, jenis dan jumlah zat terlarut).
Asam Organik Produk Metabolit BAL
Asam-asam organik yang dihasilkan oleh bakteri asam laktat
mengakibatkan akumulasi produk akhir asam dan penurunan pH yang akan
menghambat pertumbuhan bakteri baik Gram positif maupun bakteri Gram negatif.
Aktivitas asam-asam lipofilik seperti asam laktat dan asetat dalam bentuk tidak
terdisosiasi dapat menembus sel mikroba, dan pada pH intraseluler yang lebih
tinggi, berdisosiasi menghasilkan ion- ion hidrogen dan mengganggu fungsi
metabolit esensial seperti translokasi substrat dan fosforilasi oksidatif, dengan
dinyatakan oleh Jenie et al. (1996a) bahwa efek penghambatan dari asam organik
terutama berasal dari jumlah asam yang tidak terdisosiasi. Asam lipofilik seperti
asam laktat dan asam asetat dalam bentuk tidak terdisosiasi dapat menembus sel
mikroba. Stratford (2000) menyatakan asam lemah dapat menurunkan pH
sitoplasma, mempengaruhi struktur membran dan fluiditasnya serta mengkelat
ion-ion dinding sel bakteri. Penurunan pH sitoplasma akan mempengaruhi protein
struktural sel, enzim-enzim, asam nukleat dan fosfolipid membran (Davidson dan
Branen 1994).
Mekanisme asam lemah (asam organik) dalam menginaktivasi sel bakteri
dapat dilihat pada Gambar 2.1. Hanya molekul asam lemah yang tidak bermuatan
(HA) dapat masuk melalui membran plasma. Anion (A- ) dan proton (H+) akan
terbentuk di dalam sel, selanjutnya proton yang berlebih di dalam sitoplasma akan
dikeluarkan oleh enzim ATP-ase yang terdapat pada membran (Garbutt 1997).
pH internal berubah, protein sel dan DNA terganggu
R-COOH kondisi internal R-COOH- + H+
RCOO- + H+ RCOO- + H+ sel membran tidak dapat
(Bentuk tidak terurai masuk) (ditembus dalam bentuk terurai)
Gambar 2.1. Mekanisme asam lemah (organik) dalam menginaktivasi bakteri
(Garbutt 1997)
Beberapa penelitian telah melaporkan efek penghambatan dari berbagai
asam organik terhadap mikroba patogen atau perusak, diantaranya adalah Bloom et
al. (1997) yang menyatakan bahwa penggunaan asam organik berupa 2,5% asam
laktat dan 0,25% asam asetat pada penyimpanan suhu rendah mampu
memperpanjang masa simpan dari daging babi panggang hingga 5 minggu.
larutan asam laktat pada konsentrasi 4% (volume 500 ml) dengan cara
menyemprotkan pada karkas sapi ternyata efektif dalam mereduksi mikroba
patogen, yakni koliform dan E. coli. Pitt et al. (2000) melaporkan hasil temuannya
yang menggunakan berbagai jenis asam organik produksi bakteri asam laktat pada
susu pasteurisasi yang mampu menghambat pertumbuhan Listeria monocytogenes.
Monoasilgliserol
Monoasilgliserol merupakan suatu emulsifier yang bersifat non ionik dan
tidak terlalu berpengaruh (tidak sensitif) terhadap suasana asam. Sifat emulsifier
pada monoasilgliserol disebabkan oleh monoasilgliserol memiliki dua gugus
bersifat polar dan satu gugus bersifat non polar atau mengandung gugus hidrofilik
dan hidrofobik (Igoe dan Hui 1996). Dalam industri pangan monoasilgliserol
digunakan sebagai surfaktan, emulsifier pada pengolahan margarin, mentega
kacang, puding, roti, biskuit dan kue-kue kering yang mengandung lemak.
Twillman dan White (1988) melaporkan bahwa monoasilgliserol dapat
memperbaiki tekstur adonan roti dan juga memperpanjang masa simpan tortila
jagung. Monoasilgliserol dalam adonan akan bereaksi dengan amilopektin
membentuk senyawa kompleks yang berperan memperbaiki tekstur roti serta
memperpanjang masa simpan dari roti (Hasenhuetti dan Hartel 1997).
Monoasilgliserol terbentuk dari reaksi antara asam lemak dengan gliserol atau
gliserol dengan triasilgliserol (minyak/lemak), sedangkan mono dan diasilgliserol
terbentuk dari reaksi antara gliserol dengan triasilgliserol (minyak). Reaksi tersebut
dikenal dengan nama reaksi gliserolisis. Reaksi ini dapat berlangsung dengan
adanya katalis alkali (gliserolisis cara kimia) maupun dengan biokatalis lipase
(gliserolisis cara enzimatik). Gliserolisis cara enzimatik mempunyai beberapa
kelebihan dibandingkan dengan gliserolisis cara kimia. Kelebihan tersebut antara
lain reaksi berlangsung pada suhu relatif rendah, hasil samping yang rendah dan
produk reaksi dikelompokkan sebagai produk alami dalam arti aman untuk
dikonsumsi (Siswohutomo et al. 2002).
Rendemen monoasilgliserol yang terbentuk tergantung pada jenis minyak,
sumber lipase, perbandingan antara minyak dan gliserol, atau pH substrat.
Penggunaan lipase dengan jumlah yang sama pada pembuatan monoasilgliserol
dari minyak kelapa dan lemak susu menghasilkan rendemen yang berbeda,
lemak susu tidak lebih dari 60 persen (August 2000). Hasil penelitian Mappiratu
(1999) menemukan produksi monoasilgliserol minyak kelapa untuk produksi
antimikroba mencapai maksimum pada kisaran rasio gliserol : minyak : dedak :
heksana sebesar 0,3 : 0,75 : 2,5 :10 (b/b/b/v), dengan suhu reaksi 37 oC, pH 7,
waktu reaksi 72 jam.
Sifat Antimikroba Monoasilgliserol Minyak Kelapa
Monoasilgliserol (MAG) minyak kelapa mempunyai peluang yang cukup
tinggi untuk digunakan sebagai bahan pengawet pangan, sebab monoasilgliserol
minyak kelapa mempunyai sifat antimikroba yang tidak dimiliki oleh MAG dari
minyak nabati lain. Beberapa peneliti melaporkan bahwa MAG tertentu
mempunyai kemampuan dalam menghambat pertumbuhan bakteri gram positif,
yeast, virus, fungi dan sel tumor. Menur ut Blaszyk et al. (1998) monolaurin sangat
efektif terhadap bakteri Gram positif dan jamur, tetapi tidak efektif terhadap bakteri
Gram negatif. Hal ini diperkuat dengan hasil penelitian Ouattara (1997) tentang
pengaruh monolaurin terhadap bakteri Gram positif dan bakteri Gram negatif. Hasil
penelitiannya menunjukkan bahwa efek penghambatan hanya terjadi pada bakteri
Gram positif. Hasil penelitian Mappiratu (1999) menunjukkan diameter zona
penghambatan monoasilgliserol terhadap bakteri Gram positif lebih tinggi dari pada
bakteri Gram negatif, dan terhadap khamir dan kapang zona penghambatannya
lebih rendah.
Beuchat (1980) melakukan suatu pengujian dengan membandingkan
aktivitas antibakteri dari monolaurin dengan natrium benzoat dan asam sorbat
menggunakan Vibrio parahaemoliticus sebagai bakteri penguji. Hasil pengujian
menunjukkan bahwa monolaurin lebih aktif dibandingkan dengan natrium benzoat
dan asam sorbat. Fenomena ini sejalan dengan pernyataan Branen dan Davidson
(1993) bahwa ester monoasilgliserol dalam bentuk monolaurin dan monokaprin
memiliki daya antibakteri yang kuat terhadap B. cereus, S. aureus dan B. subtilis
dengan nilai MIC sekitar 17-123 µg/ml. Jika dibandingkan dengan asam sorbat,
daya antibakteri tersebut lebih tinggi dengan nilai MIC pada asam sorbat sebesar
4000 µg/ml. Secara rinci nilai MIC untuk bakteri uji tertera pada Tabel 2.1,
Tabel 2.1. Aktivitas antibakteri monolaurin dan bahan pengawet pangan lainya
Antib akteri
Konsentrasi minimum yang menghambat bakteri (µg/ml)
Bacillus cereus Bacillus subtilis Staphylococcus
aureus
Sukrosa dikaprilin 74 74 148
Monokaprin (MC 10) 123 123 123
Monolaurin (MC 12) 17 17 17
Butil-p- hidroksi benzoat 400 200 200
Asam sorbat 4000 4000 4000
Sumber : Branen dan Davidson (1993).
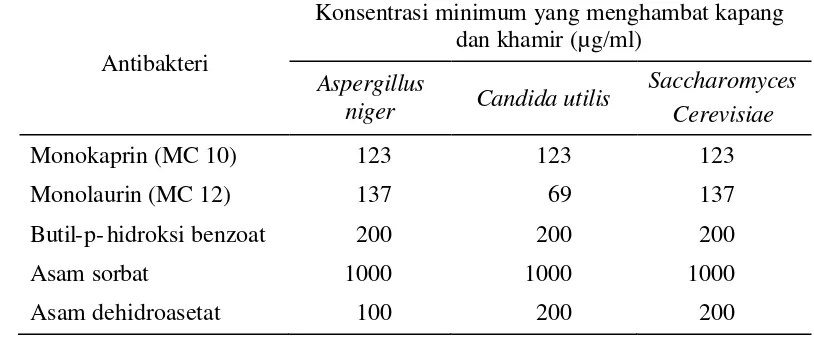
Tabel 2.2. Aktivitas antikapang monolaurin dan bahan pengawet pangan lain
Antibakteri
Konsentrasi minimum yang menghambat kapang dan khamir (µg/ml)
Aspergillus
niger Candida utilis
Saccharomyces Cerevisiae
Monokaprin (MC 10) 123 123 123
Monolaurin (MC 12) 137 69 137
Butil-p- hidroksi benzoat 200 200 200
Asam sorbat 1000 1000 1000
Asam dehidroasetat 100 200 200
Sumber : Branen dan Davidson ( 1993).
Monolaurin dapat menghambat produksi aflatoksin dari A. flavus dan A.
parasiticus pada perbandingan konsentrasi asam sorbat 1000 ppm, dan monolaurin
750 ppm (Chipley et al. 1981). Hal ini menunjukkan bahwa monolaurin lebih
efektif dibandingkan dengan asam sorbat. Asam sorbat merupakan jenis bahan
pengawet yang umumnya digunakan sebagai antibakteri dan antikapang.
Menurut Oh dan Marshall (1994) monolaurin termasuk komponen utama
monoasilgliserol minyak kelapa dan mempunyai aktivitas antimikroba dengan
spektrum luas mencakup bakteri Gram positif, khamir dan kapang serta sebagian
efektif diantara turunan asam lemak. Asam lemak monoasilgliserol minyak kelapa
termasuk jenis asam lemak jenuh rantai pendek dan menengah (C8-C14). Asam
lemak rantai pendek dan menengah dari monoasilgliserol tersebut berperan sebagai
antimikroba (Wang et al. 1993).
Tabel 2.3. Komposisi asam lemak beberapa jenis minyak nabati
Jenis minyak Persen mol asam lemak bebas beratom karbon
8:1 10:0 12:0 14:0 16:0 18:0 18;1 18;2 18:3
Kelapa 7,6 7,3 48,2 16,6 8,0 3,8 5,0 2,5 -
Sawit - - 0,1 12 46,8 3,8 37,6 10,0 -
Kacang kedele - - - 0,1 46,8 3,8 37,6 10,0 8,3
Biji kapas - - - 0,1 10,5 3,2 22,3 54,5 -
Jagung - - - - 11,5 2,2 26,6 58,7 0,8
Kacang tanah - - - - 11,0 2,3 51,0 30,9 -
Zaitun - - - - 16,9 1,7 59,1 22,8 8,2
Biji lobak - - - - 4,3 1,7 59,1 22,8 8,2
Dedak padi - - - 0,49 13,8 - 43,6 23,6 1,2
Sumber : Salunke et al. (1992)
Selain itu, monolaurin dan monokaprin juga dilaporkan mempunyai
aktivitas antimikroba yang banyak digunakan dalam produksi makanan dan
kosmetika (August 2000). Nair et al. (2005) melaporkan temuannya terhadap
penggunaan monokaprilin pada jus apel yang disimpan pada suhu 4 dan 23 oC
selama 14 dan 21 hari efektif memb unuh bakteri E. coli O157:H7. Lebih lanjut
dinyatakan bahwa penyimpanan pada suhu 23 oC lebih efektif dibanding dengan
suhu 4 oC, baik pada penyimpanan 14 hari maupun pada penyimpanan 21 hari.
Mekanisme aktivitas antibakterial monoasilgliserol minyak kelapa belum
diketahui dengan pasti, namun monoasilgliserol yang bersifat lipofilik ini
memungkinkan untuk menembus membran plasma dan menghambat aktivitas
enzim yang terlibat dalam produksi energi dan transport nutrien. Monolaurin
menyebabkan kerusakan yang ekstensif pada membran dengan cara merusak
protein ekstraseluler, asam nukleat dan menurunkan aktivitas enzim tertentu.
dan Branen (1994). Pengaruh dari asam lemak dan mono gliserida terhadap sistim
oksidasi NADH2 memiliki kesamaan. Aktivitas sistem ini menurun 50% dengan
menggunakan 0,64 nmol asam lemak atau 0,14 nmol monogliserol per gram
protein. Pengaruh dari kedua kelompok lipid ini terhadap respirasi seluler dan
penelitian mengenai efek penghambatan monogliserida terhadap beberapa sistem
enzim menunjukkan bahwa monogliserida hanya bekerja pada sisi oksigen pada
gugus flavin dari NADH2 dehidrogenase, sedangkan asam lemak merupakan
penghambatan kurang spesifik yang bekerja pada beberapa sisi.
Antimikroba monolaurin mempunyai efek sinergi dengan bahan pengawet
pangan lain, seperti asam sitrat, asam atau garam laktat dan asam atau garam
sorbat. Davidson dan Branen (1994) melaporkan bahwa penggunaan campuran
monolaurin denga n kalsium laktat meningkatkan waktu simpan kamaboko (pasta
ikan) dari 6 hari menjadi 20 hari. Catsara et al. (1987) melaporkan bahwa
penggunaan laurilak (campuran monolaurin dengan asam laktat ) sebanyak 500
ppm dalam daging sapi giling dapat mereduksi total koloni Salmonella
typhymurium dari 2,47 x 105 CFU/gram menjadi kurang dari 102 CFU/gram.
Selanjutnya Unda et al. (1991) melaporkan bahwa monolaurin dan natrium laktat
sangat efektif menghambat pertumbuhan bakteri anerobik pada suhu tinggi, dan
menurutnya kombinasi laktat dan monolaurin sangat potensial mengontrol
Clostridia dan Listeria pada produk daging sapi dalam mikrowave. Hal yang sama
dilaporkan oleh Blaszyk et al. (1998) yang menggunakan monolaurin dan asam
sitrat maupun garam sitrat, campuran monolaurin dan asam/garam sitrat tersebut
ternyata mampu menghambat pertumbuhan dari L. monocytogenes dan E. coli pada
daging. Selain itu menurut Liskar dan Poster (1982) monolaurin lebih efektif
menghambat pertumbuhan kapang dan khamir bila dicampur denga n asam sorbat.
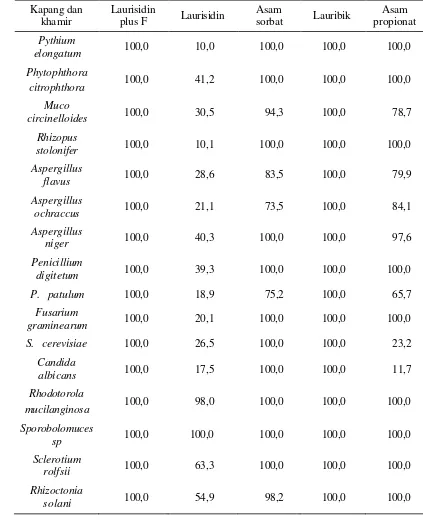
Penurunan massa sel (%) kapang dan khamir pada beberapa jenis antimikroba
Tabel 2.4. Penurunan massa sel (%) kapang dan khamir pada beberapa
Temuan-temuan tersebut di atas menunjukkan bahwa monolaurin bersifat
sinergi dengan asam-asam organik. Efek sinergi dari campuran mo nolaurin dan
asam sitrat (asam organik) dijelaskan oleh Blaszyk et al. (1998) karena berbagai
membran sel sedangkan asam sitrat (asam organik) bersifat merusak atau
mengganggu kestabilan zat pelindung dari dinding sel, yaitu lipopolisakarida
(LPS).
Mikroba Patogen pada Bahan Pangan
Aspek mikrobiologis pada bahan pangan memiliki peranan yang cukup
penting karena bahan pangan dapat merupakan salah satu sumber timbulnya suatu
penyakit. Gangguan terhadap kesehatan yang diakibatkan oleh makanan khususnya
gangguan pada saluran pencernaan yang berkaitan dengan konsumsi pangan
diklasifikasikan sebagai penyakit yang disebabkan melalui rantai makanan (Food
borne desease).
Penyakit yang disebabkan oleh bakteri yang masuk ke dalam tubuh melalui
makanan diklasifikasikan ke dalam dua kelompok: (a) infeksi yang disebabkan oleh
pertumbuhan patogen dari patogen yang terbawa oleh makanan; dan (b) infeksi
yang disebabkan oleh pertumbuhan bakteri patogen dengan makanan sebagai media
kultur untuk pertumbuhannya hingga mencapai jumlah yang memadai untuk
menimbulkan infeksi bagi yang mengkonsumsi makanan tersebut, misalnya infeksi
Salmonella spp, Listeria monocytogenes dan E. coli (Frazier et al. 1987 ).
Penerapan suatu senyawa antimikroba pada bahan pangan memerlukan
pengujian terlebih dahulu, karena aktivitas suatu bahan antimikroba berbeda-beda
dan sangat dipengaruhi oleh komponen yang ada pada senyawa tersebut, serta jenis
mikroba ujinya. Mikroba- mikroba tersebut dapat digolongkan ke dalam bakteri dan
kapang yang bersifat patogen, yang akan dihambat pertumbuhannya dengan
senyawa antimikroba dari metabolit BAL-MAG.
Mikroba pembentuk spora
Bacillus cereus merupakan salah satu kelompok pembentuk spora yang
penyebarannya sangat luas dan dapat menyebabkan infeksi baik pada manusia
maupun pada hewan. Bakteri ini berbentuk batang, bersifat aerob sampai aerob
fakultatif, katalase positip dan kebanyakan bersifat gram positif. Suhu pertumbuhan
minimum 4-5 oC, pertumbuhan maksimum pada suhu 48-50 oC dengan suhu
optimal 30-45 oC, dan tumbuh pada pH antara 4,9-9,3 (Granum dan Baird-Parker
2000). Bahan pangan yang terkontaminasi B. cereus selain menimbulkan kerusakan
menyebabkan septikemia dan meningitis dengan waktu inkubasi 0,5-5 jam (Ryu et
al. 2005).
Berdasarkan sifat patogenik, bakteri dibagi ke dalam tiga kelompok (Ryu et
al. 2005), yaitu: (1) galur penyebab diare (memproduksi toksin piogenik) dengan
gejala mual- mual, keram perut, diare dan kadang-kadang muntah setelah inkubasi
selama 8-6 jam; (2) galur penyebab muntah (memproduksi toksin emetik) dengan
gejala mual- mual dan muntah setelah inkubasi 1-6 jam (rata-rata 2-5 jam) dan (3)
tidak memproduksi enterotoksin.
Keberadaan bakteri di dalam tubuh manusia perlu diwaspadai, karena
masyarakat Indonesia seringkali menyimpan makanan matang tanpa perlakuan
khusus atau memasak tanpa pemanasan suhu yang tinggi. Hal ini dapat
menimbulkan kerusakan terhadap makanan tersebut terutama karena tercemar oleh
B. cereus.
Bakteri Gram Negatif
Escherechia coli merupakan bakteri patogen Gram negatif, oksidase negatif
berbentuk batang dengan ukuran 1,1-1,5 µm x 2-6 µm, dan bersifat motil karena
adanya flagella. Bakteri ini banyak menimbulkan gangguan kesehatan pada
manusia dan merupakan flora normal yang terdapat pada saluran pencernaan
manusia dan hewan, dan umumnya ditemukan pada daging giling dan produk
olahan sejenisnya. Suhu pertumbuhan berada dalam kisaran yang luas, mulai dari
1-45 oC, sehingga kemungkinan pangan tercemar oleh bakteri ini sangat besar jika
penanganannya kurang memadai. Berdasarkan gejala dan karakteristik penyakit
yang ditimbulkan, E. coli dikelompokkan menjadi lima kelompok, yaitu
Enteroaggregative E. coli (EaggEC), Enterohemorrhagic E. coli (EHEC),
Enteroinvasive E. coli (EIEC), Enteropathogenic E. coli (EPEC), dan
Enterotoxigenic E. coli (ETEC).
E. coli sangat sensitif terhadap panas dan dapat diaktifkan pada suhu
pasteurisasi atau selama pemasakan makanan (Supardi dan Sukamto 1999).
Kontaminasi bakteri ini pada makanan biasanya berasal dari kontaminasi air yang
digunakan. Dosis yang dapat menimbulkan gejala infeksi E. coli pada makanan
berkisar antara 106-109 sel. Bahan makanan yang sering terkontaminasi oleh E.
coli antara lain daging babi, daging ayam, ikan, telur dan olahannya serta makanan
Salmonella sp juga merupakan kelompok bakteri Gram negatif dan
merupakan bakteri patogen yang tidak diperkenankan ada dalam produk – produk
pangan. Bakteri ini dapat tumbuh pada kisaran suhu 5-45 oC, dengan suhu optimum
37 oC, meskipun dapat tumbuh pada suhu di bawah 10 oC, dengan pH optimum
6,5-7,5. Salmonella memiliki ketahanan panas yang tinggi pada pH 5,5 dan aw rendah
(Portilo 2000). Salmonella dibagi menjadi 3 spesies yaitu S. Typhi, S. enterica dan
S. enteritidis. Salmonella Typhimurium merupakan spesies Salmonella enterica
serovar Typhimurium (D, Aost 2000). Bakteri ini dapat menimbulkan infeksi, dan
jika tertelan masuk ke dalam tubuh akan menimbulkan gejala yang disebut
salmonellosis. Infeksi ini berakibat fatal, terutama jika menyerang bayi. Oleh sebab
itu infeksi Salmonella pada makanan mendapat perhatian yang serius, karena
bakteri ini seringkali menimbulkan penyakit terutama di negara-negara industri.
Bakteri Gram Positif
Listeria monocytogenes merupakan bakteri patogen pada manusia dan
seringkali ditemukan pada bahan pangan segar meskipun disimpan pada suhu
rendah, seperti buah melon dan beberapa jenis buah lainnya maupun sayuran
ditemukan telah terkontaminasi dengan L. monocytogenes selama penyimpanan
pada suhu rendah (Leverentz et al. 2006). Bakteri ini berbentuk batang, berukuran
panjang 0,5-2,0 µm, diameter 0,4-0,5 µm, mempunyai flagella (motil positif) yang
bersifat anerobik fakultatif, dan memproduksi asam dan dekstrosa atau maltosa
(tanpa gas). Kisaran suhu pertumbuhan L. monocytogenes antara 1-45 oC dengan
suhu optimum 30 – 37 oC, namun dapat pula tumbuh pada suhu 2,5-44 oC dan
bersifat fermentatif (Fardiaz 1989).
Keberadaan bakteri ini dalam bahan pangan perlu menjadi perhatian penting
terutama dalam industri pengolahan pangan termasuk produk-produk olahan daging
dan unggas (Ming et al. 1997). Berdasarkan laporan hasil penelitian diketahui
bahwa bakteri ini dapat tumbuh pada suhu 0 oC, dan dapat hidup pada suhu 37 oC
selama 15 hari pada substrat yang mengandung NaCL 10,5% atau 10 hari pada
substrat NaCl 13% atau 5 hari pada substrat NaCl 20% pada suhu 4 oC. Oleh
karena itu jumlah bakteri ini dalam bahan pangan harus dikendalikan dan tidak
diperkenankan berada pada bahan pangan lebih dari satu sel per gram bahan. L.
monocytogenes dapat direduksi pertumbuhannya sebesar 1,5 unit log dengan
Kapang Aspergillus flavus
A. flavus merupakan salah satu jenis kapang yang mudah ditemukan di
mana-mana, baik di udara, air maupun di tanah, dan tumbuh pada bahan pangan
maupun pakan, seperti pada jagung, beras dan kacang tanah (Moreau dan Moss
1997).
A. flavus tumbuh pada kelembaban relatif 82-85% dengan suhu minimum
10-12 oC, suhu maksimum 43-48 oC dan suhu optimum pertumbuhan sekitar 33 oC.
Pertumbuhan A. flavus mencakup kisaran pH yang sangat luas, yaitu dari 2,1-11,2,
dengan pH optimum pertumbuhan 3,4-10 dan aktivitas air (aw) sekitar 0,78-0,84
(Pitt dan Hocking 1996). Pertumbuhan optimum A. flavus pada kadar air 15-30%.
A. flavus merupakan penghasil utama aflatoksin, yang merupakan
mikotoksin terpenting dalam penyimpanan makanan. Aflatoksin merupakan
kelompok metabolit sekunder yang terbentuk setelah fase logaritmik pertumbuhan
kapang A. flavus pada suhu antara 7,5-40 oC dengan suhu optimum 24-28 oC.
Menurut Jay (1996), pembentukan aflatoksin pada kacang tanah terjadi pada aw
optimum 0,93-0,98, RH 83% atau lebih tinggi pada suhu 30 oC dan pH 5,5-7,0.
Toksin ini bersifat akut dan kronis terhadap hewan dan manusia. Sebagai contoh,
dari tahun 1991-1996 tidak kurang dari 17000 sampel jagung, kacang tanah,
kedelai, gandum dan rempah-rempah di Asia Tenggara dilaporkan telah banyak
terkontaminasi Aspergillus flavus (Pitt dan Hocking 1996).
Mekanisme Kerja Senyawa Antimikroba
Kemampuan suatu senyawa antimikroba dalam menghambat pertumbuhan
mikroba merupakan suatu kriteria yang penting dalam pemilihan suatu senyawa
antimikroba yang berfungsi sebagai bahan pengawet. Semakin kuat efek
penghambatannya semakin efektif digunakan. Suatu senyawa dikatakan bersifat
antimikroba karena dapat menimbulkan kerusakan pada sel mikroba yang akhirnya
akan menimbulkan kematian. Kerusakan yang ditimbulkan ini ada yang bersifat
mikrosidal (kerusakan tetap) atau mikrostatik (kerusakan yang dapat kembali).
Sifat kerusakan tergantung pada konsentrasi komponen dan kultur yang digunakan
(Bloomfield 1991).
Mekanisme kerusakan sel akibat senyawa antimikroba secara umum telah
monoasilgliserol belum diketahui secara pasti. Namun dapat diasumsikan bahwa
baik asam organik maupun monoasilgliserol dapat menimbulkan kerusakan
terhadap mikroba dengan mekanisme yang hampir sama dengan mekanisme
antimikroba secara umum.
Secara umum mekanisme kerja dari suatu senyawa antimikroba dapat
dilakukan melalui mekanisme yang berbeda, yaitu: (1) mengganggu atau merusak
komponen penyusun dinding sel, (2) bereaksi dengan membran sel yang
menyebabkan peningkatan permeabilitas seluler, (3) inaktivasi enzim-enzim
esensial dan (4) destruksi atau inaktivasi fungsi dari materi genetik (Brannen dan
Davidson 1993). Terjadinya penghambatan senyawa antimikroba terhadap sel-sel
mikroba disebabkan oleh adanya pelekatan senyawa antimikroba pada permukaan
sel mikroba atau adanya difusi dari senyawa antimikroba tersebut ke dalam sel
(Fardiaz et al. 1989).
Gangguan pada Komponen Penyusun Dinding Sel
Unit dasar dari dinding sel bakteri disusun oleh peptidoglikan yang secara
mekanis memberikan ketegaran pada sel bakteri, disamping sebagai dasar membran
sitoplasma. Peptidoglikan tersebut terdiri dari turunan gula, yaitu asam
N-asetilglukosamin dan N-asetilmuramat serta asam amino L-alanin, alanin,
D-glutamat, dan lisin. Struktur dinding sel bakteri Gram positif mengandung 90%
peptidoglikan serta lapisan tipis asam teikoat dan asam teikuronat yang bermuatan
negatif, struktur sel pada bakteri Gram negatif memiliki komponen dinding sel
5-10% peptidoglikan, selebihnya terdiri dari protein, lipoprotein dan lipopolisakarida.
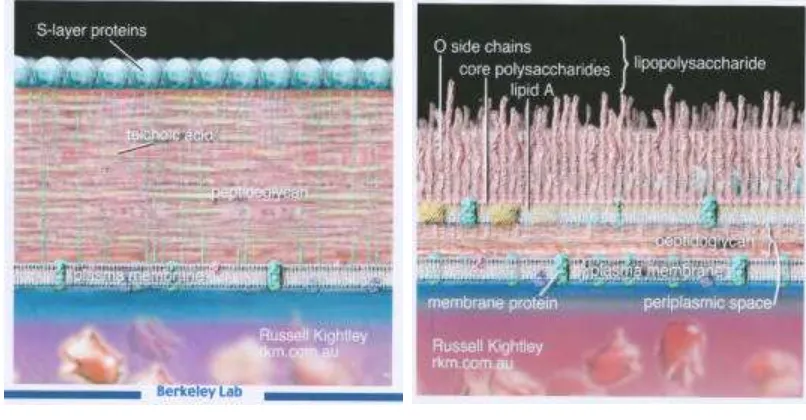
Dinding sel bakteri Gram negatif lebih kompleks dibandingkan Gram positif
(Gambar 2.4). Perbedaan utama terletak pada lapisan membran luar, yang meliputi
lipopolisakarida (Madigan et al. 2003). Kehadiran membran ini menyebabkan
dinding sel bakteri Gram negatif kaya kandungan lipida (11-22%). Membran
tersebut tidak hanya terdiri dari fosfolipida saja seperti pada membran plasma tetapi
juga mengandung lipida lainnya, seperti polisakarida dan protein. Lipida dan
polisakarida ini berhubungan erat dan membentuk struktur khas yang disebut
Lipopolisakarida ini terikat satu sama lain dengan kation divalent Ca2+ dan Mg2+
(Murray et al. 1998).
a) Bakteri Gram positif b) Bakteri Gram negatif
Gambar 2.2. Struktur dinding sel bakteri Gram positif dan Gram negatif (Russel Kightley, 2006)
Membran luar bakteri Gram negatif mempunyai peranan sebagai barrier
masuknya senyawa-senyawa yang tidak dibutuhkan sel, diantaranya bakteriosin,
enzim dan senyawa yang bersifat hidrofobik (Alakomi et al. 2000). Dalam upaya
untuk mencapai sasaran, senyawa antimikroba dapat menembus LPS dari
dinding sel tersebut. Molekul- molekul yang bersifat hidrofilik lebih mudah
melewati LPS dibandingkan dengan yang bersifat hidrofobik. Bakteri Gram positif,
tidak mempunyai LPS, sehingga fungsi penghalangnya tidak ada dan molekul
senyawa antimikroba yang bersifat hidrofilik dan hidrofobik dapat melewatinya
(Best 1999). Bakteri Gram negatif mempunyai sisi hidrofilik, yaitu karboksil, asam
amino dan hidroksil. Asam-asam organik seperti asam sitrat, asam malat, asam
tartrat dan asam laktat dapat menghambat pertumbuhan bakteri Gram negatif
dengan mengkelat kation divalen Ca2+ dan Mg2+. Ketika kedua kation tersebut
terlepas dari membran luar maka senyawa antimikroba akan lebih mudah masuk ke
Penghambatan senyawa antimikroba merupakan kemampuan suatu senyawa
antimikroba untuk mempengaruhi dinding sel mikroba (Ultee et al. 2000). Menurut
Kabara (1993) asam-asam lemak terutama asam laurat dapat menghambat enzim
yang terlibat pada produksi energi dan pembentukan komponen struktural sehingga
pembentukan dinding sel bakteri terganggu.
Mekanisme kerusakan dinding sel dapat disebabkan oleh adanya akumulasi
komponen lipofilik yang terdapat pada dinding sel atau membran sel, sehingga
menyebabkan perubahan komposisi penyusun dinding sel. Terjadinya akumulasi
senyawa antibakteri dipengaruhi oleh bentuk tak terdisosiasi. Pada pH rendah asam
organik maupun asam lemak yang terdapat dalam metabolit BAL-MAG minyak
kelapa kebanyakan berbentuk tidak terdisosiasi, dan adanya gugus hidrofobik
sehingga dapat mengikat daerah hidrofobik membran protein serta melarut baik
pada fase lipid dari membran bakteri.
Umumnya senyawa antimikroba yang menghambat sintesis peptidoglikan
karena kemampuan dari senyawa tersebut dalam menghambat enzim- enzim yang
berperan dalam pembentukan peptidoglikan, seperti karboksipeptidase,
endopeptidase dan transpeptidase. Jika aktivitas enzim-enzim tersebut dihambat
oleh senyawa antibakteri maka sifat enzim autolitik sebagai regulator hilang dan
enzim tidak mampu mengendalikan aktivitasnya sehingga dinding sel tersebut akan
mengalami degradasi (Murray et al. 1998).
Bereaksi dengan membran sel
Senyawa antimikroba dapat mengganggu dan mempengaruhi integritas
membran sitoplasma, yang dapat mengakibatkan kebocoran materi intraseluler,
seperti asam lemak pada monoasilgliserol yang dapat mengakibatkan gangguan
pada permeabilitas membran, yang ditandai dengan terjadinya peningkatan
permeabilitas membran sebagai akibat adanya perubahan komposisi fosfolipid.
Kondisi ini menyebabkan monoasilgliserol lebih mudah menembus membran sel
dan akhirnya terjadi kebocoran sel, yang diikuti dengan keluarnya materi
intraseluler.
Sel bakteri dikelilingi oleh struktur kaku yang disebut dinding sel, yang
melindungi membran sitoplasma, baik osmotik maupun mekanik. Setiap zat yang
terbentuknya sel-sel yang peka terhadap osmotik. Adanya tekanan osmotik dalam
sel bakteri akan menyebabkan terjadinya lisis, yang merupakan dasar efek
bakterisidal pada bakteri yang peka (Setiabudy 2000).
Kebocoran membran sitoplasma dapat pula terjadi karena asam-asam
organik. Asam organik yang tidak terdisosiasi mampu menembus dinding sel dan
mengganggu permeabilitas membran. Selain itu setelah berada dalam sitoplasma
akan terdisosiasi menghasilkan proton, dan proton yang berlebihan akan
menyebababkan keseimbangan terganggu. Gangguan tersebut berakibat pada
berkurangnya energi sel untuk pertumbuhan karena dialihkan untuk
menyeimbangkan proton, dan juga akan mengganggu transport asam amino dan
gula.
Menginaktifkan Enzim Esensial
Komponen antibakteri dapat menghambat pertumbuhan atau membunuh
mikroorganisme dengan cara mengganggu aktivitas enzim-enzim metaboliknya.
Beberapa senyawa antibakteri yang diketahui dapat menginaktivasi enzim seperti
asam benzoat, asam lemak, sulfit dan nitrit. Nitrit dapat menghambat sistem enzim fosfat dehidrogenase, sehingga mengakibatkan reduksi ATP dan ekskresi piruvat
dalam bakteri S. aureus. Asam benzoat dapat menghambat aktivitas a-ketoglutarat
dehidrogenase dan suksinat dehidrogenase. Hal ini akan menghambat konversi
a-ketoglutarat menjadi suksinil Co-A dan suksinat menjadi fumarat.
Kim et al. (1995) mengemukakan bahwa senyawa antimikroba dapat
merusak sistim metabolisme di dalam sel dengan cara menghambat sintesis protein
bakteri dan menghambat kerja enzim intraseluler. Sistem enzim yang terpengaruh
akan mengakibatkan gangguan pada produksi energi penyusun sel dan sintesis
komponen secara struktural. Selain itu asam-asam lemak mampu bereaksi dengan
enzim dehidrogenase dan akan mengakibatkan hilangnya aktivitas enzim tersebut.
Gangguan aktivitas enzim dapat terjadi pada saat mikroba mensintesis asam
dihidrofolat dari p-aminobenzoat (Davidson dan Branen 1994).
Menginaktifkan fungsi material genetik
Umumnya suatu senyawa antimikroba yang akan menghambat sintesis
protein yang mampu mengikat ribosom. Sebagaimana diketahui bahwa sintesis
senyawa antimikroba menghambat salah satu dari kedua proses tersebut maka
sintesis protein akan terhambat (Best 1999). Menurut Leive (1979) dalam Rahayu
(1999) penghambatan sintesis DNA dapat disebabkan oleh adanya penghambatan
proses transkripsi ikatan RNA polimerase, seperti yang diakibatkan aktinomisin
atau rifamisin. Kondisi ini dapat mengakibatkan terhambatnya pembentukan
komponen penyusun asam nukleat, yaitu purin-pirimidin nukleotida, dan
polimerisasi pembentukan asam nukleat akan terganggu pula. Gangguan ini dapat
menyebabkan penghambatan pada pertumbuhan sel yang dapat berlanjut pada
kematian sel. Hal yang sama juga dikemukakan oleh Kim et al. (1995) bahwa suatu
senyawa yang bersifat antimikroba dapat mengganggu pembentukan asam nukleat
(DNA dan RNA), sehingga transfer informasi genetik akan terganggu. Hal ini
disebabkan karena senyawa antimikroba akan menghambat aktivitas enzim RNA
polimerase dan DNA polimerase, yang selanjutnya dapat menginaktivasi atau
merusak materi genetik sehingga mengganggu proses pembelahan sel untuk
pembiakan.
DAFTAR PUSTAKA
Alakomi HL, Skytta E, Saarela M, Mattila-Sandholm T. 2000. Lactic acid permeabilizes Gram- negatif bacteria by disrupting the outer membrane. J.
Appl. Environ. Microbiol. 66:2001-2005.
August EG. 2000. Kajia n Penggunaan Lipase Amobil dari Aspergillus niger pada Pembuatan Monoasilgliserol yang Bersifat Antibakteri dari Minyak Kelapa. Thesis Program Pascasarjana I P B. Bogor.
Bautista DA, Hill AR, Griffiths MW. 1993. An all natural approach to preserve cottage cheese. Modern Dairy 72 (1):12-13.
Best GK. 1999. Antibacterial Chemotheraphy. http://pharminto.com/publ/msb/ Newdrgs.html. (18 Agustus 1999).
Blaszyk M, Holley RA. 1998. Interaction of monolaurin, eugenol and sodium citrace on growth of common meat spoilage and pathogenic organisms. Int.
J. of Food Microbiol. 39:175-183.
Blom H. 1997. Addition of 2,5% Lactate and 0,25% acetate control growth of
Listeria monocytogenes in vacuum-packed, sensory-acceptable servelat
sausage and cooked ham stored at 4 oC. Int. J. of Food Microbiol. 38:71-76.
Bloomfield SF. 1991. Methods for Assessing Antimicrobial Activity. Di dalam: Denyer S P, Hugo WB (ed). Mechanism of action of chemical biocides their
Brannen AL. 1993. Introduction to Use of Antimicrobials. Di dalam: Davidson PM, Branen AL (ed) Antimicrobial in Food. Marcel Dekker.New York.
Cabo ML, Braber AF, Koenreaad PM. 2002. Apparent antifungal activity of several lactic acid bacteria againts Penicillium discolor is due to acetic acid in the medium. J. of Food Protec. 65: 1309-1316.
Castilo A, Lucia LM, Mercado I, Acuff GR. 2001. In-plant evaluation of a lactic acid treatment for reductio n of bacteria on chilled beef carcasses. J. of Food
Protec, vol 64 no 5:738-740.
Chipley JR, Story LD, Todd PT. 1981. Inhibition of Aspergillus growth and extracellular aflatoxin accumulation by sorbic acid and derivative of fatty acid. J. Food Safety 3:109-120.
Cuesta M. 2000. Requirement of autolytic activity for bacteriocin- induced lysis.
Appl. and Env. Microbiology. 2000. p. 3174-3179.
Daeschei MA. 1989. Antimicrobial substances from lactic acid bacteria for use as food preservatives. Food Technology.
Davidson PM, Branen AL. 1994. Antimicrobials in Food. Marcel Dekker, New York.
D, Aost JY. 2000. Salmonella. Di dalam: Lund BM, Baird-Parker TC, Gould GW (ed). The Microbiological Safety and Quality of Food. Volume 3. Aspen Publisher Inc. Maryland.
Duxbury DD. 1986. Combination emulsifier/acidulant extend cheese seauce shelf life. Food Proc. 46(9): 38-39.
Fardiaz S. 1989. Mikrobiologi Pangan. Depdikbud, Dirjen Dikti, PAU Pangan dan Gizi, IPB. Bogor.
Frazier WC, Westhof DC. 1987. Food Microbiology. McGraw Hill Publishing Iowa USA.
Garburtt J. 1997. Essentials of Food Microbiology. Arnold, London, Sydney, Auckland.
Gourama H, Bullerman B. 1995. Antimycotic and antiaflatoxigenik effect of lactic acid bacteria. J. of Food Protec. Vol. 57, No. 11: 1275-1280.
Granum PE, Baird – Parker TC. 2000. Bacillus species. Di dalam: Lund BM, Baird-Parker TC, Gould GW (ed). The Microbial Safety and Quality of
Food Vol II. Maryland: Aspen. Hlm 1029-1039.
Hasenhuetti G L, Hartel RW. 1997. Food Emulsifies and Their Applications. International Thomson Publishing. New York.
Hofvendahl K, Barebel H. 2000. Factor affecting the fermentative lactic acid production from renewable resources. Enzyme and Microbial Technology
26: 87-107.
Igoe RS, Hui YH 1996. Dictionary of Food Ingredient 3 rd ed Chapman and Hall, New York.
Indriyati W. 2004. Kajian Aktivitas Antimikroba Campuran Mono dan Diasilgliserol Hasil Pemanfaatan Destilat Asam Lemak Minyak Kelapa. Thesis Sekolah Pascasarjana Institut Pertanian Bogor, Bogor.
Jay JM.1996. Modern Food Microbiology 5th edition. Chapman and Hall, New York.
Jenie BSL.1996a. Peranan bakteri asam laktat sebagai pengawet hayati makanan.
J. Ilmu dan Teknol. Pangan. 1 (2):60 – 73.
Jenie BSL, Fardiaz S, Tandriarto N. 1996b. Produksi kultur kering Lactobacillus
plantarum dan aplikasinya pada pengawetan ikan lamuru. Seminar Permi,
11 – 13 November 1996.
Jenie BSL. 1999. Peranan Bakteri Asam Laktat Sebagai Pangawet Pangan Non Fermentasi. Materi Pengajaran Mata Kuliah Bioteknologi Bakteri Asam Laktat. Program Studi Ilmu Pangan Program Sarjana Institut Pertanian Bogor.
Jenie BSL, Atifah N, Suliantari. 2001. Peningkatan keamanan dan mutu pindang ikan kembung (Rastellinger sp) dengan aplikasi kombinasi natrium asetat, bakteri asam laktat dan pengemasan Vakum. J. Ilmu dan Teknol. Pangan.
XII (1): 21 – 27.
Kabara JJ. 1993. Medium-Chain Fatty Acids and Esters. Di dalam: Davidson, P. M danA. L Branen (ed), Antimicrobial in Food 2nd ed. Marcel Dekker, New York.
Kanazawa A, Ikeda T dan Endo T. 1995. A novel approach to mode of action of cationic biocides morphological effect on antibacterial activity. J Appl
Bacteriol 78:55-60.
Kim JM, Marshall MR, Wei CI, 1995. Antibacterial activity in extracts of Camelia
japonica L. petals and its application to a model food system. J. Food
Protec. 1255-1260.
Leverentz B, et al. 2006. Biocontrol of the food-borne pathogens Listeria
monocytogenes and Salmonella enterica serovar poona on fresh-cut apples
with naturally occurring bacterial and yest antagonists. Appl. Environ.
Microbiol. 72 : 1135-1140.
Lisker N, Poster N. 1982. Antifungal activity of lauricidin and related compounds.
J. Food Safety 4:27-32.
Loessner M, Susane G, Sandra S, Siegfried S. 2003. A pediocin – producing
Lactobacillus plantarum strain inhibits Listeria monocytogenes in a
multispesies cheese surface microbial ripening consortium. App and Env.
Microbiol p. 1854-1857.