INHIBISI EKSTRAK ETANOL KUMIS KUCING, PEGAGAN,
SAMBILOTO, DAN TEMPUYUNG TERHADAP AKTIVITAS
ENZIM PENGUBAH ANGIOTENSIN I SECARA
IN VITRO
LANY YULINDA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
LANY YULINDA. Inhibisi Ekstrak Etanol Kumis Kucing, Pegagan, Sambiloto,
dan Tempuyung terhadap Aktivitas Enzim Pengubah Angiotensin I secara
In Vitro
.
Dibimbing oleh DYAH ISWANTINI PRADONO dan LATIFAH K.
DARUSMAN.
Kumis kucing, pegagan, sambiloto, dan tempuyung merupakan tanaman obat
yang berpotensi sebagai antihipertensi. Ekstrak etanol 30% tanaman ini diteliti
daya inhibisinya terhadap aktivitas enzim pengubah angiotensin I (ACE) secara
in
vitro
. Penelitian dilakukan pada kondisi optimum (suhu 32 °C, pH 8.3, dan
konsentrasi ACE 25 mU/mL) menggunakan ekstrak tunggal dengan konsentrasi
14, 25, 50, dan 100 ppm serta ekstrak gabungan dengan komposisi tertentu.
Hasilnya dibandingkan dengan kaptopril sebagai kontrol positif. Uji inhibisi ACE
dengan ekstrak tunggal menunjukkan bahwa ekstrak tunggal kumis kucing 50
ppm, pegagan 100 ppm, sambiloto 100 ppm, dan tempuyung 14 ppm, memiliki
daya inhibisi terbesar, berturut-turut sebesar 76.98, 58.69, 53.74, dan 62.89%.
Gabungan ekstrak kumis kucing, pegagan, dan tempuyung dengan komposisi
25:50:7 memiliki inhibisi sebesar 76.87%, lebih besar daripada kaptopril.
ABSTRACT
LANY YULINDA. In Vitro Inhibition of Ethanol Extract of
Kumis Kucing
,
Pegagan
,
Sambiloto
, and
Tempuyung
towards Angiotensin I Converting Enzyme
Activity. Supervised by DYAH ISWANTINI PRADONO and LATIFAH K.
DARUSMAN
INHIBISI EKSTRAK ETANOL KUMIS KUCING, PEGAGAN,
SAMBILOTO, DAN TEMPUYUNG TERHADAP AKTIVITAS
ENZIM PENGUBAH ANGIOTENSIN I SECARA
IN VITRO
LANY YULINDA
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Inhibisi Ekstrak Etanol Kumis Kucing, Pegagan, Sambiloto, dan
Tempuyung terhadap Aktivitas Enzim Pengubah Angiotensin I secara
In
Vitro
Nama : Lany Yulinda
NIM : G44086007
Menyetujui
Pembimbing I
Dr. Dyah Iswantini Pradono, MAgr
NIP
19670730 199103 2 001Pembimbing II
Prof. Dr. Ir. Latifah K. Darusman, MS
NIP 19530824 197603 2 001
Mengetahui:
Ketua Departemen Kimia,
Prof. Dr. Ir. Tun Tedja Irawadi, MS
NIP 19501227 197603 2 002
PRAKATA
Alhamdulillah, puji syukur ke hadirat Allah SWT karena berkat rahmat dan
hidayah-Nya, penulis dapat menyusun dan menyelesaikan karya ilmiah. Karya
ilmiah ini disusun berdasarkan penelitian yang dilaksanakan pada bulan Juni
sampai November 2010 bertempat di Laboratorium Pusat Studi Biofarmaka,
Institut Pertanian Bogor.
Penulis mengucapkan terima kasih kepada Dr. Dyah Iswantini Pradono,
MAgr dan Prof. Dr. Ir. Latifah K. Darusman, MS selaku pembimbing yang telah
memberi banyak arahan, motivasi, saran, dan solusi dari setiap permasalahan yang
dihadapi penulis selama melaksanakan penelitian dan penulisan karya ilmiah ini.
Penulis mengucapkan terima kasih kepada Pusat Studi Biofarmaka melalui
penelitian KKP3T atas materi dan bantuan dana yang diberikan pada penelitian ini.
Penulis juga berterima kasih kepada Ibu
Nunuk, Mba Ina, Mba Dina, Bapak Didi,
Wiwi, Endi dan Nio di Pusat Studi Biofarmaka yang telah membantu penulis
dalam pemakaian alat dan bahan di laboratorium tersebut.
Ungkapan terima kasih kepada Ibu dan kakak atas dukungannya baik secara
rohani maupun material. Tak lupa, ungkapan terima kasih penulis sampaikan
kepada teman-teman seperjuangan di kelas penyelenggaraan khusus angkatan
2008, teman satu bimbingan (Anggi, Mba Rani, dan Eka) dan teman satu
laboratorium (Paul, Ayu, Mitha, Irul, Danang) yang telah memberikan semangat
dan motivasi dalam menyusun karya ilmiah ini.
Semoga tulisan ini bermanfaat dan dapat menambah wawasan ilmu
pengetahuan khususnya bagi penulis dan pembaca pada umumnya.
Bogor, Agustus 2011
RIWAYAT HIDUP
Penulis dilahirkan di Sumedang pada tanggal 19 Juli 1986 dari Ayah (Alm)
Khaidir dan Ibu Tisnawati. Putri kedua dari dua bersaudara.
Penulis menyelesaikan pendidikan menengah atas di SMU Negeri 1
Cikampek pada tahun 2000 dan pada tahun yang sama, lulus seleksi masuk
Akademi Kimia Analisis Bogor (AKA). Setelah lulus dari AKA pada tahun 2006,
bekerja sebagai staf
Quality Assurance
(QA) di PT Kalbe Morinaga Indonesia
selama periode tahun 2007
˗
2008. Pada tahun 2008 melanjutkan kembali
pendidikan di Institut Pertanian Bogor Kelas Penyelenggaraan Khusus Program
Studi Kimia.
DAFTAR ISI
Halaman
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... vii
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Hipertensi... 1
Enzim Pengubah Angiotensin I (ACE) ... 2
Kumis Kucing ... 2
Pegagan... 2
Sambiloto ... 3
Tempuyung ... 3
BAHAN DAN METODE
Bahan dan Alat ... 3
Metode Penelitian ... 3
HASIL DAN PEMBAHASAN
Kadar Flavonoid ... 5
Kadar Air ... 6
Ekstraksi ... 6
Uji Toksisitas Larva Udang ... 6
Inhibisi Ekstrak Tunggal terhadap Aktivitas ACE secara
In Vitro
... 7
Inhibisi Ekstrak Gabungan terhadap Aktivitas ACE secara
In Vitro
... 8
SIMPULAN DAN SARAN
Simpulan ... 9
Saran ... 9
DAFTAR PUSTAKA ... 9
DAFTAR GAMBAR
Halaman
1
Reaksi yang dikatalisis oleh ACE... 2
2
Tanaman kumis kucing ... 2
3
Tanaman pegagan ... 2
4
Tanaman sambiloto ... 3
5
Tanaman tempuyung ... 3
6
Nilai LC
50ekstrak etanol kumis kucing, pegagan, sambiloto dan
tempuyung terhadap
A. salina
... 7
7
Persen inhibisi ekstrak etanol kumis kucing, pegagan, sambiloto
dan tempuyung terhadap aktivitas enzim ACE ... 8
8
Persen inhibisi kontrol positif dan gabungan ekstrak kumis kucing
(K), pegagan (P), sambiloto (S), dan tempuyung (T) terhadap aktivitas
enzim ACE ... 8
9
Struktur kaptopril ... 9
10
Struktur ACE ... 9
DAFTAR LAMPIRAN
Halaman
1
Bagan alir penelitian ... 13
2
Kurva standar kuersetin ... 14
3
Kadar flavonoid kumis kucing, pegagan, sambiloto, dan tempuyung ... 15
4
Kadar air kumis kucing, pegagan, sambiloto, dan tempuyung ... 16
5
Aktivitas ekstrak sampel terhadap larva
A. salina
setelah 24 jam ... 17
6
Contoh perhitungan nilai LC
50ekstrak sampel menggunakan
metode probit ... 18
7
Kurva standar asam hipurat ... 19
8
Hasil uji aktivitas ekstrak sampel terhadap enzim ACE secara
in vitro
... 20
PENDAHULUAN
Indonesia dikelilingi oleh 17 000 pulau dan merupakan negara kepulauan terbesar di dunia. Hampir 60% wilayahnya tertutup oleh hutan, sehingga menjadi rumah bagi sekitar 90% spesies tanaman obat di kawasan Asia Tenggara (Handa et al. 2006). Berbagai macam tanaman obat telah diteliti untuk diketahui aktivitasnya terhadap berbagai macam penyakit. Salah satu penyakit yang mengancam masyarakat sekarang ini adalah hipertensi.
Obat antihipertensi yang sekarang ini banyak digunakan adalah inhibitor enzim pengubah angiotensin I (ACE). Inhibitor ACE bekerja dengan cara menurunkan atau mencegah pembentukan angiotensin II yang dapat meningkatkan tekanan darah. Hansen et al. (1995) meneliti berbagai tanaman obat yang berasal dari India, Cina, dan Cili melalui pendekatan terhadap ACE, begitu pula Yingsukpisarn (2005) yang meneliti berbagai tanaman di Thailand. Tanaman lain yang juga telah diteliti sebagai inhibitor ACE antara lain Ruellia praetermissa oleh Salah et al. (2001) dan Lee et al. (2004) yang meneliti sejenis jamur Tricholoma giganteum sebagai inhibitor ACE.
Pegagan, kumis kucing, sambiloto, dan tempuyung telah dikenal sebagai obat-obatan herbal alami. Kumis kucing dan sambiloto telah lama digunakan oleh masyarakat Asia sebagai tanaman obat tradisional untuk mengobati hipertensi (Hembing 1997; Jarukamjorn dan Nemoto 2008; BIT-LIPI 2009). Pegagan serta tempuyung juga telah diteliti oleh Darusman et al. (2009) sebagai tanaman yang berpotensi menjadi obat antihipertensi. Oleh karena itu, keempat tanaman tersebut dipilih untuk diteliti daya inhibisinya terhadap ACE. Selain telah dipercaya sebagai antihipertensi, tanaman ini mengandung senyawa golongan flavonoid (Olah et al. 2003; Krishnaiah et al. 2009; Roy et al. 2010; Sriningsih et al. 2005). Pendekatan aktivitas senyawa golongan flavonoid terhadap ACE belum banyak diteliti di Indonesia. Sementara hasil penelusuran dokumen paten di Kantor Paten pada tanggal 6 Juli 2010 menunjukkan telah terdapat paten mengenai senyawaan flavonoid sebagai antihipertensi, di antaranya kuersetin (Jalili 2004), flavonoid dari tanaman Passiflora sp. (Foo et al. 2006), dan flavonol glikosida (Verhoeyen dan Wiseman 2008).
Penelitian Darusman et al. (2009) terhadap tanaman pegagan dan tempuyung merupakan
yang pertama kalinya di Indonesia. Daya inhibisi yang diperoleh masih relatif rendah, sehingga perlu dilakukan kembali penelitian berbagai tanaman obat sebagai inhibitor ACE, dengan terlebih dahulu melakukan uji kuantitatif senyawa flavonoid. Dalam penelitian ini, daya inhibisi ekstrak etanol dari kumis kucing, pegagan, sambiloto, dan tempuyung yang mempunyai kandungan flavonoid tertinggi terhadap enzim ACE diuji secara in vitro.
TINJAUAN PUSTAKA
Hipertensi
Hipertensi (tekanan darah tinggi) adalah kenaikan tekanan arteri melebihi normal dan tekanan itu bertahan. Menurut WHO, definisi hipertensi ialah arus tekanan darah sistolik 140 mmHg atau lebih atau arus tekanan darah diastolik 90 mmHg atau lebih. Pada kebanyakan kasus, hipertensi terdeteksi saat pemeriksaan fisik karena penyakit tertentu,
sehingga sering disebut sebagai “the silent killer” dan tanpa disadari, penderita mengalami komplikasi pada organ-organ vital seperti jantung, otak, atau ginjal. Hipertensi menjadi penyebab kematian nomor 3 setelah strok dan tuberkulosis, yakni mencapai 6.7% dari populasi kematian pada semua umur di Indonesia (Depkes RI 2009).
Flavonoid merupakan senyawa kimia polifenol yang dapat dicirikan melalui aktivitas farmakologi seperti antioksidan, antihelmintik, antiradang, antivirus, dan antitumor. Kebanyakan aktivitas tersebut karena kemampuan flavonoid untuk menghambat enzim seperti tripsin, protein kinase, dan topoisomerase (Barolli et al. 2000). Penelitian-penelitian lain secara umum memperlihatkan bahwa senyawa aktif untuk antihipertensi berasal dari senyawa golongan flavonoid, di antaranya flavan-3-ol dan prosianidin (Actis-Goretta et al. 2003). Senyawa aktif kuersetin menjadi salah satu senyawa flavonoid yang telah diuji antihipertensi secara in vitro (Duarte et al. 2001; Perez-Viscaino et al. 2009).
Enzim Pengubah Angiotensin I (ACE)
peptida ini pada dasarnya mengatalisis reaksi angiotensin I menjadi angiotensin II, dengan memecah dipeptida histidil-leusina dari
ujung˗C angiotensin I menghasilkan
angiotensin II dan asam hipurat (Gambar 1) (Actis-Goretta et al. 2003). Jika hidrolisis angiotensin I berlebihan, maka tekanan darah akan meningkat (Shalaby et al. 2004).
Gambar 1 Reaksi yang dikatalisis oleh ACE (Chusman dan Cheung 1971).
Potensi inhibitor ACE sebelumnya telah dilaporkan oleh Salah et al. (2001) pada tanaman R. praetermissa, oleh Lee et al. (2004) pada sejenis jamur yaitu, T. giganteum, dan secara in vivo oleh Zhao et al. (2007) pada hidrolisat gelatin yang berasal dari timun laut. Di Indonesia sendiri penelitian tentang inhibisi ACE telah dilakukan oleh Darusman et al. (2009) pada tanaman pegagan dan tempuyung.
Kumis Kucing
Kumis kucing (Gambar 2) termasuk famili Lamiaceae dengan marga Orthosiphon dan memiliki nama Latin Orthosiphon stamineus Benth. Tanaman kumis kucing adalah salah satu tanaman obat yang populer, digunakan secara turun-temurun di kawasan Asia Tenggara dalam pengobatan bermacam-macam penyakit.
Gambar 2 Tanaman kumis kucing.
Olah et al. (2003) melakukan penelitian untuk mengetahui komponen-komponen utama yang terkandung di dalam tanaman kumis kucing dengan menggunakan 2 pelarut yang berbeda, etanol 50% dan etanol 70%. Hasil yang diperoleh memperlihatkan bahwa pada kedua ekstrak terdapat senyawa
polifenol, yaitu sinesetin, eufatorin, rosmarinat, kikhorat, dan asam kafeat. Berdasarkan pengujian farmakologi, ekstrak etanol 50% memiliki kemampuan yang lebih baik sebagai diuretik dan urikosurik.
Penelitian untuk membandingkan kumis kucing dengan tanaman lain juga telah dilakukan. Tanaman kumis kucing dibandingkan dengan tanaman dalam famili yang sama, tanaman ground ivy atau Glechoma hederacea L, dalam hal kemampuan sebagai antioksidan. Kedua tanaman ini diuji dalam bentuk ekstrak kasar maupun fraksi menggunakan berbagai pelarut. Hasil yang diperoleh menunjukkan keduanya merupakan antioksidan yang efisien. Tanaman kumis kucing bekerja lebih baik dalam bentuk ekstrak kasar dibandingkan dengan tanaman ground ivy yang perlu melalui tahapan fraksionasi untuk meningkatkan kemampuannya sebagai antioksidan (Matkowski 2008).
Pegagan
Tanaman pegagan (Gambar 3) berdasarkan ilmu taksonomi termasuk famili Apiaceae, marga Centella, dan jenis Centella asiatica L. Tanaman ini biasa digunakan sebagai sayuran tradisional di Cina, India, Srilanka, dan Indonesia, dan telah dibudidayakan di berbagai negara berkembang.
Gambar 3 Tanaman pegagan.
Krishnaiah et al. (2009) telah meneliti komponen-komponen yang terdapat pada 6 tanaman obat, salah satunya pegagan. Hasil penelitian tersebut menyatakan bahwa pegagan mengandung alkaloid, tanin, saponin, flavonoid, dan fenol. Zainol et al. (2008) meneliti lebih jauh lagi kandungan senyawa aktif yang terdapat pada tanaman pegagan, dan diketahui tanaman tersebut mengandung senyawa aktif utama asiatikosida, madekasosida, dan asam asiatat.
antioksidan, dan juga berpotensi sebagai antimikrob serta antifungi.
Sambiloto
Sambiloto (Gambar 4) termasuk famili Acanthaceae, marga Andrographis, dan jenis Andrographis paniculata Nees. Bagian yang digunakan umumnya seluruh bagian tanaman. Sifat khas tanaman ini adalah pahit, mendinginkan dan membersihkan darah.
Gambar 4 Tanaman sambiloto.
Andrografolida merupakan senyawa aktif pada sambiloto yang berpotensi sebagai antibakteri dan antidiabetes. Peranan sambiloto sebagai antioksidan juga telah banyak diteliti, salah satunya oleh Ojha et al. (2009) dengan menggunakan pelarut metanol. Hasil penelitian tersebut menunjukkan sambiloto memiliki kemampuan sebagai antioksidan. Sambiloto dalam ekstrak kloroform menunjukkan fungsi sebagai antimikrob, antara lain pada Escherichia coli dan Salmonella typhymurium. Berdasarkan hasil tersebut, dilakukan analisis komponen yang terkandung pada ekstrak tanaman sambiloto, dan diketahui tanaman tersebut mengandung senyawa fenol, asam karboksilat aromatik, dan ester (Roy et al. 2010).
Tempuyung
Tempuyung (Gambar 5) termasuk tanaman obat asli Indonesia dari famili Asteraceae, marga Sonchus, dan jenis Sonchus arvensis L. Tempuyung tumbuh liar di tempat terbuka yang terkena sinar matahari atau sedikit terlindung. Tumbuhan yang berasal dari Eurasia ini bisa ditemukan pada daerah yang banyak turun hujan pada ketinggian 50˗1.650 m dpl (BIT-LIPI 2009).
Tempuyung mengandung banyak senyawa kimia, seperti golongan flavonoid, kumarin, taraksasterol, dan asam fenolat bebas. Pustaka lain menyebutkan daun tempuyung mengandung senyawa kimia antara lain luteolin, flavon, flavonol, dan auron.
Gambar 5 Tanaman tempuyung.
Sriningsih et al. (2005) meneliti herba tempuyung untuk mengetahui jenis flavonoid yang terkandung di dalamnya menggunakan pelarut metanol. Hasil yang diperoleh menunjukkan kandungan senyawa flavonoid golongan flavon, yakni 7,4’-hidroksiflavon.
Tanaman tempuyung dikenal memiliki efek diuretik. Pada tahun 2006, Imelda dan Andani meneliti efek diuretik tanaman ini dibandingkan dengan furosemida. Furosemida merupakan obat diuretik kuat yang telah teruji secara medis ilmiah dengan kemampuan 60% lebih tinggi dibandingkan dengan diuretik yang lain, dan hasil penelitian tersebut membuktikan tanaman tempuyung mempunyai efek diuretik yang lebih baik daripada furosemida pada dosis tertentu.
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah simplisia pegagan, sambiloto, kumis kucing, dan tempuyung yang diperoleh dari 3 tempat berbeda, yaitu Bogor (Kebun Percobaan Biofarmaka), Sukabumi (Kebun Percobaan Cicurug), dan Bandung (Kebun Percobaan Manoko), etanol 96%, aseton, HCl, AlCl3, air, etanol 30%, telur udang Artemia salina, air laut, Tween-80, hipuril-L-histidil-L-leusina (Sigma), NaCl, NaOH, bufer HEPES (Sigma), ACE (Sigma), kaptopril, dan etil asetat.
Alat yang digunakan adalah spektrofotometer ultraviolet-tampak (UV-Vis) Hitachi, penguap putar, oven, pengering vakum, vial uji, dan inkubator.
Metode Penelitian
Bagan alir penelitian ditunjukkan pada Lampiran 1.
Analisis Kandungan Flavonoid Secara Kuantitatif (Depkes RI 2000)
Analisis kandungan flavonoid dilakukan terhadap simplisia pegagan, kumis kucing, sambiloto, dan tempuyung dari 3 tempat berbeda. Setiap 5 g simplisia diekstraksi dengan cara maserasi dengan etanol 96% (24 jam), selanjutnya direfluks selama 6 jam pada suhu 70 °C dan pelarut diuapkan dengan penguap putar.
Ekstrak ditimbang setara dengan 200 mg simplisia lalu dimasukkan ke dalam labu alas bulat. Sistem hidrolisis ditambahkan ke dalamnya: 1.0 mL larutan heksametilena- tetramina 0.5% (b/v), 20.0 mL aseton, dan 2.0 mL larutan HCl 25%, kemudian dipanaskan sampai mendidih selama 30 menit, dan disaring menggunakan kapas. Selanjutnya ditambahkan kembali aseton sebanyak 20 mL untuk dididihkan kembali selama 30 menit. Pengerjaan dilakukan sebanyak 2 kali. Seluruh filtrat dikumpulkan ke dalam labu takar. Setelah labu mendingin, volume ditepatkan dengan aseton sampai 100 mL dan dikocok hingga tercampur sempurna.
Filtrat hasil hidrolisis diambil sebanyak 20 mL, dimasukkan ke dalam corong pemisah, ditambahkan akuades sebanyak 20 mL, kemudian ditambahkan 15 mL etil asetat untuk pengocokan pertama dan 10 mL etil asetat untuk pengocokan kedua dan ketiga. Fraksi etil asetat dikumpulkan ke dalam labu ukur 50 mL dan ditambahkan etil asetat sampai tepat 50 mL. Sepuluh mL filtrat yang dihasilkan dipindahkan ke dalam labu takar 25 mL, kemudian ditambahkan 1 mL larutan 2 g AlCl3 dalam 100 mL asam asetat glasial 5% (v/v). Larutan asam asetat glasial 5% (v/v) lalu ditambahkan secukupnya sampai tepat 25 mL. Absorbans diukur dengan menggunakan spektrofotometer pada panjang gelombang 370.8 nm dengan kuersetin sebagai standar.
Penetapan Kadar Air (AOAC 1984)
Cawan porselen yang bersih dipanaskan ke dalam oven bersuhu (105+3) °C selama 30 menit dan ditimbang hingga diperoleh bobot konstan cawan kosong. Serbuk simplisia kering ditimbang sebanyak +3 g ke dalam cawan tersebut dan dipanaskan kembali dalam oven (105+3) °C selama 3 jam. Setelah itu, cawan dipindahkan ke dalam desikator selama 15 menit lalu ditimbang. Pengeringan dan
penimbangan sampel dilakukan lagi setiap 1 jam sampai diperoleh bobot konstan.
Ekstraksi Sampel (Darusman et al. 2009)
Serbuk kering simplisia kumis kucing, pegagan, sambiloto, dan tempuyung, yang memiliki kandungan flavonoid tertinggi, masing-masing sebanyak 1 000 g dimaserasi dengan pelarut etanol 30% (2×24 jam), lalu disaring. Filtrat yang diperoleh dipekatkan dengan penguap putar hingga diperoleh ekstrak pekat, kemudian dikeringkan dengan pengering vakum dan disimpan pada suhu -20 °C sampai dilakukan analisis.
Uji Toksisitas Larva Udang (Meyer et al. 1982)
Telur udang A. salina ditetaskan dalam gelas piala yang berisi air laut yang telah disaring. Penetasan dibantu oleh aerasi agar kadar oksigen terlarut dalam air tercukupi sehingga telur udang tersebut menetas menjadi larva. Larutan ekstrak dibuat menjadi 2 000 ppm, yaitu sebanyak 0.02 g ekstrak dilarutkan dalam 10 mL air laut. Ekstrak yang sukar larut dapat dibantu dengan penambahan Tween-80. Setelah 48 jam, sebanyak 10 ekor larva udang dan 1 000 µL air laut dimasukkan ke dalam vial uji. Selanjutnya diikuti dengan penambahan 1 000 µL larutan ekstrak sehingga konsentrasi akhir dalam vial adalah 1 000 ppm. Penambahan 500 µL larutan ekstrak dan 1 500 µL air laut dilakukan untuk konsentrasi 500 ppm, 100 µL larutan ekstrak dan 1 900 µL air laut untuk 100 ppm, dan 10 µL larutan ekstrak dan 1 990 µL air laut untuk 10 ppm. Setiap konsentrasi dilakukan 3 kali pengulangan. Kontrol dilakukan tanpa penambahan larutan ekstrak. Setelah 24 jam, larva udang yang mati dihitung.
Penentuan Daya Inhibisi Terhadap
Aktivitas ACE Secara In Vitro (Chusman dan Cheung 1971)
Aktivitas inhibisi ACE diukur dengan metode Chusman dan Cheung (1971) dengan sedikit modifikasi pada komposisi substrat.
Larutan sampel sebanyak 50 L dengan 50 L
larutan ACE (25 mU/mL) di pra-inkubasi pada 32 oC selama 10 menit, kemudian
campuran diinkubasi dengan 50 L substrat
penambahan 1.5 mL etil asetat, dan disentrifugasi (4000×g) selama 15 menit. Satu mL supernatan dipindahkan ke tabung reaksi yang lain dan diuapkan pada suhu kamar selama 2 jam dalam vakum atau pengering oven. Setelah kering, dilarutkan dalam 3 mL air distilasi dan absorbans ditentukan pada panjang gelombang 228 nm menggunakan spektrofotomer UV-Vis.
HASIL DAN PEMBAHASAN
Kadar Flavonoid
Tanaman obat sebanyak 16 sampel dari 4 jenis tanaman yang berbeda diuji kadar flavonoidnya untuk mengetahui pengaruh kadar flavonoid terhadap nilai inhibisi ACE, karena senyawa flavonoid diduga berperan sebagai inhibitor ACE. Perbedaan sampel dijumpai pada jenis tanaman kumis kucing dan pegagan asal Sukabumi dan Bandung.
Kumis kucing yang diuji kadar flavonoid ada 2 jenis yang berbeda, yaitu kumis kucing bunga putih dan bunga ungu. Sementara tanaman pegagan yang diuji ada beberapa jenis yang dibedakan dengan nomor harapan, yaitu nomor jenis tanaman pegagan yang berpotensi sebagai obat antihipertensi. Pemberian nomor harapan pada pegagan diawali dengan kata CASI, yang berarti Centella asiatica.
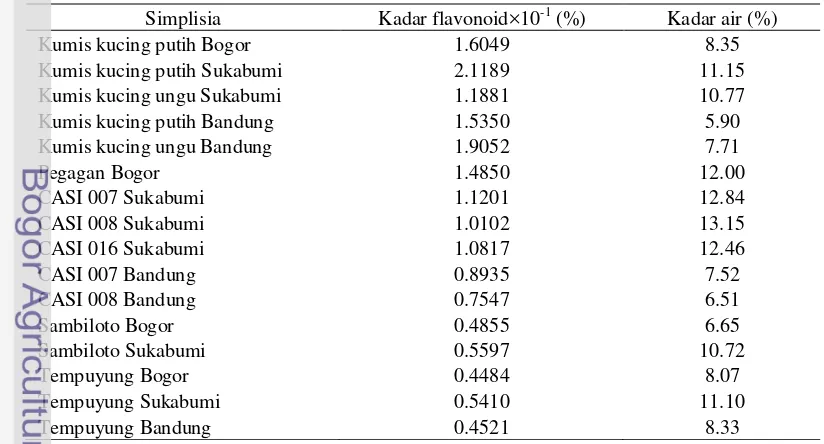
Hasil analisis kadar flavonoid dari keseluruhan sampel dapat dilihat pada Tabel 1. Penggunaan simplisia dari 3 tempat berbeda memungkinkan adanya perbedaan kandungan hara. Kadar flavonoid tertinggi yang diperoleh pada masing-masing jenis tanaman dapat digunakan sebagai rujukan untuk pembudidayaan tanaman dari segi kandungan flavonoid. Variasi hasil yang diperoleh mencerminkan variasi informasi kimiawi contoh yang timbul akibat perbedaan asal dan kondisi lingkungan. Chew et al. (2004) menyatakan bahwa asal contoh yang berbeda memiliki pengaruh yang dominan terhadap variasi kandungan kimia contoh.
Day dan Underwood (1981) menggolongkan perolehan analit hasil analisis kuantitatif dalam 3 kelompok, yaitu analit yang merupakan penyusun utama, penyusun minor dan penyusun kelumit. Analisis kuantitatif pada seluruh ekstrak simplisia memperlihatkan keberadaan flavonoid sebagai penyusun minor karena kadar yang dimiliki berada di antara 0.01 dan 1%. Dengan demikian, walaupun flavonoid pada tanaman berperan strategis dalam mekanisme pengobatan, jumlahnya dalam seluruh tanaman tersebut tidak begitu banyak. Lampiran 2 memberikan persamaan kurva standar kuersetin yang digunakan untuk menentukan kadar flavonoid, sedangkan perhitungan kadar flavonoid terdapat pada Lampiran 3
Tabel 1 Kadar flavonoid dan kadar air tanaman
Simplisia Kadar flavonoid×10-1 (%) Kadar air (%)
Kumis kucing putih Bogor 1.6049 8.35
Kumis kucing putih Sukabumi 2.1189 11.15
Kumis kucing ungu Sukabumi 1.1881 10.77
Kumis kucing putih Bandung 1.5350 5.90
Kumis kucing ungu Bandung 1.9052 7.71
Pegagan Bogor 1.4850 12.00
CASI 007 Sukabumi 1.1201 12.84
CASI 008 Sukabumi 1.0102 13.15
CASI 016 Sukabumi 1.0817 12.46
CASI 007 Bandung 0.8935 7.52
CASI 008 Bandung 0.7547 6.51
Sambiloto Bogor 0.4855 6.65
Sambiloto Sukabumi 0.5597 10.72
Tempuyung Bogor 0.4484 8.07
Tempuyung Sukabumi 0.5410 11.10
Kadar Air
Kandungan air dalam suatu bahan memengaruhi daya tahannya terhadap serangan mikrob, sehingga dapat diperkirakan cara penanganan terbaik bagi sampel dalam hal tempat dan waktu penyimpanan. Data kadar air ditunjukkan pada Tabel 1, sedangkan perhitungannya di Lampiran 4.
Kadar air yang diperoleh dari masing-masing serbuk tanaman bergantung pada asal tanaman tersebut diperoleh. Menurut Winarno (1997), apabila kadar air yang terkandung dalam suatu bahan kurang dari 10%, maka kestabilan optimum bahan akan tercapai dan pertumbuhan mikrob dapat dikurangi. Menurut Fardiaz (1989), air dapat memengaruhi penampakan, tekstur, serta cita rasa makanan. Air juga akan memengaruhi daya tahan bahan pangan terhadap serangan mikrob yang dinyatakan dengan aw, yaitu
jumlah air bebas yang dapat digunakan oleh mikroorganisme untuk pertumbuhannya.
Berdasarkan kadar air yang diperoleh pada penelitian, serbuk tanaman dari daerah Bogor dan Bandung relatif stabil terhadap serangan mikrob, sedangkan serbuk tanaman dari daerah Sukabumi dengan nilai kadar air di atas 10% mungkin dikarenakan kelembapan yang lebih di daerah tersebut atau hasil pengukuran yang belum konstan. Serbuk tanaman dengan nilai kadar air lebih dari 10% harus langsung digunakan agar tidak terjadi penyimpangan, atau dapat dikeringkan kembali untuk menghindari aktivitas mikrob.
Ekstraksi
Ekstraksi digunakan untuk memperoleh kandungan senyawa yang larut dalam pelarut. Ekstraksi dilakukan secara maserasi dengan menggunakan pelarut etanol 30% selama 2×24 jam. Maserasi merupakan metode ekstraksi komponen dengan merendam contoh dalam pelarut yang sesuai selama waktu tertentu. Maserasi cocok digunakan untuk senyawa yang belum diketahui sifat-sifatnya, karena dapat menjaga kandungan senyawa dalam sampel yang tidak tahan panas agar tidak rusak, sehingga ekstrak diperoleh dalam jumlah yang besar.
Etanol 30% dipilih sebagai pelarut ekstraksi berdasarkan penelitian sebelumnya yang dilakukan oleh Darusman et al. (2009): ekstrak etanol 30% memiliki aktivitas inhibisi yang optimum. Simplisia tanaman yang diektraksi adalah yang memiliki kandungan flavonoid setara kuersetin tertinggi, yaitu
kumis kucing bunga putih asal Sukabumi, pegagan asal Bogor, dan sambiloto asal Bogor.
Rendemen ekstrak etanol kumis kucing, pegagan, sambiloto, dan tempuyung berturut-urut adalah 6.82, 5.96, 7.12 dan 9.05%. Hasil tersebut menunjukkan bahwa pelarut etanol 30% bekerja lebih efektif pada simplisia tanaman tempuyung, mungkin dikarenakan perbedaan kandungan senyawa dari masing-masing simplisia tanaman tersebut.
Uji Toksisitas Larva Udang
Nilai konsentrasi letal 50% (LC50) yang dihasilkan dari uji letalitas larva udang (BSLT) secara umum memberikan indikasi adanya senyawa toksik yang terkandung dalam suatu bahan alam. Larva udang yang digunakan adalah yang berada pada kondisi paling peka terhadap kondisi lingkungannya. Membran kulitnya yang sangat tipis, memungkinkan terjadinya difusi zat dari lingkungan yang memengaruhi metabolisme dalam tubuhnya. Biasanya dipilih larva berumur 2 hari atau 48 jam. Jika berumur lebih dari 48 jam, dikhawatirkan kematian larva bukan disebabkan toksisitas ekstrak, melainkan oleh terbatasnya persediaan makanan (Meyer et al. 1982).
Uji toksisitas diperlukan untuk mengetahui konsentrasi yang dapat menyebabkan keracunan sehingga dapat diketahui jumlah penggunaan yang tepat. LC50 adalah konsentrasi dari suatu bahan yang dapat menyebabkan 50% kematian dalam suatu populasi, dalam hal ini A. salina. Jumlah larva udang yang mati dihitung setelah penambahan ekstrak selama 24 jam (Lampiran 5). Contoh perhitungan nilai LC50 menggunakan metode probit diberikan pada Lampiran 6.
Gambar 6 Nilai LC50 ekstrak etanol kumis kucing, pegagan, sambiloto dan tempuyung terhadap A. salina.
Inhibisi Ekstrak Tunggal terhadap Aktivitas ACE secara In Vitro
Seluruh ekstrak tanaman yang telah diperoleh nilai toksisitasnya diuji aktivitas ACE secara in vitro menggunakan metode Chusman dan Cheung (1981) dengan sedikit modifikasi pada komposisi substrat (Hip-His-Leu 8 mM dalam buffer HEPES 50 mM yang mengandung NaCl 300 mM pada pH 8.3). Konsentrasi yang digunakan pada pengujian berada di bawah nilai LC50 dari masing-masing ekstrak, maka menurut LC50 yang diperoleh, dipilih konsentrasi terendah hingga mencapai 400 ppm. Namun, konsentrasi ekstrak di atas 100 ppm membuat ACE sangat tidak stabil yang akan berpengaruh pada hasil yang diperoleh. Karena itu, dalam pengujian digunakan konsentrasi 14, 25, 50, dan 100 ppm.
Pengujian pada konsentrasi bervariasi ini dimaksudkan untuk melihat pengaruh penambahan konsentrasi ekstrak terhadap peningkatan daya inhibisi. Pengujian dilakukan dengan blangko (tanpa penambahan ekstrak) dan kontrol positif (kaptopril pada konsentrasi 14 dan 100 ppm). Hasil yang diperoleh berupa absorbans. Semakin rendah nilai absorbans yang dihasilkan, semakin besar daya inhibisi terhadap aktivitas ACE. Uji enzimatik dilakukan pada kondisi optimum, yakni pada suhu inkubasi 32 °C, pH 8.3, konsentrasi enzim ACE 25 mU/mL, dan waktu inkubasi 30 menit. Panjang gelombang maksimum yang digunakan sebesar 228 nm (Darusman et al. 2009). Absorbans yang terukur berasal dari sisa asam hipurat hasil reaksi antara substrat dan ACE yang tidak dihambat oleh ekstrak tanaman. Absorbans ini kemudian diubah menjadi konsentrasi asam hipurat berdasarkan persamaan linear kurva standar, yakni y = 0.0547x + 0.0068 dengan
nilai R2 sebesar 0.999 (Lampiran 7). Nilai y adalah absorbans asam hipurat yang terukur dan x adalah konsentrasi asam hipurat tersebut. Hasil uji (Lampiran 8) menunjukkan bahwa semua ekstrak yang diuji berpotensi menghambat aktivitas ACE, kecuali ekstrak tempuyung pada konsentrasi 50 dan 100 ppm. Kedua konsentrasi tersebut menghasilkan nilai negatif, berturut-turut sebesar ˗26.30% dan
˗141.01%. Hasil negatif pada inhibisi ACE tidak berarti bahwa tanaman tersebut tidak bekerja sebagai obat, sebaliknya mungkin dapat bekerja pada mekanisme reaksi hipotensi (Hansen et al. 1995). Daya inhibisi ekstrak tidak selalu mengalami peningkatan seiring dengan meningkatnya onsentrasi ekstrak, hal ini mungkin dikarenakan ketidakstabilan ACE.
Gambar 7 menunjukkan daya inhibisi dari variasi konsentrasi masing-masing ekstrak etanol kumis kucing, pegagan, sambiloto, dan tempuyung. Terlihat bahwa masing-masing ekstrak memiliki daya inhibisi terbesar di konsentrasi yang berbeda-beda. Ekstrak etanol kumis kucing memiliki inhibisi terbesar pada konsentrasi 50 ppm, pegagan pada konsentrasi 100 ppm, sambiloto 100 ppm, dan tempuyung 14 ppm. Hasil yang diperoleh pada ekstrak etanol pegagan dan tempuyung sesuai dengan penelitian sebelumnya (Darusman et al. 2009). Senyawa metabolit sekunder dalam ekstrak etanol kumis kucing, pegagan, sambiloto, dan tempuyung yang diduga dapat menginhibisi aktivitas ACE adalah flavonoid. Namun, berdasarkan data kadar flavonoid, inhibisi pegagan seharusnya lebih besar daripada tempuyung. Diperoleh hasil sebaliknya, hal ini menunjukkan bahwa hasil inhibisi tidak bergantung pada besarnya kandungan flavonoid pada tanaman.
Flavonoid merupakan kelas utama senyawa polifenol yang menunjukkan berbagai aktivitas farmakologi. Senyawa ini menarik bagi para peneliti dan farmakologis karena beberapa alasan, di antaranya sebagian besar bahan makanan yang kaya akan flavonoid seperti teh, anggur, bawang putih, apel, dan cokelat hitam secara umum diketahui memiliki efek terhadap kardiovaskular sehingga tanaman obat yang mengandung senyawa flavonoid banyak digunakan sebagai obat-obatan (Perez-Vizcaino et al. 2009). Senyawa bioaktif flavonoid yang telah diteliti dapat mencegah terjadinya hipertensi melalui pendekatan terhadap aktivitas ACE adalah flavan-3-ol, prosianidin Actis-Goretta et al. 2003) dan kuersetin (Duarte et al. 2001).
Gambar 7 Persen inhibisi ekstrak etanol kumis kucing, pegagan, sambiloto dan tempuyung terhadap aktivitas enzim ACE.
Berdasarkan rekomendasi JNC VII (2003), mekanisme obat yang dapat digunakan sebagai antihipertensi adalah diuretik, penyekat-β, inhibitor ACE, antagonis kalsium (CCB), dan penghambat reseptor angiotensin (ARB). Inhibitor ACE menyebabkan penurunan angiotensin II dan kenaikan bradikinin, senyawa vasodilator yang potensial, sehingga menyebabkan efek samping hiperkalemia, angiodema, dan batuk kering, akibat dari kenaikan bradikinin (Walker 2007).
Inhibisi Ekstrak Gabungan terhadap Aktivitas ACE secara In Vitro
Ekstrak etanol tunggal yang memiliki daya inhibisi terbesar, yaitu kumis kucing 50 ppm, pegagan 100 ppm, sambiloto 100 ppm, dan tempuyung 14 ppm, digabungkan menjadi beberapa gabungan dan diuji daya inhibisinya
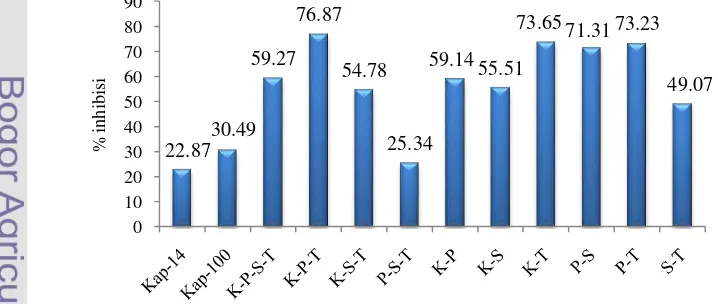
terhadap aktivitas ACE secara in vitro. Gambar 8 menunjukkan daya inhibisi dari kontrol positif kaptopril dan berbagai gabungan ekstrak dengan nisbah yang bervariasi (Lampiran 9). Penggabungan ekstrak tunggal dimaksudkan untuk mendapatkan persen inhibisi yang lebih tinggi. Selain itu, diharapkan diperoleh formulasi obat yang lebih efisien jika diaplikasikan dalam skala industri. Gabungan ekstrak etanol kumis kucing, pegagan, dan tempuyung dengan komposisi 25:50:7 mempunyai daya inhibisi terbesar, yakni 76.87%. Darusman et al. (2009) menyatakan bahwa gabungan ekstrak pegagan dan tempuyung menghasilkan daya inhibisi sebesar 51.27% dengan komposisi 1:2 pada konsentrasi 14 ppm. Dari kedua hasil ini terlihat bahwa komposisi 3 ekstrak tanaman menghasilkan nilai inhibisi lebih baik.
Gambar 8 Persen inhibisi kontrol positif dan gabungan ekstrak kumis kucing (K), pegagan (P), sambiloto (S) dan tempuyung (T) terhadap aktivitas enzim ACE.
76.98 58.69 53.74 62.89 -50 -25 0 25 50 75 100
14 25 50 100
% in h ib is i Konsentrasi (ppm)
Kumis kucing Pegagan Sambiloto Tempuyung
22.87 30.49 59.27 76.87 54.78 25.34 59.14 55.51
73.65 71.31 73.23
49.07 0 10 20 30 40 50 60 70 80 90 % i nhi bi si
Penelitian terhadap pegagan telah dilakukan sebelumnya oleh Hansen et al. (1995) melalui reaksi penghambatan ACE. Penelitian tersebut memperlihatkan bahwa tanaman pegagan memiliki daya inhibisi terbesar dibandingkan dengan tanaman lain yakni sebesar 50% dalam ekstrak etanol 96%. Inhibisi oleh gabungan ekstrak tanaman lebih besar dibandingkan dengan ekstrak tunggalnya maupun dengan kontrol positif (kaptopril 14 dan 100 ppm), yaitu sebesar 22.87 dan 30.49%. Kaptopril (Gambar 9) merupakan obat yang lazim diberikan pada penderita hipertensi. Kaptopril memiliki afinitas yang tinggi terhadap ACE dan berkompetisi dengan angiotensin I, sebagai substrat alami, untuk mencegah terjadinya angiotensin II. Pada penelitian digunakan substrat hipuril-L -histidil-L-leusina sebagai pengganti angiotensin I.
Gambar 9 Struktur kaptopril (Jurca dan Laura 2010).
Chusman dan Ondetti telah melakukan berbagai penelitian sejak 1967 mengenai inhibitor ACE. Hasil-hasil penelitian yang diperoleh membawa keduanya kepada simpulan bahwa inhibitor ACE bekerja dengan cara mengikat tapak aktif dari ACE, yaitu S1, S1' dan S2 (Gambar 10).
Gambar 10 Struktur ACE (Chusman dan Ondetti 1999).
Pengikatan ACE oleh kaptopril dilakukan pada ketiga tapak aktif ACE, namun pengikatan Zn tidak dilakukan oleh
gugus karboksil seperti pada inhibitor lainnya, tetapi oleh gugus –SH. Ternyata hal ini mengakibatkan potensi kaptopril sebagai obat antihipertensi menjadi 1 000 kali lebih kuat (Chusman dan Ondetti 1999). Mekanisme yang terjadi pada inhibitor ACE dapat dijadikan rujukan mekanisme inhibisi yang mungkin terjadi pada ekstrak tanaman, namun harus dibuktikan dengan penelitian lebih lanjut.
SIMPULAN DAN SARAN
Simpulan
Kadar flavonoid tertinggi terdapat pada ekstrak tanaman kumis kucing bunga putih asal Sukabumi (0.21%), pegagan asal Bogor (0.15%), sambiloto asal Bogor (0.056%) dan tempuyung asal Sukabumi (0.054%). Ekstrak etanol 30% tunggal kumis kucing 50 ppm, pegagan 100 ppm, sambiloto 100 ppm, dan tempuyung 14 ppm memiliki daya inhibisi terbesar untuk masing-masing jenis sampel berturut-turut sebesar 76.98, 58.69, 53.74, dan 62.89%. Gabungan ekstrak kumis kucing, pegagan dan tempuyung dengan komposisi 25:50:7 memiliki persen inhibisi sebesar 76.87%.
Saran
Perlu dilakukan penelitian lebih lanjut untuk mengetahui senyawa spesifik yang memengaruhi daya inhibisi terhadap aktivitas ACE.
DAFTAR PUSTAKA
Actis-Goretta L, Ottaviani JI, Keen CL, Fraga CG. 2003. Inhibition of angiotensin converting enzyme (ACE) activity by flavan-3-ols and procyanidin. FEBS Lett 555:597-600.
[AOAC]. 1984. Official Methods of Analysis Virginia: AOAC Int.
Barolli MG, Werner AR, Slep LD, Pamillo AB. 2000. Formation of complexes of flavonoids and metals, determination of the stochiometry and stability constants. Molecules 5:516-517.
http://www.bit.lipi.go.id/pangan_kesehat an/artikel_hipertensi/tanaman_obat.pdf [27 Mei 2010].
Chew OS, Hamdan MR, Ismail Z, Ahmad MN. 2004. Assessment of herbal medicine by chemometrics: assisted interpretation of FTIR spectra. Malaysia: Universiti Sains Malaysia.
Cushman DW, Cheung HW. 1981. Spectrophotometric assay and properties of the angiotensin converting enzyme of the rabbit lung. Biochem Pharmacol 20:1637-1648.
Chusman DW, Ondetti MA. 1999. Design of angiotensin converting enzyme inhibitors. Nat America Inc 5:1110-1113.
Darusman LK, Iswantini D, Indariani S. 2009. Formulasi dan mikroenkapsulasi ekstrak pegagan (Centella asiatica) dan tempuyung (Sonchus arvensis) sebagai antihipertensi: Daya inhibisinya terhadap angiotensin I converting enzyme (ACE) secara in vitro [laporan penelitian]. Bogor: Pusat Studi Biofarmaka.
Day RA, Underwood AL. 1981. Analisa Kimia Kuantitatif. Soendoro R, Widaningsih, Rahadjeng S, penerjemah. Jakarta: Erlangga. Terjemahan dari: Quantitative Analysis.
[Depkes RI] Departemen Kesehatan Republik Indonesia. 2000. Penentuan Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Depkes RI.
[Depkes RI] Departemen Kesehatan Republik Indonesia. 2009. Hipertensi penyebab kematian nomor tiga
[terhubung berkala].
http://www.depkes.go.id/index.php/berit a/press-release/810-hipertensi-penyebab-kematian-nomor-tiga.html [2 April 2010].
Duarte J et al. 2001. Antihypertensive effects of the flavonoid quercetin in spontaneously hypertensive rats. Brit J Pharmacol 133:177-124.
Fardiaz S. 1989. Analisis Mikrobiologi Pangan. Jakarta: Raja Grapindo Persada.
Foo LY, Lu Y, Watson RR, penemu; New Zealand Patent. 24 Jun 2008. Extract of passion fruit and uses there of. US 7390517 B2.
Handa SS, Rakesh DD, Vasisht K. 2006. Compendium of Medicinal and Aromatic
Plants Asia. Italia: United Nations
Industrial Development Organization and The International Centre for Science and High Technology.
Hansen K et al. 1995. In vitro screening of traditional medicines for anti-hypertensive effect based on inhibiton of the angiotensin converting enzyme (ACE). J Ethnopharmacol 48:43-51.
Hembing. 1997. Hidup Sehat Cara Hembing. Jakarta: Elex Media Komputido.
Imelda ER, Andani. 2006. Perbandingan efek diuretika serta kadar natrium dalam darah antara pemberian ekstrak etanol daun tempuyung (Sonchus arvensis Linn) dengan furosemida. J Sains Teknol Farm 11:76-80.
Jalili, penemu; Neddle & Rosenberg. 31 Jan 2008. Quercetine supplementation to treat hypertension. US 0026076 A1.
Jarukamjorn K, Nemoto N. 2008. Pharmacological aspect of Andrographis paniculata on health and its major diterpenoid constituent andrographolide. J Health Sci 54:370-381.
[JNC] Joint National Committe. 2003. The Seventh Report of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure. Maryland: NIH Publication No. 03-5233.
Jurca T, Vicas L. 2010. Complexes of the ACE-inhibitor captopril. Farmacia 58:198-202.
Krishnaiah, Devi, Bono, Sarbatly. 2009. Studies of phytochemical constituents of six Malaysian medicinal plants. J Med Plan 3:067-072.
inhibitory peptide derived from the edible mushroom Tricholoma giganteum. Peptides 25:621-627.
Matkowski A. 2008. Antioxidant activity of extract and different solvent fraction of Glechoma hederacea L. and Orthosiphon stamineus (Benth.) Kudo. Adv Clin Exp Med 615-624.
Meyer BN et al. 1982. Brine shrimp: A convenient general bioassay for active plant constituents. Planta Med 45:31-34.
Ojha SK, Nandave M, Kumari S, Arya DS. 2009. Antioxidant activity of Andrographis paniculata in ischemic myocardium of rats. Glo J Pharm 3:154-157.
Olah N-K, Radu L, Mogosan C, Hanganu D, Gocan S. 2003. Phytochemical and pharmacological studies on Orthosiphon stamineus Benth. (Lamiaceae) hydroalcoholic extract. J Pharm Biomed Anal 33:117-123.
Perez-Vizcaino F, Duarte J, Jimenez R, Santos-Buelga C, Osuna A. 2009. Antihypertensive effects of the flavonoid quercetin. Pharm Rep 61:67-75.
Roy S, Rao K, Bhuvaneswari Ch, Giri A, Mangamoori LK. 2010. Phytochemical analysis of Andrographis paniculata extract and its antimicrobial activity. World J Microbiol Biotechnol 26:85-91.
Salah AM, Dongmo AB, Kamanyi A, Bopelet M, Wagner H. 2001. Angiotensin-converting enzyme-inhibitory effect by Ruellia praetermissa. Pharm Biol 39:16-19.
Setiawan MP. 2006. Inhibisi ekstrak air dan etanol sambiloto (Andographis paniculata [Burm.f.] Ness) terhadap aktivitas tirosin kinase [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Shalaby SM, Zakora M, Otte J. 2006. Performance of two commonly used angiotensin-converting enzyme inhibition assays using FA-PGG and HHL as substrates. J Dairy Res 73:178-186.
Sriningsih et al. 2005. Analisa senyawa golongan flavonoid herba tempuyung (Sonchus arvensis L.). Jakarta: Universitas Pancasila.
Ullah MO, Sultana S, Haque A, Tasmin S. 2009. Antimicrobial, cytotoxic and antioxidant activity of Centella asiatica. Eur J Sci 30:260-264.
Verhoeyen ME, Wiseman SA. penemu; Unilever Intelectual Property Group. 8 Mei 2008. Use of plants with increased levels of flavonol glycosides in reducing hypertension. US 0107792 A1.
Walker L. 2007. Antihypertensive drugs [terhubung berkala].
http://www.drexelmed.edu/documents/ph armacology_physiology/lectures/nov-20-07.pdf [27 Mei 2010].
Winarno FG. 1997. Kimia Pangan dan Gizi. Jakarta: Gramedia Pustaka Utama.
Yingsukpisarn S. 2005. Angiotensin converting enzyme inhibition activity and antihypertensive effect of Thai medical plants [tesis]. Thailand: Faculty of Graduate Studies, Mahidol University.
Zainol NA, Voo SC, Sarmidi MR, Aziz RA. 2008. Profiling of Centella asiatica (L.) urban extract. Malay J Anal Sci 12:322-327.
Lampiran 1 Bagan alir penelitian
Kumis kucing, pegagan, sambiloto, dan tempuyung
Evaluasi kandungan flavonoid secara kuantitatif
Simplisia dengan kandungan flavonoid
tertinggi
Penentuan kadar air, ekstraksi semua sampel, dengan
etanol 30% dan penentuan nilai LC
50semua ekstrak
Lampiran 2 Kurva standar kuersetin
Konsentrasi
kuersetin (ppm)
Absorbans
(
= 370.8 nm
)
0
0.000
1
0.027
3
0.090
6
0.177
12
0.353
24
0.713
50
1.329
y= 0.026x+ 0.016
R²= 0.996
0,000 0,200 0,400 0,600 0,800 1,000 1,200 1,400 1,600
0 10 20 30 40 50 60
A
b
so
rb
an
s
Lampiran 3 Kadar flavonoid kumis kucing, pegagan, sambiloto, dan tempuyung
Sampel
Kadar flavonoid (ppm)
Kadar flavonoid × 10
-1(%)
Rerata kadar flavonoid × 10
-1(%)
Ulangan 1
Ulangan 2
Ulangan 1
Ulangan 2
Sampel asal Bogor
Kumis kucing bunga putih
12.8209
12.8582
1.6026
1.6072
1.6049
Pegagan
11.9254
12.2612
1.4643
1.5056
1.4850
Sambiloto
3.8657
3.9030
0.4832
0.4879
0.4855
Tempuyung
2.9701
3.0075
0.4455
0.4513
0.4484
Sampel asal Sukabumi
Kumis kucing bunga putih
16.8134
17.2239
2.0933
2.1444
2.1189
Kumis kucing bunga ungu
9.5000
9.5373
1.1857
1.1904
1.1881
CASI 007
9.2388
9.2015
1.1223
1.1178
1.1201
CASI 008
8.1194
8.1567
1.0079
1.0125
1.0102
CASI 016
8.7910
8.8284
1.0794
1.0840
1.0817
Sambiloto
4.3881
4.5746
0.5480
0.5713
0.5597
Tempuyung
4.3881
4.4761
0.5480
0.5340
0.5410
Sampel asal Bandung
Kumis kucing bunga putih
12.2985
12.2612
1.5373
1.5327
1.5350
Kumis kucing bunga ungu
15.2836
15.3209
1.9028
1.9075
1.9052
CASI 007
7.1866
7.2239
0.8912
0.8958
0.8935
CASI 008
6.0672
6.1045
0.7524
0.7570
0.7547
Tempuyung
3.0448
3.0821
0.4494
0.4549
0.4521
Kadar flavonoid (%) =
Lampiran 4 Kadar air kumis kucing, pegagan, sambiloto, dan tempuyung
Sampel
Bobot sampel (g)
Bobot sampel kering (g)
Kadar air (%)
Rerata kadar air (%)
Ulangan 1
Ulangan 2
Ulangan 1
Ulangan 2
Ulangan 1
Ulangan 2
Sampel asal Bogor
Kumis kucing bunga putih
2.0004
2.0004
1.8325
1.8342
8.39
8.31
8.35
Pegagan
2.0003
2.0005
1.7613
1.7577
11.95
12.04
12.00
Sambiloto
2.0007
2.0004
1.8672
1.8677
6.67
6.63
6.65
Tempuyung
2.0003
2.0002
1.8383
1.8394
8.10
8.04
8.07
Sampel asal Sukabumi
Kumis kucing bunga putih
2.0002
1.9999
1.7779
1.7762
11.11
11.19
11.15
Kumis kucing bunga ungu
2.0003
2.0004
1.7841
1.7859
10.81
10.72
10.77
CASI 007
2.0008
2.0006
1.7429
1.7448
12.89
12.79
12.84
CASI 008
2.0001
2.0003
1.7350
1.7392
13.25
13.05
13.15
CASI 016
2.0004
2.0004
1.7506
1.7510
12.45
12.47
12.46
Sambiloto
2.0005
2.0000
1.7853
1.7867
10.76
10.67
10.72
Tempuyung
2.0008
2.0007
1.7785
1.7790
11.11
11.08
11.10
Sampel asal Bandung
Kumis kucing bunga putih
2.0005
2.0006
1.8815
1.8836
5.95
5.85
5.90
Kumis kucing bunga ungu
2.0002
2.0002
1.8457
1.8464
7.72
7.69
7.71
CASI 007
2.0009
2.0007
1.8502
1.8505
7.53
7.50
7.52
CASI 008
2.0006
2.0009
1.8712
1.8704
6.49
6.52
6.51
Tempuyung
2.0009
2.0003
1.8349
1.8333
8.30
8.35
8.33
Kadar air (%)
Lampiran 5 Aktivitas ekstrak sampel terhadap larva
A. salina
setelah 24 jam
Nilai LC
50ekstrak kumis kucing bunga putih asal Cicurug
Konsentrasi (ppm)
Jumlah larva udang yang mati
Ulangan 1
Ulangan 2
0
0
0
10
0
0
100
0
0
500
0
0
1000
1
1
Nilai LC
50ekstrak pegagan asal Bogor
Konsentrasi (ppm)
Jumlah larva udang yang mati
Ulangan 1
Ulangan 2
0
0
0
10
0
0
100
3
3
500
5
5
1000
9
9
Nilai LC
50ekstrak sambiloto asal Bogor
Konsentrasi (ppm)
Jumlah larva udang yang mati
Ulangan 1
Ulangan 2
0
0
0
10
0
0
100
0
0
500
2
2
1000
3
3
Nilai LC
50ekstrak tempuyung asal Bogor
Konsentrasi (ppm)
Jumlah larva udang yang mati
Ulangan 1
Ulangan 2
0
0
0
10
0
0
100
0
0
500
2
2
Lampiran 6 Contoh perhitungan nilai LC
50ekstrak sampel menggunakan metode
probit
Confidence Limits
Probability
95% Confidence Limits for
VAR00002
Estimate
Lower
Bound
Upper
Bound
PROBIT
.010
801.305
.
.
.020
853.283
.
.
.030
886.262
.
.
.040
911.070
.
.
.050
931.250
.
.
.060
948.426
.
.
.070
963.487
.
.
.080
976.971
.
.
.090
989.235
.
.
.100
1000.524
.
.
.150
1047.262
.
.
.200
1084.409
.
.
.250
1116.277
.
.
.300
1144.895
.
.
.350
1171.415
.
.
.400
1196.579
.
.
.450
1220.926
.
.
.500
1244.887
.
.
.550
1268.848
.
.
.600
1293.194
.
.
.650
1318.359
.
.
.700
1344.878
.
.
.750
1373.497
.
.
.800
1405.365
.
.
.850
1442.511
.
.
.900
1489.250
.
.
.910
1500.539
.
.
.920
1512.802
.
.
.930
1526.287
.
.
.940
1541.347
.
.
.950
1558.523
.
.
.960
1578.703
.
.
.970
1603.512
.
.
.980
1636.491
.
.
Lampiran 7 Kurva standar asam hipurat
Konsentrasi asam
hipurat (ppm)
Absorbans
(
= 228 nm)
0
-0.001
2
0.110
4
0.225
6
0.340
8
0.454
10
0.558
12
0.832
25
1.367
y= 0.054x+ 0.006
R²= 0.999
-0,2 0 0,2 0,4 0,6 0,8 1 1,2 1,4 1,6
0 5 10 15 20 25 30
A
b
so
rb
an
s
Lampiran 8 Hasil uji aktivitas ekstrak sampel terhadap ACE secara
in vitro
Sampel
Konsentrasi asam
hipurat (ppm)
Inhibisi
(%)
Rerata
inhibisi
(%)
Ulangan
1
Ulangan
2
Ulangan
1
Ulangan
2
Ekstrak kumis kucing
14 ppm
0.9543
1.0457
60.21
56.40
58.31
25 ppm
0.9909
1.0274
58.69
57.16
57.93
50 ppm
0.5338
0.5704
77.74
76.22
76.98
100 ppm
1.9598
2.0512
18.29
14.48
16.39
Ekstrak pegagan
14 ppm
1.3931
1.3565
41.42
43.44
42.68
25 ppm
1.2561
1.2834
47.25
46.49
46.87
50 ppm
1.1554
1.1371
51.83
52.59
52.21
100 ppm
0.9360
1.0457
60.98
56.40
58.69
Ekstrak sambiloto
14 ppm
1.3382
1.3382
44.21
44.21
44.21
25 ppm
1.3784
1.3931
42.68
41.92
42.30
50 ppm
1.3748
1.2651
42.68
47.25
44.97
100 ppm
1.0640
1.1554
55.64
51.83
53.74
Ekstrak tempuyung
14 ppm
0.8446
0.9360
64.79
60.98
62.89
25 ppm
1.9598
1.8684
18.29
22.10
20.20
50 ppm
3.0937
2.9853
-28.96
-23.63
-26.30
100 ppm
5.8720
5.6892
-144.82
-137.20
-141.01
Kaptopril
14 ppm
1.8684
1.8318
22.10
23.63
22.87
100 ppm
1.6856
1.6490
29.73
31.25
30.49
Persen inhibisi =
Lampiran 9 Hasil uji aktivitas ekstrak gabungan terhadap ACE secara
in vitro
Sampel
Konsentrasi asam
hipurat (ppm)
Inhibisi
(%)
Rerata
inhibisi (%)
Ulangan 1
Ulangan 2
Ulangan 1
Ulangan 2
K-P-S-T
4.2084
4.0622
60.32
58.21
59.27
K-P-T
2.2717
2.4351
78.58
77.04
77.81
K-S-T
2.4539
2.5265
76.87
76.18
76.53
P-S-T
7.8830
7.9561
25.68
24.99
25.34
K-P
1.7952
1.7038
58.07
60.21
59.14
K-S
1.9049
1.9049
55.51
55.51
55.51
K-T
1.1005
1.1540
74.30
73.05
73.68
P-S
1.2102
1.2468
71.73
70.87
71.30
P-T
1.1188
1.1737
73.87
72.58
73.23
S-T
5.1956
5.1042
42.84
39.33
41.08
Keterangan :
Sampel
Keterangan