APLIKASI HORMON PERTUMBUHAN REKOMBINAN
MELALUI PERENDAMAN UNTUK MEMACU PERTUMBUHAN
BENIH IKAN GURAMI (Osphronemus goramy)
ARAS SYAZILI
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis “Aplikasi Hormon Pertumbuhan Rekombinan melalui Perendaman untuk Memacu Pertumbuhan Benih Ikan Gurami (Osphronemus goramy)” adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulisan lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Juni 2012
Aras Syazili
ABSTRACT
ARAS SYAZILI. Application of Recombinant Growth Hormone for Growth
Stimulation in Giant Gourami Juvenile (Osphronemus goramy) by Immersion. Under
direction of ALIMUDDIN and KOMAR SUMANTADINATA
This study aimed to determine the immersion frequency of recombinant common carp (CcGH) and giant gourami (OgGH) growth hormone in the growth stimulation of giant gourami juvenile. A total of 50 larvae at second day after first feeding, were immersed in 30 ppt salt water for 2 minutes, then transferred into 200 mL of 9 ppt saline water containing 30 mg/L CcGH in inclusion bodies form. Immersion was performed for 60 minutes with a frequency of 2, 3, 4 and 5 times at interval 7 days. The results showed that the highest (p<0.05) average body weight of giant gourami juvenile (2.232±0.190 g) was obtained at 4 times immersion treatment. The total dosage of 4 times immersion (120 mg/L OgGH) from the first experiment was then used in the second experiment to determine whether immersion frequency could be minimized. Fish larvae were immersed once a week, twice a week, and once a week for 2 weeks. The results showed that the highest (p<0.05) biomass (5482.58±110.70 g), and survival rate (87.38±8.84%) were obtained by once immersion time. Hence, both CcGH and
OgGH could improve growth of giant gourami juvenile. The IGF-I mRNA expression level was increased significantly at 24 hours after OgGH immersion, and this suggested that IGF-I was involved in growth stimulation. Lower plasma cortisol levels in Og GH-treated fish after 180 minutes may also plays important role in growth induction. Thus, immersion of juvenile once a week in 120 mg/L OgGH solution can be applied to enhance the growth of giant gourami with a high survival rate.
RINGKASAN
ARAS SYAZILI. Aplikasi Hormon Pertumbuhan Rekombinan melalui Perendaman untuk Memacu Pertumbuhan Benih Ikan Gurami (Osphronemus goramy). Dibimbing oleh ALIMUDDIN, dan KOMAR SUMANTADINATA.
Pertumbuhan ikan gurami relatif lambat, sehingga waktu yang diperlukan untuk mencapai ukuran konsumsi adalah relatif lama (SNI 2006). Alternatif metode cepat yang dapat ditempuh untuk meningkatkan pertumbuhan ikan gurami secara signifikan adalah aplikasi hormon pertumbuhan rekombinan (HPr). Tujuan penelitian ini adalah untuk menentukan frekuensi optimum penggunaan hormon pertumbuhan rekombinan dari ikan mas dan ikan gurami dalam memacu pertumbuhan, dan tingkat kelangsungan hidup benih ikan gurami. Karena kerja hormon pertumbuhan dalam memacu pertumbuhan terkait dengan Insulin-like Growth Factor (IGF-I) dalam hati. Pada penelitian ini juga dilakukan analisis ekspresi gen IGF-I. Selain itu, perbedaan frekuensi perendaman berpotensi menyebabkan perbedaan tingkat stres ikan gurami. Oleh karena itu, pada penelitian ini dilakukan pengukuran kadar kortisol plasma tubuh untuk menganalisis tingkat stres ikan yang diberi hormon pertumbuhan rekombinan dengan frekuensi berbeda. Hasilnya diharapkan dapat memberi kontribusi terhadap peningkatan produksi budidaya ikan gurami.
Produksi HPr dilakukan menggunakan bakteri Escherichia coli BL21 yang mengandung plasmid pCold-HPim untuk ikan mas, dan pCold-HPig untuk ikan gurami. Bakteri dikultur pada media 2xYT pada suhu inkubasi 15o
Percobaan dibagi menjadi 2 tahap. Percobaan satu menggunakan 50 ekor larva ikan gurami umur 2 hari setelah mulai makan, direndam dalam air bersalinitas 30 ppt selama 2 menit, dan dilanjutkan dalam 200 mL air bersalinitas 9 ppt yang mengandung 30 mg/L HPr dari ikan mas. Perendaman HPr dilakukan selama 60 menit, dan diulang seminggu sekali dengan frekuensi 2, 3, 4, dan 5 kali. Sebagai kontrol, ikan direndam dengan protein badan inklusi tanpa HPr (kontrol-1), albumin serum sapi (kontrol-2), air bersalinitas 9 ppt tanpa protein (kontrol-3), dan dalam air tawar (kontrol-4). Ikan dipelihara dalam akuarium volume 7 liter selama 4 minggu pertama, dalam akuarium volume 50 liter selama 2 minggu kedua, dan di hapa berukuran 2x1x1 m selama 2 minggu terakhir. Percobaan kedua dilakukan dengan menggunakan 800 ekor larva ikan gurami yang direndam dengan HPr ikan gurami. Total dosis percobaan pertama (frekuensi perendaman 4 kali) digabung menjadi 1 kali (dosis 120 mg/L), dan 2 kali perendaman (@60 mg/L).
Hasil percobaan pertama menunjukkan bahwa rerata bobot juvenil ikan gurami tertinggi (p<0,05) diperoleh pada perlakuan perendaman 4 kali (2,232 ± 0,190 g). Rerata bobot ikan yang direndam 2 kali (1,719±0,289 g), 3 kali (1,682±0,338 g), dan 5 kali (1,808±0,169 g) adalah sama. Bobot ikan pada semua kontrol adalah sama, dan lebih rendah daripada ikan perlakuan HPr ikan mas. Kelangsungan hidup ikan yang direndam 4 kali (96,67±1,15%), dan 5 kali (95,33±4,16%) relatif sama, serta lebih tinggi dibandingkan perlakuan lainnya, dan kontrol (77,33 s.d 89,33%). Hasil percobaan dua menunjukkan bahwa rerata bobot benih ikan gurami tertinggi (p<0,05) diperoleh pada perendaman HPr dari ikan gurami 1 kali (5482,58±110,70 g), selanjutnya perendaman HPr 2 kali @60 mg/L interval 3 hari (4480,95±858,82 g), perendaman HPr dari ikan gurami 2 kali @60 mg/L interval 7 hari (4569,28±242,87 g), kontrol-1 (3488,75±155,38 g), dan kontrol-2 (3488,75±155,38 g). Hal ini menunjukkan bahwa HPr dari ikan gurami dapat diberikan 1 kali, dengan efek pertumbuhan yang tinggi. Kelangsungan hidup ikan hasil perendaman 1 kali (87,38±8,84%) tidak berbeda (p>0,05) dengan perlakuan perendaman lainnya, tetapi lebih tinggi (p<0,05) daripada kontrol-2 (64,00±7,25%).
Perendaman 1 kali dengan HPr ikan gurami (120 mg/L) mampu menginduksi ekspresi gen IGF-I lebih tinggi (p<0,05) pada benih ikan gurami dibandingkan dengan perlakuan lainnya. Kadar hormon kortisol pada benih ikan gurami setelah diberi kejutan salinitas 30 ppt (9,04 ng/mL) meningkat 190,23% dibandingkan dengan sebelum diberi kejutan salinitas (3,12 ng/mL). Perendaman hormon pertumbuhan rekombinan dari ikan gurami 1 kali meningkatkan hormon kortisol hingga mencapai 20,72 ng/mL sesaat setelah perendaman, namun lebih cepat turun, lebih rendah daripada perlakuan lainnya, dan cenderung stabil sampai akhir pengamatan. Kondisi ini diduga berperan dalam mendukung pertumbuhan, dan tingkat kelangsungan hidup yang tinggi pada benih ikan gurami.
Sebagai kesimpulan, perendaman 1 kali dengan dosis 120 mg/L optimum memacu pertumbuhan dan kelangsungan hidup benih ikan gurami. Hormon pertumbuhan rekombinan ikan mas dan ikan gurami memiliki biokativitas relatif sama pada juvenil ikan gurami. Pemberian hormon pertumbuhan rekombinan berpengaruh terhadap pertumbuhan somatik dan diduga melibatkan IGF-I. Pertumbuhan dan kelangsungan hidup yang tinggi pada ikan yang diberi perlakuan hormon pertumbuhan rekombinan ikan gurami terkait penurunan kadar kortisol yang cepat, dan tetap rendah. Kata kunci: rekombinan, hormon pertumbuhan, perendaman, IGF-I, kortisol, ikan
© Hak Cipta milik IPB, tahun 2012
Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah: dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
APLIKASI HORMON PERTUMBUHAN REKOMBINAN
MELALUI PERENDAMAN UNTUK MEMACU PERTUMBUHAN
BENIH IKAN GURAMI (Osphronemus goramy)
ARAS SYAZILI
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Akuakultur
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul : Aplikasi Hormon Pertumbuhan Rekombinan melalui Perendaman untuk Memacu Pertumbuhan Benih Ikan Gurami (Osphronemus goramy) Nama : Aras Syazili
NIM : C151090091
Disetujui Komisi Pembimbing
Dr. Alimuddin, S.Pi, M.Sc
Ketua Anggota
Prof. Dr. Ir. Komar Sumantadinata, M.Sc
Diketahui
Ketua Program Studi Dekan Sekolah Pascasarjana Ilmu Akuakultur
Prof. Dr. Ir. Enang Harris, M.S Dr. Ir. Dahrul Syah, M.Sc.Agr
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tesis “Aplikasi Hormon Pertumbuhan Rekombinan melalui Perendaman pada Benih Ikan Gurami (Osphronemus goramy)” dilaksanakan di Laboratorium Reproduksi dan Genetika Organisme Akuatik Departemen Budidaya Perairan, FPIK, IPB. Penelitian dilaksanakan pada bulan Januari 2011 hingga Desember 2011.
Penulis mengucapkan terima kasih penulis ucapkan kepada Dr. Alimuddin, S.Pi, M.Sc dan Prof. Dr. Ir. Komar Sumantadinata, M.Sc selaku dosen pembimbing, dan Dr. Ir Muhammad Agus Suprayudi, M.Si, selaku dosen penguji luar komisi pada ujian tesis. Irmawati, S.Pi, M.Si, Anna Octavera, S.Pi, M.Si dan rekan-rekan di Laboratorium Reproduksi dan Genetika Organisme Akuatik, serta rekan-rekan mahasiswa Ilmu Akuakultur IPB 2009. Ungkapan terima kasih juga penulis sampaikan kepada kedua orang tua dan saudara penulis atas segala dukungan, doa, dan kasih sayangnya, serta untuk istri saya Nurmawati dan anak kami Naufal Biruni Nawawi atas perhatian dan pengertiannya selama ini.
Semoga karya ini dapat bermanfaat bagi penulis maupun semua pihak yang membutuhkan.
Bogor, Juni 2012
RIWAYAT HIDUP
Penulis dilahirkan di Bua, Kabupaten Luwu, Sulawesi Selatan pada tanggal 31 Januari 1977 dari ayah Nawawi BA (Alm.) dan Ibu Hj. Asma. Penulis merupakan anak ke lima dari enam bersaudara. Tahun 1997 lulus seleksi masuk Universitas Hasanuddin pada Program Studi Budidaya Perairan, dan lulus pada tahun 2002. Pada Tahun 2006 penulis diterima sebagai dosen di Universitas Khairun Ternate Maluku Utara, dan melanjutkan pendidikan S2 pada Program Studi Ilmu Akuakultur IPB tahun 2009. Penulis menerima Beasiswa Pendidikan Pascasarjana (BPPS) Direktorat Pendidikan Tinggi Departemen Pendidikan Nasional. Sebagai bagian dari tesis ini, telah dibuat artikel ilmiah dengan judul: “Kinerja pertumbuhan dan kelangsungan hidup juvenil ikan gurami direndam hormon pertumbuhan rekombinan dengan frekuensi berbeda”
dan sudah diterima untuk diterbitkan dalam Jurnal Akuakultur Indonesia
DAFTAR ISI
2.4 Metode Penggunaan Hormon Pertumbuhan Rekombinan (HPr) 6 2.5 Hormon Insulin-like Growth Factor-I (IGF-I) ... 7
2.6 Hormon Kortisol ... 8
III BAHAN DAN METODE ... 10
3.1 Produksi Hormon Pertumbuhan rekombinan... 10
3.2 Percobaan Pertama . ... 11
4.1 Ekspresi dan Analisis Hormon Pertumbuhan Rekombinan ... 16
4.2 Percobaan Pertama ... 17
4.3 Percobaan Kedua ... 21
4.4 Ekspresi Gen Insulin-like Growth Factor-I (IGF-I) ... 23
4.5 Kadar Hormon Kortisol ... 25
V. SIMPULAN DAN SARAN ... 31
5.1 Simpulan ... 31
5.2 Saran ... 31
DAFTAR PUSTAKA ... 32
DAFTAR TABEL
Halaman
1 Rancangan percobaan pertama ... 11 2 Rancangan percobaan kedua ... 12 3 Rerata bobot akhir dan kelangsungan hidup juvenil ikan gurami
DAFTAR GAMBAR
Halaman
1 Analisis SDS-PAGE protein HPr; M = marker, 1 = protein dari bakteri Escherichia coli BL21 yang membawa plasmid C-mOgGH; 2 = protein dari bakteri Escherichia coli BL21 yang membawa plasmid C-mCcGH, tanda panah menunjukkan protein HPr; angka di sebelah kiri menunjukkan ukuran marker (M). ... 16 2 Pertumbuhan bobot rerata (g) juvenil ikan gurami yang dipelihara
di akuarium volume 7 liter selama 4 minggu pertama dan dilanjutkan di akuarium volume 50 liter selama 2 minggu kedua. Perendaman ikan dalam air mengandung hormon pertumbuhan rekombinan dari ikan mas dilakukan seminggu sekali selama 2 minggu (perendaman HPr 2 minggu), 3 minggu (perendaman HPr 3 kali), 4 minggu (perendaman HPr 4 kali), dan 5 minggu (perendaman HPr 5 kali). Ikan kontrol direndam dalam air yang mengandung protein badan inklusi tanpa HPr (kontrol-1), albumin serum sapi 2), media salinitas 9 ppt tanpa protein
(kontrol-3), dan air tawar tanpa protein (kontrol-4) ... 19 3 Pertumbuhan bobot biomassa (g) juvenil ikan gurami yang
dipelihara di akuarium volume 250 liter selama 4 minggu pertama dan dilanjutkan kolam dengan luas hapa 3x2x1m. Angka 1, 2, 3, 4, 5 menunjukkan perlakuan. 1 = Perendaman albumim serum sapi (kontrol-1), 2 = Perendaman hormon pertumbuhan rekombinan dari
ikan gurami 4 kali @ 30 mg/L (kontrol-2; interval 7 hari), 3 = Perendaman hormon pertumbuhan rekombinan dari ikan
gurami 2 kali @ 60 mg/L (interval 7 hari), 4 = Perendaman hormon pertumbuhan rekombinan dari ikan gurami 2 kali @ 60 mg/L (interval 3 hari), 5 = Perendaman hormon pertumbuhan
rekombinan dari ikan gurami 1 kali (120 mg/L) ... 21 4 Kelangsungan hidup ikan gurami pada akhir percobaan. Angka 1,
2, 3,4,5 menunjukkan perlakuan. 1 = Perendaman albumim serum sapi (kontrol-1), 2 = Perendaman HPr dari ikan gurami 4 kali @ 30 mg/L (kontrol-2; interval 7 hari), 3 = Perendaman HPr dari ikan gurami 2 kali @ 60 mg/L (interval 7 hari), 4 = Perendaman HPr
5 Ekspresi gen IGF-I (A), dan gen β-aktin (B) yang diamati 24 jam setelah perendaman hormon pertumbuhan rekombinan (HPr) dari ikan gurami. M = marker DNA. Angka 1, 2, 3, 4, 5, 6, dan 7, menunjukkan perlakuan. 1 = Perendaman HPr 1 kali (120 mg/L), 2 = Perendaman HPr 2 kali (@ 60 mg/L, 3 = Perendaman 4 kali @ 30 mg/L (kontrol-2; Interval 7 hari), 4 = Perendaman dengan albumin serum sapi (kontrol-1), 5 = kontrol sebelum kejutan salinitas, 6 = kontrol setelah kejutan salinitas,7 = sampel hasil PCR tanpa DNA cetakan ... 23 6 Level ekspresi gen IGF-I pada larva ikan gurami, 24 jam setelah
perendaman hormon pertumbuhan rekombinan. Data telah dinormalkan dengan menggunakan gen β-aktin. Angka 1, 2, 3, 4, 5 dan 6 menunjukkan perlakuan 1 = kontrol sebelum kejutan salinitas, 2 = kontrol setelah kejutan salinitas 3 = Perendaman dengan albumin serum sapi (kontrol-1), 4 = Perendaman HPr 4 kali @ 30 mg/L (kontrol-2; interval 7 hari), 5 = Perendaman HPr 2 kali (@ 60 mg/L), 6 = Perendaman HPr 1 kali (120 mg/L) ... 24 7 Perubahan kadar hormon kortisol benih ikan gurami setelah
direndam HPr dari ikan gurami. (■) Perendaman HPr 1 kali, (x) Perendaman HPr 2 kali, (▲) Perendaman HPr 4 kali
(kontrol-2), ( • ) Perendaman albumin serum sapi (kontrol-1). ... 26
DAFTAR LAMPIRAN
Halaman
1 Data pertambahan bobot, dan kelangsungan hidup ikan guramiselama percobaan pertama ... 40 2 Hasil analisis sidik ragam (ANOVA) dan uji lanjut Duncan
pertumbuhan ikan gurami percobaan pertama ... 42 3 Hasil analisis sidik ragam (ANOVA) dan uji lanjut Duncan
kelangsungan hidup (SR) ikan gurami percobaan pertama ... 44 4 Data bobot ikan gurami penelitian dua berdasarkan ukuran pada
akhir percobaan kedua ... 46 5 Kelangsungan hidup ikan gurami selama percobaan kedua ... 47 6 Hasil analisis sidik ragam (ANOVA) dan uji lanjut Duncan
pertumbuhan ikan gurami percobaan kedua ... 48 7 Hasil analisis sidik ragam (ANOVA) dan uji lanjut Duncan
kelangsungan hidup ikan gurami percobaan kedua ... 50 8 Data pengukuran ketebalan pita hasil elektroforesis gen IGF-I dan
gen β-aktin ikan gurami menggunakan program UN-SCAN-IT gel 6.1 ... 52 9 Data pengukuran hormon kortisol benih ikan gurami yang diberi
perlakuan perendaman hormon pertumbuhan rekombinan ... 54
I. PENDAHULUAN
1.1 Latar Belakang
Ikan gurami (Osphronemus goramy) merupakan salah satu jenis ikan
budidaya yang termasuk dalam 10 jenis yang menjadi target peningkatan produksi
perikanan budidaya 353% pada tahun 2009-2014 yang dicanangkan oleh
Kementerian Kelautan dan Perikanan RI. Pertumbuhan ikan gurami relatif lambat,
sehingga waktu yang diperlukan untuk mencapai ukuran konsumsi adalah relatif
lama (SNI 2006). Performa pertumbuhan yang relatif lambat ini merupakan salah
satu masalah utama pengembangan budidaya ikan gurami, yang diduga sebagai
konsekuensi langsung dari laju pertumbuhan somatik yang rendah.
Berbagai metode dapat dilakukan untuk meningkatkan pertumbuhan ikan
budidaya; seperti seleksi, hibridisasi, triploidisasi dan transgenesis. Namun
upaya-upaya tersebut terhalang dengan waktu yang relatif lama untuk
mendapatkan perbaikan kualitas yang memadai. Penggunaan metode seleksi
membutuhkan waktu sekitar 10 tahun untuk menghasilkan 12 generasi dengan
kecepatan tumbuh 12,4% per generasi pada ikan nila (Bolivar dan Newkirk
2002). Aplikasi teknologi transgenesis menghasilkan laju pertumbuhan 30 kali
lebih cepat (Nam et al. 2001). Namun demikian, teknologi transgenesis masih
menimbulkan kontroversi terhadap keamanan pangan organisme hasil
transgenesis atau disebut dengan GMO (genetically modified organism).
Penerapan teknologi hibridisasi dan triploidisasi dapat dilakukan pada ikan yang
sudah diketahui teknik pemijahan buatannya.
Alternatif metode cepat yang dapat ditempuh untuk meningkatkan
pertumbuhan ikan gurami adalah aplikasi hormon pertumbuhan rekombinan
(HPr). Pemberian HPr ikan nila pada benih ikan nila mampu meningkatkan
pertumbuhan lebih dari 50% (Acosta et al. 2007). Alimuddin et al. (2010)
melaporkan bahwa terjadi peningkatan bobot ikan nila hingga 20,94% dengan
pemberian HPr ikan kerapu kertang. Aplikasi HPr ikan giant catfish
(Pangasianodon gigas) terhadap ikan mas koki mengalami peningkatan
2 Penggunaan HPr dapat juga meningkatkan kelangsungan hidup hingga
80-85% pada mysis (Arenal et al. 2008), dan meningkatkan sistem kekebalan
terhadap penyakit (McCormick 2001). Selanjutnya, ikan yang diberi HPr tidak
termasuk GMO (Acosta et al. 2007). Selain itu, penggunaan hormon pertumbuhan
lebih mudah diaplikasikan, karena dapat digunakan dengan metode perendaman
(Putra 2011; Tsai et al. 1997), penyuntikan (McLean et al. 1997; Silverstein et al.
2000; Leedom et al. 2002), dan pakan (Moriyama et al. 1993), serta waktu yang
dibutukan relatif lebih singkat, dan biaya yang dikeluarkan lebih murah jika
dibandingkan dengan metode lainnya.
Pemberian HPr melalui perendaman dengan frekuensi berbeda pada
spesies ikan berbeda. Moriyama dan Kawauchi (1990) telah melakukan
perendaman HPr sebanyak 9 kali untuk memacu pertumbuhan juvenil ikan
salmon. Santiesteban et al. (2010) merendam larva udang vaname 7 kali dalam
larutan HPr 100 µg/L. Putra (2011) menyatakan benih ikan gurami mengalami
peningkatan pertumbuhan setelah direndam 3 kali dalam larutan HPr 30 mg/L.
Perendaman HPr 3 kali semingu selama 6 minggu meningkatkan bobot tubuh
larva ikan mas koki (Acosta et al. 2009). Perendaman dengan frekuensi berbeda
dilakukan untuk mencari respons optimum ikan terhadap pertumbuhan dan
kelangsungan hidup, dan tingkat stres ikan yang rendah. Selanjutnya, frekuensi
perendaman yang minimum menggunakan total dosis HPr dari frekuensi
perendaman berbeda diduga merupakan alternatif terbaik.
Mekanisme kerja hormon pertumbuhan dapat bersifat langsung ke organ
target, dan bersifat tidak langsung dengan melibatkan insulin-like growth factor
(IGF-I) dalam hati (Bjornsson et al. 2004). Hormon pertumbuhan berfungsi pada
proses pertumbuhan, metabolisme (Castillo et al. 2004), perkembangan (Pozios et
al. 2001), reproduksi (Weber dan Sullivan 2000), dan osmoregulasi (McCormick
2001). Penyuntikan hormon pertumbuhan pada ikan salmon coho dapat
meningkatkan mRNA IGF-I hati secara signifikan (Sakamoto et al. 1995). Pada
penelitian ini, HPr diberikan dengan frekuensi berbeda, dan hal ini diduga
mempengaruhi tingkat ekspresi IGF-I.
Kandungan hormon kortisol dalam darah yang tinggi merupakan indikator
3 dan Pankhrust 2000), aklimatisasi (Lankford et al. 2003), dan status nutrisi
(Pottinger et al. 2003) merupakan pemicu meningkatnya kadar kortisol darah.
Stres dapat mengakibatkan pertumbuhan lambat, mudah terkena penyakit,
kematian (Wendelaar-Bonga 1997), dan gangguan keseimbangan cairan tubuh
ikan (Lowe dan Davison 2005). Oleh karena itu, pada penelitian ini dilakukan
analisis kadar hormon kortisol ikan yang diberi perlakuan HPr dengan frekuensi
berbeda, untuk mengetahui pengaruh perlakuan frekuensi perendaman terhadap
benih ikan gurami.
1.2 Tujuan Penelitian
Tujuan penelitian ini adalah untuk menentukan frekuensi optimum
penggunaan hormon pertumbuhan rekombinan dari ikan mas dan ikan gurami
dalam memacu pertumbuhan, dan tingkat kelangsungan hidup benih ikan gurami.
Karena kerja hormon pertumbuhan dalam memacu pertumbuhan terkait dengan
insulin-like growth factor (IGF-I) dalam hati. Pada penelitian ini juga dilakukan
analisis ekspresi gen IGF-I. Selain itu, perbedaan frekuensi perendaman
berpotensi menyebabkan perbedaan tingkat stres ikan gurami. Oleh karena itu,
pada penelitian ini dilakukan pengukuran kadar kortisol plasma tubuh untuk
menganalisis tingkat stres ikan yang diberi hormon pertumbuhan rekombinan
dengan frekuensi berbeda.
1.3 Manfaat Penelitian
Penelitian ini diharapkan dapat memberi kontribusi terhadap peningkatan
produksi budidaya ikan gurami. Selanjutnya, peningkatan produksi budidaya
ikan gurami diharapkan dapat meningkatkan pendapatan pembudidaya.
II. TINJAUAN PUSTAKA
2.1 Pertumbuhan Ikan Gurami
Pertumbuhan didefinisikan sebagai perubahan ukuran, dimana variabel
yang mengalami perubahan dapat berupa panjang dan dimensi fisik lainnya,
termasuk volume, berat atau massa, baik pada keseluhan tubuh organisme atau
pada berbagai jaringan. Perubahan ini juga dapat berkaitan dengan kandungan
protein, lemak atau komponen kimia lainnya dari keseluruhan tubuh, perubahan
kandungan kalori (energi) dari seluruh tubuh atau dari komponen jaringannya
(Weatherley dan Gill 1987).
Ikan membutuhkan energi untuk pertumbuhan yang diperoleh dari pakan.
Komponen pakan yang berkontribusi terhadap penyediaan energi untuk tumbuh
adalah protein, karbohidrat dan lemak. Protein adalah nutrien yang sangat
dibutuhkan untuk perbaikan jaringan tubuh yang rusak, pemeliharaan protein
tubuh, penambahan protein untuk pertumbuhan dan sebagai sumber energi.
Kebutuhan protein ikan dipengaruhi oleh berbagai faktor, seperti ukuran ikan,
suhu air, kadar pemberian pakan, kandungan energi dari pakan yang dicerna dan
kualitas protein. Kualitas protein bergantung pada kecernaan dan nilai biolologis
yang dilihat dari jumlah dan kualitas asam aminonya (Furuichi 1988).
Energi metabolisme dan pertumbuhan pada ikan secara langsung di
kontrol oleh sistem endokrin yang kompleks atau secara tidak langsung
dipengaruhi oleh beberapa hormon. Hormon pertumbuhan (HP), Insulin-like
Growth Factor (IGF-I) dan insulin merupakan hormon yang sangat penting untuk
metabolisme dan percepatan pertumbuhan. Beberapa aksi hormon pertumbuhan
bersifat tidak langsung dan dimediasi oleh IGF-I yang diproduksi di hati serta
organ lainnya (Bjornsson et al. 2002).
2.2 Hormon Pertumbuhan
Hormon pertumbuhan merupakan polipeptida yang disekresikan oleh
bagian anterior dari kelenjar pituitari yang memacu pertumbuhan tubuh,
khususnya dengan merangsang pelepasan somatomedin, dan mempengaruhi
5 yang besar yang terdiri dari 191 asam amino dan relatif spesies-spesifik. Sekresi
hormon pertumbuhan dikendalikan di hypothalamus oleh growth hormone
releasing hormone (GHRH), ghrelin, protein pakan, kandungan gula darah yang
rendah, peningkatan sekresi androgen, dan arginin, sedangkan yang menghambat
antara lain somatostatin, konsentrasi hormon pertumbuhan dan insulin-like growth
factor-I (IGF-I) yang bersirkulasi, kandungan gula darah yang tinggi,
glukokortikoid, dan estradiol ataupun estrogen lainnya. Kandungan HP dalam
tubuh ikan berkisar antara 0,2-111,2 ng/ml plasma darah (Bjornsson et al. 1998 ).
HP memiliki berbagai fungsi yang berbeda pada proses fisiologis dalam
tubuh ikan seperti pengaturan ion dan lemak, protein, keseimbangan osmotik, dan
metabolisme karbohidrat, pertumbuhan jaringan keras dan jaringan lunak,
reproduksi dan fungsi kekebalan tubuh. Fungsi biologis HP tidak terbatas pada
peningkatan pertumbuhan, tetapi juga dapat mobilisasi energi, pengembangan
gonad, peningkatan nafsu makan, dan aspek tingkah laku. Penelitian menunjukkan
bahwa HP mempengaruhi beberapa aspek perilaku, termasuk merangsang nafsu
makan, perilaku mencari makan, agresi, dan menghindari pemangsa
(Perez-Sanchez 2000). Sebagian besar peneliti mengklaim bahwa aksi homon
pertumbuhan bersifat tidak langsung, namun berkoordinasi dengan hormon lain
seperti IGF-I untuk melakukan berbagai aksi fisiologi (Bjornsson et al. 2004)
Beberapa pengaruh hormon pertumbuhan dalam tubuh antara lain
meningkatkan retensi kalsium, meningkatkan massa otot, merangsang lipolisis,
meningkatkan sintesis protein, merangsang pertumbuhan dari seluruh organ
internal kecuali otak, berperan dalam pemenuhan homeostasis, mengurangi
pengambilan glukosa oleh hati, merangsang glukoneogenesis dalam hati,
berkontribusi dalam pemeliharaan fungsi islet pankreas, dan merangsang sistem
imun (Yada et al. 2005)
2.3 Hormon Pertumbuhan Rekombinan
Penggunaan protein hormon pertumbuhan rekombinan (HPr) ikan diduga
sebagai salah satu metode alternatif untuk meningkatkan pertumbuhan ikan
budidaya. Penggunaan protein HPr ikan dalam meningkatkan produktivitas atau
6 yang diberi HPr bukan merupakan organisme GMO (Acosta et al. 2007) dan HPr
tersebut tidak ditransmisikan ke keturunannya. Pada ikan teleostei secera khusus
telah banyak pustaka yang menyatakan dampak hormon pertumbuhan rekombinan
dapat mempercepat pertumbuhan (McLean et al. 1997). Bioaktivitas protein HPr
dalam meningkatkan pertumbuhan telah dilaporkan pada beberapa jenis ikan
seperti ikan rainbow trout (Onchorhynchus mykiss) dengan menggunakan HPr
ikan salmon (Moriyama et al. 1993), ikan mas dengan menggunakan HPr ikan
giant catfish (Pangasianodon gigas) (Promdonkoy et al. 2004), dan ikan flounder
(Paralichtys olivaceus) dengan menggunakan HPr juga dari ikan flounder (Jeh et
al. 1998).
Pemberian 0,5% HPr dalam pakan selama 12 minggu pada juvenil ikan
sea bream hitam menunjukkan perbedaan bobot sebesar 41,67% dengan ikan
kontrol setelah pemeliharaan selama 18 minggu (Tsai et al. 1997). Menurut Flik
et al. (1993), pemberian HPr pada ikan mujair dapat meningkatkan pertumbuhan
sebesar 44,9% dibandingkan dengan ikan mujair yang tidak diberi perlakuan HPr,
sedangkan pada benih ikan baronang, pemberian HPr sebesar 0,5 μg/g bobot
tubuh sebanyak 1 kali per minggu selama 4 minggu dapat meningkatkan bobot
tubuh sebesar 20% dari kontrol (Funkenstein et al. 2005).
Lesmana (2010) melaporkan bahwa pemberian HPr yang berbeda pada
ikan nila melalui teknik penyuntikan atau injeksi dengan meningkatkan bobot
20,94% (HPr ikan kerapu kertang), 18,09% (HPr ikan mas), dan 16,99% (HPr
ikan gurami). Pemberian melalui penyuntikan dapat dikatakan kurang aplikatif
dan memperlihatkan respons yang lambat, hal ini diduga terjadi karena reseptor
memerlukan faktor intermediat atau waktu untuk mengenali HPr yang
diinjeksikan. Berbeda dengan penelitian Utomo (2010) bahwa penyuntikan HPr
ikan mas pada ikan mas meningkatkan pertumbuhan sebesar 106,56% bila
dibandingkan dengan ikan mas yang tidak diinjeksi.
2.4 Metode Penggunaan Hormon Pertumbuhan Rekombinan (HPr)
Aplikasi HPr dapat dilakukan melalui metode injeksi, perendaman dan
melalui pakan. Pemberian HPr melalui penyuntikan telah berhasil dilakukan pada
7 (Ictalurus punctatus) (Silverstein et al. 2000), dan ikan mujair (Oreochromis
mossambicus) (Leedom et al. 2002). Metode Perendaman HPr pada ikan gurami
dapat meningkatkan pertumbuhan hingga 75,04% (Putra 2011). Pemberian HPr
melalui pakan telah dilakukan oleh Moriyama et al. (1993) pada ikan rainbow
trout.
Metode perendaman telah diteliti untuk mengetahui peningkatan
pertumbuhan juvenil ikan salmon (Moriyama dan Kawauchi 1990). Morse (1984)
menyatakan bahwa hormon pertumbuhan sapi dapat mempercepat pertumbuhan
pascalarva abalon (Haliotis rufescens) melalui perendaman. Demikian pula pada
eastern oyster (Virginica crassostrea) HPr rainbow trout dapat meningkatkan
pertambahan bobot larva pada dosis 107 dan 108
Teknik penyuntikan dirasa kurang aplikatif karena ikan harus diinjeksi
satu per satu. Oleh karena itu, dibutuhkan metode yang lebih efisien dan efektif
dalam penerapan pemberian HPr, sehingga diharapkan dapat meningkatkan
efektivitas penyerapan HPr untuk meningkatkan laju pertumbuhan ikan.
Sementara pemberian HPr melalui oral masih menjadi perdebatan karena ada
kemungkinan HPr yang diberikan akan dicerna sebagai protein sebelum mencapai
organ target.
M selama 5 jam dengan interval
7 hari dengan metode perendaman (Paynter dan Chen 1991). Acosta et al. (2009)
menyatakan bahwa pemberian HP ikan nila dengan metode perendaman pada
larva ikan mas koki dapat meningkatkan bobot tubuh hingga 3,5 kali
dibandingkan kontrol.
2.5 Hormon Insulin-like growth factor-I (IGF-I)
Insulin-like growth factor-I (IGF-I) merupakan famili polipeptida dengan
berat molekul 7 kDa dan dikenal dengan nama lain somatomedin C. Hormon
pertumbuhan merangsang produksi IGF-I di hati (Bjornsson et al. 2004) yang
berperan penting dalam mengatur beberapa proses fisiologi seperti pertumbuhan,
metabolisme, perkembangan (Pozios et al. 2001), reproduksi (Weber dan
Sullivan, 2000), dan osmoregulasi (McCormick 2001). Seperti halnya pada
8 jaringan lain menghasilkan IGF-I secara lokal (Duan 1997). Reseptor IGF-I pada
ikan banyak terdapat di ovari, hati, otak, dan otot (Parrizas et al. 1995).
Penyuntikan hormon pertumbuhan terhadap ikan salmon coho dapat
meningkatkan mRNA IGF-I hati secara signifikan (Sakamoto et al. 1995).
Pemberian hormon pertumbuhan secara eksogen baik yang homolog dan
heterolog dapat menyebabkan peningkatan mRNA IGF-I di hati ikan sidat Jepang
(Anguilla japonica) (Duan et al. 1993), ikan salmon (Oncorhynchus kisutch)
(Duguay et al. 1994), dan ikan mas (Cyprinus carpio) (Vong et al. 2003). Pedroso
et al. (2009) menyatakan bahwa pemberian HPr dosis tinggi pada ikan ekor
kuning (Seriola quinqueradiata) meningkatkan mRNA IGF-I secara signifikan
setelah 24 jam.
2.6 Hormon Kortisol
Kortisol adalah glukokortikoid yang disekresikan oleh jaringan interrenal,
yang terletak pada ginjal ikan bagian atas (Iwama et al. 1999). Ketika dalam
kondisi stres, ikan menanggapi secara langsung, dan tidak langsung. Secara
langsung ikan melepaskan hormon kortisol melalui aktivasi sumbu
hipotalamus-hipofisis-interrenal (HPI) yang melepaskan corticotropin-releasing factor (CRF)
ke dalam sirkulasi darah. Polipeptida ini kemudian merangsang sekresi
adrenocorticotrophic hormone (ACTH) dari kelenjar anterior hipofisis yang
mengaktifkan pelepasan kortisol oleh jaringan interrenal (Mommsen et al. 1999).
Respons tidak langsung terjadi karena akibat pelepasan hormon stres yang
menyebabkan perubahan kimia darah, dan jaringan, serta peningkatan plasma
glukosa yang membutuhkan energi yang besar untuk menghadapi situasi kritis.
Stres adalah kondisi fisiologis internal yang disebabkan oleh kondisi
eksternal. Stres juga dapat digambarkan sebagai respon hormonal internal dari
organisme hidup yang disebabkan oleh lingkungan atau faktor eksternal lainnya
yang menyebabkan kondisi fisiologis organisme dalam keadaan yang tidak
normal. Stres dapat mengganggu keseimbangan fisiologis ikan atau homeostasis
dengan mempercepat aliran energi dalam sistem. Kandungan kortisol dalam darah
9 Stres mempengaruhi ikan dalam dua cara, yaitu menghasilkan efek yang
mengganggu keseimbangan homeostatis, dan menginduksi respons perilaku serta
fisiologis adaptif. Seiring dengan pelepasan hormon stres, dan perubahan
fisiologis dan kimia, lalu diikuti dengan modifikasi perilaku. Perubahan ini pada
dasarnya adaptif dan berfungsi untuk meningkatkan kelangsungan hidup ketika
terancam dari situasi berbahaya. Kondisi plasma kimia dalam tubuh ikan dapat
digunakan untuk mengetahui kondisi kesehatan atau stres pada ikan, karena stres
III. BAHAN DAN METODE
3.1 Produksi Hormon Pertumbuhan Rekombinan
Produksi hormon pertumbuhan rekombinan dilakukan sesuai dengan
metode Alimuddin et al. (2010). Satu koloni bakteri Escherichia coli dipilih dari
media 2xYT padat untuk diinokulasi ke dalam 5 mL media LB yang mengandung
1% ampisilin dan ditumbuhkan semalam pada suhu 37oC sambil dikocok lembut
menggunakan shaker. Selanjutnya, sebanyak 5 µL kultur ini disubkultur di dalam
5 mL media LB yang mengandung 100 µL ampisilin pada suhu media 37oC
sambil dikocok lembut dengan shaker. Setelah dua jam kultur E. coli diberi cold
shock pada suhu 15oC selama 30 menit. Ekspresi rekombinan HPr kemudian
diinduksi pada kondisi OD600 dengan isopropyl-b-D-thiogalac-topyranoside
(IPTG) dengan dosis 800 µL dan selanjutnya ditumbuhkan pada suhu 15oC
selama 24 jam. Sel bakteri kemudian dipanen dengan sentrifugasi pada 4000 rpm
selama 5 menit, kemudian disimpan pada suhu -80o
Lisis dinding sel bakteri dilakukan secara kimiawi dengan menggunakan
lisozim. Pelet bakteri hasil sentifugasi dicuci menggunakan 1 mL TE buffer
per 200 mg bakteri dan diinkubasi pada suhu 37
C hingga akan digunakan.
Proses selanjutnya dilakukan lisis dinding sel bakteri dan analisis protein HPr
menggunakan teknik SDS-PAGE.
o
C selama 20 menit, disentrifugasi
pada 12.000 rpm (4oC) selama 1 menit dan kemudian supernatant dalam tabung
mikro dibuang. Pelet bakteri sebanyak 200 mg dalam tabung mikro ditambahkan
500 µL larutan lisozim ( 10 mg dalam 1 mL buffer TE), diinkubasi pada suhu
37oC selama 20 menit lalu disentrifugasi pada 12.000 rpm selama 1 menit.
Supernatan dibuang, dan pelet yang terbentuk merupakan protein HPr dalam
bentuk badan inklusi (inclusion body). Pelet HPr dicuci dengan PBS sebanyak 1
kali dan disimpan pada suhu -800
Analisis protein HPr dilakukan menggunakan teknik SDS-PAGE
berdasarkan metode Blackshear (1984) dalam Bollag et al. (1996). Gel yang
dibuat dalam SDS-PAGE terdapat 2 lapisan gel dalam proses SDS-PAGE yaitu
running gel dan stacking gel (12%) mengandung 4,62 mL H C hingga digunakan.
2O; 5,60 ml
11 µL APS 10%; dan 5,6 µL TEMED, stacking gel (5%) mengandung 3,4 mL H2O;
0,83 mL acrilamide/Bis 29:1; 0,63 ml gel buffer 1,5 M (pH 6,8); 50 µl SDS 10%;
50 µL APS 10% dan 50 µL TEMED. Protein HPr sebanyak 1 mg ditambahkan
10 µL PBS dan 10 µL loading buffer, kemudian diinkubasi pada suhu 1000C
selama 10 menit. Loading buffer mengandung 1,5 M tris-HCl (pH 6,8), 2 M
Dithiothreitol, SDS 10%. Bromophenol blue, gliserol 87%, dan ddH2O,
coomassie brilliant blue R-250 dan asam asetat glasial selama 3 jam. Gel
dimasukkan ke dalam de-staining solution (etanol, ddH2
3.2 Percobaan Pertama
O, asam asetat glacial)
selama 24 jam. Ukuran protein HPr diprediksi berdasarkan konsensus bahwa 10
kDa protein sama dengan 270 bp DNA.
Tujuan percobaan pertama adalah untuk mengetahui frekuensi perendaman
HPr terbaik dalam memacu pertumbuhan dan kelangsungan hidup benih ikan
gurami. Rancangan percobaan yang digunakan pada percobaan pertama adalah
rancangan acak lengkap (RAL) dengan delapan perlakuan, dan tiga ulangan
(Tabel 1). Perlakuan penelitian adalah frekuensi perendaman HPr 2, 3, 4, dan 5
kali. Dosis hormon pertumbuhan rekombinan dari ikan mas yang diberikan pada
setiap waktu perendaman adalah 30 mg/L (Putra 2011).
Tabel 1 Rancangan percobaan pertama
Perlakuan
Protein badan inklusi tanpa HPr (Kontrol -1)
5 150 1, 2, 3, 4,5
Albumim serum sapi (kontrol-2) 5 0,5 1, 2, 3, 4,5
Media salinitas 9 ppt tanpa
12 Benih ikan gurami berumur 2 hari setelah habis kuning telur, dipuasakan
selama satu hari. Ikan gurami direndam dalam air bersalinitas 30 ppt selama 2
menit dengan padat penebaran 50 ekor, lalu dimasukkan ke dalam media yang
mengandung HPr selama 60 menit. Larutan perendaman sebanyak 1 liter terdiri
dari HPr, NaCl 0,9%, dan albumin serum sapi 0,01%. Ikan diberi pakan berupa
naupli Artemia segar dilanjutkan dengan cacing sutera setelah berumur 7 hari, dan
pakan buatan. Pergantian air di akuarium volume 7 liter dilakukan setiap hari
sebanyak 50% dan pada akuarium volume 50 liter 80%. Suhu dipertahankan
sekitar 29oC selama percobaan menggunakan pemanas otomatis. Setelah berumur
4 minggu ikan dipindahkan ke wadah yang berukuran lebih besar dengan volume
air 50 liter. Setelah berumur 6 minggu ikan dipindahkan ke kolam dan dipelihara
hingga berumur 8 minggu.
3. 3 Percobaan Kedua
Percobaan kedua dilakukan untuk mengetahui respons pertumbuhan ikan
gurami melalui perendaman hormon pertumbuhan rekombinan ikan gurami
dengan dosis optimum. Rancangan percobaan yang digunakan adalah RAL
dengan lima perlakuan, dan tiga ulangan (Tabel 2).
Tabel 2 Rancangan percobaan kedua
Perlakuan (3 ulangan)
Frekuensi perendaman terbaik dari hasil percobaan pertama digunakan
dalam percobaan kedua. Setiap perlakuan mendapat total dosis hormon
13 ekor larva umur 2 hari setelah menetas, direndam selama 2 menit dalam air
volume 1 liter bersalinitas 30 ppt, dan selanjutnya direndam selama 1 jam dalam
air mengandung BSA 0,01% dan NaCl 0,9%. Ikan diberi pakan berupa naupli
Artemia segar selama 7 hari, dilanjutkan dengan cacing sutera sampai berumur 30
hari Setelah berumur 4 minggu ikan dipindahkan ke kolam dan dipelihara hingga
berumur 12 minggu dan diberi pakan buatan.
3.4 Analisis Ekspresi Gen IGF-I
3.4.1 Isolasi RNA Total
Sampel ikan gurami dikumpulkan 24 jam setelah perlakuan perendaman
hormon pertumbuhan rekombinan dari ikan gurami. Sebagai kontrol dikumpulkan
sampel ikan tanpa perlakuan perendaman HPr, dan sampel ikan setelah kejutan
salinitas. Total RNA jaringan tubuh diekstraksi menggunakan isogen (Nippon
Gen, Japan) sesuai prosedur dalam manual. Jaringan dimasukkan ke dalam tabung
berisi isogen 200 µL, dihancurkan menggunakan penggerus yang sebelumnya
telah disterilkan dengan DEPC 1%. Ke dalam tabung ditambahkan larutan isogen
sampai mencapai volume akhir 400 µL. Sebanyak 200 µL kloroform
ditambahkan ke dalam tabung, dan disentrifugasi pada kecepatan 12.000 rpm
selama 5 menit pada suhu ruang. Supernatan yang terbentuk dipindahkan ke
dalam tabung baru yang telah berisi 400 µL isopropanol. Larutan disentrifugasi
pada kecepatan 12.000 rpm selama 15 menit pada suhu 4oC. Supernatan dibuang,
kemudian RNA difiksasi dengan 1 mL etanol 70%, disentrifugasi dengan
kecepatan 12.000 rpm selama 15 menit pada suhu 4o
3.4.2 Sintesis cDNA
C. RNA dikeringkan dengan
cara membuang larutan yang terdapat pada tabung. RNA dilarutkan dengan cara
menambahkan 30 µL DEPC 1%. Konsentrasi RNA total hasil isolasi diukur
menggunakan alat pengukur konsentrasi RNA/DNA (GenQuant). Absorbansi
diukur pada panjang gelombang 260, dan 280 nm.
Sintesis cDNA IGF-I ikan gurami dilakukan menggunakan kit
Ready-To-Go You-Prime First Strand Beads (Amersham Pharmacia Biotech, USA). RNA
14 kemudian didinginkan di atas es. Larutan RNA dipindahkan ke dalam tabung
berisi kit sintesis cDNA, dan ditambahkan 1 µg primer dT3’RACE-VECT
(5’-GTAATACTCACTATAGGGCACGCGTGGTCGACGGCCCGGGCTGGTT
TTTTTTTTTTTTTTTTT-’). Larutan dihomogenkan, dan diinkubasi pada suhu
37o
3.4.3 PCR dan Kuantifikasi Ekspresi Gen IGF-I
C selama 1 jam. cDNA yang terbentuk ditambahkan 30 µL SDW steril, dan
disimpan dalam refrigerator hingga akan digunakan.
Ekspresi gen IGF-I dideteksi dengan menggunakan teknik RT-PCR
menggunakan primer F (5’-TTCAAGAGTGTCATGTGCTGTA-3’) dan
R (5’-CATAGCCTGTTGGTTTACTGAA-3’) (Irmawati, komunikasi pribadi).
Kontrol internal menggunakan gen β-aktin. Gen β-aktin dilacak dengan
menggunakan metode RT-PCR dengan primer F (5’-AACCATGGATGATGAA
ATCGCCGCA-3’) dan R (5’-TGATGCCTGGGGCGA-CCGACGATGG-3’)
(Irmawati, komunikasi pribadi). PCR gen IGF-I dilakukan dengan program: 94oC
selama 1 menit; ( 94oC selama 30 detik; 57oC selama 30 detik; 72oC selama 30
detik) sebanyak 35 siklus; 72oC selama 1 menit; dan 4oC (tak hingga). PCR gen β-aktin dilakukan dengan program: 94oC selama 1 menit; (94oC selama 30 detik; 59oC selama 30 detik; 72oC selama 30 detik) sebanyak 30 siklus; 72oC selama
1 menit; dan 4o
3.5 Analisis Kadar Hormon Kortisol
C (tak hingga). Pengecekan hasil amplifikasi PCR dilakukan
dengan elektroforesis menggunakan gel agarose 1%. Pengukuran level ekspresi
gen IGF-I dilakukan dengan mengukur ketebalan pita DNA hasil elektroforesis
menggunakan program UN-SCAN-IT gel 6.1. Hasil pengukuran level ekspresi
gen IGF-I dibandingkan dengan gen beta aktin yang berfungsi sebagai kontrol
loading RNA dalam sintesis cDNA.
Sampel ikan dikumpulkan 1 menit setelah peredaman HPr, dilanjutkan
pada jam ke-0, 3, 6, 9, 12, 24, dan 36. Sebagai kontrol, ikan dikumpulkan
sebelum, dan sesaat setelah diberi kejutan salinitas. Benih ikan gurami sebanyak
2 g diambil, digerus menjadi halus, lalu ditambahkan 10 mL dietil eter, dan
diinkubasi selama 48 jam pada suhu ruang. Ke dalam tabung ditambahkan PBS
15 disentrifugasi pada 3000 rpm selama 10 menit. Supernatan yang terbentuk
dipindahkan ke dalam tabung baru, dan disimpan pada suhu -20oC hingga akan
digunakan. Pengukuran RIA (radioimmunoassay) dilakukan untuk mengetahui
kadar hormon kortisol menggunakan Ria Kit Kortisol [125
3.6 Analisis Data
I] (Institute of Isotopes
Ltd, Budapest) dengan prosedur sesuai manual.
Data yang diperoleh dianalisis dengan menggunakan sidik ragam pada
tingkat kepercayaan 95%, dan dilanjutkan dengan uji Duncan untuk melihat
pengaruh antar perlakuan terhadap masing-masing parameter yang diuji. Analisis
IV. HASIL DAN PEMBAHASAN
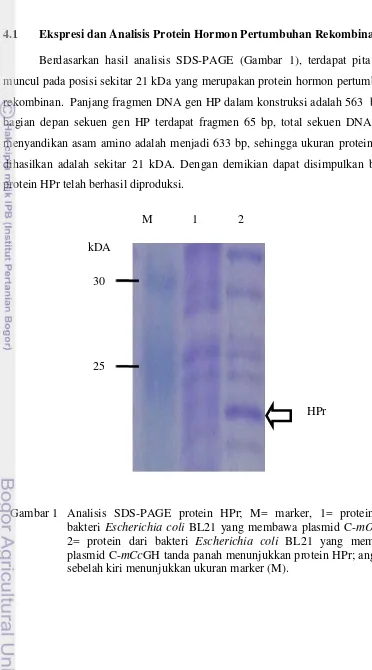
4.1 Ekspresi dan Analisis Protein Hormon Pertumbuhan Rekombinan
Berdasarkan hasil analisis SDS-PAGE (Gambar 1), terdapat pita yang
muncul pada posisi sekitar 21 kDa yang merupakan protein hormon pertumbuhan
rekombinan. Panjang fragmen DNA gen HP dalam konstruksi adalah 563 bp. Di
bagian depan sekuen gen HP terdapat fragmen 65 bp, total sekuen DNA yang
menyandikan asam amino adalah menjadi 633 bp, sehingga ukuran protein yang
dihasilkan adalah sekitar 21 kDA. Dengan demikian dapat disimpulkan bahwa
protein HPr telah berhasil diproduksi.
Gambar 1 Analisis SDS-PAGE protein HPr; M= marker, 1= protein dari
bakteri Escherichia coli BL21 yang membawa plasmid C-mOgGH;
2= protein dari bakteri Escherichia coli BL21 yang membawa plasmid C-mCcGH tanda panah menunjukkan protein HPr; angka di sebelah kiri menunjukkan ukuran marker (M).
30
25 kDA
M 1 2
17 4.2 Percobaan Pertama
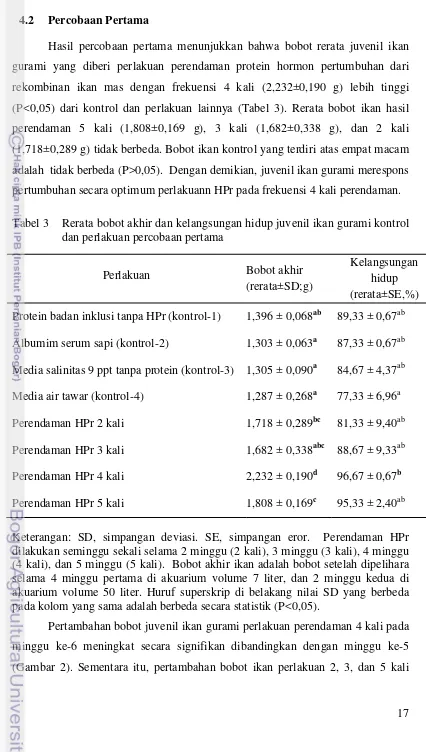
Hasil percobaan pertama menunjukkan bahwa bobot rerata juvenil ikan
gurami yang diberi perlakuan perendaman protein hormon pertumbuhan dari
rekombinan ikan mas dengan frekuensi 4 kali (2,232±0,190 g) lebih tinggi
(P<0,05) dari kontrol dan perlakuan lainnya (Tabel 3). Rerata bobot ikan hasil
perendaman 5 kali (1,808±0,169 g), 3 kali (1,682±0,338 g), dan 2 kali
(1,718±0,289 g) tidak berbeda. Bobot ikan kontrol yang terdiri atas empat macam
adalah tidak berbeda (P>0,05). Dengan demikian, juvenil ikan gurami merespons
pertumbuhan secara optimum perlakuann HPr pada frekuensi 4 kali perendaman.
Tabel 3 Rerata bobot akhir dan kelangsungan hidup juvenil ikan gurami kontrol dan perlakuan percobaan pertama
Perlakuan Bobot akhir
(rerata±SD;g)
Kelangsungan hidup (rerata±SE,%)
Protein badan inklusi tanpa HPr (kontrol-1)
Albumim serum sapi (kontrol-2)
Media salinitas 9 ppt tanpa protein (kontrol-3)
Media air tawar (kontrol-4)
Perendaman HPr 2 kali
Perendaman HPr 3 kali
Perendaman HPr 4 kali
Perendaman HPr 5 kali
1,396 ± 0,068
Keterangan: SD, simpangan deviasi. SE, simpangan eror. Perendaman HPr dilakukan seminggu sekali selama 2 minggu (2 kali), 3 minggu (3 kali), 4 minggu (4 kali), dan 5 minggu (5 kali). Bobot akhir ikan adalah bobot setelah dipelihara selama 4 minggu pertama di akuarium volume 7 liter, dan 2 minggu kedua di akuarium volume 50 liter. Huruf superskrip di belakang nilai SD yang berbeda pada kolom yang sama adalah berbeda secara statistik (P<0,05).
Pertambahan bobot juvenil ikan gurami perlakuan perendaman 4 kali pada
minggu ke-6 meningkat secara signifikan dibandingkan dengan minggu ke-5
18 perendaman HPr, serta kontrol cenderung menurun. Hal ini menunjukkan bahwa
wadah pemeliharaan telah mempengaruhi potensi pertumbuhan ikan. Oleh karena
itu, ikan dipindahkan ke hapa yang dipasang di kolam. Kepadatan ikan dalam
hapa adalah 100 ekor. Setelah dipelihara selama 2 minggu dalam hapa, bobot ikan
perlakuan perendaman HPr 4 kali (4,010 g) meningkat sekitar 1,80 kali lipat
dibandingkan pada minggu ke-6, sedangkan bobot ikan perlakuan lainnya (2,554
– 2,794 g) hanya meningkat sekitar 1,41 – 1,63 kali lipat. Bobot ikan perlakuan
perendaman HPr 4 kali adalah lebih tinggi sekitar 70% dibandingkan dengan
kontrol (1,962 – 2,359 g). Dengan demikian, pertumbuhan ikan perlakuan
perendaman HPr 4 kali tetap lebih tinggi dibandingkan dengan kontrol dan
perlakuan lainnya.
Seperti ditampilkan dalam Tabel 3, tingkat kelangsungan hidup tertinggi
diperoleh pada perlakuan perendaman HPr 4 kali (96,67%), sedangkan yang
terendah pada perlakuan kontrol-4 ikan direndam dalam air tawar (77,33%).
Kelangsungan hidup ikan perlakuan perendaman hormone pertumbuhan
rekombinan ikan mas 4 kali juga lebih tinggi daripada perlakuan kontrol-1, 2, dan
3. Hal ini menunjukkan bahwa perendaman hormon pertumbuhan rekombinan
dari ikan mas 4 kali memberikan kondisi optimum bagi kelangsungan hidup
juvenil ikan gurami. Selanjutnya, kelangsungan hidup ikan saat diperlihara di
kolam adalah 100% untuk semua perlakuan dan kontrol. Dengan demikian,
juvenil ikan gurami yang telah dipelihara selama 6 minggu di akurium relatif kuat
dipelihara pada kondisi lingkungan tidak terkendali dengan baik di kolam.
Pertumbuhan ikan gurami relatif lambat sehingga waktu yang dibutuhkan
untuk mencapai ukuran konsumsi (>300 g/ekor) relatif lama. Perbaikan
pertumbuhan ikan gurami menggunakan metode perendaman hormon
pertumbuhan rekombinan dari ikan mas merupakan alternatif metode cepat. Hasil
percobaan ini menunjukkan bahwa bobot juvenil ikan gurami yang direndam
hormon pertumbuhan rekombinan dari ikan mas sekali seminggu selama
4 minggu 71% lebih tinggi (P<0,05) dibandingkan dengan kontrol-2 albumin
serum sapi. Kelangsungan hidup ikan perlakuan perendaman hormon
pertumbuhan rekombinan dari ikan mas 4 kali (96,67%) juga lebih tinggi daripada
19 hidup juvenil ikan gurami dapat ditingkatkan dengan perlakuan perendaman HPr
4 kali. Bobot dan kelangsungan hidup merupakan faktor penentu tingkat produksi
budidaya ikan, sehingga perlakuan perendaman hormon pertumbuhan rekombinan
dari ikan mas berpotensi tinggi untuk diterapkan oleh pembudidaya untuk
meningkatkan produksi budidayanya.
Gambar 2 Pertumbuhan bobot rerata (g) juvenil ikan gurami yang dipelihara di akuarium volume 7 liter selama 4 minggu pertama dan dilanjutkan di akuarium volume 50 liter selama 2 minggu kedua. Perendaman ikan dalam air mengandung hormon pertumbuhan rekombinan dari ikan mas dilakukan seminggu sekali selama 2 minggu (perendaman HPr 2 minggu), 3 minggu (perendaman HPr 3 kali), 4 minggu (perendaman HPr 4 kali), dan 5 minggu (perendaman HPr 5 kali). Ikan kontrol direndam dalam air yang mengandung protein badan inklusi tanpa HPr (kontrol-1), albumin serum sapi (kontrol-2), Media salinitas 9 ppt tanpa protein (kontrol-3), dan air tawar tanpa protein (kontrol-4).
Frekuensi perendaman HPr 4 kali lebih baik daripada 2, 3, dan 5 kali. Hal
ini menunjukkan bahwa perendaman 4 kali adalah yang optimum untuk memacu
pertumbuhan juvenil ikan gurami. Namun demikian, peningkatan bobot ikan hasil
perlakuan perendaman 4 kali pada percobaan ini sedikit lebih rendah
dibandingkan dengan yang diperoleh oleh Putra (2011) yang melakukan
perendaman HPr sebanyak 3 kali. Salah satu faktor yang diduga berpengaruh
adalah perbedaan HPr yang digunakan, percobaan ini menggunakan HPr ikan
mas, sedangkan Putra (2011) menggunakan HPr ikan gurami. Faktor lain yang 0,0 Protein badan inklusi tanpa rHP (kontrol-1)
Albumin serum sapi (kontrol-2)
Media salinitas 9 ppt tanpa protein (kontrol-3)
Media air tawar (kontrol-4)
Perendaman HPr 2 kali
Perendaman HPr 3 kali
Perendaman HPr 4 kali
20 dapat menjadi penyebab adalah ikan uji yang digunakan bukan ikan klon yang
memiliki karakteristik genetik sama. Pengujian kedua HPr ini secara bersamaan
pada populasi juvenil ikan gurami dari induk yang sama diduga dapat memberikan
jawaban apakah perbedaan hasil percobaan tersebut terkait dengan sumber gen
yang digunakan dalam pembuatan HPr.
Peningkatan frekuensi perendaman HPr cenderung meningkatkan
kelangsungan hidup juvenil ikan gurami. Frekuensi perendaman HPr 4 dan 5 kali
adalah sama, dan lebih tertinggi dibandingkan dengan perlakuan lainnya dan
kontrol termasuk kontrol air tawar. Hal yang sama juga dilaporkan oleh Putra
(2010) bahwa kelangsungan hidup perlakuan HPr (100%) lebih tinggi daripada
kontrol (94%). Pemberian HPr dapat meningkatkan daya tahan ikan terhadap
stres (McCormick 2001; Acosta et al. 2009), dan infeksi penyakit (Sakai et al.
1997; Acosta et al. 2009). Kondisi media dan metode pemeliharaan ikan pada
semua perlakuan pada percobaan ini adalah sama. Oleh karena itu, peningkatan
kelangsungan hidup tersebut diduga disebabkan oleh peningkatkan daya tahan
tubuh ikan terhadap stres. Stres dapat berasal dari perlakuan salinitas, dan
gangguan fisik dalam pemeliharaan ikan seperti pengambilan ikan dari akuarium
untuk diberi perlakuan HPr dan pergantian air akuarium yang dilakukan setiap
hari.
Pemberian HPr dengan frekuensi 3 kali atau lebih adalah umum dilakukan,
seperti Leedom et al. (2002) menginjeksi ikan nila dengan HPr sekali seminggu
selama 4 minggu, dan Acosta et al. (2009) merendam juvenil ikan mas 3 kali
seminggu. Namun demikian, pemberian HPr dengan frekuensi sering adalah tidak
praktis dilakukan oleh pembudidaya. Oleh karena itu, perlakuan HPr dengan
sekali perendaman pada juvenil ikan gurami perlu diteliti. Sonnenschein (2001)
melaporkan peningkatan pertumbuhan ikan grass carp secara signifikan dengan
hanya sekali perendaman HPr menggunakan dosis tinggi 300 mg/L. Penggunaan
total HPr 4 kali pemberian hasil percobaan ini menjadi sekali pemberian (120
mg/L) diduga juga dapat meningkatkan pertumbuhan juvenil ikan gurami secara
signifikan, dan hal ini akan meningkatkan daya tarik HPr untuk diaplikasikan oleh
21 4.3 Percobaan Kedua
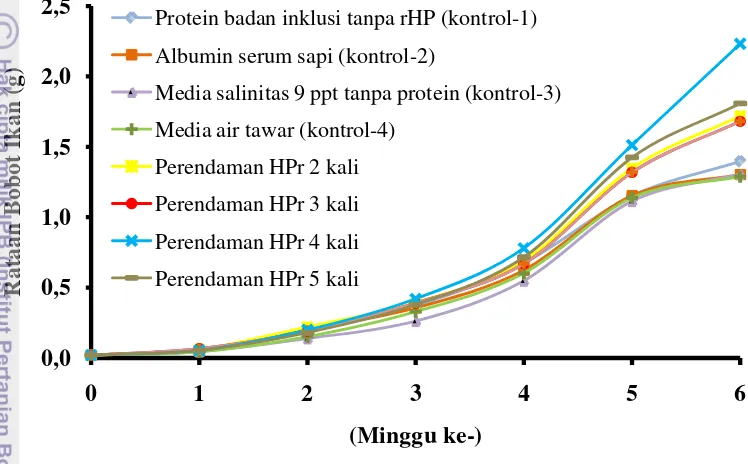
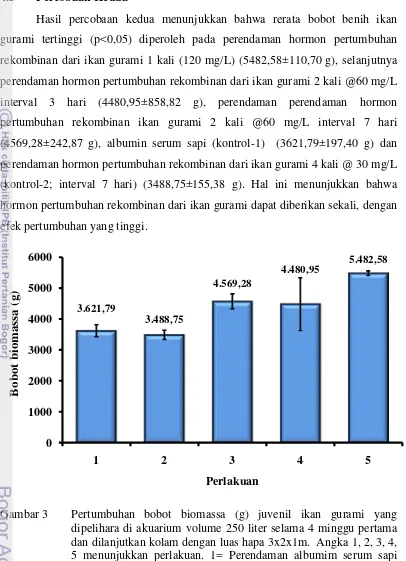
Hasil percobaan kedua menunjukkan bahwa rerata bobot benih ikan
gurami tertinggi (p<0,05) diperoleh pada perendaman hormon pertumbuhan
rekombinan dari ikan gurami 1 kali (120 mg/L) (5482,58±110,70 g), selanjutnya
perendaman hormon pertumbuhan rekombinan dari ikan gurami 2 kali @60 mg/L
interval 3 hari (4480,95±858,82 g), perendaman perendaman hormon
pertumbuhan rekombinan ikan gurami 2 kali @60 mg/L interval 7 hari
(4569,28±242,87 g), albumin serum sapi (kontrol-1) (3621,79±197,40 g) dan
perendaman hormon pertumbuhan rekombinan dari ikan gurami 4 kali @ 30 mg/L
(kontrol-2; interval 7 hari) (3488,75±155,38 g). Hal ini menunjukkan bahwa
hormon pertumbuhan rekombinan dari ikan gurami dapat diberikan sekali, dengan
efek pertumbuhan yang tinggi.
Gambar 3 Pertumbuhan bobot biomassa (g) juvenil ikan gurami yang
dipelihara di akuarium volume 250 liter selama 4 minggu pertama dan dilanjutkan kolam dengan luas hapa 3x2x1m. Angka 1, 2, 3, 4, 5 menunjukkan perlakuan. 1= Perendaman albumim serum sapi (kontrol-1), 2= Perendaman hormon pertumbuhan rekombinan dari
ikan gurami 4 kali @ 30 mg/L (kontrol-2; interval 7 hari), 3= Perendaman hormon pertumbuhan rekombinan dari ikan gurami
2 kali @ 60 mg/L (interval 7 hari), 4= Perendaman hormon pertumbuhan rekombinan dari ikan gurami 2 kali @ 60 mg/L (interval 3 hari), 5= Perendaman hormon pertumbuhan rekombinan dari ikan gurami 1 kali (120 mg/L)
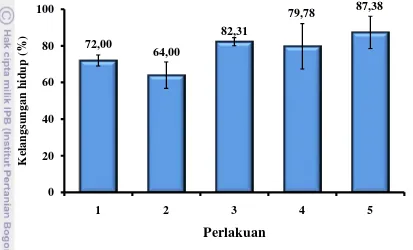
22 Kelangsungan hidup ikan (Gambar 4) hasil perendaman 1 kali
(87,38±8,84%) tidak berbeda (p>0,05) dengan perlakuan perendaman lainnya,
tetapi lebih tinggi (p<0,05) daripada kontrol-2 (64,00±7,25%). Perendaman 1 kali
dengan dosis tinggi mampu memberikan tingkat kelangsungan hidup benih ikan
gurami yang lebih tinggi dibandingkan dengan perlakuan lain, dan kontrol.
Gambar 4 Kelangsungan hidup ikan gurami pada akhir percobaan. Angka 1, 2, 3, 4, 5 menunjukkan perlakuan. 1= Perendaman albumim serum sapi (kontrol-1), 2= Perendaman HPr dari ikan gurami 4 kali @ 30 mg/L (kontrol-2; interval 7 hari), 3= Perendaman HPr dari ikan gurami 2 kali @ 60 mg/L (interval 7 hari), 4= Perendaman HPr dari ikan gurami 2 kali @ 60 mg/L (interval 3 hari), 5= Perendaman HPr dari ikan gurami 1 kali (120 mg/L)
Perendaman HPr dari ikan gurami dosis tinggi memacu pertumbuhan
bobot benih ikan gurami yang diamati pada percobaan ini. Terlihat bahwa
perendaman HPr sekali dengan dosis tinggi memberikan pertumbuhan yang
signifikan (P<0,05) dengan perlakuan lainnya. Agellon et al. (1988) telah meneliti
perendaman sekali larva ikan raibow trout dalam larutan HPr 500 µg/L dapat
memacu pertumbuhan. Sementara Schulte et al. (1995) melaporkan bahwa HPr
sapi dapat mempercepat pertumbuhan benih ikan rainbow trout setelah direndam
pada dosis 1-100 mg/L. Peterson et al. (2004) menyatakan bahwa penyuntikan
23 0,5-
0,5-
kb M 1 2 3 4 5 6 7
Kelangsungan hidup ikan hasil perendaman 1 kali (87,29±8,76) berbeda
(p<0,05) dengan perlakuan perendaman lainnya. Perendaman tunggal dengan
dosis tinggi mampu memberikan tingkat kelangsungan hidup benih ikan gurami
yang lebih tinggi dibanding dengan perlakuan lainnya. Putra (2011) mendapatkan
kelangsungan hidup 100% pada perendaman benih ikan gurami dosis 30 mg/L.
Selanjutnya Acosta et al. (2009) menyatakan bahwa pemberian HPr pada larva
dapat meningkatkan kelangsungan hidup dan daya tahan terhadap stres dan infeksi
penyakit. Pemberian HPr pada ikan rainbow trout juga efektif meningkatkan
resistensi terhadap Vibrio anguilarum (Sakai et al. 1997).
4.4 Ekspresi Gen IGF-I
Hasil elektroforesis RT-PCR ekspresi gen IGF-I, 24 jam setelah direndam
dengan HPr dari ikan gurami dapat dilihat pada Gambar 5A. Sebagai kontrol
internal digunakan gen β-aktin (Gambar 5B). Dari hasil analisis level ekspresi
(Gambar 6) pemberian HPr pada ikan gurami 1 kali perendaman dapat
menginduksi peningkatan ekspresi gen IGF-I yang signifikan setelah 24 jam
dibandingkan dengan perlakuan lain.
\
Gambar 5 Ekspresi gen IGF-I (A), dan gen β-aktin (B) yang diamati 24 jam
setelah perendaman hormon pertumbuhan rekombinan (HPr) dari ikan gurami. M = marker DNA. Angka 1, 2, 3, 4, 5, 6, dan 7, menunjukkan perlakuan. 1= Perendaman HPr 1 kali (120 mg/L), 2 = Perendaman HPr 2 kali (@ 60 mg/L, 3= Perendaman 4 kali @ 30 mg/L (kontrol-2; interval 7 hari), 4= Perendaman dengan albumin serum sapi (kontrol-1), 5= kontrol sebelum kejutan salinitas, 6= kontrol setelah kejutan salinitas, 7= sampel hasil PCR tanpa DNA cetakan.
A
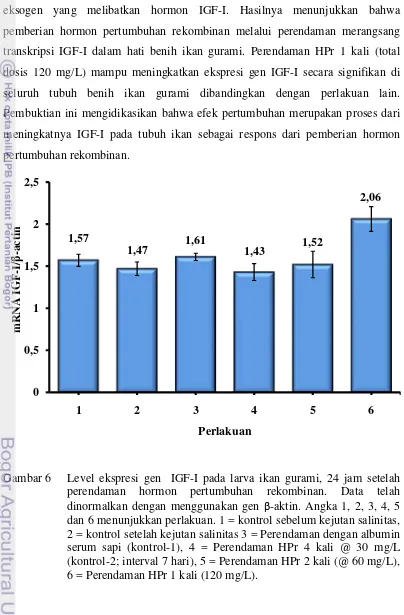
24 Penelitian ini ingin membuktikan mekanisme kerja hormon pertumbuhan
eksogen yang melibatkan hormon IGF-I. Hasilnya menunjukkan bahwa
pemberian hormon pertumbuhan rekombinan melalui perendaman merangsang
transkripsi IGF-I dalam hati benih ikan gurami. Perendaman HPr 1 kali (total
dosis 120 mg/L) mampu meningkatkan ekspresi gen IGF-I secara signifikan di
seluruh tubuh benih ikan gurami dibandingkan dengan perlakuan lain.
Pembuktian ini mengidikasikan bahwa efek pertumbuhan merupakan proses dari
meningkatnya IGF-I pada tubuh ikan sebagai respons dari pemberian hormon
pertumbuhan rekombinan.
Gambar 6 Level ekspresi gen IGF-I pada larva ikan gurami, 24 jam setelah perendaman hormon pertumbuhan rekombinan. Data telah
dinormalkan dengan menggunakan gen β-aktin. Angka 1, 2, 3, 4, 5
25 Peningkatan IGF-I setelah direndam rHP yang ditemukan pada penelitian
ini serupa dengan pola IGF-I pada ikan ekor kuning (Pedroso et al. 2009), ikan
salmon (Pierce et al. 2004) dan ikan seabream (Leung et al. 2008) yang
menunjukkan adanya pengaruh hormon pertumbuhan yang besar dalam hati ketika
diberikan hormon pertumbuhan eksogen dengan dosis tinggi. Pemberian hormon
pertumbuhan secara eksogen baik yang homolog dan heterolog juga dapat
menyebabkan peningkatan mRNA IGF-I di hati ikan salmon (Oncorhynchus
kisutch) (Duguay et al. 1994), ikan sidat Jepang (Anguilla japonica) (Duan et al.
1993) dan ikan mas (Cyprinus carpio) (Vong et al. 2003). IGF-I berperan penting
dalam mengatur beberapa proses fisiologi ikan seperti pertumbuhan, metabolisme,
perkembangan, reproduksi dan osmoregulasi. Pemberian hormon pertumbuhan
pada ikan juga dapat meningkatkan toleransi terhadap salinitas (Bolton et al.
1987) sehingga dapat mengurangi tingkat stres ikan gurami yang diberi kejutan
salinitas dan perendaman HPr.
Efek hormon pertumbuhan pada jaringan target dimediasi oleh reseptor
hormon pertumbuhan. Hal ini telah dilaporkan oleh Gahr et al. (2008) bahwa
pemberian hormon pertumbuhan rekombinan akan meningkatkan ekspresi
reseptor hormon pertumbuhan pada hati. Ekspresi IGF-I dipengaruhi oleh hormon
pertumbuhan, dan pada percobaan kedua digunakan hormon pertumbuhan
rekombinan ikan gurami. Penggunaan hormon pertumbuhan rekombinan yang
homolog diduga memegang peranan penting dalam mengenali dan merespons
sinyal reseptor serta memiliki tingkat afinitas tinggi. Hormon pertumbuhan
berikatan dengan reseptor di hati, dan merangsang pelepasan hormon IGF-I
(Moriyama et al. 2000).
4.5 Kadar Hormon Kortisol
Hasil pengukuran hormon kortisol pada benih ikan gurami yang diberi
kejutan salinitas dan direndam dengan hormon pertumbuhan rekombinan dapat
dilihat pada Gambar 7. Sebelum diberi kejutan salinitas, kadar kortisol yang
terukur adalah 3,12 ng/mL kemudian mengalami peningkatan sebanyak 190,23%
ke level 9,04 ng/mL setelah kejutan salinitas selama 2 menit. Level kortisol terus
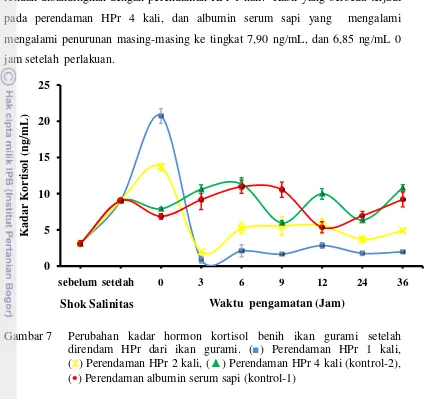
26 mencapai 20,72 ng/mL sesaat setelah perendaman. Perendaman HPr 2 kali juga
mencapai puncak sesaat setelah perendaman HPr pada 13,70 ng/mL, tetapi lebih
rendah dibandingkan dengan perendaman HPr 1 kali. Hasil yang berbeda terjadi
pada perendaman HPr 4 kali, dan albumin serum sapi yang mengalami
mengalami penurunan masing-masing ke tingkat 7,90 ng/mL, dan 6,85 ng/mL 0
jam setelah perlakuan.
Gambar 7 Perubahan kadar hormon kortisol benih ikan gurami setelah
direndam HPr dari ikan gurami. (■) Perendaman HPr 1 kali,
(x) Perendaman HPr 2 kali, (▲) Perendaman HPr 4 kali (kontrol-2), (•) Perendaman albumin serum sapi (kontrol-1)
Pada jam ke-3 setelah perendaman HPr, tingkat hormon kortisol yang
terukur pada perlakuan perendaman HPr 1 kali mengalami penurunan ke tingkat
0,89 ng/mL dan cendenrung normal sampai pada jam ke-36. Pola yang sama juga
ditunjukkan pada perendaman HPr 2 kali yaitu pada jam ke-3 setelah perendaman
juga mengalami penurunan ke level 1,97 ng/mL. Pada perendaman HPr 4 kali dan
albumin serum sapi, hormon kortisol kembali meningkat masing-masing hingga
7,90 ng/mL dan 6,85 ng/mL, 0 jam setelah perendaman dan mengalami fluktuasi
sampai akhir pengamatan. Puncak hormon kortisol pada perendaman HPr 4 kali
terjadi pada jam ke-3 (11,35 ng/mL) dan pada perendaman albumin serum sapi
27 Hormon kortisol merupakan salah satu indikator untuk mengukur tingkat
stres pada ikan (Haukenes et al. 2008). Meningkatnya kadar hormon kortisol
setelah setelah diberi kejutan salinitas merupakan reaksi adaptif ikan dalam
menanggapi perubahan kondisi lingkungan yang ekstrim. Beberapa penelitian
telah menujukkan bahwa perubahan salinitas dapat meningkatkan konsentrasi
hormon kortisol dalam dalam darah ikan seperti yang dilaporkan oleh Young et al.
(1989) pada ikan salmon coho (Oncorhynchus kisutch) dan (Morgan et al.1997)
pada ikan mujair (Oreochromis mossambicus).
Perendaman hormon pertumbuhan rekombinan dari ikan gurami 1 kali
meningkatkan kadar hormon kortisol ikan gurami yang diamati sesaat setelah
perendaman hingga mencapai 20,72 ng/mL. Hal yang sama juga terlihat pada
perendaman HPr 2 kali, namun hanya meningkat hingga 13,70 ng/mL. Tingginya
kadar hormon kortisol sesaat setelah direndam diduga karena terjadinya
peningkatan ACTH (Adrenocorticortropic Hormone) sebagai respon terhadap
terganggunya fungsi biokimia tubuh (Porchas et al. 2009), sehingga merangsang
produksi hormon kortisol. Hal yang sama terjadi pada Rainbow trout
(Oncorhynchus mykiss) (Benguira et al. 2002) yang mengalami peningkatan kadar
hormon kortisol setelah diekspos dalam larutan kimia.
Ada kecenderungan bahwa perendaman HPr 1 kali dan 2 kali
mengakibatkan ikan lebih cepat kembali pulih setelah mengalami stres. Pada
percobaan ini ditemukan bahwa level kortisol menurun ke tingkat yang paling
rendah 3 jam setelah mengalami stres. Sementara pada beberapa ikan, butuh
waktu selama 6 jam untuk kembali ke tingkat normal setelah stres (Iwama et al.
1995). Tingkat kortisol ikan red drum mengalami peningkatan saat penangkapan
dan menurun ke tingkat bawah dalam waktu 48 jam (Robertson et al. 1987). Ikan
mas mengalami peningkatan hormon kortisol ketika ditangkap dengan jaring dan
kembali normal setelah 4 jam (Pottinger 1998). Namun Biga (2004) menyatakan
bahwa pemberian hormon pertumbuhan meningkatkan sirkulasi kortisol dalam
darah ikan rainbow trout (Oncorhynchus mykiss).
Pada percobaan ini ditemukan bahwa tingkat hormon kortisol terendah
28 hormon kortisol diduga berhubungan dengan kinerja hormone pertumbuhan yang
memberikan kontrol negatif terhadap jaringan interrenal yang merupakan tempat
sekresi utama hormon kortisol (Nishioka et al. 1985). Kondisi hormon kortisol
yang cenderung stabil setelah mengalami stres mempengaruhi kinerja
pertumbuhan yang optimal bagi ikan gurami dibandingkan dengan perlakuan lain.
Pada perendaman HPr 1 kali, kisaran kortisol dari jam ke-3 sampai jam ke-36
berkisar antara 0,89 ng/mL hingga 2,84 ng/mL, lebih rendah sebelum diberi
kejutan salinitas (3,12 ng/mL). Data bobot biomassa dan tingkat kelangsungan
hidup benih ikan yang terbaik pada perendaman HPr 1 kali juga ditunjang oleh
keadaan hormon kortisol yang cepat pulih dan tetap rendah dan lebih stabil selama
percobaan. Penelitian Flick et al. (1993) membuktikan bahwa pemberian hormon
pertumbuhan rekombinan mampu memberikan pertumbuhan biomassa terbaik
setelah 44 hari dan hormon kortisol yang lebih rendah 94,8% dibandingkan
dengan kontrol.
Data bobot biomassa (Gambar 3) dan kelangsungan hidup (Gambar 4)
terbaik didapatkan dari perendaman HPr 1 kali berhubungan dengan keadaan
plasma kortisol darah tubuh ikan selama percobaan. Rendahnya kadar kortisol
pada percobaan pertama diduga merupakan kondisi yang efisien untuk memacu
pertumbuhan, dan aman dari serangan bakteri atau virus yang dapat
mengakibatkan kematian. Yada et al. (2005) menyatakan bahwa pemberian HPr
dapat mengatifkan sistem kekebalan pada tubuh ikan. Hal yang sama diduga juga
terjadi pada penelitian ini.
Kadar hormon kortisol yang berfluktuasi terlihat pada perlakuan kontrol-1
dan kontrol-2 dari awal sampai akhir percobaan. Peningkatan hormon kortisol
diduga kerena adanya gangguan pada saat penangkapan dan pemindahan ikan ke
wadah yang baru sehingga merangsang hipotalamus untuk melepaskan
corticotropin-releasing factor (CRF) ke dalam sirkulasi darah. Polipeptida ini
kemudian mengaktifkan pelepasan adrenocorticotrophic hormon (ACTH) dari
kelenjar anterior hipofisis untuk merangsang pelepasan hormon kortisol yang
diproduksi di jaringan interrenal (Mommsen et al. 1999). Rendahnya tingkat
pertumbuhan dan kelangsungan hidup pada perlakuan kontrol-1 dan kontrol-2
29 berulang-ulang. Hal ini merupakan proses yang maladaptif sehingga dapat
mengakibatkan pertumbuhan ikan menjadi lambat, peningkatan konsumsi
oksigen, pengunaan energi yang lebih banyak, dan dapat meningkatn kerentanan
terhadap penyakit (Jentoft et al. 2005).
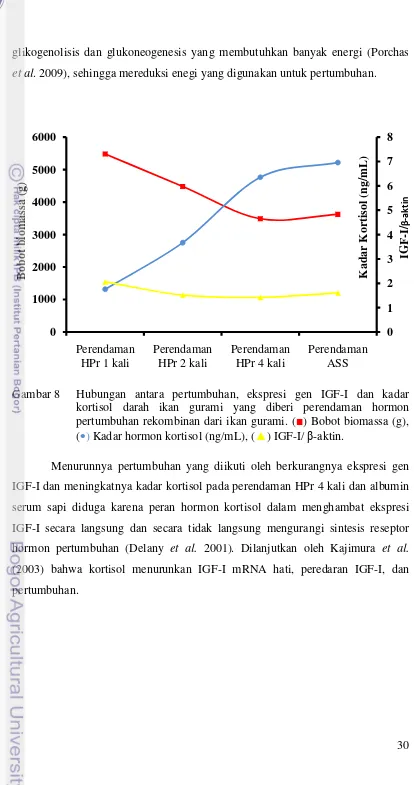
4.6 Hubungan antara Pemberian Hormon Pertumbuhan Rekombinan, Pertumbuhan, Ekspresi Gen IGF-1 dan Kadar Hormon Kortisol
Pemberian hormon pertumbuhan rekombinan melalui perendaman dapat
meningkatkan pertumbuhan ikan gurami, melibatkan hormon IGF-I baik secara
langsung maupun tidak langsung, dan berhubungan dengan kadar hormon kortisol
dalam tubuh ikan gurami (Gambar 8). Perendaman HPr 1 kali menghasilkan
bobot biomassa yang tinggi, ekspresi gen IGF-I yang meningkat dan kadar
hormon kortisol. Pada perendaman HPr 2 kali terlihat pertambahan bobot
biomassa mulai menurun, ekspresi IGF-I menurun dan meningkatnya kadar
hormon kortisol. Sementara perendaman HPr 4 kali menghasilkan bobot biomassa
yang rendah, ekspresi gen IGF-1 yang menurun dan kadar hormon kortisol yang
semakin tinggi. Pola yang sama terjadi pada perendaman albumin serum sapi yang
direndam selama 4 kali. Perendaman HPr yang berulang-ulang dapat menurunkan
pertambahan bobot biomassa, ekspresi gen IGF-I berkurang dan meningkatkan
kadar kortisol sehingga perendaman HPr 1 kali efektif dilakukan untuk memacu
pertumbuhan ikan gurami.
Peningkatan pertumbuhan ikan gurami yang diberi hormon pertumbuhan
rekombinan 1 kali disebabkan karena HPr yang diberikan efektif merangsang
ekspresi gen IGF-I (Silverstein et al. 2000; Biga et al. 2005). Bukti ini
menguatkan bahwa peningkatan pertumbuhan disebabkan karena hormon
pertumbuhan mampu memediasi produksi IGF-I di hati dan memperjelas bahwa
hormon pertumbuhan merupakan pengatur utama produksi IGF-I pada ikan
(Moriyama et al. 2000).
Perendaman berulang-ulang mempengaruhi pertumbuhan ikan diduga
karena ikan mengalami stres yang berlangsung lama. Pada penelitian ini
ditemukan bahwa semakin sering ikan direndam dalam larutan HPr akan