EKSTRAKSI CAIR-CAIR UNTUK PEMURNIAN XANTORIZOL
DARI MINYAK ATSIRI TEMULAWAK: PENENTUAN
KOEFISIEN PARTISI DAN EFISIENSI EKSTRAKSI
AJENG WIDYASWARI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Ekstraksi Cair-cair untuk Pemurnian Xantorizol dari Minyak Atsiri Temulawak: Penentuan Koefisien Partisi dan Efisiensi Ekstraksi adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
ABSTRAK
AJENG WIDYASWARI. Ekstraksi Cair-cair untuk Pemurnian Xantorizol dari Minyak Atsiri Temulawak: Penentuan Koefisien Partisi dan Efisiensi Ekstraksi. Dibimbing oleh RUDI HERYANTO dan IRMANIDA BATUBARA.
Berbagai metode telah banyak diterapkan untuk memurnikan xantorizol dari minyak atsiri temulawak. Pada penelitian ini, minyak atsiri dari pelepah temulawak diisolasi menggunakan metode distilasi uap, sedangkan xantorizolnya diekstraksi dari minyak atsiri menggunakan metode ekstraksi cair-cair menggunakan sistem pelarut HEMWat yang terdiri atas n-heksana, etil asetat, metanol, dan air. Xantorizol dalam ekstrak tersebut ditentukan nilai koefisien partisinya (K) dalam sistem pelarut HEMWat. Sistem pelarut 13 dipilih dari 15 sistem pelarut karena memiliki nilai K terbesar yaitu 430. Xantorizol dalam minyak atsiri awal yang dilarutkan dalam metanol dan dianalisis menggunakan kromatografi cair kinerja tinggi muncul pada waktu retensi 9 menit dengan konsentrasi relatif 35 . Setelah dilakukan 3 kali ekstraksi, nilai efisiensi adalah 68 dan konsentrasi relatifnya yaitu 39 . Hasil analisis kromatografi gas-spektrometer massa memperlihatkan keberhasilan ekstraksi bertingkat xantorizol dari minyak atsiri pelepah temulawak.
Kata kunci: ekstraksi bertingkat, HEMWat, temulawak, xantorizol
ABSTRACT
AJENG WIDYASWARI. Liquid-liquid Extraction for the Xanthorrhizol Purification of Temulawak Essential Oil: Determination of Partition Coefficient and Extraction Efficiency. Supervised by RUDI HERYANTO and IRMANIDA BATUBARA.
Various methods had been widely performed for purifying xanthorrhizol of temulawak essential oils. In this study, essential oils from the stem of temulawak was isolated using steam distillation method, whereas the xanthorrhizol was extracted from essential oils using liquid-liquid extraction method with HEMWat solvent system consisted of n-hexane, ethyl acetate, methanol, and water. Partition coefficient (K) of xanthorrhizol in that extract was determined in the HEMWat solvent system. Solvent system 13 was selected of the 15 solvent system because it had the highest K value of 430. Xanthorrhizol in the initial essential oils that was dissolved in methanol was analyzed using high performance liquid chromatography appeared at retention time of 9 minutes with the relative concentration of 35 . The value of efficiency after 3 times of extraction was 68 and the relative concentration of 39 . Analysis result of gas chromatography-mass spectrometer showed that xanthorrhizol in essential oils from the stem of temulawak had been successfully extracted using multistage extraction.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Kimia
EKSTRAKSI CAIR-CAIR UNTUK PEMURNIAN XANTORIZOL
DARI MINYAK ATSIRI TEMULAWAK: PENENTUAN
KOEFISIEN PARTISI DAN EFISIENSI EKSTRAKSI
AJENG WIDYASWARI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Penelitian yang dilakukan dari Mei sampai Oktober 2015 ini berjudul Ekstraksi Cair-cair untuk Pemurnian Xantorizol dari Minyak Atsiri Temulawak: Penentuan Koefisien Partisi dan Efisiensi Ekstraksi.
Terima kasih penulis ucapkan kepada Rudi Heryanto, MSi dan Dr Irmanida Batubara, MSi selaku pembimbing atas bimbingan, arahan, dan sarannya kepada penulis. Ungkapan terima kasih juga penulis sampaikan kepada Ayah (alm) dan Ibu atas doa dan kasih sayangnya. Di samping itu, penghargaan penulis sampaikan kepada Muhamad Mahfudin, Nur Chasanah, Arum Vitasari, Kak Palupi Dwi Antari, Kak Aprilia Inggri, Kak Hanhan Nur Handayani, Windi Prasetyawati, Liana Farida, Andini Chandra, Wira Prihandini, Intan Agustina, Natalia Verolina, Nabila Swarna, Khammia, dan Riztrya Novedliani yang telah memberikan semangat dan motivasinya kepada saya dalam menyelesaikan penelitian dan skripsi ini.
Semoga karya ilmiah ini bermanfaat.
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
PENDAHULUAN 1
METODE 2
Alat dan Bahan 2
Metode Penelitian 2
HASIL DAN PEMBAHASAN 4
Profil Minyak Atsiri Pelepah Temulawak 4
Koefisien Partisi Xantorizol dalam Berbagai Sistem Pelarut 5
Optimasi Efisiensi Ekstraksi 6
Pemastian Xantorizol Menggunakan KG-SM 8
SIMPULAN DAN SARAN 9
Simpulan 9
Saran 9
DAFTAR PUSTAKA 10
LAMPIRAN 13
DAFTAR TABEL
1 Komposisi sistem pelarut HEMWat untuk ekstraksi cair-cair 3 2 Nilai koefisien partisi (K) dari rentang sistem pelarut terpilih 6
DAFTAR GAMBAR
1 Kromatogram minyak atsiri dalam metanol 5
2 Grafik nilai koefisien partisi (K) dari 5 sistem pelarut 6 3 Kromatogram fase atas sistem pelarut 13 tahap 3 (a) dan tahap 2 (b) 7 4 Kromatogram fase atas campuran dari ekstraksi tahap 1, 2, dan 3
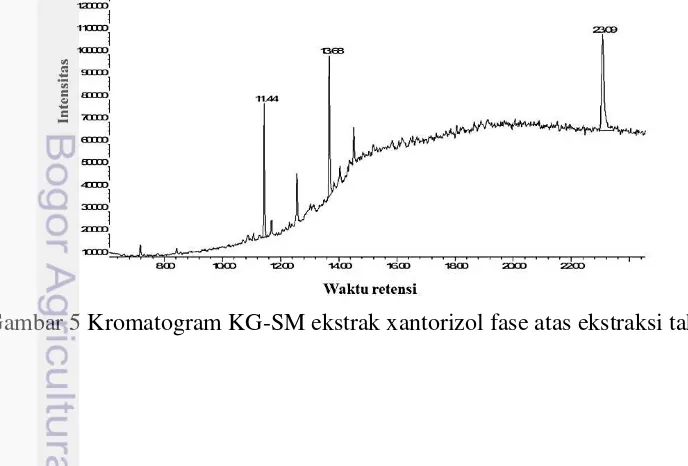
menggunakan metanol (a) dan minyak atsiri dalam metanol (b) 8 5 Kromatogram KG-SM ekstrak xantorizol fase atas ekstraksi tahap 2 8 6 Spektrum massa KG-SM ekstrak xantorizol fase atas ekstraksi tahap 2 9
DAFTAR LAMPIRAN
1 Diagram alir penelitian 13
2 Kromatogram standar xantorizol dan sistem pelarut HEMWat 14
3 Polaritas sistem pelarut 18
PENDAHULUAN
Temulawak (Curcuma xanthorrhiza) merupakan tumbuhan rumpun berbatang semu yang digunakan sebagai tanaman obat, baik dalam bentuk tunggal maupun campuran. Temulawak telah banyak digunakan masyarakat Indonesia sebagai obat untuk mengatasi batu empedu, batu ginjal, kolesterol tinggi, nyeri sendi, nyeri haid, pelancar ASI, demam, sembelit, dan eksim (Herdiyanto 2014). Temulawak juga diketahui memiliki khasiat sebagai antioksidan (Masuda et al. 1992), antibakteri (Hwang et al. 2000, Darusman et al. 2006), antilipidemia (Yasni et al. 1994), antijamur (Rukayadi dan Hwang 2007), antikanker (Ravindran et al. 2007), antitumor (Sudewo 2004), hepatoprotektor, antiradang (Nuratmi et al. 1996), dan berpotensi untuk penanganan penyakit flu burung (Darusman et al. 2007). Selain itu, temulawak dapat dimanfaatkan sebagai penyusun komponen jamu dan ditemukan di dalam setiap efikasi formulasi jamu (Wijaya et al. 2014).
Bagian temulawak yang paling banyak dimanfaatkan yaitu rimpang karena mengandung komponen aktif utama berupa kurkuminoid dan minyak atsiri. Kurkuminoid yang terdiri atas kurkumin, desmetoksikurkumin, dan bisdesmetoksikurkumin berkhasiat sebagai antioksidan dan memberikan warna kuning pada rimpang temulawak. Sedangkan minyak atsirinya mengandung
feladren, β-tumeron, kamfer, dan xantorizol (Rahardjo dan Rostiana 2005). Xantorizol adalah komponen khas minyak atsiri dari temulawak yang dapat membedakannya dengan tumbuhan genus Curcuma lainnya (Cho et al. 2011, Itokawa et al. 2008). Sebagai komponen bioaktif yang khas dari temulawak, xantorizol berpotensi digunakan sebagai senyawa penciri untuk kontrol kualitas berbagai produk yang berasal dari temulawak. Namun sampai saat ini keberadaan standar xantorizol di pasaran masih terbatas, seperti perusahaan penyedia bahan kimia Sigma-Aldrich yang tidak lagi menyediakan standar xantorizol. Oleh karena itu, perlu dilakukan suatu upaya untuk menyediakan standar xantorizol yang diperlukan untuk kendali mutu sebagai komponen utama dalam jamu.
Penelitian senyawa aktif pada temulawak selama ini hanya berfokus pada rimpang, padahal xantorizol juga ditemukan di berbagai bagian pada temulawak seperti daun, pelepah, dan bunga. Sukrasno (2012) telah melakukan penelitian pada rimpang temulawak menggunakan KG-SM dan mendapatkan kadar xantorizol dalam minyak atsiri rimpang sebesar 7.10 . Septyanti (2012) melakukan penelitian pada pelepah temulawak dan Julita (2013) melakukan penelitian pada daun pelindung bunga temulawak menggunakan KG-SM dan memperoleh kadar xantorizol dalam minyak atsiri masing-masing sebesar 29.87 dan 16.13 . Dari penelitian di atas menunjukkan bahwa potensi kandungan xantorizol pada pelepah lebih besar dari rimpang dan daun temulawak. Oleh karena itu, pengembangan metode pemurnian xantorizol dari minyak atsiri pelepah temulawak perlu dilakukan agar dapat diperoleh xantorizol dengan kadar yang tinggi sebagai bahan untuk membuat standar xantorizol.
2
metode Asriani (2010), namun masih terdapat senyawa pengganggu pada hasil akhirnya. Sebagai alternatif, penelitian ini akan menggunakan teknik ekstraksi cair-cair dengan memanfaatkan distribusi zat pada 2 fase terpisah untuk pemurnian xantorizol dalam minyak atsiri. Pemilihan sistem pelarut 2 fase untuk ekstraksi cair-cair dapat dilakukan dengan menggunakan sistem ARIZONA atau HEMWat. Sistem pelarut 2 fase ARIZONA terdiri atas heptana, etil asetat, metanol, dan air, sedangkan sistem pelarut 2 fase HEMWat terdiri atas n-heksana, etil asetat, metanol, dan air (Wu dan Wu 2013). Dalam penelitian ini, sistem pelarut HEMWat dipilih dan digunakan karena telah dibuktikan dari penelitian yang dilakukan oleh Wu et al. (2007), Graziose et al. (2011), Yan et al. (2012), Pinel et al. (2007), dan Wang et al. (2011) yang telah berhasil mengisolasi senyawa seskuiterpena dengan menggunakan sistem pelarut 2 fase HEMWat. Penelitian ini bertujuan mengisolasi xantorizol dengan ekstraksi cair-cair. Tujuan ini dicapai dengan menentukan koefisien partisi dari 2 fase pelarut menggunakan sistem HEMWat, menganalisis kadar xantorizol di dalam 2 fase pelarut menggunakan kromatografi cair kinerja tinggi (KCKT), dan mengoptimasi ekstraksi berdasarkan pada sistem 2 fase pelarut terpilih yang dinilai dari koefisien partisinya.
METODE
Alat dan Bahan
Bahan yang digunakan yaitu pelepah temulawak dari kebun UKBB Pusat Studi Biofarmaka Bogor sebanyak 50 kg, n-heksana, etil asetat, metanol, akuades, asam fosfat 0.2 , dan natrium sulfat. Alat-alat yang digunakan yaitu peralatan gelas, neraca analitik, distilator uap, kromatografi cair kinerja tinggi (KCKT) merk Shimadzu tipe LC-20A, dan kromatografi gas-spektrometer massa (KG-SM) merk Shimadzu tipe QP-5050A.
Metode Penelitian
Metode penelitian yang dilakukan meliputi beberapa tahap. Tahapan tersebut yaitu isolasi minyak atsiri, ekstraksi cair-cair, penentuan koefisien partisi dan efisiensi ekstraksi, optimasi pelarut dengan ekstraksi cair-cair bertingkat, dan analisis kadar xantorizol menggunakan KCKT (Lampiran 1).
3
Penentuan Koefisien Partisi dalam Sistem Pelarut (Xie et al. 2009)
Pelarut HEMWat dicampurkan masing-masing dengan nisbah volume yang sesuai dengan Tabel 1. Sebanyak 20 mg minyak atsiri dimasukkan ke dalam 20 ml sistem pelarut nomor 1, 5, 9, 13, dan 15 yang dimasukkan ke dalam corong pisah dan dikocok sampai terbentuk dua fase larutan (Xie et al. 2009).
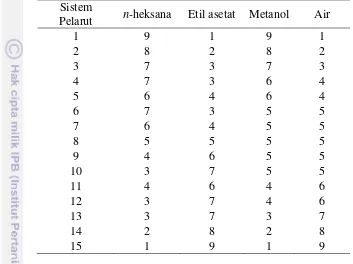
Tabel 1 Komposisi sistem pelarut HEMWat untuk ekstraksi cair-cair Sistem
Pelarut n-heksana Etil asetat Metanol Air
1 9 1 9 1 yang dipisahkan dan dihitung nilai koefisien partisinya yang ditentukan dengan mengambil 1 mL dari tiap fase pelarut yang dianalisis menggunakan KCKT. Minyak atsiri dilarutkan ke dalam metanol untuk mengetahui komposisi minyak atsiri awal pada konsentrasi 1000 g/mL. Luas puncak dari tiap fase pelarut dibandingkan dengan luas puncak minyak atsiri awal dalam metanol. Nilai koefisien partisi (K) ditentukan menggunakan persamaan:
K =
di mana Aorg adalah luas puncak dari komponen target di dalam fase atas dan Aaq adalah luas puncak dari komponen target di dalam fase bawah (Wei et al. 2012). Nilai koefisien partisi digunakan untuk memilih sistem pelarut yang akan digunakan dalam ekstraksi. Pemasti sistem pelarut ditentukan dengan mempersempit rentang sistem pelarut, dalam hal ini digunakan 1 dari sistem pelarut tersebut.
Optimasi Efisiensi Ekstraksi (Harvey 2000)
Pelarut terpilih kemudian digunakan untuk ekstraksi bertingkat dari xantorizol. Ekstraksi bertingkat dilakukan sebanyak 3 kali. Sistem pelarut dengan volume 20 mL yang mengandung xantorizol kemudian diambil fase bawahnya
4
untuk ekstraksi bertingkat menggunakan larutan fase atas dengan volume yang sama. Sistem pelarut terpilih kemudian ditentukan fraksi solut dalam fase atas dan bawah menggunakan persamaan:
( ) =
) = 1 ( )
di mana qaq dan qorg adalah fraksi solut dalam fase bawah dan fase atas, D adalah rasio distribusi, Vorg dan Vaq merupakan banyaknya volume fase organik dan fase air yang digunakan. Dari persamaan di atas, efisiensi ekstraksi (E) dapat ditentukan menggunakan fraksi solut dalam fase atas:
E = ( ) 100
Efisiensi ekstraksi dari sistem pelarut terpilih dapat dioptimasi dengan melakukan ekstraksi cair-cair bertingkat dan dihitung menggunakan persamaan berikut:
di mana n adalah banyaknya ekstraksi yang dilakukan dan Qaq adalah fraksi solut dalam fase bawah setelah n kali ekstraksi.
Analisis Xantorizol (Darusman et al. 2007)
Ekstrak yang didapat dari hasil ekstraksi cair-cair kemudian ditentukan kadar xantorizolnya dengan menggunakan KCKT. Sistem KCKT yang digunakan adalah dengan kolom XBridge C18 (150 mm 4.16 mm), detektor photodiode array (PDA) dengan panjang gelombang yang digunakan adalah 224 nm, volume injeksi 20 μL, elusi isokratik (eluen H3PO4 0.2 , asetonitril, dan metanol), dan suhu kolom 40 . Sebanyak 4 mg sampel hasil pemurnian dilarutkan dalam n-heksana dan dianalisis menggunakan KG-SM selama 30 menit dengan gas pembawa helium dan laju alir 1 mL/menit. Suhu injektor dan detektor sama, yaitu 290 , sedangkan suhu kolom terprogram diawali dengan 70 ditahan selama 4 menit, kemudian diubah perlahan-lahan dengan laju kenaikan suhu 15 /menit hingga mencapai 290 .
HASIL DAN PEMBAHASAN
Profil Minyak Atsiri Pelepah Temulawak
Isolasi minyak atsiri dari pelepah temulawak dilakukan menggunakan metode distilasi uap. Distilat yang diperoleh kemudian dikeringkan menggunakan natrium sulfat anhidrat. Minyak atsiri yang diperoleh kemudian diekstraksi untuk mendapatkan xantorizol menggunakan metode ekstraksi cair-cair. Metode ini dipilih karena ekstraksi cair-cair sangat berguna untuk memisahkan analat yang
(2) (3)
(4)
5 dituju dari pengganggu dengan cara melakukan partisi sampel antar 2 pelarut yang tidak saling campur. Senyawa yang bersifat polar akan ditemukan di dalam fase air, sementara senyawa yang bersifat nonpolar akan ditemukan di dalam fase organik. Analat yang terekstraksi ke dalam pelarut organik akan mudah diperoleh kembali dengan cara penguapan pelarut (Harvey 2000).
Minyak atsiri yang berhasil diekstraksi dalam penelitian ini yaitu sebanyak 5 g dari 50 kg pelepah temulawak segar, sehingga rendemen minyak atsiri yang diperoleh adalah sebesar 0.01 . Hasil yang diperoleh dalam penelitian ini lebih kecil dibandingkan dengan penelitian sebelumnya yang telah dilakukan oleh Septyanti (2012) yang berhasil mengekstraksi minyak atsiri sebanyak 3.5 g dari 5 kg pelepah temulawak segar dengan rendemen minyak atsiri sebesar 0.07 . Perbedaan rendemen minyak atsiri ini dapat disebabkan oleh umur panen temulawak (Nurcholis 2006). Pelepah temulawak yang digunakan dalam penelitian ini berumur 6 BST, sedangkan Septyanti (2012) menggunakan pelepah temulawak berumur 9 BST.
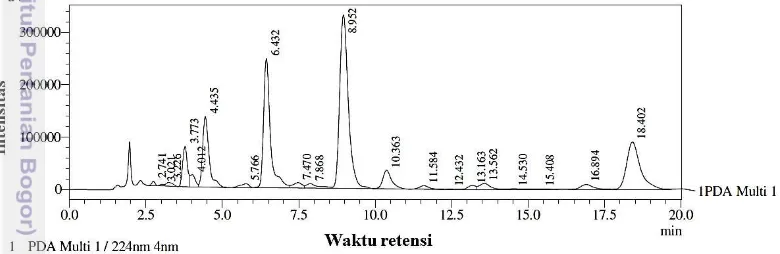
Minyak atsiri dilarutkan ke dalam metanol untuk mengetahui komposisi minyak atsiri awal dan dianalisis menggunakan KCKT. Puncak xantorizol muncul pada waktu retensi 8.952 menit dengan persen area sebesar 34.988 (Gambar 1). Waktu retensi yang diperoleh untuk xantorizol ini mendekati waktu retensi pada kromatogram standar xantorizol 200 ppm dalam metanol yaitu pada 8.904 menit (Lampiran 2).
Gambar 1 Kromatogram minyak atsiri dalam metanol
Koefisien Partisi Xantorizol dalam Berbagai Sistem Pelarut
6
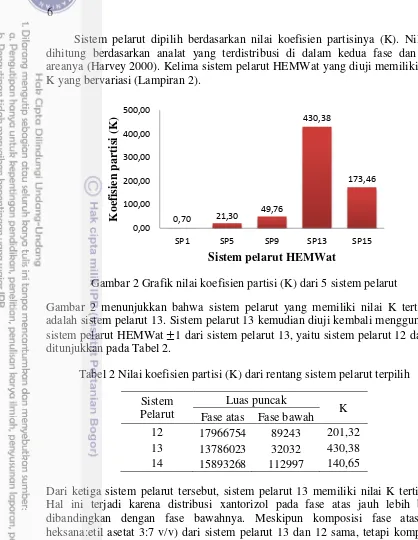
Sistem pelarut dipilih berdasarkan nilai koefisien partisinya (K). Nilai K dihitung berdasarkan analat yang terdistribusi di dalam kedua fase dan luas areanya (Harvey 2000). Kelima sistem pelarut HEMWat yang diuji memiliki nilai K yang bervariasi (Lampiran 2).
Gambar 2 Grafik nilai koefisien partisi (K) dari 5 sistem pelarut
Gambar 2 menunjukkan bahwa sistem pelarut yang memiliki nilai K tertinggi adalah sistem pelarut 13. Sistem pelarut 13 kemudian diuji kembali menggunakan sistem pelarut HEMWat 1 dari sistem pelarut 13, yaitu sistem pelarut 12 dan 14 ditunjukkan pada Tabel 2.
Tabel 2 Nilai koefisien partisi (K) dari rentang sistem pelarut terpilih Sistem dibandingkan dengan fase bawahnya. Meskipun komposisi fase atas (n-heksana:etil asetat 3:7 v/v) dari sistem pelarut 13 dan 12 sama, tetapi komposisi fase bawahnya berbeda yaitu dari komposisi metanol dan air yang digunakan, sehingga kepolaran sistem pelarut 12 dan 13 berbeda yang dapat diketahui dari gabungan nilai indeks polaritasnya berdasarkan Byers (2003) (Lampiran 3). Sistem pelarut HEMWat yang paling baik digunakan untuk ekstraksi xantorizol adalah sistem pelarut 13 yang memiliki indeks polaritas sebesar 5.45 (Lampiran 3).
Optimasi Efisiensi Ekstraksi
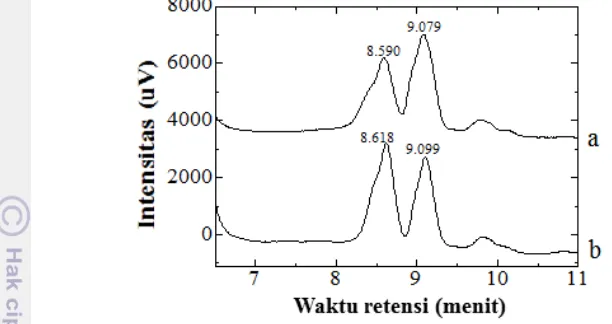
7 bertingkat tahap 2 dan 3 diperoleh dua puncak berdekatan di sekitar waktu retensi xantorizol.
Gambar 3 Kromatogram fase atas sistem pelarut 13 tahap 3 (a) dan tahap 2 (b) Dua puncak berdekatan yang dihasilkan dari kromatogram fase atas tahap 2 dan 3 merupakan splitting peak dari xantorizol. Splitting terjadi karena xantorizol yang terdeteksi di kolom berasal dari xantorizol yang terlarut di dalam n-heksana dan etil asetat sebagai fase atas yang digunakan, juga xantorizol yang terlarut dalam metanol yang berasal dari fase bawah tahap sebelumnya memberikan interaksi yang berbeda terhadap fase diamnya (Sigma-Aldrich 2009). Hal ini dibuktikan dari munculnya puncak pada waktu retensi 9.079 menit (Gambar 3a) dan 9.099 (Gambar 3b) yang berdekatan dengan waktu retensi xantorizol dalam kromatogram minyak atsiri yang dilarutkan dalam metanol (Gambar 1).
8
Gambar 4 Kromatogram fase atas sistem pelarut 13 campuran dari ekstraksi tahap 1, 2, dan 3 menggunakan metanol (a) dan kromatogram minyak atsiri dalam metanol
Kromatogram di atas menunjukkan bahwa campuran fase atas dari ekstraksi bertingkat (Gambar 4a) memiliki luas puncak yang lebih kecil dibandingkan dengan luas puncak xantorizol pada kromatogram minyak atsiri dalam metanol (Gambar 4b). Meskipun luas puncaknya berkurang, kromatogram campuran fase atas memiliki persen area yang lebih besar yaitu 38.69 . Hasil ini menunjukkan kemurnian xantorizol hanya meningkat sedikit setelah dilakukan ekstraksi bertingkat sebanyak tiga kali karena pelarut HEMWat tidak dapat memisahkan analat dari pengganggu yang memiliki kepolaran hampir sama, sehingga sistem pelarut Arizona diperlukan untuk mengekstraksi xantorizol karena komposisi pelarutnya memiliki rentang yang lebih besar sehingga dapat memisahkan xantorizol dengan kemurnian yang tinggi.
Pemastian Xantorizol Menggunakan KG-SM
Untuk membuktikan keberhasilan ekstraksi xantorizol dari fase bawah ekstraksi cair-cair tahap 1 dilakukan analisis menggunakan KG-SM. Hasil analisis KG-SM menunjukkan bahwa terdapat 3 senyawa yang masing-masing muncul pada waktu retensi 11.440, 13.679, dan 23.085 menit (Gambar 5). Senyawa yang terdeteksi pada waktu retensi 11.440 dan 23.085 menit adalah -kurkumena dan asam oleamida, sedangkan xantorizol terdeteksi pada waktu retensi 13.679 menit.
9
Gambar 6 Spektrum massa KG-SM ekstrak xantorizol fase atas ekstraksi tahap 2 Spektrum SM juga menunjukkan keberhasilan ekstraksi bertingkat dari xantorizol ditandai dengan munculnya nilai m/z sebesar 218.2 (Gambar 6). Berdasarkan pustaka, persen kemiripan struktur xantorizol yaitu sebesar 81 dan memiliki persen area sebesar 29.73 .
SIMPULAN DAN SARAN
Simpulan
Xantorizol telah berhasil diekstraksi menggunakan pelarut HEMWat dengan teknik ekstraksi cair-cair dan dioptimasi menggunakan ekstraksi cair-cair bertingkat. Sistem pelarut HEMWat yang memiliki nilai K tertinggi adalah sistem pelarut 13. Sistem pelarut 13 yang telah diekstraksi bertingkat dan dianalisis menggunakan KCKT menghasilkan pembelahan puncak xantorizol pada kromatogram. Hasil analisis menggunakan KG-SM membuktikan keberhasilan ekstraksi bertingkat xantorizol dengan munculnya nilai m/z 218. Ekstraksi bertingkat dari sistem pelarut 13 dapat dilakukan untuk menentukan efisiensi ekstraksi sehingga diperoleh nilai 67.87 dan dapat meningkatkan kemurnian xantorizol pada fase atas yaitu sebesar 38.687 .
Saran
10
DAFTAR PUSTAKA
Asriani D. 2010. Isolasi xanthorrhizol dari temu lawak terpilih berdasarkan nomor harapan [tesis]. Bogor (ID): Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Byers JA. 2003. Table Values from Phenomenex Catalog. [Internet] [diunduh 2015 Nov 25]. Tersedia pada: http://www.phenomenex.com.
Cho JY, Hwang JK, Chun HS. 2011. Xanthorrhizol attenuates dextran sulfate sodium-induced colitis via the modulation of the expression of inflammatory genes in mice. Life Sci. 88(19-20): 864-870. doi:10.1016/j.lfs.2011.03.007.
Darusman LK, Djauhari E, Nurcholis W. 2006. Kandungan xanthorrhizol temulawak (Curcuma xanthorrhiza Roxb.) pada berbagai cara budidaya dan masa tanam. Prosiding Seminar Tumbuhan Obat Indonesia XXIX. Surakarta (ID): Fakultas Kedokteran Universitas Sebelas Maret. hlm 567-580.
Darusman et al. 2007. Potensi Temu Lawak Terstandar untuk Menanggulangi Flu Burung. [Internet] [diunduh 2015 Mar 7]. Tersedia pada: http://repository.ipb.ac.id/handle/123456789/7181.
Graziose R, Rathinasabapathy T, Lategan C, Poulev A, Smith PJ, Grace M, Lila MA, Raskin I. 2011. Antiplasmodial activity of aporphine alkaloids and sesquiterpene lactones from Liriodendron tulipifera L. J Ethnopharmacol 133:26–30. doi: 10.1016/j.jep.2010.08.059.
Harvey D. 2000. Modern Analytical Chemistry. New York (US): McGraw-Hill. Hendayana S. 2006. Kimia Pemisahan: Metode Kromatografi dan Elektroforesis
Modern. Bandung (ID): PT Remaja Rosdakarya.
Herdiyanto. 2014. Pengoptimuman metode ekstraksi dan isolasi xantorizol dari temulawak (Curcuma xanthorrhiza Roxb.) [skripsi]. Bogor (ID): Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Hwang JK. 2000. Xanthorrhizol: A New Bioactive Natural Compound. Seoul (KR): Department of Biotechnology, Yonsei University.
Hwang JK, Shim JS, Pyun YR. 2000. Antibacterial activity of xanthorrhizol from Curcuma xanthorrhiza against oral pathogens. Fitoterapia 71(3): 321-323. doi:10.1016/S0367-326X(99)00170-7.
Itokawa H, Qian S, Toshiyuki A, Morris-Natschke SL, Lee KH. 2008. Recent advances in the investigation of curcuminoids. Chin Med. 3(11): 1-13. doi: 10.1186/1749-8546-3-11.
Julita I. 2013. Daun pelindung bunga temu lawak (Curcuma xanthorrhiza Roxb.) sebagai inhibitor tirosinase dan antioksidan [skripsi]. Bogor (ID): Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Masuda T, Isobe J, Jitoe A, Nakatani N. 1992. Antioxidative curcuminoids from rhizomes of Curcuma xanthorrhiza. Phytochem 31(10): 3645-3647. doi:10.1016/0031-9422(92)83748-N.
11 Nuratmi B, Adjirni, Paramitha DL. 1996. Penelitian farmakologis sambiloto
(Andrographis paniculata). Warta Tumbuhan Obat Indonesia 3: 23.
Nurcholis W. 2006. Kandungan xanthorrizol temulawak (Curcuma xanthorrhiza Roxb) pada berbagai cara budidaya dan masa tanam [skripsi]. Bogor (ID): Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor. Pinel B, Audo G, Mallet S, Lavault M, De La Poype F, Séraphin D, Richomme P.
2007. Multi-grams scale purification of xanthanolides from Xanthium macrocarpum centrifugal partition chromatography versus silica gel chromatography. J Chromatogr A 1151(1-2): 14–19. doi:10.1016/ j.chroma.2007.02.115.
Rahardjo M, Rostiana O. 2005. Budidaya Tanaman Temulawak. Bogor (ID): Balai Penelitian Tanaman Obat dan Aromatika.
Ravindran PN, Babu KN, Sivaraman K. 2007. Turmeric: The Genus Curcuma. New York (US): CRC press.
Rukayadi Y, Hwang JK. 2007. In vitro antimycotic activity of xanthorrhizol isolated from Curcuma xanthorrhiza Roxb. against opportunistic filamentous fungi. Phytother Res 5: 434-438. doi:10.1002/ptr.2092.
Septyanti C. 2012. Potensi pelepah temulawak sebagai antikanker dan antioksidan [skripsi]. Bogor (ID): Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Sigma-Aldrich. 2009. HPLC Troubleshooting Guide. [Internet] [diunduh 2015 Nov 25]. Tersedia pada: http://www.sigmaaldrich.com/etc/medialib/ docs/Supelco/Bulletin/4497.Par.0001.File.tmp/4497.pdf
Sudewo B. 2004. Tanaman Obat Populer Penggempur Aneka Penyakit. Jakarta (ID): Agro Media Pustaka.
Sukrasno, Kartika, Fidrianny I, Elfahmi, Anam K. 2012. Influence of storage on the volatile oil content of Curcuma rhizome. Res J Med Plant : 1-7. doi:10.3923/rjmp.2012.274.280.
Wang D, Fang L, Wang X, Qiu Z, Huang L. 2011. Preparative separation and purification of sesquiterpenoids from Tussilago farfara L. by high-speed counter-current chromatography. Quim Nova 34(5): 804–807. doi:10.1590/S0100-40422011000500014.
Wijaya SH, Husnawati, Afendi FM, Darusman LK, Batubara I, Md. Altaf-Ul-Amin, Sato T, Ono N, Sugiura T, Kanaya S.2014. Supervised Clustering Based on DPClusO: Prediction of Plant-Disease Relations Using Jamu Formulas of KNApSAcK Database. BioMed Res Int 2014: 1-15. doi:10.1155/2014/831751.
Wu D, Wu S. 2013. Comprehensive solvent system for counter-current chromatographic separation of natural antioxidant flavonoids from traditional chinese medicines. J Med Res Dev 2(1): 1-14.
Wu H, Su Z, Yang Y, Ba H, Aisa HA. 2007. Isolation of three sesquiterpene lactones from the roots of Cichorium glandulosum Boiss. et Huet. by high-speed counter-current chromatography. J Chromatogr A 1176(1-2):217– 222. doi:10.1016/j.chroma.2007.11.013.
12
Yan G, Ji L, Luo Y, Hu Y. 2012. Preparative isolation and purification of three sesquiterpenoid lactones from Eupatorium lindleyanum DC. by high-speed counter-current chromatography. Molecules 17: 9002–9009. doi:10.3390/molecules17089002.
Yasni S, Imaizumi K, Sin K, Sugano M, Nonaka G, Sidik. 1994. Identification of an active principle in essential oils and hexane-soluble fractions of Curcuma xanthorrhiza Roxb. Showing triglyceride-lowering action in rats. Food Chem Toxicol 32(3): 273-278.
13 Lampiran 1 Diagram alir penelitian
Sistem pelarut terpilih Minyak atsiri kering Kedua fase pelarut dipisahkan
Distilasi uap selama 6 jam, kemudian dikeringkan menggunakan natrium sulfat
Penentuan koefisien partisi dalam 2 fase pelarut
Optimasi efisiensi ekstraksi dari sistem pelarut terpilih Isolasi minyak atsiri
dari pelepah temulawak
Analisis xantorizol Ekstraksi cair-cair dengan sistem pelarut HEMWat
Analisis menggunakan KCKT
Ekstraksi cair-cair bertingkat
14
Lampiran 2 Kromatogram standar xantorizol dan minyak atsiri dalam sistem pelarut HEMWat 1, 5, 9, 13, dan 15
Kromatogram standar xantorizol 1000 ppm
Kromatogram fase atas sistem pelarut 1
15 Lampiran 2 Kromatogram standar xantorizol dan minyak atsiri dalam sistem
pelarut HEMWat 1, 5, 9, 13, dan 15 (lanjutan)
Kromatogram fase atas sistem pelarut 9
Kromatogram fase atas sistem pelarut 13
16
Lampiran 2 Kromatogram standar xantorizol dan minyak atsiri dalam sistem pelarut HEMWat 1, 5, 9, 13, dan 15 (lanjutan)
Kromatogram fase bawah sistem pelarut 1
Kromatogram fase bawah sistem pelarut 5
17 Lampiran 2 Kromatogram standar xantorizol dan minyak atsiri dalam sistem
pelarut HEMWat 1, 5, 9, 13, dan 15 (lanjutan)
Kromatogram fase bawah sistem pelarut 13
Kromatogram fase bawah sistem pelarut 15
Nilai koefisien partisi (K) dari 5 sistem pelarut Sistem
Pelarut
Luas puncak
K Fase atas Fase bawah
1 3995685 5700961 0.7
5 10860041 509940 21.3
9 11412007 229336 49.76
13 13786023 32032 430.38
18
Lampiran 3 Polaritas sistem pelarut berdasarkan Byers (2003)
Indeks polaritas komponen pelarut HEMWat Pelarut Indeks polaritas
n-heksana 0
etil asetat 4.4
metanol 5.1
air 9
Indeks polaritas sistem pelarut HEMWat Sistem pelarut Indeks polaritas
gabungan
12 5.26
13 5.45
14 5.87
Contoh perhitungan indeks polaritas sistem pelarut 13:
=
19 Lampiran 4 Efisiensi ekstraksi cair-cair bertingkat xantorizol teoritis
Kromatogram fase atas sistem pelarut 13 ekstraksi tahap 1
Kromatogram fase bawah sistem pelarut 13 ekstraksi tahap 1
Perhitungan koefisien partisi xantorizol:
K =
K =
K = 320.5429
Perhitungan fraksi solut dalam fase bawah (bila suatu solut hanya berbentuk tunggal pada masing-masing fase, D = K):
( ) =
( ) =
20
Lampiran 4 Efisiensi ekstraksi cair-cair bertingkat xantorizol teoritis (lanjutan)
Perhitungan fraksi solut dalam fase atas: ) = 1 ( )
) = 1 – (3.1100 10-3) ) = 0.9969
Perhitungan efisiensi ekstraksi E = ( ) 100
E = 0.9969 100 E = 99.69
Perhitungan fraksi solut dalam fase bawah setelah tiga kali ekstraksi:
= 3.0081 10-8
Perhitungan fraksi solut dalam fase atas setelah tiga kali ekstraksi: ) = 1 ( )
) = 1 – (3.0081 10-8) ) = 0.9999
Perhitungan optimasi efisiensi ekstraksi setelah tiga kali ekstraksi: E = ( ) 100
21 Lampiran 5 Efisiensi ekstraksi cair-cair bertingkat xantorizol sebenarnya
Massa xantorizol tahap 1 fase atas:
=
⁄ = 7620.57 = 7.6206 mg
Massa xantorizol tahap 1 fase bawah:
=
⁄ = 4882.33 = 4.8823 mg
Massa xantorizol tahap 2 fase atas:
=
= 0.6716 mg
Massa xantorizol tahap 2 fase bawah:
=
= 2.0248 mg
Massa xantorizol tahap 3 fase atas:
=
22
Lampiran 5 Efisiensi ekstraksi cair-cair bertingkat xantorizol sebenarnya (lanjutan)
Efisiensi ekstraksi bertingkat sebenarnya:
E =
E =
23
RIWAYAT HIDUP
Penulis lahir di Karawang pada 24 Juni 1994 dari ayah Drs Sumarman (alm) dan ibu Herliawati. Tahun 2011, penulis lulus dari SMA Negeri 1 Subang dan pada tahun yang sama lulus Seleksi Nasional Masuk Perguruan Tinggi (SNMPTN) undangan di Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.