ANALISIS KANDUNGAN LOGAM BERAT TIMBAL (Pb) DAN
TEMBAGA (Cu) DALAM AIR DAN KERANG HIJAU (
Perna
viridis
) DI MUARA ANGKE, TELUK JAKARTA
ILMU DAN TEKNOLOGI KELAUTAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN INSTITUT PERTANIAN BOGOR
BOGOR 2015
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi yang berjudul Analisis Kandungan Logam Berat Timbal (Pb) dan Tembaga (Cu) dalam Air dan Kerang Hijau (Perna viridis) di Muara Angke, Teluk Jakarta adalah benar karya saya dengan arahan dari Komisi Pembimbing dan belum diajukan dalam bentuk apa pun kepada Perguruan Tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, April 2015
ABSTRAK
ENDANG GINONG PRATIDINA. Analisis Kandungan Logam Berat Timbal (Pb) dan Tembaga (Cu) dalam Air dan Kerang Hijau (Perna viridis) di Muara Angke, Teluk Jakarta. Dibimbing oleh TRI PRARTONO.
Teluk Jakarta telah tercemar logam berat dan dimanfaatkan sebagai tempat budidaya kerang hijau. Penelitian ini bertujuan menganalisis kondisi terkini Pb dan Cu dalam air dan kerang hijau di Teluk Jakarta terhadap beberapa penelitian sebelumnya. Pengambilan sampel air dan kerang hijau dilakukan tanggal 22 Mei 2014 di satu lokasi perairan Muara Angke dan analisis logam berat menggunakan Spektrofotometri Serapan Atom (AAS). Kandungan logam berat Pb di perairan Teluk Jakarta saat ini adalah 0.012 ppm sedangkan Cu sebesar 0.005 ppm. Kandungan Pb dalam kerang hijau berkisar antara 6.620-11.593 mg/kg sedangkan Cu berkisar antara 8.714-12.206 mg/kg. Hasil analisis menunjukkan variasi konsentrasi Pb dan Cu pada setiap kelas ukuran kerang hijau, serta tidak ada korelasi yang erat antara ukuran cangkang dengan kandungan logam berat yang terserap dalam jaringan tubuh kerang hijau. Berat total logam Pb dan Cu yang diakumulasi oleh kerang hijau mengacu data hasil tangkapan di Teluk Jakarta tahun 2000-2014 diperkirakan mencapai 2,433.41 kg dan 2,194.59 kg. Hal ini mengindikasikan bahwa pencemaran logam berat dari daratan masih terjadi hingga saat ini.
Kata kunci: Cu, Pb, kerang hijau, pencemaran, Teluk Jakarta
ABSTRACT
ENDANG GINONG PRATIDINA. Analysis of Heavy Metal Content of Lead (Pb) and Copper (Cu) in water and Green Mussels (Perna viridis) at Muara Angke, Jakarta Bay. Under direction of TRI PRARTONO.
Jakarta Bay has been polluted by heavy metals and is used for green mussel cultivation. This study aimed to analyze current condition of Pb and Cu in seawater and green mussels from Jakarta Bay, and compare them to previous studies. Seawater and green mussels sample were collected on 22 May 2014 at single site in Muara Angke, and analyzed by Atomic Absorption Spectrophotometry (AAS). Current condition of Pb in seawater of Jakarta Bay was 0.012 ppm while that of Cu was 0.005 ppm. Concentrations of Pb in green mussels were 6.620-11.593 mg/kg, while that of Cu were 8.714-12.206 mg/kg. Varying concentration of Pb and Cu were measured from each green mussel and no significant correlation between the shell size of green mussel and heavy metal content within were absorbed. Total weight of Pb and Cu, according to green mussels harvest data from 2000-2014 was estimated at 2,433.41 kg and reached 2,194.59 kg Cu. This study indicates that heavy metals pollution from the mainland still continues until present.
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Ilmu Kelautan
pada
Departemen Ilmu dan Teknologi Kelautan
ANALISIS KANDUNGAN LOGAM BERAT TIMBAL (Pb) DAN
TEMBAGA (Cu) DALAM AIR DAN KERANG HIJAU (
Perna
viridis
) DI MUARA ANGKE, TELUK JAKARTA
ENDANG GINONG PRATIDINA
DEPARTEMEN ILMU DAN TEKNOLOGI KELAUTAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya sehingga karya ilmiah berjudul “Analisis Kandungan Logam Berat Timbal (Pb) dan Tembaga (Cu) dalam Air dan Kerang Hijau (Perna viridis) di Muara Angke, Teluk Jakarta” berhasil diselesaikan.
Terima kasih penulis ucapkan kepada Bapak Dr Ir Tri Prartono MSc selaku pembimbing, Ibu Yunesfi Sofyan SPi selaku pembimbing lapang, dan Bapak Dr Ir Sigit Hariyadi MSc selaku dosen penguji. Terima kasih penulis sampaikan kepada Yuriska Andiri, Annisya Rosdiana, dan Ness Kaptarina yang telah banyak membantu penulis pada penelitian sebelumnya, Adhimas Agung, Anma Hari Kusuma, Lucia Pamungkasih, Rahmad, Muhammad Idris, Isnaini Prihatiningsih, Muqtasidun Saifullah, Anna Farida, Alfin Khairi, Ikhsanul Khairi, Sayid Geubry Al-Farisi, M Faisi Ikhwali, Azwinur, Ferdy Gustian, Khasanah Dwi Astuti, Titan Budi Setyawan, Ismatullah Jay, dan seluruh pihak yang telah membantu dalam pelaksanaan penelitian ini. Terima kasih pula kepada Rahmah Utami yang tidak henti-hentinya memberikan bantuan, semangat dan dukungan kepada penulis. Ungkapan terima kasih tak terhingga juga penulis sampaikan kepada papa, mama, serta adik-adik atas segala kesabaran, doa, dukungan, dan kasih sayangnya sehingga penulis mampu menyelesaikan pendidikan di IPB.
Semoga karya ilmiah ini bermanfaat untuk lingkungan dan ilmu pengetahuan.
Bogor, April 2015
DAFTAR ISI
DAFTAR GAMBAR x
DAFTAR LAMPIRAN x
PENDAHULUAN 1
Latar Belakang 2
Tujuan 2
METODE 2
Waktu dan Tempat 2
Alat dan Bahan 2
Pengambilan Contoh Kerang Hijau dan Air Laut 3
Analisis Laboratorium 3
Analisis Data 5
HASIL DAN PEMBAHASAN 6
Logam Timbal (Pb) dan Tembaga (Cu) dalam Air 6
Logam Timbal (Pb) dan Tembaga (Cu) dalam Kerang Hijau 7 Korelasi Ukuran Cangkang dengan Kandungan Timbal (Pb) dan
Tembaga (Cu) dalam Kerang Hijau 10
Pendugaan Berat Pb dan (Cu) dalam Kerang Hijau di Teluk Jakarta 13
KESIMPULAN 15
DAFTAR PUSTAKA 15
LAMPIRAN 18
DAFTAR GAMBAR
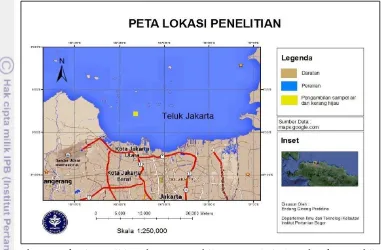
1 Peta lokasi penelitian dan pengambilan sampel air laut dan kerang hijau
di Muara Angke, Teluk Jakarta 3
2 Konsentrasi logam Pb dan Cu terlarut dalam contoh air laut (ppm) di
Muara Angke, Teluk Jakarta 6
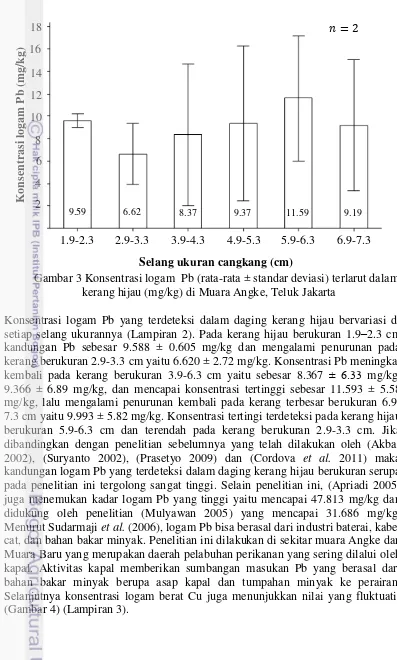
3 Konsentrasi logam Pb terlarut dalam kerang hijau (mg/kg) di Muara
Angke, Teluk Jakarta 8
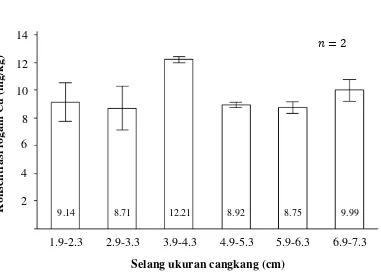
4 Konsentrasi logam Cu terlarut dalam kerang hijau (mg/kg) di Muara
Angke, Teluk Jakarta 9
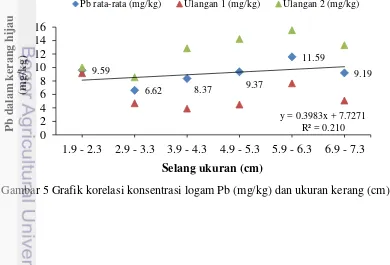
5 Grafik korelasi antara konsentrasi logam berat Pb (mg/kg) dan ukuran
kerang hijau (cm) 10
6 Grafik korelasi antara konsentrasi logam berat Cu (mg/kg) dan ukuran
kerang hijau (cm) 11
7 Tingkat akumulasi logam Pb (mg) pada kerang hijau dari berbagai
selang ukuran cangkang (cm) 12
8 Tingkat akumulasi logam Cu (mg) pada kerang hijau dari berbagai
selang ukuran cangkang (cm) 12
9 Produksi kerang hijau di Teluk Jakarta pada kurun waktu tahun
2000-2014 14
10 Pendugaan berat total rata-rata logam Pb dan Cu dalam kerang hijau
hasil tangkapan pada kurun waktu 2000-2014 15
DAFTAR LAMPIRAN
1 Kandungan logam berat Pb dan Cu pada air laut (ppm) 18 2 Kandungan logam berat Pb pada kerang hijau (mg/kg) 18 3 Kandungan logam berat Cu pada kerang hijau (mg/kg) 18
PENDAHULUAN
Latar Belakang
Teluk Jakarta telah mengalami pencemaran logam berat akibat masukan dari berbagai aktivitas pemukiman, industri, dan pelabuhan di sekitarnya melalui aliran sungai (Sachoemar dan Wahjono 2007; Ratnawati dan Sunarko 2008). Timbal (Pb) dan tembaga (Cu) merupakan logam yang bersifat racun yang terdeteksi di perairan tersebut (Tresnasari 2001, Akbar 2002). Tembaga adalah logam yang banyak dihasilkan dalam industri cat, tekstil, penyepuhan logam dan dipakai dalam pembuatan pestisida (Primaharinastiti et al. 2004). Tembaga biasa digunakan dalam industri bahan bakar, baterai, kabel, dan industri kimia yang menggunakan bahan pewarna (Sudarmaji et al. 2006). Jika logam berat terakumulasi dalam tubuh organisme dengan jumlah yang tinggi dan dikonsumsi oleh manusia, maka akan menimbulkan gejala keracunan seperti gangguan fungsi ginjal (Widaningrum et al. 2007) dan sistem syaraf (Sudarmaji et al. 2006).
Muara Angke merupakan salah satu tempat berlangsungnya aktivitas budidaya kerang hijau (Perna viridis). Pada tahun 2000, jumlah produksi kerang hijau di Teluk Jakarta mencapai 118,920 ton, tahun 2001 sebanyak 125,660 ton, dan tahun 2004 sebanyak 122,000 ton (Hartanto 2007). Berbagai penelitian menjelaskan bahwa kerang hijau mampu mengakumulasi logam berat terlarut dalam air laut (Akbar 2002; Suryanto 2002; Ratnawati dan Sunarko 2008; Jalius et al. 2008; Winarno 2009; Sitorus 2011; Cordova et al. 2011), sehingga dibutuhkan studi terbaru mengenai kondisi kerang hijau di perairan Teluk Jakarta.
Penelitian mengenai logam berat di perairan Teluk Jakarta telah dilakukan sejak tahun 1979 oleh Yatim et al. (1979) dan dilaporkan bahwa terjadi peningkatan kandungan logam berat baik dalam air, sedimen, dan biota hingga saat ini. Beberapa penelitian sebelumnya menunjukkan bahwa konsentrasi logam Pb dan Cu di air bervariasi antara <0.001-1.750 ppm. Diniah (1995) melaporkan bahwa kandungan Pb mencapai 1.320-1.750 ppm. Pada tahun 2000 dan 2001, kadar Pb berkisar antara 0.002-0.029 ppm (Tresnasari 2001) dan antara <0.001-0,001 ppm pada tahun 2002 (Akbar 2002). Pada tahun 2005, Siantiningsih melaporkan kandungan Pb berkisar antara 0.005 ppm dan Cu <0.001-0.002 ppm, kemudian tahun 2009 kandungan Pb berkisar antara 0.001-0.004 ppm (Prasetyo 2009) dan tahun 2011 dilaporkan konsentrasi Pb sebesar 0.005 ppm (Cordova et al. 2011). Selanjutnya, logam berat juga telah ditemukan pada berbagai organisme seperti ikan sokang dengan konsentrasi Pb sebesar 3.214-5.165 mg/kg (Bangun 2005) ; ikan barracuda dengan konsentrasi Pb pada daging sebesar 3.448 mg/kg (Khaisar 2006) ; mangrove dengan konsentrasi Cu sebesar 12.17-37.68 mg/kg dan Pb sebesar 20.98-68.78 mg/kg (Hamzah dan Setiawan 2010).
2
(Suryanto 2002). Selanjutnya pada kerang hijau berukuran < 4 cm hingga > 6 cm, konsentrasi Pb berkisar antara 12.135-47.813 mg/kg (Apriadi 2005), tahun 2009 berkisar antara 0.920-1.485 mg/kg (Prasetyo 2009) dan tahun 2011 berkisar antara 0.017-0.042 mg/kg (Cordova et al. 2011). Beberapa pengamatan tersebut menunjukkan adanya hubungan antara kadar logam berat dengan panjang cangkang kerang hijau. Hal ini bisa disebabkan oleh faktor biologis kerang hijau khususnya filtrasi dan metabolisme, sehingga semakin lama usia hidup kerang hijau menyebabkan logam berat yang terakumulasi dalam jaringan tubuhnya juga akan semakin tinggi.
Konsentrasi Pb dan Cu pada kerang hijau diukur dengan selang ukuran cangkang yang lebih beragam dengan harapan memperoleh data yang lebih detil dan akurat. Penelitian ini diharapkan dapat memberikan informasi terkini mengenai kondisi logam Pb dan Cu di sekitar perairan Teluk Jakarta yang bermanfaat bagi studi selanjutnya.
Tujuan Penelitian
Penelitian ini bertujuan untuk :
1. mengukur kondisi terkini logam berat yang terdeteksi di perairan dan dalam jaringan tubuh kerang hijau hasil budidaya di Muara Angke, Teluk Jakarta, 2. menduga korelasi antara konsentrasi logam berat dalam jaringan tubuh kerang
hijau dengan usia hidupnya dilihat dari ukuran cangkang, dan
3. menduga jumlah logam berat Pb dan Cu yang terakumulasi dalam kerang hijau dari hasil tangkapan per tahun.
METODE
Waktu dan Tempat
Penelitian ini dilakukan pada tanggal 22-23 Mei 2014 sebanyak 1 kali pengamatan. Contoh air dan kerang hijau diambil dari Muara Angke, Teluk Jakarta pada posisi 6° 3.01542’ LS dan 106° 44.01273’ BT (Gambar 1). Analisis kandungan Pb dan Cu pada contoh air dan kerang hijau dilakukan di Laboratorium Produktivitas Lingkungan, Departemen Manajemen Sumberdaya Perairan, Fakultas Perikanan dan Ilmu Kelautan, IPB.
Alat dan Bahan
Alat yang digunakan terdiri dari corong pemisah (250 ml), gelas ukur (500 ml), pipet (5 ml, 10 ml, dan 25 ml), labu semprot, botol polyetilen ukuran 250 ml dan 1000 ml, neraca analitik, gelas piala, pengering beku (freeze dryer), pompa vakum (vacuum pump), kotak pendingin, jangka sorong, dan Spektrofotometri Serapan Atom (AAS).
3 Ditiokarbamat (APDC), Metil Iso Butil Keton (MIBK), pekat, anhidrat, , Hidroksilamin-HCl, dan air jenuh MIBK. Preparasi contoh kerang hijau menggunakan pekat, HCl pekat, pekat, , air suling, dan larutan standar untuk logam Pb dan Cu.
Gambar 1 Lokasi penelitian dan pengambilan sampel air laut dan kerang hijau di Teluk Jakarta
Pengambilan Contoh Kerang Hijau dan Air Laut
Contoh biota kerang hijau diambil di bagan budidaya pada saat pemanenan dengan menggunakan perahu nelayan. Selanjutnya kerang hijau dimasukkan ke dalam karung dan diangkut ke daratan. Contoh kerang hijau diambil sebanyak 10-25 ekor setiap selang ukuran, dimasukkan ke wadah plastik dan kotak pendingin untuk pendistribusian menuju laboratorium.
Pengambilan contoh air dilakukan menggunakan water sampler dari bahan polyetilen. Sebelum digunakan, botol contoh terlebih dahulu direndam dengan larutan asam HClselama 24 jam, kemudian dibilas dan dicuci dengan aquades. Pengambilan contoh air dilakukan pada kedalaman ± 2 m di tepi bagan budidaya. Kemudian botol dibungkus plastik dan disimpan dalam kotak pendingin untuk mencegah kontaminasi logam selama pengangkutan ke laboratorium. Untuk memisahkan zat padat terlarut dan tersuspensi, contoh air disaring menggunakan kertas saring nucleopore 0,45 µm menggunakan vacuum pump (APHA 2012).
Analisis Laboratorium
Pengukuran Contoh Kerang Hijau
4
3.9-4.3 cm, 4.9-5.3 cm, 5.9-6.3 cm, 6.9-7.3 cm. Kemudian daging kerang hijau dipisahkan dari cangkangnya menggunakan pisau yang berbahan plastik. Hal ini bertujuan mencegah kontaminasi logam. Lalu berat basah kerang hijau ditimbang menggunakan neraca digital. Kerang hijau yang telah dipisah berdasarkan selang ukuran yang berbeda kemudian dimasukkan ke dalam plastik dan diberi label. Selanjutnya daging kerang hijau dikeringkan menggunakan freeze dryer.
Analisis contoh air
Sebanyak 250 ml contoh air disaring menggunakan vacuum pump melewati kertas saring 0.45 µm, kemudian dimasukkan ke dalam corong pemisah.
diteteskan hingga pH contoh air laut mencapai 3, yaitu pH optimum untuk melakukan pemisahan logam berat pada air laut sehingga logam terpisah dengan baik. Untuk melakukan ekstraksi, ditambahkan 2.5 ml APDC lalu dikocok selama kurang lebih 30 detik agar homogen. Larutan APDC berfungsi membentuk senyawa kompleks organik yang tidak larut dalam fasa air ketika logam berat dalam contoh air bersifat asam. Setelah itu larutan MIBK ditambahkan sebanyak 25 ml, dan dikocok kembali selama 30 detik. Contoh air tersebut didiamkan selama ± 60 menit hingga terbentuk dua lapisan; lapisan atas disebut fase air dan lapisan bawah disebut fase organik. Kemudian fase air dibuang dan fase organik ditampung dalam tabung reaksi untuk diukur menggunakan AAS/ICP yang memiliki deteksi limit 0.001 ppm menggunakan nyala api campuran asetilen (APHA 2012).
Analisis contoh kerang hijau
Contoh kerang dikeringkan menggunakan freeze dryer pada suhu -20 °C dengan metode sublimasi dalam kondisi vakum hingga daging kerang benar-benar kering. Daging kerang yang telah kering ditandai dengan bentuknya yang mudah hancur saat dipegang. Pengeringan pada suhu rendah bertujuan untuk menghindari penguapan logam berat dan menjaga daging kerang hijau dari kerusakan (Suryanto 2002). Kemudian contoh kerang dihaluskan menggunakan cawan porselen hingga berbentuk serbuk. Ditimbang 1 gram contoh menggunakan neraca analitik, lalu dimasukkan ke dalam gelas piala 100 ml, ditambahkan 5 ml seluruh material padat, cairan jernih, dan pada bagian dasar tersisa serbuk kuning sampai putih. Larutan dihomogenkan dan kembali dipanaskan di atas hotplate pada suhu 180 °C sampai uap hilang. Ketika volume larutan tersisa sekitar 1-2 ml, gelas piala diangkat dari hotplate kemudian didinginkan. Setelah itu larutan diencerkan menggunakan aquades sambil dibilas perlahan hingga volume 100 ml. Penyaringan menggunakan vacuum pump dilakukan agar sisa contoh yang kasar tidak ikut masuk ke dalam botol. Larutan siap untuk dianalisis dengan alat Spektrofotometrik Serapan Atom (AAS) (APHA 2012).
5 senyawa logam harus diubah menjadi bentuk atom dengan pembakaran pada suhu 2000° C (Akbar 2002). Untuk mendapatkan konsentrasi logam berat yang sebenarnya, dilakukan perhitungan menggunakan persamaan berikut (1).
K sebenarnya = K AAS x V penetapan ... (1) BK
Keterangan :
K sebenarnya : Konsentrasi logam berat sesungguhnya (mg/kg)
K AAS : Konsentrasi logam berat yang terbaca oleh AAS (ppm) V penetapan : Volume penetapan (ml)
BK : Berat kering kerang hijau yang digunakan untuk analisa (g)
Analisis Data
Kandungan Logam Berat dalam Air dan Kerang Hijau
Analisis data dilakukan dengan membandingkan konsentrasi logam Pb dan Cu yang terdeteksi dalam contoh air laut dan daging kerang hijau dengan penelitian-penelitian sebelumnya. Hal ini bertujuan mengetahui gambaran kondisi pencemaran oleh logam Pb dan Cu dalam kurun waktu beberapa tahun yang lalu hingga saat ini.
Korelasi Panjang Cangkang dan Kandungan Logam Berat
Untuk menguji keterkaitan antara hubungan variabel terikat (Y) yaitu konsentrasi logam berat Pb dan Cu (mg) yang terdeteksi dalam daging kerang hijau per satuan kilogram dengan variabel (X) yaitu ukuran kerang hijau digunakan analisis statistik linear satu variabel. Pola garis dihasilkan berdasarkan hubungan antara kedua variabel berupa diagram titik. Model persamaan regresi (2) yang digunakan sebagai berikut:
Y = b0 + b1 X ...... (2) Keterangan:
Y = Variabel terikat (logam berat dalam kerang hijau) X = Variabel bebas (ukuran cangkang kerang hijau) b0 = Nilai tengah/rataan umum
b1 = Koefisien regresi
Nilai koefisien korelasi (r) mendekati positif 1 menunjukkan hubungan antar variabel yang kuat, sedangkan nilai r mendekati 0 menunjukkan bahwa antar variabel memiliki hubungan yang sangat lemah bahkan mendekati tidak ada.
Pendugaan Berat Pb dan Cu dalam Kerang Hijau di Teluk Jakarta
6
persentase berat daging kerang hijau adalah sekitar 35% dari berat totalnya (Niswari 2004). Perhitungan dapat dilakukan menggunakan persamaan (3) berikut:
= Berat kerang hijau keseluruhan (g)
= Produksi kerang hijau dalam 1 tahun (ton)
Selanjutnya dilakukan pendugaan terhadap jumlah total logam berat yang terkandung dalam jumlah total hasil tangkapan kerang hijau dalam satu tahun
= Berat jaringan lunak total dari hasil tangkapan (kg)
HASIL DAN PEMBAHASAN
Logam Berat Pb dan Cu dalam Air
Logam Pb dan Cu yang terdeteksi dalam contoh air laut ditunjukkan pada Gambar 2 berikut ini,
7 Secara alami, kadar Pb dan Cu dalam air laut adalah sebesar 0.003 ppm dan 0.002 ppm (Lestari dan Edward 2004). Berdasarkan pengukuran, diperoleh konsentrasi Pb dan Cu pada contoh air laut masing-masing adalah 0.012 ± 0.001 ppm dan 0.005 ± 0.001 ppm (Lampiran 1). Sejak tahun 1979 hingga sekarang, konsentrasi logam Pb dan Cu dalam air laut di Teluk Jakarta sudah melebihi nilai normal yang berada di alam sehingga menunjukkan adanya penambahan zat Pb dan Cu dari luar lingkungan laut. Menurut (Prasetyo 2009) sumber pencemaran laut di Teluk Jakarta berasal dari limbah pabrik penghasil peralatan listrik, pabrik baterai, industri penghasil tinta, percetakan, dan limbah solar kapal di pelabuhan perikanan yang kemudian masuk melalui sungai yang bermuara ke perairan Teluk Jakarta. Sumber pencemar tersebut sangat berpotensi meningkatkan konsentrasi logam berat di sekitar perairan Teluk Jakarta.
Dibandingkan dengan penelitian sebelumnya yang dilakukan oleh Tresnasari (2001), Akbar (2002), Siantiningsih (2005), Prasetyo (2009), dan Cordova et al. (2011), konsentrasi Pb dan Cu pada penelitian ini secara umum mengalami kenaikan yang tidak terlalu signifikan. Meskipun demikian, belum dapat disimpulkan bahwa perairan Teluk Jakarta terbebas dari masukan logam berat dari luar lingkungan. Hamzah dan Setiawan (2010) menyebutkan bahwa pada umumnya konsentrasi Pb dan Cu di air memiliki nilai yang lebih rendah dikarenakan daya larutnya yang rendah. Hal tersebut didukung oleh Jalius et al. (2008) yang menyebutkan bahwa logam berat di air lebih cenderung terakumulasi di dasar perairan. Kondisi fisika perairan seperti arus akan berpengaruh besar dalam proses pengadukan maupun pengendapan partikel-partikel yang melayang di kolom perairan (Maslukah 2007). Oleh sebab itu, kadar logam berat terlarut dalam air laut yang terdeteksi dalam penelitian ini belum bisa menentukan kondisi pencemaran perairan yang sebenarnya.
Logam Berat Pb dan Cu dalam Kerang Hijau
8
Gambar3 Konsentrasi logam Pb (rata-rata ± standar deviasi) terlarut dalam kerang hijau (mg/kg) di Muara Angke, Teluk Jakarta
9
Gambar 4 Konsentrasi logam Cu (rata-rata ± standar deviasi) terlarut dalam kerang hijau (mg/kg) di Muara Angke, Teluk Jakarta
Konsentrasi logam Cu terendah terdeteksi pada kerang berukuran 2.9-3.3 cm yaitu 8.714 ± 1.59 mg/kg, dan tertinggi pada kerang berukuran 3.9-4.3 cm yaitu 12.206 ± 0.201 mg/kg. Kerang berukuran paling kecil mengandung logam Cu sebesar 9.14 ± 1.379 mg/kg, kemudian menurun pada kerang berukuran 2.9-3.3 cm dengan konsentrasi sebesar 8.714 ± 1.59 mg/kg. Konsentrasi Cu naik pada kerang ukuran 3.9-4.3 cm, yaitu 12.206 ± 0.201 mg/kg, lalu turun kembali pada ukuran 4.9-5.3 sebesar 8.924 ± 0.194 hingga ukuran 5.9-6.3 sebesar 8.753 ± 0.440, kemudian meningkat pada kerang berukuran terbesar yaitu 9.993 ± 0.787 mg/kg. Penelitian yang dilakukan sebelumnya oleh (Akbar 2002) dan (Suryanto 2002) mendeteksi keberadaan Cu dengan kadar lebih kecil dibandingkan pada penelitian saat ini yaitu hanya berkisar 0.005-0.012 mg/kg dan 0.004-0.007 mg/kg. Logam Cu merupakan salah satu elemen yang dibutuhkan dalam kehidupan organisme akuatik. Hasil penelitian Arifin dan Fadhlina (2009) menyebutkan bahwa pada daerah sekitar pantai hingga ± 5 km dari garis pantai, komponen logam Cu yang ditemukan masih tergolong tinggi, sehingga sangat berpotensi dikonsumsi oleh biota-biota akuatik termasuk kerang hijau.
Berdasarkan sifat logam berat yang sulit terlarut dan mudah berikatan dengan partikel, maka diduga logam berat yang masuk ke perairan cenderung berikatan dengan partikel-partikel tidak terlarut kemudian mengendap ke dasar perairan atau menjadi bahan makanan bagi fitoplankton dan kerang hijau. Unsur logam berat dapat masuk ke dalam tubuh organisme melalui rantai makanan, insang, dan difusi melalui permukaan kulit (Hutagalung 1991). Apriadi (2005) juga menyebutkan bahwa akumulasi logam berat dalam tubuh kerang hijau dipengaruhi oleh jumlah bahan pencemar dalam air, kemampuan biota dalam mengakumulasi, sifat biota seperti ukuran dan jenis, serta lamanya pernapasan.
10
Pada penelitian ini, konsentrasi logam berat yang terkandung dalam kerang hijau terlihat jauh lebih tinggi daripada yang terdeteksi di air. Hal tersebut dikarenakan kecenderungan kerang hijau untuk mengakumulasi logam berat dalam jaringan tubuhnya dapat terjadi dalam waktu yang lama. Dalam proses metabolisme, kerang hijau juga memiliki sistem penyerapan sari-sari makanan sehingga kemungkinan logam ikut terserap akan semakin besar. Logam berat yang tidak keluar dalam proses ekskresi biasanya akan tertinggal di dalam jaringan tubuh. Hal tersebut akan terjadi berulang-ulang selama masa hidupnya sehingga terjadi penumpukan yang menyebabkan kandungan logam berat dalam jaringan tubuhnya akan semakin tinggi. Dengan demikian, logam berat yang terakumulasi dalam jaringan tubuh kerang hijau dapat meningkat dan menurun seiring perkembangannya.
Korelasi Ukuran Cangkang dengan Konsentrasi Pb dan Cu dalam Kerang Hijau
Kerang hijau telah banyak digunakan sebagai indikator biologis dalam pemantauan pencemaran perairan karena organisme ini mudah diperoleh dalam jumlah yang banyak, memiliki ketahanan terhadap kondisi lingkungan tercemar, dan berusia panjang. Selain itu, sifat hidup kerang hijau yang menetap pada suatu tempat dalam waktu yang lama memungkinkan terjadinya akumulasi dalam jaringan tubuhnya sehingga timbul dugaan bahwa usia hidup kerang hijau berbanding lurus dengan jumlah logam yang terakumulasi dalam jaringan tubuhnya. Pada penelitian ini dilakukan pengamatan untuk menentukan korelasi usia hidup kerang hijau dilihat dari ukuran cangkang dengan konsentrasi logam Pb dan Cu yang terkandung dalam jaringan tubuhnya.
Berdasarkan perhitungan regresi-korelasi diperoleh koefisien korelasi r pada logam Pb adalah 0.458 atau mendekati 0 sehingga keterkaitan koefisien X dan Y cenderung lemah (Gambar 5). Hal tersebut menunjukkan korelasi negatif antara ukuran cangkang kerang hijau dengan konsentrasi Pb dalam jaringan tubuhnya.
Gambar 5 Grafik korelasi konsentrasi logam Pb (mg/kg) dan ukuran kerang (cm) 9.59
11
Cu rata-rata (mg/kg) Ulangan 1 (mg/kg) Ulangan 2 (mg/kg)
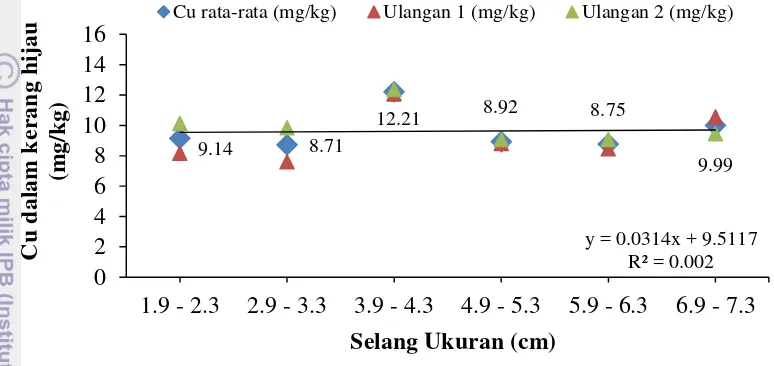
Uji regresi pada logam Cu juga menunjukkan hubungan yang lemah antara koefisien X dan Y dengan nilai r = 0.044, sehingga korelasi antara panjang cangkang dan konsentrasi logam Cu dalam daging kerang hijau bersifat negatif (Gambar 6). Hal ini diduga terjadi karena jumlah sampel kerang hijau yang digunakan hanya sedikit sehingga simpangan baku yang terbentuk cenderung lebih besar.
Gambar 6 Grafik korelasi konsentrasi logam Cu (mg/kg) dan ukuran kerang (cm) Pada Gambar 2 dan 3 terlihat bahwa kerang yang berukuran paling kecil memiliki konsentrasi logam yang tinggi, kemudian mengalami penurunan pada selang ukuran selanjutnya. Secara teoritis, semakin lama usia hidup kerang hijau akan menyebabkan kenaikan jumlah logam berat yang terakumulasi dalam jaringan tubuhnya. Penelitian yang telah dilakukan oleh Akbar (2002) dan Apriadi (2005) menunjukkan bahwa ukuran cangkang berkorelasi positif dengan konsentrasi logam berat yang terkandung dalam tubuh kerang hijau. (Fauziah et al. 2012) juga menyebutkan bahwa kerang berukuran kecil memiliki konsentrasi yang paling sedikit dan semakin meningkat hingga kerang berukuran paling besar.
12
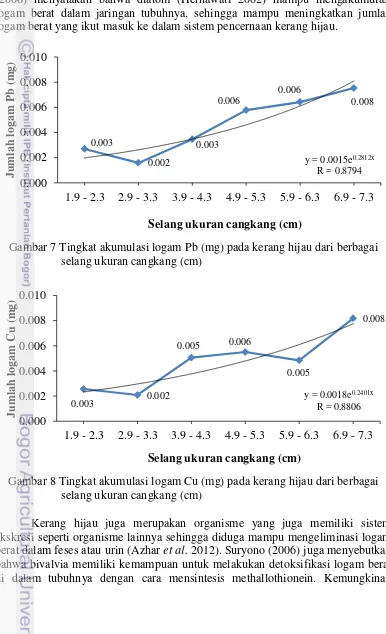
melalui rantai makanan. Pada pengamatan ini terlihat adanya akumulasi jumlah logam berat yang cenderung meningkat dari kerang hijau berukuran paling kecil hingga yang paling besar (Gambar 7 dan 8). Meskipun konsentrasi Pb dan Cu pada pengamatan ini menunjukkan kondisi yang relatif sama, namun akumulasi logam berat tetap terjadi seiring dengan besarnya ukuran cangkang. Suryono (2006) menyatakan bahwa diatom (Hernawati 2002) mampu mengakumulasi logam berat dalam jaringan tubuhnya, sehingga mampu meningkatkan jumlah logam berat yang ikut masuk ke dalam sistem pencernaan kerang hijau.
Gambar 7 Tingkat akumulasi logam Pb (mg) pada kerang hijau dari berbagai selang ukuran cangkang (cm)
Gambar 8 Tingkat akumulasi logam Cu (mg) pada kerang hijau dari berbagai selang ukuran cangkang (cm)
13 lainnya juga didukung oleh penelitian Niswari (2004) yang melihat adanya penyimpangan morfometrik pada kerang hijau di perairan Teluk Jakarta yang mengalami hambatan perkembangan gonad, diduga disebabkan oleh tingginya tekanan lingkungan sekitar khususnya keberadaan logam berat. Di samping itu, Mulyawan (2005) juga menemukan adanya fluktuasi kandungan logam berat pada selang ukuran yang berbeda. Penumpukan logam berat dalam jaringan tubuh kerang hijau terjadi dalam waktu yang lama sehingga dapat menyebabkan kerusakan fungsi organ-organ tertentu seperti hati, ginjal, insang, gonad, dan organ lainnya sehingga fluktuasi jumlah logam dalam tubuh kerang hijau merupakan suatu kewajaran yang mungkin terjadi. Dengan demikian, konsentrasi logam berat yang berfluktuasi di setiap selang ukuran diduga terjadi karena organisme tersebut telah melakukan ekskresi atau detoksifikasi logam berat di dalam tubuhnya saat pengambilan sampel, dan dapat disebabkan oleh kerusakan fungsi organ tubuh kerang hijau akibat terpapar logam berat berbahaya di perairan.
Pendugaan Berat Pb dan Cu dalam Kerang Hijau di Teluk Jakarta
Kegiatan budidaya kerang hijau saat ini cukup mengkhawatirkan karena limbah yang terus mencemari perairan Teluk Jakarta semakin banyak. Kasus kematian massal hasil tangkapan ikan, udang, kepiting, dan remis pada tahun 2006 membuktikan bahwa perairan Teluk Jakarta sudah mengalami penurunan kualitas (Hartanto 2007). Penurunan kualitas perairan ini berimplikasi pada hasil budidaya kerang hijau. Banyak penelitian juga membuktikan adanya kandungan logam yang terakumulasi dalam jaringan tubuh kerang.
Pada tahun 2000 hingga 2004, budidaya kerang hijau di Teluk Jakarta mencapai angka produksi 125.000 ton per tahunnya (Hartanto 2007), namun hasil penelusuran melalui website Kementerian Kelautan dan Perikanan, Suku Dinas Kelautan Muara Angke, dan konsultan yang bergerak di bidang kelautan dan perikanan tidak diperoleh data hasil tangkapan pada tahun 2005-2011. Pada tahun 2014 perkiraan dilakukan berdasarkan hasil wawancara dengan nelayan sekitar (Umar 22 Mei 2014, komunikasi pribadi) yang memberi keterangan bahwa dalam sebuah bagan mampu menghasilkan kerang hijau sebanyak kurang lebih 4-5 ton dalam sekali panen dan sekitar 10 ton dalam setahun. Jumlah bagan budidaya kerang hijau di Teluk Jakarta diperkirakan sebanyak 1,900 unit, sehingga diperkirakan jumlah kerang hasil budidaya di Teluk Jakarta sekitar 19,000 ton.
Dari data yang ada terlihat bahwa hampir semua kerang yang diukur tidak ada perbedaan konsentrasi, namun data yang digunakan untuk menduga jumlah logam dalam hasil tangkapan per tahun adalah konsentrasi pada kerang berukuran konsumsi (5.9-7.3 cm). Hal itu dikarenakan kerang hijau berukuran 5.9-7.3 cm merupakan hasil utama yang diperoleh saat panen. Berat total jaringan lunak dalam 19,000 ton hasil tangkapan kerang hijau adalah,
...... (3) = 35% x 19,000 ton
14
Berat total rata-rata logam Pb pada kerang ukuran konsumsi sebesar,
= x ...... (4) = (10.393 ± 5.701) mg/kg x 6,650,000 kg
= 69,113,450 ± 5.701 mg = 69.113 ± 5.701 kg
Berat total rata-rata logam Cu pada kerang ukuran konsumsi sebesar,
= x ...... (5) = (9.373 ± 0.613) mg/kg x 6,650,000 kg
= 62,330,450 ± 0.613 mg = 62.330 ± 0.613 kg
Hasil produksi kerang hijau di Teluk Jakarta dalam beberapa tahun terakhir dapat dilihat pada Gambar (9) berikut.
Gambar 9 Produksi kerang hijau di Teluk Jakarta pada kurun waktu tahun 2000-2014 (Sumber : Hartanto 2007)
Masa budidaya kerang hijau mengalami periode yang sangat baik pada tahun 2000-2004 dikarenakan kontribusi pemerintah dalam membina kelompok-kelompok nelayan sehingga pada masa tersebut produksi kerang hijau mencapai angka 125,000 ton per tahun. Tidak diperoleh data hasil tangkapan kerang di Teluk Jakarta pada tahun 2005-2011. Dari tahun 2012 hingga sekarang, data hasil tangkapan kerang hijau menunjukkan penurunan produksi yaitu 22,800 ton di tahun 2013. Jika diasumsikan bahwa berat total rata-rata logam berat dalam jaringan lunak kerang hijau hasil budidaya di Teluk Jakarta setiap tahunnya sama dengan berat yang terukur pada pengamatan ini, maka perkiraan jumlah logam Pb dan Cu dalam hasil tangkapan setiap tahun dapat dilihat pada Gambar 10.
15
Gambar 10 Pendugaan berat total logam Pb dan Cu dalam kerang hijau hasil tangkapan 2000-2014
Produksi kerang hijau tahun 2000-2004 di Teluk Jakarta jauh lebih tinggi dibandingkan beberapa tahun terakhir ini, sehingga perkiraan berat total logam Pb pada tahun tersebut berkisar antara 432.58-454.69 kg dan Cu antara 390.12-410.07 kg. Produksi kerang hijau menurun drastis tahun 2012-2014 karena lahan budidaya yang sudah semakin berkurang oleh kegiatan reklamasi, sehingga perkiraan berat total logam Pb berkisar antara 62.75-82.94 kg dan Cu berkisar antara 56.59-74.80 kg. Data ini menggambarkan bahwa dalam kurun waktu 3 tahun terakhir ini perairan Teluk Jakarta belum berhenti memperoleh masukan bahan pencemar logam berat.
KESIMPULAN
Konsentrasi rata-rata logam Pb terlarut pada air laut sebesar 0.012 ± 0.001 ppm dan Cu sebesar 0.005 ± 0.001 ppm, sedangkan Pb dalam daging kerang hijau berkisar antara 6.620 ± 2.72 mg/kg sampai 11.593 ± 5.58 mg/kg dan Cu berkisar antara 8.714 ± 1.59 mg/kg sampai 12.206 ± 0.201 mg/kg. Pada pengamatan ini menunjukkan bahwa ukuran cangkang kerang hijau berkorelasi negatif dengan konsentrasi logam Pb dan Cu yang terakumulasi dalam jaringan tubuhnya. Perkiraan berat total logam Pb dalam hasil tangkapan kerang hijau pada tahun 2014 sebesar 69.113 ± 5.701 kg dan Cu sebesar 62.330 ± 0.613 kg. Hal ini mengindikasikan bahwa kontaminasi logam berat di perairan Teluk Jakarta khususnya Muara Angke masih berlangsung hingga saat ini.
DAFTAR PUSTAKA
Akbar 2002. Pendugaan Tingkat Akumulasi Logam Berat Pb, Cd, Cu, Zn, dan Ni pada Kerang Hijau (Perna viridis) Ukuran <5 cm di Perairan Kamal Muara, Teluk Jakarta [skripsi]. Bogor (ID): Institut Pertanian Bogor.
16
[APHA] American Public Health Association. 2012. Standard Method for The Examination of Water and Wastewater. 22th edition. Washington, 3111 b. Apriadi 2005. Kandungan Logam Berat Hg, Pb, dan Cr pada Air, Sedimen, dan
Kerang Hijau (Perna viridis) di Perairan Kamal Muara, Teluk Jakarta [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Arifin Z, Fadhlina D. 2009. Fraksinasi Logam Berat Pb, Cd, Cu, dan Zn dalam Sedimen dan Bioavailabilitasnya bagi Biota di Perairan Teluk Jakarta. Ilmu Kelautan. 14(1):27-32.
Azhar H, Widowati I, Suprijanto J. 2012. Studi Kandungan Logam Berat Pb, Cu, Cd, Cr pada Kerang Simping (Amusium pleuronectes), Air dan Sedimen di Perairan Wedung, Demak Serta Analisis Maximum Tolerable Intake pada Manusia. Journal of Marine Research. 1(2):35-44.
Bangun JM. 2005. Kandungan Logam Berat Pb dan Cd dalam Air, Sedimen, dan Organ Tubuh Ikan Sokang (Triachantus nieuhofi) di Perairan Ancol, Teluk Jakarta [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Cordova MR, Zamani NP, Yulianda F. 2011. Akumulasi Logam Berat pada Kerang Hijau (Perna viridis) di Perairan Teluk Jakarta. Jurnal Moluska Indonesia. 2(1):1-8
Diniah 1995. Korelasi Antara Kandungan Logam Berat Hg, Cd, dan Pb Pada Beberapa Ikan Konsumsi dengan Tingkat Pencemaran di Perairan Teluk Jakarta [tesis]. Bogor (ID): Institut Pertanian Bogor.
Fauziah AR, Rahardja BS, Cahyoko Y. 2012. Korelasi Ukuran Kerang Darah (Anadara granosa) dengan Konsentrasi Logam Berat Merkuri (Hg) di Muara Sungai Ketingan, Sidoarjo, Jawa Timur. Journal of Marine and Coastal Science. 1(1):34-44.
Hamzah F, Setiawan A. 2010. Akumulasi Logam Berat Pb, Cu, dan Zn di Hutan Mangrove Muara Angke, Jakarta Utara. Jurnal Ilmu dan Teknologi Kelautan Tropis. 2(2):41-52.
Hartanto 2007. Analisis Biaya Manfaat Lokasi Budidaya Kerang Hijau (Mytilus viridis) di Perairan Teluk Jakarta [skripsi]. Bogor (ID): Institut Pertanian Pencemaran Laut di Indonesia dan Teknik Pemantauannya. Jakarta (ID): P3O LIPI.
Jalius, Setiyanto DD, Sumantadinata K, Riani E, Ernawati Y. 2008. Akumulasi Logam Berat dan Pengaruhnya terhadap Spermatogenesis Kerang Hijau (Perna viridis). Jurnal Ilmu-Ilmu Perairan dan Perikanan Indonesia. 15(1):77-83.
Khaisar O. 2006. Kandungan Timah Hitam (Pb) dan Kadmium (Cd) dalam Air, Sedimen, dan Bioakumulasi serta Respon Hitopatologis Organ Ikan Alu-Alu (Sphyraena barracuda) di Perairan Teluk Jakarta [skripsi]. Bogor (ID): Institut Pertanian Bogor.
17 Liliandari P, Aunurohim. 2013. Kecepatan Filtrasi Kerang Hijau (Perna viridis) Terhadap Chaetoceros sp. dalam Media Logam Tercemar Kadmium, Surabaya. Jurnal Sains dan Seni Pomits. 2(2):149-154.
Maslukah L. 2007. Konsentrasi Logam Berat (Pb, Cd, Cu, Zn) Terlarut dalam Seston dan dalam Sedimen di Estuari Banjir Kanal Barat, Semarang. Jurnal Sumberdaya Perairan. 2(1):1-4.
Mulyawan I. 2005. Korelasi Kandungan Logam Berat Hg, Pb, Cd, dan Cr pada Air Laut, Sedimen, dan Kerang Hijau (Perna viridis) di Perairan Kamal Muara, Teluk Jakarta [tesis]. Bogor (ID): Institut Pertanian Bogor.
Niswari AP. 2004. Studi Morfometrik Kerang Hijau (Perna viridis) di Perairan Cilincing, Jakarta Utara [skripsi]. Bogor (ID): Institut Pertanian Bogor. Prasetyo AD. 2009. Penentuan Kandungan Logam (Hg, Pb, dan Cd) Dengan
Penambahan Bahan Pengawet dan Waktu Perendaman yang Berbeda pada Kerang Hijau (Perna viridis) di Perairan Muara Kamal, Teluk Jakarta [skripsi]. Jakarta (ID): Universitas Islam Negeri Syarif Hidayatullah.
Primaharinastiti R, Poernomo AT dan Erma N. 2004. Bioakumulasi Logam Berat Cu oleh Bacillus sp. Berk. Penel. Hayati. 10:19-23.
Ratnawati E dan Sunarko. 2008. Penentuan Kandungan Logam pada Kerang Hijau Dengan Metode Analisis Aktivasi Neutron Komparatif. Prosiding Seminar Nasional Penelitian dan Pengelolaan Perangkat Nuklir; 2008 Agustus 28; Yogyakarta, Indonesia. Yogyakarta (ID): Pusat Teknologi Akselerator dan Proses Bahan. hlm 146-151.
Rudiyanti S. 2009. Biokonsentrasi Kerang Darah (Anadara granosa) Terhadap Logam Berat Cd yang Terkandung dalam Media Pemeliharaan yang Berasal dari Perairan Kaliwungu, Kendal. Seminar Nasional Semarang Perikanan Expo; 2009; Semarang (ID): Universitas Diponegoro. hlm 184-195.
Sachoemar SI dan Wahjono HD. 2007. Kondisi Pencemaran Lingkungan Perairan di Teluk Jakarta. Jurnal Akuakultur Indonesia. 3(1):1-14.
Setyono DED. 2006. Karakteristik Biologi dan Produk Kekerangan Laut. Oseana. 31(1):1-7.
Siantiningsih A. 2005. Pendugaan Sebaran Spasial Logam Berat Pb, Cd, Cu, Zn, dan Ni dalam Air dan Sedimen di Perairan Teluk Jakarta. [skripsi]. Bogor(ID): Institut Pertanian Bogor.
Sitorus H. 2011. Analisis Beberapa Parameter Lingkungan Perairan yang Mempengaruhi Akumulasi Logam Berat Timbal dalam Tubuh Kerang Darah di Perairan Pesisir Timur Sumatera Utara. VISI. 19(1):374-385. Sudarmadji, Mukono J dan IP Corie. 2006. Toksikologi Logam Berat B3 dan
Dampaknya Terhadap Kesehatan. Jurnal Kesehatan Lingkungan. 2(2):129-142.
Suryanto D. 2002. Pendugaan Laju Akumulasi Pb, Cd, Cu, Zn, dan Ni pada Kerang Hijau (Perna viridis) Ukuran Lebih dari 4.7 cm di Perairan Kamal Muara, Teluk Jakarta [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Suryono CA. 2006. Bioakumulasi Logam Berat Melalui Sistem Jaringan Makanan dan Lingkungan pada Kerang Bulu Anadara inflata. Ilmu Kelautan. 11(1):19-22.
18
Indonesia. Yogyakarta (ID): Pusat Teknologi Akselerator dan Proses Bahan. hlm 167-174.
Tresnasari SW. 2001. Kandungan Logam Berat Pb dan Cd pada Kerang Hijau (Perna viridis), Air dan Sedimen di Perairan Muara Kamal, Teluk Jakarta [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Widaningrum, Miskiyah dan Suismono 2007. Bahaya Kontaminasi Logam Berat dalam Sayuran dan Alternatif Pencegahan Cemarannya. Buletin Teknologi Pascapanen Pertanian. 3:16-27.
Winarno EK, Andayani W, Sumartono A. 2009. Metil Merkuri dalam Kerang Hijau (Mytilus viridis) dari Pasar Pelelangan Ikan Muara Angke: Sebelum dan Setelah Pemasakan. Indo. J. Chem. 9(1): 77-83.
Yatim S, Surtipanti, Suwirma, Lubis E. 1979. Distribusi Logam Berat dalam Air Permukaan Teluk Jakarta. Majalah Batan. 12:1-19.
LAMPIRAN
Lampiran 1 Kandungan logam berat Pb dan Cu pada air laut (ppm)
Logam
Lampiran 2 Kandungan logam Pb pada kerang hijau (mg/kg)
Ukuran
Lampiran 3 Kandungan logam Cu pada kerang hijau (mg/kg)
19 Lampiran 4 Dokumentasi kegiatan penelitian
Bagan budidaya kerang hijau Pengambilan sampel air laut
Pengukuran sampel kerang hijau Pemisahan daging dengan cangkang
Penyaringan sampel air laut Pemanasan sampel
20