DENGAN PENAMBAHAN BAHAN PENGAWET
DAN WAKTU PERENDAMAN YANG BERBEDA
PADA KERANG HIJAU (
Perna viridis
L.)
DI PERAIRAN MUARA KAMAL, TELUK JAKARTA
ALFIAN DWI PRASETYO
PROGRAM STUDI BIOLOGI
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
JAKARTA
PADA KERANG HIJAU (
Perna viridis
L.)
DI PERAIRAN MUARA KAMAL, TELUK JAKARTA
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains Pada Program Studi Biologi Fakultas Sains dan Teknologi
Universitas Islam Negeri Syarif Hidayatullah Jakarta
ALFIAN DWI PRASETYO
104095003046
DENGAN PENAMBAHAN BAHAN PENGAWET
DAN WAKTU PERENDAMAN YANG BERBEDA
PADA KERANG HIJAU (
Perna viridis
L.)
DI PERAIRAN MUARA KAMAL, TELUK JAKARTA
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains Pada Program Studi Biologi Fakultas Sains dan Teknologi
Universitas Islam Negeri Syarif Hidayatullah Jakarta
ALFIAN DWI PRASETYO 104095003046
Menyetujui:
Pembimbing I, Pembimbing II,
DR. Lily Surayya Eka Putri, M.Env. Stud. Zainal Arifin, Ph.D NIP. 150 375 182 NIP. 320 005 012
Mengetahui:
Ketua Program Studi Biologi
PENAMBAHAN BAHAN PENGAWET DAN WAKTU PERENDAMAN YANG BERBEDA PADA KERANG HIJAU (Perna viridis L.)
DI PERAIRAN MUARA KAMAL, TELUK JAKARTA
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains Pada Program Studi Biologi Fakultas Sains dan Teknologi
Universitas Islam Negeri Syarif Hidayatullah Jakarta
ALFIAN DWI PRASETYO 104095003046
Menyetujui,
Pembimbing I Pembimbing II
DR. Lily Surayya Eka Putri, M.Env. Stud. Zainal Arifin, Ph.D
NIP. 150 375 182 NIP. 320 005 012
Mengetahui,
Skripsi Berjudul “Penentuan Kandungan Logam (Hg, Pb dan Cd) dengan Penambahan Bahan Pengawet dan Waktu Perendaman yang Berbeda pada Kerang Hijau (Perna viridis L.) di Perairan Muara Kamal, Teluk Jakarta” yang ditulis oleh Alfian Dwi Prasetyo, NIM 104095003046 telah diuji dan dinyatakan LULUS dalam sidang Munaqosah Fakultas Sains dan Teknologi Universitas Islam Negeri Syarif Hidayatullah Jakarta pada tanggal 19 Juni 2009. Skripsi ini telah diterima sebagai salah satu syarat untuk memperoleh gelar Sarjana Strata Satu (S1) Program Studi Biologi.
Menyetujui
Penguji I, Penguji II,
Dra. Nani Radiastuti, M.Si Fahma Wijayanti, M.Si
NIP. 150 318 610 NIP. 150 326 910
Pembimbing I, Pembimbing II,
DR. Lily Surayya Eka Putri, M.Env. Stud. Zainal Arifin, Ph.D NIP. 150 375 182 NIP. 320 005 012
Mengetahui:
Dekan Ketua Program Studi Biologi
Fakultas Sains dan Teknologi
ATAU LEMBAGA MANAPUN.
“Dengan Bacalah “Tel kare mer mereka “Tia pula) Sesun Kupersem A nama Alla h dengan m
lah nampak ena perbua reka sebah a kembali ada suatu pada dir kitab (la ngguhnya y mbahkan Un Adikku yan
ah yang m menyebut k kerusak atan manu hagian da (ke jala bencanap rimu send auhul Mah yang demi ntuk Ayah ng selalu maha penga nama tuha tuhan
an di dar sia, supa ri (akiba n yang be
un yang m iri melai fuzh) seb kian itu dan Ummi menyayan asih, lagi anmu yang nmulah yan
rat dan di aya Allah at) perbua enar).” (Q menimpa di inkan tela belum Kami adalah mu (Q.S i Tercinta ngi dan me
i Maha pe mencipta ng Maha p
i laut di merasaka atan mere Q.S.Ar–Ru
i bumi da ah tertul i mencipt udah bagi S. Al-Had
a serta K encintai nyayang. kan, dan emurah”. sebabkan n kepada ka, agar um : 41)
n (tidak is dalam akannya. Allah.” id : 22)
Dibimbing oleh LILY SURAYYA EKA PUTRI dan ZAINAL ARIFIN.
Penelitian untuk mengetahui konsentrasi dan waktu perendaman formalin, rhodamin B dan metanil yellow yang dapat mempengaruhi kenaikan kandungan logam Hg, Pb dan Cd pada kerang hijau (Perna viridis L.) dan mengetahui konsentrasi dan waktu perendaman Na2CaEDTA yang dapat menurunkan
kandungan logam Hg, Pb dan Cd pada kerang hijau (Perna viridis L.) telah dilakukan di Laboratorium Ekologi dan Lingkungan Pusat Laboratorium Terpadu Universitas Islam Negeri Syarif Hidayatullah Jakarta dari bulan Februari sampai dengan April 2009. Rancangan percobaan yang digunakan adalah Rancangan Acak Kelompok (RAK) pola faktorial 3 x 3 dengan tiga ulangan. Faktor pertama adalah konsentrasi beda pengawet yang terdiri atas tiga taraf yaitu: tanpa bahan pengawet (p0), konsentrasi 5 % (p1) dan konsentrasi 10 % (p2). Faktor kedua
adalah waktu perendaman terdiri atas tiga taraf yaitu : 30 menit (t1), 45 menit (t2)
dan 60 menit (t3). Pengamatan meliputi kandungan awal logam Hg, Pb dan Cd
pada tubuh kerang hijau maupun di perairan dan penurunan kandungan Hg, Pb dan Cd setelah perlakuan. Hasil penelitian menunjukkan bahwa analisis AAS (Atomic Absorption Spectophotometry) menunjukkan bahwa rata-rata kandungan awal logam Hg pada tubuh kerang hijau sebesar 0,005 ppm, rata-rata kandungan awal logam Cd sebesar 0,6292 ppm dan rata-rata kandungan logam Pb sebesar 1,258 ppm. Kandungan logam Hg, Pb dan Cd tersebut masih di bawah baku mutu menurut WHO dan Dirjen POM No. 03725/B/SK/VII/1989 yaitu 0,5 ppm untuk Hg, 1 ppm untuk Cd dan 2 ppm untuk Pb. Hasil penelitian menunjukkan bahwa perlakuan perendaman pada konsentrasi Na2CaEDTA 0,5 % selama 60 menit
dapat menurunkan kadar Hg sebanyak 99,98 % dan konsentrasi Na2CaEDTA 1,0
% selama 60 menit menurunkan kadar Pb sebanyak 99,92 %. Berdasarkan analisis sidik ragam menunjukkan bahwa tidak ada interaksi antara konsentrasi Na2CaEDTA dengan waktu perendaman yang dapat menurunkan kadar Hg, Cd
dan Pb secara bersamaan pada tubuh kerang hijau.
ALFIAN DWI PRASETYO. Determination of Heavy Metals Contents (Hg, Pb and Cd) with Preservative Addition and Different Soaking Time at Green Mussel (Perna viridis L.) in Estuary Kamal Waters, Jakarta Bay. Advisor : LILY SURAYYA EKA PUTRI and ZAINAL ARIFIN.
The research was conducted to find out the concentration of Formalin, Rhodamin B and Metanil Yellow and soaking time to increase the content of Hg, Pb and Cd in green mussel (Perna viridis L.) and to find out the concentration of Na2CaEDTA and soaking time to decrease the content of Hg, Pb and Cd in green
mussel (Perna viridis L.). These research was carried out in Ecology and Environment Laboratory Center Inwrought Laboratory “State Islamic University Syarif Hidayatullah of Jakarta, from February to April 2009. The experimental design was 3 x 3 factorial Randomized Complete Block Design with three replications. The first factor was different preservative concentration with three levels i.e. without preservative (p0), concentration 0.5 % (p1) and concentration
1.0 % (p2). The second factor was soaking time with three levels i.e. 30 minutes
(t1), 45 minutes (t2) and 60 minutes (t3). The observation included the initial
content of Hg, Pb and Cd in green mussel and also in territorial water and decreasing of Hg, Pb and Cd after treatments. Atomic Absorption Spectophotometry (AAS) analysis indicated that the content of Hg in green mussel was 0.005 ppm, the content of Cd was 0.6292 ppm and the content of Pb was 1.258 ppm, lower than standard 0.5 ppm of Hg, 1 ppm of Cd and 2 ppm of Pb recommended by WHO and “Kep. Dirjen POM No. 03725/B/SK/VII/1989”. The result showed that concentration of Na2CaEDTA 0.5 % during 60 minutes
decreased 99.98 % of Hg and Na2CaEDTA 1.0 % during 60 minutes decreased
99.92 % of Pb. Based on analysis of variance showed that there is no interaction between Na2CaEDTA concentration with soaking time in decreasing the content
of Hg, Cd and Pb together in green mussel.
Key words : Heavy Metal Hg, Pb and Pb – Formalin, Rhodamin B, Metanil Yellow, Na2CaEDTA – Concentration and Soaking Time
KATA PENGANTAR
Bismillahirrahmanirrahim…
Alhamdulillah segala puji syukur kepada Allah SWT Tuhan semesta alam.
Sembah sujud tiada terkatakan atas segala limpahan rahmat, karunia dan inayah-Nya
yang telah dilimpahkan kepada penulis sehingga penulis dapat menyelesaikan
penulisan Skripsi ini. Lantunan shalawat serta salam semoga senantiasa tercurahkan
kepada idola umat Islam dan pembela kebenaran sejati, yaitu Baginda Nabi Besar
Muhammad SAW. Adapun Skripsi ini berjudul : “PENENTUAN KANDUNGAN
LOGAM (Hg, Pb dan Cd) DENGAN PENAMBAHAN BAHAN PENGAWET
DAN WAKTU PERENDAMAN YANG BERBEDA PADA KERANG HIJAU
(
Perna viridis
L.) DI PERAIRAN MUARA KAMAL, TELUK JAKARTA”
disusun sebagai salah satu syarat untuk menyelesaikan pendidikan jenjang strata satu
(S-1) pada Program Studi Biologi Fakultas Sains dan Teknologi Universitas Islam
Negeri (UIN) Syarif Hidayatullah Jakarta.
Dengan penuh rasa kesadaran, penulis mengakui bahwa penulisan Skripsi ini
tidak akan terselesaikan tanpa uluran tangan ikhlas dari berbagai pihak yang tidak
dapat penulis membalas pengorbanan semuanya. Pada kesempatan inilah penulis
ingin mengucapkan banyak terima kasih yang tak terhingga kepada semua pihak yang
1.
Kepada keluargaku tercinta yang selalu memberikan bantuan moril maupun
materiil dengan penuh keikhlasan hati, kedua orang tuaku (Alm. Ayahanda H.
Agus Salim & Ibunda Rusmini) serta saudara/i saya (Kakak Evadiah & Adik
Andi Subchan Jaya) atas dukungan dan do’a dari kalian semua.
2.
Ibu DR. Lily Surayya Eka Putri, M. Env. Stud.
sebagai Ketua Program StudiBiologi selaku pembimbing I dan Bapak
Zainal Arifin, Ph.D
sebagaiKepala Bidang
Dinamika Laut Puslit Oseanografi LIPI selaku
pembimbing II yang telahmemberikan bimbingan, meluangkan waktu, pikiran, kesabaran, saran dan kritik
untuk berdiskusi dengan penulis sehingga membantu dalam proses penyusunan
skripsi ini.
3.
DR. Syopiansyah Jaya Putra, M.Sis selaku Dekan Fakultas Sains dan Teknologibeserta jajarannya yang telah membantu penulis selama melaksanakan studi di
Fakultas Sains dan Teknologi.
4.
Ketua Program Studi Biologi Ibu DR. Lily Surayya Eka Putri, M. Env. Stud. yangturutserta memberikan dukungan dalam menyelesaikan skripsi ini.
5.
Ibu Nani Radiastuti, M.Si selaku Dosen Penasehat Akademis yang telahmemberikansaran dan solusi atas perkuliahan.
6.
Untuk para pengajar terutama para dosen-dosen Program Studi Biologi MIPA
Fakultas Sains dan Teknologi yaitu Ibu Nani Radiastuti, M.Si; Ibu Megga
Ratnasari Pikoli, M.Si; Ibu Fahma Wijayanti, M.Si; Ibu Dasumiati, M.Si; Ibu
Priyanti, M.Si; Ibu Deni Zulfiana, M.Si, Ibu Narti Fitriana, M.Si; Ibu Reno Fitri,
7.
Ibu Nurhasni, M.Si dan Bapak Drs. Paskal Sukandar, M.Si selaku penguji seminarproposal dan seminar hasil.
8.
Ibu Nani Radiastuti, M.Si dan Ibu Fahma Wijayanti, M.Si selaku penguji sidangmunaqosah (skripsi).
9.
Laboran Laboratorium Biologi (Mba Siti Nurdiana, Ka Syaiful Bahri, Mba PujiAstuti dan MbaFarida Ahmad) yang telah memberikan bantuan kepada penulis.
10.
Untuk Ridho S.Si, Fachruroji, Achmad Junaidi S.Si, Rasyidawati S.Si, Teguh
Hadi Wibowo S.Si, Mutiara Ramasenjawati Dwi Gustini S.Si, Din Fitri
Rochmawati S.Si dan Choirul Basyar dari FST-UIN Program Studi Biologi
selaku teman yang selama ini telah bekerja sama dalam pelaksanaan kegiatan
sampling air laut dan kerang hijau di Teluk Jakarta.
11.
Untuk Akhmad Taufiq Maulana, Aminullah, Eko Prasetyo S.Si, Fahmi Rizaldi,
Nasrulloh, Susfa Atmarwa Yahya, Arkanza Dewi Ranni S.Si, Cut Dhien Keumala
Meutia S.Si, Fitri Maimunah S.Si, Fitriyah S.Si, Khayu Wahyunita S.Si, Khoirul
Bariyah, Mawarsih, Miniarti, Neni Nuraeni S.Si, Novi Prasetyowati S.Si, Ofi
Ihsan Karya ‘Arofi S.Si, Sarah Marselia S.Si, Sofiah Rohmat, Suci Kartika Wati
S.Si, Suryani Eva S.Si dan Zulfana S.Si dari FST-UIN Program Studi Biologi
selaku teman-teman Biologi Angkatan 2004 yang telah begitu banyak
memberikan inspirasi baik secara langsung ataupun tidak langsung, terima kasih
12.
Kepada sponsorship foto copy “Ridho” & “Office Boy” (Mas Purwanto
”Darsono”) terima kasih atas perbanyakan copyright skripsi saya menjadi
beberapa eksemplar.
Dengan segala kerendahan hati penulis menyadari bahwa skripsi ini masih banyak kekurangan dan masih jauh dari kesempurnaan, oleh karena itu penulis sangat mengharapkan adanya kritik dan saran yang sifatnya membangun untuk ke arah perbaikan. Semoga skripsi ini dapat bermanfaat bagi penulis dan pembaca semua. Semoga Allah SWT selalu membimbing kita bersama dalam mendalami ilmu-ilmunya.
Jakarta, Juni 2009
DAFTAR ISI
Halaman
KATA PENGANTAR ...
i
DAFTAR ISI ...
v
DAFTAR GAMBAR ...
vii
DAFTAR TABEL ...
viii
DAFTAR LAMPIRAN ...
ix
BAB I PENDAHULUAN
1.1. Latar Belakang ...
1
1.2. Perumusan Masalah ...
4
1.3. Hipotesis ...
4
1.4. Tujuan Penelitian ...
4
1.5. Manfaat Penelitian ...
5
1.6. Kerangka Berpikir ...
6
BAB II TINJAUAN PUSTAKA
2.1. Pencemaran Laut ...
7
2.2. Logam Berat ...
8
2.2.1. Pencemaran Logam Berat ...
9
2.2.2. Sumber dan Bentuk Logam Berat ...
10
2.2.3. Sifat Fisik dan Kimia Beberapa Logam Berat ...
12
2.3. Kerang Hijau (Perna viridis L.) ...
14
2.4. Formalin, Rhodamin B dan Metanil Yellow ...
18
2.5. EDTA (Etilene Diamine Tetra-acetate Acid) ...
21
2.6. Hubungan Kerang Hijau dengan Logam Berat ...
23
2.7. Keadaan Umum Perairan Teluk Jakarta ...
25
3.4.1. Pengambilan Sampel Air Laut ...
29
3.4.2. Pengambilan Sampel Kerang Hijau (Perna viridis L.) ...
30
3.4.3. Pengukuran Logam Berat pada Sampel Air Laut ...
31
3.4.4. Pengukuran Logam Berat pada Sampel Kerang Hijau ...
32
3.4.5. Pembuatan Deret Standar Logam Berat Biota Laut ...
34
3.4.6. Perhitungan Kadar Logam Berat ...
35
3.4. Analisis Data ...
35
BAB IV HASIL DAN PEMBAHASAN
4.1. Parameter Lingkungan (Fisika dan Kimia) ...
37
4.2. Kandungan Logam Berat Hg, Pb dan Cd dalam Air Laut ...
42
4.3. Kandungan Logam Berat pada Kerang Hijau Pra Perlakuan ...
44
4.4. Kandungan Logam Berat pada Kerang Hijau Pasca Perlakuan ....
47
4.5. Penurunan Kandungan Logam Berat dengan Na
2CaEDTA ...
55
4.6. Faktor Konsentrasi ...
58
4.7. Hubungan Parameter dengan Kandungan Logam Kerang ...
62
BAB V KESIMPULAN DAN SARAN
5.1. Kesimpulan ...
66
5.2. Saran ...
66
DAFTAR PUSTAKA ...
67
DAFTAR GAMBAR
Halaman
Gambar 1. Proses Transport Logam Berat di Perairan ...
11
Gambar 2. Kerang Hijau (Perna viridis L.) ...
16
Gambar 3. Struktur EDTA dalam Mengikat Ion Logam ...
23
Gambar 4. Peta Lokasi Sampling ...
27
Gambar 5. Suhu Perairan Muara Kamal ...
38
Gambar 6. Kekeruhan Perairan Muara Kamal ...
39
Gambar 7. pH Perairan Muara Kamal ...
40
Gambar 8. Salinitas Perairan Muara Kamal ...
41
Gambar 9. Kandungan Logam Berat Air Laut ...
43
Gambar 10. Kandungan Awal Logam Berat Kerang Hijau ...
45
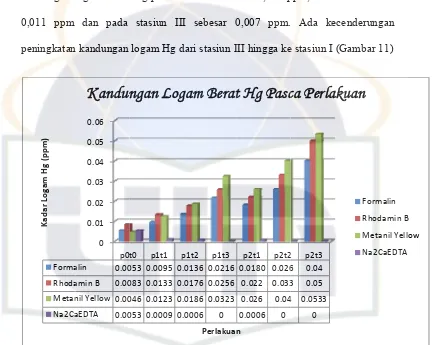
Gambar 11. Kandungan Logam Hg Pasca Perlakuan ...
48
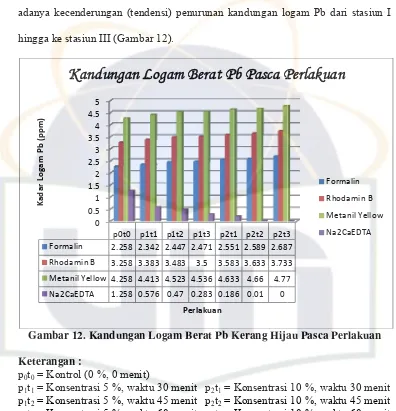
Gambar 12. Kandungan Logam Pb Pasca Perlakuan ...
50
Gambar 13. Kandungan Logam Cd Pasca Perlakuan ...
52
Gambar 14. Persentase Penurunan Kadar Logam Kerang Hijau ...
56
Gambar 15. Faktor Konsentrasi Logam Hg pada Kerang Hijau ...
59
Gambar 16. Faktor Konsentrasi Logam Pb pada Kerang Hijau...
60
DAFTAR TABEL
[image:17.612.114.525.119.550.2]Halaman
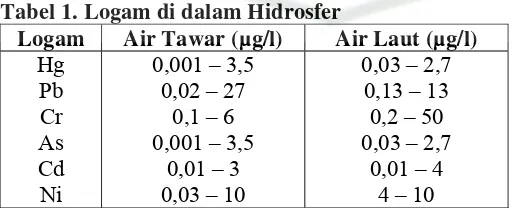
Tabel 1. Logam di dalam Hidrosfer ...
8
Tabel 2. Parameter Kualitas Air dan Biota Air yang Diamati ...
31
Tabel 3. Hasil Analisis PCA untuk Logam Hg ...
62
Tabel 4. Hasil Analisis PCA untuk Logam Pb ...
62
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Parameter Lingkungan Muara Kamal Februari – April 2009 ...
75
Lampiran 2. Kandungan Logam di Perairan Muara Kamal Feb – Apr 2009 ....
76
Lampiran 3. Kandungan Awal Logam Hg, Pb dan Cd Kerang Hijau ...
76
Lampiran 4. Rata-Rata Kadar Hg pada Konsentrasi Na
2CaEDTA Berbeda ...
77
Lampiran 5. Rata-Rata Kadar Pb pada Konsentrasi Na
2CaEDTA Berbeda ...
77
Lampiran 6. Rata-Rata Kadar Cd pada Konsentrasi Na
2CaEDTA Berbeda ...
77
Lampiran 7. Lokasi Titik Pengambilan Sampel Air & Kerang Hijau ...
78
Lampiran 8. Sampel Air Laut Murni & Air Laut + HNO
3Pekat ...
79
Lampiran 9. Perlakuan Basah & Kering Sampel Kerang Hijau ...
80
Lampiran 10. Siklus Proses Budidaya Kerang Hijau ...
81
Lampiran 11. Peralatan Kegiatan Sampling & Analisis Logam ...
82
Lampiran 12. Kriteria Kualitas Air yang Baik Untuk Perikanan ...
83
Lampiran 13. Kriteria Standar Kualitas Air Limbah ...
84
BAB I PENDAHULUAN
1.1. Latar Belakang
Kerang hijau (Perna viridis L.) merupakan salah satu komoditi perikanan
yang telah lama dibudidayakan sebagai salah satu usaha sampingan masyarakat
pesisir. Teknik budidayanya mudah dikerjakan, tidak memerlukan modal yang
besar dan dapat dipanen setelah berumur 6 – 7 bulan. Hasil panen kerang hijau per
hektar per tahun dapat mencapai 200 – 300 ton kerang utuh atau sekitar 60 – 100
ton daging kerang (Porsepwandi, 1998). Oleh karena kerang hijau bersifat filter
feeder non selective dan sessile (menetap) maka kandungan logam berat relatif
cukup tinggi ditemukan dalam tubuhnya karena adanya akumulasi logam berat
tersebut. Kerang genus Perna ini sering disebut highly specialized filter feeder dan
digunakan sebagai bioindikator pencemaran perairan karena biota ini bersifat
menetap, penyebarannya luas, masih mampu hidup pada daerah tercemar, dapat
mengakumulasi logam berat dengan faktor konsentrasi sebesar 105 (Hartanti,
1998). Akumulasi logam berat seperti merkuri (Hg) dan timbal (Pb) sering terjadi
pada kerang mentah dan menyebabkan keracunan bagi masyarakat yang
mengkonsumsinya karena toksisitasnya tinggi (Hutagalung, 1991; Connell dan
Miller, 1995).
Besarnya kandungan logam berat yang terakumulasi dalam jaringan tubuh
hewan air yang masih layak dikonsumsi manusia ditentukan oleh suatu standar.
kadar Hg maksimum pada biota laut yang boleh dikonsumsi sebesar 0,5 ppm dan
kadar Pb sebesar 2 ppm. Menurut Inswiasri dkk. (1997), rata-rata kadar Hg dan Pb
di perairan Teluk Jakarta masing-masing adalah 0,004 ppm dan berkisar antara
0,00 – 1,57 ppm. Kadar logam berat tersebut akan terakumulasi apabila limbah
buangan industri di sekitar perairan Teluk Jakarta meningkat terutama oleh pabrik
penghasil peralatan listrik, pabrik baterai dan industri penghasil tinta (Darmono,
1995).
Pengawetan ikan dan bahan laut sejenis lainnya dilakukan dengan
menggunakan garam yang dicampur dengan es batu. Tanpa pengawet, kerang
sudah tercemar logam berat karena cemaran industri sudah masuk ke biota laut di
pelabuhan. BPOM baru-baru ini menemukan beragam jenis makanan yang biasa
dikonsumsi masyarakat sehari-hari mengandung zat kimia (formalin) untuk
membuat awet makanan. Produk makanan itu antara lain kerang, tahu, ikan asin,
daging, dan makanan olahan. Bahkan, BPOM menemukan kandungan cat tembok
yang mengandung tras, pewarna kimiawi, semen, dan perekat semen pada
makanan tersebut. Saat es lebih mahal, formalin menjadi pengawet ikan.
kerang hijau dan ikan laut dilumuri cat merah agar harga jual lebih tinggi. Hasil
tangkapan laut yang umumnya telah mati (ikan, cumi, kerang, udang) dimasukkan
ke dalam air tawar yang telah dicampur dengan formalin, yang dapat bertahan 2
hari dibandingkan dengan menggunakan es yang hanya sampai 3 jam. Setelah di
tersebut akan terlihat lebih fresh, mengkilap, bersih sekali. Barulah seafood
tersebut seperti yang terlihat di pasar ikan muara karang di dalam peti es
(Kompas, 2004).
Penelitian ini dilakukan sebagai tindak lanjut dalam pendugaan kandungan
logam berat pada kerang hijau dengan tiga jenis logam berat yang berbeda yaitu
Hg, Pb dan Cd sehingga diharapkan dapat memberikan informasi yang baru dan
melengkapi hasil penelitian-penelitian terdahulu. Namun penelitian baru relatif
belum didapatkan padahal logam berat diakumulasi dalam tubuh makhluk hidup
sehingga diperlukan informasi terbaru mengenai logam berat dalam tubuh kerang
hijau dengan perlakuan bahan pengawet yaitu menambahkan formalin dan zat
pewarna tembok oleh para penjual kerang hijau di pasar ikan Muara Angke.
Pada penelitian ini, untuk mendukung data akumulasi logam berat pada
kerang hijau dibutuhkan beberapa data penunjang. Data tersebut adalah data
konsentrasi logam berat pada contoh air laut, salinitas, pH, suhu, kecerahan dan
Total Suspended Solid (TSS) dari perairan sekitar lokasi pengambilan contoh
kerang hijau tersebut. Sedangkan untuk mengetahui konsentrasi logam berat pada
tubuh kerang hijau tersebut dapat digunakan peralatan Spektrofotometri Serapan
Atom (AAS).
Pada penelitian yang dilakukan ini, lokasi yang dipilih adalah Perairan
Muara Kamal, Teluk Jakarta. Dari lokasi ini diharapkan dapat menggambarkan
konsentrasi logam berat yang terdapat pada contoh kerang hijau yang hidup di
buangan limbah dari Jakarta dan sekitarnya yang pada umumnya mengandung
logam berat.
1.2. Perumusan Masalah
Bagaimana pengaruh penambahan bahan pengawet (formalin, rhodamin B,
metanil yellow dan Na2CaEDTA) dengan konsentrasi dan waktu perendaman
yang berbeda terhadap kandungan logam berat (Hg, Pb dan Cd) dalam tubuh
kerang hijau ?
1.3. Hipotesis
Hipotesis yang digunakan dalam penelitian ini adalah penambahan bahan
pengawet (formalin, rhodamin B, metanil yellow dan Na2CaEDTA) dengan
konsentrasi dan waktu perendaman yang berbeda berpengaruh nyata terhadap
kandungan logam berat (Hg, Pb dan Cd) dalam kerang hijau.
1.4. Tujuan Penelitian
Penelitian ini mempunyai tujuan untuk mengetahui pengaruh penambahan
bahan pengawet (formalin, rhodamin B, metanil yellow dan Na2CaEDTA) dengan
konsentrasi dan waktu perendaman yang berbeda terhadap kandungan logam berat
1.5. Manfaat Penelitian
Dari hasil penelitian ini diharapkan dapat :
1. Dijadikan sebagai bahan standarisasi metode atau tren positif dalam
sistem pengendalian dan pemantauan kadar logam berat pada hasil laut
yang dikonsumsi khususnya kerang hijau.
2. Dijadikan sebagai baku mutu pengendalian keamanan pangan (food
1.6. Kerangka Berpikir
Terakumulasi
Rumah Tangga
Industri
Limbah / Zat Pencemar
Udara
Kontaminasi Logam Berat
Perairan
Kualitas Air (Peningkatan Kadar Logam Hg, Pb dan Cd)
Penambahan Zat Pengawet
Aktivitas Manusia
Pertanian / Pertambakan
Biota Air (Kerang Hijau)
Pengendalian & Pemantauan Kadar Logam Berat pada Hasil Laut yang
Dikonsumsi
Tanah
Solusi ???
BAB II
TINJAUAN PUSTAKA
2.1. Pencemaran Laut
Pencemaran laut didefinisikan sebagai dampak negatif (pengaruh yang
membahayakan) bagi kehidupan biota, sumber daya, kenyamanan ekosistem laut,
serta kesehatan manusia, dan nilai guna ekosistem laut, baik disebabkan secara
langsung maupun tidak langsung oleh pembuangan bahan-bahan atau limbah ke
dalam laut yang berasal dari kegiatan manusia (Dahuri, 2003). Menurut definisi
lain, Pencemaran laut adalah perubahan kondisi laut yang tidak menguntungkan
yang disebabkan oleh adanya benda-benda asing sebagai akibat perbuatan
manusia (Soegiarto, 1976).
Sebagian besar bahan pencemar yang ditemukan di laut berasal dari
kegiatan manusia di daratan. Pada umumnya bahan pencemar tersebut berasal dari
berbagai kegiatan industri, pertanian dan rumah tangga. Sumber pencemaran
dapat dikelompokkan menjadi tujuh kelas, yaitu : (1) industri, (2) limbah cair
permukaan (sewage), (3) limbah cair perkotaan (stormwater), (4) pertambangan,
(5) pelayaran (shipping), (6) pertanian, dan (7) perikanan budidaya. Sedangkan
jenis-jenis bahan pencemar utamanya terdiri dari sedimen, unsur hara, logam
beracun (toxic metals), pestisida, organisme eksotik, organisme patogen, dan
oxygen depleting substance (bahan-bahan yang menyebabkan oksigen terlarut
2.2. Logam Berat
Definisi logam adalah elemen yang dalam larutan air dapat melepas satu
atau lebih elektron dan menjadi kation. Logam mempunyai beberapa karakteristik
penting, yaitu: reflektivitas tinggi, mempunyai kilau logam, konduktivitas listrik
tinggi, konduktivitas termal tinggi, mempunyai kekuatan dan kelenturan. Logam
dikelompokkan menjadi:
1. Logam berat dan logam ringan, dimana logam berat mempunyai berat
jenis >5 dan yang ringan < 5.
2. Logam esensial bagi kehidupan dan yang tidak esensial.
3. Logam yang terdapat hanya sedikit (trace mineral) dan yang bukan trace
mineral. Bila konsentrasi logam di kerak bumi ≥1000 ppm, maka logam
tersebut bukan trace mineral. Atas definisi ini semua logam akan
tergolong trace mineral, kecuali oksigen, hidrogen, silikon, aluminium,
titanium, magnesium, natrium, kalium, kalsium, besi, fosfor dan mangan.
Dari 80 elemen yang tergolong logam hanya atau baru 50 saja yang berarti secara
[image:26.612.133.391.533.637.2]ekonomis dan industrial (Duffus, 1980).
Tabel 1. Logam di dalam Hidrosfer
Logam Air Tawar (µg/l) Air Laut (µg/l) Hg
Pb Cr As Cd Ni
0,001 – 3,5 0,02 – 27
0,1 – 6 0,001 – 3,5
0,01 – 3 0,03 – 10
0,03 – 2,7 0,13 – 13 0,2 – 50 0,03 – 2,7
0,01 – 4 4 – 10
2.2.1. Pencemaran Logam Berat
Menurut keputusan Menteri Negara Kependudukan dan Lingkungan
Hidup No.02/MENKLH/I/1988 yang dimaksud dengan polusi atau pencemaran
air dan udara adalah masuk dan dimasukkannya makhluk hidup, zat, energi dan
atau komponen lain ke dalam air atau udara dan atau berubahnya tatanan
(komposisi) air atau udara oleh kegiatan manusia atau proses alam, sehingga
kualitas air atau udara turun sampai ke tingkat tertentu yang menyebabkan air atau
udara menjadi kurang atau tidak berfungsi lagi sesuai dengan peruntukannya.
Bahan pencemar (polutan) adalah material atau energi yang dibuang ke
lingkungan yang mengakibatkan kerusakan lingkungan baik abiotik maupun
biotik (Quano, 1993). Berdasarkan sumber, pencemaran dapat dibagi menjadi dua
kelompok (Soegiharto, 1976), yakni:
a. Dari laut, misalnya tumpahan minyak baik dari sumbernya langsung
maupun hasil pembuangan kegiatan pertambangan di laut, sampah dan air
ballast dari kapal tanker.
b. Kegiatan darat melalui udara dan terbawa oleh arus sungai yang akhirnya
bermuara ke laut.
Berdasarkan sifatnya, pollutan dibagi menjadi zat yang mudah terurai
(biodegradable) dan zat yang sukar terurai (non biodegradable). Contoh zat yang
mudah terurai adalah sampah organik sedangkan contoh zat yang sukar terurai
adalah minyak dan logam berat (Odum, 1971).
Menurut UU Pangan Nomor 7 Tahun 1996, istilah keamanan pangan
kemungkinan cemaran biologis, kimia dan benda lain yang dapat mengganggu,
merugikan dan membahayakan kesehatan manusia. Pencemaran dapat
digolongkan berdasarkan bentuk bahan pencemarannya pada makanan, yaitu :
1. Cemaran biologis (bakteri, virus, kapang, parasit, protozoa).
2. Cemaran kimia (logam berat, pestisida, bahan tambahan pangan dan
racun).
3. Cemaran fisik (pecahan gelas, potongan tulang, kerikil, kawat dan
sebagainya).
2.2.2. Sumber dan Bentuk Logam Berat
Logam berat masuk ke perairan laut melalui run off air sungai, angin,
proses hidrotermal, difusi dari sedimen dan kegiatan antropogenik. Jalur-jalur
tersebut akan berinteraksi membentuk suatu pola yang disebut dengan siklus
biogeokimia logam berat (Romimohtarto, 1991).
Dalam perairan, logam berat dapat ditemukan dalam bentuk terlarut dan
tidak terlarut. Logam berat terlarut adalah logam yang membentuk kompleks
dengan senyawa organik dan anorganik sedangkan logam berat yang tidak terlarut
merupakan partikel yang berbentuk koloid dan kelompok senyawa logam yang
[image:29.612.35.581.53.579.2]
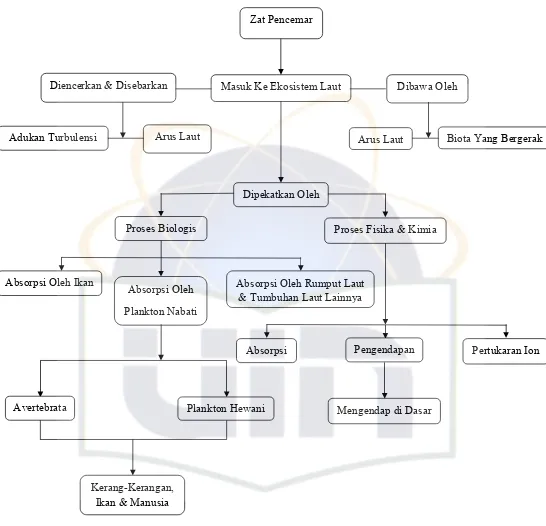
Gambar 1. Perjalanan Logam Berat dari Kolom Air Menuju Dasar Perairan (Sumber: Romimohtarto, 1991)
Zat Pencemar
Diencerkan & Disebarkan Masuk Ke Ekosistem Laut Dibawa Oleh
Arus Laut
Adukan Turbulensi Arus Laut Biota Yang Bergerak
Dipekatkan Oleh
Proses Biologis Proses Fisika & Kimia
Absorpsi Oleh Ikan
Absorpsi Oleh
Plankton Nabati
Absorpsi Oleh Rumput Laut & Tumbuhan Laut Lainnya
Absorpsi Pengendapan Pertukaran Ion
Plankton Hewani Mengendap di Dasar
Avertebrata
2.2.3. Sifat Fisik dan Kimia Beberapa Logam Berat
Logam berat adalah unsur-unsur kimia dengan berat jenis lebih besar dari
5 g/cm3, terletak di sudut kanan bawah daftar berkala, mempunyai afinitas yang
tinggi terhadap unsur S dan biasanya bernomor atom 22 sampai 92 dari periode 4
sampai 7 (Miettinen, 1977). Afinitas yang tinggi terhadap unsur S mendorong
terjadinya ikatan logam berat dengan S pada setiap kesempatan. Sebagian logam
berat merupakan zat pencemar yang berbahaya. Logam-logam ini bereaksi dengan
unsur belerang dalam enzim, sehingga enzim menjadi tidak mobile. Gugus
karboksilat (-COOH) dan amino (-NH2) dalam asam amino juga bereaksi dengan
logam berat. Kadmium, tembaga, dan merkuri diikat dalam membran yang
menghambat proses transport melalui dinding sel. Logam berat juga
mengendapkan senyawa fosfat biologis atau dapat juga mengkatalisis
penguraiannya (Manahan, 1994).
Beberapa ini dijelaskan rincian sifat-sifat beberapa logam berat :
a) Merkuri atau Air Raksa (Hg)
Logam merkuri bernomor atom 80, berat atom 200,59, titik didih 356,9 ºC,
dan massa jenis 13,6 gr/ml (Reilly, 1991). Merkuri dalam perairan dapat berasal
dari buangan limbah industri kelistrikan dan elektronik, baterai, pabrik bahan
peledak, fotografi, pelapisan cermin, pelengkap pengukur, industri bahan
pengawet, pestisida, industri kimia, petrokimia, limbah kegiatan laboratorium dan
terakumulasi dalam hati dan ginjal yang dikeluarkan melalui cairan empedu
(Suryadiputra, 1995).
b) Timbal (Pb)
Timbal atau timah hitam adalah sejenis logam lunak berwarna cokelat
dengan nomor atom 82, berat atom 207,19, titik leleh 327,5 ºC, titik didih 1725 ºC
dan berat jenis 11,4 gr/ml. Logam ini mudah dimurnikan sehingga banyak
digunakan oleh manusia pada berbagai kegiatan misalnya pertambangan, industri
dan rumah tangga. Pada pertambangan timbal berbentuk senyawa sulfida (PbS)
(Reilly, 1991).
Logam Pb bersifat toksik pada manusia dan dapat menyebabkan
keracunan akut dan kronis. Keracunan akut biasanya ditandai dengan rasa
terbakar pada mulut, adanya rangsangan pada sistem gastrointestinal yang disertai
dengan diare. Sedangkan gejala kronis umumnya ditandai dengan mual, anemia,
sakit di sekitar mulut, dan dapat menyebabkan kelumpuhan (Darmono, 2001).
Fardiaz (1992) menambahkan bahwa daya racun dari logam ini disebabkan terjadi
penghambatan proses kerja enzim oleh ion-ion Pb2+. Penghambatan tersebut
menyebabkan terganggunya pembentukan hemoglobin darah. Hal ini disebabkan
adanya bentuk ikatan yang kuat (ikatan kovalen) antara ion-ion Pb2+ dengan
gugus sulfur di dalam asam-asam amino. Untuk menjaga keamanan dari
keracunan logam ini, batas maksimum timbal dalam makanan laut yang
ditetapkan oleh Departemen Kesehatan RI dan FAO adalah sebesar 2,0 ppm. Pada
organisme air kadar maksimum Pb yang aman dalam air adalah sebesar 50 ppb
c) Kadmium (Cd)
Kadmium adalah salah satu unsur logam berat yang bersama-sama dengan
unsur Zn dan Hg termasuk pada golongan II B daftar berkala. Kadmium jarang
sekali ditemukan di alam dalam bentuk bebas. Keberadaannya di alam dalam
berbagai jenis batuan, tanah, dalam batubara dan minyak. Kadmium dapat terikat
pada protein dan molekul organik lainnya dan membentuk garam dengan
asam-asam organik. Dalam bentuk mineral, Cd berada dalam batuan greenochite (CdS)
yang berasosiasi dengan batuan ZnS. Pada ekstraksi pertambangan, Cd sebagai
hasil samping dari tambang seng (kandungan Cd sebesar lebih kurang 3 kg dalam
1 ton Zn). Pelapisan Cd pada suatu logam mengakibatkan logam menjadi
antikorosi bila digunakan dalam air laut, air alkalis dan di lingkungan tropis
(Fergusson, 1991).
Agar tidak terjadi keracunan karena mengkonsumsi makanan yang
terkontaminasi logam Hg, Pb dan Cd, maka ada suatu ketentuan yang disarankan
oleh Food Agricultural Organization – World Health Organization, yaitu 0,3 mg
per orang/minggu untuk Hg total dan tidak lebih dari 0,2 mg Hg jika dalam
bentuk metil merkuri, 0,4 – 0,5 mg per orang/minggu untuk Cd, serta 3 mg Pb
total per orang/minggu (Saeni, 1989).
2.3. Kerang Hijau (Perna viridis L.)
restoran Cina dikenal dengan nama Kaung-kaung. Di Malaysia dikenal dengan
sebutan Siput Kudu, Chay Luan atau Tham Chay (Singapura), Ta Hong (Filipina)
dan Hoi Mong Pong (Thailand) (Kastoro, 1988).
Kerang hijau (Perna viridis Linnaeus, 1758) atau Green Mussels
merupakan spesies spesifik Benua Asia. Spesies ini tersebar luas di sepanjang
wilayah Indo-Pasifik, meluas ke bagian utara hingga Hongkong mulai dari
perairan di Propinsi Guang Dong dan Fujian, China, Selatan Jepang, Thailand,
Filipina, Indonesia hingga perairan Papua Nugini (Vakily, 1989).
Kerang hijau adalah organisme yang dominan pada ekosistem litoral
(wilayah pasang surut) dan sublitoral yang dangkal. Kerang hijau dapat hidup
dengan subur pada perairan teluk, estuaria, perairan sekitar area mangrove dan
muara, dengan kondisi lingkungan yang dasar perairannya berlumpur campur
pasir, dengan cahaya dan pergerakan air yang cukup, serta kadar garam yang tidak
terlalu tinggi (Setyobudiandi, 2000). Kerang hijau merupakan kerang yang
memiliki ukuran tubuh cukup panjang. Ukuran tubuhnya bisa mencapai 80 – 100
mm, bahkan terkadang dapat berukuran panjang hingga 165 mm (Linnaeus,
1758).
Persyaratan yang baik menurut Direktorat Jenderal Perikanan (1985) untuk
kehidupan kerang hijau adalah perairan bersubstrat lumpur dengan metode bagan
rakit tancap, kedalaman 3 – 10 m, kecepatan arus 25 cm/detik, salinitas 27 – 35 ‰
dan suhu 26 – 32 ºC. Berdasarkan cara memperoleh makanannya, moluska
bivalvia ini digolongkan dalam kelompok filter feeder. Apabila makanan
disebut sebagai suspension feeder. Apabila makanan atau bahan organik diambil
dari substratum tempat hidupnya maka disebut sebagai deposit feeder
(Setyobudiandi, 2000). Kelas bivalvia ini telah digunakan oleh ahli ekologi dalam
menganalisis pencemaran air, karena sifatnya yang menetap dan cara makannya
yang pada umumnya bersifat filter feeder sehingga mempunyai kemampuan
mengakumulasi bahan-bahan polutan seperti bakteri dan logam berat (Roberts,
1976).
Menurut Linnaeus (1758), taksonomi dari kerang hijau dapat
diklasifikasikan secara sistematika menjadi :
Filum : Mollusca
Infra Kelas : Pelecypoda
Kelas : Bivalvae (Bivalvia)
Sub Kelas : Lamellibranchia (Pteriomorphia)
Ordo : Mytiloida (Anisomyria)
Sub Ordo : Filibranchia
Super Famili : Mytiloidea (Mytilacea)
Famili : Mytilidae (Pernadae)
Genus : Perna
[image:34.612.115.504.230.669.2]
Menurut Roberts (1976) kelas bivalvia telah digunakan oleh ahli ekologi
dalam menganalisis pencemaran air. Hal ini karena sifatnya yang menetap dan
cara makan pada umumnya filter feeder, sehingga mempunyai kemampuan
mengakumulasi bahan-bahan polutan seperti logam berat. Dilihat dari sumber
energi, kandungan protein kerang hijau 21,9 %, lemak 14,5 %, dan karbohidrat
18,5 %, itu setara dengan kandungan gizi daging sapi dan telur ayam.
Secara morfologi anggota famili Mytilidae mempunyai cangkang yang
tipis. Kedua cangkang tersebut simetris dan umbonya melengkung ke depan.
Persendiannya halus dengan beberapa gigi yang sangat kecil (Abbott, 1974).
Genus Perna L. berbentuk pipih, cangkang padat dan mempunyai umbo pada tepi
vertikal. Tipe alur cangkang konsentrik, bersinar, berwarna hijau dan terkadang di
bagian tepi berwarna kebiruan. Kedua cangkang berukuran sama meskipun satu
cangkang sedikit lebih cembung daripada yang lainnya (Dance, 1977).
Kerang hijau umumnya hidup di laut tropis seperti Indonesia terutama di
perairan pantai, perairan teluk, estuaria, mangrove dan muara-muara sungai
dengan kondisi perairannya lumpur berpasir dengan cahaya pergerakan yang
cukup serta kadar garam yang tidak terlalu tinggi (Setyobudiandi, 2000). Mereka
umumnya hidup menempel secara bergerombol pada dasar atau substrat keras
seperti kayu, bambu, batu, tanggul-tanggul pelabuhan, karang dan lumpur keras
dengan bantuan byssus atau serabut penempel (Kastoro, 1988).
Kerang hijau adalah organisme sessil yang hidup bergantung pada
ketersediaan zooplankton kecil, fitoplankton serta material yang kaya akan
kerang, termasuk golongan binatang lunak (Mollusca), bercangkang dua
(Bivalvae), mempunyai insang berlapis-lapis (Lamellibranchia), berkaki kapak
(Pelecypoda) dan hidup di laut. Di Indonesia, daerah penyebaran kerang hijau
belum ditemukan secara pasti, namun karakteristik perairan yang sesuai untuk
pembudidayaannya adalah pada suhu 27 – 37°C, salinitas 27 – 34 ‰, pH 6 – 8,
kecerahan 3.5 – 4.0 m, arus dan angin tidak terlalu kuat dan umumnya hidup di
kedalaman 3 – 10 m di daerah estuaria serta kandungan oksigen terlarut 6 mg/L
(Ismail, 1999).
2.4. Formalin, Rhodamin B dan Metanil Yellow
Formalin adalah larutan 37 % formaldehida dalam air yang biasanya
mengandung 10 – 15 % metanol untuk mencegah polimerisasi. Formalin
berfungsi sebagai antiseptik untuk membunuh bakteri kapang, terutama untuk
pensterilan peralatan dokter atau proses pengawetan mayat atau spesimen biologi
lainnya. Formalin merupakan zat pengawet berbentuk cair yang paling sering
digunakan oleh produsen makanan yang tak bertanggung jawab. Formalin banyak
digunakan sebagai desinfektan untuk pembersih lantai, kapal, gudang dan
pakaian; sebagai germisida dan fungisida pada tanaman dan sayuran, serta sebagai
pembasmi lalat dan serangga lainnya. Formaldehida biasa digunakan oleh industri
plastik, busa, dan resin untuk kertas, karpet, tekstil, cat, dan furnitur (WHO,
mudah diserap melalui saluran pernafasan dan pencernaan. Penggunaan formalin
dalam jangka panjang dapat berakibat buruk pada organ tubuh, seperti potensi
menimbulkan kanker, kerusakan hati, gangguan ginjal dan sistem reproduksi. Zat
ini juga banyak ditemukan pada ikan, ikan asin, daging, daging ayam, boraks.
Karena beracun, kemasan formalin diberi label dengan tanda gambar tengkorak
pada dasar kotak berwarna jingga (WHO, 1984).
Rhodamin B adalah zat pewarna yang tersedia di pasar untuk industri
tekstil dan zat kimia berbahaya ini tidak boleh dicampurkan ke dalam makanan.
Ciri fisik rhodamin B adalah zat warna sintetik berbentuk serbuk kristal, berwarna
hijau atau ungu kemerahan, tidak berbau; sangat mudah larut dalam air, alkohol,
HCl, NaOH dan dalam larutan berwarna merah terang berfluoresens. Rhodamin B
memiliki rumus molekul C28H31N2O3Cl, dengan berat molekul sebesar 479.000.
Zat ini sering disalahgunakan sebagai zat pewarna makanan dan kosmetik di
berbagai Negara. Makanan yang ditemukan mengandung rhodamin B diantaranya
kerupuk (58%), terasi (51%) dan makanan ringan (42%). Zat ini juga banyak
ditemukan pada kembang gula, sirup, manisan, dawet, bubur, ikan asap dan
cendol. Zat pewarna makanan alami sejak dulu telah dikenal dalam industri
makanan untuk meningkatkan daya tarik produk makanan tersebut, sehingga
konsumen tergugah untuk membelinya. Namun celakanya sudah sejak lama pula
terjadi penyalahgunaan dengan adanya pewarna buatan yang tidak diizinkan untuk
digunakan sebagai zat aditif. Contoh yang sering ditemui di lapangan dan
Rhodamine B, yaitu zat pewarna yang lazim digunakan dalam industri kertas dan
tekstil, namun digunakan sebagai pewarna makanan (WHO, 1984).
Di dalam laboratorium digunakan sebagai pereaksi untuk identifikasi Pb,
Bi, Co, Au, Mg dan Th. Bahan ini bila dikonsumsi bisa menyebabkan gangguan
pada fungsi hati, bahkan kanker hati. Bila mengkonsumsi makanan yang
mengandung rhodamin B, dalam tubuh akan terjadi penumpukan lemak, sehingga
makin lama jumlahnya terus bertambah. Dampaknya baru akan kelihatan setelah
puluhan tahun kemudian. Berikut ini adalah nama-nama lain dari Rhodamine B,
yaitu : (1) Acid Bruliant Pink B, (2) ADC Rhodamine B, (3) Aizen Rhodamine
BH, (4) Aizen Rhodamine BHC, (5) Akiriku Rhodamine B, (6) Briliant Pink B,
(7) Calcozine Rhodamine BL, (8) Calcozine Rhodamine BX, (9) Calcozine
Rhodamine BXP, (10) Cerise Toner, (11)
9-(orto-Karboksifenil)-6-(dietilamino)-3H-xantin-3-ylidene dietil ammonium klorida, (12) Cerise Toner X127, (13)
Certiqual Rhodamine, (14) Cogilor Red 321.10, (15) Cosmetic Briliant Pink
Bluish D conc, (16) Edicol Supra Rose B, (17) Elcozine rhodamine B, (18)
Geranium Lake N, (19) Hexacol Rhodamine B Extra, (20) Rheonine B, (21)
Symulex Magenta, (22) Takaoka Rhodmine B dan (23) Tetraetilrhodamine
(WHO, 1984).
Metanil yellow adalah zat pewarna kimia sintesis yang mengandung logam
berat berbentuk serbuk berwarna kuning kecoklatan, mudah larut dalam air, agak
menimbulkan tumor dalam berbagai jaringan hati, kandung kemih, saluran
pencernaan atau jaringan kulit. Berdasarkan kriteria WHO, metanil yellow
memiliki tingkat keracunan tingkat III. Zat ini juga banyak ditemukan pada
gorengan, manisan mangga, tahu kuning, sirup limun, saus, kue basah, es cendol,
es kelapa, es mambo, pewarna Ponceau 3R, Ponceau SX dan Amarath (WHO,
1984).
2.5. EDTA (Etilene Diamine Tetra-acetate Acid)
Sifat toksik logam Hg dan Pb dikarenakan logam tersebut sangat efektif
berikatan dengan gugus sulfuhidril (SH) yang terdapat dalam sistem enzim sel
membentuk ikatan metaloenzim dan metaloprotein sehingga aktivitas enzim untuk
proses kehidupan sel tidak dapat berlangsung (Connel dan Miller, 1995).
Toksisitas dan sifat letal logam berat Hg, Pb dan Cd pada tubuh biota air dapat
dihilangkan dengan penambahan Etilene Diamine Tetra-acetate Acid (EDTA)
(Hutagalung, 1991; Palar, 1994). Hal ini dikarenakan senyawa EDTA mampu
mengikat dan menarik ion logam berat tersebut keluar dari jaringan tubuh (Linder,
1992). Terjadinya reaksi antara zat pengikat logam (EDTA) dengan ion logam
menyebabkan ion logam kehilangan sifat ionnya dan mengakibatkan logam berat
tersebut kehilangan sebagian besar toksisitasnya (Irwansyah, 1995). Sifat dan
pengaruh negatif logam berat akan hilang dengan adanya zat pengikat logam
karena zat pengikat tersebut akan membentuk ikatan kompleks dengan logam.
berikatan dengan ion logam (Lehninger, 1982). Umumnya EDTA digunakan
untuk mengobati keracunan oleh logam berat Hg dan Pb (Palar, 1994).
Garam-garam EDTA yang digunakan umumnya berbentuk Na2CaEDTA
sebagai pengental pada mentega dan saus, bumbu masak pada kuah untuk sayuran
atau sebagai pengawet untuk mencegah pembusukan yang disebabkan logam
berat pada produk ikan dan kerang-kerangan sehingga dapat bertahan dalam
beberapa hari (Furia, 1972). Penggunaan Na2CaEDTA sebagai zat pengikat logam
pada filet ikan yang mengandung 0,5 – 5 ppm logam berat dapat menghilangkan
sifat toksisitasnya dengan cara melakukan perendaman pada konsentrasi 0,8 – 1,5
% selama 30 – 60 menit. Waktu perendaman berpengaruh nyata terhadap
penurunan logam berat, semakin lama waktu yang digunakan maka logam berat
yang tereduksi semakin banyak (Hartanti, 1998). Dengan demikian diperlukan
penelitian mengenai konsentrasi dan waktu perendaman Na2CaEDTA pada kerang
hijau (Perna viridis L.) dalam upaya menurunkan kadar Hg dan Pb yang
terkandung dalam tubuhnya.
Kemampuan Na2CaEDTA sebagai pengikat logam berat disebabkan
Na2CaEDTA tersebut mampu membentuk ikatan kompleks dengan ion logam
yang terdapat dalam tubuh kerang. Molekul EDTA mampu mengikat ion logam
dengan pembentukan 6 ikatan yaitu 2 untuk atom nitrogen pada gugus amino dan
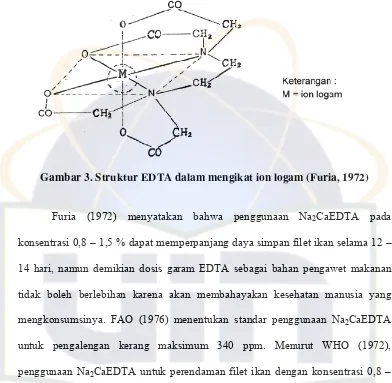
4 untuk atom oksigen pada gugus karboksil (Winarno, 1995 ; Furia, 1972).
Gambar 3. Struktur EDTA dalam mengikat ion logam (Furia, 1972)
Furia (1972) menyatakan bahwa penggunaan Na2CaEDTA pada
konsentrasi 0,8 – 1,5 % dapat memperpanjang daya simpan filet ikan selama 12 –
14 hari, namun demikian dosis garam EDTA sebagai bahan pengawet makanan
tidak boleh berlebihan karena akan membahayakan kesehatan manusia yang
mengkonsumsinya. FAO (1976) menentukan standar penggunaan Na2CaEDTA
untuk pengalengan kerang maksimum 340 ppm. Menurut WHO (1972),
penggunaan Na2CaEDTA untuk perendaman filet ikan dengan konsentrasi 0,8 –
1,5 % selama 30 – 60 menit, diperoleh residu pada filet sebanyak 0,02 – 0,03 %
atau 200 – 300 ppm.
2.6. Hubungan Kerang Hijau dengan Logam Berat
Logam berat (Hg, Cd dan Pb) dalam air kebanyakan berbentuk ion dan
logam tersebut diserap oleh kerang secara langsung melalui air yang melewati
masuk melalui kulit (kutikula) dan lapisan mukosa yang selanjutnya diangkut
darah dan dapat tertimbun dalam jantung dan ginjal kerang (Noviana, 1994; Laws,
1981). Menurut Hutagalung (1991), kemampuan biota laut (ikan, udang dan
moluska) dalam mengakumulasi logam berat di perairan tergantung pada jenis
logam berat, jenis biota, lama pemaparan serta kondisi lingkungan seperti pH,
suhu dan salinitas. Semakin besar ukuran biota air, maka akumulasi logam berat
semakin meningkat. Toksisitas logam berat dalam kerang yang ditimbulkan akibat
akumulasi dalam jaringan tubuh mengakibatkan keracunan dan kematian bagi
biota air yang mengkonsumsinya (Sukiyanti, 1987). Sifat toksik logam Hg dalam
bentuk senyawa HgCl2 dengan konsentrasi 0,027 ppm menyebabkan kematian
pada larva bivalvia (moluska) dan konsentrasi Pb sekitar 2,75 ppm mulai bersifat
letal bagi biota perairan seperti krustasea (Mulyaningsih, 1998).
Urutan toksisitas logam berat dari yang tertinggi sampai terendah adalah
Hg2+ > Cd2+ > Ag2+ > Ni2+ > Pb2+ > As2+ > Zn2+. Metil merkuri merupakan
senyawa logam berat yang sangat berbahaya bagi kesehatan manusia, seperti
terjadinya kasus Minamata di Jepang akibat keracunan memakan kerang dan ikan
yang dagingnya mengandung metil merkuri sehingga mengakibatkan kelainan
susunan saraf pusat, yang dikenal dengan Minamata Disease. Keracunan yang
diakibatkan oleh logam merkuri dalam tubuh umumnya bersifat permanen yang
menyebabkan toksisitas akut dan kronis (Sukiyanti, 1987; Palar, 1994). Batas
Sebaliknya batas maksimum untuk kadar logam Pb dalam tubuh biota air yang
aman dikonsumsi manusia sebesar 0,7 mg atau 700 μg per 70 kg berat badan per
minggu (WHO, 1989).
2.7. Keadaan Umum Perairan Teluk Jakarta
Secara geografis Teluk Jakarta terletak pada koordinat 05°54’40’’LS –
06°00’40’’LS dan 106°40’45’’BT – 107°01’19’’BT (Kantor Kependudukan dan
Lingkungan Hidup, 1989). Teluk ini berbatasan dengan Tanjung Pasir di sebelah
Barat dan Tanjung Karawang di sebelah Timur, serta mempunyai rentangan
pantai sepanjang kurang lebih 40 km dan luas kira-kira 490 km2 (Sutjahjo, Riani
dan Mulyawan, 2004). Bagian yang jauh menjorok ke dalam, berjarak kurang
lebih 18 km dari garis yang menghubungkan kedua ujung teluk. Teluk ini juga
merupakan muara dari beberapa sungai yaitu Sungai Angke, Sungai Ciliwung,
Sungai Sunter, Sungai Bekasi dan cabang Sungai Citarum. Umumnya daerah
tangkapan hujan dari sungai ini sudah banyak dipengaruhi oleh aktivitas
penduduk dan industri (Parjaman, 1977).
Teluk Jakarta tergolong perairan semi tertutup (semi enclosed bay),
dicirikan oleh sirkulasi massa air yang berhubungan bebas terbatas dengan laut
lepas (Laut Jawa), karena adanya penyebaran pulau-pulau di Kepulauan Seribu.
Perairan semi tertutup merupakan daerah peralihan antara daratan dan laut, yang
ditandai oleh adanya perubahan sifat ekologi. Tingkat perubahan parameter
ekologi pada perairan semi tertutup sangat dipengaruhi oleh tingkat keterbukaan
Secara umum, limbah yang masuk ke Teluk Jakarta sebagian besar berasal
dari kegiatan industri pengolahan, industri pertanian (agroindustri), dan sumber
domestik. Berdasarkan pemantauan yang dilakukan KPPL tahun 1997, sumber
limbah terbesar berasal dari aktivitas pengolahan (97,82% atau 1.632.896,47 ribu
m3/tahun), limbah domestik (2,17% atau 36.229,90 ribu m3/tahun) dan limbah
BAB III
METODE PENELITIAN
3.1. Waktu dan Tempat Penelitian
Penelitian ini dimulai dari bulan Desember 2008 sampai dengan April
2009. Kegiatan penelitian meliputi pengamatan di lapangan yaitu pengambilan
sampel air dan kerang hijau (Perna viridis L.) di Perairan Muara Kamal Teluk
Jakarta, sedangkan kegiatan analisis sampel dilakukan di Laboratorium Ekologi &
Lingkungan Pusat Laboratorium Terpadu Universitas Islam Negeri Syarif
Hidayatullah Jakarta.
3.2. Peta Lokasi Sampling
Lokasi sampling penelitian ini terdiri dari tiga titik sampling yang
masing-masing titik berjarak 1 km dengan titik lainnya dari muara menuju ke tengah laut.
Pada tiap titik sampling diambil tiga kali ulangan pada sampel air laut dan kerang
[image:45.612.121.510.90.668.2]hijau yang akan dianalisis kandungan logam beratnya.
Gambar 4. Peta Lokasi Sampling Keterangan :
3.3. Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah biota air berupa
kerang hijau (Perna viridis Linnaeus, 1758) yang diambil dari setiap stasiun
pengamatan dan sampel air laut (air permukaan). Bahan yang dibutuhkan pada
penelitian ini keseluruhannya menggunakan spesifikasi pro analisis yang
diproduksi oleh Merck. Bahan kimia untuk keperluan analisis logam berat,
kualitas air maupun untuk keperluan pengawetan yaitu formalin, rhodamin B,
metanil yellow, larutan asam nitrat pekat (HNO3 pekat), larutan Bouin, ammonium
pirolidin ditiokarbamat (APDC), metil isobutil keton (MIBK), asam peroksida
(H2O2), aquadest, buffer asetat, air suling ganda bebas ion atau air destilasi
(DDDW), es batu, label, sarung tangan plastik, plastik berbagai ukuran, kertas
saring Whatman 0,45 µm (Millipore), aluminium foil, larutan aqua regia, larutan
standar Hg 1000 ppm, larutan standar Pb 1000 ppm dan larutan standar Cd 1000
ppm.
Bahan lain yang digunakan adalah EDTA (Na2CaEDTA), air suling bebas
ion (akuabides), asam nitrat pekat (HNO3), asam perklorat pekat (HClO4), dan
asam sulfat (H2SO4). Pembuatan larutan Na2CaEDTA sesuai dengan konsentrasi
perlakuan dengan cara menimbang Na2CaEDTA sebanyak 0,5 g dan 1,0 g yang
kemudian dilarutkan dengan akuabides sebanyak 100 ml dalam erlenmeyer untuk
mendapatkan konsentrasi 0,5% dan 1,0%.
freezer atau refrigerator, timbangan digital, pH meter, oven, kamera digital, alat
bedah atau pisau bedah steril, pinset polietilen, cawan penguap polietilen,
desikator, mortar, beaker glass, beaker teflon, pipet berbagai ukuran, sentrifuse
polyetilen, labu takar, labu ekstraksi polietilen, saringan plastik, spatula polietilen,
AAS (Atomic absorption spectrophotometry) Model Spectra 20 Plus Varian, botol
semprot dan peralatan analisis kimia lainnya.
3.4. Cara Kerja
3.4.1. Pengambilan Sampel Air Laut
Sampel air laut diambil dengan menggunakan botol Van Dorn atau water
sampler di perairan Muara Kamal pada 9 titik sampling yang berjarak 1 km dari
garis pantai ke kiri dan ke kanan sehingga dapat mewakili kondisi perairan dalam
penentuan kadar logam. Sampel air laut dimasukkan ke dalam botol polyetilen.
Sampel air yang telah diambil dibagi dua botol yaitu botol pertama untuk analisis
kekeruhan dan salinitas. Sedangkan botol kedua untuk analisis logam berat yang
ditambahkan HNO3 pekat sebanyak 10 tetes hingga pH sampel air laut berada di
bawah 2.
Sampel air laut yang diambil untuk kebutuhan analisis logam berat adalah
sekitar 1 liter. Sampel air laut yang telah diperoleh kemudian disimpan di dalam
ice box yang telah terisi es batu dan baru dibuka setelah sampai di laboratorium.
Setiap botol yang akan digunakan diberi label tanggal, waktu dan kode sampel.
Frekuensi pengambilan sampel air laut dilakukan secara bersamaan dengan
pengambilan sampel air, yaitu saat berada di atas perahu. Pengukuran parameter
in situ yang dilakukan pada penelitian ini adalah mengukur kecerahan perairan
sekitar dengan menggunakan secchi disk, suhu air dengan menggunakan
termometer serta salinitas air laut dengan menggunakan refraktometer.
3.4.2. Pengambilan Sampel Kerang Hijau (Perna viridis L.)
Selain dilakukan pengambilan sampel air, pada penelitian ini juga
dilakukan pengambilan sampel biota air berupa kerang hijau. Pengambilan sampel
kerang hijau dilakukan empat kali dalam selang waktu dua minggu di perairan
Muara Kamal. Sampel dimasukkan ke dalam kantong plastik untuk mencegah
kontaminasi logam selama pengangkutan ke laboratorium dan dimasukkan ke
dalam ice box.
Kerang hijau dibagi atas tiga kelompok ukuran panjang, yaitu: ukuran
kecil (< 4 cm), sedang (4 – 6 cm) dan besar (> 6 cm). Penetapan ini berdasarkan
pada ukuran kerang yang dikelompokkan di pasar ikan Muara Angke.
Pengambilan sampel biota air ini dilakukan untuk melihat kandungan logam berat.
Untuk keperluan ini dibutuhkan kerang hijau sebanyak 25 g daging kerang yang
telah dibedah dan dibungkus dengan alumunium foil, kemudian dimasukkan ke
dalam freezer pada suhu -29 ºC sampai siap untuk dianalisis. Pengeringan pada
suhu rendah bertujuan untuk menghindari penguapan logam berat dan menjaga
Tabel 2. Parameter Kualitas Air dan Biota Air yang Diamati.
Parameter Satuan Metode Analisis Tempat Analisis Kualitas Air
Fisika Air
1. Suhu Air ºC Pemuaian Lapangan
2. Kekeruhan Air NTU Nephelometrik Lapangan
3. Salinitas ‰ Ion-ion terlarut Lapangan
Kimia Air
1. pH - Komparasi warna Lapangan
2. Hg mg/l Serapan atom Laboratorium
3. Pb mg/l Serapan atom Laboratorium
4. Cd mg/l Serapan atom Laboratorium
Biota Kimia Biota
1. Hg mg/l Serapan atom Laboratorium
2. Pb mg/l Serapan atom Laboratorium
3. Cd mg/l Serapan atom Laboratorium
3.4.3. Pengukuran Logam Berat pada Sampel Air Laut
Sebanyak 1 liter air laut yang disiapkan disaring dengan menggunakan
kertas saring berukuran pori 0,45 µm dengan bantuan pompa vakum. Hasil
saringan air laut ini kemudian diberi 5 ml HNO3 pekat untuk pengawetan. Sampel
air laut ini kemudian diambil sebanyak 250 ml dan dimasukkan ke dalam corong
pemisah polyetilen. pH larutan sampel air laut ini diatur dengan menggunakan
HNO3 5 M atau NaOH 5 M sehingga pHnya menjadi 3,5 – 4,0. pH ini merupakan
pH optimum untuk melakukan pemisahan logam berat pada sampel air laut,
sehingga logam berat yang diinginkan terpisah dengan baik.
Setelah pH sesuai, sampel air laut ditambahkan 4 ml ammonium pirolidin
ditiokarbamat (APDC), lalu diekstraksi selama 5 menit, kemudian ditambahkan
10 ml metil isobutil keton (MIBK) dan diekstraksi kembali selama 5 menit, lalu
larutan standar. Pada fase organik, ditambahkan 10 ml HNO3 pekat dan
diekstraksi kembali selama 5 menit dan didiamkan selama 15 menit. Setelah 15
menit, pada sampel air laut ini ditambahkan 9 ml air suling bebas ion dan
diekstraksi kembali selama 2 menit, lalu didiamkan hingga kedua fase terpisah
kembali. Fase organik dibuang, sedangkan fase air ditampung dan siap diukur
dengan menggunakan AAS (Hutagalung, 1997).
3.4.4. Pengukuran Logam Berat pada Sampel Kerang Hijau
Sampel kerang hijau yang telah dipisahkan berdasarkan ukurannya,
dagingnya diambil lalu dimasukkan ke dalam cawan penguap. Daging kerang
hijau ini kemudian dimasukkan ke dalam oven dan dipanaskan pada suhu 105°C
selama 12 jam sampai kering. Sampel daging kerang hijau ini lalu digerus agar
menjadi homogen. Penggerusan ini dilakukan hingga daging kerang hijau tersebut
menjadi seperti serpihan-serpihan kecil. Sampel daging kerang hijau yang telah
homogen ini kemudian ditimbang beratnya sekitar 4 gram di dalam beaker glass.
Pada sampel kerang hijau ini lalu ditambahkan 10 ml HNO3 pekat dan
dipanaskan di atas hot plate pada suhu 85°C selama 8 jam (proses destruksi
basah). Satu jam sebelum proses destruksi berakhir, ke dalam sampel kerang hijau
ditambahkan 3 ml H2O2. Setelah dingin, maka sampel kerang hijau ini ditepatkan
volumenya menjadi 20 ml dengan menggunakan air suling bebas ion di dalam
yang tidak hancur selama proses destruksi berlangsung, selain itu hal ini juga
membuat larutan sampel menjadi lebih bersih agar ketika diukur dengan
menggunakan AAS tidak terjadi penyumbatan. Hasil dekantasi ini lalu diukur
dengan menggunakan AAS.
Perendaman daging kerang dengan berbagai perlakuan konsentrasi dengan
cara memasukkan daging tersebut kedalam masing-masing erlenmeyer yang telah
diisi larutan Na2CaEDTA 0,5% dan 1,0% selama 30 menit, 45 menit dan 60
menit. Sampel kerang ditiriskan pada saringan plastik kemudian dicuci untuk
dianalisis.
Analisis logam Hg pada tubuh kerang hijau menggunakan alat Atomic
Absorption Spectrophotometry (AAS) merk GBC tipe 906 AA yang dilengkapi
grafit furnace dan hybrid vapour generator dengan panjang gelombang 253,7 nm.
Sementara untuk logam Pb menggunakan AAS merk Shimidzu tipe 680 AA
dengan panjang gelombang 217 nm. Sebelum dianalisis dengan AAS, daging
kerang terlebih dahulu diperlakukan dengan destruksi asam yang mengacu pada
prosedur Hutagalung (1997).
Logam Hg yang diukur kadarnya dengan metode AAS yaitu kerang
diambil dagingnya dan ditimbang sebanyak 5 g, kemudian dimasukkan ke dalam
botol BOD. Tahap selanjutnya menambahkan 10 ml HNO3 pekat dan 30 ml asam
sulfat pekat, lalu botol ditutup untuk dibiarkan selama 24 jam. Botol dipanaskan
pada suhu 60°C selama 2 jam di atas penangas air. Seluruh isi botol dipindahkan
kecepatan 2 L udara/menit di dalam tabung reduksi air raksa serta menambahkan
SnCl2 sebanyak 5 ml. Sampel kerang siap dianalisis dengan AAS tanpa nyala.
Tahapan analisis kadar Pb dan Cd pada tubuh kerang hijau yaitu kerang
diambil dagingnya dan dikeringkan di dalam oven (105°C) selama 24 jam.
Sampel kerang kemudian didinginkan dalam desikator dan ditimbang sebanyak 2
g. Sampel tersebut selanjutnya dimasukkan ke dalam teflon bomb yang kemudian
dibiarkan selama 24 jam. Contoh kerang tersebut kemudian dipanaskan di atas
penangas air pada suhu 60 – 70°C selama 2 – 3 jam. Selanjutnya ditambahkan 3
ml air suling bebas ion (akuabides) dan dipanaskan kembali hingga larutan hampir
kering (Hutagalung dkk., 1997).
Proses berikutnya adalah mendinginkan sampel tersebut pada suhu ruang
yang diikuti dengan penambahan 1 ml HNO3 pekat dan diaduk pelan-pelan serta
ditambahkan kembali 9 ml akuabides. Sampel siap diukur kadarnya dengan AAS
menggunakan nyala udara asetilen.
3.4.5. Pembuatan Deret Standar Logam Berat Dalam Biota Laut
Deret standar yang digunakan untuk menentukan kadar logam berat dalam
sampel biota laut yaitu sebesar 0,000 ppm; 0,050 ppm; 0,100 ppm; 1 ppm dan 3
ppm. Deret standar ini dibuat dari larutan induk 1000 ppm dengan menggunakan
rumus pengenceran untuk masing-masing jenis logam (Hg, Pb, dan Cd). Deret
digunakan untuk membuat kurva kalibrasi pada alat AAS dan mengukur kadar
logam berat pada sampel biota laut (Hutagalung, 1989).
3.4.6. Perhitungan Kadar Logam Berat
Parameter uji yang digunakan meliputi kandungan logam Hg, Pb dan Cd
pada awal dan akhir penelitian serta tingkat penurunan kadar logam berat tersebut.
1. Kandungan logam Hg pada tubuh kerang hijau dihitung menurut rumus :
Kadar Hg = a / b ppm (Hutagalung dkk., 1997)
Ket : a = jumlah μg Hg dari hasil pengukuran dengan AAS b = berat contoh (5 g)
2. Kandungan logam Pb atau Cd pada tubuh kerang hijau dihitung dengan
rumus:
Kadar Pb atau Cd = a x b / c ppm (Hutagalung dkk., 1997)
Ket : a = jumlah μg Pb atau Cd dari hasil pengukuran dengan AAS b = volume akhir larutan contoh (faktor pengenceran)
c = berat contoh kerang (2 g)
3. Tingkat penurunan kandungan logam berat dihitung menggunakan rumus :
I = (Io – It) / Io x 100 % (Porsepwandi, 1998)
Ket : I = tingkat penurunan kandungan logam berat (%) Io = kandungan logam berat pada awal penelitian (ppm) It = kandungan logam berat pada akhir penelitian (ppm)
3.5. Analisis Data
Rancangan percobaan yang digunakan dalam penelitian ini adalah
Rancangan Acak Kelompok (RAK) dengan pola faktorial 3 x 3 dengan 3 kali
taraf yaitu : tanpa bahan pengawet (p0), konsentrasi 5 % (p1) dan konsentrasi 10 %
(p2) masing-masing perlakuan pengawet diberikan sebanyak 15 ml per sampel
kerang hijau. Faktor kedua adalah waktu perendaman yang terdiri atas tiga taraf
yaitu : 30 menit (t1), 45 menit (t2) dan 60 menit (t3). Data yang diperoleh diolah
dengan uji F (Anova) dan uji lanjut Duncan (α = 0,05) untuk mengetahui
perbedaan antar perlakuan dengan software SPSS.v15.0 (Gasperz, 1995).
Pendugaan kandungan logam berat dalam daging kerang hijau dengan
kandungan logam berat di air, dilakukan dengan mencari Indeks Faktor
Konsentrasi (FK) (Prartono, 1985):
Kadar logam berat daging kerang hijau (mg/l) FK =
Kadar logam berat dalam air laut (mg/l)
Van Esch (1977 dalam Fitriati, 2004) mengatakan bahwa semakin mudah
logam diabsorbsi dan terakumulasi pada tubuh organism air, semakin besar indeks
faktor konsentrasi dan logam berat tersebut dapat semakin bersifat racun. Besar
kecilnya indeks faktor konsentrasi dipengaruhi oleh beberapa hal, antara lain :
jenis-jenis logam berat, jenis organisme, lama pernapasan dan kondisi lingkungan
BAB IV
HASIL DAN PEMBAHASAN
4.1. Parameter Lingkungan (Fisika dan Kimia)
Parameter penunjang yang dibutuhkan untuk penentuan konsentrasi logam
berat pada sampel kerang hijau adalah salinitas, pH, suhu, dan kekeruhan pada air
laut di perairan sekitar lokasi pengambilan sampel. Pengukuran parameter
penunjang ini pada umumnya dilakukan secara in situ. Pada pengamatan
parameter fisika dan kimia yaitu, suhu, kekeruhan, pH dan salinitas secara
keseluruhan masih menunjukkan kondisi yang memungkinkan untuk kerang hijau
melakukan proses-proses biologis dalam hidupnya, baik untuk pertumbuhan
maupun untuk kebutuhan reproduksi.
Logam berat yang masuk ke dalam suatu perairan, baik di sungai ataupun
di laut akan dipindahkan dari badan air melalui tiga proses, yaitu pengendapan,
adsorbsi dan absorpsi oleh organisme perairan (Bryan, 1976). Logam-logam
dalam lingkungan perairan umumnya berada dalam bentuk ion-ion seperti ion-ion
bebas, pasangan ion organik, ion-ion kompleks dan bentuk-bentuk ion lainnya
(Palar, 1994).
[image:55.612.113.507.122.522.2]a. Suhu Perairan Muara Kamal
Gambar 5 memperlihatkan bahwa rata-rata nilai suhu perairan di tiap titik
menunjukkan kisaran antara 26 – 31°C, dengan suhu tertinggi 31°C dan terendah
26°C. Hal ini sesuai dengan persyaratan yang dikeluarkan oleh Direktorat
k P m y y p b p a b p kerang hijau Pengukuran mempelajari yang hidup yang terjadi penurunan d bahan terte pemanasan
air akan berb
b. Kekeruh Gam pada peraira Su hu (° C) u disarankan suhu dila i proses-pro
di suatu p
i dalam tub
daya larut ok
entu. Suhu
matahari ya
banding luru
Gam
han Peraira mbar 6 mem
an Muara K 23 24 25 26 27 28 29 30 31
Titik I
Titik II
Titik III
Su
hu
(
C)
n agar suhu
akukan me
ses fisika, k
erairan, suh
buh kerang h
ksigen terlaru
air terutam
ang intensita
us dengan pe
mbar 5. Suh
an Muara K mperlihatkan Kamal, Teluk Februari 26 27.2 27.2
u perairan b
engingat pe
kimia dan b
hu mempeng
hijau. Penin
ut dan juga a
ma di lapi
asnya beruba
erubahan inte
u Perairan
Kamal bahwa rat
k Jakarta se Maret 31 29 28 Bulan
Suhu
berada dalamentingnya p
iologi. Pada garuhi prose ngkatan suhu akan menaik san permuk ah terhadap ensitas peny Muara Kam a-rata nilai elama penga April 30 29 28
m kisaran 2
parameter
a biota atau
es-proses m
u dapat me
kkan daya ra
kaan ditentu waktu, sehi yinaran mata mal kekeruhan amatan berk
26 – 32°C.
ini dalam organisme metabolisme enyebabkan cun bahan-ukan oleh ingga suhu ahari.
(turbidity)
kisar antara Titik I
Titik II
t m r u d m d 2 c T H p
titik I diseb
muara yang
rumah tangg
umumnya p
dengan pera
menyerap s
disebabkan
2003).
c. pH Pera Seca
Teluk Jakart
Hal ini dise
penyangga,
Kekeruhan
(NTU)
babkan oleh
g merupakan
ga dan indus
perairan laut airan tawar. inar mataha oleh partike Gamba airan Muar ara umum n
ta di tiap sta
ebabkan oleh sehingga ma 0 1 2 3 4 5
Titik I
Titik II
Titik III
Kekeruhan
(NTU)