PEMANFAATAN KERANG HIJAU (
Perna viridis
Linn.)
SEBAGAI BIOINDIKATOR PENCEMARAN LOGAM
TIMBAL (Pb) DI PERAIRAN KAMAL MUARA, TELUK
JAKARTA
Oleh :
Lucky Cahyo Kencono
G34101068
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
LUCKY CAHYO KENCONO. Pemanfaatan Kerang Hijau (Perna viridis Linn.) sebagai Bioindikator Pencemaran Logam Timbal (Pb) di Perairan Kamal Muara, Teluk Jakarta. Dibimbing oleh DEDE SETIADI dan TRI HERU WIDARTO
Penelitian ini bertujuan untuk mencari penanda biologi (biomarker) pencemaran logam timbal pada kerang hijau dan mencari hubungan antara kandungan logam timbal dan tingkat pencemaran di perairan Kamal Muara, Teluk Jakarta dengan morfometri tubuh kerang. Untuk itu parameter fisika, kimia air pada teluk Jakarta dianalisis. Selain itu bagian cangkang serta daging dari kerang hijau yang didapatkan juga dianalisis menggunakan atomic absorption spectrophotometry. Korelasi kandungan logam timbal dengan morfometri tubuh dilakukan dengan menggunakan metode regresi linier berganda. Kelainan pada cangkang (abnormalitas) kerang hijau juga dicatat. Stasiun 1, 2, 3, 4 terletak pada koordinat secara berturut-turut 06’04”.921oLS dan 106’44”480o BT, 06’04” 831o LS dan 106’44”906o BT, 06’04”213o LS dan 106’45”180o BT, 06’02”090o LS dan 106’44”090o BT. Konsentrasi logam timbal pada ke-4 stasiun berturut-turut sebesar 0.023 ppm, 0.022 ppm, 0.025 ppm dan <0.001 ppm. Kisaran logam timbal di dalam cangkang pada ke-4 stasiun sebesar 0–21.35 ppm, 0–22.65 ppm, 9.5–18.35 ppm, dan 7.4–10.85 ppm. Sedangkan konsentrasi logam timbal dalam daging sebesar 3.4–11.70 ppm, 2.167–25 ppm, 11.625–25.6 ppm, dan 15.7–31.167 ppm. Kelainan pada 200 cangkang yang berhasil dicatat pada ke-4 stasiun adalah, rasio panjang/tinggi abnormal, rasio panjang/lebar abnormal, cangkang tumbuh 2 kali dan bentuk pinggir cangkang abnormal.
Hasil penelitian ini menunjukkan bahwa kandungan timbal perairan Kamal Muara Teluk Jakarta sudah melebihi baku mutu KEPMENLH 51/2004 (<0.008 ppm) kecuali pada stasiun 4. Selain itu konsentrasi timbal pada tubuh kerang (daging dan cangkang) juga melebihi baku mutu DepKes/1989 (<2 ppm). Oleh karena itu daging kerang hijau pada perairan Kamal Muara, Teluk Jakarta kurang layak dikonsumsi. Hasil penelitian juga menunjukkan jika bobot cangkang dan bobot daging bertambah maka konsentrasi timbal di dalamnya akan berkurang, dan jika panjang cangkang bertambah maka konsentrasi timbal di dalamnya akan bertambah pula. Kelainan yang terdapat pada morfologi tubuh kerang hijau dapat dijadikan biomarker pencemaran timbal.
ABSTRACT
LUCKY CAHYO KENCONO. The Usage of Green-Lipped Mussel (Perna viridis Linn) as a Lead (Pb) Pollution Bioindicator at Kamal Muara Waters, Jakarta Bay. Supervised by DEDE SETIADI and TRI HERU WIDARTO
This research was conducted to find biomarker for lead-pollution on Green-Lipped Mussel (Perna viridis Linn.) and to find correlation between body-lead concentration and body morphometrics. Physical and chemistry parameter of the water in Jakarta bay was analyzed due to the goals. The amount of lead present was estimated too by using atomic absorption spectrophotometry. Correlation between body morphometrics and lead concentration was conducted by using multiple linier regression. Deformities of the shell was marked also.
The sampling sites lies at 06’04”.921o SL and 106’44”480o EL, 06’04” 831o SL and 106’44”906o EL, 06’04”213o SL and 106’45”180o EL, 06’02”090o SL and 106’44”090o EL. Lead concentration in the water in all sampling sites was 0.023 ppm, 0.022 ppm, 0.025 ppm and <0.001 ppm. Lead concentration in the shell in all sampling sites was between 0.00–21.35 ppm, 0.00– 22.65 ppm, 9.5–18.35 ppm and 7.4–10.85 ppm while in the soft tissue was between 3.4–11.70 ppm, 2.167–25 ppm, 11.625–25.6 ppm and 15.7–31.167 ppm. The deformities that was marked in all sampling sites were, abnormality in the length/height ratio, abnormality in the length/width ratio, shell growed twice and deformity in peripheral shell.
PEMANFAATAN KERANG HIJAU (
Perna viridis
Linn.)
SEBAGAI BIOINDIKATOR PENCEMARAN LOGAM
TIMBAL (Pb) DI PERAIRAN KAMAL MUARA, TELUK
JAKARTA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Oleh :
Lucky Cahyo Kencono
G34101068
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : PEMANFAATAN KERANG HIJAU (
Perna viridis
Linn.) SEBAGAI
BIOINDIKATOR PENCEMARAN LOGAM TIMBAL (Pb) DI
PERAIRAN KAMAL MUARA, TELUK JAKARTA
Nama : Lucky Cahyo Kencono
NRP :
G34101068
Menyetujui:
Pembimbing I,
Pembimbing II,
Dr. Ir. Dede Setiadi, M.S
Ir. Tri Heru Widarto, M.Sc
NIP 130779509 NIP 131663018
Mengetahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Dr. Ir. Yonny Koesmaryono, M.S
NIP 131473999
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas karunia dan hidayah-Nya sehingga karya ilmiah ini berhasil diselesaikan. Shalawat serta salam penulis haturkan kepada manusia panutan semua umat, nabi akhir zaman, Nabi Muhammad SAW. Karya ilmiah ini disusun berdasarkan penelitian yang dilaksanakan sejak bulan November 2005 sampai dengan bulan Maret 2006, dengan judul Pemanfaatan Kerang Hijau (Perna viridis Linn.) sebagai Bioindikator Pencemaran Logam Timbal (Pb) di Perairan Kamal Muara, Teluk Jakarta.
Terima kasih penulis ucapkan kepada Bapak Dr. Ir. Dede Setiadi, M.S dan Ir. Tri Heru Widarto, M. Sc. selaku pembimbing yang telah memberikan bimbingan, pengarahan, selama pelaksanaan penelitian sampai penulisan karya ilmiah ini. Terima kasih juga penulis ucapkan kepada ibu Dr. Yulin Lestari yang telah bersedia memberikan saran dalam penulisan karya ilmiah ini.
Penulis mengucapkan terima kasih kepada seluruh staf Laboratorium Analisis Lingkungan FMIPA, Laboratorium Zoologi serta Laboratorium Produktivitas dan Lingkungan Departemen Manajemen Sumber Daya Perairan atas bantuannya selama melaksanakan penelitian. Ucapan terima kasih juga diberikan kepada mama, papa, Antie, Iyank, Dina dan mamah Nani atas motivasi dan doa yang tidak pernah putus serta kasih sayangnya, Pak Maga dan keluarga atas bantuannya di teluk Jakarta, Bu Anna, Pak Heri, Bu Hendarti atas masukan dan kerjasamanya di lab selama penelitian, Zoologi’ers 38 dan 39, Kharisma, Riza, Aries, Huang, pengurus DKM Al-Ghifari dan IM3, serta semua teman-teman dan staf Biologi terima kasih atas dukungan, persahabatan, dan kebersamaannya selama ini.
Semoga karya ilmiah ini dapat menambah perbendaharaan ilmu pengetahuan Indonesia
Bogor, Juni 2006
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 19 Mei 1983 dari ayah Tribusono dan ibu Mardiati. Penulis merupakan putra ketiga dari tiga bersaudara.
Tahun 2001 penulis lulus dari SMU Negeri 47 Jakarta Selatan dan pada tahun yang sama lulus seleksi masuk IPB melalui jalur Seleksi Penerimaan Mahasiswa Baru IPB. Penulis memilih Program Studi Biologi, Departemen Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam. Pada tahun 2004 penulis melaksanakan praktik lapang di PT Toyota Motor Manufacturing Indonesia, Sunter, Jakarta Utara dengan judul ”Pengolahan Limbah Cair dan Upaya Pemeliharaan Kesehatan dan Keselamatan Kerja di PT Toyota Motor Manufacturing Indonesia Sunter I Plant”.
DAFTAR ISI
Halaman
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... viii
PENDAHULUAN Latar Belakang ... 1
Tujuan Penelitian ... 1
Waktu dan Tempat ... 2
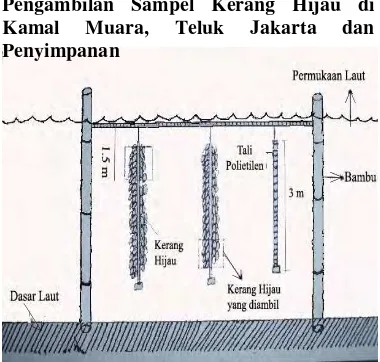
BAHAN DAN METODE Pengambilan Sampel Kerang Hijau di Lapangan dan Penyimpanan ... 2
Pengambilan Sampel Air di Perairan Kamal Muara, Teluk Jakarta ... 2
Pengukuran Kandungan Parameter Fisika dan Kimia Air pada Perairan Kamal Muara, Teluk Jakarta ... 2
Pengukuran Logam Timbal pada Perairan Kamal Muara, Teluk Jakarta ... 3
Analisis Logam Timbal di Jaringan Lunak dan Cangkang Kerang Hijau ... 3
Hubungan Ukuran Tubuh Kerang Hijau dengan Konsentrasi Timbal pada Tubuh ... 3
Analisis Kondisi Morfologi Kerang Hijau ... 3
HASIL Pengambilan Sampel Kerang Hijau di Kamal Muara, Teluk Jakarta dan Penyimpanan 3
Parameter Fisika dan Kimia Air pada Perairan Kamal Muara, Teluk Jakarta ... 4
Konsentrasi Logam Timbal pada Perairan Kamal Muara, Teluk Jakarta ... 4
Konsentrasi Logam Timbal di Jaringan Lunak dan Cangkang Kerang Hijau ... 4
Hubungan Ukuran Tubuh Kerang Hijau dengan Konsentrasi Timbal pada Tubuh ... 5
Analisis Kondisi Morfologi Kerang Hijau ... 5
PEMBAHASAN Kondisi Perairan Kamal Muara, Teluk Jakarta ... 6
Parameter Fisika dan Kimia Air pada Perairan Kamal Muara, Teluk Jakarta ... 6
Konsentrasi Logam Timbal pada Perairan Kamal Muara, Teluk Jakarta ... 6
Konsentrasi Logam Timbal di Jaringan Lunak dan Cangkang Kerang Hijau ... 7
Hubungan Ukuran Tubuh Kerang Hijau dengan Konsentrasi Timbal pada Tubuh ... 8
Kondisi Abnormal Morfologi Kerang Hijau ... 9
SIMPULAN ... 9
SARAN ... 9
DAFTAR PUSTAKA ... 10
DAFTAR GAMBAR
Halaman
1 Keramba kerang hijau (Perna viridis Linn) pada setiap stasiun ... 3
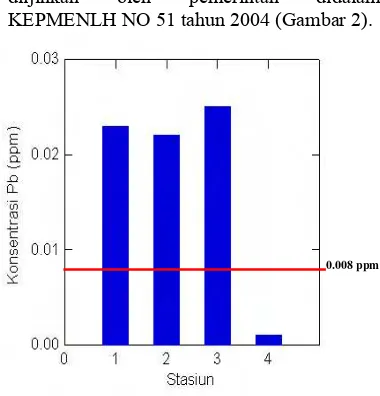
2 Kisaran konsentrasi Pb pada perairan Kamal Muara, Teluk Jakarta ... 4
3 Kisaran konsentrasi Pb pada cangkang Perna viridis (L) ... 5
4 Kisaran konsentrasi Pb pada daging Perna viridis (L) ... 5
5 Grafik regresi perbandingan panjang cangkang dengan tebal cangkang ... 5
6 Grafik regresi perbandingan panjang cangkang dengan tinggi cangkang ... 5
7 Kelainan pada cangkang (abnormalitas) ... 8
DAFTAR LAMPIRAN
Halaman 1 Peta stasiun pengamatan ... 132 Profil cangkang bivalvia secara umum ... 13
3 Profil jaringan lunak kerang hijau ... 13
4 Data aspek morfometrik dan kandungan timbal kerang dari 4 stasiun ... 14
5 Grafik kenormalan galat konsentrasi timbal ... 15
6 Analisis regresi linier berganda pada cangkang ... 16
7 Analisis regresi linier berganda pada daging ... 16
8 Klasifikasi nama ilmiah kerang hijau (Perna viridis Linn.) ... 16
1
PENDAHULUAN
Latar Belakang
Perkembangan teknologi dan industri termasuk di Indonesia, telah membawa dampak negatif terhadap lingkungan hidup manusia. Limbah industri yang tidak dikelola secara baik dan ramah lingkungan akan merusak banyak komponen biotik dalam suatu relung ekologi. Apabila hal ini berlangsung terus-menerus akhirnya akan merugikan manusia.
Pada umumnya limbah industri pada akhirnya akan terbuang ke laut. Bergantung pada sumbernya, limbah industri tersebut dapat mengandung logam berat yang sangat besar. Logam berat ini dapat masuk ke dalam rantai makanan dan memiliki potensi untuk membahayakan tumbuhan dan hewan laut (Nursita et al. 2003) dan akhirnya manusia yang mengkonsumsinya.
Kontaminasi logam berat dalam sistem perairan pada umumnya diketahui dengan pengukuran pada air, sedimen, dan biota laut (Camusso et al. 1995). Selain terdapat dalam perairan, logam berat terakumulasi juga dalam makanan, tanah, sedimen, dan organisme di perairan (Colognesi et al. 1997). Dua ciri-ciri logam berat utama yang membedakan dari polutan beracun lainnya adalah; tidak bisa didegradasi secara biologi (Walker 2001) dan sifat racunnya dipengaruhi oleh bentuk kimia-fisiknya.
Logam berat dapat membahayakan jika batas konsentrasinya melebihi ambang batas yang telah ditentukan. Timbal adalah salah satu logam berat yang memiliki efek yang sangat merugikan untuk komponen biotik. Pada manusia timbal terakumulasi di bagian sumsum tulang belakang dan otak. Keracunan logam ini yang akut pada tubuh manusia dapat mengganggu perubahan ALA (asam δ-amino levulinat) menjadi prophobilinogen dan terikatnya ion besi pada protophyrin IX pada proses pembentukan hemoglobin (WHO 1972). Hal ini dapat mengakibatkan meningkatnya ekskresi heme prekursor yang terbawa lewat urin (hemoglobinuria).
Timbal dianggap sebagai senyawa racun (toksikan) yang utama terhadap beberapa organisme perairan serta merupakan racun yang nonspesifik yang mempengaruhi secara luas sistem fisiologi pada organisme (Pain 1997 diacu dalam Rabitto 2005). Kadarnya cenderung meningkat dalam lingkungan. Hal ini disebabkan oleh berbagai kegiatan manusia seperti penambangan, peleburan, pembersihan, dan berbagai penggunaannya
dalam industri (Lu 1995; Muda 2003). Penggunaannya dalam industri sebagai zat tambahan bahan bakar dan zat warna timbal dalam cat merupakan penyebab utama dalam peningkatan konsentrasinya di lingkungan. Tingkat pencemaran timbal dapat diketahui dengan meneliti kadarnya pada biota laut yang hidup pada lingkungan yang tercemar. Pada penelitian ini diteliti kadar timbal pada kerang hijau(Perna viridis (L)).
Kerang hijau telah banyak digunakan ilmuwan untuk memantau pencemaran pada perairan. Salah satu sebabnya adalah kerang hijau merupakan organisme yang tersebar luas di dunia (Yap 2004). Kerang hijau adalah salah satu bivalvia yang merupakan kerang spesifik di Benua Asia. Kerang ini hidup tersebar dari daerah Indo Pasifik, selatan perairan Jepang, perairan-perairan India, semenanjung Malaysia, Singapura, Laut Cina Selatan, Thailand, Filipina, Indonesia, hingga Papua New Guinea (Setyobudiandi 2004).
Selain itu, program ”Mussel Watch” yang dicanangkan oleh dunia internasional juga menggunakan jaringan lunak dari kerang bivalvia untuk memantau polusi perairan (Gillikin et al. 2005). Alasan lainnya adalah karena jenis ini merupakan biota yang dalam perkembangannya menetap pada suatu tempat, berumur panjang, mudah didapatkan dan diidentifikasi, jumlahnya berlimpah dan mudah diperoleh setiap tahunnya serta tahan terhadap fluktuasi kondisi alami lingkungannya dan polusi (Yap 2004).
Kerang hijau ini merupakan sumber mineral yang penting (Ca, Fe) dan beberapa vitamin (niasin, thiamin, dan riboflavin) untuk tubuh manusia. Hal ini juga menguatkan alasan para ilmuwan untuk selalu meneliti biota laut ini dan menentukan batasan konsentrasi polutan yang beresiko untuk dikonsumsi manusia (Yap 2004).
Untuk mengetahui tingkat pencemaran dalam tingkat individu dapat digunakan sebuah penanda biologis (biomarker). Secara umum biomarker adalah parameter pada organisme yang memperlihatkan efek tertentu dikarenakan terpapar suatu polutan pada tingkat individu/spesies. Biomarker bisa dilihat pada biomolekuler, biokimia atau fisiologi dari individu tersebut. Biomarker
yang diamati pada penelitian ini adalah bentuk morfologi dari cankang dan ukuran tubuh dari kerang hijau.
Tujuan
2
timbal pada kerang hijau (Perna viridis (L.)) di perairan Kamal Muara, Teluk Jakarta dan mencari hubungan antara kandungan logam timbal dan tingkat pencemaran di teluk Jakarta dengan morfometri tubuh kerang.
Waktu dan Tempat
Pengambilan contoh kerang hijau (Perna viridis (L.)) dilakukan di Teluk Jakarta di bagian perairan Kamal Muara. Stasiun 1 berada 1.4 km dari muara, stasiun 2 berada 1.9 km dari muara, stasiun 3 berada 2.7 km dari muara, stasiun 4 berada 5.4 km dari muara. Penelitian ini dilakukan dari bulan November 2005 sampai dengan bulan Maret 2006. Rentang waktu ini bertepatan dengan musim hujan. Analisis kimia kadar timbal (Pb) dan kualitas air laut dilakukan di Laboratorium Produktivitas dan Lingkungan Perairan (ProLing) Departemen Manajemen Sumber Daya Perairan, Fakultas Perikanan dan Ilmu Kelautan serta Laboratorium Analisis Lingkungan FMIPA IPB. Kajian morfometrik dilakukan di Laboratorium Zoologi Departemen Biologi Fakultas Matematika dan Ilmu Pengetahuan IPB Bogor.
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah kerang hijau (Perna viridis (L.)) sebanyak 240 ekor, dari daerah Muara Kamal perairan Teluk Jakarta. Contoh air dikoleksi dari Teluk Jakarta. Bahan lain yang digunakan adalah larutan HNO3 pekat, larutan MnSO4, larutan
NaOH-KI, larutan H2SO4, larutan amilum,
larutan Na-tiosulfat 0.0231 N, larutan Zn-Asetat. Alat yang digunakan antara lain water sampler (LaMotte Water Sampler CODE 1077), syringe 3 ml, kertas pH MERCK dengan trayek pH 0-14, termometer. GPS (Global Positioning System), botol kaca BOD, botol plastik, jangka sorong dan penggaris, neraca analitik digital, gelas piala, Erlenmeyer, gelas ukur 50 ml, spektrofotometer serapan atom (AAS), kamera digital.
Metode
Pengambilan Sampel Kerang Hijau di Lapangan dan Penyimpanan
Lokasi pengambilan sampel dilakukan di 4 stasiun dalam keramba milik nelayan kerang hijau pada perairan Kamal Muara (Gambar 2). Stasiun pengambilan sampel dipilih di Kamal Muara karena di perairan tersebut mudah
dicapai serta karena banyak nelayan yang memiliki peternakan kerang hijau.
Stasiun 1, 2, 3, dan 4 berturut-turut terletak pada koordinat 06’04”.921o lintang selatan dan 106’44”480o bujur timur, 06’04” 831o lintang selatan dan bujur timur 106’44”906o, 06’04”213o lintang selatan dan 106’45”180o bujur timur, 06’02”090o lintang selatan dan 106’44”090o bujur timur. Stasiun 1, 2, 3, dan 4 berturut-turut berjarak 1.4 km, 1.9 km, 2.7 km, dan 5.4 km dari garis pantai.
Kerang hijau diambil dari tali tempat menempelnya (Gambar 1) yang berada dibawah permukaan laut dengan menggunakan pisau. Setelah terpisah dari tempat menempelnya, kerang hijau tersebut kemudian dimasukkan ke dalam cooler box
sampai dilakukan pengukuran, penimbangan dan dianalisis kandungan timbalnya.
Pengambilan Sampel Air di Perairan Kamal Muara, Teluk Jakarta
Air contoh diambil pada stasiun yang sama pada pengambilan kerang. Air diambil dengan menggunakan water sampler. Water sampler ditenggelamkan sampai kedalaman yang sama dengan posisi menempelnya kerang hijau. Jika water sampler tersebut sudah terisi penuh, maka alat tersebut kemudian diangkat dari dalam air. Air yang tertampung kemudian dipindahkan kedalam botol plastik (± 1500 ml). Air contoh pada masing-masing stasiun diambil sebanyak 3 botol plastik (± 1500 ml) dan 2 botol kaca BOD (300 ml).
Pengukuran Kandungan Parameter Fisika dan Kimia Air pada Perairan Kamal Muara, Teluk Jakarta
Sifat fisik dan kimia air yang lainnya juga dianalisis. Sifat fisik yang dianalisis adalah suhu, kebauan, kekeruhan, padatan tersuspensi total, sampah. Sedangkan sifat kimia yang dianalisis adalah pH, salinitas, DO (dissolved oxygen), ammonia (NH3), BOD 5
(biological oxygen demand), total fosfat (PO4), Nitrit (NO2), fenol total, sulfida (H2S).
3
Pengukuran Logam Timbal pada Perairan Kamal Muara, Teluk Jakarta
Air sampel sebanyak 100 ml dimasukkan ke dalam gelas piala, lalu ke dalam gelas piala tersebut ditambahkan kristal NaSO4 (sodium
sulfat). Setelah itu asam sulfat pekat sebanyak 1 ml ditambahkan ke dalam gelas piala tersebut, lalu campuran tersebut dipanaskan diatas hot-plate, kemudian didihkan. Sampel tersebut lalu didinginkan sebentar. Kemudian air destilata sebanyak 25 ml dan asam nitrat pekat sebanyak 2 ml ditambahkan ke dalamnya. Setelah itu sampel didihkan sampai larutan kering diatas hot-plate. Lalu didinginkan kembali. Kemudian air destilata sebanyak 25 ml, asam nitrat pekat sebanyak 1 ml, dan asam perklorat sebanyak 1 ml ditambahkan kedalam gelas piala yang sama. Larutan dididihkan sampai kering diatas hot-plate. Larutan didinginkan kembali. Setelah itu sisa larutan diambil kemudian dimasukkan ke dalam 1 % asam hidroklorat (jika perlu disaring terlebih dahulu). Setelah itu sampel dimasukkan ke dalam instrumen spektrofotometri serapan atom (atomic absorption spectrofotometry). Hasil dari analisis kemudian dibandingkan dengan baku mutu air laut untuk biota perairan berdasarkan Keputusan Menteri Lingkungan Hidup no 51 tahun 2004 sebesar 0.008 ppm.
Analisis Logam Timbal di Jaringan Lunak dan Cangkang Kerang Hijau
Proses ini terdiri dari dua perlakuan. Pertama masing-masing sampel dari jumlah total 40 buah (cangkang dan jaringan lunak) harus dihancurkan secara fisika. Jaringan lunak dan cangkang dihancurkan dengan cara digerus. Jika sudah hancur, dilanjutkan dengan penghancuran secara kimia. Sebanyak 2 gram sampel dimasukkan ke dalam gelas piala. Lalu ke dalam gelas piala tersebut ditambahkan kristal NaSO4 (sodium sulfat).
Setelah itu ditambahkan 1 ml asam sulfat pekat ke dalam gelas piala tersebut, lalu campuran tersebut dipanaskan diatas hot-plate, kemudian didihkan. Sampel tersebut lalu didiinginkan sebentar. Kemudian 25 ml air destilata dan 2 ml asam nitrat pekat ditambahkan ke dalamnya. Setelah itu didihkan sampel sampai larutan kering diatas
hot-plate. Lalu didiinginkan kembali. Kemudian 25 ml air destilata, 1 ml asam nitrat pekat, dan 1 ml asam perklorat ditambahkan kedalam gelas piala yang sama. Larutan dididihkan sampai kering diatas hot-plate. Larutan didinginkan kembali. Setelah itu sisa larutan diambil kemudian dimasukkan ke
dalam 1 % asam hidroklorat (jika perlu disaring terlebih dahulu). Setelah itu sampel dimasukkan ke dalam instrumen spektrofotometri serapan atom (atomic absorption spectrofotometry).
Hasil analisis timbal pada cangkang kerang hijau kemudian dibandingkan dengan baku mutu Keputusan Menteri Lingkungan Hidup no 51 tahun 2004 sebesar 0.008 ppm. Sedangkan hasil analisis timbal pada daging kerang hijau dibandingkan dengan baku mutu Departemen Kesehatan tahun 1989 sebesar 2 ppm.
Hubungan Ukuran Tubuh Kerang Hijau dengan Konsentrasi Timbal pada Tubuh
Kerang hijau difoto untuk mendapatkan gambar sesuai aslinya. Kemudian dilakukan pengukuran morfologi yang meliputi pengukuran panjang cangkang, lebar cangkang, tebal cangkang, panjang hinge, bobot cangkang serta bobot jaringan lunak/daging dari kerang hijau tersebut berdasarkan Niswari (2004). Analisis korelasi dilakukan dengan menggunakan persamaan regresi berganda.
Analisis Kondisi Morfologi Kerang Hijau
Pengamatan bentuk morfologi dilakukan pada total 200 kerang hijau untuk mengetahui kelainan pada bentuk cangkangnya. Kerang hijau difoto lalu diamati kelainan yang ada pada cangkangnya, kemudian dilakukan kuantifikasi abnormalitas per stasiun (50 cangkang per stasiun).
HASIL
Pengambilan Sampel Kerang Hijau di Kamal Muara, Teluk Jakarta dan Penyimpanan
4
Tabel 1 Parameter fisika
0.008 ppm
Telah didapatkan kerang hijau sebanyak 40 organisme yang berasal dari keramba kerang hijau (Gambar 1) pada keempat stasiun yang digunakan untuk analisis konsentrasi timbal pada cangkang dan daging. Kemudian sebanyak 200 kerang hijau digunakan untuk analisis bentuk morfologi. Jumlah ini merupakan hasil yang didapatkan secara acak tanpa memperhatikan umur dan ukuran dari kerang hijau.
Parameter Fisika dan Kimia Air pada Perairan Kamal Muara, Teluk Jakarta
Beberapa dari parameter fisika dan kimia air dalam perairan Kamal Muara, Teluk Jakarta masih berada dibawah baku mutu pemerintah. Hanya sebagian dari parameter ini yang memiliki nilai diatas baku mutu pemerintah. Parameter tersebut adalah konsentrasi ammonia (NH-3), konsentrasi sulfida, logam timbal, logam tembaga, logam arsen dan logam seng. Konsentrasi logam tembaga yang melebihi baku mutu pemerintah hanya berada pada stasiun 3. Sedangkan untuk pembahasan mengenai logam timbal akan dijelaskan pada subbab selanjutnya.
Konsentrasi Logam Timbal pada Perairan Kamal Muara, Teluk Jakarta.
Konsentrasi timbal (Pb) pada keempat stasiun sudah melebihi batas baku mutu yang
, kimia perairan Kamal Muara, Teluk Jakarta
Paramater yang dujikan berdasarkan Keputusan Menteri Lingkungan Hidup No 51/ 2004 tentang Baku Mutu Air Laut untuk Biota Perairan
diijinkan oleh pemerintah didalam KEPMENLH NO 51 tahun 2004 (Gambar 2).
Gambar 2 Kisaran konsentrasi Pb pada perairan Kamal Muara, Teluk Jakarta (garis merah: baku mutu pemerintah)
Konsentrasi Logam Timbal di Jaringan Lunak dan Cangkang Kerang Hijau
5
Gambar 5 Grafik regresi perbandingan panjang cangkang dengan tebal cangkang (titik merah: ukuran normal cangkang; titik hijau: ukuran abnormal; garis hitam: garis regresi; garis merah: garis selang kepercayaan [95 %])
Gambar 6 Grafik regresi perbandingan panjang cangkang dengan tinggi cangkang (titik merah: ukuran normal cangkang; titik hijau: ukuran abnormal;
garis hitam: garis regresi; garis merah: garis selang kepercayaan [95 %])
Tebal Cangkang P a n ja n g C a n g k a n g 35 30 25 20 15 10 100 90 80 70 60 50 40 30 20 Regression 95% CI
Tinggi Cangkang P a n ja n g C a n g k a n g 45 40 35 30 25 20 15 110 100 90 80 70 60 50 20 40 30 Regression
95% CI
Konsentrasi logam timbal (Pb) pada daging Perna viridis (L) memiliki kisaran yang berbeda pada setiap stasiun. Konsentrasi timbal berturut-turut pada keempat stasiun adalah 3.40–11.70 ppm, 2.167–25 ppm, 11.625–25.6 ppm, 15.7–31.167 ppm (Gambar 4).
Hubungan Ukuran Tubuh Kerang Hijau dengan Konsentrasi Timbal pada Tubuh
Dari persamaan regresi berganda didapatkan persamaan untuk konsentrasi timbal pada cangkang; y1 = - 0.012 + 0.510 x1 - 0.336 x2 - 0.250 x3 + 0.318 x4 - 2.15 x5 - 0.48 x6 serta y2 = 30.1 + 0.027 x1 + 1.83 x2 - 0.91 x3 - 0.856 x4 + 2.02 x5 - 2.72 x6. Dimana X1 merupakan peubah untuk panjang cangkang (Lampiran 9), X2 peubah tebal cangkang, X3 tinggi cangkang, X4 peubah panjang hinge, X5 peubah bobot cangkang dan X6 bobot daging.
Analisis Kondisi Morfologi Kerang Hijau Didapatkan 4 kelainan (deformitas) pada total 200 cangkang kerang hijau yang diteliti. Rasio panjang/tinggi cangkang abnormal, rasio panjang/tebal cangkang abnormal, bentuk cangkang tumbuh 2 kali serta bentuk pinggir cangkang abnormal. Ukuran cangkang normal didapatkan dari hasil persamaan
regresi linier yang terdapat pada grafik di dalam Gambar 5 dan Gambar 6. Hasil kuantifikasi tersebut terdapat pada Tabel 2.
25 20 15 10 5 0
Ukuran cangkang normal pada gambar 5 dan 6 adalah titik-titik berwarna merah yang berada diantara garis berwarna merah (selang kepercayaan) pada grafik tersebut. Nilai ini hanya digunakan sebagai ukuran cangkang normal pada analisis abnormalitas cangkang yaitu, perbandingan panjang cangkang dengan tebal cangkang abnormal dan perbandingan panjang cangkang dengan tinggi cangkang abnormal.
Kelainan Tubuh Jumlah (%)
Stasiun1 Stasiun 2 Stasiun 3 Stasiun 4 1. Rasio P/Tinggi 82 % 66 % 72 % 76 % Abnormal
2. Rasio P/Tebal 78 % 80 % 86 % 86 % Abnormal
3. Cangkang tumbuh 26 % 18 % 10 % 12 % 2 kali
4. Bentuk pinggir 6 % 0 % 16 % 0 % Cangkang abnormal K o n s e n tr a s i P b ( p p m ) 0.008 St asiun_4_D St asiun_3_D St asiun_2_D St asiun_1_
Stasiun 1 Stasiun 2 Stasiun 3 Stasiun 4
Tabel 2 Kelainan pada tubuh kerang hijau pada stasiun pengamatan
K o n s e n tr a s i (p p m ) 35 30 25 20 15 10 5 0 Stasiun 4 Stasiun 3 Stasiun 2 Stasiun 1 2
Gambar 3 Kisaran konsentrasi Pb pada cangkang Perna
viridis (L) (garis merah: baku mutu pemerintah)
Gambar 4 Kisaran konsentrasi Pb pada daging Perna
6
PEMBAHASAN
Kondisi Perairan Kamal Muara, Teluk Jakarta
Perairan teluk Jakarta termasuk dalam zona perairan fotik, dimana perairan ini merupakan kawasan perairan pelagik yang masih mendapatkan cahaya matahari Teluk Jakarta juga merupakan perairan yang tergolong dalam perairan estuaria (Nybakken 1982). Hal ini ditandai adanya peralihan dan pertemuan antara air tawar yang berasal dari sungai sekitar daerah di Jakarta dengan air laut yang berasal dari laut Jawa. Suhu pada daerah ini lebih bervariasi. Hal ini disebabkan masukkan air yang berasal dari sungai di Jakarta membuat suhu lebih cepat panas dan lebih cepat dingin (Nybakken 1982). Arus air pada daerah ini dipengaruhi oleh kegiatan pasang surut dan aliran sungai. Ada sekitar 15 sungai yang bermuara di Teluk Jakarta (Diniah 1995) Kekeruhan pada teluk Jakarta disebabkan oleh padatan tersuspensi yang berasal dari sungai. Beberapa sifat tersebut mendukung mobilitas bahan pencemar di perairan Kamal Muara, Teluk Jakarta.
Industri yang terdapat di sekitar muara Teluk Jakarta banyak menyumbang bahan pencemar, salah satunya logam timbal, yang masuk ke sungai yang kemudian bermuara di teluk. Industri itu antara lain; industri kimia, petroleum dan bahan kimia sebanyak 353 pabrik; industri bahan galian bukan logam sebanyak 41 logam; industri dasar logam 38 pabrik;industri barang–barang dari logam, mesin 322 pabrik (Anggraeni 2002).
Parameter Fisika dan Kimia Air pada Perairan Kamal Muara, Teluk Jakarta
Pada beberapa parameter sifat fisik dan kimia perairan Muara Kamal, Teluk Jakarta ada yang telah melebihi baku mutu air laut berdasarkan keputusan Menteri Lingkungan Hidup no 51 tahun 2004. Parameter tersebut adalah, amonia, sulfida, logam tembaga, logam kromium, logam arsen dan logam seng. Konsentrasi amonia (NH3) yang tinggi
disebabkan oleh limbah domestik, limbah industri, limbah peternakan dan pupuk (Saeni 1989). Hal ini terbukti dari kondisi sekitar perairan Kamal Muara di teluk Jakarta yang dipadati oleh perumahan penduduk dan industri. Tingkat konsentrasi amonia yang tinggi dapat meracuni organisme yang hidup di perairan. Daya racun ini meningkat seiring dengan meningkatnya pH dan suhu serta konsentrasi CO2 yang rendah di perairan
(Anggraeni 2002).
Konsentrasi sulfida di perairan merupakan hasil dari buangan industri, misalnya gips. Menurut Saeni (1989) pada daerah yang memiliki pencemaran udara berat, khususnya karena gas SOx, akan mengalami peningkatan konsentrasi sulfida dalam perairannya. Tetapi hal ini bukan penyebab tingginya konsentrasi sulfida di teluk Jakarta, karena berdasarkan laporan gubernur DKI Jakarta tahun 2005 konsentrasi gas SO2 pada propinsi DKI
Jakarta masih di bawah baku mutu pemerintah.
Sumber dari logam kromium dalam perairan adalah bijih tambang, baja antikarat, logam alloy (campuran) dan pigmen yang terlarut dalam perairan. Pabrik yang berbahan bakar fosil dan pabrik semen juga menyumbang sejumlah kromium kedalam lingkungan perairan (Lu 1995). Hal ini dibuktikan dengan banyaknya pabrik di sekitar teluk Jakarta yang masih memakai bahan bakar fosil serta ada 38 pabrik yang merupakan pengolah bahan dasar logam (Anggraeni 2002).
Sumber dari logam arsen di lingkungan adalah salah satunya industri peleburan tembaga dan pestisida yang mengandung arsen. Efek dari paparan arsen pada manusia adalah sirosis pada hati (Lu 1995).
Logam seng merupakan logam penting yang dibutuhkan oleh tubuh Konsentrasi yang berlebih tidak akan menginduksi efek toksik pada manusia (Lu 1995).
Menurut Yap (2004) tembaga merupakan salah satu logam penyebab penyakit Parkinson apabila logam tersebut terpapar secara kronis pada suatu lingkungan.
Konsentrasi logam timbal yang berlebih juga dapat menyebabkan penyakit Parkinson. Hal ini dikarenkan timbal dapat menghambat neurotransmiter yang diperlukan oleh sel syaraf. Pembahasan mengenai logam ini akan dijelaskan secara rinci pada subbab selanjutnya.
Konsentrasi Logam Timbal pada Perairan Kamal Muara, Teluk Jakarta
7
konsentrasi Pb pada kolom air masih berada pada taraf yang aman. Hal ini dimungkinkan stasiun 4 sudah mendekati bagian terluar dari Teluk Jakarta. Arus, pH, suhu juga mempengaruhi mobilitas zat pencemar didaerah stasiun 4 ini. Oleh karena itu pencemaran logam timbal tidak terdeteksi di stasiun ini. Hal ini yang menyebabkan analisis timbal pada perairan tidak dapat dijadikan acuan tunggal untuk menentukan tingkat pencemaran timbal dan zat polutan lain secara umum.
Perbedaan konsentrasi timbal pada tiga stasiun pertama dengan stasiun ke-4 disebabkan juga karena dalam pengambilan sampel air dilakukan hanya sekali dan tidak secara berkala (time series). Hal ini disebabkan karena pada pengambilan sampel secara berkala dapat diperoleh data yang lebih akurat mengenai kondisi kimia perairan.
Konsentrasi timbal yang tinggi disebabkan banyaknya industri yang beroperasi di sekitar muara kamal Jakarta. Beberapa industri penyumbang timbal yang beroperasi antara lain; PLTU, industri pembuat bahan kimia, industri tekstil, industri logam dan pengolahannya. Industri-industri ini jika tidak memiliki IPAL (Instalasi Pengolahan Air Limbah) dapat menyumbang timbal ke dalam perairan. Anggraeni (2002) mengidentifikasi ada sekitar 2.276 industri pada tahun 1999 di Jakarta. Sebagian besar diduga penyumbang bahan pencemar berupa logam, yaitu industri dasar logam, industri pengolahan logam, mesin dan perlengkapannya. Pada tahun 2002 jumlah industri besar dan sedang pada kotamadya Jakarta Utara berjumlah 777 industri. Menurut WALHI (2004) hanya 10 persen dari 200 perusahaan di Jakarta yang memiliki IPAL. Hal inilah yang mendukung banyaknya bahan pencemar lolos ke sungai tanpa pengolahan lebih lanjut, yang nantinya akan bermuara di Teluk Jakarta.
Pada stasiun 2 dan 3 juga memiliki konsentrasi timbal (Pb) yang diatas baku mutu pemerintah. Hal ini menunjukkan pencemaran di Teluk Jakarta sudah mencapai jarak yang cukup jauh dari garis pantai/muara.
Kondisi perairan yang tercemar dapat juga dideteksi dari sedimen yang berada pada dasar perairan. Oleh karena itu kemungkinan tingginya konsentrasi pada 3 stasiun pertama disebabkan oleh resuspensi sedimen perairan. Hal ini diperkuat pernyataan Diniah (1995), konsentrasi timbal (Pb) pada sedimen pada beberapa stasiun di teluk Jakarta berkisar antara 0.84–6.820 ppm. Sedangkan Gillikin (2005) menyatakan sumber timbal pada
perairan juga berasal dari proses pelongsoran tanah (run off) yang kemudian terbawa oleh arus sungai ke teluk akibat hujan.
Konsentrasi Logam Timbal di Jaringan Lunak dan Cangkang Kerang Hijau
Penggunaan cangkang kerang hijau sebagai indikator pencemar, khususnya logam berat sudah banyak dipakai (Yap 2003). Konsentrasi timbal (Pb) pada cangkang kerang hijau pada keempat stasiun pengamatan sudah berada diatas baku mutu yang ditetapkan oleh pemerintah. Hal ini dikarenakan struktur matriks dari cangkang memiliki afinitas yang besar terhadap logam timbal (Yap 2003). Menurut Gillikin (2005) perbandingan antara Pb/Ca pada cangkang bivalvia Mercenaria mercenaria tinggi. Hal ini disebabkan proses pembentukan CaCO3
cangkang terganggu akibat logam timbal. Tingginya konsentrasi timbal pada cangkang kerang hijau juga disebabkan karena pada proses kalsifikasi, cangkang menyerap Ca dari lingkungan. Jika pada lingkungan konsentrasi logam lain lebih besar maka logam tersebut akan terserap juga pada proses kalsifikasi dari cangkang kerang hijau (Yap 2003).
Hal ini sesuai dengan hasil yang didapatkan, yaitu semua cangkang dan daging memiliki konsentrasi timbal yang tinggi diatas baku mutu pemerintah yang ditentukan . Hal ini juga membuktikan selama hidupnya kerang hijau pada Kamal Muara, Teluk Jakarta telah mengakumulasi logam timbal pada cangkangnya secara berlebih.
Penggunaan daging kerang hijau bertujuan untuk memberikan informasi konsentrasi logam timbal terkait dengan kesehatan lingkungan. Pada keempat stasiun kosentrasi logam timbal pada daging kerang hijau sudah melewati batas baku mutu yang ditetapkan oleh Departemen Kesehatan tahun 1989 sebesar 2 ppm. Logam timbal masuk kedalam organisme laut dengan tiga cara, yaitu melalui rantai makanan, insang dan difusi melalui permukaan kulit (Fitriati 2004). Sebagian besar logam timbal masuk kedalam kerang hijau melalui rantai makanan dan air.
Bioakumulasi terjadi karena logam berat yang masuk ke tubuh kerang hijau membentuk senyawa kompleks dengan zat-zat organik yang terdapat organ tubuh, khususnya organ pencernaan, reproduksi dan insang (Yap 2004).
8
Gambar 7 Kelainan pada cangkang (abnormalitas). A rasio panjang/tinggi abnormal (garis merah:
cangkang normal, panah: cangkang abnormal). B rasio panjang/tebal abnormal (1: normal, 2: abnormal). C bentuk pinggir cangkang abnormal (panah: bentuk pinggir cangkang abnormal). D bentuk cangkang seperti tumbuh 2 kali (panah: cangkang bertingkat)
cangkang. Hal ini dikarenakan proses masuknya timbal pada daging dapat melalui air dan makanan. Sedangkan proses masuk logam Pb pada cangkang hanya berasal dari air. Berdasarkan hasil penelititan Yap (2003) pada 2 hari paparan timbal cangkang kerang hijau mampu mengakumulasi 41 ppm timbal dan 220 ppm pada daging. Hal ini menunjukkan daging kerang hijau memiliki kemampuan untuk menyerap timbal secara cepat. Lalu menurunnya akumulasi disebabkan oleh faktor fisiologi dari kerang hijau seperti, kemampuan mengeliminasi logam, kecepatan makan dan laju akumulasi dan depurasi (Yap 2003).
Hal tersebut menjelaskan perbedaan kisaran konsentrasi timbal yang ada pada setiap cangkang dan daging. Perbedaan daya akumulasi ini juga dikarenakan kerang hijau yang digunakan memiliki ukuran yang tidak sama. Sesuai dengan penelitian Jumariyah (2001) yang menyebutkan bahwa kerang hijau yang berukuran kecil memiliki kemampuan akumulasi lebih tinggi daripada ukuran yang lebih besar.
Hubungan Ukuran Tubuh Kerang Hijau dengan Konsentrasi Timbal pada Tubuh
Persamaan Y1 tersebut menunjukkan hasil yang tidak signifikan (nilai P untuk semua peubah > 0.05) (Mattjik 2002), dan permodelan yang kurang bagus (R2 = 26.5 %). Nilai korelasi antar peubah juga tinggi. Hal ini ditunjukkan dari nilai VIF (variance inflation factors) yang diatas angka 10. Oleh karena itu dilakukan analisis bertatar forward untuk memilih peubah bebas yang dapat menerangkan persamaan.
Hasil analisis regresi bertatar forward
menunjukkan peubah bobot cangkang dan panjang cangkang secara signifikan (P= 0.006 dan 0.041) mempengaruhi konsentrasi timbal pada cangkang. Tetapi untuk model persamaan yang digunakan masih kurang tepat dikarenakan nilai dari R2 menunjukkan angka 24.9 %. Hal ini disebabkan model persamaan dapat digunakan apabila memiliki nilai R2 lebih dari 50 %.
9
Hasil analisis regresi forward
menunjukkan peubah bobot daging secara signifikan (P=0.022) mempengaruhi konsentrasi timbal pada cangkang. Tetapi untuk model persamaan yang digunakan masih kurang tepat (R2 = 13.1 %).
Berdasarkan persamaan tersebut didapatkan bahwa semakin besar bobot daging maka semakin kecil konsentrasi timbal dalam daging kerang hijau. Hal ini dikarenakan kerang yang berukuran kecil memiliki kemampuan akumulasi lebih besar dibandingkan kerang berukuran besar (Jumariyah 2001).
Kondisi Abnormal Morfologi Kerang Hijau
Kondisi abnormal ini telah dialami oleh kerang hijau di setiap stasiun. Hal ini ditunjukkan dari banyaknya (dalam persen) cangkang yang mengalami abnormalitas (Tabel 2).
Menurut Lu (1995) TEL yang berada di lingkungan berasal dari larutan bahan bakar kendaraan bermotor dan senyawa ini adalah salah satu senyawa timbal yang mencemari perairan. Larva dari tiram Crassostrea gigas (Kelas Bivalvia) menunjukkan perbedaan panjang tubuh rata-rata sebesar 1 mm lebih pendek daripada tiram kontrol selama 14 hari terpapar Pb(NO )/Pb Nitrat 3 (WHO 1989).
Perubahan yang terjadi pada morfologi kerang hijau pada penelitian (Gambar 5) ini di setiap stasiun diduga disebabkan oleh timbal organik, salah satunya oleh cemaran timbal tetraetil/tetraethyl lead (TEL) yang berasal dari perahu yang melintas di permukaan air teluk Jakarta dan juga berasal dari pencemaran udara yang berdifusi ke kolom air. Oleh karena itu apabila kerang hijau (Kelas Bivalvia) terpapar timbal organik tersebut selama pertumbuhan dan perkembangan tubuhnya diduga akan terjadi kelainan bentuk tubuh yang sangat signifikan (berbeda) seperti yang terjadi pada penelitian ini.
Hal ini didukung pula oleh penelitian European Commision (2002) yang menyatakan bahwa konsentrasi timbal pada tingkat tertentu dapat mengakibatkan kelainan bentuk (deformity) pada tulang belakang dari ikan. Semua kondisi diatas tersebut membuktikan bahwa timbal organik adalah salah satu logam pencemar yang dapat mengubah bentuk dari suatu organisme. Hal ini juga menunjukkan morfologi kerang hijau dapat dijadikan biomarker yang lebih akurat
untuk mengetahui tingginya pencemaran timbal pada perairan Kamal Muara.
SIMPULAN
Kualitas air pada perairan Kamal Muara, Teluk Jakarta sudah melewati batas baku mutu pemerintah, khususnya parameter logam timbal berdasarkan KEPMENLH no 51/2004. Konsentrasi logam timbal pada tubuh kerang hijau (Perna viridis (L)) dari Kamal Muara, Teluk Jakarta sudah melewati batas baku mutu pemerintah (DEPKES 1989 untuk baku mutu di dalam daging dan KEPMENLH 2004 untuk baku mutu dalam cangkang). Hal ini dilihat dari konsentrasi timbal pada cangkang dan daging. Hal ini menunjukkan daging kerang hijau pada ukuran tertentu tidak layak untuk dikonsumsi.
Bobot cangkang, panjang cangkang, dan bobot daging merupakan penanda biologis (biomarker) pencemaran timbal di Kamal Muara, Teluk Jakarta. Hal ini ditunjukkan pada pertambahan bobot cangkang dan bobot daging yang diikuti oleh penurunan konsentrasi timbal didalam keduanya.
Kelainan morfologi yang terdapat pada kerang hijau juga menunjukkan bahwa hewan ini dapat dijadikan indikator pencemaran timbal di lingkungan. Abnormalitas ini diduga disebabkan oleh konsentrasi timbal organik yang melebihi baku mutu. Hal tersebut diatas menunjukkan bahwa uji biologis lebih baik dalam menggambarkan kondisi suatu lingkungan dibandingkan dengan uji kimiawi.
SARAN
Metode pengambilan sampel harus lebih akurat karena pada pengambilan sampel air harus dilakukan pada waktu yang bersamaan dan dilakukan secara berkala (time series). Perlu dilakukan penelitian dengan pengambilan sampel yang mewakili kondisi semua bagian perairan Teluk Jakarta. Perlu dilakukan perbandingan antara uji time series
dan uji laboratorium. Hal ini akan memberikan gambaran yang akurat akan laju akumulasi dan depurasi (proses penghilangan senyawa) dari logam berat secara umum pada tubuh kerang hijau. Perlu dilakukan uji biomarker dan analisis lanjutan terhadap logam berat yang lain. Perlu dilakukan uji/analisis bahan pencemar logam berat pada
10
biomarker dapat bersinergi untuk memberikan kesimpulan yang lebih akurat.
DAFTAR PUSTAKA
Adamson L. 2002. Anti-fouling systems. London: International Maritime Organization.
Anggraeni I. 2002. Kualitas Air Perairan Laut Teluk Jakarta Selama Periode 1996 – 2002. [skripsi]. Bogor: Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Camusso M, Vigano L, Balestrini R. 1995. Bioconcentration of Trace Metals in Rainbow Trout: A Field Study.
Ecotoxicology and Environmental Safety
31: 133-141.
Colognesi M et al. 1997. Flow injection determination of Pb and Cd traces with graphite furnace atomic absorption spectrometry. Talanta 44: 867-875
Diniah. 1995. Korelasi Antara Kandungan Logam Berat Hg, Cd dan Pb Pada Beberapa Ikan Konsumsi Dengan Tingkat Pencemaran Di Perairan Teluk Jakarta. [Tesis]. Bogor: Program Pascasarjana, Institut Pertanian Bogor.
[EC] European Commision. 2002. Heavy Metal in Waste. Denmark: EC.
Fitriati M. 2004. Bioakumulasi Logam Raksa (Hg), Timbal (Pb), dan Kadmium (Cd) Pada Kerang Hijau (Perna viridis) yang Dibudidaya di Perairan Pesisir Kamal dan Cilincing Jakarta. [Tesis]. Bogor: Program Pascasarjana, Institut Pertanian Bogor.
Gillikin DP et al. 2005. Inter-and intra-annual variations of Pb/Ca ratios in clam shells (Mercenaria mercenaria): A record of anthropogenic lead pollution?. Marine Pollution Bulletin, in press.
Jumariyah. 2001. Kandungan Logam Berat Kadmium (Cd), Timbal (Pb) dan Tembaga (Cu) pada Kerang Hijau (Perna viridis L.) di Teluk Banten. [skripsi]. Bogor: Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Lu FC. 1995. Toksikologi Dasar: asas, organ sasaran, dan penilaian risiko. Edi Nugroho, penerjemah. Jakarta: UI Press. Terjemahan dari: Basic Toxicology: fundamentals, target organs, and risk assessment.
Mattjik AA, Sumertajaya IM. 2002.
Perancangan Percobaan dengan Aplikasi SAS dan Minitab Jilid 1. Bogor: IPB PRESS.
Muda I. 2003. Toksisitas Logam Berat Timbal (Pb) Terhadap Ikan Bandeng (Chanos chanos Forskal) pada Salinitas Yang Berbeda [skripsi]. Bogor: Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Niswari AP. 2004 Studi Morfometrik Kerang Hijau (Perna viridis, L.) Di Perairan Cilincing, Jakarta Utara [skripsi]. Bogor: Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Nursita IA, Singh B, Lees E. 2005. The effects of cadmium, copper, lead, and zinc on the growth and reproduction of
Proisotoma minuta Tullberg
(Collembola). Ecotoxicology and
Environmental Safety 60: 306–314.
Nybakken JW. 1982. Biologi Laut: suatu pendekatan ekologis. Jakarta: PT Gramedia Pustaka Utama.
Pain DJ. 1997. Lead in Waterfowl [ catatan penelitian ]. Ecotoxicology and Environmental Safety 60:147
Rabitto IS et al. 2005. Effects of dietary Pb(II) and tributylin on neo tropical fish,
Hoplias malabaricus: hitopathological and biochemical findings. Ecotoxicology and Environmental Safety 60: 147-156.
Setyobudiandi I. 2004. Beberapa Aspek Biologi Reproduksi Kerang Hijau Perna viridis Linnaeus, 1978 Pada Kondisi Perairan Berbeda. [disertasi]. Bogor: Sekolah Pascasarjana, Institut Pertanian Bogor.
11
bah_teljkt_250504. html [Desember 2004]
Walker CH, Hopkin SP, Sibly RM, Peakall DB. 2001. Principles of Ecotoxicology. New York: Taylor & Francis Inc.
[WHO] World Health Organization. 1972.
Evaluation of Mercury, Lead , Cadmium and the Food Additives Amaranth, Diethylpyrocarbonate and Octyl Gallate.
Geneva: WHO.
[WHO] World Health Organization. 1989.
Environmental Health Criteria 85, Lead-Environmental Aspects. Geneva: WHO.
Yap et al. 2003. Can the shell of the green-lipped mussel Perna viridis from the west coast of Peninsular Malaysia be a potential biomonitoring material for Cd, Pb and Zn? Estuarine, Coastal and Shelf Science 57: 623-630
——.2004. Heavy metal (Cd, Cu, Pb, and Zn) concentrations in the green-lipped mussel Perna viridis (Linnaeus) collected from some wild and aquaculture sites in the west coast of Peninsular Malaysia.
13
Lampiran 1 Peta stasiun pengamatan
06
06””0404’’.921 LS.921 LS 106
106””4444’’480 BT480 BT
06
06””0404’’. 831 LS. 831 LS 106
106””4444’’906 BT906 BT 06
06””0404’’. 213 LS. 213 LS 106
106””4545’’180 BT180 BT 06
06’’0202””.090 LS.090 LS 106
106’’4444””090 090 BTBT
06
06””0404’’.921 LS.921 LS 106
106””4444’’480 BT480 BT
06
06””0404’’. 831 LS. 831 LS 106
106””4444’’906 BT906 BT 06
06””0404’’. 213 LS. 213 LS 106
106””4545’’180 BT180 BT 06
06’’0202””.090 LS.090 LS 106
106’’4444””090 090 BTBT
Lampiran 2 Profil cangkang bivalvia secara umum
Pertambahan pertumbuhan tahunan
Garis pertumbuhan
Lapisan luar
Lapisan tengah
Lapisan dalam
(Gillikin 2005)
Lampiran 3 Profil jaringan lunak kerang hijau
14
Lampiran 4 Data aspek morfometrik dan kandungan timbal kerang dari 4 stasiun
Stasiun No A B C D E F G H
I 1 68.74 21.44 29.42 30.48 8.352 6.599 0.1 6.4
I 2 77.4 23.32 34.65 31.04 11.202 10.317 1.8 11.7
I 3 77.59 21.17 36.87 37.28 11.954 7.34 1.4 11
I 4 77.03 24.86 35.93 36.68 11.273 8.701 <0.001 4
I 5 74.91 22.91 31.37 36.57 10.861 9.72 <0.001 3.4
I 6 77.89 23 32.95 32.18 10.319 8.049 1.8 11.4
I 7 65.61 18.89 31.43 28.95 8.435 6.323 5.5 5.1
I 8 70.79 21.6 32.18 34.09 8.019 8.639 6.05 3.8
I 9 75.01 21.68 33.94 32.61 9.036 7.843 19.65 5.6
I 10 66.83 21.44 29.56 31.75 8.196 6.837 21.35 5.2
II 1 44.74 14.29 20.42 20.99 2.861 2.706 22.65 2.167
II 2 45.29 13.8 22.43 19.16 3.38 3.159 12.85 17.375
II 3 43.82 15.1 21.13 18.76 3.083 2.472 <0.001 19.5
II 4 47.79 13.87 22.94 20.36 2.871 3.683 <0.001 12.667
II 5 47.5 14.2 21.34 20.53 2.968 3.121 15.45 18.375
II 6 44.66 13.44 22.28 21.44 3.231 2.685 15.45 8.5
II 7 55.66 16.86 25.84 24.55 4.735 4.198 15.3 14.5
II 8 45.69 12.83 21.66 21.23 2.938 2.427 15.15 18.125
II 9 40.61 12.53 20.55 21.71 2.663 2.193 9.9 2.667
II 10 45.85 13.44 21.81 21.08 2.679 2.633 8.4 25
III 1 60.5 17.06 28.01 24.95 5.732 3.864 12.1 11.625
III 2 68.97 21.54 31.91 34.59 5.864 4.623 17.45 17.2
III 3 61.72 19.22 25.34 28.81 5.895 4.109 14.95 23
III 4 56.55 15.26 23.75 24.78 4.965 3.235 13.5 20.3
III 5 59.09 16.67 25.94 27.26 5.314 4.186 11.75 18.2
III 6 69.46 20.7 30.96 27.38 7.227 6.181 18.35 21
III 7 57.1 16.95 26.55 24.14 4.643 3.353 14.25 19.5
III 8 59.61 17.42 25.43 25.87 5.025 4.568 9.5 25.6
III 9 54.24 15.58 24.88 23.03 4.105 3.211 13.85 18.4
III 10 64.3 18.46 26.69 25.85 5.895 4.337 15.05 22.5
IV 1 45.83 17.06 24.81 24.41 4.976 3.464 9.85 30
IV 2 65.11 20.34 29.55 30.39 8.213 7.435 10.85 15.7
IV 3 62.48 18.67 28.48 28.9 7.132 6.26 10.45 22.5
IV 4 53.05 16.3 24.48 24.51 4.526 4.112 8.9 20
IV 5 64.92 22.89 31.06 31.32 9.795 8.123 7.7 26.9
IV 6 78.27 22.61 32.82 35.8 11.604 9.49 7.9 20.2
IV 7 57.32 25.06 27.62 29.23 4.42 3.339 8.55 22.9
IV 8 71.26 23.37 31.02 32.85 10.504 9.104 7.4 18.7
IV 9 43.21 15.14 21.21 21.85 2.962 2.029 9.35 23.875
IV 10 40.32 14.48 20.69 20.25 2.409 1.976 10.35 31.167
A : Panjang Cangkang D : Panjang Hinge G : Konsentrasi timbal di cangkang
B : Tebal Cangkang E : Bobot Cangkang H : Konsentrasi timbal di daging
15
Lampiran 5 Grafik Kenormalan Galat Konsentrasi Timbal
RESI 2
P
e
rc
e
n
t
20 10
0 - 10
- 20
99
95 90
80 70 60 50 40 30 20
10 5
1
M ean
> 0.150 - 2.30038E- 14 StD ev 6.907
N 4
KS 0.096
P- Valu e
R e si dua l Konse nt r a si D a ging N or ma l it y Te st
Nor m al
0
Test Normalitas berdasarkan Kolmogorov-Smirnov Jumlah N= 40
Nilai Dhitung (KS) = 0.096, nilai D tabel= 0.165 Ho: Data galat normal
Dhitung < Dtabel : terima Ho P-value > 0.150 : signifikan
RESI 1
P
e
rc
e
n
t
15 10
5 0
-5 - 10
99
95
90
80
70
60 50 40 30
20
10
5
1
Mean
> 0.150 - 7.86038E- 15
StDev 5.312
N 4
KS 0.107
P- Valu e Residual Konsentr asi Cangkang N or mality Test
Nor m al
0
Test Normalitas berdasarkan Kolmogorov-Smirnov Jumlah N= 40
Nilai Dhitung (KS) = 0.107, nilai D tabel= 0.165 Ho: Data galat normal
16
Lampiran 6 Analsis Regresi Linier Berganda pada konsentrasi Pb di cangkang
Peubah Bebas Coef SE Coef T P VIF R-sq Panjang Cangkang (x1) 0.5101 0.3160 1.61 0.116 17.0 26.5% Tebal Cangkang (x2) -0.3358 0.6397 -0.52 0.603 6.7
Tinggi Cangkang (x3) -0.2503 0.8051 -0.31 0.758 17.2 Panjang Hinge (x4) 0.3181 0.5680 0.56 0.579 11.3 Bobot Cangkang (x5) -2.155 1.454 -1.48 0.148 22.5 Bobot Daging (x6) -0.479 1.317 -0.36 0.718 12.8 tercetak tebal: tidak signifikan pada α = 0.05
Hasil Regresi forward
Peubah Bebas Coef SE Coef T P VIF R-sq
Konstanta (α) -1.232 8.034 -0.15 0.879
Bobot Cangkang (x5) -2.5355 0.8617 -2.94 0.006 8.7 24.9% Panjang Cangkang (x1) 0.4561 0.2153 2.12 0.041 8.7
Tercetak tebal: signifikan pada taraf α= 0.05
Lampiran 7 Analisis Regresi Linier berganda pada konsentrasi Pb di daging
Peubah Bebas Coef SE Coef T P VIF R-sq
Panjang Cangkang (x1) 0.0267 0.4109 0.06 0.949 17.0 25.7% Tebal Cangkang (x2) 1.8319 0.8317 2.20 0.035 6.7
Tinggi Cangkang (x3) -0.910 1.047 -0.87 0.391 17.2 Panjang Hinge (x4) -0.8557 0.7385 -1.16 0.255 11.3
Bobot Cangkang (x5) 2.015 1.890 1.07 0.294 22.5
Bobot Daging (x6) -2.720 1.713 -1.59 0.122 12.8
tercetak tebal: tidak signifikan pada α = 0.05
Hasil Regresi forward
Peubah Bebas Coef SE Coef T P R-sq
Konstanta (α) 21.869 2.767 7.90 0.000
Bobot Daging (x6) -1.1567 0.4830 -2.40 0.022 13.1%
Tercetak tebal: signifikan pada taraf α= 0.05
Lampiran 8 Klasifikasi Nama Ilmiah Kerang Hijau (Perna viridis Linn)
Filum : Mollusca
Kelas : Bivalvia
Sub Kelas : Lamelibranchiata Super Ordo : Filibranchia
Ordo : Arisomiria
Famili : Mytilidae
Genus : Perna
Spesies : Perna viridis Linn
Nama Umum : Kerang Hijau (Green Mussel)
(Vakily 1989 diacu dalam Setyobudiandi 2004)
Lampiran 9 Metode Analsis Parameter Fisika dan Kimia Perairan
Suhu
1. Celupkan termometer kedalam perairan 2. Tunggu beberapa menit
3. Angkat termometer
17
Sampah
1. Lihat secara visual mata
pH
1. Celupkan kertas pH ke dalam perairan 2. Cocokan dengan trayek pH yang ada
Oksigen Terlarut
1. Ambil sampel → botol DO 125 cc (penuh, no bubbles) 2. Tambah ½ ml (10 tetes) MnSO4
3. Tambah ½ ml (10 tetes) NaOH+KI. Tutup, aduk (diamkan sampai mengendap) 4. + ½ ml H2SO4 (sampai larut)
5. Pipet 50 ml air contoh → erlenmeyer 6. Titrasi → Na-tiosulfat → kuning muda 7. + amilum → titrasi → tak berwarna 8. Catat ml titran yang terpakai
Konsentrasi DO = (V.N) Na2SO3 x be O2 x 1000 V contoh x V botol / (v botol-4 ml)
BOD 5
1. Ambil sampel → 1-2 liter
2. (apabila keruh) encerkan sampel 2-3 x akudes bebas biota 3. (apabila jernih) aerasi sampel → O2 meningkat (sbg cadangan)
4. Bagi air menjadi 2: a. pindahkan ke botol terang; b. pindahkan ke botol gelap 5. Botol terang → analisis DO
6. Botol gelap → + nutrien (3 tetes) , buffer fosfat, MgSO4, CaCl2, FeCl2. 7. Inkubasi 5 hari (suhu 20 oC)
8. Setelah 5 hari → analisis DO
Total Fosfat
1. 50 ml sampel → mikrokjedahl. + 1 ml H2SO4 pekat, 5 ml HNO3 pekat. Pemanasan 2. STOP → larutan tidak berwarna
3. Dinginkan, + 20 ml air suling, 1 tetes indikator pp, 1 ml NaOH 1M → larutan berwarna merah muda.
4. Pindahkan larutan ke dalam gelas ukur 100 ml. + air suling → volume larutan menjadi 100 ml
5. Pipet 50 ml → 100 ml erlenmeyer 6. + 2 ml Ammonium molibdat-asam sulfat 7. + 5 tetes larutan SnCl2 → kocok
8. Bandingkan biru sampel dengan larutan standar.
Ammonia
1. Saring sampel dengan milipore
2. Pipet 50 ml sampel → gelas piala 50 ml
3. + 1 ml pereaksi Nessler. Kocok, biarkan 10 menit 4. Ukur absorbansi larutan
Nitrit
1. Pipet 50 ml sampel (sudah disaring) 2. + 1 ml larutan sulfanilamid
3. Biarkan selama 2menit
4. + 1 ml larutan N-(1-naftil)-etilendiammin dihidroklorida, kocok 5. Diamkan 10 menit
18
Sulfida
1. Isi penuh botol BOD ukuran 100 ml dengan air contoh
2. Tambahkan 1 ml MnCl2 dan tutuplah botol BOD dan ratakan campuran dengan
membalikkan botol berulang-ulang
3. Tambahkan 1 ml NaOH-KI, kemudian tutuplah botol dan ratakan campuran dengan membalikkan botol berulang-ulang
4. Biarkan sampai pengendapan terjadi sempurna
5. Buka botol dan buang air jernih dalam botol sebanyak 11 ml dengan pipet 6. Tambahkan 10 ml larutan iodate dengan pipet
7. Tambahkan 1 ml H2SO4 dengan segera dan ratakan campuran dengan membalikkan botol
berulang-ulang setelah botol ditutup
8. Ambil 50 ml air dari botol dan tuangkan dalam sebuah erlenmeyer ukuran 100 ml
9. Titrasi dengan Na2S2O3 sampai terjadi perubahan warna kuning menjadi kuning pucat,
lalu tambahkan 1 tetes amilum dan teruskan titrasi sampai terjadi perubahan warna biru menjadi tidak berwarna (Catat volume total Na2S2O3 sebelum dan sesudah titrasi)
10. Tentukan nilai dengan rumus H2S (ml/l) = 223.92 x f (a-b)
V-2
Kekeruhan
A. Pembuatan Kurva Kalibrasi
1. siapkan 6 buah labu takar 100 ml bersih dan kering
2. Isilah 6 labu tersebut dengan larutan SiO2 100 ppm sebagai berikut:
Kekeruhan (ppm SiO2) Volume Larutan SiO2 100 ppm yang harus
diambil (ml)
2 2 5 5 10 10 20 20 50 50 70 70
3. Tambahkan ke dalam 6 tabung tadi dengan air destilata kemudian ditera sampai 100 ml. 4. Penentuan dilakukan dengan metode fotometrik yang menggunakan alat turbidimeter
a. Cabutlah cell holder. Tabung yang lebih dalam diisi dengan air destilata sebagai blanko dan tabung bagian luar diisi dengan larutan standar yang telah dibuat
b. Masukkan cell holder ke dalam tempatnya, sedemikian rupa sehingga sel yang mengandung air destilata tepat dilalui cahaya.
c. Aturlah zero knob, sehingga skala menunjukkan posisi nol pada waktu posisi air destilata dilalui cahaya.
d. Masukkan larutan standar ke posisi lebih dalam, sehingga dilalui cahaya e. Bacalah skala turbidimeter
f. Setelah pengukuran selesai, cuci dan bilaslah sel itu sampai bersih
g. Catatlah nilai skala transmitan dari larutan standar. Plot kekeruhan pada sumbu x dan nilai skala transmitan sebagai sumbu y. Buatlah garis linear dari kedua hubungan itu.
B. Penentuan Contoh
1. Dengan cara yang sama lakukan pengukuran contoh air 2. Plot kekeruhan pada kurva kalibrasi
Pengukuran Logam Terlarut
1. Masukkan 100 ml air sampel ke dalam gelas piala. Lalu 2. Tambahkan kristal NaSO4 (sodium sulfat).
3. Setelah itu tambahkan 1 ml asam sulfat pekat ke dalam gelas piala tersebut. 4. Panaskan campuran tersebut diatas hot-plate, kemudian didihkan.
5. Sampel tersebut lalu didiinginkan sebentar.
19
7. Didihkan sampel sampai larutan kering diatas hot-plate. 8. Lalu didiinginkan kembali.
9. Kemudian tambahkan 25 ml air destilata, 1 ml asam nitrat pekat, dan 1 ml asam perklorat kedalam gelas piala yang sama.
10. Larutan dididihkan sampai kering diatas hot-plate. 11. Larutan didinginkan kembali.
12. Setelah itu ambil sisa larutan kemudian masukkan ke dalam 1 % asam hidroklorat (jika perlu disaring terlebih dahulu). Setelah itu sampel dimasukkan ke dalam instrumen spektrofotometri serapan atom (atomic absorption spectrofotometry).
Total Suspended Solid
1. Cetakkan kertas saring dalam cawan alumunium 2. Timbang bobot kertas saring + cawan
3. Saring larutan sampel yang memiliki kisaran residu 2.5 – 200 mg 4. Kocok larutan sampel (bila perlu dengan magnetic stirer). 5. Bilas dengan 3 x 10 ml air suling
6. Pindahkan kertas saring ke dalam cawan alumunium 7. Keringkan di dalam oven pada suhu 103 – 105 0C 8. Keringkan dalam eksikator
9. Timbang hingga bobot tetap atau perubahan bobot < 4% dari bobot penimbang sebelumnya
10. Hitung hasil dengan rumus:
TSS (mg/l) = (A-B) x 1000 ml sampel
Keterangan : A= bobot kertas saring + residu B= bobot kertas saring
Fenol Total
1. Masukkan 500 ml sampel yang telah disuling ke dalam gelas beaker 1 liter. Kemudian siapkan juga larutan aquades sebagai blanko sebanyak 500 ml. Lalu siapkan juga larutan standar fenol 5, 10, 20, 30, 40 dan 50 μg ke dalam 500 ml air.
2. Lakukan prosedur berikut secara bersamaan untuk sampel, blanko dan larutan standar 3. Tambahkan 12 ml 0.5 N NH4OH lalu segera sesuaikan pH larutan dengan menambahkan
bufer fosfat.
4. Pindahkan campuran ke dalam corong pemisah 1 liter, lalu tambahkan 3 ml larutan aminoantipiren. Lalu aduk rata. Tambahkan 3 ml K3Fe(CN)6, aduk rata. Diamkan, warna
campuran akan berubah menjadi kuning terang selama 15 menit
5. Lakukan ekstraksi dengan CHCl3. Kocok rata. Diamkan. Kemudian kocok lagi 10 kali.
Diamkan.
6. Saring ekstrak dengan menggunakan kertas saring yang mengandung 5 g lapisan anhidrous Na2SO4.