PEMBUATAN HIDROLISAT PROTEIN DARI IKAN SELAR
KUNING (
Caranx leptolepis
) DENGAN MENGGUNAKAN
ENZIM PAPAIN
Oleh :
Taufik Hidayat
C34101008
PROGRAM STUDI TEKNOLOGI HASIL PERIKANAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
RINGKASAN
TAUFIK HIDAYAT. C34101008. Pembuatan Hidrolisat Protein dari Ikan Selar Kuning (Caranx leptolepis) dengan Menggunakan Enzim Papain. Dibimbing oleh ELLA SALAMAH dan TATI NURHAYATI.
Ikan- ikan yang merupakan kelompok ikan pelagis khususnya yang berukuran kecil (panjang total 16-20 cm) sampai saat ini masih merupakan sumber daya yang terbatas pemanfaatannya. Salah satu jenis ikan tersebut adalah ikan selar kuning (Caranx leptolepis). Kurangnya pemanfaatan ikan tersebut lebih disebabkan oleh faktor teknis yaitu karena lebih sulitnya pemisahan bagian daging dari tubuh lainnya. Padahal ikan tersebut dapat diolah menjadi produk hidrolisat protein. Penelitian ini bertujuan untuk meningkatkan pemanfaatan ikan selar kuning melalui proses pengolahan secara hidrolisis dengan menggunakan enzim proteolitik komersial yaitu enzim papain.
Metode penelitian yang digunakan terdiri dari penelitian pendahuluan dan penelitian utama. Penelitian pendahuluan bertujuan untuk mengetahui kandungan kimia ikan selar kuning, mengetahui aktivitas optimum enzim papain terhadap substrat (ikan) dalam berbagai konsentrasi dan untuk mencari waktu dan pH optimum reaksi hidrolisis protein ikan selar kuning. Konsentrasi enzim papain terhadap substrat yang digunakan adalah 0 %, 1 %, 2 %, 3 %, 4 %, 5 % dan 6 %. Adapun parameter yang digunakan untuk mengetahui aktivitas optimum enzim papain adalah jumlah padatan sisa. Sedangkan untuk mencari pH dan waktu optimum proses hidrolisis protein ikan selar kuning, digunakan pH yang terdiri dari 3 taraf yaitu 6,5, 7 dan 7,5 serta waktu yang terdiri dari 3 taraf yaitu 5, 5,5 dan 6 jam. Parameter untuk menentukan kesempurnaan proses hidrolisis adalah proses yang menghasilkan kandungan a-amino nitrogen bebas yang paling tinggi.
Hasil penelitian pendahuluan diperoleh kandungan kimia ikan selar kuning dalam basis basah yaitu air 75,71 %, abu 2,31 %, protein 15,61 % dan lemak 2,94 %. Aktivitas enzim papain terhadap substrat (ikan) berdasarkan analisis ragam dan uji lanjut BNT terbaik pada konsentrasi enzim papain 5 %. Selanjutnya diperoleh bahwa kandungan a-amino nitrogen bebas terbesar dihasilkan oleh kombinasi antara perlakuan pH 7 dan waktu 6 jam, yaitu sebesar 0,04 gr/100gr.
Kombinasi antara waktu proses dan pH optimum yang memberikan nilai a-amino nitrogen bebas tertinggi hasil penelitian pendahuluan digunakan untuk membuat produk hidrolisat protein ikan yang menjadi penelitian utama. Produk hidrolisat protein ikan ini dianalisis baik analisis proksimat (air, abu, lemak, protein), kandungan a-amino nitrogen bebas, daya cerna in vitro dan kandungan asam aminonya. Setelah dilakukan analisis ternyata produk hidrolisat protein ikan ini mempunyai kadar protein 66,17 % (bk), kadar lemak 5,37 % (bk), kadar air 91,99 % (bb), kadar abu 16,98 % (bk), kandungan a-amino nitrogen bebas 0,06 gr/100gr, nilai perbandingan a-amino nitrogen bebas dengan nitrogen total 0,07 dan daya cerna in vitro sebesar 65,25 %. Sedangkan untuk kandungan asam amino, produk hidrolisat protein ikan ini menghasilkan asam amino yaitu asam aspartat, asam glutamat, serin, glisin, histidin, arginin, threonin, alanin, prolin, tirosin, valin, methionin, sistin, isoleusin, leusin, phenilalanin dan lisin.
PEMBUATAN HIDROLISAT PROTEIN DARI IKAN SELAR KUNING (Caranx leptolepis) DENGAN MENGGUNAKAN
ENZIM PAPAIN
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada Fakultas Perikanan dan Ilmu Kelautan
Institut Pertanian Bogor
Oleh : Taufik Hidayat
C34101008
PROGRAM STUDI TEKNOLOGI HASIL PERIKANAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
Judul : PEMBUATAN HIDROLISAT PROTEIN DARI IKAN SELAR KUNING (Caranx leptolepis) DENGAN MENGGUNAKAN ENZIM PAPAIN
Nama : Taufik Hidayat NRP : C34101008
Menyetujui,
Pembimbing I Pembimbing II
Dra. Ella Salamah, M.Si Tati Nurhayati, S.Pi, M.Si NIP. 131 788 597 NIP. 132 149 436
Mengetahui,
Dekan Fakultas Perikanan dan Ilmu Kelautan
Dr. Ir. Kadarwan Soewardi NIP. 130 805 031
RIWAYAT HIDUP
Penulis dilahirkan di Indramayu pada tanggal 11 Mei 1983, sebagai anak pertama dari tiga bersaudara, putra dari pasangan Bapak Supyan dan Ibu Kunaeni.
Tahun 1998-2001 penulis menyelesaikan pendidikan Lanjutan Tingkat Atas di SMU Negeri 1 Sindang, Kabupaten Indramayu,
Jawa Barat. Pada tahun 2001 penulis diterima sebagai mahasiswa Institut Pertanian Bogor, Fakultas Perikanan dan Ilmu Kelautan, Departemen Teknologi Hasil Perikanan melalui jalur Undangan Seleksi Masuk IPB (USMI).
Selama masa perkuliahan penulis aktif sebagai staf Departemen Kewirausahaan, Forum Keluarga Muslim FPIK-IPB (FKM-C) periode 2003-2004, pengurus Ikatan Keluarga dan Mahasiswa Darma Ayu (IKADA) Bogor periode 2002-2003. Penulis juga pernah menjadi Asisten dosen pada mata kuliah Teknologi Pengolahan Hasil Perikanan Tradisional (TPHPT) pada tahun 2004-2005. Penulis pernah mengikuti kegiatan pelatihan Pengolahan Hasil Perikanan pada bulan November 2001 yang diselenggarakan oleh Fish Procesing Club
(FPC) kerja sama dengan HIMASILKAN.
KATA PENGANTAR
Syukur Alhamdulillah penulis panjatkan kehadirat Allah SWT, karena atas rahmat dan hidayah-Nya penulis dapat menyelesaikan penulisan skripsi yang
berjudul ”Pembuatan Hidrolisat Protein dari Ikan Selar Kuning (Caranx leptolepis) dengan Menggunakan Enzim Papain”.
Pembuatan skripsi ini adalah sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Pada kesempatan ini penulis mengucapkan terima kasih kepada :
1) Ibu Dra. Ella Salamah, M.Si dan Ibu Tati Nurhayati, S.Pi, M.Si selaku ketua dan anggota komisi pembimbing yang telah banyak memberikan saran selama penelitian sampai penulisan skripsi.
2) Bapak Ir. Dadi R. Sukarsa dan Bapak Sugeng Heri Suseno, S.Pi, M.Si selaku dosen penguji yang telah banyak memberikan masukan demi kesempurnaan skripsi ini.
3) Bapak Uju, S.Pi yang telah berkenan menjadi moderator dalam seminar hasil penelitian.
4) Bapak dan Ibuku atas kasih sayang dan doanya serta dukungan baik moril maupun materil yang diberikan selama ini.
5) Adik-adikku tersayang ”Ruri dan Irna” atas kasih sayang dan dukungannya kepada penulis.
6) Keluarga besar H. Khomarudin dan H. Abdullah (Alm) atas dukungan baik moril maupun materil kepada penulis.
7) Ibu Ema, Pak Gandi, Pak Sobirin dan Pak Danu yang telah membantu penulis selama penelitian.
8) Ulum, Edoy, Ii- Boy, Intan, Ari, Bang Dian dan Mas Mail atas bantuannya mempersiapkan pelaksanaan seminar dan ujian skripsi.
9) Teman-teman THP’38 atas persahabatan dan kebersamaannya selama perkuliahan.
membangun dari semua pihak sebagai masukan dan bahan pertimbangan untuk perbaikan pada penulisan selanjutnya.
Akhir kata semoga skripsi ini dapat memberikan manfaat yang sebesar-besarnya bagi penulis khususnya dan bagi pihak-pihak yang berkepentingan pada umumnya.
3.5.7. Analisis asam amino (Nur, Adijuwana 1989) ... 27
4. HASIL DAN PEMBAHASAN ... 29
4.1. Penelitian Pendahuluan... 29
4.1.1. Komposisi kimia ikan selar kuning... 29
4.1.2. Aktivitas enzim papain terhadap substrat... 30
4.1.3. Kondisi optimum proses hidrolisis protein ikan ... 31
4.2. Penelitian Utama ... 33
4.2.1. Kadar air ... 34
4.2.2. Kadar abu ... 35
4.2.3. Kadar protein... 36
4.2.4. Kadar lemak ... 36
4.2.5. Kadar a-amino nitrogen bebas... 37
4.2.6. Daya cerna in vitro ... 38
4.2.7. Asam amino... 39
5. KESIMPULAN DAN SARAN ... 42
5.1. Kesimpulan... 42
5.2. Saran... 42
DAFTAR PUSTAKA ... 43
DAFTAR TABEL
Nomor Halaman
1. Komposisi kimia daging ikan selar dalam setiap 100 gram bahan... 5
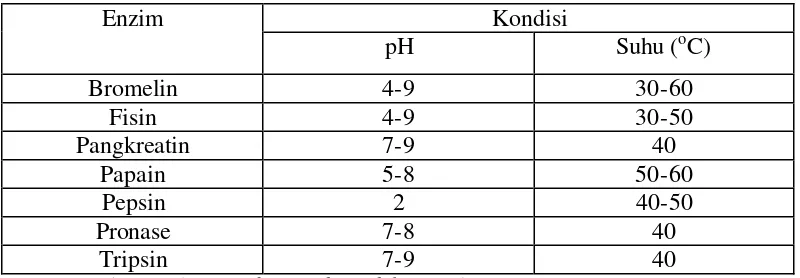
2. Enzim komersial penghidrolisis protein ikan... 7
3. Penggolongan enzim berdasarkan reaksi yang dikatalisisnya ... 8
4. Komposisi hidrolisat protein ikan... 14
5. Perlakuan hidrolisis pada penelitian pendahuluan tahap kedua ... 18
6. Perlakuan hidrolisis pada penelitian pendahuluan tahap ketiga... 19
7. Komposisi kimia ikan selar kuning (Caranx leptolepis)... 29
8. Kandungan α-amino nitrogen bebas hasil hidrolisis ikan selar kuning .. 32
9. Hasil analisa produk hidrolisat protein ikan selar kuning ... 34
DAFTAR GAMBAR
Nomor Halaman
1. Ikan selar kuning (Caranx leptolepis) ... 4
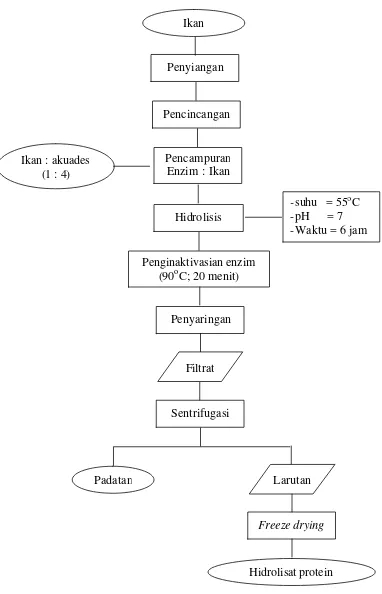
2. Diagram alir produksi hidrolisat protein ... 12
3. Diagram alir proses pembuatan hidrolisat protein ikan ... 20
4. Hasil pengukuran padatan sisa hidrolisis protein ikan... 30
DAFTAR LAMPIRAN
Nomor Halaman
1. Rekapitulasi data analisis kimia ikan selar kuning segar ... 49
2. Rekapitulasi data padatan sisa hidrolisat protein ikan selar kuning pada penelitian pendahuluan... 49
3. Uji ANOVA dan uji lanjut BNT padatan sisa hidrolisat protein ikan selar kuning pada penelitian pendahuluan ... 49
4. Rekapitulasi data nilai a-amino nitrogen bebas hidrolisat protein ikan selar kuning pada penelitian pendahuluan... 50
5. Uji ANOVA dan uji lanjut BNJ nilai a-amino nitrogen bebas hidrolisat protein ikan selar kuning pada penelitian pendahuluan... 50
6. Rekapitulasi data analisis produk hidrolisat protein ikan selar kuning pada penelitian utama ... 53
7. Berat molekul asam amino ... 53
8. Kromatogram hasil analisis asam amino... 54
9. Produk hidrolisat protein ikan terbaik pada penelitian pendahuluan... 56
10. Produk hidrolisat protein ikan selar kuning pada penelitian utama ... 56
1. PENDAHULUAN
1.1. Latar Belakang
Ketersediaan panga n bernilai gizi protein tinggi masih merupakan masalah di negara-negara berkembang termasuk Indonesia. Di negara kita masalah kekurangan kalori protein (KKP) merupakan masalah gizi utama bersama-sama dengan masalah kekurangan vitamin A, yodium dan zat besi (Karyadi et al. 1994). Telah umum diketahui bahwa protein merupakan komponen zat makanan yang amat penting bagi tubuh karena fungsi utamanya sebagai zat pembangun dan pengatur. Fungsi tersebut dilaksanakan melalui berbagai macam bentuk seperti sebagai reseptor, enzim, antibodi, pembentuk jaringan dan lain - lain. Protein dapat berasal dari sumber nabati dan hewani. Protein hewani terutama sekali berasal dari hewan ternak, ikan, telur dan susu (Hadiwiyoto 1993).
Potensi lestari (Maksimum Sustanable Yield, MSY) sumber daya ikan di perairan laut Indonesia diperkirakan mencapai 6,4 juta ton pertahun. Produksi perikanan dalam periode 2000-2003 mengalami peningkatan rata-rata pertahun sebesar 5,21 % yaitu dari 5,107 juta ton pada tahun 2000 menjadi 5,948 juta ton pada tahun 2003. Produksi perikanan nasional tersebut masih didominasi oleh usaha penangkapan di laut (74,49 % dari produksi tahun 2003). Melalui skenario GMB (Gerbang Mina Bahari) pemerintah menargetkan jumlah produksi perikanan pada tahun 2006 mencapai 9,5 juta ton (Dahuri 2004). Ikan- ikan yang merupakan kelompok ikan pelagis khususnya yang berukuran kecil (panjang total 16-20 cm) sampai saat ini masih merupakan sumberdaya yang terbatas pemanfaatannya. Kurangnya pemanfaatan ikan- ikan tersebut lebih disebabkan oleh kurangnya informasi tentang nilai gizi dan adanya faktor teknis yaitu karena lebih sulitnya pemisahan bagian daging dari tubuh lainnya. Hal ini menunjukkan ikan-ikan tersebut belum tentu memiliki nilai gizi yang lebih rendah dibandingkan ikan-ikan komersial lainnya (Suparno, Dwiponggo 1994).
terbatas untuk diolah menjadi ikan asin atau digoreng langsung. Padahal ikan ini mempunyai kandungan protein yang cukup tinggi dan mempunyai flavor yang khas. Ikan ini dapat dijadikan sebagai bahan baku dalam pembuatan produk hidrolisat protein. Produk pengolahan ini tidak memerlukan kondisi penyimpanan beku, hal ini menyebabkan penyebarluasan produk ini lebih memungkinkan dibandingkan dengan produk surimi dan lain- lain (Huda 1994). Pengolahan ikan selar kuning sebagai bahan baku dalam pembuatan hidrolisat protein diharapkan memberikan nilai tambah (added value) ikan tersebut.
Hidrolisat protein ikan memiliki beberapa kegunaan pada industri pangan maup un farmasi. Pada industri pangan, hidrolisat protein ikan dapat ditambahkan ke dalam formula makanan non-alergenik untuk bayi dan suplemen makanan diet. Hidrolisat protein ikan juga dapat digunakan pada pembuatan produk-produk dermatologis, seperti krim pembersih muka dan krim pelembab kulit. Selain itu, hidrolisat protein ikan dapat digunakan secara fungsional sebagai bahan pengemulsi (Pigot, Tucker 1990).
Pepaya termasuk kedalam kelompok buah-buahan yang banyak ditanam di Indonesia. Salah satu penggunaan pepaya dalam skala besar adalah pemanfaatannya untuk produksi enzim papain. Papain merupakan enzim proteolitik hasil isolasi dari getah pepaya. Enzim tersebut dapat diproduksi dalam bentuk tepung maupun larutan. Kelebihan enzim papain adalah kemampuannya untuk mendegradasi kolagen atau elastin yang terdapat pada daging sehingga diperoleh jaringan yang lebih lunak akibat proses hidrolisa.
Pembuatan hidrolisat protein dari ikan dengan menggunakan enzim papain sudah pernah dilakukan baik oleh Kusnaeni (1993) maupun Dewi (2002) namun hasilnya masih kurang maksimal dilihat dari total padatan dan amino nitrogen bebas yang dihasilkan. Hal ini karena kondisi proses hidrolisis yang belum sempurna, sehingga perlu dilakukan penelitian lebih lanjut untuk mendapatkan hasil yang lebih baik.
1.2. Tujuan
Secara umum, penelitian ini bertujuan untuk mempelajari pemanfaatan ikan selar kuning (Caranx leptolepis) menjadi produk hidrolisat dengan bantuan enzim papain sebagai bahan penghidrolisa. Secara khusus tujuan penelitian ini adalah sebagai berikut :
- memproduksi hidrolisat protein dari ikan selar kuning.
- mengetahui karakteristik produk hidrolisat protein ikan yang dihasilkan. - mengevaluasi kandungan asam amino dari hidrolisat protein yang dihasilkan.
2. TINJAUAN PUSTAKA
2.1. Deskripsi Ikan Selar Kuning (Caranx leptolepis)
Klasifikasi ikan selar kuning (Caranx leptolepis) berdasarkan Saanin (1984) adalah sebagai berikut :
Filum : Chordata
Sub Filum : Vertebrata Kelas : Pisces
Sub kelas : Teleostei Ordo : Percomorphi
Sub Ordo : Perciformes Famili : Carangidae Genus : Caranx
Spesies :Caranx leptolepis
Gambar 1. Ikan selar kuning (Caranx leptolepis)
ditandai dengan garis lebar berwarna kuning dari mata sampai ekor. Sirip punggung ikan selar kuning terpisah dengan jelas, bagian depan disokong oleh jari-jari keras dan banyak jari- jari lunak. Sirip ekor becagak dua dengan lekukan yang dalam. Sirip perut terletak di bawah sirip dada. Ikan selar kuning termasuk ikan laut perenang cepat dan kuat. Daerah penyebaran ikan ini adalah semua laut di daerah tropis dan semua lautan Indofasifik, ikan ini banyak tertangkap di
perairan pantai serta hidup berkelompok sampai kedalaman 80 m (Djuhanda 1981).
Komposisi kimia daging ikan sangat bervariasi tergantung pada spesies, tingkat umur, musim, habitat dan kebiasaan makan. Nilai gizi daging ikan terutama ditentukan oleh kandungan lemak dan proteinnya. Ikan selar kuning termasuk kategori ikan yang berkadar lemak rendah karena kurang dari 5 % dan memiliki protein yang tergolong tinggi yaitu antara 15 % - 20 % (Stansby 1982). Tabel 1 memperlihatkan komposisi kimia ikan selar.
Tabel 1. Komposisi kimia daging ikan selar dalam setiap 100 gram bahan
Sumber : Direktorat Gizi Departemen Kesehatan RI (1989)
2.2. Protein Ikan dan Asam Amino
Protein merupakan komponen utama dalam semua sel hidup. Fungsinya terutama sebagai unsur pembentuk sel, misalnya dalam rambut, wool, kolagen, jaringan penghubung, membran sel, dan lain- lain. Selain itu dapat pula sebagai protein yang aktif, seperti enzim yang berperan sebagai katalis segala proses biokimia dalam sel (Wirahadikusumah 1989).
Protein merupakan makromolekul yang paling melimpah di dalam sel. Unit pembangunnya adalah asam amino yang berikatan secara kovalen untuk menghubungkan molekul- molekul menjadi rantai. Apabila protein dihidrolisis dengan asam, alkali atau enzim akan dihasilkan campuran asam-asam amino.
Jenis kandungan Jumlah (gram)
Air 75,4
Abu 1,36
Protein 18,8
Sebuah asam amino terdiri dari gugus R (rantai cabang), sebuah gugus asam amino, sebuah gugus karboksil, dan sebuah atom hidrogen (Winarno 1997).
Senyawa protein merupakan konstituen pengisi jaringan otot ikan yang cukup penting. Pada umumnya, ikan mengandung protein antara 18 hingga 25 persen. Berdasarkan sifat kelarutannya, protein ikan dapat dikelompokkan menjadi tiga jenis, yaitu protein mioplastik, protein miofibril dan protein miostroma (Okuzumi, Fujii 2000). Protein mioplastik pada otot ikan berkisar antara sepersepuluh hingga seperlima dari total protein otot. Protein tersebut larut didalam air serta larutan garam berkekuatan ionik rendah pada pH 7,58 (Govindan 1985).
Di dalam otot ikan juga terkandung senyawa protein penunjang lainnya, yaitu protein miofibril. Protein miofibril terdapat di dalam otot ikan dengan kadar yang lebih tinggi dari pada protein mioplastik, yaitu antara 75 hingga 85 persen dari total protein otot ikan. Protein tersebut larut di dalam larutan berkekuatan ion yang tinggi tetapi tidak larut di dalam air (Govindan 1985). Protein miofibril pada otot ikan mengandung miosin, aktin, aktomiosin dan tropomiosin. Miosin merupakan komponen miofibril yang mampu mengalami denaturasi dan agregasi. Pada proses denaturasi dihasilkan molekul- molekul gel dari miosin dengan sifat elastis yang akan tergabung akibat adanya proses agregasi (Wong 1989). Ramirez et al. (2000) menyatakan bahwa proses agregasi miosin juga dapat terbentuk akibat adanya ikatan disulfida yang cukup kuat selama penyimpanan beku.
2.3. Enzim
Kata enzim diperkenalkan oleh Willy Kuchne pada tahun 1876 untuk suatu zat yang bekerja pada suatu substrat. Kata enzim berasal dari bahasa yunani yang berarti di dalam sel. Enzim sulit didefinisikan secara tepat, definisi yang dikemukakan adalah enzim merupakan protein yang mempunyai daya katalitik karena aktivitas spesifiknya (Winarno 1987).
Enzim memiliki beberapa sifat (Delvin 1978) yaitu : -enzim dapat aktif walaupun dalam jumlah yang sangat sedikit;
-enzim merupakan katalis sejati yang tidak dipengaruhi oleh reaksi yang dikatalisnya;
-walaupun enzim dapat mempercepat reaksi secara keseluruhan tetapi tidak mempengaruhi kesetimbangan reaksi;
-aksi katalitik enzim bersifat spesifik.
Beberapa enzim komersial penghidrolisis protein ikan disajikan pada Tabel 2.
Tabel 2. Enzim komersial penghidrolisis protein ikan
Kondisi
Sumber :Muliati (1986) yang diacudalam Herdiana (1999)
2.4. Enzim Proteolitik
Proteolitik termasuk dalam kelas utama enzim golongan hidrolase. Enzim hidrolase mengkatalisis reaksi-reaksi hidrolisis, yaitu reaksi yang melibatkan unsur air pada ikatan spesifik dari substrat atau bahan (Winarno 1987). Enzim proteolitik atau protease mempunyai dua pengertian, yaitu proteinase yang mengkatalisa hidrolisa molekul protein menjadi fragmen- fragmen yang lebih sederhana, dan peptidase yang menghidrolisa fragmen polipeptida menjadi asam amino. Klasifikasi proteolitik pada mulanya didasarkan pada enzim-enzim alamiah misalnya papain, fisin, dan bromelin yang berasal dari tumbuh-tumbuhan, tripsin dari pankreas, serta pepsin dan renin dari lambung (Yamamoto 1975).
Beberapa faktor yang mempengaruhi kecepatan tingkat degradasi enzim proteolitik diantaranya spesifikasi enzim, tingkat denaturasi protein sebagai substrat sesuai dengan konsentrasi substrat dan enzim, pH, suhu dan kekuatan ion yang bereaksi dengan medium, dan adanya inhibitor (Fujimaki et al. 1997). Selain itu juga dipengaruhi oleh berbagai pereaksi kimia yang digunakan, perlakuan fisik, radiasi dan vibrasi, dimana semuanya dapat mendenaturasi protein.
Tabel 3. Penggolongan enzim berdasarkan reaksi yang dikatalisisnya
No. Kelas Utama Jenis reaksi yang dikatalisis 1.Oksidoreduktase Pemindahan elektron
2.Transferase Reaksi pemindahan gugus fungsional
3.Hidrolase Reaksi hidrolisis (pemindahan gugus fungsional ke air ) 4.Liase Penambahan gugus ke ikatan ganda atau sebaliknya
5.Isomerase Pemindahan gugus di dalam molekul menghasilkan isomer 6.Ligase Pembentukan ikatan C-C, C-S, C-O dan C-N oleh reaksi
kondensasi yang berkaitan dengan penguraian ATP
Sumber : Muchtadi et al. (1992)
2.5. Enzim Papain
Papain merupakan enzim proteolitik hasil isolasi dari getah penyadapan buah pepaya (Carica papaya L.). Selain mengandung papain sebanyak 10 %, getah buah pepaya juga tersusun atas enzim kemopapain dan lisozim sebesar 45% dan 20% (Winarno 1987).
itu, Wong (1989) menjelaskan bahwa di dalam molekul papain juga terdapat sisi aktif yang terdiri atas gugus histidin dan sistein. Selama katalisis berlangsung, sisi aktif tersebut berfungsi sebagai ion zwitter (zwitter ion). Selain sistein dan histidin, pada molekul papain juga terdapat sebuah gugus sulfhidril bebas, sehingga papain dapat digolongkan ke dalam protease sulfhidril (Beveridge 1996).
Aktivitas katalisis papain dilakukan melalui hidrolisa yang berlangsung pada sisi-sisi aktif papain. Pada proses tersebut, berlangsung pemisahan
gugus-gugus amida yang terdapat di dalam protein melalui pemutusan ikatan peptida (Wong 1989).
Selama proses katalisis hidrolisa gugus-gugus amida, mula- mula gugus sistein (Cys-25) yang bersifat sangat reaktif berikatan dengan substrat pada sisi aktif papain sehingga dihasilkan ikatan kovalen substrat dengan enzim yang berbentuk tetrahedral. Kemudian, gugus histidin (His-159) terprotonasi sehingga berikatan dengan nitrogen yang terdapat di dalam substrat. Akibatnya, gugus amin pada substrat terdifusi dan kedudukannya digantikan oleh molekul- molekul air yang pada akhirnya menghidrolisa hasil intermediat sehingga mengembalikan enzim ke dalam bentuk dan fungsinya seperti semula (Be veridge 1996). Oleh karena itu, berdasarkan mekanisme pengikatan enzim terhadap substrat, proses hidrolisa tersusun atas dua tahap reaksi. Reaksi pertama adalah reaksi asilasi untuk membentuk ikatan kompleks enzim substrat, sedangkan reaksi kedua adalah reaksi deasilasi yang ditandai dengan hidrolisa ikatan kompleks enzim substrat menjadi produk dan enzim (Wong 1989).
Mengingat fungsinya sebagai enzim proteolitik, maka hingga saat ini papain dapat digunakan untuk menghasilkan beberapa produk. Pada industri makanan papain digunakan di dalam produksi pengempuk daging, konsentrat protein dan hidrolisat protein. Papain juga dapat digunakan untuk menurunkan viskositas bahan. Di bidang kesehatan, papain dimanfaatkan untuk mencegah
deformasi luka pada kornea mata dan pembersih lensa mata (Leipner, Saller 2000). Selain itu, papain berfungsi dalam industri keju,
membuang sisa-sisa serat dari kain pada industri detergen serta bahan aktif dalam pembuatan krim pembersih kulit (Muhidin 1999).
2.6. Hidrolisis
Kata hidrolisis pada umumnya berhubungan dengan reaksi yang meliputi air dan dua atau lebih komponen produk (Kirk, Othmer 1953). Pada hidrolisis, sebuah ikatan antara dua atom dipecah. Meskipun demikian istilah hidrolisis kadang-kadang berkembang pada reaksi pemecahan banyak ikatan menjadi satu ikatan. Reaksi hidrolisis dapat dibagi dalam beberapa tipe, yaitu :
-hidrolisis murni, hanya air yang digunakan untuk proses hidrolisis; -hidrolisis dengan larutan asam;
-hidrolisis dengan larutan alkali;
-hidrolisis dengan peleburan alkali yang menggunakan air atau tanpa air pada temperatur tinggi;
-hidrolisis dengan enzim sebagai katalisator.
Hidrolisis protein dapat dilakukan secara kimia dan enzimatik (Johnson, Peterson 1974). Selain itu hidrolisis protein dapat dilakukan dengan
menggunakan uap panas, kapang, khamir dan bakteri (Eircle 1950
yang diacu dalam Syahrizal 1991).
Ikatan peptida pada protein dapat dihidrolisis dengan perebusan dalam asam atau basa kuat untuk menghasilkan komponen asam amino dalam bentuk bebas. Ikatan ini dapat juga dihidrolisis dengan enzim tertentu, seperti tripsin dan khimotripsin (Lehninger 1993). Hidrolisis asam tidak menguntungkan karena komponen triptofan, glutamin dan sejumlah asam amino lainnya dapat hancur dan hidrolisis selanjutnya diperlukan untuk membebaskan semua asam amino tersebut. Disamping itu hidrolisis asam juga dapat mengakibatkan terbentuknya humin atau bahan-bahan lain serupa humin yang secara kompleks memisahkan asam amino dari hidrolisat (Johnson, Peterson 1974).
Secara teoritis metoda hidrolisis protein yang paling efisien adalah menggunakan enzim, karena enzim menghasilkan peptida-peptida yang kurang kompleks dan mudah dipecah. Disamping itu hidrolisis enzim dapat menghasilkan produk hidrolisat yang terhindar dari perubahan dan kerusakan produk yang bersifat non hidrolitik (Johnson, Peterson 1974). Hidrolisis protein dipengaruhi oleh konsentrasi bahan-bahan penghidrolisis, suhu dan waktu hidrolisis serta tekanan udara (Mitchel et al. 1929 yang diacu dalam Hasnan 1991). Peningkatan konsentrasi enzim ternyata akan meningkatkan volume hidrolisat protein ikan yang bersifat tak larut menjadi senyawa nitrogen yang bersifat larut (Syahrizal 1991). Kecepatan katalis enzim meningkat pada konsentrasi enzim yang lebih besar, tetapi bila konsentrasi enzim berlebih, maka proses tersebut tidak efisien. Untuk meningkatkan aktivitas hid rolisis, maka dapat digunakan enzim- enzim proteolitik komersial (Hale 1969).
2.7. Hidrolisat Protein
Hidrolisat protein merupakan sumber protein alami yang dihidrolisis secara parsial sehingga lebih mudah diasimilasi oleh mahluk hidup. Hidrolisis secara parsial mampu memecah molekul protein menjadi beberapa gugus asam
amino maupun peptida melalui pemutusan ikatan rantai peptida (Rehm, Reed 1995).
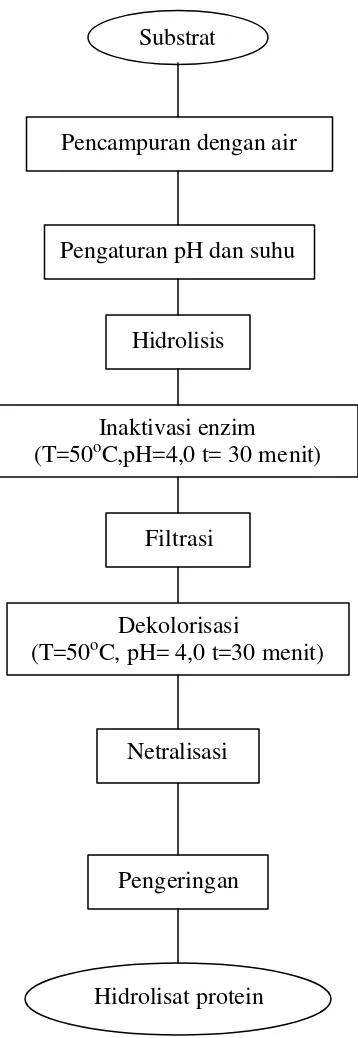
melalui penambahan asam (Govindan 1985). Proses pembentukan hidrolisat protein diperlihatkan pada Gambar 2.
Gambar 2. Diagram alir produksi hidrolisat protein (Shahidi, Botta 1994)
Hidrolisis protein untuk menghasilkan peptida dan asam amino dapat dilakukan secara parsial dengan menggunakan penambahan asam maupun basa.
Substrat
Inaktivasi enzim (T=50oC,pH=4,0 t= 30 menit)
Hidrolisis
Filtrasi
Pengaturan pH dan suhu Pencampuran dengan air
Dekolorisasi
(T=50oC, pH= 4,0 t=30 menit)
Netralisasi
Pengeringan
Mengingat proses penambahan asam maupun basa pada proses hidrolisis dapat merusak beberapa gugus asam amino serta menghasilkan senyawa karsinogenik, maka fungsi asam atau basa digantikan oleh enzim secara spesifik. Akibat sifat enzim yang sangat spesifik, maka diperlukan pula pemilihan kondisi hidrolisis yang tepat. Kondisi yang perlu diperhatikan selama hidrolisis berlangsung adalah suhu, nilai pH dan waktu hidrolisis (Gesualdo, Li-Chan 1999).
Hidrolisis menggunakan enzim berlangsung secara spesifik, maka proses hidrolisis secara ekstensif mampu mempengaruhi pembentukan peptida dan asam-asam amino. Melalui proses hidrolisis diharapkan terjadi proses modifikasi karakteristik fungsional protein untuk meningkatkan kualitas protein. Selain itu, kualitas hidrolisat protein juga dipengaruhi oleh tingkat hidrofobisitas bagian rantai non polar pada protein, derajat hidrolisis serta tipe enzim proteolitik yang digunakan (Shahidi, Botta 1994).
2.8. Hidrolisat Protein Ikan
Hidrolisat protein ikan merupakan produk hidrolisis protein dengan bahan baku ikan. Pada pembuatan hidrolisat protein ikan digunakan bahan penghidrolisis asam, basa kuat atau enzim. Silase ikan merupakan hasil hidrolisis ikan secara kimiawi dengan menggunakan asam. Produk hidrolisis ikan secara enzimatis diolah dengan cara mencampur ikan yang telah digiling atau dilumatkan dengan air dan enzim proteolitik (Wheaton, Lawson 1985).
Faktor-faktor yang mempengaruhi kecepatan hidrolisis dan kekhasan hidrolisat yang dihasilkan adalah suhu, waktu, pH, konsentrasi dan perbandingan enzim dengan protein. Sedangkan warna, bau, rasa dan tingkat kerusakan asam amino dipengaruhi oleh kemurnian protein dari bahan awal, kondisi serta bahan penghidrolisis yang digunakan. Bila hidrolisis berjalan sempurna maka akan dihasilkan hidrolisat yang terdiri dari campuran 18-20 macam asam amino (Kirk, Othmer 1953).
Bahan kimia yang umum digunakan untuk menghidrolisis protein adalah HCl, H2SO4, NaOH, dan Ba(OH)2 (West, Todd 1964). Bahan kimia HCl memiliki beberapa keuntungan diantaranya adalah konsentrasi HCl yang dibutuhkan untuk
Hidrolisat protein pertama kali diperkenalkan di Cina dan Jepang sekitar tahun 1900 dan merupakan hasil sampingan pembuatan monosodium Glutamat (MSG). Setelah proses kristalisasi MSG selesai, tersisa asam amino yang telah dinetralisir dan dikeringkan. Hidrolisat protein dapat berbentuk cair, pasta atau tepung yang bersifat higroskopis. Hidrolisat protein yang berbentuk cair mengandung 30% padatan, sedangkan bentuk pasta mengandung 65% padatan. Flavor yang khas dari hidrolisat tergantung dari komposisi asam amino bahan awalnya, misalnya hidrolisat yang dihasilkan dari gelatin relatif lebih manis rasanya karena kandungan glisinnya tinggi. Hidrolisat protein dalam bentuk cair yang diproduksi secara komersial mempunyai kadar garam berkisar antara 10-21 %, kadar amino nitrogen 0,5-2 % dan kadar padatan terlarut 10-21 % (Johnson, Peterson 1974).
2.8.1. Mutu hidrolisat protein ikan
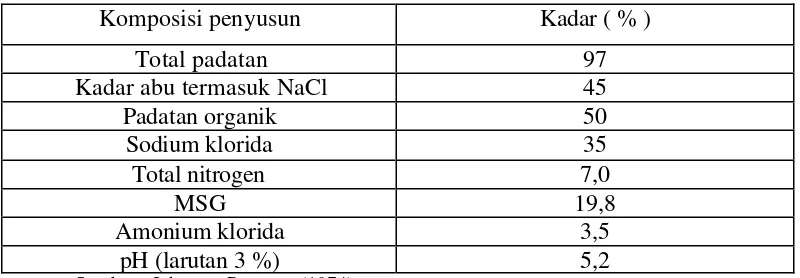
Hasil hidrolisis antara lain adalah a-amino nitrogen bebas yang umumnya digunakan untuk menentukan derajat kesempurnaan proses hidrolisis. Perbandingan antara a-amino nitrogen bebas dengan total nitrogen digunakan untuk menentukan mutu hidrolisat protein. Angka perbandingan yang tinggi menunjukkan mutu hidrolisat protein yang tinggi pula (Yokotsuka 1960). Produk hidrolisat protein mempunyai kelebihan karena kelarutannya tinggi dan kondisinya stabil. Rasio a-amino nitrogen bebas dengan total nitrogen produk hidrolisat sebagai supplement makanan yang telah disampaikan oleh Food Chemical Codex bervariasi antara 0,02 sampai 0,67 (Lahl, Braun 1994). Salah satu komposisi hidrolisat protein ikan dapat dilihat pada Tabel 4.
Tabel 4. Komposisi hidrolisat protein ikan
Komposisi penyusun Kadar ( % )
Total padatan 97
Kadar abu termasuk NaCl 45
Padatan organik 50
2.8.2. Kegunaan hidrolisat protein ikan
Pada umumnya hidrolisat protein yang diproduksi digunakan untuk berbagai kegunaan seperti memperbaiki karakteristik berbagai produk pangan dan juga sebagai penyedap rasa (Pedersen 1994). Kirk, Othmer (1953) mengemukakan tujuan pembuatan hidrolisat protein yaitu sebagai penyedap, sebagai lanjutan untuk isolasi asam amino, serta untuk pengobatan. Selain itu hidrolisat protein juga dapat disertakan sebagai menu para penderita gangguan pencernaan. Aplikasi produk hidrolisat protein ikan diantaranya digunakan dalam pengolahan bahan makanan tambahan dengan tujuan selain menambah sumber protein yang kaya dengan asam amino juga meningkatkan cita rasa produk.
2.9. Freeze Drying (Pengeringan Beku)
Pengeringan beku adalah proses pengeringan yang didahului oleh proses pembekuan. Pengeringan beku juga dikenal dengan istilah pengeringan sublimasi atau iyophilisasi. Bahan pangan terlebih dahulu dibekukan, kemudian air langsung dikeluarkan dari bahan pangan secara sublimasi (Mellor 1978).
Metode pengeringan beku merupakan salah satu metode pengeringan dengan prinsip yang berbeda dibanding metode pengering lainnya, yaitu proses mengurangi sebagian besar air bahan pada suhu dibawah titik beku dengan cara sublimasi. Walaupun merupakan metode yang relatif mahal tetapi pengeringan ini menghasilkan produk dengan mutu yang relatif baik dibandingkan dengan metode lainnya (Considine 1974 yang diacu dalam Tiyasmainar 2000). Proses pengeringan beku mempunyai keuntungan-keuntungan yang membuat baha n makanan menjadi produk yang sangat menarik. Produk kering beku mempunyai sifat tidak mengkerut, bahkan bentuk dan dimensi aslinya dapat dipertahankan, mempunyai stabilitas selama penyimpanan dan menghambat pertumbuhan bakteri (Mellor 1978).
Proses pengeringan beku akan dapat mengatasi semua permsalahan perubahan karakteristik produk yang tidak diinginkan, mencegah terjadinya penyusutan padatan dan migrasi bahan terlarut serta menghambat reaksi- reaksi kimia. Beberapa keuntungan proses pengeringan beku yang dilakukan pada suhu pengeringan yang relatif rendah adalah untuk mengatasi terjadinya reaksi kimia
”browning” (reaksi non enzimatis), pengerasan pada permukaan luar (case hardening), denaturasi protein, reaksi enzimatis dan juga mengurangi
3. METODOLOGI
3.1. Waktu dan Tempat
Penelitian ini dilaksanakan selama empat bulan, yaitu mulai bulan April sampai dengan bulan Juli 2005. Tempat yang digunakan selama penelitian adalah Laboratorium Kimia dan Biokimia, Departeme n Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan; Laboratorium Kimia dan Biokimia Pangan, Departemen Teknologi Pangan dan Gizi; Laboratorium Pilot Plant, PAU Pangan dan Gizi, Institut Pertanian Bogor; dan Balai Besar Penelitian dan Pengembangan Pasca Panen Pertanian, Departemen Pertanian.
3.2. Bahan dan Alat
Bahan baku yang digunakan dalam penelitian ini adalah ikan selar kuning segar yang berukuran kecil dan enzim papain komersial merek ”PAYA”. Bahan kimia yang digunakan untuk menga nalisa produk hidrolisat adalah K2SO4, MgO, H2SO4, H3PO3, MgCO3, NaOH, CH3COOH, HCl, Na2S2O3, AgNO3, BaCl2, heksana, asam asetat glasial, larutan kuprifosfat, larutan buffer, larutan trikloroasetat (TCA), akuades dan bahan-bahan kimia untuk analisa asam amino.
Peralatan yang digunakan pada penelitian ini antara lain adalah kain saring, gelas ukur, erlenmeyer dan pendingin tegak, pemanas air (hot plate) dengan pengatur suhu, centrifuge dan pengering beku (freeze dryer), seperangkat peralatan laboratorium untuk analisa kimia produk hidrolisat ikan seperti labu kjeldahl, perangkat alat destilasi, perangkat alat ekstraksi soxlet, oven, desikator, cawan porselin, tanur pengabuan, kertas saring whatman, pH meter, stirrer serta alat untuk analisa asam amino seperti HPLC.
3.3. Metode Penelitian
Penelitian ini dilakukan dalam dua tahap, yaitu penelitian pendahuluan dan penelitian utama.
3.3.1. Penelitian pendahuluan
mengetahui aktivitas enzim papain terhadap substrat dan tahap ketiga bertujuan untuk mencari waktu dan pH optimum reaksi enzim papain dalam proses hidrolisis protein ikan selar kuning yang menghasilkan a-amino nitrogen bebas yang paling tinggi. Sebagaimana diketahui parameter untuk mengetahui derajat kesempurnaan proses hidrolisis protein adalah a-amino nitrogen bebas.
Langkah- langkah yang dilakukan dalam penelitian pendahuluan adalah sebagai berikut :
(1) Penelitian pendahuluan tahap pertama
Ikan selar kuning yang digunakan sebagai bahan baku dalam pembuatan hidrolisat protein dianalisis proksimat yang meliputi uji kadar air, kadar abu, kadar protein dan kadar lemak.
(2) Penelitian pendahuluan tahap kedua
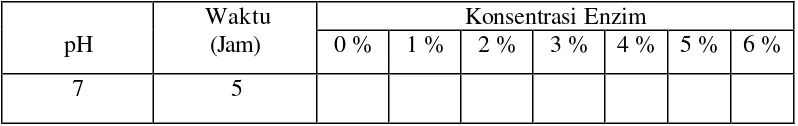
Daging ikan yang telah dicincang dicampur dengan air (1 : 4) dan enzim papain pada berbagai konsentrasi, kemudian dilakukan hidrolisis pada suhu 55oC dengan menggunakan pemanas air dengan pengatur suhu. Perlakuan hidrolisis pada penelitian pendahuluan tahap kedua dapat dilihat pada Tabel 5. Untuk menjaga kestabilan pH pada saat proses hidrolisis berlangsung digunakan CH3COOH sebagai pengatur suasana asam dan NaOH sebagai pengatur suasana basa, kemudian dari hasil hidrolisis masing- masing perlakuan dilakukan pengamatan terhadap padatan sisa hasil hidrolisis. Selanjutnya variabel terbaik yang menunjukkan aktivitas enzim papain yang paling tinggi digunakan dalam penelitian pendahuluan tahap ketiga.
Tabel 5. Perlakuan hidrolisis pada penelitian pendahuluan tahap kedua Konsentrasi Enzim
pH
Waktu
(Jam) 0 % 1 % 2 % 3 % 4 % 5 % 6 %
7 5
(3) Penelitian pendahuluan tahap ketiga
nitrogen bebasnya, kemudian perlakuan yang menghasilkan kandungan a-amino nitrogen bebas paling tinggi digunakan dalam penelitian utama.
Tabel 6. Perlakuan hidrolisis pada penelitian pendahuluan tahap ketiga
Waktu pH 6,5 7 7,5
5 jam 5,5 jam
6 jam
3.3.2. Penelitian utama
Penelitian utama bertujuan untuk membuat hidrolisat protein ikan berdasarkan variabel terbaik dari penelitian pendahuluan, mempelajari karakteristik produk hidrolisat yang dihasilkan, serta mengevaluasi kandungan asam aminonya.
Langkah- langkah yang dilakukan dalam penelitian utama ini adalah sebagai berikut :
Ikan selar kuning dicincang, kemudian dicampur air dengan perbandingan (1 : 4) serta dicampur enzim papain dengan perlakuan konsentrasi terbaik yang diambil dari penelitian pendahuluan tahap kedua, kemudian dilakukan proses hidrolisis pada suhu 55oC, sedangkan untuk perlakuan pH dan waktu diambil dari penelitian pendahuluan tahap ketiga yang terbaik. Tahap berikutnya adalah penginaktivan enzim pada suhu 90oC selama 20 menit, penyaringan, sentrifuse sehingga diperoleh fraksi larutan yang kemudian dipekatkan dengan freeze dryer
Gambar 3. Diagram alir proses pembuatan hidrolisat protein ikan modifikasi dari Imm, Lee (1999)
Ikan : akuades (1 : 4)
Ikan
Pencincangan Penyiangan
Pencampuran Enzim : Ikan
Hidrolisis
Penginaktivasian enzim (90oC; 20 menit)
o
Penyaringan
Sentrifugasi
Padatan
Hidrolisat protein
Freeze drying
Filtrat
Larutan
3.4. Analisis Data
(1) Untuk mencari konsentrasi enzim yang mempunyai aktivitas terbaik
Uji statistik yang digunakan pada tahap ini adalah rancangan acak lengkap pola searah dengan dua kali ulangan. Model analisis datanya menurut Steel, Torrie (1991), sebagai berikut :
Yij = µ + Ai + Eij
Keterangan :
Yij = Respon percobaan karena pengaruh perlakuan konsentrasi enzim taraf ke-i, ulangan ke-j
µ = Pengaruh rata-rata
Ai = Taraf ke- i perlakuan konsentrasi enzim
Eij = Pengaruh kesalahan percobaan karena pengaruh perlakuan ke- i ulangan ke-j i = 1,2,3,4,5,6,7
J = 1,2
Data peubah yang diamati dianalisis secara statistik dengan analisis sidik ragam (ANOVA). Jika analisisnya berbeda nyata, dilanjutkan dengan uji lanjut Beda Nyata Terkecil (BNT).
(2) Untuk mencari pH dan waktu optimum proses hidrolisis
Uji statistik yang digunakan pada tahap ini adalah rancangan acak lengkap pola percobaan faktorial dengan dua kali ulangan yang diberikan meliputi :
A = perlakuan terhadap waktu (A1 = 5 jam, A2 = 5,5 jam dan A3 = 6 jam). B = perlakuan terhadap pH (B1 = pH 6,5, B2 = pH 7, B3 = pH 7,5).
Model rancangan acak lengkap pola faktorial (Steel, Torrie 1991) adalah sebagai berikut :
Yijk = µ + Ai + Bj + ABij + eijk
Keterangan :
Yijk : respon dari faktor A taraf ke-i dan faktor B taraf ke-j pada ulangan ke-k µ : pengaruh rata-rata
Ai : pengaruh dari faktor A taraf ke- i Bj : pengaruh dari faktor B taraf ke-j
Apabila hasil analisis ragam yang diperoleh menunjukkan adanya interaksi, maka dilakukan analisa lanjutan untuk mengetahui perlakuan mana yang paling berpengaruh pada percobaan. Jika interaksi tidak menunjukkan adanya pengaruh yang nyata tetapi ada pengaruh yang nyata pada perlakuan A maupun B, selanjutnya dilakukan uji beda nyata jujur (BNJ). Uji lanjutan ini berfungsi untuk mengetahui perbedaan setiap pasangan perlakuan.
3.5. Analisis Produk
Analisis yang dilakukan terhadap produk hidrolisat meliputi analisis kadar air, kadar abu, kadar protein, kadar lemak, kadar a-amino nitrogen bebas, daya cerna in vitro dan analisis asam amino.
3.5.1. Kadar air (AOAC 1995)
Prinsip analisis kadar air adalah proses penguapan air dari suatu bahan dengan cara pemanasan. Penentuan kadar air didasarkan pada perbedaan berat contoh sebelum dan sesudah dikeringkan.
Prosedur analisis kadar air adalah sebagai berikut : mula- mula cawan kosong yang akan digunakan dikeringkan dalam oven selama 15 menit atau sampai didapat berat tetap, kemudian didinginkan selama 30 menit dalam desikator, setelah dingin beratnya ditimbang. Sampel sebanyak 5 gram ditimbang dan dimasukkan ke dalam cawan kemudian dikeringkan dalam oven selama 6 jam pada suhu 100oC sampai 102oC. Cawan kemudian didinginkan dalam desikator selama 30 menit dan setelah dingin ditimbang kembali. Persentase kadar air (berat basah) dapat dihitung dengan rumus sebagai berikut :
Kadar air (%) 1 2 X 100% B
B B − =
Keterangan : B = Berat sampel (gram)
3.5.2. Kadar abu (AOAC 1995)
Prinsip analisis kadar abu adalah proses pembakaran senyawa organik sehingga didapat residu anorganik yang disebut abu.
Prosedur analisis kadar abu adalah sebagai berikut : cawan kosong dipanaskan dalam oven kemudian didinginkan dalam desikator selama 30 menit dan ditimbang beratnya. Sampel ditimbang sebanyak 5 gram dan diletakkan dalam cawan, kemudian dibakar dalam kompor listrik sampai tidak berasap. Cawan kemudian dimasukkan dalam tanur. Pengabuan dilakukan dalam dua tahap yaitu pada suhu 450oC dan pada suhu 550oC, pengabuan dilakukan sekitar 2-3 jam. Cawan kemudian didinginkan dalam desikator, setelah dingin cawan kemudian ditimbang. Persentase dari kadar abu dapat dihitung menggunakan rumus sebagai berikut :
3.5.3. Kadar protein dan total nitrogen (AOAC 1995)
Prinsip analisis kadar protein dan total nitrogen adalah proses pembebasan nitrogen dari protein dalam bahan menggunakan asam sulfat dengan pemanasan. Penentuan total nitrogen dan kadar protein menggunakan metode mikrokjeldahl.
Prosedur analisis kadar protein dan total nitogen adalah sebagai berikut : contoh (0,2 g) dimasukkan ke dalam tabung kjeldahl 30 ml. Ditambahkan 1,9 gram K2SO4, 40 mg HgO dan 2,5 ml H2SO4, serta beberapa tablet kjeldahl. Contoh dididihkan selama 1-1,5 jam sampai cairan menjadi jernih kemudian didinginkan. Isi labu dituangkan ke dalam alat destilasi, labu dibilas sebanyak 5-6 kali dengan akuades (20 ml). Air bilasan juga dimasukkan ke dalam alat destilasi dan ditambahkan larutan NaOH 40 % sebanyak 20 ml.
Kadar protein dihitung berdasarkan kadar N dalam bahan dengan dikali faktor
3.5.4. Kadar lemak (AOAC 1995)
Prinsip analisis kadar lemak adalah ekstraksi yaitu pemisahan lemak dari contoh dengan cara mensirkulasikan pelarut lemak ke dalam contoh, sehingga senyawa-senyawa lain tidak dapat larut dalam pelarut tersebut.
Ada dua metode yang digunakan dalam penelitian ini yaitu : (a) metode soxhlet untuk sampel padat dan (b) metode hidrolisis untuk sampel cair.
(a) Metode soxhlet
Contoh sebanyak 5 g ditimbang dan dibungkus dengan kertas saring dan diletakkan pada alat ekstraksi soxhlet yang dipasang diatas kondensor serta labu lemak dibawahnya. Pelarut heksana dituangkan ke dalam labu lemak secukupnya sesuai dengan ukuran soxhlet yang digunakan dan dilakukan refluks selama minimal 16 jam sampai pelarut turun kembali ke dalam labu lemak. Pelarut di dalam labu lemak didestilasi dan ditampung. Labu lemak yang berisi lemak hasil ekstraksi kemudian dikeringkan dalam oven pada suhu 105oC selama 5 jam. Labu lemak kemudian didinginkan dalam desikator selama 20-30 menit dan ditimbang. (b) Metode hidrolisis
Prinsip analisis kadar lemak metode hidrolisis adalah membebaskan lemak dari senyawa-senyawa lain melalui proses hidrolisis dengan pelarut asam sebelum dilakukan proses ekstraksi.
Kaca penutup dibilas dengan 100 ml air panas dan disatukan dengan hancuran. Hancuran/hasil hidrólisis disaring melalui kertas saring berlipat bebas lemak. Gelas piala dibilas beberapa kali dengan air panas (±70oC) dan air cucian tadi dituangkan ke dalam penyaring. Kertas saring dicuci dengan air panas hingga saringan bebas asam. Kertas saring beserta isinya dikeringkan dalam oven pada suhu 100oC-105oC, kemudian dimasukkan ke dalam selongsong kertas saring atau asbes (extraction thinble). Selongsong beserta isinya dimasukkan ke dalam alat soxhlet. Kemudian alat soxhlet dihubungkan dengan labu ekstraksi 250 ml yang berisi beberapa butir batu didih dan telah diketahui bobotnya. Jumlah heksana dalam labu tidak kurang dari 50 ml. Alat soxhlet dihubungkan dengan pendingin (cooler), kemudian labu ekstraksi dipanaskan dan diekstrak selama 6 jam. Kemudian labu dikeringkan dalam oven, didinginkan dalam desikator selama 30 menit dan ditimbang hingga bobotnya tetap.
Perhitungan kadar lemak :
3.5.5. Kadar a-amino nitrogen bebas (LPTP 1974)
Prinsip analisis kadar a-amino nitrogen bebas adalah pada penambahan suspensi kupripospat ke dalam filtrat yang dibuat dari ekstrak contoh dalam larutan asam tricloroasetat (TCA 7%), maka tembaga (Cu++) akan membentuk senyawa kompleks dengan gugus asam amino yang berbanding langsung dengan grup amino yang ada.
5 ml, kemudian dititrasi dengan larutan standar natrium tiosulfat 0,01 N lalu ditambahkan 4 tetes indikator kanji 1% dan dititrasi lagi hingga warna biru tepat menghilang. Penetapan blanko dilakukan dengan mengganti contoh dengan 10 ml TCA 7 %.
Rumus perhitungannya adalah sebagai berikut :
Prinsip analisis daya cerna protein in vitro adalah mengukur kadar nitrogen yang tidak dicerna oleh enzim pada kondisi yang menyerupai metabolisme tubuh mencerna makanan.
Prosedur analisis daya cerna secara in vitro adalah sebagai berikut : sampel ditimbang sebanyak 1 gram dan ditambah larutan HCl 0,1 N 15 ml yang mengandung 1,5 mg pepsin. Lalu dikocok dalam shaker sela ma 3 jam pada suhu 37oC, kemudian ditambah larutan NaOH 0,5 N sehingga pH 6,8 dan ditambah 4 mg pankreatin yang telah dilarutkan dalam bufer fosfat 0,2 M. Lalu dikocok dalam shaker selama 24 jam pada suhu 37oC. Residu padatan dipisahkan dengan cara sentrifuse (20.000 G suhu 5oC selama 10 menit). Kemudian dicuci 5 kali dengan 30 ml akuades (untuk setiap kali pencucian, supernatan dipisahkan dengan cara sentrifuse). Terakhir residu disaring dengan milipore filter (1,2 mikron), dikeringkan dan dianalisa kadar nitrogennya dengan metode mikrokjeldhal.
3.5.7. Analisis asam amino (Nur, Adijuwana 1989)
Prinsip analisis asam amino dengan menggunakan HPLC adalah memisahkan asam amino berdasarkan sifat asam dan basanya menggunakan
kolom pico tag amino acid water. Jenis HPLC yang digunakan dalam penelitian ini adalah HPLC Water. Prosesnya menggunakan Na-asetat : asetonitril (60 : 40) sebagai fase gerak dan trimetilxylena sebagai fase diam. Uraian proses selengkapnya adalah sebagai berikut :
a) Hidrolisis asam
Ditimbang 0,25 gram contoh dalam tabung reaksi tertutup, kemudian ditambahkan 5 ml HCl 6 N dan dialiri dengan gas N2 dan ditutup. Setela h itu, dimasukkan ke dalam oven bersuhu 100oC selama 18-24 jam, cairan contoh disaring dengan menggunakan kertas saring.
b) Pengeringan
Cairan contoh hasil hidrolisis dipipet sebanyak 10 µl ke dalam tabung reaksi dan ditambahkan sebanyak 30 µl larutan pengering (methanol : Na-asetat : trietilasetat = 2 : 2 : 1). Setelah itu bahan tersebut dikeringkan dengan pompa vakum bertekanan 50 Torr (3x).
c) Derivatisasi
Larutan derivat (methanol : trimetilasetat : penilisotiosianat = 7 : 1 : 1). Ditambahkan sebanyak 30 µl ke dalam contoh yang telah dikeringkan. Kemudian dibiarkan ± 20 menit, lalu dikeringkan dengan pompa vakum bertekanan 50 Torr. Setelah itu, contoh yang telah kering diencerkan dengan 200 µl larutan pengencer (Na-asetat 1M), sehingga diperoleh larutan contoh yang siap dianalisis.
d) Analisis asam amino dengan alat HPLC Kondisi alat HPLC pada saat dilakukan analisis : 1. Temperatur kolom : 38oC
2. Kolom : Pico tag 3,9 x 150 nm coulomb 3. Kecepatan alir : 1,5 ml/menit
4. Batas tekanan : 3000 psi 5. Program : Gradient
6. Fase gerak : - Asetonitril 60 %
7. Detektor : UV
8. Panjang gelombang : 254 nm
Untuk analisis kuantitatif dapat dihitung dengan cara :
Asam amino (%)
contoh Bobot
x BM x Fp x dar s
C x dar s
LA
sampel LA
100 tan
tan
=
Keterangan : C = Konsentrasi
LA = Luas area
4. HASIL DAN PEMBAHASAN
4.1. Penelitian Pendahuluan
Penelitian pendahuluan dilakukan untuk mengetahui kandungan kimia ikan selar kuning, mengetahui aktivitas optimum enzim papain terhadap substrat (ikan) dalam berbagai konsentrasi dan untuk mencari waktu dan pH optimum reaksi hidrolisis protein ikan selar kuning.
4.1.1. Komposisi kimia ikan selar kuning (Caranx leptolepis)
Hasil analisis kandungan kimia ikan selar kuning yang digunakan dalam penelitian ini dapat dilihat dalam Tabel 7. Ikan selar kuning yang digunakan di dalam penelitian ini adalah ikan selar kuning segar. Analisis kimia dilakukan untuk mengetahui kandungan gizi ikan selar kuning. Melalui analisis tersebut diketahui bahwa ikan selar kuning memiliki komposisi kimia dalam basis basah yaitu kadar air sebesar 75,71 %, kadar abu 2,31 %, kadar protein 15,61 % serta kadar lemak sebesar 2,94 %.
Tabel 7. Komposisi kimia ikan selar kuning (Caranx leptolepis)
Nilai rata – rata (%)
Parameter Basis Basah (BB) Basis Kering (BK)
Kadar Air 75,71 -
Kadar Abu 2,31 9,51
Kadar Protein 15,61 64,27
Kadar Lemak 2,94 12,10
(Stansby 1982). Pada penelitian ini dipilih ikan selar kuning karena ikan ini termasuk jenis ikan yang selalu ada tiap musim dan harganya relatif murah.
4.1.2. Aktivitas enzim papain terhadap substrat
Pada proses hidrolisis dengan menggunakan enzim, substrat yang digunakan diubah menjadi produk hidrolisat, tetapi masih ada jumlah substrat yang masih tersisa yang dalam hal ini disebut padatan sisa.
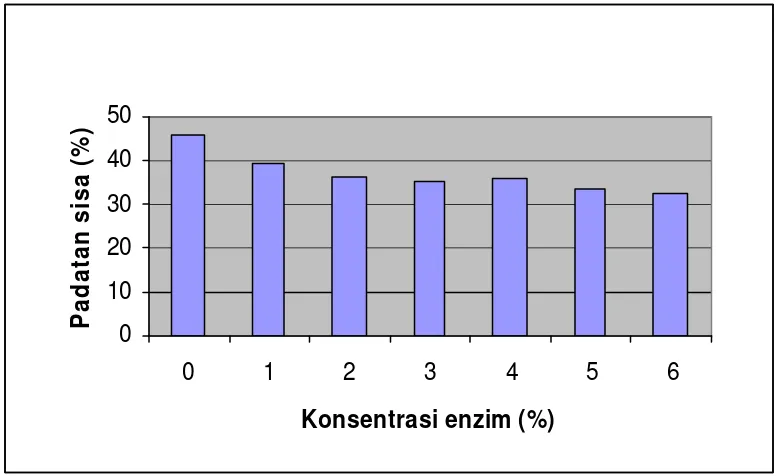
Hasil penelitian menunjukkan bahwa padatan sisa yang dihasilkan rata-rata berkisar antara 45,98 % - 32,65 %. Nilai padatan sisa yang dihasilkan dapat dilihat pada Gambar 4.
0 10 20 30 40 50
0 1 2 3 4 5 6
Konsentrasi enzim (%)
Padatan sisa (%)
Gambar 4. Hasil pengukuran padatan sisa hidrolisis protein ikan
Gambar 4 memperlihatkan grafik yang menunjukkan penuruna n nilai padatan sisa dengan semakin besar penambahan enzim. Untuk hidrolisis substrat dengan perlakuan tanpa penambahan enzim papain (perlakuan kontrol) terlihat bahwa padatan sisa yang dihasilkan masih besar jika dibandingkan dengan perlakuan yang lain ya itu sebesar 45,98 %. Hal ini berarti subsrtat yang digunakan hanya terhidrolisis menjadi produk dalam jumlah yang sedikit.
dihasilkan padatan sisa yang semakin menurun yaitu dari mulai 39,24 % sampai dengan 32,65 %.
Berdasarkan analisis sidik ragam (Lampiran 3) konsentrasi enzim memberikan pengaruh nyata (Fhit > Ftab) terhadap padatan sisa yang dihasilkan. Hasil uji lanjut Beda Nyata Terkecil (BNT) menunjukkan bahwa perlakuan konsentrasi enzim papain 0 % sampai 5 % secara umum memberikan pengaruh yang berbeda nyata antar perlakuan, sedangkan antara perlakuan 5 % dengan perlakuan 6 % tidak berbeda nyata. Hal ini menunj ukkan bahwa peningkatan konsentrasi enzim berpengaruh terhadap peningkatan kecepatan pembentukan produk atau hidrolisis substrat. Pada proses hidrolisis substrat kecepatan aktivitas katalitik enzim semakin naik dan akhirnya akan mencapai suatu batas maksimum dan setelah batas ini terlampaui, kecepatan reaksi tetap meningkat tapi dengan nilai yang semakin kecil. Pada kondisi tersebut enzim menjadi jenuh oleh substratnya dan tidak dapat berfungsi lebih cepat (Lehninger 1993). Sehingga jumlah produk yang dihasilkan tidak mengalami peningkatan atau jumlah sisa substrat yang dihidrolisis tidak dapat dikurangi lagi. Berdasarkan penjelasan di atas diambil konsentrasi enzim terbaik yaitu pada konsentrasi 5 % untuk tahap penelitian selanjutnya.
Di dalam penelitian digunakan perlakuan penambahan enzim papain dalam jumlah yang cukup besar, hal ini dikarenakan enzim yang digunakan mempunyai aktivitas sangat kecil yaitu sebesar 1,0593 unit/gram menit (Kusnaeni 1993). Sedangkan jika menggunakan enzim papain murni denga n aktivitas sebesar 488 unit/gram menit, bisa digunakan enzim dalam konsentrasi yang lebih kecil dan waktu hidrolisis yang lebih singkat (Hasnan 1991).
4.1.3. Kondisi optimum proses hidrolisis protein ikan
Tabel 8. Kandungan a-amino nitrogen bebas hasil hidrolisis ikan selar kuning
a - amino nitrogen bebas (gr/100gr) pH
Waktu (jam) 6,5 7 7,5
5 0,03 0,03 0,02
5,5 0,03 0,02 0,02
6 0,03 0,04 0,03
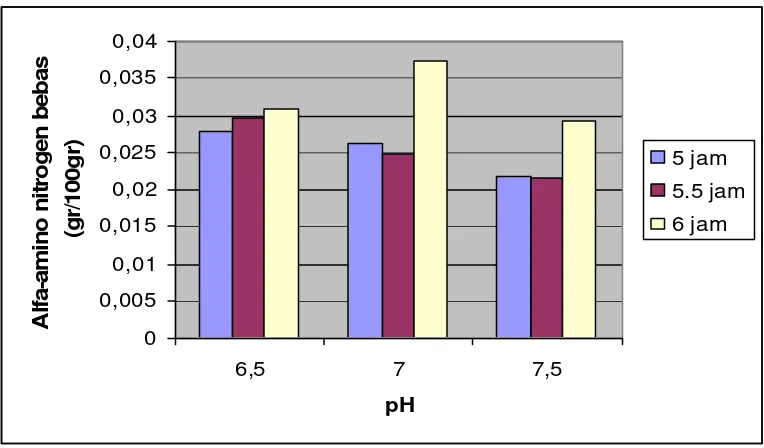
Tabel 8 memperlihatkan bahwa nilai rata-rata kadar a-amino nitrogen bebas pada berbagai perlakuan berkisar antara 0,02 sampai 0,04. Histogram nilai a-amino nitrogen bebas dapat dilihat pada Gambar 5.
0
Gambar 5. Histogram kandungan a-amino nitrogen bebas selama proses hidrolisis ikan selar kuning
Gambar 5 me mperlihatkan bahwa nilai terendah diperoleh pada perlakuan pH 7,5 dan waktu hidrolisis 5,5 jam, sedangkan nilai tertinggi diperoleh pada perlakuan pH 7 dan waktu hidrolisis 6 jam.
tidak berbeda nyata. Untuk perlakuan waktu, menunjukkan bahwa waktu hidrolisis 6 jam berbeda nyata dengan perlakuan yang lain, sedangkan antara waktu hidrolisis 5 jam dengan waktu hidrolisis 5,5 jam tidak berbeda nyata. Sedangkan untuk interaksi keduanya kombinasi perlakuan pH 7 dan waktu hidrolisis 6 jam memberikan pengaruh yang berbeda nyata terhadap perlakuan yang lain.
Secara umum kandungan a-amino nitrogen bebas cenderung meningkat dengan semakin lamanya waktu hidrolisis untuk masing- masing perlakuan pH yang digunakan. Hal ini karena salah satu faktor yang mempengaruhi proses hidrolisis adalah waktu, dimana semakin lama waktu yang digunakan maka proses hidrolisis berjalan lebih sempurna. Dengan proses hidrolisis yang berjalan semakin sempurna maka semakin tinggi nilai a-amino nitrogen bebas yang dihasilkan (Hall 1946 yang diacudalam Susana 1981).
Hidrolisis protein akan menambah kepolaran protein sehingga molekul protein yang tidak larut dalam air akan larut dengan adanya proses hidrolisis. Hal ini menyebabkan kenaikan kadar amino nitrogen bebas dengan bertambahnya waktu hidrolisis (Harrow, Mazur 1971 yang diacu dalam Indrawaty 1983). Nilai pH dan waktu optimum dalam proses hidrolisis ini dihubungkan dengan sifat enzim yang digunakan, yaitu enzim papain yang mempunyai keaktifan pada pH 5 sampai 8 dan stabil pada pH mendekati netral (EDC 1999). Berdasarkan hasil penelitian ini terbukti bahwa pH 7 dan waktu hidrolisis 6 jam memberikan nilai a-amino nitrogen bebas paling tinggi yaitu sebesar 0,04 gr/100gr.
4.2. Penelitian Utama
Berdasarkan hasil penelitian pendahuluan, diketahui bahwa proses hidrolisis protein ikan selar kuning dengan menggunakan enzim papain sebesar 5 % terhadap substrat pada pH 7 dan waktu hidrolisis 6 jam menghasilkan protein hidrolisat yang terbaik. Selanjutnya variabel hasil penelitian pendahuluan tersebut digunakan untuk memproduksi protein hidrolisat ikan selar kuning. Produk hidrolisat protein ikan selar kuning pada penelitian ini dalam bentuk pekatan. Untuk melihat kemungkinan pemakaian hidrolisat protein ikan sebagai bahan suplemen makanan, maka terhadap produk hidrolisat dilakukan analisa yang
uji a-amino nitrogen bebas, uji daya cerna in vitro dan analisis asam amino. Hasil analisa produk hidrolisat protein ikan selar kuning tercantum pada Tabel 9.
Tabel 9. Hasil analisa produk hidrolisat protein ikan selar kuning Nilai rata -rata
Parameter Basis Basah Basis Kering
Kadar Air (%) 91,99 - Nilai perbandingan a-amino nitrogen bebas
dan nitrogen total
0,07 -
Daya Cerna In vitro (%) 65,25 -
4.2.1. Kadar air
Air merupakan komponen utama bahan makanan, air dalam bahan makanan sangat menentukan kesegaran dan daya tahan bahan tersebut karena kandungan air berkaitan dengan perkembangan mikroorganisme dalam produk tersebut. Kandungan air bahan pangan tidak dapat ditentukan hanya dengan melalui bentuk fisiknya. Air juga dapat mempengaruhi tekstur, rupa maupun cita rasa bahan makanan (Winarno 1997).
Penambahan air secara berlebihan yang dilakukan dalam penelitian ini karena beberapa alasan, yang pertama yaitu mempermudah proses pengadukan selama hidrolisis berjalan yang berpengaruh terhadap kelancaran homogenasi antara enzim dengan substrat yang tersedia. Yang kedua mempercepat laju reaksi enzimatik, karena kadar air bebas yang rendah mengakibatkan penghambatan difusi enzim dan substrat sehingga proses hidrolisis hanya berlangsung pada
bagian substrat yang langsung berhubungan dengan enzim (Tucker 1995
yang diacu dalam Dewi 2002). Yang ketiga yaitu memperluas bidang kontak antara substrat dengan enzim, sehingga pada rentang waktu tertentu dapat dihasilkan produk hidrolisat yang lebih besar. Ikatan yang terbentuk antara enzim (sebagai reseptor) dengan makromolekul lain melibatkan kekuatan kovalen berupa
ikatan Van der Waals, ikatan hidrogen atau interaksi elektrostatik (Wilson, Walker 2000 yang diacu dalam Dewi 2002). Kemudahan pengikatan
enzim dengan substrat pada proses hidrolisis dipengaruhi oleh ikatan hidrogen. Ikatan hidrogen terbentuk akibat adanya reaksi pengikatan satu molekul air dengan tiga sampai empat molekul air lain yang ada disekelilingnya (Lehninger 1993). Molekul air merupakan molekul yang bersifat polar, sehingga memiliki muatan positif pada salah satu atom (ion H+) serta muatan negatif pada sisi lainnya (ion OH-). Pada saat hidrolisis berlangsung, ikatan peptida terputus dan sebagai gantinya lokasi pemutusan ikatan tersebut berikatan dengan enzim melalui pengikatan oleh ion-ion positif atau negatif dari molekul air. Hal inilah yang mengakibatkan pengikatan substrat pada sisi aktif enzim menjadi lebih mudah (Wilson, Walker 2000 yang diacudalam Dewi 2002).
4.2.2. Kadar abu
Sebagian besar bahan makanan (96 %) terdiri dari bahan organik dan air. Dalam proses pembakaran sampai suhu 600oC bahan organik mudah terbakar, sedangkan zat anorganik tidak terbakar. Zat anorganik yang tidak terbakar tersebut disebut abu yang terdiri dari mineral seperti Ca, Mg, Na, P, K, Fe, Mn dan Cu. Abu yang terbentuk berwarna putih abu-abu, berpartikel halus dan mudah dilarutkan (Winarno 1997).
dibandingkan dengan kadar abu produk hidrolisat yang pernah dilakukan oleh Jonhson, Peterson (1974), yaitu sebesar 45 % yang disebabkan oleh adanya penambahan NaCl dan Amonium klorida sehingga kadar abunya tinggi.
4.2.3. Kadar protein
Protein merupakan komponen terpenting dalam produk hidrolisat. Salah satu tujuan memproduksi produk hidrolisat ini adalah untuk memenuhi kebutuhan protein hewani, khususnya dari hasil perikanan. Tingkat mutu dari produk hidrolisat ini sangat ditentukan oleh kadar zat terlarut, terutama kadar proteinnya,
yang dihitung dengan kadar total nitrogen (Sutedja et al. 1981
yang diacudalam Syahrizal 1991).
Selama hidrolisis terjadi konversi protein yang bersifat tidak larut menjadi senyawa nitrogen yang bersifat larut, selanjutnya terurai menjadi senyawa-senyawa yang lebih sederhana, seperti peptida-peptida, asam amino dan amonia sehingga mudah diserap oleh tubuh. Apabila hidrolisis berlangsung sempurna, maka akan dihasilkan hidrolisat yang terdiri dari campuran 18-20 macam asam amino (Kirk, Othmer 1953).
Berdasarkan Tabel 9 terlihat bahwa kandungan protein produk hidrolisat sebesar 66,17 % (bk). Protein yang dikandung oleh produk hidrolisat ini adalah protein terlarut, sedangkan protein tidak terlarut sudah terbuang pada saat sentrifuse.
Kadar protein produk hidrolisat meningkat jika dibandingkan dengan kadar protein bahan baku ikan yang digunakan yaitu dari 64,27 % (bk) menjadi 66,17 % (bk). Peningkatan yang terjadi hanya sedikit, karena dalam proses hidrolisis dengan menggunakan enzim ini hanya terjadi proses pemecahan protein menjadi unsur-unsur yang lebih sederhana yaitu asam amino. Peningkatan tersebut bisa disebabkan oleh ikut terdeteksinya enzim yang digunakan dalam analisis protein yang dilakukan, karena enzim juga adalah protein.
4.2.4. Kadar lemak
Produk hidrolisat protein ikan dengan kadar lemak rendah umumnya mempunyai nilai mutu yang lebih stabil dan tahan lama jika dibandingkan dengan produk hidrolisat yang mempunyai kadar lemak yang tinggi.
Berdasarkan Tabel 9 dapat dilihat kandungan lemak yang dimiliki oleh produk hidrolisat protein ikan ini adalah sebesar 5,37 % (bk). Kadar lemak yang diperoleh pada produk hidrolisat protein ikan ini mengalami penurunan bila dibandingkan dengan kadar lemak bahan baku ikan yang digunakan yaitu dari 12,10 % (bk) menjadi 5,37 % (bk).
Rendahnya kadar lemak pada produk hidrolisat dapat digunakan sebagai bahan makanan diet yaitu makanan dengan kandungan lemak kurang dari 5 %. Selain itu produk ini dapat berfungsi sebagai suplemen pada pembuatan roti tawar dan makanan bayi (Pigot, Tucker 1990).
4.2.5. Kadar a-amino nitrogen bebas
Selama proses hidrolisis berlangsung, dihasilkan produk berupa peptida dan asam-asam amino yang dibebaskan oleh protein yang terhidrolisis. Jumlah produk berupa asam amino yang terdapat dalam hidrolisat protein disebut kadar a-amino nitrogen bebas.
Pada Tabel 9 di atas, terlihat bahwa nilai rata-rata kadar a-amino nitrogen bebas produk hidrolisat sebesar 0,06 gr/100gr. Nilai ini lebih tinggi jika dibandingkan dengan kadar a-amino nitrogen bebas produk hidrolisat yang dilakukan oleh Zakki (1999) yaitu sebesar 0,0392 gr/100gr. Hal ini menunjukkan bahwa proses hidrolisis yang dilakukan berjalan lebih sempurna. Semakin tinggi nilai a-amino nitrogen bebas produk hidrolisat berarti proses hidrolisis berjalan semakin baik. Proses hidrolisis yang berjalan baik dengan sempurna akan menghasilkan produk hidrolisat yang memiliki flavor dan mutu yang baik (Yokotsuka 1960).
perbandingan a-amino nitrogen bebas dengan nitrogen total bervariasi antara 0,02 sampai 0,67.
Berdasarkan Tabel 9 dapat dilihat bahwa nilai perbandingan a-amino nitrogen bebas dan nitrogen total sebesar 0,07. Nilai ini masih berada dalam kisaran nilai yang ditetapkan oleh Food Chemical Codex yaitu berada pada kisaran 0,02 sampai 0,67. Hal ini berati produk hidrolisat yang dihasilkan dapat digunakan sebagai suplemen makanan.
4.2.6. Daya cerna in vitro
Daya cerna in vitro protein adalah kemampuan suatu protein unuk dihidrolisis menjadi asam-asam amino oleh enzim-enzim pencernaan. Beberapa macam enzim pencernaan yang telah digunakan antara lain yaitu pepsin, pankreatin, tripsin, kimotripsin, peptidase atau campuran dari beberapa macam enzim tersebut. Daya cerna secara singkat dapat diartikan sebagai perbandingan jumlah nitrogen yang diserap tubuh dengan jumlah nitrogen yang dikonsumsi tubuh (Muchtadi 1989).
Suatu protein yang mudah dicerna menunjukkan bahwa jumlah asam-asam amino yang diserap dan digunakan oleh tubuh mempunyai daya cerna tinggi dan sebaliknya, suatu protein yang sukar dicerna berarti jumlah asam-asam amino yang diserap dan digunakan oleh tubuh mempunyai daya cerna rendah karena sebagian besar akan dibuang oleh tubuh bersama feses (Muchtadi 1989).
mengukur daya cerna telur dan ikan adalah secara in vivo berbeda dengan metode yang digunakan dalam penelitian ini yaitu secara in vitro.
Hidrolisis protein yang sempurna akan menghasilkan asam-asam amino yang semakin meningkat pula sehingga makin banyak yang diserap oleh usus. Protein yang diserap oleh usus adalah berbentuk asam amino. Namun kadang-kadang peptida dan molekul- molekul protein kecil, dapat juga diserap melalui dinding usus dan masuk ke dalam pembuluh darah (Winarno 1997).
Daya cerna yang cukup tinggi pada produk hirdolisat dapat digunakan sebagai food suplement pada makanan bayi dan anak-anak. Selain itu, sifatnya yang higroskopis produk hidrolisat ini dapat ditambahkan pada minuman kesehatan yang dapat menambah kandungan asam amino dalam minuman tersebut.
4.2.7. Asam amino
Kualitas protein dapat ditentukan dengan melihat kandungan asam amino penyusunnya. Tidak semua protein mempunyai nilai gizi yang sama karena perbedaan jumlah dan jenis asam amino yang terkandung dalam tiap protein. Apabila suatu protein mengandung semua asam amino yang penting dalam jumlah yang diperlukan tubuh, maka protein ini disebut protein “lengkap” dan bila mengalami kekurangan salah satu saja asam amino esensialnya maka dapat
digolongkan dalam protein yang “tidak lengkap” (Harper et al. 1988
yang diacudalam Napitupulu 2003).
Analisis asam amino ditujukan untuk mengetahui jenis dan jumlah asam amino esensial yang terkandung dalam suatu protein bahan pangan. Di samping itu juga analisis asam amino berguna untuk memperkirakan nilai- nilai gizi protein tersebut (Muchtadi 1989).
Semua protein akan menghasilkan asam-asam amino bila dihidrolisis, tetapi ada beberapa protein yang disamping menghasilkan asam amino juga menghasilkan molekul- molekul protein yang masih berikatan (West, Todd 1964).
Tabel 10. Kandungan asam-asam amino produk hidrolisat protein ikan
Jumlah (%)
No Jenis Asam Amino Produk hidrolisat Capelin hidrolisat*
1 Asam Aspartat 0,185 9,89
Asam amino yang perlu mendapat perhatian khusus bagi nutrisi protein adalah asam amino yang termasuk asam amino esensial. Dimana asam amino yang termasuk asam amino esensial untuk manusia, yaitu lisin, leusin, isoleusin, treonin, triptofan, fenilalanin, valin, metionin, arginin dan histidin. Arginin merupakan asam amino esensial untuk bayi dan histidin merupakan asam amino esensial untuk anak-anak, tetapi keduanya tidak esensial bagi orang dewasa (Muchtadi 1989). Pada produk hidrolisat ini hampir semua jenis asam amino esensial tersebut dihasilkan kecuali triptofan yang dalam hal ini tidak dianalisis, karena mengalami kerusakan pada saat proses hidrolisis asam. Untuk menganalisis asam amino tersebut harus dengan proses hidrolisis basa.
Sebagai bahan pangan, asam amino serin, glisin, alanin dan valin memiliki rasa yang manis. Sedangkan rasa gurih disebabkan oleh asam glutamat (West, Todd 1964).
5. KESIMPULAN DAN SARAN
5.1. Kesimpulan
Hasil penelitian pendahuluan menunjukkan ikan selar kuning layak untuk dihidrolisis karena mempunyai kandungan protein yang cukup tinggi yaitu 15,61 % (bb). Kondisi optimum untuk menghidrolisis ikan selar kuning menjadi produk hidrolisat protein adalah pada konsentrasi enzim papain 5 %, pH 7 dan waktu proses selama 6 jam.
Berdasarkan hasil analisis produk yang dilakukan pada hidrolisat protein yang berupa pekatan diperoleh bahwa kadar abu 16,98 % (bk), kadar protein sebesar 66,17 % (bk), kadar lemak sebesar 5,37 % (bk), sedangkan kadar air sebesar 91,99 % (bb). Kandungan a-amino nitrogen bebasnya sebesar 0,06 gr/100gr. Nilai perbandingan a-amino nitrogen bebas dan nitrogen total yang dihasilkan sebesar 0,07. Nilai daya cerna in vitro yang dimiliki produk hidrolisat adalah sebesar 65,25 %. Sedangkan kandungan asam amino produk hidrolisat protein ini terdiri dari 17 macam asam amino, dan hampir semua asam amino esensial pada produk hidrolisat protein ini dihasilkan.
5.2. Saran
Disarankan untuk melakukan penelitian lebih lanjut dengan menggunakan enzim papain yang lebih murni dengan keaktifan yang tinggi serta dalam proses hidrolisis digunakan perbandingan air yang tidak terlalu besar. Perlu dilakukan penelitian tentang pembuatan produk hidrolisat dalam bentuk serbuk ataupun tepung dengan menggunakan metode pengeringan yang lebih baik dan murah serta diaplikasikan produk hidrolisat yang dihasilkan ke dalam makanan.
DAFTAR PUSTAKA
[AOAC] Association of Official Analytical Chemists. 1995. Official Methods of Analysis of The Association of Official Analytical Chemist. Arlington Virginia USA : Published by The Association of Official Analytical Chemists, Inc.
Baker B. 1996. Plant nutrition from the sea. Farmer to Farmer. No.16.
Beveridge AJ. 1996. A.Theoretical study of the active sites of papain and S195C rat trypsin: implications for the low reactivity of mutant serine proteinases.
Journal of Protein Science. Cambridge University Press. 5:1355-1365. Delvin RM. 1978. Immobilized Enzymes Research and Development. New York :
Jonh Willey and Sons.
Djuhanda T. 1981. Dunia Ikan. Bandung : Penerbit Armico.
[Direktorat Gizi Departemen Kesehatan R.I]. 1989. Daftar Komposisi Bahan Makanan. Jakarta : Bharata. 56 hal.
Dewi GC. 2002. Studi penggunaan enzim papain pada produksi hidrolisat protein ikan [skripsi]. Bogor : Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Dahuri R. 2004. Membangun Perekonomian Nasional untuk Mewujudkan Indonesia yang Maju, Makmur dan Berkeadilan Melalui Pembangunan Kelautan dan Perikanan. Jakarta : Departemen Kelautan dan Perikanan Republik Indonesia.
[EDC] Enzyme Development Corporation. 1999. Meat Tenderezing, A Brief Discussion. New York : Enzyme Development Corporation.
Fujimaki M, Arai S, Yamashita M. 1997. Enzymatic protein degradation and resynthesis for protein improvement. Di dalam : Food Protein. Editor Feeney R E dan Whitaner J R. Advances in chemistry series. Washington DC : American Chemical Soc.
Gesualdo AML, Li-Chan ECY. 1999. Functional properties of fish protein hydrolisate from herring(Clupea harengus). Journal of Food Science. 64 (6):1000-1004.
Govindan TK. 1985. Fish Processing Technology. New Delhi : Oxford and IBH Publishing Co. PVT. LTD.