EFEKTIVITAS
MATRICONDITIONING
PLUS AGENS
HAYATI DALAM PENGENDALIAN PATOGEN
TERBAWA BENIH, PENINGKATAN VIGOR
DAN HASIL PADI
AMIYARSI MUSTIKA YUKTI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN
Dengan ini saya menyatakan dengan sebenar-benarnya bahwa tesis yang berjudul:
EFEKTIVITAS MATRICONDITIONING PLUS AGENS HAYATI DALAM PENGENDALIAN PATOGEN TERBAWA BENIH, PENINGKATAN VIGOR,
DAN HASIL PADI
Merupakan karya saya sendiri di bawah bimbingan komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Semua data dan informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Agustus 2009
ABSTRACT
AMIYARSI MUSTIKA YUKTI, Effectiveness of Matriconditioning plus Biological Agents in Controlling Seed Borne Pathogens and Increasing Seed Vigor and Yield of Rice. Under direction of SATRIYAS ILYAS, SUDARSONO dan UDIN SUDINTA NUGRAHA.
The objective of the experiment was to develop technique of biological seed treatment by using biological agent incorporated in matriconditioning as to control seed borne pathogens and to improve seed vigor, plant growth and yield. The experiment used two seed lots of rice cv. IR 64 obtained from PT. Sang Hyang Seri, Subang, West Java. The seed lot I, harvested on 6 Juny 2007, was assigned as medium vigor with 88% germination, 13.8%/etmal speed of germination and 0% vigor index. The seed lot II, harvested on 10 September 2007, was assigned as high vigor with 97% germination, 17.14%/etmal speed of germination and 70% vigor index. Morphological fungal identification resulted three kinds of seed borne diseases for Lot I (Alternaria padwickii, Drechslera oryzae, and Fusarium moniliforme) and two kinds of seed borne diseases for Lot II (A. padwickii and D. oryzae). Bacterial identification based on morphological and biochemical analysis (gram, oxidase, starch hydrolyze, fluorescence and arginine) found three kinds of bacterial seed borne which are Xanthomonas oryzae
pv. oryzae, Xanthomonas campestris pv. oryzicola and Pseudomonas avenae. In the pre-experiment, Bacillus subtilis 5/B and 11/C obtained from BB Padi were used as biological agents to control growth of seed borne pathogens in-vitro. The effectivenessof the B. subtilis to control the seed borne pathogens was evaluated by using in-vitro dual culture. Bacillus subtilis 5/B inhibited not only the fungal growth of A. padwickii and D. oryzae (16.8 and 17.3%) but also the bacterial growth of X. oryzae pv. oryzae and X. campestris pv. orizycola. Meanwhile, B. subtilis 11/C could inhibit the fungal growth of A. padwickii and
D. oryzae (14.1 and 13.8%) but it did not inhibit the growth of bacteria. Therefore, B. subtilis 5/B was used as biological control for the main experiment.
The main experiment was conducted using completely randomized design with two factors. The first factor was seed vigor levels (high and medium), and the second one was seed treatment (untreated, Agrept 0.2% + Benlox 0.2%,
B. subtilis 5/B, matriconditioning, matriconditioning + Agrept 0.2% + Benlox 0.2%, matriconditioning + B. subtilis 5/B). Result of the laboratory experiment showed that all seed treatments not only increased seed viability i.e. germination and vigor (speed of germination and vigor index), but also reduced infection level of fungal and bacteria. Results of the screen house experiment showed that all seed treatments increased seedling height, number of productive tillers, and seed yield. In high vigor seed, matriconditioning plus B. subtilis 5/B as effective as matriconditioning plus Benlox 0.2% and Agrept 0.2% in increasing seed yield. Key words: biocontrol agents, rice seed, matriconditioning, seedborne pathogen,
RINGKASAN
AMIYARSI MUSTIKA YUKTI, Efektivitas Matriconditioning plus Agens Hayati dalam Pengendalian Patogen Terbawa Benih, Peningkatan Vigor Benih, dan Hasil Padi. Dibimbing oleh SATRIYAS ILYAS (Ketua), SUDARSONO dan UDIN SUDINTA NUGRAHA (Anggota).
Penelitian ini bertujuan untuk mengembangkan teknik inovatif perlakuan benih secara biologis menggunakan agens hayati yang diintegrasikan dengan
matriconditioning untuk dapat mengendalikan patogen terbawa benih sekaligus mencegah penyebaran penyakit, serta meningkatkan vigor benih, pertumbuhan tanaman dan hasil padi. Penelitian ini menggunakan dua sampel benih padi varietas IR-64 yang berasal dari PT. Sang Hyang Seri, Subang, Jawa Barat. Benih Lot I dipanen pada 6 Juni 2007, memiliki nilai daya berkecambah 88 %, kecepatan tumbuh 13.80 %/etmal dan indeks vigor 0 %, dikategorikan sebagai benih vigor sedang. Benih Lot II dipanen pada 10 September 2007, memiliki nilai daya berkecambah 97 %, kecepatan tumbuh 17.14%/etmal dan indeks vigor 70%, dikategorikan sebagai benih vigor tinggi. Pengamatan cendawan secara morfologi mengidentifikasi tiga patogen terbawa benih untuk vigor sedang (Alternaria padwickii, Drechslera oryzae, and Fusarium moniliforme) dan dua patogen terbawa benih untuk vigor tinggi (A. padwickii and D. oryzae). Berdasarkan pengujian morfologi dan biokimia (gram, oksidase, hidrolisa pati, fluoresen, dan arginin) ditemukan tiga jenis bakteri patogen terbawa benih, yaitu Xanthomonas oryzae pv. oryzae, Xanthomonas campestris pv. oryzicola dan Pseudomonas avenae.
Untuk pengujian awal, isolat agens hayati yang digunakan merupakan koleksi dari BB-Padi yaitu isolat Bacillus subtilis 5/B and 11/C sebagai agens hayati untuk menghambat pertumbuhan patogen terbawa benih secara in-vitro. Efektivitas B. subtilis untuk menghambat pathogen terbawa benih dievaluasi secara in-vitro dual culture. Bacillus subtilis 5/B dapat menghambat tidak hanya pertumbuhan cendawan A. padwickii dan D. oryzae (16.8 dan 17.3 %) tetapi juga pertumbuhan bakteri X. oryzae pv. oryzae dan X. campestris pv. oryzicola. Bacillus subtilis 11/C dapat menghambat pertumbuhan cendawan A. padwickii
and D. oryzae (14.1 and 13.8 %) tetapi tidak dapat menghambat pertumbuhan bakteri.
Berdasarkan hasil pengujian pendahuluan, B. subtilis 5/B digunakan sebagai agen hayati untuk pengujian utama. Pengujian menggunakan rancangan percobaan RAL dengan dua faktor. Faktor pertama adalah tingkat vigor benih (benih vigor sedang dan benih vigor tinggi) dan faktor kedua adalah perlakuan benih : tanpa perlakuan, Agrept 0.2 % + Benlox 0.2%, B. subtilis 5/B, matricondi-tioning, matriconditioning + Agrept 0.2% + Benlox 0.2%, matriconditioning +
jumlah malai produktif,dan berat gabah bernas per rumpun. Dalam meningkatkan hasil padi (berat gabah bernas per rumpun), pada benih vigor tinggi perlakuan benih dengan matriconditioning + B. subtilis 5/B sama efektifnya dengan matri-conditioning + Agrept 0.2% + Benlox 0.2%.
© Hak cipta milik Institut Pertanian Bogor, tahun 2009
Hak cipta dilindungi
Dilarang mengutip dan memperbanyak, sebagian atau seluruhnya dalam bentuk apa pun
EFEKTIVITAS
MATRICONDITIONING
PLUS AGENS
HAYATI DALAM PENGENDALIAN PATOGEN
TERBAWA BENIH, PENINGKATAN VIGOR,
DAN HASIL PADI
AMIYARSI MUSTIKA YUKTI
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Agronomi
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Efektivitas Matriconditioning plus Agens Hayati dalam Pengendalian Patogen Terbawa Benih, Peningkatan Vigor Benih, dan Hasil Padi
Nama : Amiyarsi Mustika Yukti
NIM : A151060181
Disetujui Komisi Pembimbing
Prof. Dr. Ir. Satriyas Ilyas, M.S. Ketua
Prof. Dr. Ir. Sudarsono, M.Sc. Anggota
Dr. Ir. Udin Sudinta Nugraha, M.S. Anggota
Diketahui
Ketua Program Studi Agronomi
Dr. Ir. Munif Ghulamahdi, M.S.
Dekan Sekolah Pascasarjana
Prof. Dr. Ir. Khairil A. Notodipuro, M.S.
PRAKATA
Syukur Alhamdulillah penulis panjatkan kepada Allah SWT atas segala karunia-Nya sehingga tesis ini dapat diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan dari bulan Desember 2007 sampai dengan September 2008 ini adalah perlakuan benih, dengan judul Efektivitas
Matriconditioning plus Agens Hayati dalam Pengendalian Patogen Terbawa Benih, Peningkatan Vigor Benih dan Hasil Padi. Tesis ini merupakan laporan penelitian yang dilakukan dalam empat tahap percobaan yaitu (1) Evaluasi Mutu dan Kesehatan Benih Padi Varietas IR 64 yang Berbeda Saat Panen, (2) Evaluasi Daya Hambat Agens Hayati terhadap Patogen Utama Terbawa Benih Padi, (3) Efektivitas Perlakuan Benih dalam Mengendalikan Patogen Utama Terbawa Benih dan Meningkatkan Vigor Benih, (4) Efektivitas Perlakuan Benih dalam Meningkatkan Hasil Padi di Rumah Kaca.
Terima kasih penulis sampaikan kepada Prof. Dr. Ir. Satriyas Ilyas, M.S.,
Prof. Dr. Sudarsono, M.Sc., dan Dr. Ir. Udin Sudinta Nugraha, M.S. selaku pembimbing dan Dr. Ir. Endang Murniati, M. S. serta Dr. Ir. Munif Ghulamahdi, M.S. selaku dosen penguji yang telah banyak memberikan saran sehingga tesis ini menjadi lebih baik. Penelitian ini dibiayai oleh proyek Kerjasama Kemitraaan Penelitian Pertanian dengan Perguruan Tinggi (KKP3T) dengan judul “Teknik Peningkatan Kesehatan dan Mutu Benih Padi” yang diketuai oleh Prof. Dr. Ir. Satriyas Ilyas, MS. Untuk itu penulis ucapkan terima kasih. Penghargaan penulis sampaikan pula kepada Menteri Pertanian, Sekretaris Direktorat Jenderal Tanaman Pangan dan Kepala Balai Besar Pengembangan Pengujian Mutu Benih Tanaman Pangan dan Hortikultura (BB-PPMBTPH) atas ijin, dukungan, biaya dan fasilitas yang diberikan selama penulis menempuh pendidikan di Sekolah Pascasarjana IPB. Ucapan terima kasih juga disampaikan kepada teman-teman di BB-PPMBTPH, terutama Ola, Dhila, Endang, Mbak Sri dan Bu Iyam, teman-teman mahasiswa pascasarjana PS. Agronomi atas bantuan yang diberikan. Untuk Rukmono Cahyadi suamiku, Akbar, Ageng dan Agung anak-anakku, Bapak H. R. Poerwandi, BA (Alm), Ibu Hj. Swabandilah, BA., Bapak dan Ibu Marsudi serta seluruh keluarga, terimakasih atas segala dukungan, doa dan kasih sayangnya.
Semoga tesis ini bermanfaat.
Bogor, Agustus 2009
RIWAYAT HIDUP
Penulis dilahirkan di Yogyakarta pada tangal 26 Maret 1968 dari ayah H.R. Poerwandi, BA. (Alm) dan ibu Hj. Swabandilah, BA. sebagai putri keempat dari lima bersaudara. Penulis menikah dengan Rukmono Cahyadi dan telah dikaruniai tiga orang putra, Akbar Andika Cahyadi, Ageng Irsyad Cahyadi dan Agung Ilham Cahyadi.
Tahun 1986 penulis diterima sebagai mahasiswi Fakultas Teknologi Pertanian Universitas Gadjah Mada Yogyakarta dan mendapat gelar sarjana Teknologi Pertanian (Ir) pada tahun 1991. Terhitung mulai 1 April 1994 penulis diangkat sebagai Pegawai Negeri Sipil Departemen Pertanian dan ditugaskan pada Balai Pengawasan dan Sertifikasi Benih Tanaman Pangan dan Hortikultura (BPSBTPH) I Provinsi Jawa Barat di Bandung sampai tahun 1996. Penulis beberapa kali berpindah tugas dikarenakan mengikuti tugas suami, yaitu tahun 1996-1998 bertugas di BPSBTPH III Provinsi Jawa Timur, tahun 1998-2000 bertugas di BPSBTPH VII Provinsi Bali dan tahun 2000 sampai saat ini bertugas di BPSBTPH XXVI Provinsi DKI Jakarta, yang kemudian instansi ini mengalami dua kali perubahan nama karena adanya perubahan eselon yaitu Balai Pengembangn Mutu Benih Tanaman Pangan dan Hortikultura (BPMBTPH) dan Balai Besar Pengembangan Pengujian Mutu Benih Tanaman Pangan dan Hortikultura sebagai pejabat fungsional Pengawas Benih Tanaman Ahli Muda.
DAFTAR ISI
Halaman
DAFTAR TABEL...
vii
DAFTAR GAMBAR...
ix
DAFTAR LAMPIRAN...
xi
PENDAHULUAN... 1
Latar Belakang...
1
Tujuan Penelitian...
5
Manfaat Penelitian... 5
EVALUASI MUTU DAN KESEHATAN BENIH PADI VARIETAS IR 64 YANG BERBEDA VIGOR
Pendahuluan... 7
Bahan dan Metode... 8
Hasil dan Pembahasan...
15
Kesimpulan... 19
EVALUASI AYA HAMBAT AGENS HAYATI TERHADAP PATOGEN
UTAMA TERBAWA BENIH PADI
Pendahuluan... 21
Bahan dan Metode... 22
Hasil dan Pembahasan...
25
EFEKTIVITAS PERLAKUAN BENIH DALAM MENGENDALIKAN
PATOGEN UTAMA TERBAWA BENIH
DAN MENINGKATKAN
VIGOR BENIH
Pendahuluan... 29
Bahan dan Metode... 31
Hasil dan Pembahasan...
35
Kesimpulan... 41
EFEKTIVITAS PERLAKUAN BENIH DALAM MENINGKATKAN
HASIL PADI DI RUMAH KACA
Pendahuluan... 42
Bahan dan Metode... 43
Hasil dan Pembahasan...
45
Kesimpulan ...
54
PEMBAHASAN UMUM...
55
KESIMPULAN DAN SARAN...
58
DAFTAR PUSTAKA...
59
DAFTAR TABEL
Halaman
1 Penyakit yang disebabkan oleh cendawan patogen pada benih padi... 3 2 Penyakit yang disebabkan oleh bakteri patogen pada benih
padi... 3 3 Karakter morfologi dan biokimia yang digunakan untuk
membedakan patogen Pseudomonas ... 12 4 Karakter morfologi dan biokimia yang digunakan untuk
membedakan patogen Xanthomonas ... 12 5 Hasil pengujian viabilitas dan vigor benih padi IR 64... 15 6 Persentase infeksi cendawan patogen terbawa benih pada benih padi
IR 64... 17 7 Kerapatan cendawan patogen terbawa benih pada benih padi
IR 64... 17 8 Hasil identifikasi koloni bakteri secara morfologi dan
biokimia... 18 9 Hasil penghitungan jumlah koloni bakteri patogen terbawa benih
padi IR 64 (cfu/ml)... 19 10 Pengaruh Bacillus subtilis terhadap penghambatan pertumbuhan
koloni Alternaria padwickii... 26 11 Pengaruh Bacillus subtilis terhadap penghambatan pertumbuhan
koloni Drechslera oryzae.... 26 12 Kemampuan penghambatan Bacillus subtilis terhadap ketiga bakteri
patogen terbawa benih... 27 13 Pengaruh interaksi perlakuan benih dan tingkat vigor terhadap daya
berkecambah (%)... 36 14 Pengaruh interaksi perlakuan benih dan tingkat vigor terhadap
indeks vigor (%)... 37 15 Pengaruh interaksi perlakuan benih dan tingkat vigor terhadap
16 Pengaruh interaksi perlakuan benih dan tingkat vigor terhadap jumlah bakteri Xanthomonas oryzae pv. oryzae (cfu/ml)... 39
17 Pengaruh interaksi perlakuan benih dan tingkat vigor terhadap jumlah bakteri Xanthomonas campestris pv. oryzicola (cfu/ml)... 39 18 Pengaruh interaksi perlakuan benih dan tingkat vigor terhadap
jumlah bakteri Pseudomonas avenae (cfu/ml)... 40 19 Pengaruh interaksi perlakuan benih dan tingkat vigor terhadap daya
tumbuh hari ke-5 (%)... 46 20 Pengaruh interaksi perlakuan benih dan tingkat vigor terhadap gabah
bernas per rumpun (g)... 50 21 Jenis dan jumlah cendawan yang ditemukan pada benih hasil rumah
kaca yang berasal dari benih vigor sedang (%)... 52 22 Jenis dan jumlah cendawan yang ditemukan pada benih hasil rumah
kaca yang berasal dari benih vigor sedang (%)... 53 23 Pengaruh perlakuan benih terhadap peningkatan viabilitas dan vigor
benih (%)... 56 24 Pengaruh perlakuan benih terhadap penurunan tingkat infeksi (%)
cendawan dan penurunan jumlah bakteri (cfu/ml)... 56 25 Pengaruh perlakuan benih terhadap peningkatan pertumbuhan dan
DAFTAR GAMBAR
Halaman
1 Alur
penelitian
efektivitas
matriconditioning
plus agens hayati dalam
pengendalian patogen terbawa benih, peningkatan vigor benih dan
hasil padi...
6
2
Spora cendawan yang ditemukan pada benih padi dengan perbesaran
100 x,
Alternaria padwickii
(a)
, Drechslera oryzae
(b)
,
dan
Fusarium moniliforme
(c)...
16
3
Koloni bakteri patogen terbawa benih
yang ditemukan pada benih
padi:
Xanthomonas oryzae
pv
oryzae
(a),
Xanthomonas campestris
pv.
oryzicola
(b) dan
Pseudomonas avenae
(c)...
18
4 Isolat
murni
cendawan patogen terbawa benih
Alternaria
padwickii
(a)
,
Dreschlera oryzae
(b)
,
dan
Fusarium moniliforme
(c).
22
5 Isolat
murni
bakteri
patogen terbawa benih
Xanthomonas oryzae
pv.
oryzae
(a),
Xanthomonas campestris
pv.
oryzicola
(b) dan
Pseudomonas avenae
(c)...
23
6
Isolat murni bakteri agens hayati
Bacillus subtilis
5/B (a) dan
11/C (b)...
23
7 Penghambatan
Bacillus subtilis
5/B (a) dan 11/C terhadap
Alternaria padwickii.
...
26
8 Penghambatan
Bacillus subtilis
5/B (a) dan 11/C (b) terhadap
Dreschlera oryzae.
...
27
9 Penghambatan
Bacillus subtilis
5/B tarhadap
Xanthomonas oryzae
pv
. oryzae
(a)
danXanthomonas campestris
pv.
oryzicola
(b)...
27
10
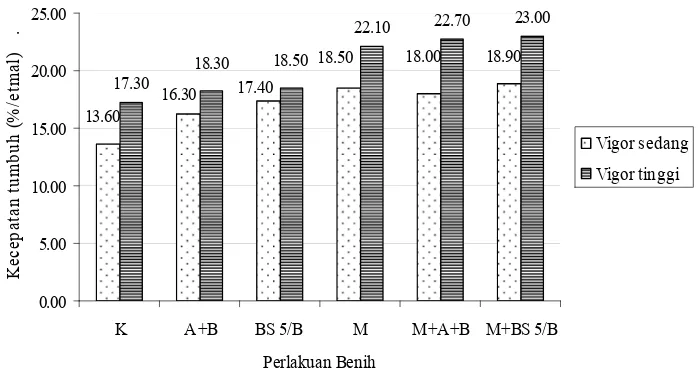
Pengaruh perlakuan benih terhadap kecepatan tumbuh (%/etmal)
benih padi vigor sedang dan vigor tinggi...
37
11
Pengaruh perlakuan pada benih padi vigor sedang dan vigor tinggi
terhadap tinggi tanaman (cm) pada minggu ke-2 ...
47
12
Pengaruh perlakuan pada benih padi vigor sedang dan vigor tinggi
13
Pengaruh perlakuan pada benih padi vigor sedang dan vigor tinggi
terhadap tinggi tanaman minggu ke-4 (cm)...
47
14 Pengaruh
perlakuan
pada benih padi vigor sedang dan vigor
tinggi
terhadap jumlah malai produktif per rumpun...
49
15
Pengaruh perlakuan pada benih padi vigor sedang dan vigor tinggi
DAFTAR LAMPIRAN
Halaman
1 Kondisi awal benih sumber yang digunakan dalam penelitian... 66
2 Analisis ragam pengujian daya berkecambah... 66
3 Analisis ragam pengujian kecepatan tumbuh... 66
4 Analisis ragam pengujian indeks vigor... 66
5 Analisis ragam persen infeksi cendawan Alternaria padwickii... 66
6 Analisis ragam persen infeksi cendawan Dreschlera oryzae... 66
7 Analisis ragam persen infeksi cendawan Fusarium moniliforme... 67
8 Analisis ragam jumlah colony forming unit per mililiter bakteri Xanthomonas oryzae pv. oryzae... 67
9 Analisis ragam jumlah colony forming unit per mililiter bakteri Xanthomonas campestris... 67
10 Analisis ragam jumlah colony forming unit per mililiter bakteri Pseudomonas avenae... 67
11 Uji Kruskal-Wallis pengaruh perlakuan benih dan tingkat vigor terhadap daya berkecambah... 68
12 Analisis ragam pengaruh perlakuan benih dan tingkat vigor terhadap kecepatan tumbuh... 70
13 Uji Kruskal-Wallis pengaruh perlakuan benih dan tingkat vigor terhadap indeks vigor... 70
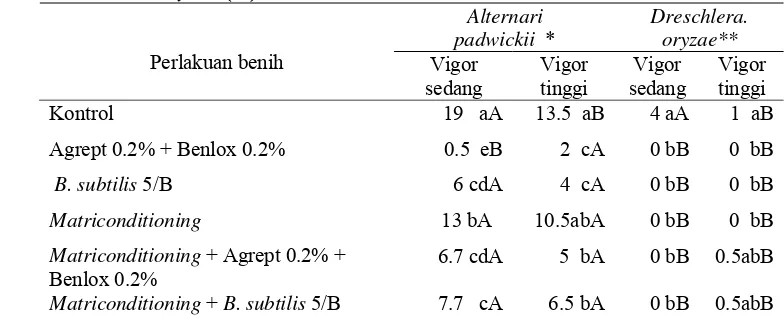
14 Analisis ragam pengaruh perlakuan benih dan tingkat vigor terhadap tingkat infeksi cendawan Alternaria padwickii... 72
15 Uji Kruskal-Wallis pengaruh perlakuan benih dan tingkat vigor terhadap persen infeksi cendawan Dreschlera oryzae... 72
17 Uji Kruskal-Wallis pengaruh perlakuan benih dan tingkat vigor terhadap jumlah colony forming unit per mililiter Xanthomonas campestris pv. oryzicola... 74 18 Uji Kruskal-Wallis pengaruh perlakuan benih dan tingkat vigor
terhadap jumlah colony forming unit per mililiter bakteri
Pseudomonas avenae... 76 19 Analisis ragam pengaruh perlakuan benih dan tingkat vigor
terhadap daya tumbuh hari ke-5 ... 77 20 Analisis ragam pengaruh perlakuan benih dan tingkat vigor
terhadap tinggi tanaman minggu ke-2... 78 21 Analisis ragam pengaruh perlakuan benih dan tingkat vigor
terhadap tinggi tanaman minggu ke-3... 78 22 Analisis ragam pengaruh perlakuan benih dan tingkat vigor
terhadap tinggi tanaman minggu ke-4... 78 23 Analisis ragam pengaruh perlakuan benih dan tingkat vigor
terhadap jumlah malai produktif per rumpun ... 79 24 Analisis ragam pengaruh perlakuan benih dan tingkat vigor
terhadap berat gabah bernas per rumpun... 79 25 Kondisi klimatologi rata-rata bulanan selama penelitian di rumah
PENDAHULUAN
Latar Belakang
Salah satu prioritas Departemen Pertanian dalam rangka revitalisasi pertanian adalah revitalisasi perbenihan. Pemerintah memberikan benih gratis kepada petani untuk meningkatkan produksi padi nasional sebanyak 3.5 juta ton gabah kering giling atau setara 2 juta ton beras pada 2007 dan selanjutnya 5% setiap tahun sampai tahun 2009. Pemerintah telah mengalokasikan anggaran sebanyak Rp 1 triliun pada tahun 2007 untuk program pemberian benih gratis tersebut. Dengan adanya bantuan benih gratis diharapkan mampu meningkatkan penggunaan benih bermutu menjadi 80% dari saat ini hanya 30% (Dirjentan 2007).
Agar tujuan program revitalisasi perbenihan dapat tercapai maka benih yang akan diberikan seyogyanya merupakan benih yang bermutu. Peranan benih adalah sebagai delivery mechanism artinya suatu benih dari varietas unggul yang dihasilkan oleh pemulia akan dirasakan manfaatnya oleh pelanggan hanya bila benih bermutu dari varietas tersebut tersedia dalam skala komersial. Bermutu berarti benih harus asli, hidup, sehat agar tidak menyebarkan penyakit terbawa benih, dan bersih (Nugraha 2004).
Mugnisjah dan Setiawan (1990) menyatakan bahwa benih dikatakan sehat kalau benih tersebut bebas dari patogen, baik berupa cendawan, bakteri, virus maupun nematoda. Patogen yang terbawa benih merupakan salah satu faktor yang mempengaruhi mutu benih.
Di dalam ISTA (2006) dinyatakan bahwa pengujian kesehatan benih mempunyai empat kepentingan:
1. Inokulum yang terbawa benih dapat berkembang menjadi penyakit yang menyerang pertanaman di lapang sehingga mengurangi nilai komersialnya. 2. Benih yang didatangkan ke daerah baru kemungkinan mengintroduksikan
2
3. Pengujian kesehatan benih mungkin dapat menjelaskan evaluasi kecambah dan penyebab rendahnya persentase daya berkecambah atau buruknya pertumbuhan benih di lapang, sehingga akan menjadi pelengkap uji daya berkecambah.
4. Hasil pengujian kesehatan benih dapat menunjukkan perlu tidaknya treatment
dalam suatu lot benih untuk mengendalikan patogen terbawa benih atau mengurangi resiko penyebaran penyakit.
Cendawan merupakan kelompok mikroorganisme yang paling banyak diketahui menginfeksi dan menginfestasi benih dibandingkan virus, bakteri maupun nematoda. Cendawan patogenik yang terbawa benih selain dapat menimbulkan penyakit pada tanaman dari benih yang bersangkutan, dapat juga menjadi sumber infeksi untuk tanaman lain yang masih sehat, baik di persemaian maupun di lapang. Salah satu patogen penting yang terbawa benih padi adalah
Alternaria padwickii penyebab penyakit stack burn dan seedling blight (Ou 1985). Jumlah pengujian kesehatan benih padi yang dilaksanakan oleh Laboratorium Benih Balai Pengawasan dan Sertifikasi Benih (BPSB) di seluruh Indonesia pada tahun fiskal 1990/1991, 1991/1992, 1992/1993 dan 1992/1994 berturut-turut adalah 459, 1027, 679 dan 679. Insiden tertinggi dari patogen pada padi adalah A. padwickii. Pada beberapa sampel infeksinya cukup tinggi mendekati 70%, Fusarium moniliforme adalah urutan deteksi berikutnya
meliputi hampir setengah sampel yang diuji. Cendawan Pyricularia oryzae hanya terdeteksi satu kali dari 1811 sampel, sedangkan Fusarium spp. cukup umum terdeteksi pada contoh benih yang diuji (Budiarti dan Haryanti 1996). Mew et al. (1988) mengemukakan bahwa terdapat beberapa cendawan patogen terbawa benih yang menyebabkan penyakit pada batang, daun, dan benih padi (Tabel 1).
Bakteri yang terbawa benih tidak jarang menyebabkan kerugian yang
berarti di lapang. Infeksi bakteri terjadi melalui pembungaan atau polong secara sistemik atau dari infeksi lokal dan kemudian berlokasi pada
permukaan atau dalam kulit biji, pada endosperma atau pada jaringan embrio, dan melalui jaringan vaskuler menuju ke bagian akar dan koleoptil
3
Berdasarkan laporan evaluasi kerusakan tanaman padi karena serangan organisme pengganggu tanaman (OPT), serangan OPT tahun 2003 mencapai areal seluas 360.965 ha. Penyakit yang menyebabkan pertanaman padi puso paling tinggi adalah bacterial leaf blight (hawar daun bakteri atau kresek) yang disebabkan bakteri Xanthomonas oryzae pv. oryzae (Direktorat Perlindungan Tanaman 2004). Siwi (2007) melaporkan bahwa kehilangan hasil padi akibat penyakit hawar daun bakteri (HDB) di Indonesia diperkirakan 40% per tahun.
Tabel 1. Penyakit yang disebabkan oleh cendawan patogen pada benih padi
Cendawan Penyakit
Pyricularia oryzae Drechslera oryzae Alternaria padwickii Fusarium moniliforme Cercospora janseana Gerlarcia oryzae Sarocladium oryzae
blast brown spot stack burn bakanae
narrow brown leaf spot leaf scald
sheath rot
Penularan atau penyebaran bakteri melalui benih penting untuk keberlangsungan hidup bakteri dan menentukan epidemi penyakit. Sutakaria (1984) melaporkan bahwa beberapa bakteri patogen terbawa benih padi telah diketahui menyebabkan penyakit penting pada tanaman padi (Tabel 2).
Tabel 2. Penyakit yang disebabkan oleh bakteri patogen pada benih padi
Bakteri Penyakit
Erwinia herbicola
Pseudomonas avenae
Pseudomonas fuscovaginae Pseudomonas glumae
Pseudomonas plantarii
Pseudomonas syringae pv syringae Xanthomonas oryzae pv oryzae Xanthomonas oryzae pv oryzicola
palea browning stripe
busuk pelepah busuk bulir padi hawar pada bibit bercak
4
Dari 59 sampel benih padi yang diuji tahun 2006 oleh Laboratorium Bakteri Balai Pengembangan Pengujian Mutu Benih Tanaman Pangan dan Hortikultura, bakteri terbawa benih yang teridentifikasi adalah X. oryzae pv.
oryzae (45 sampel), Xanthomonas campestris pv oryzicola (42 sampel),
P. glumae (17 sampel) dan P. avenae (15 sampel) (BPMBTPH 2006).
Salah satu alternatif pengendalian penyakit terbawa benih adalah pengendalian hayati menggunakan mikroorganisme yang berasosiasi secara alami dan sinergis dengan tanaman inang. Teknik pengendalian ini semakin populer karena meningkatnya kepedulian masyarakat terhadap permasalahan keamanan hayati dan permasalahan kesehatan lingkungan sehubungan dengan fitotoksisitas akibat penggunaan pestisida sintetik yang berlebihan. Hasil penelitian sebelumnya menunjukkan bahwa penggunaan mikroorganisme melalui aplikasi pada benih sebelum tanam secara nyata meningkatkan produksi padi (Kazempour 2004), kedelai (Bai et al. 2002), jagung (Thuar et al. 2004), dan cabai (Ilyas 2006).
Selain memacu pertumbuhan tanaman (biofertilizer), beberapa jenis mikro-organisme juga telah banyak dilaporkan mampu mengendalikan berbagai patogen tanaman (biopesticide). Sebagai contoh Bacillus spp. efektif mengendalikan Alternaria solani, Stemphilium solani pada benih tomat (Silva
et al. 2004), dan Colletotrichum capsici pada benih cabai (Sutariati et al. 2006). Penggunaan mikroorganisme menguntungkan yang secara alami berasosiasi dengan tanaman melalui aplikasi pada benih diharapkan dapat menjadi solusi strategis untuk memecahkan dua permasalahan utama dalam budidaya tanaman yaitu adanya tekanan biotik (mikroorganisme pengganggu penyebab penyakit) dan abiotik (ketidaktersediaan unsur hara atau hormon yang dibutuhkan untuk memacu dan meningkatkan pertumbuhan tanaman). Metode aplikasi agens hayati pada benih akan diintegrasikan dengan teknik invigorasi benih yang terbukti efektif meningkatkan viabilitas dan vigor benih berdasarkan hasil-hasil penelitian sebelumnya.
Upaya yang umum dilakukan dalam pengendalian penyakit tanaman adalah dengan menggunakan pestisida sintetik. Penggunaan pestisida sintetik ini dapat berdampak negatif terhadap lingkungan, organisme bukan sasaran,
5
dan dapat menimbulkan fitotoksisitas pada benih bila pemakaian tidak sesuai dengan peraturan yang berlaku.
Upaya pengendalian penyakit terbawa benih yang diintegrasikan dengan benih padi belum pernah dilaporkan. Dalam penelitian ini pengendalian penyakit terbawa benih dan peningkatan mutu benih padi dilakukan dengan perlakuan invigorasi benih menggunakan matriconditioning plus agens hayati Penelitian dilakukan dalam empat percobaan yaitu evaluasi mutu dan kesehatan benih padi varietas IR 64 yang berbeda vigornya berdasarkan perbedaan saat panen (percobaan 1), evaluasi daya hambat agens hayati terhadap patogen utama terbawa benih padi (percobaan 2), efektivitas perlakuan beni dalam mengendalikan patogen utama terbawa benih dan meningkatkan vigor benih (percobaan 3), dan efektivitas perlakuan benih dalam meningkatkan hasil padi di rumah kaca (percobaan 4). Alur penelitian dapat dilihat pada Gambar 1.
Tujuan Penelitian
Tujuan penelitian ini adalah mengembangkan teknik inovatif perlakuan benih secara biologis (biological seed treatment) menggunakan agens hayati yang diintegrasikan dengan matriconditioning untuk dapat mengendalikan patogen terbawa benih sekaligus mencegah penyebaran penyakit, serta meningkatkan vigor benih, pertumbuhan tanaman, dan hasil padi.
Manfaat Penelitian
Selain sebagai bahan perbanyakan tanaman, benih juga dapat menjadi sumber penyebaran penyakit di lapangan apabila benih tersebut membawa patogen bersamanya. Penelitian ini dilaksanakan sebagai salah satu alternatif untuk mengatasi permasalahan kesehatan benih padi melalui teknik pengendalian patogen terbawa benih berdasar strategi pengendalian ramah lingkungan dengan menggunakan agens hayati.
6
Gambar 1. Alur penelitian efektivitas matriconditioning plus agens hayati dalam pengendalian patogen terbawa benih, peningkatan vigor benih dan hasil padi.
Percobaan 1
Evaluasi mutu dan kesehatan benih padi varietas IR 64 yang berbeda vigo
Percobaan 2
Evaluasi daya hambat agens hayati terhadap patogen utama terbawa benih padi
Benih padi dengan dua tingat vigor yang terinfeksi cendawan dan bakteri patogenterbawa benih
Persentase daya hambat agens hayati 5/B dan 11/C serta kemampuan membentuk lingkaran bening (halo)
Percobaan 3
Efektivitas perlakuan benih dalam mengendalikan patogen utama terbawa benih dan meningkatkan vigor benih
Perlakuan benih yang terbaik di laboratorium
Percobaan 4
Efektivitas perlakuan benih dalam meningkatkan hasil padi di rumah kaca
Perlakuan benih yang efektif untuk skala rumah kaca
Formula
matriconditioning
Dua isolat
B. subtilis
EVALUASI MUTU DAN KESEHATAN BENIH PADI
VARIETAS IR 64 YANG BERBEDA VIGOR
PENDAHULUAN
Ilyas (2004) mengemukakan tentang mutu benih yang terdiri atas: 1) mutu
genetis, menjabarkan sifat unggul yang diwariskan oleh tanaman induk; 2) mutu
fisik yaitu struktur morfologis, ukuran, berat, dan penampakan benih; 3) mutu
fisiologis meliputi viabilitas dan vigor benih, dan 4) mutu patologis yang
ditujukan oleh keberadaan infeksi penyakit terbawa benih (seedborne) atau
kesehatan benih (seed health).
Sebagian besar ahli teknologi benih dan kalangan perdagangan
mengartikan viabilitas sebagai kemampuan benih untuk berkecambah dan
menghasilkan kecambah normal (Copeland & McDonald 1995). Pengujian daya
berkecambah adalah metode yang paling umum untuk menentukan viabilitas
benih. Pengujian daya berkecambah adalah prosedur analisis untuk mengevaluasi
perkecambahan benih pada kondisi yang optimum (favourable) dan
terstandardisasi yang jarang sekali sesuai dengan kondisi di lapang.
Vigor didefinisikan ISTA (2006) sebagai kumpulan sifat yang dimiliki
benih yang menentukan tingkat potensi aktivitas dan performance benih atau lot
benih selama perkecambahan dan munculnya kecambah. Tujuan pengujian vigor
adalah mempersiapkan informasi tentang planting value dalam jangkauan
lingkungan yang luas dan atau potensi daya simpan dari lot benih tersebut.
Dalam industri perbenihan yang semakin maju, maka kerugian akibat
beberapa patogen terbawa benih (seedborne) yang dianggap penting akan semakin
mendapat perhatian. Hal ini disebabkan karena penggunaan benih yang sehat
merupakan salah satu cara pengendalian penyakit yang diharapkan dapat menekan
biaya pengendalian penyakit di lapangan dan dapat meningkatkan kualitas
maupun kuantitas produksi. Pengujian kesehatan benih memegang peranan
penting untuk mengetahui status kesehatan suatu kelompok benih dengan cara
mendeteksi dan mengidentifikasi ada tidaknya patogen bawaan yang dapat
8
Sutakaria (1984) menyatakan bahwa pentingnya pengujian kesehatan
benih secara umum dapat digambarkan karena adanya beberapa tujuan,
diantaranya yaitu:
1. Untuk keperluan sertifikasi benih dalam usaha menghilangkan atau
mengurangi patogen yang terbawa benih. Dalam hal ini pengujian hanya
dilaksanakan apabila ada permintaan dari pengirim benih. Disamping itu
pengujian tersebut dapat menjadi pelengkap dari pengujian daya tumbuh
karena dapat dicari penyebab ketidak normalan bibit.
2. Untuk mengetahui perlu tidaknya dilakukan perlakuan benih sebelum
diadakan pertanaman atau penyimpanan.
Tujuan percobaan ini adalah untuk mengetahui mutu fisiologi dan patologi
awal dari benih padi yang akan digunakan pada percobaan selanjutnya.
BAHAN DAN METODE
Tempat dan Waktu Penelitian
Penelitian dilaksanakan di Laboratorium Pengujian Benih Balai Besar
Pengembangan Pengujian Mutu Benih Tanaman Pangan dan Hortikultura
(BB-PPMBTPH) Cimanggis, Depok. Penelitian dilaksanakan pada bulan Desember
2007.
Metodologi
Pengambilan Sampel Benih Padi Varietas IR 64
Pengambilan sampel dilakukan di PT. Sang Hyang Seri, Subang, Jawa
Barat. Dua sampel yang diambil merupakan benih padi varietas IR 64 yang
dipanen pada tanggal 6 Juni 2007 (Lot I) dan 10 September 2007 (Lot II).
Sampel benih padi dari PT. Sang Hyang Seri sudah dalam kemasan plastik
masing-masing seberat 1 kg, selanjutnya disimpan di Ruang Koleksi Benih
BB-PPMBTPH pada suhu 20-25 ºC. Untuk evaluasi mutu dan kesehatan benih,
dilakukan pengambilan contoh kerja dengan menggunakan soil devider, dan
dilaksanakan analisis kemurnian terlebih dulu untuk memisahkan benih murni
9
Pengujian Viabilitas dan Vigor Benih Padi
Pengujian viabilitas dan vigor dilakukan untuk mengetahui mutu fisiologis
awal dari sampel benih. Pengujian dilakukan dengan uji antar kertas (between
paper). Benih ditabur antara dua lapis kertas basah lalu digulung kemudian
dimasukkan dalam kantong plastik. Benih dikecambahkan di germinator pada
suhu 25ºC, benih yang digunakan berjumlah 200 benih (empat ulangan @ 50
benih) untuk pengujian viabilitas dan 200 benih untuk vigor. Pengamatan
dilakukan terhadap parameter viabilitas dan vigor benih:
1. Daya Berkecambah (DB), menggambarkan viabilitas potensial benih (Sadjad
et al. 1999), dihitung berdasarkan persentase kecambah normal (KN) hitungan
pertama yaitu 5 hari setelah tanam (HST) dan kedua (14 HST) dengan rumus:
DB(%) = ∑ KN hitungan I + ∑ KN hitungan II x100% ∑ benih yang ditanam
2. Indeks Vigor (IV), menggambarkan vigor kecepatan tumbuh (Copeland dan
McDonald 1995), dihitung berdasarkan persentase kecambah normal (KN)
pada hari hitungan pertama (5 HST) dengan rumus :
IV (%) = ∑ KN hitungan I x 100%
∑ benih yang ditanam
3. Kecepatan Tumbuh (%/etmal)
Pengamatan terhadap persentase kecambah normal per etmal dilakukan setiap
hari hingga pengamatan terakhir (final count) (Sadjad 1993). Rumus yang
digunakan adalah:
tn
KCT = Σ N/t 0
Keterangan : t : waktu pengamatan
N : % KN setiap waktu pengamatan
10
Pengujian Kesehatan Benih
Pengujian kesehatan benih adalah pemeriksaan pada benih dengan
menggunakan metode khusus untuk mengetahui adanya mikroorganisme atau
penyakit pada benih (ISTA 2006). Pengujian kesehatan benih dilakukan terhadap
cendawan dan bakteri patogenterbawa benih.
Identifikasi dan Penghitungan Kerapatan Cendawan Patogen Terbawa Benih
Pengujian cendawan dilakukan dengan metode Blotter test, yaitu
menanam 200 benih padi (empat ulangan @ 50 benih) yang sudah didisinfeksi
dengan natrium hipoklorit 1 % dan dicuci dengan air steril serta dikeringkan
dengan tisu dan dikeringanginkan. Identifikasi dilakukan setelah 7 hari inkubasi
pada inkubator suhu 20-25 ºC dengan penyinaran near ultra violet (NUV) 12 jam
terang dan 12 jam gelap. Pengamatan dilakukan dengan mikroskop stereo dan
mikroskop compound terhadap semua jenis cendawan terbawa benih dengan
rumus :
% infeksi = Jumlah benih yang terinfesi x 100 % Jumlah benih yang di tanam
Pada pengujian cendawan patogen terbawa benih dihitung pula jumlah
kerapatan cendawan dengan haemocytometer dan mikroskop compound. Rumus
perhitungan (Mathur 2003) :
= jumlah spora per ml
Cendawan patogen terbawa benih yang berhasil diidentifikasi dimurnikan
dengan potato dextrose agar (PDA) untuk digunakan pada pengujian selanjutnya.
Ekstraksi, Isolasi dan Identifikasi Bakteri Patogen Terbawa Benih
Dalam pengujian bakteri patogen terbawa benih langkah yang dilakukan
untuk menentukan ada tidaknya bakteri patogen dalam suatu kelompok benih adalah
dengan cara ekstraksi bakteri, isolasi dan pemurnian serta identifikasi isolat bakteri. Jumlah spora x volume dari suspensi spora (ml)
(luas area perhitungan (mm2 ) x kedalaman (mm) ml
11
Ekstraksi dan isolasi bakteri langsung dari benih dengan metode penghancuran
(liquid assay). Benih sebanyak 400 butir direndam dalam natrium hipoklorit
selama 1 menit, selanjutnya dibilas dengan air steril tiga kali, setelah itu benih
dihancurkan dengan mortar dan pestle serta ditambahkan air steril sebanyak (1.9 x
berat 100 butir) + 50 ml. Hasil ekstraksi diinkubasikan selama 2 jam. Suspensi
bakteri diambil dengan pipet steril sebanyak 1 ml dan dimasukkan dalam tabung
reaksi yang berisi air steril 9 ml, sehingga diperoleh perbandingan suspensi baru
1:10 (10-1), kemudian dikocok hingga homogen. Cara pengenceran ini diulang
dua kali sehingga mendapatkan tingkat pengenceran 10-3. Dari pengenceran yang
dibuat, diambil 100 µl suspensi dan ditabur pada nutrient agar (NA). Cawan petri
diinkubasi dalam keadaan terbalik pada suhu 28-30 ºC selama 2-3 hari
(BBPPMBTPH 2007).
Koloni yang diduga sebagai patogen dimurnikan pada media NA/Kings’B,
kemudian diinkubasi pada suhu 28-30 ºC selama 2-3 hari. Isolat yang didapat
selanjutnya diidentifikasi berdasarkan karakter fisiologi dan biokimi pada patogen
Pseudomonas dan patogen Xanthomonas ( Tabel 3 dan 4).
Karakter Morfologi Koloni
Koloni bakteri dapat dilihat dari morfologinya yaitu bentuk koloni
cembung, bulat, tepinya licin atau bergerigi (BBPPMBTPH 2007).
Uji Reaksi Gram
Uji reaksi gram dilakukan untuk membedakan antara bakteri yang bersifat
gram positif dengan gram negatif dengan cara mencampurkan satu lup bakteri
dengan dua tetes larutan KOH 3%, selanjutnya dilakukan pengamatan, apabila
terbentuk lendir setelah diaduk dengan jarum ose artinya bakteri tersebut bersifat
gram negatif (Mortensen 1989).
Uji Hidrolisis Pati
Koloni bakteri digoreskan pada medium pati, diinkubasi selama 4 hari
pada temperatur 28°C. Koloni yang sudah tumbuh pada goresan disiram dengan
larutan Lugol’s Iodin dan dilakukan pengamatan. Apabila media pati berwarna
12
Tabel 3. Karakter morfologi dan biokimia yang digunakan untuk membedakan patogen Pseudomonas
Karakter P.s P.f P.a P.g
Warna putih putih-coklat
terang putih seperti kapur putih keabu-abuan Morfologi bundar, licin, timbul bundar, licin, timbul, bening, mengkilap bulat, licin, timbul, lengket, mengkilap bulat, licin, timbul
Hidrolisa pati - + +/- +/-
Fluoresen + + - -
Oksidase - + +/- -
Arginin - + - -
Sumber : Mortensen 1989; Mew et al. 1994
Keterangan : P.s : Pseudomonas syringae, P.f : Pseudomonas fuscovaginae,
P.a : Pseudomonas avenae, P.g : Pseudomonas glumae
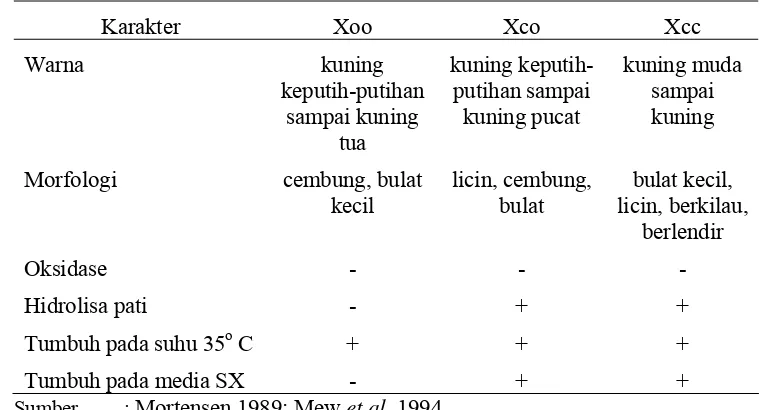
Tabel 4. Karakter morfologi dan biokimia yang digunakan untuk membedakan patogen Xanthomonas
Karakter Xoo Xco Xcc
Warna kuning keputih-putihan sampai kuning tua kuning keputih-putihan sampai kuning pucat kuning muda sampai kuning
Morfologi cembung, bulat
kecil licin, cembung, bulat bulat kecil, licin, berkilau, berlendir
Oksidase - - -
Hidrolisa pati - + +
Tumbuh pada suhu 35o C + + +
Tumbuh pada media SX - + +
Sumber : Mortensen 1989; Mew et al. 1994
Keterangan : Xoo: Xanthomonas oryzae pv. oryzae Xco: Xanthomonas campestris pv.
oryzicola, Xcc: Xanthomonas campestris pv. campestris
Uji Fluorescence
Bakteri digoreskan pada media King’s B yang sudah dituangkan ke dalam
cawan petri. Cawan petri yng telah digoree bakteri iinkubasi pada ruang dengan
suhu 25-28 ºC. Setelah 48 jam dilakukan pengamatan ada/tidaknya warna
[image:31.612.126.506.364.569.2]13
Uji Oksidase Kovac’s
Bakteri ditumbuhkan pada media nutrient glucose agar (NGA) dengan
glukosa tidak boleh lebih dari 0,25% selama 24 jam. Larutan oksidase kovac’s
(larutan Tetramethyl-paraphenylene diamine dihydrochloride 1%) dibuat
secukupnya dan diletakkan pada tempat yang terhindar dari cahaya. Kertas filter
Whatman No.1 diletakkan di dalam cawan petri dan ditetesi larutan tersebut
sebanyak 3 – 4 tetes. Isolat bakteri yang tumbuh pada media King’s B sebanyak
satu lop diambil dengan ose platina atau tusuk gigi steril, kemudian digoreskan
pada tetesan larutan tersebut. Jika dalam waktu ≤ 10 detik terjadi perubahan warna menjadi ungu, maka bakteri tersebut bereaksi positif (Mortensen 1989).
Uji Arginin
Bakteri yang berumur 24-48 jam diinokulasikan dalam tabung reaksi yang
berisi media Thornley’s sebanyak 3 ml dengan cara ditusukkan. Tabung reaksi
yang sudah diinokulasi kemudian dilapisi dengan 1 ml mineral oil agar
kondisinya anaerob. Tabung reaksi diinkubasikan selama 3 hari pada ruang
dengan suhu 25-28 ºC. Pengamatan dilakukan terhadap warna media. Jika media
berubah menjadi merah maka bakteri tersebut bereaksi positif. Sebaliknya jika
tidak ada perubahan warna berarti bakteri tersebut bereaksi negatif (Mortensen
1989).
Penghitungan Jumlah Bakteri Terbawa Benih
Penghitungan jumlah koloni yang tumbuh menggunakan metode plate
counting (BBPPMBTPH 2007). Dasar perhitungan dalam metode ini adalah
jumlah bakteri yang tumbuh pada media dengan asumsi bahwa satu koloni
berasal dari satu sel bakteri. Dengan demikian jumlah koloni yang muncul pada
cawan petri merupakan suatu indeks bagi jumlah sel bakteri yang hidup dalam
sampel. Oleh karena yang terhitung adalah jumlah koloni yang masing-masing
berasal dari satu sel, sehingga satuannya adalah colony forming unit per ml
(cfu/ml).
Benih sebanyak 400 butir direndam dengan natrium hipoklorit selama 1
menit, selanjutnya dibilas dengan air steril tiga kali, setelah itu benih
14
Hasil ekstraksi diinkubasikan selama 2 jam. Suspensi bakteri diambil dengan
pipet steril sebanyak 1 ml dan dimasukkan dalam tabung reaksi yang berisi air
steril 9 ml, sehingga diperoleh perbandingan suspensi baru 1:10 (10-1), kemudian
dikocok hingga homogen. Cara pengenceran ini diulang dua kali sehingga
mendapatkan tingkat pengenceran 10-3. Dari pengenceran yang dibuat, diambil
100µl suspensi dan ditabur pada nutrient agar (NA). Cawan petri diinkubasi
dalam keadaan terbalik pada suhu 28-30 ºC selama 2-3 hari. Jumlah koloni yang
tumbuh pada tiap-tiap pengenceran dihitung berdasarkan karakter morfologi
(BBPPMBTPH 2007).
Rumus perhitungan koloni : Y = X . n . 10
Keterangan Y = jumlah bakteri per ml
X = jumlah rata-rata koloni per petri pada suatu tingkat
pengenceran
n = tingkat pengenceran
10 = menunjukan per ml karena yang ditabur per petri 0.1 ml
Rancangan Percobaan
Banjai dan Barabas (2002) menyebutkan bahwa data daya berkecambah
dan kemurnian mengikuti distribusi binomial. Distribusi binomial ini juga
berlaku untuk data pengujian kecepatan tumbuh, indeks vigor, persen infeksi
cendawan dan jumlah koloni bakteri.
Untuk pengujian daya berkecambah, kecepatan tumbuh, indeks vigor dan
kesehatan benih digunakan Rancangan Acak Lengkap dengan faktor tunggal yaitu
sampel benih yang terdiri atas dua tanggal panen yang berbeda. Analisis statistik
yang digunakan adalah sidik ragam dengan model sebagai berikut:
Yi = μ + αi + εi
Yi : nilai pengamatan pada tanggal panen α ke-i
μ : rataan umum
αi : pengaruh tanggal panen α taraf ke-i
€i : galat percobaan tanggal panen α taraf ke-i
Apabila terdapat pengaruh nyata terhadap peubah yang diamati, dilakukan uji
15
HASIL DAN PEMBAHASAN
Mutu Fisiologis Benih Padi Varietas IR 64 yang Berbeda Vigornya
Mutu fisiologis identik dengan daya berkecambah dimana daya
berkecambah menunjukkan kemampuan benih untuk tumbuh normal pada kondisi
optimum (AOSA 1983). Tujuan pengujian daya berkecambah adalah untuk
menentukan potensi perkecambahan maksimum dari suatu lot benih yang dapat
digunakan untuk membandingkan mutu dari lot yang berbeda dan untuk menduga
mutu benih sebagai bahan tanaman (the field planting value) (ISTA 2006).
Hasil pengujian awal mutu fisiologis (daya berkecambah, kecepatan tumbuh dan
indeks vigor) dua sampel benih padi IR 64 menunjukkan nilai daya berkecambah
yang berbeda nyata (Tabel 5). Benih padi Lot 1 yang dipanen pada 6 Juni 2007
(6 bulan masa simpan) mempunyai daya berkecambah 88%, sedangkan padi
Lot 2yang dipanen pada tanggal 10 September 2007 (3 bulan masa simpan) 97%.
Perbedaan nilai daya berkecambah ini disebabkan banyak faktor. Faktor eksternal
dan internal sangat berpengaruh pada proses perkecambahan dan pada hasil akhir
(ISTA 2003).
Tabel 5. Hasil pengujian viabilitas dan vigor benih padi IR 64
Jenis Pengujian Lot I
(6 Juni 2007)
Lot II
(10 September 2007)
Daya berkecambah (%) 88 b 97 a
Kecepatan tumbuh (%/etmal) 13.80 b 17.14 a
Indeks vigor (%) 0 b 70 a
Keterangan: Huruf yang berbeda pada baris yang sama menunjukkan berbeda nyata
pada DMRT 5%. Koefisen keragaman (kk) DB: 0.8827, kk. KCT: 0.7613,
kk. IV: 114.1712
Kecepatan tumbuh (KCT) mengindikasikan vigor kekuatan tumbuh karena
benih yang cepat tumbuh lebih mampu menghadapi kondisi lapang yang
sub optimum. Kecepatan tumbuhdiukur dengan cara menjumlahkan pertambahan
kecambah normal setiap hari atau etmal pada kurun waktu perkecambahan dalam
kondisi optimum (Sadjad 1993). Nilai KCT dengan satuan %/etmal menunjukkan
jumlah benih yang tumbuh menjadi kecambah normal setiap 24 jam.
16
perkecambahan hingga 100% membutuhkan waktu 100/13.80 atau 7.2 hari
sedangkan benih padi Lot II dengan KCT = 17.14%/etmal membutuhkan waktu
5.7 hari. Semakin tinggi nilai KCT semakin cepat benih tersebut tumbuh menjadi
kecambah normal.
Nilai indeks vigor yang tinggi menunjukkan benih berkecambah lebih
cepat, sehingga digolongkan dalam vigor kuat. Benih yang cepat tumbuh
menunjukkan benih tersebut mampu mengatasi segala macam kondisi
sub optimum (Sadjad 1984). Benih padi Lot I mempunyai nilai indeks
vigor (IV) = 0%, berarti pada pengamatan pertama belum ada benih yang
berkecambah normal, sedangkan benih padi Lot II mempunyai nilai IV = 70%.
Nilai IV yang tinggi menunjukkan benih berkecambah lebih cepat sehingga
digolongkan dalam benih yang vigor (Sadjad 1984).
Benih padi Lot I ( KCT=13.80%/etmal dan IV = 0%) dapat dikategorikan
sebagai benih vigor sedang, sedangkan benih padi Lot II (KCT= 17.14%/etmal
dan IV = 70%) dapat dikategorikan sebagai benih vigor tinggi.
Kesehatan Benih Padi Varietas IR 64 yang Berbeda Vigor
Hasil dentifikasi cendawan berdasarkan bentuk morfologi (Gambar 2),
pada benih padi Lot I ditemukan tiga jenis cendawan terbawa benih yaitu,
Alternaria padwickii, Drechslera oryzae, dan Fusarium moniliforme, sedangkan
pada benih padi Lot II hanya ditemukan dua jenis cendawan yaitu A. padwickii
dan D. oryzae (Tabel 6).
a b c
Gambar 2 Spora cendawan yang ditemukan pada benih padi dengan perbesaran 100x,
Alternaria padwickii (a), Drechslera oryzae (b), dan Fusarium
moniliforme (c).
Persentase infeksi cendawan patogen terbawa benih setiap lot
17
Alternaria padwickii merupakan cendawan yang ditemukan dengan tingkat infeksi
paling tinggi pada benih vigor sedang dan vigor tinggi (22% dan 10%)
dibandingkan Drechslera oryzae, dan Fusarium moniliforme. Alternaria
padwickii merupakan salah satu cendawan terbawa benih yang dilaporkan paling
banyak menginfeksi benih padi, 75 % dari 400 sampel benih padi terinfeksi A.
padwickii (Neergard 1977), persentase infeksi A. padwickii pada padi berkisar
1.33-44.0% (Pham et al. 2001) atau 2.85-24.10% (Islam et al. 2000).
Kerapatan cendawan A. padwickii, D. oryzae, dan F. moniliforme adalah
berkisar 106 pada benih Lot I maupun benih Lot II (Tabel 7). Jumlah kerapatan
cendawan per mililiter dapat digunakan untuk memprediksi perkecambahan
benih.
Tabel 6. Persentase infeksi cendawan patogen terbawa benih padi IR 64
Jenis cendawan Lot I
(6 Juni 2007)
Lot II
(10 September 2007)
A. padwickii 22 a 10 b
D. oryzae 8 a 3 b
F. moniliforme 5 a 0 b
Keterangan : Keterangan: Huruf yang berbeda pada baris yang sama menunjukkan
berbeda nyata pada DMRT 5%. Koefisen keragaman (kk) A. padwickii:
8.8388, kk. D. oryzae: 15.1448, kk. F. moniliforme: 23.0940
Tabel 7. Kerapatan cendawan patogen terbawa benih padi IR 64
Jenis cendawan Lot I
(6 Juni 2007)
Lot II
(10 September 2007)
A. padwickii 1 x 106 1 x 106
D. oryzae 1 x 106 1 x 106
F. moniliforme 3 x 106 0
Salah satu penyebab keabnormalan kecambah adalah
adanya cendawan terbawa benih (ISTA 2003). Nghiep dan
Gaur (2004) menyatakan bahwa kecambah abnormal pada beberapa varietas padi
di India disebabkan oleh D. oryzae, A. padwicki, dan Culvularia.
Merca et al. (1999) melaporkan bahwa F. moniliforme, A. padwickii,
18
Infeksi yang sangat tinggi dari A. padwickii sebesar 80% pada benih padi
dilaporkan terjadi di Filipina. Infeksi benih menyebabkan penurunan daya
berkecambah, busuk benih, busuk akar dan koleoptil, dan kematian. Cendawan ini
biasanya melakukan penetrasi ke dalam endosperma, dan dapat menurunkan mutu
benih (Ou 1985). Konsentrasi inokulum A. padwickii 2 x 104 per mililiter dapat
menimbulkan gejala penyakit di pertanaman (ISPaVe 1996).
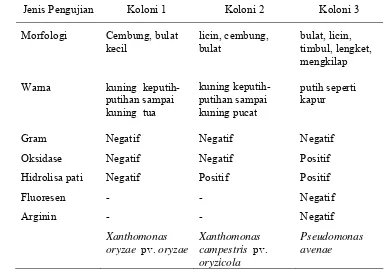
Berdasarkan pengujian morfologi dan biokimia (Tabel 8 dan Gambar 3)
pada benih padi Lot I dan Lot II ditemukan tiga bakteri patogen terbawa benih,
yaitu Xanthomonas oryzae pv. oryzae, Xanthomonas campestris pv. oryzicola,
dan Pseudomonas avenae. Jumlah koloni ketiga bakteri pada benih padi Lot I dan
[image:37.612.117.501.322.594.2]Lot II berkisar antara 103- 104 (Tabel 9).
Tabel 8. Hasil identifikasi koloni bakteri secara morfologi dan biokimia
Jenis Pengujian Koloni 1 Koloni 2 Koloni 3
Morfologi Cembung, bulat
kecil
licin, cembung, bulat
bulat, licin, timbul, lengket, mengkilap
Warna kuning
keputih-putihan sampai kuning tua
kuning keputih-putihan sampai kuning pucat
putih seperti kapur
Gram Negatif Negatif Negatif
Oksidase Negatif Negatif Positif
Hidrolisa pati Negatif Positif Positif
Fluoresen - - Negatif
Arginin - - Negatif
Xanthomonas oryzae pv. oryzae
Xanthomonas campestris pv. oryzicola
Pseudomonas avenae
Bakteri X. oryzae pv. oryzae paling banyak ditemukan pada benih yang
diuji. Benih merupakan sumber utama dan pertama penularan X. oryzae pv.
oryzae di lapangan. Koloni X. oryzae pv. oryzae dijumpai pada endosperma
dan gluma. Bakteri dapat bertahan hidup dalam benih selama semusim hingga
19
[image:38.612.189.451.77.190.2]
a b c
Gambar 3. Koloni bakteri patogen terbawa benih yang ditemukan pada benih padi:
Xanthomonas oryzae pv oryzae (a), Xanthomonas campestris
pv. oryzicola (b) dan Pseudomonas avenae (c).
Tabel 9. Hasil penghitungan jumlah koloni bakteri patogen terbawa benih padi IR 64 (cfu/ml)
Jenis bakteri Lot I
(6 Juni 2007)
Lot II
(10 September 2007)
X. oryzae pv. oryzae 2 x 104 a 4 x103 b
X. campestris pv. oryzicola 1.2 x 104 a 3.6 x 103 b
P. avenae 8.4 x103 a 1 x 103 b
Keterangan : Huruf yang berbeda pada baris yang sama menunjukkan berbeda nyata
pada DMRT 5%. Koefisen keragaman X. oryzae pv oryzae: 1.1015
(transformasi logaritma), kk. Xanthomonas campestris pv. oryzicola:
0.3797 (transformasi logaritma) dan kk. Pseudomonas Avenae: 1.5689
(transformasi akar kuadrat)
KESIMPULAN
Berdasarkan hasil pengujian mutu fisiologis dapat disimpulkan bahwa
pada benih padi varietas IR 64 yang dipanen tanggal 6 Juni 2007 (Lot I)
mempunyai nilai daya DB = 88 %, KCT = 1 3.80 %/etmal, IV = 70 %, dan benih
padi varietas IR 64 yang dipanen pada tanggal 10 September 2007 (Lot II)
mempunyai nilai DB = 97 %, KCT =17.14 %/etmal, IV =0 %. Benih padi Lot I
dapat dikategorikan sebagai benih vigor sedang, dan benih padi Lot II sebagai
benih vigor tinggi. Benih padi dengan dua tingkat vigor ini kemudian digunakan
pada percobaan-percobaan selanjutnya.
Pada benih padi Lot I ditemukan tiga jenis cendawan terbawa benih yaitu,
A. padwickii (22%), D. oryzae (8%), dan F. moniliforme (5%), sedangkan pada
benih padi Lot II hanya ditemukan dua jenis cendawan yaitu A. padwickii (10%)
[image:38.612.139.506.275.376.2]20
Hasil identifikasi secara morfologi dan biokimia pada benih padi Lot I dan
Lot II ditemukan tiga jenis bakteri patogen terbawa benih, yaitu X. oryzae pv.
oryzae (2 x 104 dan 4 x103 cfu/ml), X. campestris pv. oryzicola (1.2 x 104 dan 3.6
EVALUASI DAYA HAMBAT AGENS HAYATI TERHADAP
PATOGEN UTAMA TERBAWA BENIH PADI
PENDAHULUAN
Pengendalian hayati menggunakan agens hayati merupakan pengendalian
alternatif yang ramah lingkungan dibandingkan penggunakaan bahan kimia dan
pestisida dalam menekan penyakit tanaman (Warrior et al. 2002).
Terdapat beberapa definisi mengenai pengendalian hayati, yaitu:
1. Pengurangan jumlah inokulum dalam keadaan aktif maupun dorman atau
pengurangan aktivitas patogen sebagai parasit oleh satu atau lebih
mikroorganisme yang berlaku secara alami atau melalui manipulasi
lingkungan, inang atau antagonis atau dengan introduksi secara massal
organisme antagonis (Cook dan Baker 1983).
2. Pengurangan jumlah inokulum atau aktivitas suatu patogen yang
menghasilkan penyakit dengan satu atau lebih organisme lain selain manusia
(Gnanamanickam 2002).
3. Keseluruhan atau sebagian populasi patogen yang dapat ditekan oleh
organisme lain yang selalu ada di alam (Agrios 2005).
Pengendalian dengan agens hayati memiliki beberapa keunggulan, antara
lain efektif untuk mengendalikan penyakit tanaman, tidak berdampak negatif
terhadap lingkungan, efektif selama masa hidup tanaman dan dapat menghasilkan
senyawa yang bermanfaat ganda bagi tanaman (Silva et al. 2004).
Agens hayati adalah 1) mikroba seperti bakteri, cendawan,pengendali
hama dan penyakit, 2) eksotik agens hayati yang dapat berkembang biak seperti
parasitoid, predator, parasit, arthropoda pemakan tumbuhan dan patogen
(Keputusan Ketua Komisi Agens Hayati 2006), 3) tiap organisme yang meliputi
spesies, subspesies, varietas, semua jenis serangga, nematoda, protozoa, cendawan
(fungi), bakteri, virus, mikoplasma dan organisme lainnya dalam semua tahap
perkembangannya yang dapat dipergunakan untuk keperluan pengendalian hama
dan penyakit atau organisme pengganggu, proses produksi, pengolahan hasil
22
Secara umum kelompok bakteri antagonis dari kelompok Pseudomonas
dan Bacillus merupakan bakteri yang paling banyak digunakan sebagai agens
hayati. Bacillus adalah bakteri gram positif yang memproduksi endospore, toleran
terhadap panas dan pengeringan. Pseudomonas bersifat gram negatif dan
membutuhkan sedikit nutrisi. Kedua kelompok bakteri ini mempunyai
kemampuan kolonisasi yang sangat bagus dan mempunyai kemampuan hidup
yang tinggi pada rhizophere padi (Weller 1998). Agens hayati bakteri ini dapat
menghasilkan antibiotik, kompetisi, induksi resistensi, lytic enzimes, dan
mycrobial cyanides atau induksi sistemik pada inang (Handelsman 1996) .
Percobaan ini merupakan langkah awal untuk mengetahui efektivitas
Bacillus subtilis sebagai agens hayati terhadap patogen terbawa benih padi
varietas IR 64 yang didapat dari hasil uji kesehatan benih.
BAHAN DAN METODE
Tempat dan Waktu Penelitian
Penelitian dilaksanakan di Laboratorium Pengujian Benih Balai Besar
Pengembangan Pengujian Mutu Benih Tanaman Pangan dan Hortikultura
Cimanggis Depok. Penelitian dilaksanakan pada bulan Januari 2008.
Metodologi
Isolat Cendawan dan Bakteri Patogen Terbawa Benih
Isolat murni patogen terbawa benih padi yang diperoleh dari percobaan
pertama ada enam isolat. Tiga isolat cendawan (Gambar 4) yaitu Alternaria
padwickii, Dreschlera oryzae, Fusarium moniliforme yang dimurnikan pada
media potato dextrosa agar (PDA).
[image:41.612.131.507.527.686.2]
a b c
23
Tiga isolat bakteri (Gambar 5) yaitu Xanthomonas oryzae pv. oryzae,
Xanthomonas campestris pv. oryzicola, dan Pseudomonas avenae dimurnikan
pada media nutrient agar (NA).
[image:42.612.132.508.159.293.2]
a b c
Gambar 5. Isolat murni bakteri patogen terbawa benih Xanthomonas oryzae pv. oryzae (a), Xanthomonas campestris pv. oryzicola (b) dan Pseudomonas avenae (c).
Isolat Agens hayati
Untuk percobaan ini digunakan dua isolat agens hayati Bacillus subtilis
5/B dan 11/C yang merupakan koleksi dari BB-Padi Sukamandi tahun 2007
(Gambar 6).
a b
Gambar 6. Isolat murni bakteri agens hayati Bacillus subtilis 5/B (a) dan 11/C (b).
Daya Hambat Bacillus subtillis terhadap Cendawan Patogen Terbawa Benih
Secara In Vitro
Cendawan hasil identifikasi pengujian kesehatan benih direjuvinasi
sampai umur 7 hari sebelum digunakan untuk perlakuan uji daya hambat.
[image:42.612.156.477.409.538.2]24
diameter 0.5 cm, dipindahkan ke dalam media PDA baru dengan jarak 3 cm dari
tepi cawan petri dan diinkubasikan selama 48 jam. Isolat agens hayati B. subtilis
5/B dan 11/C diambil dari biakan murni pada media NA. Masing-masing isolat
digores memanjang satu lup penuh dengan jarak 3 cm dari tepi cawan berlawanan
arah letak cendawan yang telah ditumbuhkan sebelumnya. Untuk masing-masing
isolat agens hayati dilakukan pengujian dengan pengulangan tiga kali.
Pengamatan dilakukan setiap hari terhadap pertumbuhan cendawan dan
persentase daya hambat agens hayati (DH) dihitung dengan rumus:
DH = R1 - R2 x 100%
R2
Keterangan :
R1 = jari-jari pertumbuhan patogen ke arah tepi cawan petri
R2 = jari-jari pertumbuhan patogen ke arah agens hayati
Daya Hambat Bacillus subtilis terhadap BakteriPatogen Terbawa Benih
Secara In Vitro
Isolat murni bakteri hasil pengujian kesehatan benih dan agens hayati B.
subtilis (5/B dan 11/C) direjuvinasi pada media NA/King’s B. Setelah 48 jam,
pada ketiga isolat murni bakteri patogen terbawa benih dan isolat agens hayati B.
subtilis 5/B dan 11/C ditambahkan 100 μl akuades steril kemudian diratakan. Potongan kertas saring steril dengan diameter 1 cm dicelupkan pada suspensi
agens hayati dan diletakkan pada medium yang berisi inokulum bakteri patogen
terbawa benih. Kultur diinkubasikan dalam ruang bersuhu 26 – 28 ºC selama 7
hari. Daya hambat agens hayati ditunjukkan dengan adanya area transparan (halo)
disekitar potongan kertas.
Rancangan Percobaan
Analisa daya hambat B. subtilis terhadap cendawan patogen terbawa
benih menggunakan Rancangan Acak Lengkap faktor tunggal yaitu perbedaan
nilai tengah daya hambat. Analisis statistik yang digunakan adalah sidik ragam
25
Yi = μ + αi + εi
Yi : nilai pengamatan pada perbedaan nilai tengah daya hambat α ke-i
μ : rataan umum
αi : pengaruh perbedaan nilai tengah daya hambat α taraf ke-i
€i : galat percobaan perbedaan nilai tengah daya hambat α taraf ke-i
Apabila terdapat pengaruh nyata terhadap peubah yang diamati, dilakukan uji
lanjut dengan Duncan Multiple Range Test (DMRT) pada α 5%.
HASIL DAN PEMBAHASAN
Daya Hambat Bacillus subtilis terhadap Cendawan Patogen Terbawa Benih
Agrios (2005) mengemukakan bahwa mekanisme dan antagonisme
terhadap patogen yaitu (a) parasit atau lisis secara langsung sampai patogen mati,
(b) kompetisi makanan, (c) efek racun secara langsung pada patogen dengan zat
antibiotik yang dihasilkan oleh agens hayati, (d) efek racun secara tidak langsung
dari bahan volatil yang ada pada agens hayati.
Hasil in-vitro dual culture menunjukkan bahwa B. subtilis 5/B mampu
menghambat pertumbuhan cendawan A. padwickii (Tabel 10 dan Gambar 7) dan
D. oryzae (Tabel 11 dan Gambar 8), lebih baik dibandingkan B. subtilis 11/C.
Kemampuan penghambatan isolat B. subtilis 5/B berbeda nyata dengan
kemampuan penghambatan isolat B. subtilis 11/C. Cendawan patogen terbawa
benih padi tidak mampu tumbuh dimungkinkan karena terhambat oleh antibiotik
yang dihasilkan oleh bakteri B. subtilis. Potensi B. subtilis sebagai agens hayati
ditunjukkan dengan terbentuknya zona penghambatan yaitu merupakan zona
pembatas antara titik terluar koloni patogen dan difusi antibiotik pada media
PDA.
Muhammad dan Amusa (2003) melaporkan bahwa B. subtilis mampu
menghambat cendawan patogen pada jagung, penghambatan terhadap
pertumbuhan mycelia cendawan disebabkan oleh dua mekanisme yaitu produksi
metabolit biologis dan pertumbuhan yang cepat dan menyebar dari B. subtillis
Agens hayati B. subtilis menghasilkan senyawa antibiotik berupa peptida
26
Antibiotik yang dihasilkan agens hayati kelompok bakteri berperan sebagai kunci
pengendalian berbagai penyakit tanaman (Anderson et al. 2004).
Kedua agens hayati B. subtillis 5/B dan 11/C tidak mampu menghambat
pertumbuhan koloni cendawan Fusarium moniliforme. Rosales et al. (1993)
menyatakan bahwa agens hayati bakteri yang berasal dari benih, daun padi yaitu
bakteri yang termasuk dalam genera Bacillus, Pseudomonas, Serratia dan
Erwinia. Semua agens hayati bakteri ini dapat menghambat pertumbuhan mycelia
dari Rhizoctonia solani, hanya beberapa agens hayati dapat menghambat
[image:45.612.131.508.287.356.2]pertumbuhan cendawan Fusarium moniliforme.
Tabel 10. Pengaruh Bacillus subtilis terhadap penghambatan pertumbuhan koloni Alternaria padwickii
Perlakuan Rata-rata penghambatan (%)
Tanpa B. subtilis 0 c
B. subtilis 5/B 16.8 a
B. subtilis 11/C 14.1 b
Keterangan : Huruf yang berbeda pada kolom yang sama menunjukkan berbeda nyata pada DMRT 5%. Koefisien keragaman: 0.7929.
a b
[image:45.612.130.512.575.654.2]Gambar 7. Penghambatan Bacillus subtilis 5/B (a) dan 11/C (b) terhadap Alternaria padwickii.
Tabel 11. Pengaruh Bacillus subtilis terhadap penghambatan pertumbuhan koloni Drechslera oryzae
Perlakuan Rata-rata penghambatan (%)
Tanpa B. subtilis 0 c
B. subtilis 5/B 17.3 a
B. subtilis 11/C 13.8 b
27
a b
Gambar 8. Penghambatan Bacillus subtilis 5/B (a) dan 11/C (b) terhadap Dreschlera oryzae.
Daya Hambat Bacillus subtillis terhadap Bakteri Patogen Terbawa Benih
Pada pengujian daya hambat B. subtilis 5/B terhadap ketiga bakteri
patogen terbawa benih menunjukkan bahwa agens hayati B. subtilis 5/B mampu
menghambat bakteriX. oryzae pv. oryzae dan X. campestris pv. oryzicola, namun
tidak mampu menghambat P. avenae (Tabel 12 dan Gambar 9). Bacillus subtilis
11/C tidak mampu menghambat X. oryzae pv. oryzae, X. campestris pv.
[image:46.612.181.465.80.196.2]oryzicola, dan P. Avenae.
Tabel 12. Kemampuan penghambatan Bacillus subtilis terhadap ketiga bakteri patogen terbawa benih
Bacillus subtilis Jenis Bakteri
5/B 11/C
Xanthomonas oryzae pv. oryzae + -
Xanthomonas campestris pv. oryzicola + -
Pseudomonas avenae - -
Keterangan : +: menghambat, - : tidak menghambat
a b
28
Penghambatan B. subtilis 5/B terhadap X. oryzae pv. oryzae dan X.
campestris pv. oryzicola ditunjukkan adanya lingkaran bening (halo) di sekitar
agens hayati. Terbentuknya zona penghambatan dalam bentuk halo ini
kemungkinan juga disebabkan oleh antibiotik yang dihasilkan oleh B. subtilis.
Banyak strain B. subtilis memproduksi antibiotik untuk menghambat bakteri dan
cendawan patogen tanaman (USPTO 2008). Bacillus sp. merupakan mikroba yang
potensial dalam mengendalikan bakteri Rastolnia solanasearum penyebab
penyakit layu bakteri pada tanaman jahe (Bustaman 2006).
KESIMPULAN
Pada penelitian uji daya hambat agens hayati secara in-vitro, isolat B.
subtilis 5/B mampu menghambat pertumbuhan cendawan A. padwickii (16.8%)
dan D. oryzae (17.3%), bakteri X. oryzae pv. oryzae dan X. campestris pv.
oryzicola namun tidak mampu menghambat cendawan F. moniliforme dan bakteri
P. avenae yang terbawa benih padi.
Isolat B. subtilis 11/C hanya mampu menghambat pertumbuhan cendawan
A. padwickii (14.1%) dan D. oryzae (13.8%). Isolat B. subtilis 5/B lebih baik dari
isolat B. subtilis 11/C, sehingga isolat B. subtilis 5/B digunakan pada penelitian
EFEKTIVITAS PERLAKUAN BENIH DALAM
MENGENDALIKAN PATOGEN UTAMA TERBAWA BENIH
DAN MENINGKATKAN VIGOR BENIH
PENDAHULUAN
Perlakuan benih merupakan bagian yang tidak dapat dipisahkan dari
sistem produksi tanaman. Setelah panen dan prosesing, benih harus diberi
perlakuan (seed treatment) untuk berbagai kepentingan yang berbeda. Pertama,
menghilangkan sumber infeksi dari benih (disinfeksi) untuk melawan patogen
tular benih dan hama. Kedua, perlindungan terhadap benih melawan hama dan
patogen yang mungkin berada di tanah atau di udara ketika bibit muncul
dipermukaan tanah. Ketiga, perlakuan benih seperti priming, coating , pelleting,
dan sebagainya untuk meningkatkan perkecambahan atau melindungi benih dari
patogen dan hama (Desai et al. 1997).
Maude (1986) melaporkan bahwa definisi perlakuan benih bersifat umum
dan merujuk kepada benih sebagai subyek dari senyawa (kimia, nutrisi, hormon),
proses (imbibisi, pengeringan) atau berbagai bentuk energi (radiasi, panas, listrik)
Dalam konteks patologi ta