SIFAT ANTIBAKTERI HASIL HIDROLISIS
MINYAK KELAPA MURNI TERHADAP
Staphylococcus aureus DAN Escherichia coli
SKRIPSI
OLEH:
HENNY PUJIATI
NIM 101524051
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
SIFAT ANTIBAKTERI HASIL HIDROLISIS
MINYAK KELAPA MURNI TERHADAP
Staphylococcus aureus DAN Escherichia coli
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh
gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
HENNY PUJIATI
NIM 101524051
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
SIFAT ANTIBAKTERI HASIL HIDROLISIS
MINYAK KELAPA MURNI TERHADAP
Staphylococcus aureus DAN Escherichia coli
OLEH:
HENNY PUJIATI
NIM 101524051
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: Agustus 2012
Pembimbing I, Panitia Penguji,
Pembimbing II, NIP 195001260183631002
Prof. Dr. Jansen Silalahi, M.App.Sc., Apt. Dra. Masfria, M.S., Apt. NIP 195006071979031001 NIP 195707231986012001
Drs. Maralaut Batubara, M.Phill., Apt. NIP 195101311976031003
KATA PENGANTAR
Bismillahirrahmanirrahiim,
Puji syukur penulis ucapkan kepada Allah SWT atas segala limpahan
rahmat dan karuniaNya, sehingga penulis dapat menyelesaikan penelitian dan
penyusunan skripsi ini, serta Shalawat dan Salam kepada Nabi Allah: Rasulullah
Muhammad SAW sebagai suri tauladan dalam kehidupan.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar
Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul:
“Sifat Antibakteri Hasil Hidrolisis Minyak Kelapa Murni Terhadap
Staphylococcus aureus dan Escherichia coli”.
Penulis mempersembahkan rasa terima kasih yang tak terhingga dan
penghargaan yang sebesar-besarnya kepada Ibunda, Ayahanda, suamiku M.
Muliadi, S.T., putra kecilku tercinta M.F. Al Faatin Muliadi, serta abang, kakak,
adik dan seluruh keponakanku atas segala doa, kasih sayang, dorongan moril dan
materil kepada penulis selama ini.
Pada kesempatan ini dengan segala kerendahan hati penulis juga
mengucapkan terima kasih yang sebesar-besarnya kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., sebagai Dekan Fakultas
Farmasi, beserta seluruh staf yang telah memberikan fasilitas dan membantu
kelancaran pendidikan penulis selama perkuliahan hingga selesai.
2. Bapak Drs. Immanuel S. Meliala, M.Si., Apt., dan Prof. Dr. Jansen Silalahi,
M.App.Sc., Apt., selaku pembimbing yang telah meluangkan waktu dan
kesabaran yang begitu besar dalam membimbing penulis selama penelitian
3. Bapak Hari Ronaldo Tanjung, S.Si, M.Sc., Apt., selaku penasihat akademik
yang telah memberikan bimbingan kepada penulis selama masa perkuliahan.
4. Bapak dan Ibu beserta seluruh staf Laboratorium Fitokimia dan Mikrobiologi
yang telah memberikan petunjuk dan saran serta fasilitas laboratorium selama
penulis melakukan penelitian.
5. Sahabat-sahabatku Nina, Dewi, Wati, Rapita, Vera, Uci, Adhe, teman
seperjuangan penelitian Dede dan seluruh teman-teman Ekstensi angkatan
2010 terima kasih untuk perhatian, semangat, doa, dan kebersamaannya
selama ini serta seluruh pihak yang tidak mungkin penulis sebutkan satu
persatu yang telah banyak memberikan bantuan, motivasi dan inspirasi bagi
penulis selama masa perkuliahan sampai penyusunan skripsi ini.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih
jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis
menerima kritik dan saran demi kesempurnaan skripsi ini.
Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat
bagi kita semua.
Medan, Agustus 2012
Penulis,
SIFAT ANTIBAKTERI HASIL HIDROLISIS MINYAK KELAPA MURNI TERHADAP Staphylococcus aureus DAN Escherichia coli
ABSTRAK
Minyak kelapa murni banyak mengandung asam lemak berantai sedang terutama asam laurat. Di dalam tubuh, asam laurat yang merupakan komponen utama minyak kelapa murni akan diubah menjadi senyawa monogliserida yang disebut monolaurin. Hidrolisis menggunakan NaOH akan menghasilkan asam laurat, monolaurin, dan dilaurin. Asam laurat dan monolaurin aktif sebagai antibakteri. Tujuan dari penelitian ini adalah untuk melihat pengaruh hidrolisis dengan NaOH terhadap sifat antibakteri minyak kelapa murni dalam whipped cream.
Minyak kelapa murni yang digunakan dalam penelitian ini adalah minyak kelapa murni yang diproduksi oleh Noery Vico Lhokseumawe – NAD. Hidrolisis penyabunan dilakukan dengan penambahan 25%, 50%, 75%, dan 100% NaOH dihitung dari bilangan penyabunan total. Sampel yang digunakan adalah whipped cream yang dibuat sendiri yang ditambahkan dengan minyak kelapa murni yang telah dihidrolisis. Pengujian daya hambat bakteri dilakukan terhadap bakteri Staphylococcus aureus (gram positif) dan Escherichia coli (gram negatif) dengan metode angka lempeng total.
Hasil penelitian menunjukkan bahwa semakin tinggi tingkat hidrolisis minyak kelapa murni maka sifat antibakteri juga akan semakin meningkat. Pada pengujian terhadap bakteri Staphylococcus aureus, untuk blanko jumlah koloninya 51x105 cfu, dan untuk pengujian minyak kelapa murni dalam whipped cream diperoleh 31x105 cfu. Angka lempeng total pada whipped cream dengan penambahan hasil hidrolisis minyak kelapa murni pada bakteri Staphylococcus aureus dengan konsentrasi 25% dan 50% berturut-turut adalah 25x105 cfu dan 19x105 cfu sedangkan dengan konsentrasi 75% dan 100% koloni bakteri tidak tumbuh. Pada pengujian terhadap bakteri Escherichia coli, untuk blanko diperoleh jumlah koloni 58x105 cfu dan untuk pengujian minyak kelapa murni dalam whipped cream diperoleh 55x105 cfu sedangkan pada whipped cream dengan penambahan hasil hidrolisis minyak kelapa murni konsentrasi 25%, 50%, 75% dan 100% berturut-turut adalah 50x105 cfu, 39x105 cfu, 29x105 cfu dan 26x105 cfu. Hasil penelitian yang dilakukan
menunjukkan bahwa hasil hidrolisis minyak kelapa murni dalam whipped cream efektif dalam menghambat pertumbuhan bakteri Staphylococcus aureus (gram positif) tetapi kurang efektif terhadap bakteri Escherichia coli (gram negatif).
CHARECTERISTIC ANTIBACTERIAL OF HYDROLYSIS RESULT VIRGIN COCONUT OIL TO Staphylococcus aureus AND Escherichia coli
ABSTRACT
Virgin coconut oil contains the fatty acid chain is mainly lauric acid. In the body, lauric acid which is a major component of virgin coconut oil is converted into a compound called monoglyceride monolaurin. Hydrolysis using NaOH will produce lauric acid, monolaurin, and dilaurin. Lauric acid and monolaurin active as antibacterial. Purpose of this study was to see the effect of hydrolysis with NaOH to the antibacterial properties of virgin coconut oil in a whipped cream.
Virgin coconut oil used in this study were produced by Noery Vico Lhokseumawe - NAD. Hydrolysis carried out by the addition of saponification of 25%, 50%, 75%, and 100% NaOH saponification number was calculated from the total. The sample used is a self-made whipped cream is added with virgin coconut oil that has been hydrolyzed. Tests conducted on the inhibition of the bacteria Staphylococcus aureus bacteria (gram positive) and Escherichia coli (gram negative) to the total plate count method.
The results showed that the higher degree of hydrolysis of the virgin coconut oil antibacterial properties will also increase. On examination of the bacteria Staphylococcus aureus, for blank the number of colonies 51x105 cfu, and testing of virgin coconut oil in whipped cream is 31x105 cfu. Total plate count on whipe cream with the addition results of hydrolysis of virgin coconut oil for the bacteria Staphylococcus aureus with concentration of 25% and 50% respectively is 25x105 cfu and 19x105 cfu but the concentration of 75% and 100% of bacterial colonies did not grow. On examination of the bacteria Escherichia coli, the number of colonies for the blank is 58x105 cfu and examination of the virgin coconut oil in whipped cream is 55x105 cfu but on whipped cream with the addition results of hydrolysis of virgin coconut oil concentration of 25%, 50%, 75% and 100% respectively is 50x105 cfu, 39x105 cfu, 29x105 cfu and 26x105 cfu. The results have shown that the results of hydrolysis of virgin coconut oil in whipped cream is effective in inhibiting the growth of the bacteria Staphylococcus aureus (gram positive) but less effective against the bacteria Escherichia coli (gram negative).
DAFTAR ISI
Halaman
JUDUL ………... i
LEMBAR PENGESAHAN …... iii
KATA PENGANTAR ……… iv
ABSTRAK ………... vi
ABSTRACT ………... vii
DAFTAR ISI ……….………... viii
DAFTAR TABEL ……….…………... viii
DAFTAR GAMBAR ……….…………... ix
DAFTAR LAMPIRAN ……….………... x
BAB I PENDAHULUAN ……….………... 1
1.1 Latar Belakang …... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ………... 4
BAB II TINJAUAN PUSTAKA ..…………... 5
2.1 Minyak Kelapa Murni ... 5
2.2 Asam Lemak ...….………... ... 7
2.3 Trigliserida ….……… ……….. 9
2.4 Hidrolisis Lemak ……… 10
2.6 Penentuan Aktivitas Antibakteri ………. 13
2.7 Bilangan Asam …... .……….. ... 15
BAB III METODE PENELITIAN ……….………. 16
3.1 Alat-alat ……….. 16
3.2 Bahan ……….. 16
3.3 Penyiapan Bahan ……….... 17
3.3.1 Pembuatan Larutan Pereaksi ………. 17
3.3.1.1 Larutan HCl 0,5 N ……… 17
3.3.1.2 Larutan NaOH metanol 0,5 N ……….. 17
3.3.1.3 Larutan Merah Metil ………. 17
3.3.1.4 Larutan Fenolftalein ……….. 18
3.3.1.5 Larutan KOH 0,1 N ………... 18
3.3.1.6 Larutan Alkohol 95% Netral ……...………….. 18
3.3.2 Penyiapan Alat dan Bahan untuk Pengujian Sifat Antibakteri .…. ………. 18
3.3.2.1 Sterilisasi Alat ………... 18
3.3.2.2 Pembuatan Media Nutrient Agar ……….. 18
3.3.2.3 Pembuatan Media Plate Count Agar …………. 19
3.3.2.4 Pembuatan Larutan NaCl 0,9 % ... 19
3.3.2.5 Pembuatan Agar Miring ……… 19
3.4 Hidrolisis Minyak Kelapa Murni .………..……… 20
3.5 Penentuan Bilangan Asam Minyak Kelapa Murni dan Hasil Hidrolisis Minyak Kelapa Murni ……….. 21
3.6 Pembuatan Whipped Cream ……..………. 21
3.6.2 Pembuatan Campuran Whipped Cream dengan Hasil
Hidrolisis Minyak Kelapa Murni ………..………. 22
3.7 Pengujian Sifat Antibakteri Minyak Kelapa Murni dan Hasil Hidrolisis Minyak Kelapa Murni dalam Whipped Cream .... 22
3.7.1 Peremajaan Bakteri ……….. 22
3.7.2 Pembuatan Inokulum ……….……… 22
3.7.3 Pengenceran Inokulum ………..……. 23
3.7.4 Pengujian Pertumbuhan Bakteri dalam Whipped Cream (Blanko) ………..…... 23
3.7.5 Pengujian Sifat Antibakteri pada Campuran Whipped Cream dengan Minyak Kelapa Murni ……….… 23
3.7.6 Pengujian Sifat Antibakteri pada Campuran Whipped Cream dengan Hasil Hidrolisis Minyak Kelapa Murni ……….… 24
BAB IV HASIL DAN PEMBAHASAN ………. .. 25
4.1 Bilangan Asam Minyak Kelapa Murni dan Hasil Hidrolisis Minyak Kelapa Murni ………. 25
4.2 Sifat Antibakteri Minyak Kelapa Murni dan Hasil Hidrolisis Minyak Kelapa Murni dalam Whipped Cream …..…………. 26
BAB V KESIMPULAN DAN SARAN ... 31
5.1 Kesimpulan ... 31
5.2 Saran ... 31
DAFTAR PUSTAKA... 32
DAFTAR TABEL
Halaman
Tabel 2.1 Standar Mutu Minyak Kelapa Murni Berdasarkan
SNI 7381:2008 ……….... 6
Tabel 2.2 Kandungan Asam Lemak per 100 g Minyak Kelapa …………. 9
Tabel 4.1 Bobot Minyak Kelapa Murni dan Bilangan Asam Sebelum
dan Setelah Hidrolisis ………..….…… 25
Tabel 4.2 Sifat Antibakteri Minyak Kelapa Murni dan Hasil Hidrolisis Minyak Kelapa Murni terhadap Bakteri Staphylococcus
DAFTAR GAMBAR
Halaman
Gambar 4.1 Angka Lempeng Total pada Bakteri Uji Staphylococcus
aureus dan Escherichia coli ………..………….. 27
Gambar 4.2 Grafik Sifat Antibakteri Minyak Kelapa Murni dan HasilHidrolisis Minyak Kelapa Murni dalam Whipped
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Minyak Kelapa Murni yang Digunakan dalam Penelitian .. 34
Lampiran 2 Perhitungan Bilangan Penyabunan Total Minyak Kelapa
Murni ………... 35
Lampiran 3 Perhitungan Jumlah NaOH-metanol yang Digunakan
dalam Hidrolisis Metode Penyabunan ………..…..…. 38
Lampiran 4 Perhitungan Bilangan Asam ………..….…. 47
Lampiran 5 Gambar Angka Lempeng Total Bakteri Uji ………. 49
Lampiran 6 Sifat Antibakteri Minyak Kelapa Murni dan Hasil Hidrolisis Minyak Kelapa Murni dalam Whipped
Cream ………..…………. 51
Lampiran 7 Grafik Sifat Antibakteri Minyak Kelapa Murni dan Hasil Hidrolisis Minyak Kelapa Murni dalam Whipped
SIFAT ANTIBAKTERI HASIL HIDROLISIS MINYAK KELAPA MURNI TERHADAP Staphylococcus aureus DAN Escherichia coli
ABSTRAK
Minyak kelapa murni banyak mengandung asam lemak berantai sedang terutama asam laurat. Di dalam tubuh, asam laurat yang merupakan komponen utama minyak kelapa murni akan diubah menjadi senyawa monogliserida yang disebut monolaurin. Hidrolisis menggunakan NaOH akan menghasilkan asam laurat, monolaurin, dan dilaurin. Asam laurat dan monolaurin aktif sebagai antibakteri. Tujuan dari penelitian ini adalah untuk melihat pengaruh hidrolisis dengan NaOH terhadap sifat antibakteri minyak kelapa murni dalam whipped cream.
Minyak kelapa murni yang digunakan dalam penelitian ini adalah minyak kelapa murni yang diproduksi oleh Noery Vico Lhokseumawe – NAD. Hidrolisis penyabunan dilakukan dengan penambahan 25%, 50%, 75%, dan 100% NaOH dihitung dari bilangan penyabunan total. Sampel yang digunakan adalah whipped cream yang dibuat sendiri yang ditambahkan dengan minyak kelapa murni yang telah dihidrolisis. Pengujian daya hambat bakteri dilakukan terhadap bakteri Staphylococcus aureus (gram positif) dan Escherichia coli (gram negatif) dengan metode angka lempeng total.
Hasil penelitian menunjukkan bahwa semakin tinggi tingkat hidrolisis minyak kelapa murni maka sifat antibakteri juga akan semakin meningkat. Pada pengujian terhadap bakteri Staphylococcus aureus, untuk blanko jumlah koloninya 51x105 cfu, dan untuk pengujian minyak kelapa murni dalam whipped cream diperoleh 31x105 cfu. Angka lempeng total pada whipped cream dengan penambahan hasil hidrolisis minyak kelapa murni pada bakteri Staphylococcus aureus dengan konsentrasi 25% dan 50% berturut-turut adalah 25x105 cfu dan 19x105 cfu sedangkan dengan konsentrasi 75% dan 100% koloni bakteri tidak tumbuh. Pada pengujian terhadap bakteri Escherichia coli, untuk blanko diperoleh jumlah koloni 58x105 cfu dan untuk pengujian minyak kelapa murni dalam whipped cream diperoleh 55x105 cfu sedangkan pada whipped cream dengan penambahan hasil hidrolisis minyak kelapa murni konsentrasi 25%, 50%, 75% dan 100% berturut-turut adalah 50x105 cfu, 39x105 cfu, 29x105 cfu dan 26x105 cfu. Hasil penelitian yang dilakukan
menunjukkan bahwa hasil hidrolisis minyak kelapa murni dalam whipped cream efektif dalam menghambat pertumbuhan bakteri Staphylococcus aureus (gram positif) tetapi kurang efektif terhadap bakteri Escherichia coli (gram negatif).
CHARECTERISTIC ANTIBACTERIAL OF HYDROLYSIS RESULT VIRGIN COCONUT OIL TO Staphylococcus aureus AND Escherichia coli
ABSTRACT
Virgin coconut oil contains the fatty acid chain is mainly lauric acid. In the body, lauric acid which is a major component of virgin coconut oil is converted into a compound called monoglyceride monolaurin. Hydrolysis using NaOH will produce lauric acid, monolaurin, and dilaurin. Lauric acid and monolaurin active as antibacterial. Purpose of this study was to see the effect of hydrolysis with NaOH to the antibacterial properties of virgin coconut oil in a whipped cream.
Virgin coconut oil used in this study were produced by Noery Vico Lhokseumawe - NAD. Hydrolysis carried out by the addition of saponification of 25%, 50%, 75%, and 100% NaOH saponification number was calculated from the total. The sample used is a self-made whipped cream is added with virgin coconut oil that has been hydrolyzed. Tests conducted on the inhibition of the bacteria Staphylococcus aureus bacteria (gram positive) and Escherichia coli (gram negative) to the total plate count method.
The results showed that the higher degree of hydrolysis of the virgin coconut oil antibacterial properties will also increase. On examination of the bacteria Staphylococcus aureus, for blank the number of colonies 51x105 cfu, and testing of virgin coconut oil in whipped cream is 31x105 cfu. Total plate count on whipe cream with the addition results of hydrolysis of virgin coconut oil for the bacteria Staphylococcus aureus with concentration of 25% and 50% respectively is 25x105 cfu and 19x105 cfu but the concentration of 75% and 100% of bacterial colonies did not grow. On examination of the bacteria Escherichia coli, the number of colonies for the blank is 58x105 cfu and examination of the virgin coconut oil in whipped cream is 55x105 cfu but on whipped cream with the addition results of hydrolysis of virgin coconut oil concentration of 25%, 50%, 75% and 100% respectively is 50x105 cfu, 39x105 cfu, 29x105 cfu and 26x105 cfu. The results have shown that the results of hydrolysis of virgin coconut oil in whipped cream is effective in inhibiting the growth of the bacteria Staphylococcus aureus (gram positive) but less effective against the bacteria Escherichia coli (gram negative).
BAB I
PENDAHULUAN
1.1 Latar Belakang
Minyak kelapa murni (VCO) merupakan salah satu hasil olahan dari buah
kelapa (Cocos nucifera L). Tanaman kelapa banyak tumbuh didaerah tropis
sehingga minyaknya disebut juga minyak tropis (tropical oil). Sejak zaman
dahulu, minyak kelapa sudah sering digunakan. Namun, dalam dekade 90-an,
minyak kelapa hilang dari peredaran. Kini, VCO banyak diminati orang karena
diyakini berkhasiat obat (Sutarmi dan Rozaline, 2005).
Kandungan asam lemak jenuh dalam VCO didominasi oleh asam laurat
dan asam miristat, sedangkan kandungan asam lemak lainnya rendah. Tingginya
asam lemak jenuh yang dikandungnya menyebabkan VCO tahan terhadap proses
ketengikan akibat oksidasi (Syah, 2005).
Minyak kelapa sebenarnya memiliki banyak kelebihan, 50% asam lemak
pada minyak kelapa adalah asam laurat dan 7% asam kaprilat. Kedua asam
tersebut merupakan asam lemak jenuh rantai sedang yang mudah dimetabolisme
dan bersifat antimikroba (antivirus, antibakteri, dan antijamur) sehingga dapat
meningkatkan imun tubuh (kekebalan tubuh) dan mudah menjadi energi (Sutarmi
dan Rozaline, 2005).
Sifat antimikroba dari minyak kelapa terutama tergantung pada adanya
monogliserida, dan asam lemak bebas. Monogliserida aktif sebagai antimikroba
tetapi digliserida dan trigliserida tidak. Asam lemak yang paling aktif adalah asam
Di dalam tubuh, asam laurat akan diubah menjadi monogliserida yang
disebut monolaurin. Senyawa ini merupakan bahan dalam sistem kekebalan tubuh.
Sistem kekebalan tubuh kita dapat dengan mudah menghancurkan
mikroba-mikroba dengan bantuan monolaurin tersebut. Asam lemak bebas mampu
menghambat pertumbuhan bakteri gram positif, misalnya Staphylococcus aureus,
tetapi untuk bakteri gram negatif, misalnya Escherichia coli, asam lemak bebas
tidak mampu mengatasinya. Uji aktivitas antibakteri minyak kelapa murni
terhadap Staphylococcus aureus dan Escherichia coli pernah dilakukan di LIPI
dan hasilnya diketahui bahwa minyak kelapa murni mampu menghambat
pertumbuhan bakteri Staphylococcus aureus (garm positif) tetapi sama sekali
tidak mampu menghambat pertumbuhan bakteri Escherichia coli (gram negatif)
(Darmoyuwono, 2006; Subroto, 2006).
Untuk memperoleh monogliserida dari trigliserida yang terkandung dalam
minyak kelapa murni adalah dengan melakukan hidrolisis. Penambahan NaOH
yang berlebih akan menghidrolisis semua trigliserida menjadi gliserol dan sabun
(Ketaren, 2005).
Untuk mendapatkan manfaat bagi kesehatan, minyak kelapa murni bisa
dikonsumsi langsung ataupun digunakan untuk menggoreng atau menumis
makanan. Saran lain dalam mengkonsumsi minyak kelapa murni adalah dengan
mengoleskannya pada roti, selayaknya menggunakan mentega. Butter cream atau
yang biasa dikenal dengan whipped cream merupakan salah satu produk makanan
yang terbuat dari mentega. Whipped cream sering digunakan untuk menghias roti
oleh masyarakat dan toko roti pada khususnya dan biasanya whipped cream ini
disebabkan oleh adanya mikroba. Bakteri Staphylococcus aureus dan Escherichia
coli merupakan bakeri yang sering terdapat dalam makanan (Sutarmi, 2005;
Anonim, 2011).
Berdasarkan hal tersebut di atas, peneliti ingin membuat whipped cream
yang ditambahkan dengan hasil hidrolisis minyak kelapa murni dan melihat sifat
antibakteri dari hasil hidrolisis minyak kelapa murni terhadap pertumbuhan
bakteri Staphylococcus aureus (gram positif) dan Escherichia coli (gram negatif)
dengan mengetahui berapa banyak jumlah bakteri yang dapat dihambat oleh hasil
hirolisis minyak kelapa murni tersebut. Penelitian ini dilakukan dengan
menggunakan metode Angka Lempeng Total (ALT), dimana metode ini
didasarkan pada jumlah kolini yang tumbuh pada media merupakan jumlah
mikroba yang hidup yang terkandung didalam sampel.
1.2Perumusan Masalah
Berdasarkan uraian dari latar belakang penelitian di atas, dapat disusun
rumusan masalah sebagai berikut:
1. Apakah hasil hidrolisis minyak kelapa murni efektif dalam menghambat
pertumbuhan bakteri Staphylococcus aureus tetapi tidak efektif terhadap
bakteri Escherichia coli.
2. Bagaimana pengaruh tingkat hidrolisis minyak kelapa murni dalam
menghambat pertumbuhan bakteri Staphylococcus aureus dan Escherichia
1.3Hipotesis
Hipotesis dari penelitian ini adalah sebagai berikut:
1. Hasil hidrolisis minyak kelapa murni efektif dalam menghambat
pertumbuhan bakteri Staphylococcus aureus tetapi tidak efektif terhadap
bakteri Escherichia coli.
2. Semakin tinggi tingkat hidrolisis maka semakin tinggi pula sifat
antibakteri hasil hidrolisis minyak kelapa murni dalam menghambat
pertumbuhan bakteri Staphylococcus aureus dan Escherichia coli.
1.4 Tujuan Penelitian
Tujuan dari penelitian ini adalah sebagai berikut:
1. Untuk mengetahui sifat antibakteri hasil hidrolisis minyak kelapa murni
yang ditambahkan kedalam whipped cream dalam menghambat
pertumbuhan bakteri Staphylococcus aureus dan Escherichia coli.
2. Untuk mengetahui hubungan penambahan NaOH dalam hidrolisis minyak
kelapa murni terhadap peningkatan sifat antibakteri hasil hidrolisis minyak
kelapa murni dalam menghambat pertumbuhan bakteri Staphylococcus
aureus dan Escherichia coli.
1.5 Manfaat Penelitian
Manfaat dari penelitian ini adalah memberikan informasi tentang pengaruh
hidrolisis minyak kelapa murni terhadap pertumbuhan bakteri Staphylococcus
BAB II
TINJAUAN PUSTAKA
2.1 Minyak Kelapa Murni
Buah kelapa memilki cukup banyak manfaat, yaitu sebagai minyak makan
atau santan dalam sayur-sayuran. Minyak kelapa murni mengandung asam laurat
yang tinggi. Asam laurat adalah asam lemak jenuh yang berantai medium atau
biasa disebut Medium Chain Fatty Acid (MCFA). Dalam minyak kelapa murni
terkandung energi sebanyak 6,8 kal/gr dan MCFA sebanyak 92% (Gani, 2005).
Saat ini minyak kelapa banyak digunakan sebagai obat. Minyak kelapa
yang dijadikan sebagai obat biasanya disebut minyak kelapa murni (virgin
coconut oil/ VCO). Berbagai penyakit yang berasal dari virus dapat ditangkal
dengan mengkonsumsi minyak kelapa murni, seperti flu burung, HIV/AIDS,
hepatitis, dan jenis virus lainnya. Selain itu, minyak kelapa murni dapat juga
mengatasi kegemukan, penyakit kulit, darah tinggi, dan diabetes (Sutarmi dan
Rozaline, 2005).
Menurut SNI 7381:2008 minyak kelapa murni adalah minyak yang
diperoleh dari daging buah kelapa (Cocos nucifera L.) tua yang segar dan diproses
dengan diperas dengan atau tanpa penambahan air, tanpa pemanasan atau
pemanasan tidak lebih dari 60OC dan aman untuk dikonsumsi. Minyak kelapa
murni tidak berwarna (bening), tidak berasa, serta mempunyai aroma yang harum
dan khas (Gani, 2005). Standar mutu minyak kelapa murni dapat dilihat pada
Tabel 2.1. Standar Mutu Minyak Kelapa Murni Berdasarkan SNI 7381:2008
No. Jenis Uji Satuan Persyaratan
1. 6.5 Asam miristat (C14:0) 6.6 Asam palmitat (C16:0)
Khas kelapa segar, tidak tengik Normal, khas minyak kelapa
Minyak kelapa murni mempunyai sifat tahan terhadap panas, cahaya,
oksigen, dan proses degradasi. Sifat itu membuat minyak kelapa murni dapat
disimpan dalam jangka waktu yang lama. Dalam pemanfaatannya, minyak kelapa
murni dapat dikonsumsi secara langsung ataupun dicampur dengan makanan
(Gani, 2005).
VCO mempunyai kandungan asam lemak jenuh yang tinggi. VCO
mengandung sekitar 92% asam lemak jenuh yang terdiri dari asam laurat, miristat,
dan palmitat. Kandungan asam lemak jenuh dalam VCO didominasi oleh asam
laurat dan asam miristat, sedangkan kandungan asam lemak lainnya rendah.
Tingginya asam lemak jenuh yang dikandungnya menyebabkan VCO tahan
terhadap proses ketengikan akibat oksidasi (Syah, 2005).
2.2Asam Lemak
Asam lemak terdiri dari elemen karbon (C), hidrogen (H), dan oksigen (O)
yang tersusun berupa rantai karbon dengan gugus karboksil (-COOH) padasalah
satu ujungnya. Asam lemak diperoleh dari hasil hidrolisis lemak. Asam lemak
digolongkan menjadi tiga yaitu berdasarkan panjang rantai asam lemak, tingkat
kejenuhan, dan bentuk isomer geometrisnya (Darmoyuwono, 2005).
a. Asam lemak berdasarkan panjang rantai terbagi atas:
1. Asam lemak rantai pendek (Short Chain Fatty Acid, SCFA), mempunyai
atom karbon lebih rendah dari 8
2. Asam lemak rantai sedang (Medium Chain Fatty Acid, MCFA),
mempunyai atom karbon 8 sampai 12
3. Asam lemak rantai panjang (Long Chain Fatty Acid, LCFA), mempunyai
b. Asam lemak berdasarkan ada tidaknya ikatan rangkap terbagi atas:
1. Asam lemak jenuh (Saturated Fatty Acid), tidak mempunyai ikatan
rangkap
2. Asam lemak tak jenuh rantai tunggal (Mono Unsaturated Fatty Acid),
memiliki satu ikatan rangkap
3. Asam lemak tak jenuh rantai jamak (Poly Unsaturated Fatty Acid),
memiliki lebih dari satu ikatan rangkap.
c. Asam lemak berdasarkan bentuk isomer geometrisnya terbagi atas:
1. Asam lemak tak jenuh bentuk cis
2. Asam lemak tak jenuh bentuk trans
Perbedaan asam lemak yang dimiliki setiap minyak membuat proses
pencernaan dan metabolisme di dalam tubuh berbeda. Perlu diketahui bahwa
semua minyak sayur yang banyak dijual dipasaran tergolong asam lemak rantai
panjang. Jenis-jenis asam lemak yang terkandung dalam minyak sayur (kedelai,
jagung, biji bunga matahari) terdiri atas 18 atau lebih atom karbon dan sebagian
besar adalah golongan asam lemak tidak jenuh. Berbeda dengan minyak kelapa
yang 92% merupakan asam lemak golongan rantai karbon medium (MCFA) yang
terdiri atas 12 atom karbon yang diikat jenuh (tidak ada ikatan rangkap) (Gani,
2005).
Minyak kelapa mengandung asam laurat dengan kadar paling tinggi seperti
pada Air Susu Ibu (ASI, sekitar 50%). Asam laurat ini berkhasiat sebagai
antimikroba alami yang ampuh membunuh berbagai kuman, virus dan jamur.
Kandungan asam lemak yang terdapat didalam minyak kelapa dapat dilihat pada
Tabel 2.2. Kandungan Asam Lemak per 100 g Minyak Kelapa
Asam lemak tidak jenuh :
Asam palmitoleat
Trigliserida adalah komponen utama minyak sayur dan lemak hewan.
Trigliserida memiliki berat jenis lebih rendah dibanding air dan pada suhu kamar
normal dapat berada dalam keadaan padat atau cair. Apabila padat maka disebut
lemak, sedangkan apabila cair disebut minyak. Trigliserida disebut juga
triacilgliserol (TAG), yaitu senyawa kimia yang terbentuk dari satu molekul
gliserol dan tiga asam lemak (Darmoyuwono, 2005).
Gliserol adalah alkohol trihidrat (mengandung tiga gugus hidroksil, atau
–OH) yang dapat bergabung dengan sampai tiga asam lemak sehingga
membentuk monogliserida, digliserida, dan trigliserida. Monogliserida,
yang terbentuk dari reaksi antara asam dan alkohol yang melepaskan air (H2O)
sebagai hasil samping (Darmoyuwono, 2005).
2.4 Hidrolisis Lemak
Dalam reaksi hidrolisis, minyak akan diubah menjadi asam-asam lemak
bebas dan gliserol. Reaksi hidrolisis dapat mengakibatkan kerusakan minyak.
Reaksi hidrolisis ini dapat terjadi karena terdapatnya sejumlah air dalam minyak.
Reaksi ini akan mengakibatkan bau tengik pada minyak. Proses hidrolisis yang
disengaja, biasanya dilakukan dengan penambahan sejumlah basa seperti KOH
atau NaOH. Proses ini dikenal sebagai reaksi penyabunan. Proses penyabunan ini
banyak dipergunakan dalam industri (Ketaren, 2005).
Pada proses penyabunan, pemberian KOH atau NaOH yang berlebih akan
menyebabkan terjadinya penyabunan yang sempurna atau hidrolisis total
(Fessenden dan Fessenden 1989, Ketaren 2005). Tetapi apabila jumlah KOH atau
NaOH yang digunakan lebih sedikit dari jumlah minyak yang akan dihidrolisis
maka tidak semua minyak akan tersabunkan atau disebut juga hidrolisis parsial
(Darmoyuwono, 2006).
Bilangan penyabunan adalah jumlah miligram KOH yang dibutuhkan
untuk menyabunkan satu gram minyak atau lemak. Besarnya bilangan
penyabunan tergantung dari berat molekul. Minyak yang mempunyai berat
molekul rendah akan mempunyai bilangan penyabunan yang tinggi dan
sebaliknya minyak yang mempunyai berat molekul tinggi mempunyai bilangan
penyabunan yang rendah. Dalam penetapan bilangan penyabunan biasanya
dipergunakan adalah larutan KOH. Bilangan penyabunan untuk minyak kelapa
Reaksi penyabunan:
O O
CH2 – O – C – R1 R1 – C – O – Na
O CH2 OH O
CH – O – C – R2 + 3NaOH CH OH + R2 – C – O – Na
O CH2 OH O
CH2 – O – C – R3 R3 – C – O – Na
trigliserida basa gliserol sabun
Penetapan bilangan penyabunan dapat dilakukan dengan cara ditimbang
sebanyak 5 gram minyak di dalam labu erlenmeyer 250 ml. Ditambahkan
sebanyak 50 ml NaOH metanol 0,5 N. Labu erlenmeyer dihubungkan dengan
pendingin tegak kemudian dididihkan selama 3 jam. Larutan didinginkan dan
bagian dalam dari pendingin tegak dibilas dengan sedikit air. Larutan
ditambahkan 1 ml indikator fenolftalein kemudian dititrasi dengan HCl 0,5 N
sampai warna merah muda menghilang (Ketaren, 2005). Bilangan penyabunan
dihitung dengan rumus:
(ml NaOH x N NaOH) – (ml HCl x N HCl)
Bilangan Penyabunan = x BM NaOH
g minyak
Untuk hidrolisis parsial dari minyak dilakukan dengan memodifikasi
prosedur bilangan penyabunan diatas, yaitu dengan mengurangi volume NaOH
yang digunakan sesuai dengan tingkat hidrolisis. Misalnya untuk hidrolisis 50%,
maka volume NaOH yang ditambahkan adalah setengah dari volume NaOH yang
2.5 Sifat Antibakteri Minyak Kelapa Murni
Minyak kelapa murni memiliki beberapa keunggulan yaitu kandungan
asam laurat tinggi, komposisi asam lemak rantai mediumnya tinggi dan berat
molekulnya rendah. Asam laurat merupakan asam lemak rantai sedang karena
jumlah karbonnya 12. Banyak penelitian yang telah dilakukan dan diperoleh
bahwa asam laurat di dalam tubuh manusia akan diubah menjadi monolaurin.
Monolaurin ini bersifat sebagai antivirus, antibakteri, dan antijamur. Minyak
kelapa murni juga mengandung asam kaprat yang berantai sedang dengan jumlah
karbon 10. Asam kaprat ini pun bermanfaat bagi kesehatan dimana di dalam tubuh
asam kaprat akan diubah menjadi monokaprin. Monokaprin sangat bermanfaat
sebagai antivirus seperti virus HIV (Rindengan, 2004).
Asam laurat pertama kali ditemukan dalam minyak kelapa oleh prof. Dr.
John J Kabara, dari Departement of Chemistry and Pharmacology, Michigan State
University, Amerika, tahun 1960an. Manfaat asam laurat antara lain dapat
membunuh berbagai jenis mikroba. Sifat asam laurat dapat melarutkan membran
virus sehingga akan menggangu kekebalan virus. Hal ini akan membuat virus
tersebut inaktivasi. Sementara itu asam kaprilat yang terdapat pada minyak kelapa
murni sangat potensi untuk mematikan jamur (Sutarmi dan Rozaline, 2005).
Trigliserida terdiri dari tiga asam lemak yang diikat bersama oleh gliserol.
Bila kita mengkonsumsi VCO maka trigliseridanya di dalam tubuh akan dipecah
menjadi digliserida, monogliserida, dan asam lemak bebas. Asam lemak dalam
VCO yang paling aktif sebagai antibakteri adalah asam laurat dan asam kaprat
Sistem kekebalan tubuh kita dapat dengan mudah menghancurkan
mikroba-mikroba dengan bantuan monolaurin. Produksi monolaurin ini hanya
dimungkinkan apabila kita mengkonsumsi asam laurat, misalnya dari minyak
kelapa (Darmoyuwono, 2005).
Aktifitas antimikroba dari asam lemak dipengaruhi oleh pH yang
merupakan faktor penentu bakteri dapat mati atau hanya terinaktivasi. pH dari
asam lemak rantai pendek (asam kaproat, asam kaprilat, dan asam kaprat) yang
berfungsi baik sebagai antimikroba adalah 6,5-7,5. Namun untuk asam lemak
rantai sedang (asam laurat dan asam miristat), pH minimum 6,5 sudah mampu
membunuh bakteri (Syah, 2005).
2.6Penentuan Aktivitas Antibakteri
Secara umum, ada dua metode yang dapat digunakan untuk penentuan
aktivitas antibakteri dari suatu zat. Yang pertama yaitu penentuan aktivitas
antibakteri dengan menggunakan lempeng silinder. Metode ini berdasarkan difusi
antibiotik dari silinder yang dipasang tegak lurus pada lapisan agar padat dalam
cawan petri sehingga bakteri yang ditambahkan akan dihambat pertumbuhannya
pada daerah berupa lingkaran atau zona bening disekeliling silinder yang berisi
larutan antibiotik. Metode kedua yaitu penentuan dengan cara menggunakan
tabung atau turbidimetri. Metode ini berdasarkan atas hambatan pertumbuhan
biakan mikroba dalam larutan serba sama antibiotik dalam media cair yang dapat
menumbuhkan mikroba dengan cepat bila tidak terdapat antibiotik (Ditjen POM,
1995).
Banyak penelitian yang telah dilakukan untuk mengetahui aktivitas
Sulistiyaningsih, dkk., (2007), melakukan pengujian aktivitas antibakteri minyak
kelapa murni dengan menggunakan metode difusi agar. Pada penelitian tersebut
menunjukkan bahwa minyak kelapa murni dengan konsentrasi 55% (550000 ppm)
aktivitas terhadap Staphylococcus aureus dan Pseudomonas aeruginosa
masing-masing sebanding dengan 16,788 ppm dan 152,405 ppm baku tetrasiklin. Untuk
pengujian aktivitas antibakteri monolaurin terhadap Staphylococcus aureus, telah
dilakukan oleh Widiyarti dkk (2009) dengan menggunakan metode perforasi.
Hasil penelitian tersebut menunjukkan bahwa aktivitas antibakteri senyawa α
-monolaurin hasil sintesis sama dengan α-monolaurin standar sedangkan pengujian
terhadap VCO dan krem yang mengandung VCO telah dilakukan oleh Ginting
(2008) dengan menggunakan pencadang gelas. Pada penelitian tersebut juga
menunjukkan bahwa VCO mempunyai aktivitas antibakteri terhadap
Staphylococcus aureus dan Pseudomonas aeruginosa.
Pada penelitian ini, pengujian sifat antibakteri hasil hidrolisis minyak
kelapa murni terhadap pertumbuhan bakteri Staphyllococcus aureus dan
Escherichia coli dilakukan dengan menggunakan metode Angka Lempeng Total
(ALT). Metode ini didasarkan pada anggapan bahwa setiap sel yang dapat hidup
akan berkembang menjadi suatu koloni. Jumlah koloni yang muncul pada cawan
merupakan jumlah mikroba yang hidup yang terkandung dalam sampel.
Prinsip dari metode Angka Lempeng Total adalah bila sel mikroba yang
masih hidup ditumbuhkan pada medium, maka mikroba tersebut akan
berkembang biak dan membentuk koloni yang dapat dilihat langsung dan
kemudian dihitung tanpa menggunakan mikroskop. Pada metode ini dilakukan
dalam cawan petri. Setelah inkubasi, akan terbentuk koloni pada cawan tersebut
dalam jumlah yang dapat dihitung, dimana jumlah yang terbaik adalah antara
30-300 koloni. Jumlah mikroba dalam sampel ditentukan dengan mengalikan jumlah
koloni dengan faktor pengenceran pada cawan yang bersangkutan. Metode ini
dibedakan atas dua cara, yaitu metode tuang dan metode sebar (Waluyo, 2008).
2.7 Bilangan Asam
Bilangan asam dinyatakan sebagai jumlah miligram KOH yang
dibutuhkan untuk menetralkan asam-asam lemak bebas yang terdapat dalam 1
gram minyak atau lemak. Bilangan asam dipergunakan untuk mengukur jumlah
asam lemak bebas yang terdapat dalam minyak atau lemak. Untuk penetapan
bilangan asam dapat dilakukan dengan cara ditimbang 10 gram minyak atau
lemak ke dalam erlenmeyer 200 ml. Selanjutnya ditambahkan 50 ml alkohol 95%
netral, kemudian dipanaskan selama 10 menit dalam penangas air. Larutan ini
kemudian dititrasi dengan KOH 0,1 N dengan menggunakan indikator fenolftalein
sampai tepat terlihat warna merah muda (Ketaren, 2005).
Bilangan asam dihitung dengan rumus:
A x N x BM KOH Bilangan Asam =
G
Keterangan:
A = jumlah ml KOH untuk titrasi
N = normalitas larutan KOH
G = bobot minyak (gram)
BAB III
METODE PENELITIAN
Penelitian ini dilakukan di Laboratorium Fitokimia dan Mikrobiologi
Fakultas Farmasi USU Medan. Penelitian dilakukan berdasarkan metode
eksperimental dengan meneliti pengaruh variabel bebas yaitu tingkat hidrolisis
25%, 50%, 75% dan 100% minyak kelapa murni terhadap variabel terikat yaitu
daya hambat terhadap pertumbuhan bakteri Staphylococcus aureus dan
Escherichia coli di dalam whipped cream yang dilakukan dengan metode Angka
Lempeng Total.
3.1 Alat-alat
Alat yang digunakan dalam penelitian ini adalah neraca listrik maximum
(Sartorius, Jepang), Hotplate (Heidolp, Jerman), Pendingin Tegak, Buret, Statif,
Penangas air, klem, bola karet, autoklaf (Fisons), inkubator (Fiber Scientific),
jarum ose, Laminar Air Flow Cabinet (Astec HLF 1200L), lemari pendingin
(Toshiba), Hand Mixer (Tiger), cawan petri, pipet tetes, mikroskop (Olympus
CX31), oven (Memmert), kamera (Sony), indikator universal (Merck), dan
alat-alat gelas sesuai kebutuhan.
3.2Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah natrium
hidroksida, kalium hidroksida, metanol, asam klorida, n-heksan, natrium sulfat,
indikator fenolftalein, akuades. Bahan untuk pembuatan whipped cream yaitu
mentega putih dan susu kental manis produksi PT. Frisian Flag Indonesia. Bahan
Agar (Oxoid), natrium klorida. Bakteri yang digunakan adalah bakteri
Staphylococcus aureus ATCC 29737 dan Escherichia coli ATCC 87064, serta
minyak kelapa murni produksi Noery Vico Lhokseumawe – NAD. Gambar
minyak kelapa murni yang digunakan dapat dilihat pada Lampiran 1.
3.3Penyiapan Bahan
3.3.1 Pembuatan Larutan Pereaksi
3.3.1.1Larutan HCl 0,5 N
Sebanyak 41,39 ml asam klorida pekat diencerkan dalam air suling hingga
1000 ml. Kemudian dilakukan pembakuan HCl 0,5 N dengan cara ditimbang
sebanyak 0,25 gram natrium karbonat yang sebelumnya telah dipanaskan pada
suhu 270OC selama 1 jam, kemudian dilarutkan dalam 100 ml air. Dititrasi dengan
larutan asam klorida menggunakan indikator merah metil sampai berwarna merah
muda. Larutan dipanaskan hingga mendidih, kemudian didinginkan dan dititrasi
kembali. Dipanaskan lagi hingga mendidih, dan dititasi lagi hingga warna merah
muda tidak hilang dengan pendidihan lebih lanjut (Ditjen POM, 1995).
3.3.1.2Larutan NaOH metanol 0,5 N
Ditimbang sebanyak 20 gram pelet natrium hidroksida, kemudian
dilarutkan dalam metanol hingga 1000 ml. Kemudian dilakukan pembakuan
NaOH metanol 0,5 N dengan cara dipipet sebanyak 10 ml NaOH metanol 0,5 N
kemudian dititrasi dengan HCl 0,5 N dengan menggunakan indikator fenolftalein
sampai warna merah muda.
3.3.1.3Larutan Merah Metil
3.3.1.4Larutan Fenolftalein
Dilarutkan 1 gram fenolftalein dalam 100 ml etanol.
3.3.1.5Larutan KOH 0,1 N
Ditimbang sebanyak 5,61 gram pelet kalium hidroksida, kemudian
dilarutkan dalam air hingga 1000 ml. Kemudian dilakukan pembakuan KOH 0,1
N dengan cara ditimbang sebanyak 0,3 gram kalium biftalat yang sebelumnya
telah dihaluskan dan dikeringkan pada suhu 120OC selama 2 jam, dan dilarutkan
dalam 75 ml air bebas karbon dioksida. Ditambahkan 2 tetes fenolftalein dan
dititrasi dengan larutan kalium hidroksida hingga terjadi warna merah muda
mantap.
3.3.1.6Larutan Alkohol 95% Netral
Sebanyak 480 ml alkohol 99% dilarutkan dalam air suling sampai 500 ml.
Kemudian larutan dipindahkan ke dalam erlenmeyer, ditambahkan beberapa tetes
indikator fenolftalein dan dititrasi dengan larutan KOH 0,1 N sampai terbentuk
warna merah muda.
3.3.2Penyiapan Alat dan Bahan untuk Pengujian Sifat Antibakteri
3.3.2.1Sterilisasi Alat
Alat-alat dan bahan untuk pemeriksaan mikrobiologi harus disterilkan
terlebih dahulu sebelum dipakai. Alat-alat gelas disterikan di oven pada suhu
170OC selama 2 jam dan media yang digunakan disterilkan di autoklaf pada suhu
121OC selama 15 menit, jarum ose dibakar dengan lampu bunsen.
3.3.2.2Pembuatan Media Nutrient Agar
Komposisi: Beef Extract 3 gram
Agar 15 gram
Air suling sampai 1 liter
Sebanyak 28 gram serbuk Nutrient Agar (NA) dilarutkan dalam air suling
hingga 1 liter dengan bantuan pemanasan sampai semua bahan larut sempurna.
Kemudian disterilkan dalam autoklaf pada suhu 121OC selama 15 menit (Oxoid,
2006).
3.3.2.3Pembuatan Media Plate Count Agar
Komposisi: Trypton 5,0 gram
Ekstrak yeast 2,5 gram
Glukosa 1,0 gram
Agar 9,0 gram
Air suling sampai 1 liter
Sebanyak 17,5 gram serbuk Plate Count Agar (PCA) dilarutkan dalam air
suling sebanyak 1 liter, dipanaskan sampai mendidih sampai semua serbuk PCA
larut, disterilkan dalam autoklaf pada suhu 121OC selama 15 menit (Oxoid, 2006).
3.3.2.4Pembuatan Larutan NaCl 0,9%
Natrium klorida ditimbang sebanyak 9 gram lalu dilarutkan dalam air
suling sedikit demi sedikit dalam labu ukur 1000 ml sampai larut sempurna. Lalu
ditambahkan air suling sampai garis tanda. Larutan kemudian dipindahkan ke
dalam wadah kaca dan disterilkan di autoklaf pada suhu 121OC selama 15 menit.
3.3.2.5Pembuatan Agar Miring
Kedalam tabung reaksi dimasukkan 3 ml media nutrien agar, didiamkan
pada suhu kamar sampai sediaan membeku pada posisi miring 45O kemudian
3.4 Hidrolisis Minyak Kelapa Murni
Untuk penentuan bilangan penyabunan dilakukan prosedur sebagai berikut
yaitu sejumlah 10 gram minyak ditimbang dalam labu alas 250 ml. Ditambahkan
100 ml NaOH metanol 0,5 N. Labu alas dihubungkan dengan pendingin tegak dan
dipanaskan sampai tersabunkan sempurna (3 jam). Selanjutnya larutan
didinginkan dan ditambahkan 1 ml larutan indikator fenolftalein, kemudian
dititrasi dengan HCl 0,5 N sampai warna merah jambu menghilang. Bilangan
Penyabunan dihitung dengan rumus:
(ml NaOH x N NaOH) – (ml HCl x N HCl)
Bilangan Penyabunan = x BM NaOH
gram minyak
Untuk hidrolisis parsial dari minyak dilakukan dengan memodifikasi
prosedur bilangan penyabunan diatas, yaitu dengan mengurangi volume NaOH
yang digunakan sesuai dengan tingkat hidrolisis. Volume NaOH yang digunakan
dapat dilihat pada Lampiran 3.
Sejumlah 50 gram minyak ditimbang kemudian ditambahkan NaOH
metanol 0,5 N sesuai tingkat hidrolisis 25%, 50%, 75% dan 100% kemudian labu
alas dihubungkan dengan pendingin tegak dan dipanaskan selama 3 jam. Setelah
penyabunan selesai maka campuran ditambahkan HCl 0,5 N untuk membebaskan
asam lemak yang tersabunkan, selanjutnya diekstraksi 2 kali masing-masing
dengan 50 ml heksan sehingga terbentuk dua lapisan. Lapisan atas (fraksi
n-heksan) dikumpulkan kemudian ditambahkan 50 mg Na2SO4 anhidrat dan
didiamkan selama 15 menit. Selanjutnya diuapkan di atas penangas air dalam
ditambahkan dalam pembuatan whipped cream dan diuji sifat antibakterinya
(Permata, 2012).
3.5 Penentuan Bilangan Asam Minyak Kelapa Murni dan Hasil Hidrolisis Minyak Kelapa Murni
Penentuan bilangan asam dilakukan dengan cara ditimbang minyak kelapa
murni sebanyak 5 gram di dalam erlenmeyer 200 ml. Ditambahkan 25 ml alkohol
netral 95%, kemudian dipanaskan selama 10 menit dalam penangas air sambil
diaduk. Larutan ini kemudian dititrasi dengan KOH 0,1 N dengan menggunakan
indikator fenolftalein sampai tepat terlihat warna merah jambu. Dihitung bilangan
asam dari minyak (Ketaren, 2005).
A x N x BM KOH Bilangan Asam =
G
Keterangan:
A = jumlah ml KOH untuk titrasi
N = normalitas larutan KOH
G = bobot minyak (gram)
BM KOH = 56,1
3.6 Pembuatan Whipped Cream
Untuk pembuatan whipped cream dilakukan prosedur sebagai berikut yaitu
sebanyak 400 gram mentega putih dan 50 ml susu kental manis dicampur dalam
suatu wadah kemudian dikocok menggunakan mixer hingga mengembang dan
3.6.1 Pembuatan Campuran Whipped Cream dengan Minyak Kelapa Murni
Minyak kelapa murni yang ditambahkan ke dalam whipped cream adalah
2% (Ginting, 2008). Ditimbang sebanyak 4,9 gram whipped cream kemudian
ditambahkan 0,1 gram minyak kelapa murni dan selanjutnya campuran tersebut
dilarutkan dengan n-heksan dengan perbandingan 1 : 1 kemudian diaduk hingga
homogen.
3.6.2 Pembuatan Campuran Whipped Cream dengan Hasil Hidrolisis Minyak Kelapa Murni
Ditimbang sebanyak 4,9 gram whipped cream kemudian ditambahkan 0,1
gram hasil hidolisis minyak kelapa murni 25%, selanjutnya campuran tersebut
dilarutkan dengan n-heksan dengan perbandingan 1 : 1 kemudian diaduk hingga
homogen. Dilakukan hal yang sama untuk hasil hidrolisis minyak kelapa murni
50%, 75% dan 100%.
3.7 Pengujian Sifat Antibakteri Minyak Kelapa Murni dan Hasil Hidrolisis Minyak Kelapa Murni dalam Whipped Cream
3.7.1 Peremajaan Bakteri
Satu koloni bakteri diambil dari stok kultur dengan menggunakan jarum
ose steril, lalu ditanam pada media NA miring dengan cara menggores. Kemudian
diinkubasi dalam inkubator pada suhu 36-37OC selama 24 jam (Ditjen POM,
1995).
3.7.2 Pembuatan Inokulum
Koloni bakteri diambil dari peremajaan bakteri dengan jarum ose steril
lalu disuspensikan dalam tabung reaksi yang berisi 10 ml larutan NaCl 0,9%.
Kemudian diukur kekeruhan larutan pada panjang gelombang 580 nm sampai
3.7.3 Pengenceran Inokulum
Dari suspensi bakteri (konsentrasi bakteri 1x106 cfu/ml) diambil 1 ml lalu
dimasukkan kedalam tabung reaksi yang berisi 9 ml NaCl 0,9% sehingga
diperoleh pengenceran 10-1. Dari pengenceran 10-1 dipipet 1 ml dan dimasukkan
kedalam tabung reaksi yang berisis 9 ml NaCl 0,9% sehingga diperoleh
pengenceran 10-2. Dilakukan hal yang sama sampai diperoleh pengenceran 10-5.
3.7.4 Pengujian Pertumbuhan Bakteri pada Whipped Cream (Blanko)
Dari pengenceran suspensi bakteri 10-5 dipipet sebanyak 0,1 ml dan
dimasukkan kedalam cawan petri. Kemudian dituang media PCA sebanyak 20 ml
kedalam cawan petri, cawan petri segera digoyang dan diputar sedemikian rupa
hingga suspensi tersebar merata. Setelah media memadat, dimasukkan 0,1 ml
whipped cream dengan metode sebar dan selanjutnya diinkubasi pada suhu 35–37OC
selama 24 jam dengan posisi dibalik. Setelah itu diamati dan dihitung jumlah koloni
yang tumbuh dengan menggunakan colony counter, dilakukan percobaan triplo.
3.7.5 Pengujian Sifat Antibakteri pada Campuran Whipped Cream dengan Minyak Kelapa Murni
Dari pengenceran suspensi bakteri 10-5 dipipet sebanyak 0,1 ml dan
dimasukkan kedalam cawan petri. Kemudian dituang media PCA sebanyak 20 ml
kedalam cawan petri, cawan petri segera digoyang dan diputar sedemikian rupa
hingga suspensi tersebar merata. Setelah media memadat, dimasukkan 0,1 ml
campuran whipped cream dengan minyak kelapa murni dengan metode sebar.
Cawan diinkubasi pada suhu 35–37OC selama 24 jam dengan posisi dibalik. Setelah
itu diamati dan dihitung jumlah koloni yang tumbuh dengan menggunakan colony
3.7.6 Pengujian Sifat Antibakteri pada Campuran Whipped Cream dengan Hasil Hidrolisis Minyak Kelapa Murni
Dari pengenceran suspensi bakteri 10-5 dipipet sebanyak 0,1 ml dan
dimasukkan kedalam cawan petri. Kemudian dituang media PCA sebanyak 20 ml
kedalam cawan petri, cawan petri segera digoyang dan diputar sedemikian rupa
hingga suspensi tersebar merata. Setelah media memadat, dimasukkan 0,1 ml
campuran whipped cream dengan hasil hidolisis minyak kelapa murni 25% dengan
metode sebar. Cawan diinkubasi pada suhu 35–37OC selama 24 jam dengan posisi
dibalik. Setelah itu diamati dan dihitung jumlah koloni yang tumbuh dengan
menggunakan colony counter, dilakukan percobaan triplo. Dilakukan hal yang sama
BAB IV
HASIL DAN PEMBAHASAN
4.1 Bilangan Asam Minyak Kelapa Murni dan Hasil Hidrolisis Minyak Kelapa Murni
Hidrolisis minyak kelapa murni akan menghasilkan gliserol yang larut
dalam air, sedangkan asam lemak bebas, monogliserida dan digliserida tidak larut
dalam air tetapi larut dalam pelarut non polar seperti n-heksan. Pada saat
hidrolisat diekstraksi dengan n-heksan, maka gliserol tidak akan terekstraksi
sehingga bobot minyak kelapa murni yang dihasilkan menurun. Semakin banyak
NaOH yang ditambahkan maka semakin sedikit minyak yang dihasilkan
(Ketaren,2005; Widiyarti dan Hanafi,2008). Bobot hasil hidrolisis minyak kelapa
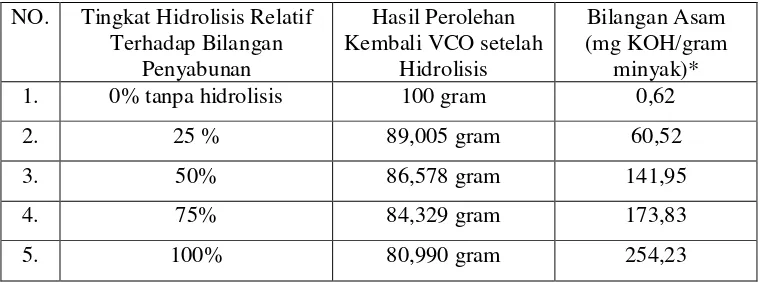
murni dan bilangan asam dapat dilihat pada Tabel 4.1 di bawah ini.
Tabel 4.1 Bobot Minyak Kelapa Murni dan Bilangan Asam Sebelum dan Setelah Hidrolisis
NO. Tingkat Hidrolisis Relatif Terhadap Bilangan
Keterangan: *) hasil rata-rata tiga kali pengulangan
Minyak kelapa murni yang dihidrolisis akan menghasilkan minyak kelapa
murni dengan kandungan asam lemak bebas yang tinggi. Bilangan asam
merupakan salah satu ukuran dari jumlah asam lemak bebas yang terdapat dalam
KOH yang digunakan untuk menetralkan asam lemak bebas yang terdapat dalam
1 gram minyak atau lemak (Ketaren,2005).
Berdasarkan tabel di atas dapat dilihat bahwa setelah minyak kelapa murni
dihidrolisis maka akan terjadi peningkatan bilangan asam. Peningkatan bilangan
asam hasil hidrolisis minyak kelapa murni sebanding dengan peningkatan jumlah
NaOH yang ditambahkan dalam hidrolisis. Bilangan asam yang paling tinggi
ditunjukkan pada hidrolisis penyabunan 100%.
Hidrolisis minyak merupakan suatu proses penyabunan, dimana asam
lemak akan terlepas dari molekul trigliserida dengan adanya bantuan logam alkali
sebagai sabun dan melepaskan gliserol. Pemberian alkali yang berlebih mungkin
akan menyebabkan terjadinya penyabunan yang sempurna, atau dengan kata lain
hidrolisis total (Fessenden dan Fessenden 1989, Ketaren 2005). Tetapi apabila
jumlah alkali yang ditambahkan tidak sebanding dengan jumlah minyak yang
dihidrolisis maka tidak semua trigliserida akan tersabunkan (Darmoyuwono,
2006).
4.2 Sifat Antibakteri Minyak Kelapa Murni dan Hasil Hidrolisis Minyak Kelapa Murni dalam Whipped Cream
Pengujian sifat antibakteri minyak kelapa murni dan hasil hidrolisisnya
dilakukan dengan menggunakan metode angka lempeng total. Pada metode ini
pengenceran dilakukan sampai 10-5 sehingga setelah inkubasi terbentuk koloni
dalam jumlah yang dapat dihitung dimana jumlah yang terbaik adalah antara
30-300 koloni. Jumlah bakteri yang terdapat dalam whipped cream ditentukan dengan
mengalikan jumlah koloni dengan faktor pengenceran pada cawan yang
bersangkutan. Hasil pengujian sifat antibakteri minyak kelapa murni dan hasil
Staphylococcus aureus dan Escherichia coli. Gambar hasil pengujian sifat
antibakteri minyak kelapa murni dan hasil hidrolisisnya dapat dilihat pada
Lampiran 5, Lampiran 6 dan Gambar 4.1 dibawah ini.
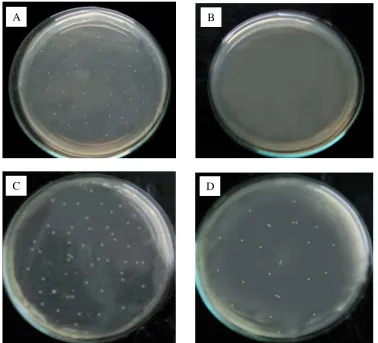
Gambar 4.1 Angka lempeng total pada bakteri uji Staphylococcus aureus dan Escherichia coli.
Keterangan:
A: Blanko pada pengujian terhadap bakteri Staphylococcus aureus
B: Hidrolisis 100% pada pengujian terhadap bakteri Staphylococcus aureus
C: Blanko pada pengujian terhadap bakteri Escherichia coli
D: Hidrolisis 100% pada pengujian terhadap bakteri Escherichia coli
Data hasil pengamatan sifat antibakteri minyak kelapa murni dan hasil
A B
aureus (gram positif) dan Escherichia coli (gram negatif) dapat dilihat pada
Lampiran 7, Tabel 4.2 dan Gambar 4.2 di bawah ini.
Tabel 4.2 Sifat antibakteri minyak kelapa murni dan hasil hidrolisis minyak kelapa murni terhadap bakteri Staphylococcus aureus dan Escherichia coli.
No Perlakuan Tingkat Hidrolisis
Jumlah Koloni Bakteri yang Tumbuh* (cfu)
4. Minyak kelapa murni hidrolisis 50%
19x105 39x105
5. Minyak kelapa murni hidrolisis 75%
- 29x105
6. Minyak kelapa murni hidrolisis 100%
- 26x105
Keterangan: *): Hasil adalah rata-rata tiga kali pengulangan
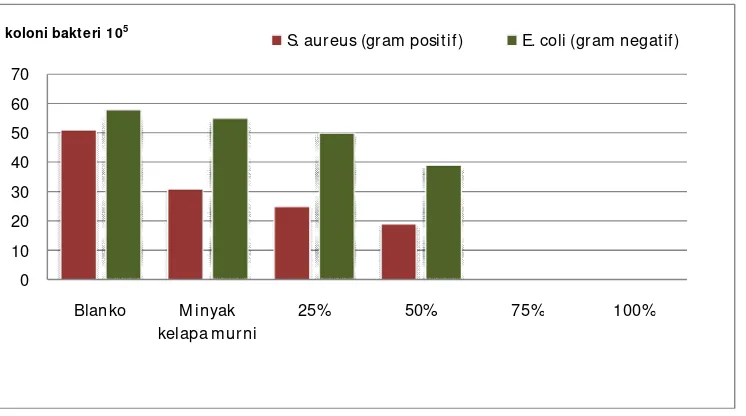
minyak kelapa murni dalam whipped cream
pertumbuhan bakteri. Dari hasil pengujian tersebut diketahui bahwa minyak
kelapa murni dan hasil hidrolisis minyak kelapa murni dapat menghambat
pertumbuhan bakteri yang ada didalam whipped cream. Pada pengujian terhadap
bakteri Staphylococcus aureus, jumlah koloni bakteri pada blanko adalah 51x105
cfu sedangkan pada campuran whipped cream dengan minyak kelapa murni
jumlah koloninya 31x105 cfu. Pada pengujian terhadap bakteri Escherichia coli,
jumlah koloni pada blanko adalah 58x105 cfu sedangkan pada campuran whipped
cream dengan minyak kelapa murni jumlah koloninya 55x105 cfu.
Dari hasil pengujian diatas juga dapat diketahui bahwa semakin tinggi
tingkat hidrolisis maka sifat antibakteri juga akan semakin meningkat. Pada pengujian
terhadap campuran whipped cream dengan minyak kelapa murni hasil hidrolisis 25%,
50%, 75% dan 100% untuk bakteri Escherichia coli secara berturut-turut adalah
50x105 cfu, 39x105 cfu, 29x105 cfu dan 26x105cfu. Sedangkan pada bakteri
Staphylococcus aureus jumlah koloninya 25x105 cfu dan 19x105 cfu tetapi pada
hasil hidrolisis 75% dan 100% tidak ada koloni bakteri yang tumbuh. Dari data
tersebut juga diketahui bahwa sifat antibakteri minyak kelapa murni dan hasil
hidrolisisnya efektif terhadap bakteri Staphylococcus aureus (gram positif) tetapi
kurang efektif terhadap bakteri Escherichia coli (gram negatif).
Hasil penelitian ini didukung oleh hasil penelitian yang telah dilakukan
oleh Ginting (2009), dimana pada penelitian tersebut minyak kelapa murni sangat
efektif sebagai antibakteri terhadap Staphylococcus aureus didalam sedian krim.
Sama halnya dengan penelitian yang telah dilakukan oleh Widiyarti (2009),
Pada penelitian yang telah dilakukan oleh Nuraida (2008), juga
menunjukkan bahwa monogliserida memiliki aktivitas antibakteri terhadap
Staphylococcus aureus dan aktivitas antibakteri terhadap Staphylococcus aureus
(gram positif) lebih tinggi dibandingkan terhadap Escherichia coli (gram negatif)
tetapi aktivitas antibakteri terhadap Escherichia coli dapat meningkat dengan
penurunan pH.
Apabila minyak kelapa murni dihidrolisis, maka trigliseridanya akan
dipecah menjadi digliserida, monogliserida, dan asam lemak bebas. Asam lemak
dan monogliserida menginaktivasi bakteri dengan cara merusak membran plasma
dari bakteri tersebut. Aktivitas antimikroba dari asam lemak juga dipengaruhi oleh
pH yang merupakan faktor penentu bagi bakteri dapat mati atau hanya
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil yang diperoleh dapat diambil kesimpulan bahwa:
1. Hasil hidrolisis minyak kelapa murni mempunyai sifat antibakteri dimana
sifat antibakteri hasil hidrolisis minyak kelapa murni efektif terhadap
bakteri Staphylococcus aureus (gram positif) tetapi kurang efektif terhadap
bakteri Escherichia coli (gram negatif).
2. Hidrolisis menggunakan NaOH meningkatkan kandungan asam lemak
bebas sebanding dengan peningkatan NaOH yang digunakan dalam proses
hidrolisis sehingga semakin tinggi tingkatan hidrolisis maka semakin
tinggi pula sifat antibakteri hasil hidrolisis minyak kelapa murni.
5.2Saran
Dari hasil penelitian ini disarankan kepada peneliti selanjutnya agar dapat
melakukan penelitian lebih lanjut terhadap minyak kelapa murni sebagai bahan
DAFTAR PUSTAKA
Anonim. (2011). Cara Membuat Butter Cream. En.petitchef.com/recipes/cara-membuat-butter-cream/html. Tanggal Akses 5 Maret 2012.
Darmoyuwono, W. (2006), Gaya Hidup Sehat Dengan Virgin Coconut Oil. Jakarta: Penerbit PT Indeks Kelompok Gramedia. Hal. 62-63.
Oxoid. (2006). The Oxoid Manual. Edisi 9. England: Limited Oxoid. Hal. 269-339.
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan RI. Hal. 891-897.
Fessenden, R.J., dan Fessenden, J.S. (1989). Kimia Organik. Jilid 2. Edisi III. Jakarta: Penerbit Erlangga. Hal. 408-412.
Ginting, D.P. (2008). Pembuatan dan Uji Aktivitas Antibakteri Krim Minyak Kelapa Murni (VCO/Virgin Coconut Oil) Terhadap Staphylococcus aureus ATCC 29737 dan Pseudomonas aureginosa ATCC 25629. Skripsi. Medan: Fakultas Farmasi Universitas Sumatera Utara.
Ketaren, S. (2005). Minyak dan Lemak Pangan. Jakarta: Penerbit Universitas Indonesia. Hal. 49-65.
Lieberman, S., Enig, M.G., dan Preuss, H.G. (2006). A Review of Monolaurin and Lauric Acid. Natural Virucidal and Bactericial Agent. Alternative & Complementary Therapies. Desember. Hal. 310.
Nuraida, L., Dhenok, A., Indriana, S.M., dan Tri, H. (2008). Kajian Aktivitas Antibakteri Monoasilgliserol (MAG) dan Mono-Diasilgliserol (MDAG) dari Minyak Kelapa dan Minyak Inti Sawit. Penelitian dan Pengembangan untuk Mendukung Agribisnis Kelapa Sawit Nasional. Departemen Ilmu dan Teknologi Pangan Fakultas Teknologi Pertanian Institut Pertanian Bogor. Hal. 124-213.
Permata, M.Y. (2012). Pengaruh Hidrolisis Parsial Terhadap Aktivitas Antibakteri Minyak Kelapa Murni. Tesis. Medan: Fakultas Farmasi Universitas Sumatera Utara.
Rindengan, B., dan Novarianto. (2005). Pembuatan dan Pemanfaatan Minyak Kelapa Murni. Seri Agretekno. Cetakan Keempat. Jakarta: Penebar Swadaya. Hal. 22-23.
Sulistiyahningsih, Dewi, R. dan Sheli, O.Y. (2007). Aktivitas Antimikroba Minyak Kelapa Murni dengan Beberapa Metode Pembuatan Terhadap Staphylococcus aureus, Pseudomonas aeruginosa, dan Candida albicans dengan Metode Difusi Agar. Farmaka. 5(1): 1-5.
Sutarmi, dan Hartin, R. (2005). Taklukkan Penyakit dengan VCO. Jakarta: Penebar Swadaya. Hal. 6-9.
Syah, A.N.A. (2005). Virgin Coconut Oil. Cetakan Kedua. Jakarta: Agromedia Pustaka. Hal. 8.
Widiyarti, G., dan Hanafi, M. (2008). Study on the Synthesis of Monolaurin As Antibacterial Agent Againts Staphylococcus aureus. Indo. J. Chem. 9(1): 99-106.
Lampiran 2. Perhitungan bilangan penyabunan total minyak kelapa murni
1. Pembakuan HCl untuk penentuan bilangan penyabunan total
Perhitungan Pembakuan
No. Berat Na2CO3 (mg) Volume titrasi (ml)
1. 254 9,2
2. Pembakuan NaOH metanol untuk penyabunan total
Normalitas rata-rata NaOH metanol
No. Normalitas
Jadi normalitas NaOH metanol adalah 0,4985 N
3. Perhitungan Bilangan Penyabunan
Berat sampel (minyak kelapa murni) = 5,011 gram
Volume HCl 0,5247 N = 3,3 ml
Volume NaOH metanol 0,4985 N = 50 ml
mili ekivalen NaOH awal = V x N NaOH
= 50 ml x 0,4985 N
= 24,925 mmol
mili ekivalen NaOH yang bereaksi dengan HCl = V x N HCl
= 3,3 ml x 0,5247 N
= 1,7315 mmol
mili ekivalen NaOH yang bereaksi dengan minyak kelapa murni
= 24,925 mmol – 1,7315 mmol
= 23,1935 mmol
mg NaOH yang bereaksi = mili ekivalen x Mr
= 23,1935 mmol x 40 gram/mol
= 23,1935 mmol x 40 mg/mol
= 927,74 mg
1
Bilangan Penyabunan = x mg NaOH gram minyak
1
= x 927,74 5,001
Lampiran 3. Perhitungan jumlah NaOH metanol yang digunakan dalam hidrolisis metode penyabunan
1. Penyabunan 25%
Pembakuan NaOH metanol untuk penyabunan
Perhitungan pembakuan:
Data normalitas rata-rata NaOH metanol untuk penyabunan 25%
No. Normalitas
Jadi Normalitas NaOH metanol adalah 0,5063 N
Volume NaOH metanol yang ditambahkan untuk hidrolisis 25%
Minyak kelapa murni yang disabunkan = 100,169 gram
NaOH = 185,14 mg/gram minyak
Jumlah NaOH metanol yang ditambahkan
= 25% x 185,14 mg/gram minyak x 100,169 gram minyak
25
= x 185,14 mg/gram minyak x 100,69 gram minyak 100
= 4636,32 mg NaOH
mol NaOH = 4636,32 mg/ (40 gram/mol)
= 4636,32 mg / (40 mg/mmol)
= 115,908 mmol
Volume NaOH = mol / N
= 115,908 mmol / 0,5063 N
= 228,93 ml ~ 229 ml
HCl yang ditambahkan setelah penyabunan untuk melepaskan alkali dari asam
lemak bebas
= V NaOH x N NaOH / N HCl
= 229 ml x 0,5063 N / 0,5247 N
2. Penyabunan 50%
Pembakuan HCl untuk pembakuan NaOH metanol
Perhitungan Pembakuan
miligrek Na2CO3 = miligrek HCl
mg / BE N =
ml
Data Pembakuan HCl 0,5 N
No. Berat Na2CO3 (mg) Volume titrasi
Pembakuan NaOH metanol untuk penyabunan 50%
Data Pembakuan NaOH metanol untuk penyabunan 50%
Normalitas rata-rata:
Data normalitas rata-rata NaOH metanol untuk penyabunan 50%
No. Normalitas
Jadi Normalitas NaOH metanol adalah 0,4913 N