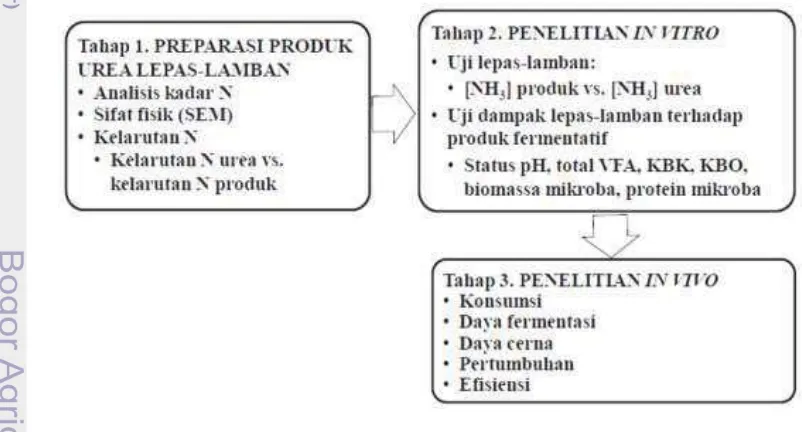
UREA LEPAS-LAMBAN DALAM RANSUM BERBASIS
JERAMI PADI UNTUK MENINGKATKAN EFISIENSI
PRODUKSI SAPI BALI
DEDE KARDAYA
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI DISERTASI DAN SUMBER
INFORMASI
Dengan ini saya menyatakan bahwa disertasi Urea Lepas-Lamban dalam Ransum Berbasis Jerami Padi untuk Meningkatkan Efisiensi Produksi Sapi Bali adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir disertasi ini.
Bogor, Mei 2010
Dede Kardaya
ABSTRACT
DEDE KARDAYA. Slow-Release Urea in Rice Straw Based Diets to Increase Efficiency of Bali Cattle Production.
Under direction of KOMANG G. WIRYAWAN, AMINUDDIN PARAKKASI, and HM. WINUGROHO.
Urea is the most frequently used for substituting natural feed protein in ruminant rations. However, because it is hydrolyzed to ammonia and absorbed into circulatory system, urea may contribute negative impact on ruminant animals. Any effort to optimize urea usage as NPN source for ruminant must consider its negative effect. In this study, the effort was accomplished by characterizing and examining slow-release urea (SLU) products used in vitro and in vivo techniques. The in vitro study was intended to reveal SLU characteristics of zinc-urea (US), zeolites-urea (UZ), and zeolites-zinc-urea (USZ) under different molasses levels in relation to the ruminal fermentative changes observed in different incubation time. The experimental design was randomized block design with a 4 x 3 factorial arrangement plus a control treatment, and conducted in two replications. The factors were urea (U), US, UZ, and USZ and molasses concentrations (0%, 6%, and 12%). The control treatment was the rice straw based diets containing neither urea nor molasses (TU). Diets consisted of 45% rice straw and 55% concentrates (DM basis) were formulated to have similar N and TDN levels. The in vitro diet showed the best ruminal fermentative response was applied in the in vivo study. Under the in vivo study, SLU characteristics of US, UZ, and USZ were examined using 20 Bali bulls (145.3 ± 2.5 kg of BW) allocated to five treatments and four replications in a completely randomized design to evaluate the effects on Bali bull performances. Treatments consisted of diets contained no urea (TU), U, US, UZ, and USZ. Results of solubility study showed that N solubility of US (61.96%), UZ (39.71%), or USZ (40.12%) was lower (P<0.05) than the N solubility of U (91.02%) in two hours of incubation period. The results of the in vitro study revealed that the best impact of the in vitro SLU characteristics of US, UZ, and USZ on the ruminal fermentative changes (NH3, VFA, pH, DMD, OMD, microbial biomass, microbial protein, and efficiency of microbial protein synthesis) was well attributed to the diets contained 6% molasses. The results of the in vivo study revealed that US or UZ might effectively substitute for U in increasing (P<0.05) feed intake. SLU characteristics of US or USZ decreased rumen ammonia concentrations whereas UZ increased total VFA and acetate concentrations (P<0.05) without affecting other fermentative products. US, UZ, or USZ increase crude protein total tract apparent digestibility and nitrogen retention whereas US or UZ increased fiber total tract apparent digestibility when substituted for U (P<0.05). Efficiency of rumen microbial protein synthesis and the microbial protein inflow to post rumen tracts increased with UZ when substituted for U (P<0.05). Finally, UZ increased live weight gain and feed efficiency when substituted for U or TU diets (P<0.05). In conclusion, urea-zeolite showed a slow-release urea characteristic that had a positive impact on feed intake, ruminal fermentative system, digestibility traits and in turn, increased efficiency of Bali bull production.
RINGKASAN
DEDE KARDAYA. Urea Lepas-Lamban dalam Ransum Berbasis Jerami Padi untuk Meningkatkan Efisiensi Produksi Sapi Bali.
Dibimbing oleh KOMANG G. WIRYAWAN, AMINUDDIN PARAKKASI, dan H. WINUGROHO.
Urea merupakan sumber nitrogen bukan protein (NPN) yang paling sering digunakan untuk menggantikan sebagian dari protein ransum pada ruminansia. Namun karena urea bersifat mudah terhidrolisis menjadi amoniak di dalam rumen dan dengan cepat pula diserap memasuki sistem darah, maka dalam praktiknya penggunaan urea dapat berdampak negatif bagi ternak, mulai dari penurunan konsumsi dan performa ternak sampai kematian akibat keracunan urea.
Upaya untuk mengoptimalkan nilai guna dari urea sebagai sumber NPN yang ekonomis bagi ruminansia harus mempertimbangkan dampak negatif dari sifat urea tersebut. Pada penelitian ini, upaya tersebut diwujudkan dengan menguji tiga macam produk urea lepas-lamban, yakni: urea-seng sulfat (US), urea-zeolit (UZ), dan urea-seng sulfat-zeolit (USZ) yang diuji dalam tiga tahap (preparasi dan penentuan sifat produk, in vitro, dan in vivo).
Penelitian tahap pertama bertujuan mempelajari kelarutan preparat US, UZ, dan USZ sebagai suplemen sumber NPN lepas-lamban pada ruminansia. Pada tahap ini, zeolit dipanaskan pada suhu 100 0C lalu kerapatan ruah dan keporiannya diukur untuk menentukan daya serapnya. Selanjutnya, urea dicampurkan dengan zeolit, seng sulfat, atau zeolit dan seng sulfat dengan metode pelelehan urea pada suhu 80 – 110 0C. Rasio urea:zeolit ditetapkan berdasarkan daya serap zeolit, sedangkan rasio urea:seng sulfat ditetapkan berdasarkan reaksi pembentukan kompleks urea-seng sulfat. Produk yang dihasilkan lalu dipindai dengan scanning electron microscopy untuk mengetahui tingkat ketercampuran antara zeolit dan urea. Produk tersebut dilarutkan dalam larutan McDougall dan kelarutan nitrogennya diukur pada rentang waktu: 0, 0.25, 0.5, 0.75, 1, 2, 4, 6, 8, 10, 12, 24, dan 48 jam. Rancangan percobaan yang digunakan untuk uji kelarutan ini adalah Rancangan Acak Lengkap dan setiap perlakuan terdiri atas 2 ulangan.
Penelitian tahap kedua bertujuan mempelajari potensi preparat US, UZ, dan USZ sebagai sumber NPN lepas-lamban untuk mengoptimalkan kemampuan aktivitas fermentasi mikrob rumen. Pada tahap ini penelitian dilakukan secara in
vitro. Sampel dari preparat tersebut dicampurkan dalam sampel ransum yang
Penelitian tahap ketiga bertujuan mempelajari pengaruh penggunaan preparat US, UZ, dan USZ sebagai sumber NPN lepas-lamban terhadap performa sapi Bali. Pada tahap ini penelitian dilakukan secara in vivo. Sifat urea lepas-lamban dari US, UZ, dan USZ diuji menggunakan 20 ekor sapi Bali jantan muda umur berumur sekitar 1 tahunan (sepasang gigi seri tengah tetap) dengan rataan bobot hidup 145.3 ± 2.5 kg. Perlakuan terdiri atas 5 jenis ransum (TU, U, US, UZ, dan USZ) dan rancangannya adalah rancangan acak lengkap dengan 4 ulangan. Peubah yang diukur terdiri atas: pH, amoniak dan VFA (asetat, propionat, butirat, valerat) cairan rumen; kecernaan zat makanan (bahan kering dan bahan organik), retensi N, dan kadar derivat purin (alantoin dan asam urat) urin untuk menghitung sintesis protein mikrob, kadar Zn, glukosa, kolesterol, dan amoniak plasma; konsumsi ransum, pertambahan bobot hidup, dan efisiensi penggunaan ransum.
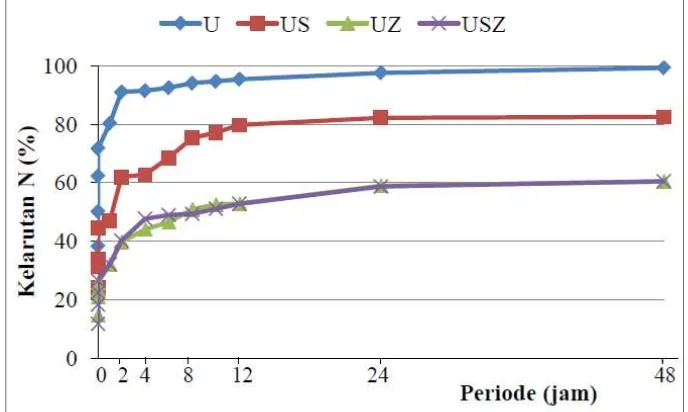
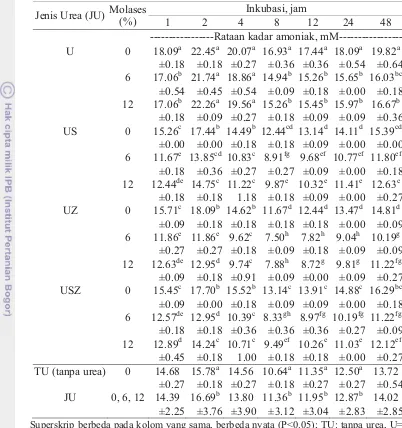
Hasil penelitian tahap pertama memperlihatkan bahwa zeolit alam yang digunakan dalam penelitian ini berkerapatan ruah 0.6127 ± 0.0053 g/ml, keporian 37.2 ± 0.32%, dan daya serap terhadap air 60.72 ± 0.1%. Foto hasil pemindaian mikroskop elektron (SEM) memperlihatkan permukaan UZ dan USZ yang kompak, padat dan berisi yang menandakan pori-pori kristal zeolit telah terisi. Hal ini jelas sekali perbedaannya dibandingkan dengan foto permukaan zeolit alam yang tampak berpori meruah seperti kapas. Preparat US yang tersusun atas 59.81% urea mengandung 26.88% N, sedangkan UZ dan USZ yang masing tersusun atas 37.77% urea mengandung kadar N yang sama, masing-masing 16.98 dan 16.96%. Hasil uji kelarutan memperlihatkan kelarutan N dari US (61.96%), UZ (39.71%), dan USZ (40.12%) lebih rendah (P<0.05) daripada kelarutan N dari U (91.02%) dalam 2 jam periode inkubasi.
dugaan kisaran maksimum produksi biomassa mikrob (2.33 – 2.95) dicapai pada kisaran periode inkubasi 28.3 – 31.5 jam dan nilai dugaan sintesis protein mikrob (1 402 – 1 704 mg/l) dicapai pada periode inkubasi 32.6 – 34.3 jam. Terdapat korelasi positif (r = 0.80; P<0.05) antara bahan organik tercerna dan sintesis protein mikrob (SPM), dan korelasi negatif terjadi antara kadar amoniak cairan rumen (r = -0.96; P<0.05), atau rasio NH3:VFA (r = -0.88; P<0.05) dan SPM.
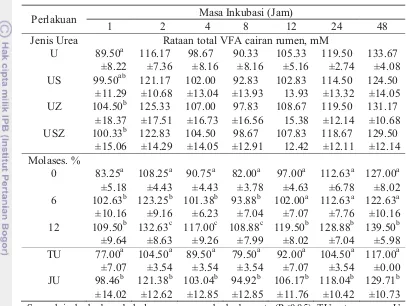
Hasil penelitian tahap ketiga (in vivo) pada sapi Bali memperlihatkan substitusi U oleh US meningkatkan (P<0.05) konsumsi ransum, asupan protein mikrob, kecernaan BK, BO, serat, PK dan retensi N serta menurunkan (P<0.05) kadar NH3 cairan rumen, plasma, dan kadar N feses dan urin. Substitusi U oleh UZ meningkatkan (P<0.05) konsumsi ransum, kadar asetat cairan rumen, kolesterol plasma, asupan dan efisiensi sintesis protein mikrob, kecernaan BK, BO, serat, PK, retensi N, laju pertumbuhan, dan efisiensi penggunaan ransum; menurunkan (P<0.05) kadar NH3 plasma, N feses dan urin, dan biaya ransum. Substitusi U oleh USZ meningkatkan (P<0.05) kecernaan BK dan PK, serta retensi N; menurunkan (P<0.05) kadar NH3 plasma, N feses dan urin. Efisiensi sintesis protein mikroba meningkat sampai 31% dan asupan protein mikroba ke dalam usus halus meningkat sampai 42%. Efisiensi penggunaan ransum dan laju pertumbuhan meningkat sampai 9.5% dan biaya ransum dapat dikurangi sampai 23%. Sementara, ekskresi N melalui feses dan urin berkurang sampai 7%.
Berdasarkan pada hasil penelitian ini disimpulkan bahwa preparat urea-zeolit yang dikombinasikan dengan kadar molases 6% memperlihatkan sifat lepas-lamban yang berdampak positif terhadap konsumsi ransum, sistem fermentasi dan pencernaan sehingga meningkatkan efisiensi produksi dan performa sapi Bali.
© Hak Cipta milik IPB, tahun 2010 Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan penulisan tersebut tidak merugikan kepentingan yang wajar IPB
UREA LEPAS-LAMBAN DALAM RANSUM BERBASIS
JERAMI PADI UNTUK MENINGKATKAN EFISIENSI
PRODUKSI SAPI BALI
DEDE KARDAYA
Disertasi
Sebagai salah satu syarat untuk memperoleh gelar Doktor pada Program Studi Ilmu Ternak
PROGRAM STUDI ILMU TERNAK
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Penguji pada Ujian Tertutup : 1. Prof. Dr. Ir. Toto Toharmat, M.Agr.Sc. 2. Dr. Ir. Nahrowi, M.Sc.
Judul Disertasi : Urea Lepas-Lamban dalam Ransum Berbasis Jerami Padi untuk Meningkatkan Efisiensi Produksi Sapi Bali
Nama : Dede Kardaya NRP : D061060041 Program Studi : Ilmu Ternak (PTK)
Disetujui
Komisi Pembimbing
Prof. Dr. Ir. Komang Gede Wiryawan Ketua
Prof.Dr.Ir.H.M.Winugroho, M.Sc.APU Prof.Dr.drh.H.Aminuddin Parakkasi, MSc. Anggota Anggota
Diketahui
Ketua Departemen Dekan Sekolah Pasca Sarjana Ilmu Nutrisi dan Teknologi Pakan
Dr. Ir. Idat Galih Permana, M.Sc. Prof. Dr. Ir. Khairil A. Notodiputro, M.Sc.
PRAKATA
Segala puji dan syukur dipanjatkan kepada Allah SWT yang telah melimpahkan hidayah dan taufik-Nya kepada penulis sehingga pada akhirnya penulis dapat menyelesaikan disertasi ini. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Juni 2007 ini ialah urea lepas-lamban dengan judul Urea Lepas-Lamban dalam Ransum Berbasis Jerami Padi untuk Meningkatkan Efisiensi Produksi Sapi Bali.
Penelitian ini dilaksanakan dalam tiga tahap, yakni: preparasi dan penentuan sifat produk urea lepas-lamban, penelitian in vitro, dan penelitian in vivo. Sebagian dari naskah artikel hasil penelitan in vitro telah diajukan ke jurnal ilmiah terakreditasi dan telah diterbitkan pada tahun 2009 (JITV 14(3): 177-191).
Ungkapan terima kasih dan penghargaan tinggi penulis sampaikan kepada Bapak Prof. Dr. Komang G Wiryawan, Prof. Dr. H. Aminuddin Parakkasi M.Sc., dan Prof. Dr. H.M. Winugroho, M.Sc., APU selaku komisi pembimbing yang telah memberikan arahan dan bimbingan kepada penulis sejak penyusunan usulan penelitian sampai penyusunan disertasi ini. Ungkapan terima kasih penulis sampaikan pula kepada: Dirjen DIKTI; Rektor, Dekan Sekolah Pascasarjana, Dekan FAPET, Ketua Departemen dan Ketua Program Studi INTP IPB; Rektor, Wakil Rektor, Dekan FATEN, dan Kajur TNK UNIDA; Ketua YPSPI Indonesia; Badan Litbang Pertanian melalui program KKP3T; serta seluruh instansi dan perseorangan yang telah menyediakan fasilitas dan bantuan bagi penulis. Ungkapan terima kasih dan penghargaan yang tak terhingga penulis sampaikan kepada ayah dan ibu (alm.) yang telah membimbing dan mengasihi penulis sejak masih kecil, kakak dan adik-adik, istri dan anak-anak, serta ayah (alm.) dan ibu mertua penulis yang telah memberi dukungan dengan tulus. Teman-teman mahasiswa pascasarjana PTK IPB, dan teman-teman sejawat di Faten Unida, terima kasih atas dukungan dan kebersamaannya. Semoga Allah meridai apa yang telah penulis kerjakan ini dan menjadikan karya ilmiah ini bermanfaat. Amin!
Bogor, Mei 2010
RIWAYAT HIDUP
Penulis dilahirkan di Ciamis pada tanggal 24 Juli 1961 dari ayah H. Aan Ardi Supriyadi dan ibu Hj. Siti Nuriah. Penulis merupakan putra kedua dari lima bersaudara.
ix
DAFTAR ISI
Halaman DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xiii DAFTAR LAMPIRAN ... xv PENDAHULUAN ... 1 TINJAUAN PUSTAKA ... 5 Potensi Jerami Padi sebagai Pakan Ruminansia ... 5 Performa Sapi Bali ... 6 Metabolisme NPN dalam Rumen... 7 Penggunaan Urea pada Ruminansia ... 8 Penggunaan Urea Lepas-Lamban pada Ruminansia ... 10 Penggunaan Mineral Seng dan Urea pada Ruminansia ... 11 Penggunaan Zeolit dan Urea pada Ruminansia ... 12 BAHAN DAN METODE ... 17 Preparasi Produk Urea Lepas-Lamban ... 18 Bahan ... 18 Prosedur Preparasi Produk ... 18 Penentuan Sifat Fisik Mikroskopik dan Kadar N Produk ... 20 Kelarutan Nitrogen Produk ... 20 Percobaan In Vitro ... 21
Bahan ... 22 Rancangan Percobaan ... 23 Pengelolaan Sampel ... 23 Analisis Laboratorium dan Perhitungan ... 25 Analisis Data ... 25 Percobaan pada Ternak (In Vivo) ... 26
x
Kadar Nitrogen Produk Urea Lepas-Lamban ... 34 Kelarutan Nitrogen ... 34 Respons Sistem Rumen terhadap Daya Lepas-lamban Berbagai Jenis
xi
DAFTAR TABEL
Halaman
1 Sifat fisik dan kimiawi zeolit alam yang digunakan dalam penelitian ... 18 2 Kadar bahan kering, bahan organik, dan nitrogen sampel ransum yang
diuji secara in vitro ... 23 3 Komposisi pakan dan kandungan zat makanan dalam ransum yang
diberikan pada sapi Bali... 26 4 Kadar NH3 cairan rumen in vitro akibat pengaruh interaksi jenis urea
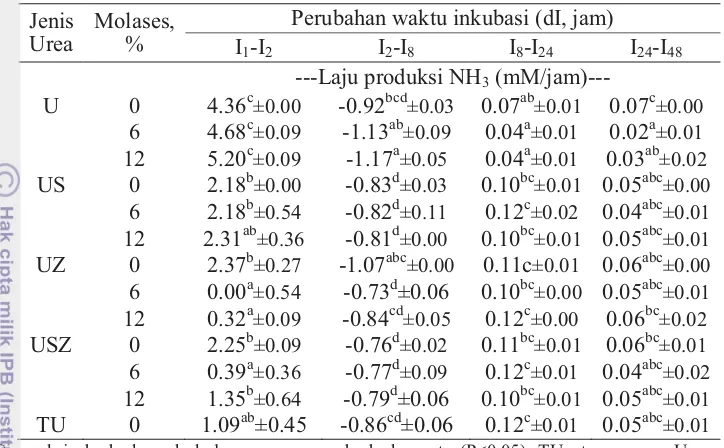
dan kadar molases ... 37 5 Laju produksi NH3 (dNH3/dI) cairan rumen in vitro akibat pengaruh
perlakuan jenis urea dan kadar molases... 38 6 Kadar VFA cairan rumen in vitro akibat perlakuan jenis urea dan
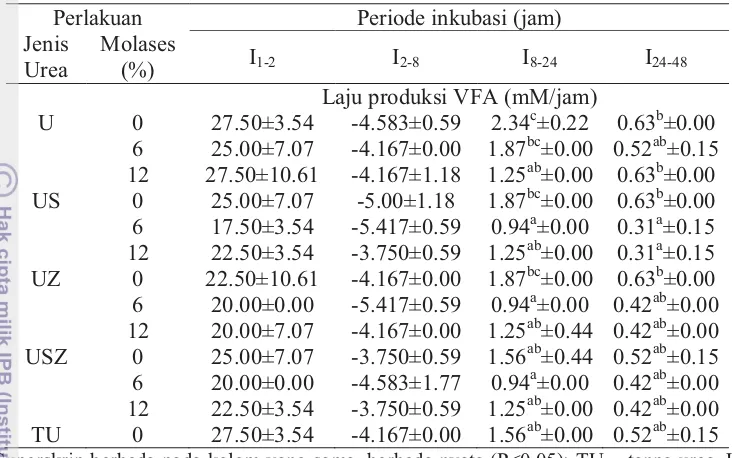
kadar molases... 41 7. Laju produksi total VFA cairan rumen in vitro akibat perlakuan
berbagai jenis urea antara dan kadar molases ... 42 8 Rataan pH cairan rumen in vitro akibat perlakuan jenis urea dan kadar
molases ... 44 9 Laju perubahan pH cairan rumen in vitro akibat perlakuan jenis urea
dan kadar molases ... 45 10 Rasio NH3:VFA cairan rumen sebagai akibat perlakuan jenis urea dan
kadar molases... 45 11 Kecernaan bahan kering in vitro akibat perlakuan jenis urea dan kadar
molases ... 47 12 Laju cerna bahan kering in vitro akibat perlakuan jenis urea dan kadar
molases ... 48 13 Kecernaan bahan organik in vitro akibat perlakuan jenis urea dan
kadar molases... 51 14 Laju cerna bahan organik in vitro akibat perlakuan jenis urea dan
kadar molases... 53 15 Produksi biomassa mikrob in vitro akibat perlakuan jenis urea dan
xii
16 Laju produksi biomassa mikrob in vitro akibat perlakuan jenis urea dan kadar molases ... 56 17 Nilai dugaan puncak produksi biomassa mikrob dan waktu inkubasi
saat biomass mikrob maksimum akibat perlakuan jenis urea dan kadar molases secara in vitro ... 57 18 Sintesis protein mikrob cairan rumen in vitro sebagai perlakuan jenis
urea dan kadar molases pada berbagai periode inkubasi ... 59 19 Laju sintesis protein mikrob in vitro akibat perlakuan jenis urea dan
kadar molases ... 60 20 Nilai dugaan puncak sintesis protein mikrob dan waktu inkubasi saat
protein mikrob maksimum akibat perlakuan jenis urea dan kadar molases secara in vitro ... 61 21 Efisiensi sintesis protein mikrob in vitro akibat perlakuan jenis urea
dan kadar molases ... 62 22 Korelasi parsial antara beberapa peubah rumen dan sintesis protein
mikrob pada periode inkubasi 12, 24, dan 48 jam ... 64 23 Efisiensi penggunaan amoniak oleh mikrob rumen untuk sintesis
protein mikrob in vitro akibat perlakuan jenis urea dan kadar molases ... 66 24 Respons konsumsi sapi Bali terhadap ransum tanpa urea dan berbagai
jenis urea ... 67 25 Status pH dan produk fermentasi cairan rumen sapi Bali yang diberi
ransum tanpa urea dan berbagai jenis urea ... 70 26 Protein mikrob dari sapi Bali yang diberi ransum tanpa urea dan
berbagai jenis urea... 72 27 Nilai dugaan asupan protein mikrob yang memasuki usus halus dari
kadar alantoin urin pada sapi Bali berdasar regresi linier*) ... 74 28 Kecernaan zat makanan dari sapi Bali yang diberi ransum tanpa urea
dan berbagai jenis urea ... 75 29 Kadar NH3, glukosa, kolesterol, dan Zn plasma sapi Bali yang diberi
ransum tanpa urea dan berbagai jenis urea ... 76 30 Transaksi nitrogen pada sapi Bali yang diberi ransum tanpa urea dan
berbagai jenis urea... 80 31 Performa sapi Bali yang diberi ransum tanpa urea dan berbagai jenis
xiii
DAFTAR GAMBAR
Halaman
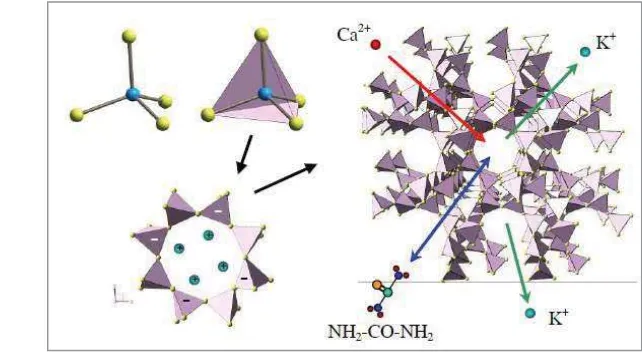
1 Rangka tetrahedra SiO4 dan AlO4- membentuk struktur kerangka kristal zeolit. Jalur masuk dan keluar rongga struktur kerangka bagian dalam melalui saluran (Elliot & Zhang 2005). ... 13 2 Foto permukaan kristal zeolit alam (klinoptilolit) hasil SEM (Minceva
et al. 2007). ... 14 3 Alur tahap pelaksanaan kegiatan penelitian. ... 17 4 Hasil pemindaian mikroskop elektron (SEM) zeolit alam (a),
urea-zeolit (b), dan urea-seng sulfat-urea-zeolit (c). ... 33 5 Kelarutan N (%) produk urea lepas-lamban pada berbagai periode
waktu... 35 6 Kadar VFA cairan rumen in vitro akibat pengaruh interaksi antara
jenis urea dan kadar molases pada periode inkubasi 12 dan 24 jam. ... 41 7 Kecernaan bahan kering (KBK) in vitro dan nilai dugaannya berdasar
regresi logaritma natural.. ... 49 8 Kecernaan bahan organik (KBO) in vitro dan nilai dugaannya
berdasar regresi logaritma natural.. ... 52 9 Produksi biomassa mikrob in vitro akibat pengaruh interaksi jenis urea
dan kadar molases pada periode inkubasi 8 dan 24 jam.. ... 56 10 Sintesis protein mikrob in vitro akibat pengaruh interaksi antara jenis
xv
DAFTAR LAMPIRAN
Halaman
1 Analisis ragam dan uji Duncan kelarutan N berbagai jenis urea
(JU) pada setiap periode inkubasi (I) ... 101 2 Analisis model linier umum multivariat dan uji Duncan pengaruh
perlakuan jenis urea dan kadar molases terhadap kadar NH3
cairan rumen in vitro ... 103 3 Analisis kontras kadar NH3 cairan rumen antara perlakuan tanpa
urea (TU) dan jenis urea (JU) pada setiap periode inkubasi (I) ... 107 4 Analisis model linier umum multivariat dan uji Duncan pengaruh
perlakuan berbagai jenis urea dan kadar molses terhadap kadar
total VFA cairan rumen in vitro... 108 5 Analisis kontras total VFA antara perlakuan tanpa urea (TU) dan
berbagai jenis urea (JU) pada setiap periode inkubasi (I)... 110 6 Analisis model linier umum multivariat dan uji Duncan pengaruh
jenis urea dan kadar molases terhadap pH cairan rumen in vitro ... 110 7 Analisis kontras status pH antara perlakuan tanpa urea (TU) dan
berbagai jenis urea (JU) pada setiap periode inkubasi (I)... 114 8 Analisis model linier umum multivariat dan uji Duncan pengaruh
jenis urea (JU) dan kadar molases (M) terhadap rasio NH3:VFA
cairan rumen in vitro ... 115 9 Analisis model linier umum multivariat dan uji Duncan pengaruh
perlakuan berbagai jenis urea (JU) dan kadar molasses (M)
terhadap kecernaan bahan kering in vitro ... 119 10 Analisis model linier umum multivariat dan uji Duncan pengaruh
perlakuan berbagai jenis urea (JU) dan kadar molases (M)
terhadap kecernaan bahan organik (KBO) in vitro ... 121 11 Analisis kontras kecernaan bahan kering (KBK) dan kecernaan
bahan organik (KBO) antara perlakuan tanpa urea (TU) dan
berbagai jenis urea (JU) pada setiap periode inkubasi (I)... 124 12 Analisis model linier umum multivariat dan uji Duncan pengaruh
berbagai jenis urea (JU) dan kadar molasses (M) terhadap
biomassa mikrob cairan (BM) rumen in vitro ... 125 13 Analisis kontras produksi biomassa mikrob (BM) in vitro antara
xvi
14 Analisis model linier umum multivariat dan uji Duncan pengaruh jenis urea (JU) dan kadar molases (M) terhadap sintesis protein
mikrob (PM) cairan rumen in vitro ... 128 15 Analisis kontras sintesis protein mikrob (PM) in vitro antara
perlakuan tanpa urea (TU) dan perlakuan berbagai jenis urea (JU) ... 131 16 Analisis kontras efisiensi sintesis protein mikrob (ESPM) in vitro
antara perlakuan tanpa urea (TU) dan perlakuan berbagai jenis
urea (JU) ... 131 17 Analisis ragam dan uji Duncan pengaruh perlakuan terhadap
konsumsi ransum sapi Bali ... 132 18 Analisis ragam dan uji Duncan pengaruh perlakuan terhadap
beberapa peubah dalam sistem rumen sapi Bali ... 134 19 Analisis ragam dan uji Duncan pengaruh perlakuan terhadap
asupan dan efisiensi sintesis protein mikrob pada sapi Bali ... 136 20 Analisis ragam dan uji Duncan pengaruh perlakuan terhadap
kecernaan dan absorbsi zat makanan pada sapi Bali ... 138 21 Analisis ragam dan uji Duncan pengaruh perlakuan terhadap
beberapa metabolit plasma sapi Bali ... 141 22 Analisis ragam dan uji Duncan pengaruh perlakuan terhadap
transaksi N pada sapi Bali ... 142 23 Analisis ragam dan uji Duncan pengaruh perlakuan terhadap
performa sapi Bali ... 144 24 Prosedur preparasi larutan penyangga McDougall (Galyean 1997) ... 146 25 Prosedur preparasi larutan penyangga Menke & Steingass (1988) ... 146 26 Prosedur preparasi asai fenol hipoklorit untuk analisis amoniak
(Broderick & Kang 1980) ... 147 27 Prosedur preparasi pereaksi Lowry untuk analisis kadar protein
PENDAHULUAN
Di antara sumber NPN yang paling sering digunakan sebagai sumber nitrogen bagi ruminansia adalah urea karena mudah diperoleh dan murah harganya. Namun urea mudah larut dalam cairan rumen sehingga sangat mudah dan cepat dihidrolisis oleh mikrob rumen menjadi amoniak. Kebutuhan mikrob akan amoniak tersebut berkaitan dengan ketersediaan energi dari ransum ternak. Apabila kadar amoniak rumen melebihi jumlah energi yang tersedia, maka amoniak tidak dapat digunakan seluruhnya oleh mikrob dan lebihan amoniak tersebut diserap melalui dinding rumen ke dalam aliran darah dan diangkut menuju hati. Di dalam hati, amoniak bebas tersebut dinetralkan (detoksifikasi) dengan cara mengubahnya menjadi urea dan mendaurulangnya kembali menuju rumen dan saliva, serta mengekskresikannya melalui urin. Apabila laju serap amoniak dari rumen terlalu cepat dan melebihi kapasitas detoksifikasi hati, maka amoniak akan memasuki sistem darah utama dan dapat menyebabkan kematian.
Potensi urea dalam menghasilkan kadar amoniak yang tinggi dan cepat di dalam rumen inilah yang menjadi pusat perhatian untuk menggunakan sumber NPN dan/atau teknologi yang dapat memperlamban laju lepas amoniak di dalam rumen. Beberapa sumber NPN yang laju lepas amoniaknya lamban (slow-release NPN) telah diteliti, di antaranya biuret (Loest et al. 2001; Currier et al. 2004), penghambat aktivitas enzim urease atau urease inhibitor (Varel et al. 1999; Ludden et al. 2000a, 200b), pelapisan urea dengan campuran talk dan minyak linseed (Owens et al. 1980) atau dengan polimer (Galo et al. 2003; Taylor-Edwards et al. 2009a, 2009b). Teknologi yang terkait dengan pengaturan penggunaan amoniak dan energi oleh mikrob rumen juga telah diteliti (Onwuka 1999; Jain et al. 2005) menggunakan urea dan molases.
dalam ransum berurea secara in vitro menghambat hidrolisis urea dan akumulasi amoniak dalam rumen.
Urea lepas-lamban seperti yang telah dibuat oleh Holladay (1998) berpatokan pada pembentukan senyawa kompleks urea-logam sehingga urea menjadi tidak mudah dihidrolisis oleh urease mikrob rumen. Afinitas urea terhadap ion logam memungkinkan pembentukan beragam kompleks urea-logam (Balarew et al. 2006). Pada dasarnya, urea yang berumus molekul CO(NH2)2 dapat bereaksi dengan garam dari logam alkali dan logam unsur transisi seperti Zn. Menurut Sadeek (1993), seng sulfat dapat bereaksi dengan urea membentuk kompleks urea-seng sulfat [Zn(urea)4]SO4. Kendati demikian, sampai sejauh ini belum ditemukan publikasi tentang penggunaannya sebagai sumber NPN lepas-lamban pada ruminansia. Penggunaan urea-seng sulfat sebagai suplemen pada ruminansia, selain berfungsi sebagai sumber NPN lepas-lamban, juga berfungsi sebagai sumber mineral seng dan sulfur bagi mikrob rumen.
Penggunaan zeolit sebagai suplemen dalam ransum untuk mengontrol kadar amoniak rumen juga telah banyak diteliti (Bosi et al. 2002; Migliorati et al. 2007). Kemampuan zeolit mengontrol kadar amoniak rumen didasarkan atas sifat-sifatnya sebagai penukar kation, katalitik, dehidrasi dan rehidrasi. Sebagai penukar kation, zeolit dengan cepat menukar ion NH4+ yang terbentuk dari dekomposisi senyawa NPN dan menahannya beberapa jam sampai dilepaskan oleh Na+ saliva yang memasuki rumen.
3
alam banyak terdapat di Indonesia terutama di sekitar daerah gunung berapi seperti di pulau Jawa (Senda et al. 2009) sehingga zeolit dengan sifat fisik dan kimiawinya yang khas, merupakan sumberdaya alam yang memerlukan eksplorasi lebih lanjut untuk meningkatkan nilai gunanya.
Kebaruan dari produk urea-zeolit adalah proses pembuatannya berdasarkan kerapatan ruah dan keporian zeolit. Hal ini berbeda dari produk amoniak lepas-lamban (amonium-zeolit) yang dibuat berdasarkan kapasitas tukar kation zeolit. Di dalam rumen, produk urea-zeolit bekerja ganda, yakni menurunkan kelarutan urea sehingga memperlamban hidrolisis urea menjadi amoniak dan menjerap lebihan amoniak dalam rumen. Sementara, amonium zeolit bekerja dengan cara menukar kation amonium dalam zeolit dengan kation lain dalam cairan rumen. Keunikan dari urea-seng sulfat adalah rasionya tertentu karena proses pembuatannya mengacu pada reaksi pembentukan kompleks urea-seng sulfat. Hal ini berbeda dari produk serupa yang dibuat dengan teknologi perlapisan (zinc sulfate coated urea). Produk ini juga berbeda dari teknologi suplementasi seng sulfat dalam ransum berurea. Perbedaan yang mendasar terletak pada mekanisme kerjanya dalam rumen. Kompleks urea-seng sulfat bekerja menurunkan kelarutan urea sehingga memperlamban hidrolisis urea menjadi amoniak dan mineral sengnya menghambat aktivitas enzim urease. Sementara, teknologi perlapisan dan suplementasi seng sulfat hanya mengandalkan kemampun mineral seng dalam menghambat aktivitas enzim urease. Produk urea-seng sulfat-zeolit memiliki keunikan gabungan dari urea-zeolit dan urea-seng sulfat-zeolit.
TINJAUAN PUSTAKA
Potensi Jerami Padi sebagai Pakan Ruminansia
Total produksi padi Indonesia tahun 2007 mencapai 57 157 435 ton dari luas lahan yang dipanen 12 147 637 hektare (BPS 2008). Karena dari setiap kg padi yang dipanen dihasilkan 0.8 – 1 kg jerami (Devendra 1997; Nguyen 1998) maka pada tahun 2007 Indonesia menghasilkan sekitar 45 725 948 - 57 157 435 ton jerami berdasar bahan kering. Dengan asumsi satu unit ternak (UT) setara dengan sapi dewasa berbobot tubuh 325 kg dan konsumsi bahan keringnya 2% dari bobot tubuhnya (Madyono & Anggraeny 2008), maka jerami padi yang tersedia dapat menampung 7 034 761 – 8 793 452 UT.
Walaupun jerami padi merupakan sumber karbohidrat yang melimpah bagi ruminansia, namun pemanfaatannya sebagai pakan masih terbatas karena nilai nutrisinya tergolong rendah (Hadjipanayiotou et al. 1993; Nguyen 1998; Haifeng
et al. 2006). Jerami padi mengandung kadar N yang rendah, kadar silika dan
lignin yang tinggi dan mengikat hemiselulosa dan selulosa sehingga kecernaannya rendah. Kadar protein kasarnya 3.7% dan bahan organiknya 40.2% (Hadjipanayiotou et al. 1993) dengan total zat makanan tercerna (TDN) 26% dari bahan keringnya (Stewart & Silcox 2001). Karena kualitasnya yang rendah dan beragam antarvaritas dan daerah, maka jumlah jerami padi yang dapat dikonsumsi oleh seekor ruminansia pun tidak dapat mencukupi untuk kebutuhan tingkat produksi yang wajar (Nguyen 1998).
Berbagai teknologi untuk memperbaiki kualitas nutrisi jerami padi telah tersedia, antara lain melalui perlakuan secara fisik, kimiawi, biologis, suplementasi, atau kombinasi di antaranya (Nguyen 1998; Abou-El-Enin et al. 1999; Yulistiani, et al. 2000; Stewart & Silcox 2001; Haifeng et al. 2006). Metode perbaikan penyimpanan jerami padi untuk mempertahankan dan memperbaiki kualitasnya juga telah diperkenalkan oleh Al-Mamun et al. (2002).
Performa Sapi Bali
Sapi Bali (Bos sundaicus) adalah sapi asli Indonesia sebagai hasil domestikasi dari banteng liar yang telah berjalan lama. Sapi Bali telah menunjukkan pewarnaan yang seragam dengan sedikit kelainan-kelainan yang sering timbul, tetapi karena kelainan warna ini tidak disukai oleh peternak maka dengan cepat menghilang dari populasi (Talib 2002). Sapi Bali betina mempunyai tanda-tanda yang meliputi warna bulu merah, lutut ke bawah putih, pantat putih berbentuk setengah bulan, ujung ekor hitam dan ada garis belut warna hitam pada punggung; tanduk pendek dan kecil; bentuk kepala panjang dan sempit serta leher ramping. Sapi Bali jantan mempunyai tanda-tanda meliputi warna bulu hitam, lutut ke bawah putih, pantat putih berbentuk setengah bulan, ujung ekor hitam; tanduk tumbuh baik dan berwarna hitam; bentuk kepala lebar dengan leher kompak dan kuat (KBTN 2008).
Sapi Bali tergolong tipe sapi kecil dengan kemampuan reproduksi yang baik dan daya adaptasi yang sangat baik pada pemeliharaan intensif maupun ekstensif-padang penggembalaan. Bobot lahir sapi Bali berkisar 12 – 18 kg dan bobot dewasanya 280 – 329 kg (Talib 2002). Bobot hidup sapi Bali umur 18 bulan berkisar 146 – 185 kg dengan pertambahan bobot hidup antara 6 dan 18 bulan berkisar 0.2 – 0.75 kg/hari dengan rataan 0.23 kg/ekor/hari (Panjaitan et al. (2003). Rataan pertambahan bobot hidup sapi Bali berumur 12-18 bulan, tanpa membedakan jantan dan betina, berkisar 0.2163 – 0.3336 kg/ekor/hari di dataran rendah dan di daerah berbukit (Kadarsih 2004).
Sapi Bali memperlihatkan respons yang baik terhadap berbagai upaya perbaikan nilai gizi ransum. Sariubang et al. (2002) melaporkan peningkatan pertambahan bobot hidup sapi Bali dari 0.19 – 0.35 kg/ekor/hari menjadi 0.37 – 0.45 kg/ekor/hari dengan teknologi fermentasi jerami padi yang diperkaya dengan suplementasi urea, dedak padi halus, garam dapur, dan mineral sulfur. Ahmad et al. (2004) melaporkan bahwa sapi Bali yang diberi ransum campuran rumput,
legum, dan dedak halus yang disuplemen probiotik memperlihatkan peningkatan
7
Metabolisme NPN dalam Rumen
Urease merupakan enzim yang mengandung nikel yang mengkatalis hidrolisis urea membentuk amoniak dan karbamat. Selanjutnya senyawa karbamat ini terurai secara spontan menghasilkan molekul kedua amoniak dan karbon dioksida (Moharrery 2004; Gaballa et al. 2007). Urease bakteri berperan penting dalam metabolisme nitrogen dalam rumen. Urea, baik yang berasal dari ransum maupun yang didaur ulang melalui saliva dan pembuluh darah, dihidrolisis menjadi amoniak. Amoniak ini selanjutnya digabungkan dengan asam-asam keto (ketoacids) oleh mikrob rumen untuk sintesis asam amino (Moharrery 2004).
Karena amoniak yang dihasilkan dalam rumen digunakan untuk pertumbuhan mikrob, yang juga bergantung pada ketersediaan energi, maka penting sekali bahwa laju produksi amoniak dalam rumen harus diselaraskan dengan laju cerna karbohidrat (Galo et al. 2003). Mikrob rumen akan terus mengubah urea menjadi amoniak bahkan ketika kekurangan atau ketiadaan asam-asam keto. Jika laju produksi amoniak, misalnya urea menjadi amoniak hasil perombakan oleh urease, atau hasil dari mengonsumsi amoniak (misalnya dari pakan amoniasian), melebihi kemampuan mikrob untuk menggunakannya untuk membentuk asam amino, maka akan terjadi penumpukan amoniak dalam rumen (Moharrery 2004). Mikrob rumen menghidrolisis urea menjadi amonium (NH4+) dan amoniak (NH3) untuk mensintesis protein selnya. Umumnya, sebagian besar urea yang diubah menjadi amonium tersedia bagi mikrob rumen. Sebaliknya, sebagian kecil amoniak yang dihasilkan, yang bersifat senyawa larut lemak, mudah terserap ke dalam aliran darah (Coutinho et al. 2004).
meningkatkan kadarnya dalam darah, cairan serebrospinal, dan jaringan lainnya, sehingga menyebabkan keracunan amoniak (Moharrery 2004; Haliburton & Morgan 1989; Visek 1984). Ternak yang terbiasa dengan ransum berkadar protein tinggi atau yang telah teradaptasi dengan urea mempunyai kemampuan yang lebih tinggi untuk menetralkan amoniak dalam hatinya. Karena hati berperan penting dalam menetralkan amoniak, maka ketidakberfungsian hati menyebabkan kerentanan yang lebih tinggi terhadap keracunan amoniak (Parkins et al. 1973).
Sumber nitrogen bagi ruminansia dapat berasal dari NPN seperti urea, amoniak, dan biuret, karena ruminansia mampu memanfaatkan NPN sebagai sumber protein melalui aktivitas mikrob rumennya, atau dari protein sejati. Idealnya, sumber N bagi mikrob berasal dari senyawa NPN, bukan berasal dari protein sejati. Menurut Mlay et al. (2003), kebutuhan asam amino ternak ruminansia yang diberi ransum hijauan berkualitas rendah hampir sepenuhnya bergantung pada pasokan protein mikrob karena hampir tidak ada protein sejati yang lolos dari aksi mikrob rumen yang tersedia dari pakan tersebut. Oleh karena itu, upaya optimalisasi sintesis protein mikrob pada ruminansia yang diberi ransum hijauan berkualitas rendah sangat penting dilakukan.
Penggunaan Urea pada Ruminansia
Urea, yang juga dikenal sebagai karbamid dan karbonil diamid, merupakan senyawa kristal berumus molekul CH4N2O, mempunyai titik leleh (melting point) 132.7 °C, dan sangat mudah larut dalam air. Urea ditemukan pada tahun 1773 oleh Rouelle dan komposisinya ditetapkan oleh Prout pada tahun 1818 (Loosli & McDonald 1968). Tahun 1828, F. Wohler untuk pertama kalinya berhasil mensintesis molekul organik ini dari bahan-bahan anorganik (Sci-Tech Encyclopedia 2005). Tahun 1891 Zuntz mengungkapkan bahwa mikroflora rumen mampu merombak selulosa sebagai sumber energi dan mengubah NPN menjadi protein sejati. Pada kurun waktu 1904 – 1925, Morgen menemukan bahwa urea dapat menggantikan 30 – 50% dari protein dalam ransum sapi dan domba (Loosli & McDonald 1968). Sekarang, urea banyak digunakan dalam pakan ruminansia.
9
dan kordinat sebagai monodentate, baik melalui atom oksigennya maupun nitrogennya, atau sebagai bidentate chelating atau bridging ligand bergantung pada tipe ion logamnya (Gaballa et al. 2007). Urea digunakan sebagai bahan awal untuk sintesis beberapa senyawa terapan, membentuk ikatan koordinat dengan beberapa ion logam pada suhu kamar dalam media cair dan noncair melalui atom oksigen atau nitrogennya, bergantung pada tipe ion logam yang digunakan (Refat
et al. 2005).
Jika urea diberikan dalam pakan ruminansia, urea akan segera dihidrolisis menjadi amoniak dalam rumen sehingga amoniak yang dilepaskan tidak digunakan secara efisien untuk sintesis protein mikrob (Chalupa et al. 1984; Jain
et al. 2005; Huntington et al. 2006). Lebih daripada itu, Huntington et al. (2006) melaporkan bahwa sebagian besar amoniak rumen dengan cepat pula memasuki sistem sirkulasi darah dan dapat menimbulkan pengaruh buruk mulai dari penurunan konsumsi ransum dan performa ternak, sampai kematian akibat keracunan amoniak.
Keracunan amoniak dapat terjadi secara periodik jika ruminansia mengonsumsi urea dalam jumlah besar, tidak teradaptasi dengan urea, urea tidak tercampur sempurna dalam ransum, atau jika kadar urea yang tinggi terkandung dalam ransum berserat tinggi, berenergi dan protein rendah (Ortolani et al. 2000). Berlangsungnya tanda-tanda klinis keracunan amoniak beragam, mulai dari beberapa menit sampai beberapa jam setelah ternak mengonsumsi NPN dan biasanya beberapa kasus yang bersifat akut dan drastis menyebabkan kematian (Haliburton & Morgan 1989; Ortolani et al. 2000). Dosis toksik urea yang digunakan oleh Coutinho et al. (2004) adalah 0.5 g urea per kg bobot hidup atau lebih dari 2 kali lipat dari dosis baku yang biasa diberikan pada sapi yang telah teradaptasi, yakni 0.22 g/kg bobot hidup.
mengandung NPN, memperbaiki retensi nitrogen. Penggunaan urea pada ransum ruminansia berkisar antara 0.5% - 1.5% dari bahan kering ransum (Galyean 1996). Jain et al. (2005) memperoleh kadar nitrogen amoniak, total nitrogen, dan NPN yang lebih tinggi dalam cairan rumen domba muda yang diberi campuran urea molases mineral daripada ternak yang diberi ransum basal. Currier et al. (2004) melaporkan bahwa urea atau biuret dapat digunakan secara efektif sebagai suplemen sumber N oleh sapi pedaging yang mengonsumsi hijauan berkualitas rendah, namun biuret lebih aman daripada urea karena hidrolisis biuret menjadi amoniak lebih lamban daripada hidrolisis urea menjadi amoniak dalam rumen.
Penggunaan Urea Lepas-Lamban pada Ruminansia
Potensi urea yang dengan cepat menghasilkan kadar amoniak yang tinggi dalam rumen sehingga dapat menimbulkan keracunan, telah menjadi pusat perhatian untuk menggunakan sumber NPN dan teknologi yang dapat mengontrol atau memperlamban laju lepas amoniak di dalam rumen. Hal ini antara lain dapat dilakukan dengan cara: menggunakan sumber NPN yang kelarutannya lebih rendah daripada urea, menyelaraskan penggunaan amoniak dan energi oleh mikrob rumen, menghambat aktivitas enzim urease mikrob, menurunkan kelarutan atau memperlamban laju lepas N. Chalupa et al. (1984) melaporkan bahwa sumber N yang kelarutannya lebih rendah menghasilkan nilai guna yang lebih tinggi bagi ternak ruminansia. Beberapa sumber NPN yang laju lepas amoniaknya lamban (slow-release NPN) telah diteliti, di antaranya biuret (Slyter
et al. 1971; Loest et al. 2001; Currier et al. 2004), penghambat aktivitas enzim urease atau urease inhibitor (Varel et al. 1999; Ludden et al. 2000a, 2000b), pelapisan urea dengan campuran talk dan minyak linseed (Owens et al. 1980) atau dengan polimer (Galo et al. 2003). Penyelarasan penggunaan amoniak dan energi oleh mikrob rumen yang menggunakan urea dan molases atau karbohidrat yang mudah terfermentasi lainnya juga telah diteliti (Onwuka 1999; Galina et al. 2003; Jain et al. 2005; Golombeski et al. 2006).
11
terhadap pemberian NBPT yang terus menerus. Suplementasi NBPT yang mampu menurunkan aktivitas urease rumen sampai 77% tersebut ternyata tidak mampu menghasilkan amoniak yang sinambung dari urea. Galo et al. (2003) melaporkan bahwa urea yang dilapisi polimer tidak mempengaruhi konsumsi bahan kering dan tidak efektif dalam mengurangi ekskresi nitrogen pada sapi perah.
Penggunaan produk urea lepas-lamban pada sapi jantan pedaging yang diteliti oleh Duff et al. (2000) dapat menggantikan kombinasi bungkil kedelai dan urea sampai 90 persen dalam konsentrat dan dapat memperbaiki efisiensi pertambahan bobot tubuh. Sapi jantan pedaging yang diberi suplemen urea lepas-lamban juga memperlihatkan perbaikan tingkat konsumsi ransum dan kecernaan zat makanan (Galina et al. 2003). Huntington et al. (2006) melaporkan bahwa urea-kalsium efektif dalam mitigasi penglepasan amoniak yang cepat dalam rumen dan pengaruhnya terhadap metabolisme glukosa dan laktat pada sapi. Golombeski et al. (2006) melaporkan bahwa penggantian bungkil kedelai dengan urea lepas-lamban, menggunakan urea-kalsium klorida, dapat memperbaiki secara nyata efisiensi penggunaan ransum pada sapi perah.
Penggunaan Mineral Seng dan Urea pada Ruminansia
Penggunaan seng sulfat sebagai sumber Zn pada ruminansia telah banyak diteliti. Arelovich et al. (2000) menyimpulkan bahwa suplementasi 250 ppm Zn dapat menunda laju hidrolisis urea menjadi amoniak, sehingga mengurangi insiden keracunan urea dan meningkatkan efisiensi energetik dari fermentasi mikrob rumen. Mullis et al. (2003) menggunakan seng sulfat sebagai sumber Zn untuk mengetahui pengaruhnya terhadap status mineral pada sapi jantan pedaging. Kathirvelan & Balakrishnan (2006) mengungkapkan bahwa suplementasi 10 ppm Zn memperlamban hidrolisis urea secara in vitro sehingga sangat efektif dalam menanggulangi keracunan amoniak.
sebagai pupuk urea lepas-lamban dengan berhasil (Rattan 2004) namun belum diketahui publikasi tentang penggunaannya pada ternak.
Reaksi antara beragam ion logam transisi dengan urea telah diteliti dan banyak kompleks urea-logam yang telah dihasilkan dan telah diisolasi (Gaballa et al. 2007). Afinitas urea terhadap ion logam memungkinkan pembentukan beragam kompleks urea-logam (Balarew et al. 2006). Teknologi yang memanfaatkan sifat urea ini yang berkaitan dengan pembentukan produk urea lepas-lamban adalah kompleks urea-kalsium klorida yang dikembangkan oleh Holladay (1998). Sadeek (1993) melaporkan bahwa seng sulfat dapat bereaksi dengan urea membentuk kompleks urea-seng sulfat [Zn(urea)4]SO4. Kompleks urea-seng sulfat tersebut diharapkan akan memiliki sifat seperti kompleks urea-kalsium klorida sebagai sumber NPN lepas-lamban.
Berdasar temuan dalam keputusan kelaikan penilaian kembali toleransi untuk urea dan asam sulfat (garam-garam sulfat), dan disosiasi urea-sulfat dari masing-masing produk yang dihasilkannya, Agen Perlindungan Lingkungan Amerika (U.S. Environmental Protection Agency; EPA) menetapkan bahwa penggunaan produk yang mengandung urea sulfat sebagai bahan aktif tidak menimbulkan bahaya untuk kesehatan manusia dan publik. Ditetapkan pula bahwa tidak ada risiko diet akibat dari mengonsumsi makanan dan/atau minuman dari produk yang mengandung urea sulfat sebagai bahan aktif tunggal (EPA 2005). Oleh karena itu, kompleks urea-seng sulfat yang juga termasuk ke dalam kriteria penilaian EPA (2005) tersebut layak untuk diujicobakan pada ternak.
Penggunaan Zeolit dan Urea pada Ruminansia
Mineral zeolit pertama kali ditemukan tahun 1756 oleh seorang ahli mineralogi Swedia bernama F.A.F. Cronstedt. Sekarang telah ditemukan sekitar 50 jenis zeolit alam dan lebih dari 100 jenis zeolit sintetis. Potensi penggunaan zeolit alam dan zeolit sintetik bergantung pada sifat fisik dan kimianya yang secara langsung berhubungan dengan struktur kristal dan komposisi kimia dari masing-masing jenis zeolitnya (Mumpton 2006).
13
terhingga (Mumpton 1999; 2006). Struktur kristal tiga dimensi tetrahedra silikon-oksigen (SiO4) tersebut lazim disebut tektosilikat.
Gambar 1 Rangka tetrahedra SiO4 dan AlO4- membentuk struktur kerangka kristal zeolit. Jalur masuk dan keluar rongga struktur kerangka bagian dalam melalui saluran (Elliot & Zhang 2005).
Dalam struktur zeolit, keempat sudut atom oksigen dari setiap tetrahedra dikoordinasikan dengan tetrahedra yang berdampingan. Susunan tetrahedra silikat seperti ini, mengurangi total rasio oksigen:silikon menjadi 2:1, dan jika setiap tetrahedron dalam kerangka ini mengandung silikon sebagai pusat atomnya, maka struktur tersebut menjadi netral seperti kwarsa (SiO2). Namun dalam struktur zeolit, sebagian aluminium bervalensi empat digantikan oleh silikon bervalensi tiga sehingga kekurangan muatan positif. Kekurangan muatan tersebut diimbangi oleh unsur-unsur bervalensi satu atau dua seperti Na+, Ca2+, dan K+ dalam struktur tersebut. Dengan demikian, rumus kimia untuk zeolit ini adalah: M2/nO.Al2O3.xSiO2.yH2O. Huruf M dalam rumus tersebut adalah kation logam alkali atau alkali tanah. Huruf n menunjukkan valensi kation M, huruf x bilangan 2 – 10, dan y merupakan bilangan 2 – 7 (Mumpton 2006).
dalam zeolit Na-Pc adalah 95% untuk Pb, 76% untuk Zn, dan 27% untuk Ni (Moirou et al. 2000).
Kandungan molekul air dalam susunan kristal zeolit menunjukkan jumlah pori-pori atau ruang hampa yang akan terbentuk jika unit sel kristal zeolit dipanaskan. Dalam kondisi normal, rongga atau ruang hampa yang besar dalam kristal zeolit terisi oleh molekul air bebas yang membentuk bulatan di sekitar kation. Bila kristal tersebut dipanaskan selama beberapa jam, biasanya pada suhu 300 – 4000C, maka kristal zeolit dapat berfungsi menyerap gas atau cairan (Mumpton 2006). Daya serap zeolit terhadap gas CO2 meningkat dari 28 ml/g menjadi 100 ml/g jika suhu pemanasan ditingkatkan dari 140 0C menjadi 200 0C (Jadhav et al. 2007). Ulfah et al. (2006) mengungkapkan bahwa suhu operasi yang optimum pada pembuatan zeolit X sebagai penjerap logam Fe adalah 92.30C.
Daya serap zeolit tergantung pada jumlah ruang hampa dan luas permukaan. Biasanya mineral zeolit mempunyai luas permukaan beberapa ratus meter persegi untuk setiap gram beratnya. Beberapa jenis mineral zeolit mampu menyerap gas sebanyak 30% dari bobot keringnya. Volume dan ukuran garis tengah ruang hampa dalam kisi-kisi kristal ini pula yang menjadi dasar penggunaan mineral zeolit sebagai bahan penyaring (molecular sieving), dan bahan penyerap (Mumpton 2006). Zeolit mampu menahan air sampai 60% dari bobotnya sebagai akibat dari tingginya keporian struktrur kristal zeolit (Polat et al. 2004).
Sifat fisik permukaan kristal zeolit dapat dipindai dengan alat pemindaian mikroskop elektron (scanning electron microscopy, SEM). Permukaan kristal zeolit alam memperlihatkan keporian yang meruah seperti kapas (Gambar 2).
15
Zeolit bersifat ampoterik, oleh karena itu sebagian zeolit dapat larut dalam media asam atau alkali, namun kelarutannya rendah dalam kisaran pH fisiologis (Trckova et al. 2004). Zeolit juga bersifat hidrofilik (mempunyai afinitas terhadap air) dan hidrofobik, mempunyai afinitas terhadap bahan organik (EPA 1998). Sifat hidrofilik dan hidrofobik zeolit erat kaitannya dengan rasio Si/Al dalam kerangka kristal zeolit. Dalam hal ini, sifat hidrofobik zeolit meningkat dengan meningkatnya rasio Si/Al tersebut (Shirazi et al. 2008).
Klinoptilolit memiliki afinitas yang khas untuk ion amonium dan amoniak. Menurut Mumpton (2006), klinoptilolit dapat digunakan sebagai tambahan pakan alami untuk mengurangi kandungan hara feses karena sifat penyaring kationnya, daya tukar kationnya yang tinggi, daya serap dan afinitasnya yang tinggi terhadap ion NH4+ dan K+.
Di Indonesia, zeolit banyak ditemukan di pulau Jawa, Sumatera Selatan, Kalimantan, Nusatenggara Barat, serta Sulawesi (Senda et al. 2009). Kendati demikian, sebagian besar lokasi endapan zeolit terdapat di pulau Jawa mulai dari Jawa Timur, Jawa Tengah, dan Jawa Barat (Darnin 1995). Jenis mineral zeolit tersebut umumnya adalah klinoptilolit dan mordenit (Senda et al. 2009).
Salah satu yang menjadi pusat perhatian dari penggunaan zeolit dalam nutrisi ruminansia adalah potensi daya serap (adsorbent) dan pengikatannya
(binding effect) pada beberapa zat makanan atau komponen lainnya yang
mempengaruhi metabolisme dan penyerapannya (Katsoulos et al. 2005). Zeolit digunakan dalam pakan sebagai pengikat pelet (pellet binder), untuk memperbaiki penggunaan amoniak, mengikat racun dan logam berat, sebagai agen untuk mengurangi masalah kembung perut (bloat) dan gangguan metabolik (Bechtel & Hutchenson 2003). Pavelic et al. (2001) menggunakan klinoptilolit yang digiling halus sebagai adjuvant dalam terapi kanker.
oleh Na+ saliva yang memasuki rumen. Terlepasnya nitrogen secara bertahap ini memungkinkan mikrob rumen mensintesis protein selnya (Mumpton 1999).
Hasil penelitian Bosi et al. (2002) tentang penambahan klinoptilolit dalam ransum sapi perah mengungkapkan bahwa klinoptilolit tidak mempengaruhi produksi susu, lemak susu, protein susu, dan hitungan sel somatik. Kadar urea susu meningkat dengan penambahan klinoptilolit dalam ransum. Hasil analisis cairan rumen mengungkapkan bahwa klinoptilolit memiliki selektivitas yang rendah terhadap ion amonium. Thilsing-Hansen et al. (2002) yang meneliti pengaruh zeolit terhadap status mineral pada sapi perah periode kering mengungkapkan bahwa suplementasi zeolit meningkatkan kadar kalsium plasma dan kadar 1,25(OH)2D serum, namun kadar magnesium dan fosfat anorganik plasma menurun. Diungkapkan pula bahwa konsumsi ransum pada sapi yang diberi perlakuan zeolit menurun pada dua minggu akhir kebuntingan, namun tidak mempengaruhi produksi susu, lemak susu, dan protein susu pada periode laktasinya. Bosi et al. (2002) dan Migliorati et al. (2007) menyimpulkan bahwa penggunaan klinoptilolit dalam ransum sapi perah tidak berpengaruh negatif terhadap produksi dan kualitas susu.
Koknaroglu et al. (2006) melaporkan bahwa penggunaan zeolit dalam ransum meningkatkan performa sapi pedaging dan pengaruh zeolit tersebut lebih besar pada sapi pedaging yang bobot tubuhnya lebih ringan. Wehl & McLDryden (2005) menyimpulkan bahwa zeolit mampu memperbaiki penggunaan N urea pada domba yang diberi hijauan berkualitas rendah.
Zeolit juga telah digunakan sebagai media untuk pembuatan sumber N lepas-lamban, baik untuk tanaman maupun untuk ternak. Penggunaan zeolit beramonium yang kandungan logam alkalinya rendah telah dikembangkan oleh Cooper (1995) sebagai pupuk N lepas-lamban dengan memanfaatkan daya tukar kation dari zeolit. Eberl (2002) telah mengembangkan chip zeolit berurea dengan cara melelehkan urea dan mencampurkannya dengan zeolit sebagai pupuk N lepas-lamban. Sebelumnya, Hsin-Jen (1997) juga telah mengembangkan pupuk lepas-lamban menggunakan zeolit dan urea.
BAHAN DAN METODE
Kegiatan penelitian dilaksanakan dalam tiga tahap, yakni: preparasi produk urea lepas-lamban, penelitian in vitro, dan penelitian in vivo (Gambar 3). Pada penelitian tahap pertama dilakukan penentuan sifat fisik secara visual dan uji kelarutan nitrogen terhadap produk urea lepas-lamban yang dihasilkan. Produk urea lepas-lamban yang kelarutan nitrogennya lebih rendah daripada kelarutan nitrogen urea, diuji lebih lanjut pada penelitian tahap kedua. Pada penelitian tahap kedua dilakukan uji responsi aktivitas fermentasi mikrob rumen terhadap produk urea lepas-lamban dimaksud pada penelitian tahap pertama secara in vitro. Produk urea lepas-lamban yang menghasilkan kadar amoniak yang lebih rendah daripada kadar amoniak dari urea, diuji lebih lanjut pada penelitian tahap ketiga. Pada penelitian tahap ketiga dilakukan uji responsi ternak terhadap produk urea lepas-lamban. Penelitian tahap pertama dan kedua dilaksanakan selama empat bulan di Laboratorium Pusat Penelitian Sumberdaya Hayati dan Bioteknologi PAU IPB, sementara penelitian tahap ketiga dilaksanakan sekitar dua bulan di kandang sapi lokal pedaging di wilayah Depok.
Preparasi Produk Urea Lepas-Lamban
Penelitian tahap pertama ini bertujuan menghasilkan produk urea lepas-lamban yang kelarutan nitrogennya lebih rendah daripada kelarutan nitrogen urea. Data yang diperoleh dari penelitian ini mencakup: kadar N, foto hasil scanning electron microscopy (SEM), dan kelarutan N.
Bahan
Bahan yang digunakan dalam percobaan ini terdiri atas: urea dan campuran urea-seng sulfat, urea-zeolit, dan urea-seng sulfat-zeolit sebagai produk urea lepas-lamban. Urea yang digunakan adalah urea pupuk berbentuk butir (prill) dengan kandungan nitrogen 45%. Seng sulfat yang digunakan adalah seng sulfat teknis yang mengandung 1 238 ppm Zn. Zeolit yang digunakan adalah zeolit alam bentuk tepung berukuran sekitar 60 mesh. Zeolit ini merupakan sumberdaya lokal yang diperoleh dari Pabrik Karang Mulya Desa Citatah Km 25, terletak di daerah pegunungan di Citatah Padalarang Bandung. Sifat fisik dan kimiawi zeolit dimaksud yang diperoleh dari distributornya disajikan pada Tabel 1.
Tabel 1 Sifat fisik dan kimiawi zeolit alam yang digunakan dalam penelitian
Sifat fisik Sifat kimiawi
Bentuk kristal Mordenit, klinoptilolit, Daya tukar kation > 120 meq/100 g montmorilonit, kuarsa SiO2 > 65%
Warna Abu-abu kehijauan Al2O3 12.88 %
Titik lebur 1 368 0C Fe2O3 1.16 %
pH 8.0 - 10.0 MgO 0.44 %
Massa jenis 2.37 CaO 1.71 %
Volume pori 28 - 34 % MnO2 0.01 %
Diameter pori 2.9 - 7.0 0A Cr2O3 < 0.01 % Susut
pembakaran
8.60 - 13.44 % Na2O 1.13 %
Kadar air < 12.0 % K2O 0.88 %
Serapan amoniak 44.68 % TiO2 0.19 %
Prosedur Preparasi Produk
Prosedur pelaksanaan penelitian pada tahap ini terdiri atas preparasi bahan untuk membuat produk urea lepas-lamban, penentuan sifat fisik produk dengan
19
pembuatannya mengacu pada metode Hsin-jen (1997), yakni terdiri atas pelelehan urea, pencampuran, pengadukan, pendinginan, dan penggilingan.
Zeolit. Zeolit dipanaskan dalam oven bersuhu 100 0C selama 8 jam untuk menguapkan air yang terperangkap dalam pori-pori kristal zeolit. Zeolit kering tersebut lalu ditentukan kerapatan ruah (bulk density), keporian, dan daya serapnya. Kerapatan ruah zeolit ditentukan menurut metode Suliman et al. (2006). Sampel zeolit kering (± 2 g) disaring dengan penyaring berdiameter 1 mm, lalu dimasukkan ke dalam tabung sentrifuse berskala ukur, dimampatkan dengan cara divortek, permukaan zeolit diratakan sejajar dengan garis skala ukur pada tabungnya, lalu diukur volumenya. Kerapatan ruah zeolit ditetapkan berdasar persamaan berikut: ρ = m/v. Dalam hal ini, ρ = kerapatan ruah zeolit, m = massa total zeolit, dan v = volume zeolit. Keporian zeolit yang merupakan rasio antara volume pori total dengan volume total sampel, ditentukan dengan metode saturasi air destilasi (Rakhmatullah et al. 2007). Sampel zeolit dalam tabung sentrifuse yang telah ditentukan kerapatan ruahnya dituangi 2 ml air destilasi (menggunakan pipet volumetrik kapasitas 2 ml), lalu disentrifuse pada 3 000 rpm selama 45 menit sehingga zeolitnya mengendap. Airnya (supernatan) yang bening dibuang dan air yang menempel pada bagian dalam dinding tabungnya diseka dengan kertas tisu. Zeolit yang telah menyerap air tersebut lalu ditimbang untuk menentukan bobotnya (bobot basah). Keporian zeolit ditetapkan berdasar persamaan berikut: keporian = [(BBs – BKs) x Vs-1] x 100%. Dalam hal ini, BBs = bobot basah sampel zeolit, BKs = bobot kering sampel zeolit, Vs = volume sampel zeolit. Daya serap zeolit ditetapkan berdasar persamaan berikut: Daya serap = [(BBs – BKs) x BBs-1] x 100%. Keporian dan daya serap dimaksud, dijadikan acuan untuk menentukan rasio zeolit dan urea dalam preparasi produk urea-zeolit.
Urea-zeolit. Urea-zeolit dibuat dengan mencampurkan 62% zeolit dan 38%
dicurahkan ke dalam lelehan urea sambil diaduk sampai campurannya merata selama 10 menit, lalu didinginkan sambil tetap diaduk sampai produk urea-zeolit memadat. Selanjutnya, produk urea-zeolit dibuat tepung dengan penggiling atau penumbuk, lalu disaring dengan penyaring berdiameter 1 mm.
Urea-seng sulfat. Bahan untuk membuat urea-seng sulfat terdiri atas 40%
seng sulfat dan 60% urea. Rasio ini berdasarkan pada reaksi pembentukan kompleks urea-seng sulfat [Zn(urea)4]SO4 (Sadeek 1993). Pelelehan urea dilakukan seperti pada prosedur preparasi produk urea-zeolit. Seng sulfat dicurahkan ke dalam lelehan urea sambil diaduk sampai campurannya merata selama 10 menit, lalu didinginkan sambil tetap diaduk sampai terbentuk adonan padat. Setelah memadat, produk seng-urea tersebut dijadikan tepung dengan cara menggiling atau menumbuknya dan disaring dengan penyaring berdiameter 1 mm.
Urea-seng sulfat-zeolit. Produk urea-seng sulfat-zeolit terdiri atas 37%
zeolit, 25% seng sulfat, dan 38% urea. Tahapan preparasi urea-seng sulfat-zeolit terdiri atas pelelehan urea, pencurahan seng sulfat yang diikuti dengan pencurahan zeolit seperti pada prosedur preparasi bahan urea-seng sulfat dan urea-zeolit.
Urea yang digunakan untuk membuat ketiga produk di atas adalah urea berbentuk butir (prill). Untuk keperluan uji kelarutan nitrogen, urea berbentuk butir digiling dulu seperti bahan lainnya.
Penentuan Sifat Fisik Mikroskopik dan Kadar N Produk
Penentuan sifat fisik produk urea lepas-lamban dilakukan dengan scanning
electron microscopy (SEM, tipe JSM-5000, ACCV 20 kV) untuk mengetahui
tingkat ketercampuran antara zeolit dan urea. Kadar nitrogen produk dianalisis dengan metode Kjehdahl (AOAC 1991).
Kelarutan Nitrogen Produk
21
untuk uji kelarutan ini adalah Rancangan Acak Lengkap, setiap perlakuan terdiri atas 2 ulangan.
Uji kelarutan N dari bahan uji ini dilakukan mengikuti prosedur Yang et al.
(2001) dengan mengganti pelarutnya, yakni larutan penyangga borat fosfat yang digunakan oleh Yang et al. (2001) diganti dengan larutan penyangga McDougall (saliva buatan) tanpa nitrogen (Galyean 1997). Tabung fermentasi berkapasitas 50 ml diisi secara terurut dengan 10 ml larutan penyangga McDougall yang sebelumnya telah dipanaskan pada suhu 39 0C dan 2 g sampel (untuk setiap bahan uji), lalu diinkubasikan dalam shaking-water bath bersuhu 39 0C sesuai waktu inkubasi yang telah ditentukan. Setelah tiba saatnya, isi dari masing-masing tabung dimaksud lalu disaring dengan 2 lapis kertas saring (Whatman#40). Selanjutnya dari masing-masing filtrat yang diperoleh dipipet sebanyak 200 µl lalu ditimbang untuk dianalisis kadar nitrogen terlarutnya. Kadar nitrogen sampel dan kadar nitrogen terlarut dianalisis dengan metode Kjehdahl (AOAC 1991). Rumus yang digunakan untuk menghitung kelarutan N dari bahan yang diuji adalah:
Kelarutan N = bobot N terlarut (g) x 100% bobot N sampel bahan (g)
Pengaruh perlakuan terhadap kelarutan N dianalisis dengan menggunakan sidik ragam dan jika terdapat pengaruh perlakuan, analisis dilanjutkan dengan uji jarak ganda Duncan. Selanjutnya, produk urea lepas lamban yang kelarutan nitrogennya lebih rendah daripada kelarutan nitrogen urea diuji lebih lanjut dengan uji laju lepas amoniak hasil fermentasi cairan rumen in vitro.
Percobaan In Vitro
Bahan
Media Inkubasi dan Sumber Mikrob. Media inkubasi in vitro yang
dilaksanakan mengacu pada Menke & Steingass (1988) yang dimodifikasi oleh Makkar et al. (1995), yakni tersusun atas: larutan mikromineral 0.02%, larutan penyangga 45.34%, larutan makromineral 45.34%, larutan resazurin 0.23%, dan larutan pereduksi 9.07%. Sumber mikrob sebagai fermen adalah cairan rumen yang berasal dari 2 ekor sapi lokal yang diperoleh dari rumah potong hewan Kotamadya Bogor. Termos, yang sebelumnya telah dihangatkan dengan air hangat, dituangi isi rumen utuh dan cairan rumen hasil perasan dengan rasio sekitar 1:1, lalu segera dibawa ke laboratorium. Di laboratorium, cairan rumen tersebut diblender selama 30 detik, lalu disaring melalui 4 lapis kain kasa. Larutan media inkubasi dibuat dengan cara mencampur 1 bagian cairan rumen hasil penyaringan tersebut dengan 3 bagian larutan penyangga. Masing-masing tabung fermentasi yang berisi 0.5 g sampel dituangi 40 ml larutan media inkubasi, lalu diinkubasikan pada shaking-water bath bersuhu 39 0C selama 1 (I1), 2 (I2), 4 (I4), 8 (I8), 12 (I12), 24 (I24), dan 48 (I48) jam.
Sampel Ransum. Sampel ransum yang akan diuji terdiri atas jerami padi
dan konsentrat yang disusun secara isonitrogen (12% ± 0.09% protein kasar), dengan rasio 45% jerami padi dan 55% konsentrat berdasar bahan kering. Bahan penyusun konsentrat terdiri atas: bungkil kedelai (hanya untuk ransum tanpa urea), jagung giling, dedak halus, bungkil kelapa, dan onggok, 4 jenis preparat urea (U = urea; US = seng sufat: 60% urea, 40% seng sulfat; UZ = urea-zeolit: 38% urea, 62% zeolit; USZ = urea-seng sulfat-urea-zeolit: 38% urea, 25% seng sulfat, 37% zeolit), dan 3 taraf molases (M = taraf molases, M0 = 0% molases, M6 = 6% molases, dan M12 = 12% molases dari bahan kering ransum). Perbedaan kadar molases tersebut dimaksudkan untuk mengetahui laju lepas amoniak dari ransum yang mengandung produk urea lepas-lamban apabila kadar sumber karbohidrat yang mudah terfermentasinya berbeda.
23
memasok 33.33% dari total N ransum berdasar bahan kering. Sampel ransum dalam kondisi kering jemur, digiling halus dan disaring melalui saringan ± 1 mm sebelum dicampurkan untuk membuat ransum lengkap.
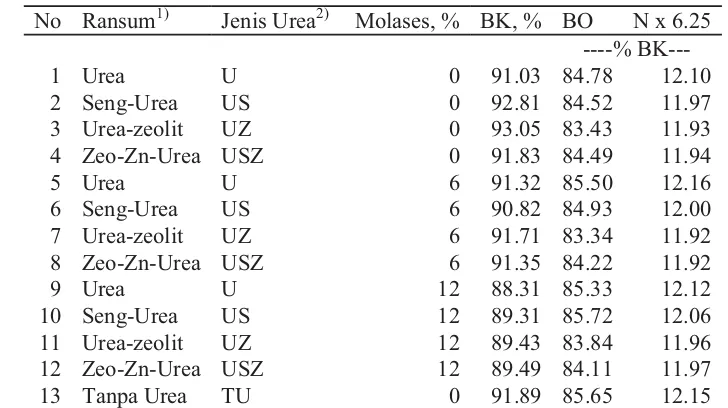
Tabel 2 Kadar bahan kering, bahan organik, dan nitrogen sampel ransum yang diuji secara in vitro
No Ransum1) Jenis Urea2) Molases, % BK, % BO N x 6.25 ----% BK---
1 Urea U 0 91.03 84.78 12.10
2 Seng-Urea US 0 92.81 84.52 11.97
3 Urea-zeolit UZ 0 93.05 83.43 11.93
4 Zeo-Zn-Urea USZ 0 91.83 84.49 11.94
5 Urea U 6 91.32 85.50 12.16
6 Seng-Urea US 6 90.82 84.93 12.00
7 Urea-zeolit UZ 6 91.71 83.34 11.92
8 Zeo-Zn-Urea USZ 6 91.35 84.22 11.92
9 Urea U 12 88.31 85.33 12.12
10 Seng-Urea US 12 89.31 85.72 12.06
11 Urea-zeolit UZ 12 89.43 83.84 11.96
12 Zeo-Zn-Urea USZ 12 89.49 84.11 11.97
13 Tanpa Urea TU 0 91.89 85.65 12.15
1)
Ransum terdiri atas 45% jerami padi dan 55% konsentrat (berdasar BK); konsentrat terdiri atas: bungkil kedelai (hanya untuk ransum TU), bungkil kelapa, jagung kuning, dedak padi halus, onggok, dikalsium fosfat, dan premiks.2)Kadar N dari berbagai jenis urea memasok 33.33% dari total N ransum.
Rancangan Percobaan
Fermentasi in vitro sampel ransum yang mengandung 4 jenis preparat urea (U, US, UZ, USZ) dan 3 taraf kadar molases (0, 6, dan 12%), dan sampel ransum kontrol (tanpa urea tanpa molases, TU) dijadikan sebagai perlakuan dan dilaksanakan dalam dua kelompok ulangan. Percobaan dirancang dalam rancangan acak kelompok berfaktor 4 x 3 dengan 1 perlakuan kontrol (Gomez & Gomez 1995). Peubah yang diukur adalah: nilai pH, kadar NH3, total VFA, kecernaan bahan kering (KBK), kecernaan bahan organik (KBO), biomassa dan protein mikrob.
Pengelolaan Sampel
disentrifugasi dengan kecepatan 3 000 rpm selama 15 menit sehingga padatannya yang terdiri atas partikel pakan dan protozoa mengendap terpisah dari cairannya yang bening (supernatan). Untuk menghentikan fermentasi, supernatan dimaksud ditetesi 2 – 3 tetes asam sulfat pekat, H2SO4 9 M (Kim et al. 2007). Dua ml dari supernatan tersebut, dituangkan ke dalam tabung effendorf berskala ukur (kapasitas 2.5 ml) untuk disentrifugasi lagi dengan kecepatan 15 000 rpm pada suhu 4 0C selama 30 menit sehingga terbentuk endapan biomassa mikrob yang melekat kuat pada bagian dasar tabung effendorf dimaksud. Supernatan hasil sentrifugasi kedua ini dituangkan ke dalam tabung effendorf lainnya, lalu dibekukan dalam lemari es bersuhu -4 0C untuk keperluan analisis NH3. Endapan biomassa mikrob yang terbentuk akibat sentrifugasi kedua tersebut dibilas dengan akuades secara seksama, lalu disentrifugasi lagi pada 15 000 rpm pada suhu 4 0C selama 30 menit. Supernatan hasil sentrifugasi ketiga ini dibuang dan endapan biomassa mikrobanya ditiriskan dengan cara menempatkan tabung effendorf secara terbalik selama 24 jam pada suhu kamar.
Endapan biomassa mikrob hasil penirisan tersebut ditimbang untuk menentukan bobot segar biomassa mikrob, lalu dikeringkan dalam oven bersuhu 65 0C selama 48 jam, lalu ditimbang untuk menentukan bobot keringnya. Selanjutnya, biomassa mikrob kering tersebut disuspensikan dengan 2 ml NaOH 1 N, divortex selama 1 menit, lalu dipanaskan dalam air bersuhu 60 – 70 0C selama 10 menit. Setelah dingin, suspensi biomassa mikrob tersebut disentrifugasi lagi pada 15 000 rpm pada suhu 4 0C selama 30 menit. Supernatan yang diperoleh dapat digunakan secara langsung untuk analisis protein mikrob, sementara sampel yang tidak langsung dianalisis, disimpan di dalam lemari es bersuhu -4 0C untuk keperluan analisis protein mikrob pada waktu berikutnya.
25
Analisis Laboratorium dan Perhitungan
Kadar protein kasar (N x 6.25) sampel ransum, kadar bahan kering (BK) dan abu sampel ransum dan residu fermentasi dianalisis menurut metode AOAC (1990). Kadar bahan organik (BO), kecernaan bahan kering (KBK), dan kecernaan bahan organik (KBO) secara in vitro dihitung berdasarkan persamaan berikut:
BO = bobot BK sampel – (bobot abu) x 100% bobot BK sampel
KBK = bobot BK sampel asal – (bobot BK residu – bobot BK blanko) x 100% bobot BK sampel asal
KBO = bobot BO sampel asal – (bobot BO residu – bobot BO blanko) x 100% bobot BO sampel asal
Kadar NH3 cairan rumen diukur secara kolorimetrik, menggunakan spektrofotometer pada 630 nm berdasar metode Broderick & Kang (1980) dan kadarnya dihitung berdasar kurva standar dalam satuan mM. Kadar total VFA diukur dengan metode destilasi uap (AOAC, 1990) menggunakan mikroburet. Kadar total VFA dihitung berdasar persamaan: Total VFA (mM) = (ml titer blanko – ml titer sampel) x N HCl x 1 000/ ml sampel. Kadar protein mikrob ditentukan dengan metode Lowry et al. (1951) menggunakan larutan BSA (bovine serum albumin) sebagai standar.
Analisis Data
Percobaan pada Ternak (In Vivo)
Percobaan pada ternak menggunakan ransum berurea lepas-lamban berbasis jerami padi dengan kadar molases yang sama hasil percobaan in vitro yang laju lepas amoniaknya lebih rendah dari ransum berurea (U). Sementara, ransum tanpa urea (TU) dan ransum berurea tetap digunakan sebagai pembanding. Percobaan pada ternak ini bertujuan untuk mengetahui pengaruh penggunaan preparat urea-seng sulfat, urea-zeolit, dan/atau urea-urea-seng sulfat-zeolit sebagai sumber NPN lepas-lamban terhadap performa sapi pedaging.
Bahan
Bahan yang digunakan sebagai perlakuan dalam percobaan pada ternak ini terdiri atas ransum yang telah diuji pada percobaan in vitro. Ternak yang digunakan adalah sapi Bali jantan muda berumur sekitar 1 tahunan (sepasang gigi seri tengah tetap) dengan rataan bobot hidup 145.3 ± 2.5 kg. Jumlah sapi yang digunakan dalam penelitian ini sebanyak 20 ekor berasal dari Nusa Tenggara Barat.
Ransum dasar yang digunakan terdiri atas 45% jerami padi dan 55% konsentrat berdasar bahan kering. Ransum dimaksud terdiri atas satu jenis ransum tanpa urea dan 4 jenis ransum yang mengandung berbagai jenis preparat urea yang masing-masing dikombinasikan dengan molases berkadar 6% (Tabel 3).
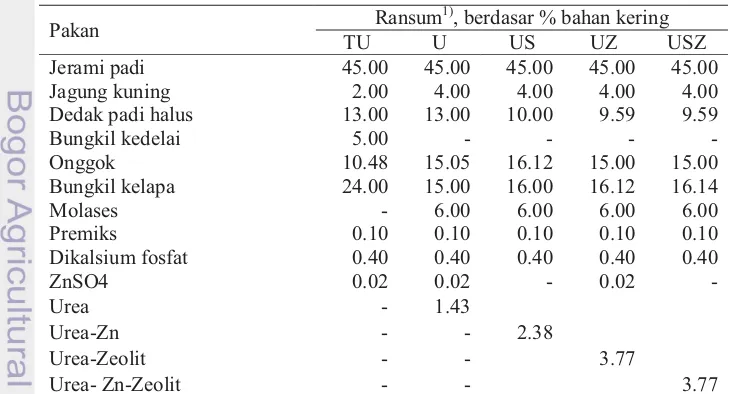
Tabel 3 Komposisi pakan dan kandungan zat makanan dalam ransum yang diberikan pada sapi Bali
Pakan Ransum
1)
, berdasar % bahan kering
TU U US UZ USZ
Jerami padi 45.00 45.00 45.00 45.00 45.00 Jagung kuning 2.00 4.00 4.00 4.00 4.00 Dedak padi halus 13.00 13.00 10.00 9.59 9.59 Bungkil kedelai 5.00 - - - -Onggok 10.48 15.05 16.12 15.00 15.00 Bungkil kelapa 24.00 15.00 16.00 16.12 16.14 Molases - 6.00 6.00 6.00 6.00 Premiks 0.10 0.10 0.10 0.10 0.10 Dikalsium fosfat 0.40 0.40 0.40 0.40 0.40
ZnSO4 0.02 0.02 - 0.02
-Urea - 1.43
Urea-Zn - - 2.38
Urea-Zeolit - - 3.77
27
Pakan Ransum
1)
, berdasar % bahan kering
TU U US UZ USZ
Bahan Kering (BK), % 89.66 88.71 90.25 89.15 88.99 Komposisi: berdasar % BK
Protein kasar (PK) 12.91 11.66 12.20 12.18 12.10 Lemak kasar (LK) 6.03 4.95 4.17 4.52 3.81 Serat kasar (SK) 18.00 17.73 17.55 17.37 16.60 BETN 50.58 53.07 53.67 53.00 54.78 Abu 12.48 12.59 12.41 12.93 12.72 Ca 0.10 0.12 0.11 0.13 0.13 P 0.04 0.06 0.07 0.07 0.07 Zn, mg/kg 34.85 33.75 34.30 33.75 34.85 SDN (NDF) 52.68 50.81 48.61 51.48 48.84 SDA (ADF) 34.45 34.88 33.81 34.47 34.05 Selulosa 21.89 22.33 21.66 21.98 21.41 Lignin 4.56 4.05 4.03 4.65 4.08 Hemiselulosa 18.23 15.94 14.80 17.01 14.79 Silika 8.17 8.11 8.13 8.27 8.29
TDN1) 60.07 59.44 60.47 59.73 59.62
1)
TDN = 0.67 x BK (NRC 1985); BETN: bahan ekstraks tanpa nitrogen, SDN: serat deterjen netral, SDA: serat deterjen asam; TU: tanpa urea, U: urea, US: urea-seng sulfat, UZ: urea-zeolit, USZ: urea-seng sulfat-zeolit. Kadar N dari urea dalam ransum U, US, UZ, dan USZ = 33% dari total N ransum.
Rancangan Percobaan
Penelitian menggunakan rancangan acak lengkap (RAL) yang terdiri atas 5 perlakuan dengan 4 ulangan. Kelima perlakuan tersebut adalah sebagai berikut: 1. Ransum dasar tanpa urea tanpa molases (TU)
2. Ransum bersuplemen urea (U)
3. Ransum bersuplemen urea-seng sulfat (US), 4. Ransum bersuplemen urea-zeolit (UZ)
5. Ransum bersuplemen urea-seng sulfat-zeolit (USZ) Peubah yang diukur terdiri atas:
1. Kondisi rumen: amoniak, pH, dan VFA (asetat, propionat, butirat, valerat). 2. Kecernaan zat makanan (bahan kering dan bahan organik), retensi N, dan
kadar derivat purin (alantoin dan asam urat) urin untuk menghitung sintesis protein mikrob.
3. Kadar Zn, glukosa, kolesterol, dan amoniak plasma.